NUR AENY PRIHATIN. Pola Keragaman Genetik Tanaman Kunyit (
Linn.) dan Temulawak (
Roxb.) Asal Pulau Jawa
dengan PCR(RAPD. Dibimbing oleh LAKSMI AMBARSARI dan WARAS
NURCHOLIS.
Tanaman kunyit (
Linn.) dan temulawak (
Roxb.) merupakan tanaman obat Indonesia yang berkhasiat untuk
meningkatkan kesehatan tubuh. Pola keragaman genetik dan hubungan
kekerabatan kedua tanaman rimpang ini belum banyak diketahui. Penelitian ini
bertujuan menganalisis pola keragaman genetik kedua tanaman dan hubungan
kekerabatannya dengan
DNA (PCR(RAPD). Sampel yang digunakan dalam penelitian ini
adalah enam tanaman kunyit yang berasal dari Bogor, Wonogiri, Karanganyar,
Sukabumi, dan Ngawi; serta lima tanaman temulawak yang berasal dari Bogor,
Wonogiri, Karanganyar, Sragen dan Sukabumi. Tahapan penelitian ini meliputi
isolasi DNA, amplifikasi DNA serta analisis pola keragaman genetik dan
hubungan genetik dengan NTSYS 2.02. Hasil penelitian menunjukkan bahwa
isolasi DNA kunyit dan temulawak berhasil dilakukan dengan nilai kemurnian
kunyit dan temulawak secara berurutan adalah 1.093(1.417 dan 1.044(1.544.
Jumlah pita yang muncul dari amplifikasi DNA kunyit dan temulawak masing(
masing 131 dan 132 lokus. Jumlah pita hasil amplifikasi yang beragam dan
ukuran yang berbeda pada tiap sampel menunjukkan pola keragaman genetik yang
terdapat pada tanaman kunyit dan temulawak. Koefisien kemiripan genetik
tanaman kunyit dan temulawak secara berurutan 54%(92% dan 55%(83%.
Hubungan kekerabatan terdekat ditunjukkan oleh tanaman kunyit asal Sukabumi
dengan Ngawi dan tanaman temulawak asal Bogor dan Sukabumi.
Kata kunci : Kunyit (
Linn.), temulawak (
NUR AENY PRIHATIN. The Pattern of Genetic Diversity of Origin Java Island
Turmeric (
Linn.) and Temulawak (
Roxb.)
with PCR(RAPD. Under direction of LAKSMI AMBARSARI and WARAS
NURCHOLIS.
Turmeric (
Linn.) and Temulawak (
Roxb.) are Indonesian medicinal plants which nutritious for improving health. The
pattern of genetic diversity and genetic relationship of these rhizome plants are
not well known yet. The purpose of this research to analyze the pattern of genetic
diversity and genetic relationship both plants using
DNA (PCR(RAPD). The sample used in this
research include 6 turmeric plants from Bogor, Wonogiri, Karanganyar, Sukabumi
and Ngawi; and 5 temulawak plants from Bogor, Wonogiri, Sragen, Karanganyar
and Sukabumi. Stage of these research include DNA isolation; DNA
amplification; and analysis pattern of genetic diversity and genetic relationship
using NTSYS 2.02. The result of these research showed that isolation DNA was
done successfully. The result of DNA isolation generally has a fairly good purity.
The purity values of turmeric and temulawak in sequence were 1.093(1.417 and
1.044(1.544. The number of bands that arise from DNA amplification of turmeric
and temulawak in sequence were 131 and 132 locus. The number of amplification
bands mixed results and different sizes for each sample show the patterns of
genetic diversity found in turmeric and temulawak plants. The closest genetic
relationship showed by turmeric plants from Sukabumi and Ngawi; and
temulawak plants from Bogor and Sukabumi. Genetic similarity coefficient
ranged from turmeric plants and temulawak plants in sequence are 54%(92% and
55 %(83 %.
Keywords : Turmeric (
Linn.) temulawak (
Skripsi
Sebagai salah satu syarat untuk memperoleh gelar
Sarjana Sains pada
Departemen Biokimia
Judul Skripsi : Pola Keragaman Genetik Tanaman Kunyit (
Linn.) dan Temulawak (
Roxb.) Asal Pulau
Jawa dengan PCR(RAPD
Nama
: Nur Aeny Prihatin
NIM
: G84080029
Disetujui,
Komisi Pembimbing
Dr. Laksmi Ambarsari, MS.
Waras Nurcholis, M. Si.
Ketua
Anggota
Diketahui,
Dr. Ir. I Made Artika, M. App. Sc.
Ketua Departemen Biokimia
Puji dan syukur penulis panjatkan atas kehadirat Allah Yang Maha Esa
yang telah menganugerahkan berkat dan rahmat(Nya sehingga karya ilmiah ini
dapat terselesaikan dengan baik. Penelitian dilakukan di Laboratorium Penelitian
Departemen Biokimia, Fakultas Matematika dan Ilmu Pengetahuan Alam, Institut
Pertanian Bogor, Dramaga, Bogor. Adapun judul dari karya ilmiah ini adalah Pola
Keragaman Genetik Tanaman Kunyit (
Linn.) dan Temulawak
(
Roxb.) Asal Pulau Jawa dengan PCR(RAPD.
Ucapan terima kasih penulis sampaikan kepada Dr. Laksmi Ambarsari
MS. selaku pembimbing utama dan Waras Nurcholis, M.Si. selaku pembimbing
anggota atas bimbingan, arahan dan masukan yang diberikan kepada penulis
selama penelitian dan penyusunan karya ilmiah ini. Penulis juga mengucapkan
terima kasih kepada Popi Asri Kurniatin, S.Si., Apt., M.Si., Pak Nana, Pak Yadi,
Bu Merry, Bu Tini, Bu Tuti, Pa Arya, Bu Retno, Pa Erik dan Mba Eli yang telah
banyak membantu penulis. Terima kasih juga penulis sampaikan kepada Grahan,
Annisa, Riani, Adit, Rian, Faris, Yuanita, An(Nisa, Lusi atas dukungan dan
semangat yang diberikan. Rasa terima kasih yang begitu besar juga penulis
sampaikan kepada orang tua penulis tercinta atas segala dukungan, bantuan dan
doa yang telah diberikan untuk kelancaran kegiatan ini. Ucapan terima kasih juga
penulis sampaikan kepada PT. Indofood Sukses Makmur Tbk. sebagai donatur
beasiswa BISMA, Yayasan Karya Salemba Empat, dan Paguyuban KSE IPB yang
sangat membantu kelancaran masa perkuliahan dan DIKTI yang membantu
penyelesaian tugas akhir penulis.
Penulis dilahirkan di kota Bogor, pada tanggal 28 Mei 1990. Penulis
merupakan anak kedua dari pasangan Utay Hidayat dan Uun Karsunah.
Penulis bersekolah dasar di SDN Tanah Sareal 1 selama 6 tahun, terhitung
tahun 1996 hingga 2002. Sekolah menegah pertama penulis adalah SMPN 8
Bogor. Selanjutnya, penulis melanjutkan sekolah menegah atas di SMAN 2 Bogor
dan menempuh jalur USMI IPB pada tahun 2008, tepatnya di Departemen
Biokimia, Fakultas Matematika dan Ilmu Pengetahuan Alam.
Kegiatan yang penulis lakukan selama perkuliahan di antaranya menjadi
asisten praktikum Kimia Dasar pada tahun 2010, asisten praktikum Biokimia
Umum pada tahun 2012, asisten praktikum Teknologi Asam Nukleat, dan
Metabolisme pada tahun yang sama. Selain itu, penulis juga menjadi pengajar di
salah satu bimbingan belajar khusus untuk mahasiswa, pengajar privat siswi SD
dan SMA. Penulis juga melakukan praktik lapangan yang bertempat di
Laboratorium Mikrobiologi, LIPI, Cibinong pada tahun 2011 dengan judul
Seleksi dan Identifikasi Isolat Bakteri Proteolitik serta Uji Aktivitas Enzim
Protease yang Dihasilkan.
Organisasi yang penulis ikuti adalah himpunan mahasiswa Biokimia,
FMIPA, IPB, yakni CREBs pada tahun 2011 sebagai staf divisi CIC
(
). Selain itu, penulis merupakan anggota
dari paguyuban Karya Salemba Empat IPB pada tahun 2009 hingga 2012.
Kepanitiaan yang penulis ikuti adalah Lomba Karya Ilmiah Populer tingkat SMA
se(Indonesia dalam acara Pesta Sains FMIPA IPB pada tahun 2010; Seminar
Kesehatan Nasional dan
buku “Teknik Penelitian Biokimia” oleh Prof.
Dr. drh. Maria Bintang, MS., dan Biokimia
. Tahun 2011, penulis
%&%'%
DAFTAR TABEL ... viii
DAFTAR GAMBAR ... viii
DAFTAR LAMPIRAN ... viii
PENDAHULUAN ... 1
TINJAUAN PUSTAKA
Kunyit (
Linn.) ... 2
Temulawak (
Roxb.)... 3
(PCR) ... 3
DNA (RAPD) ... 4
BAHAN DAN METODE
Alat dan Bahan ... 5
Metode ... 5
HASIL DAN PEMBAHASAN
DNA Genom ... 7
Kuantifikasi DNA Genom………... 9
Amplikon RAPD ... 9
Matriks Kemiripan Genetik ... 11
Filogenetik ... 11
SIMPULAN DAN SARAN
Simpulan ... 12
Saran ... 13
DAFTAR PUSTAKA ... 13
%&%'%
1
Matriks kemiripan genetik enam tanaman kunyit lokal ... 11
2
Matriks kemiripan genetik lima tanaman temulawak lokal ... 11
%&%'%
1
Tanaman kunyit (
Linn.) ... 3
2
Tanaman temulawak (
Roxb.) ... 3
3
Reaksi PCR(RAPD ... 5
4
Elektroforegram pita DNA temulawak C
3(Bogor) dengan modifikasi ... 7
5
Elektroforegram pita DNA ... 8
6
Elektroforegram amplikon DNA tanaman kunyit ... 10
7
Elektroforegram amplikon DNA tanaman temulawak ... 10
8
Pohon filogenetik tanaman kunyit ... 12
9
Pohon filogenetik tanaman temulawak ... 12
%&%'%
1
Strategi penelitian ... 17
2
Bagan alir modifikasi metode isolasi DNA ... 18
3
Hasil analisis kuantitatif DNA kunyit dan temulawak ... 21
4
Data jumlah amplikon kunyit ... 22
5
Data jumlah amplikon temulawak ... 23
6
Bobot molekul DNA genom tanaman kunyit dan temulawak ... 24
Indonesia merupakan negara mega biodiversitas. Flora dan fauna yang terdapat di Indonesia sangat beragam. Iklim Indonesia yang tropis menunjang pertumbuhan berbagai organisme, termasuk tanaman obat (Indena 2002). Tanaman obat umumnya diolah secara tradisional dan dibuat menjadi jamu. Dua jenis tanaman obat yang termasuk ke dalam resep
jamu tradisional adalah kunyit dan
temulawak. Kunyit dan temulawak merupakan tanaman yang termasuk ke dalam famili Zingiberaceae atau jahe(jahean. Khasiat utama dari kedua tanaman ini adalah meningkatkan kesehatan tubuh (Pribadi 2009).
Kunyit merupakan tanaman rimpang yang mudah ditemukan. Hampir di sebagian wilayah di Indonesia terdapat tanaman kunyit. Keragaman kunyit di Indonesia sangat tinggi. Hal ini dibuktikan dengan adanya penelitian yang dilakukan oleh Jan (2011) yang mengemukakan bahwa Indonesia sekurang( kurangnya memiliki 40 jenis spesies tanaman kunyit. Berbagai penelitian yang mengkaji tanaman ini telah banyak dilakukan. Sebagian besar penelitian yang telah ada bertujuan menganalisis khasiat dari tanaman ini. Bagian yang umum digunakan adalah rimpang kunyit. Penelitian yang mengulas metabolit yang
terkandung dalam rimpang kunyit
menunjukkan bahwa senyawa kurkuminoid yang terdapat pada kunyit memiliki berbagai peranan penting dalam bidang pengobatan.
Aggarwal (2005) menyatakan bahwa
kurkuminoid memiliki kemampuan sebagai antikanker. Selain itu, kurkuminoid berperan sebagai antifungal (Indena 2002).
Tidak jauh berbeda dengan kunyit, temulawak telah banyak dieksplorasi dan diteliti terkait peranannya sebagai obat tradisional. Rimpang temulawak mengandung senyawa kurkuminoid dan xanthorizol. Kedua senyawa ini berperan sebagai antibakteri, antioksidan, antitumor, antidiabetik, antiinflamasi, antihepatotoksik, diuretika, depresan dan hipolipidemik (Raharjo & Rostiana 2003). Selain itu, temulawak dapat membantu perbaikan fungsi hati serta menurunkan kadar SGPT (! "
# $ ) dan SGOT (!
" % $ )
(Hadipoentyanti & Syahid 2001).
Kunyit dan temulawak memiliki lokasi sentra budi daya yang berada di Pulau Jawa. Lokasi sentra budi daya kunyit terdapat di Jawa Tengah (Warintek 2005). Lokasi sentra budi daya temulawak sulit ditentukan karena
umumnya ditanam secara konvensional dan hampir ditemukan di dataran sedang dan tinggi yang teduh (sekitar 5 hingga 1000 m/dpl) (BPPT 2010). Perbedaan lokasi ini
akan mempengaruhi jumlah metabolit
sekunder yang terkandung pada tanaman. Hal ini disebabkan adanya perbedaan iklim seperti curah hujan; media tanam; dan ketinggian tempat (Nurcholis 2008). Selain faktor lingkungan, kadar metabolit dalam suatu tanaman dipengaruhi oleh pola genetik tertentu (Hayakawa 2011).
Khasiat dari tanaman kunyit dan temulawak telah dibuktikan dan diakui. Namun, pengetahuan yang terkait genetika dari kedua tanaman ini belum banyak diketahui. Pengetahuan mengenai genetika tanaman penting untuk pemuliaan tanaman dan eksplorasi terhadap tanaman tersebut. Oleh sebab itu, diperlukan penelitian yang mengulas tentang genetika dari kedua tanaman rimpang ini. Langkah awal dari pembukaan pengetahuan mengenai genetika tanaman kunyit dan temulawak adalah mencari pola genetik kedua tanaman tersebut dan hubungan kekerabatan dari berbagai tanaman kunyit dan temulawak yang ditanam pada lokasi yang berbeda.
Penelitian mengenai genetika umumnya
dilakukan dengan penanda molekular.
Penanda molekular merupakan teknik yang digunakan untuk menganalisis genom suatu tanaman berbasis reaksi PCR. Penanda molekular yang umum digunakan di antaranya
(RFLP),
(AFLP),
DNA (RAPD), dan !
! & (SSR) (Santos 2000). Teknik RAPD merupakan teknik yang paling mudah digunakan dibanding teknik lainnya. Teknik RAPD tidak memerlukan enzim restriksi
untuk memotong fragmen DNA (' (
) yang akan diamplifikasi seperti pada teknik RFLP dan AFLP. Teknik RAPD juga tidak memerlukan senyawa pelabel untuk hasil amplifikasi. Selain itu, biaya yang diperlukan tidak terlalu besar, tidak memerlukan informasi tentang genom yang akan dianalisis dan dapat menghasilkan polimorfisme DNA yang banyak karena primer yang digunakan bersifat acak (NCBI 2011).
OPD (11(15) serta menganalisis hubungan kekerabatan antar tanaman kunyit dan antar
tanaman temulawak. Sebelumnya telah
dilakukan amplifikasi tanaman kunyit dan temulawak dengan primer OPA(OPD 01(05 (Utami 2012), 06(10 (Prahaditya 2013) dan 16(20 (Meryalita 2012). Pemilihan primer OPA hingga OPD didasarkan pada penelitian
Jan (2011) yang berhasil
mengamplifikasi tanaman kunyit lokal Pakistan dengan primer tersebut. Tanaman kunyit yang digunakan berasal dari Bogor,
Wonogiri, Karanganyar, Sukabumi dan
Ngawi. Temulawak yang digunakan berasal dari Bogor, Wonogiri, Karanganyar, Sragen
dan Sukabumi. seluruh tanaman yang
digunakan ditanam di kebun percobaan Pusat Studi Biofarnaka. Hipotesis dari penelitian ini adalah pola keragaman genetik tanaman kunyit dan temulawak yang berasal dari berbagai daerah dapat dianalisis dengan RAPD dan dapat ditemukan hubungan
kekerabatannya. Pola genetik dapat
dimanfaatkan untuk mencari hubungan
genetik melalui konstruksi suatu pohon filogenetik. Selain itu, pola genetik yang diperoleh dapat dijadikan sebagai dasar untuk penelusuran asal suatu tanaman kunyit dan temulawak dengan marka ini.
( ) *
Klasifikasi kunyit secara taksonomi meliputi divisi, kelas, ordo, famili (keluarga), genus dan spesies. Kunyit termasuk ke dalam
divisi Spermatophyta dan subdivisi
Angiospermae. Kunyit berada dalam kelas
Monocotyledonaeae. Kunyit berordo
Zingiberales. Kunyit berasal dari keluarga Zingiberaceae. Genus dari tanaman rimpang ini adalah . Spesies kunyit terdiri
dari dan
(Akram 2010).
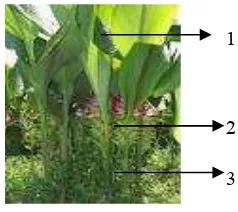
Tanaman kunyit (Gambar 1) tumbuh dengan tinggi mencapai 40(100 cm. Tanaman ini memiliki batang semu, berbatang bulat, tegak, dan membentuk rimpang. Batang kunyit berwarna hijau kekuningan dan disusun oleh pelepah daun. Daun tanaman ini tunggal, berbentuk bulat telur memanjang dengan ukuran 10(40 cm dengan lebar 8(12.5 cm. Tulang daun menyirip dengan warna hijau pucat. Bagian ujung dan pangkal daun meruncing. Tepi daun rata. Bunga kunyit majemuk, berambut dan bersisik dari pucuk hingga batang semu. Mahkota bunga kunyit
berukuran 3 cm dan lebar 1.5 cm. Mahkota bunga berwarna putih atau kekuningan. Kulit luar rimpang berwarna jingga kecoklatan.
Daging buah berwarna merah jingga
kekuningan (Rahardjo & Rostiana 2005). Kunyit ditemukan di Asia Selatan dan Asia Tenggara. Beberapa spesies tanaman ini ditemukan di Cina, Australia, dan selatan Pasifik. Keragaman kunyit yang tinggi ditemukan pada dua negara, yakni India dan Thailand. Negara lain seperti Burma, Bangladesh, Indonesia dan Vietnam sekurang( kurangnya memiliki 40 spesies tanaman kunyit (Jan . 2011). Tanaman kunyit juga ditemukan di daerah Kasur, Sahiwal dan Okara, Punjab dan Bannu, daerah Pubbi dan Haripur di provinsi Khyber Pakhtunkhwa, Pakistan (Shinwari 2010). Kunyit di Indonesia dapat ditemukan dengan mudah di Jawa Timur dan Jawa Barat (Rahardjo & Rostiana 2005).
Kunyit mengandung berbagai senyawa bioaktif, di antaranya kurkuminoid, berbagai minyak volatil, flavonoid, karbohidrat, protein dan resin (Akram 2010). Kurkuminoid kunyit terdiri atas tiga bentuk isomer, yakni demetoksi kurkumin, bisdemetoksi kurkumin dan kurkumin. Minyak volatil kunyit terdiri atas tueron, atlanton, dan zingiberon (Araujo & Leon 2001).
Tanaman kunyit telah banyak
dimanfaatkan oleh manusia. Akar kunyit
dapat dijadikan sebagai bubuk yang
digunakan untuk bahan pewarna, termasuk untuk obat. Kunyit memiliki peranan penting dalam sektor industri, yakni sebagai pengganti pewarna sintetik (Rahardjo & Rostiana 2005). Selain itu, minyak kunyit dapat berperan
sebagai antifungal, dan
. Senyawa bioaktif yang memiliki ketiga fungsi tersebut adalah karminatif (Lee 2006). Selain karminatif, minyak kunyit mengandung beberapa senyawa monoterpen dan seskuiterpen lain seperti zingiberen, arturmeron dan turmeron (Rahardjo & Rostiana 2005).
Kunyit memiliki senyawa kurkumin yang sangat bermanfaat. Kurkumin memiliki kemampuan sebagai antikanker kolon (Reddy & Rao 2002) dan payudara (Ramachandaran 2002). Kurkumin dapat berperan sebagai
agen kemoterapi untuk kanker kolon
(Chauhan 2002), kanker payudara
(Somasundaram 2002) dan kanker
prostat (Dorai 2001). Selain sebagai antikanker, kurkumin juga berperan dalam
menurunkan kadar kolesterol darah,
menghambat agregasi keping darah, menghambat proliferasi sel otot polos, menghambat infraksi miokardial, menekan diabetes dan menstimulasi regenerasi otot. Bahkan, kurkumin dapat bertindak sebagai
inhibitor * +
$ , (HIV(1) integrase (Aggarwal .
2005).
Gambar 1 Tanaman kunyit (
Linn.) meliputi daun (1); dan batang (2) (foto pribadi)
+'(&%,%-Tanaman temulawak tersebar di daerah Asia Tenggara. Negara tempat ditemukannya
temulawak meliputi Cina, IndoCina,
Bardabos, India, Jepang, Korea, Amerika
Serikat dan sebagian negara Eropa.
Temulawak juga dapat ditemui dengan mudah
di Indonesia (BPPT 2010). Wilayah
pengembangan temulawak di Indonesia
meliputi 13 provinsi, yakni Sumatera Utara, Riau, Jambi, Daerah Khusus Ibu kota Jakarta, Jawa Barat, Jawa Tengah, Jawa Timur,
Daerah Istimewa Yogyakarta, Bali,
Kalimantan Barat, Kalimantan Timur,
Sulawesi Utara dan Sulawesi Selatan (Rahardjo 2010).
Klasifikasi temulawak (taksonomi)
meliputi divisi, subdivisi, kelas, ordo, famili, genus dan spesies. Temulawak termasuk ke dalam divisi Spermatophyta. Berada dalam
subdivisi Angiospermae. Temulawak
menempati kelas Monocotyledonae.
Temulawak memiliki famili Zingiberaceae
genus C dan spesies
Roxb (BPPT 2010).
Tanaman temulawak (Gambar 2)
memiliki tinggi mencapai 1 meter. Tanaman ini berbatang semu dengan warna hijau atau coklat gelap. Akar rimpangnya terbentuk sempurna dengan cabang yang kuat dan warna hijau gelap. Daunnya tumbuh pada bagian batang sebanyak dua hingga sembilan helai tiap batang. Daun temulawak berbentuk bundar memanjang dan berwarna hijau atau coklat keunguan terang hingga gelap. Panjang
daun temulawak mencapai 31(84 cm dengan lebar antara 10(18 meter. Tanaman temulawak memiliki perbungaan lateral. Tangkai bunga temulawak ramping dan bersisik. Panjang tangkai bunga mencapai 9(23 cm dengan lebar 4(6 cm. Kelopak bunga sepanjang 8(13 mm, berwarna putih, berbulu, berbentuk tabung dengan panjang mencapai 4.5 cm secara keseluruhan. Warna helaian bunga temulawak adalah putih dengan bagian ujung berwarna merah, berbentuk bundar, dan panjang mencapai 1.25(2 cm dan lebar 1 cm (BPPT 2010).
Kandungan senyawa bioaktif utama
temulawak adalah kurkumin. Namun, berbeda halnya dengan kunyit. Temulawak hanya memiliki dua bentuk isomer kurkumin, yakni demetoksikurkumin dan kurkumin. Selain itu, temulawak pun mengandung minyak atsiri, pati dan protein. Minyak atsiri dari temulawak meliputi felandren, kamfer, borneol, sineal dan xantorizol (Rahardjo & Rostiana 2003).
Temulawak sering dimanfaatkan sebagai obat tradisional. Berdasarkan Hadipoentyanti dan Syahid (2001), masyarakat telah banyak menggunakan rimpang temulawak sebagai bahan baku pembuatan obat untuk penyakit liver. Secara klinis, temulawak membantu perbaikan fungsi hati, serta menurunkan kadar SGPT dan SGOT. Selain itu, temulawak dapat dijadikan sebagai pewarna alami, minuman
yang bermanfaat dalam meningkatkan
imunitas tubuh. Temulawak berperan sebagai antimikrob (Wibowo 2012), antitumor, antidiabetik, antioksidan, antiinflamasi, antihepatotoksik, diuretika, depresan, dan hipolipodemik (Purnomowati 2008).
Gambar 2 Tanaman temulawak (
Roxb.) meliputi daun (1); bunga (2); dan batang (3) (foto pribadi)
(PCR) adalah metode molekuler yang dimanfaatkan
untuk menggandakan DNA secara #
Penggandaan DNA ini dilakukan dengan 1
2
1
2
menggunakan enzim dan sepasang primer. Primer yang digunakan bersifat spesifik terhadap DNA target. Dengan metode PCR, penggandaan DNA dapat dilakukan dengan lebih cepat. Hal ini termasuk salah satu keuntungan yang ditawarkan dari metode PCR. Konsep metode PCR awalnya diajukan oleh Khorana pada tahun 1970an. Penerapan teknik PCR sendiri dilakukan pertama kali oleh Kary Mullis pada tahun 1983 (Bartlett & Stirling 2010).
Secara umum, PCR melibatkan beberapa tahapan reaksi. Tahapan reaksi tersebut meliputi tahap denaturasi, tahap
dan tahap elongasi. Tahap denaturasi merupakan tahap pemisahan utas ganda DNA menjadi utas tunggal pada suhu tinggi. Suhu yang umum digunakan berkisar antara 940 C hingga 960 C. Utas tunggal tersebut kemudian akan menjadi DNA cetakan untuk proses
transkripsi. Tahap adalah tahap
penempelan primer pada bagian DNA cetakan. Primer akan menempel secara spesifik pada fragmen DNA cetakan, yakni menempel pada fragmen DNA cetakan yang komplemen dengan urutan basa primer. Tahap ini umumnya dilakukan pada suhu antara 450 C hingga 600 C. Primer universal yang umum digunakan adalah 20F dan 1500R. Tahap elongasi adalah tahap pemanjangan primer menjadi utas baru DNA dengan bantuan enzim DNA polimerase (Sambrook & Russel 2001). DNA polimerase umumnya bersifat tahan panas sehingga dapat digunakan dengan baik untuk PCR. Umumnya, enzim DNA polimerase yang tahan panas diisolasi dari bakteri termofilik atau hipertermofilik. Contoh dari enzim DNA polimerase yang sering digunakan adalah Taq polimerase (Carroll & Casimir 2010). Taq polimerase diisolasi dari
$ & yang termasuk ke dalam golongan arkea termofilik (Brown 2007).
Prinsip dasar PCR sama seperti
mekanisme replikasi DNA yang terjadi di dalam sel. Saat awal proses PCR, utas ganda DNA diurai menjadi utas tunggal. Kedua utas tunggal yang terbentuk akan menjadi cetakan untuk pembentukan DNA baru. Selanjutnya, primer menempel pada utas tunggal DNA cetakan dan primer diperpanjang oleh enzim DNA polimerase sehingga terbentuk dua utas ganda baru DNA. Umumnya, siklus PCR terus diulang sebanyak 25 hingga 30 kali. Seiring dengan penambahan jumlah siklus PCR, jumlah DNA hasil amplifikasi akan bertambah secara logaritmik. Selanjutnya, PCR akan mengalami fase pendinginan DNA pada suhu 40C dalam waktu yang tidak
terbatas (Hofreiter 2010). Komponen
PCR meliputi DNA cetakan dengan
konsentrasi antara 1 pg hingga 1 µg, Mg2+ dengan konsentrasi 1.5 mM, dNTP dengan konsentrasi 200 mM, sepasang primer dengan konsentrasi masing(masing 1 µM, DNA polimerase sebanyak 1 hingga 5 subunit dan larutan buffer dengan pH 8.3 (Grunenwald 2010).
Selain PCR, marka molekul lain yang dapat digunakan untuk penggandaan DNA adalah hibridisasi. Teknik ini memerlukan enzim restriksi dalam pengoperasiannya. Penggunaan enzim restriksi ini diharapkan dapat mengungkapkan perbedaan pola antara fragmen DNA pada ukuran tertentu dari individu yang berbeda. Hal ini didasarkan pada adanya perbedaan sekuen DNA yang dapat disebabkan oleh mutasi titik, insersi atau delesi, translokasi, inversi dan duplikasi. Perbedaan sekuen ini, terutama yang terdapat pada situs restriksi akan menghasilkan fragmen sekuen yang berbeda dengan ukuran yang berbeda bila dipotong oleh enzim restriksi tertentu. Enzim restriksi yang umum digunakan berasal dari bakteri, seperti - RI, I, dan lainnya. Contoh dari marka molekular yang telah banyak dikenal adalah
(RFLP) (Semagn 2006).
'
(RAPD) termasuk ke dalam salah satu jenis reaksi PCR. Umumnya, pada reaksi PCR amplifikasi dilakukan pada gen yang telah diketahui. Namun, pada RAPD fragmen yang akan diamplifikasi belum diketahui dan amplifikasi tersebut bersifat acak. Saat
beroperasi, RAPD memerlukan marker.
Marker RAPD berupa fragmen DNA hasil amplifikasi yang diperoleh secara acak dengan primer tunggal yang tidak tentu. Ukuran primer yang digunakan biasanya terdiri atas 10 pasang basa (NCBI 2011).
serta 3 dan 6 akan menghasilkan produk PCR. Produk A dihasilkan dari titik antara 2 dan 5. Produk B dihasilkan dari sekuen antara titik 3 dan 6. Sekuen antara titik 1 dan 4 tidak akan menghasilkan produk. Hal ini disebabkan jarak antara kedua titik yang cukup jauh. Akibatnya, pasangan primer pada kedua titik tersebut tidak berhadapan sehingga tidak dapat dihasilkan produk. Penggunaan primer yang berbeda akan menghasilkan produk PCR yang berbeda pula (NCBI 2011).
Setelah amplifikasi, pemastian produk PCR yang mengandung fragmen yang tidak diketahui tersebut dilakukan dengan elektroforesis gel agarosa. Munculnya fragmen DNA hasil amplifikasi yang tidak diketahui dalam proses elektroforesis dipengaruhi oleh komplementaritas antara posisi sekuen primer dengan sekuen DNA cetakan. Bila sekuen primer berada pada bagian fragmen yang terlalu jauh (ujung 3’)
maka tidak akan ada fragmen yang
diproduksi. Selain itu, bila terjadi mutasi pada ruas sebelum titik komplementer pada primer maka produk PCR juga tidak akan dihasilkan (NCBI 2011).
Penggunaan RAPD memiliki berbagai keunggulan. Keunggulan tersebut mencakup segi ekonomi, yakni harga yang tidak mahal. Pengetahuan spesifik tentang sekuen DNA organisme target juga tidak diperlukan dalam
penggunaan RAPD (William 1990).
Teknik RAPD bersifat ) , yaitu dapat mengamplifikasi DNA dalam jumlah besar, menghasilkan pita dengan intensitas yang terang dan tebal, serta menghasilkan banyak fragmen. Selain itu, RAPD banyak digunakan untuk spesies bakteri. Teknik ini dapat
digunakan untuk mengidentifikasi
polimorfisme DNA dalam sekuen DNA cetakan (NCBI 2011).
Gambar 3 Reaksi PCR(RAPD (NCBI 2011)
&%* .% %/%
Peralatan yang digunakan dalam
penelitian ini meliputi peralatan gelas, neraca
analitik, mortar, pipet mikro beserta tip, mikrosentrifus 200 R, tabung Eppendorf, inkubator, lemari asam, autoklaf, pHmeter, spektrofotometer beserta kuvet, perangkat mesin elektroforesis BioRad, mesin Geldoc dan mesin PCR ESCO.
Bahan yang digunakan dalam penelitian ini antara lain daun kunyit (
Linn.) asal Bogor, Wonogiri, Karanganyar, Ngawi, dan Sukabumi; daun temulawak
( Roxb.) asal Bogor,
Wonogiri, Karanganyar, Sragen dan
Sukabumi yang ditanam di Kebun Percobaan Pusat Studi Biofarmaka ; nitrogen cair; larutan buffer ekstraksi
yang mengandung 2% CTAB (
$ . ) (b/v), 1.4 M NaCl,
mM EDTA, 100 mM Tris(HCl pH 8; polivinil pirolidon (PVP); dan 2% 2( merkaptoetanol (v/v). Bahan lain yang diperlukan dalam penelitian ini adalah kloroform, isoamilalkohol, larutan etanol 76%, buffer TE (10 mM Tris(HCl pH 8 dan 0.1 mM EDTA pH 8), akuabides
/ , ) alkohol
teknis, akuades, gel agarosa, larutan buffer TBE (Tris(Borat(EDTA), ethidium bromida 0.5 µg/mL, marker DNA ʎ, DreamTaqTM
DNA , MgCl2, dan primer OPA,
OPB, OPC, OPD 11(15.
+* .+
+* .+ 0 &%0 *+1' . 2 -%0 /%1'%,%* !""3
. 2 -%0 #. Daun temulawak C3
(Bogor) ditimbang sebanyak 1 gram dan
dimasukkan ke dalam mortar. Daun
ditambahkan dengan PVP dan nitrogen cair lalu digerus hingga menjadi tepung. Bufer ekstraksi hangat ditambahkan sebanyak 9.8 mL dan 2(merkaptoetanol sebanyak 0.2 mL. Sampel diinkubasi selama 1 jam pada suhu 550 C dan kecepatan 150 rpm. Selanjutnya, sampel dipindahkan ke dalam 9 tabung
Eppendorf masing(masing 1 mL dan
ditambahkan kloroform:isoamil alkohol (24:1) dengan volume yang sama. Sampel disentrifugasi pada kecepatan 1000 g selama 5 menit. Ekstraksi dengan kloroform:isoamil alkohol dilakukan sebanyak dua kali. Aliquot dipindahkan ke dalam tabung Eppendorf baru dan ditambahkan dengan isopropanol dingin sebanyak 2/3 volume. Campuran diinversi sebanyak 10 kali dan disentrifugasi pada kecepatan 12000 g selama 20 menit. Setelah disentrifugasi, pelet dikoleksi dan supernatan dibuang. Satu tabung disimpan pada suhu (200
DNA cetakan
Reaksi PCR
C dan tabung lainnya digunakan untuk modifikasi selanjutnya.
. 2 -%0 ! Pelet yang diperoleh pada modifikasi 1 dicuci dengan etanol 76% dan disentrifugasi pada kecepatan 14000 g selama 10 menit. Pelet dikoleksi dan disimpan pada suhu (200 C.
. 2 -%0 $ Pelet yang diperoleh pada modifikasi 1 dicuci dengan etanol 76% dan disentrifugasi pada kecepatan 14000 g selama 10 menit. Pelet ditambahkan dengan 50 µL TE. Campuran diinversi dan ditambahkan dengan RNase A dengan konsentrasi akhir 10 µg/mL. Campuran diinkubasi pada suhu 370 C selama 30 menit dan disentrifugasi pada kecepatan 7500 g selama 5 menit. Pelet dikoleksi dan disimpan pada suhu (200 C.
. 2 -%0 4 Sebelum ekstraksi dengan
kloroform:isoamil alkohol, dilakukan
penambahan proteinase K dengan konsentrasi akhir 10 µg/mL. Selanjutnya diinkubasi pada suhu 370 C selama 30 menit dan 650 C selama 20 menit. Pelet yang diperoleh pada modifikasi 1 dicuci dengan larutan pencuci (ammonium asetat dan etanol 76%) dan disentrifugasi pada kecepatan 14000 g selama 10 menit. Pelet ditambahkan dengan 50 µL TE. Campuran diinversi dan ditambahkan dengan RNase A dengan konsentrasi akhir 10 µg/mL. Campuran diinkubasi pada suhu 370 C selama 30 menit dan sidentrifugasi pada kecepatan 7500 g selama 5 menit. Pelet dikoleksi dan disimpan pada suhu (200 C.
. 2 -%0 5 Seperti modifikasi 4 tetapi pelet yang diperoleh dari modifikasi 1 dicuci dengan etanol 76%.
. 2 -%0 6 Seperti modifikasi 5 tetapi penambahan proteinase K dilakukan setelah penambahan TE.
. 2 -%0 7 Seperti modifikasi 6 tetapi pelet yang diperoleh dari modifikasi 1 dicuci dengan larutan pencuci (ammonium asetat dan etanol 76%).
. 2 -%0 8 Seperti modifikasi 3 tetapi pelet yang diperoleh dari modifikasi 1 dicuci dengan larutan pencuci (ammonium asetat dan etanol 76%).
. 2 -%0 3 Pelet yang diperoleh pada modifikasi 1 dicuci dengan larutan pencuci (ammonium asetat dan etanol 76%) dan disentrifugasi pada kecepatan 14000 g selama 10 menit. Pelet dikoleksi dan disimpan pada suhu (200 C.
%& 0 0 (% * *%* 2 0 9* #334
Sebanyak 3.5 OL DNA sampel
ditambahkan dengan ) hingga
350 OL. Campuran diinversi hingga homogen. Nilai serapan sampel diukur pada panjang gelombang 230 nm, 260 nm dan 280 nm. Selanjutnya, nilai serapan sampel pada panjang gelombang 260 nm dihitung rasionya terhadap nilai serapan panjang gelombang 230 nm dan 280 nm. Nilai rasio A260/280 dan A260/230 yang berkisar antara 1.6(1.8 dan 2.0(2.2 dianggap telah murni.
+%-0 && %' #33"
Campuran reaksi PCR untuk amplifikasi mengandung 1x buffer PCR, 1.5 mM MgCl2,
200 OM masing(masing dNTP, 0.2 OM primer OP, 1 unit Taq DNA polimerase, dan 50 ng
DNA cetakan. Amplifikasi dilakukan
sebanyak 45 siklus. Satu siklus untuk pradenaturasi pada suhu 920 C selama 2 menit, denaturasi pada suhu 920 C selama 3 menit dan 30 detik, penempelan primer pada suhu 350 C selama 1 menit dan pemanjangan primer pada suhu 720 C selama 1 menit. Sebanyak 44 siklus untuk denaturasi pada suhu 920 C selama 1 menit, penempelan primer pada suhu 350 C selama 1 menit, pemanjangan primer pada suhu 720 C selama 2 menit dan pemanjangan akhir pada suhu 720 C selama 7 menit. Setelah seluruh siklus tercapai suhu dijaga pada 40 C dengan waktu yang tidak dibatasi.
: 0(%& 0%0 .% + + *(% * &+-(& %' 1 - ; (00+& #383
Visualisasi DNA dilakukan dengan
elektroforesis gel agarosa. Sebanyak 0.51 gram agarosa ditimbang. Agarosa dilarutkan dalam 30 mL buffer TBE 0.5x. Agarosa dipanaskan hingga mendidih. Larutan agarosa dibiarkan hingga hangat lalu ditambahkan dengan 2 OL ethidium bromida. Larutan diaduk kemudian dituang pada cetakan gel. Gel dibiarkan hingga memadat kemudian sisir pencetak sumur diangkat. Elektroforesis dilakukan dengan arus 80 V selama 60 menit. DNA diamati dengan Geldoc. Konsentrasi DNA ditentukan dengan membandingkan tingkat perpendaran DNA dengan marker DNA ʎ.
%& 0 0 %0 & &+-*1 2 1+0 0 (&2 !""!
Fragmen DNA yang terlihat saat
perangkat lunak NTSYS koefisien kemiripan genetik filogenetik.
+
Tahap awal analisis m dengan isolasi DNA gen yang telah diisolasi akan DNA cetakan untuk PCR( tanaman kunyit dan tem dengan buffer CTAB (
. ). Metode yang d
pada Doyle & Doyle (1 merupakan metode isola tahapan yang relatif mudah dan sampel yang dibutuh
(Tibbits 2006).
Beberapa modifikasi m tanaman kunyit dan tem sebelum mengisolasi DN tersebut dengan metode t ini dilakukan agar dapat DNA yang baik dengan sedikit. Modifikasi ini metode isolasi daun " #
dioptimasi untuk dianal dengan PCR(RAPD (Phar ini dilakukan karena belum yang efektif untuk memp kedua tanaman rimpang in dilakukan meliputi pe Proteinase K dan pemilih DNA. Penambahan enz dilakukan pada tahap awal ekstraksi. Larutan DNA di pencuci (ammonium asetat 76%) dan etanol 76%.
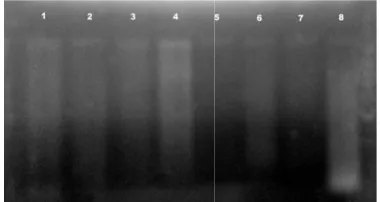
Hasil elektroforesis pita yang cukup tebal metode terbaik, yaitu modi 6 (Gambar 4). Modif menunjukkan pita yang memiliki banyak terbentuk dapat disebabka RNase yang kurang efisien dipengaruhi oleh keber Tahap yang penting kloroform dari sampel DNA adalah saat pemind debris sel daun. Pengam lapisan atas yang kuran mengikutsertakan klorofor lapisan tengah. Klorofo bersama aliquot akan RNase bahkan menghilang
TSYS adalah matriks genetik sampel dan pohon
+ '
isis molekuler dilakukan genom. DNA genom akan digunakan sebagai (RAPD. Isolasi DNA n temulawak dilakukan
B ( $
ang digunakan mengacu yle (1990). Metode ini isolasi yang memiliki mudah dan cepat, praktis ibutuhkan tidak banyak
kasi metode isolasi DNA n temulawak dilakukan i DNA kedua tanaman tode terpilih. Modifikasi dapat diperoleh kualitas engan kontaminan yang ini didasarkan pada
# sp. yang telah dianalisis lebih lanjut (Pharmawati 2009). Hal belum ada metode isolasi memperoleh DNA dari ang ini. Modifikasi yang
i penambahan enzim
emilihan larutan pencuci enzim Proteinase K awal ekstraksi dan akhir NA dicuci dengan larutan asetat 10 mM dan etanol
resis menunjukkan dua ebal dengan modifikasi modifikasi metode 5 dan odifikasi metode 5 yang tebal meskipun
. ! yang
ebabkan oleh kerja dari efisien. Aktivitas RNase keberadaan kloroform. ing dalam pemisahan pel yang mengandung pemindahan aliquot dari ngambilan aliquot pada kurang hati(hati dapat oroform yang berada di loroform yang terambil kan menghambat kerja
hilangkan RNAse A.
Gambar 4 Elektroforegr temulawak C3
modifikasi meto metode 3 (lajur 2 3), metode 5 (la (lajur 5), meto metode 8 (lajur (lajur 8)
Berbeda dengan pita pa yang terbentuk pada lajur kurang tebal. Meskipun dem terbentuk pun lebih tipis d lajur 4 (modifikasi 5). Seca yang dilakukan pada mod adalah sama. Namun, ter dalam penambahan proteina proteinase K dilakukan p isolasi (modifikasi 5) dan 6).
! terbanyak ditun
pada lajur 8 (metode 9). T pada lajur 8, yakni pita b dan pita bagian bawah (R bawah terlihat dengan san tidak ada penambahan RN 9. Pita pada lajur 1 pun yang cukup tebal dan terd RNA bagian bawah. H pelet dikoleksi setelah p etanol 76%.
Penambahan proteinas
memiliki pengaruh yang
Penambahan proteinase sebelum ekstraksi denga isoamil alkohol (modifikas setelah penambahan bufer dan 7). Modifikasi 4 dan 5 yang lebih tebal diban modifikasi 6 dan 7. Selain dan 8 yang tidak ditam proteinase K menunjukkan tipis d ibanding dengan m perlakuan proteinase K.
Berdasarkan uraian di paling efektif untuk isolasi adalah modifikasi metode banyak dihasilkan deng
foregram pita DNA
3 (Bogor) dengan
metode 2 (lajur 1), lajur 2), metode 4 (lajur 5 (lajur 4), metode 6 metode 7 (lajur 6), (lajur 7), dan metode 9
ita pada lajur 4, pita lajur 5 (modifikasi 6)
n demikian, yang
tipis dibanding dengan . Secara umum, tahapan modifikasi 5 dan 6 n, terdapat perbedaan oteinase K. Penambahan kan pada bagian awal dan akhir (modifikasi
ditunjukkan oleh pita ). Terdapat dua pita pita bagian atas (DNA) ah (RNA). Pita bagian n sangat jelas karena RNase pada metode pun memiliki n terdapat kontaminan
Hal ini disebabkan lah pencucian dengan
teinase K ternyata yang cukup besar. K dilakukan dengan kloroform : difikasi 4 dan 5) dan bufer TE (modifikasi 6 5 menghasilkan pita
dibanding dengan
Selain itu, modifikasi 3 ditambahkan dengan kkan pita yang lebih an metode yang diberi
ian di atas, metode yang isolasi daun temulawak tode 5. DNA yang lebih
proteinase K sebelum penambahan kloroform : isoamil alkohol dan mencuci pelet dengan
etanol 76%. Kontaminasi RNA dapat
dihilangkan dengan penambahan RNase A. Tahapan isolasi DNA meliputi pelisisan sel, pemisahan DNA dengan makromolekul lain dan pemekatan DNA. Pelisisan sel dilakukan dengan dua cara, yakni pelisisan secara mekanik dan secara kimia. Lisis sel
secara mekanik dilakukan dengan
penggerusan. Tekstur daun yang licin umumnya akan menyulitkan penggerusan. Oleh sebab itu, digunakan nitrogen cair untuk mempermudah penggerusan daun. Nitrogen cair memiliki suhu yang sangat rendah. Dengan kondisi seperti ini, daun yang ditambahkan nitrogen cair akan menjadi beku. Selain nitrogen cair, ditambahkan PVP saat penggerusan. Penambahan PVP bertujuan mencegah kerusakan DNA akibat oksidasi dan
menarik senyawa fenolik pada daun
(Padmalatha & Prasad 2006). Lisis sel secara kimia dilakukan dengan menggunakan buffer ekstraksi yang mengandung CTAB. Buffer CTAB sangat baik digunakan untuk tanaman yang memiliki kandungan polisakarida yang tinggi (Pharmawati 2009). Selain itu, buffer CTAB dapat mendegradasi senyawa metabolit sekunder seperti tanin dan senyawa fenolik. Tiga molekul tersebut merupakan kontaminan yang dapat mempengaruhi kualitas hasil isolasi. Kandungan kontaminan yang tinggi dapat menurunkan kualitas DNA sehingga timbul saat elektroforesis. Penambahan buffer CTAB diikuti dengan penambahan larutan 2(merkaptoetanol. Larutan ini berperan dalam penghilangan polifenol (Padmalatha & Prasad 2006).
Tahap selanjutnya adalah pemisahan DNA dengan molekul lain, seperti protein, lipid dan sisa polisakarida. Ekstraksi protein dilakukan dengan penambahan campuran kloroform : isoamilkohol (24:1). Setelah penambahan senyawa tersebut akan terbentuk 3 lapisan. Lapisan bawah merupakan debris sel, lapisan tengah berupa gumpalan yang mengandung protein sedangkan lapisan atas berisi DNA, RNA dan protein berukuran kecil. Sisa protein yang terdapat pada lapisan atas didegradasi dengan proteinase K. Enzim proteinase K aktif pada suhu 370C dan inaktif pada suhu 650C atau lebih (Tibbits 2006).
Tahap akhir isolasi DNA adalah
pemekatan DNA. Endapan DNA dipekatkan dengan isopropanol. Semakin lama waktu inkubasi dengan isopropanol, maka jumlah DNA yang didapat akan semakin besar. Sisa larutan dihilangkan dengan pencucian
menggunakan etanol 76%. Kemudian
dilakukan pemisahan DNA dan RNA dengan penambahan enzim RNAse. Enzim RNAse berperan dalam mendegradasi RNA (Tibbits
. 2006).
Keberhasilan metode dalam mengisolasi
DNA tanaman kunyit dan temulawak
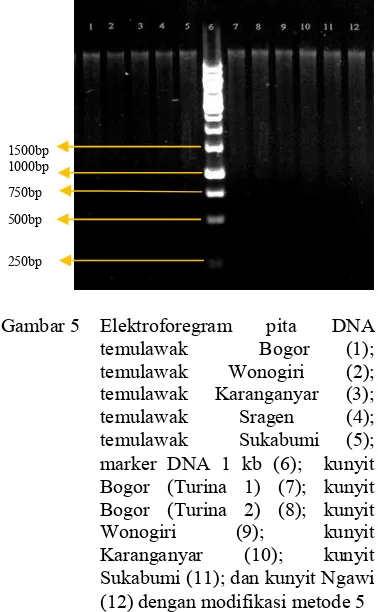
ditunjukkan dengan munculnya pita DNA saat elektroforesis. Analisis kualitatif dilakukan dengan elektroforesis gel agarosa 0.8 % dalam buffer TBE 0.5x. Hasil analisis kualitatif tanaman kunyit dan temulawak ditunjukkan oleh Gambar 5. Terdapat 12 lajur yang terdiri atas lima tanaman temulawak, DNA marker dan enam tanaman kunyit. Tanaman yang diisolasi merupakan tanaman yang unggul secara metabolik, yakni memiliki kandungan kurkumin atau dan xantorizol yang tinggi (Rahardjo 2010; Syukur 2006).
Sampel yang digunakan tidak berasal dari daerah asli tanaman tersebut. Daun yang diisolasi berasal dari Kebun Percobaan Pusat Studi Biofarmaka. Menurut Campbell
(2002), DNA genom suatu tanaman berbeda dengan tanaman lain yang hidup pada daerah yang berbeda. Hal ini merupakan bentuk adaptasi dari tanaman terhadap lingkungan. Susunan genom tersebut akan diwariskan kepada keturunannya dan bersifat tetap (Campbell 2002).
Gambar 5 Elektroforegram pita DNA
temulawak Bogor (1);
temulawak Wonogiri (2);
temulawak Karanganyar (3);
temulawak Sragen (4);
temulawak Sukabumi (5);
marker DNA 1 kb (6); kunyit Bogor (Turina 1) (7); kunyit Bogor (Turina 2) (8); kunyit
Wonogiri (9); kunyit
Karanganyar (10); kunyit
Sukabumi (11); dan kunyit Ngawi (12) dengan modifikasi metode 5
1500bp 1000bp 750bp 500bp
Secara umum, pita yang dihasilkan masih memiliki pada bagian bawah. Bentuk
pita DNA yang dihasilkan berupa “ ”.
Hal ini menunjukkan adanya kontaminan polisakarida yang terbawa saat isolasi (Pharmawati 2009). Namun, pita yang dihasilkan berjumlah 1 buah. Hal ini menandakan DNA yang dihasilkan cukup baik. Ukuran DNA temulawak yang diperoleh berkisar antara 15333 bp (( ) hingga 15500 bp. Ukuran DNA kunyit yang dihasilkan berkisar antara 15333 bp hingga 16000 bp. Marker DNA yang digunakan
berasal dari $ ! berukuran 1 kb
dengan 14 fragmen DNA. Fragmen DNA marker berukuran 10000 bp, 8000 bp, 6000 bp, 5000 bp, 4000 bp, 3500 bp, 3000 bp, 2500 bp, 2000 bp, 1500 bp, 1000 bp, 750 bp, 500 bp dan 250 bp.
(% * 2 -%0 + '
Analisis kuantitatif DNA dilakukan dengan metode spektrofotometri. Larutan DNA diukur nilai serapannya pada tiga panjang gelombang, yakni 230 nm, 260 nm, dan 280 nm. Penyerapan sinar UV oleh DNA disebabkan adanya ikatan rangkap pada basa nitrogen DNA. Panjang gelombang untuk pengukuran DNA adalah 260 nm. Panjang gelombang 230 nm digunakan untuk pengukuran protein, polisakarida dan sebagian DNA. Panjang gelombang 280 nm digunakan untuk pengukuran RNA dan sebagian DNA (Brescia 2012).
Nilai kemurnian DNA kunyit hasil isolasi berkisar antara 1.093 hingga 1.417 (Lampiran 3). Rerata nilai kemurnian DNA kunyit adalah 1.242. Nilai kemurnian DNA kunyit tertinggi diperoleh dari tanaman kunyit asal Sukabumi. Nilai kemurnian DNA kunyit terendah diperoleh dari tanaman kunyit asal Bogor, yakni Turina 2. Konsentrasi DNA kunyit yang diperoleh berkisar antara 80 ng/μL hingga 1625 ng/μL.
Nilai kemurnian DNA tanaman temulawak berada pada rentang 1.044 hingga 1.544. Rerata nilai kemurnian DNA temulawak
adalah 1.326. Nilai kemurnian DNA
temulawak tertinggi diperoleh dari tanaman temulawak asal Wonogiri. Nilai kemurnian DNA temulawak terendah diperoleh dari tanaman temulawak asal Bogor. Konsentrasi DNA temulawak terkecil diperoleh dari tanaman kunyit asal Sragen, yaitu 525 ng/μL.
Konsentrasi DNA temulawak terbesar
diperoleh dari tanaman temulawak asal Wonogiri, yakni 965 ng/μL.
Nilai kemurnian DNA tanaman kunyit dan temulawak yang telah diisolasi hanya mencapai 1.544. Nilai kemurnian ini masih berada di bawah rentang nilai DNA murni, yakni 1.8 hingga 2.0 (Hoisington 1994). Hal ini menunjukkan bahwa DNA hasil isolasi
kedua tanaman masih mengandung
kontaminan protein. Kontaminan protein dapat terbawa saat pengambilan aliquot. Kemurnian DNA hasil isolasi dari tanaman kunyit dan temulawak yang tidak begitu tinggi tidak mempengaruhi analisis molekuler selanjutnya dengan RAPD. Hal ini disebabkan RAPD toleran terhadap tingkat kemurnian DNA (Prana & Hartati 2003). Nilai kemurnian DNA temulawak lebih tinggi dibanding dengan DNA kunyit. Hal ini menunjukkan bahwa kualitas DNA hasil isolasi dipengaruhi oleh jenis tanaman dan kandungan senyawa dalam tanaman tersebut. Hal ini berhubungan dengan komponen dinding sel tiap tanaman (Pharmawati 2009).
'<&
-Amplifikasi DNA kunyit dan temulawak dilakukan dengan teknik RAPD. Teknik RAPD membutuhkan primer untuk memulai perbanyakan salinan DNA. Primer yang digunakan untuk RAPD terdiri atas banyak seri. Primer yang digunakan dalam penelitian ini adalah primer seri OPA (11, 12, 13, 14, 15); OPB (11, 12, 13, 14, 15); OPC (11, 12, 13, 14, 15); dan OPD (11, 12, 13, 14, 15). Pemilihan primer seri ini didasarkan pada
penelitian Jan (2011) yang
mengamplifikasi kunyit lokal Pakistan dengan keempat seri primer ini dan memperoleh jumlah pita DNA yang cukup beragam.
Analisis hasil amplifikasi DNA dilakukan dengan elektroforesis gel agarosa. Konsentrasi gel yang digunakan adalah 1.7% dalam buffer TBE 0.5x. Konsentrasi gel 1.7% dipilih
karena kemampuan gel yang dapat
memisahkan fragmen DNA yang berukuran 100 bp hingga 4000 bp. Grattapaglia
(1992) mengemukakan bahwa ukuran
amplikon tanaman yang dihasilkan dengan menggunakan primer acak berkisar antara 200 pb hingga 3500 pb. Penggunaan gel dengan konsentrasi tersebut diharapkan dapat memisahkan fragmen amplikon dengan baik.
Amplikon yang dianalisis saat
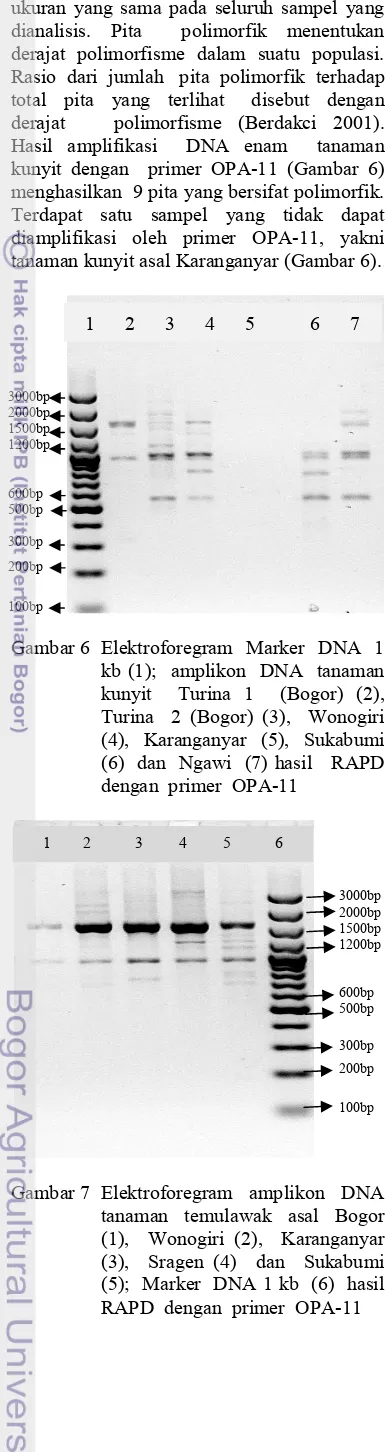
ukuran yang sama pada seluruh sampel yang dianalisis. Pita polimorfik menentukan derajat polimorfisme dalam suatu populasi. Rasio dari jumlah pita polimorfik terhadap total pita yang terlihat disebut dengan derajat polimorfisme (Berdakci 2001). Hasil amplifikasi DNA enam tanaman kunyit dengan primer OPA(11 (Gambar 6) menghasilkan 9 pita yang bersifat polimorfik. Terdapat satu sampel yang tidak dapat diamplifikasi oleh primer OPA(11, yakni tanaman kunyit asal Karanganyar (Gambar 6).
Gambar 6 Elektroforegram Marker DNA 1 kb (1); amplikon DNA tanaman kunyit Turina 1 (Bogor) (2), Turina 2 (Bogor) (3), Wonogiri (4), Karanganyar (5), Sukabumi (6) dan Ngawi (7) hasil RAPD dengan primer OPA(11
Gambar 7 Elektroforegram amplikon DNA tanaman temulawak asal Bogor (1), Wonogiri (2), Karanganyar (3), Sragen (4) dan Sukabumi (5); Marker DNA 1 kb (6) hasil RAPD dengan primer OPA(11
Amplifikasi DNA kunyit dengan 20 primer acak menghasilkan 131 lokus (Lampiran 4). Secara umum, amplikon yang tampak sudah menunjukkan polimorfisme. Polimorfisme merupakan variasi yang terdapat dalam sekuen DNA. Hal inilah yang mendasari adanya keragaman dalam suatu populasi (NCBI 2011). Munculnya polimorfisme saat analisis disebabkan oleh ketidakcocokan sisi primer, adanya penampakan sisi primer baru, dan perbedaan panjang daerah amplifikasi di antara sisi primer (Berdakci 2001).
Amplifikasi DNA lima tanaman
temulawak dengan primer OPA(11 (Gambar 7) menghasilkan 12 pita. Satu pita bersifat monomorfik dan sebelas pita lainnya bersifat
polimorfik. Primer OPA(11 dapat
mengamplifikasi DNA sampel yang
dianalisis. Amplifikasi DNA lima tanaman
temulawak dengan 20 primer acak
menghasilkan 132 lokus. Hanya 16 primer yang dapat mengamplifikasi DNA lima
tanaman temulawak yang digunakan
(Lampiran 5).
Jumlah amplikon yang dihasilkan tiap primer berbeda. Tiap primer menghasilkan 4 hingga 12 lokus untuk enam tanaman kunyit (Lampiran 2). Jumlah lokus yang dihasilkan dari lima tanaman temulawak berkisar antara 3 hingga 15 lokus (Lampiran 4). Umumnya, amplifikasi dengan primer acak RAPD dapat menghasilkan 5 hingga 20 lokus untuk setiap primer (Grattapaglia . 1992). Menurut
Campbell (2002), lokus merupakan
lokasi spesifik suatu gen yang berada di sepanjang kromosom. Lokus ditunjukkan oleh amplikon yang terlihat saat elektroforesis. Hampir seluruh primer menunjukkan pola amplikon yang berbeda (Lampiran 7).
Perbedaan jumlah lokus yang dihasilkan dipengaruhi oleh sekuen primer yang
digunakan. Suatu primer dapat
mengamplifikasi DNA cetakan bila terdapat ruas yang komplemen. Semakin banyak ruas DNA cetakan yang bersifat komplemen dengan sekuen primer, maka hasil amplifikasi akan menunjukkan jumlah pita yang semakin banyak. Sebaliknya, semakin sedikit primer yang komplemen dengan DNA cetakan, maka jumlah pita hasil amplifikasi akan semakin sedikit. Bila antara primer dan DNA cetakan tidak memiliki sekuen yang komplemen, maka primer tersebut tidak akan dapat mengamplifikasi DNA cetakan sehingga tidak akan ada pita yang muncul (Semagn 2006).
Elektroforegram amplikon tanaman kunyit menunjukkan tidak terdapat pita monomorfik 1 2 3 4 5 6 7
3000bp 2000bp 1500bp 1200bp 600bp 500bp 300bp 200bp 100bp
1 2 3 4 5 6
untuk tanaman ini. Artinya, seluruh amplikon yang dihasilkan bersifat polimorfik. Derajat polimorfisme dari tanaman kunyit adalah 100%. Berbeda halnya dengan kunyit, tanaman temulawak memiliki tiga amplikon
yang bersifat monomorfik. Amplikon
monomorfik diperoleh dari amplifikasi
dengan primer OPA(11 dan OPA(13
(Lampiran 7). Tanaman temulawak memiliki derajat polimorfime sebesar 97.73%. Derajat polimorfisme yang diperoleh dari tanaman kunyit dan temulawak sangat tinggi. Derajat
polimorfisme menggambarkan keadaan
genom suatu organisme. Semakin tinggi derajat polimorfime maka semakin tinggi pula keragaman genetik yang terdapat dalam populasi (Grattapaglia 1992). Intensitas pita yang dihasilkan tiap primer dan sampel berbeda. Perbedaan ini dipengaruhi oleh kualitas dan kemurnian DNA yang diperoleh dan penyebaran situs penempelan primer pada DNA cetakan yang berbeda pula.
Intensitas pita menunjukkan konsentrasi DNA yang teramplifikasi. Ukuran amplikon yang dihasilkan dari tanaman kunyit berkisar antara 100 bp hingga 3000 bp. Temulawak memiliki amplikon dengan ukuran 100 bp hingga 3500 bp. Hal ini sesuai dengan
Grattapaglia (1992) yang mengemukakan
bahwa ukuran amplikon tanaman yang berkisar antara 200 bp hingga 5000 bp. Ukuran amplikon tanaman akan berbeda
bergantung pada jenis tanaman dan
konsentrasi DNA cetakan (Grattapaglia 1992). Konsentrasi DNA cetakan yang digunakan dalam penelitian ini adalah 50 ng/µL.
%*1 -0 +' 1 <% + +*
-Analisis kemiripan genetik dilakukan untuk mengetahui hubungan genetik antara tanaman yang diuji. Hal ini diperlukan untuk mengetahui tingkat keragaman genetik dalam suatu populasi. Hubungan genetik antar individu ditunjukkan oleh matriks kemiripan genetik. Analisis kemiripan genetik dilakukan dengan bantuan perangkat lunak NTSYS 2.02. Keluaran dari perangkat lunak ini berupa matriks kemiripan genetik. Matriks kemiripan genetik didasarkan pada proporsi fragmen RAPD. Proporsi pita yang muncul menjadi dasar yang digunakan untuk menentukan tingkat kemiripan genetik (Jan 2011).
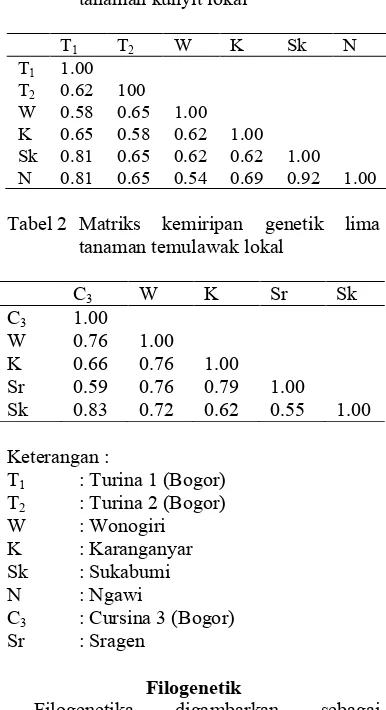
Matriks kemiripan genetik enam tanaman kunyit ditunjukkan oleh Tabel 1. Kemiripan genetik tanaman kunyit lokal berkisar antara
54% hingga 92%. Kemiripan genetik
tertinggi ditunjukkan oleh pasangan tanaman
kunyit asal Sukabumi dan Ngawi. Selanjutnya diikuti oleh pasangan tanaman kunyit asal Bogor (Turina 1) dengan Sukabumi dan Turina 1 dengan Ngawi dengan kemiripan genetik sebesar 81%.
Matriks kemiripan genetik lima tanaman temulawak ditunjukkan oleh Tabel 2. Kemiripan genetik antar lima tanaman temulawak lokal berkisar antara 55% hingga 83%. Kemiripan genetik tertinggi ditunjukkan oleh pasangan tanaman temulawak asal Bogor dan Sukabumi. Kemiripan genetik terendah
ditunjukkan oleh pasangan tanaman
temulawak asal Sukabumi dengan Sragen. Informasi mengenai tingkat kemiripan genetik bermanfaat dalam kegiatan pemuliaan tanaman. Tanaman dengan tingkat kemiripan genetik yang tinggi dapat ditanam secara
terpisah. Hal ini bertujuan untuk
mempertahankan keragaman genetik populasi tanaman tersebut. Selain itu, dapat pula digunakan sebagai acuan untuk melakukan persilangan tanaman (Wulandari 2008).
Tabel 1 Matriks kemiripan genetik enam tanaman kunyit lokal
T1 T2 W K Sk N
T1 1.00
T2 0.62 100
W 0.58 0.65 1.00
K 0.65 0.58 0.62 1.00 Sk 0.81 0.65 0.62 0.62 1.00 N 0.81 0.65 0.54 0.69 0.92 1.00
Tabel 2 Matriks kemiripan genetik lima tanaman temulawak lokal
C3 W K Sr Sk
C3 1.00
W 0.76 1.00
K 0.66 0.76 1.00
Sr 0.59 0.76 0.79 1.00
Sk 0.83 0.72 0.62 0.55 1.00
Keterangan :
T1 : Turina 1 (Bogor)
T2 : Turina 2 (Bogor)
W : Wonogiri
K : Karanganyar
Sk : Sukabumi
N : Ngawi
C3 : Cursina 3 (Bogor)
Sr : Sragen
& 9+ +*
-Filogenetika digambarkan sebagai
evolusinya. Analisis filogenetik didasarkan pada kemiripan karakter sebagai parameter
perbandingan. Parameter yang umum
digunakan adalah sekuen DNA, dan sekuen asam amino. Analisis filogenetik umumnya direpresentasikan sebagai sistem percabangan seperti diagram pohon. Diagram ini dikenal sebagai pohon filogenetik. Salah satu tujuan dari penyusunan pohon filogenetik adalah mengonstruksi hubungan antara organisme dengan tepat (Dharmayanti 2011).
Terdapat berbagai metode untuk
melakukan konstruksi pohon filogenetik, salah satunya adalah UPGMA. Metode
UPGMA ( ) )
) adalah metode sederhana untuk konstruksi pohon (Nei & Li 1979). Metode ini mengukur nilai kemiripan antar organisme yang dianalisis. Metode UPGMA merupakan metode yang mendasari perangkat lunak NTSYS. Penyusunan dendogram didasarkan pada data pola pita hasil elektroforesis. Data pola pita hasil elektroforesis diterjemahkan menjadi data biner dengan ketentuan khusus. Nilai 1 diberikan untuk pita yang muncul. Nilai 0 diberikan untuk pita yang tidak
muncul. Dendogram yang dihasilkan
merupakan turunan dari matriks kemiripan genetik (Dharmayanti 2011).
Dendogram yang diperoleh merupakan keluaran dari hasil skoring pita amplikon DNA yang muncul saat elektroforesis. Skoring dilakukan secara manual. Skoring dilakukan berdasarkan ukuran amplikon yang banyak dihasilkan saat elektroforesis. Masukan hasil skoring yang konsisten akan menghasilkan keluaran berupa matriks kemiripan genetik dan dendogram yang konsisten pula.
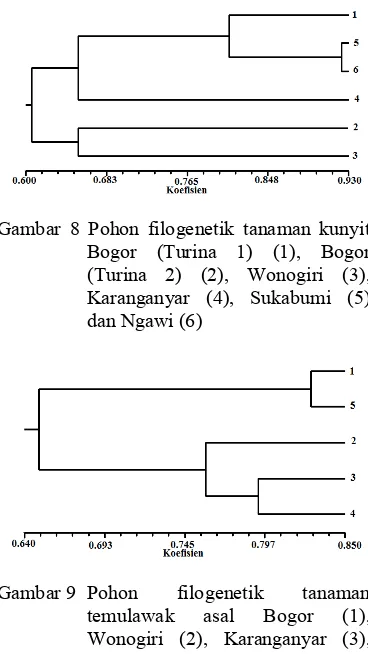
Pohon yang menggambarkan hubungan enam tanaman kunyit lokal ditunjukkan oleh Gambar 8. Terdapat dua kelompok besar pada tingkat kemiripan 0.606 yakni kelompok I dan II. Kelompok I terdiri atas empat tanaman, yaitu tanaman kunyit asal Bogor (Turina 1),
Sukabumi, Ngawi, dan Karanganyar;
sedangkan kelompok II terdiri atas dua tanaman, yakni tanaman kunyit asal Bogor (Turina 2) dan Wonogiri. Subkelompok IA dan IB menunjukkan tingkat kemiripan 0.654. Subkelompok IA1 dan IA2 menunjukkan
tingkat kemiripan 0.808. Anggota kelompok II menunjukkan tingkat kemiripan 0.654.
Pohon filogenetik lima tanaman
temulawak ditunjukkan oleh Gambar 9. Secara umum, terdapat dua kelompok yang terbagi pada tingkat kemiripan 0.649. Kelompok I terdiri atas dua tanaman, yakni
tanaman kunyit asal Bogor dan Sukabumi. Tingkat kemiripan kedua tanaman ini adalah 0.828. Kelompok II terdiri atas tiga tanaman, yakni tanaman temulawak asal Wonogiri, Sragen dan Karanganyar. Kelompok II terbagi menjadi dua subkelompok pada tingkat kemiripan 0.758.
Secara umum, semakin tinggi koefisien
kemiripan genetik akan menimbulkan
pengelompokkan yang semakin banyak. Nilai koefisien kemiripan genetik yang tinggi menggambarkan kedekatan hubungan genetik antar individu dalam populasi. Sebaliknya,
hubungan genetik yang relatif jauh
ditunjukkan dengan koefisien kemiripan genetik yang rendah. Informasi ini sangat berguna sebagai dasar persilangan tanaman untuk pemuliaan (Setiyo 2001).
Gambar 8 Pohon filogenetik tanaman kunyit Bogor (Turina 1) (1), Bogor (Turina 2) (2), Wonogiri (3), Karanganyar (4), Sukabumi (5) dan Ngawi (6)
Gambar 9 Pohon filogenetik tanaman
temulawak asal Bogor (1),
Wonogiri (2), Karanganyar (3), Sragen (4) dan Sukabumi (5)
'<(&%
berbeda pada tiap sampel menunjukkan pola keragaman genetik yang terdapat pada tanaman kunyit dan temulawak. Koefisien kemiripan genetik 6 tanaman kunyit berkisar antara 53.8% hingga 92.3%. Koefisien kemiripan genetik 5 tanaman temulawak berkisar antara 55.2% hingga 82.8%. Hubungan genetik terdekat ditunjukkan oleh tanaman kunyit asal Sukabumi dengan Ngawi dan tanaman temulawak asal Sukabumi dengan Bogor.
%1%
Perlu dilakukan penambahan jumlah
larutan 2(merkaptoetanol untuk
menghilangkan kontaminan polisakarida saat isolasi DNA. Analisis lebih lanjut dapat
dilakukan dengan menggunakan primer
RAPD lainnya. Selain itu, dapat pula ditambahkan jenis sampel yang dianalisis agar kekerabatan tanaman temulawak dan kunyit lokal lebih tereksplorasi. Analisis lainnya dapat digunakan dengan metode marka molekuler lain seperti AFLP, RFLP atau SSR.
Aggarwal BB, Kumar A, Aggarwal MS, Shishodia S. 2005. Curcumin derived
from tumeric ( ) : a spice
for all seasons. (05) : 349(
386.
Akram 2010. and
curcumin : a review article. 0 .
55 (2) : 65(70.
Araujo CAC, Leon LL. 2001. Biological
activities of L. 1
% ) 96 (5) : 723(728.
Bartlett JMS, Stirling D. 2010. 1
1 . 2 ! *
Ed. 226 : 1(6.
Berdakci F. 2001. Random amplified
polymorphic DNA (RAPD) markers [review]. $ 3 0 . 25: 185(196.
[BPPT] Badan Pengkajian dan Penerapan Teknologi. 2010. Temulawak. [terhubung berkala]
http://lc.bppt.go.id/ttg/Data/bididaya%20 pertanian/obat/temulawak.pdf [4 Juni 2012].
Brescia P. 2012. Micro(volume purity assessment of nucleic acid using A260/A280 ratio and spectral scanning.
[terhubung berkala]
http://www.biotek.com [10 Desember 2012].
Brown TA. 2007. " '
2 !
-New York : John Wiley and Sons.
Campbell NA, Reece JB, Mitchell LG. 2002.
. 4 - . Jakarta: Erlangga.
Carroll P, Casimir D. 2010. 1
1 . :
Ed. 226 : 7(14.
Chauhan DP. 2002. Chemoteurapeutic
potential of curcumin for colorectal
cancer. ' 8 : 1695(1706.
Dharmayanti NLPI. 2011. Filogenetika molekuler : metode taksonomi organisme berdasarkan sejarah evolusi [review].
5 Vol. 21(1): 1(10.
Dorai T, Cao YC, Dorai B. 2001. Therapeutic potential of curcumin in human prostate cancer. III. curcumin inhibits proliferation, induces apoptosis, and inhibits angiogenesis of LNCaP prostate cancer cells # # .
47:293(303.
Grattapaglia D . 1992. Mapping in woody plants with RAPD markers: Application to breeding in forestry and holticulture. ' : Application of RAPD Technology to Plant Breeding. Joint Plant Breeding Symposia. Minneapolis, 1 November 1992.
Grunenwald H, Bartlett JMS, Stirling D,
editor. 2010. 1 1
. : %
Ed. 226:89(100.
Hadipoentyanti E, Syahid SF. 2001.
Pertumbuhan dan produksi rimpang temulawak di polibag yang benihnya
hasil kultur # . 0 .
III(2) : 118(125.
Hayakawa . 2011. Development of
molecular marker to candidate line
of turmeric ( ) with a
high curcumin content.
Hofreiter M, Rompler H, Bustin SA, editor.
2010. $ # 2 .
$ . New York
: Cambridge University Pr.
Hoisington D, Khairallah M, Leon G. 1994.
( 2 117$
. 6
-Mexico : DF CIMMYT.
Indena. 2002. Curcuma longa. #
1 # ) 1 : 119(
125.
Jan HU, Rabbani MA, Shinwari ZK. 2011. Assesment of genetic diversity of
indigenous turmeric ( L.)
germplasm from Pakistan using RAPD
markers. 0 1
Vol. 5(5) : 823(830.
Lee HS. 2006. Antiplatelet property of L. rhizome derived ar(
turmeron. . $ 97:1372(
1376.
Meryalita R. 2012. Analisis keragaman
genetik kunyit ( Linn.)
dan temulawak (
Roxb.) budidaya tanah jawa berdasarkan penanda molekuler RAPD [skripsi]. Bogor : Fakultas Matematika dan Ilmu Pengetahuan Alam, Institut Pertanian Bogor.
[NCBI] .
. 2011. Random amplified polymorphic DNA (RAPD). [terhubung berkala]
http://www.ncbi.nlm.nih.gov/projects/gen ome/probe/doc/TechRAPD.shtml[4 Juni 2011].
Nei M, Li W. 1979. Mathematical model for studying genetic variation in terms of restriction endonucleasis.
! 76: 5269(5273.
Nurcholis W. 2008. Profil senyawa penciri dan bioaktivitas tanaman temulawak pada agrobiofisik berbeda [tesis]. Bogor: Program Pascasarjana, Institut Pertanian Bogor.
Padmalatha K, Prasad MNV. 2006.
Optimazion of DNA isolation and PCR protocol for RAPD analysis of selected medicinal and aromatic plants of conservation concern from Peninsular
India. 0 .
5:230(234.
Pharmawati M. 2009. Optimalisasi ekstraksi DNA dan PCR(RAPD pada " #
(proteaceae). 0 . 8 (1) :
12(16.
Prahaditya D. 2013. Analisis keragaman genetika tanaman kunyit dan temulawak secara
DNA (RAPD(PCR) menggunakan primer OPA(OPD 6(10 [skripsi]. Bogor :
Fakultas Matematika dan Ilmu
Pengetahuan Alam, Institut Pertanian Bogor.
Prana T, Hartati S. 2003. Identifikasi sidik jari
talas ( L. Schott)
indonesia dengan teknik RAPD (
' ): skrining primer dan optimalisasi kondisi PCR.
0 5 (2) : 107(112.
Pribadi ER. 2009. Pasokan dan permintaan tanaman obat Indonesia serta arah
penelitian dan pengembangannya.
3 Vol. 8(1):52(64.
Purnomowati S. 2008. Khasiat temulawak : tinjauan literatur tahun 1980(1997.
[terhubung berkala]
http://www.indofarma.co.id/index.php?op tion=com_content&task=view&id=21&It emid=125.[5 Juni 2012].
Ramachandaran C, Fonseca HB, Jhabvala P. 2002. Curcumin inhibits telomerase activity through human telomerase reverse transcriptase in MCF(7 breast
cancer cell line. 184:1(6.
Rahardjo M, Rostiana O. 2003. Standar
prosedur operasional budidaya
temulawak. ! 3 9 : 33(38.
Rahardjo M, Rostiana O. 2005. Standar prosedur operasional budidaya kunyit.
! 3 No. 11:1(6.
Rahardjo M. 2010. Penerapan SOP budidaya untuk mendukung temulawak sebagai
bahan baku obat potensial. 3
Vol. 9 (2):78(93.
Reddy BS, Rao CV. 2002. Novel approaches
for colon cancer prevention by
cyclooxigenase(2 inhibitors. 0 - #
Roulf FJ. 2002. $!7!
$ 1 #
! # 6 :,. New York : Exeter
Publishing Ltd.
Sambrook J, Russel DW. 1989. 1
2 ( 1 Ed.
Ke(2. USA: Cold Spring Harbor
Laboratory Pr.
Sambrook J, Russel DW. 2001. 1
2 ( 1 Ed. Ke(3.
USA: Cold Spring Harbor Laboratory Pr.
Santos SR. 2000. Amplified fragment
length polymorphism protocol.
[terhubung berkala]
http://biologi.uio.no/FellesAvdelinger/DN A_KAFFE/Kaffe_Resource/AFLP.html [10 Januari 2012].
Semagn K, Bjornstad A, Ndjiondjop MN. 2006. An overview of molecular marker methods for plants [review]. 0
. Vol. 5(25):2540(2568.
Setiyo IE. 2001. Pemetaan dan keragaman genetik RAPD pada kelapa sawit sungai pancur (RISPA) [tesis]. Bogor: Program Pasca Sarjana, Institut Pertanian Bogor.
Shinwari ZK. 2010. Medicinal plants research
in Pakistan. 0 1 4:161(176.
Somasundaram S, Edmund NA, Moore DT.
2002. Dietary curcumin inhibits
chemotherapy(induced apoptosis in models of human breast cancer.
62:3868(3875.
Syukur C, Udarno L, Supriadi, Rostiana O, dan Syahid SF. 2006. Usulan pelepasan varietas kunyit. Balitro, Puslitbangun, Bogor.
Tibbits JFG, McManus LK, Spokevicius AV, Bossinger G. 2006. A rapid method for tissue collection and high(throughput isolation of genomic DNA from mature
trees. 1 .
24: 81(91.
Utami A. 2012. Analisis polimorfisme DNA
tanaman kunyit ( L.) dan
temulawak (C
Roxb.) lokal menggunakan marka RAPD [skripsi]. Bogor : Fakultas Matematika dan Ilmu Pengetahuan Alam, Institut Pertanian Bogor.
Warintek. 2005. Kunyit (
Val.).[terhubung berkala]. http:// http://www.iptek.net.id/ind/warintek/?mn u=6&ttg=2&doc=2d4[21 Januari 2012].
Wibowo M, Deasywaty, Tepy U. 2012. Antimicrobial and identification of active
compound Roxb.
0 . ; ! Vol.
12(01):69(78.
William 1990. DNA polymorphisms
amplified by arbitary primers are useful as a genetic markers.
18:6531(6535.
Wulandari Y. 2008. Analisis keragaman genetik kayu afrika (1
Engl.) berdasarkan penanda
Lampiran 1 Strategi Penelitian
L
Pengambilan
sampel
Isolasi DNA
Amplifikasi
DNA
Analisis data
Daun kunyit
dan daun
temulawak
Optimasi
metode isolasi
DNA
Analisis
kualitatif
DNA
Analisis
kuantitatif
DNA
PCR(RAPD
Elektroforesis
gel agarosa
Skoring pita
hasil
elektroforesis
Analisis
polimorfisme
dan
kekerabatan
dengan
)
Lampiran 2 Bagan alir modifikasi metode isolasi DNA
Daun temulawak 1 gram
+PVP, N
2cair,gerus halus
+ 9.8 mL bufer ekstraksi
hangat + 0.2 mL 2(
merkaptoetanol
Inkubasi 55
0C, 150 rpm, 1
jam
+10 mL CIA (24:1)
Sentrifugasi 1000 g, 5
menit
Aliquot
+isopropanol dingin (2/3v)
Pelet
Sentrifugasi 12000 g, 20
menit
+ proteinase K (10
µg/mL)
Inkubasi 37
0C, 30
menit
Inkubasi 65
0C, 20
menit
Simpan di suhu (20
0C