PENETAPAN KADAR FOSFOR DALAM BUAH JAMBU BIJI
MERAH (Psidium guajava L.) SECARA
SPEKTROFOTOMETRI SINAR TAMPAK
SKRIPSI
OLEH:
PAHALA A. R. SINAGA
NIM 071501046
FAKULTAS FARMASI
UNIVERSITAS SUMATERA UTARA
MEDAN
PENETAPAN KADAR FOSFOR DALAM BUAH JAMBU BIJI
MERAH (Psidium guajava L.) SECARA
SPEKTROFOTOMETRI SINAR TAMPAK
SKRIPSI
Diajukan untuk melengkapi salah satu syarat untuk memperoleh gelar Sarjana Farmasi pada Fakultas Farmasi
Universitas Sumatera Utara
OLEH:
PAHALA A. R. SINAGA
NIM 071501046
FAKULTAS FARMASI
UNIVERSITAS SUMATERA UTARA
MEDAN
PENGESAHAN SKRIPSI
PENETAPAN KADAR FOSFOR
DALAM BUAH JAMBU BIJI MERAH (Psidium guajava L.)
SECARA SPEKTROFOTOMETRI SINAR TAMPAK
OLEH:
PAHALA A. R. SINAGA
NIM 071501046
Dipertahankan di hadapan Panitia Penguji Fakultas Farmasi
Universitas Sumatera Utara Pada tanggal:
Pembimbing I, Panitia Penguji,
Drs. Chairul Azhar Dalimunthe, M.Sc., Apt Dra. Masfria, M.S., Apt. NIP 194907061980021001 NIP 195707231986012001
Pembimbing II Drs. Chairul Azhar D., M.Sc., Apt
NIP 194907061980021001
Drs. Fathur Rahman Harun, M.Si., Apt.
NIP 195201041980031002 Dra. Siti Nurbaya, Apt. NIP 195008261974122001
Dra. Salbiah, M.Si., Apt. NIP 194810031987012001
Dekan,
KATA PENGANTAR
Puji dan syukur kepada Tuhan Yang Maha Kuasa yang telah melimpahkan
berkat-Nya, sehingga penulis dapat menyelesaikan skripsi dengan judul
“Penetapan Kadar Fosfor dalam Buah Jambu Biji Merah (Psidium guajava L.)
secara Spektrofotometri Sinar Tampak”. Tujuan penelitian ini adalah untuk
menetapkan kadar fosfor dalam buah jambu biji merah dan mengetahui pengaruh
faktor penghalusan dan pengupasan terhadap kadar fosfor dalam buah jambu biji
merah. Skripsi ini diajukan sebagai salah satu syarat guna memperoleh gelar
Sarjana Farmasi dari Fakultas Farmasi Universitas Sumatera Utara.
Pada kesempatan ini penulis mengucapkan terima kasih dan penghargaan
yang tulus kepada orang tua tercinta, Papa Drs. R Sinaga dan Mama R. Siregar,
S.Pd., juga kepada kakak-kakak dan adikku tersayang Juniar Sinaga, S.Hut.,
Wiwik Sinaga, S.Si., May Arcan Sinaga, S.E., Marathur Sinaga, S.Pd., dan
Novrista Sinaga serta semua keluarga yang tidak dapat disebutkan satu per satu,
yang telah banyak memberikan doa dan dorongan serta bantuan moril dan materil
kepada penulis selama menempuh pendidikan S-1 Farmasi.
Penulis mengucapkan terima kasih yang sebesar-besarnya kepada Bapak
Drs. Chairul Azhar Dalimunthe, M.Sc., Apt., dan Bapak Drs. Fathur Rahman
Harun, M.Si., Apt., selaku dosen pembimbing yang telah banyak memberikan
bimbingan dan bantuan yang sangat berarti mulai dari penelitian hingga selesainya
Pada kesempatan ini penulis juga menyampaikan ucapan terima kasih
kepada:
1. Bapak Prof. Dr. Sumadio Hadisahputra, Apt., selaku Dekan Fakultas
Farmasi, Universitas Sumatera Utara.
2. Ibu Dra. Siti Nurbaya, Apt., selaku Dosen Penasehat Akademik yang telah
memperhatikan dan membimbing penulis selama masa perkuliahan.
3. Ibu Dra. Masfria, M.S., Apt., Ibu Dra. Siti Nurbaya, Apt., dan Ibu Dra.
Salbiah, M.Si., Apt., selaku dosen penguji yang telah memberikan
masukan dan saran kepada penulis hingga selesainya penulisan skripsi ini.
4. Seluruh Staf Pengajar dan Pegawai Tata Usaha di Fakultas Farmasi, serta
seluruh Asisten di Laboratorium yang telah banyak membimbing penulis
selama perkuliahan dan membantu penulis dalam menyelesaikan
penelitian ini.
5. Kelompok kecilku (Kak Christina, S.Farm., Apt., Debi, Sari, dan Ira).
6. Sahabat-sahabatku “Rejoicing in Love” ( Santa, Ira, Debi, Rachmad, Eva,
Novalina, Via, Triwati, Martianus, Vintha, Juwita, Sari, Jimmy, Sandro,
Melati, Cory, Elfrida, Ernal, Hendry, Febri, Wandi, Fanny, Silvana,
Melisa, dan Sylvia).
7. Teman-teman Farmasi 2007 khususnya konsentrasi Sains dan Teknologi
Farmasi serta semua pihak yang tidak dapat disebutkan satu per satu.
Tidak ada gading yang tak retak. Penulis menyadari bahwa tulisan ini
hati penulis bersedia menerima kritik dan saran yang membangun pada skripsi ini.
Semoga skripsi ini bermanfaat bagi kita semua.
Medan, Juni 2011
Penulis,
PENETAPAN KADAR FOSFOR DALAM BUAH JAMBU BIJI MERAH (Psidium guajava L.) SECARA SPEKTROFOTOMETRI SINAR TAMPAK
ABSTRAK
Penyakit Demam Berdarah Dengue (DBD) merupakan salah satu penyakit yang cukup berbahaya di Indonesia. Sampai saat ini belum ada obat yang tepat untuk mengatasi penyakit DBD. Namun, ada sebagian masyarakat mencoba dengan mengkonsumsi buah jambu biji merah untuk membantu kepulihan pasien penderita DBD. Buah jambu biji merah mengandung fosfor, yaitu mineral yang berperan dalam pembentukan energi dalam bentuk ATP. Pasien DBD membutuhkan asupan energi yang cukup, sehingga dengan adanya pembentukan ATP asupan energi pasien dapat terpenuhi dan dapat membantu kepulihan pasien tersebut. Sehubungan dengan itu, dilakukan penelitian tentang penetapan kadar fosfor dalam buah jambu biji merah dengan variasi perlakuan cara penghalusan dan pengupasan.
Pemeriksaan fosfor dilakukan secara kualitatif dan kuantitatif. Analisis kualitatif dilakukan dengan menggunakan pereaksi ammonium molibdat menghasilkan endapan kuning dan dengan menggunakan pereaksi barium klorida menghasilkan endapan putih. Hasil analisis kualitatif menunjukkan bahwa buah jambu biji merah mengandung fosfor.
Analisis kuantitatif dilakukan dengan metode Spektrofotometri Sinar Tampak pada panjang gelombang 713 nm. Dari hasil analisis kuantitatif diperoleh kadar fosfor pada buah jambu biji merah yang di-blender (tanpa dikupas dan dikupas) sesuai dengan literatur, sedangkan kadar fosfor dalam buah jambu biji merah di-juicer (tanpa dikupas dan dikupas) tidak sesuai dengan literatur. Metode penelitian ini memiliki %recovery 98,9%, RSD 0,08%, LOD 0,2602 µg/ml, dan
LOQ 0,8672 µg/ml dengan konsenrasi minimum 5,8802 µg/ml yang menunjukkan
bahwa metode ini memiliki tingkat akurasi dan presisi yang baik.
Berdasarkan hasil analisis variansi menunjukkan bahwa perlakuan cara penghalusan dan pengupasan berpengaruh terhadap kadar mineral ini, sedangkan berdasarkan hasil analisis lanjutan uji HSD menunjukkan bahwa cara penghalusan memberikan perbedaan yang signifikan terhadap kadar fosfor dalam buah jambu biji merah, tetapi faktor pengupasan tidak memberikan perbedaan yang signifikan terhadap kadar fosfor dalam buah jambu biji merah.
DETERMINATION OF PHOSPHORUS IN RED GUAVA FRUIT (Psidium guajava L.) WITH VISIBLE SPECTROPHOTOMETRY
ABSTRACT
Disease of dengue haemorraghic fever is one of the dangerous disease in Indonesia. Until now there is no correct drug to overcome dengue haemorraghic fever. But, there are some societies try by red guava fruit consumption to recovery dengue haemorraghic fever. Red guava fruit contain phosphorus, that is mineral which play a part in forming of energy in the form of ATP. Patient DBD require the input of energy which enough, so that with the existence of forming of ATP the input of energy of patient can be fullfiled and can assist convalesce of the patient. Refering to the mentioned, a research about determination of phosphorus in the red guava fruit with the variation of treatment of attenuation way and peel.
The determination of phosphorus was done by using qualitative and quantitative methods. The qualitative analysis did reacted by ammonium molibddenum formed yellow precipitate and reacted by barium chloridum formed white precipitate. Qualitative analysis showed the red guava fruit content phosphorus.
The quantitative examine did by visible spectrophotometry at maximum wavelength of 713 nm. The result of quantitative analysis get phosphorus value on the sample which blender (without peeled and peeled) is equal to literature, on the other hand phosphorus value on sample which juicer (without peeled and peeld) is not equal to literature. This method has %recovery 98,9%, RSD 0,08%, LOD 0,2602 µg/ml, dan LOQ 0,8672 µg/ml with minimum concentration 5,8802 µg/ml showed that this method has good accuration and precition level.
Pursuant to the result analysis of variance showed that attenuation way and peeling have an effect to this mineral rate, on the other hand pursuant to the result of continuation analyse HSD test showed that attenuation way give significant difference, but peeling factor doesn’t give significant difference.
DAFTAR ISI
Halaman
JUDUL ... i
HALAMAN PENGESAHAN ... ii
KATA PENGANTAR ... iii
ABSTRAK ... iv
ABSTRACT ... v
DAFTAR ISI ... vi
DAFTAR TABEL ... x
DAFTAR GAMBAR ... xi
DAFTAR LAMPIRAN ... xii
BAB I PENDAHULUAN ... 1
1.1 Latar Belakang ... 1
1.2 Perumusan Masalah ... 3
1.3 Hipotesis ... 3
1.4 Tujuan Penelitian ... 4
1.5 Manfaat Penelitian ... 4
BAB II TINJAUAN PUSTAKA ... 5
2.1 Uraian Tumbuhan ... 5
2.1.1 Taksonomi Buah Jambu Biji Merah ... 5
2.1.2 Deskripsi Buah Jambu Biji Merah ... 5
2.1.3 Macam-macam Jambu Biji ... 6
2.1.4 Kandungan Kimia Jambu Biji Merah ... 7
2.2 Demam Berdarah Dengue ... 8
2.3 Mineral ... 9
2.3.1 Fosfor ... 9
2.3.2 Kekurangan Fosfor ... 11
2.3.3 Kelebihan Fosfor ... 11
2.4 ATP (Adenosine Tri Phosphate) ... 11
2.5 Spektrofotometri ... 12
2.6 Parameter Validasi ... 15
BAB III METODOLOGI PENELITIAN ... 18
3.1 Lokasi dan Waktu Penelitian ... 18
3.2 Bahan-bahan ... 18
3.2.1 Sampel ... 18
3.2.2 Pereaksi ... 18
3.3 Alat-alat ... 18
3.4 Pembuatan Pereaksi ... 19
3.4.1 Larutan HNO3 5 N ... 19
3.4.2 Larutan H2SO4 5N ... 19
3.4.3 Larutan Ammonium Molibdat 4% b/v ... 19
3.4.4 Larutan Asam Askorbat 0,1N ... 19
3.4.5 Larutan Kalium Antimonil Tartrat 0,274% b/v ... 19
3.4.6 Larutan Pereaksi Warna Fosfor ... 20
3.5 Rancangan Penelitian ... 20
3.6 Prosedur Penelitian ... 22
3.6.2 Analisis Kualitatif ... 23
3.6.3 Analisis Kuantitatif ... 24
3.6.3.1 Pembuatan Larutan Induk Baku KH2PO4 ... 24
3.6.3.2 Penentuan Waktu Kerja ... 24
3.6.3.3 Pembuatan Kurva Serapan Larutan KH2PO4 . 25 3.6.3.4 Penentuan Kurva Kalibrasi Larutan Baku Fosfor 25 3.6.4 Analisis Fosfor dalam Sampel ... 25
3.6.5 Prosedur Uji Ketepatan ... 26
3.6.6 Simpangan Baku Relatif ... 27
3.6.7Analisis Data secara Statistik ... 28
3.6.8 Penentuan Batas/Limit Deteksi dan Batas/Limit Kuantitasi ... 28
BAB IV HASIL DAN PEMBAHASAN ... 29
4.1 Destruksi Kering ... 29
4.2 Analisis Fosfor dalam Buah Jambu Biji Merah ... 29
4.2.1 Analisis Kualititatif Fosfor ... 29
4.2.2 Analisis Kuantitatif Fosfor ... 29
4.2.2.1 Penentuan Panjang Gelombang Maksimum Senyawa Kompleks Fosfor Molibdat ... 29
4.2.2.2 Penentuan Waktu Kerja Kompleks Fosfor Molibdat pada Panjang Gelombang 713 nm ... 30
4.2.2.3 Kurva Kalibrasi Fosfor ... 30
4.2.2.4 Analisis Kadar Fosfor pada Buah Jambu Biji Merah 32 4.3 Analisis Data Secara Statistik ... 34
4.3.1 Analisis Variansi ... 34
4.4 Uji Perolehan Kembali (Recovery) ... 36
4.5 Simpangan Baku Relatif ... 36
4.6 Batas/Limit Deteksi (LOD) dan Batas/Limit Kuantitasi (LOQ) ... 36
BAB V KESIMPULAN DAN SARAN ... 38
5.1 Kesimpulan ... 38
5.2 Saran ... 38
DAFTAR PUSTAKA ... 39
DAFTAR TABEL
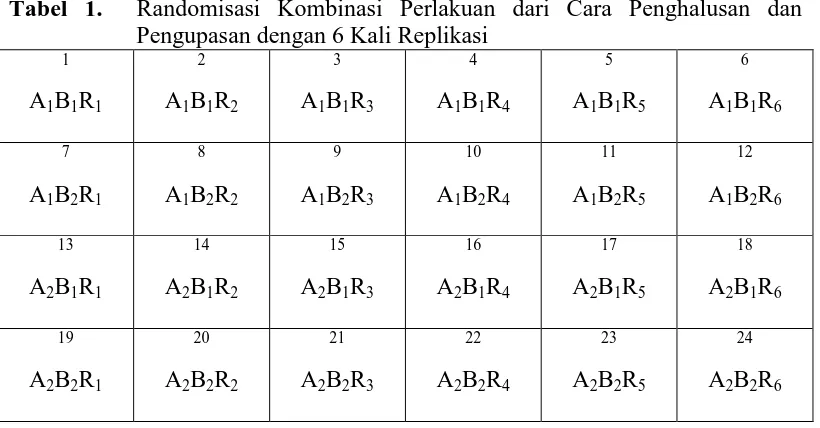
Halaman Tabel 1. Randomisasi Kombinasi Perlakuan dari Cara Penghalusan
dan Pengupasan dengan 6 Kali Replikasi ... 22
Tabel 2. Hasil Kadar Total dan Kadar Rata-rata Fosfor pada Setiap
Kombinasi perlakuan dengan 6 Kali Replikasi ... 32
Tabel 3. Kadar Fosfor Sebenarnya dalam Buah Jambu Biji Merah ... 33
Tabel 4. Data Hasil Analisis Variansi Pengaruh Cara Penghalusan
dan Pengupasan terhadap Kadar Fosfor ... 34
DAFTAR GAMBAR
Halaman Gambar 1. Kurva Serapan Senyawa Fosfor pada
Konsentrasi 8 µg/ml ... 30
Gambar 2. Serapan Kurva Kalibrasi Larutan Standar Fosfor
pada Panjang Gelombang 713 nm ... 31
Gambar 3. Kurva Kalibrasi Larutan Standar Fosfor pada
DAFTAR LAMPIRAN
Halaman
Lampiran 1. Gambar Sampel Buah Jambu Biji Merah ... 42
Lampiran 2. Gambar Penguapan Kandungan Air, Hasil Pengarangan, dan Hasil Pengabuan Sampel ... 43
Lampiran 3. Flowsheet Destruksi Kering ... 44
Lampiran 4. Gambar Hasil Analisis Kualitatif ... 45
Lampiran 5. Data Penentuan Waktu Kerja Senyawa Fosfor Molibdat pada Panjang Gelombang 713 nm ... 46
Lampiran 6. Perhitungan Persamaan Regresi ... 48
Lampiran 7. Daftar Berat Sampel dan Berat Abu ... 49
Lampiran 8. Contoh Perhitungan Hasil Penetapan Kadar Fosfor dalam Sampel dengan Menggunakan Persamaan Regresi . 50
Lampiran 9. Data Serapan Sampel, Konsentrasi, dan Kadar Fosfor pada Setiap Kombinasi Perlakuan dengan 6 Kali Replikasi ... 51
Lampiran 10. Perhitungan Kadar Fosfor Sebenarnya dalam Buah Jambu Biji Merah secara Spektrofotometri Sinar Tampak ... 52
Lampiran 11. Perhitungan Kadar Fosfor dalam Buah Jambu Biji Merah Setelah Penambahan Larutan Standar dan Perhitungan Uji Perolehan Kembali (Recovery) ... 60
Lampiran 12. Data Uji Perolehan Kembali (Recovery) ... 64
Lampiran 13. Analisis Variansi ... 65
Lampiran 14. Perhitungan Batas Deteksi dan Batas Kuantitasi ... 66
Lampiran 15. Perhitungan Konsentrasi Larutan Induk Baku KH2PO4 ... 67
Lampiran 16. Daftar Nilai Distribusi t ... 68
PENETAPAN KADAR FOSFOR DALAM BUAH JAMBU BIJI MERAH (Psidium guajava L.) SECARA SPEKTROFOTOMETRI SINAR TAMPAK
ABSTRAK
Penyakit Demam Berdarah Dengue (DBD) merupakan salah satu penyakit yang cukup berbahaya di Indonesia. Sampai saat ini belum ada obat yang tepat untuk mengatasi penyakit DBD. Namun, ada sebagian masyarakat mencoba dengan mengkonsumsi buah jambu biji merah untuk membantu kepulihan pasien penderita DBD. Buah jambu biji merah mengandung fosfor, yaitu mineral yang berperan dalam pembentukan energi dalam bentuk ATP. Pasien DBD membutuhkan asupan energi yang cukup, sehingga dengan adanya pembentukan ATP asupan energi pasien dapat terpenuhi dan dapat membantu kepulihan pasien tersebut. Sehubungan dengan itu, dilakukan penelitian tentang penetapan kadar fosfor dalam buah jambu biji merah dengan variasi perlakuan cara penghalusan dan pengupasan.
Pemeriksaan fosfor dilakukan secara kualitatif dan kuantitatif. Analisis kualitatif dilakukan dengan menggunakan pereaksi ammonium molibdat menghasilkan endapan kuning dan dengan menggunakan pereaksi barium klorida menghasilkan endapan putih. Hasil analisis kualitatif menunjukkan bahwa buah jambu biji merah mengandung fosfor.
Analisis kuantitatif dilakukan dengan metode Spektrofotometri Sinar Tampak pada panjang gelombang 713 nm. Dari hasil analisis kuantitatif diperoleh kadar fosfor pada buah jambu biji merah yang di-blender (tanpa dikupas dan dikupas) sesuai dengan literatur, sedangkan kadar fosfor dalam buah jambu biji merah di-juicer (tanpa dikupas dan dikupas) tidak sesuai dengan literatur. Metode penelitian ini memiliki %recovery 98,9%, RSD 0,08%, LOD 0,2602 µg/ml, dan
LOQ 0,8672 µg/ml dengan konsenrasi minimum 5,8802 µg/ml yang menunjukkan
bahwa metode ini memiliki tingkat akurasi dan presisi yang baik.
Berdasarkan hasil analisis variansi menunjukkan bahwa perlakuan cara penghalusan dan pengupasan berpengaruh terhadap kadar mineral ini, sedangkan berdasarkan hasil analisis lanjutan uji HSD menunjukkan bahwa cara penghalusan memberikan perbedaan yang signifikan terhadap kadar fosfor dalam buah jambu biji merah, tetapi faktor pengupasan tidak memberikan perbedaan yang signifikan terhadap kadar fosfor dalam buah jambu biji merah.
DETERMINATION OF PHOSPHORUS IN RED GUAVA FRUIT (Psidium guajava L.) WITH VISIBLE SPECTROPHOTOMETRY
ABSTRACT
Disease of dengue haemorraghic fever is one of the dangerous disease in Indonesia. Until now there is no correct drug to overcome dengue haemorraghic fever. But, there are some societies try by red guava fruit consumption to recovery dengue haemorraghic fever. Red guava fruit contain phosphorus, that is mineral which play a part in forming of energy in the form of ATP. Patient DBD require the input of energy which enough, so that with the existence of forming of ATP the input of energy of patient can be fullfiled and can assist convalesce of the patient. Refering to the mentioned, a research about determination of phosphorus in the red guava fruit with the variation of treatment of attenuation way and peel.
The determination of phosphorus was done by using qualitative and quantitative methods. The qualitative analysis did reacted by ammonium molibddenum formed yellow precipitate and reacted by barium chloridum formed white precipitate. Qualitative analysis showed the red guava fruit content phosphorus.
The quantitative examine did by visible spectrophotometry at maximum wavelength of 713 nm. The result of quantitative analysis get phosphorus value on the sample which blender (without peeled and peeled) is equal to literature, on the other hand phosphorus value on sample which juicer (without peeled and peeld) is not equal to literature. This method has %recovery 98,9%, RSD 0,08%, LOD 0,2602 µg/ml, dan LOQ 0,8672 µg/ml with minimum concentration 5,8802 µg/ml showed that this method has good accuration and precition level.
Pursuant to the result analysis of variance showed that attenuation way and peeling have an effect to this mineral rate, on the other hand pursuant to the result of continuation analyse HSD test showed that attenuation way give significant difference, but peeling factor doesn’t give significant difference.
PENETAPAN KADAR FOSFOR DALAM BUAH JAMBU BIJI MERAH (Psidium guajava L.) SECARA SPEKTROFOTOMETRI SINAR TAMPAK
ABSTRAK
Penyakit Demam Berdarah Dengue (DBD) merupakan salah satu penyakit yang cukup berbahaya di Indonesia. Sampai saat ini belum ada obat yang tepat untuk mengatasi penyakit DBD. Namun, ada sebagian masyarakat mencoba dengan mengkonsumsi buah jambu biji merah untuk membantu kepulihan pasien penderita DBD. Buah jambu biji merah mengandung fosfor, yaitu mineral yang berperan dalam pembentukan energi dalam bentuk ATP. Pasien DBD membutuhkan asupan energi yang cukup, sehingga dengan adanya pembentukan ATP asupan energi pasien dapat terpenuhi dan dapat membantu kepulihan pasien tersebut. Sehubungan dengan itu, dilakukan penelitian tentang penetapan kadar fosfor dalam buah jambu biji merah dengan variasi perlakuan cara penghalusan dan pengupasan.
Pemeriksaan fosfor dilakukan secara kualitatif dan kuantitatif. Analisis kualitatif dilakukan dengan menggunakan pereaksi ammonium molibdat menghasilkan endapan kuning dan dengan menggunakan pereaksi barium klorida menghasilkan endapan putih. Hasil analisis kualitatif menunjukkan bahwa buah jambu biji merah mengandung fosfor.
Analisis kuantitatif dilakukan dengan metode Spektrofotometri Sinar Tampak pada panjang gelombang 713 nm. Dari hasil analisis kuantitatif diperoleh kadar fosfor pada buah jambu biji merah yang di-blender (tanpa dikupas dan dikupas) sesuai dengan literatur, sedangkan kadar fosfor dalam buah jambu biji merah di-juicer (tanpa dikupas dan dikupas) tidak sesuai dengan literatur. Metode penelitian ini memiliki %recovery 98,9%, RSD 0,08%, LOD 0,2602 µg/ml, dan
LOQ 0,8672 µg/ml dengan konsenrasi minimum 5,8802 µg/ml yang menunjukkan
bahwa metode ini memiliki tingkat akurasi dan presisi yang baik.
Berdasarkan hasil analisis variansi menunjukkan bahwa perlakuan cara penghalusan dan pengupasan berpengaruh terhadap kadar mineral ini, sedangkan berdasarkan hasil analisis lanjutan uji HSD menunjukkan bahwa cara penghalusan memberikan perbedaan yang signifikan terhadap kadar fosfor dalam buah jambu biji merah, tetapi faktor pengupasan tidak memberikan perbedaan yang signifikan terhadap kadar fosfor dalam buah jambu biji merah.
DETERMINATION OF PHOSPHORUS IN RED GUAVA FRUIT (Psidium guajava L.) WITH VISIBLE SPECTROPHOTOMETRY
ABSTRACT
Disease of dengue haemorraghic fever is one of the dangerous disease in Indonesia. Until now there is no correct drug to overcome dengue haemorraghic fever. But, there are some societies try by red guava fruit consumption to recovery dengue haemorraghic fever. Red guava fruit contain phosphorus, that is mineral which play a part in forming of energy in the form of ATP. Patient DBD require the input of energy which enough, so that with the existence of forming of ATP the input of energy of patient can be fullfiled and can assist convalesce of the patient. Refering to the mentioned, a research about determination of phosphorus in the red guava fruit with the variation of treatment of attenuation way and peel.
The determination of phosphorus was done by using qualitative and quantitative methods. The qualitative analysis did reacted by ammonium molibddenum formed yellow precipitate and reacted by barium chloridum formed white precipitate. Qualitative analysis showed the red guava fruit content phosphorus.
The quantitative examine did by visible spectrophotometry at maximum wavelength of 713 nm. The result of quantitative analysis get phosphorus value on the sample which blender (without peeled and peeled) is equal to literature, on the other hand phosphorus value on sample which juicer (without peeled and peeld) is not equal to literature. This method has %recovery 98,9%, RSD 0,08%, LOD 0,2602 µg/ml, dan LOQ 0,8672 µg/ml with minimum concentration 5,8802 µg/ml showed that this method has good accuration and precition level.
Pursuant to the result analysis of variance showed that attenuation way and peeling have an effect to this mineral rate, on the other hand pursuant to the result of continuation analyse HSD test showed that attenuation way give significant difference, but peeling factor doesn’t give significant difference.
BAB I PENDAHULUAN
1.1 Latar Belakang
Penyakit Demam Berdarah Dengue (DBD) merupakan salah satu penyakit
yang cukup berbahaya di Indonesia. Tanda-tandanya demam tinggi mendadak
selama 2 – 7 hari, pembesaran hati, penurunan denyut nadi sampai timbul
bintik-bintik merah pada tubuh (Andika, J., G. dan Rejeki, S., C., 2009).
Sampai saat ini belum ada obat yang tepat untuk mengatasi penyakit DBD.
Namun, ada sebagian masyarakat mencoba dengan mengkonsumsi buah jambu
biji merah untuk mengatasi penyakit DBD. Selain mengkonsumsi buahnya dalam
bentuk utuh, masyarakat juga sering mengkonsumsi jambu biji merah dalam
bentuk minuman yang di-blender atau di-juicer.
Kandungan gizi dalam 100 gram buah jambu biji merah adalah 36-50
kalori; 77-86 g air; 2,8-5,5 g serat; 0,9-1,0 g protein; 0,1-0,5 g lemak; 0,43-0,7 g
abu; 9,5-10 g karbohidrat; 9,1-17 mg kalsium; 17,8-30 mg fosfor; 0,3-0,7 mg besi;
200-400 IU vitamin A; 200-400 mg vitamin C; 0,046 mg vitamin B1; 0,03-0,04
mg vitamin B2; 0,6-1,068 mg vitamin B3; dan 82% bagian yang dimakan
(Cahyono, 2010).
Fosfor merupakan salah satu mineral yang dibutuhkan dengan jumlah
lebih kurang 22% dari seluruh mineral yang terdapat dalam tubuh. Di dalam tubuh
mineral ini berada dalam bentuk kalsium fosfat yang mempunyai peranan dalam
metabolisme karbohidrat, lemak dan protein. Sebagai fosfolipid, fosfor merupakan
Fosfor berperan pula dalam mempertahankan keseimbangan asam-basa
(Pudjiadi,2000). Di samping itu, fosfor juga memegang peranan penting dalam
reaksi biokimia yang berkaitan dengan penyimpanan atau pelepasan energi dalam
bentuk Adenin Trifosfat (ATP) (Almatsier, 2004).
Penderita DBD mengkonsumsi buah jambu biji merah dalam bentuk jus
yang disebabkan karena penderita tidak mampu mengkonsumsi buah jambu biji
merah dalam bentuk utuh. Masyarakat yang mengkonsumsi buah jambu biji
merah disarankan untuk tidak mengkonsumsi buahnya dengan biji karena biji
jambu biji merah dapat menyebabkan penyakit usus buntu (Cahyono, 2010).
Penderita DBD memerlukan asupan energi dan cairan yang cukup untuk
memulihkan kesehatannya (Suharso, 2009). Kandungan fosfor yang terdapat
dalam buah jambu biji merah yang berperan dalam penyimpanan energi seperti
disebutkan di atas dan pemberian buah jambu biji merah dalam bentuk jus dapat
mencukupi kebutuhan energi dan cairan penderita DBD sehingga dapat membantu
kepulihannya.
Untuk mengkonsumsi buah jambu biji merah, buahnya dapat dikupas
terlebih dahulu atau dapat juga dikonsumsi tanpa dikupas. Belum ada literatur
yang menyatakan kandungan mineral dalam buah jambu biji merah berbeda antara
buah yang dikonsumsi tanpa dikupas dan dikupas kulitnya.
Sebelum dilakukan penetapan kadar, terlebih dahulu dilakukan destruksi
untuk mengubah fosfor organik menjadi fosfor anorganik. Penetapan kadar fosfor
dapat dilakukan secara spektrofotometri sinar tampak dengan menggunakan tiga
metode, yaitu metode asam vanamolibdofosfor, metode stanium klorida, dan
karena metode ini lebih sederhana dan lebih sensitif (Lim, 1991). Pereaksi warna
yang digunakan terdiri dari campuran larutan H2SO4 5N, Ammonium molibdat
4% b/v, Asam Askorbat 0,1N, dan Kalium Antimonil Tartrat 0,274% b/v yang
diukur pada panjang gelombang 700-723 nm (Lanchasire, 2006).
Berdasarkan uraian di atas, penulis tertarik untuk meneliti kandungan
fosfor yang terdapat pada buah jambu biji merah secara spektrofotometri sinar
tampak dengan metode asam askorbat.
1.2 Perumusan Masalah
1. Apakah kadar fosfor dalam buah jambu biji merah yang diukur dengan
metode spektrofotometri sinar tampak dengan variasi perlakuan cara
penghalusan dan pengupasan sesuai dengan kadar fosfor dalam buah
jambu biji merah yang terdapat dalam literatur?
2. Apakah terdapat perbedaan kadar fosfor antara buah jambu biji merah
yang dihaluskan dengan cara di-blender dan di-juicer tanpa dikupas dan
dikupas kulitnya?
1.3 Hipotesis
1. Kadar fosfor dalam buah jambu biji merah yang diukur dengan metode
spektrofotometri sinar tampak dengan variasi perlakuan cara penghalusan
dan pengupasan sesuai dengan kadar fosfor dalam jambu biji merah yang
terdapat dalam literatur.
2. Terdapat perbedaan kadar fosfor antara buah jambu biji merah yang
dihaluskan dengan cara di-blender dan di-juicer tanpa dikupas dan dikupas
1.4 Tujuan Penelitian
1. Untuk mengetahui apakah kadar fosfor dalam buah jambu biji merah yang
di-blender yang di-juicer tanpa dikupas dan dikupas sesuai dengan kadar
fosfor dalam buah jambu biji merah yang terdapat dalam literatur.
2. Untuk mengetahui perbedaan kadar fosfor antara buah jambu biji merah
yang dihaluskan dengan cara di-blender dan di-juicer tanpa dikupas dan
dikupas kulitnya.
1.5 Manfaat Penelitian
Penelitian ini bermanfaat bagi masyarakat sebagai informasi kandungan
fosfor dalam buah jambu biji merah (Psidium guajava) yang berperan dalam
pembentukan ATP sehingga dapat membantu kepulihan penderita demam
BAB II
TINJAUAN PUSTAKA
2.1 Uraian Tumbuhan
2.1.1 Taksonomi Buah Jambu Biji Merah Kerajaan : Plantae
Divisi : Spermatophyta
Sub divisi : Angiospermae
Kelas : Dicotyledoneae
Bangsa : Myrtales
Suku : Myrtaceae
Marga : Psidium
Jenis : Psidium guajava L.
(Cahyono, 2010).
2.1.2 Deskripsi Buah Jambu Biji Merah
Jambu biji atau bahasa latinnya Psidium guajava L. merupakan jenis
tanaman perdu dengan cabang yang banyak. Tinggi pohon ini rata-rata sekitar
10-12 meter. Tanaman ini berasal dari Amerika Tengah yang dapat tumbuh di dataran
rendah maupun dataran tinggi. Ketinggian tempat yang sesuai untuk tanaman ini
sekitar 1.200 meter dari permukaan laut. Daunnya berbentuk bulat telur, kasar,
dan kusam. Bunganya relatif kecil dan berwarna putih. Besar buahnya sangat
bervariasi, berisi banyak biji kecil-kecil dan ada juga yang tidak mempunyai biji
Buah jambu biji yang banyak digemari oleh masyarakat adalah yang
mempunyai sifat unggul antara lain berdaging lunak dan tebal, rasanya manis,
tidak mempunyai biji, dan buahnya berukuran besar. Terdapat beberapa jenis
jambu biji yang diunggulkan yaitu jambu pasar minggu, jambu bangkok, jambu
palembang, jambu sukun, jambu apel, jambu sari, jambu merah, dan jambu merah
getas (Wirakusumah, 2000).
2.1.3 Macam-macam Jambu Biji
Buah jambu biji memiliki jenis yang banyak antara lain :
1. Jambu biji delima
Jambu biji delima buahnya berbentuk bulat dan bermoncong
dipangkalnya, walaupun kulitnya agak tebal dan banyak bijinya, tapi dengan
dagingnya yang berwarna merah dan rasanya yang manis jenis jambu biji ini
sangat menarik sekali untuk dinikmati.
2. Jambu biji gembos atau jambu biji susu
Jenis yang ini mempunyai bentuk buah bulat agak lonjong dengan
meruncing kepangkalnya. Sama seperti jambu biji delima, kulit jambu jenis ini
juga tebal dan jika buahnya matang berwarna agak kuning, dagingnya berwarna
putih, bijinya tidak banyak, rasanya kurang manis tetapi harum baunya.
3. Jambu biji manis
Bentuk buahnya bulat meruncing ke pangkal, kulit buahnya tipis dan jika
matang berwarna kuning muda. Jenis yang ini juga mempunyai biji yang banyak
4. Jambu biji Perawas (Getas)
Jambu biji perawas berbentuk bulat lonjong dan buahnya lebih besar dari
jenis biasanya, kulitnya agak tebal, bila buahnya matang berwarna kuning,
dagingnya merah, bijinya tidak banyak, rasanya agak asam, baunya harum.
5. Jambu biji Pipit
Berbentuk bulat kecil-kecil, kulitnya tipis, bila matang buahnya berwarna
kuning dan dagingnya berwarna putih, rasanya manis dan harum baunya.
6. Jambu biji sukun
Berbentuk bulat besar dan kulitnya tebal, bila matang buahnya berwarna
kuning, bijinya sedikit bahkan hampir tidak berbiji, tapi rasanya hambar dan
harum baunya (Anonim, 2010).
2.1.4 Kandungan Kimia Jambu Biji Merah
Jambu biji merah banyak mengandung zat kimia : pada buah, daun dan
kulit batang pohonnya mengandung tanin, tapi pada bunganya tidak banyak
mengandung senyawa tersebut. Selain mengandung tanin daun jambu biji merah
juga mengandung zat lain seperti asam oleanolat, minyak atsiri, asam kratogolat,
asam ursolat, asam psidiolat, asam guajaverin dan vitamin (Anonim, 2010).
Kandungan gizi dalam 100 gram buah jambu biji merah adalah 36-50
kalori; 77-86 g air; 2,8-5,5 g serat; 0,9-1,0 g protein; 0,1-0,5 g lemak; 0,43-0,7 g
abu; 9,5-10 g karbohidrat; 9,1-17 mg kalsium; 17,8-30 mg fosfor; 0,3-0,7 mg besi;
200-400 IU vitamin A; 200-400 mg vitamin C; 0,046 mg vitamin B1; 0,03-0,04
mg vitamin B2; 0,6-1,068 mg vitamin B3; dan 82% bagian yang dimakan
2.1.5 Khasiat Jambu Biji
Selain banyak digemari karena buahnya yang manis dan segar jambu biji
juga mempunyai khasiat untuk mengobati berbagai macam penyakit seperti :
maag, diabetes melitus, diare (sakit perut), masuk angin, mencret, sariawan dan
sakit kulit (Cahyono, 2010).
Selain daunnya, buah jambu biji terutama dari jenis berwarna merah sering
digunakan untuk mengobati penyakit demam berdarah. Jus jambu ini dapat
meningkatkan nilai trombosit penderita demam berdarah, namun sampai ini belum
diketahui senyawa yang dapat meningkatkan nilai trombosit (Yuliani et al, 2003).
2.2 Demam Berdarah Dengue
Penyakit Demam Berdarah Dengue (DBD) merupakan salah satu penyakit
yang cukup berbahaya di Indonesia. Tanda-tandanya demam tinggi mendadak
selama 2 – 7 hari, pembesaran hati, penurunan denyut nadi sampai timbul
bintik-bintik merah pada tubuh (Andika, J., G. dan Rejeki, S., C., 2009). Secara umum 2,5 sampai 3 milyar orang beresiko terserang penyakit DBD. Aedes aegypti merupakan vektor epidemi utama (WHO, 2001).
Tidak ada pengobatan yang spesifik ataupun vaksin untuk demam
berdarah. Bila seseorang terserang demam berdarah, berikan cairan sebanyak
mungkin, bawa ke puskesmas terdekat, dan hindarkan dari nyamuk untuk
menghindari penularan. Penyakit ini dapat berlangsung hingga 10 hari, dan
pemulihannya dapat memakan waktu 1 minggu hingga 4 minggu (Chen, Pohan,
2.3 Mineral
Mineral dalam tubuh manusia mengalami proses biokimia untuk
membantu proses fisiologis. Dalam sistem fisiologis manusia, unsur tersebut juga
dibagi menjadi dua bagian yaitu makroelemen, yang ditemukan dalam jumlah
relatif besar (lebih dari 0,005% dari berat badan) dan mikroelemen yang
ditemukan dalam jumlah relatif kecil (kurang dari 0,005% dari berat badan)
(Darmono, 1995).
Di samping itu mineral berperan dalam berbagai tahap metabolisme,
terutama sebagai kofaktor dalam aktivitas enzim-enzim. Yang termasuk mineral
makro antara lain: natrium, klorida, kalium, kalsium, fosfor, magnesium, dan
sulfur (Almatsier, 2004).
Secara tidak langsung, mineral banyak yang berperan dalam proses
pertumbuhan. Peran mineral dalam tubuh kita berkaitan satu sama lainnya, dan
kekurangan atau kelebihan salah satu mineral akan berpengaruh terhadap kerja
mineral lainnya (Poedjiadi, 2006).
2.3.1 Fosfor
Fosfor merupakan mineral kedua terbanyak di dalam tubuh, yaitu 1% dari
berat badan. Kurang lebih 85% fosfor di dalam tubuh terdapat sebagai garam
kalsium fosfat di dalam tulang dan gigi yang tidak dapat larut. Fosfor di dalam
tulang berada dalam perbandingan 1 : 2 dengan kalsium. Fosfor selebihnya
terdapat di dalam semua sel tubuh, separuhnya di dalam otot dan di dalam cairan
ekstraseluler. Sebagai fosfolipid, fosfor merupakan komponen struktural dinding
berkaitan dengan penyimpanan atau pelepasan energi dalam bentuk Adenin
Trifosfat (ATP) (Almatsier, 2004).
Fosfor mempunyai peranan dalam metabolisme karbohidrat, lemak, dan
protein, sebagai fosfolipid, fosfor merupakan komponen esensial bagi banyak sel
dan merupakan alat transport asam lemak. Fosfor berperan pula dalam
mempertahankan keseimbangan asam-basa (Pudjiadi, 2000).
Pada umumnya bahan makanan yang mengandung banyak kalsium
merupakan juga sumber fosfor, seperti susu, keju, daging, ikan, telur, dan serelia.
Akan tetapi fosfor dalam serelia pada umumnya terdapat dalam bentuk asam
fosfat yang dapat mengikat kalsium hingga terbentuk komponen yang tidak dapat
dicerna dan diserap. Biasanya kira-kira 70% dari fosfor yang berada dalam
makanan dapat diserap oleh tubuh. Penyerapan akan lebih baik bila fosfor dan
kalsium dimakan dalam jumlah yang sama (Poedjiadi, 2006).
Fosfor dapat diabsorpsi secara efisien sebagai fosfor bebas di dalam usus
setelah dihidrolisis dan dilepas dari makanan. Bila konsumsi fosfor rendah, taraf
absorpsi dapat mencapai 90% dari konsumsi fosfor. Fosfor dibebaskan dari
makanan oleh enzim alkalin fosfatase di dalam mukosa usus halus dan diabsorpsi
secara aktif dan difusi pasif. Sebagian besar fosfor di dalam darah terutama
terdapat sebagai fosfat anorganik atau sebagai fosfolipida (Almatsier, 2004).
Faktor-faktor makanan lain yang menghalangi absorpsi fosfor adalah
magnesium dan antasid yang mengandung aluminium, karena membentuk garam
yang tidak larut dalam air. Angka kecukupan fosfor rata-rata sehari adalah
2.3.2 Kekurangan Fosfor
Konsumsi pangan kurang fosfor jarang dijumpai pada manusia. Oleh
karena peranannya yang sangat penting dalam metabolisme pada jaringan hewan
dan tanaman, maka mineral ini umumnya terdapat dalam setiap bahan makanan
(Almatsier, 2004).
Adakalanya gejala kekurangan fosfor terdapat pada individu yang dapat
nutrisi parenteral lama atau mereka yang memakai sangat banyak antasida
(Pudjiadi, 2000). Aluminium hidroksida yang terdapat dalam antasida dapat
mengikat fosfor sehingga tidak dapat diabsorpsi. Kekurangan fosfor menyebabkan
kerusakan tulang. Gejalanya adalah rasa lelah, kurang nafsu makan dan kerusakan
tulang. Bayi prematur juga dapat menderita kekurangan fosfor karena cepatnya
pembentukan tulang sehingga kebutuhan fosfor tidak bisa dipenuhi oleh ASI
(Almatsier, 2004).
2.3.3 Kelebihan Fosfor
Kelebihan fosfor karena makanan jarang terjadi. Bila kadar fosfor darah
terlalu tinggi, ion fosfat akan mengikat kalsium sehingga dapat menimbulkan
kejang (Almatsier, 2004).
2.4 ATP (Adenosine Tri Phosphate)
ATP dan produk hidrolisis selanjutnya, adenosine diphosphate (ADP) dan
adenosine monophosphate (AMP) merupakan nukleotida. Nukleotida terdiri dari
basa purin dan pirimidin heterosiklik, gula dengan 5-karbon, dan satu atau lebih
gugus fosfat. Di dalam ATP, ADP, dan AMP basa yang terkandung adalah purin
Adenosin trifosfat adalah fosfat berenergi tinggi yang mengikat energi
yang dilepas oleh oksidasi hasil pencernaan. Sebagai energi kimia ATP digunakan
untuk beberapa fungsi spesifik dalam tubuh dimana molekulnya dipecah terlebih
dahulu menjadi adenosin difosfat (ADP) dan Pi. Apa yang terjadi selanjutnya
adalah tubuh kembali membentuk energi kimia dari pencernaan makanan dan
ADP kembali mengikat Pi (Holum, 1983).
Adenosin trifosfat berperan sebagai senyawa antara yang menghubungkan
reaksi kimia penghasil energi dan reaksi yang membutuhkan energi. Selama
katabolisme, atau pemecahan dari bahan bakar sel berenergi tinggi, sebagian di
antara energi bebasnya diambil, untuk membuat ATP dari adenosin difosfat dan
fosfat (Pi), suatu proses yang memerlukan input energi bebas. ATP lalu
memberikan sejumlah energi kimianya kepada proses-proses yang memerlukan
energi dengan memecah diri menjadi ADP dan fosfat. ATP, karenanya berperan
sebagai pembawa energi kimia dari proses-proses penghasil energi menuju
aktivitas sel dasar yang memerlukan energi (Lehninger, 1982).
2.5 Spektrofotometri
Spektrofotometri serapan merupakan pengukuran satu interaksi antara
radiasi elektromagnetik dan molekul atau atom dari suatu zat kimia. Teknik yang
sering digunakan dalam analisis farmasi meliputi spektroskopi serapan ultraviolet,
sinar tampak, infra merah, dan serapan atom (Ditjen POM, 1995). Keuntungan
utama dari metode spektrofotometri, yaitu dapat menetapkan kadar suatu zat yang
sangat kecil (Basset, 1991).
Spektrofotometri ultraviolet-visibel adalah suatu metode pengukuran
diabsorpsi oleh sampel. Sinar ultraviolet dan cahaya tampak memiliki energi yang
cukup untuk mempromosikan elektron pada kulit terluar ke tingkat energi yang
lebih tinggi. Spektrofotometer ultraviolet-visibel biasanya digunakan untuk
molekul dan ion organik atau kompleks di dalam larutan. Spektrum
ultraviolet-visibel sangat berguna untuk pengukuran secara kuantitatif. Konsentrasi dari
analit di dalam larutan bisa ditentukan dengan mengukur absorbansi pada panjang
gelombang tertentu dengan menggunakan hukum Lambert-Beer. Sinar ultraviolet
berada pada panjang gelombang 200-400 nm, sedangkan sinar tampak berada
pada panjang gelombang 400-800 nm (Dachriyanus, 2004).
Panjang gelombang cahaya UV atau cahaya tampak bergantung pada
mudahnya promosi elektron. Molekul-molekul yang memerlukan lebih banyak
energi untuk promosi elektron, akan menyerap pada panjang gelombang yang
lebih pendek. Molekul yang memerlukan energi yang lebih sedikit akan menyerap
pada panjang gelombang yang lebih besar. Senyawa yang menyerap cahaya dalam
daerah tampak mempunyai elektron yang lebih mudah dipromosikan daripada
senyawa yang menyerap pada panjang gelombang UV yang lebih pendek
(Fessenden and Fessenden, 1982).
Warna sinar tampak dapat dihubungkan dengan panjang gelombangnya.
Sinar putih mengandung radiasi pada semua panjang gelombang di daerah sinar
tampak. Sinar pada panjang gelombang tunggal (radiasi monokromatik) dapat
dipilih dari sinar putih. Spektrofotometer yang sesuai untuk pengukuran di daerah
spektrum ultraviolet dan sinar tampak terdiri atas suatu sistem optik dengan
kemampuan menghasilkan sinar monokromatis dalam jangkauan panjang
Alat spektrofotometri pada dasarnya terdiri atas sumber sinar,
monokromator, tempat sel untuk zat yang diperiksa, detektor, penguat arus, dan
alat ukur atau pencatat. Spektrofotometer dapat bekerja secara otomatik ataupun
tidak, dan dapat mempunyai sistem sinar tunggal atau ganda (Ditjen POM, 1979).
Sebagai sumber cahaya biasanya digunakan lampu hidrogen atau
deuterium untuk pengukuran UV dan lampu tungsten untuk pengukuran pada
cahaya tampak. Panjang gelombang dari sumber cahaya akan dibagi oleh pemisah
atau monokromator (Dachriyanus, 2004).
Analisis kuantitatif secara spektrofotometri dapat dilakukan dengan
metode regresi dan pendekatan.
1. Metode Regresi
Analisis kuantitatif dengan metode regresi dengan menggunakan
persamaan garis regresi yang didasarkan pada harga serapan dan konsentrasi baku
yang dibuat dalam berbagai konsentrasi, paling sedikit menggunakan lima
konsentrasi yang meningkat yang dapat memberikan serapan linier, kemudian
diplot menghasilkan suatu kurva kalibrasi. Konsentrasi suatu sampel dapat
dihitung berdasarkan kurva tersebut (Holme and Peck, 1983).
2. Metode Pendekatan
Analisis kuantitatif dengan cara ini dilakukan dengan membandingkan
serapan baku yang konsentrasinya diketahui dengan serapan sampel. Konsentrasi
sampel dapat dihitung melalui perbandingan Cs = As.Cb/Ab dimana As = serapan
sampel, Cs = konsentrasi sampel, Ab = serapan baku, dan Cb = konsentrasi baku
2.6 Parameter Validasi
Pensahihan adalah kerja yang dicatat dalam dokumen untuk membuktikan
bahwa prosedur analisis yang diuji akan dapat memenuhi fungsi sesuai dengan
tujuannya dengan konsisten dan betul-betul memberikan hasil seperti yang
diharapkan. Tujuan pensahihan adalah agar prosedur analisis tersebut diketahui
akurasi dan variabilitasnya, gangguan yang mungkin ada teridentifikasi dan
diketahui pula kespesifikan, presisi, serta kepekaannya (limit deteksi). Parameter
analisis khas yang ditentukan pada pensahihan adalah akurasi, presisi,
kespesifikan, limit deteksi, kelinieran, dan rentang (Satiadarma, dkk., 2004).
Akurasi dari suatu metode analisis adalah kedekatan nilai hasil uji yang
diperoleh dengan prosedur tersebut dari harga yang sebenarnya. Akurasi
merupakan ukuran ketepatan posedur analisis (Satiadarma, dkk., 2004).
Presisi dari suatu metode analisis adalah derajat kesesuaian di antara
masing-masing hasil uji, jika prosedur analisis diterapkan berulangkali pada
sejumlah cuplikan yang diambil dari satu sampel homogen. Presisi dinyatakan
sebagai deviasi standar atau deviasi standar relatif (koefisien variasi) (Satiadarma,
dkk., 2004).
Kespesifikan dari suatu metode analisis adalah kemampuannya untuk
mengukur kadar analit secara khusus dengan akurat, di samping komponen lain
yang terdapat dalam matriks sampel. Kespesifikan seringkali dinyatakan sebagai
derajat bias dari hasil analisis sampel yang mengandung pencemar, hasil
degradasi, senyawa sejenis yang ditambahkan atau komponen matriks,
dibandingkan dengan hasil uji sampel analit tanpa zat tambahan (Satiadarma, dkk,
Limit deteksi dari suatu metode analisis adalah nilai parameter uji batas,
yaitu konsentrasi analit terendah yang dapat dideteksi, tetapi tidak dikuantitasi
pada kondisi percobaan yang dilakukan. Limit deteksi dinyatakan dalam
konsentrasi analit (persen, bagian per milyar) dalam sampel (Satiadarma, dkk.,
2004).
Limit kuantitasi dari suatu metode analisis adalah nilai parameter
penentuan kuantitatif senyawa yang terdapat dalam konsentrasi rendah dalam
matriks. Limit kuantitasi adalah konsentrasi analit terendah dalam sampel yang
dapat ditentukan dengan presisi dan akurasi yang dapat diterima pada kondisi
eksperimen yang ditentukan. Limit kuantitasi dinyatakan dalam konsentrasi analit
(persen, bagian per milyar) dalam sampel (Satiadarma, dkk., 2004).
Kelinieran suatu metode analisis adalah kemampuan untuk menunjukkan
bahwa nilai hasil uji langsung atau setelah diolah secara matematika, proporsional
dengan konsentrasi analit dalam sampel dalam batas rentang konsentrasi tertentu.
Kelinieran dinyatakan sebagai varians di sekitar landaian garis regresi yang
dihitung menurut hubungan matematika yang mapan dari hasil uji sampel yang
mengandung analit dengan konsentrasi yang bervariasi (Satiadarma, dkk., 2004).
Rentang suatu metode analisis adalah interval antara batas konsentrasi
tertinggi dan konsentrasi terendah analit yang terbukti dapat ditentukan
menggunakan prosedur analisis, dengan presisi, akurasi dan kelinieran yang
memadai. Rentang biasanya dinyatakan dalam satuan yang sama dengan hasil uji
(persen, bagian per sejuta) (Satiadarma, dkk., 2004).
Penentuan linieritas suatu prosedur analisis dilakukan dengan perlakuan
analit dalam rentang konsentrasi yang dituntut oleh prosedur. Perlakuan tersebut
pada umumnya adalah perhitungan garis regresi dengan metode least squares
lawan konsentrasi analit. Untuk mendapatkan hasil proporsional antara penentuan
kadar dan konsentrasi sampel, kadang-kadang data uji harus mendapatkan
transformasi matematika sebelum regresi. Landaian garis regresi dan variansnya
memberikan ukuran matematika dari linearitas (Satiadarma, dkk., 2004).
Rentang dari prosedur analisis disahihkan dengan jalan memverifikasi data
yang menunjukkan bahwa prosedur analisis menghasilkan presisi, akurasi, dan
linieritas yang dapat diterima, jika diterapkan pada sampel yang mengandung
analit dengan konsentrasi analit di ujung rentang dan di dalam rentang
BAB III
METODE PENELITIAN
3.1 Lokasi dan Waktu Penelitian
Penelitian dilakukan di dua laboratorium, yaitu penyiapan dan pengukuran
kadar sampel dilakukan di Laboratorium Kimia Farmasi Kualitatif Fakultas
Farmasi Universitas Sumatera Utara, sedangkan pengabuan sampel dilakukan di
Laboratorium Penelitian FMIPA Universitas Sumatera Utara pada bulan Januari
sampai Maret 2011.
3.2 Bahan-bahan 3.2.1 Sampel
Pengambilan sampel dilakukan secara acak dengan menggunakan metode
sampling purposif, yaitu tanpa membedakan asal buah jambu biji merah. Sampel
yang digunakan dalam penelitian ini adalah buah jambu biji merah (Psidium
guajava L.) yang diperoleh dari Berastagi Supermarket.
3.2.2 Pereaksi
Bahan kimia yang digunakan kecuali dinyatakan lain adalah bahan
berkualitas untuk analisis (p.a.) merek dagang E.Merck, yaitu asam nitrat 65%
b/v, ammonium molibdat, asam sulfat 96% v/v, asam askorbat, kalium dihidrogen
fosfat, kalium antimonil tartrat, dan air suling buatan Laboratorium Penelitian
FMIPA Universitas Sumatera Utara.
3.3 Alat-alat
Alat yang digunakan antara lain, Spektrofotometer UV/Visibel (UV mini
Ltd.Shenstone), Oven, Hot plate, blender, juicer, krus porselen, botol kaca, dan
alat-alat gelas (Pyrex).
3.4 Pembuatan Pereaksi 3.4.1 Larutan HNO3 5N
Larutan HNO3 65% b/v sebanyak 350 ml diencerkan dengan air suling
hingga 1000 ml (Ditjen POM, 1979).
3.4.2 Larutan H2SO4 5N
Diukur 70 ml H2SO4 96% v/v, dimasukkan perlahan-lahan melalui dinding
labu tentukur 500 ml yang telah berisi air suling setengahnya. Dicukupkan
volumenya dengan air suling hingga garis tanda (Lancashire, 2006).
3.4.3 Larutan Ammonium Molibdat 4% b/v
Ditimbang seksama 20 g ammonium molibdat. Dilarutkan dalam labu
tentukur 500 ml dengan air suling dan dicukupkan volumenya dengan air suling
hingga garis tanda (Lancashire, 2006).
3.4.4 Larutan Asam Askorbat 0,1N
Ditimbang seksama 0,88 g asam askorbat dan dilarutkan dalam labu
tentukur 50 ml dengan air suling dan dicukupkan volumenya dengan air suling
hingga garis tanda (Lancashire, 2006).
3.4.5 Larutan Kalium Antimonil Tartrat 0,274% b/v
Ditimbang seksama 0,274 g Kalium Antimonil Tartrat. Dilarutkan dalam
labu tentukur 100 ml dengan air suling dan dicukupkan volumenya dengan air
3.4.6 Larutan Pereaksi Warna Fosfor
Dicampurkan 500 ml H2SO4 5 N, 150 ml Ammonium molibdat 4% b/v,
300 ml Asam Askorbat 0,1 N, dan 50 ml Kalium Antimonil Tatrat 0,274% b/v
(Lancashire, 2006).
3.5 Rancangan Penelitian
Cara penelitian dilakukan berdasarkan bagan berikut ini:
Metode penelitian yang dilakukan adalah metode eksperimental untuk
memeriksa kadar fosfor pada buah jambu biji merah yang diperoleh dari Berastagi
Supermarket berdasarkan pengaruh antara variabel bebas dengan variabel terikat.
Dalam penelitian ini yang menjadi variabel terikat adalah buah jambu biji merah
(Psidium guajava L.), sedangkan yang menjadi variabel bebas adalah cara
penghalusan dan pengupasan. Penelitian ini menggunakan rancangan faktorial
dengan 2 faktor perlakuan, yaitu:
1. Faktor A : Cara penghalusan dengan 2 variasi
A1 : di-blender
A2 : di-juicer
2. Faktor B : pengupasan dengan 2 variasi
Sehingga kombinasi perlakuan (t) = m faktor A x n faktor B
= m.n kombinasi perlakuan
= 2 x 2 = 4
Dengan replikasi (r) setiap kombinasi perlakuan, yaitu : (t-1) (r-1) ≥ 15
(4-1) (r-1) ≥ 15
r ≥ 6
Ini berarti bahwa replikasi (r) dapat dilakukan minimal sebanyak 6 kali. Replikasi
ditandai sebagai berikut:
R1 : Replikasi 1 R4 : Replikasi 4
R2 : Replikasi 2 R5 : Replikasi 5
R3 : Replikasi 3 R6 : Replikasi 6
Jadi, rancangan penelitian ini adalah rancangan faktorial desain 2 x 2 dan setiap
kombinasi perlakuan dilakukan 6 kali replikasi.
Jumlah unit penelitian = m faktor A x n faktor B x r ulangan
= m.n.r
= 2 x 2 x 6
= 24
Keterangan : m = jumlah variasi faktor A
n = jumlah variasi faktor B
r = jumlah ulangan
Atas dasar kondisi yang homogen, randomisasi dilakukan secara lengkap.
Hasil randomisasi kombinasi perlakuan dari cara penghalusan dan pengupasan
Tabel 1. Randomisasi Kombinasi Perlakuan dari Cara Penghalusan dan Pengupasan dengan 6 Kali Replikasi
1
Model matematika rancangan penelitian ini adalah sebagai berikut:
Y = µ + τ + ε
= µ + αi + βj + αβij + ε
Keterangan: µ = Nilai rerata (mean)
τ = Pengaruh faktor kombinasi perlakuan (α + β + αβ)
αi = Pengaruh faktor A (cara penghalusan) ke-I (i = 1,2)
βj = Pengaruh faktor B (pengupasan) ke-j (j = 1,2)
αβij = Pengaruh interaksi cara penghalusan ke-i dengan
pengupasan ke-j
ε = Pengaruh galat (experimental error)
Model rancangan ini bertujuan untuk meneliti pengaruh-pengaruh faktor utama
dan interaksi dengan ketelitian yang sama (Hanafiah, 1995).
3.6 Prosedur Penelitian 3.6.1 Proses Destruksi Kering
Buah jambu biji merah sebanyak ± 1kg dicuci bersih, lalu dikeringkan,
50 g dalam krus porselen, dipanaskan di atas hot plate untuk menguapkan
kandungan air yang terdapat pada buah jambu biji merah sampai kering dan
mengarang. Diabukan di tanur dengan temperatur awal 100o C dan perlahan-lahan
temperatur dinaikkan menjadi 600oC dengan interval 25o C setiap 5 menit.
Pengabuan dilakukan selama 48 jam dan dibiarkan dingin pada desikator.
Prosedur yang sama dilakukan pada buah jambu biji merah yang
di-blender dan dikupas kulitnya. Destruksi kering juga dilakukan untuk buah jambu
biji merah yang dihaluskan dengan cara di-juicer tanpa dikupas dan yang dikupas
kulitnya. Hasil dalam bentuk Oksida Fosfor (P2O5).
Hasil destruksi yang berupa P2O5 dilarutkan dalam 10 ml HNO3 5N
kemudian dipanaskan di atas hot plate hingga larutan menjadi bening. Kemudian
hasilnya dimasukkan ke dalam labu tentukur 100 ml dan krus porselen dibilas
sebanyak 3 kali. Setelah itu dicukupkan volumenya dengan air suling hingga garis
tanda. Lalu disaring dengan kertas saring Whatman N0. 42 dengan membuang 10
ml larutan pertama hasil penyaringan. Larutan ini digunakan untuk analisis
kualitatif dan analisis kuantitatif fosfor (Chapple dan Nick, 1991). Hasil yang
diperoleh dalam bentuk PO43-. Gambar penguapan kandungan air, hasil
pengarangan, dan hasil pengabuan sampel dapat dilihat pada Lampiran 2.
Flowsheet dekstruksi kering dapat dilihat pada Lampiran 3.
3.6.2 Analisis Kualitatif Fosfor
Analisis kualitatif fosfor menurut Vogel (1985), dapat dilakukan dengan
a. Ke dalam tabung reaksi dimasukkan 5 ml sampel hasil destruksi kering berupa
PO43-, ditambah pereaksi ammonium molibdat 4% b/v ± 2 ml, dikocok dan
didiamkan, maka akan terbentuk endapan kuning.
b. Ke dalam tabung reaksi dimasukkan 5 ml sampel hasil destruksi kering berupa
PO43-, lalu ditambahkan larutan barium klorida 4% b/v ± 1 ml. Terbentuk
endapan putih.
Gambar hasil kualitatif fosfor dapat dilihat pada Lampiran 4.
3.6.3 Analisis Kuantitatif Fosfor
3.6.3.1 Pembuatan Larutan Induk Baku (LIB) KH2PO4
Ditimbang 1,1 g KH2PO4 yang telah dikeringkan di dalam oven ± 2 jam
dengan suhu 105oC, kemudian dimasukkan ke dalam labu tentukur 250 ml,
ditambahkan 12,5 ml larutan HNO3 5 N, dikocok hingga larut, dicukupkan
volumenya dengan air suling hingga garis tanda. Diperoleh konsentrasi fosfor
pada Larutan Induk Baku ( LIB) I adalah 1000 µ g/ml.
Dari LIB I dipipet 10 ml, dimasukkan ke dalam labu tentukur 250 ml,
dicukupkan volumenya dengan air suling hingga garis tanda. Diperoleh
konsentrasi fosfor pada Larutan Induk Baku (LIB) II adalah 40 µg/ml.
3.6.3.2 Penentuan Waktu Kerja
Dari LIB II dipipet 20 ml, dimasukkan ke dalam labu tentukur 100 ml,
ditambahkan air suling sehingga volume larutan menjadi 50 ml, ditambahkan 13
ml larutan pereaksi warna fosfor, dikocok, dicukupkan volume dengan air suling
hingga garis tanda (konsentrasi 8 µ g/ml), dan didiamkan kemudian diukur
serapan pada λ maksimum 713 nm mulai menit ke-5 hingga menit tertentu dengan
3.6.3.3 Pembuatan Kurva Serapan Larutan KH2PO4
Dari LIB II dipipet 20 ml, dimasukkan ke dalam labu tentukur 100 ml,
ditambahkan air suling sehingga volume larutan menjadi 50 ml, ditambahkan 13
ml larutan pereaksi warna fosfor, dikocok, dicukupkan volume dengan air suling
hingga garis tanda (konsentrasi 8 µ g/ml), dan didiamkan kemudian diukur
serapan pada λ maksimum 700-713 nm pada waktu kerja yang diperoleh.
3.6.3.4 Penentuan Kurva Kalibrasi Larutan Baku Fosfor
Dari LIB I tersebut dipipet 10 ml, 15 ml, 20 ml, 25 ml, dan 30 ml untuk
mendapatkan konsentrasi 4 µg/ml, 6 µg/ml, 8 µg/ml, 10 µg/ml, dan 12 µg/ml,
dimasukkan ke dalam labu tentukur 100 ml, ditambahkan air suling sehingga
volume masing-masing larutan menjadi 50 ml, ditambahkan 13 ml larutan
pereaksi warna fosfor, dikocok, dicukupkan volumenya dengan air suling hingga
garis tanda, kemudian didiamkan. Diukur serapan pada λ maksimum yang
diperoleh pada waktu kerja yang diperoleh.
3.6.4 Analisis Fosfor Dalam Sampel Buah Jambu Biji Merah
Larutan sampel dipipet 10 ml, dimasukkan ke dalam labu tentukur 100 ml,
ditambahkan akuades sehingga volume larutan menjadi 50 ml, ditambahkan 13 ml
larutan pereaksi warna fosfor, dikocok, dicukupkan volume dengan air suling
hingga garis tanda, kemudian didiamkan. Diukur serapan pada λ maksimum yang
diperoleh pada waktu kerja yang diperoleh. Nilai serapan yang diperoleh berada di
dalam rentang nilai kurva kalibrasi larutan baku, Dengan demikian konsentrasi
fosfor dapat dihitung berdasarkan persamaan garis regresi linier dari kurva
kalibrasi.
Kadar (µg/g) =
Keterangan : C = Konsentrasi larutan sampel setelah pengenceran (µg/ml)
V = Volume labu kerja (ml)
Fp = Faktor pengenceran
W = Berat sampel (g)
Contoh perhitungan hasil penetapan kadar fosfor dalam sampel dapat dilihat pada
Lampiran 8 dan data hasil analisis kadar fosfor seluruhnya untuk setiap kombinasi perlakuan dengan 6 kali replikasi dapat dilihat pada Lampiran 9.
Kadar fosfor sebenarnya dalam sampel dapat dihitung dengan rumus:
µ = x ± (t(α/2, dk) x SD/
Keterangan: x : kadar rata-rata sampel
SD : Standar Deviasi
dk : derajat kebebasan (dk = n-1)
α : tingkat kepercayaan
n : banyak data
(Walpole, 1995). Perhitungan kadar fosfor sebenarnya dalam sampel dapat dilihat
pada Lampiran 10.
3.6.5 Prosedur Uji Perolehan Kembali
Uji perolehan kembali dilakukan dengan metode penambahan larutan
standar (standard addition method). Pertama-tama dilakukan penentuan kadar
fosfor dalam sampel , selanjutnya dilakukan penentuan kadar fosfor dalam sampel
setelah penambahan larutan standar dengan konsentrasi tertentu (Harmita, 2004).
100% dari kadar fosfor dalam sampel. Konsentrasi larutan standar fosfor yang
digunakan adalah 1000 µg/ml.
Sampel buah jambu biji merah ditimbang ± 50 g dalam krus porselen, lalu
ditambahkan larutan standar fosfor. Kemudian dilanjutkan dengan prosedur
destruksi sama seperti prosedur destruksi untuk fosfor. Selanjutnya dilakukan cara
yang sama seperti 3.6.4.
Uji perolehan kembali dilakukan terhadap sampel yang sama dan
dianalisis dengan cara yang sama dengan pengerjaan sampel awal. Uji perolehan
kembali dilakukan untuk mengetahui ketepatan metode yang digunakan. Persen
recovery dapat dihitung dengan persamaan sebagai berikut:
% recovery
Perhitungan kadar fosfor dalam buah jambu biji merah setelah penambahan
larutan standar dan perhitungan uji perolehan kembali dapat dilihat pada
Lampiran 11 dan data %recovery dapat dilihat pada Lampiran 12. 3.6.6 Simpangan Baku Relatif
Keseksamaan atau presisi diukur sebagai simpangan baku relatif (RSD)
atau koefisien variasi. Keseksamaan atau presisi merupakan ukuran yang
menunjukkan derajat kesesuaian antara hasil uji individual ketika suatu metode
dilakukan secara berulang untuk sampel yang homogeny. Nilai simpangan baku
relatif yang memenuhi persyaratan menunjukkan adanya keseksamaan metode
Adapun rumus untuk menghitung simpangan baku relatif (Harmita, 2004)
adalah:
RSD = x 100%
3.6.7 Analisis Data secara Statistik
Pada penelitian dilakukan analisis statistik dari data yang didapatkan
dengan menggunakan analisis variansi (analysis of variance / ANAVA) yang
bertujuan untuk mengetahui apakah ada pengaruh dari perlakuan cara penghalusan
dan pengupasan terhadap kadar fosfor pada buah jambu biji merah. Data hasil
ANAVA dapat dilihat pada Lampiran 13. Untuk mengetahui beda pengaruh
masing-masing variasi perlakuan dilakukan analisis lanjutan, yaitu uji HSD.
3.6.8 Penentuan Batas/Limit Deteksi dan Batas/Limit Kuantitasi
Penentuan batas deteksi dapat dihitung berdasarkan pada standar deviasi
(SD) respon dan kemiringan (slope) linieritas baku (Harmita, 2004) yang dapat
dihitung dengan rumus:
(SY) =
LOD =
Sedangkan untuk penentuan batas kuantitasi dapat digunakan rumus:
LOQ =
BAB IV
HASIL DAN PEMBAHASAN
4.1 Destruksi Kering
Fosfor organik setelah didestruksi berubah menjadi fosfor oksida dalam
valensi 3, yaitu P2O3 dan akhir destruksi akan terbentuk fosfor oksida valensi 5,
yaitu P2O5 yang bila dilarutkan dalam HNO3 5 N akan menjadi PO43-.
4.2 Analisis Fosfor pada Buah Jambu Biji Merah 4.2.1 Analisis Kualitatif Fosfor
Analisis kualitatif fosfor dalam sampel dilakukan dengan:
1. Reaksi menggunakan ammonium molibdat 4%, terbentuk endapan kuning.
2. Reaksi menggunakan BaCl2, terbentuk endapan putih.
Hal ini menunjukkan bahwa buah jambu biji merah mengandung fosfor.
4.2.2 Analisis Kuantitatif Fosfor
4.2.2.1 Penentuan Panjang Gelombang Serapan Maksimum Senyawa Kompleks Fosfor Molibdat
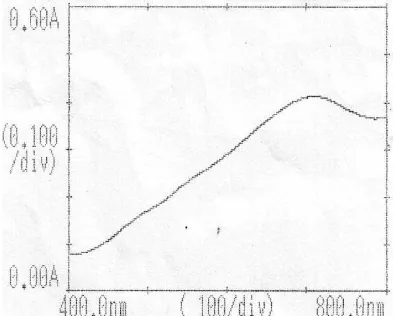
Kurva penentuan λ serapan maksimum senyawa kompleks fosfor molibdat
dapat dilihat pada Gambar 1. Dari gambar tersebut terlihat λ gelombang serapan
maksimum yang diperoleh dalam penelitian ini adalah 713 nm. Kompleks
fosfomolibdat memberikan serapan pada daerah sinar tampak pada panjang
Gambar 1. Kurva Serapan Senyawa Fosfor pada Konsentrasi 8 µg/ml
4.2.2.2 Penentuan Waktu Kerja Kompleks Fosfor Molibdat pada Panjang Gelombang Maksimum 713 nm
Untuk menentukan waktu kerja senyawa kompleks fosfor molibdat,
digunakan larutan baku KH2PO4 dengan konsentrasi 8 µg/ml dan diukur
serapannya pada λ 713 nm pada menit ke-5 sampai menit ke-74. Hasil pengukuran
menunjukkan serapan stabil pada menit ke-20 hingga menit ke-25. Data
pengukuran waktu kerja kompleks fosfor molibdat dapat dilihat pada Lampiran
5.
4.2.2.3 Kurva Kalibrasi Fosfor
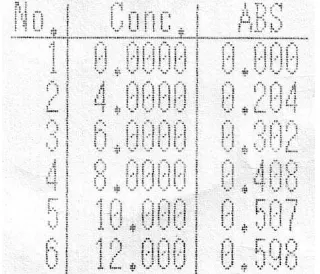
Kurva kalibrasi fosfor diperoleh dengan cara mengukur serapan dari
larutan standar fosfor dengan konsentrasi larutan kerja yang berbeda, yaitu 0
µg/ml, 4 µg/ml, 6 µg/ml, 8 µg/ml, 10 µg/ml, dan 12 µg/ml. Berdasarkan hasil
pengukuran serapan vs konsentrasi larutan standar tersebut diperoleh kurva
Gambar 2. Serapan Kurva Kalibrasi Larutan Standar Fosfor pada Panjang Gelombang 713 nm
Gambar 3. Kurva Kalibrasi Larutan Standar Fosfor pada Panjang Gelombang 713 nm
Berdasarkan data kurva kalibrasi di atas, diperoleh persamaan regresi
untuk larutan standar fosfor, yaitu y = 0,0501 x + 0,0025 dengan nilai r (koefisien
korelasi) 0,9999. Nilai koefisien korelasi ≥ 0,95 menunjukkan bukti adanya
korelasi linier yang menyatakan adanya hubungan antara x dan y (Shargel dan
Andrew, 1988). Kurva ini menunjukkan terdapat korelasi yang positif antara
konsentrasi (x) dengan serapan (y) yang berarti meningkatnya konsentrasi akan
meningkat pula serapannya (Sudjana, 2005). Perhitungan persamaan regresi dapat
4.2.2.4 Analisis Kadar Fosfor pada Buah Jambu Biji Merah
Larutan hasil destruksi yang mengandung PO43- diukur dengan
spektrofotometer UV-Vis pada λ = 713 nm, pengukuran menghasilkan serapan
dan konsentrasi dapat dihitung berdasarkan persamaan garis regresi.
Hasil analisis fosfor pada buah jambu biji merah yang diberi perbedaan
perlakuan dalam hal cara penghalusan dan pengupasan menunjukkan hasil yang
berbeda. Pengukuran fosfor dengan Spektrofotometri Sinar Tampak dilakukan
dengan penambahan 13 ml larutan pereaksi warna fosfor. Larutan pereaksi warna
yang digunakan campuran asam sulfat, ammonium molibdat, asam askorbat, dan
kalium antimonil tartrat. Tujuan penambahan larutan ini adalah untul membentuk
senyawa berwarna biru dan diukur serapannya pada λ maksimum 713 nm.
Hasil destruksi yang berupa P2O5 yang diubah menjadi PO43- bereaksi
dengan ammonium molibdat yang berasal dari campuran larutan pereaksi warna
yang terdiri dari asam sulfat, ammonium molibdat, asam askorbat, dan kalium
antimonil tartrat membentuk senyawa kompleks fosfomolibdat. Senyawa
kompleks ini akan menghasilkan senyawa berwarna biru yang stabil selama 6
menit yang diukur pada menit ke-20 pada λ 713 nm.
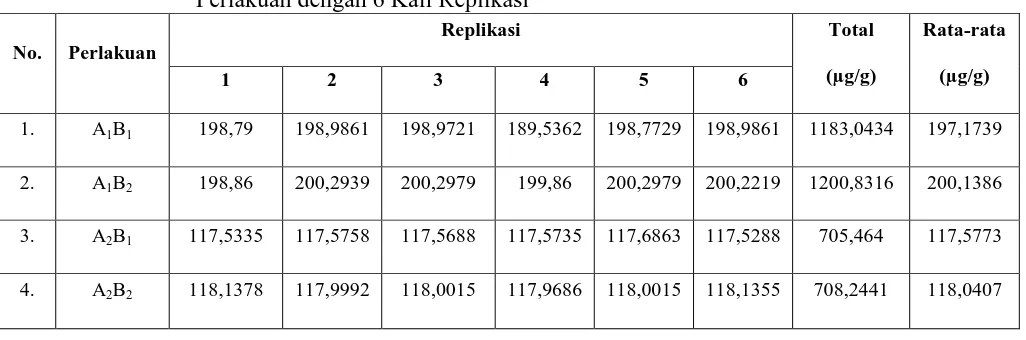
Tabel 2. Hasil Kadar Total dan Kadar Rata-rata Fosfor Pada Setiap Kombinasi Perlakuan dengan 6 Kali Replikasi
Keterangan:
A1B1 : Di-blender; tanpa dikupas A1B2 : Di-blender; Dikupas A2B1 : Di-juicer; tanpa dikupas A2B2 : Di-juicer; Dikupas
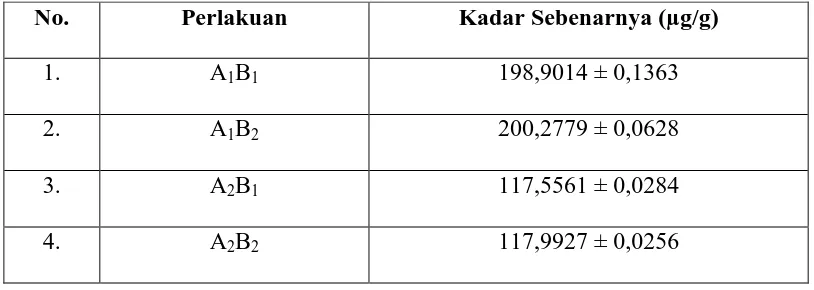
Tabel 3. Kadar Fosfor Sebenarnya dalam Buah Jambu Biji Merah
No. Perlakuan Kadar Sebenarnya (µg/g)
1. A1B1 198,9014 ± 0,1363
2. A1B2 200,2779 ± 0,0628
3. A2B1 117,5561 ± 0,0284
4. A2B2 117,9927 ± 0,0256
Tabel di atas menunjukkan bahwa sampel mengandung fosfor dengan
kadar yang berbeda-beda untuk setiap kombinasi perlakuan. Menurut US
Department Agriculture dalam buku Cahyono (2010), kadar fosfor dalam buah
jambu biji merah sebesar 178 – 300 µg/g. Hasil di atas menunjukkan bahwa
kadar fosfor yang dihaluskan dengan cara di-blender lebih tinggi dibandingkan
dengan kadar fosfor yang dihaluskan dengan cara di-juicer. Hal ini disebabkan
karena semua bagian buah (kecuali biji) yang di-blender ikut terdestruksi,
sedangkan yang di-juicer hanya sari buah saja yang ikut terdestruksi. Selain itu,
hasil analisis juga menunjukkan bahwa kadar fosfor pada buah yang dihaluskan
baik dengan cara di-blender maupun di-juicer tanpa dikupas lebih rendah
dibandingkan dengan kadar fosfor pada buah yang dikupas. Hal ini menunjukkan
bahwa kandungan fosfor lebih besar terdapat pada daging buah. Untuk
membuktikan pengaruh setiap perlakuan terhadap kadar fosfor dalam buah jambu
4.3 Analisis Data secara Statistik 4.3.1 Analisis Variansi
Hasil analisis data secara statistik menurut analisis variansi dapat dilihat
pada tabel di bawah ini:p
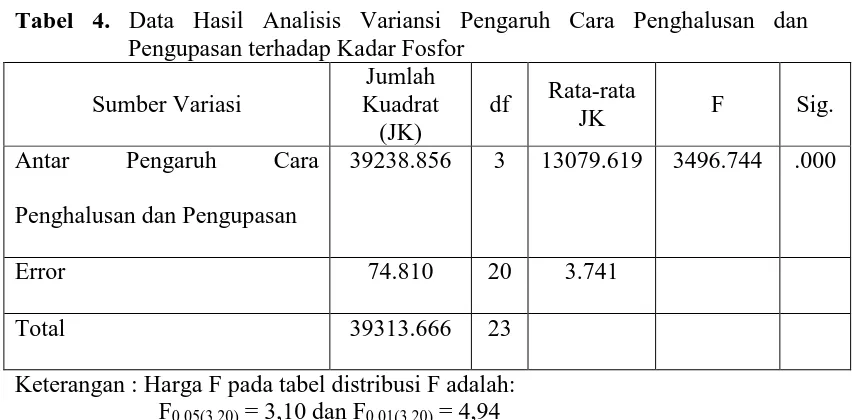
Tabel 4. Data Hasil Analisis Variansi Pengaruh Cara Penghalusan dan Pengupasan terhadap Kadar Fosfor
Sumber Variasi
Keterangan : Harga F pada tabel distribusi F adalah: F0.05(3,20) = 3,10 dan F0.01(3,20) = 4,94
Hasil analisis variansi di atas menunjukkan bahwa harga Fhitung lebih besar
daripada harga Ftabel, berarti beda rata-rata dari kadar fosfor dalam buah jambu biji
merah dengan pengaruh cara penghalusan dan pengupasan adalah sangat
signifikan atau nyata.
Setelah diperoleh hasil analisis variansi, maka dilakukan analisis lebih
lanjut untuk mengetahui perbedaan antara di-blender tanpa dikupas, di-blender
dikupas, di-juicer tanpa dikupas, dan di-juicer dikupas. Analisis lanjutan yang
dilakukan adalah uji dengan mencari Highly Significance Difference (HSD)
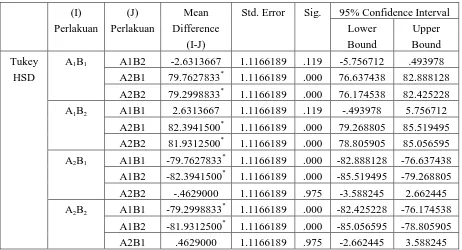
4.3.2 Analisis Lanjutan (Uji HSD) Tabel 5. Data Hasil Uji HSD
Tanda bintang (*) pada tabel di atas menunjukkan adanya perbedaan yang
signifikan antara masing-masing perlakuan yang dibandingkan pada tingkat
kepercayaan 0,05. Dari tabel dapat dilihat bahwa terdapat perbedaan yang
signifikan jika ditinjau dari faktor cara penghalusan. Sementara jika ditinjau dari
faktor pengupasan, hasil pada tabel tidak menunjukkan perbedaan yang signifikan.
Hal ini terlihat pada sampel yang diberi perlakuan cara penghalusan yang sama
dengan perbedaan perlakuan tanpa dikupas dan dikupas tidak dibubuhi tanda
bintang (*), sedangkan pada sampel yang diberi perlakuan cara penghalusan yang
berbeda dengan sama-sama tanpa dikupas dan dikupas dibubuhi tanda bintang (*).
Berarti, kadar fosfor hanya dipengaruhi oleh bagaimana buah jambu biji merah
dihaluskan dan faktor pengupasan tidak memberikan pengaruh terhadap kadar
fosfor dalam buah jambu biji merah.
(I)
Std. Error Sig. 95% Confidence Interval
Lower
A2B1 79.7627833* 1.1166189 .000 76.637438 82.888128 A2B2 79.2998833* 1.1166189 .000 76.174538 82.425228 A1B2 A1B1 2.6313667 1.1166189 .119 -.493978 5.756712
A2B1 82.3941500* 1.1166189 .000 79.268805 85.519495 A2B2 81.9312500* 1.1166189 .000 78.805905 85.056595 A2B1 A1B1 -79.7627833
*
1.1166189 .000 -82.888128 -76.637438
A1B2 -82.3941500* 1.1166189 .000 -85.519495 -79.268805 A2B2 -.4629000 1.1166189 .975 -3.588245 2.662445
A2B2 A1B1 -79.2998833 *