PEMBUATAN BIOETANOL DENGAN BAHAN BAKU
KIMPUL (Xanthosoma sagittifolium)
SKRIPSI
OLEH :
JOI SAPUTERA KARO-KARO 070308001
PROGRAM STUDI KETEKNIKAN PERTANIAN
FAKULTAS PERTANIAN
PEMBUATAN BIOETANOL DENGAN BAHAN BAKU
KIMPUL (Xanthosoma sagittifolium)
SKRIPSI
OLEH :
JOI SAPUTERA KARO-KARO 070308001/KETEKNIKAN PERTANIAN
Skripsi sebagai salah satu syarat untuk dapat menerima gelar sarjana di Program Studi Keteknikan Pertanian Fakultas Pertanian
Universitas Sumatera Utara
PROGRAM STUDI KETEKNIKAN PERTANIAN
FAKULTAS PERTANIAN
Judul Skripsi : Pembuatan Bioetanol dengan Bahan Baku Kimpul (Xanthosoma sagittifolium)
Nama : Joi Saputera Karo-Karo
NIM : 070308001
Program Studi : Keteknikan Pertanian
Disetujui Oleh : Komisi Pembimbing
Mengetahui,
Ir. Edi Susanto, M.Si Anggota Ainun Rohanah, STP, M.Si
Ketua
ABSTRAK
JOI SAPUTERA KARO-KARO : Pembuatan Bioetanol dengan Bahan Baku Kimpul (Xanthosoma sagittifolium), dibimbing oleh AINUN ROHANAH dan EDI SUSANTO.
Bioetanol merupakan teknologi alternatif dalam mengatasi semakin menipisnya bahan bakar yang tidak dapat diperbaharui. Penelitian ini dilakukan pada bulan Mei-Juni 2011 di Laboratorium Keteknikan Pertanian Fakultas Pertanian USU, Medan dengan menggunakan rancangan acak lengkap faktorial 2 faktor yaitu konsentrasi ragi (3%, 5% dan 7%) dan lama waktu fermentasi (2 hari, 3 hari dan 4 hari). Parameter yang diamati adalah kadar alkohol setelah proses fermentasi, kadar alkohol setelah proses destilasi, jumlah etanol dan jumlah etanol perkilogram bahan baku.
Hasil penelitian menunjukkan bahwa konsentrasi ragi memberikan pengaruh yang sangat nyata terhadap semua parameter. Lama waktu fermentasi memberikan pengaruh yang sangat nyata terhadap semua parameter kecuali kadar alkohol setelah proses destilasi. Interaksi perlakuan berpengaruh sangat nyata terhadap jumlah etanol dan berpengaruh nyata terhadap jumlah etanol perkilogram bahan baku. Hasil yang terbaik diperoleh pada kombinasi konsentrasi ragi 7% dengan lama waktu fermentasi 4 hari.
Kata kunci : Bioetanol, Konsentrasi Ragi, Lama Waktu Fermentasi
ABSTRACT
JOI SAPUTERA KARO-KARO : Bioetanol from Tannia (Xanthosoma
sagittifolium), supervised by AINUN ROHANAH and EDI SUSANTO
Bioetanol is an alternative technology in surpassing the diminishing of unrenewable fuel. This research was done in March untill May 2011 in Agricultural Engineering Laboratory, College of Agriculture, USU, Medan using factorial completely randomized design with two factors, i. l yeast concentration (3%, 5% and 7%) and time of fermentation (2 days, 3 days and 4 days). Parameters measured were alcohol concentration after fermentation, alcohol concentration after destilation, etanol concentration and etanol concentration for each kilogram of Tannia.
The results showed that yeast concentration had significanltly affected all parameters. Time of fermentation had significantly affected all parameters except alcohol concentration after destilation process. The interaction of the two factors had only significantly affected the etanol concentration and etanol concentration for each kilogram of Tannia. The best result was found in the combination of yeast concentration of 7% in 4 days time of fermentation.
RIWAYAT HIDUP
Penulis lahir di Kabanjahe, Kabupaten Karo pada tanggal 25 April 1989 dari ayah Maju Karo-Karo dan ibu Suwarni br. Sembiring. Penulis merupakan putra pertama dari dua bersaudara.
Tahun 2007 penulis lulus dari SMA Negri 1 Pulau Rayat, Kabupaten Asahan dan pada tahun 2007 lulus melalui jalur Panduan Minat dan Prestasi (PMP) masuk ke Program Studi Keteknikan Pertanian Fakultas Pertanian Universitas Sumatera Utara.
Selama mengikuti perkuliahan, penulis menjadi asisten mata kuliah Mekanisasi Pertanian. Penulis mengikuti kegiatan organisasi ATM (Agriculture
Technology Moslem), IMATETA (Ikatan Mahasiswa Teknik Pertanian).
KATA PENGANTAR
Puji dan syukur penulis panjatkan kehadirat Allah SWT atas rahmat dan karunia-Nya sehingga penulis dapat menyelesaikan skripsi yang berjudul “Pembuatan Bioetanol dengan Bahan Baku Kimpul (Xanthosoma sagittifolium)” yang merupakan salah satu syarat untuk mendapat gelar sarjana di Program Studi Keteknikan Pertanian Fakultas Pertanian Universitas Sumatera Utara, Medan.
Pada kesempatan ini penulis mengucapkan terima kasih kepada Ibu Ainun Rohanah, STP, M.Si selaku ketua komisi pembimbing dan Bapak Ir. Edi Susanto, M.Si selaku anggota komisi pembimbing yang telah
membimbing dan memberikan berbagai masukan, saran serta kritikan berharga kepada penulis sehingga skripsi ini dapat diselesaikan dengan baik.
Penulis juga mengucapkan terima kasih kepada semua staf pengajar, pegawai di Program Studi Keteknikan Pertanian, ayah, ibu serta seluruh keluarga yang telah memberi dukungan moril maupun materil, termasuk teman-teman yang membantu penulisan skripsi ini. Akhir kata penulis mengucapkan terima kasih dan semoga skripsi ini bermanfaat.
Medan, Juni 2011
DAFTAR ISI
Kimpul (Xanthosoma sagittifolium) ... 4Karbohidrat ... 6
Proses Pembuatan Bioetanol ... 16
BAHAN DAN METODE
Parameter Penelitian ... 24
Kadar Alkohol Setelah Fermentasi ... 24
Kadar Alkohol Setelah Destilasi ... 24
Jumlah Etanol. ... 24
Jumlah Etanol Perkilogram Bahan Baku ... 24
HASIL DAN PEMBAHASAN Kadar Alkohol Setelah Fermentasi ... 28
Pengaruh Konsentrasi Ragi ... 28
Pengaruh Lama Waktu Fermentasi ... 29
Pengaruh Interaksi ... 31
Kadar Alkohol Setelah Destilasi... 32
Pengaruh Konsentrasi Ragi ... 32
Pengaruh Lama Waktu Fermentasi ... 33
Jumlah Etanol yang Dihasilkan. ... 34
Pengaruh Konsentrasi Ragi ... 34
Pengaruh Lama Waktu Fermentasi ... 36
Pengaruh Interaksi ... 37
Jumlah Etanol Perkilogram Bahan Baku ... 40
Pengaruh Konsentrasi Ragi ... 40
Pengaruh Lama Waktu Fermentasi ... 41
Pengaruh Interaksi ... 43
KESIMPULAN DAN SARAN Kesimpulan ... 46
Saran ... 46
DAFTAR PUSTAKA ... 48
DAFTAR TABEL
No. Hal.
1. Kandungan zat makanan yang terdapat pada kimpul ... 5
2. Sifat-sifat fisika maupun kimia etanol ... 13
3. Pengaruh konsentrasi ragi terhadap parameter yang diamati ... 26
4. Pengaruh lama fermentasi terhadap parameter yang diamati ... 26
5. Uji LSR efek konsentrasi ragi terhadap kadar alkohol setelah proses fermentasi ... 28
6. Uji LSR efek lama waktu fermentasi terhadap kadar alkohol setelah proses fermentasi ... 30
7. Uji LSR efek konsentrasi ragi terhadap kadar alkohol setelah proses destilasi ... 32
8. Uji LSR efek konsentrasi ragi terhadap jumlah etanol yang dihasilkan 35 9. Uji LSR efek lama waktu fermentasi terhadap jumlah etanol yang dihasilkan ... 36
10. Uji LSR efek utama interaksi pengaruh konsentrasi ragi dan lama waktu fermentasi terhadap jumlah etanol yang dihasilkan ... 38
11. Uji LSR efek konsentrasi ragi terhadap jumlah etanol perkilogram bahan baku yang dihasilkan ... 40
12. Uji LSR efek lama waktu fermentasi terhadap jumlah etanol perkilogram bahan baku yang dihasilkan ... 41
DAFTAR GAMBAR
No. Hal.
1. Kimpul (Xanthosoma sagittifolium) ... 4 2. Pengaruh konsentrasi ragi terhadap kadar alkohol setelah
proses fermentasi ... 29 3. Pengaruh lama waktu fermentasi terhadap kadar alkohol
setelah proses fermentasi ... 31 4. Pengaruh konsentrasi ragi terhadap kadar alkohol setelah
proses destilasi ... 33
5. Pengaruh konsentrasi ragi terhadap jumlah etanol yang
dihasilkan ... 35 6. Pengaruh lama waktu fermentasi terhadap jumlah etanol
yang dihasilkan ... 37 7. Pengaruh kombinasi konsentrasi ragi dan lama waktu
fermentasi terhadap jumlah etanol yang dihasilkan ... 39 8. Pengaruh konsentrasi terhadap rendemen alkohol ... 41
9. Pengaruh lama waktu fermentasi terhadap jumlah etanol
perkilogram bahan baku ... 42 10. Pengaruh interaksi kombinasi konsentrasi ragi dan lama waktu
DAFTAR LAMPIRAN
No. Hal.
1. Flow chart prosedur penelitian ... 50
2. Gambar teknik alat destilasi ... 51
3. Spesifikasi alat destilasi bioetanol ... 52
4. Kadar alkohol setelah fermentasi ... 53
5. Kadar alkohol yang dihasilkan setelah proses destilasi ... 54
6. Jumlah etanol yang dihasilkan ... 55
7. Jumlah etanol perkilogram bahan baku yang didapat ... 58
8. Massa endapan setelah proses fermentasi ... 59
9. Volume Beer/ Sake Setelah Proses Pemerasan ... 59
ABSTRAK
JOI SAPUTERA KARO-KARO : Pembuatan Bioetanol dengan Bahan Baku Kimpul (Xanthosoma sagittifolium), dibimbing oleh AINUN ROHANAH dan EDI SUSANTO.
Bioetanol merupakan teknologi alternatif dalam mengatasi semakin menipisnya bahan bakar yang tidak dapat diperbaharui. Penelitian ini dilakukan pada bulan Mei-Juni 2011 di Laboratorium Keteknikan Pertanian Fakultas Pertanian USU, Medan dengan menggunakan rancangan acak lengkap faktorial 2 faktor yaitu konsentrasi ragi (3%, 5% dan 7%) dan lama waktu fermentasi (2 hari, 3 hari dan 4 hari). Parameter yang diamati adalah kadar alkohol setelah proses fermentasi, kadar alkohol setelah proses destilasi, jumlah etanol dan jumlah etanol perkilogram bahan baku.
Hasil penelitian menunjukkan bahwa konsentrasi ragi memberikan pengaruh yang sangat nyata terhadap semua parameter. Lama waktu fermentasi memberikan pengaruh yang sangat nyata terhadap semua parameter kecuali kadar alkohol setelah proses destilasi. Interaksi perlakuan berpengaruh sangat nyata terhadap jumlah etanol dan berpengaruh nyata terhadap jumlah etanol perkilogram bahan baku. Hasil yang terbaik diperoleh pada kombinasi konsentrasi ragi 7% dengan lama waktu fermentasi 4 hari.
Kata kunci : Bioetanol, Konsentrasi Ragi, Lama Waktu Fermentasi
ABSTRACT
JOI SAPUTERA KARO-KARO : Bioetanol from Tannia (Xanthosoma
sagittifolium), supervised by AINUN ROHANAH and EDI SUSANTO
Bioetanol is an alternative technology in surpassing the diminishing of unrenewable fuel. This research was done in March untill May 2011 in Agricultural Engineering Laboratory, College of Agriculture, USU, Medan using factorial completely randomized design with two factors, i. l yeast concentration (3%, 5% and 7%) and time of fermentation (2 days, 3 days and 4 days). Parameters measured were alcohol concentration after fermentation, alcohol concentration after destilation, etanol concentration and etanol concentration for each kilogram of Tannia.
The results showed that yeast concentration had significanltly affected all parameters. Time of fermentation had significantly affected all parameters except alcohol concentration after destilation process. The interaction of the two factors had only significantly affected the etanol concentration and etanol concentration for each kilogram of Tannia. The best result was found in the combination of yeast concentration of 7% in 4 days time of fermentation.
PENDAHULUAN
Latar Belakang
Manusia memiliki kehausan yang tidak terpuaskan terhadap energi. Itu terbukti dari permintaan global terhadap energi yang telah meningkat sejak tahun 1950. Hingga sekarang penggunaannya setara dengan 10.000 juta ton minyak setahun. Sebagian besar peningkatan permintaan terjadi di negara-negara berkembang (emerging markets). Namun mayoritas pasokan energi tersebut masih tergantung pada bahan bakar fosil, yakni batu bara, minyak bumi dan gas (Hendroko, 2007).
Menipisnya cadangan bahan bakar fosil dan meningkatnya populasi sangat kontradiktif dengan kebutuhan energi bagi kelangsungan hidup manusia beserta aktivitas ekonomi dan sosialnya. Sejak lima tahun terakhir, Indonesia mengalami penurunan produksi minyak nasional akibat menurunnya cadangan minyak pada sumur-sumur produksi secara ilmiah, padahal dengan pertambahan jumlah penduduk, meningkat pula kebutuhan akan sarana transportasi dan aktivitas industri .
Bioetanol merupakan salah satu bahan bakar nabati yang saat ini menjadi alternatif untuk mengggantikan minyak bumi. Minyak bumi saat ini harganya semakin meningkat, selain kurang ramah lingkungan juga termasuk sumber daya yang tidak dapat diperbaharui. Bioetanol mempunyai kelebihan selain ramah lingkungan, penggunaannya sebagai campuran BBM terbukti dapat mengurangi emisi karbon monoksida dan asap lainnya dari kendaraan. Saat ini bioetanol juga bisa dijadikan pengganti bahan bakar minyak tanah. Selain hemat, pembuatannya bisa dilakukan di rumah dengan mudah, lebih ekonomis dibandingkan menggunakan minyak tanah. Dengan demikian bisnis bioetanol di Indonesia mempunyai prospek yang cerah karena melimpahnya baku.
Kimpul berpotensi sebagai bahan baku pembuatan bioetanol, di Indonesia kimpul dimanfaatkaan sebagai bahan makanan tambahan dan pakan ternak. Di Sumatera Utara sendiri tanaman kimpul belum cukup dikenal, Kimpul hanya dijadikan pakan ternak dan tanaman pembatas pada kebun. Kimpul mudah di dapat karena tanaman ini sangat mudah tumbuh terutama di areal perkebunan. Kimpul mengandung karbohidrat sekitar 34%, Kandungan karbohidrat ini berpotensi untuk dijadikan bahan baku pembuatan bioetanol (Kay, 1973).
Tujuan Penelitian
Untuk menghitung jumlah etanol perkilogram bahan baku dan kadar alkohol dengan bahan baku kimpul yang dihasilkan pada penelitian.
Batasan Penelitian
Penelitian ini membahas tentang proses pembuatan etanol yang menggunakan bahan baku kimpul dengan alat destilasi satu tingkat serta pengaruh pemberian ragi dengan konsentrasi dan lama waktu fermentasi yang telah ditentukan dengan menggunakan metode rancangan acak lengkap (RAL).
Kegunaan Penelitian
• Bagi penulis yaitu sebagai bahan untuk menyusun skripsi yang merupakan syarat untuk menyelesaikan pendidikan di Program Studi Keteknikan Pertanian Fakultas Pertanian Universitas Sumatera Utara.
• Bagi mahasiswa, sebagai informasi pendukung untuk melakukan penelitian lebih lanjut mengenai cara pembuatan bioetanol.
TINJAUAN PUSTAKA
Kimpul (Xanthosoma Sigittifolium)
Tanaman kimpul merupakan tanaman asli daerah tropika benua Amerika. Tanaman Kimpul merupakan tanaman tahunan, tidak berkayu, terdiri dari akar, pelepah daun, daun, bunga dan umbi. Tinggi tanaman dapat mencapai dua meter, tangkai daun tegak, tumbuh dari tunas yang berasal dari umbi yang merupakan umbi yang tumbuh dari bawah tanah (Nur 1955).
Taksonomi tumbuhan kimpul adalah sebagai berikut: Kingdom : Plantae
Divisi : Spermatophyta
Class : Monocotyledoneae
Ordo : Arecales
Famili : Araceae
Genus : Xanthosoma
Spesies : Xanthosoma sagittifolium (Purseglove, 1972).
Tanaman kimpul dapat tumbuh baik di daerah tropika basah dengan curah hujan merata sepanjang tahun. Umumnya tanaman kimpul akan memberikan hasil yang optimum pada lahan yang kering dan gembur, sedangkan pada lahan yang becek atau tergenang air tanaman ini tidak dapat tumbuh dengan baik
(Kay, 1973).
Bentuk umbi kimpul silinder sampai agak bulat, terdapat internode atau ruas dengan beberapa bakal tunas. Jumlah umbi anak dapat mencapai 10 atau lebih dengan panjang sekitar 12-25 cm dan diameter 12-15 cm dan umbi yang
dihasilkan biasanya berukuran 300-1000 gr. Irisan melintang umbi
memperlihatkan bahwa strukturnya terdiri dari kulit, korteks, pembuluh floem dan xylem. Kulit umbi mempunyai tebal sekitar 0,1 cm. Pada pembuluh xylem dan floem terdapat butir-butir pati (Muchtadi dan Sugiono, 1989)
Umbi induk tanaman kimpul tidak pernah dimakan, karena member rasa gatal. Umbi anak juga memberi rasa gatal, rasa gatal tersebut disebabkan adanya kristal-kristal kalsium oksalat yang berbentuk jarum. Kalsium oksalat ini dapat dikurangi dengan pencucian dengan menggunakan air (Greenwell, 1974).
Tabel 1. Kandungan zat makanan per 100 gr umbi kimpul
Kandungan Jumlah
Bagian yang dapat dimakan (%)
Karbohidrat
Karbohidrat adalah sumber energi utama yang sebagian besar dihasilkan dari serealia dan sayuran berpati. Karbohidrat mengandung karbon, hidrogen dan oksigen; strukturnya dapat sederhana dan kompleks. Monosakarida dan disakarida merupakan contoh karbohidrat sederhana, sedangkan polisakarida seperti pati dan fruktosa merupakan karbohidrat kompleks (Rubatzky dan Yamaguchi, 1998).
Pati merupakan polisakarida yang ditemukan begitu melimpah dalam padi-padian, serta umbi-umbian. Pati adalah salah satu sumber energi. Dilihat dari susunannya pati merupakan suatu campuran amilosa (polisakarida yang berantai lurus dan berantai cabang). Pati tidak larut dalam air dingin. Didalam pangan mentah pati tersebut terdapat dalam butiran yang kalau dipanaskan dalam air akan mengambang, pecah dan selanjutnya melepaskan pati. Selanjutnya pati akan membentuk suatu bahan yang rekat dan mudah dicerna. Pada hidrolisis pati
pertama-tama pati akan membentuk dekstrosa lalu amilosa dan glukosa
(Harper, dkk, 1986).
Tahapan-tahapan proses perubahan pati menjadi alkohol adalah sebagai berikut :
1. Hidratasi pati : umbi-umbian digiling dan serbuk unbi-umbian diberi air sehingga terjadi disperse.
2. Gelatinisasi pati : ditentukan oleh tipe pati hubungan suhu dan waktu, ukuran partikel dan konsentrasi bubur (merupakan tahap pemula penting untuk proses).
3. Hidrolisis pati : konversi pati untuk menghasilkan gula yang tidak terfermentasi terjadi karena hidrolisis enzimatis.
4. Konversi gula menjadi alkohol : gula sangat disukai oleh hampir semua makhluk hidup sebagai sumber energi. Khamir dapat memfermentasi glukosa, maltosa dan galaktosa tetapi tidak dapat memecah pentosa. Disakarida seperti sukrosa dan maltosa difermentasi dengan khamir karena memiliki enzim sukrase dan maltase untuk mengubah maltosa menjadi heksosa (Hidayat, dkk., 2006).
Enzim
Enzim yang tahan suhu tinggi digunakan dalam proses likuifikasi, sedangkan yang labil terhadap suhu tinggi digunakan dalam proses sakarifikasi. Likuifikasi mengkonversi pati menjadi dekstrin (yang terdiri dari glukosa, maltosa, maltotriosa dan oligosakarida), sedangkan sakarifikasi mengkonversi dekstrin menjadi glukosa (Norman, 1980).
Ragi
Ragi merupakan kumpulan spora mikroba yang ditempatkan pada media tertentu misalnya tepung beras. Mikroba dari berbagai golongan aktif dalam kegiatan fermentasi, namun hanya beberapa yang bersifat dominan, tergantung media yang disediakan. Jenis ragi bermacam-macam, masing-masing dengan kandungan spora dan mikroba yang berlainan sehingga setiap ragi memiliki kemampuan yang berbeda dalam memfermentasi bahan. Ragi diberi nama sesuai dengan kemampuannya dalam memfermentasi bahan misalnya ragi tempe (memfermentasi kedelai menjadi tempe), ragi tapai (memfermentasi singkong atau ketan menjadi tapai) dan ragi roti (memfermentasi terigu menjadi roti). Kualitas ragi tidak dapat dideteksi hanya dengan dilihat, namun harus dicoba untuk digunakan dalam fermentasi setelah 2-3 hari dicampurkan. Dengan demikian, kualitas ragi akan diketahui dari produk yang dihasilkan. Kualitas ragi salah satunya ditentukan oleh proses pembuatan ragi (Suprapti, 2005).
fermentasi tape. Kultur yang dipilih harus dapat tumbuh dengan baik dan mempunyai toleransi yang tinggi terhadap alkohol serta mampu menghasilkan alkohol dalam jumlah banyak (Irianto, 2006).
Sebuah sel ragi mampu memfermentasi glukosa dengan massa yang sama
dengan massa selnya sendiri dalam jangka waktu satu jam. Ragi dapat bereproduksi
secara aseksual dengan membentuk tunas ataupun secara seksual dengan
pembentukan ascospora. Selama proses reproduksi aseksual, sebuah tunas baru
tumbuh dari ragi dengan kondisi tertentu dan saat mencapai ukuran dewasa ia akan
melepaskan diri dari sel induknya (European Bioinformatics Institute, 1996).
Fermentasi
Dalam pengertian yang luas, fermentasi adalah proses pemecahan gula-gula sederhana (glukosa dan fruktosa) menjadi etanol dan CO2 dengan melibatkan enzim yang dihasilkan pada ragi agar dapat bekerja pada suhu optimum. Proses fermentasi tergantung pada banyak sedikitnya penambahan khamir dalam bahan. Semakin banyak jumlah ragi yang diberikan berarti semakin banyak jumlah khamir yang terlibat, sehingga kadar alkohol meningkat (Tarigan, 1990).
Waktu fermentasi yang biasa dilakukan 3-14 hari. Jika waktunya terlalu cepat Saccharomyces cereviseae masih dalam masa pertumbuhan sehingga alkohol yang dihasilkan dalam jumlah sedikit dan jika terlalu lama
Saccharomyces cereviseae akan mati maka alokhol yang dihasilkan tidak
maksimal (Prescott and Dunn, 1959).
Syarat-syarat yang dipergunakan dalam memilih ragi untuk fermentasi, adalah :
1. Cepat berkembang biak 2. Tahan terhadap alkohol tinggi 3. Tahan terhadap suhu tinggi 4. Mempunyai sifat yang stabil
5. Cepat mengadakan adaptasi terhadap media yang difermentasi
Untuk memperoleh jenis ragi yang mempunyai sifat-sifat seperti di atas, harus dilakukan percobaan-percobaan di laboratorium dengan teliti. Pada umumnya ragi yang dipakai untuk pembuatan alkkohol adalah jenis
Saccharomyces cerevisiae yang mempunyai pertumbuhan sempurna pada suhu ±
30oC dan pH 4,8 (Hamidah, 2003).
Dalam ragi banyak terdapat Sacharomoces cerevisae yang mempunyai daya konversi gula yang sangat tinggi karena menghasilkan enzim zimase dan intervase. Enzim zimase berfungsi sebagai pemacu. Perubahan sukrosa menjadi monosakarida (glukosa dan fruktosa). Sedangkan enzim intervase mengubah glukosa menjadi alkohol. (Judoamidjoyo, dkk., 1990).
dari kemampuan ragi untuk mengubah karbohidrat menjadi alkohol. Pemilihan ragi yang akan digunakan dan proses penyulingan merupakan hal yang paling penting dalam pembuatan alkohol. (Briggs, et al., 1981).
Tahap inti dari produksi bioetanol adalah fermentasi gula sederhana, baik yang berupa glukosa, sukrosa, maupun fruktosa dengan menggunakan ragi/yeast terutama Saccharomyces sp. atau bakteri Zyomomonas mobilis. Dalam proses ini, gula akan dikonversi menjadi etanol dan gas karbon dioksida.
C6 H12 O6 2 C2 H5 OH + 2 CO2 gula etanol karbondioksida (Waller, J.C., dkk. 1981).
Faktor-faktor yang mempengaruhi kehidupan ragi: a. Nutrisi (zat gizi)
Dalam kegiatannya ragi memerlukan penambahan nutrisi untuk pertumbuhan dan perkembangbiakan, misalnya:
− Unsur C: ada pada karbohidrat
− Unsur N: dengan penambahan pupuk yang mengandung nitrogen,
ZA, Urea, Anomia, Pepton dan sebagainya.
− Unsur P: penambahan pupuk fospat dari NPK, TSP, DSp dan
lain-lain.
− Mineral-mineral dan
b. Keasaman (pH)
Untuk fermentasi alkoholis, ragi memerlukan media suasana asam, yaitu antara pH 4,8–5,0. Pengaturan pH dilakukan penambahan asam sulfat jika substratnya alkalis atau natrium bikarbonat jika substratnya asam.
c. Temperatur
Temperatur optimum untuk pengembangbiakan adalah 28–30ºC pada waktu fermentasi, terjadi kenaikan panas, karena ekstrem. Untuk mencegah agar suhu fermentasi tidak naik, perlu pendinginan supaya suhu dipertahankan tetap 28-30ºC.
d. Udara
Fermentasi alkohol berlansung secara anaerobik (tanpa udara). Namun demikian, udara diperlukan pada proses pembibitan sebelum fermentasi, untuk pengembangbiakan ragi sel (Hamidah, 2003).
Bioetanol
Bioetanol merupakan alternatif penyedia energi yang merupakan senyawa alkohol yang dapat diperoleh melalui proses-proses fermentasi biomassa dengan bantuan mikroorganisme. Bahan baku bioetanol merupakan segala jenis tanaman yang mengandung karbohidrat. Tanaman-tanaman ini sangat mudah ditemukan di Indonesia karena keadaan iklim dan tanah yang sangat mendukung pertumbuhan tanaman-tanaman tersebut (Karmawati, 2009).
bebas air (anhydrous alcohol) dan berkadar lebih dari 99,5% atau disebut dengan
fuel grade ethanol (FGE) campuran premium dan FGE disebut dengan gasohol
(Hambali, dkk, 2008).
Etanol memiliki banyak manfaat bagi masyarakat karena memiliki sifat yang tidak beracun. Selain itu etanol juga memiliki banyak sifat-sifat, baik secara fisika maupun kimia. Adapun sifat-sifat fisika etanol dapat dilihat pada Tabel 2. dibawah ini:
Tabel 2. Sifat-sifat fisika maupun kimia etanol
Sifat-sifat fisika etanol Keterangan
Alat Destilasi Etanol
Destilasi merupakan suatu metode pemisahan bahan kimia berdasarkan perbedaan kemudahaan menguap (volatilitas) bahan. Dalam penyulingan, campuran zat dididihkan sehingga menguap, dan uap ini kemudian didinginkan sehingga kembali kedalam bentuk cair. Zat yang memiliki titik didih lebih rendah akan menguap lebih dulu. Metode ini termasuk unit operasi kimia jenis perpindahan massa. Penerapan proses ini berdasarkan pada teori bahwa pada suatu larutan, masing-masing komponen akan menguap pada titik didihnya. Bahan yang akan didestilasikan pada drum pemasakan tidak boleh penuh, melainkan harus menyediakan sedikitnya 10% ruang kosong dari kapasitas penuh drum pemasakan (Kister, 1992).
Prinsip dari proses destilasi yaitu memisahkan etanol dari campuran etanol dan air. Untuk larutan yang terdiri dari komponen-komponen yang berbeda nyata suhu didihnya, destilasi merupakan cara yang paling mudah dioperasikandan juga merupakan cara pemisahan yang secara thermal efisien. Pada tekanan atmosfir, air mendidih pada suhu 100ºC dan etanol mendidih pada suhu sekitar 77ºC. perbedaan dalam titik didih inilah yang memungkinkan pemisahan campuran etanol air (Lurgi, 1989).
Alat destilasi yang digunakan memiliki komponen sebagai berikut : 1. Drum 30 liter
Drum ini berfungsi sebagai tempat bahan baku (beer/sake) yang akan didestilasi. Drum ini dilengkapi dengan termometer yang berfungsi untuk mengontrol suhu di dalam drum selama proses pemanasan. Drum ini berbentuk silinder yang pada bagian tutupnya diberi lubang keluaran uap yang dihubungkan dengan pipa tembaga yang berfungsi sebagai saluran uap yang akan dikondensasi.
2. Pipa Tembaga
Pipa tembaga ini berdiameter ¼ inci yang berfungsi sebagai saluran uap etanol yang dihasilkan dari proses pemanasan bahan baku (beer/sake) di drum pemasakan menuju pipa ulir di dalam kondensor.
3. Pipa Ulir
Pipa ini terbuat dari tembaga dan berbentuk ulir yang berada di dalam kondensor. Pipa ulir ini berfungsi untuk mengubah etanol yang dihasilkan dari proses pemanasan yang berupa fasa uap menjadi fasa cair melalui proses kondensasi pada kondensor.
4. Kondensor
5. Pipa Keluaran
Pipa ini berfungsi untuk mengeluarkan hasil proses destilasi, pada pipa ini terdapat kran pembuka dan pengunci pipa.
6. Kompor Gas
Kompor gas berfungsi sebagai alat pemanas untuk memanaskan drum yang berisi bahan berupa bioetanol dan air. Selama proses pemanasan diusahakan suhu yang dihasilkan antara 78 – 98oC, karena apabila suhu mencapai 100oC, uap yang dihasilkan akan banyak mengandung air yang mengakibatkan penurunan kadar bioetanol yang dihasilkan
7. Erlenmeyer dan Gelas Ukur
Erlenmeyer dan gelas ukur berfungsi sebagai pengukur bioetanol yang dihasilkan melalui proses distilasi ini (Dwinarso, 2010).
Kadar alkohol setelah proses destilasi hanya dipengaruhi oleh alat destilasi yang digunakan. Alat destilasi yang digunakan merupakan alat destilasi satu tingkat yang hanya mampu menghasilkan etanol dengan kadar alkohol 40% (Shidik, 2010).
Proses Pembuatan Bioetanol
gula seperti molase dapat secara langsung difermentasi. Bahan padatan dikenai perlakuan pengecilan ukuran dan juga tahap pemasakan. Proses pengecilan ukuran dapat dilakukan dengan menggiling bahan (singkong, sagu, dan jagung) sebelum memasuki tahap pemasakan. Tahap pemasakan bahan meliputi proses liquifikasi dan sakarifikasi. Pada tahap ini, tepung/pati dikonversi menjadi gula (Hambali, E., dkk. 2008).
Alkohol dibuat dengan cara memfermentasi bahan yang mengandung gula. Secara alami, gula terdapat dalam buah-buahan misalnya anggur. Gula juga dapat dihasilkan dari pati dalam padi-padian dan umbi-umbian. Fermentasi minuman beralkohol dilakukan oleh jamur jenis Saccharomyces cerevisiae (jenis utama) dan beberapa jenis lainya seperti ragi. Pembuatan alkohol diperlukan kondisi asam (pH yang rendah), perlu ditambahkan asam. Adapun suhu yang dibutuhkan berkisar antara 29-37oC. Agar kadar alkohol yang dihasilkan tinggi selain proses fermentasi dilakukan juga proses penyulingan (Arisworo dan Yusa, 2006).
Bahan baku bioetanol bisa diperoleh dari berbagai tanaman yang menghasilkan gula dan tepung. Pada tahap persiapan, bahan baku berupa padatan harus dikonversi terlebih dahulu menjadi larutan gula sebelum akhirnya difermentasi untuk menghasilkan etanol, sedangkan bahan yang sudah berbentuk larutan gula dapat langsung difermentasi. Bahan padatan dikenai perlakuan pengecilan ukuran dan tahap pemasakan.
ditandai dengan parameter cairan seperti sup. Tahap sakarifikasi dilakukan pada
suhu 50-60oC. Enzim yang ditambahkan pada tahap ini adalah enzim
glukoamilase. Pada tahap sakarifikasi akan terjadi pemecahan gula kompleks menjadi gula sederhana. Proses liquifikasi yang menggunakan enzim alphaamilase dan sakarifikasi yang menggunakan enzim glukoamilase secara langsung dapat digantikan oleh penggunaan cendawan Aspergillus sp. Hal ini disebabkan karena cendawan ini menghasilkan enzim alphaamilase dan glukoamilase yang akan berperan dalam mengurai pati menjadi glukosa atau gula sederhana (Hambali, dkk., 2008).
Pada proses fermentasi alkohol diupayakan konsentrasi gulanya menjadi 15%-20%. Untuk memenuhi kebutuhan nutrisi, maka ditambahkan amonium sulfat, sedangkan untuk menurunkan pH-nya digunakan asam sulfat.
Saccharomyces cerevisiae merupakan khamir yang umum digunakan dalam
industri fermentasi etanol.. Proses fermentasi membutuhkan waktu sekitar 28-72 jam, tetapi biasanya 44 jam untuk menghasilkan etanol dengan konsentrasi 8-10% dengan suhu optimum berkisar 32oC–33oC (Riegel, 1992).
Tahap fermentasi merupakan tahap kedua dalam proses produksi bioetanol. Pada tahap ini terjadi proses pemecahan gula-gula sederhana menjadi etanol dengan melibatkan enzim dan ragi. Fermentasi dilakukan pada kisaran suhu 27 - 32oC. pada tahap ini akan dihasilkan gas CO2 sebagai produk sampingan dan
Tahap berikutnya adalah pemurnian etanol. Tahap ini dilakukan melalui metode destilasi. Destilasi dilakukan pada suhu diatas titik didih etanol murni, yaitu pada kisaran 78 – 100oC. Produk yang dihasilkan pada tahap ini memiliki kemurnian hingga 96 %. Akan tetapi, sebelum memasuki tahap pemurnian dilakukan pemisahan etanol dengan sludge yang diperoleh dari hasil fermentasi etanol yang dihasilkan. Salah satu pemanfaatan limbah sludge yang telah berhasil dilakukan yaitu pengolahan sludge menjadi pupuk kalium majemuk dengan kadar kalium 40 %.
Jika etanol yang dihasilkan akan digunakan sebagai bahan bakar maka etanol hasil destilasi ini harus dikeringkan terlebih dahulu. Pengeringan ini dapat dilakukan dengan metode purifikasi molecular sieve bertujuan untuk meningkatkan kemurnian etanol hingga memenuhi spesifikasi bahan bakar.
Molecular sieve adalah suatu bahan yang memiliki pori-pori kecil dan digunakan
BAHAN DAN METODE
Tempat dan Waktu Penelitian
Penelitian ini dilaksanakan di Laboratorium Keteknikan Pertanian Program Studi Keteknikan Pertanian Fakultas Pertanian Universitas Sumatera Utara pada bulan Mei-Juni 2011.
Bahan dan Alat Penelitian
Adapun bahan yang digunakan adalah kimpul, enzim alfa-amilase, enzim glukoamilase, Saccharomyces cerevisiae (ragi roti), urea, air dan LPG.
Sedangkan alat yang digunakan adalah termometer, dandang, timbangan, ember, alat destilasi alkohol, alat pemarut ubi, kompor gas, batang pengaduk, cawan petri, corong, selang plastik, alkohol meter, timbangan, saringan, wadah fermentasi, Erlenmeyer, gelas ukur, kalkulator, alat tulis dan komputer.
Metode Penelitian
Penelitian ini dilakukan dengan cara studi literatur (kepustakaan), dengan melakukan pengamatan tentang cara pembuatan bioetanol. Selanjutnya dicari bahan dan cara pembuatan yang cocok digunakan. Setelah itu, dilakukan proses pembuatan bioetanol dan pengamatan parameter.
Faktor I : Konsentrasi Ragi (C) yang terdiri dari 3 taraf yaitu :
C1 = 3%
C2 = 5%
C3 = 7%
Faktor II : Lama Fermentasi (T) yang terdiri dari 3 taraf yaitu :
T1 = 2 hari
T2 = 3 hari
T3 = 4 hari
Jumlah kombinasi perlakuan sebanyak (Tc) = 3 X 3 = 9, dengan jumlah minimum ulangan percobaan (n) sehingga banyak ulangan percobaan dapat dihitung dengan :
Tc (n – 1) ≥ 15
9 (n – 1) ≥ 15
9n – 9 ≥ 15
9n ≥ 24
n ≥ 2,67
n = 3
Dengan demikian penelitian ini dilakukan sebanyak 3 kali ulangan, dengan kombinasi perlakuan sebagai berikut :
C1T1 C1T2 C1T3
C2T1 C2T2 C2T3
Model Rancangan Penelitian
Model rancangan yang digunakan adalah rancangan acak lengkap (RAL) yang terdiri dari dua faktor perlakuan yaitu faktor konsentrasi ragi (C) dan faktor lama fermentasi (T) dengan kode rancangan :
Yijk = µ + αi + βj + (αβ)ij + εijk Dimana :
Yijk = Hasil pengamatan dari faktor C pada taraf ke–i dan faktor T pada taraf ke– j pada ulangan ke– k
µ = Nilai tengah sebenarnya
αi = Efek faktor C pada taraf ke-i
βj = Efek faktor T pada taraf ke-j
(αβ)ij = Efek interaksi faktor C pada taraf ke-i dengan faktor T pada
taraf ke-j
Εijk = Pengaruh galat (pengacakan)
Prosedur Penelitian
1. Dikuliti umbi kimpul lalu dicuci dengan air hingga bersih 2. Ditimbang sebanyak 4 kg.
3. Diparut dengan alat pemarut umbi. 4. Ditambahkan air dengan volume 8 liter. 5. Dimasukkan ke dalam dandang.
6. Dipanaskan hingga suhu 100°C atau sampai mendidih sambil terus diaduk hingga hancur menjadi bubur.
8. Dimasukkan enzim alfa-amilase sebanyak 0,5 ml dan diaduk hingga homogen dan dibiarkan 5 menit.
9. Dimasukkan campuran bubur ke wadah fermentasi.
10. Dimasukkan enzim glukoamilase sebanyak 0,4 ml dan diaduk hingga homogen saat suhu bubur 50 - 60oC.
11. Dimasukkan 8 gr urea dan jamur Saccaromyces cerevisiae sesuai dengan perlakuan ke dalam bubur tersebut saat suhu bubur sama dengan suhu ruangan.
12. Ditutup wadah fermentasi agar jamur Saccaromyces cerevisiae bekerja dengan baik.
13. Difermentasikan bubur tersebut selama waktu yang telah ditentukan. 14. Setelah sesuai dengan waktu perlakuan, diperas bubur untuk mengambil
larutan etanol yang terkandung dalam hasil fermentasi bubur.
15. Ditimbang ampas yang dihasilkan dan diukur volume serta kadar alkohol dari larutan etanol hasil fermentasi yang telah diperas.
16. Dilakukan destilasi atau penyulingan menggunakan alat destilasi etanol dengan suhu 78 - 98°C.
17. Ditampung hasil penyulingan pada wadah yang telah disiapkan. 18. Diukur volume dan kadar etanol yang dihasilkan.
Parameter Penelitian
1. Kadar Alkohol setelah Fermentasi (%)
Kadar alkohol merupakan indikator kandungan alkohol pada cairan yang telah mengalami proses fermentasi. Kadar alkohol yang ada pada bioetanol dapat diukur menggunakan alkohol meter.
2. Kadar Alkohol Proses Destilasi (%)
Kadar alkohol ini merupakan indikator kandungan alkohol pada cairan yang telah mengalami proses penyulingan dengan menggunakan alat destilasi. Kadar alkohol yang terkadung dalam bioetanol dapat diukur menggunakan alkohol meter juga.
3. Jumlah Etanol (ml)
Jumlah alkohol yang dihasilkan dapat diketahui dengan mengukur banyaknya etanol yang dihasilkan melalui proses penyulingan menggunakan alat destilasi menggunakan erlenmeyer dan gelas ukur.
4. Jumlah Etanol Perkilogram Bahan Baku (ml/kg)
Jumlah etanol perkilogram bahan baku dapat diketahui dengan cara membagikan banyak alkohol yang didapat dengan massa kimpul, atau dapat ditulis dengan rumus :
HASIL DAN PEMBAHASAN
Pada proses pembuatan bioetanol dengan bahan baku kimpul terlebih dahulu dilakukan pemarutan terhadap bahan baku kimpul yang bertujuan untuk memudahkan proses hidolisis pati oleh enzim. Menurut Hambali dkk (2008) Bahan padatan dikenai perlakuan pengecilan ukuran dan juga tahap pemasakan. Proses pengecilan ukuran dapat dilakukan dengan menggiling bahan (singkong, sagu, dan jagung) sebelum memasuki tahap pemasakan. Tahap pemasakan bahan meliputi proses liquifikasi dan sakarifikasi. Pada tahap ini, tepung/pati dikonversi menjadi gula.
Pada proses hidrolisis digunakan enzim alfa-amilase dan enzim glukoamilase. Enzim alfa-amilase ini berfungsi sebagai pemecah pati (polisakarida) yang telah berbentuk gel (bubur) menjadi dekstrin atau senyawa disakarida (liquifikasi).. Menurut Hambali dkk (2008) Proses liquifikasi ini dilakukan pada saat suhu berada pada kisaran 80-90oC. Setelah proses liquifikasi berlangsung sempurna maka dilanjutkan dengan proses sakarifikasi. Proses sakarifikasi merupakan proses penguraian disakarida menjadi monosakarida (glukosa). Menurut Hambali dkk (2008) Proses sakarifikasi dilakukan dengan penambahan enzim glukoamilase pada saat suhu bahan 50 – 60oC. Glukosa hasil sakarifikasi inilah yang nantinya akan diubah menjadi etanol oleh jamur
Saccaromyces cerevisiae pada proses fermentasi.
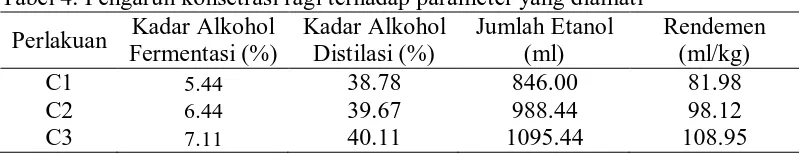
Tabel 4. Pengaruh konsetrasi ragi terhadap parameter yang diamati Perlakuan Kadar Alkohol
Fermentasi (%)
Dari Tabel 4 dapat dilihat bahwa kadar alkohol setelah proses fermentasi tertinggi diperoleh pada perlakuan C3 (konsentrasi 7%) sebesar 7,11% dan yang terendah pada perlakuan C1 (konsentrasi 3%) sebesar 5,44%. Kadar alkohol setelah proses destilasi tertinggi diperoleh pada perlakuan C3 sebesar 40,11% dan yang terendah pada C1 sebesar 38,78%. Jumlah etanol yang dihasilkan tertinggi diperoleh pada perlakuan C3 sebanyak 1095,44 ml dan yang terendah pada C1 sebanyak 846,00 ml. Rendemen alkohol tertinggi diperoleh pada perlakuan C3 sebesar 108,95 ml/kg dan yang terendah pada perlakuan C1 sebesar 81,98 ml/kg.
Lama waktu fermentasi memberikan pengaruh terhadap kadar alkohol setelah proses fermentasi, kadar alkohol setelah proses destilasi, jumlah etanol dan rendemen alkohol yang dihasilkan. Hal ini dapat dilihat pada Tabel 5.
Tabel 5. Pengaruh lama waktu fermentasi terhadap parameter yang diamati Perlakuan Kadar Alkohol
Fermentasi (%)
Rendemen alkohol tertinggi diperoleh pada perlakuan T3 sebesar 112,54 ml/kg dan yang terendah pada perlakuan T1 sebesar 76,48 ml/kg.
Hasil analisa statistik pengaruh konsentrasi ragi (C) dan lama waktu fermentasi (T) terhadap masing-masing parameter yang diamati dapat dilihat pada uraian berikut.
Kadar Alkohol Setelah Proses Fermentasi
Pengaruh konsentrasi ragi
Daftar analisis sidik ragam pada Lampiran 4 menunjukkan bahwa konsentrasi ragi memiliki pengaruh yang sangat nyata terhadap kadar alkohol setelah proses fermentasi. Hasil uji LSR (Least Significant Range) pengaruh konsentrasi ragi terhadap kadar alkohol setelah proses fermentasi yang dihasilkan untuk tiap-tiap perlakuan dapat dilihat pada Tabel 6.
Tabel 6. Uji LSR efek konsentrasi ragi terhadap kadar alkohol setelah proses fermentasi
Jarak LSR
Perlakuan Rataan Notasi
P F 0,05 F 0,01 F 0,05 F 0,01
- - - C1 5.44 a A
2 0.4260 0.5838 C2 6.44 b B 3 0.4475 0.6125 C3 7.11 c C Keterangan : Notasi huruf yang berbeda pada kolom yang sama menunjukkan
berbeda nyata pada taraf 5% dan berbeda sangat nyata pada taraf 1%
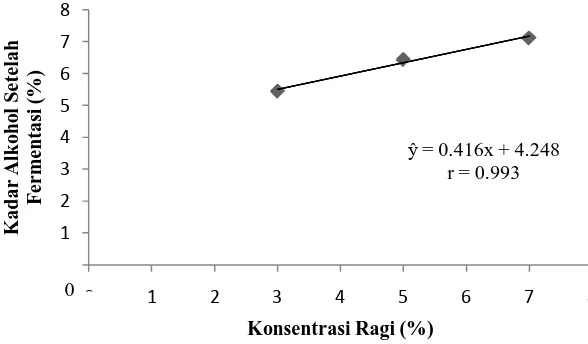
Pengaruh konsentrasi ragi terhadap kadar alkohol setelah proses fermentasi mengikuti garis regresi linear seperti gambar berikut.
Gambar 2. Pengaruh konsentrasi ragi terhadap kadar alkohol setelah fermentasi Gambar 2 menunjukkan bahwa semakin tinggi konsentrasi ragi yang ditambahkan pada bahan yang akan difermentasi maka semakin tinggi kadar alkohol yang dihasilkan. Hal ini terjadi karena semakin banyak jumlah ragi yang ditambahkan maka akan semakin banyak mikroorganisme yang memfermentasi bahan menjadi alkohol. Pernyataan ini sesuai dengan literatur dari Tarigan (1990) Proses fermentasi tergantung pada banyak sedikitnya penambahan khamir dalam bahan. Semakin banyak jumlah ragi yang diberikan berarti semakin banyak jumlah khamir yang terlibat, sehingga kadar alkohol meningkat.
Pengaruh lama waktu fermentasi
Daftar analisis sidik ragam pada Lampiran 4 menunjukkan bahwa lama waktu fermentasi memiliki pengaruh yang sangat nyata terhadap kadar alkohol setelah proses fermentasi. Hasil uji LSR (Least Significant Range) pengaruh lama waktu fermentasi terhadap kadar alkohol setelah proses fermentasi untuk tiap-tiap perlakuan dapat dilihat pada Tabel 7.
Tabel 7. Uji LSR efek lama waktu fermentasi terhadap kadar alkohol setelah Keterangan : Notasi huruf yang berbeda pada kolom yang sama menunjukkan
berbeda nyata pada taraf 5% dan berbeda sangat nyata pada taraf 1%
Dari Tabel 7 dapat dilihat bahwa perlakuan T1 berbeda sangat nyata tehadap perlakuan perlakuan T2 demikian juga terhadap perlakuan T3. Perlakuan T2 juga berbeda sangat nyata terhadap perlakuan T3. Kadar alkohor tertinggi diperoleh pada perlakuan T3 yaitu sebesar 7,44% dan kadar alkohol terendah diperoleh pada perlakuan T1 yaitu sebesar 5,22%.
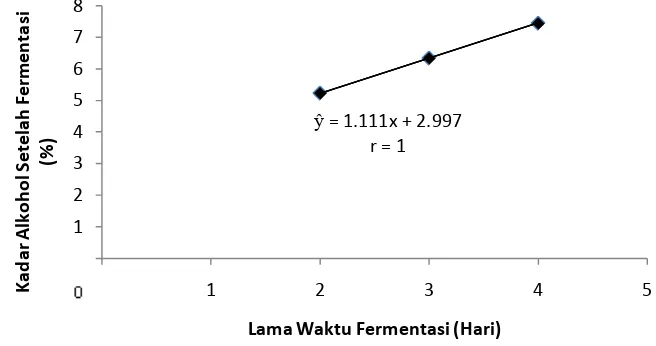
Pengaruh lama waktu fermentasi terhadap kadar alkohol setelah proses fermentasi mengikuti garis regresi linear seperti gambar berikut.
Gambar 3. Pengaruh lama waktu fermentasi terhadap kadar alkohol
Gambar 3 menunjukkan bahwa semakin lama waktu fermentasi alkohol oleh ragi (Saccharomyces cerevisiae) maka kadar alkohol yang dihasilkan juga semakin tinggi. Hal ini dapat dilihat pada lama waktu fermentasi 2 hari diperoleh kadar alkohol terendah sebesar 5,22% dan mengalami peningkatan pada
lama waktu fermentasi 3 hari dan 4 hari. Kadar alkohol tertinggi sebesar 7,44% diperoleh pada perlakuan lama waktu fermentasi 4 hari. Ini dikarenakan ragi akan mengalami perkembang biakan secara terus menerus sampai tingkat dimana konsentrasi alkohol yang dihasilkan menghambat pertumbuhan ragi. Semakin lama waktu fermentasi maka jumlah ragi juga akan semakin meningkat sampai batas tertentu. Hal ini sesuai dengan literatur dari Bioinformatics Institute (1996) dimana sebuah sel ragi mampu memfermentasi glukosa dengan massa yang sama dengan massa selnya sendiri dalam jangka waktu satu jam. Ragi dapat bereproduksi
secara aseksual dengan membentuk tunas ataupun secara seksual dengan
pembentukan ascospora. Selain itu dari data hasil fermentasi dapat dilihat bahwa
kadar alkohol hasil fermentasi hanya mampu mencapai 8% pada kombinasi perlakuan C3T3. Hal ini sesuai dengan pernyataan Riegel (1992) Proses fermentasi membutuhkan waktu sekitar 28-72 jam, tetapi biasanya 44 jam untuk menghasilkan etanol dengan konsentrasi 8-10% dengan suhu optimum berkisar 32oC–33oC.
Pengaruh interaksi
Kadar Alkohol Setelah Proses Destilasi
Pengaruh konsentrasi ragi
Daftar analisis sidik ragam pada Lampiran 5 menunjukkan bahwa konsentrasi ragi memiliki pengaruh yang sangat nyata terhadap kadar alkohol setelah proses destilasi. Hasil uji LSR (Least Significant Range) pengaruh konsentrasi ragi terhadap kadar alkohol setelah proses destilasi yang dihasilkan untuk tiap-tiap perlakuan dapat dilihat pada Tabel 8.
Tabel 8. Uji LSR efek konsentrasi ragi terhadap kadar alkohol setelah proses destilasi
Keterangan : Notasi huruf yang sama pada kolom yang sama menunjukkan berbeda tidak nyata pada taraf 5% dan 1%.
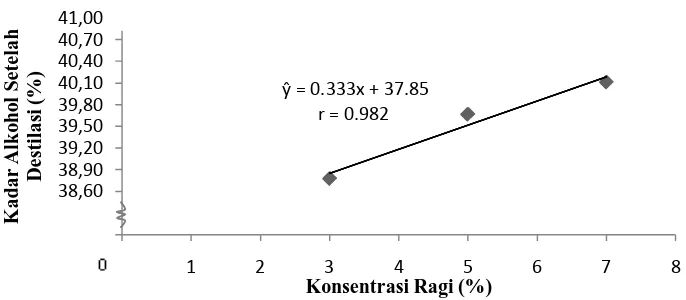
Pengaruh konsentrasi ragi terhadap kadar alkohol setelah proses destilasi mengikuti garis regresi linear seperti gambar berikut.
Gambar 4. Pengaruh konsentrasi ragi terhadap kadar alkohol
Gambar 4 menunjukkan bahwa semakin tinggi jumlah ragi yang ditambahkan maka kadar alkohol yang dihasilkan semakin tinggi. Namun peningkatan kadar alkohol ini tidak sepenuhnya dipengaruhi oleh konsentrasi ragi. Hal ini sesuai dengan pernyataan Shidik (2011) Kadar alkohol setelah proses destilasi hanya dipengaruhi oleh alat destilasi yang digunakan.
Pengaruh lama waktu fermentasi
Daftar analisis sidik ragam pada Lampiran 5 menunjukkan bahwa lama waktu fermentasi memiliki pengaruh yang tidak nyata terhadap kadar alkohol setelah proses destilasi. Sehingga uji LSR (Least Significant Range) pengaruh lama waktu fermentasi terhadap kadar alkohol yang dihasilkan tidak dilanjutkan. Pengaruh interaksi
Daftar analisis sidik ragam Lampiran 5 menunjukkan bahwa pengaruh interaksi antara konsentrasi ragi dan lama waktu fermentasi memiliki pengaruh yang tidak nyata terhadap kadar alkohol setelah proses destilasi. Sehingga uji LSR (Least Significant Range) tidak dilanjutkan.
Jumlah Etanol yang Dihasilkan
Pengaruh konsentrasi ragi
Daftar analisis sidik ragam Lampiran 6 menunjukkan bahwa konsentrasi ragi memiliki pengaruh yang sangat nyata terhadap jumlah etanol yang dihasilkan. Hasil uji LSR (Least Significant Range) pengaruh konsentrasi ragi terhadap jumlah etanol yang dihasilkan untuk tiap-tiap perlakuan dapat dilihat pada Tabel 9.
Tabel 9. Uji LSR efek konsentrasi ragi terhadap jumlah etanol yang dihasilkan
Jarak LSR
Perlakuan Rataan Notasi
P 0,05 0,01 0,05 0,01
- - - C1 846.00 a A
2 42.4603 58.1863 C2 988.44 b B
3 44.6047 61.0456 C3 1095.44 c C
Keterangan : Notasi huruf yang berbeda pada kolom yang sama menunjukkan berbeda nyata pada taraf 5% dan berbeda sangat nyata pada taraf 1%
Dari Tabel 9 dapat dilihat bahwa perlakuan C1 berbeda sangat nyata dengan C2 dan C3. Perlakuan C2 dan perlakuan C3 merupakan perlakuan yang berbeda sangat nyata juga. Jumlah etanol yang dihasilkan tertinggi diperoleh pada perlakuan C3 sebesar 1095,44 ml dan terendah pada perlakuan C1 sebesar 846,00 ml.
Gambar 5. Pengaruh konsentrasi ragi terhadap jumlah etanol
Gambar 5 menunjukkan bahwa semakin banyak jumlah ragi yang ditambahkan maka jumlah etanol yang dihasilkan semakin tinggi. Semakin tinggi kadar alkohol bahan baku hasil fermentasi (beer/sake) yang akan mengalami proses destilasi maka semakin tinggi pula jumlah alkohol yang akan dihasilkan.
Pengaruh lama waktu fermentasi
Daftar analisis sidik ragam pada Lampiran 6 menunjukkan bahwa lama waktu fermentasi memiliki pengaruh yang sangat nyata terhadap jumlah etanol yang dihasilkan pada proses destilasi. Hasil uji LSR (Least Significant Range) pengaruh pengaruh lama waktu fermentasi terhadap jumlah etanol yang dihasilkan pada proses destilasi untuk tiap-tiap perlakuan dapat dilihat pada Tabel 10.
Tabel 10. Uji LSR efek lama waktu fermentasi terhadap jumlah etanol yang dihasilkan pada proses destilasi
Jarak LSR
Perlakuan Rataan Notasi
P 0,05 0,01 0,05 0,01
- - - T1 784.89 a A
2 42.4603 58.1863 T2 1006.11 b B
3 44.6047 61.0456 T3 1138.89 c C
Dari Tabel 10 dapat dilihat bahwa perlakuan T1 berbeda sangat nyata dengan T2 dan T3. Dan perlakuan T2 dan perlakuan T3 merupakan perlakuan yang berbeda sangat nyata juga. Jumlah etanol yang dihasilkan pada proses destilasi tertinggi diperoleh pada perlakuan T3 sebesar 1138.89 ml dan terendah diperoleh pada perlakuan T1 sebesar 784,89 ml.
Pengaruh lama waktu fermentasi terhadap jumlah etanol yang dihasilkan pada proses destilasi mengikuti garis regresi linear seperti gambar berikut.
Gambar 6. Pengaruh lama waktu fermentasi terhadap jumlah etanol yang dihasilkan
Gambar 6. menunjukkan bahwa semakin lama waktu fermentasi maka jumlah alkohol yang dihasilkan semakin tinggi. Hal ini dapat dilihat pada lama waktu fermentasi 2 hari diperoleh jumlah alkohol yang dihasilkan terendah sebesar 784,89 ml dan mengalami peningkatan pada lama waktu fermentasi 3 hari dan 4 hari. Jumlah alkohol yang dihasilkan tertinggi sebesar 1138.89 ml diperoleh pada perlakuan lama waktu fermentasi 4 hari.
Pengaruh interaksi
Daftar analisis sidik ragam Lampiran 6 menunjukkan bahwa pengaruh interaksi antara konsentrasi ragi dan lama waktu fermentasi memiliki pengaruh sangat nyata terhadap jumlah etanol yang dihasilkan. Hasil uji LSR (Least
Significant Range) pengaruh interaksi tersebut dapat dilihat pada Tabel 11.
Tabel 11. Uji LSR efek utama interaksi pengaruh konsentrasi ragi dan lama waktu fermentasi terhadap jumlah etanol yang dihasilkan
Jarak LSR Perlakuan Rataan Notasi
Keterangan : Notasi huruf yang berbeda pada kolom yang sama menunjukkan berbeda nyata pada taraf 5% dan berbeda sangat nyata pada taraf 1%
Pengaruh interaksi konsentrasi ragi dan lama waktu fermentasi terhadap jumlah etanol yang dihasilkan pada proses destilasi dapat dilihat pada Gambar 7.
Gambar 7. Pengaruh kombinasi konsentrasi ragi dan lama waktu fermentesi terhadap jumlah etanol yang dihasilkan
Gambar 7 menunjukkan bahwa semakin banyak jumlah ragi yang ditambahkan maka jumlah etanol yang dihasilkan semakin tinggi. Dari gambar diatas kita dapat melihat perbedaan kombinasi perlakuan berdasarkan garis regresi linear yang ada sangat signifikan (berbeda sangat nyata). Hal ini disebabkan karena perlakuan konsentrasi ragi dan lama waktu fermentasi memiliki pengaruh yang sangat nyata terhadap jumlah etanol yang dihasilkan. Dimana semakin tinggi konsentrasi ragi dan semakin lama waktu fermentasi maka kadar alkohol bahan baku semakin tinggi sehingga semakin tinggi pula jumlah etanol yang dihasilkan .
Jumlah Etanol Perkilogram Bahan Baku yang Dihasilkan
Pengaruh konsentrasi ragi
Daftar analisis sidik ragam pada Lampiran 7 menunjukkan bahwa konsentrasi ragi memiliki pengaruh sangat nyata terhadap jumlah etanol. Hasil uji LSR (Least Significant Range) tiap perlakuan dapat dilihat pada Tabel 12.
Tabel 12. Uji LSR efek konsentrasi ragi terhadap rendemen alkohol yang dihasilkan
Keterangan : Notasi huruf yang berbeda pada kolom yang sama menunjukkan berbeda nyata pada taraf 5% dan berbeda sangat nyata pada taraf 1%
Dari Tabel 12. dapat dilihat bahwa perlakuan C1 berbeda sangat nyata dengan C2 dan C3. Rendemen alkohol yang dihasilkan tertinggi diperoleh pada perlakuan C3 dengan konsentrasi ragi 7% sebesar 108.95 ml/kg dan terendah diperoleh pada perlakuan C1 dengan konsentrasi ragi 3% sebesar 81,98 ml/kg.
Pengaruh konsentrasi ragi terhadap jumlah etanol mengikuti garis regresi linear seperti gambar berikut.
Gambar 8 menunjukkan bahwa semakin banyak jumlah ragi yang ditambahkan maka jumlah rendemen yang dihasilkan semakin tinggi hingga mencapai batas tertentu. Hal ini terjadi karena semakin banyak jumlah ragi yang ditambahkan maka akan semakin banyak mikroorganisme yang memfermentasi bahan. Pernyataan ini sesuai dengan literatur dari Tarigan (1990) Proses fermentasi tergantung pada banyak sedikitnya penambahan khamir dalam bahan. Semakin banyak jumlah ragi yang diberikan berarti semakin banyak jumlah khamir yang terlibat, sehingga kadar alkohol meningkat.
Pengaruh lama waktu fermentasi
Daftar analisis sidik ragam Lampiran 7 menunjukkan bahwa lama waktu fermentasi memiliki pengaruh yang sangat nyata terhadap jumlah etanol yang dihasilkan. Hasil uji LSR (Least Significant Range) pengaruh lama waktu fermentasi terhadap rendemen alkohol untuk tiap perlakuan dapat dilihat pada Tabel 13.
Tabel 13. Uji LSR efek lama waktu fermentasi terhadap jumlah etanol
Jarak LSR
Keterangan : Notasi huruf yang berbeda pada kolom yang sama menunjukkan berbeda nyata pada taraf 5% dan berbeda sangat nyata pada taraf 1%
lama waktu fermentasi 4 hari yaitu sebesar 112,54 ml/kg. Sedangkan rendemen alkohol terendah diperoleh pada perlakuan T1 sebesar 76,48 ml/kg.
Pengaruh lama waktu fermentasi terhadap jumlah etanol yang dihasilkan mengikuti garis regresi linear seperti gambar berikut.
Gambar 9. Pengaruh lama waktu fermentasi terhadap jumlah etanol
Gambar 9 menunjukkan bahwa semakin lama waktu fermentasi maka rendemen alkohol yang dihasilkan semakin tinggi hingga mencapai batas tertentu. Ini dikarenakan ragi akan mengalami perkembang biakan secara terus menerus sampai tingkat dimana konsentrasi alkohol yang dihasilkan menghambat pertumbuhan ragi.. Hal ini sesuai dengan literatur dari Bioinformatics Institute (1996) dimana sebuah sel ragi mampu memfermentasi glukosa dengan massa yang sama dengan massa selnya sendiri dalam jangka waktu satu jam.
Pengaruh interaksi
Daftar analisis sidik ragam pada Lampiran 4 menunjukkan bahwa pengaruh interaksi antara konsentrasi ragi dan lama waktu fermentasi memiliki pengaruh yang nyata terhadap jumlah etanol. Hasil uji LSR (Least Significant
Range) pengaruh interaksi konsentrasi ragi dan lama waktu fermentasi terhadap
ŷ = -5.518x2 + 51.14x - 3.733
Lama Waktu Fermentasi (Hari)
Tabel 14. Uji LSR efek utama interaksi pengaruh konsentrasi ragi dan lama waktu fermentasi terhadap jumlah etanol
Jarak LSR Perlakuan Rataan Notasi
Keterangan : Notasi huruf yang berbeda pada kolom yang sama menunjukkan berbeda nyata pada taraf 5% dan berbeda sangat nyata pada taraf 1%
Dari tabel 14 dapat dilihat bahwa jumlah alkohol tertinggi diperoleh pada kombinasi perlakuan konsentrasi ragi 7% dan lama waktu 4 hari (C3T3) sebesar 118,27 ml/kg, sedangkan yang terendah pada kombinasi pelakuan konsentrasi ragi 3% dengan lama waktu 2 hari (C1T1) sebesar 57,78 ml.
Pengaruh interaksi kombinasi konsentrasi ragi dan lama waktu fermentasi terhadap jumlah alkohol dilihat pada Gambar 10.
Gambar 10. Pengaruh interaksi kombinasi konsentrasi ragi dan lama waktu fermentesi terhadap jumlah alkohol.
Gambar 10 menunjukkan bahwa semakin banyak jumlah ragi yang ditambahkan maka jumlah alkohol yang dihasilkan semakin tinggi. Rendemen alkohol tertinggi diperoleh pada kombinasi perlakuan C3T3 dengan penambahan ragi sebanyak 95,2 gr dan lama waktu fermentasi selama 4 hari yaitu sebesar 118,27 ml/kg dan terendah diperoleh pada kombinasi perlakuan C1T1 penambahan ragi sebanyak 40,8 gr dan lama waktu fermentasi selama 2 hari yaitu sebesar 57.78 ml/kg. Dari gambar diatas kita dapat melihat perbedaan kombinasi perlakuan berdasarkan garis regresi linear yang ada sangat signifikan. Hal ini menunjukkan rendemen yang dihasilkan sangat dipengaruhi oleh konsentrasi ragi dan lama waktu fermentasi, selain itu rendemen yang dihasilkan juga dipengaruhi oleh kemampuan alat dalam mendestilasi larutan hasil fermentasi. Hal ini sesuai dengan pernyataan dari Briggs, et al., (1981) Proses fermentasi dalam pembuatan alkohol sulit untuk dikontrol. Terkadang proses fermentasi terjadi dengan waktu yang cukup lama tergantung pemilihan ragi yang akan digunakan dan proses penyulingan.
KESIMPULAN DAN SARAN
Kesimpulan
1. Kadar alkohol setelah fermentasi tertinggi diperoleh pada perlakuan C3T3 sebesar 8 %, dan terendah pada perlakuan C1T1 sebesar 4%.
2. Jumlah etanol tertinggi diperoleh pada perlakuan C3T3 sebesar 1186,33 ml dengan kadar alkohol 41% dan terendah pada perlakuan C1T1 sebesar 592,67 ml dengan kadar alkohol 39%.
3. Jumlah etanol perkilogram bahan baku tertinggi diperoleh pada perlakuan C3T3 sebesar 108,27 ml/kg dan terendah pada perlakuan C1T1 sebesar 57,78 ml/kg.
4. Kombinasi perlakuan terbaik dari hasil penelitian ini adalah perlakuan C3T3 (konsentrasi ragi 7% dan lama waktu fermentasi 4 hari).
5. Proses liquifikasi (pemecahan polisakarida menjadi disakarida) merupakan proses yang paling menentukan dalam keberhasilan pembuatan bioetanol yang berasal dari bahan berpati.
6. Konsetrasi ragi memberikan pengaruh yang sangat nyata terhadap kadar alkohol setelah proses fermentasi, kadar alkohol setelah proses destilasi, jumlah etanol yang dihasilkan dan jumlah etanol perkilogram bahan baku yang dihasilkan.
8. Interaksi perlakuan konsentrasi ragi dan lama waktu fermentasi memberikan pengaruh yang sangat nyata terhadap jumlah etanol yang dihasilkan jumlah etanol perkilogram bahan baku yang dihasilkan.
9. Semakin tinggi konsentrasi ragi yang digunakan maka kadar alkohol setelah proses fermentasi, jumlah etanol dan jumlah etanol perkilogram bahan baku yang dihasilkan semakin meningkat.
10. Semakin lama waktu fermentasi yang dilakukan maka kadar alkohol setelah proses fermentasi, jumlah etanol dan jumlah etanol perkilogram bahan baku yang dihasilkan semakin meningkat.
Saran
1. Perlu dirancang alat pemeras mekanis agar proses pemerasan ampas berlangsung sempurna.
2. Perlu dilakukan penggantian terhadap pipa tembaga saluran uap dengan diameter yang lebih besar untuk mengurangi kebocoran.
3. Sebaiknya pada tutup drum pemasakan digunakan bahan yang tahan
terhadap uap panas agar tidak terjadi kebocoran pada tutupnya.
4. Setelah pemakaian alat, sebaiknya alat dibersihkan kembali agar alat dapat digunakan lebih lama.
DAFTAR PUSTAKA
Archunan, G., 2004. Microbiology. First Edition. Sarup & Sons, New Delhi. Arisworo, D., dan Yusa, 2006. Biologi. Grafindo Media Perkasa, Jakarta.
Briggs, D. E., J. S. Hough, R. Stevens and T. W. Young, 1981. Malting and
Brewing Science. Chapman and Hall, London.
Buckle, K.A. 1985, Ilmu Pangan, UI.Press. Jakarta.
Dwinarso, B., 2010. Skripsi : Rancang Bangun Alat Destilasi Bioetanol Berbahan Baku Ubi Kayu (Manihot esculenta Crantz). USU, Medan.
European Bioinformatics Institute (1996). Eukaryotes Genomes-Saccharomyces cerevisiae. http://www.embl ebi.com/Saccharomyces_cerevisiae.html [5 Februari 2011].
Fessenden and Fessenden, 1986. Organic Chemistry. Third Edition. Wadsworth, Inc., California.
Greenwell, A.B.H.1974. Tarowith Spesial Reference to Its Culture and Uses In
Hawai. Economic Botany 1. Applied Science Publisher Ltd. London
Hambali, E., S, Mujdalipah, A. H. Tambunan, A. W. Pattiwiri dan R. Hendroko, 2008. Teknologi Bioenergi. Agro Media, Jakarta.
Hamidah, H., 2003. Produksi Alkohol. USU Press, Medan.
Harper., Laura, J., 1986. Pangan, Gizi dan Pertanian. UI Press, Jakarta. Hendroko, R., 2007. Energi Hijau. Agromedia. Jakarta.
Hidayat, N., M. C. Padaga dan S. Suhartini, 2006. Mikrobiologi Industri. Andi, Yogyakarta
.
Irianto, K. 2006, Mikrobiologi: Menguak Dunia Mikroorganisme Jilid 2, CV. Yrama Widya. Bandung.
Judoamidjojo, M. Darwis, A., Sa”id, E.G. 1992. Teknologi Fermentasi. Penerbit Rajawali Pers, Jakarta.
Karmawati, 2009. Tanaman Perkebunan Penghasil Bahan Bakar Nabati. IPB Press, Bogor.
Kister, H. Z., 1992. Distillation Design. Mc Graw-Hill, California.
Lurgi, G., 1989. Alcohol Destilation, Gulf Publishing Company, Frankurt.
Muchtadi,T.R dan Sugiono.1992. Petunjuk Laboratorium Ilmu Pengetahuan Bahan Pangan. PAU Pangan dan Gizi. IPB, Bogor.
Norman, B. E. 1980. New Developments in Starch Syrup Technology Processing. Applied Science Publ. Ltd., London.
Nur, M. 1995. Tanaman Talas (Colocasia dan beberapa genus yang lain). Kementrian Pertanian . Jakarta
Perry, R. H., D. W. Green and J. O. Maloney, 1999. Perry’s Chemical Engineers
Handbook 7th Edition. McGraw Hill Book Company, New York.
Poedjiaji, A., dan T, Supriyanti. 1994. Dasar-Dasar Biokimia. UI Press, Jakarta. Prescott, S. G and C. G. Dunn, 1959, “Industrial Microbiology”. McGraw-Hill
BookCompany, New York.
Purseglove, J.W. 1972. Tropicals Crops Monocotyledons. John Wiley and Sons. Inc. New York
Riegel, R., 1992. Riegel’s Handbook of Industrial Chemistry. Van Nostrad Reinhold, New York.
Rubatzky, V. E., dan M. Yamaguchi, 1998. Sayuran Dunia 1 Prinsip Produksi dan Gizi. Penerjemah: Ir. Catur Herison, M.Sc. ITB Press, Bandung.
Shidik, I., 2011. Skripsi : Pembuatan Bioetanol Dengan Bahan Baku Menir Padi (Oryza sativa). USU, Medan.
Sumarsih, S., 2003. Mikrobiologi Dasar. Universitas Pembangunan Nasional Veteran, Yogyakarta.
Suprapti, M. L., 2005. Kecap Tradisional. Kanisus, Yogyakarta.
Susana. 1989. Biokonversi. Edisi I cetakan I. Rajawali Pustaka, Jakarta.
Tarigan, J., 1988, Pengantar Mikrobiologi Umum. Departemen Pendidikan dan Kebudayaan Direktorat Jenderal Pendidikan Tinggi. Jakarta.
Lampiran 3. Spesifikasi Alat Destilasi Bioetanol yang Digunakan 1. Drum Pemasakan
Dimensi
Diameter : 37 cm
Tinggi : 34,5 cm
2. Kondensor Dimensi
Diameter : 40 cm
Tinggi : 49 cm
3. Pipa Saluran Uap Dimensi
Diameter : 5 mm
Panjang : 5 m
Tebal Plat : 1,2 mm
Kapasitas Efektif : 831,255 ml/jam
Lampiran 4. Kadar Alkohol Setelah Fermentasi (%)
Total 58.00 56.00 57.00 171.00
Rataan 6.44 6.22 6.33 19.00 6.33
Analisa Sidik Ragam Kadar Alkohol Setelah Fermentasi
Lampiran 5. Kadar Alkohol Setelah Destilasi
Analisa Sidik Ragam Kadar Alkohol Setelah Proses Destilasi
Lampiran 6. Jumlah Etanol yang Dihasilkan
Perlakuan Ulangan (ml) Total (ml) Rataan (ml)
I II III
Analisa Sidik Ragam Jumlah Etanol yang Dihasilkan
Lampiran 7. Rendemen Alkohol yang Didapat
Perlakuan Ulangan (ml/Kg) Total (Kg) Rataan (Kg)
I II III
Analisa Sidik Ragam Rendemen Alkohol
Lampiran 8. Massa Endapan Setelah Proses Pemerasan
Perlakuan Ulangan (Kg) Total (Kg) Rataan (Kg)
I II III
Volume Beer/Sake Setelah Proses Pemerasan
Perlakuan Ulangan (ml) Total (ml) Rataan
(ml)
Total 65848.00 66320.00 66197.00 198365.00
Lampiran 12. Dokumentasi Penelitian
Tanaman Kimpul (Xanthosoma sagittifolium)
Kimpul
Pembuatan Bubur
Pengukuran Enzim
Ampas Sisa Perasan
Larutan etanol hasil perasan dari hasil fermentasi
Alat Destillasi yang Digunakan
Drum Pemasakan
Tetes Etanol