UJI TOKSISITAS EKSTRAK ETIL ASETAT TERAKTIF
DAUN DANDANG GENDIS (
Clinacanthus nutans
)
MENGGUNAKAN UJI LETALITAS LARVA UDANG
DWI CAHYA AGUSTINA
DEPARTEMEN KIMIA
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM
INSTITUT PERTANIAN BOGOR
ABSTRAK
DWI CAHYA AGUSTINA. Uji Toksisitas Ekstrak Etil Asetat Teraktif Daun Dandang
Gendis (
Clinacanthus nutans
) Menggunakan Uji Letalitas Larva Udang. Dibimbing oleh
DUDI TOHIR dan GUSTINI SYAHBIRIN.
Dandang gendis (
Clinacanthus nutans
) merupakan tumbuhan obat yang biasa
digunakan masyarakat sebagai obat tradisional untuk antimalaria dan antidiabetes.
Penelitian diawali dengan maserasi serbuk daun dandang gendis menggunakan etanol,
kemudian ekstrak kasar etanol dipartisi menggunakan
n
-heksana. Fraksi etanol bebas
senyawa nonpolar kemudian dipartisi menggunakan etil asetat. Uji toksisitas
menggunakan uji letalitas larva udang terhadap ekstrak kasar etanol, fraksi
n
-heksana,
dan fraksi etil asetat. Fraksi etil asetat memiliki aktivitas paling tinggi dengan konsentrasi
mematikan 50%
sebesar 64.32 mg/L. Ekstraksi kembali fraksi etanol bebas senyawa
nonpolar menggunakan pelarut etil asetat dengan kondisi waktu ekstraksi 90 menit,
jumlah ekstraksi 3 kali, dan nisbah sampel:pelarut 1:2 menghasilkan nilai LC
50sebesar
29.02 mg/L. Hasil uji fitokimia positif saponin, alkaloid, steroid, dan flavonoid.
Kandungan flavonoid ekstrak etil asetat re-ekstraksi lebih besar dibandingkan kandungan
flavonoid ekstrak etil asetat pada ekstraksi awal.
ABSTRACT
DWI CAHYA AGUSTINA. Toxicity Assay of The Most Active Ethyl Acetate Extract
from
Clinacanthus nutans
Leaves by Using Brine Shrimp Lethality Test. Supervised by
DUDI TOHIR and GUSTINI SYAHBIRIN.
Dandang gendis
(
Clinacanthus nutans
) is a medical herb commonly used as a traditional
medicine as antimalarial and antidiabetic. This study was started with maceration of the
dried leaves of dandang gendis with ethanol,and then partitioned using
n
-hexane. The
ethanol extract free of nonpolar compounds was then partitioned with ethyl acetate. The
ethanol crude extract,
n
-hexane fraction, and ethyl acetate fraction were tested by using
brine shrimp lethality test to determine the toxicity of each extract. The ethyl acetate
fraction showed the highest activity with 50% lethal concentration (LC
50) of 32 mg/L.
Re-extraction of ethanol extract free of nonpolar compounds by using ethyl acetate in 90
minutes by three times extraction with material:solvent ratio of 1:2 resulted LC
50value of
UJI TOKSISITAS EKSTRAK ETIL ASETAT TERAKTIF
DAUN DANDANG GENDIS (
Clinacanthus nutans
)
MENGGUNAKAN UJI LETALITAS LARVA UDANG
DWI CAHYA AGUSTINA
Skripsi
sebagai salah satu syarat untuk memperoleh gelar
Sarjana Sains pada
Departemen Kimia
DEPARTEMEN KIMIA
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM
INSTITUT PERTANIAN BOGOR
Judul Skripsi : Uji Toksisitas Ekstrak Etil Asetat Teraktif Daun Dandang Gendis
(Clinacanthus nutans) Menggunakan Uji Letalitas Larva Udang
Nama
: Dwi Cahya Agustina
NIM : G44052565
Disetujui,
Pembimbing I
Pembimbing II
Drs Dudi Tohir, MS
Dr Gustini Syahbirin, MS
NIP 19571104 198903 1 001 NIP 19600819 198903 2 002
Diketahui,
Ketua Departemen Kimia
Prof Dr Ir Tun Tedja Irawadi, MS
NIP 19501227 197603 2 002
PRAKATA
Puji dan syukur penulis panjatkan ke hadirat Allah SWT atas rahmat dan
karunia-Nya sehingga penulis dapat menyelesaikan karya ilmiah ini. Karya ilmiah
yang berjudul Uji Toksisitas Ekstrak Etil Asetat Teraktif Daun Dandang Gendis
(Clinacanthus nutans) Menggunakan Uji Letalitas Larva Udang merupakan salah
satu syarat untuk memperoleh gelar sarjana sains pada Departemen Kimia FMIPA
IPB.
Penulis mengucapkan terima kasih kepada Bapak Drs Dudi Tohir, MS dan
Ibu Dr Gustini Syahbirin, MS sebagai pembimbing yang telah memberikan
arahan, saran, dan dorongan selama pelaksanaan penelitian dan penulisan karya
ilmiah ini. Ungkapan terima kasih penulis sampaikan kepada keluarga tercinta,
Bapak, Ibu, Mba Eka, Mas Didi, Yoga, dan Rara yang selalu memberikan
semangat, doa, dan kasih sayang dalam berbagai bentuk yang tak pernah putus.
Penulis mengucapkan terima kasih juga kepada Kak Budi Arifin, SSi, MSi, Pak
Sabur, Ibu Yeni, Ibu Aah, Teh Nia dan seluruh staf Laboratorium Kimia Organik
atas fasilitas dan bantuan yang diberikan selama penelitian. Ucapan terima kasih
tak lupa penulis berikan kepada Mba Sherly, Vicky, Rita, Irma, Gae, Ayu, dan
Noe yang turut membantu, memberikan semangat dan dukungannya dalam
penyusunan karya ilmiah, serta semua pihak yang tidak dapat penulis sebutkan
satu per satu. Semoga karya ilmiah ini dapat bermanfaat.
Bogor, September 2012
RIWAYAT HIDUP
Penulis dilahirkan di Cirebon pada tanggal 15 Agustus 1986 sebagai putri
kedua dari tiga bersaudara dari pasangan Agnan Lukito dan Kusriyati Tedas.
Tahun 2004 penulis lulus dari SMU Negeri 2 Brebes dan pada tahun 2005
lulus seleksi masuk Institut Pertanian Bogor (IPB) melalui jalur Seleksi
Penerimaan Mahasiswa Baru (SPMB). Penulis memilih Program Studi Kimia,
Departemen Kimia, Fakultas Matematika dan Ilmu Pengetahuan Alam.
vi
DAFTAR ISI
Halaman
DAFTAR TABEL ... vii
DAFTAR GAMBAR ... vii
DAFTAR LAMPIRAN ... vii
PENDAHULUAN ... 1
BAHAN DAN METODE
Bahan dan Alat ... 2
Penentuan Kadar Air ... 2
Ekstraksi ... 2
Uji Fitokimia ... 2
Uji Toksisitas ... 2
HASIL DAN PEMBAHASAN
Kadar Air ... 3
Ekstrak ... 3
Hasil Uji Fitokimia ... 3
Hasil Uji Toksisitas ... 4
SIMPULAN DAN SARAN
Simpulan ... 4
Saran ... 5
DAFTAR PUSTAKA ... 5
vii
DAFTAR TABEL
Halaman
1 Hasil uji fitokimia ekstrak etanol ... 3
2 Hasil uji fitokimia ekstrak etil asetat awal dan re-ekstraksi... 4
3 Nilai LC
50hasil ekstraksi daun dandang gendis . ... 4
DAFTAR GAMBAR
Halaman
1 Daun dandang gendis. ... 1
2
Struktur 5 senyawa dandang gendis yang mengandung sulfur
... 13
A. salina
... 4
DAFTAR LAMPIRAN
Halaman
1 Diagram alir penelitian ... 8
2 Uji fitokimia ... 9
3 Pembuatan stok ekstrak 5000 ppm dan penetasan larva
A. salina
... 9
4 Uji toksisitas terhadap
A. salina
... 9
5 Penentuan kadar air ... 10
6 Rendemen ekstrak etanol ... 10
7 Hasil uji fitokimia ... 11
8 Data uji toksisitas ekstrak etil asetat daun dandang gendis pada
A salina
... 12
1
PENDAHULUAN
Dandang gendis (Gambar 1) merupakan salah satu tumbuhan obat tradisional yang lazim digunakan masyarakat sebagai antidiabetes dan antimalaria. Kemampuan ekstrak daun dandang gendis sebagai obat alami dikarenakan terdapat kandungan senyawa bioaktif di dalamnya. Dandang gendis yang termasuk ke dalam famili Acanthaceae memiliki banyak kandungan kimia seperti alkaloid, flavonoid, dan terpenoid (Suharty 1984).
Gambar 1 Daun dandang gendis.
Berbagai penelitian yang telah dilakukan menunjukkan khasiat ekstrak daun dandang gendis. Ekstrak etanol dapat dijadikan sebagai antimalaria dan antimikrob karena mengandung senyawa trans -3-metilsulfonil-2-propenol dan trans-3-metilsulfinil-2-propenol (Tuntiwachwuttikul et al. 2003). Ekstrak daun dandang gendis berpotensi sebagai antikanker (Sofyan 2008), larvasida Aedes aegypti
(Andriani 2008), antivirus Herpes simplex
(Yoosook et al. 1999; Thongchai et al. 2008), dan antioksidan (Pannangpetch et al. 2007; Akbar 2010; Agustina 2011). Ekstrak air dari daun dandang gendis juga berpotensi sebagai antidiabetes, dibuktikan setelah pemberian glukosa 2 g/kg (b/b) terjadi penurunan kadar glukosa darah pada mencit (Nurulita 2005).
Penelitian Teshima et al. (1997)
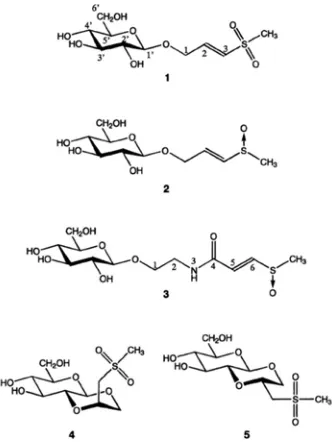
menunjukkan 6 senyawa dalam ekstrak n -butanol daun dan batang dandang gendis, yaitu senyawa C-glikosil flavon, viteksin, isoviteksin, shaftosida, isomolupentin 7-Ο-β -glukopiranosida, dan orientin. Penelitian lanjutan Teshima et al. (1997) juga menghasilkan 5 senyawa yang mengandung sulfur dengan rumus molekul diantaranya C10H18O8S (1), C10H18O7S (2), C12H21NO8S
(3), C10H18O8S (4), dan C10H18O8S (5).
(Gambar 2).
Gambar 2 Struktur 5 senyawa dandang gendis yang mengandung sulfur (Teshima
et al. 1997)
Salah satu metode untuk menentukan potensi bioaktif ekstrak tanaman adalah uji kematian larva udang atau brine shrimp lethality test (BSLT). Metode ini memiliki beberapa kelebihan antara lain sederhana, cepat, tidak memerlukan peralatan khusus, dan hanya menggunakan sedikit ekstrak contoh. Uji ini tidak spesifik untuk antitumor, tetapi kemampuannya mendeteksi 14 dari 24 ekstrak Euphorbiaceaeyang aktif terhadap uji leukemia secara in vivo pada mencit dan mendeteksi 2 dari 6 spesies yang aktif terhadap uji karsinoma nasofaring menunjukkan bahwa uji ini dapat dipakai untuk penapisan awal senyawa bioaktif (Meyer et al. 1982).
Penelitian Setiawan (2009) meragamkan parameter suhu, jumlah ekstraksi, dan nisbah sampel:pelarut menghasilkan nilai konsentrasi mematikan 50% (LC50) terendah sebesar
2
penelitian ini adalah ekstraksi padat-cair secara maserasi, dilanjutkan dengan ekstraksi cair-cair untuk memperoleh ekstrak paling aktif. Ekstrak paling aktif berdasarkan uji BSLT kemudian di re-ekstraksi dan ditentukan kembali nilai LC50 dengan parameter waktu
ekstraksi 90 menit, jumlah ekstraksi 3 kali, dan nisbah sampel:pelarut 1:2. Re-ekstraksi dengan perlakuan 3 parameter tersebut diharapkan meningkatkan bioaktivitas ekstrak terhadap hewan uji. Penelitian ini bertujuan menentukan nilai LC50 ekstrak teraktif daun
dandang gendis berdasarkan BSLT.
BAHAN DAN METODE
Bahan dan Alat
Bahan-bahan yang digunakan adalah daun dandang gendis dari daerah Batuhulung Bogor, A. salina, serbuk Mg, pereaksi Meyer, Dragendorf, Wagner, Lieberman-Buchard, FeCl3 1%, dan air laut.
Alat-alat yang digunakan adalah peralatan kaca, mikropipet, pelat tetes, penguap putar, sumur uji BSLT, dan peralatan penetasan telur
A. salina.
Penentuan Kadar Air
Pinggan porselen dikeringkan pada suhu 105 ºC selama 30 menit, didinginkan dalam eksikator, dan ditimbang. Daun yang telah dikeringudarakan kurang lebih sebanyak 3 g dimasukkan ke dalam pinggan, dikeringkan pada suhu 105 ºC selama 3 jam, didinginkan dalam eksikator dan ditimbang. Pengeringan diulangi lagi selama 3 jam pada suhu 105 ºC, didinginkan, kemudian ditimbang kembali. Prosedur ini diulangi hingga didapat bobot yang tetap (stabil). Kadar air dihitung dengan persamaan sebagai berikut:
Keterangan:
a = bobot contoh awal (g)
b = bobot contoh akhir (g)
Ekstraksi
Sebanyak 400 g serbuk daun dandang gendis dimaserasi beberapa kali hingga filtrat tidak berwarna hijau lagi. Filtrat disaring dengan kertas saring lalu dipekatkan pada suhu 40 oC. Ekstrak etanol yang diperoleh diuji BSLT dan fitokimia (Lampiran 1) kemudian dipartisi menggunakan n-heksana. Fraksi n-heksana dipekatkan lalu diuji BSLT dan fitokimia. Fraksi etanol bebas senyawa nonpolar ditambahkan air dan dipartisi menggunakan etil asetat. Dihasilkan fraksi etil asetat dan fraksi etanol-air. Kedua fraksi tersebut juga dipekatkan dan diuji BSLT dan fitokimia. Fraksi paling aktif dari hasil uji di re-ekstraksi menggunakan 3 parameter yaitu waktu ekstraksi 90 menit, nisbah sampel:pelarut 1:2, dan jumlah ekstraksi 3 kali, lalu ditentukan kembali nilai LC50.
Uji Fitokimia
Uji fitokimia (flavonoid, alkaloid, saponin, triterpenoid, steroid, dan tanin) dilakukan berdasarkan prosedur Harborne (1987) (Lampiran 2)
Uji Toksisitas
Sepuluh ekor A. salina yang telah ditetaskan dimasukkan ke dalam sumur uji BSLT yang berisi air laut dan dibuat konsentrasi ekstrak 0, 10, 100, 500, dan 1000 mg/L (Lampiran 3 dan 4). Pengamatan dilakukan 24 jam setelah penetasan dengan menghitung jumlah A. salina yang mati dengan bantuan kaca pembesar. Data persen mortalitas diolah menggunakan analisis probit dengan tingkat kepercayaan 95%. Kurva penentuan LC50 dibuat menghubungkan log
konsentrasi dengan nilai probit. Nilai LC50
3
HASIL DAN PEMBAHASAN
Kadar Air
Daun dandang gendis yang telah dikering kan dan digiling menjadi serbuk ditentukan kadar airnya menggunakan metode gravimetri taklangsung pada suhu 105 ºC. Kadar air yang ditentukan adalah yang terikat secara fisik dan dapat dihilangkan pada suhu 100 - 105 ºC (Harjadi 1993). Kadar air digunakan sebagai parameter ketahanan bahan dalam penyimpanan dan sebagai faktor koreksi untuk rendemen. Menurut Winarno (1997), apabila kadar air suatu bahan kurang dari 10%, pertumbuhan mikrob dapat dihindari sehingga bahanl dapat disimpan dalam waktu relatif lama.
Kadar air daun dandang gendis kering diperoleh sebesar
9.69%
(Lampiran 5). Hasil ini masih di bawah 10% sehingga sampel dapat disimpan dalam waktu relatif lama.Ekstrak
Proses diawali dengan maserasi sampel menggunakan etanol. Maserasi dilakukan berulang kali sampai filtrat tidak berwarna hijau lagi, sehingga dapat dianggap semua senyawa yang berbobot molekul rendah telah terekstraksi (Harborne 1987). Penggunaan etanol yang bersifat polar didasarkan pada sifat senyawa polar yang akan diekstraksi yaitu flavonoid, alkaloid, tanin. Diharapkan semua senyawa tersebut dapat terekstraksi dengan baik oleh pelarut dengan sifat kepolaran yang sama. Selain itu etanol memiliki titik didih yang rendah sehingga mudah diuapkan kembali, dan sifatnya tidak setoksik pelarut polar lainnya seperti metanol. Maserasi dengan etanol menghasilkan rendemen sebesar 25.46%(Lampiran 6).
Ekstrak etanol selanjutnya dipartisi dengan
n-heksana untuk menarik senyawa nonpolar. Fraksi etanol bebas senyawa nonpolar ditambahkan akuades dan dipartisi kembali dengan etil asetat. Akuades ditambahkan untuk meningkatkan kepolaran, sebab etil asetat memiliki kepolaran yang tidak jauh berbeda dengan etanol. Hal ini dapat memperjelas batas pemisahan pada proses partisi etil asetat (Afif 2006).
Parameter waktu re-ekstraksi dipilih 90 menit karena pada saat itu ekstrak telah menjadi lebih jernih dibandingkan dengan waktu ekstraksi 30 dan 60 menit. Semakin lama waktu ekstraksi semakin banyak senyawa bioaktif akan terambil, ditandai dengan perubahan warna ekstrak. Demikian pula dengan jumlah ekstraksi, ekstraksi beberapa kali dengan sedikit pelarut lebih efektif dibandingkan dengan menggunakan pelarut dalam jumlah banyak sekaligus.
Hasil Uji Fitokimia
Uji kualitatif fitokimia digunakan untuk mengetahui jenis senyawa metabolit sekunder yang terkandung dalam ekstrak. Golongan senyawa dapat ditentukan dari perubahan warna setelah penambahan pereaksi spesifik untuk setiap uji kualitatif. Hasil uji fitokimia ekstrak kasar daun dandang gendis (Tabel 1) ialah terbentuknya warna putih, cokelat, dan jingga dengan pereaksi Meyer, Wagner, dan Dragendorf; terbentuk buih yang stabil setelah pengocokan; terbentuk warna jingga pada lapisan amil alkohol; terbentuk warna hijau dengan pereaksi Lieberman-Buchard; dan warna hitam dengan FeCl3 1%. Hasil ini
berturut-turut menunjukkan bahwa ekstrak kasar daun dandang gendis positif mengandung senyawa alkaloid, saponin, flavonoid, steroid, dan tanin. Sementara ekstrak etil asetat hasil re-ekstraksi mengandung alkaloid, saponin, steroid, dan flavonoid (Tabel 2). Kandungan flavonoid ekstrak etil asetat re-ekstraksi lebih besar daripada kandungan flavonoid ekstrak etil asetat awal, terlihat dari lebih pekatnya warna yang dihasilkan. Gambar hasil uji fitokimia dapat dilihat pada Lampiran 7.
Tabel 1 Hasil uji fitokimia ekstrak etanol
Golongan Senyawa Etanol
Alkaloid +++
Saponin +++
Flavonoid +++
Triterpenoid -
Steroid +++
Tanin +++
4
Tabel 2 Hasil uji fitokimia ekstrak etil asetat awal dan re-ekstraksi
Golongan Senyawa Etil Asetat Awal *Etil Asetat Re-ekstraksi
Alkaloid ++ ++
Saponin ++ ++
Flavonoid ++ +++
Triterpenoid - -
Steroid ++ ++ Tanin ++ - Keterangan : *re-ekstraksi dilakukan pada kondisi
waktu ekstraksi 90 menit, jumlah ekstraksi 3 kali, dan nisbah sampel:pelarut 1:2
Hasil Uji Toksisitas
Proses penetasan larva udang A. salina
(Gambar 3) menggunakan air laut dengan bantuan aerator untuk menjaga kadar oksigen yang terlarut. Gelembung udara dari aerator juga berfungsi untuk mengaduk telur agar tidak mengendap di dasar wadah. Telur akan sulit menetas jika oksigen dalam air kurang. Penyinaran selama proses penetasan berfungsi menjaga kondisi air laut agar tetap hangat. Umur larva udang yang digunakan adalah 24 jam setelah menetas. Kondisi membran sel larva udang pada umur tersebut masih lunak sehingga memudahkan senyawa asing dalam air laut masuk dan menyebabkan kematian. Kematian larva udang yang disebabkan masuknya senyawa asing dijadikan dasar untuk pengujian toksisitas ekstrak aktif daun dandang gendis dalam penelitian ini.
Gambar 3 A. salina.
Suatu senyawa memiliki potensi bioaktif jika nilai LC50-nya di bawah 1000 mg/L. Hasil
pengujian toksisitas larva udang ekstrak kasar (fraksi etanol), fraksi n-heksana, fraksi etanol-air, fraksi etil asetat, dan fraksi etil asetat re-ekstraksi dapat dilihat pada Tabel 3.
Tabel 3 Nilai LC50 hasil ekstraksi daun
dandang gendis
Pelarut LC50 (mg/L) Etanol
n-heksana Etanol-air Etil asetat
Etil asetat re-ekstraksi
124.42 668.95 276.94 64.32 29.02
LC50 yang diperoleh menunjukkan bahwa
semua ekstrak memiliki potensi bioaktif. Ekstrak etil asetat paling aktif dengan nilai LC50 64.32 mg/L (Lampiran 8). Selanjutnya
dilakukan re-ekstraksi terhadap fraksi paling aktif dengan menggunakan 3 parameter, yaitu waktu ekstraksi 90 menit, jumlah ekstraksi 3 kali, dan nisbah sampel:pelarut 1:2 yang kemudian ditentukan kembali nilai LC50 nya.
Ekstrak etil asetat hasil re-ekstraksi menghasilkan nilai LC50 sebesar 29.02 mg/L
dengan R2 = 99.2% (Lampiran 9). LC50 yang
dihasilkan lebih rendah dari penelitian Setiawan (2009) yang menggunakan parameter suhu 40 ºC, nisbah sampel:pelarut 1:4, dan jumlah ekstraksi 3 kali dan menghasilkan nilai LC50 sebesar 59.15 mg/L.
Setelah dilakukan re-ekstraksi, nilai LC50
fraksi etil asetat turun menjadi 29.02 mg/L. Semakin kecil nilai LC50, semakin tinggi
aktivitasnya. Hal ini menunjukkan bahwa lamanya waktu, jumlah ekstraksi, dan nisbah sampel:pelarut dapat meningkatkan keaktifan ekstrak dalam penelitian ini. Turunnya nilai LC50 dapat juga disebabkan karena kandungan
flavonoid ekstrak etil asetat hasil re-ekstraksi lebih besar dibandingkan dengan kandungan flavonoid pada ekstrak etil asetat awal. Keaktifan etil asetat hasil re-ekstraksi ini tergolong sangat aktif menurut National Cancer Institute (NCI) Amerika yang menyatakan bahwa standar efektivitas komponen bioaktif untuk melawan sel kanker adalah ≤ 30 mg/L (Albuntana et al. 2011).
SIMPULAN DAN SARAN
Simpulan
Setelah dilakukan re-ekstraksi, nilai LC50
5
menunjukkan etil asetat re-ekstraksi mengandung alkaloid, saponin, steroid, dan flavonoid dengan kandungan flavonoid lebih besar dibandingkan kandungan flavonoid ekstrak etil asetat ekstraksi awal.
Saran
Perlu penelitian lanjutan ke arah potensi daun dandang gendis sebagai antikanker secara in vitro menggunakan sel kanker.
DAFTAR PUSTAKA
Afif KH. 2006. Peningkatan kadar kurkumin ekstrak etanol temulawak dengan metode ekstraksi cair-cair [skripsi]. Bogor: Fakultas Matematika dan Ilmu Pengetahuan Alam, Institut Pertanian Bogor.
Agustina S. 2011. Isolasi golongan flavonoid sebagai antioksidan dari daun dandang gendis (Clinacanthus nutans) [skripsi]. Bogor: Fakultas Matematika dan Ilmu Pengetahuan Alam, Institut Pertanian Bogor.
Akbar HR. 2010. Isolasi dan identifikasi golongan flavonoid daun dandang gendis (Clinacanthus nutans) berpotensi sebagai antioksidan [skripsi]. Bogor: Fakultas Matematika dan Ilmu Pengetahuan Alam, Institut Pertanian Bogor.
Albuntana A, Yasman, Wardhana W. 2011. Uji toksisitas ekstrak empat jenis teripang suku Holothuriidae dari Pulau Penjaliran Timur, Kep. Seribu, Jakarta menggunakan BSLT. J Ilmu Teknol Kelautan Trop 3:65-72.
Andriani A. 2008. Identifikasi senyawa golongan aktif ekstrak daun Clinacanthus nutans yang berpotensi sebagai larvasida pada Aedes aegypti [skripsi]. Bogor: Fakultas Matematika dan Ilmu Pengetahuan Alam, Institut Pertanian Bogor.
Harborne JB. 1987. Metode Fitokimia.
Padmawinata K, Sudiro I, penerjemah.
Bandung: Institut Teknologi Bandung. Terjemahan dari: Phytochemical Method.
Harjadi W. 1993. Ilmu Kimia Analitik Dasar. Jakarta: Gramedia Pustaka Utama.
Meyer BN et al. 1982. Brine shrimp: a convenient general bioassay for active plant constituent. Planta Med 45:31-34.
Nurulita Y. 2005. Penapisan aktivitas antidiabetes isolat ekstrak air daun dandang gendis (Clinacanthus nutans) pada mencit Swiss Webster jantan [skripsi]. Bandung: Fakultas Matematika dan Ilmu Pengetahuan Alam, Institut Teknologi Bandung.
Pannangpetch P et al. 2007. Antioxidant activity and protective effect against oxidative hemolysis of Clinacanthus nutans (Burm.f) Lindau. J Sci Technol 1: 1-9.
Setiawan I. 2009. Optimalisasi ekstraksi cair-cair fraksi etanol ekstrak daun dandang gendis (Clinacanthus nutans) pada uji toksisitas Artemia salina [skripsi]. Bogor: Fakultas Matematika dan Ilmu Pengetahuan Alam, Institut Pertanian Bogor.
Sofyan D. 2008. Inhibisi fraksi aktif daun dandang gendis (Clinacanthus nutans) pada pertumbuhan Saccharomyces cerevisiae sebagai uji potensi antikanker [skripsi]. Bogor: Fakultas Matematika dan Ilmu Pengetahuan Alam, Institut Pertanian Bogor.
Suharty NS. 1984. Isolasi terpenoid dari daun
Clinacanthus nutans [tesis]. Bandung: Program Pascasarjana, Institut Teknologi Bandung.
Teshima I et al. 1997. Sulfur-containing glucosides from Clinacanthus nutans.
Phytochemistry 48:831-835.
Thongcai S et al. 2008. Anti-herpes simplex virus type 1 activity of crude ethyl acetate extract derived from leaves of
Clinacanthus nutans Lindau. JSci Technol
6
Tuntiwachwuttikul P, Yupa P, Pootchana P, Thongchai S, Walter CT. 2003. Sulfur-containing compounds from Clinacanthus siamensis [abstrak]. Pharm Soc Japan
51:1423-1425.
Winarno FG. 1997. Kimia Pangan dan Gizi. Jakarta: Gramedia Pustaka Utama.
8
Lampiran 1 Diagram alir penelitian
Dipekatkan
Uji BSLT
Uji Fitokimia
Fraksi
n
-Heksana
Fraksi Etanol-Air
*Fraksi Etil Asetat
+Akuades
Partisi dengan etil asetat
Maserasi dengan etanol sampai filtrat
tak berwarna
Partisi dengan n-heksana
Daun Kering
Ekstrak Etanol
Dipekatkan
Uji Fitokimia
Uji BSLT
Fraksi Etanol
*fraksi paling aktif di re-ekstraksi
menggunakan parameter waktu 90 menit, 3
kali jumlah ekstraksi, dan nisbah
bahan:pelarut 1:2
9
Lampiran 2 Uji fitokimia
Uji alkaloid
. Sebanyak 0.1 g sampel dilarutkan dalam 10 mL kloroform dan 4 tetes
NH
4OH kemudian disaring dan filtratnya dimasukkan ke dalam tabung reaksi tertutup.
Ekstrak kloroform dalam tabung reaksi dikocok dengan 6 mL H
2SO
42 M dan lapisan
asamnya dipisahkan ke dalam tabung reaksi yang lain. Lapisan asam ini diteteskan pada
lempeng tetes dan ditambahkan pereaksi Meyer, Wagner, dan Dragendorf yang akan
menimbulkan endapan dengan warna berturut-turut putih, cokelat, dan merah jingga.
Uji saponin dan flavonoid
. Sebanyak 0.1 g sampel dimasukkan ke dalam gelas piala
kemudian ditambahkan 100 mL air panas dan didihkan selama 5 menit. Setelah itu,
disaring dan filtratnya digunakan untuk pengujian. Untuk uji saponin, 10 mL filtrat
dimasukkan ke dalam tabung reaksi tertutup kemudian dikocok selama 10 detik dan
dibiarkan selama 10 menit. Adanya saponin ditunjukkan dengan terbentuknya buih yang
stabil. Sebanyak 10 mL filtrat yang lain ditambahkan 0.5 g serbuk Mg, 1 mL HCl pekat,
dan 1 mL amil alkohol kemudian dikocok dengan kuat. Terbentuknya warna merah,
kuning, dan jingga pada lapisan amil alkohol menunjukkan adanya flavonoid.
Uji triterpenoid dan steroid
. Sebanyak 0.1 g sampel dilarutkan dengan 25 mL etanol
panas (50
oC) kemudian hasilnya disaring ke dalam pinggan porselen dan diuapkan
sampai kering. Residu ditambahkan eter dan ekstrak eter dipindahkan ke dalam lempeng
tetes kemudian ditambahkan 3 tetes anhidrida asetat dan 1 tetes H
2SO
4pekat (uji
Lieberman-Buchard). Warna merah atau ungu menunjukkan adanya triterpenoid dan
warna hijau atau biru menunjukkan adanya steroid.
Uji Tanin
. Sebanyak 0.1 g sampel ditambahkan 100 mL air panas, dididihkan selama
5 menit, dan disaring. Sebagian filtrat yang diperoleh ditambah larutan FeCl
31%.
Terbentuknya warna hitam kehijauan menunjukkan adanya tanin (Harborne 1987).
Lampiran 3 Pembuatan stok ekstrak 5000 ppm dan penetasan larva
A. salina
Pembuatan stok ekstrak 5000 ppm
Ekstrak ditimbang sebanyak 0.25 g lalu dimasukkan ke dalam gelas piala 25 mL yang
berisi air laut kemudian diaduk sampai larut sempurna. Bila tidak larut, ditambahkan
Tween 80 secukupnya. Larutan ekstrak dimasukkan ke dalam labu takar 50 mL lalu ditera
dengan air laut.
Penetasan larva
A. salina
.
Kista
A. salina
yang sudah siap ditetaskan ditimbang sebanyak 50 mg lalu dimasukkan
ke dalam wadah yang berisi air laut yang sudah disaring; setelah itu, diaerasi. Kista
dibiarkan selama 48 jam di bawah pencahayaan lampu agar menetas sempurna. Larva
yang sudah menetas diambil untuk digunakan dalam uji toksisitas.
Lampiran 4 Uji toksisitas terhadap
A. salina
10
Lampiran 5 Penentuan kadar air
Ulangan
a
(g)
b
(g)
c
(g)
Kadar air
(%
b
/
b
)
1
3.0112
23.8117 23.5198
9.69
2 3.0055
24.8111
24.5091 10.00
3 3.0048
23.4497
23.1482 10.03
Rataan
9.93
Keterangan:
a
: bobot sampel (g)
b
: bobot sampel dan cawan petri sebelum dikeringkan (g)
c
: bobot sampel dan cawan petri setelah dikeringkan (g)
Contoh perhitungan:
Lampiran 6 Rendemen ekstrak etanol
Bobot sampel
= 400.00 g
Bobot labu bulat kosong
= 244.25 g
Bobot labu bulat + isi
= 335.95 g
Bobot isi
= 91.70 g
11
Lampiran 7 Hasil uji fitokimia
Ekstrak kasar etanol
Meyer Wagner Dragendorf
(Alkaloid) (Steroid)
(Flavonoid)
Ekstrak etil asetat ekstraksi awal
Meyer
Wagner Dragendorf
( Alkaloid)
(Steroid)
(Flavonoid)
Ekstrak etil asetat re-ekstraksi
Meyer Wagner Dragendorff
(Alkaloid) (Steroid)
12
Lampiran 8 Data uji toksisitas ekstrak etil asetat daun dandang gendis pada
A. salina
10 0
0 10 0
10 0
10 2 20
10 10 2 20 16.67 4.05 1
10 1 10
10 4 40
100 10 5 50 53.33 5.08 2
10 7 70
10 8 80
500 10 8 80 83.33 5.95 2.6989
10 9 90
10 9 90
1000 10 10 100 96.67 6.88 3
10 10 100
Log (mg/L) Konsentrasi (mg/L) Jumlah Larva Artemia Jumlah yang mati %Mortalitas Rerata Probit
Contoh perhitungan:
Konsentrasi 10 ppm ulangan 1
Keterangan:
Nilai probit diperoleh dengan merefleksikan nilai % mortalitas ke dalam tabel probit,
kemudian dibuat kurva linear hubungan antara log konsentrasi dengan nilai probit.
Persamaan garis yang diperoleh:
13
Lampiran 9 Data uji toksisitas ekstrak etil asetat daun dandang gendis pada
A salina
menggunakan parameter waktu ekstraksi 90 menit, jumlah ekstraksi 3 kali,
dan nisbah sampel:pelarut 1:2
10 0
0 10 0
10 0
10 3 30
10 10 4 40 33.33 4.56 1
10 3 30
10 7 70
100 10 6 60 70 5.52 2
10 7 70
10 9 90
500 10 9 90 86.67 6.13 2.6989
10 8 80
10 10 100
1000 10 10 100 100 8 3
10 10 100
Konsentrasi (mg/L) Jumlah Larva Artemia Jumlah yang mati %Mortalitas Rerata Probit Log (mg/L)
Nilai probit diperoleh dengan merefleksikan nilai % mortalitas ke dalam tabel probit,
kemudian dibuat kurva linear hubungan antara log konsentrasi dengan nilai probit.
Persamaan garis yang diperoleh: