VIABILITAS DAN FERTILITAS SPERMATOZOA DALAM
MODIFIKASI PENGENCER BTS DAN ZORLESCO DENGAN
PENYIMPANAN BERBEDA DALAM RANGKAIAN
INSEMINASI BUATAN PADA BABI
NI LUH GDE SUMARDANI
SEKOLAH PASCA SARJANA
INSTITUT PERTANIAN BOGOR
SURAT PERNYATAAN
Dengan ini saya menyatakan bahwa tesis yang berjudul ”Viabilitas dan Fertilitas Spermatozoa dalam Modifikasi Pengencer BTS dan Zorlesco dengan Penyimpanan Berbeda dalam Rangkaian Inseminasi Buatan pada
Babi” adalah karya saya sendiri dan belum pernah diajukan dalam bentuk apa pun
kepada perguruan tinggi mana pun. Sumber informasi yang berasal atau dikutip dari karya yang diterbitkan maupun yang tidak diterbitkan dari penulis lain telah disebutkan dalam teks dan dicantumkan dalam Daftar Pustaka di bagian akhir tesis ini.
Bogor, 1 Agustus 2007
Ni Luh Gde Sumardani
ABSTRAK
NI LUH GDE SUMARDANI. Viabilitas dan Fertilitas Spermatozoa dalam
Modifikasi Pengencer BTS dan Zorlesco dengan Penyimpanan Berbeda dalam Rangkaian Inseminasi Buatan pada Babi. Dibimbing oleh TUTY L. YUSUF dan
POLLUNG H. SIAGIAN
Semen cair babi dapat disimpan dalam temperatur optimum 17 - 18 °C, dan perubahan temperatur dapat menurunkan viabilitas spermatozoa selama penyimpanan. Penelitian ini bertujuan untuk mendapatkan pengencer semen babi yang digunakan dalam rangkaian Inseminasi Buatan (IB) ke wilayah jangkauan tertentu. Dalam hal ini, dilakukan pengamatan viabilitas dan fertilitas spermatozoa dalam modifikasi pengencer Beltsville Thawing Solution (M-BTS) dan Zorlesco (M-Zorlesco) pada penyimpanan berbeda, serta pengaruh sistem penyimpanan dalam ruang terbuka, lemari es dan kotak styrofoam. Semen dikoleksi dengan metode manual (hand method) dua kali dalam seminggu, dari tiga ekor babi pejantan Yorkshire berumur tiga tahun. Karakteristik dan kualitas semen dievaluasi secara makroskopis dan mikrokospis. Secara makrokospis meliputi volume, warna, konsistensi, dan pH, sedangkan secara mikroskopis meliputi persentase motilitas (M%), konsentrasi, viabilitas dan abnormalitas spermatozoa. Semen yang telah ditampung ditambahkan pengencer M-BTS dan M-Zorlesco dengan perbandingan 1 : 3 dengan asumsi menggunakan dosis IB yakni konsentrasi spermatozoa motil mencapai 2 - 3 x 109 sel dalam 80 mL. Semen yang telah diencerkan masing-masing dibagi ke dalam tiga tempat kemudian disimpan dalam ruang terbuka (22 °C), kotak styrofoam (18 °C) dan lemari es (15 °C). Pengamatan terhadap motilitas dan spermatozoa hidup dilakukan setiap enam jam sampai jam ke 42.
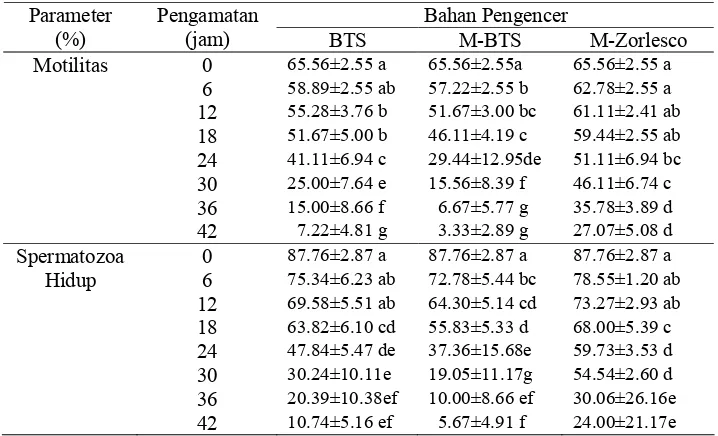
Hasil penelitian menunjukkan, karakteristik semen segar adalah baik dengan motilitas 65.56 ± 3.91% dan spermatozoa hidup 87.70 ± 6.34%. Pengencer yang paling baik selama 42 jam pengamatan adalah M-Zorlesco dengan rataan M% mencapai 54.76 ± 12.76% dalam kotak styrofoam, dan 54.17 ± 12.60% dalam lemari es. Sedangkan dengan pengencer BTS (kontrol) sedikit lebih rendah, namun secara statistik tidak berbeda nyata, yakni M% mencapai 49.37 ± 17.37% dalam kotak styrofoam dan 50.19 ± 17.36% dalam lemari es. Penyimpanan semen dengan pengencer M-Zorlesco dalam kotak styrofoam selama 42 jam menunjukkan hasil yang paling baik Hal ini menunjukkan bahwa kualitas spermatozoa babi dapat dipertahankan dalam kisaran temperatur 15 - 18 °C. Angka konsepsi dengan pengencer M-Zorlesco dan M-BTS cukup tinggi yaitu mencapai 83.33%.
Kesimpulan dari penelitian ini adalah pengencer M-Zorlesco dapat mempertahankan kualitas spermatozoa yang disimpan dalam kotak styrofoam dan lemari es, selama 42 jam dengan M% mencapai 40 - 50%, dan penggunaan kotak styrofoam dapat dilakukan sebagai alternatif tempat penyimpanan semen untuk kegiatan inseminasi dilapangan.
ABSTRACT
NI LUH GDE SUMARDANI. Viability and Fertility of Spermatozoa in
Modified BTS and Zorlesco Extender Stored in Different Places for Swine Artificial Insemination Program. Under the direction of TUTY L. YUSUF and
POLLUNG H. SIAGIAN.
The optimal storage temperature for preserve boar semen is 17 - 18 °C. The temperature fluctuations can decrease sperm viability. The aim of this study was to obtain a boar semen extender for Artificial Insemination (AI) at certain distance area. The observation on viability and fertility of spermatozoa in Modified Beltsville Thawing Solution (M-BTS) and Zorlesco (M-Zorlesco) extender in different storage, and the effect of storage system i.e : room temperature, refrigerator, and styrofoam box were conducted for this purpose. Semen from three years old Yorkshire boar (n = 3) were collected twice a week by hand method. Semen characteristics and their quality were evaluated macro and microscopically. These semen were added with M-BTS and M-Zorlesco extender up to fourfold volume (ratio 1 : 3). This is base on the assumption of AI dose of 2 - 3 x 109cells/80mL. All samples were divided into three tube and stored at room temperature (22 °C), styrofoam box (18 °C) and refrigerator (15 °C), and their motility and viability were evaluated every six hours for 42 hours observation.
The results showed that fresh semen characteristics were good, with sperm motility of 65.56 ± 3.91% and viability of 87.70 ± 6.34 %. The best extender found in this experiment of 42 hours observation was M-Zorlesco extender with average sperm motility of 54.76 ± 12.76% in styrofoam box and 54.17 ± 12.60% in refrigerator. On the other hand, their average of sperm motility in BTS (control) of 49.37 ± 17.37% in styrofoam box and 50.19 ± 17.36 % in refrigerator were slightly lower than that of the former one, but statistically it is not significant. The semen diluted in M-Zorlesco extender stored for 42 hours in styrofoam box that showed the best result. This show that quality of boar’s sepermatozoa can be maintained at 15 - 18 oC. Conception rate with semen diluted in M-Zorlesco and M-BTS extenders were high (83.33%).
In conclusion, M-Zorlesco extender can maintain the quality of spermatozoa stored in styrofoam box and refrigerator for about 42 hours with sperm motility 40 - 50%, and the styrofoam box can be used as an alternatif container for insemination program in the field.
@ Hak cipta milik IPB, tahun 2007
Hak cipta dilindungi
VIABILITAS DAN FERTILITAS SPERMATOZOA DALAM
MODIFIKASI PENGENCER BTS DAN ZORLESCO DENGAN
PENYIMPANAN BERBEDA DALAM RANGKAIAN
INSEMINASI BUATAN PADA BABI
NI LUH GDE SUMARDANI
Tesis
sebagai salah satu syarat untuk memperoleh gelar Magister Sains pada
Program Studi Biologi Reproduksi
SEKOLAH PASCASARJANA
INSTITUT PERTANIAN BOGOR
Judul Tesis : Viabilitas dan Fertilitas Spermatozoa dalam Modifikasi Pengencer BTS dan Zorlesco dengan Penyimpanan Berbeda dalam Rangkaian Inseminasi Buatan pada Babi
Nama : Ni Luh Gde Sumardani
Nrp : B.051050011
Disetujui Komisi Pembimbing
Dr. drh. Tuty Laswardi Yusuf, MS. Dr. Ir. Pollung H. Siagian, MS.
Ketua Anggota
Diketahui
Ketua Program Studi Biologi Dekan Sekolah Pascasarjana
Reproduksi
Dr. drh. Tuty L. Yusuf, MS. Prof. Dr. Ir. Khairil Anwar Notodiputro,MS.
PRAKATA
Puji syukur Penulis panjatkan kehadapan Tuhan Yang Maha Esa karena atas rahmatNya penulisan tesis ini dapat diselesaikan pada waktunya. Tesis ini merupakan salah satu syarat untuk memperoleh gelar Magister Sains pada Program Studi Biologi Reproduksi, Sekolah Pascasarjana, Institut Pertanian Bogor.
Selesainya tugas ini tidak lepas dari bantuan beberapa pihak. Pada kesempatan ini Penulis mengucapkan terimakasih yang sebesar-besarnya kepada Dr. drh. Tuty L. Yusuf, MS dan Dr. Ir. Pollung H. Siagian, MS selaku komisi pembimbing yang telah banyak memberikan arahan, bimbingan serta perhatian dalam penelitian dan penulisan tesis ini; Ketua Program Studi Biologi Reproduksi beserta seluruh staf pengajar Program Studi Biologi Reproduksi, Departemen Klinik, Reproduksi dan Patologi. Terimakasih kepada Departemen Pendidikan Nasional Ditjen Dikti yang telah memberikan Bantuan Dana Pendidikan Program Pascasarjana (BPPS); Rektor Universitas Udayana beserta staf atas pemberian izin kepada Penulis untuk tugas belajar; Kepala Unit Pelaksana Teknis Daerah (UPTD) Dinas Peternakan Provinsi Bali beserta staf atas pemberian izin kepada Penulis untuk melaksanakan penelitian.
Penulis juga mengucapkan terimakasih kepada ibu Dr. Iis Arifiantini yang banyak membantu penelitian Penulis selama dilapangan maupun di laboratorium; Terimakasih kepada teman seperjuangan: Ir.Yanhendri, drh. Erma Najmiyati, Rosa Helmita S.Si, atas semangat dan masukan-masukan positifnya; Ucapan terimakasih dan salut kepada rekan-rekan di Punhawacana Bali: Ir.Gede Rai Maya Temaja MP, Mbak Wayan Sudatri MSi, Dr.Wayan Batan, drh.Agung Artha Putra MSi, Mas Khamdan dan Mbak Helen, teman-teman di Gardu Raya: Bu Made, Pak Nyoman, Puspa, Ketut, Gus Yoga, Wayan, dan Rai, yang banyak membantu, memberi semangat, dan memberi suasana kekeluargaan bagi Penulis, serta berbagai pihak yang tidak dapat Penulis sebutkan satu persatu atas bantuan dan dorongan semangat kepada Penulis selama studi.
Terimakasih tak terhingga selamanya kepada yang tercinta Ayahanda dan Ibunda serta Bapak dan Ibu Mertua yang telah banyak membantu dalam mengasuh anak-anak selama Penulis tugas belajar. Ucapan terimakasih yang dalam Penulis sampaikan kepada Suami dan Anak-anak tersayang (Putri dan Ari) atas semangat, pengertian, cinta dan kasih sayangnya selama ini.
Penulis menyadari bahwa tulisan ini masih banyak kekurangannya, maka masukan dari berbagai pihak sangat Penulis harapkan agar dalam penulisan-penulisan berikutnya menjadi lebih baik. Penulis berharap tulisan ini dapat bermanfaat bagi semua pihak yang berkepentingan dan memberikan sumbangan informasi baru bagi kemajuan ilmu pengetahuan.
Bogor, Agustus 2007
RIWAYAT HIDUP
Penulis dilahirkan di Gianyar tanggal 08 Nopember 1975 dari pasangan bapak I Ketut Suja Arinata dan ibu Ni Nengah Sumartini. Penulis menyelesaikan pendidikan SD sampai SMA di Gianyar pada tahun 1994, kemudian melanjutkan S1 di Jurusan Produksi Ternak, Fakultas Peternakan, Universitas Udayana, Denpasar, dan lulus tahun 1998. Pada tahun 2002 diterima sebagai staf pengajar di Laboratorium Reproduksi Ternak Jurusan Produksi Ternak, Fakultas Peternakan Universitas Udayana.
DAFTAR ISI
Halaman
DAFTAR TABEL ... xii
DAFTAR GAMBAR ... xiii
DAFTAR LAMPIRAN ... xiv
PENDAHULUAN Latar Belakang ... 1
Kerangka Pemikiran ... 3
Hipotesis ... 4
Tujuan Penelitian ... 5
Manfaat Penelitian ……….. 5
TINJAUAN PUSTAKA Ternak Babi ... 6
Karakteristik Semen Babi ... 7
Evaluasi Semen ... 11
Pengenceran Semen ... 13
Penyimpanan Semen ... 17
Inseminasi Buatan pada Babi ... ... 20
Teknik Inseminasi Buatan ... 22
Keberhasilan Inseminasi Buatan ... 24
MATERI DAN METODE Tempat dan Waktu Penelitian ... 26
Materi Penelitian ... 26
Sumber Semen ... 26
Kandang dan Pakan ... 27
Induk ... 27
Alat dan Bahan ... 27
Alat ... 27
Bahan ... 27
Metode Penelitian ... 28
Karakteristik Semen Segar ... 28
Evaluasi Semen ... 29
Teknik Pewarnaan ... 30
Pengenceran dan Penyimpanan Semen ... 31
Inseminasi Buatan ... 31
Dosis Inseminasi ... 31
VIABILITAS DAN FERTILITAS SPERMATOZOA DALAM
MODIFIKASI PENGENCER BTS DAN ZORLESCO DENGAN
PENYIMPANAN BERBEDA DALAM RANGKAIAN
INSEMINASI BUATAN PADA BABI
NI LUH GDE SUMARDANI
SEKOLAH PASCA SARJANA
INSTITUT PERTANIAN BOGOR
SURAT PERNYATAAN
Dengan ini saya menyatakan bahwa tesis yang berjudul ”Viabilitas dan Fertilitas Spermatozoa dalam Modifikasi Pengencer BTS dan Zorlesco dengan Penyimpanan Berbeda dalam Rangkaian Inseminasi Buatan pada
Babi” adalah karya saya sendiri dan belum pernah diajukan dalam bentuk apa pun
kepada perguruan tinggi mana pun. Sumber informasi yang berasal atau dikutip dari karya yang diterbitkan maupun yang tidak diterbitkan dari penulis lain telah disebutkan dalam teks dan dicantumkan dalam Daftar Pustaka di bagian akhir tesis ini.
Bogor, 1 Agustus 2007
Ni Luh Gde Sumardani
ABSTRAK
NI LUH GDE SUMARDANI. Viabilitas dan Fertilitas Spermatozoa dalam
Modifikasi Pengencer BTS dan Zorlesco dengan Penyimpanan Berbeda dalam Rangkaian Inseminasi Buatan pada Babi. Dibimbing oleh TUTY L. YUSUF dan
POLLUNG H. SIAGIAN
Semen cair babi dapat disimpan dalam temperatur optimum 17 - 18 °C, dan perubahan temperatur dapat menurunkan viabilitas spermatozoa selama penyimpanan. Penelitian ini bertujuan untuk mendapatkan pengencer semen babi yang digunakan dalam rangkaian Inseminasi Buatan (IB) ke wilayah jangkauan tertentu. Dalam hal ini, dilakukan pengamatan viabilitas dan fertilitas spermatozoa dalam modifikasi pengencer Beltsville Thawing Solution (M-BTS) dan Zorlesco (M-Zorlesco) pada penyimpanan berbeda, serta pengaruh sistem penyimpanan dalam ruang terbuka, lemari es dan kotak styrofoam. Semen dikoleksi dengan metode manual (hand method) dua kali dalam seminggu, dari tiga ekor babi pejantan Yorkshire berumur tiga tahun. Karakteristik dan kualitas semen dievaluasi secara makroskopis dan mikrokospis. Secara makrokospis meliputi volume, warna, konsistensi, dan pH, sedangkan secara mikroskopis meliputi persentase motilitas (M%), konsentrasi, viabilitas dan abnormalitas spermatozoa. Semen yang telah ditampung ditambahkan pengencer M-BTS dan M-Zorlesco dengan perbandingan 1 : 3 dengan asumsi menggunakan dosis IB yakni konsentrasi spermatozoa motil mencapai 2 - 3 x 109 sel dalam 80 mL. Semen yang telah diencerkan masing-masing dibagi ke dalam tiga tempat kemudian disimpan dalam ruang terbuka (22 °C), kotak styrofoam (18 °C) dan lemari es (15 °C). Pengamatan terhadap motilitas dan spermatozoa hidup dilakukan setiap enam jam sampai jam ke 42.
Hasil penelitian menunjukkan, karakteristik semen segar adalah baik dengan motilitas 65.56 ± 3.91% dan spermatozoa hidup 87.70 ± 6.34%. Pengencer yang paling baik selama 42 jam pengamatan adalah M-Zorlesco dengan rataan M% mencapai 54.76 ± 12.76% dalam kotak styrofoam, dan 54.17 ± 12.60% dalam lemari es. Sedangkan dengan pengencer BTS (kontrol) sedikit lebih rendah, namun secara statistik tidak berbeda nyata, yakni M% mencapai 49.37 ± 17.37% dalam kotak styrofoam dan 50.19 ± 17.36% dalam lemari es. Penyimpanan semen dengan pengencer M-Zorlesco dalam kotak styrofoam selama 42 jam menunjukkan hasil yang paling baik Hal ini menunjukkan bahwa kualitas spermatozoa babi dapat dipertahankan dalam kisaran temperatur 15 - 18 °C. Angka konsepsi dengan pengencer M-Zorlesco dan M-BTS cukup tinggi yaitu mencapai 83.33%.
Kesimpulan dari penelitian ini adalah pengencer M-Zorlesco dapat mempertahankan kualitas spermatozoa yang disimpan dalam kotak styrofoam dan lemari es, selama 42 jam dengan M% mencapai 40 - 50%, dan penggunaan kotak styrofoam dapat dilakukan sebagai alternatif tempat penyimpanan semen untuk kegiatan inseminasi dilapangan.
ABSTRACT
NI LUH GDE SUMARDANI. Viability and Fertility of Spermatozoa in
Modified BTS and Zorlesco Extender Stored in Different Places for Swine Artificial Insemination Program. Under the direction of TUTY L. YUSUF and
POLLUNG H. SIAGIAN.
The optimal storage temperature for preserve boar semen is 17 - 18 °C. The temperature fluctuations can decrease sperm viability. The aim of this study was to obtain a boar semen extender for Artificial Insemination (AI) at certain distance area. The observation on viability and fertility of spermatozoa in Modified Beltsville Thawing Solution (M-BTS) and Zorlesco (M-Zorlesco) extender in different storage, and the effect of storage system i.e : room temperature, refrigerator, and styrofoam box were conducted for this purpose. Semen from three years old Yorkshire boar (n = 3) were collected twice a week by hand method. Semen characteristics and their quality were evaluated macro and microscopically. These semen were added with M-BTS and M-Zorlesco extender up to fourfold volume (ratio 1 : 3). This is base on the assumption of AI dose of 2 - 3 x 109cells/80mL. All samples were divided into three tube and stored at room temperature (22 °C), styrofoam box (18 °C) and refrigerator (15 °C), and their motility and viability were evaluated every six hours for 42 hours observation.
The results showed that fresh semen characteristics were good, with sperm motility of 65.56 ± 3.91% and viability of 87.70 ± 6.34 %. The best extender found in this experiment of 42 hours observation was M-Zorlesco extender with average sperm motility of 54.76 ± 12.76% in styrofoam box and 54.17 ± 12.60% in refrigerator. On the other hand, their average of sperm motility in BTS (control) of 49.37 ± 17.37% in styrofoam box and 50.19 ± 17.36 % in refrigerator were slightly lower than that of the former one, but statistically it is not significant. The semen diluted in M-Zorlesco extender stored for 42 hours in styrofoam box that showed the best result. This show that quality of boar’s sepermatozoa can be maintained at 15 - 18 oC. Conception rate with semen diluted in M-Zorlesco and M-BTS extenders were high (83.33%).
In conclusion, M-Zorlesco extender can maintain the quality of spermatozoa stored in styrofoam box and refrigerator for about 42 hours with sperm motility 40 - 50%, and the styrofoam box can be used as an alternatif container for insemination program in the field.
@ Hak cipta milik IPB, tahun 2007
Hak cipta dilindungi
VIABILITAS DAN FERTILITAS SPERMATOZOA DALAM
MODIFIKASI PENGENCER BTS DAN ZORLESCO DENGAN
PENYIMPANAN BERBEDA DALAM RANGKAIAN
INSEMINASI BUATAN PADA BABI
NI LUH GDE SUMARDANI
Tesis
sebagai salah satu syarat untuk memperoleh gelar Magister Sains pada
Program Studi Biologi Reproduksi
SEKOLAH PASCASARJANA
INSTITUT PERTANIAN BOGOR
Judul Tesis : Viabilitas dan Fertilitas Spermatozoa dalam Modifikasi Pengencer BTS dan Zorlesco dengan Penyimpanan Berbeda dalam Rangkaian Inseminasi Buatan pada Babi
Nama : Ni Luh Gde Sumardani
Nrp : B.051050011
Disetujui Komisi Pembimbing
Dr. drh. Tuty Laswardi Yusuf, MS. Dr. Ir. Pollung H. Siagian, MS.
Ketua Anggota
Diketahui
Ketua Program Studi Biologi Dekan Sekolah Pascasarjana
Reproduksi
Dr. drh. Tuty L. Yusuf, MS. Prof. Dr. Ir. Khairil Anwar Notodiputro,MS.
PRAKATA
Puji syukur Penulis panjatkan kehadapan Tuhan Yang Maha Esa karena atas rahmatNya penulisan tesis ini dapat diselesaikan pada waktunya. Tesis ini merupakan salah satu syarat untuk memperoleh gelar Magister Sains pada Program Studi Biologi Reproduksi, Sekolah Pascasarjana, Institut Pertanian Bogor.
Selesainya tugas ini tidak lepas dari bantuan beberapa pihak. Pada kesempatan ini Penulis mengucapkan terimakasih yang sebesar-besarnya kepada Dr. drh. Tuty L. Yusuf, MS dan Dr. Ir. Pollung H. Siagian, MS selaku komisi pembimbing yang telah banyak memberikan arahan, bimbingan serta perhatian dalam penelitian dan penulisan tesis ini; Ketua Program Studi Biologi Reproduksi beserta seluruh staf pengajar Program Studi Biologi Reproduksi, Departemen Klinik, Reproduksi dan Patologi. Terimakasih kepada Departemen Pendidikan Nasional Ditjen Dikti yang telah memberikan Bantuan Dana Pendidikan Program Pascasarjana (BPPS); Rektor Universitas Udayana beserta staf atas pemberian izin kepada Penulis untuk tugas belajar; Kepala Unit Pelaksana Teknis Daerah (UPTD) Dinas Peternakan Provinsi Bali beserta staf atas pemberian izin kepada Penulis untuk melaksanakan penelitian.
Penulis juga mengucapkan terimakasih kepada ibu Dr. Iis Arifiantini yang banyak membantu penelitian Penulis selama dilapangan maupun di laboratorium; Terimakasih kepada teman seperjuangan: Ir.Yanhendri, drh. Erma Najmiyati, Rosa Helmita S.Si, atas semangat dan masukan-masukan positifnya; Ucapan terimakasih dan salut kepada rekan-rekan di Punhawacana Bali: Ir.Gede Rai Maya Temaja MP, Mbak Wayan Sudatri MSi, Dr.Wayan Batan, drh.Agung Artha Putra MSi, Mas Khamdan dan Mbak Helen, teman-teman di Gardu Raya: Bu Made, Pak Nyoman, Puspa, Ketut, Gus Yoga, Wayan, dan Rai, yang banyak membantu, memberi semangat, dan memberi suasana kekeluargaan bagi Penulis, serta berbagai pihak yang tidak dapat Penulis sebutkan satu persatu atas bantuan dan dorongan semangat kepada Penulis selama studi.
Terimakasih tak terhingga selamanya kepada yang tercinta Ayahanda dan Ibunda serta Bapak dan Ibu Mertua yang telah banyak membantu dalam mengasuh anak-anak selama Penulis tugas belajar. Ucapan terimakasih yang dalam Penulis sampaikan kepada Suami dan Anak-anak tersayang (Putri dan Ari) atas semangat, pengertian, cinta dan kasih sayangnya selama ini.
Penulis menyadari bahwa tulisan ini masih banyak kekurangannya, maka masukan dari berbagai pihak sangat Penulis harapkan agar dalam penulisan-penulisan berikutnya menjadi lebih baik. Penulis berharap tulisan ini dapat bermanfaat bagi semua pihak yang berkepentingan dan memberikan sumbangan informasi baru bagi kemajuan ilmu pengetahuan.
Bogor, Agustus 2007
RIWAYAT HIDUP
Penulis dilahirkan di Gianyar tanggal 08 Nopember 1975 dari pasangan bapak I Ketut Suja Arinata dan ibu Ni Nengah Sumartini. Penulis menyelesaikan pendidikan SD sampai SMA di Gianyar pada tahun 1994, kemudian melanjutkan S1 di Jurusan Produksi Ternak, Fakultas Peternakan, Universitas Udayana, Denpasar, dan lulus tahun 1998. Pada tahun 2002 diterima sebagai staf pengajar di Laboratorium Reproduksi Ternak Jurusan Produksi Ternak, Fakultas Peternakan Universitas Udayana.
DAFTAR ISI
Halaman
DAFTAR TABEL ... xii
DAFTAR GAMBAR ... xiii
DAFTAR LAMPIRAN ... xiv
PENDAHULUAN Latar Belakang ... 1
Kerangka Pemikiran ... 3
Hipotesis ... 4
Tujuan Penelitian ... 5
Manfaat Penelitian ……….. 5
TINJAUAN PUSTAKA Ternak Babi ... 6
Karakteristik Semen Babi ... 7
Evaluasi Semen ... 11
Pengenceran Semen ... 13
Penyimpanan Semen ... 17
Inseminasi Buatan pada Babi ... ... 20
Teknik Inseminasi Buatan ... 22
Keberhasilan Inseminasi Buatan ... 24
MATERI DAN METODE Tempat dan Waktu Penelitian ... 26
Materi Penelitian ... 26
Sumber Semen ... 26
Kandang dan Pakan ... 27
Induk ... 27
Alat dan Bahan ... 27
Alat ... 27
Bahan ... 27
Metode Penelitian ... 28
Karakteristik Semen Segar ... 28
Evaluasi Semen ... 29
Teknik Pewarnaan ... 30
Pengenceran dan Penyimpanan Semen ... 31
Inseminasi Buatan ... 31
Dosis Inseminasi ... 31
Rancangan Percobaan ... 33
Parameter yang Diamati ……….... 33
Model Matematika ………..…... 35
Analisis Data ... 35
HASIL DAN PEMBAHASAN Karakteristik Semen Segar ... 36
Volume Semen ... 36
Warna, Konsistensi dan Gerakan Massa Semen ... 37
Derajat Keasaman (pH) Semen ... 38
Motilitas dan Spermatozoa Hidup ... 39
Konsentrasi Spermatozoa ... 39
Morfologi (Normalitas) dan Morfometri Spermatozoa ... 40
Daya Tahan Semen Segar dalam Tempat Penyimpanan Berbeda ... 41
Daya Tahan Semen Cair dalam Tempat Penyimpanan Berbeda ... 45
Ruang Terbuka (22 °C) ... 45
Kotak Styrofoam (18 °C) ... 47
Lemari Es (15 °C) ... 50
Perbandingan Persentase Motilitas dan Spermatozoa Hidup dalam Pengencer dan Tempat Penyimpanan Berbeda ... 53
Inseminasi Buatan pada Babi ...………….………... 54
PEMBAHASAN UMUM ... 57
SIMPULAN DAN SARAN Simpulan ……… 59
Saran ……….. 59
DAFTAR PUSTAKA ………... 60
DAFTAR TABEL
Halaman
1 Karakteristik semen babi …………... 11 2 Komposisi plasma semen babi ... 12
3 Komposisi kimia BTS, Kiev, Zorlesco dan Androhep ... 15
4 Pengaruh kotak styrofoam terhadap viabilitas spermatozoa selama 24 jam penyimpanan ………....…...…… 18
5 Metode evaluasi perubahan kualitas spermatozoa babi pada
temperatur yang berbeda …... 19
6 Komposisi bahan pengencer semen babi ... 28
7 Nilai karakteristik semen segar babi ... 36
8 Persentase motilitas dan spermatozoa hidup semen segar dalam
tempat penyimpanan berbeda …...…………... 42
9 Persentase motilitas dan spermatozoa hidup semen cair dalam
penyimpanan ruang terbuka ... 45
10 Persentase motilitas dan spermatozoa hidup semen cair dalam
penyimpanan kotak styrofoam ... 48
11 Persentase motilitas dan spermatozoa hidup semen cair dalam
penyimpanan lemari es ... 51
12 Rataan persentase motilitas dan spermatozoa hidup semen cair dalam pengencer dan tempat penyimpanan berbeda selama 42 jam penyimpanan ... 53
DAFTAR GAMBAR
Halaman
1 Saluran reproduksi babi jantan ... 10
2 Spermatozoa normal pada babi ... 12
3 Saluran reproduksi babi betina ... 21
4 Pedoman waktu inseminasi pada babi ... 21
5 Aktivitas hormonal dan ovarium pada babi betina ... 22
6 Posisi kateter pada pelaksanaan inseminasi buatan ... 23
7 Metode penampungan semen babi ... 26
8 Alur penelitian ... 34
9 Spermatozoa babi hasil pewarnaan Williams ... 41
10 Penurunan persentase motilitas (M) dan spermatozoa hidup (SH) semen segarpada penyimpanan ruang terbuka (RT), kotak styrofoam (KS) dan lemari es (LE) ……… 43
11 Penurunan persentase motilitas (M) dan spermatozoa hidup (SH) semen cair pada penyimpanan ruang terbuka (RT), dalam pengencer BTS, M-BTS, dan M-Zorlesco ... 47
12 Penurunan persentase motilitas (M) dan spermatozoa hidup (SH) semen cair pada penyimpanan kotak styrofoam (KS) dalam pengencer BTS, M-BTS, dan M-Zorlesco ... 50
13 Penurunan persentase motilitas (M) dan spermatozoa hidup (SH) semen cair pada penyimpanan lemari es, dalam pengencer
BTS, M-BTS, dan M-Zorlesco ... 52
14 Rataan persentase motilitas (M) spermatozoa semen cair pada pengencer dan tempat penyimpanan berbeda selama 42 jam
DAFTAR LAMPIRAN
Halaman
1 Persentase motilitas spermatozoa dari pejantan 1 ... 65
2 Persentase motilitas spermatozoa dari pejantan 2 ... 65
3 Persentase motilitas spermatozoa dari pejantan 3 ... 65
4 Persentase spermatozoa hidup dari pejantan 1 ... 66
5 Persentase spermatozoa hidup dari pejantan 2 ... 66
6 Persentase spermatozoa hidup dari pejantan 3 ... 66
7 Pengenceran semen ... 67
PENDAHULUAN
Latar Belakang
Peternakan babi yang ada di Indonesia khususnya di daerah Bali masih merupakan peternakan rakyat dalam skala kecil atau skala rumah tangga, dimana mutu genetiknya masih kurang mendapat perhatian. Disamping itu populasi babi yang ada masih sangat terbatas, dengan demikian perlu adanya peningkatan mutu genetik baik untuk keperluan konsumsi maupun untuk keperluan ekspor.
Salah satu usaha untuk mencapai tujuan peningkatan genetik dan populasi ternak babi tersebut adalah dengan pemanfaatan teknologi inseminasi buatan (IB) melalui penyediaan sumber spermatozoa yang berasal dari pejantan berkualitas unggul. Dengan teknik IB diharapkan pengawinan yang dilakukan akan lebih efektif dan efisien dibandingkan dengan pengawinan secara alami. Disamping itu pula diharapkan dengan teknik IB dapat meningkatkan nilai mutu dari ternak tersebut baik dalam hal peningkatan bobot badan maupun produksi daging. Dalam dua tahun terakhir ini, penggunaan teknik IB pada babi khususnya di daerah Bali telah berkembang dan mulai dilakukan secara langsung melalui pengenceran, namun belum terdapat rumusan secara ilmiah. Teknik IB sudah melibatkan pemeliharaan babi jenis unggul, seperti persilangan Yorkshire dengan Landrace. Pada sentra Balai Inseminasi Buatan Daerah (BIBD) Bali, telah memiliki beberapa bangsa pejantan unggul dengan mutu genetik tinggi, yang dikembangkan dengan teknik IB kepada betina lokal.
Inseminasi buatan merupakan suatu rangkaian kegiatan yang komplek dan teratur, yang meliputi penampungan semen dan pengolahan semen cair maupun semen beku. Pada babi, penampungan semen dilakukan dengan teknik secara manual (glove hand method) dan IB umumnya menggunakan semen cair, dimasukkan secara intrauterine dengan menggunakan suatu alat khusus yaitu kateter menyerupai bentuk penis babi pejantan berbentuk spiral pada bagian ujungnya.
kisaran temperatur 15 - 20 °C (Paulenz et al. 2000) serta daya simpan yang relatif singkat yaitu kisaran 3 - 7 hari tergantung bahan pengencer yang digunakan (Johnson et al. 1982; Gadea 2003; Robert 2006).
Produksi semen cair babi sering dihadapkan pada kendala penyimpanan semen, yaitu terjadinya perubahan temperatur pada saat penyimpanan khususnya saat pendistribusian semen cair kepada konsumen. Hal ini mengingat bahwa semen yang sudah ditampung, umumnya harus dipakai dalam waktu tidak lebih dari dua jam. Apabila dilakukan penundaan dalam beberapa jam saja akan menyebabkan penurunan fertilitas spermatozoa.
Watson (1996) menyatakan bahwa cekaman perubahan temperatur (cold shock) berpengaruh terhadap komposisi membran plasma spermatozoa. Pada temperatur rendah terjadi perubahan pada struktur phospholipid membran plasma dari fase cair menjadi fase gel. Hal ini menunjukkan reaksi membran sel pada temperatur rendah sangat kuat, yang dapat menyebabkan kerusakan membran sel secara permanen. De Leeuw et al. (1990) menambahkan komposisi asam lemak membran plasma spermatozoa sapi dan babi pada fase perubahan phospholipid sangat berbeda. Berdasarkan perbedaan komposisi phospholipid tersebut, persentase phosphatidyiethanolamine dan sphingomyelin pada sapi sangat rendah yaitu 9.7% dan 11.5%, sedangkan pada babi persentase phosphatidylethanolamine dan sphingomyelin sangat tinggi, masing-masing mencapai 24% dan 14% (White 1993). Hal ini menyebabkan membran plasma spermatozoa babi sangat sulit stabil pada temperatur rendah.
Bahan pengencer semen mengandung sumber nutrisi, buffer, bahan anti cold shock, antibiotik, dan krioprotektan yang dapat melindungi spermatozoa selama proses pengolahan dan penyimpanan. Karbohidrat terutama fruktosa paling banyak digunakan sebagai sumber nutrisi karena lebih mudah dimetabolisis oleh spermatozoa. Karbohidrat juga berperan sebagai pelindung spermatozoa terhadap cekaman perubahan temperatur (cold shock). Tris (hydroxymethyl) aminomethan digunakan dalam bahan pengencer karena memiliki sifat peyangga (buffer) yang baik dengan toksisitas yang rendah dalam konsentrasi yang tinggi (Steinbach dan Foote 1967; Toelihere 1993). Glisin yang terkandung dalam pengencer Zorlesco adalah asam amino yang merupakan sumber nutrisi dan protein bagi kelangsungan metabolisme spermatozoa selama penyimpanan dan sebagai bahan yang mampu melindungi spermatozoa dari pengaruh cold shock. Zorlesco juga mengandung Bovine Serum Albumin (BSA) yang dapat berperan dalam menjaga kelangsungan pertumbuhan dan perkembangan dari sel (Bassol et al. 2005). Menurut Waberski et al. (1989) BSA dapat mempertahankan motilitas spermatozoa sampai enam hari penyimpanan.
Berdasarkan latar belakang dan pemikiran tersebut maka dilakukan penelitian yang berkaitan dengan karakteristik semen babi, pengaruh modifikasi bahan pengencer BTS dan Zorlesco terhadap viabilitas dan fertilitas spermatozoa babi, serta pemilihan tempat penyimpanan semen cair kaitannya dengan mempertahankan kualitas semen cair babi selama pendistribusian untuk dapat digunakan dalam IB.
Kerangka Pemikiran
Penggunaan bahan pengencer BTS dan Zorlesco adalah sebagai sumber energi, buffer, melindungi spermatozoa terhadap cold shock, dan mencegah perubahan pH serta tekanan osmotik dalam semen cair, sehingga dapat mempertahankan viabilitas dan fertilitas spermatozoa selama pengolahan dan penyimpanan.
bersifat buffer, berfungsi sebagai pengatur tekanan osmotik dan juga menetralisir asam laktat yang dihasilkan dari sisa metabolisme spermatozoa. Bahan pengencer Zorlesco mengandung glisin salah satu asam amino yang merupakan sumber nutrisi dan protein bagi kelangsungan metabolisme spermatozoa selama penyimpanan dan sebagai bahan yang mampu melindungi membran spermatozoa dari pengaruh cold shock. Zorlesco juga mengandung BSA yang dapat berperan dalam menjaga kelangsungan pertumbuhan dan perkembangan dari sel. Modifikasi pengencer BTS dan Zorlesco dengan penambahan fruktosa sebagai sumber nutrisi diharapkan mampu mempertahankan viabilitas dan fertilitas spermatozoa selama penyimpanan.
Perlindungan terhadap spermatozoa selain tergantung dari bahan pengencer yang digunakan, juga tergantung dari temperatur penyimpanan yang berkisar 15 - 20 °C. Perubahan temperatur dapat berpengaruh terhadap komposisi membran plasma spermatozoa, terutama pada struktur phospholipid membran plasma dari fase cair menjadi fase gel yang dapat menyebabkan kerusakan membran plasma sel secara permanen. Hal tersebut dapat menurunkan kualitas spermatozoa selama penyimpanan termasuk motilitas, viabilitas dan fertilitas spermatozoa.
Pengaturan temperatur penyimpanan 15 - 20 °C dilakukan dengan menggunakan lemari es dan kotak styrofoam. Penyimpanan semen cair babi dalam lemari es yang diformat low temperature pada rak paling bawah diperkirakan mempunyai temperatur 15 - 20 °C. Demikian pula dalam kotak styrofoam yang diatur dengan menggunakan es yang dilapisi handuk diperkirakan mempunyai temperatur 15 - 20 °C.
Hipotesis
a. Pengenceran semen babi dengan modifikasi pengencer BTS dan Zorlesco mampu mempertahankan viabilitas dan fertilitas spermatozoa babi dalam waktu tertentu.
c. Semen cair dengan modifikasi pengencer BTS dan Zorlesco dapat digunakan dalam kegiatan IB.
Tujuan Penelitian
Tujuan dari penelitian ini adalah untuk mendapatkan pengencer yang baik dalam usaha mempertahankan kualitas spermatozoa terutama dalam kegiatan transportasi semen ke luar daerah dan dalam jangka waktu tertentu. Secara khusus penelitian ini bertujuan untuk :
a. Menguji modifikasi pengencer BTS dan Zorlesco dalam mempertahankan viabilitas dan fertilitas spermatozoa.
b. Mendapatkan suatu sistem penyimpanan semen cair dalam mempertahankan viabilitas dan fertilitas spermatozoa.
c. Menguji modifikasi pengencer BTS dan Zorlesco dalam kegiatan IB.
Manfaat Penelitian
TINJAUAN PUSTAKA
Ternak Babi
Pengembangan ternak babi di Indonesia, khususnya di beberapa daerah, diantaranya Jawa Timur, Bali, Nusa Tenggara, serta Sumatera Utara sudah menerapkan pemeliharaan babi jenis unggul yang berasal dari luar, seperti bangsa Duroc, Landrace, Yorkshire, Hampshire, maupun persilangannya, yang digunakan sebagai induk maupun pejantan. Pengembangan ternak babi masih dilakukan melalui pengawinan alami, sedangkan pengawinan melalui inseminasi masih dilakukan menggunakan semen segar dimana mutu dan kualitas semen yang digunakan belum dikaji secara ilmiah.
Babi merupakan salah satu ternak penghasil daging yang cukup produktif dan memiliki berbagai keuntungan dibandingkan dengan ternak lain. Keuntungan beternak babi adalah pertumbuhannya cepat, beranak banyak (6 - 12 ekor), dapat melahirkan anak dua kali dalam setahun, bahkan lima kali dalam dua tahun. Produksi utama dalam beternak babi adalah karkas atau dagingnya. Hasil ikutan yang juga bernilai ekonomis adalah kulit dan organ dalam (usus) yang dapat digunakan sebagai sosis, serta kotoran babi juga dapat digunakan sebagai kompos (Aritonang 1993).
Bangsa babi di dunia sangat banyak antara lain : Berkshire, Poland China, Spotted Poland China, Hampshire, Duroc, Tamworth, Chester White, Yorkshire, Landrace dan Hereford. Jenis babi yang banyak dipelihara di Indonesia adalah Landrace dan Large White atau Yorkshire yang mempunyai kualitas daging yang tinggi (Aritonang 1993). Babi yang dikembangkan di Indonesia antara lain dari bangsa Landrace, Duroc, Yorkshire, Hampshire, dan Berckshire.
berbobot sekitar 250 - 340 kg (Girisonta 1981; Sihombing 2006). Babi Landrace lebih panjang daripada bangsa babi lainnya karena memiliki tulang punggung yang panjang (Blakely dan Bade 1985). Babi Duroc merupakan persilangan dari dua bangsa babi yaitu Jersey Reds dengan Duroc dari New York. Warnanya merah terang hingga gelap dan merah cherry, kukunya hitam, tubuhnya padat dan prolifik, serta mudah stres terhadap perubahan lingkungan. Babi Duroc betina memiliki litter size yang tinggi. Babi jantan dewasa umumnya berbobot sekitar 295 - 455 kg, induk umumnya berbobot sekitar 275 - 320 kg (Blakely dan Bade 1985; Sihombing 2006). Babi Yorkshire berasal dari Inggris dan di beberapa negara ada yang menamakannya Large White. Ada dua tipe yang berbeda pada bangsa Yorkshire yaitu Large Yorkshire dan Middle Yorkshire. Warna babi Yorkshire putih, tetapi adakalanya terdapat totol pigmen hitam di kulit, serta memiliki kualitas daging yang tinggi. Babi jantan dewasa berbobot sekitar 320 - 455 kg dan induk berbobot sekitar 225 - 365 kg (Blakely dan Bade 1985; Sihombing 2006).
Secara umum babi jantan mencapai dewasa kelamin pada umur 5 - 6 bulan ditandai adanya spermatozoa di dalam ejakulat, dan dibiarkan mencapai umur 8 - 9 bulan sebelum digunakan untuk mengawini induk. Sedangkan babi betina mencapai dewasa kelamin pada umur 5 - 8 bulan ditandai dengan munculnya berahi dan terjadinya ovulasi, dan rata-rata pengawinan pertama dianjurkan pada umur 8 - 10 bulan (Toelihere 1993; Anderson 2000).
Karakteristik Semen Babi
mengikat radikal oksigen untuk mencegah terbentuknya peroksidasi lipid yang dapat menghambat glikolisis maupun motilitas, (3) kalium, natrium, dan klorida yang berperan dalam menjaga integritas fungsional membran plasma spermatozoa serta mempertahankan tekanan osmotik sel spermatozoa, (4) bikarbonat berperan sebagai agen penyanggah untuk mencegah perubahan pH semen selama proses penyimpanan, dan (5) fruktosa yang dimanfaatkan spermatozoa sebagai sumber energi baik dalam kondisi anaerob atau pada saat penyimpanan, dan kondisi aerob pada saluran reproduksi betina (Toelihere 1993).
Ciri khas semen babi adalah volumenya yang tinggi mencapai 150 – 200 ml dan konsentrasi spermatozoanya rendah yaitu 200 - 300 x 106 sel/ml dibandingkan dengan semen ternak lainnya (Garner dan Hafez 2000). Semen babi (fresh semen) dapat dievaluasi dengan baik pada kisaran temperatur 35 - 37 °C selama 1 - 3 jam. Semen babi yang telah diencerkan dapat disimpan pada temperatur rendah dengan kisaran 15 - 20 °C (Paulenz et al. 2000) dalam waktu rata-rata 3 - 7 hari tergantung dari pengencer yang digunakan (Johnson et al. 1982; Gadea 2003; Robert 2006).
Pada semen babi terdapat dua istilah penting yaitu whole semen dan fractionated semen. Whole semen merupakan semen secara keseluruhan yang bahan gelatinnya telah dihilangkan melalui suatu penyaringan menggunakan saringan yang halus. Fractionated semen merupakan semen yang seluruhnya berasal dari fraksi yang kedua atau sperm-rich fraction (First 1970). Untuk keperluan penyimpanan semen maka bahan gelatin perlu dihilangkan karena bahan gelatin dapat menyerap sebagian besar cairan semen sehingga hampir seluruh semen akan menjadi bersifat gelatin. Fractioned semen memiliki sifat yang berbeda dengan whole semen. Pada fractioned semen, lama hidup spermatozoa menjadi lebih lama bila disimpan pada temperatur rendah. Pada temperatur 37 °C maupun pada temperatur 15 - 20 °C lama hidup spermatozoa baik pada fractioned semen maupun whole semen adalah sama, namun spermatozoa pada fractioned semen yang didinginkan pada temperatur 5 °C akan tetap mempertahankan motilitasnya untuk periode waktu yang relatif sangat lama. Fractioned semen juga lebih tahan terhadap cekaman temperatur dibandingkan dengan whole semen, dan seperti halnya pada whole semen, fractioned semen harus dihangatkan dan dikocok dalam suasana aerob selama dua jam agar motilitas spermatozoa terlihat jelas (First 1970).
Proses ejakulasi pada babi pejantan berlangsung relatif lama yaitu dapat berkisar 3 - 20 menit untuk satu proses ejakulasi yang sempurna. Pola ejakulasi semen babi pejantan adalah sangat khas. Awal dari gerakan - gerakan memasukkan penis akan berakhir beberapa menit dan dibarengi oleh sekresi cairan yang terlihat hampir bening, agak lengket dan mengandung sejumlah bahan gelatin yang menyerupai jelly. Segera setelah gerakan-gerakan memasukkan penis selesai, pejantan menjadi tenang dan volume semen meningkat drastis. Cairan yang diejakulasikan pada saat ini bersifat kental dan berwarna putih dan mengandung sedikit gelatin dalam bentuk gumpalan-gumpalan seperti kanji. Terakhir, ketika pejantan masih dalam keadaan tenang, cairan yang diejakulasikan hampir bening kembali dan dibarengi oleh sejumlah besar gelatin.
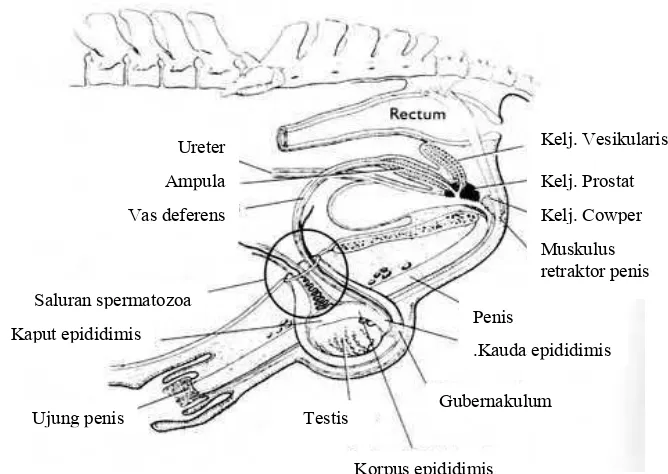
berulang sebelum terjadinya ejakulasi yang sempurna, sehingga semen yang diejakulasikan terdiri atas beberapa fraksi yaitu pra-spermatozoa, kaya-spermatozoa dan pasca-kaya-spermatozoa. Fraksi pra-kaya-spermatozoa tidak mengandung spermatozoa, hanya berupa gelatin dari kelenjar bulbouretralis (kelenjar Cowper) yang mencapai 20% dari total volume semen. Fraksi kaya-spermatozoa mengandung 20 - 30% spermatozoa dengan konsentrasi 600 - 1000 x 106 spermatozoa/ml, dan fraksi pasca-spermatozoa sedikit mengandung spermatozoa, lebih banyak mengandung cairan dari kelenjar asesories lainnya, yaitu kelenjar prostat dan kelenjar vesicularis. Saluran reproduksi babi jantan beserta kelenjar asesories diperlihatkan dalam Gambar 1. Adapun faktor-faktor yang mempengaruhi total volume dan konsentrasi semen adalah umur, makanan, lingkungan, musim, prosedur penampungan semen, frekuensi penampungan, perbedaan bangsa, dan kesehatan reproduksi pejantan (Ax et al. 2000a).
Gambar 1 Saluran reproduksi babi jantan (Frandson 1965)
Kelj. Vesikularis
Kelj. Prostat
Kelj. Cowper
Muskulus retraktor penis
Penis
.Kauda epididimis
Testis Kaput epididimis
Ujung penis
Korpus epididimis Gubernakulum Ureter
Ampula
Vas deferens
Evaluasi Semen
Evaluasi semen perlu dilakukan untuk mengetahui kualitas semen yang dikoleksi dan untuk mengetahui kadar pengenceran serta jumlah pelayanan terhadap betina yang akan diinseminasi. Secara umum evaluasi yang dilakukan adalah evaluasi secara makroskopis untuk mengetahui volume, pH, warna dan konsistensi, serta evaluasi mikroskopis untuk mengetahui konsentrasi spermatozoa, gerakan individu (motilitas), dan morfologi spermatozoa.
Pemeriksaan secara mikroskopis dapat dilakukan dengan metode pewarnaan eosin-nigrosin dan pewarnaan Williams. Pewarnaan spermatozoa berfungsi untuk membantu proses pengamatan morfologi dan morfometri spermatozoa. Pewarna eosin merupakan zat warna yang bersifat asam dan mampu berpendar karena mengandung brom, dan dapat mewarnai sitoplasma. Pewarna eosin-nigrosin merupakan double staining untuk memberikan efek kontras sehingga memberi batas yang jelas pada sel (Gunarso 1989).
Pewarnaan Williams merupakan pewarnaan dengan zat warna eosin dan zat warna dasar basic fuchsin golongan trifenil methan yang umum digunakan untuk mewarnai sitoplasma. Keunggulan dari pewarnaan Williams yaitu preparat ulasan semen segar dapat disimpan terlebih dahulu sebelum dilakukan pewarnaan Williams, dan tingkat kejernihan preparat sangat jelas sehingga memudahkan pengamatan morfologi dan morfometri spermatozoa.
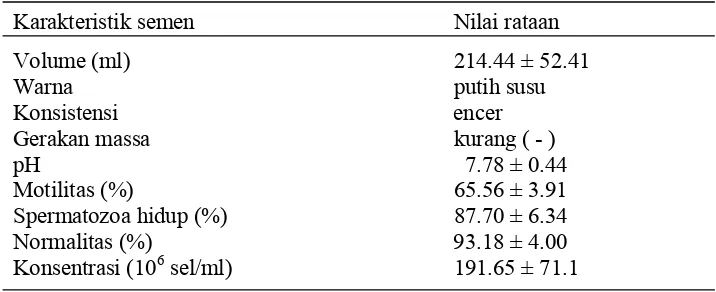
Karakteristik semen dan komposisi plasma semen babi (Ax et al. 2000b; Garner dan Hafez 2000) masing-masing dapat dilihat pada Tabel 1 dan 2.
Tabel 1 Karakteristik semen babi
Kriteria Jumlah
Volume (ml) tanpa gelatin 150-200
Konsentrasi (106/ml) 200-300
Total sperma (109) 30-60
Sperma motil (%) 50-80
Morfologi sperma normal (%) 70-90
Ejakulat/minggu (kali) 2-3
pH 7.3-7.8
Jumlah sel hidup/inseminasi (106) 2000-3000
Tabel 2 Komposisi plasma semen babi
Kandungan Jumlah
Fructose (mg/100ml) 9
Sorbitol (mg/100ml) 6-18
Citrid acid (mg/100ml) 173
Inositol (mg/100ml) 380-630
Ergothioneine (mg/100ml) 17
Glycerylphosphorylcholine (mg/100ml) 110-240
Sodium (mg/100ml) 587
Potassium (mg/100ml) 197
Chloride (mg/100ml) 260-430
Calcium (mg/100ml) 6
Magnesium (mg/100ml) 5-14
Sumber : Garner dan Hafez (2000)
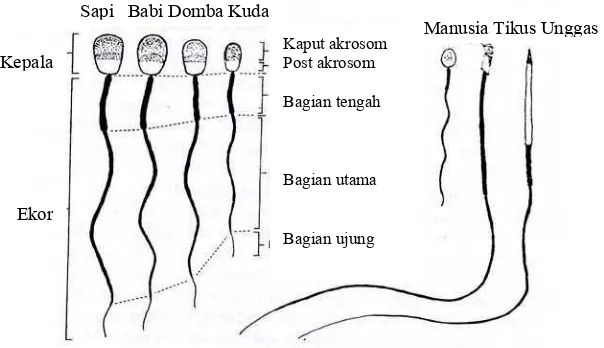
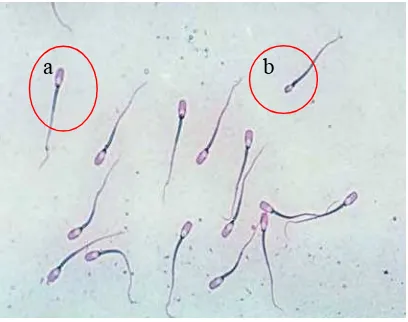
Spermatozoa normal pada babi terdiri dari kepala dan ekor (Gambar 2). Bagian kepala memegang peranan penting dalam keberhasilan proses fertilisasi, karena terdapat enzim hyaloronidase yang dapat menembus dinding sel telur dan membawa kromosom (heredity) yang mengandung deoxy-ribonucleid acid (DNA) serta dilindungi oleh tudung akrosom. Sementara bagian ekor berperan sebagai sarana penggerak bagi spermatozoa untuk mencapai tempat fertilisasi dengan bantuan sel-sel mitokhondria yang terdapat pada pangkal ekor spermatozoa dengan memanfaatkan karbohidrat dan fruktosa sebagai sumber energi (Toelihere 1993; Garner dan Hafez 2000).
Gambar 2 Spermatozoa normal pada babi (Garner dan Hafez 2000)
Kepala
Ekor
Sapi Babi Domba Kuda
Manusia Tikus Unggas
Kaput akrosom Post akrosom
Bagian tengah
Bagian utama
Menurut Hirai et al. (2001) secara morfometri, panjang dan lebar kepala spermatozoa babi (Sus scrofa domestica) adalah masing-masing 9.27 ± 0.05µm dan 4.66 ± 0.02µm. Abnormalitas spermatozoa pada babi yang digunakan dalam program IB tidak boleh lebih dari 20%. Abnormalitas spermatozoa dapat terjadi selama proses spermatogenesis maupun setelah keluar dari saluran epididymis (Toelihere, 1993; Bonet et al. 1993; Ax et al. 2000a dan Johnson et al. 2000). Faktor-faktor yang menyebabkan terjadinya abnormalitas spermatozoa adalah genetik, umur, breed, cahaya dan temperatur, manajemen pemeliharaan, frekuensi penampungan, pengenceran, dan lingkungan.
Pengenceran Semen
Fresh semen memiliki kemampuan bertahan untuk hidup (viability) secara in vitro yang terbatas, sehingga untuk meningkatkan daya viabilitas maupun daya fertilisasi optimum dari semen yang ditampung maka semen dan atau spermatozoa harus dipreservasi atau diawetkan untuk beberapa lama sesudah penampungan. Salah satu cara untuk mengawetkan semen secara in vitro adalah dengan penambahan larutan pengencer pada semen, yang dapat menjamin kebutuhan fisik dan kimiawi dari spermatozoa serta dapat disimpan pada temperatur dan waktu tertentu untuk kemudian dipakai sesuai dengan kebutuhan (Toelihere 1993). Bahan pengencer memiliki fungsi mekanis, fisik dan biokimia (Supriatna dan Pasaribu 1992). Hal penting yang perlu diperhatikan dalam pembuatan pengencer semen adalah penggunaan peralatan yang bersih dan steril, serta bahan-bahan tidak bersifat toksik terhadap spermatozoa dan alat kelamin betina. Bahan pengencer umumnya dapat disimpan paling lama hanya satu minggu.
pertumbuhan kuman dengan menggunakan bahan antibiotik (Toelihere 1993; Gadea 2003).
Bahan pengencer semen babi telah banyak diteliti dan dikembangkan untuk mendukung program IB diantaranya adalah susu skim, Tris, maupun pengencer laktosa, dimana komponen dasar dari pengencer sintetis umumnya merupakan kombinasi dari penyangga, karbohidrat, dan kuning telur. Bahan pengencer untuk semen babi berdasarkan daya simpannya dari hari pertama semen dikoleksi dapat diklasifikasikan menjadi dua tipe yaitu berdaya simpan pendek/short-term extender (1 - 3 hari) dan berdaya simpan panjang/long-term extender (5 - 7 hari) (Johnson et al. 1982; Gadea 2003; Robert 2006).
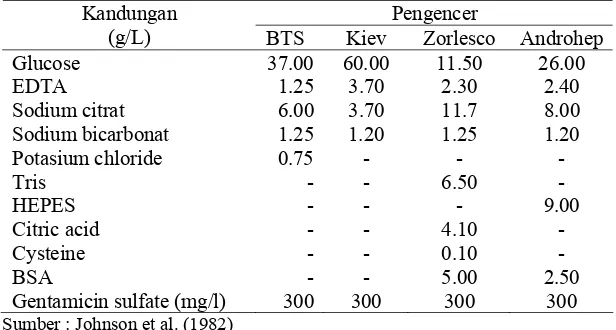
Bahan pengencer tipe short-term seperti Beltsville Liquid (BL-1), Beltsville Thawing Solution (BTS), Illinois Variable Temperature (IVT) dan Kiev, sedangkan bahan pengencer tipe long-term seperti Acromax®, Androhep®, Modena, Mulberry III®, X-Cell®, Zorlesco dan Zorpva (Johnson et al. 1982; Li-Jun et al. 2002; Gadea 2003, Dube et al. 2004; Beauliu et al. 2005; Garcia-Casado et al. 2005; Kadirvel et al. 2005; Vyt et al. 2005). Komposisi beberapa bahan pengencer yang dimaksud, diperlihatkan pada Tabel 3.
Tris (hydroxymethyl) aminomethan merupakan salah satu buffer yang umum digunakan, karena mempunyai kemampuan sebagai penyangga yang baik dengan toksisitas yang rendah dalam konsentrasi yang tinggi (Steinbach dan Foote 1967). Tris sudah lama digunakan sebagai komponen dasar pengencer semen sapi, babi dan domba (Maxwell dan Salamon 1993). Tris dapat memperpanjang daya hidup spermatozoa pada temperatur -5 °C hingga -196 °C (Bearden dan Fuquay 1997).
Hasil penelitian Paulenz et al. (2002) dengan semen cair domba menunjukkan bahwa pengencer dasar Tris dapat mempertahankan daya hidup spermatozoa lebih baik daripada pengencer sitrat maupun susu skim pada temperatur penyimpanan 5 dan 20 °C. Hasil penelitian Drajad (1994) menunjukkan bahwa bahan pengencer Tris-sitrat kuning telur yang digunakan untuk pengenceran semen rusa, kemudian dikemas dalam bentuk pelet maupun straw dan dibekukan menggunakan CO2 kering, maupun N2 cair diperoleh hasil
Tabel 3 Komposisi kimia BTS, Kiev, Zorlesco, dan Androhep
Pengencer Kandungan
(g/L) BTS Kiev Zorlesco Androhep
Glucose 37.00 60.00 11.50 26.00
EDTA 1.25 3.70 2.30 2.40
Sodium citrat 6.00 3.70 11.7 8.00
Sodium bicarbonat 1.25 1.20 1.25 1.20
Potasium chloride 0.75 - - -
Tris - - 6.50 -
HEPES - - - 9.00
Citric acid - - 4.10 -
Cysteine - - 0.10 -
BSA - - 5.00 2.50
Gentamicin sulfate (mg/l) 300 300 300 300
Sumber : Johnson et al. (1982)
Natrium sitrat telah digunakan sebagai pengenceran semen ruminansia kecil. Natrium sitrat merupakan penyangga yang mampu mempertahankan kestabilan pH pada pengencer, sehingga menguntungkan untuk memelihara kelangsungan hidup spermatozoa. Ethylenediamine-tetra-acetic acid (EDTA) merupakan bahan berbasis ion khususnya Ca++ yang dapat melindungi membran plasma spermatozoa (Watson 1990).
Kuning telur umumnya ditambahkan pada pengencer semen karena berperan sebagai sumber energi, agen protektif dan sebagai bahan anti cold shock. Kuning telur mengandung lipoprotein dan lesitin yang dapat melapisi membran plasma sel (Toelihere 1993). Bagian yang berperan sebagai agen protektif adalah lipoprotein berkepekatan rendah (low density lipoprotein), khususnya phospholipid yang diidentifikasi sebagai komponen efektif dalam melindungi membran spermatozoa terhadap pengaruh pendinginan yang cepat (Park dan Graham 1992), dan mencegah peningkatan aliran ion kalsium ke dalam sel yang dapat merusak spermatozoa (White 1993). Penggunaan kuning telur sebesar 15% sampai 20% dalam pengencer semen kambing untuk proses pembekuan telah direkomendasikan oleh Trejo et al. (1996).
pengaruh cold shock selama proses penyimpanan, mengingat protein mampu melindungi membran spermatozoa dari pengaruh cold shock (Johnson et al. 2000; Huo 2002; Zhou 2004). Disamping itu juga BSA dalam bahan pengencer berperan untuk menjaga kelangsungan pertumbuhan dan perkembangan dari suatu sel (Bassol 2005). Menurut Waberski et al. (1989) yang dikutip dalam Johnson et al. (2000) BSA dapat mempertahankan motilitas spermatozoa sampai enam hari penyimpanan.
Karbohidrat merupakan sumber energi bagi spermatozoa. Karbohidrat yang ditambahkan ke dalam pengencer semen memiliki beberapa fungsi yaitu menyediakan sumber energi yang mendukung motilitas spermatozoa selama inkubasi dan mempertahankan tekanan osmotik cairan sel spermatozoa. Kemampuan jenis karbohidrat dalam melindungi sel spermatozoa berbeda tergantung pada temperatur penyimpanan semen, berat molekul dari jenis karbohidrat dan tipe dari penyangga yang digunakan dalam pengencer. Menurut Molinia et al. (1994) jenis karbohidrat monosakarida yang ditambahkan ke dalam pengencer Tris lebih cocok dibandingkan dengan disakarida dalam mempertahankan motilitas spermatozoa semen cair anjing. Garcia dan Graham (1989) yang diacu dalam Yildiz et al. (2000) menunjukkan bahwa trisakarida tidak efektif dibandingkan dengan monosakarida dan disakarida dalam mempertahankan motilitas semen cair maupun motilitas pasca thawing spermatozoa sapi. Meskipun disakarida khususnya sukrosa dan maltosa dapat menurunkan kematian sperma dan menurunkan kerusakan tudung akrosom akan tetapi monosakarida seperti glukosa dan galaktosa, lebih tinggi dalam mempertahankan motilitas sperma, viabilitas dan kerusakan tudung akrosom dalam waktu yang lebih lama.
Glukosa dan fruktosa merupakan monosakarida atau gula sederhana dengan rumus molekul (C6H12O6) yang tidak dapat dihidrolisis menjadi bentuk yang lebih
plasma semen yang berguna dalam proses metabolisme spermatozoa untuk menghasilkan energi dan daya hidup bagi spermatozoa. Ponglowhapan et al. (2004) melaporkan bahwa penambahan glukosa 70 mM ke dalam pengencer Tris-kuning telur pada proses preservasi semen anjing mampu mempertahankan motilitas 59.10%, sedangkan jika menggunakan fruktosa 70 mM mampu mempertahankan motilitas 60.90% setelah disimpan selama 10 hari pada temperatur 5 °C. Penggunaan fruktosa sebanyak 1 g dalam pengencer sitrat kuning telur pada proses preservasi semen sapi perah terbukti mampu mempertahankan motilitas 53.30% setelah disimpan selama 24 jam dalam lemari es. Sementara hasil penelitian Hirotada et al. (2006) menggunakan kombinasi glukosa dan fruktosa (5.0 dan 0.5 mmol) sebagai pengencer semen babi menunjukkan terjadi peningkatan motilitas progresif, reaksi akrosom dan kemampuan fertilisasi pada spermatozoa babi.
Dewasa ini pengencer BTS banyak digunakan oleh pengelola program IB, karena dari sudut ekonomis harganya paling murah dengan hasil yang memuaskan. Penelitian oleh Kommisrud et al. (2002) menggunakan pengencer BTS selama enam jam penyimpanan dalam temperatur 16 - 18 °C menunjukkan persentase motilitas sebesar 79.8%. Hasil dari peneliti lainnya, Kadirvel et al. (2005) menunjukkan BTS dan Modena dapat digunakan sebagai pengencer semen babi dengan daya simpan selama empat hari dalam temperatur 17 °C, dengan motilitas pada pengamatan hari keempat mencapai 64.43% dengan pengencer BTS, dan 61.87% dengan pengencer Modena. Pengencer lain yang telah digunakan oleh peneliti diantaranya adalah Zorlesco. Menurut hasil peneltian Huo et al. (2002) menunjukkan lebih dari 50% spermatozoa yang dapat dipertahankan selama 13 hari penyimpanan dengan pengencer Zorlesco dan Androhep dalam temperatur 17 °C. Sementara hasil penelitian Zhou et al. (2004) menunjukkan penggunaan pengencer Zorlesco dapat mempertahankan kualitas spermatozoa selama 5 - 8 hari dalam temperatur 20 °C.
Penyimpanan Semen
dan penyimpanan. Semen babi dapat dikemas dan disimpan dalam bentuk semen cair serta dapat dikirim ke beberapa tempat melalui transportasi darat maupun udara. Temperatur optimum untuk penyimpanan semen babi adalah 15 - 20 °C (Paulenz et al. 2000), dan perubahan 1 - 2 °C dapat menurunkan viabilitas spermatozoa selama disimpan.
Penambahan pengencer dapat mempertahankan viabilitas spermatozoa sampai siap digunakan dalam program IB. Semen harus dikemas dan disimpan dalam sebuah kontainer atau kotak, dan dilindungi dari stres fisik (guncangan), dengan menggunakan material dari styrofoam, untuk menjaga temperatur 15 °C. Penggunaan sytrofoam memiliki beberapa kelebihan, diantaranya adalah lebih ringan, bentuk dan ukuran dapat diatur, serta dapat ditambahkan es (ice block). Penelitian Flowers (1996) yang dikutip oleh Kevin (2000) menunjukkan tentang perubahan viabilitas spermatozoa selama transportasi (Tabel 4).
Tabel 4 Pengaruh kotak styrofoam terhadap viabilitas spermatozoa selama 24 jam penyimpanan
Perlakuan Viabilitas (%)
Kotak styrofoam + tanpa es 70.3
Kotak styrofoam + es 88.9
Kantong plastik + tanpa es 77.7
Kantong plastik + es 86.8
Sumber : Kevin (2000)
Tabel 5 Metode evaluasi perubahan kualitas spermatozoa babi pada temperatur yang berbeda
Test (%) 39 °C 20 °C 15 °C 4 °C
Trypan blue Æ viability 1,6 46,9 42,0 31,0
HOST Æ coiled-tail 1,7 28,7 24,1 20,1
Coomassie blue Æ TAU 4,5 35,5 55,7 22,8
FITC-PNA Æ % TAU 4,3 43,2 17,3 14,8
Sumber : Chun-Xia dan Zeng-Ming 2000
Hasil dari keempat metode evaluasi semen tersebut sangat berkorelasi dan dapat digunakan secara efektif dalam penentuan kualitas sperma. Hasil penelitian dalam Tabel 5 memperlihatkan bahwa integritas membran dan viabilitas spermatozoa dapat diawetkan secara in vitro dengan hasil yang baik pada temperatur 20 dan 15 °C selama 48 jam, dimana viabilitas spermatozoa mencapai 46.9% pada temperatur 20 °C dan 42.0% pada temperatur 15 °C.
Spermatozoa mengalami beberapa kerusakan selama proses penyimpanan. Kerusakan tersebut dapat disebabkan oleh beberapa faktor seperti adanya cekaman osmotik, dan cekaman dingin. Tekanan osmotik harus dipertahankan selama proses penyimpanan semen karena bila tidak dipertahankan dapat mengakibatkan tekanan osmotik di dalam dan di luar sel berbeda sehingga air akan mengalir ke daerah yang bertekanan osmotik tinggi. Bila hal ini terjadi dapat menimbulkan cekaman osmotik pada spermatozoa dan menyebabkan spermatozoa mati. Gejala cekaman osmotik memainkan peranan yang sangat penting terhadap kerusakan membran sel selama proses penyimpanan semen. Tanda - tanda adanya cekaman osmotik adalah peningkatan kejadian spermatozoa dengan ekor melingkar, serta menurunkan viabilitas dan integritas membran plasma spermatozoa.
Penurunan temperatur pada spermatozoa akan menyebabkan terjadinya penurunan aktivitas flagela, kerusakan organel intraseluler dan kerusakan membran sel. Terdapat dua tipe kerusakan sel akibat cekaman dingin, yaitu kerusakan langsung dan kerusakan laten. Kerusakan langsung akan mempengaruhi struktur dan fungsi - fungsi seluler (penurunan proses metabolisme) dari spermatozoa, sedangkan kerusakan laten sulit untuk diamati dan baru akan terlihat setelah dihangatkan kembali. Pengaruh utama dari cekaman dingin terhadap spermatozoa adalah penurunan motilitas, viabilitas, perubahan permiabilitas membran dan perubahan komponen lipid membran atau struktur phospholipid membran plasma.
Adenosin triphosphat (ATP) merupakan faktor utama yang berperan dalam motilitas spermatozoa, sehingga spermatozoa harus mampu menghasilkan ATP dalam jumlah tertentu sebagai sumber energi. Kerusakan membran spermatozoa menyebabkan terlepasnya enzim aspartat-aminotransferase (AspAT) dari mitokondria spermatozoa ke dalam plasma semen, sehingga produksi ATP akan terhenti dan menyebabkan spermatozoa tidak bisa bergerak (Colenbrander et al. 1992).
Inseminasi Buatan pada Babi
Pelaksanaan inseminasi yang umum dilakukan oleh peternak adalah inseminasi dengan siklus alamiah. Deteksi berahi atau estrus pada induk memegang peranan penting dalam optimalisasi program IB, karena dengan ketepatan pendeteksian berahi akan memberikan hasil konsepsi yang tinggi, selain harus didukung oleh nilai persentase motilitas dan konsentrasi spermatozoa, serta volume semen.
Gambar 3 Saluran reproduksi babi betina (Sterle dan Safranski 1997)
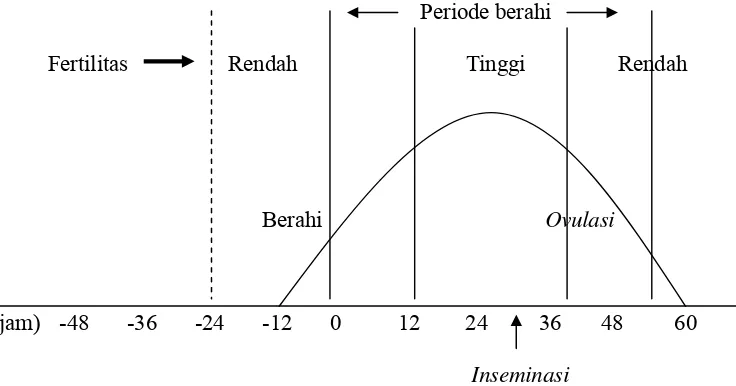
Siklus berahi pada babi adalah 19 - 23 hari, rata-rata 21 hari, dengan lama berahi 1 - 2 hari pada babi dara (gilts) dan 2 - 3 hari pada babi induk (sows). Sel telur dilepaskan 38 - 42 jam setelah munculnya tanda-tanda berahi (Anderson 2000), dan inseminasi dilakukan 30 - 35 jam setelah munculnya tanda-tanda berahi. Inseminasi dengan angka fertilitas yang tinggi dapat dicapai pada saat periode berahi 12 - 36 jam seperti yang diperlihatkan pada Gambar 4.
Periode berahi
Fertilitas Rendah Tinggi Rendah
Berahi Ovulasi
(jam) -48 -36 -24 -12 0 12 24 36 48 60
Inseminasi
Gambar 4 Pedoman waktu inseminasi pada babi (Anderson 2000)
Kantong urine Tuba fallopii Ovarium
[image:46.612.137.505.490.683.2]Berahi pada babi betina ditandai dengan warna vulva merah, hangat, dan adanya cairan kental pada vulva. Disamping itu juga ditandai dengan posisi telinga berdiri tegak (ear popping response) dan menunjukkan posisi diam (standing heat) saat diberikan tekanan pada punggung bagian belakang (Hafez dan Hafez 2000).
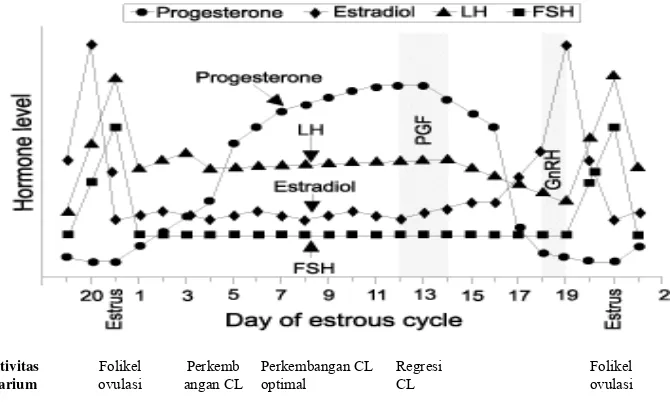
Setelah ovulasi perkembangan corpus luteum (CL) dimulai, dan hormon progesteron meningkat dimulai setelah dua hari ovulasi dan bertahan selama 14 - 15 hari pada fase luteal, dimana pada akhir fase luteal terjadi pengeluaran PGF2α
yang akan melisiskan CL dan mengalami siklus kembali. Aktifitas hormonal pada babi betina diperlihatkan dalam Gambar 5.
[image:47.612.153.488.285.486.2]
Gambar 5 Aktivitas hormonal dan ovarium babi betina (Coffey et.al 2007)
Teknik Inseminasi Buatan
Inseminasi buatan pada babi umumnya menggunakan semen cair, dimasukkan secara transcervical dengan menggunakan sebuah kateter yaitu suatu alat khusus terbuat dari karet yang pada bagian ujungnya berbentuk spiral menyerupai bentuk penis babi pejantan, dengan panjang kateter 50 - 55 cm. Sebelum digunakan, kateter diolesi sedikit semen sebagai bahan pelumas. Inseminasi secara transcervical menggunakan kateter diperlihatkan dalam Gambar 6.
Aktivitas ovarium
Folikel ovulasi
Perkemb angan CL
Perkembangan CL optimal
Regresi CL
Gambar 6 Posisi kateter pada pelaksanaan inseminasi buatan (Sterle dan Safranski 1997)
Secara umum alat inseminasi pada babi ada dua tipe yakni rubber-spirette (berbentuk spiral dari bahan karet) dan plastic-bovine (berbetuk seperti spiral pendek dari bahan plastik). Tipe rubber-spirette lebih umum digunakan karena bentuknya menyerupai penis babi jantan dan sesuai dengan saluran reproduksi babi betina, serta fleksibel dan tidak menimbulkan rasa sakit bagi induk yang diinseminasi, dan mudah dibersihkan setelah digunakan. Sedangkan tipe plastic-bovine jarang digunakan karena diameternya kecil sehingga memberikan peluang keluarnya semen yang sudah dideposisikan ke dalam saluran kelamin betina, serta teksturnya keras dan menimbulkan rasa sakit bagi induk yang diinseminasi.
Posisi kateter setelah melewati servik akan terkunci dan semen cair dideposisikan tepat didepan uterus, yang selanjutnya semen cair akan mengalir masuk ke dalam uterus mengikuti kontraksi uterus (Sterle dan Safranski 1997).
Inseminasi buatan dengan metoda transcervical menggunakan semen cair, yang dikemas per dosis dalam botol plastik, botol kecil atau sachet dengan volume per dosis 80 - 90 ml. Konsentrasi spermatozoa dalam satu dosis inseminasi mengandung rata-rata 2000 - 3000 x 106 sel untuk fertilitas yang optimum (Ax et al. 2000b). Menurut Singleton (2001) volume per dosis 70 - 100
Kateter melalui servik dan terkunci
ml dengan konsentrasi spermatozoa mencapai 2500 - 4000 x 106 sel. Menurut Kommisrud et al. (2002) volume per dosis 80 ml dengan konsentrasi spermatozoa mencapai 2700 x 106 sel untuk angka fertilitas yang optimum. Konsentrasi spermatozoa per ejakulat dengan motilitas lebih dari 65% dan mengandung kurang dari 20% sperma abnormal, dapat diencerkan dengan perbandingan satu bagian semen dengan 4 - 8 bagian pengencer, untuk memenuhi konsentrasi yang digunakan dalam IB (Ax et al. 2000b).
Keberhasilan Inseminasi Buatan
Keberhasilan inseminasi pada babi induk dipengaruhi oleh beberapa faktor diantaranya munculnya estrus setelah penyapihan, lamanya estrus, serta waktu antara munculnya estrus dan ovulasi, serta dua faktor penting dalam inseminasi yakni jumlah spermatozoa dan volume semen.
Diagnosa kebuntingan dapat dilihat dengan tidak adanya berahi, namun berhentinya berahi tidak selalu berarti telah terjadi kebuntingan karena berahi dapat pula terjadi selama kebuntingan muda, dan induk yang tidak bunting dapat juga tidak memperlihatkan berahi. Perubahan-perubahan histologik pada epithel vagina yang diambil dengan biopsy dari hari ke-21 sampai ke-90 masa kebuntingan dan memperlihatkan adanya 2 - 3 lapis sel-sel epithel dapat dijadikan indikasi kebuntingan karena selama fase luteal atau fase folikel siklus berahi terdapat empat atau lebih lapisan sel-sel epithel (Toelihere 1993). Masa kebuntingan adalah selama 111 - 117 hari atau rata-rata 114 hari (Toelihere 1993; Jainudeen dan Hafez 2000). Adapun faktor-faktor yang mempengaruhi lamanya kebuntingan yakni litter size (jumlah anak), umur induk, dan kondisi lingkungan.
Beltsville-1. Dosis inseminasi yang digunakan dalam penelitian tersebut yakni 100 ml dengan konsentrasi mencapai 3000 x 106 spermatozoa.
MATERI DAN METODE
Tempat dan Waktu Penelitian
Pengambilan dan pemeriksaan semen babi dilakukan di Balai Inseminasi Buatan Daerah (BIBD) Unit Pelaksana Teknis Dinas (UPTD) Peternakan Propinsi Bali di Baturiti selama tiga bulan (Desember 2006 - Maret 2007). Selanjutnya dilakukan pemeriksaan semen secara lebih akurat selama satu bulan (Maret - April 2007) di Laboratorium Fisiologi dan Reproduksi Unit Rehabilitasi Reproduksi (URR), Fakultas Kedokteran Hewan, Institut Pertanian Bogor.
Materi Penelitian
Sumber Semen
Ternak yang digunakan sebagai sumber semen pada penelitian ini adalah tiga ekor babi jantan dewasa kelamin, dari bangsa Yorkshire, umur tiga tahun, dalam kondisi sehat, dan mempunyai kualitas semen baik, yaitu konsentrasi spermatozoa lebih dari 150 x 106sel/ml dan motilitas spermatozoa lebih dari 60%. Penampungan semen dilakukan pada pagi hari, dua kali seminggu, dengan metode manual (glove hand method) dibantu peralatan tabung penampungan (Gambar 7). Pemisahan fraksi gelatin dilakukan dengan melapisi kain kassa pada mulut tabung.
(a) (b)
Kandang dan Pakan
Pejantan babi dipelihara dalam kandang, lantainya terbuat dari beton, dinding kandang dibuat dari anyaman besi berukuran 2 x 3 x 1 meter dan atapnya asbes. Masing-masing kandang pejantan dilengkapi dengan tempat pakan dan kran air otomatis (water nipple). Pakan yang diberikan untuk pejantan mengandung protein 18% dan energi 16 MJ (3824.16 kkal/kg), yang terdiri dari dedak padi, dedak jagung, polar, gandum, konsentrat 152, mineral, lisin, dan starbio, dengan total pemberian pakan sebanyak 2,5 kg/ekor/hari, serta air minum diberikan ad libitum (selalu tersedia).
Induk
Babi induk yang digunakan sebagai akseptor IB sebanyak 18 ekor, dengan kondisi induk sudah pernah beranak kedua atau ketiga yang ditempatkan dalam kandang model batterey. Masing-masing kandang induk dilengkapi dengan tempat pakan dan kran air otomatis (water nipple).
Alat dan Bahan
Alat
Peralatan yang digunakan dalam penelitian ini adalah dummy-sow, penampung semen babi, water bath (pemanas air), gelas ukur, timbangan analitik dalam satuan miligram sampai gram, tabung berskala, epemdorf, mikropipet, pipet tetes, spuit, pH meter, termometer, obyek gelas, kotak preparat, api bunsen, meja pemanas, mikroskop-binokuler, sperm-vision, plastic shocket (plastik semen), lemari es, kotak styrofoam, dan alat-alat bantu lainnya yang dipergunakan sesuai dengan fungsinya.
Bahan
glisin sebagai pengganti sistein karena glisin mudah diperoleh dan memiliki fungsi yang sama dengan sistein. Komposisi bahan pengencer yang digunakan dalam penelitian ini dapat dilihat pada Tabel 6.
[image:53.612.151.489.327.550.2]Bahan-bahan pewarnaan yang digunakan dalam penelitian ini adalah bahan pewarnaan eosin-nigrosin dan pewarnaan Williams. Penggunaan pewarnaan eosin-nigrosin dan pewarnaan Williams bertujuan untuk mengamati morfologi dan morfometri spermatozoa. Pewarnaan eosin-nigrosin terdiri atas 20 gr nigrosin, 1.5 gr sodium sitrat, 300 ml aquabidest, dan 3.3 gr eosin yellow. Pewarnaan Williams terdiri atas 10 gr basic fuchsin dalam 100 ml alkohol 95%, saturated bluish eosin dalam alkohol 95% dan 10 ml basic fuchsin (hasil larutan pertama) dalam 170 ml larutan fenol 5%.
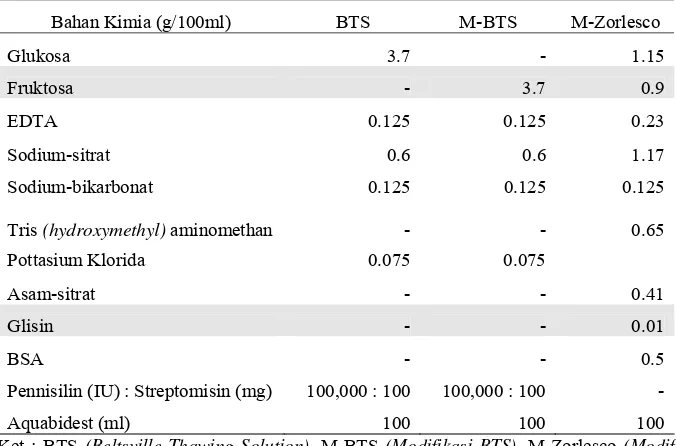
Tabel 6 Komposisi bahan pengencer semen babi
Bahan Kimia (g/100ml) BTS M-BTS M-Zorlesco
Glukosa 3.7 - 1.15
Fruktosa - 3.7 0.9
EDTA 0.125 0.125 0.23
Sodium-sitrat 0.6 0.6 1.17
Sodium-bikarbonat 0.125 0.125 0.125
Tris (hydroxymethyl) aminomethan - - 0.65
Pottasium Klorida 0.075 0.075
Asam-sitrat - - 0.41
Glisin - - 0.01
BSA - - 0.5
Pennisilin (IU) : Streptomisin (mg) 100,000 : 100 100,000 : 100 -
Aquabidest (ml) 100 100 100
Ket : BTS (Beltsville Thawing Solution), M-BTS (Modifikasi BTS), M-Zorlesco (Modifikasi
Zorlesco), BSA (Bovine Serum Albumin), EDTA (Ethylenediamine-tetra-acetic acid).
Metode Penelitian
Karakteristik Semen Segar
dalam satu minggu pada pagi hari sebanyak satu ejakulat menggunakan alat penampung semen untuk babi, dengan metode manual (glove hand method), dan betina pemancing berupa dummy-sow. Pemisahan fraksi gel dilakukan dengan memasang kain kassa beberapa lapis pada mulut tabung koleksi.
Semen yang diperoleh dievaluasi secara makroskopis dan mikroskopis. Evaluasi secara makroskopis meliputi pemeriksaan volume (ml), warna, pH dan pemeriksaan konsistensi atau kekentalan. Evaluasi secara mikroskopis meliputi gerakan massa ( 0, +, ++ dan +++), konsentrasi spermatozoa (106 sel/ml), persentase sperma motil (M%) dan persentase sperma hidup (SH%) dengan pewarnaan eosin-nigrosin, serta persentase normalitas dan abnormalitas spermatozoa dengan pewarnaan Williams.
Evaluasi Semen
Semen yang telah ditampung dievaluasi secara makroskopis dan mikroskopis. Segera setelah semen diperoleh pemeriksaan makroskopis dilakukan meliputi volume, pH, konsistensi dan warna, sedangkan pemeriksaan mikroskopis ditujukan untuk mengetahui kualitas spermatozoa.
Pemeriksaan mikroskopis meliputi :
a) Gerakan massa diperiksa dengan menggunakan mikroskop c