BAKTERI YANG BERASOSIASI DENGAN SPONS
Jaspis
sp. :
ANALISIS PENGHASIL SENYAWA ANTIMIKROB DAN
KERAGAMAN GENETIKNYA
HERMAWATY ABUBAKAR
SEKOLAH PASCASARJANA
INSTITUT PERTANIAN BOGOR
Dengan ini saya menyatakan bahwa tesis Bakteri yang Berasosiasi dengan Spons Jaspis sp.: Analisis Penghasil Senyawa Antimikrob dan Keragaman Genetiknya adalah karya saya dengan arahan dari komisi pembimbing dan belum diajukan dalam bentuk apa pun kepada perguruan tinggi mana pun. Sumber informasi yang berasal atau dikutip dari karya yang diterbitkan maupun tidak diterbitkan dari penulis lain telah disebutkan dalam teks dan dicantumkan dalam Daftar Pustaka di bagian akhir tesis ini.
Bogor, Juli 2009
ABSTRACT
HERMAWATY ABUBAKAR. Spons (Jaspis sp.) – Associated Bacteria: Antimicrobial Production and Genetic Diversity Analyses. Under Direction of Aris Tri Wahyudi and Munti Yuhana.
ABSTRACT
Living benthic marine organisms such as sponges are frequently assosiated with bacteria which may produce useful antimicrobial compounds. Genetic diversity of bacteria isolated from marine spongeJaspissp. which has capability in producing antibacterial subtances was investigated. As many as 32 isolates (45,71%) and 20 (29,41%) isolates originating from mesohyl and sponge surface respectively, showed the antibacterial activity againstStaphylococcus aureus, Vibrio harveyi, Escherichia coli, Pseudomonas aeruginosa, Enterophatogenic Escherichia coli (EPEC K-11),
Candida albicans, and C. tropicalis. Thirty most potential isolates were further studied by amplified ribosomal DNA restriction analysis (ARDRA) to asses their genetic diversity. Restriction analysis using enzymes RsaI, HaeIII, and HinfI of the 16S rRNA genes resulted seven phylotipes. The 16S rRNA gene sequence of choosen isolates i.e. SAB E-8, SAB E-33, SAB E-35, SAB E-38, SAB E-40 and SAB S-43 that showed inhibition of the growth for all microorganism target were identified. The use of a few phenotypic tests for those isolate can be applied to differentiate them. Gram staining technique was used to distinguish Gram negative from Gram positive ones. Isolates designed as SAB E-8, SAB E-35, and SAB E-40 were identified as Gram negative, whereas SAB E-33, SAB E-38, and SAB S-43 were Gram positive. For Gram positive isolates, further test were performed including spora staining and catalase test forBacillusidentification. Based on their 16S rRNA gene sequences, there were 3 isolates closely related to Pseudomonas sp. while the remaining 3 isolates were members ofBacillusgroup.
Analisis Penghasil Senyawa Antimikrob dan Keragaman Genetiknya. Dibimbing oleh Aris Tri Wahyudi dan Munti Yuhana.
Spons merupakan salah satu komponen biota penyusun terumbu karang yang mempunyai potensi bioaktif yang belum banyak dimanfaatkan. Hewan laut ini mengandung senyawa aktif yang persentase keaktifannya lebih besar dibandingkan dengan senyawa-senyawa yang dihasilkan oleh tumbuhan darat. Spons umumnya dapat bertahan hidup di perairan laut yang miskin nutrisi karena adanya assosiasi dengan organisme lain khususnya bakteri.
Bakteri banyak ditemukan secara komensal di permukaan dan bagian mesohyl spons. Pola makan spons yang khas yaitu filter feeder (menghisap dan menyaring) dapat memanfaatkan jasad renik disekitarnya sebagai sumber nutrien, diantaranya bakteri yang hidup pada perairan tersebut. Namun seringkali bakteri juga dijumpai hidup dan berkolonisasi dengan memanfaatkan nutrien yang terdapat pada spons tersebut.
Produk alami laut sebagai hasil metabolik sekunder kemungkinan dihasilkan oleh kehadiran mikroorganisme pada jaringan spons sebagai simbion, baik simbion intraselluler ataupun ekstraselluler. Senyawa-senyawa organik tersebut dapat ditransport karena adanya kerjasama antara simbion dan inangnya. Kehadiran kedua pasangan simbion ini juga menjadi syarat untuk menghasilkan metabolik sekunder seperti senyawa bioaktif yang bersifat antimikrob. Penelitian ini bertujuan untuk mengisolasi dan mengkarakterisasi bakteri (endosimbion dan ektosimbion) penghasil senyawa antimikrob dan menganalisis keragaman genetiknya berdasarkan amplified ribosomal DNA restriction analysis(ARDRA) dan sekuensing gen 16S rRNA.
Metode untuk mengisolasi bakteri simbion yang diduga memiliki potensi antimikrob dibagi atas dua metode yaitu untuk mengisolasi bakteri dari permukaan dan bagian mesohylJaspis sp. Total jumlah bakteri hasil isolasi dari permukaan dan mesohyl diuji kemampuan antimikrobnya dengan menggunakan bakteri target
Escherichia coli, EPEC K-11, Vibrio harveyi, Pseudomonas aeruginosa, Staphylococcus aureus dan dua jenis khamir yaitu Candida albicans dan C. tropicalis. Bakteri yang memiliki aktivitas antimikrob dianalisis keragaman genetiknya dengan Amplified ribosomal DNA restriction analysis (ARDRA) serta didentifikasi dengan pewarnaan Gram, uji parsial dan sekuensing gen 16S rRNA.
berasosiasi dengan cara vertikal transmisi. Isolat bakteri yang berasal dari permukaan dan memiliki aktivitas antimikrob diduga adalah bakteri yang memiliki kemampuan untuk melindungi spons dari patogen, predator danbiofouler.
Meskipun jumlah isolat bakteri yang berasal dari permukaan hampir sama dengan isolat endofit, namun aktivitas antimikrob isolat permukaan lebih rendah dibandingkan isolat endofit. Berdasarkan jumlah isolat yang mempunyai aktivitas antimikrob dan jumlah mikrob target yang dapat dihambat pertumbuhannya, isolat yang berasal dari bagian endofit spons Jaspis sp. lebih banyak dibandingkan isolat yang diisolasi dari permukaan. Bakteri simbion yang berasal dari bagian endofit yaitu mesohyl umumnya memiliki populasi yang berlimpah dan merupakan mikroba spesifik dari spons inangnya. Bakteri simbion yang berasal dari permukaan spons merupakan bakteri yang tidak spesifik dengan inangnya dan memiliki kemiripan dengan komunitas mikrob yang berada di lingkungan perairan dimana spons tersebut berada.
Hasil skrening terhadap semua isolat bakteri yang berasal dari endofit dan permukaan menunjukkan ada enam isolat bakteri yang mampu menghambat pertumbuhan semua mikrob target. Enam isolat tersebut terdiri dari lima isolat endofit yaitu SAB E-8, SAB E-33, SAB E-35, SAB E-38, dan SAB E-40 serta satu isolat permukaan yaitu SAB S-43. Berdasarkan hasil uji antagonis terhadapC. albicans dan
C. tropicalis,hanya isolat SAB E-33, SAB E-38 dan SAB E-40 yang memperlihatkan aktivitas antagonis yang baik. Kemampuan isolat bakteri yang berasosiasi dengan sponsJaspissp. dalam menghambat pertumbuhan mikroba target, merupakan bentuk aktivitas antagonis yang diduga dilakukan dengan menghasilkan kandungan senyawa yang bersifat antimikrobial. Biosintesis senyawa antimikrobial berperan penting dalam proses pelekatan, kolonisasi target hingga kompetisi dalam mendapatkan ruang dan nutrisi dengan mikroba lainnya.
Keragaman genetik dilakukan pada 30 isolat yang memiliki aktivitas antimikrob dilakukan dengan ARDRA. Amplifikasi gen 16S rRNA terhadap 30 isolat yang memiliki aktivitas antimikrob dilakukan dengan menggunakan primer spesifik yaitu 63f dan 1387r. Hasil elektroforesis amplifikasi gen 16S rRNA menampakkan pita yang berukuran sekitar 1300 pb. Primer 63f dan 1387r yang digunakan merupakan primer untuk gen yang menyandikan gen 16S rRNA yang telah didesain untuk seluruh domain bakteri. Primer ini dapat digunakan pada kultur murni bakteri maupun sampel alami dimana gen 16S rRNAnya sulit untuk diamplifikasi. Hasil pemotongan gen 16S rRNA memperlihatkan pola pita gen 16S rRNA yang beragam dengan jumlah 2-4 pita.
pewarnaan Gram dari ke enam isolat terbaik. Isolat SAB 8, SAB 35 dan SAB E-40 dari hasil pewarnaan Gram merupakan bakteri Gram negatif. Bakteri Gram positif yaitu isolat SAB E-33, SAB E-38 dan SAB S-43. Uji fisiologis tambahan untuk bakteri Gram positif diarahkan ke kelompok Bacillus dengan melakukan uji parsial yang meliputi pewarnaan Gram, endospora dan katalase. Hasil uji parsial menunjukkan bahwa ketiga isolat tersebut adalah kelompokBacillus, dicirikan oleh sel yang berbentuk batang, pewarnaan Gram positif, terdapat endospora yang terletak pada bagian sentral dan uji katalase positif.
BlastN sekuen gen 16S rRNA enam isolat dengan aktivitas mikrob terbaik, terbagi menjadi dua kelompok filogenetik yang berbeda yaitu genus Pseudomonas
(50%) dan Bacillus (50%). Isolat SAB E-8, SAB E-35, dan SAB E-40 termasuk dalam kelompokPseudomonaskarena ketiga isolat tersebut masing-masing homolog dengan Pseudomonas sp. HN-07, Pseudomonas sp. LPK2 dan Pseudomonas
sp.LD116, dengan tingkat identitas maksimum 97% - 98. Tingkat identitas maksimum 98% - 99% diperoleh dari tingkat homologi isolat SAB E-33, SAB E-38, dan SAB S-43 dengan isolat yang terdapat dalam Gen Bank, yaitu masing-masing
Bacillussp. strain K3,Bacillus pumilusstrain 210-50, danBacillussp.E287.
Pohon filogenetik yang menggunakan data sekuen parsial gen 16S rRNA isolat dengan aktivitas antimikrob terbaik dan beberapa galur acuan (reference strains) menunjukkan adanya kedekatan hubungan kekerabatan. Pohon filogenetik menunjukkan SAB-35 berdekatan secara evolusi dengan Pseudomonas sp. J451 dengan nilai boostrap 56%. Pohon filogenetik menunjukkan SABS-43 dan SABE-33 memiliki kedekatan kekerabatan dengan Bacillus sp. EGU72 sedangkan SAB E-38 denganBacillussp. D203.
© Hak Cipta milik IPB, tahun 2009 Hak Cipta dilindungi Undang-Undang
Dilarang mengutip sebagian atau seluruh karya tulis ini tanpa mencantumkan atau menyebutkan sumbernya. Pengutipan hanya untuk kepentingan pendidikan, penelitian, penulisan karya ilmiah, penyusunan laporan, penulisan kritik, atau tinjauan suatu masalah; dan pengutipan tersebut tidak merugikan kepentingan yang wajar IPB
KERAGAMAN GENETIKNYA
HERMAWATY ABUBAKAR
Tesis
Sebagai salah satu syarat untuk memperoleh gelar Magister Sains pada Mayor Mikrobiologi
SEKOLAH PASCASARJANA
INSTITUT PERTANIAN BOGOR
Judul Penelitian : Bakteri yang Berasosiasi dengan Spons Jaspis sp.: Analisis Penghasil Senyawa Antimikrob dan Keragaman Genetiknya Nama Mahasiswa : Hermawaty Abubakar
NRP : G351070021
Disetujui, Komisi Pembimbing
Dr. Aris Tri Wahyudi, MSi Dr. Munti Yuhana, MSi
Ketua Anggota
Diketahui,
Koordinator Mayor Mikrobiologi An. Dekan Sekolah Pascasarjana Sekretaris Program S2
Dr.Ir. Gayuh Rahayu Dr.Ir. Naresworo Nugroho, M.Sc.
Puji syukur penulis panjatkan ke Hadirat Allah SWT karena atas segala rahmat dan karuniahNya sehingga karya ilmiah ini berhasil diselesaikan. Topik yang dipilih adalahBakteri yang Berasosiasi dengan Spons Jaspis sp.:Analisis Penghasil Senyawa Antimikrob dan Keragaman Genetiknya, yang dilaksanakan sejak bulan Oktober 2008 sampai Mei 2009.
Penulis menyampaikan penghargaan dan ucapan terima kasih yang sebesar-besarnya terutama kepada pembimbing, yaitu Dr. Aris Tri Wahyudi, Msi. dan Dr. Munti Yuhana, Msi. yang telah banyak memberikan bimbingan dan saran selama penulis menempuh S2. Terimakasih juga penulis sampaikan kepada Dr. Dinamella Wahjuningrum, MSi. selaku Penguji Luar Komisi yang telah memberikan koreksi dan arahan untuk perbaikan tesis.
Ungkapan terima kasih juga disampaikan kepada kedua orang tua, Ayahanda H. Abubakar Makkarumpa dan Ibunda Hj. Bunga Matahari, Suami dan kedua Anakku atas keikhlasan, doa dan kasih sayangnya. Tidak lupa kepada saudara dan sahabat khususnya Ari Susilowati, MSi., Rika I. Astuti, MSi., dan Syamsul Bahri, SSi, penulis mengucapkan banyak terima kasih atas bantuan saran, kritik dan kebersamaanya.
Penulis menyadari bahwa tulisan ini masih jauh dari sempurna, sehingga kritik dan saran sangat diharapkan. Penulis berharap semoga karya ilmiah ini dapat bermanfaat bagi pembaca.
BAKTERI YANG BERASOSIASI DENGAN SPONS
Jaspis
sp. :
ANALISIS PENGHASIL SENYAWA ANTIMIKROB DAN
KERAGAMAN GENETIKNYA
HERMAWATY ABUBAKAR
SEKOLAH PASCASARJANA
INSTITUT PERTANIAN BOGOR
Dengan ini saya menyatakan bahwa tesis Bakteri yang Berasosiasi dengan Spons Jaspis sp.: Analisis Penghasil Senyawa Antimikrob dan Keragaman Genetiknya adalah karya saya dengan arahan dari komisi pembimbing dan belum diajukan dalam bentuk apa pun kepada perguruan tinggi mana pun. Sumber informasi yang berasal atau dikutip dari karya yang diterbitkan maupun tidak diterbitkan dari penulis lain telah disebutkan dalam teks dan dicantumkan dalam Daftar Pustaka di bagian akhir tesis ini.
Bogor, Juli 2009
ABSTRACT
HERMAWATY ABUBAKAR. Spons (Jaspis sp.) – Associated Bacteria: Antimicrobial Production and Genetic Diversity Analyses. Under Direction of Aris Tri Wahyudi and Munti Yuhana.
ABSTRACT
Living benthic marine organisms such as sponges are frequently assosiated with bacteria which may produce useful antimicrobial compounds. Genetic diversity of bacteria isolated from marine spongeJaspissp. which has capability in producing antibacterial subtances was investigated. As many as 32 isolates (45,71%) and 20 (29,41%) isolates originating from mesohyl and sponge surface respectively, showed the antibacterial activity againstStaphylococcus aureus, Vibrio harveyi, Escherichia coli, Pseudomonas aeruginosa, Enterophatogenic Escherichia coli (EPEC K-11),
Candida albicans, and C. tropicalis. Thirty most potential isolates were further studied by amplified ribosomal DNA restriction analysis (ARDRA) to asses their genetic diversity. Restriction analysis using enzymes RsaI, HaeIII, and HinfI of the 16S rRNA genes resulted seven phylotipes. The 16S rRNA gene sequence of choosen isolates i.e. SAB E-8, SAB E-33, SAB E-35, SAB E-38, SAB E-40 and SAB S-43 that showed inhibition of the growth for all microorganism target were identified. The use of a few phenotypic tests for those isolate can be applied to differentiate them. Gram staining technique was used to distinguish Gram negative from Gram positive ones. Isolates designed as SAB E-8, SAB E-35, and SAB E-40 were identified as Gram negative, whereas SAB E-33, SAB E-38, and SAB S-43 were Gram positive. For Gram positive isolates, further test were performed including spora staining and catalase test forBacillusidentification. Based on their 16S rRNA gene sequences, there were 3 isolates closely related to Pseudomonas sp. while the remaining 3 isolates were members ofBacillusgroup.
Analisis Penghasil Senyawa Antimikrob dan Keragaman Genetiknya. Dibimbing oleh Aris Tri Wahyudi dan Munti Yuhana.
Spons merupakan salah satu komponen biota penyusun terumbu karang yang mempunyai potensi bioaktif yang belum banyak dimanfaatkan. Hewan laut ini mengandung senyawa aktif yang persentase keaktifannya lebih besar dibandingkan dengan senyawa-senyawa yang dihasilkan oleh tumbuhan darat. Spons umumnya dapat bertahan hidup di perairan laut yang miskin nutrisi karena adanya assosiasi dengan organisme lain khususnya bakteri.
Bakteri banyak ditemukan secara komensal di permukaan dan bagian mesohyl spons. Pola makan spons yang khas yaitu filter feeder (menghisap dan menyaring) dapat memanfaatkan jasad renik disekitarnya sebagai sumber nutrien, diantaranya bakteri yang hidup pada perairan tersebut. Namun seringkali bakteri juga dijumpai hidup dan berkolonisasi dengan memanfaatkan nutrien yang terdapat pada spons tersebut.
Produk alami laut sebagai hasil metabolik sekunder kemungkinan dihasilkan oleh kehadiran mikroorganisme pada jaringan spons sebagai simbion, baik simbion intraselluler ataupun ekstraselluler. Senyawa-senyawa organik tersebut dapat ditransport karena adanya kerjasama antara simbion dan inangnya. Kehadiran kedua pasangan simbion ini juga menjadi syarat untuk menghasilkan metabolik sekunder seperti senyawa bioaktif yang bersifat antimikrob. Penelitian ini bertujuan untuk mengisolasi dan mengkarakterisasi bakteri (endosimbion dan ektosimbion) penghasil senyawa antimikrob dan menganalisis keragaman genetiknya berdasarkan amplified ribosomal DNA restriction analysis(ARDRA) dan sekuensing gen 16S rRNA.
Metode untuk mengisolasi bakteri simbion yang diduga memiliki potensi antimikrob dibagi atas dua metode yaitu untuk mengisolasi bakteri dari permukaan dan bagian mesohylJaspis sp. Total jumlah bakteri hasil isolasi dari permukaan dan mesohyl diuji kemampuan antimikrobnya dengan menggunakan bakteri target
Escherichia coli, EPEC K-11, Vibrio harveyi, Pseudomonas aeruginosa, Staphylococcus aureus dan dua jenis khamir yaitu Candida albicans dan C. tropicalis. Bakteri yang memiliki aktivitas antimikrob dianalisis keragaman genetiknya dengan Amplified ribosomal DNA restriction analysis (ARDRA) serta didentifikasi dengan pewarnaan Gram, uji parsial dan sekuensing gen 16S rRNA.
berasosiasi dengan cara vertikal transmisi. Isolat bakteri yang berasal dari permukaan dan memiliki aktivitas antimikrob diduga adalah bakteri yang memiliki kemampuan untuk melindungi spons dari patogen, predator danbiofouler.
Meskipun jumlah isolat bakteri yang berasal dari permukaan hampir sama dengan isolat endofit, namun aktivitas antimikrob isolat permukaan lebih rendah dibandingkan isolat endofit. Berdasarkan jumlah isolat yang mempunyai aktivitas antimikrob dan jumlah mikrob target yang dapat dihambat pertumbuhannya, isolat yang berasal dari bagian endofit spons Jaspis sp. lebih banyak dibandingkan isolat yang diisolasi dari permukaan. Bakteri simbion yang berasal dari bagian endofit yaitu mesohyl umumnya memiliki populasi yang berlimpah dan merupakan mikroba spesifik dari spons inangnya. Bakteri simbion yang berasal dari permukaan spons merupakan bakteri yang tidak spesifik dengan inangnya dan memiliki kemiripan dengan komunitas mikrob yang berada di lingkungan perairan dimana spons tersebut berada.
Hasil skrening terhadap semua isolat bakteri yang berasal dari endofit dan permukaan menunjukkan ada enam isolat bakteri yang mampu menghambat pertumbuhan semua mikrob target. Enam isolat tersebut terdiri dari lima isolat endofit yaitu SAB E-8, SAB E-33, SAB E-35, SAB E-38, dan SAB E-40 serta satu isolat permukaan yaitu SAB S-43. Berdasarkan hasil uji antagonis terhadapC. albicans dan
C. tropicalis,hanya isolat SAB E-33, SAB E-38 dan SAB E-40 yang memperlihatkan aktivitas antagonis yang baik. Kemampuan isolat bakteri yang berasosiasi dengan sponsJaspissp. dalam menghambat pertumbuhan mikroba target, merupakan bentuk aktivitas antagonis yang diduga dilakukan dengan menghasilkan kandungan senyawa yang bersifat antimikrobial. Biosintesis senyawa antimikrobial berperan penting dalam proses pelekatan, kolonisasi target hingga kompetisi dalam mendapatkan ruang dan nutrisi dengan mikroba lainnya.
Keragaman genetik dilakukan pada 30 isolat yang memiliki aktivitas antimikrob dilakukan dengan ARDRA. Amplifikasi gen 16S rRNA terhadap 30 isolat yang memiliki aktivitas antimikrob dilakukan dengan menggunakan primer spesifik yaitu 63f dan 1387r. Hasil elektroforesis amplifikasi gen 16S rRNA menampakkan pita yang berukuran sekitar 1300 pb. Primer 63f dan 1387r yang digunakan merupakan primer untuk gen yang menyandikan gen 16S rRNA yang telah didesain untuk seluruh domain bakteri. Primer ini dapat digunakan pada kultur murni bakteri maupun sampel alami dimana gen 16S rRNAnya sulit untuk diamplifikasi. Hasil pemotongan gen 16S rRNA memperlihatkan pola pita gen 16S rRNA yang beragam dengan jumlah 2-4 pita.
pewarnaan Gram dari ke enam isolat terbaik. Isolat SAB 8, SAB 35 dan SAB E-40 dari hasil pewarnaan Gram merupakan bakteri Gram negatif. Bakteri Gram positif yaitu isolat SAB E-33, SAB E-38 dan SAB S-43. Uji fisiologis tambahan untuk bakteri Gram positif diarahkan ke kelompok Bacillus dengan melakukan uji parsial yang meliputi pewarnaan Gram, endospora dan katalase. Hasil uji parsial menunjukkan bahwa ketiga isolat tersebut adalah kelompokBacillus, dicirikan oleh sel yang berbentuk batang, pewarnaan Gram positif, terdapat endospora yang terletak pada bagian sentral dan uji katalase positif.
BlastN sekuen gen 16S rRNA enam isolat dengan aktivitas mikrob terbaik, terbagi menjadi dua kelompok filogenetik yang berbeda yaitu genus Pseudomonas
(50%) dan Bacillus (50%). Isolat SAB E-8, SAB E-35, dan SAB E-40 termasuk dalam kelompokPseudomonaskarena ketiga isolat tersebut masing-masing homolog dengan Pseudomonas sp. HN-07, Pseudomonas sp. LPK2 dan Pseudomonas
sp.LD116, dengan tingkat identitas maksimum 97% - 98. Tingkat identitas maksimum 98% - 99% diperoleh dari tingkat homologi isolat SAB E-33, SAB E-38, dan SAB S-43 dengan isolat yang terdapat dalam Gen Bank, yaitu masing-masing
Bacillussp. strain K3,Bacillus pumilusstrain 210-50, danBacillussp.E287.
Pohon filogenetik yang menggunakan data sekuen parsial gen 16S rRNA isolat dengan aktivitas antimikrob terbaik dan beberapa galur acuan (reference strains) menunjukkan adanya kedekatan hubungan kekerabatan. Pohon filogenetik menunjukkan SAB-35 berdekatan secara evolusi dengan Pseudomonas sp. J451 dengan nilai boostrap 56%. Pohon filogenetik menunjukkan SABS-43 dan SABE-33 memiliki kedekatan kekerabatan dengan Bacillus sp. EGU72 sedangkan SAB E-38 denganBacillussp. D203.
© Hak Cipta milik IPB, tahun 2009 Hak Cipta dilindungi Undang-Undang
Dilarang mengutip sebagian atau seluruh karya tulis ini tanpa mencantumkan atau menyebutkan sumbernya. Pengutipan hanya untuk kepentingan pendidikan, penelitian, penulisan karya ilmiah, penyusunan laporan, penulisan kritik, atau tinjauan suatu masalah; dan pengutipan tersebut tidak merugikan kepentingan yang wajar IPB
KERAGAMAN GENETIKNYA
HERMAWATY ABUBAKAR
Tesis
Sebagai salah satu syarat untuk memperoleh gelar Magister Sains pada Mayor Mikrobiologi
SEKOLAH PASCASARJANA
INSTITUT PERTANIAN BOGOR
Judul Penelitian : Bakteri yang Berasosiasi dengan Spons Jaspis sp.: Analisis Penghasil Senyawa Antimikrob dan Keragaman Genetiknya Nama Mahasiswa : Hermawaty Abubakar
NRP : G351070021
Disetujui, Komisi Pembimbing
Dr. Aris Tri Wahyudi, MSi Dr. Munti Yuhana, MSi
Ketua Anggota
Diketahui,
Koordinator Mayor Mikrobiologi An. Dekan Sekolah Pascasarjana Sekretaris Program S2
Dr.Ir. Gayuh Rahayu Dr.Ir. Naresworo Nugroho, M.Sc.
Puji syukur penulis panjatkan ke Hadirat Allah SWT karena atas segala rahmat dan karuniahNya sehingga karya ilmiah ini berhasil diselesaikan. Topik yang dipilih adalahBakteri yang Berasosiasi dengan Spons Jaspis sp.:Analisis Penghasil Senyawa Antimikrob dan Keragaman Genetiknya, yang dilaksanakan sejak bulan Oktober 2008 sampai Mei 2009.
Penulis menyampaikan penghargaan dan ucapan terima kasih yang sebesar-besarnya terutama kepada pembimbing, yaitu Dr. Aris Tri Wahyudi, Msi. dan Dr. Munti Yuhana, Msi. yang telah banyak memberikan bimbingan dan saran selama penulis menempuh S2. Terimakasih juga penulis sampaikan kepada Dr. Dinamella Wahjuningrum, MSi. selaku Penguji Luar Komisi yang telah memberikan koreksi dan arahan untuk perbaikan tesis.
Ungkapan terima kasih juga disampaikan kepada kedua orang tua, Ayahanda H. Abubakar Makkarumpa dan Ibunda Hj. Bunga Matahari, Suami dan kedua Anakku atas keikhlasan, doa dan kasih sayangnya. Tidak lupa kepada saudara dan sahabat khususnya Ari Susilowati, MSi., Rika I. Astuti, MSi., dan Syamsul Bahri, SSi, penulis mengucapkan banyak terima kasih atas bantuan saran, kritik dan kebersamaanya.
Penulis menyadari bahwa tulisan ini masih jauh dari sempurna, sehingga kritik dan saran sangat diharapkan. Penulis berharap semoga karya ilmiah ini dapat bermanfaat bagi pembaca.
RIWAYAT HIDUP
Penulis dilahirkan di Pinrang propinsi Sulawesi Selatan pada tanggal 5 Agustus 1978 dari pasangan H. Abubakar Makkarumpa dan Hj. Bunga Matahari. Penulis merupakan anak ke empat dari enam bersaudara.
Tahun 1996 penulis lulus dari SMU Muhammadiyah Pinrang dan pada tahun 1997 lulus seleksi masuk Universitas Hasanuddin Makasar pada jurusan Biologi melalui jalur UMPTN dan lulus tahun 2002. Kesempatan untuk melanjutkan ke program Magister Sains pada mayor Mikrobiologi FMIPA-IPB diperoleh pada tahun 2007. Beasiswa diperoleh dari BPPS Departemen Pendidikan Nasional.
DAFTAR TABEL ... xiii DAFTAR GAMBAR ... xiv DAFTAR LAMPIRAN ... xv PENDAHULUAN ... 1 Latar Belakang ... 1 Tujuan ... 3 TINJAUAN PUSTAKA ... 4 Tinjauan Umum Spons ... 4 Asosiasi Spons dengan Bakteri ... 5 Potensi Senyawa Bioaktif dari Assosiasi Bakteri dengan Spons ... 7 Senyawa Antimikrob ... 9
DAFTAR TABEL
Halaman
1 Aktivitas antibakteri dan antikhamir isolat-isolat bakteri endofit asal sponsJaspissp. ... 21 2 Aktivitas antibakteri dan antikhamir isolat-isolat bakteri permukaan
asal sponsJaspissp. ... 23 3 Ukuran fragmen DNA gen 16S rRNA yang dipotong dengan beberapa
enzim restriksi ………... 32
Halaman
1 Tahapan-tahapan yang dilakukan dalam penelitian ini ... 13 2 Penampilan spons Jaspis sp., asal perairan sebelah barat Pulau
Waigeo, Raja Ampat Papua Barat ... 14 3 Penampilan koloni bakteri ektosimbion hasil isolasi dari spons Jaspis
sp pada Medium SWC, setelah diinkubasi selama 24 jam pada suhu 27oC ...
20
4 Penampilan koloni bakteri endosimbion hasil isolasi dari sponsJaspis
sp pada Medium SWC, setelah diinkubasi selama 24 jam pada suhu 27oC ...
20
5 Senyawa Antibakteri yang dihasilkan (terlihat dari zona bening yang terbentuk) dari beberapa isolat bakteri endofit asal spons Jaspis sp. terhadap pertumbuhan bakteri a.S. aureus, b.V. harveyii, c.E. coli, d. EPEC-K11, e.P. aeruginosadan f. S. aureus……….
22
6 Senyawa Antikhamir yang dihasilkan (terlihat dari zona bening yang terbentuk) dari isolat bakteri endofit asal sponsJaspissp. SAB E-35 dan SAB E-38 terhadap pertumbuhan khamir a.C. albicansdan b.C.
tropicalis..……….
22
7 Senyawa Antibakteri yang dihasilkan (terlihat dari zona bening yang terbentuk) dari beberapa bakteri permukaan asal spons Jaspis sp. terhadap pertumbuhan a. S. aureus, b. V. harveyii dan c. P. Aeruginosa...
25
8 Profil koloni pada media SWC dan hasil pewarnaan bakteri Gram negatif isolat SAB E-35 …………...
25 9 Uji parsial genus Bacillus untuk isolat bakteri gram positif (SAB
S-43); Profil koloni pada media SWC; Pewarnaan Gram; Pewarnaan Spora ...………...
25
10 Amplifikasi gen 16S rRNA dari beberapa isolat yang memiliki aktivitas antimikrob terbaik, M: standar ukuran molekul DNA 1kb ladder ………...……….
27
11 Elektroforesis gel agarose gen 16S rRNA dari beberapa isolat bakteri asal spons Jaspis sp. yang mempunyai aktivitas antimikroba terbaik yang dipotong dengan Enzim RsaI (A),HaeIII (B) danHinfI (C). M: standar ukuran molekul DNA (1kb ladder) ...………
28
12 Profil gen 16S rRNA dari 30 isolat bakteri yang berasosiasi dengan sponsJaspissp. yang dipotong dengan enzim restriksiRsaI ………
29 13 Profil gen 16S rRNA dari 30 isolat bakteri yang berasosiasi dengan
sponsJaspissp. yang dipotong dengan enzim restriksiHaeIII ……… 30 14 Profil gen 16S rRNA dari 30 isolat bakteri yang berasosiasi dengan
sponsJaspissp. yang dipotong dengan enzim restriksiHinfI ………
15 Pohon filogenetik (internode rooted) hubungan kekerabatan antar isolat bakteri yang berasosiasi dengan spons Jaspis sp. dengan aktivitas antimikrob terbaik yang dianalisis dengan ARDRA dan dikonstruksi berdasarkan metodeNeighbor-Joining. Angka 10% pada bagian atas pohon menunjukkan skala persentase perbedaan (distance scale) antar profil isolat bakteri. Angka pada nodus adalah nilai bootstrap dengan 100 ulangan ...
33
16 Pohon filogenetik berdasarkan hasil sekuensing gen 16S rRNA enam isolat bakteri dengan aktivitas antimikrob terbaik asal sponsJaspissp.
Halaman
PENDAHULUAN
Latar Belakang
Mikroorganisme laut merupakan sumber senyawa bioaktif baru yang banyak menjadi perhatian sekarang ini. Bakteri penghuni perairan laut yang miskin nutrisi banyak dijumpai hidup dengan cara berasosiasi dengan berbagai organisme laut bentik, seperti spons dan karang.
Spons merupakan biota laut yang tersebar pada daerah perairan pantai yang dangkal hingga kedalaman 5,5 km. Tubuh hewan ini terdiri dari jaringan rangka yang disebut spikula. Spikula tersebut mengandung senyawa kimia yaitu kalsium karbonat, silika, serat kolagen dan serat spongin yang lentur (Castro & Huber 2005). Spons adalah hewan berpori yang termasuk filter feeder yaitu hewan yang mengumpulkan nutriennya dengan cara menyaring air laut melalui pori-pori (ostium). Makanan porifera berupa sisa organisme yang telah mati atau mikroorganisme yang berada di kolom air. Menurut Tayloret al.(2007), selain dijadikan sumber protein sel tunggal, mikroorganisme juga sebagai simbion dari spons karena mikroorganisme mengkolonisasi tubuh sponge yang berpori-pori sebagai tempat hidup dan berlindung. Hal ini dapat dijumpai sebagai asosiasi antara spons dengan bakteri. Bakteri dapat memberikan kontribusi untuk pertahanan inangnya dengan eksresi antibiotik dan substansi bioaktif lainnya. Secara khusus organisme laut yang sesil seperti spons diperkirakan sangat bergantung pada mekanisme pertahanan simbionnya, yaitu dengan menghasilkan senyawa bioaktif untuk mempertahankan diri terhadap hewan-hewan predator dan dari kolonisasi dari mikroorganisme patogenik.
Jenis senyawa metabolit sekunder yang berhasil diisolasi dari bakteri yang bersimbiosis dengan spons memperlihatkan kuantitas yang lebih banyak dari mikroorganisme laut lainnya. Hal ini terutama dikarenakan kemudahan dalam kultur massalnya. Jenis senyawa metabolit sekunder dari bakteri yang bersimbiosis dengan spons sangat bervariasi yaitu dari golongan terpenoid, alkaloid, polyketida, peptida siklik, derivat dari asam lemak dengan berat molekul kecil, heterosklik, hingga
brominated pyrroles,(Tayloret al.2007).
Vibrio spp. yang berasosiasi dengan spons Dysidea sp menunjukkan adanya sintesis cytotoksik dan antibakteri tetrabromodiphenyl eter demikian pula pada asosiasi antara Micrococcus dengan Tedania ignis ditemukan adanya aktifitas antimikroba (Kanagasabhapathy et al. 2005). Hasil penelitian Kim et al. (2006); Montalvo et.al 2005; Zhang et al. (2006), Actinomyetes yang bersimbiosis dengan spons Pseudoceratina clavalata, Xestospongia spp., Hymeniacidon perlevis dan Craniella australiensisjuga menunjukkan adanya aktifitas antimikrobial.
3
menganalisis komunitas bakteri pada berbagai lingkungan, termasuk spons sebagai simbion dari berbagai bakteri laut.
Tujuan Penelitian
Tinjauan Umum Spons
Spons (filum Porifera) adalah hewan multisellular (Metazoa) yang paling
tua dan mempunyai struktur yang sangat sederhana. Susunan pada struktur spons
tidak sama dengan filum yang lainnya, morfologi spons sangat mempengaruhi
aspek biologi spons itu sendiri termasuk interaksinya dengan mikroorganisme
(Simpson 1984).
Susunan sel-sel spons berbeda pada setiap lapisan strukturnya. Pada
permukaan paling luar, atau yang biasa disebut dengan pinacoderm, dibentuk oleh
sel-sel epitel yang disebut sebagai pinacocyte. Pori-pori (ostia) pada permukaan
luar merupakan saluran yang menembus sampai pada bagian kanal interior.
Bagian dalam spons, terdapat sebuah sel-sel berflagella (choanocyte) yang berasal
dari sebuah ruang yang disusun oleh choanoderm dimana makanan disimpan.
Flagel dari choanocyte akan bergerak untuk memompa air yang akan masuk
melalui ostia, choanosyte juga akan menyaring keluar partikel-partikel makanan
(termasuk bakteri dan mikroalga) dari air dan akan ditransfer ke mesohyl yang
merupakan perluasan lapisan yang berhubungan dengan jaringan. Di dalam
mesohyl partikel makanan akan dicerna dengan phagositosis oleh sel-sel spons
lainnya yang disebut archaeosyte. Sel-sel totipotensi yang dapat berdiferensiasi
menjadi tipe sel spons yang baru juga berada pada mesohyl yang padat dengan
komunitas mikroorganisme. Setiapkali choanocyte menyaring air yang masuk,
maka air juga akan dikeluarkan dari spons melalui osculum, diperkirakan lebih
dari 24.000 liter air yang dipompakan oleh 1 kg spons perhari (Castro & Huber
2005).
Pertumbuhan spons juga memiliki tipe yang bermacam-macam dengan
warna-warna yang menarik, seperti tipe encrusting, bercabang, cup dan massive
dengan ukuran yang hanya beberapa millimeter hingga yang memiliki diameter
lebih dari satu meter. Konstruksi struktur spons dibentuk oleh silika dan spikula
kalkareus, komponen ini seringkali dibuat sebagai bahan dalam penyusunan
5
memengang peranan dalam menyokong struktur pada spons (Castro & Huber
2005).
Spons yang berwarna orange cerah yaitu Jaspis johnstoni adalah spons
dengan struktur yang rapuh, lembut dan padat. Spons ini dapat dijumpai pada
permukaan karang sehingga dengan mudah dapat dikonsumsi oleh predator.
Spons ini mempunyai kandungan senyawa bioaktif yang dapat membunuh
predator, hasil penelitian Vanderloos (1997) mengidentifikasi senyawa tersebut
adalah Jasplakinolide yang dapat menghambat pertumbuhan sel-sel kanker.
Asosiasi Spons dengan Bakteri
Interaksi antara spons dan bakteri terjadi dalam banyak bentuk. Untuk
spons, mikroba yang berbeda dapat diartikan sebagai sumber makanan,
patogen/parasit atau sebagai simbion mutualisme. Bakteri yang berasosiasi
dengan spons dapat mencapai 40% dari jaringan spons dengan kepadatan 109sel bakteri per ml jaringan spons (Hofman et al. 2005). Berdasarkan sekuen 16S
rRNA dan Denaturing Gradient Gel Electrophoresis (DGGE) hasil sensus oleh
Taylor et al. (2007), bakteri yang berassosiasi dengan spons antara lain adalah
Acidobacteria, Actinobacteria, Bacteroides, Chloroflexi, Cyanobacteria,
Deinococcus-Thermus, Firmicutes, Gemmatimonadetes, Nitrospira,
Planctomycetes, Poribacteria, Proteobacteria, Sphirochaetes dan
Verrucomicrobia.
Sangat jelas keuntungan yang diperoleh spons dari sistem metabolisme
simbionnya yaitu bakteri dan mikroba lainnya. Fotosintesis dan fiksasi nitrogen
yang dilakukan oleh cyanobakteri kiranya merupakan faktor kunci mengapa
spons dapat bertahan dalam kondisi lingkungan peraiaran yang miskin nutrisi
(Ariilo et al. 1993). Seperti yang diungkapkan oleh Hoffman et al.(2006), yang
menjelaskan bahwa bakteri anaerobik dapat mentransfer asam karboksilat pada
spons Geodia baretti. Bakteri metanotropik dapat mensuplemen nutrisi pada
spons tanpa proses filter feeding dalam habitat laut yang kaya akan metan
(Faceletet al.1995). Namun, mikroba simbion dapat pula dikonsumsi oleh spons,
ini dilaporkan pertamakali pada awal 1970-an, bahwa simbion cyanobakteri
ditemukan pada bagian intra dan ekstraseluler dari spons Synecoccus spp.
tertentu dari spons Ircinia virabilis asal Mediterania, yang merupakan sebuah
sumber fotosintesis dan pemfiksasi karbon bagi spons (Yahel et al. 2006).
Bentuk asosiasi mikroba juga memberikan kontribusi dalam siklus nutrisi
bagi kebutuhan spons inangnya. Sumber nutrisi spons berupa mikroalga dan
zooplankton terdiri atas berbagai komponen makrokolekul. Mikroalga yang kaya
akan karbon dan nitrogen serta zooplankton yang sebagian struktur tubuhnya
terdiri atas kitin dapat dengan mudah dipecah oleh bakteri-bakteri pengahsil
enzim protease dan kitinase sehingga menjadi molekul yang lebih kecil (Reiswig
1975). Keuntungan lain yang diperoleh oleh spons dari simbionnya yaitu bakteri
adalah penambahan struktur yang lebih kaku akibat produksi mukus yang
dihasilkan oleh mikroba. Dalam beberapa kasus senyawa-senyawa yang
dihasilkan oleh mikroba simbion potensial digunakan sebagai prekusor untuk
metabolisme biosintesis pertahanan spons dari patogen dan predator lainnya.
Penelitian tentang interaksi antara spons dan mikroorganisme,
menunjukkan bahwa suatu mikroorganisme akan berasosiasi pada spesies spons
tertentu. Hal ini telah dibuktikan melalui pengamatan dengan mikroskop maupun
analisa genetik dan studi kultur yang bertujuan untuk isolasi antibiotik dari bakteri
yang berasosiasi dengan spons yang berbeda-beda. Suberitas domuncula,
misalnya menunjukkan hanya sedikit bakteri yang tampak pada bagian permukaan
dalamnya, sementara spons Halichondria panicea dan Ircinia fascikulata
menunjukkan bakteri yang berlimpah dengan variasi yang bermacam-macam. Ini
dapat dilihat dengan mikroskop elektron yang juga menggambarkan tingginya
keanekaragaman isolat bakteri dari spons-spons ini (Imhoff & Stohr 2003).
Spesies spons yang berasosiasi dengan bakteri spesifik dapat ditunjukkan
dengan membandingkan komunitas bakteri yang berasosiasi dengan sampel yang
berbeda dari spons Mediteranian yaitu Chondrilla nucula dari laut Adriatic dan
laut Liguria. Sekuen DNA klon yang identik ditemukan dalam sampel spons dari
lokasi yang berbeda. Menariknya, spons Thetya aurantium menunjukkan dua
komunitas bakteri yang diperlihatkan dengan bentuk morfologi yang berbeda dari
bagian eksterior dan interior sel, yang dapat dilihat dengan mikroskopik dan
diperjelas dengan DGGE dan percobaan cloning gen 16S rRNA. Penemuan ini
7
adalah spesies khusus yang berasosiasi dengan kelompok porifera tersebut serta
mempunyai bentuk adaptasi sepanjang proses evolusi pada lingkungan dimana
spons berada (Imhoff & Stohr 2003).
Kesuksesan usaha dalam mengisolasi mikroorganisme penghasil senyawa
bioaktif yang bersimbiosis dengan spons tergantung oleh beberapa faktor. Faktor
yang paling signifikan yaitu bahwa mikroba dapat melakukan sistem metabolisme
yang berbeda-beda tergantung kondisi lingkungannya. Banyak penelitian yang
berhasil mengkultur bakteri yang berasal dari spons pada medium-medium yang
sebelumnya dicampur dengan ekstrak dari jaringan spons. Meskipun demikian,
bakteri yang dapat menghasilkan senyawa bioaktif yang diisolasi jumlahnya
cukup rendah yaitu berkisar 0,06; 0,1; 0,15 dan 0,7 % dari total bakteri yang
dapat dikultur dari spons Candidaspongia flabellata, Rhopaloides odorabile,
Aplysinaaerophoba(Burjaet al.1999; Thomset al.2003)
Kebutuhan nutrisi mikroba yang bersimbiosis dengan spons sangat susah
untuk dipenuhi bila dikultur dalam laboratorium. Bagaimanapun, ada beberapa
bakteri yang dapat diisolasi tetapi sudah tidak dapat memproduksi
senyawa-senyawa bioaktif lagi, kemungkinan bakteri-bakteri tersebut mengharuskan
adanya perantara sistem metabolisme dari spons sebagai inangnya. Adapula
beberapa isolat bakteri yang belum diketahui alasannya berhenti menghasilkan
produk-produk senyawa bioaktif setelah dikulturkan beberapa waktu pada media
buatan. Ini diduga karena adanya keterlibatan faktor genetik, dimana gen yang
menyandikan senyawa bioaktif tersebut hilang karena akibat mutasi atau
kehilangan penggerak elemen-elemen genetik yang mensintesis gen-gen tersebut
(Prokschet al. 2002).
Potensi Senyawa Bioaktif dari Assosiasi Bakteri dengan Spons
Spons dianggap sebagai organisme yang potensial karena lebih dari 200
senyawa metabolit baru yang ditemukan setiap tahun, dibandingkan dengan
organisme laut lainnya. Spons dianggap sebagai salah sumber substansi natural
yang paling penting seperti antibiotik, antitumor, aktivitas antiviral,
antiplasmodial, dan anti-inflammatory. Ini membuat spons sebagai sumber
hal ini tidak bisa membuktikan apakah sel-sel spons atau bakteri yang berasosiasi
memproduksi substansi senyawa bioaktif (Bluntet al.2006).
Meskipun awalnya penemuan senyawa bioaktif banyak ditemukan sebagai
hasil ekstraksi dari jaringan spons tetapi arah penelitian sekarang ini lebih banyak
dieksplorasi pada mikroorganisme yang bersimbiosis dengan spons. Hal tersebut
lebih menguntungkan dibandingkan dengan mengisolasi dari inangnya (spons).
Menurut Westet al.(2002), senyawa makrosiklik lactone yaitu Peluruside A yang
diisolasi dari demosphongia Mycale hentscheli di perairan New Zaeland
menunjukkan potensi sebagai antikanker dan untuk mendapatkan 2 gram
Peluruside A murni dibutuhkan 200 kg ekstrak spons, hal ini tentu saja dapat
menghabiskan kekayaan laut bumi ini.
Kenyataanya, banyak kasus yang dapat menunjukkan bahwa bakteri yang
berasosiasi yang memproduksi kandungan senyawa bioaktif dan bukan inangnya.
Chondramide D yang dihasilkan oleh deltaproteobacterium Chondromyces
crocatus memperlihatkan rumus struktur yang sama dengan senyawa Jaspamide
yang berasal dari ekstrak sponsJaspis sp.(Tayloret al.2007).
Spons yang bersimbiosis dengan Actinomycetes dari genus
Micromonospora menghasilkan Manzamine yaitu alkaloid yang berpotensi
sebagai antimalaria. Manzamine pertama diisolasi dari mikroba yang berasal dari
spons yang tidak hanya berbeda spesies, tetapi juga secara geografis berbeda.
Namun perkembangan sekarang, manzamine yang dihasilkan tidak selalu
bergantung pada komunitas atau jenis mikrobanya. Manzamine yang diisolasi di
Indonesia dihasilkan oleh bakteri yang bersimbiosis dengan spons 01IND 35 dan
01IND 52 (Naglaa et al. 2004).
Spons Hyatella sp. yang bersimbiosis dengan Vibrio sp. menghasilkan
senyawa peptida yang bersifat antibakterial, sementara itu glycoglycerolipid
dihasilkan oleh Halichondria panicea yang bersimbiosis denganMicrobacterium
sp. yang berpotensi sebagai anti tumor (Miyashiro & Ikegami 1994; Wickeet al.
2000). Menurut Mitova et al. (2003), sebuah senyawa baru yaitu
Cyclotetrapeptida dan dihasilkan oleh bakteri Pseudomonas sp. (IM1) yang
diisolasi dari sebuah spesimen spons Ircinia muscarum dari teluk Naples (Italia).
9
(KS) strain Salinispora sp. (actinobacteria) diindikasikan memiliki sekuen gen
polyketide synthase (PKS) yang sama dengan Amycolatopsis mediterranei
penghasil Rifamycin B. Strains Salinispora diisolasi dari spons laut
Pseudoceratina clavata. Pada penelitian lainnya, beberapa golongan Quinolon
memiliki aktivitas antimikrobial dan cytotoksin dari Pseudomonas asosiasi
dengan Homophinia sp. yang berasal dari lautan pasifik (Burja et al. 1999).
Asosiasi antara sponsAplysina aerophoba dan A. cavernicola yang berada di laut
Mediterania dengan 27 isolat bakteri yang belum teridentifikasi, menunjukkan
bahwa beberapa isolat tersebut berpotensi untuk menghambat pertumbuhan
bakteri-bakteri klinikal yang multiresisten seperti, Staphylococcus aureus dan S.
epidermidis(Hentschelet al.2001).
Arah penelitian yang semakin dikembangkan yaitu berfokus pada produksi
substansi antibiotik dari bakteri yang bersimbiosis dengan spons. Bagaimanapun
penambahan bakteri resisten menyebabkan beberapa masalah dalam dunia
kedokteran dan menguatkan penelitian-penelitian baru untuk mencari kandungan
senyawa aktif melawan patogen multiresisten.
Senyawa Antimikrob
Senyawa antimikroba adalah senyawa yang dihasilkan oleh fungi dan
bakteri yang dapat menghambat atau membunuh mikroorganisme lain.
Kebanyakan senyawa antimikroba yang telah dipergunakan secara luas dikenal
dengan nama antibiotik. Target penting dari antibiotik bakteri adalah ribosom
(translasi), dinding sel, membran sitoplasma, proses repilikasi DNA dan
transkripsi (Madiganet al.2006).
Antibiotik yang menghambat sintesis protein pada tahap inisiasi adalah
streptomycin sedangkan puromycin, chloramphenicol, cyckloheximide dan
tetracyclin pada tahap elongasi. Antibiotik yang berperan pada transkripsi antara
lain rifampin dan streptovaricin yang menghambat sintesis RNA yaitu dengan
berikatan dengan sub unit β dari RNA polimerase, sedangkan aktinomycin
menghambat sintesis RNA dengan menghentikan proses elongasi RNA.
Antibiotik β-lactam seperti penicillin dan cephalosporin berpotensi untuk
menghambat sintesis dinding sel salah satunya dengan menghasilkan penicillin
Amplified Ribosomal DNA Restriction Analysis(ARDRA)
Salah satu alternatif untuk mengetahui komposisi komunitas suatu
lingkungan yaitu dengan mengembangkan teknik biologi molekular. Teknik ini
mencakup penentuan variasi pola pita gen 16S rRNA setelah dipotong dengan
beberapa enzim restriksi yang dapat dianalisis pada komunitas prokariot yang
dijumpai pada habitat tertentu. Gen 16S rRNA adalah bagian dari DNA prokariot
yang dapat ditemukan pada bakteri dan archaea. Gen ini mengkodekan rRNA,
dimana rRNA merupakan bagian pembentuk dari ribosom. Huruf ”r” pada rRNA
merujuk pada kata ribosomal, sedangkan struktur ribosom terdiri dari dua unit
yaitularge subunit (LSU) dansmall subunit(SSU). Pada bakteri SSU dikodekan
oleh gen 16S rRNA sedangakn LSU dikodekan oleh gen gen 5S rRNA dan 23S
rRNA (Snyder & Wendy 2002).
Gen 16S rRNA merupakan gen yang sangat stabil, karena susah temutasi
meskipun dalam jangka waktu yang lama. Gen 16S RNA mengandung informasi
yang dapat dijadikan sebagai biomarker terhadap suatu bakteri. Gen 16S rRNA
terdiri dari daerah konservatif yang dapat dijumpai pada semua organisme dan
daerah hypervariabel yang unik pada setiap organisme atau organisme yang
memiliki hubungan kekerabatan yang dekat yang dapat digunakan untuk
identifikasi (Moyeret al.1994).
Analisis filogeni dari komunitas mikroba yang menggunakan Amplified
Ribosomal DNA Restriction Analysis (ARDRA) merupakan sebuah metode
sederhana yang didasarkan pada adanya polimorfisme panjang fragmen gen 16S
rRNA setelah dipotong dengan enzim restriksi. Istilah polimorfisme adalah hasil
pemotongan gen 16S rRNA dari bakteri asal yang berbeda akan memberikan pola
fragmen yang berbeda. Panjang fragmen ditentukan melalui proses elektroforesis
gel agarose dengan penanda ukuran DNA (DNA marker) sebagai pembanding
(Yogiara 2004). Sama halnya hibridisasi dan pelacakan DNA, ARDRA digunakan
untuk menganalisis komunitas bakteri pada berbagai lingkungan. Meskipun
ARDRA hanya memberikan sedikit atau sama sekali tidak ada informasi
mengenai tipe mikroorganisme yang terdapat dalam suatu sampel, namun hasilnya
11
membandingkan suatu komunitas mikroorganisme pada kondisi lingkungan yang
berbeda.
Pada penelitian Moyer et al. (1994) analisis 16S rRNA menggunakan
kombinasi enzim restriksi tetramerik (situs pengenalan 4 basa DNA) untuk
menghasilkan suatu pola pita DNA yang emadai sebagai satuan operasional
taksonomi (operational taxonomic unit/OTU). Masing-masing OTU akan menjadi
ciri dari kelompok 16S rRNA asal bakteri yang hidup dalam komunitas tertentu.
Penggunaan enzim restriksi HhaI (isochizomer dengan Hinp1 I),RsaI dan BstUI
sebagai enzim yang digunakan dalam studi keragaman mikrob menggunakan
ARDRA, karena enzim tersebut dapat menghasilkan pola pita DNA yang relatif
Waktu dan Tempat
Penelitian ini dilakukan di Laboratorium Mikrobiologi, Departemen Biologi,
FMIPA-Institut Pertanian Bogor, yang dimulai bulan Oktober 2008 sampai bulan
Mei 2009.
Bahan
Bahan yang digunakan dalam penelitian ini adalah sampel spons Jaspis sp
yang diambil dari perairan sebelah barat pulau Waigeo, Kabupaten Raja Ampat,
Papua Barat. Bakteri uji yang digunakan untuk uji produksi senyawa antibakteri
terdiri dari bakteri Gram negatif yaitu Escherichia coli (koleksi laboratorium
Mikrobiologi, departemen Biologi IPB), EPEC (Enteropathogenic Escherichia
coli) K-11 (koleksi Dr.dr. Sri Budiarti – Departemen Biologi IPB),Vibrio harveyi
patogen udang (koleksi Dr. Widanarni – Departemen Budidaya Perikanan IPB),
Pseudomonas aeruginosa patogen manusia (koleksi laboratorium Bioteknologi
PAU) serta bakteri Gram positif yaitu Staphylococcus aureus patogen manusia
(koleksi laboratorium Bioteknologi PAU), Bacillus subtilis dan Staphylococcus
aureus (koleksi laboratorium Mikrobiologi, Departemen Biologi IPB). Pengujian
antikhamir menggunakan Candida albicans dan C. tropicalis patogen manusia
(koleksi Laboratorium Mikrobiologi dan Parasitologi, Fakultas Kedokteran
Universitas Indonesia)
Metode Penelitian
Metode ini meliputi pengambilan sampel, lalu dilanjutkan dengan isolasi
bakteri yang berpotensi menghasilkan senyawa antimikrob yang berasal dari
permukaan dan mesohyl spons Jaspis sp. Penapisan isolat bakteri yang
menghasilkan senyawa antimikrob, yang dilakukan terhadap organisme prokariot
(bakteri) dan Eukariotik (khamir). Untuk keragaman genetik isolat bakteri yang
memiliki aktivitas antimikrob dilakukan dengan Amplified ribosomal DNA
restriction analysis (ARDRA) dan dilanjutkan dengan uji fisiologis (pewarnaan
Gram dan uji parsial) serta sekuensing gen 16S rRNA untuk identifikasi isolat
13
Gambar 1. Tahapan-tahapan yang dilakukan dalam penelitian ini. Pengambilan Sampel
sponsJaspissp.
Isolasi Bakteri dari Sampel Spons
Penapisan Isolat Bakteri Penghasil Senyawa Bioaktif
Pengujian Aktivitas Antibakteri
Pengujian Aktivitas Antikamir
Uji fisiologis (Pewarnaan Gram dan Uji Parsial)
Amplified rDNA Restriction Analysis (ARDRA)
Pengambilan Sampel
Sampel spons diambil dari perairan sebelah barat pulau Waigeo, Kabupaten
Raja Ampat, Papua Barat, pada kedalaman +10 meter dengan menggunakan alat
bantu snorkel dan masker. Pengambilan sampel ini dilakukan secara acak, yaitu
dengan menyusuri dasar laut. Sampel spons Jaspis sp. yang digunakan dalam
penelitian ini dapat dilihat pada Gambar 2. Sampel kemudian dimasukkan ke
dalam plastik sampel (Whirl-Pak, Nasco, USA) yang telah diisi dengan oksigen
murni, selanjutnya ditempatkan dalam cool box untuk dianalisis secara
mikrobiologis di laboratorium.
Gambar 2. Penampilan spons Jaspis sp., asal perairan sebelah barat Pulau Waigeo, Raja Ampat Papua Barat.
Isolasi Bakteri dari SampelSpons
Permukaan sampel spons dibilas dengan air laut steril, sehingga hanya
bakteri dengan daya simbiosis yang kuat saja yang akan tersampling (Amstronget
al.2001). Untuk isolasi bakteri pada bagian dalam jaringan spons diambil dengan
cara memisahkan bagian pinacoderm dengan bagian mesohyl. Bagian mesohyl
diambil dengan ukuran + 1 x 1 cm, digerus dan diencerkan dengan Phosphate
Buffer Saline (PBS) steril dengan perbandingan 1 : 1 (Kim et al 2006).
Selanjutnya dibuat suspensi dari pengenceran 10-1sampai 10-7. Pada pengenceran 10-5,10-6, dan 10-7dipipet 0,1 ml secara aseptik dan disebar ke dalam cawan petri yang telah berisi media Sea Water Complete (SWC), kemudian diinkubasi pada
15
tumbuh pada media tersebut. Untuk mengisolasi bakteri dari permukaan luar
menggunakan swab steril (Wahl et al. 1994). Swab steril diusapkan pada
permukaan luar spons, kemudian dicelupkan ke dalam botol pengenceran yang
berisi PBS steril dengan perbandingan 1 : 1. Selanjutnya, dari suspensi tersebut
dibuat pengenceran 10-1 sampai 10-7. Pada pengenceran 10-5, 10-6, dan 10-7dipipet 0,1 ml secara aseptik dan dimasukkan ke dalam cawan petri yang telah berisi
media SWC, kemudian diinkubasi pada suhu 26oC selama 24 - 36 jam dan diamati pertumbuhan koloni bakterinya. Setiap koloni bakteri yang tumbuh dipisahkan
berdasarkan warna dan bentuk koloni, serta dimurnikan dengan menggunakan
media yang sama.
Penapisan Bakteri Penghasil Senyawa Bioaktif (Antibakteri dan Antikhamir)
Pengujian Aktivitas Antibakteri. Metode ini dilakukan dengan teknik
bilayer yaitu, kultur cair bakteri uji yang telah diinkubasi selama 18 jam, diambil
sebanyak 1ml lalu dimasukkan ke dalam 100 ml media SWC steril. Campuran
antara kultur bakteri dan media SWC sebagai lapisan kedua dituangkan ke dalam
cawan petri yang telah berisi dengan media SWC yang telah padat (lapisan
pertama). Setelah padat, isolat bakteri yang telah murni digoreskan pada
permukaan media yang telah mengandung kultur bakteri uji, kemudian diinkubasi
selama 24 jam pada suhu 37oC. Senyawa bioaktif antibakteri yang dihasilkan diindikasikan dengan terbentuknya zona jernih disekitar koloni isolat murni.
Pengujian Aktivitas Antikhamir. Metode yang dilakukan sama dengan
pengujian antibakteri yaitu dengan teknik bilayer. Kultur cairCandida yang telah
diinkubasi selama 24 jam, diambil sebanyak 1ml lalu dimasukkan ke dalam 100
ml media PDA (Potato Dextrose Agar) steril. Campuran antara kultur khamir dan
media PDA sebagai lapisan kedua dituangkan ke dalam cawan petri yang telah
berisi dengan media PDA yang telah padat (lapisan pertama). Setelah padat, isolat
yang telah murni digoreskan pada permukaan media yang telah mengandung
kultur khamir, lalu diinkubasi selama 24 jam pada suhu 37oC. Senyawa bioaktif antibakteri yang dihasilkan diindikasikan dengan terbentuknya zona jernih
disekitar koloni isolat yang digoreskan murni maka dapat menghambat
Pewarnaan Gram dan Uji Parsial
Karakterisasi tambahan yang dilakukan pada isolat bakteri yang
menghasilkan senyawa bioaktif yaitu dengan pewarnaan Gram. Isolat yang
menghasilkan Gram positif dilanjutkan dengan identifikasi parsial yang merujuk
ke kelompokBacillusyaitu dengan pewarnaan spora dan uji katalase.
Analisis Molekuler Gen 16S rRNA
Isolasi Genom.30 Isolat bakteri yang menunjukkan kemampuan antibakteri
dan antikhamir masing-masing ditumbuhkan pada media SWC dan diinkubasi
shaker selama 24 jam, dengan komposisi media 5 gr/l bacto pepton, 1 gr/l yeast
extract dan 3 ml/l glycerol. Isolat bakteri yang telah ditumbuhkan pada media
SWC diambil sebanyak 1,5 ml dan disentrifugasi (18.000xg) selama 10 menit
untuk mendapatkan pelet bakteri. Pelet ini digunakan untuk mengekstraksi DNA
genom dengan metode standar (Sambrook & Russel 2001). Setelah disentrifugasi
supernatannya dibuang dan ditambahkan ke dalamnya buffer Tris-EDTA (TE)
sebanyak 250 μl, lalu disentrifugasi 8000 rpm selama 10 menit. Supernatannya
dibuang dan dilakukan resuspensi dengan TE sebanyak 2 kali. Ditambahkan
dengan 250 μl TE dan 5 μl lisozym, lalu tabung eppedorf dibolakbalik dan
diinkubasi selama 30 menit pada suhu 37oC. Larutan TE dan lisozym dibuang, kemudian diganti 500 μl SDS 10% dan 10 μl proteinase K lalu tabung
dibolakbalik dan diinkubasi selama 37oC selama 60 menit. Larutan SDS dan proteinase K diganti dengan 80 μl NaCl dan 100 μl CTAB 10% lalu diinkubasi
selama 20 menit pada suhu 65oC. Setelah inkubasi larutan sebelumnya diganti dengan 650 μl PCl lalu dikocok kuat dan disentrifugasi 14000 rpm selama 10
menit. Bagian atas atau fase aquosenya dipindahkan ke tabung ependorf baru lalu
ditambahkan 650 μl CI dan disentrifugasi 14000 rpm selama 10 menit. Larutan
sebelumnya diganti dengan etanol absolut 2X vol; Na asetat 3 M 0,1 vol lalu
diinkubasi frezeer selama semalam. Setelah diinkubasi semalam etanol 2X vol;
Na asetat 3 M 0,1 vol diganti dengan etanol 70% dingin sebanyak 1 ml lalu
disentrifuges 14000 rpm selama 15 menit. Supernatannya dibuang lalu pelet
dikering udarakan selama semalam. Setelah dikering udarakan selama semalam
17
Amplifikasi Gen 16S rRNA dengan PCR. Amplfikasi gen 16S rRNA
digunakan (PCR Perkin Elmer 2400), dengan menggunakan primer 63f
(5’-CAGGCCTAACACATGCAAGTC-3’) dan 1387r
(5’-GGGCGGWGTGTACAAGGC-3’) (Marchesi et al 1998) yang akan
memperbanyak fragmen pada target sekitar 1300 pb. Total volume reaksi yang
digunakan adalah 25 μl, terdiri atas 12,5 μl 2x GC Buffer,4 μl dNTPs,
masing-masing 1 μl primer 63f dan 1387r, 0,25 Taq polimerase, 4 μl DNA template dan
2,25μl aquabidest steril. Kondisi PCR pada pra denaturasi pada suhu 95oC selama 5 menit; untuk siklus 30, denaturasi pada suhu 95oC selama 30 detik, anneling pada suhu 54oC selama 30 detik, polimerisasi pada suhu 72oC selama 30 detik dan post PCR pada suhu 72oC selama 7 menit. Produk PCR dapat diketahui dengan elektroforesis pada gel agarose 10% (wt/vol) selama 45 menit pada 70V/cm
dengan TAE buffer 1X. Produk PCR selanjutnya dipurifikasi dengan
menggunakan kit purifikasi (Promega, USA) sesuai dengan instruksi pemakaian.
Amplified Ribosomal DNA Restriction Analysis (ARDRA). Setiap hasil
purifikasi produk PCR gen 16S rRNA dipotong dengan menggunakan empat
enzim restriksi yaitu RsaI, HaeIII,dan HinfI (Fermentas, Life Science). Volume
reaksi tiap-tiap enzim restriksi terdiri atas 5 μl amplicon (1.5 μg), 2 μl buffer
Tango 10X, 2 U/μl enzim restriksi, dan ddH2O hingga volume 20 μl, kemudian
diinkubasi selama 3 – 4 jam pada suhu 37oC. Inaktivasi enzim dilakukan dengan menginkubasi pada suhu 65oC selama 20 menit. Produk restriksi selanjutnya dielektroforesis dengan menggunakan gel agarose 1% (wt/vol) selama 45 menit
pada 70V/cm dalam buffer TAE 1X. fragmen-fragmen dari hasil pemotongan pita
gen 16S rRNA tiap-tiap isolat dibuat data biner dan dianalisis menggunakan
software Treecon pada windows ver1.3b (Van de Peer dan De Watcher 1994).
Sekuensing Gen 16S rRNA dan Analisis Filogenetik. Sekuensing gen 16S
rRNA dilakukan di PT Charoen Phokpand Indonesia, terhadap enam isolat terpilih
(SAB E-8, SAB E-33, SAB E-35, SAB E-38, SAB E-40 dan SAB S-43) dengan
menggunakan metode dideoksi Sanger. Analisis sekuen gen 16S rRNA dilakukan
Sekuen gen 16S rRNA disejajarkan dengan menggunakan program clustalW
HASIL DAN PEMBAHASAN
Hasil
Isolasi Bakteri dari Sampel Spons
Hasil isolasi diperoleh 138 isolat bakteri masing-masing 70 isolat bakteri
endofit dan 68 isolat bakteri permukaan, yang ditandai dengan warna dan bentuk
koloni yang berbeda-beda (Gambar 3 dan 4). Seluruh isolat tersebut dikumpulkan
lalu diamati warna dan morfologi koloninya. Profil koloni isolat endosimbion dan
ektosimbion dapat dilihat pada Lampiran 1 dan 2. Pemberian nama isolat
berdasarkan asal sampel dimana bakteri-bakteri tersebut diisolasi, SAB E-1 yang
berarti Sponge – Assosiated Bacteria Endofit-1 (nomor urut isolat) yaitu bakteri
yang diisolasi dari bagian endofit spons, serta SAB S-1 yang berarti Sponge –
Assosiated Bacteria Surfaces-1 (nomor urut isolat) yaitu bakteri yang diisolasi
dari bagian surfaces (permukaan) spons. Isolat-isolat bakteri endofit dan surface
hasil isolasi diduga memiliki aktivitas antimikrob, yang selanjutnya dilakukan uji
lanjut untuk mengetahui sifat antimikrobnya.
Penapisan Isolat Penghasil Senyawa Bioaktif (Antibakteri dan Antikhamir)
Penapisan ini dilakukan secara kualitatif dengan menggunakan dua
kelompok mikroorganisme unicelluler target yaitu bakteri (prokariotik) dan
khamir (eukariotik). Hasil penapisan menunjukkan beberapa isolat bakteri endofit
dapat menghambat pertumbuhan bakteri target dan khamir target sekaligus,
meskipun dengan kemampuan yang berbeda-beda. Isolat-isolat tersebut antara lain
isolat SAB 8, SAB 31, SAB 32, SAB 33, SAB 35, SAB 36, SAB
E-37, SAB E-38, SAB E-40, dan SAB E-41 (Tabel 1). Hasil uji aktivitas antibakteri
isolat-isolat tersebut baik terhadap pertumbuhan bakteri uji maupun pertumbuhan
khamir uji berupa zona bening yang terbentuk, masing-masing dapat dilihat pada
Gambar 5 dan 6.
Pengujian aktivitas antibakteri dan antikhamir yang dilakukan pada isolat
bakteri permukaan juga merupakan penapisan awal. Adanya aktivitas antibakteri
dan antikhamir ditandai dengan terbentuknya zona bening disekitar goresan isolat
bakteri permukaan. Hasil pengujian isolat bakteri permukaan dapat dilihat pada
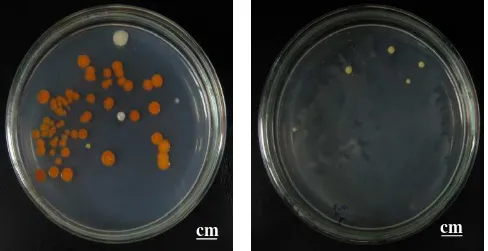
Gambar 3. Penampilan koloni bakteri ektosimbion hasil isolasi dari sponsJaspis
sp pada Medium SWC, setelah diinkubasi selama 24 jam pada suhu 27oC.
Gambar 4. Penampilan koloni bakteri endosimbion hasil isolasi dari sponsJaspis
sp pada Medium SWC, setelah diinkubasi selama 24 jam pada suhu 27oC.
cm cm
21
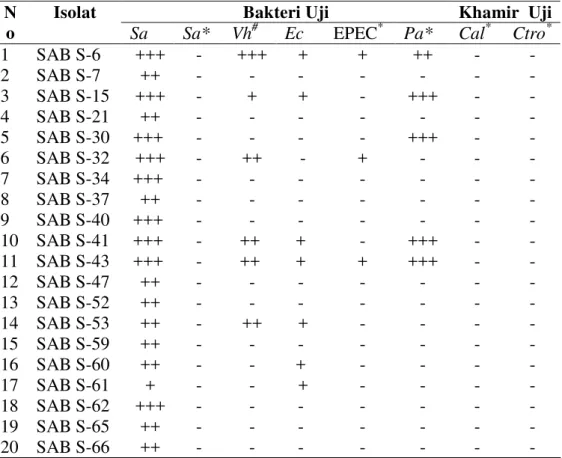
Tabel 1. Aktivitas antibakteri dan antikhamir isolat-isolat bakteri endofit asal sponsJaspissp.
Bakteri Uji Khamir Uji
N
Sa :Staphylococcus aureus; Sa* :Staphylococcus aureus; Vh#: Vibrio harveyii; Ec :Escherichia coli; EPEC* K-11 :Escherichia coli; Pa* :Pseudomonas aeruginosa; Cal* :Candida albicans;
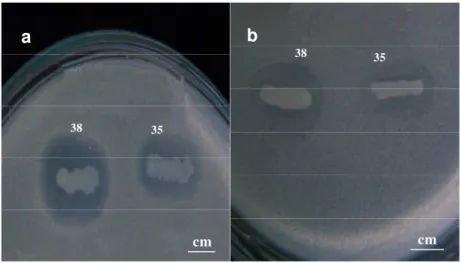
Gambar 5. Senyawa antibakteri yang dihasilkan (terlihat dari zona bening yang terbentuk) dari beberapa isolat bakteri endofit asal spons Jaspis sp. terhadap pertumbuhan bakteri a. S. aureus, b. V. harveyii, c.E. coli, d. EPEC-K11, e.P. aeruginosadan f. S. aureus.
Gambar 6. Senyawa antikhamir yang dihasilkan (terlihat dari zona bening yang terbentuk) dari isolat bakteri endofit asal sponsJaspissp. SAB E-35 dan SAB E-38 terhadap pertumbuhan khamir a. C. albicans dan b. C.
23
Tabel 2. Aktivitas antibakteri dan antikhamir isolat-isolat bakteri permukaan asal sponsJaspissp.
Bakteri Uji Khamir Uji
N
Sa :Staphylococcus aureus; Sa* :Staphylococcus aureus; Vh#: Vibrio harveyii; Ec :Escherichia coli; EPEC* K-11 :Escherichia coli; Pa* :Pseudomonas aeruginosa; Cal* :Candida albicans;
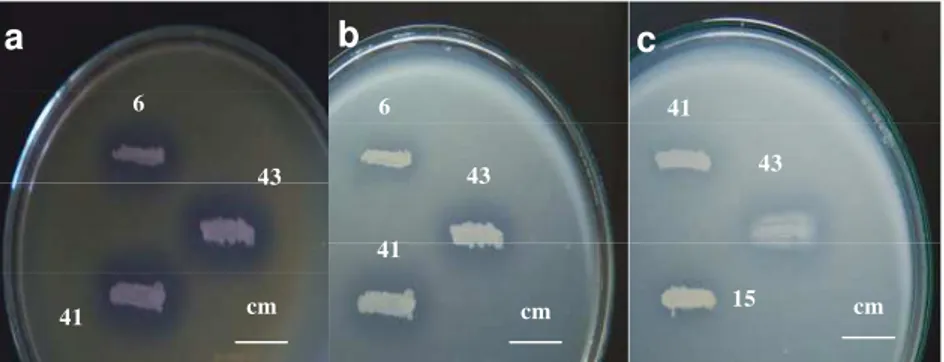
Beberapa isolat bakteri permukaan mampu menghambat beberapa
pertumbuhan bakteri uji namun tidak satupun isolat bakteri permukaan mampu
menghambat C. albicansdan C.tropicalis (Tabel 4). Isolat-isolat tersebut adalah
SAB S-6, SAB S-15, SAB S-30, SAB S-32, SAB S-41 dan SAB S-43, dimana
terdapat zona bening disekitar pertumbuhan isolat-isolat tersebut (Gambar 7).
Pada Tabel 2 dan 3 menunjukkan semua isolat bakteri endofit dan permukaan
tidak memperlihatkan adanya aktivitas dalam menghambat pertumbuhan terhadap
bakteriB. subtillis.
Aktivitas antibakteri dari semua isolat bakteri endofit dan permukaan
terhadap pertumbuhan bakteri E. coli dan EPEC*-K11, hampir semuanya membutuhkan waktu yang lama hingga terbentuk zona bening. Waktu inkubasi
yang dibutuhkan hingga terbentuk zona bening rata-rata adalah 5 x 24 jam.
Pewarnaan Gram dan Uji parsial
Pewarnaan Gram dan uji parsial dilakukan hanya pada beberapa isolat
yang memiliki aktivitas yang baik dalam menghambat pertumbuhan bakteri dan
khamir target. Isolat-isolat tersebut adalah SAB E-8, SAB E-33, SAB E-35, SAB
E-38, SAB E-40 dan SAB S-43 karena mampu menghambat minimal lima
mikroba uji dengan kemampuan penghambatan yang baik. Pewarnaan Gram
menunjukkan isolat SAB E-8, SAB E-35, dan SAB E-40 adalah bakteri kelompok
Gram negatif (Gambar 8). Hasil pewarnaan Gram positif pada isolat SAB E-33,
25
Gambar 7. Senyawa antibakteri yang dihasilkan (terlihat dari zona bening yang terbentuk) dari beberapa bakteri permukaan asal spons Jaspis sp. terhadap pertumbuhan a.S. aureus,b.V. harveyiidan c.P. aeruginosa.
Gambar 8. A. Profil koloni pada media SWC dan B. Hasil pewarnaan bakteri Gram negatif isolat SAB E-35.
Identifikasi parsial yang mengarahkan isolat yang memiliki gram positif
adalah dari kelompok Bacillus meliputi pewarnaan Gram, pewarnaan spora dan
uji katalase (Gambar 9).
Gambar 9. Uji parsial genusBacillusuntuk isolat bakteri gram positif (SAB S-43); A. Profil koloni pada media SWC; B. Pewarnaan Gram; C. Pewarnaan Spora.
a b c
cm cm cm
6
43
41
41
43
15 41
6
43
a. b.
cm
(A) (B)
a. b. c.
Endospora cm
Amplified Ribosomal DNA Restriction Analysis(ARDRA)
Berdasarkan hasil uji antimikroba, diperoleh 30 isolat yang memiliki
aktivitas antimikroba yang terdiri dari 24 isolat bakteri endofit dan 6 isolat bakteri
yang berasal dari permukaan. Isolat yang terpilih akan digunakan untuk
mengetahui hubungan kekerabatan antar bakteri dengan metode ARDRA.
Ekstraksi genom seluruh isolat dilanjutkan dengan amplifikasi gen 16S rRNA
dengan PCR yang menunjukkan produk PCR gen 16S rRNA sekitar 1300pb
(Gambar 10)
Gen 16S rRNA hasil amplifikasi PCR didigesti dengan tiga enzim restriksi
yaitu RsaI, HaeIII dan HinfI. Hasil restriksi memperlihatkan pola pita gen 16S
rRNA (profil) yang beragam dengan jumlah 2 – 4 pita. Hasil restriksi gen 16S
rRNA dari beberapa isolat yang dipotong dengan RsaI, HaeIII dan HinfI dapat
dilihat pada Gambar 11, sedangkan hasil interpretasi profil pola pemotongan
untuk ke 30 isolat dengan ARDRA memperlihatkan lebih banyak variasi pola dan
jumlah pita berdasarkan enzim restriksi yang digunakan, yaituRsaI (Gambar 12),
HaeIII (Gambar 13) danHinfI (Gambar 14).
Berdasarkan profil gen 16S rRNA tersebut, dibuat pohon filogenetik untuk
melihat kelompok filotipe dari seluruh isolat terbaik. Hasil restriksi gen 16S
rRNA dengan tiga enzim restriksi dipadukan dan ditransfer menjadi sebuah
hitungan biner (nilai 1 dan 0) berdasarkan keberadaan pita potongan DNA pada
ukuran panjang tertentu (Tabel 3). Data biner ini mempermudah dalam pembuatan
pohon filogenetik. Konstruksi pohon filogenetik dilakukan dengan menggunakan
27
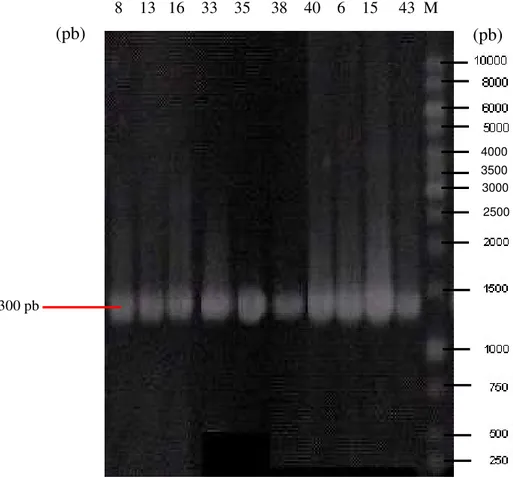
Gambar 10. Amplifikasi gen 16S rRNA dari beberapa isolat yang memiliki aktivitas antimikrob terbaik, M: standar ukuran molekul DNA 1kb ladder.
8 13 16 33 35 38 40 6 15 43 M
1300 pb
4000 3500 3000
Gambar 11. Elektroforesis gel agarose gen 16S rRNA dari beberapa isolat bakteri asal sponsJaspis sp. yang mempunyai aktivitas antimikroba terbaik yang dipotong dengan EnzimRsaI (A),HaeIII (B) danHinfI (C). M: standar ukuran molekul DNA (1kb ladder).
29
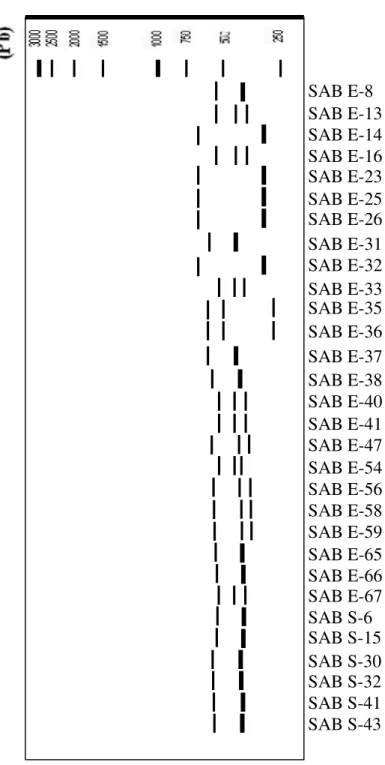
Gambar 12. Profil gen 16S rRNA dari 30 isolat bakteri yang berasosiasi dengan spons Jaspis sp. yang dipotong dengan enzim restriksiRsaI .
31
Tabel 3. Ukuran fragmen DNA gen 16S rRNA yang dipotong dengan beberapa enzim restriksi
Ukuran fragmen DNA (pb) yang dipotong dengan enzim restriksi
Isolat
RsaI HaeIII HinfI
33
Gambar 15. Pohon filogenetik (internode rooted) hubungan kekerabatan antar isolat bakteri yang berasosiasi dengan spons Jaspis sp. dengan aktivitas antimikrob terbaik yang dianalisis dengan ARDRA dan dikonstruksi berdasarkan metode Neighbor-Joining. Angka 10% pada bagian atas pohon menunjukkan skala persentase perbedaan (distance scale) antar profil isolat bakteri. Angka pada nodus adalah nilai bootstrap dengan 100 ulangan.
Filotipe VII
Filotipe VI
Filotipe V Filotipe IV Filotipe III Filotipe I