PENENTUAN JUMLAH H2SO4 PADA PROSES PENURUNAN
ALKALINITAS PADA AIR OLAHAN DI PT. COCA COLA
BOTTLING INDONESIA
TUGAS AKHIR
OLEH:
MALISA TRI HANDAYANI
NIM 122410075
PROGRAM STUDI DIPLOMA III
ANALIS FARMASI DAN MAKANAN
FAKULTAS FARMASI
UNIVERSITAS SUMATERA UTARA
MEDAN
LEMBAR PENGESAHAN
PENENTUAN JUMLAH H2SO4 PADA PROSES PENURUNAN
ALKALINITAS PADA AIR OLAHAN DI PT. COCA COLA
BOTTLING INDONESIA
TUGAS AKHIR
Diajukan Untuk Memenuhi Salah Satu Syarat Untuk Memperoleh Gelar Ahli Madya Pada Program Studi Diploma III Analis Farmasi dan Makanan
Fakultas Farmasi Universitas Sumatera Utara
Oleh:
MALISA TRI HANDAYANI NIM 122410075
Medan, Juni 2015 Disetujui Oleh: Dosen Pembimbing,
Drs. Suryadi Achmad, M.Sc., Apt. NIP 195109081985031002
Disahkan Oleh: a.n Dekan, Wakil Dekan I,
KATA PENGANTAR
Bismillahirahmanirrahim,
Puji syukur penulis ucapkan kepada Allah SWT atas segala limpahan
rahmat dan karunia-Nya yang telah memberikan pengetahuan, kekuatan, kesehatan
dan kesempatan kepada penulis sehingga penulis dapat menyelesaikan tugas akhir
ini, serta sholawat beriring salam untuk Rasulullah Nabi Muhammad SAW
sebagai contoh tauladan dalam kehidupan.
Tugas akhir ini berjudul ”PENENTUAN JUMLAH H2SO4 PADA
PROSES PENURUNAN ALKALINITAS PADA AIR OLAHAN DI PT. COCA
COLA BOTTLING INDONESIA”. Tugas akhir ini disusun untuk memenuhi
salah satu syarat untuk menyelesaikan pendidikan pada Program Studi Diploma
III Analis Farmasi dan Makanan di Fakultas Farmasi Universitas Sumatera Utara.
Penulis menyadari sepenuhnya bahwa tanpa bantuan dari berbagai pihak,
penulis tidak akan dapat menyelesaikan tugas akhir ini sebagaimana mestinya.
Untuk itu penulis mengucapkan terima kasih yang sebesar-besarnya kepada
berbagai pihak antara lain :
Bapak Prof. Dr. Sumadio Hadisaputra, Apt., selaku Dekan Fakultas
Farmasi Universitas Sumatera Utara. Ibu Prof. Dr. Julia Reveny, M.Si., Apt.,
selaku Wakil Dekan I Fakultas Farmasi Universitas Sumatera Utara. Bapak Prof.
Dr. Jansen Silalahi, M.App.Sc., Apt., selaku Ketua Program Studi Diploma III
Analis Farmasi dan Makanan. Bapak Drs. Suryadi Achmad, M.Sc., Apt., selaku
Dosen Pembimbing Tugas Akhir yang telah banyak memberikan bimbingan dan
Marline Nainggolan, M.S., Apt., selaku Dosen Penasehat Akademis yang telah
memberikan nasehat dan pengarahan kepada penulis dalam hal Akademis setiap
semester. Bapak Muhammad Arif, ST., selaku Pembimbing Praktek Kerja
Lapangan di PT. Coca Cola Bottling Indonesia Plant Medan yang telah
membimbing dan memberikan banyak ilmu dan arahan pada saat Praktek Kerja
Lapangan. Dosen dan Pegawai Fakultas Farmasi Program Studi Diploma III
Analis Farmasi dan Makanan yang berupaya mendukung kemajuan mahasiswa.
Kedua orang tua penulis serta seluruh keluarga besar yang telah
memberikan perhatian, doa, dorongan dan pengorbanan baik moril maupun
materil dalam penyelesaian tugas akhir ini. Saudara-saudara penulis yang selalu
memberikan doa serta semangat.
Penulis menyadari sepenuhnya bahwa dalam penulisan maupun penyajian
tugas akhir ini terdapat kekurangan dan kelemahan serta masih jauh dari
kesempurnaan, oleh karena itu dengan segala kerendahan hati penulis
mengharapkan saran dan kritik yang sifatnya membangun demi kesempurnaan
tugas akhir ini. Akhir kata, semoga Allah SWT melimpahkan rahmat dan
karunia-Nya kepada kita semua dan harapan penulis semoga tugas akhir ini dapat
memberikan manfaat bagi kita semua. Aamiin yaa Rabbal Alamin.
Medan, Juni 2015 Penulis,
2.8. Alkalinitas ... 13
2.8.1. Peranan Alkalinitas ... 13
2.9. Metode Analisa Alkalinitas ... 14
2.9.1. Metode Titrasi Volumetri ... 14
2.9.1.1. Metode Indikator Warna ... 14
2.9.2. Metode Potensiometri ... 16
2.9.3. Gangguan Pada Analisa Alkalinitas ... 17
BAB III METODOLOGI ... 19
3.1. Tempat ... 19
3.2. Alat-alat ... 19
3.3. Bahan-bahan ... 19
3.4. Prosedur Pemeriksaan ... 19
3.4.1. Pembuatan Larutan H2SO4 96 N ... 19
3.4.2. Prosedur Alkalinitas ... 19
3.4.3. Perhitungan ... 20
BAB IV HASIL DAN PEMBAHASAN ... 21
4.1. Hasil ... 21
4.2. Pembahasan ... 22
BAB V KESIMPULAN DAN SARAN ... 23
5.1. Kesimpulan ... 23
5.2. Saran ... 23
DAFTAR TABEL
Halaman
Tabel 2.1. Indikator Yang Dapat Digunakan Untuk Titrasi Alkalinitas ... 15
DAFTAR LAMPIRAN
Halaman
Lampiran 1. Perhitungan Penurunan Alkalinitas ... 25
Lampiran 2. Gambar Alat Neraca Analitis Digital ... 26
Lampiran 3. Gambar Alat Titration Plus Automatic ... 27
BAB I
PENDAHULUAN
1.1 Latar Belakang
Air merupakan unsur utama bagi makhluk hidup di planet ini. Manusia
mampu bertahan hidup tanpa makan dalam beberapa minggu, namun tanpa air ia
akan mati dalam beberapa hari saja. Dalam bidang kehidupan ekonomi modern,
air berfungsi penting untuk budidaya pertanian, industri pembangkit tenaga listrik
dan transportasi (Sanim, 2011).
Air merupakan sumber alam yang sangat penting di dunia, karena tanpa air
kehidupan tidak dapat berlangsung. Air juga banyak mendapat pencemaran.
Berbagai pencemaran air berasal dari sumber domestik (rumah tangga),
perkampungan, kota, pasar, jalan dan sebagainya. Sedangkan sumber
non-domestik (pabrik, industri, pertanian, peternakan, perikanan serta sumber-sumber
lainnya) (Hanum, 2002).
Salah satu sumber air yang dapat di manfaatkan adalah air tanah atau air
sumur. Air sumur adalah air tanah dangkal sampai kedalaman kurang dari 30
meter, air sumur umumnya pada kedalaman 15 meter dan dinamakan juga sebagai
air tanah bebas karena lapisan air tanah tersebut tidak berada di dalam tekanan
(Suryana, 2013).
Untuk keperluan air minum, rumah tangga dan industri, secara umum
dapat digunakan sumber air yang berasal dari air sungai, mata air, danau, sumur
dan air hujan yang telah dihilangkan zat-zat kimianya, gas racun, atau
Alkalinitas air adalah pengukur kapasitas untuk menetralisir asam-asam.
Pada air alamiah, alkalinitas dikaitkan dengan konsentrasi bikarbonat, karbonat
dan hidroksidanya. Alkalinitas keseluruhan biasanya dinyatakan dengan padanan
kalsium karbonat dalam miligram per liter. Keasaman dinyatakan dalam jumlah
kalsium karbonat yang dibutuhkan untuk menetralisir air (Linsley, 1985).
Oleh karena hal tersebut diatas, penulis telah melakukan penelitian ini
pada air sumur PT. Coca Cola Bottling Indonesia, sehingga penulis memilih judul
tentang ”Penentuan Jumlah H2SO4 Pada Proses Penurunan Alkalinitas Pada
Air Olahan dengan Metode Titrasi Volumetri yaitu Metode Indikator
Warna”.
1.2 Tujuan dan Manfaat
1.2.1 Tujuan
Untuk mengetahui apakah mutu bahan baku air yang nantinya akan
digunakan menjadi air produksi dalam proses produksi minuman dan memenuhi
syarat atau standar air produksi.
1.2.2 Manfaat
Untuk mengetahui mutu air yang dapat di produksi, serta menambah
pengetahuan dan keterampilan, khususnya tentang penentuan jumlah asam sulfat
pada proses penurunan alkalinitas pada air olahan menggunakan metode titrasi
BAB II
TINJAUAN PUSTAKA
2.1 Pengertian Air
Air merupakan kebutuhan dasar bagi kehidupan, juga manusia selama
hidupnya selalu memerlukan air. Dengan demikian semakin naik jumlah
penduduk serta laju pertumbuhannya semakin naik pula laju pemanfaatan
sumber-sumber air. Untuk dapat memenuhi kebutuhan hidup masyarakat yang semakin
meningkat diperlukan industrialisasi yang dengan sendirinya akan meningkatkan
lagi aktivitas penduduk serta beban penggunaan sumber daya air. Beban
pengotoran air juga bertambah cepat sesuai dengan cepatnya pertumbuhan.
Sebagai akibatnya saat ini, sumber air tawar dan bersih menjadi semakin langkah.
Pengolahan sumber daya air ini sebaiknya dilakukan secara terpadu baik dalam
pemanfaatan maupun dalam pengolahan kualitas. Integrasi ini tidak saja terbatas
pada hidrosfir, tetapi juga dengan atmosfir, lithosfir, biosfir dan sosiosfir
(Soemirat, 1994).
Penyediaan air bersih, selain kuantitasnya, kualitasnya pun harus
memenuhi standar yang berlaku. Untuk ini perusahaan air minum, selalu
memeriksa kualitas airnya sebelum didistribusikan pada pelanggan. Karena air
baku belum tentu memenuhi standard, maka seringkali dilakukan pengolahan air
untuk memenuhi standar air minum. Tergantung kualitas air bakunya, pengolahan
air minum dapat sangat sederhana sampai sangat kompleks. Apabila air bakunya
baik, maka tidak mungkin diperlukan pengolahan sama sekali. Apabila hanya ada
semakin jelek kualitasnya, maka pengolahan harus lengkap, yakni melalui proses
koagulasi, sedimentasi, filtrasi dan desinfeksi. Ataupun mungkin diperlukan suatu
proses pengolahan seperti pra-khlorinasi, aerasi dan seterusnya (Soemirat, 1994).
Air adalah segala-galanya bagi kehidupan, juga peradaban bagi manusia,
bagi tanaman dan bagi hewan, bagi pertanian, bagi industri dan bagi
keseimbangan alam. Persediaan air yang mencukupi pada saat yang tepat dan
dengan kualitas yang memadai adalah soal hidup atau mati. Manusia masih
mungkin dapat bertahan hidup selama beberapa minggu tanpa makanan, tetapi
tanpa air ia hanya akan bertahan hidup paling lama sepuluh hari. Beberapa jenis
bakteri hidup subur tanpa oksigen, namun tak satupun dapat tumbuh tanpa air. Air
untuk konsumsi indutri lebih rumit lagi permasalahannya. Sebagai pembangkit
energi untuk menggerakkan mesin-mesin indutsri yang ada, mungkin bisa
digunakan sebarang air. Akan tetapi sebagai bagian dari bahan yang akan
diproses, air untuk industri ini harus pula memenuhi syarat-syarat kualitas tertentu
(Dumairy, 1992).
Air merupakan suatu zat yang istimewa. Ia tampil dalam tiga wujud
sekaligus ; sebagai benda cair, benda padat (es, gletser) dan benda gas (uap). Ia
terdapat di tiga ruang : di permukaan bumi, di dalam tanah dan di atmosfir bumi.
Di permukaan bumi, ia berwujud sebagai samudera, padang es atau salju, sungai
dan danau secara umum disebut dengan istilah air permukaan. Wilayahnya
mencakup hampir tiga perempat permukaan bumi, dengan volume sekitar 1.350
Air ada di mana-mana dan diyakini tersedia secara berlimpah ruah. Ia
masih terus menunjang segala kehidupan. Beberapa organisme yang sangat
sederhana dapat hidup tanpa udara, namun tak satupun dapat hidup tanpa air. Air
merupakan sumber lahirnya banyak peradaban besar, tapi kadang kala juga
bertanggung jawab atas kehancurannya. Bukan itu saja, air juga merupakan
arsitek bumi. Selama jutaan tahun air telah menjadi salah satu pelaku yang paling
menentukan dalam membentuk kembali wajah bumi. Air juga turut menentukan
iklim, membentuk tanah tempat berakarnya tanaman dan hutan. Sebagai uap atau
daya hidroelektrik, ia menciptakan energi dan menggerakkan mesin teknologi
modern untuk keperluan industri (Dumairy, 1992).
Air adalah sangat penting bagi kehidupan manusia. Manusia akan lebih
cepat meninggal karena kekurangan air daripada kekurangan makanan. Di dalam
tubuh manusia itu sendiri sebagian besar terdiri dari air. Tubuh orang dewasa,
sekitar 55 – 60 % berat badan terdiri dari air, untuk anak-anak sekitar 65 %, dan
untuk bayi sekitar 80 % (Notoatmodjo, 2003).
Kebutuhan manusia akan air sangat kompleks antara lain untuk minum,
masak, mandi, mencuci (bermacam-macam cucian) dan sebagainya. Menurut
perhitungan WHO di negara-negara maju tiap orang memerlukan air antara
60-120 liter per hari. Sedangkan di negara-negara berkembang, termasuk Indonesia
tiap orang memerlukan air antara 30-60 liter per hari (Notoatmodjo, 2003).
2.2 Sumber-sumber Air
Jumlah air di dunia sangat relatif tetap dan mengikuti suatu aliran yang
bumi menguap dan membentuk uap air. Air permukaan yang mengalir di atas
permukaan bumi, umumnya berbentuk sungai-sungai dan jika melalui suatu
tempat yang rendah (cekung) maka air akan berkumpul membentuk suatu danau
atau telaga. Tetapi banyak diantara air yang mengalir ke laut kembali dan
kemudian akan mengikuti siklus hidrologi. Sumber-sumber air yang ada pada
bumi, dapat berasal dari :
1. Air Permukaan
Air permukaan yang mengalir di permukaan bumi akan membentuk air
permukaan. Air ini umumnya mendapat pengotoran selama pengalirannya.
Pengotoran tersebut misalnya oleh lumpur, batang-batang kayu, daun-daun,
kotoran industri dan lain sebagainya. Secara umum air permukaan dibagi menjadi
air sungai dan air rawa atau danau. Air sungai pada umumnya mempunyai derajat
pengotoran yang tinggi sekali. Dalam penggunaanya sebagai air minum harus
melalui proses panjang. Sedangkan pada air danau kebanyakan berwarna yang
disebabkan oleh zat-zat organik yang telah membusuk.
2. Air Tanah
Air tanah secara umum terbagi menjadi :
- Air Tanah Dangkal
Air tanah dangkal terjadi akibat proses penyerapan air dari permukaan
tanah. Lumpur akan tertahan, demikian juga dengan sebagai bakteri, sehingga air
dangkal terlihat jernih tetapi banyak mengandung zat-zat kimia (garam-garam
terlarut) karena melalui lapisan tanah yang memiliki unsur-unsur tertentu untuk
- Air Tanah Dalam
Air tanah dalam terdapat pada lapis rapat air yang pertama. Pengambilan
air tanah dalam lebih sulit daripada air tanah dangkal. Pada umumnya kualitas air
tanah dalam lebih baik daripada air tanah dangkal, karena terjadi penyaringan
yang lebih sempurna terutama untuk bakteri.
- Mata Air
Mata air adalah air tanah yang keluar dengan sendirinya ke permukaan
tanah.
3. Air hujan
Air hujan memiliki sifat agresif terutama terhadap pipa-pipa penyalur
maupun bak-bak reservoir, sehingga mempercepat terjadinya karatan (korosi).
4. Air laut
Air laut mempunyai sifat asin, karena mengandung berbagai garam,
misalnya NaCl. Kadar garam NaCl dalam air laut lebih kurang 3 %. Oleh karena
itu air laut tanpa diolah terlebih dahulu tidak memenuhi syarat untuk air minum
(Waluyo, 2009).
2.3 Sifat-Sifat air
2.3.1 Sifat Fisik Air
Ciri-ciri fisik yang utama dari air adalah bahan padat keseluruhan yang
terapung dan yang terlarut, kekeruhan, warna, rasa dan bau, dan suhu. Bahan
padat keseluruhan ditetapkan dengan menguapkan suatu contoh air dan
menimbang sisanya yang telah kering. Bahan padat terapung didapat dengan
diakibatkan oleh pencemar-pencemar yang terbagi halus, dari manapun asalnya,
yang ada di dalam air. Kekeruhan biasanya disebabkan oleh lempung, lanau,
partikel-partikel tanah dan pencemar-pencemar koloidal lainnya. Air
kadang-kadang mengandung warna yang banyak diakibatkan oleh jenis-jenis tertentu dari
bahan organik yang terlarut dan koloidal yang terbilas dari tanah atau
tumbuh-tumbuhan yang membusuk. Rasa dan bau pada air disebabkan oleh adanya bahan
organik yang membusuk atau bahan kimia yang mudah menguap. Suhu air
merupakan hal yang penting jika dikaitkan dengan tujuan penggunaan,
pengolahan untuk membuang bahan-bahan pencemar serta pengangkutannya
(Linsley, 1985).
2.3.2 Sifat Kimiawi Air
Sifat-sifat kimiawi air antara lain pH, kation dan anion-anion, alkalinitas,
keasaman dan kesadahan. Ion hydrogen bersifat asam, sehingga keberadaan ion
hydrogen menggambarkan nilai pH (derajat keasaman) yang dinyatakan dengan
persamaan: pH=- Log [H+]
Kation-kation dan Anion-anion yang umumnya terdapat pada kebanyakan
air didunia adalah:
Kation-kation terlarut yaitu Kalsium (Ca2+), Magnesium (Mg2+), Pottasium (K+), Sodium (Na+). Anion-anion terlarut yaitu Bikarbonat (HCO3-), Karbonat
(CO3-), Klorida (Cl-), Hidroksida (OH-), Nitrat (NO3-), Sulfat (SO42). Alkalinitas
dilakukan pengujian untuk mengukur kapasitas air dalam menetralkan asam-asam.
Keasaman dilakukan pengujian untuk mengukur jumlah suatu zat basa yang
menguji perkaratan air dan kebutuhan dosis bila pengolahan kimiawi harus
dipergunakan; dapat juga memperkirakan pH bila konsentrasinya bikarbonat
diketahui. Kesadahan dilakukan pengujian untuk mengukur kapasitas konsumsi
sabun kecenderungan pembentukan skala air (Kristanto, 2002).
2.4 Kriteria Kualitas Air
Air yang digunakan untuk keperluan sehari-hari sebaiknya adalah air yang
memenuhi kriteria sebagai air bersih. Air bersih merupakan air yang dapat
digunakan untuk keperluan sehari-hari yang kualitasnya memenuhi syarat-syarat
kesehatan dan dapat diminum apabila telah dimasak. Sedangkan yang dinamakan
air minum adalah air yang melalui proses pengolahan atau tahap proses
pengolahan memenuhi syarat kesehatan dan dapat langsung diminum. Persyaratan
terbaru seperti yang telah ditetapkan oleh Menteri Kesehatan Republik Indonesia
melalui Kepmenkes RI Nomor 907/Menkes/SK/VII/2002/Tanggal 29 Juli 2002.
Jenis-jenis air minum seperti yang dimaksud adalah meliputi :
- Air yang didistribusikan melalui pipa untuk keperluan rumah tangga;
- Air yang didistribusikan melalui tangki air;
- Air kemasan;
- Air yang digunakan untuk produksi bahan makanan dan minuman yang
disajikan untuk masyarakat.
Persyaratan kesehatan untuk air bersih dan air minum meliputi persyaratan
2.5 Ciri-ciri dan Mutu Air
Air murni adalah zat cair yang tidak mempunyai rasa, warna dan bau, yang
terdiri dari hidrogen dan oksigen dengan rumus kimiawi H2O. Karena air
merupakan suatu larutan yang hampir-hampir bersifat universal, maka zat-zat
yang paling alamiah maupun buatan manusia hingga tingkat tertentu terlarut di
dalamnya. Dengan demikian, air di dalam mengandung zat-zat terlarut. Di
samping itu, akibat daur hidrologi air juga mengandung berbagai zat lainnya,
termasuk gas. Zat-zat ini sering di sebut pencemar yang terdapat di dalam air
(Linsley, 1985).
2.6 Air Sumur
Umumnya air sumur itu selalu bersih, namun hal itu terjadi bila sumur
tersebut benar-benar terjaga kebersihannya. Sumur dikatakan benar-benar terjaga
kebersihannya bila :
- Paling sedikit berjarak 20 meter dari kakus atau tempat penimbunan sampah.
- Paling sedikit kedalamannya adalah 3 meter.
- Dinding bagian dalamnya lurus dan dibuat dari batu bersemen.
- Terdapat dinding batu yang mengelilinginya, dan tingginya paling sedikit
adalah setengah meter.
- Mempunyai penutup yang dapat secara mudah diangkat, mempunyai pompa
tangan dan bila mungkin terdapat alat lain yang dapat digunakan untuk
mengambil air sumur.
- Mempunyai parit di sekelilingnya sehingga memudahkan air hujan untuk
- Orang-orang tidak diperkenankan memasukkan kotoran ke dalam dan mereka
tidak diperbolehkan memasukkan air bekas cucian ke dalam sumur.
- Mempunyai saluran air kotor sehingga yang tidak terpakai itu tidak masuk ke
dalam sumur (Asih, 1995).
Air sumur pompa, terutama air sumur pompa dalam sudah cukup
memenuhi persyaratan. Tetapi sumur pompa ini di daerah pedesaan masih mahal,
di samping itu, teknologi masih dianggap tinggi untuk masyarakat pedesaan. Yang
lebih umum di daerah pedesaan adalah sumur gali. Agar air sumur pompa gali ini
tidak tercemar oleh kotoran di sekitarnya perlu adanya syarat-syarat sebagai
berikut :
- Harus ada bibir sumur, agar bila musim hujan tiba, air tanah tidak akan masuk
ke dalamnya.
- Pada bagian atas kurang lebih 3 cm dari permukaan tanah harus ditembok, agar
air dari atas tidak dapat mengotori air sumur.
- Perlu diberi lapisan kerikil di bagian bawah sumur tersebut untuk mengurangi
kekeruhan (Notoatmodjo, 2003).
Kebanyakan air permukaan dapat terkena kontaminasi, sehingga disinfeksi
biasanya merupakan hal yang penting. Air dari sumur dalam biasanya bebas dari
bakteri patogen, sehingga pemurnian mungkin tidak diperlukan. Kebanyakan air
sumur bersifat sadah, sehingga pelembutan bersama-sama dengan pembuangan
besi dan mangan mungkin diperlukan. Air sumur biasanya cukup jernih, sehingga
tidak diperlukan usaha menghilangkan kekeruhan. Bila ada kemungkinan
Suatu sumur yang dibangun dengan tepat hanya akan memerlukan sedikit
pemeliharaan, kecuali bila dipompa berlebihan. Pemompaan berlebihan dapat
mengakibatkan pergerakan bahan tanah berbutir halus di dalam akifier sehingga
terjadi penyumbatan di dekat saringan. Tersumbatnya sumur oleh bakteri
kadang-kadang diatasi dengan klorinasi. Serangkaian bahan peledak kecil yang
diledakkan berturut-turut akan menimbulkan gelombang-gelombang gas yang
dapat memaksa air membentur ke luar dan masuk saringan, serta menimbulkan
juga getaran yang akan turut menggoncangkan karang kotoran hingga terlepas.
Setelah pelaksanaan hal-hal tersebut, sumur haruslah dipompa dengan keras untuk
membuang endapan-endapan yang lepas (Linsley, 1985).
Tidak banyak hal yang dapat dilakukan tentang berkaratnya saringan atau
tabung. Kebocoran akibat tabung yang berkarat kadang-kadang diatasi dengan
menyuntikkan semen ke sekeliling tabung. Bila sumurnya cukup besar, tabung
yang baru dapat dimasukkan ke dalam tabung yang lama. Bila sumurnya berada di
dalam batuan, tabung yang rusak kadang-kadang dapat ditarik dan diganti, tetapi
bila sumur terletak di dalam bahan tanah yang tidak padat, mungkin harus
ditinggalkan saja (Linsley, 1985).
2.7 Reagen (Asam Sulfat)
Sulfat merupakan senyawa yang stabil secara kimia karena merupakan
bentuk oksida paling tinggi dari unsur belerang. Sulfat dapat dihasilkan dari
oksida senyawa sulfida. Sulfat didalam lingkungan (air) dapat berada secara
ilmiah dan atau dari aktivitas manusia, misalnya dari limbah industri dan limbah
2.8 Alkalinitas
Alkalinitas adalah pengukuran kapasitas air untuk menetralkan asam-asam
lemah, meskipun asam lemah atau basa lemah juga dapat sebagai penyebabnya.
Penyusunan alkalinitas perairan adalah anion bikarbonat (HCO3-), karbonat (CO3
-),dan hidroksida (OH-). Garam dari asam lemah lain seperti : Borat (H2BO3-),
silikat (HsiO3-), fosfat (HPO4- dan H2PO4-), sulfida (HS-), dan amonia (NH3) juga
memberikan kontribusi terhadap alkalinitas dalam jumlah sedikit. Meskipun
banyak komponen penyebab alkalinitas perairan, penyebab utama dari alkalinitas
tersebut adalah : (1) hidroksida, (2) karbonat, (3) bikarbonat (Limbong, 2008).
2.8.1 Peranan Alkalinitas
Alkalinitas berperan dalam hal-hal sebagai berikut :
a. Sistem Penyangga
Bikarbonat yang terdapat pada perairan dengan nilai alkalinitas total tinggi
berperan sebagai penyangga perairan terhadap perubahan pH yang drastis. Jika
basa kuat ditambahkan kedalam perairan maka basa tersebut akan bereaksi dengan
asam karbonat membentuk garam bikarbonat dan akhirnya menjadi karbonat. Jika
asam ditambahkan kedalam perairan maka asam tersebut akan digunakan untuk
mengonversi karbonat menjadi bikarbonat dan bikarbonat menjadi asam karbonat.
Hal ini dapat menjadikan perairan dengan nilai alkalinitas total tinggi tidak
mengalami perubahan pH secara drastis (Limbong, 2008).
b. Koagulasi Bahan Kimia
Bahan kimia yang digunakan dalam proses koagulasi air atau limbah
yang dilepaskan bereaksi dengan ion-ion penyusun alkalinitas, sehingga
alkalinitas berperan sebagai penyangga untuk mengetahui kisaran pH yang
optimum bagi penggunaan koagulan. Dalam hal ini nilai alkalinitas sebaiknya
berada pada kisaran optimum untuk mengikat ion hidrogen yang dilepaskan pada
proses koagulasi.
c. Pelunakan Air
Alkalinitas adalah parameter kualitas air yang harus dipertimbangkan
dalam menentukan jumlah soda abu dan kapur yang diperlukan dalam proses
pelunakan dengan metode pengendapan. Pelunakan air bertujuan untuk
menurunkan kesadahan.
d. Pengendalian Korosi
Alkalinitas merupakan parameter yang sangat penting termasuk didalam
pengendalian korosi.
e. Limbah Industri
Banyak para agen yang mencegah pengecekan terhadap campuran limbah
yang disebabkan (hidoksida) alkalinitas untuk penerimaan air. Sebaiknya pH
alkalinitas ialah suatu faktor yang penting didalam penentuan kemampuan dari
limbah untuk pengolahan secara biologi (Limbong, 2008).
2.9 Metode Analisa Alkalinitas
2.9.1 Metode Titrasi Volumetri
2.9.1.1 Metode Indikator Warna
Alkalinitas dapat diukur dengan titrasi volumetri dengan H2SO4 di dalam
dengan pH diatas 8,3 titrasi dilakukan dalam dua tahap. Pada tahap pertama titrasi
sampai pH 8,2 dengan phenolpthalein sebagai indikator yang ditunjukkan dari
perubahan warna merah menjadi tidak berwarna. Selain itu titrasi dilanjutkan
dengan menambahkan indikator metil orange sampai pH 4,5 (larutan tidak
berwarna). Untuk sampel yang pHnya kurang dari 8,3 hanya dilakukan titrasi satu
tahap dengan metil orange sebagai indikator sampai pH 4,5 (warna berubah dari
kuning menjadi merah).
- Pemilihan indikator yang sesuai
Indikator adalah suatu zat yang warnanya berbeda-beda sesuai dengan
konsentrasi ion-hidrogen. Jika asam kuat dititrasi maka perubahan yang besar
dalam pH pada titik ekivalen cukup untuk menjangkau indikator dari metil orange
(3,1 sampai 4,4) dan phenolpthalein (8,0 sampai 9,8).
Tabel 2.1 : indikator yang dapat digunakan untuk titrasi alkalinitas :
Jenis Pelarut konsentra
si
- Pereaksi Asam yang sesuai
Dalam memilih asam untuk dipakai sebagai larutan standar perlu
diperhatikan faktor-faktor sebagai berikut :
a. Asam harus kuat, yaitu berdisosiasi tinggi
c. Larutan asammya harus stabil
d. Garam dari asamnya harus larut
e. Asam tidak harus merupakan suatu pereaksi oksidator yang cukup kuat untuk
merusak senyawa-senyawa organik yang digunakan seperti indikator. Asam
klorida dan asam sulfat merupakan yang paling umum digunakan sebagai
larutan standar dalam analisa alkalinitas (Limbong, 2008).
2.9.2 Metode Potensiometri
Metode potensiometri ini menggunakan pH meter dimana dalam
mengukur pH sampel memakai elektroda yang bersih. pH meter adalah suatu
voltmeter elektronik dengan resistans input yang tinggi. (Resistans input pH meter
yang baik adalah dalam daerah 1012-1013 Ω). Untuk titrasi dilakukan dengan asam sulfat dan pada setiap kurang lebih 0.5 ml penambahan asam sulfat kedalam
sampel secara perlahan diaduk untuk memberikan waktu yang cukup bagi
kesetimbangan elektroda. Nilai pH hasil titrasi dibaca setelah setiap penambahan
H2SO4 tersebut, atau dilakukan dengan pencatatan dengan rekorder. Dekat titik
ekivalensi pH mulai berubah dengan cepat dan volume titran yang ditambah harus
sekecil mungkin. Titrasi selesai sampai titik lengkungan yang keduanya terlihat
jelas (Limbong, 2008).
Pada pengukuran pH yang secara nyata untuk mengetahui titik akhir yang
setimbang didalam penentuan alkalinitas dapat jadi semakin baik dengan
menggunakan titrasi elektrometris. Pada dasar kenyataannya yang paling penting
didalam air alami dimana total alkalinitas ialah suatu tambahan dari reaksi
Metode” hanya memegang untuk kemurnian yang diutamakan dalam larutan dan
tidak harus sesuai dengan pengelompokkan untuk limbah industri atau peristiwa
air alami (Limbong, 2008).
Titik akhir titrasi ini ditentukan oleh :
1. Jenis indikator yang dipilih dimana warnanya berubah-ubah pada pH titik
akhir titrasi.
2. Perubahan nilai pH pada pH meter waktu titrasi asam-basa
memperlihatkan titik akhir titrasi/ekivalen.
2.9.3 Gangguan pada Analisa Alkalinitas
Gangguan yang dapat terjadi pada saat analisa alkalinitas serta
pencegahannya yaitu :
1. Sabun (detergen) dan Lumpur dapat mempengaruhi elektroda dan
memperlambat respon pada ph meter. Usahakan titrasi dilakukan dengan
perlahan untuk memberikan waktu yang cukup bagi keseimbangan pH
elektroda.
2. Amoniak, jangan dihilangkan tetapi ikut dianalisa karena merupakan
penyebab alkalinitas juga.
3. Karbondioksida akan mempengaruhi alkalinitas suatu sampel yang terbuka
terhadap udara. Hal ini dapat diatasi dengan melakukan pengocokan,
pengadukan dan penyaringan.
4. Pengenceran sampel tidak diperbolehkan karena air pengenceran
5. Pemanasan sampel tidak diperbolehkan karena mengurangi
karbondioksida terlarut, sehingga alkalinitas berkurang pula (Limbong,
2008).
Bila air tidak mengandung alkalinitas yang diperlukan, maka mungkin
perlu ditambahkan kapur (CaO) atau abu soda (Na2CO3) di samping alum untuk
memperoleh flokulasi yang tepat. Silika yang diaktifkan kadang-kadang
ditambahkan ke air untuk menjadi inti bagi pembentukan kumpulan. Kapur
menurunkan kesadahan karbonat dan menggantikan garam-garam kalsium dengan
garam-garam magnesium sedangkan soda bekerja pada kesadahan yang non
karbonat dari garam-garam kalsium. Jumlah kapur dan soda yang dibutuhkan
untuk menghilangkan kesadahan tergantung pada mutu kimiawi air dan jumlah
kesadahan yang ingin dihilangkan. Banyak air sadah yang mengandung
konsentrasi sulfat, klorida dan nitrat rendah; karena itu kapur seringkali
BAB III
METODOLOGI
3.1 Tempat
Pemeriksaan alkalinitas ini dilakukan di Laboratorium yang terdapat di PT.
Coca Cola Bottling Indonesia Plant Medan yang beralamat di Jl. Raya Medan
Belawan Km. 14 Simpang Martubung, PO BOX 1015, Medan.
3.2 Alat-alat
Alat-alat yang digunakan adalah Buret, Erlenmeyer, Pipet tetes, Beaker
gelas, Gelas ukur, Labu tentukur dan Pipet volume.
3.3 Bahan-bahan
Bahan-bahan yang digunakan adalah H2SO4 0,02 N, H2SO4 96 N, Indikator
phenolftalein 1 %, Indikator mix dan Deep Well (Air Sumur).
3.4 Prosedur Pemeriksaan
3.4.1 Pembuatan Larutan H2SO4 96 N
- Dipipet sebanyak 0,26 ml asam sulfat 96 N.
- Dimasukkan ke dalam labu tentukur 50 ml melalui dinding tabung secara
perlahan.
- Diaddkan dengan menambahkan akuades hingga garis tanda.
- Dikocok hingga homogen.
3.4.2 Prosedur Alkalinitas
- Dimasukkan sampel sebanyak 100 ml kedalam masing-masing
- Dipipet asam sulfat 96 N sebanyak 0,1 ml; 0,2 ml; 0,3 ml; 0,4 ml; 0,5 ml
dan 0,6 ml kedalam erlenmeyer yang berisi sampel air sumur (deep well).
- Ditambahkan indikator fenoftalein sebanyak 3 tetes (hasil=0) lalu
ditambah lagi indikator mix sebanyak 3 tetes hingga berubah menjadi
berwarna biru.
- Dititrasi dengan asam sulfat 0,02 N hingga berubah menjadi berwarna
kemerahan.
- Dicatat volume H2SO4 0,02 N yang terpakai (Vt).
3.4.3 Perhitungan
Perhitungan Alkalinitas dapat dilakukan dengan rumus :
Alkalinitas = Vt x 10
Dimana:
BAB IV
HASIL DAN PEMBAHASAN
4.1 Hasil
Berdasarkan pemeriksaan penurunan Alkalinitas yang dilakukan,
diperoleh data sebagai berikut:
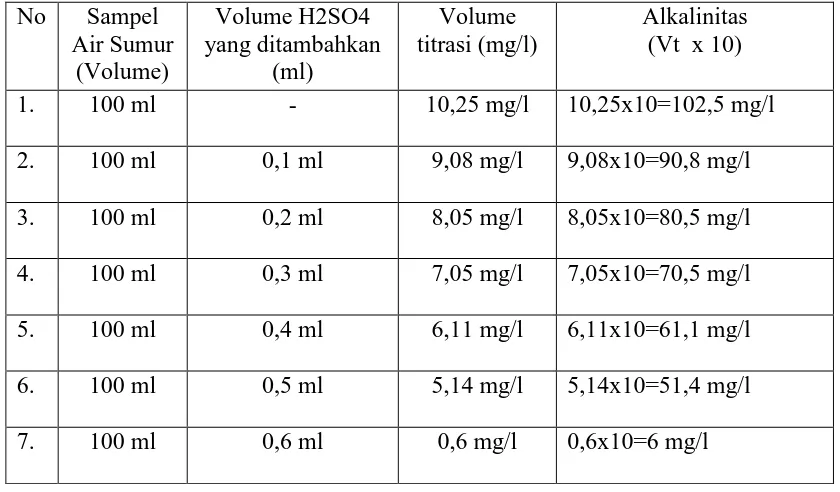
Tabel 4.1. Data Hasil Pemeriksaan Penurunan Alkalinitas
4.2 Pembahasan
Dari hasil uji penentuan jumlah asam sulfat pada proses penurunan
alkalinitas pada air olahan bahwa sampel air sumur tanpa penambahan asam sulfat
didapat volume titrasi yaitu 10,25 mg/l maka alkalinitas yang didapat yaitu 102,5
mg/l, dengan penambahan asam sulfat 0,1 ml didapat volume titrasi yaitu 9,08
mg/l maka alkalinitas yang didapat yaitu 90,8 mg/l, dengan penambahan asam
sulfat 0,2 ml didapat volume titrasi yaitu 8,05 mg/l maka alkalinitas yang didapat
yaitu 80,5 mg/l, dengan penambahan asam sulfat 0,3 ml didapat volume titrasi
yaitu 7,05 mg/l maka alkalinitas yang didapat yaitu 70,5 mg/l, dengan
penambahan asam sulfat 0,4 ml didapat volume titrasi yaitu 6,11 mg/l maka
alkalinitas yang didapat yaitu 61,1 mg/l, dengan penambahan asam sulfat 0,5 ml
didapat volume titrasi yaitu 5,14 mg/l maka alkalinitas yang didapat yaitu 51,4
mg/l, dengan penambahan asam sulfat 0,6 ml didapat volume titrasi yaitu 0,6 mg/l
maka alkalinitas yang didapat yaitu 6 mg/l. Dari data diatas dinyatakan bahwa
alkalinitas pada air olahan yang diproduksi oleh PT. Coca Cola Bottling Plant
BAB V
KESIMPULAN DAN SARAN
5.1. Kesimpulan
Dari hasil pemeriksaan alkalinitas pada air olahan yang nantinya akan
digunakan menjadi air produksi oleh PT. Coca Cola Bottling Indonesia, hasil yang
diperoleh dengan penambahan H2SO4 0,6 ml alkalinitasnya adalah 6 mg/l
sementara persyaratan dan standar alkalinitas yang ditetapkan adalah <50 mg/l
telah sesuai dengan persyaratan dan standar alkalinitas pada air olahan (deep well)
yang ditetapkan oleh PT. Coca Cola Bottling Indonesia.
5.2 Saran
Pada saat melakukan percobaan pemeriksaan alkalinitas pada air olahan,
dengan metode titrasi volumetri yaitu titrasi indikator warna sebaiknya
menggunakan sampel dari sumber-sumber air seperti air danau, air sungai dan
mata air sehingga dapat diperoleh hasil alkalinitas yang baik sesuai dengan
standar dan telah memenuhi persyaratan yang ada di PT. Coca Cola Bottling
DAFTAR PUSTAKA
Asih, Y. (1995). Kader Kesehatan Masyarakat. Jakarta. Penerbit Buku Kedokteran. Hal. 22.
Dumairy. (1992). Ekonomika Sumberdaya Air. Yogyakarta. Penerbit Universitas Gadjah Mada. Hal. 1, 2, 10, 11, 15.
Kristanto, P. (2002). Ekologi Industri. Yogyakarta. Penerbit Andi. Hal. 74, 75, 76, 77, 78.
Limbong, A. (2008). Alkalinitas : Analisa dan Permasalahannya untuk Air
Industri. Universitas Sumatera Utar
Linsley R.K. (1985). Tehnik Sumber Daya Air. Edisi 3. Jilid 1. Jakarta. Penerbit Erlangga. Hal. 91, 97.
Linsley R.K. (1985). Tehnik Sumber Daya Air. Edisi 3. Jilid 2. Jakarta. Penerbit Erlangga. Hal. 99, 101, 104, 108, 129, 131, 138.
Notoatmodjo, S. (2003). Ilmu Kesehatan Masyarakat Prinsip-Prinsip Dasar. Jakarta. Penerbit PT. Rineka Cipta. Hal. 152, 157.
Sanim, B. (2011). Sumberdaya Air dan Kesejahteraan Publik. Bogor. Penerbit IPB Press. Hal. 1, 2, 4.
Soemirat, J. (1994). Kesehatan Lingkungan. Yogyakarta. Penerbit Gadjah Mada University Press. Hal. 108, 110.
Suryana, R.H. (2013). Analisis Kualitas Air Sumur Dangkal di Kecamatan
Biringkanayya Kota Makassar. Universitas Hasanuddin.
Waluyo, L. (2009). Mikrobiologi Lingkungan. Malang. Penerbit UMM Press. Hal. 115, 116, 117, 118, 119.
Lampiran 1. Perhitungan Penurunan Alkalinitas
Perhitungan Alkalinitas dapat dilakukan dengan rumus :
Alkalinitas = Vt x 10
Dimana:
Vt = Volume total titrasi asam sulfat
Diketahui :
Vt 1 : 10,25 mg/l
Vt 2 : 9,08 mg/l
Vt 3 : 8,05 mg/l
Vt 4 : 7,05 mg/l
Vt 5 : 6,11 mg/l
Vt 6 : 5,14 mg/l
Vt 7 : 0,6 mg/l
Alkalinitas 1 : 10,25 x 10 = 102,5 mg/l
Alkalinitas 2 : 9,08 x 10 = 90,8 mg/l
Alkalinitas 3 : 8,05 x 10 = 80,5 mg/l
Alkalinitas 4 : 7,05 x 10 = 70,5 mg/l
Alkalinitas 5 : 6,11 x 10 = 61,1 mg/l
Alkalinitas 6 : 5,14 x 10 = 51,4 mg/l
Lampiran 2. Gambar Alat Neraca Analitis Digital
Lampiran 4. Gambar Alat Lemari Asam