UIN SYARIF HIDAYATULLAH JAKARTA
FORMULASI
PATCH
NATRIUM DIKLOFENAK
BERBASIS POLIMER HIDROKSI PROPIL METIL
SELULOSA (HPMC) DAN NATRIUM KARBOKSI
METIL SELULOSA (NaCMC) SEBAGAI
ANTIINFLAMASI LOKAL PADA PENYAKIT
PERIODONTAL
SKRIPSI
DELVINA GINTING
1110102000058
FAKULTAS KEDOKTERAN DAN ILMU KESEHATAN
PROGRAM STUDI FARMASI
ii
FORMULASI
PATCH
NATRIUM DIKLOFENAK
BERBASIS POLIMER HIDROKSI PROPIL METIL
SELULOSA (HPMC) DAN NATRIUM KARBOKSI
METIL SELULOSA (NaCMC) SEBAGAI
ANTIINFLAMASI LOKAL PADA PENYAKIT
PERIODONTAL
SKRIPSI
Diajukan sebagai salah satu syarat memperoleh gelar Sarjana Farmasi
DELVINA GINTING
1110102000058
FAKULTAS KEDOKTERAN DAN ILMU KESEHATAN
PROGRAM STUDI FARMASI
iii
HALAMAN PERNYATAAN ORISINALITAS
Skripsi ini adalah benar hasil karya saya sendiri, dan semua sumber baik yang dikutip maupun dirujuk
telah saya nyatakan benar.
Nama NIM
Tanda tangan
Tanggal
: : :
:
Delvina Ginting 1110102000058
iv Nama : Delvina Ginting NIM : 1110102000058 Program Studi : Farmasi
Judul Skripsi : Formulasi Patch Natrium Diklofenak Berbasis Polimer Hidroksi Propil Metil Selulosa (HPMC) dan Natrium Karboksi Metil Selulosa (NaCMC) Sebagai Antiinflamasi Lokal pada Penyakit Periodontal
Disetujui oleh
Pembimbing I
Yuni Anggraeni, M. Farm., Apt NIP. 198310282009012008
Pembimbing II
v
HALAMAN PENGESAHAN
Skripsi ini diajukan oleh :
Nama : Delvina Ginting NIM : 1110102000058 Program Studi : Farmasi
Judul Skripsi : Formulasi Patch Natrium Diklofenak Berbasis Polimer Hidroksi Propil Metil Selulosa (HPMC) dan Natrium Karboksi Metil Selulosa (NaCMC) Sebagai Antiinflamasi Lokal pada Penyakit Periodontal
Telah berhasil dipertahankan di hadapan Dewan Penguji dan diterima sebagai bagian persyaratan yang diperlukan untuk memperoleh gelar Sarjana Farmasi pada Program Studi Farmasi Fakultas Kedokteran dan Ilmu Kesehatan Universitas Islam Negeri (UIN) Syarif Hidayatullah Jakarta
DEWAN PENGUJI
Drs. Umar Mansur, M.Sc., Apt
vi Nama : Delvina Ginting Program Studi : Farmasi
Judul : Formulasi Patch Natrium Diklofenak Berbasis Polimer Hidroksi Propil Metil Selulosa (HPMC) dan Natrium Karboksi Metil Selulosa (NaCMC) Sebagai Antiinflamasi Lokal pada Penyakit Periodontal
Telah dibuat sediaan mukoadhesif patch yang mengandung natrium diklofenak sebagai sediaan antiinflamasi lokal pada penyakit periodontal. Penelitian ini bertujuan untuk memformulasi dan mengkarakterisasi sifat-sifat dari patch
natrium diklofenak yang berbasis polimer hidroksi propil metil selulosa (HPMC) dan natrium karboksi metil selulosa (NaCMC). Patch dibuat dalam 3 formula F1, F2, dan F3 dengan memvariasikan perbandingan konsentrasi HPMC:NaCMC (2% b/b) berturut-turut adalah 2:1, 1:1, dan 1:2. Patch dibuat dengan metode solvent casting. Patch yang telah dibuat menunjukkan bahwa ketiga patch dapat melekat dipermukaan membran gusi sapi dengan waktu tinggal yaitu 100 menit (F1), 101,67 menit (F2), dan 90 menit (F3). Persen kumulatif disolusi natrium diklofenak pada jam kedua dari patch F1, F2, dan F3 berturut-turut adalah 72,46±1,78%, 90,12±0,82%, dan 96,68±1,66%. Persen kumulatif difusi natrium diklofenak pada jam kedua dari patch F1, F2, dan F3 berturut-turut adalah 16,31±0,71%, 17,47±1,84%, dan 26,51±4,38%.
vii
ABSTRACT
Name : Delvina Ginting Program Study : Pharmacy
Title : Formulation of Hydroxy Propyl Methyl Cellulose (HPMC) and Sodium Carboxy Methyl Cellulose (NaCMC) Based Diclofenac Sodium Patch as Local Anti-Inflammatory in Periodontal Disease
Mucoadhesive patches containing diclofenac sodium have been made as local anti-inflammatory in periodontal disease. The objectives of this research were to formulate and to study characteristic of the resulting hydroxy propyl methyl cellulose (HPMC) and sodium carboxy methyl cellulose (NaCMC) based diclofenac sodium patch. Patches were formulated in three formulas termed F1, F2 and F3 by varying the concentration ratio of HPMC:NaCMC (2% w/w) in the formula 2:1, 1:1, and 1:2, respectively. Patches were prepared by solvent casting method. In vitro residence time showed that all formulas patch can be attachted to the mucosa gingival bovine with the residence time were 100 minutes (F1), 101,67 minutes (F2), and 90 minutes (F3). Cumulative dissolution of diclofenac sodium after two hours from F1, F2 and F3 were 72,46±1,78%, 90,12±0,82%, and 96,68±1,66%., respectively. Cumulative diffusion of diclofenac sodium after two hours from F1, F2 and F3 were 16,31±0,71%, 17,47±1,84%, and 26,51±4,38%, respectively.
viii
Alhamdulillahirabbil`alamiin, segala puji dan syukur penulis ucapkan
kehadirat Allah SWT yang telah melimpahkan rahmat dan ridho-Nya sehingga
penulis dapat menyelesaikan penyusunan skripsi ini hingga selesai. Penulisan
skripsi yang berjudul “Formulasi Patch Natrium Diklofenak Berbasis Polimer Hidroksi Propil Metil Selulosa (HPMC) dan Natrium Karboksi Metil Selulosa
(NaCMC) Sebagai Antiinflamasi Lokal pada Penyakit Periodontal” bertujuan
untuk memenuhi persyaratan guna memperoleh gelar Sarjana Farmasi pada
Fakultas Kedokteran dan Ilmu Kesehatan Universitas Islam Negeri Syarif
Hidayatullah Jakarta.
Pada kesempatan ini penulis menyadari bahwa, tanpa bantuan dan
bimbingan dari berbagai pihak, dari masa perkuliahan sampai pada penyusunan
skripsi ini, sangatlah sulit bagi saya untuk menyelesaikan skripsi ini. Oleh karena
itu, saya mengucapkan terima kasih dan penghargaan sebesar-besarnya kepada :
1. Yuni Anggraeni, M.Farm., Apt dan Sabrina, M.Farm., Apt., selaku dosen
pembimbing yang telah banyak memberikan bimbingan, waktu, tenaga, saran,
dan dukungan dalam penelitian ini.
2. Prof. Dr. (hc) dr. M. K. Tadjudin, Sp. And., selaku Dekan Fakultas
Kedokteran dan Ilmu Kesehatan Universitas Islam Negeri Syarif Hidayatullah
Jakarta.
3. Drs. Umar Mansur, M.Sc., Apt selaku ketua Program Studi Farmasi Fakultas
Kedokteran dan Ilmu Kesehatan Universitas Islam Negeri Syarif Hidayatullah
Jakarta yang telah memberikan banyak motivasi dan bantuan.
4. Seluruh dosen di Program Studi Farmasi Fakultas Kedokteran dan Ilmu
Kesehatan Universitas Islam Negeri Syarif Hidayatullah Jakarta atas ilmu
pengetahuan yang telah diberikan kepada saya.
5. Kedua orang tua, ayahanda tersayang Robinson Ginting, S.E. dan ibunda
tercinta Jusmiati, S. Pd. yang selalu memberikan kasih sayang, doa yang tidak
pernah putus dan dukungan baik moril maupun materil. Tidak ada apapun di
dunia ini yang dapat membalas semua kebaikan, cinta, dan kasih sayang yang
telah kalian berikan kepada anakmu, semoga Allah selalu memberikan
keberkahan, kesehatan, keselamatan, perlindungan, cinta, dan kasih sayang
ix
6. Adik dan kakakku tersayang Royi Aidiltra Ginting dan Delovita Ginting S.Si
yang telah memberikan doa, semangat, dan dukungan sehingga penelitian ini
dapat berjalan dengan lancar.
7. Briptu Muhaitsan Sulaksono S.H. atas segala pengertian, semangat, perhatian,
dan bantuannya.
8. Seluruh keluarga besar Prodi Farmasi FKIK yang telah memberikan
kesempatan dan kemudahan untuk melakukan penelitian serta dukungan yang
amat besar.
9. Kakak-kakak laboran FKIK, ka Eris, ka lisna, ka Liken, Mba Rani, ka Tiwi,
ka Lilis, ka Suryani, dan ka Rachmadi atas dukungan dan kerjasamanya
selama kegiatan penelitian.
10. Adina S.M. Talogo, Metharezqi Suci Arsih, Liana Puspita, Mayta Ravika,
Nirmala Kasih, Yeyet Durotul, dan Syarifatul Mufidah serta teman-teman
laboratorium yang telah banyak memberi semangat dan kebersamaannya,
terima kasih atas kerjasama dalam penelitian ini.
11. Teman teman seperjuangan farmasi angkatan 2010 atas kebersamaan kita.
12. Serta pihak-pihak lain yang tidak dapat disebutkan satu persatu, yang telah
memberikan dukungan hingga terwujudnya skripsi ini.
Penulis menyadari bahwa skripsi ini masih jauh dari sempurna, namun
penulis berharap semoga hasil penelitian ini dapat bermanfaat bagi perkembangan
ilmu pengetahuan pada umumnya dan ilmu farmasi pada khususnya. Akhir kata,
penulis berharap Allah SWT berkenan membalas segala kebaikan semua pihak
yang telah membantu saya dalam penelitian ini.
Ciputat, 13 Mei 2014
x
Sebagai sivitas akademik Universitas Islam Negeri (UIN) Syarif Hidayatullah Jakarta, saya yang bertanda tangan di bawah ini :
Nama : Delvina Ginting NIM : 1110102000058 Program Studi : Farmasi
Fakultas Jenis Karya
: :
Fakultas Kedokteran dan Ilmu Kesehatan (FKIK) Skripsi
demi pengembangan ilmu pengetahuan, saya menyetujui skripsi/karya ilmiah saya, dengan judul
FORMULASI PATCH NATRIUM DIKLOFENAK BERBASIS POLIMER
HIDROKSI PROPIL METIL SELULOSA (HPMC) DAN NATRIUM KARBOKSI METIL SELULOSA (NaCMC) SEBAGAI ANTIINFLAMASI
LOKAL PADA PENYAKIT PERIODONTAL
untuk dipublikasikan atau ditampilkan di internet atau media lain yaitu Digital Library Perpustakaan Universitas Islam Negeri (UIN) Syarif Hidayatullah Jakarta untuk kepentingan akademik sebatas sesuai dengan Undang-Undang Hak Cipta
Dengan demikian persetujuan publikasi karya ilmiah ini saya buat dengan sebenarnya.
Dibuat di : Ciputat Pada Tanggal : 13 mei 2014
Yang menyatakan,
xi HALAMAN PERSETUJUAN PUBLIKASI KARYA ILMIAH ... DAFTAR ISI ...
2.2 Anatomi Mukosa Rongga Mulut………..
2.3 Gingiva……….
2.4 Mukoadhesif………
2.5 Patch……….
2.6 Natrium Diklofenak ……….
2.7 Hidroksi Propil Metil Selulosa (HPMC) ……….
2.8 Natrium Karboksi Metil Selulosa (NaCMC)………
2.9 Poliuretan………..
BAB 3 METODE PENELITIAN...
3.1. Tempat dan Waktu Penelitian………...
xii
3.2.2 Bahan………...
3.3. Prosedur Kerja………..
3.3.1 Formula Patch………..
3.3.1.1 Preparasi Cairan Pembentuk Film (CPF) ………
3.3.1.2 Preparasi Patch……….
3.3.2 Pembuatan Larutan Buffer Fosfat pH 6,8 ………
3.3.3 Pembuatan Kurva Kalibrasi………..
3.3.3.1 Penentuan Panjang Gelombang Maksimum ( maks)………….
3.3.3.2 Pembuatan Larutan Standar Natrium Diklofenak………
3.3.4 Evaluasi Viskositas Cairan Pembentuk Film (CPF)………….
3.3.5 Organoleptis Film……….
3.3.6 Pengambilan Sampel………
3.3.6.1 Pengukuran Bobot Sampel...………
3.3.6.2 Pengukuran Ketebalan Sampel………..
3.3.6.3 Pengukuran Kandungan Natrium Diklofenak…….………….
3.3.7 Evaluasi Patch………..
3.3.7.1 Uji Pelipatan……….
3.3.7.2 Pengukuran pH Permukaan………..
3.3.7.3 Penetapan Kadar Air………..………...
3.3.7.4 Uji Derajat Pengembangan (Swelling Index Studies)………...
3.3.7.5Uji Waktu Tinggal (in vitro residence time)………
3.3.7.6 Uji Kemampuan Disolusi Zat Aktif………..
3.3.7.7 Uji Kemampuan Difusi Zat Aktif……….
BAB 4 HASIL DAN PEMBAHASAN………..
4.1 Formulasi Patch………
4.2 Karakteristik Cairan Pembentuk Film (CPF)………
4.3 Organoleptis………..
4.4 Kandungan Natrium Diklofenak pada Sampel ...……….
xiii
4.9 Derajat Pengembangan………...………..
4.10 Kemampuan Disolusi Natrium Diklofenak………
4.11 Kemampuan Difusi Natrium Diklofenak………..
BAB 5 KESIMPULAN DAN SARAN………..
5.1 Kesimpulan………...
5.2 Saran……….
DAFTAR PUSTAKA……….
LAMPIRAN………
36
38
40
45
45
45
46
xiv
Halaman
Tabel 3.1.
Tabel 4.1.
Tabel 4.2.
Tabel 4.3.
Tabel 4.4.
Tabel 4.5.
Tabel 4.6.
Tabel 4.7.
Tabel 4.8.
Tabel 4.9
Formula Patch Natrium Diklofenak………...
Viskositas Cairan Pembentuk Film………...
Kandungan Natrium Diklofenak pada Sampel …...…………..
Kadar Air Patch……….
Derajat Pengembangan Patch dalam Medium Buffer Fosfat
pH 6,8………
Jumlah Kumulatif Disolusi Natrium Diklofenak dari Sediaan
Patch………..
Fluks Disolusi Natrium Diklofenak………... Jumlah Kumulatif Difusi Natrium Diklofenak dari Sediaan
Patch………...
Fluks Difusi Natrium Diklofenak………...
Jumlah Natrium Diklofenak yang Berdifusi dihitung………... 24
32
34
35
37
39
40
41
43
xv
Keadaan Gingivitis dan Periodontitis………...
Anatomi Mukosa Rongga Mulut………..
Jenis Epitel pada Jaringan Periodontal……….
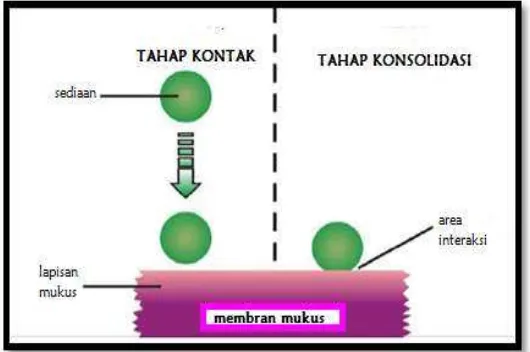
Dua Tahap dalam Proses Mukoadhesif………
Struktur Kimia Natrium Diklofenak……….
Grafik Derajat Pengembangan Patch………..……
Grafik Persentase Kumulatif Difusi Natrium Diklofenak..…..
Fluks Difusi Masing-Masing Formula……….
Grafik Persentase Kumulatif Disolusi Natrium Diklofenak …
xvi
Gambar Alat dan Bahan Penelitian…..………
Gambar Evaluasi Waktu Tinggal……….
Gambar Evaluasi Difusi Zat Aktif………
Gambar Rangkaian Alat Disolusi ………
Gambar Uji Swelling Index…………....………..
Data Kestabilan bobot………..………
Grafik Kestabilan Bobot………..………
Scanning Panjang Gelombang Maksimum Natrium
Diklofenak………... Data Absorbansi Kurva Standar Natrium Diklofenak..……
Kurva Kalibrasi Natrium Diklofenak…………...…………
Bobot, Ketebalan, dan Kandungan Natrium Diklofenak
pada Sampel yang Digunakan………..
Daya Tahan Lipatan dan pH Permukaan………..…
Nilai Viskositas Cairan Pembentuk Film……….
Uji Statistik ANOVA Viskositas Cairan Pembentuk Film..
Kadar Air Patch………
Derajat Pengembangan……….
Data Uji Difusi Natrium Diklofenak dari Sediaan Patch
Formula 1……….
Data Uji Difusi Natrium Diklofenak dari Sediaan Patch
Formula 2……….
Data Uji Difusi Natrium Diklofenak dari Sediaan Patch
Formula 3……….
Data Uji Disolusi Natrium Diklofenak dari Sediaan Patch Formula 1……….
Data Uji Disolusi Natrium Diklofenak dari Sediaan Patch
xvii
Data Uji Disolusi Natrium Diklofenak dari Sediaan Patch Formula 3………. Data Statistik Persentase Difusi Natrium Diklofenak…….. Data Statistik Fluks Difusi Natrium Diklofenak…………..
Data Statistik Persentase Disolusi Natrium Diklofenak…
Data Statistik Fluks Disolusi Natrium Diklofenak….……..
Contoh Perhitungan Persentase Difusi Sampel 1 pada F1...
Contoh Perhitungan Fluks Difusi pada F1 jam keenam…...
Contoh Perhitungan Persentase Disolui Sampel 1 pada F1.
Contoh Perhitungan Fluks Disolusi pada F1 jam keenam...
Sertifikat Analisis Natrium Diklofenak………
Sertifikat Analisis HPMC……….
1
1.1 Latar Belakang
Penyakit periodontal diklasifikasikan ke dalam dua kategori besar
yaitu gingivitis dan periodontitis. Gingivitis adalah kondisi reversible
ditandai dengan peradangan dan pendarahan pada tepi gingiva. Jika
gingivitis tidak dapat diobati maka akan berlanjut menjadi periodontitis
yaitu keadaan dimana jaringan periodontal mengalami kerusakan secara
irreversible (Clarkson et al., 2013 dan National Institutes of Health, 2011).
Untuk mencegah keadaan yang lebih buruk maka gingivitis harus diobati
secara cepat dan tepat. Terapi untuk pengobatan gingivitis ditujukan
terutama untuk mengurangi faktor etiologi dan menghilangkan inflamasi
(Manjusha et al., 2011).
Sebuah penelitian telah menunjukkan bahwa inhibitor produksi
prostaglandin, seperti obat Antiinflamasi Nonsteroid (NSAID), bisa
menghambat proses kehilangan tulang akibat penyakit periodontal. Data dari
hewan coba dan penelitian pada manusia juga mendukung konsep ini,
dimana menunjukkan bahwa obat NSAID dapat mengurangi inflamasi
gingiva dan mengurangi resorpsi tulang alveolar (Ahmed et al., 2009).
Hampir semua obat golongan NSAID memiliki efek samping terhadap
lambung dan duodenum (Wongso, 1996). Penyebab kematian akibat dari
pemakaian NSAID kebanyakan karena perdarahan lambung terutama pada
pasien usia lanjut (Wongso, 1996).
Salah satu NSAID yang terkuat antiradangnya dan berasal dari turunan
fenil asetat adalah diklofenak (Tjay, 2002). Selain permasalahan yang sering
ditimbulkan pada saluran cerna, natrium diklofenak memiliki waktu paruh
yaitu 1,9 jam dan mencapai sekitar 60% dalam darah (Dipiro et al., 2008).
Hal ini mempengaruhi frekuensi pemberian natrium diklofenak kepada
pasien. Dimana semakin sering frekuensi pemberian obat maka semakin
berkurang tingkat kepatuhan pasien. Untuk menghindari berbagai
permasalahan natrium diklofenak maka dapat dirancang suatu sediaan lokal
2
UIN Syarif Hidayatullah Jakarta
yang dapat menghantarkan obat langsung ke tempat aksi adalah sediaan
patch.
Patch terdiri dari dua lapisan, dimana lapisan utama mengandung
polimer yang adhesif dilapisi dengan lapisan backing yang impermeable
(Koyi dan Arsyad, 2013). Salah satu kelompok polimer yang memiliki sifat
mukoadhesif adalah kelompok polimer hidrofilik. Pada penelitian yang
dilakukan oleh Prabhakar Prabhu et al. (2011) dan Semalty et al. (2008)
yang memformulasikan sediaan patch dengan berbagai kombinasi polimer,
dihasilkan bahwa formulasi dengan kombinasi polimer hidroksi propil metil
selulosa (HPMC) dan natrium karboksi metil selulosa (NaCMC) dianggap
sebagai formulasi terbaik. Dalam penelitian yang dilakukan oleh Wardana
(2013) dan Fitriyah (2013) dihasilkan bahwa polimer HPMC dan NaCMC
menghasilkan film dengan karakteristik yang berbeda. film NaCMC
menunjukkan derajat pengembangan yang lebih tinggi daripada film HPMC.
Selain itu, pelepasan obat dari matriks film NaCMC lebih cepat
dibandingkan film HPMC. Namun, kemudahan NaCMC berdisolusi di
dalam air menyebabkan kemungkinan lepasnya natrium diklofenak dari film
NaCMC ke rongga mulut lebih besar serta waktu tinggal sediaan di gingiva
lebih sebentar dibandingkan dengan film HPMC. Beberapa perbedaan
karakteristik film yang dihasilkan kedua polimer ini menjadi dasar
penggunaan mereka secara kombinasi sebagai polimer patch yang diduga
mampu menghasilkan suatu film dengan karakteristik yang lebih baik seperti
derajat pengembangan dan jumlah zat aktif yang berdifusi natrium
diklofenak yang lebih tinggi. Pada penelitian ini digunakan tegaderm
sebagai backing membran yang berfungsi untuk mencegah penetrasi zat
aktif keluar dan tercampur dengan saliva. Berdasarkan hasil pengujian
kebocoran membran tegaderm yang dilakukan oleh Wardana (2013)
tegaderm dapat menahan difusi zat aktif ke saliva.
Berdasarkan uraian di atas, maka dalam penelitian ini akan dibuat
suatu sediaan lokal yang berupa mukoadhesif patch. Patch yang akan dibuat
merupakan patch yang terdiri dari dua lapisan. Lapisan utama yang
mengandung zat aktif natrium diklofenak dalam matriks kombinasi polimer
HPMC dan NaCMC dengan penambahan lapisan backing tegaderm. Selain
UIN Syarif Hidayatullah Jakarta
terhadap waktu tinggal patch pada membran gusi sapi, disolusi natrium
diklofenak secara in vitro menggunakan metode dayung putar dan difusi
natrium diklofenak secara in vitro dengan menggunakan franz diffusion cell.
1.2 Perumusan Masalah
a. Bagaimana sifat adhesifitas patch yang mengandung kombinasi polimer
HPMC dan NaCMC pada membran mukosa gusi?
b. Bagaimana kemampuan difusi dan disolusi natrium diklofenak dari
sediaan patch?
1.3 Hipotesis
a. Lapisan yang terbentuk dari kombinasi polimer HPMC dan NaCMC
yang mengandung natrium diklofenak dapat melekat pada lapisan
mukosa lebih dari 7 jam.
b. Natrium dikloflenak pada patch dengan kombinasi polimer HPMC dan
NaCMC mampu berdifusi dari sediaan patch.
c. Natrium diklofenak dikloflenak pada patch dengan kombinasi polimer
HPMC dan NaCMC mampu terdisolusi dari sediaan patch.
1.4 Tujuan
Adapun tujuan dalam penelitian ini adalah untuk memformulasi dan mengkarakterisasi sifat-sifat dari patch natrium diklofenak yang berbasis
kombinasi polimer HPMC dan NaCMC.
1.5 Manfaat
Penelitian ini dapat memberikan informasi tentang karakteristik
patch yang menggunakan kombinasi polimer HPMC dan NaCMC sebagai
matriks dalam pengembangan sediaan patch natrium diklofenak yang
digunakan secara lokal untuk penanganan inflamasi pada penyakit
4
BAB 2
TINJAUAN PUSTAKA
2.1 Penyakit Periodontal
Penyakit periodontal merupakan penyakit mulut yang paling umum
terjadi dan menjadi penyebab utama kehilangan gigi pada orang dewasa.
Akumulasi plak gigi oleh mikroba merupakan faktor etiologi utama penyakit
periodontal maupun karies gigi. Kerentanan terhadap penyakit periodontal
juga dipengaruhi oleh mekanisme pertahanan host terhadap infeksi bakteri
dan faktor risiko lain seperti kalkulus dan merokok (Clarkson et al., 2013).
Infeksi periodontal disebabkan oleh bakteri yang mengkolonisasi
permukaan gigi dan jaringan gingiva sekitarnya untuk membentuk plak gigi.
Plak gigi adalah biofilm polimikrobial kompleks. Istilah biofilm digunakan
untuk menggambarkan komunitas mikroba yang menempel pada permukaan
benda mati atau hidup. Bakteri yang tumbuh pada biofilm mengikuti
keadaan permukaan padat di mana mereka berkembang biak dan
membentuk mikrokoloni yang melekat pada matriks polimer ekstraseluler
(Panagakos FS dan Robin M. Davies, 2011).
Jaringan periodontal terdiri dari gingiva, mukosa alveolar,
sementum, ligamen periodontal, dan tulang alveolar. Komponen ini
berfungsi untuk menyokong gigi dalam tulang alveolar (Panagakos FS dan
Robin M. Davies, 2011). Penyakit periodontal akan mempengaruhi jaringan
disekitarnya dan penyangga gigi. Penyakit periodontal diklasifikasikan ke
dalam dua kategori besar yaitu gingivitis dan periodontitis (Clarkson et al.,
2013).
Gingivitis umum terjadi pada populasi anak dan dewasa, merupakan
lesi inflamasi dari jaringan gingiva dan telah terbukti bersifat reversible.
Pencegahan gingivitis merupakan langkah pertama dalam pencegahan
periodontitis. Dengan perlakuan yang tepat, proses ini dapat dibalik dan
jaringan periodontal dapat kembali ke keadaan normal. Karakteristik biofilm
plak yang menginduksi gingivitis adalah: (1) biofilm berada pada margin
gingiva, (2) perubahan warna gingiva, (3) perubahan kontur gingiva, (4)
UIN Syarif Hidayatullah Jakarta
(7) tidak adanya kehilangan perlekatan, (8) tidak adanya keropos tulang, dan
(9) perubahan histologis. Intensitas tanda dan gejala klinis akan bervariasi
antar individu serta bergantung pada bagian gigi yang terinfeksi (Panagakos
FS dan Robin M. Davies, 2011).
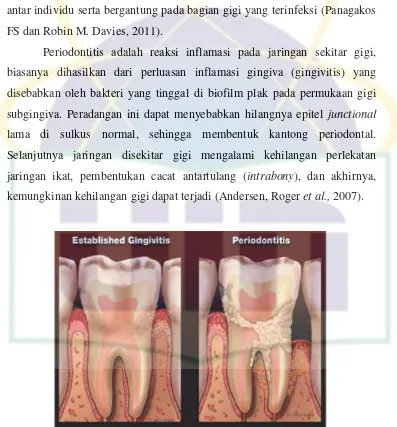
Periodontitis adalah reaksi inflamasi pada jaringan sekitar gigi,
biasanya dihasilkan dari perluasan inflamasi gingiva (gingivitis) yang
disebabkan oleh bakteri yang tinggal di biofilm plak pada permukaan gigi
subgingiva. Peradangan ini dapat menyebabkan hilangnya epitel junctional
lama di sulkus normal, sehingga membentuk kantong periodontal.
Selanjutnya jaringan disekitar gigi mengalami kehilangan perlekatan
jaringan ikat, pembentukan cacat antartulang (intrabony), dan akhirnya,
kemungkinan kehilangan gigi dapat terjadi (Andersen, Roger et al., 2007).
Keterangan: Bagian kiri: tanda-tanda klinis dari inflamasi (kemerahan, edema, perdarahan) dan tanda-tanda kehilangan perlekatan periodontal atau kehilangan tulang alveolar tidak jelas. Bagian kanan: Hasil respon inflamasi ditandai dengan kerusakan kolagen dan periodontal serta kehilangan tulang alveolar, dan tanda-tanda klinis dari peradangan.
Gambar 2.1. Keadaan Gingivitis dan Periodontitis [sumber : Panagakos FS dan Robin M. Davies, 2011]
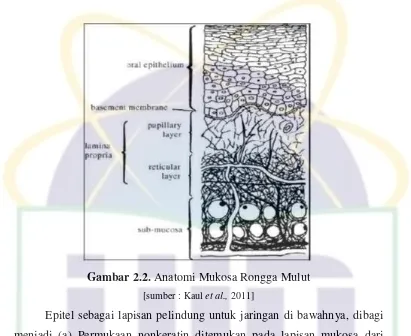
2.2 Anatomi Mukosa Rongga Mulut
Oral mukosa tersusun dari lapisan terluar epitel berlapis. Di bawahnya
terdapat sebuah membran basal, lamina propria diikuti oleh submukosa
6
UIN Syarif Hidayatullah Jakarta Gambar 2.2. Anatomi Mukosa Rongga Mulut
[sumber : Kaul et al., 2011]
Epitel sebagai lapisan pelindung untuk jaringan di bawahnya, dibagi
menjadi (a) Permukaan nonkeratin ditemukan pada lapisan mukosa dari
langit-langit lunak, permukaan ventral lidah, dasar mulut, mukosa alveolar,
vestibulum, bibir, dan pipi. (b) Epitel keratin ditemukan di palatal keras dan
area nonfleksibel dari rongga mulut. Sel-sel epitel yang berasal dari sel-sel
basal, matang, mengubah bentuk mereka, dan bertambah besar saat bergerak
menuju permukaan (Kaul et al., 2011).
Ketebalan mukosa mulut bervariasi tergantung situsnya: mukosa
bukal memiliki ketebalan 500-800 µm, sementara ketebalan mukosa dari
palatal keras dan lunak, dasar mulut, ventral lidah, dan gingiva memiliki
ukuran sekitar 100-200 µm. Secara umum, permeabilitas mukosa mulut jika
diurutkan sublingual lebih besar dari bukal, dan bukal lebih besar dari
palatal. Urutan peringkat ini didasarkan pada ketebalan relatif dan tingkat
keratinisasi jaringan ini, dimana mukosa sublingual relatif tipis dan
nonkeratin, bukal tebal dan nonkeratin, dan palatal menengah dalam
ketebalan tetapi keratin (Dwivedi et al., 2013).
Terdapat dua rute kemungkinan penyerapan obat melalui epitel
berlapis skuamosa dari mukosa mulut (Dwivedi et al., 2013) :
1) Transeluler (intraseluler, melewati sel).
UIN Syarif Hidayatullah Jakarta
Dalam rongga mukosa mulut, pengiriman obat diklasifikasikan
menjadi tiga kategori :
1) Pengiriman sublingual: terdiri dari administrasi melalui membran dari
permukaan ventral lidah dan dasar mulut. Mukosa sublingual relatif
permeabel, memberikan penyerapan yang cepat dan ketersediaan hayati
yang dapat diterima banyak obat, nyaman, mudah diakses dan umumnya
dapat diterima dengan baik (Singh et al., 2011).
2) Pengiriman bukal: terdiri dari administrasi melalui mukosa bukal,
terutama terdiri dari lapisan pipi. Mukosa bukal kurang permeabel
dibandingkan daerah sublingual, umumnya tidak mampu memberikan
penyerapan yang cepat dan ketersediaan hayati yang baik dibandingkan
administrasi sublingual (Singh et al., 2011).
3) Pengiriman lokal: terdiri dari administrasi melalui semua daerah lain
kecuali dua daerah di atas. Pengiriman lokal ke jaringan rongga mulut
memiliki sejumlah aplikasi, termasuk pengobatan sakit gigi, penyakit
periodontal, infeksi bakteri dan jamur, aphthous, dan stomaitis gigi serta
dalam memfasilitasi perpindahan gigi dengan prostaglandin (Singh et
al., 2011).
2.3 Gingiva
Gingiva adalah jaringan fibrosa berserat, ditutupi oleh epitel keratin,
yang mengelilingi gigi dan berbatasan dengan ligamen periodontal dan
jaringan mukosa mulut (The American Academy of Periodontology, 2001).
Gingiva dengan kuat terikat pada tulang di bawahnya dan terhubung dengan
mukosa alveolar yang terletak pada bagian apikal dalam keadaan tidak
terikat. Perbatasan dua jenis jaringan ini disebut mucogingival junction.
Gingiva terdiri dari gingiva bebas dan gingiva attached (Panagakos FS dan
Robin M. Davies, 2011). Gingiva bebas merupakan bagian dari gingiva yang
mengelilingi gigi dan tidak langsung melekat pada permukaan gigi
sedangkan gingiva attached merupakan bagian gingiva yang kuat, padat,
berbintik, dan terikat erat ke dasar periosteum, gigi, dan tulang (The
American Academy of Periodontology, 2001). Lebar gingiva attached
8
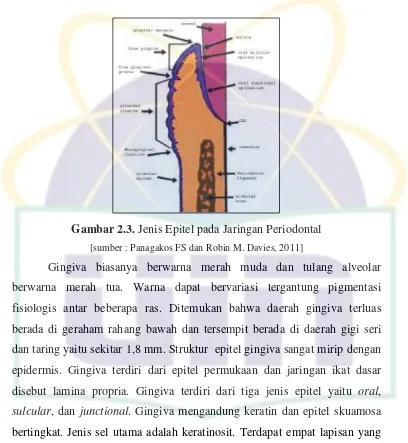
UIN Syarif Hidayatullah Jakarta Gambar 2.3. Jenis Epitel pada Jaringan Periodontal
[sumber : Panagakos FS dan Robin M. Davies, 2011]
Gingiva biasanya berwarna merah muda dan tulang alveolar
berwarna merah tua. Warna dapat bervariasi tergantung pigmentasi
fisiologis antar beberapa ras. Ditemukan bahwa daerah gingiva terluas
berada di geraham rahang bawah dan tersempit berada di daerah gigi seri
dan taring yaitu sekitar 1,8 mm. Struktur epitel gingiva sangat mirip dengan
epidermis. Gingiva terdiri dari epitel permukaan dan jaringan ikat dasar
disebut lamina propria. Gingiva terdiri dari tiga jenis epitel yaitu oral,
sulcular, dan junctional. Gingiva mengandung keratin dan epitel skuamosa
bertingkat. Jenis sel utama adalah keratinosit. Terdapat empat lapisan yang
berbeda, yaitu stratum basal, stratum spinosum, stratum granulosum, dan
stratum korneum. Tekstur gingiva bervariasi tergantung usia. Pada
umumnya halus pada masa muda, terdapat bintik-bintik pada masa dewasa,
dan menjadi lebih halus pada usia lanjut (Panagakos FS dan Robin M.
Davies, 2011).
2.4 Mukoadhesif
Istilah mukoadhesif umumnya digunakan untuk bahan-bahan yang
mengikat lapisan musin dari membran biologis. Bentuk sediaan ini meliputi
tablet, patch, tape, film, semipadat, dan bubuk. Untuk menjadi polimer
mukoadhesif, polimer harus memiliki beberapa fitur fisikokimia umum
UIN Syarif Hidayatullah Jakarta
1) Hidrofilisitas anion terutama sejumlah kelompok yang dapat membentuk
ikatan hidrogen (Dwivedi et al., 2013).
2) Sifat permukaan yang sesuai untuk membasahi lendir atau mukosa
permukaan jaringan (Dwivedi et al., 2013).
Mekanisme adhesi makromolekul tertentu ke permukaan jaringan
mukosa belum dipahami dengan baik. Mukoadhesif harus tersebar di
substrat untuk memulai kontak yang kuat sehingga meningkatkan kontak
permukaan, mendorong difusi rantai di dalam mukus. Gaya tarikan dan
tolakan akan timbul. Agar mukoadhesif berhasil, kekuatan tarik harus lebih
mendominasi. Setiap langkah dari mekanisme adhesi dipengaruhi oleh sifat
dari bentuk sediaan dan bagaimana sediaan diberikan.
Mekanisme mukoadhesi umumnya dibagi dalam dua langkah:
1) Tahap kontak
Tahap ini ditandai oleh kontak antara bahan mukoadhesif dengan selaput
lendir, disertai dengan penyebaran dan pembengkakan formulasi
selanjutnya memulai kontak lebih dalam hingga menembus lapisan
mukus (Kaul et al., 2011).
2) Tahap konsolidasi
Pada tahap ini bahan mukoadhesif diaktifkan oleh adanya kelembaban.
Sistem moisture plasticizes, yang memungkinkan molekul mukoadhesif
untuk bebas dan terhubung dengan adanya ikatan Van der waals dan
ikatan hidrogen pada lapisan mukus (Kaul et al., 2011).
10
UIN Syarif Hidayatullah Jakarta
Terdapat enam teori klasik yang diadaptasi dari studi tentang kinerja
beberapa bahan dan polimer adhesif :
1) Teori elektronik
Mekanisme : Gaya elektrostatik menarik antara glikoprotein jaringan
musin dan bahan bioadhesif. Transfer elektron terjadi antara dua bentuk
lapisan ganda muatan listrik pada permukaan (Kaul et al., 2011).
2) Teori pembasahan
Mekanisme : Kemampuan polimer bioadhesif untuk melakukan
penyebaran dan pengembangan sehingga meningkatkan kontak dengan
selaput lendir. Penyebaran koefisien polimer harus positif. Kontak sudut
antara polimer dan sel-sel harus mendekati nol (Kaul et al., 2011).
3) Teori adsorpsi
Mekanisme : gaya permukaan yang dihasilkan dari ikatan kimia. Gaya
primer kuat dihasilkan oleh ikatan kovalen. Gaya sekunder lemah
dihasilkan oleh ikatan hidrogen dan gaya Van der waals (Kaul et al.,
2011).
4) Teori difusi
Mekanisme : Keterikatan fisik untai musin dan rantai polimer fleksibel.
Untuk difusi dan kekuatan adhesi maksimum, parameter kelarutan
polimer bioadhesif dan glikoprotein mukus harus sama (Kaul et al.,
2011).
5) Teori mekanik
Mekanisme : Adhesi muncul dari keterikatan bahan adhesif cair pada
permukaan kasar yang tidak teratur. Permukaan kasar meningkatkan luas
permukaan untuk interaksi dan peningkatan viskoelastis serta
mengurangi faktor penyebab kegagalan pelekatan (Kaul et al., 2011).
6) Teori fraktur
Mekanisme : Analisis gaya yang dibutuhkan untuk memisahkan dua
permukaan setelah adhesi terbentuk. Gaya ini sering dihitung dalam uji
ketahanan terhadap pecahnya ikatan dengan rasio kekuatan pemisahan
maksimal dan total luas permukaan yang terlibat dalam interaksi
UIN Syarif Hidayatullah Jakarta
Polimer mukoadhesif terdiri dari polimer larut air dan tidak larut
air yang dapat mengembang dan digabungkan menggunakan agen
cross-linking. Polimer harus memiliki polaritas yang optimal agar terjadi
pembasahan yang cukup oleh mukus serta aliran optimal agar adsoprsi dan
interpenetrasi antar polimer dan mukus dapat berlangsung (Yadaf et al.,
2010).
Polimer mukoadhesif yang melekat pada permukaan epitel musin
secara luas dapat dibagi menjadi 3 kelas, yaitu :
1) Polimer yang menjadi lengket ketika berkontak dengan air dan
memperlihatkan sifat bioadhesifitasnya.
2) Polimer yang melekat secara tidak spesifik, melalui interaksi nonkovalen
terutama ikatan elektrostatik (seperti, ikatan hidrogen dan ikatan
hidrofobik).
3) Polimer yang berikatan secara spesifik dengan reseptor di permukaan
(Yadaf et al., 2010).
Polimer mukoadhesif yang ideal memiliki karakteristik sebagai
berikut :
1) Tidak beracun dan harus dapat diserap dari saluran pencernaan.
2) Tidak menyebabkan iritasi pada membran mukosa.
3) Sebaiknya dapat membentuk ikatan nonkovalen yang kuat dengan
permukaan sel epitel musin.
4) Harus melekat cepat pada jaringan dan harus memiliki beberapa daerah
spesifik.
5) Kompatibel dengan obat dan tidak menghambat pelepasan obat.
6) Polimer tidak terurai pada penyimpanan atau selama masa simpan
sediaan.
7) Harga polimer tidak terlalu mahal sehingga bentuk sediaan yang
dihasilkan tetap kompetitif (Yadaf et al., 2010).
Kekuatan bioadhesif polimer dipengaruhi oleh sifat polimer dan sifat
dari lingkungan maupun medium sekitarnya.
1) Faktor terkait polimer
a. Berat molekul
Berat molekul optimal untuk bioadhesi maksimum tergantung pada
12
UIN Syarif Hidayatullah Jakarta
bioadhesif polimer harus memiliki berat molekul minimal 100.000.
Misalnya, polietilen glikol (PEG) dengan berat molekul 20.000,
memiliki kemampuan bioadhesif yang kurang, sedangkan PEG
dengan berat molekul 200.000 dan PEG dengan berat molekul
400.000 memiliki sifat bioadhesif yang lebih baik. Fakta ini
menunjukkan bahwa sifat bioadhesif meningkat dengan semakin
besarnya berat molekul polimer (Yadaf et al., 2010).
b. Konsentrasi polimer aktif
Terdapat konsentrasi optimum polimer bioadhesif untuk
menghasilkan bioadhesi maksimal. Dalam sistem yang mengandung
polimer berkonsentrasi tinggi dan melampaui tingkat optimum akan
menyebabkan kekuatan adhesi turun secara signifikan karena
molekul tergulung menjadi terpisah dari media sehingga rantai yang
digunakan untuk proses interpenetrasi menjadi terbatas (Yadaf et al.,
2010).
c. Fleksibilitas rantai polimer
Hal ini merupakan faktor penting untuk proses interpenetrasi dan
membentuk gulungan. Polimer yang larut dalam air membentuk
ikatan silang, sehingga mobilitas masing-masing rantai polimer
berkurang, dengan demikian panjang rantai efektif yang dapat
menembus ke dalam lapisan mukus berkurang, hal ini akan
mengurangi kekuatan bioadhesif (Yadaf et al., 2010).
d. Konformasi spasial
Selain berat molekul atau panjang rantai, konformasi spasial dari
molekul juga penting. Meskipun dekstran memiliki berat molekul
besar dari 19.500.000, dekstran memiliki kekuatan bioadhesif yang
mirip dengan polietilen glikol dengan berat molekul 200.000.
Konformasi heliks dekstran dapat melindungi gugus aktif pada bahan
bioadhesif, terutama gugus yang bertanggung jawab terhadap sifat
adhesifnya, sedangkan polimer PEG memiliki konformasi linier
UIN Syarif Hidayatullah Jakarta
2) Faktor Lingkungan
a. Lokasi pelekatan
Lokasi pelekatan dari sistem bioadhesi mempengaruhi kekuatan
adhesinya. Kekuatan adhesi meningkat dengan kekuatan saat aplikasi
atau dengan durasi pengaplikasiannya hingga optimal. Tekanan awal
pengaplikasian pada jaringan mukoadhesif efektif dalam menentukan
kedalaman dari saling berpenetrasi. Jika tekanan tinggi diterapkan
untuk jangka waktu yang cukup lama, polimer dapat menjadi
mukoadhesif walaupun polimer tersebut tidak memiliki interaksi
yang menarik dengan mukus (Yadaf et al., 2010).
b. pH
Hal ini dapat mempengaruhi muatan pada permukaan mukus serta
polimer bioadhesif terionisasi tertentu. Mukus akan memiliki
kerapatan muatan yang berbeda bergantung pada pH. Hal ini
dikarenakan perbedaan dalam disosiasi gugus fungsi pada bagian
karbohidrat dan asam amino dari rantaipolipeptida. pH medium juga
penting untuk tingkat hidrasi asam poliakrilat silang, dimana
menunjukkan peningkatan konsisten hidrasi pada pH 4 sampai 7
kemudian mengalami penurunan pada suasana alkali dan
meningkatkan kekuatan ion (Yadaf et al., 2010).
c. Waktu kontak awal
Waktu kontak antara bahan bioadhesif dan lapisan mukus
menentukan derajat pengembangan dan interpenetrasi dari rantai
polimer bioadhesif. Selain itu, kekuatan bioadhesif meningkat
dengan peingkatan waktu kontak awal (Yadaf et al., 2010).
d. Pembengkakan
Hal ini tergantung pada konsentrasi polimer, konsentrasi ion, serta
keberadaan air (Yadaf et al., 2010).
3) Perubahan fisiologis
a. Waktu pergantian musin
Pergantian musin secara normal sangat penting karena dua alasan.
Yang pertama, pergantian musin mengakibatkan adanya batasan
pelekatan dari bahan mukoadhesif pada lapisan mukus. Walaupun
14
UIN Syarif Hidayatullah Jakarta
dapat terlepas akibat pergantian musin. Alasan yang kedua,
pergantian musin menghasilkan senyawa antara yang larut dalam
molekul musin. Molekul tersebut berinteraksi dengan bahan
mukoadhesi sebelum memberi kesempatan untuk berinteraksi
dengan lapisan mukosa. Pergantian musin bergantung pada faktor
lain seperti makanan (Yadaf et al., 2010).
b. Fisikokimia mukus
Fisikokimia dari mukus dipengaruhi oleh berbagai kondisi yang
diakibatkan suatu penyakit, seperti flu, tukak lambung, infeksi
bakteri dan jamur pada saluran reproduksi wanita (Yadaf et al.,
2010).
2.5 Patch
Patch merupakan suatu bentuk sediaan matriks tipis yang tidak larut
terdiri dari satu atau lebih lapisan atau film polimer yang mengandung obat
dan/atau eksipien lain. Patch dapat mengandung lapisan polimer
mukoadhesif yang berikatan dengan mukosa mulut, gingiva, atau gigi untuk
mengontrol pelepasan obat ke mukosa mulut (pelepasan searah), rongga
mulut (pelepasan searah), atau keduanya (pelepasan dua arah). Patch
dilepaskan dari mulut dan dibuang setelah jangka waktu tertentu. Patch ideal
harus fleksibel, elastis, dan lembut namun cukup kuat untuk menahan
kerusakan akibat aktivitas mulut. Selain itu, patch juga harus menunjukkan
kekuatan mukoadhesif yang baik sehingga dapat bertahan di mulut sesuai
waktu yang diharapkan (Shravan, et al., 2012).
Patch terdiri dari dua tipe yaitu :
1) Tipe matriks (dua arah) : patch dibuat dalam bentuk matriks
mengandung obat, bahan adhesive, dan zat tambahan yang dicampurkan
bersama. Patch dua arah melepaskan obat pada mukosa dan mulut
(Shravan, et al., 2012).
2) Tipe reservoir (searah) : patch dibuat dalam sistem reservoir
mengandung sebuah ruang untuk obat dan zat tambahan terpisah dari
bahan adhesif. Lapisan backing impermeable digunakan untuk
UIN Syarif Hidayatullah Jakarta
bentuk dan hancurnya patch ketika di mulut; dan untuk mencegah
kehilangan obat (Shravan, et al., 2012).
Proses pembuatan patch :
1) Solvent casting method : solvent casting merupakan proses yang banyak
digunakan untuk pembuatan patch. Hal ini dikarenakan prosesnya
mudah dan murah. Biasanya digunakan untuk penelitian skala labor.
Terdiri dari enam langkah :
a. Pembuatan larutan cetak
b. Deaeration larutan (menghilangkan molekul udara dari larutan)
c. Pemindahan larutan ke dalam cetakan sesuai volume yang
dibutuhkan
d. Pengeringan larutan
e. Pemotongan sediaan kering yang mengandung sejumlah obat yang
diinginkan
f. Pengemasan
Reologi larutan cetak akan menentukan derajat pengeringan dan
keseragaman kandungan zat aktif serta penampilan fisik film. Patch
yang terbentuk dari larutan yang mengandung gelembung udara akan
menghasilkan permukaan yang tidak rata dan ketebalan yang heterogen
(Shravan, et al., 2012).
2) Direct milling : pada metode ini, patch dibuat tanpa menggunakan
pelarut. Obat dan eksipien secara mekanis dicampur dengan
penggilingan langsung atau dengan meremas, tanpa adanya cairan.
Setelah proses pencampuran, bahan yang dihasilkan digulung pada
release liner sampai ketebalan yang diinginkan tercapai. Bahan backing
kemudian dilaminasi seperti yang dijelaskan sebelumnya (Shravan, et
al., 2012).
3) Hot melt extrusion : pada metode ini bahan dilelehkan dan kemudian
ditekan melalui sebuah lubang untuk menghasilkan bahan yang
homogen dalam berbagai bentuk seperti butiran, tablet, atau film.
Metode ini telah digunakan untuk pembuatan tablet matriks dengan
pelepasan terkendali, pelet dan butiran serta film yang hancur di mulut
16
UIN Syarif Hidayatullah Jakarta
4) Semisolid casting : pada metode ini, awalnya disiapkan larutan film larut
air pembentuk polimer. Larutan yang dihasilkan ditambahkan ke larutan
polimer tidak larut asam (seperti, selulosa asetat ptalat, selulosa asetat
butirat) yang disiapkan pada ammonium atau NaOH. Kemudiah
sejumlah plasticizer ditambahkan sehingga membentuk massa gel.
Setelah itu massa gel dicetak menjadi film menggunakan heat control
drums (Sharma et al., 2012).
5) Solid dispersion extrusion : pada metode ini digunakan untuk komponen
yang tidak dapat dicampur dengan obat. Selanjutnya dispersi padat
dibentuk menjadi film oleh die (Sharma et al., 2012).
6) Rolling method : dalam metode rolling larutan atau suspensi yang
mengandung obat digulung pada pembawa. Larutan utama air dan
campuran air dan alkohol. Film dikeringkan di roller dan dipotong
sesuai bentuk dan ukuran yang diinginkan (Sharma et al., 2012).
Komposisi utama patch terdiri dari :
1) Zat aktif
Menurut literatur zat aktif yang dapat ditambahkan yaitu 5%-25% b/b
dari berat total polimer. Untuk formulasi yang efektif, dosis obat yang
digunakan harus dalam milligram (kurang dari 20 mg/hari). Obat yang
mengalami first pass metabolism dan obat untuk pasien noncompliant
merupakan obat yang sesuai untuk dibuat dalam bentuk patch
mukoadhesif (R. Yogananda dan Rakesh Bulugondla, 2012).
2) Polimer mukoadhesif
Polimer mukoadhesif digunakan agar perangkat pengiriman obat
melekat pada daerah target dan menghasilkan penghantaran obat yang
maksimal karena dapat kontak dalam waktu yang lama (R. Yogananda
dan Rakesh Bulugondla, 2012).
3) Backing membran
Backing membran yang Impermeable dapat digunakan untuk mengontrol
arah pelepasan obat, mencegah hilangnya obat, dan meminimalkan
perubahan bentuk dan hancurnya device selama waktu aplikasi (R.
UIN Syarif Hidayatullah Jakarta
4) Peningkat penetrasi
Peningkat penetrasi merupakan senyawa yang dapat meningkatkan laju
permeasi pada membran mukosa. Bahan harus aman, tidak toksik, secara
farmakologi dan secara kimia inert, tidak mengiritasi serta nonalergi
(Kaul, et al., 2011).
5) Plasticizer
Merupakan unsur yang penting dalam formulasi film. Sifat mekanis
seperti daya tarik dan elongasi film dapat ditingkatkan menggunakan
plasticizer. Agen ini juga dapat meningkatkan fleksibilitas film dan
mengurangi kerapuhan film. Aliran polimer juga akan lebih baik dengan
penambahan plasticizer (R. Yogananda dan Rakesh Bulugondla, 2012).
6) Zat tambahan lain seperti bahan pengencer, bahan perasa dan pemanis
(R. Yogananda dan Rakesh Bulugondla, 2012).
2.6 Natrium Diklofenak
Natrium diklofenak memiliki nama kimia natrium
2-[(2,6-diklorofenil)amino]fenil]asetat dan rumus molekul C14H10Cl2NNaO2 dengan
berat molekul 318,1 serta memiliki titik lebur pada suhu 280ºC. Natrium
diklofenak berwarna putih atau agak kekuningan, sedikit higroskopis, dan
berbentuk bubuk kristal. Natrium diklofenak sedikit larut dalam air, mudah
larut dalam metanol, larut dalam etanol 96%, sedikit larut dalam aseton
(British Pharmacopoiea, 2009).
Gambar 2.5. Struktur Kimia Natrium Diklofenak [sumber : Sweetman, 2009]
Diklofenak, turunan asam fenilasetat, merupakan golongan NSAID.
Diklofenak sering digunakan terutama dalam bentuk garam natrium untuk
menghilangkan rasa sakit dan peradangan dalam berbagai kondisi
(Sweetman, 2009). Obat antiradang bukan steroid atau yang lazim
18
UIN Syarif Hidayatullah Jakarta
golongan obat yang terutama bekerja perifer, memiliki aktivitas penghambat
radang dengan mekanisme kerja menghambat biosintesis prostaglandin
melalui penghambatan aktivitas enzim siklooksigenase (Kartasasmita,
2002).
Pada umumnya dosis oral atau rektal natrium diklofenak adalah
75-150 mg sehari dalam dosis terbagi. Sediaan natrium diklofenak
modified-release tersedia untuk pemberian oral. Diklofenak juga diberikan secara
intramuskular, intravena, dan topikal. Natrium diklofenak digunakan sebagai
larutan tetes mata 0,1% pada sejumlah kondisi (Sweetman, 2009).
Absorpsi obat ini melalui saluran cerna berlangsung cepat dan
lengkap. Obat ini terikat 99% pada protein plasma dan mengalami efek
metabolisme lintas pertama (first pass) sebesar 40-50%. Walaupun waktu
paruh singkat yakni 1-3 jam, diklofenak diakumulasi di cairan sinovial yang
menjelaskan efek terapi di sendi jauh lebih panjang dari waktu paruh obat
tersebut (Nalfriadi dan Rianto Setiabudy, 2007). Diklofenak dimetabolisme
menjadi 4'- hidroksidiklofenak, 5-hidroksidiklofenak, 3'- hidroksidiklofenak
dan 4',5- di hidroksidiklofenak. Obat ini kemudian diekskresikan dalam
bentuk glukuronida dan konjugat sulfat, terutama dalam urin (sekitar 60%),
dan juga dalam empedu (sekitar 35%), kurang dari 1% diekskresikan
sebagai diklofenak (Sweetman, 2009).
Efek samping yang lazim adalah mual, gastritis, eritema kulit dan
sakit kepala sama seperti semua NSAID, pemakaian obat ini harus
berhati-hati pada pasien tukak lambung. Peningkatan enzim transaminase dapat
terjadi pada 15% pasien dan umumnya kembali ke normal (Nalfriadi dan
Rianto Setiabudy, 2007).
Pemberian diklofenak secara sistemik dikontraindikasikan pada
pasien dengan gangguan hati atau ginjal berat. Selain itu, penggunaan
diklofenak secara intravena dikontraindikasikan pada pasien dengan
gangguan ginjal sedang atau berat, hipovolemia, atau dehidrasi, dan tidak
boleh diberikan secara intravena pada pasien dengan riwayat hemoragik
diatesis, perdarahan serebrovaskuler (termasuk yang dicurigai), atau asma
atau pada pasien yang menjalani operasi dengan risiko tinggi perdarahan
UIN Syarif Hidayatullah Jakarta 2.7 Hidroksi Propil Metil Selulosa (HPMC)
Hidroksi Propil Metil Selulosa dengan nama lain Benecel MHPC;
hypromellose; E464; HPMC; hypromellosum; Methocel; methylcellulose
propylene glycol ether; methyl hydroxypropylcellulose; Metolose; MHPC;
Pharmacoat; Tylopur; Tylose MO; memiliki berat molekul sekitar
10.000-1.500.000 (Rowe, Paul and Marian, 2009).
Keterangan: R adalah H, CH3, atau CH3CH(OH)CH2
Gambar 2.6. Struktur Kimia HPMC [sumber : Rowe, Paul and Marian, 2009]
HPMC tidak berbau dan berasa, putih atau berserat berbentuk granul
bubuk berwarna putih kekuningan. Larut dalam air dingin, membentuk
larutan koloid kental, praktis tidak larut dalam air panas, kloroform, etanol
(95%), dan eter, tetapi larut dalam campuran etanol dan diklorometana,
campuran metanol dan diklorometana, serta campuran air dan alkohol.
Beberapa grade dari HPMC larut dalam larutan aseton, campuran aseton dan
propan-2-ol, dan pelarut organik lainnya. Beberapa grade dapat
mengembang dalam etanol. Berbagai macam jenis viskositas tersedia secara
komersial (Rowe, Paul and Marian, 2009).
HPMC sering digunakan sebagai eksipien dalam formulasi farmasi
oral, mata, hidung, dan topikal sebagai bahan bioadhesif, zat penyalut, zat
pendispersi, zat pengemulsi, penstabil emulsi, zat pembentuk film, foaming
agent, membantu proses granulasi, bahan mukoadhesif, pengikat tablet,
peningkat viskositas dan digunakan untuk mengatur kecepatan pelepasan
obat. HPMC juga digunakan secara luas dalam kosmetik dan produk
makanan. HPMC umumnya dianggap sebagai bahan nontoksik dan tidak
menyebabkan iritasi. Mengkonsumsi HPMC oral dengan berlebihan dapat
mengakibatkan efek pencahar. WHO belum menyatakan asupan harian yang
20
UIN Syarif Hidayatullah Jakarta
HPMC tidak bercampur dengan beberapa zat pengoksidasi kuat.
HPMC merupakan polimer nonionik, sehingga tidak membentuk kompleks
dengan garam logam atau ion organik dan tidak membentuk endapan yang
tidak terlarut. Larutan HPMC stabil pada pH 3-11 (Rowe, Paul and Marian,
2009).
2.8 Natrium Karboksi Metil Selulosa (NaCMC)
Natrium Karboksi Metil Selulosa dengan nama lain Akucell;
Aqualon CMC; Aquasorb; Blanose; Carbose D; carmellosum natricum;
Cel-O-Brandt; cellulose gum; Cethylose; CMC sodium; E466; Finnfix;
Glykocellan; Nymcel ZSB; SCMC; sodium cellulose glycolate; Sunrose;
Tylose CB; Tylose MGA; Walocel C; Xylo-Mucine. NaCMC memiliki bobot
molekul 90.000-700.000 dan titik lebur sekitar 227-252ºC (Rowe, Paul and
Marian, 2009).
NaCMC berwarna putih hingga hampir putih, tidak berbau dan
berasa, bubuk granular serta bersifat higroskopis setelah pengeringan.
Praktis tidak larut dalam aseton, etanol (95%), eter, dan toluena. Mudah
terdispersi dalam air pada semua suhu, membentuk larutan koloid jernih.
Kelarutan dalam air bervariasi tergantung pada derajat substitusi (Rowe,
Paul and Marian, 2009). Film oral dengan polimer NaCMC dapat stabil
ketika polimer dilarutkan dalam campuran air dan alkohol yang
ditambahkan hingga mencapai batas tertentu, ketika campuran air dan
alkohol berlebih atau alkohol murni digunakan polimer akan cepat
mengendap (Nagar, Chauhan & Yasir, 2011).
UIN Syarif Hidayatullah Jakarta
Viskositas larutan 1% b/v NaCMC memiliki nilai 5-2000 mPa
(5-2000 cP). Peningkatan konsentrasi menghasilkan peningkatan viskositas
larutan. Pemanasan yang lama pada suhu tinggi dapat menurunkan
viskositas. Larutan kental NaCMC stabil pada pH 4-10. Nilai pH optimum
adalah netral (Rowe, Paul and Marian, 2009).
NaCMC digunakan dalam beberapa formulasi oral, topikal, dan
parenteral sebagai zat penyalut, penstabil, suspending agent, disintegran
tablet dan kapsul, pengikat tablet, zat peningkat viskositas dan zat penyerap
air. NaCMC juga banyak digunakan dalam kosmetik, perlengkapan mandi
dan produk makanan. Pada umumnya NaCMC dianggap sebagai bahan
nontoksik dan noniritasi. Namun, mengkonsumsi NaCMC oral dalam
jumlah besar dapat mengakibatkan efek pencahar. WHO belum menetapkan
asupan harian yang dapat diterima untuk NaCMC sebagai bahan tambahan
makanan karena tingkat yang diperlukan untuk mencapai efek yang
diinginkan tidak dianggap berbahaya bagi kesehatan (Rowe, Paul and
Marian, 2009).
NaCMC tidak cocok dengan xanthan gum, larutan asam kuat dan
senyawa logam seperti aluminium, merkuri, dan zink. Pengendapan terjadi
apabila nilai pH kurang dari 2 dan ketika dicampur dengan etanol 95%.
Membentuk kompleks dengan gelatin, pektin, dan kolagen. NaCMC
merupakan bahan yang stabil walaupun higroskopis. Di bawah kondisi
lembab dapat menyerap sejumlah besar (>50%) air. Larutan aqueous stabil
pada pH 2-10 dan kekentalan larutan menurun dengan cepat di atas pH 10.
Secara umum viskositas dan stabilitas maksimum pada pH 7-9 (Rowe, Paul
and Marian, 2009).
Polimer NaCMC digunakan sebagai penghantar mukoadhesif karena
kemampuannya dalam membentuk ikatan hidrogen yang kuat dengan musin
pada lapisan mukosa (Grag et al., 2011). NaCMC memiliki gugus fungsi
karboksil yang memberikan muatan negatif pada nilai pH yang melebihi
nilai pKa polimer (Singh, Govind, & Bothara, 2013).
2.9 Poliuretan
Poliuretan (PU) adalah kelas polimer yang mengandung sejumlah
22
UIN Syarif Hidayatullah Jakarta
kimia antara gugus hidroksil dan kelompok isosianat. PU merupakan
kelompok polimer yang banyak digunakan sebagai biomaterial dalam
aplikasi klinis. Hal ini dikarenakan PU memiliki sifat fisik dan mekanik
yang sangat baik dan kompatibilitasnya terhadap darah relatif baik.
Kelompok polimer ini memiliki keragaman karena adanya perbedaan
komposisi kimia dan sifat seperti elastisitas, toleransi dalam tubuh, daya
tahan dan penyesuaian, yang umumnya lebih baik daripada polimer lain
(Istanbullu et al., 2013).
Tegaderm adalah film transparan dengan backing hipoallergenik,
bebas latex yang menempel dengan baik, lembut dan aman bagi kulit.
Bersifat breathable, steril, transparan dan tahan air, serta dapat melindungi
dari berbagai kontaminan eksternal. Breathability dari Tegaderm
memungkinkan terjadinya penguapan air dan pertukaran gas yang sangat
penting untuk menjaga fungsi kulit normal. Tegaderm memiliki adhesi awal
yang baik dan tidak mengakibatkan peningkatan adhesi yang berlebihan
pada waktu diaplikasikan, bahkan untuk penggunaan dalam waktu yang
lama, risiko ketidaknyamanan pasien dan trauma kulit jarang terjadi ketika
tegaderm dilepas dengan benar (3MTM, 2012).
Gambar 2.8. Struktur Kimia Poliuretan [sumber : Istanbullu et al., 2013]
Penelitian yang dilakukan Desai et al. (2012) menggunakan lapisan
backing film Tegaderm pada sediaan patch mukoadhesif oral yang
mengandung fenretinide untuk kemoprevensi penyakit kanker mulut. Selain
itu, Jadhav et al. (2009) melakukan uji iritasi primer pada manusia terhadap
sediaan patch transdermal natrium diklofenak yang mengandung backing
membran 3M (tegaderm) dan dihasilkan bahwa film transdermal tidak
23
3.1. Tempat dan Waktu Penelitian
Tempat penelitian dilaksanakan di Laboratorium Penelitian 1,
Laboratorium Penelitian 2 dan Laboratorium Sediaan Padat Program Studi
Farmasi Fakultas Kedokteran dan Ilmu Kesehatan UIN Syarif
Hidayatullah Jakarta. Laboratorium Multiguna dan Laboratorium Biologi
Program Studi Pendidikan Dokter Fakultas Kedokteran dan Ilmu
Kesehatan UIN Syarif Hidayatullah Jakarta. Penelitian berlangsung 4
bulan, dari bulan Januari hingga April 2014.
3.2. Alat dan Bahan
3.2.1 Alat
Dissolution tester (erweka DT626HH), disintegrator (electrolab
ED-2L), spektrofotometer UV visible (hitachi U-2910), mikroskop optik
(olympus IX 71, jepang), Oven (eyela NDO- 400, jepang), franz diffusion
cell, timbangan analitik (AND GH-120), viskotester HAAKE 6R,
pengaduk magnetik (advantec SRS710HA), mikrometer digital (mitutoyo,
jepang), freezer, pH meter (horiba F-52), cetakan film, Cutter, gunting,
spuit, vial, dan alat-alat gelas yang sering dipakai di laboratorium.
3.2.2 Bahan
Natrium diklofenak (PT. Indofarma), hidroksi propil metil selulosa
50 cPs (ShinEtsu, Japan), natrium karboksi metil selulosa 50 cPs
(BLANOSE® 7M1F), film tipis transparan TegadermTM 1624 W (3M health Care), propilenglikol (PT. Brataco), gliserin (PT. Brataco), etanol
70%, silica blue (PT. Brataco), natrium hidroksida (Merck), kalium
dihidrogen fosfat (Merck), aquadest, cyanoacrylate adhesive, kertas
24
UIN Syarif Hidayatullah Jakarta 3.3. Prosedur Kerja
3.3.1 Formula Patch
Melalui perhitungan, maka tiap 20 gram formula mengandung
komponen-komponen seperti yang ada dalam tabel 3.1.
3.3.1.1 Preparasi Cairan Pembentuk Film (CPF)
HPMC dan NaCMC ditimbang secara akurat. Kemudian NaCMC
dilarutkan dalam 10 gram aquadest pada gelas beker dan diaduk dengan
menggunakan pengaduk magnetik. Pada beker terpisah, HPMC dilarutkan
dalam 7,5 gram etanol 70% dan diaduk dengan menggunakan pengaduk
magnetik. Setelah kedua polimer larut, campurkan larutan polimer HPMC
ke dalam larutan polimer NaCMC dan aduk hingga homogen. Masukkan
natrium diklofenak, propilenglikol dan gliserin yang sudah dilarutkan
menggunakan sisa etanol 70% ke dalam larutan polimer dan diaduk hingga
homogen dengan bantuan pengaduk magnetik. Kemudian diamkan CPF
untuk menghilangkan molekul udara. Sebelum dimasukkan ke dalam
cetakan, viskositas larutan polimer diukur terlebih dahulu (Chaudhary
Amit, 2012, dengan modifikasi).
Tabel 3.1. Formula Patch Natrium Diklofenak
BAHAN
FORMULA (gram)
F1 F2 F3
Natrium diklofenak 0,02 0,02 0,02
HPMC 0,267 0,2 0,133
Na CMC 0,133 0,2 0,267
Gliserin 0,16 0,16 0,16
Propilen glikol 0,04 0,04 0,04
Aquadest 10 10 10
Etanol 70% add 20 20 20
3.3.1.2 Preparasi Patch
Tahap selanjutnya CPF dituang ke cetakan lalu dikeringkan di dalam oven
suhu 60ºC selama kurang lebih 24 jam. Setelah kering, CPF yang telah
UIN Syarif Hidayatullah Jakarta
disimpan dalam wadah kedap udara yang berisi silika, setelah bobot
konstan film dipotong sesuai ukuran. Sebagian film kemudian dilapisi
dengan backing membran tegaderm sehingga menjadi patch, kemudian
patch dievaluasi karakteristiknya.
3.3.2 Pembuatan Larutan Buffer Fosfat pH 6,8
Dibuat dengan mencampur sebanyak 250 mL larutan kalium dihidrogen
fosfat 0,2 M dengan 112 mL NaOH 0,2 M kemudian dicukupkan
volumenya dengan air bebas karbondioksida hingga volumenya 1000 mL.
3.3.3 Pembuatan Kurva Kalibrasi
3.3.3.1 Penentuan Panjang Gelombang Maksimum ( maks)
Dilakukan scanning panjang gelombang dari larutan standar natrium
diklofenak dengan konsentrasi 6 ppm menggunakan spektrofotometer
UV-Visibel dengan panjang gelombang 200-300 nm (Wardana, 2013).
3.3.3.2 Pembuatan Larutan Standar Natrium Diklofenak
Ditimbang secara akurat 5 mg Natrium diklofenak kemudian dilarutkan
dalam 50 mL buffer fosfat pH 6,8 sehingga diperoleh larutan induk standar
sebesar 100 g/mL. Dari larutan induk tersebut diambil sebanyak 200, 400, 600, 800, dan 1000 L kemudian dicukupkan volumenya hingga 10
mL, sehingga dihasilkan larutan dengan konsentrasi 2, 4, 6, 8, dan 10 ppm.
Masing-masing larutan standar natrium diklofenak diambil dan diukur
absorbansi larutan tersebut dengan panjang gelombang maksimum 275,5
nm sesuai hasil scanning sebelumnya (Wardana,2013).
3.3.4 Evaluasi Viskositas Cairan Pembentuk Film (CPF)
Pengujian dilakukan menggunakan viskotester HAAKE 6R terhadap
setiap CPF sesuai formula menggunakan spindel R2 dengan kecepatan
putar 100 rpm pada suhu ruang (R. Yogananda & Bulugondla, 2012
26
UIN Syarif Hidayatullah Jakarta
3.3.5 Organoleptis Film
Pengamatan mikroskopik penampang membujur dan melintang film serta
makroskopik secara visual fisik film dan patch meliputi warna dan tekstur
permukaan (J. Balasubramanian et al., 2012).
3.3.6 Pengambilan Sampel
Sampel yang akan dikarakterisasi harus memiliki kadar natrium diklofenak
yang sama atau hampir sama. Oleh karena itu, dipilih film dengan bobot
yang sama atau hampir sama, dengan asumsi bahwa film dengan bobot
yang sama memiliki kandungan natrium diklofenak yang sama. Bobot film
dengan luas yang sama dapat dipengaruhi oleh ketebalan film, sehingga
perlu diukur keragaman ketebalan film untuk mendapatkan sampel yang
sama atau hampir sama.
3.3.6.1 Pengukuran Bobot Sampel
Pengujian dilakukan dengan cara menimbang film dan dipilih film dengan
bobot yang sama atau hampir sama kemudian dihitung massa rata-ratanya
dan simpangan bakunya (R. Yogananda & Bulugondla, 2012 dengan
modifikasi).
3.3.6.2 Pengukuran Ketebalan Sampel
Ketebalan film NaCMC diukur dengan mikrometer digital di 3 titik pada
masing-masing film, kemudian dihitung rata-rata ketebalannya dan
dinyatakan dalam satuan mikrometer ( m) (R. Yogananda & Bulugondla,
2012 dengan modifikasi).
3.3.6.3 Pengukuran Kandungan Natrium Diklofenak pada Sampel
Jumlah kandungan obat dari film ditentukan berdasarkan berat kering obat
dan polimer yang digunakan dengan cara metode Spektrofotometer UV.
Tiga unit film dengan bobot yang sama atau hampir sama dari setiap
formula diambil dan dimasukkan ke dalam labu ukur 100 mL,
ditambahkan 100 mL dapar fosfat pH 6,8 dan etanol 70% (1:1) dan aduk
hingga film terlarut sempurna. Larutan disaring, diencerkan dan
UIN Syarif Hidayatullah Jakarta
film dianggap sebagai kandungan obat dalam satu unit film (Chaudhary
Amit, 2012 dengan modifikasi)
3.3.7 Evaluasi Patch
3.3.7.1 Uji Pelipatan
Pengujian dilakukan dengan cara melipat secara berulang satu patch
dengan ukuran 2x1 cm2 pada tempat yang sama hingga patch patah atau dilipat hingga 300 kali secara manual. Jumlah lipatan yang dapat dilipat
pada tempat yang sama tanpa patah memberikan nilai daya tahan lipatan
(R. Yogananda & Bulugondla, 2012 secara triplo).
3.3.7.2 Pengukuran pH Permukaan
Patch dengan ukuran 2x1 cm2 dibiarkan mengembang pada 1 mL aquadest (pH 7) selama 2 jam dalam suhu ruang, kemudian pH permukaan diukur
menggunakan kertas indikator pH universal (R. Yogananda dan
Bulugondla, 2012 dimodifikasi secara triplo).
3.3.7.3 Penetapan Kadar Air Patch
Penetapan kadar air dilakukan menggunakan metode thermogravimetri.
Botol timbang dicuci dan dikeringkan menggunakan oven pada suhu
105±5°C. setelah itu, bobot botol timbang dan sampel diukur
menggunakan timbangan analitik. Sampel dikeringkan menggunakan oven
pada suhu 105±5°C selama satu jam. Kemudian dinginkan pada desikator
selama 15 menit. Bobot sampel diukur kembali. Sampel dipanaskan
kembali hingga bobot konstan (Buckle et al., 2008 dengan modifikasi
secara duplo).
Kadar air dihitung menggunakan persamaan berikut :
Keterangan: Wo = bobot awal sampel, dan Wt = bobot akhir sampel
3.3.7.4 Uji Derajat Pengembangan (Swelling Index Studies)
Patch dengan ukuran 1x1 cm2 dari setiap formula ditimbang secara akurat, kemudian ditempatkan ke dalam cawan petri yang mengandung 25 mL