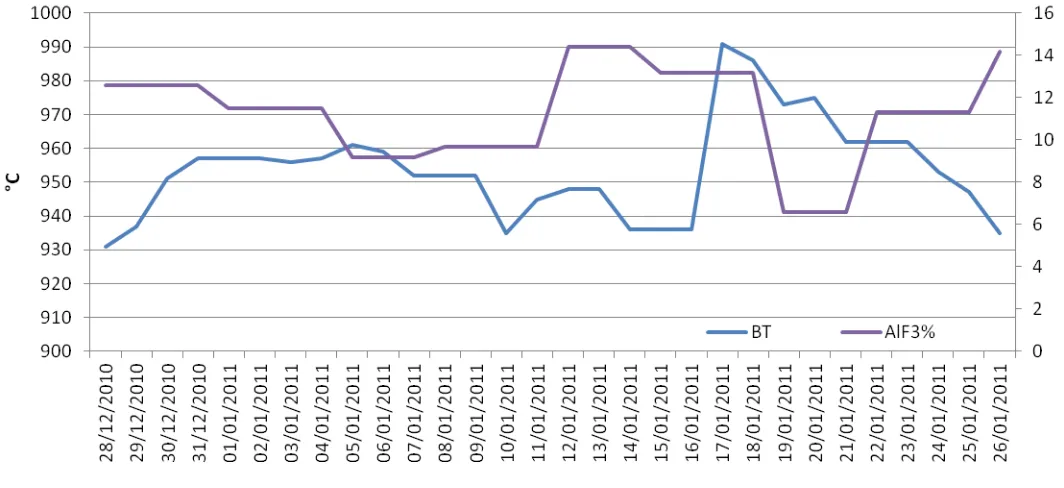
Pengaruh Temperatur Dan Keasaman Bath Terhadap Penambahan AlF3 Pada Pot Reduksi Di PT. Indonesia Asahan Aluminium
Bebas
44
0
0
Teks penuh
Gambar

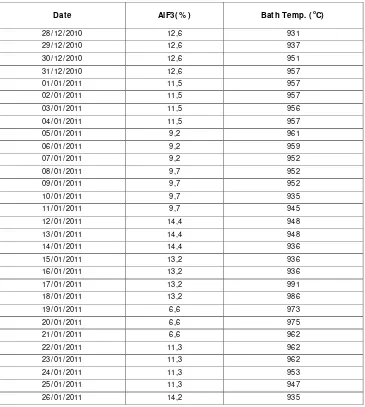
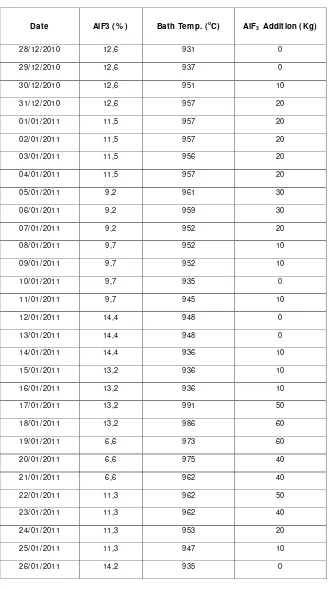
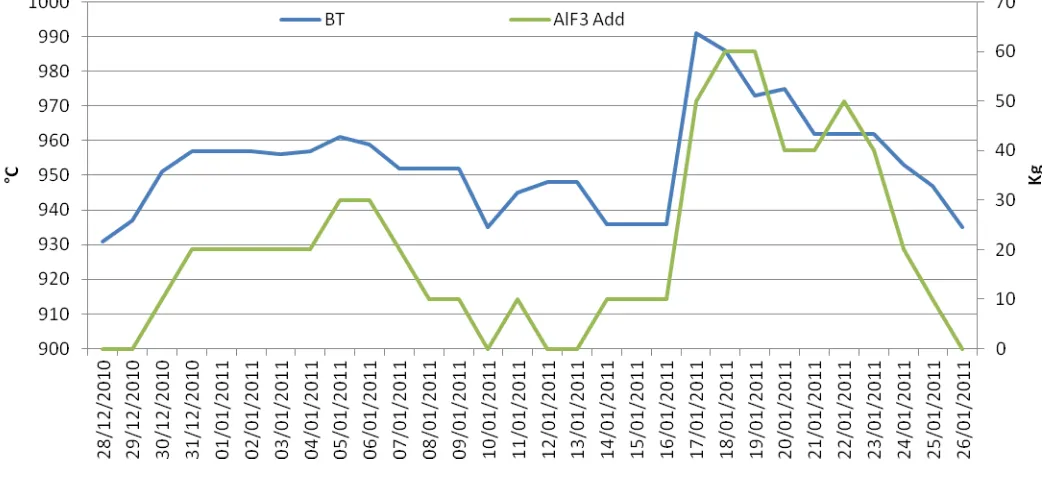
+2
Dokumen terkait