KONTAMINASI LOGAM BERAT (Hg DAN Pb) PADA AIR,
SEDIMEN DAN IKAN SELAR TETENGKEK (
Megalaspis cordyla
)
DI TELUK PALU PROVINSI SULAWESI TENGAH
MATIUS PAUNDANAN
SEKOLAH PASCASARJANA INSTITUT PERTANIAN BOGOR
PERNYATAAN MENGENAI TESIS DAN
SUMBER INFORMASI SERTA PELIMPAHAN HAK CIPTA*
Dengan ini saya menyatakan bahwa tesis berjudul Kontaminasi Logam Berat (Hg dan Pb) pada Air, Sedimen dan Ikan Selar Tetengkek (Megalaspis cordyla) di Teluk Palu Provinsi Sulawesi Tengah adalah karya saya dengan arahan pembimbing dan belum pernah diajukan dalam bentuk apapun oleh orang lain kepada perguruan tinggi manapun. Sumber informasi yang berasal atau dikutip dari karya yang diterbitkan maupun tidak diterbitkan dari penulis lain telah disebutkan dalam teks dan dicantumkan dalam Daftar Pustaka di bagian akhir tesis ini.
Dengan ini saya melimpahkan hak cipta dari karya tulis saya kepada Institut Pertanian Bogor.
Bogor, Oktober 2015
Matius Paundanan
RINGKASAN
MATIUS PAUNDANAN. Kontaminasi Logam Berat (Hg dan Pb) pada Air, Sedimen dan Ikan Selar Tetengkek (Megalaspis cordyla) di Teluk Palu Provinsi Sulawesi Tengah. Dibimbing oleh ETTY RIANI dan SYAIFUL ANWAR.
Masuknya logam berat ke dalam lingkungan perairan akan berdampak pada menurunnya kualitas lingkungan perairan. Keberadaan logam berat yang menumpuk pada air laut dan sedimen akan masuk ke dalam sistem rantai makanan dan berpengaruh pada kehidupan organisme di dalamnya. Jika konsentrasi logam berat telah melebihi baku mutu dalam perairan dapat terakumulasi pada sedimen dan pada organisme perairan. Pada konsentrasi tertentu kontaminasi logam berat Hg dan Pb pada organisme perairan dapat berdampak toksik terhadap kesehatan organisme tersebut. Ikan dapat menjadi salah satu indikator pencemaran lingkungan dari limbah kimia, termasuk logam berat pada lingkungan perairan karena siklus hidupnya lebih lama dibanding organisme akuatik lainnya dan menempati peringkat teratas dalam rantai makanan akuatik serta dapat mengakumulasi logam berat. Perairan Teluk Palu merupakan perairan yang rentan mengalami kontaminasi logam berat akibat adanya aktivitas pertambangan emas tradisional yang beroperasi di kawasan aliran Sungai Pondo dan bermuara langsung ke Teluk Palu dan limbah dari aktivitas antropogenik masyarakat Kota Palu dan sekitarnya.
Tujuan penelitian untuk menganalisis kontaminasi Hg dan Pb pada air, sedimen dan ikan selar tetengkek (Megalaspis cordyla) di Perairan Teluk Palu Sulawesi Tengah; dan menganalisis kondisi histopatologi organ insang, daging, hati dan limpa ikan selar tetengkek. Penelitian dilakukan pada bulan Februari sampai April 2015. Penetapan titik sampling dan pengambilan sampel air, sedimen dan ikan selar tetengkek dilakukan secara sengaja pada 10 titik sampling dengan pertimbangan sumber pencemar di darat. Titik sampling dibagi menjadi tiga zona masing-masing terdiri dari tiga titik sampling dan satu titik sampling yang mewakili daerah yang jauh dari sumber pencemar. Zona 1 (Titik sampling 1, 2 dan 3) terdapat kegiatan di darat seperti PLTU, perhotelan, SPBU, pusat perbelanjaan dan pemukiman. Zona 2 (Titik sampling 4, 5 dan 6) terdapat kegiatan di darat seperti pertambangan, SPBU, perhotelan, pusat perbelanjaan, pemukiman dan lainnya. Zona 3 (Titik sampling 7, 8 dan 9) terdapat kegiatan di darat seperti pemukiman, SPBU, perbengkelan dan penggaraman.
Maksimum Cemaran Logam Dalam Bahan Pangan. Preparat histopatologi dianalisis secara deskriptif.
Hasil penelitian menunjukkan konsentrasi Hg dalam air, sedimen, organ insang, daging, hati dan limpa ikan selar tetengkek masing-masing 0,0008-0,0042 mg/l, 0,017-0,287 mg/l, 0,007-0,145 mg/kg, 0,014-0,046 mg/kg, 0,052-0,106 mg/kg dan 0,043-0,414 mg/kg. Konsentrasi logam Pb dalam air, sedimen, organ insang, daging, hati dan limpa ikan selar tetengkek masing-masing 0,0130-0,0392 mg/l, 2,647-8,987 mg/kg, 0,132-0,775 mg/kg, 0,005-0,734 mg/kg, 0,295-1,871 mg/kg dan 1,654-12,92 mg/kg. Konsentrasi rata-rata Hg dan Pb dalam air telah melebihi baku mutu yang ditetapkan, sementara konsentrasi dalam sedimen masih di bawah baku mutu. Konsentrasi rata-rata Hg dalam seluruh organ ikan yang diamati masih memenuhi baku mutu, sementara Pb dalam organ insang, hati dan limpa telah melebihi baku mutu. Adanya perbedaan konsentrasi Hg dan Pb dalam air dan sedimen pada masing-masing Zona diduga karena pengaruh dari sumber pencemar yang ada di darat, kedalaman, jenis sedimen dan arus laut. Tingginya kandungan logam Hg dalam air di Teluk Palu diduga bersumber dari aktivitas pertambangan emas tradisional di Kelurahan Poboya.
Histopatologi organ ikan selar tetengkek yakni: insang terdapat peradangan lamella sekunder; pada daging terdapat timbunan mineral, degenerasi lemak dan nekrosis; hati terdapat timbunan mineral, degerasi hepatosit, dan nekrosis; serta pada limpa ditemukan timbunan mineral, degenerasi dan deplesi.
SUMMARY
MATIUS PAUNDANAN. Heavy Metals Contamination of (Hg and Pb) On Water, Sediment, and Torpedo Scad Fish (Megalaspis cordyla) in Palu Bay, Province Central Sulawesi. Supervised by ETTY RIANI and SYAIFUL ANWAR.
The entry of heavy metals into the aquatic environment will have an impact on the derease in the quality of aquatic environments. Presence of heavy metals that accumulate in marine water and sediment may enter into the food chain system and affect the life of the organism in it. If the concentration of heavy metals have exceeded the quality of the waters, it may accumulate in the sediment and in aquatic organisms. At certain concentrations of heavy metal contamination of Hg and Pb in aquatic organisms can be toxic to the organism. Fish can be an indicator of environmental contamination from chemical waste, including heavy metals in aquatic environments because of longer life cycle than other aquatic organisms, ranked top in the aquatic food chain, and can accumulate heavy metals. Palu Bay waters are waters susceptible to heavy metal contamination due to the traditional gold mining activity that operates in the upper region of Pondo River, and waste from anthropogenic activities of Palu City and surrounding communities.
The aims of this research were to analyze the contamination of Hg and Pb in water, sediment and torpedo scad fish (Megalaspis cordyla) in Palu Bay Central Sulawesi; and to analyze the histopathology of gill, meat, liver, and spleen torpedo scad fish. The study was conducted from February to April 2015. Determination of sampling points and the sampling of water, sediment and torpedo scad fish is done deliberately at 10 sampling points with consideration of the sources of pollution on land. Sampling were divided into three zones, each consisting of three sampling points and a sampling point that represent areas far from pollutant sources. Zone 1 (point sampling 1, 2 and 3) might be affected by land activities such as power plants, hotels, gas stations, shopping centers and residential areas. Zone 2 (point sampling 4, 5 and 6) might be affected by land activities such as mining, gas stations, hotels, shopping centers, residential and others. Zone 3 (point sampling 7, 8 and 9) might be affected by land activities such as residential, gas stations, workshops and salting.
Parameters of water quality measurements were done in the field for temperature, pH, brightness, turbidity, and dissolved oxygen (DO), and at laboratory analysis for salinity, chemical oxygen demand (COD), ammonia, and nitrates. Heavy metals were analized by following APHA, and Indonesian National Standard (SNI) methods. The concentration of heavy metals in water and water quality compared with MOE Decree No. 51/2004 on Sea Water Quality Standard. The concentration of heavy metals in sediment compared to the quality standards of CCME, ANZECC/ARMCANZ 2000, and NOAA. Hg, and Pb concentrations in torpedo scad fish compared to SNI No. 7387: 2009 on Limit of Metal Contamination in Food Ingredients. Histopathological preparations were analyzed descriptively.
mg/kg, 0.014-0.046 mg/kg, 0.052-0.106 mg/kg, and 0.043-0.414 mg/kg, respectively. Pb concentrations in water, sediment, gill, meat, liver, and spleen were 0.0130-0.0392 mg/l, 2.647-8.987 mg/kg, 0.132-0.775 mg/kg, 0.005-0.734 mg/kg, 0.295-1.871 mg/kg, and 1.654-12.92 mg/kg, respectively. The average of Hg and Pb concentrations in the water had exceeded the specified quality standards, while in the sediments were still below the quality standards. The average of Hg and Pb concentrations in all observed fish organs were below the quality standards, except for Pb concentrations in gill, liver, and spleen that had exceeded the quality standard. The difference in concentrations in water and sediment in each zone probably due to the influence of the sources of pollution in the upper land. The high content of Hg in the water in the bay of Palu probably sourced from traditional gold mining activities in the Village Poboya.
Based on the histopathological analysis of torpedo scad fish organs, there is abnormality in each organ. There were gill showed inflammation in secondary lamella; meat contained mineral deposits, and showed fatty degeneration and necrosis; liver contained mineral deposits and showed hepatocytes degeneration and necrosis; whils spleen contained mineral deposits and showed degeneration and depletion.
© Hak Cipta Milik IPB, Tahun 2015
Hak Cipta Dilindungi Undang-Undang
Dilarang mengutip sebagian atau seluruh karya tulis ini tanpa mencantumkan atau menyebutkan sumbernya. Pengutipan hanya untuk kepentingan pendidikan, penelitian, penulisan karya ilmiah, penyusunan laporan, penulisan kritik, atau tinjauan suatu masalah; dan pengutipan tersebut tidak merugikan kepentingan IPB
Tesis
sebagai salah satu syarat untuk memperoleh gelar Magister Sains
pada
Program Studi Pengelolaan Sumberdaya Alam dan Lingkungan
KONTAMINASI LOGAM BERAT (Hg DAN Pb) PADA AIR,
SEDIMEN DAN IKAN SELAR TETENGKEK (
Megalaspis cordyla
)
DI TELUK PALU PROVINSI SULAWESI TENGAH
SEKOLAH PASCASARJANA INSTITUT PERTANIAN BOGOR
BOGOR 2015
Judul Tesis : Kontaminasi Logam Berat (Hg dan Pb) pada Air, Sedimen dan Ikan Selar Tetengkek (Megalaspis cordyla) di Teluk Palu Provinsi Sulawesi Tengah
Nama : Matius Paundanan NIM : P052130481
Disetujui oleh Komisi Pembimbing
Dr Ir Etty Riani, MS Ketua
Dr Ir Syaiful Anwar, MSc Anggota
Diketahui oleh
Ketua Program Studi
Pengelolaan Sumberdaya Alam dan Lingkungan
Prof Dr Ir Cecep Kusmana, MS
Dekan Sekolah Pascasarjana
Dr Ir Dahrul Syah, MScAgr
Tanggal Ujian: 18 September 2015
PRAKATA
Segala Puji dan Syukur penulis panjatkan ke hadirat Tuhan Yesus Kristus atas segala berkat dan karunia-Nya sehingga penulis dapat menyelesaikan karya ilmiah ini dengan baik. Topik penelitian yang dipilih yakni tentang pencemaran logam berat dengan judul penelitian ini adalah ―Kontaminasi Logam Berat (Hg dan Pb) pada Air, Sedimen dan Ikan Selar Tetengkek (Megalaspis cordyla) di Teluk Palu Provinsi Sulawesi Tengah‖. Penulis berharap hasil dari penelitian ini dapat bermanfaat bagi kita semua dan kita memiliki kesadaran terhadap kelestarian lingkungan.
Penulis pada kesempatan ini ingin mengucapkan terimakasih kepada:
1. Dr Ir Etty Riani, MS selaku ketua komisi pembimbing dan Dr Ir Syaiful Anwar, M.Sc selaku anggota komisi pembimbing.
2. Ayahanda atas dukungan doanya dan Almarhuma Ibu meskipun telah tiada namun dukungannya selalu terasa.
3. Prof Dr Ir Herry Suhardiyanto, MSc selaku rektor Institut Pertanian Bogor.
4. Prof Dr Ir Cecep Kusmana, MS selaku ketua Program Studi Pengelolaan Sumberdaya Alam dan Lingkungan.
5. Prof Dr Ir Sulistiono, MSc selaku penguji luar komisi.
6. DIKTI sebagai lembaga sponsor yang telah memberikan beasiswa kepada penulis sehingga bisa melanjutkan pendidikan di Program Pascasarjana Institut Pertanian Bogor.
7. Semua dosen-dosen yang telah mengajar di Program Studi PSL.
8. Rekan-rekan seperjuangan Himpunan Mahasiswa Pascasarjana Sulawesi Tengah atas doa dan kebersamaannya.
9. Rekan-rekan PSL 2013 atas dukungan doa, support dan kekompakannya selama dalam perkuliahan.
10.Wahyu Mohammad dan Zaenal Muchid yang telah membantu selama pengambilan sampel di lapangan.
11.Saudara-saudara saya Kak Petrus, Kak Rina, Kak Ludia dan Kak Fitri yang selalu mendoakan dan mensupport selama perkuliahan.
12.Keluarga besar yang selalu mendukung secara moril maupun materil. Semoga karya ilmiah ini bermanfaat.
Bogor, Oktober 2015
DAFTAR ISI
DAFTAR TABEL xii
DAFTAR GAMBAR xii
DAFTAR LAMPIRAN xiii
1 PENDAHULUAN 1
Latar Belakang 1
Kerangka Pemikiran 2
Perumusan Masalah 3
Tujuan Penelitian 5
Manfaat Penelitian 5
2 TINJAUAN PUSTAKA 6
Pencemaran Perairan oleh Logam Berat 6
Karakteristik Logam Berat 7
Sumber Logam Berat di Perairan 11
Kontaminasi Logam Berat pada Organisme Perairan 12
Kontaminasi Logam Berat terhadap Manusia 13
Histopatologi 14
Ikan Selar Tetengkek 15
3 METODE 17
Waktu dan Tempat 17
Alat dan Bahan 18
Penentuan Titik dan Pengambilan Sampel 18
Prosedur Kerja 19
Analisa Data 23
4 HASIL DAN PEMBAHASAN 26
Kualitas Air di Teluk Palu 26
Kandungan Hg dan Pb pada Air 36
Kandungan Hg dan Pb pada Sedimen 39
Kandungan Hg dan Pb pada Organ Ikan Selar Tetengkek 42 Korelasi Logam Berat dalam Air, Sedimen dan Ikan Selar Tetengkek 50
Histopatologi Organ Ikan Selar Tetengkek 54
Rekomendasi dan Pengelolan Pencemaran 60
5 SIMPULAN DAN SARAN 64
Simpulan 64
Saran 64
DAFTAR PUSTAKA 65
LAMPIRAN 75
DAFTAR TABEL
1 Kadar normal dan maksimum beberapa logam berat yang masuk ke
lingkungan laut 11
2 Koordinat titik sampling, jarak dari pantai dan kedalaman 18 3 Parameter kualitas air, sedimen dan ikan yang diamati 21 4 Jenis bahan kimia dan lama perprosesan contoh 23 5 Standar baku mutu logam berat Hg dan Pb pada air, sedimen dan ikan 24 6 Korelasi konsentrasi logam berat dalam air laut dengan kandungan
logam berat dalam sedimen 51
7 Korelasi konsentrasi logam berat dalam air laut dengan kandungan
logam berat dalam organ ikan selar tetengkek 52
8 Korelasi konsentrasi logam berat dalam sedimen dengan kandungan
logam berat dalam organ ikan selar tetengkek 53
DAFTAR GAMBAR
1 Diagram kerangka pemikiran penelitian 4
2 Proses yang terjadi bila logam berat masuk ke lingkungan laut 7
3 Ikan selar tetengkek 15
4 Peta Lokasi Penelitian 17
5 Suhu di setiap titik sampling 26
6 Kecerahan di setiap titik sampling 28
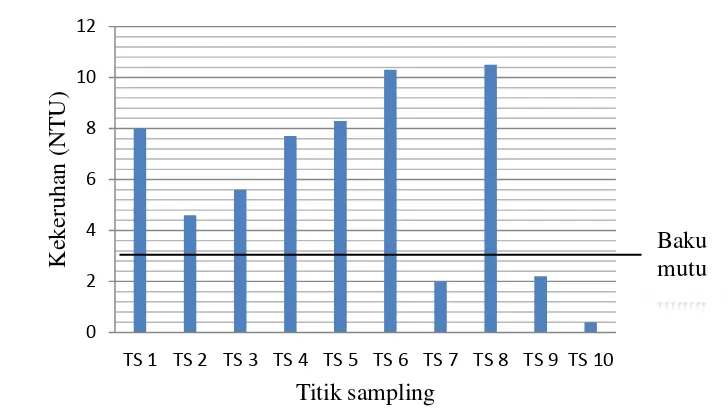
7 Kekeruhan di setiap titik sampling 29
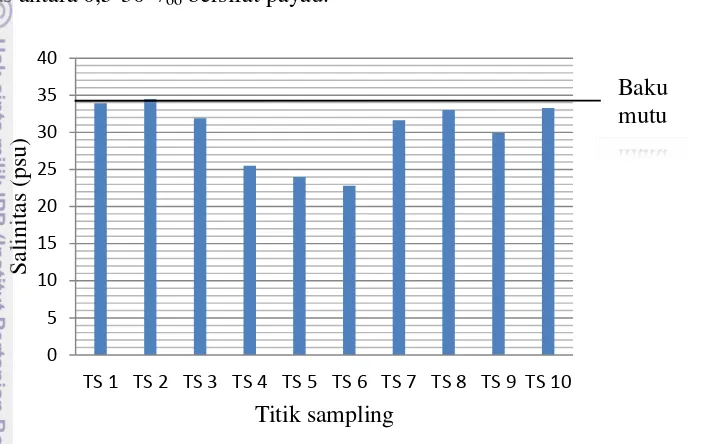
8 Konsentrasi salinitas di setiap titik sampling 30
9 Konsentrasi pH di setiap titik sampling 31
10 Konsentrasi DO di setiap titik sampling 32
11 Konsentrasi COD di setiap titik sampling 33
12 Konsentrasi ammonia di setiap titik sampling 34
13 Konsentrasi nitrat di setiap titik sampling 35
14 Konsentrasi merkuri (Hg) pada air 37
15 Konsentrasi timbal (Pb) pada air 38
16 Konsentrasi merkuri (Hg) pada sedimen 40
17 Konsentrasi timbal (Pb) pada sedimen 41
18 Konsentrasi merkuri (Hg) pada insang 43
19 Konsentrasi timbal (Pb) pada insang 44
20 Konsentrasi merkuri (Hg) pada daging 45
21 Konsentrasi timbal (Pb) pada daging 46
22 Konsentari merkuri (Hg) pada hati 47
23 Konsentrasi timbal (Pb) pada hati 48
24 Konsentrasi merkuri (Hg) pada limpa 49
25 Konsentrasi timbal (Pb) pada limpa 50
26 Histopatologi sampel insang ikan selar tetengkek (Megalaspis cordyla)
yang diambil dari lokasi penelitian 54
27 Histopatologi sampel daging ikan selar tetengkek (Megalaspis cordyla)
28 Histopatologi sampel daging ikan selar tetengkek (Megalaspis cordyla)
yang diambil dari lokasi penelitian 57
29 Histopatologi sampel limpa ikan selar tetengkek (Megalaspis cordyla)
yang diperoleh dari lokasi penelitian 59
DAFTAR LAMPIRAN
1 Dokumentasi kondisi lokasi penelitian 75
2 Beberapa pedoman mutu logam Hg dan Pb pada sedimen 77 3 Kondisi kualitas air di perairan Teluk Palu Provinsi Sulawesi Tengah
saat penelitian dilaksanakan 78
4 Konsentrasi logam berat (Hg dan Pb) pada air dan sedimen di Teluk
Palu Provinsi Sulawesi Tengah 79
5 Konsentrasi logam berat (Hg dan Pb) pada organ ikan selar tetengkek (Megalaspis cordyla) di Teluk Palu Provinsi Sulawesi Tengah 80 6 Perbandingan logam berat (Hg dan Pb) dalam air di perairan Teluk Palu
dengan beberapa perairan di Indonesia 81
7 Perbandingan logam berat (Hg dan Pb) dalam sedimen di perairan Teluk Palu dengan beberapa perairan di Indonesia 82
1
PENDAHULUAN
Latar Belakang
Lingkungan memiliki peranan yang sangat penting dalam menunjang kehidupan manusia. Lingkungan hidup merupakan kesatuan ruang dengan semua benda, termasuk manusia dan perilakunya, yang mempengaruhi alam itu sendiri, kelangsungan perikehidupan, dan kesejahteraan manusia serta mahkluk hidup lain (UU PPLH Nomor 32 Tahun 2009). Ketergantungan manusia pada lingkungan merupakan hal yang tidak terpisahkan sehingga eksistensi lingkungan patut dijaga dan dilestarikan demi kelangsungan hidup manusia. Lingkungan secara umum terdiri dari komponen subsistem air, tanah dan udara merupakan suatu kesatuan yang saling berinteraksi (Arsad et al. 2012).
Kualitas lingkungan saat ini sangat menentukan eksistensi di masa yang akan datang, sehingga perlu dijaga dan dipertahankan kelestariannya. Perkembangan ilmu pengetahuan dan teknologi dewasa ini sering dikaitkan dengan menurunnya kualitas lingkungan, khususnya lingkungan perairan. Salah satu yang sering terjadi yaitu menurunnya kualitas air akibat pencemaran limbah organik maupun anorganik. Pencemaran terhadap lingkungan perairan berasal dari berbagai macam aktivitas manusia di darat seperti perindustrian, pertanian, transportasi, rumah sakit, perbengkelan, dan kegiatan domestik. Berbagai kegiatan yang menghasilkan limbah tersebut dan tidak diolah terlebih dahulu, sehingga langsung masuk ke dalam lingkungan, dan berdampak buruk bagi ekosistem khususnya ekosistem perairan (Riani 2012). Limbah hasil aktivitas manusia tersebut mengadung berbagai jenis zat kimia yang berbahaya bagi makhluk hidup. Salah satu zat kimia yang terkandung dalam limbah adalah logam berat.
Masuknya logam berat ke dalam lingkungan perairan dapat berdampak pada menurunnya kualitas lingkungan perairan (Zhang et al. 2009; Riani 2012). Keberadaan logam berat yang menumpuk pada air laut dan sedimen akan masuk ke dalam sistem rantai makanan dan berpengaruh pada kehidupan organisme di dalamnya (Hutagalung 1984; Takarina et al. 2013). Jika konsentrasi logam berat telah melebihi baku mutu dalam perairan dapat terakumulasi pada sedimen (Rochyatun et al. 2006) dan pada organisme perairan (Riani et al. 2014). Kontaminasi logam berat Hg dan Pb pada organisme perairan dapat berdampak toksik terhadap kesehatan organisme tersebut (Darmono 2001). Merkuri dalam organisme laut, pada umumnya dalam bentuk metil merkuri maupun merkuri ion (Suseno et al. 2007). Pada konsentrasi tertentu, kontaminasi logam berat pada organisme perairan dapat menyebabkan terjadinya kecacatan pada kerang hijau (Riani 2010; Riani dan Cordova 2011), cacat bawaaan pada larva Dicrotendipes simpsoni (Diptera: Choronomidae) (Riani et al. 2014), dan menyebabkan abnormalitas organ insang, hati, ginjal dan limpa pada ikan (Rajeshkumar dan Munuswamy 2011; Coulibaly et al. 2012; Authman et al. 2012; El-Kasheif et al. 2013; Riani 2015).
2
dibanding organisme akuatik lainnya dan menempati peringkat teratas dalam rantai makanan akuatik (Farkas et al. 2001), serta ikan dapat mengakumulasi logam berat (Akan et al. 2012; El-Moselhy et al. 2014; Riani 2015). Kemudian apabila kerang dan ikan yang telah terkontaminasi logam berat dikonsumsi oleh manusia, dapat berdampak terhadap kesehatan karena logam berat bersifat karsinogenik (Darmono 2001).
Perairan Teluk Palu merupakan perairan yang rentan mengalami kontaminasi logam berat akibat adanya aktivitas pertambangan emas tradisional yang beroperasi di kawasan aliran Sungai Pondo dan bermuara langsung ke Teluk Palu. Menurut Agus et al. (2005) dan Ning et al. (2011) bahwa pertambangan emas tradisional merupakan salah satu sumber masuknya logam berat ke dalam lingkungan perairan. Selain hal tersebut aktivitas masyarakat Kota Palu yang menghasilkan limbah juga berpotensi menjadi sumber masuknya logam berat ke dalam perairan Teluk Palu. Limbah dari kegiatan domestik, perhotelan, rumah sakit, SPBU, PLTU, perbengkelan dan pertanian berpotensi mencemari Teluk Palu. Oleh karena itu, maka potensi pencemaran di Teluk Palu bukan hanya dari kegiatan pertambangan emas tradisional, tetapi juga dari kegiatan-kegiatan lain yang semuanya berpotensi mengkontaminasi air, sedimen dan ikan yang hidup di dalamnya.
Beberapa penelitian telah dilakukan tentang kandungan logam berat di perairan Teluk Palu antara lain penelitian Said et al. (2009) melaporkan kandungan logam krom rata-rata 39,24±23,67 mg/kg dan kandungan timbal dalam sedimen rata-rata 15,89± 7,43 mg/kg. Arsad et al. (2012) juga melaporkan kandungan logam berat timbal dalam ikan belanak (Liza melinoptera) sebesar 1,746±1,673 mg/kg. Hal ini telah melebihi nilai maksimum kandungan logam berat dalam bahan makanan sesuai dengan ISO 01-2729.1-2006 yaitu 0,4 mg/kg. Selanjutnya dinyatakan bahwa tingginya kandungan logam berat di perairan Teluk Palu akibat dari kegiatan antropogenik dan limbah domestik penduduk di sekitar aliran Sungai Pondo.
Oleh karena itu, untuk mencegah terjadinya penurunan kualitas lingkungan di perairan teluk Palu, maka harus dilakukan langkah-langkah konkrit, mengingat perairan Teluk Palu memiliki peranan yang sangat penting bagi penduduk di sekitarnya. Salah satu langkah tersebut adalah penelitian tentang kontaminasi logam berat merkuri (Hg) dan timbal (Pb) pada air, sedimen dan ikan selar tetengkek di perairan Teluk Palu.
Kerangka Pemikiran
3 berpotensi menjadi sumber pencemaran logam berat terutama merkuri (Hg) pada lingkungan. Hal ini akan berdampak buruk dan menimbulkan masalah terhadap menurunnya kualitas lingkungan khususnya lingkungan perairan di muara Sungai Pondo, Teluk Palu.
Di lingkungan perairan, kontaminasi logam berat pada air, sedimen dan biota dipengaruhi oleh berbagai hal seperti faktor-faktor lingkungan, faktor sifat fisik kimia logam dan faktor fisiologis dari biota (ikan). Dampak negatif akibat tercemarnya suatu perairan oleh logam berat juga dapat terkontaminasi ke sedimen dan biota perairan sehingga ekosistem perairan menjadi tidak stabil. Kontaminasi logam berat pada biota akan masuk ke sistem rantai makanan dan pada akhirnya akan sampai ke manusia. Merkuri (Hg) dan timbal (Pb) merupakan logam berat yang sukar didegradasi, afinitas yang besar terhadap gugus protein organisme air, maka logam berat tersebut akan mudah terabsorbsi dan terakumulasi pada tubuh ikan (Widowati et al. 2008).
Pengetahuan tentang seberapa besar kontaminasi bahan pencemar logam berat merkuri (Hg) dan timbal (Pb) pada air, sedimen dan biota (ikan) di muara Sungai Pondo, Teluk Palu perlu diketahui. Informasi ini dapat digunakan sebagai pedoman pengambilan keputusan bagi pihak-pihak terkait tentang pengelolaan penggunaan zat merkuri (Hg) dan timbal (Pb) serta pengelolaan lingkungan demi menjaga dan melestarikan lingkungan yang berkualitas. Adapun kerangka pemikiran penelitian ini dapat dilihat pada Gambar 1.1
Perumusan Masalah
Peningkatan jumlah penduduk berbanding lurus dengan peningkatan kebutuhan hidupnya. Hal ini mendorong manusia melakukan berbagai cara untuk memenuhi kebutuhannnya, misalnya dengan mengembangkan ilmu pengetahuan dan teknologi. Kemajuan ilmu pengetahuan dewasa ini telah mendorong manusia untuk meningkatkan taraf hidupnya dengan memanfaatkan sumberdaya yang ada di sekitarnya. Sumberdaya yang ada tidak semua dapat diperoleh dengan mudah dan langsung dimanfaatkan untuk pemenuhan kebutuhan hidup manusia, oleh karena itu membutuhkan teknologi untuk mengolah bahan-bahan tersebut sehingga dapat dimanfaatkan atau dikonsumsi. Perkembangan teknologi khususnya dalam bidang perindustrian akan menimbulkan dampak yang baru bagi menurunnya kualitas lingkungan. Berbagai kegiatan manusia yang tidak terkendali misalnya dalam bidang pertambangan, transportasi, pertanian dan domestik berdampak buruk terhadap menurunnya kualitas lingkungan hidup.
4
langsung dibuang ke lingkungan tanpa diolah terlebih dahulu. Teluk Palu merupakan salah satu perairan yang diduga telah tercemar oleh merkuri dan timbal serta biota yang hidup di perairan tersebut juga diduga telah terkontaminasi logam berat Hg dan Pb. Dalam rangka mencegah hal itu, maka perlu dilakukan penelitian yang berkaitan langsung dengan terjadinya penurunan kualitas lingkungan. Sehingga dari permasalahan di atas muncul beberapa pertanyaan penelitian sebagai berikut:
1. Berapa besaran nilai kandungan merkuri (Hg) dan Timbal (Pb) pada air, sedimen dan ikan selar tetengkek di Teluk Palu, Sulawesi Tengah saat dilakukan penelitian?
2. Bagaimana korelasi kandungan logam berat (Hg) dan timbal (Pb) pada air, sedimen dan ikan selar tetengkek di Teluk Palu, Sulawesi Tengah?
3. Bagaimana kondisi histopatologi ikan selar tetengkek yang diduga terkontaminasi logam berat merkuri (Hg) dan timbal (Pb) di Teluk Palu, Sulawesi Tengah?
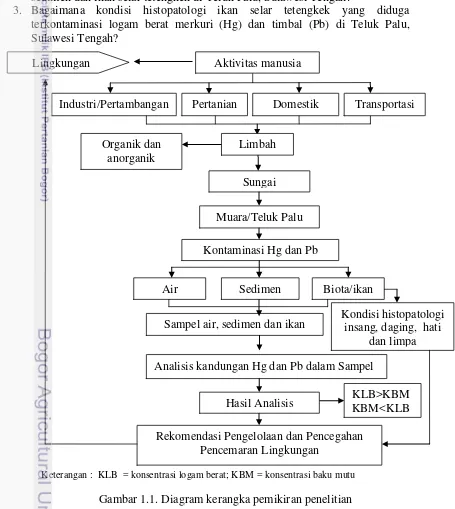
Keterangan : KLB = konsentrasi logam berat; KBM = konsentrasi baku mutu
Gambar 1.1. Diagram kerangka pemikiran penelitian
Lingkungan Aktivitas manusia
Transportasi Domestik
Pertanian Industri/Pertambangan
Organik dan anorganik
Limbah
Sungai Muara/Teluk Palu Kontaminasi Hg dan Pb
Biota/ikan Sedimen
Air
Kondisi histopatologi insang, daging, hati
dan limpa Sampel air, sedimen dan ikan
Analisis kandungan Hg dan Pb dalam Sampel KLB>KBM KBM<KLB Hasil Analisis
5
Tujuan Penelitian
Berdasarkan uraian di atas maka tujuan penelitian ini adalah sebagai berikut:
1. Menganalisis kontaminasi logam berat merkuri (Hg) dan timbal (Pb) pada air, sedimen dan ikan selar tetengkek di Teluk Palu, Sulawesi Tengah.
2. Menganalisis korelasi antara kandungan logam berat Hg dan Pb pada air dengan kandungan logam berat (Hg dan Pb) pada sedimen dan ikan selar tetengkek di Teluk Palu, Sulawesi Tengah.
3. Menganalisis kondisi histopatologi organ insang, daging, hati dan limpa ikan selar tetengkek yang diambil dari lokasi penelitian.
Manfaat Penelitian
Melalui penelitian ini diharapkan dapat memberikan manfaat sebagai berikut:
1. Memberikan informasi ilmiah bagi pihak-pihak terkait mengenai nilai konsentrasi kontaminasi logam berat merkuri (Hg) dan timbal (Pb) pada air, sedimen dan ikan selar tetengkek di Teluk Palu, Sulawesi Tengah.
2. Memberikan informasi ilmiah mengenai potensi pencemaran yang terjadi di Teluk Palu, Sulawesi Tengah.
3. Memberikan informasi kondisi histopatologi sampel ikan selar tetengkek yang diperoleh dari lokasi penelitian.
6
2
TINJAUAN PUSTAKA
Pencemaran Perairan oleh Logam Berat
Perairan adalah komponen lingkungan yang paling mudah terkena dampak kegiatan manusia, sehingga perlu mendapat perhatian khusus. Sekitar 70% permukaan bumi diselimuti oleh air. Oleh karena itu, air dapat dikatakan sebagai bagian yang essensial dari sistem kehidupan. Hampir 97,2% dari air yang ada di bumi merupakan air laut (Manahan 1994). Setiap sistim perairan memiliki kapasitas terima (receiving capacity) yang terbatas terhadap bahan pencemar, sehingga peningkatan buangan bahan pencemar ke perairan akan mengakibatkan kerusakan ekosistem perairan (Sanusi 1985). Defenisi pencemaran adalah perubahan-perubahan sifat fisik, kimia dan biologi yang tidak diinginkan pada udara, tanah dan air (Odum 1971). Perubahan tersebut dapat menimbulkan bahaya bagi kehidupan manusia atau makhluk hidup lain yang disebabkan adanya limbah dari proses industri dan kebiasaan hidup manusia.
Menurut MEN-LH (2004) pencemaran laut adalah suatu keadaan, dimana suatu zat atau energi dan unsur lain diintroduksikan ke dalam lingkungan laut oleh kegiatan manusia atau oleh proses alam sendiri dalam kadar hingga menyebabkan terjadinya perubahan yang mengakibatkan lingkungan laut itu tidak berfungsi seperti semula dalam arti kesehatan, kesejahteraan dan keselamatan hayati. Pencemaran logam berat pada perairan dipengaruhi oleh berbagai faktor. Salah satunya yaitu kondisi perairan yang mempengaruhi jumlah akumulasi logam Pb oleh karang lunak Sinularia polydactyla adalah kandungan padatan tersuspensi (Kadir et al. 2013).
Menurut Undang-Undang Republik Indonesia No. 32 tahun 2009, yang dimaksud dengan Bahan Berbahaya dan Beracun (B3) adalah zat, energi, dan/atau komponen lain karena sifat, konsentrasi, dan/atau jumlahnya, baik secara langsung maupun tidak langsung, dapat mencemarkan dan/atau merusak lingkungan hidup, dan/atau membahayakan lingkungan hidup, kesehatan serta kelangsungan hidup manusia dan makhluk hidup lain.
7
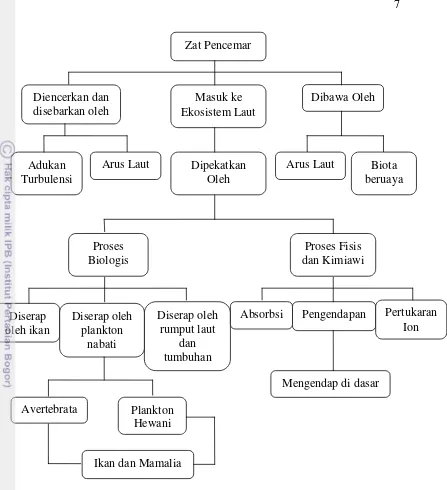
Gambar 2.1. Proses yang terjadi bila logam berat masuk ke lingkungan laut (EPA, 1973 dalam Hutagalung 1984).
Karakteristik Logam Berat
Logam berat adalah unsur-unsur kimia dengan bobot jenis lebih besar dari 5 gr/cm3, terletak disudut kanan bawah pada daftar berkala, memiliki afinitas yang tinggi terhadap unsur S dan biasanya bernomor atom 22 sampai 92 dari periode 4 sampai 7 (Miettinen 1977). Berdasarkan sifat fisika dan kimianya, tingkat atau daya racun logam berat terhadap hewan air dapat diurutkan (dari tinggi ke rendah) sebagai berikut merkuri (Hg), cadmium (Cd), seng (Zn), timbal (Pb), krom (Cr), nikel (Ni) dan cobal (Co) (Sutamihardja et al. 1982). Menurut Darmono (2001), daftar urutan toksisitas logam berat paling tinggi ke paling
Zat Pencemar
Diencerkan dan disebarkan oleh
Masuk ke Ekosistem Laut
Adukan Turbulensi
Plankton Hewani Diserap
oleh ikan
Diserap oleh rumput laut
dan tumbuhan
Dibawa Oleh
Avertebrata
Arus Laut Dipekatkan Oleh
Arus Laut
Proses Biologis
Proses Fisis dan Kimiawi
Diserap oleh plankton
nabati
Pengendapan
Mengendap di dasar
Absorbsi Pertukaran
Ion Biota beruaya
8
rendah terhadap manusia yang mengkomsumsi ikan adalah sebagai berikut Hg2+ > Cd2+ > Ag2+ > Ni2+ > Pb2+ > As2+ > Cr2+ > Sn2+ > Zn2+.
Berdasarkan sudut pandang toksikologi, logam berat dapat dibagi dalam dua jenis. Jenis pertama adalah logam berat esensial, dimana keberadaannya dalam jumlah tertentu sangat dibutuhkan oleh organisme hidup, namun dalam jumlah yang berlebihan dapat menimbulkan efek racun. Contoh logam berat ini adalah Zn, Cu, Fe, Co, Mn, dsb. Sedangkan jenis logam kedua adalah logam berat tidak esensial atau beracun, dimana keberadaannya dalam tubuh masih belum diketahui manfaatnya bahkan dapat bersifat racun seperti Hg, Cd, Pb, Cr, dll. Logam berat ini dapat menimbulkan efek kesehatan bagi manusia tergantung pada bagian mana logam berat tersebut terikat dalam tubuh.
Sedangkan menurut Kantor Menteri Negara Kependudukan dan Lingkungan Hidup (1990), sifat toksisitas logam berat dapat dikelompokkan menjadi tiga kelompok yaitu :
1. bersifat toksik tinggi yang terdiri atas unsur-unsur Hg, Cd, Pb, Cu, dan Zn, 2. bersifat toksik menengah yang terdiri dari Cr, Ni, dan Co
3. bersifat toksik sangat rendah yang terdiri dari Mn dan Fe.
Bila bahan cemaran masuk ke dalam lingkungan laut, maka bahan cemar ini akan mengalami tiga macam proses akumulai yaitu proses fisika, kimia dan biologi Akumulasi melalui proses biologi inilah yang disebut bioakumulasi. Sebagian besar logam berat masuk ke dalam tubuh organisme laut melalui rantai makanan, hanya sedikit yang diambil langsung dari air. Fitoplankton yang merupakan awal dari rantai makanan akan dimangsa oleh Zooplankton. Zooplankton dimangsa oleh ikan-ikan kecil, ikan kecil dimangsa oleh ikan yang lebih besar. Sehingga pemangsa yang berukuran besar seperti ikan tuna, akan mengandung kadar logam berat yang tinggi. Tetapi kandungan logam berat yang tinggi umumnya ditemukan pada invertebrata jenis filter feeder, seperti kerang-kerangan dan tiram (Hutagalung 1991). Dari Gambar 2 terlihat bahwa logam berat juga akan diendapkan di dalam sedimen, namun adanya aktifitas mikroorganisme akan menyebabkan logam berat tersebut larut dan kembali ke dalam kolom air.
Akumulasi terjadi karena logam berat dalam tubuh organisme cenderung membentuk senyawa kompleks dengan zat-zat organik yang terdapat dalam tubuh organisme. Dengan demikian logam berat terfiksasi dan tidak diekstraksikan oleh organisme yang bersangkutan. Organisme air mempunyai kemampuan mengabsorpsi dan mengakumulasi logam berat yang berasal dari lingkungannya. Sifat akumulasi ini disebabkan adanya kebutuhan organisme terhadap unsur-unsur yang essensial. Logam berat yang essensial seperti Cu cenderung membentuk ikatan komplek dengan bahan organik. Demikian pula dengan logam toksik seperti Hg, Cd, Pb dan lain sebagainya (Waldichuk 1974).
9 Logam berat bersifat toksik karena logam berat tersebut dapat berikatan dengan ligan dan struktur biologi. Sebagian besar logam menduduki ikatan tersebut dalam beberapa jenis enzim dalam tubuh. Ikatan-ikatan ini dapat mengakibatkan tidak akitifnya enzim yang bersangkutan, hal inilah yang menyebabkan terjadinya toksisitas logam tersebut. Logam yang terikat pada enzim sulit diidentifikasi karena tidak diketahui enzim mana yang menjadi target dari ikatan logam tersebut. Afinitas atau daya gabung dan ikatan logam dengan enzim biasanya sangat kuat (Darmono 1995). Biasanya logam tertentu terikat dalam daerah ikatan yang spesifik untuk setiap logam dan hasil ini dapat dilihat dari gejala dan tanda-tanda serta gangguan yang timbulkan. Tempat ikatan logam yang spesifik tersebut menjadi dasar perkiraan dari organ atau jaringan yang sensitif terhadap keracunan logam yang memiliki dosis rendah. Pada pemberian dosis yang lebih tinggi, jaringan lain mungkin akan terganggu juga, karena menduduki ikatan pada jenis enzim yang lebih banyak.
Logam Merkuri (Hg)
Menurut Hutagalung (1985) raksa atau merkuri (Hg) adalah unsur kimia, yang mempunyai nomor atom 80, berat atom 200,61 dan jari-jari atom 1,48 A°. Merupakan satu-satunya unsur logam yang berbentuk cair pada suhu kamar (25°C ) dan sangat mudah menguap. Membeku pada suhu -38,87°C dan mendidih pada suhu 356,9°C. Warnanya tergantung pada bentuk fasenya. Hg mudah membentuk alloy amalgama dengan logam lainnya, seperti emas (Au), perak (Ag), platinum (Pt), dan tin (Sn). Garam merkuri yang penting antara lain HgC12 yang
bersifat sangat toksik. Hg2C12 digunakan dalam bidang kesehatan, Hg(ONC)2
digunakan sebagai bahan detonator yang eksplosif, sedangkan HgS digunakan pigmen cat berwarna merah terang dan bahan antiseptik (Widowati et al. 2008).
Pada perairan alami, merkuri hanya ditemukan dalam jumlah yang sangat kecil. Merkuri merupakan satu-satunya logam yang berada dalam bentuk cairan pada suhu normal. Merkuri terserap dalam buah-buahan partikulat dan mengalami prestisipasi. Merkuri terdiri dari merkuri anorganik dan merkuri organik. Merkuri anorganik adalah logam murni yang berbentuk cair pada suhu kamar 25ºC, sehingga mudah menguap. Uap merkuri dapat menimbulkan efek samping yang sangat merugikan bagi kesehatan. Di antara sesama senyawa merkuri anorganik, uap logam merkuri (Hg), merupakan yang paling berbahaya. Ini disebabkan karena uap merkuri tidak terlihat dan sangat mudah akan terhisap seiring kegiatan pernafasan yang dilakukan (Palar 2008). Contoh senyawa-senyawa merkuri organik adalah senyawa alkil-merkuri, sekitar 80% dari peristiwa keracunan merkuri bersumber dari senyawa-senyawa merkuri. Beberapa senyawa alkil-merkuri yang banyak digunakan terutama di kawasan negaranegara sedang berkembang metil merkuri khlorida (CH3HgCL) dan etil khlorida (C2H5HgCL).
Senyawa-senyawa tersebut digunakan sebagai pestisida dalam bidang pertanian. Beberapa bentuk senyawa alkil-merkuri lainnya cukup banyak digunakan sebagai katalis dalam industri kimia (Palar 2008).
10
Merkuri dengan klor, belerang, atau oksigen akan membentuk garam yang digunakan dalam pembuatan krim pemutih dan krim antiseptik. Logam tersebut digunakan secara luas untuk mengekstrak emas (Au) dari bijihnya. Ketika Hg dicampur dengan bijih emas, Hg akan membentuk amalgama dengan emas (Au) dan perak (Ag). Amalgama tersebut harus dibakar untuk menguapkan merkuri guna menangkap dan memisahkan butir-butir emas dari butir-butir batuan. Hg bersifat sangat toksik sehingga penggunaan Hg dalam berbagai industri sebaiknya dikurangi, termasuk dalam industri farmasai, kedokteran gigi, industri pertanian, industri baterai, dan lampu fluorecence (Widowati et al. 2008).
Logam Timbal (Pb)
Timah hitam atau timbal dilambangkan dengan Pb (Plumbum), dalam sistem periodik, menduduki tempat dengan nomor atom 83, berat atom 207,9 g dan titik didih 1725 oC. Timbal dalam bentuk larutan ion Pb2+ pada kondisi yang tepat akan berubah menjadi senyawa alkil-lead. Bahan-bahan timbal sulfida dapat juga terbentuk di bawah kondisi anaerobik pada sedimen. Di perairan, Pb mempunyai dua bentuk keadaan oksidasi Pb2+ dengan bentuk utama di lingkungan laut adalah Pb2+ (Palar 2004).
Agustina (2010), menyatakan bahwa timbal banyak digunakan untuk berbagai keperluan karena sifat-sifatnya antara lain: 1) Titik cair rendah sehingga jika digunakan dalam bentuk cair, maka akan membutuhkan teknik sederhana dan murah; 2) Timbal merupakan logam berat yang lunak sehingga mudah diubah keberbagai bentuk; 3) Sifat kimia timbal menyebabkan logam berat ini dapat berfungsi sebagai lapisan pelindung, jika kontak dengan udara lembab; 4) Timbal dapat membentuk alloy dengan logam lain dan alloy yang terbentuk mempunyai sifat berbeda dengan timbal yang murni; 5) Densitas timbal lebih tinggi dibandingkan dengan logam lain, kecuali jika dibandingkan dengan emas dan merkuri. Apabila Pb dalam badan perairan melebihi konsentrasi yang semestinya, dapat mengakibatkan kematian biota laut.
Timbal merupakan salah satu logam non essensial yang sangat berbahaya dan dapat menyebabkan keracunan (toksisitas) pada makhluk hidup. Racun ini bersifat kumulatif, artinya sifat racunnya akan muncul apabila terakumulasi cukup besar dalam tubuh makhluk hidup. Timbal terdapat dalam air karena adanya kontak antara air dengan tanah atau udara tercemar timbal, air yang tercemar oleh limbah industri atau akibat korosi pipa (Riani 2012). Timbal dapat mempengaruhi organisme air yaitu mengganggu system organ seperti insangdalam proses respirasi dan ginjal dalam proses osmoregulasi, kemudian akan mempengaruhi keseimbangan energi dalam tubuh ikan sehingga mortalitas terganggu, pertumbuhan, reproduksi, system saraf dan dapat terakumulasi dalam tulang Lloyd 1992). Timbal mampu menembus membrane biologi dan terakumulasi dalam sel dan organel, selain itu timbal dapat mengganggu kerja enzim dan fungsi protein (Saeni 1989).
11
Sumber Logam Berat di Perairan
Logam berat yang masuk ke perairan dan sumber-sumber seperti melaui buangan limbah industri dan rumah tangga akan terikat pada padatan tersuspensi dan pada akhirnya akan mengendap ke sedimen dasar perairan (Gomez-Parra et al.
2000). Logam berat biasanya ditemukan sangat sedikit dalam air secara alamiah, yaitu kurang dari 1 g/l. Bila terjadi erosi alamiah, konsentrasi logam tersebut dapat meningkat. Beberapa macam logam biasanya lebih dominan daripada logam lainnya dan dalam air biasanya tergantung pada asal sumber air (air tanah dan air sungai). Disamping itu jenis air (air tawar, air payau dan air laut) juga mempengaruhi kandungan logam di dalamnya (Darmono 2001).
Menurut Supriharyono (2000) secara ilmiah logam berat terdapat di alam, namun dalam kadar yang sangat rendah. Asal masuknya unsur logam berat ke dalam perairan secara alami dibagi tiga antara lain a) berasal dari pantai termasuk sungai-sungai serta hasil pengikisan oleh gelombang dan pelapukan batuan, b) berasal dari lautan akibat aktivitas vulkanik yang berada di dalam laut, c) berasal dari atmosfir dalam bentuk partikel atau debu yang jatuh ke dalam laut.
Amin dan Nurrachmi (2005) juga mengatakan bahwa konsentrasi logam berat pada fraksi halus lebih tinggi dari fraksi kasar. Amin (2008) menyatakan bahwa konsentrasi logam berat tidak selalu terdapat pada partikel yang lebih kecil. Jumlah dari jenis logam berat yang terdapat dalam limbah industri tergantung dari jenis industri yang terdapat pada suatu daerah, dimana dapat diramalkan jenis pencemaran logam berat yang mungkin terjadi. Banyaknya masukan logam berat dalam sedimen terdapat di daerah galangan kapal/dock yard, pelabuhan kapal, dan daerah pembuangan karena logam berat akan mengendap dan terakumulasi dalam sedimen.
Tabel 2.1 Kadar normal dan maksimum beberapa logam berat yang masuk ke lingkungan laut
Unsur Kadar (ppm)
Normal (A) Maksimum (B)
Merkuri 0,15 0,1
Timbal 0,03 50
Kadmium 0,11 10
Mangan 1,9 100
Kromium 0,2 50
Sumber : (A) = Walddichuk (1974) dan (B) = EPA (1973) dalam Hutagalung (1984).
12
nilai pH yang relatif bersifat basa (pH = 7,40-8,59) di lokasi tempat logam tersebut sukar larut dan mengendap ke dasar perairan (Hutagalung 1997).
Logam berat timbal (Pb) adalah polutan di laut yang sangat berbahaya (Rompas 2010). Salah satu sumber Pb berasal dari bahan bakar minyak dari perahu-perahu nelayan. Logam ini masuk ke dalam tubuh biota laut melalui insang, permukaan tubuh dan juga rantai makanan. Logam Pb yang masuk ke dalam perairan laut akan merusak ekosistem terumbu karang (Manuputty 2002). Logam Pb yang terakumulasi dalam tubuh biota laut akan menyebabkan terhambatnya pertumbuhan, meningkatnya mortalitas, penurunan laju metabolisme serta menurunkan kemampuan reproduksi biota laut (Nganro 2009). Logam berat Pb dapat dihasilkan dari berbagai kegiatan, seperti kegiatan industri. Industri yang berpotensi sebagai sumber pencemaran Pb adalah semua industri yang memakai Pb sebagai bahan baku maupun bahan penolong, misalnya industri pengecoran maupun pemurnian, industri baterai, industri bahan bakar, industri kabel, serta industri kimia yang menggunakan bahan pewarna. Selain itu sumber Pb dapat berasal dari sisa pembakaran pada kendaraan bermotor dan proeses pertambangan.
Kadar logam berat dalam sedimen lebih tinggi dibandingkan dalam air laut. Hal ini menunjukkan adanya akumulasi logam berat dalam sedimen dan memungkinkan logam berat dalam air mengalami proses pengenceran dengan adanya pengaruh pola arus pasang surut. Rendahnya kadar logam berat dalam air laut, bukan berarti bahan cemaran yang mengandung logam berat tersebut tidak berdampak negatif terhadap perairan, tetapi lebih disebabkan oleh kemampuan perairan tersebut untuk mengencerkan bahan cemaran yang cukup tinggi.
Baku mutu logam berat di dalam lumpur atau sedimen di Indonesia belum ditetapkan, padahal senyawa-senyawa logam berat lebih banyak terakumulasi dalam sedimen (karena proses pengendapan) yang terdapat kehidupan biota dasar. Biota dasar yang resisten terhadap perubahan kualitas lingkungan akibat tercemar oleh logam berat dapat dijadikan sebagai indikator pencemaran (Amin dan Nurrachmi 2005).
Kontaminasi Logam Berat pada Organisme Perairan
13 biomagnifikasi logam berat pada manusia apabila manusia mengonsumsi organisme air maupun air yang tercemar logam berat tersebut.
Unsur-unsur logam berat dapat masuk ke dalam tubuh organisme laut melalui rantai makanan, insang, dan difusi melalui permukaan kulit. Logam berat dapat mengumpul dalam tubuh organisme dan akan tetap tinggal dalam tubuh pada waktu yang lama sebagai racun yang terakumulasi (Palar 2004). Logam berat yang terkontaminasi ke organisme perairan juga dapat mengakibatkan kecacatan pada organisme perairan tersebut maupun keturunannya misalnya pada kerang hijau (Cordova 2010; Riani dan Cordova 2011) dan pada Chironomidae (Riani et al. 2014).
Menurut Amin et al. (2011), pencemaran logam berat terhadap lingkungan laut berhubungan erat dengan penggunaan logam oleh manusia, yang esensial maupun non esensial yang secara alami selalu ditemukan dalam lingkungan laut, namun pada umumnya kadarnya masih di bawah nilai ambang yang membahayakan kehidupan organisme. Pengaruh aktivitas manusia melalui pembuangan limbah mengakibatkan meningkatnya kadar logam berat di lingkungan laut yang akan merusak lingkungan dan kehidupan organisme laut, bahkan menjadi bumerang bagi kehidupan manusia itu sendiri.
Peningkatan kadar logam berat dalam air laut akan mengakibatkan logam berat yang semula dibutuhkan untuk berbagai proses metabolisme akan berubah menjadi racun bagi organisme laut. Selain berubah menjadi racun logam berat yang akan terakumulasi dalam sedimen dan biota melalui proses gravitasi, biokonsentrasi, bioakumulasi dan biomagnifikasi oleh biota laut. Peningkatan kadar logam berat dalam air laut yang terus berlangsung akan diikuti oleh peningkatan kadar logam berat dalam tubuh biota yang berada dalam lingkungan tersebut.
Suatu logam berat dapat dipandang sebagai racun apabila logam-logam berat tersebut merugikan pertumbuhan atau metabolisme sel, bila logam berat tersebut berada di atas konsentrasi yang diperkenankan (Hutagalung 1991). Kadar logam berat yang terlalu rendah di perairan dapat menyebabkan organisme yang hidup di dalamnya menderita defisiensi. Namun unsur logam berat dalam jumlah yang berlebihan akan bersifat racun (Mulyani et al. 2012).
Menurut Thoha (1991), bahan pencemar yang masuk ke dalam perairan akan membunuh biota yang paling peka, sehingga mengganggu rantai makanan dalam perairan tersebut. Terputusnya salah satu rantai makanan dapat menyebabkan beberapa jenis biota tidak hidup normal. Selanjutnya Palar (2004) mengemukakan bahwa logam berat dapat megumpul dalam tubuh organisme dan akan tetap tinggal dalam tubuh pada waktu yang lama sebagai racun yang terakumulasi.
Kontaminasi Logam Berat Pada Manusia
14
sehingga ada nama khusus terhadap keracunan logam tertentu, yaitu : "minamata disease" karena keracunan metil Merkuri, ―itai-itai disease" karena keracunan Cd dan "plumbism" karena keracunan Pb. Keracunan akut dari logam berbahaya tersebut biasanya terjadi pada orang yang termakan dalam atau karena pengaruh pemberian obat yang mengandung logam. Hal tersebut biasanya terjadi pada kelompok orang tertentu atau perorangan. Tetapi pada keracunan kronis yang disebabkan oleh orang yang mengkonsumsi logam dalam jumlah sedikit tetapi berlangsung lama, biasanya terjadi dalam komunitas atau penduduk yang tinggal dalam suatu lingkungan yang tercemar (Darmono 2001).
Logam berat secara langsung maupun tidak langsung dapat membahayakan manusia seperti Pb dapat mengakibatkan penghambatan sistem pembentukan hemoglobin (Hb) sehingga menyebabkan anemia, terganggunya sistem syaraf pusat dan tepi, sistem ginjal, sistem reproduksi, idiot pada anak-anak, sawan (epilepsi), cacat rangka dan merusak sel-sel somatik (Darmono 2001). Walaupun jumlah Pb yang diserap oleh tubuh hanya sedikit, logam ini ternyata menjadi sangat berbahaya. Hal ini disebabkan senyawa-senyawa Pb dapat memberikan efek racun terhadap banyak organ yang terdapat dalam tubuh (Palar 2004).
Histopatologi
Toksikologi adalah ilmu yang mempelajari aksi berbahaya zat kimia atas sistem biologi. Peristiwa timbulnya pengaruh berbahaya atau efek toksik racun atas makhluk hidup, melalui beberapa proses. Pertama kali makhluk hidup mengalami pemejanan dengan racun. Berikutnya, setelah mengalami absorpsi dari tempat pemejanannya, racun atau metabolitnya kan terdistribusi ke tempat aksi (sel sasaran atau reseptor) tertentu yang ada di dalam diri makhluk hidup. Ditempat aksi ini, kemudian terjadi interaksi antara racun atau metabolitnya dan komponen penyusun sel sasaran atau reseptor. Adapun sebagai akibat sederetan peristiwa biokimia dan biofisika berikutnya, akhirnya timbul pengaruh berbahaya atau efek toksik dengan wujud dan sifat tertentu (Widowati et al. 2008).
Ketoksikan racun ditentukan oleh keberadaan racun ditempat aksi, dan keadaan ini bergantung pada keefektifan absorpsi, distribusi dan eliminasi racun tersebut. Keefektifan absorpsi racun menentukan kecepatan dan kadar atau jumlah racun yang ada dalam sirkulasi darah. Keefektifan distribusi menentukan kecepatan dan kadar jumlah racun yang ada dalam tempat aksi tertentu. Dan keefektifan eliminasi, menentukan kadar atau jumlah racun dan lama tinggal racun di tempat aksinya.
15 tentang adaptasi yang tidak cukup terhadap perubahanperubahan lingkungan eksternal dan internal (Spector 1993).
Ikan Selar Tetengkek (Megalaspis cordyla)
Ikan selar tetengkek merupakan salah satu ikan yang hidup di perairan Teluk Palu dan sering ditangkap oleh nelayan setempat. Hasil tangkapan nelayan selanjutnya dijual di pinggir pantai dan di Pasar Kota Palu. Dikenal dengan nama ikan kuli-kuli oleh masyarakat Kota Palu. Merupakan ikan pelagis yang hidup secara bergerombol di perairan pantai.
Klasifikasi berdasarkan Nelson (1994) :
Phylum : Chordata
Sub Phylum : Vertebrata Superclass : Gnathostoma
Grade : Teleostomi
Class : Actinopterygii Subclass : Neopterygii Division : Teleostei Subdivision : Eutelestei Superiorder : Ostariophysi
Ordo : Perciformes
Sub Ordo : Percoidei
Familia : Carangidae
Genus : Megalaspis
[image:31.595.99.471.147.775.2]Species : Megalaspis cordyla (Lynnaeus, 1758)
Gambar 2. 2 Ikan selar tetengkek (Sumber: Foto pribadi)
16
Ciri-ciri morfologis ikan selar tetengkek antara lain: - Ukuran tubuh maksimal sekitar 80 cm panjang total
- Tubuh bagian dorsal berwarna abu kebiruan atau kehijauan, warna tersebut memudar menjadi keperakan ke arah sisi dan perut. Di bagian belakang operkulumnya dijumpai noktah hitam yang besar.
- Tubuhnya memanjang dan subsilindris
- Sirip dorsal pertama dengan VII duri, sirip dorsal II dan I duri dan 18-20 jari-jari lemah.
- Sirip anal dengan II+I duri dan 16-17 jari-jari lemah - Di belakang sirip dorsal dan sirip anal dijumpai 7-10 finlet
- Gurat sisinya melengkung di bagian anterior, sisik pada gurat sisi 21-28. Di bagian belakang sisik tersebut lurus dengan 51-59 scutes yang besar - Matanya tertupi selaput transparan kecuali di bagian pupil
- Tergolong ikan pelagis yang berkelompok, jarang dijumpai di terumbu karang
17
3
METODE
Waktu dan Tempat Penelitian
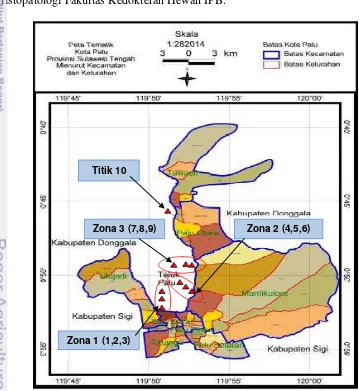
[image:33.595.117.476.337.728.2]Penelitian dilakukan pada bulan Februari – April 2015 di Teluk Palu Provinsi Sulawesi Tengah dan di laboratorium. Pengambilan sampel dilakukan pada bulan Februari 2015 dan analisis di laboratorium dilakukan pada bulan Maret sampai April 2015. Pengambilan sampel air, sedimen dan ikan selar tetengkek dilakukan pada 10 titik sampling yang ditentukan secara sengaja dengan pertimbangan sumber pencemar di darat, maka dibagi menjadi tiga zona masing-masing terdiri dari tiga titik sampling dan satu titik sampling yang mewakili daerah yang jauh dari sumber pencemar. Analisis salinitas, chemical oxigen demand (COD), ammonia dan nitrat dilakukan di Laboratorium Sumberdaya Alam dan Lingkungan, Universitas Tadulako Palu. Analisis Hg dan Pb pada air laut, sedimen dan organ insang, daging, hati dan limpa ikan selar tetengkek dilakukan di Laboratorium Kimia Fakultas MIPA IPB, dan pembuatan preparat histopatologi, pengamatan, fotografi dan analisis dilakukan di Laboratorium Histopatologi Fakultas Kedokteran Hewan IPB.
Gambar 3.1 Peta lokasi penelitian (Sumber: BPS Kota Palu 2013) Titik 10
Zona 1 (1,2,3)
18
Alat dan Bahan
Alat-alat yang digunakan dalam penelitian ini antara lain pH meter, DO meter, GPS, thermometer, turbiditymeter, sechidisk, peralatan pengambilan sampel air seperti botol sampel, dan peralatan di laboratorium seperti gelas kimia, gelas ukur, tabung reaksi, oven, pemanas (hotplate), timbangan analitik, pipet, batang pengaduk dan AAS (Atomic Absorption Spectrophotometer) merek Shimadzu tipe ASC 7000 serta alat-alat untuk pembuatan preparat histologi seperti microtome, block holder, objeck glass danMikroskop dan optilab. Sampel sedimen diambil dengan menggunakan ekman grab. Sampel ikan diambil dengan menggunakan jaring nelayan. Bahan yang digunakan dalam penelitian ini antara lain sampel air, ikan dan sedimen, aquadest, dan bahan kimia di laboratorium seperti alkohol, H2O2 dan HNO3. Pengamatan histopatologi menggunakan bahan
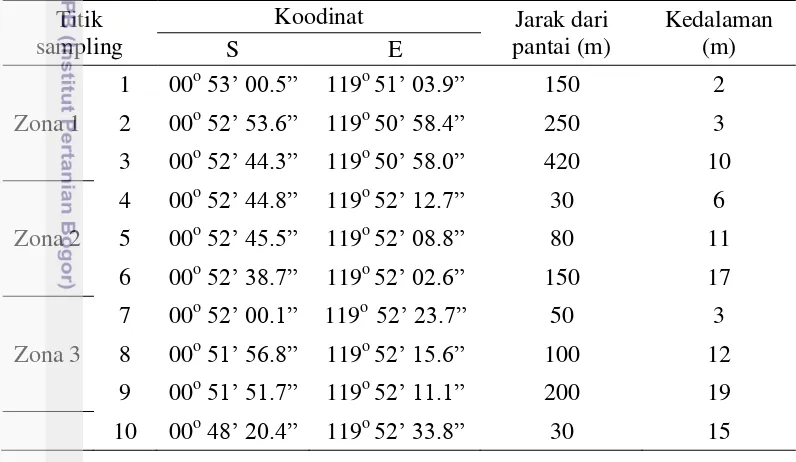
[image:34.595.83.481.304.535.2]seperti alkohol, formalin 10 %, paraffin, xyline dan minyak eosin. Tabel 3.1 Koordinat titik sampling, jarak dari pantai dan kedalaman
Titik sampling
Koodinat Jarak dari
pantai (m)
Kedalaman (m)
S E
Zona 1
1 00o53’ 00.5‖ 119o 51’ 03.λ‖ 150 2 2 00o52’ 53.6‖ 119o 50’ 58.4‖ 250 3 3 00o52’ 44.3‖ 119o 50’ 58.0‖ 420 10
Zona 2
4 00o52’ 44.8‖ 119o 52’ 12.7‖ 30 6 5 00o52’ 45.5‖ 119o 52’ 08.8‖ 80 11 6 00o52’ 38.7‖ 119o 52’ 02.6‖ 150 17
Zona 3
7 00o52’ 00.1‖ 119o 52’ 23.7‖ 50 3 8 00o51’ 56.8‖ 119o 52’ 15.6‖ 100 12 9 00o51’ 51.7‖ 119o 52’ 11.1‖ 200 19 10 00o48’ 20.4‖ 119o 52’ 33.8‖ 30 15
Penentuan Titik dan Pengambilan Sampel
19 Pada masing-masing titik dilakukan pengukuran parameter fisik-kimia air, pengambilan sampel air, sedimen dan biota ikan. Identifikiasi sampel ikan yang diambil dari lapangan dilakukan di Pusat Penelitian Biologi-LIPI, Cibinong. Koordinat titik sampling dan kedalaman dapat dilihat pada Tabel 3.1. Kondisi dan dokumentasi di lokasi penelitian dapat dilihat pada Lampiran 1.
Pengambilan sampel air dilakukan dengan menggunakan botol polietilen mengacu pada SNI 6989.57:2008. Sebelum melakukan pengambilan sampel terlebih dahulu dilakukan pengukuran parameter fisik kimia seperti suhu, pH, kecerahan dan, DO. Pengambilan sampel air langsung menggunakan botol sampel pada kedalaman ± 30 cm di setiap titik. Sampel air yang akan diukur kadar logam beratnya (Hg dan Pb) ditambahkan HNO3 sebagai pengawet sampai pH < 2
kemudian disimpan dalam cool box selanjutnya dibawa ke laboratorium untuk dianalisis. Sampel sedimen diambil dengan menggunakan ekman grab. Sedimen diambil sebanyak 300 gram lalu dimasukkan ke dalam plastik polietilen dan dan disimpan dalam cool box selanjutnya dibawa ke laboratorium untuk dianalisis kandungan Hg dan Pb. Pengambilan sampel ikan dilakukan dengan menggunakan jaring. Sampel ikan adalah ikan yang hidup secara liar di perairan Teluk Palu. Sampel ikan adalah salah satu jenis ikan yang dipilih dan hidup di lokasi penelitian. Sampel ikan dimasukkan ke dalam kantong plastik, lalu disimpan dalam cool box dan dibawa ke laboratorium untuk dianalisis kandungan logam berat (Hg dan Pb) pada organ insang, hati dan dagingnya.
Prosedur Kerja
Analisis Kualitas Air Laut
Pada penelitian ini dilakukan pengambilan sampel air di setiap titik pengambilan sampel dengan menggunakan botol polietilen. Sebelum melakukan pengambilan sampel terlebih dahulu dilakukan pengukuran parameter fisik kimia seperti suhu, pH, kecerahan, DO dan untuk mengukur kekeruhan, ammoniak, nitrat, Salinitas, COD dilakukan di Laboratorium Analisis Sumberdaya Alam dan Lingkunga Fakultas Pertanian, Universitas Tadulako Palu. Pengukuran logam berat Hg dan Pb akan dilakukan di Laboratorium Kimia Fakultas MIPA IPB dengan menggunakan AAS yang mengacu pada SNI 19-6964.2-2003 untuk Hg dan SNI 6989.8-2009 untuk Pb. Lebih jelasnya parameter-parameter kualitas air yang diamati, alat yang digunakan dan tempat analisis pada penelitian ini dapat dilihat pada Tabel 3.2.
Analisis Hg dan Pb pada Sedimen
Adapun langkah-langkah analisis logam berat Hg dan Pb pada sedimen (Siaka 2008) mengacu pada SNI 06-6992.2-2004 untuk Hg dan SNI 06-6992.3-2004 untuk Pb.
Perlakuan Sampel
Pengayakan Sampel Sedimen
20
pada ukuran tersebut lebih banyak mengikat senyawa-senyawa logam (Siaka 2008). Butiran sedimen yang bercampur dengan air laut (ukuran ≤ 63 µm) diendapkan selama paling sedikit 24 jam. Selanjutnya, cairan yang jernih didekantasi dan endapannya dikeringkan dalam oven pada suhu tidak lebih dari 60 °C hingga diperoleh berat konstan. Sedimen kering yang diperoleh digerus kemudian disimpan dalam botol kering sebelum dianalisis lebih lanjut.
Penyiapan Sampel
Ditimbang dengan teliti 2 gram sedimen kering dan dimasukkan ke dalam gelas piala, kemudian ditambahkan 20 mL campuran HNO3 dan H2O2 (1:1) dan
didestruksi selama tiga jam pada suhu 120 °C. Hasil destruksi ini disaring dan filtratnya ditampung dalam labu ukur 50 mL dan diencerkan dengan aquades sampai tanda batas. Filtrat ini kemudian diukur dengan AAS.
Pembuatan Kurva Kalibrasi
Kurva kalibrasi dibuat dengan cara mengukur absorbans dari sederetan konsentrasi larutan standar yang telah dibuat, kemudian dibuat grafik yang menunjukkan hubungan antara absorbans dengan konsentrasi larutan standar. Masing-masing larutan diukur absorbansinya pada = 217,0 nm untuk Pb dan = 324,7 nm untuk Hg
Penentuan Konsentrasi Logam Hg dan Pb
Filtrat hasil destruksi diukur dengan AAS menggunakan lebar celah 1 nm untuk Pb dan 0,5 nm untuk Hg. Penentuan konsentrasi logam Pb dan Hg pada sampel dilakukan dengan teknik kurva kalibrasi yang berupa garis linier, sehingga dapat ditentukan konsentrasi sampel dari absorbansi yang terukur. Setelah konsentrasi pengukuran diketahui, maka konsentrasi sebenarnya dari Pb dan Hg dalam sampel kering dapat ditentukan dengan perhitungan :
Ket :
M : Konsentrasi logam (Hg atau Pb) dalam sampel (mg/kg),
C : Konsentrasi yang diperoleh dari kurva kalibrasi (mg/L),
V : Volume larutan sampel (mL),
F : Faktor pengenceran, dan
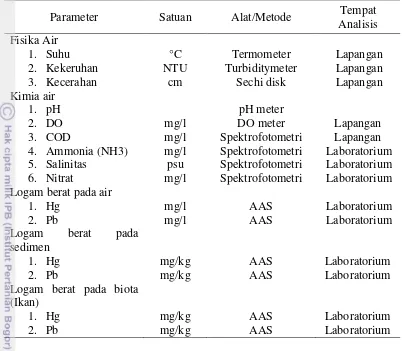
21 Tabel 3.2 Parameter kualitas air, sedimen dan ikan yang diamati.
Parameter Satuan Alat/Metode Tempat
Analisis Fisika Air 1. Suhu 2. Kekeruhan 3. Kecerahan °C NTU cm Termometer Turbiditymeter Sechi disk Lapangan Lapangan Lapangan Kimia air 1. pH 2. DO 3. COD
4. Ammonia (NH3) 5. Salinitas 6. Nitrat mg/l mg/l mg/l psu mg/l pH meter DO meter Spektrofotometri Spektrofotometri Spektrofotometri Spektrofotometri Lapangan Lapangan Laboratorium Laboratorium Laboratorium Logam berat pada air
1. Hg 2. Pb mg/l mg/l AAS AAS Laboratorium Laboratorium Logam berat pada
sedimen 1. Hg 2. Pb mg/kg mg/kg AAS AAS Laboratorium Laboratorium Logam berat pada biota
(Ikan) 1. Hg 2. Pb mg/kg mg/kg AAS AAS Laboratorium Laboratorium
Analisis Hg dan Pb pada Sampel Ikan Selar Tetengkek
Berikut tahapan kerja untuk analisis logam merkuri (Hg) pada ikan yang mengacu pada SNI 06-6992.2-2004.
1. Timbang 1 gram contoh (insang, daging, hati dan limpa) ikan dari masing-masing ikan dari setiap titik sampling, masukkan ke dalam labu dekstruksi, tambahkan 2 ml HNO3 dan 1 ml H2O2 dan masukkan ke dalam oven
microwave
2. Buat blanko dengan pemakaian pereaksi seperti yang digunakan pada contoh, kemudian siapkan deret standar.
3. Tambahkan 20 ml larutan pereduksi ke dalam, larutan dekstruksi dan larutan blanko.
4. Baca absorbansi larutan deret standar, larutan dekstruksi dan larutan blanko dengan menggunakan AAS tanpa nyala pada panjang gelombang 257,7 nm. 5. Buat kurva kalibrasi dengan sumbu Y sebagai absorbansi dan sumbu X
sebagai konsentrasi (ppm).
22
Berikut tahapan kerja untuk analisis logam timbal (Pb) pada ikan mengacu pada SNI 01-2354.6-2006.
1. Timbang contoh (insang, daging, hati, dan limpa) masing masing 1 gram dari masing-masing titik sampling, masukkan dalam cawan kuarsa 1 ml.
2. Tutup cawan tersebut dengan tutup kaca pyrek dan disangga, kemudian arangkan selama ± 24 jam di atas pemanas listrik pada suhu 300 °C.
3. Apabila contoh (insang, daging, hati, dan limpa) ikan sudah tidak berasap lagi, lanjutkan pengabuan pada suhu 400 °C selama dua jam dan sempurnakan pengabuan tersebut pada suhu 500 °C selama 20 jam.
4. Angkat cawan berisi abu dan dinginkan.
5. Larutkan dengan 5 ml asam nitrat 2 M dan hangatkan diatas pemanas air selama tiga menit.
6. Pindahkan larutan ke dalam labu ukur 10 ml. Bilas cawan dan impitkan ukur dengan HNO3 2 M.
7. Buat Larutan deret standar 1, 2, 4, 8, 10 dan 20 ppb.
8. Kerjakan blanko dengan menggunakan pereaksi yang samaseperti pada contoh. 9. Baca absorbansi larutan blanko, standard an contoh dengan menggunakan
AAS pada panjang gelombang 293,3 nm.
10.Buat kurva kalibrasi dengan sumbu Y sebagai absorbansi dan sumbu X sebagai konsentrasi.
11.Hitung timbal dengan menggunakan rumus:
Pengamatan Histopatologi
Berikut Langkah-langkah dalam mengamati jaringan histopatologi pada organ insang, daging, hati dan limpa ikan yang terkontaminasi logam berat Hg dan Pb (Setijaningsih 2009).
1. Contoh ikan
Contoh ikan yang digunakan untuk keperluan pengamatan histologi adalah ikan yang diperoleh di masing-masing titik pengambilan sampel, kemudian diambil bagian insang, hati, limfa dan dagingnya.
2. Pengawetan (fixation)
Organ insang, daging, hati, dan limpa ikan dimasukkan yaitu neutral bufferet formalin 10% dengan rasio sampel dan pengawet 1:10.
3. Pemotongan dan refiksasi
Organ yang diamati dipotong dengan menggunakan pisau kira-kira 1x1x1 cm, kemudian diletakkan dalam kotak sampel atau kaset jaringan dan fikasasi dalam larutan formalin 10% selama 1 hari. Selama pemotongan organ, specimen direndam dalam air untuk melindungi spesimen dari kekeringan. 4. Tahapan proses jaringan
Automatic tissue processor adalah alat yang digunakan untuk jaringan. Jenis bahan kimia yang digunakan, urutan dan lamanya proses berlangsung tertera pada Tabel 3.3.
23 Penanaman contoh organ insang, daging, hati, dan limpa dalam paraffin dilakukan dengan alat Tissue Embedding Centre. Alat ini harus dinyalakan dua jam sebelum proses dimulai, agar paraffin yang ada di container mencair. Ambil contoh organ letakkan dalam blok paraffin isi dengan paraffin cair, proses ini berlangsung pada tempat yang alasnya panas (hot plate) pada suhu 65 °C. Kemudian didinginkan dengan cara diapungkan ke atas permukaan air sampai paraffin membeku atau dimasukkan dalam frezer selama 5-10 menit. 6. Pemotongan
Pemotongan digunakan alat microtome, dimana contoh organ yang sudah membeku diletakkan pada block holder kemudian dipotong dengan ketebalan pemotongan sekitar 4-5 µm. Hasil potongan jaringan diletakkan dalam wadah yang berisi air pada suhu 40 °C. Langka berikutnya hasil potongan jaringan diletakkan pada kaca objek dipanaskan dengan alat pemanas (hot plate) pada suhu 60 °C selama 15 menit.
7. Pewarnaan (staining) Hematoksilin/Phloxin (HE)
Sebelum pewarnaan, paraffin yang menempel pada kaca objek direndam dengan xilene dan alkohol. Kaca objek siap diamati dengan menggunakan mikroskop pada perbesaran 40x10.
8. Mikrofotografi
Hasil pengamatan dilakukan mikrofotografi, yaitu pemotretan dan bagian yang akan difoto ditandai terlebih dahulu.
Tabel 3.3 Jenis bahan kimia dan lama pemprosesan contoh.
No Bahan Kimia Lama Proses (jam)
1 2 3 4 5 6 7 8 9 10 11 12 Alkohol 70% Alkohol 70% Alkohol 80% Alkohol 80% Alkohol 90% Alkohol 90% Alkohol 100% Alkohol 100% Xylene Xylene Parafin Parafain 1 1 1 1 1 1 1 1 2 2 2 3 Analisa Data
Kandungan Logam Berat (Hg dan Pb) dalam Air, Sedimen dan Ikan Selar Tetengkek
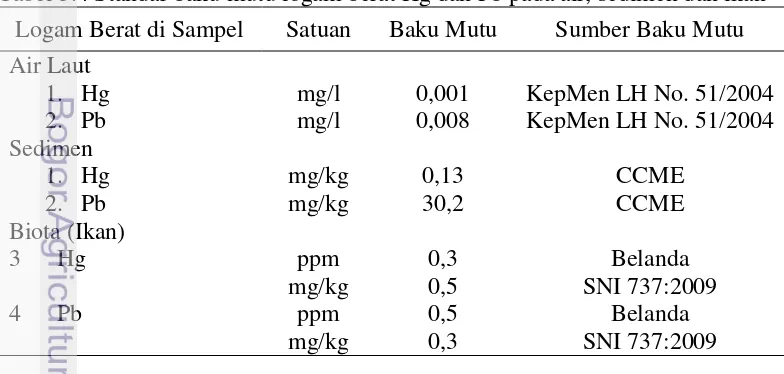
24
dan Pb dalam sedimen dibandingkan dengan standar baku mutu CCME, ANZECC dan NOAA. Standar baku mutu Hg dan Pb dalam sedimen dari beberapa pedomean mutu dapat dilihat pada Lampiran 2. Kandungan logam berat Hg dan Pb dalam organ ikan selar tetengkek dibandingkan dengan baku mutu SNI 7387:2009. Hasil pengamatan kondisi histopatologi dianalisis secara deskriptif. Standar baku mutu logam berat Hg dan Pb dapat dilihat pada Tabel 3.4.
Korelasi Kandungan Logam Berat (Hg dan Pb) dalam Air, Sedimen dan Ikan Selar Tetengkek
Keeratan hubungan antara kandungan logam berat merkuri (Hg) dan timbal (Pb) dalam air dengan kandungan logam berat merkuri (Hg dan timbal (Pb) dalam sedimen dan ikan dihitung dengan analisis korelasi (Matjik dan Sumartajaya 2000). Adapun Koefisien korelasinya dihitung berdasarkan rumus sebagai berikut :
Keterangan :
r : Koefisien korelasi
Syx : Sebaran nilai pengamatan x dan y Sx2 : Keragaman nilai x
Sy2 : Keragaman nilai y
x : Kandungan merkuri (Hg) atau timbal (Pb) di air
[image:40.595.86.478.527.714.2]y : Kandungan merkuri (Hg) atau timbal (Pb) di sedimen/ikan
Tabel 3.4 Standar baku mutu logam berat Hg dan Pb pada air, sedimen dan ikan Logam Berat di Sampel Satuan Baku Mutu Sumber Baku Mutu Air Laut 1. Hg 2. Pb mg/l mg/l 0,001 0,008
25
Analisis Histopatologi
Disamping menganalisis kandungan logam berat yang ada dalam tubuh ikan, juga dilakukan analisis preparat histopatologi jaringan tubuh ikan dari organ insang, daging, hati dan limpa. Melalui cara ini dapat diketahui jenis-jenis kerusakan yang diduga diakibatkan oleh kontaminasi logam berat Hg dan Pb pada organ-organ tersebut.
Analisis Deskriptif
Keseluruhan data hasil pengukuran dan analisis kualitas air dan kontaminasi logam berat Hg dan Pb pada sedimen, badan air maupun pada ikan selar tetengkek disajikan dalam bentuk tabel, grafik dan dianalisis secara deskriptif.
26
4
HASIL DAN PEMBAHASAN
Kondisi Kualitas Air di Teluk Palu
Suhu
Hasil analisis kulitas air yang diukur di Teluk Palu disajikan pada Lampiran 3. Suhu perairan merupakan salah satu parameter fisika yang sangat penting, karena dapat digunakan untuk mengidentifikasi badan air secara umum (Cahyana 2006), dan juga sangat penting bagi kehidupan biota air. Setiap biota memiliki batas toleransi yang berbeda-beda terhadap suhu terendah dan tertinggi untuk kelangsungan hidupnya secara optimal. Suhu perairan berpengaruh terhadap kelarutan oksigen, komposisi substrat, kekeruhan maupun kecepatan reaksi kimia di dalam air. Suhu juga berpengaruh terhadap osmoregulasi dan pernapasan pada organisme parairan. Perubahan suhu pada permukaan air laut dapat menimbulkan penurunan dan peningkatan kerapatan air pada permukaan laut. Peningkatan dan penurunan suhu perairan juga dapat berpengaruh terhadap organisme perairan dan pada kondisi ekstrim dapat menyebabkan kematian.
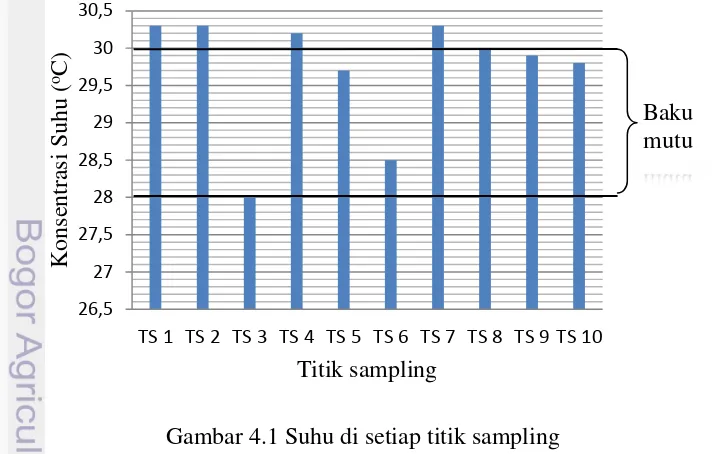
[image:42.595.102.462.466.693.2]Hasil pengukuran suhu di lokasi penelitian berkisar antara 28 °C hingga 30,30 °C (Gambar 4.1). Suhu terendah terdapat di titik sampling 3 dan tertinggi di titik sampling 1, 2 dan 7 dengan rata-rata sebesar 29,7 °C. Menurut Hadikusumah (2008) suhu permukaan air laut dipengaruhi oleh faktor-faktor seperti keseimbangan kalor dan keseimbangan masa air di lapisan permukaan laut. Lebih lanjut dikatakan bahwa distribusi suhu dan salinitas di perairan dipengaruhi oleh faktor-faktor seperti penyerapan panas (heat flux), curah hujan (presipitation), aliran sungai (flux) dan pola sirkulasi arus.
Gambar 4.1 Suhu di setiap titik sampling
Berdasarkan KepMen LH No. 51 Tahun 2004 tentang baku mutu air laut untuk
biota laut suhu air laut berkisar 28 °C– 30 °C untuk ekosistem koral dan lamun, dan
28 °C – 32 °C untuk ekosistem mangrove. Ekosistem koral dan lamun merupakan
26,5 27 27,5 28 28,5 29