PEMBUATAN PELAPIS CAMPURAN LARUTAN KITOSAN
DENGAN EMULSI LILIN LEBAH
SKRIPSI
OLEH:
DAPOT TUA SINAGA 070305028/THP
DEPARTEMEN TEKNOLOGI PERTANIAN
FAKULTAS PERTANIAN
Dapot Tua Sinaga: PEMBUATAN PELAPIS CAMPURAN LARUTAN KITOSAN DENGAN EMULSI LILIN LEBAH dibimbing oleh : Terip
Karo-Karo dan Ridwansyah ABSTRAK
Penelitian dilakukan untuk mengetahui adanya pengaruh konsentrasi larutan kitosan dan konsentrasi emulsi lilin lebah terhadap pelapis campuran. Penelitian ini menggunakan rancangan acak lengkap dengan dua faktor, yaitu konsentrasi larutan kitosan (K) : (0%, 15%, 30% dan 45%) dan konsentrasi emulsi lilin lebah (L) : (0%, 15%, 30% dan 45%). Parameter yang dianalisa adalah ukuran partikel, stabilitas relatif emulsi, viskositas, uji organoleptik warna, uji total mikroba dan pH.
Hasil penelitian menunjukkan bahwa konsentrasi larutan kitosan memberi pengaruh berbeda sangat nyata terhadap viskositas dan uji total mikroba, berbeda nyata terhadap stabilitas relatif emulsi dan berbeda tidak nyata terhadap ukuran partikel, uji organoleptik warna dan pH. Konsentrasi emulsi lilin memberi pengaruh berbeda sangat nyata terhadap ukuran partikel, stabilitas relatif emulsi, viskositas, organoleptik warna dan pH, dan berbeda tidak nyata terhadap uji total mikroba. Interaksi antara konsentrasi larutan kitosan dan konsentrasi emulsi lilin memberi pengaruh berbeda sangat nyata terhadap pH Konsentrasi larutan kitosan 45 % dan konsentrasi emulsi lilin 45 %, menghasilkan pelapis campuran yang paling baik.
Kata kunci: Larutan Kitosan, Emulsi Lilin, Pelapis Campuran.
Dapot Tua Sinaga: THE MAKING OF COATING MIXTURE FROM CHITOSAN SOLUTION AND WAX EMULSION Supervised by : Terip
Karo-Karo and Ridwansyah ABSTRACT
The experiment objective was to study the effect of chitosan solution concentration and concentration of wax emulsion on coating mixture. The design of the experiment was completely randomized design with two factors. The first factor was four levels of chitosan solution concentration : 0,15, 30 and 45 % and the second factor was four levels of concentration wax emulsion: 0, 15, 30 and 45 %. Parameters observed were particle size, emulsion relative stability, viscosity, color (organoleptic), microbe activity and pH.
The results showed that chitosan solution concentration had highly significantly affected the viscosity and microbe activity, significantly affected the emulsion relative stability, but did not affected the particle size, color (organoleptic) and pH. The concentration of wax emulsion had highly significantly affected the particle size, emulsion relative stability, viscosity, color (organoleptic) and pH, but did not affected the microbe activity. The interaction of chitosan solution concentration and concentration of wax emulsion had highly significantly affected the pH. The best characteristic of coating mixture was obtained on 45 % chitosan solution concentration and 45 % concentration of wax emulsion.
RINGKASAN
DAPOT TUA SINAGA, “Pembuatan Pelapis Campuran Emulsi Lilin
Lebah dengan Larutan Kitosan” dibimbing oleh Ir. Terip Karo-Karo, MS., selaku
ketua komisi pembimbing dan Ridwansyah, STP, Msi., selaku anggota komisi
pembimbing.
Penelitian ini bertujuan untuk mengetahui pengaruh konsentrasi larutan
kitosan dan konsentrasi emulsi lilin lebah terhadap sifat fisik pelapis campuran
yang dihasilkan.
Penelitian ini menggunakan rancangan acak lengkap faktorial dengan 2
faktor, yaitu:
Faktor I : Konsentrasi larutan kitosan dalam pelapis campuran
K1 = 0 %
K2 = 15 %
K3 = 30 %
K4 = 45 %
Faktor II : Konsentrasi emulsi lilin lebah dalam pelapis campuran
L1 = 0 %
L2 = 15 %
L3 = 30 %
L4 = 45 %
1. Ukuran Partikel
Konsentrasi larutan kitosan memberi pengaruh berbeda tidak nyata (p>0.05)
terhadap Ukuran partikel . Ukuran partikel tertinggi terdapat pada perlakuan K2
yaitu sebesar 2,76 µm dan terkecil pada perlakuan K3 yaitu sebesar 2,50 µm.
Konsentrasi emulsi lilin memberi pengaruh berbeda sangat nyata (p<0.01)
terhadap Ukuran partikel. Ukuran partikel tertinggi terdapat pada perlakuan K2
yaitu sebesar 3,74 µm dan terkecil pada perlakuan K1 yaitu sebesar 0.43 µm.
2. Stabilitas Relatif Emulsi
Konsentrasi larutan kitosan memberi pengaruh berbeda nyata (p<0.05)
terhadap stabilitas relatif emulsi. Stabilitas relatif emulsi tertinggi terdapat pada
perlakuan K4 yaitu sebesar 81.25 % dan terendah terdapat pada perlakuan K1 dan
K2yaitu sebesar 62.50 %.
Konsentrasi emulsi lilin memberi pengaruh berbeda sangat nyata (p<0.01)
terhadap stabilitas relatif emulsi. Stabilitas relatif emulsi tertinggi terdapat pada
perlakuan L1 yaitu sebesar 100 % dan terendah terdapat pada perlakuan L2 yaitu
sebesar 56.25 %
3. Viskositas
Konsentrasi larutan kitosan memberi pengaruh berbeda sangat nyata
(p<0.01) terhadap viskositas. Viskositas tertinggi terdapat pada perlakuan K4
yaitu sebesar 2.030 Centi Poise dan terendah pada perlakuan K1 yaitu sebesar
1.485 Centi Poise .
Konsentrasi emulsi lilin memberi pengaruh berbeda sangat nyata (p<0.01)
2.026 Centi Poise dan terendah terdapat pada perlakuan L1 yaitu sebesar 1.437
Centi Poise.
4. Uji Organoleptik Warna
Konsentrasi larutan kitosan memberi pengaruh berbeda tidak nyata (p>0.05)
terhadap uji organoleptik warna. Uji organoleptik warna tertinggi terdapat pada
perlakuan K2 dan K4 yaitu sebesar 2.83 dan terendah terdapat pada perlakuan K1
yaitu sebesar 2.44.
Konsentrasi emulsi lilin lebah memberi pengaruh berbeda sangat nyata
(p<0.01) terhadap uji organoleptik warna. Uji organoleptik warna tertinggi
terdapat pada perlakuan L4 yaitu 3.43 dan terendah terdapat pada perlakuan L1
yaitu sebesar 1.04.
5. Uji Total Mikroba
Konsentrasi larutan kitosan memberi pengaruh berbeda sangat nyata
(p<0.01) terhadap Uji total mikroba. Uji total mikroba tertinggi terdapat pada
perlakuan K1 yaitu 52.1 x 103 koloni/ml dan terendah terdapat pada perlakuan K4
yaitu sebesar 21.8 x 103 koloni/ml.
Konsentrasi emulsi lilin lebah memberi pengaruh berbeda tidak nyata
(p>0.05) terhadap Uji total mikroba. Uji total mikroba tertinggi pada perlakuan L1
yaitu 35.8 x 103 Koloni/ml dan yang terendah pada perlakuan L2 yaitu 35.5 x 103
koloni/ml.
6. pH
Konsentrasi larutan kitosan memberi pengaruh berbeda tidak nyata (p>0.05)
Konsentrasi emulsi lilin lebah memberi pengaruh berbeda sangat nyata
(p<0.01) terhadap pH. pH yang tertinggi terdapat pada L4 yaitu 8.75 dan
terendah terdapat pada perlakuan L1 yaitu 7.19
Interaksi konsentrasi larutan kitosan dengan konsentrasi emulsi lilin lebah
DAFTAR ISI
DAFTAR LAMPIRAN
...
xiii
PENDAHULUAN
Pendayagunaan Limbah Udang... 8
Kandungan Kimia Limbah Udang... ... 8
Kitin dan Kitosan ... 9
Kitin ... 9
Kitosan ... 9
Sifat-sifat kitin dan kitosan... 11
Kitosan sebagai anti mikroba... . 12
Standar mutu kitosan ... 12
Emulsi ... 12
Sistem emulsi ... 12
Emulsifier ... 13
Stabilitas emulsi... 14
Analisa sifat fisik emulsi ... 15
Ukuran partikel ... 15
Viskositas ... 16
pH ... 17
Penelitian Sebelumnya ... 17
BAHAN DAN METODA PENELITIAN Waktu dan Tempat Penelitian ... 18
Pelaksanaan Penelitian ... 20
Pembuatan Kitosan ... 20
Pembuatan Larutan Kitosan 2 % dalam Asam Asetat 2 % ... 21
Pengambilan Lilin dari Sarang Lebah ... 21
Pembuatan Emulsi Lilin Lebah 30 % ... 21
Pencampuran Emulsi Lilin Lebah dengan Larutan Kitosan ... 22
Pengamatan dan Pengukuran Data ... 22
Penentuan Ukuran Partikel ... 22
Stabilitas Relatif Emulsi ... 23
Penentuan Viskositas ... 23
Uji Organoleptik Warna ... 24
Skema pengambilan Lilin dari Sarang Lebah... .. 29
Skema Pembuatan Emulsi Lilin Lebah... 30
Skema Pencampuran Larutan Kitosan dengan Emulsi Lilin Lebah... ... 31
HASIL DAN PEMBAHASAN Pengaruh Konsentrasi Larutan Kitosan pada Zat Pelapis terhadap Parameter yang diamati ... 32
Pengaruh Konsentrasi Emulsi Lilin Lebah pada Zat Pelapis terhadap Parameter yang diamati ... 33
Ukuran Partikel Pengaruh Konsentrasi Larutan Kitosan pada Zat Pelapis terhadap Ukuran Partikel ... 34
Pengaruh Konsentrasi Emulsi Lilin Lebah pada Zat Pelapis terhadap Ukuran Partikel ... 34
Pengaruh Interaksi Antara Konsentrasi Larutan kitosan dan Konsentrasi Emulsi Lilin Lebah pada Zat Pelapis terhadap Ukuran Partikel... ... 36
Stabilitas Relatif Emulsi
terhadap Stabilitas Relatif Emulsi ... 37 Pengaruh Konsentrasi Emulsi Lilin Lebah pada Zat Pelapis
terhadap Stabilitas Relatif Emulsi ... 38 Pengaruh Interaksi Antara konsentrasi Larutan Kitosan dan
Konsentrasi Emulsi Lilin Lebah pada Zat Pelapis
terhadap Stabilitas Relatif Emulsi ... ... 40 Viskositas
Pengaruh Konsentrasi Larutan Kitosan pada Zat Pelapis
terhadap Viskositas ... 41 Pengaruh Konsentrasi Emulsi Lilin Lebah pada Zat Pelapis
terhadap Viskositas ... 42 Pengaruh Interaksi Antara Konsentrasi Larutan kitosan dan
Konsentrasi Emulsi Lilin Lebah pada Zat Pelapis
terhadap Viskositas... ... 44 Nilai Organoleptik Warna
Pengaruh Konsentrasi Larutan Kitosan pada Zat Pelapis
terhadap Nilai Organoleptik Warna ... 44 Pengaruh Konsentrasi Emulsi Lilin Lebah pada Zat Pelapis
terhadap Nilai Organoleptik Warna... 44 Pengaruh Interaksi Antara Konsentrasi Larutan kitosan dan
Konsentrasi Emulsi Lilin Lebah pada Zat Pelapis
terhadap Uji Organoleptik Warna... ... 46 Uji Total Mikroba
Pengaruh Konsentrasi Larutan Kitosan pada Zat Pelapis
terhadap Uji total Mikroba ... 46 Pengaruh Konsentrasi Emulsi Lilin Lebah pada Zat Pelapis
terhadap Uji Total Mikroba... 48 Pengaruh Interaksi Antara Konsentrasi Larutan kitosan dan
Konsentrasi Emulsi Lilin Lebah pada Zat Pelapis
terhadap terhadap Uji Total Mikroba ... ... 48 pH
Pengaruh Konsentrasi Larutan Kitosan pada Zat Pelapis
terhadap pH ... 48 Pengaruh Konsentrasi Emulsi Lilin Lebah pada Zat Pelapis
terhadap pH ... 49 Pengaruh Interaksi Antara Konsentrasi Larutan kitosan dan
Konsentrasi Emulsi Lilin Lebah pada Zat Pelapis
DAFTAR TABEL
No. JUDUL Hal
1. Kandungan Kimia Limbah Udang ... 8
2. Konsentrasi Kitosan Terendah yang Menghambat Pertumbuhan Mikroorganisme ... 12
3. Standar Mutu Kitosan ... 12
4. Penentuan Stabilitas Relatif Emulsi ... 23
5. Nilai Uji Organoleptik Warna ... 24
6. Pengaruh Konsentrasi Larutan Kitosan pada Zat Pelapis terhadap Parameter yang diamati ... 32
7. Pengaruh Konsentrasi Emulsi Lilin Lebah pada Zat Pelapis terhadap Parameter yang diamati ... 33
8. Uji LSR Efek Utama Pengaruh Konsentrasi Emulsi Lilin Lebah pada Zat Pelapis terhadap Ukuran Partikel ... 35
9. Uji LSR Efek Utama Pengaruh Konsentrasi Larutan Kitosan pada Zat Pelapis terhadap Stabilitas Relatif Emulsi ... 37
10. Uji LSR Efek Utama Pengaruh Konsentrasi Emulsi Lilin Lebah pada Zat pelapis terhadap Stabilitas Relatif Emulsi ... 39
11. Uji LSR Efek Utama Pengaruh Konsentrasi Larutan Kitosan Pada Zat Pelapis terhadap Viskositas ... 41
12. Uji LSR Efek Utama Pengaruh Konsentrasi Emulsi Lilin Lebah Pada zat pelapis terhadap Viskositas ... 43
13. Uji LSR Efek Utama Pengaruh Konsentrasi Emulsi Lilin Lebah Pada zat pelapis terhadap Uji Organoleptik Warna ... 45
14. Uji LSR Efek Utama Pengaruh Konsentrasi Larutan Kitosan Pada Zat Pelapis terhadap Uji Total Mikroba ... 47
15. Uji LSR Efek Utama Pengaruh Konsentrasi Emulsi Lilin Lebah Pada Zat pelapis terhadap pH ... 49
DAFTAR GAMBAR
No. JUDUL Hal
1. Struktur Kitin ... 9
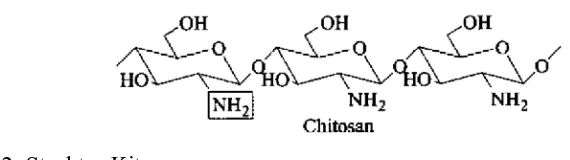
2. Struktur Kitosan ... 11
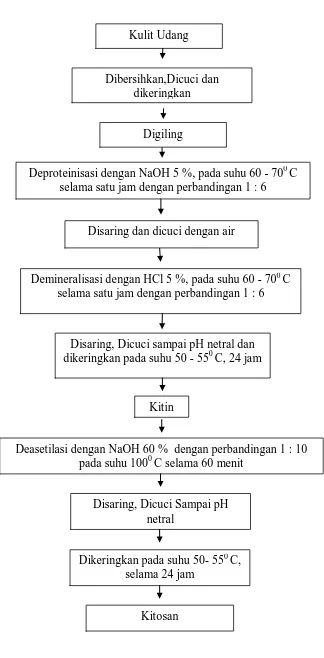
3. Proses Pembuatan Kitosan ... 27
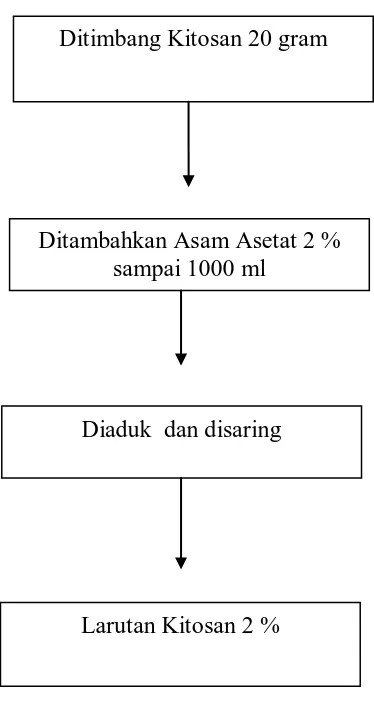
4. Proses Pembuatan Larutan Kitosan 2% ... 28
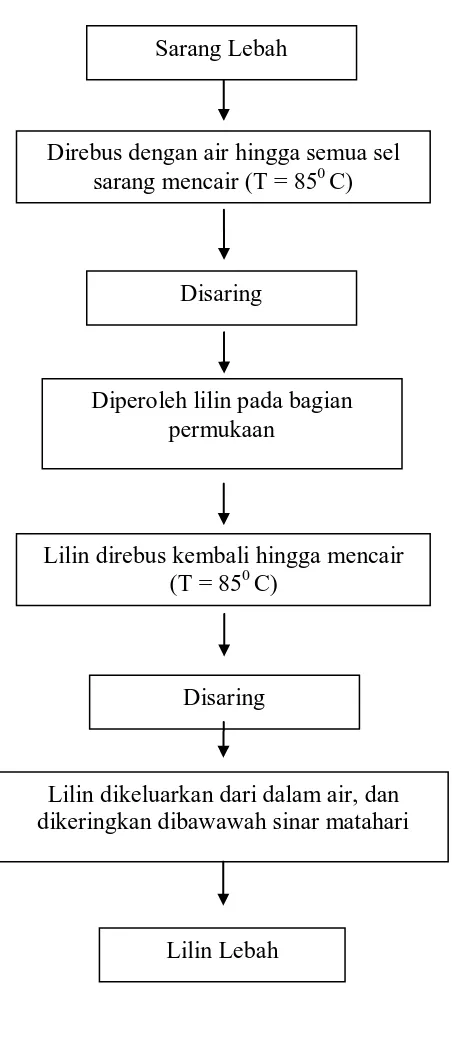
5. Proses Pembuatan Lilin Lebah ... 29
6. Proses Pembuatan Emulsi Lilin Lebah ... 30
7. Proses Pembuatan Pelapis Campuran Larutan Kitosan dengan Emulsi Lilin Lebah ... 31
8. Grafik Hubungan Konsentrasi Emulsi Lilin Lebah pada Zat Pelapis terhadap Ukuran Partikel ... 35
9. Grafik Hubungan Konsentrasi Larutan Kitosan pada Zat Pelapis terhadap Stabilitas Relatif Emulsi ... 38
10. Grafik Hubungan Konsentrasi Emulsi Lilin Lebah pada Zat Pelapis terhadap Stabilitas Relatif Emulsi ... 39
11. Grafik Hubungan Konsentrasi Larutan Kitosan pada Zat pelapis terhadap Piskositas ... 41
12. Grafik Hubungan Konsentrasi Emulsi Lilin Lebah pada Zat pelapis terhadap Piskositas ... 43
13. Grafik Hubungan Konsentrasi Emulsi Lilin Lebah pada Zat Pelapis terhadap Uji Organoleptik Warna ... 45
14. Grafik Hubungan Konsentrasi Larutan Kitosan pada Zat Pelapis terhadap Uji Total Mikroba ... 47
15. Grafik Hubungan Konsentrasi Emulsi Lilin Lebah pada Zat Pelapis terhadap pH ... 50
RIWAYAT HIDUP
DAPOT TUA SINAGA dilahirkan di Saribudolok pada tanggal 01
Desember 1988. Anak pertama dari bapak J. Sinaga dan ibu M. Br. Girsang,
Penulis merupakan anak pertama dari empat bersaudara.
Tahun 2000 penulis lulus dari SD Negeri 04 Saribudolok, tahun 2003 lulus
dari SLTP Bunda Mulia Saribudolok, dan tahun 2006 lulus dari SMA RK Serdang
Murni Lubuk Pakam. Pada tahun 2007 penulis lulus seleksi masuk Universitas
Sumatera Utara (USU) melalui jalur SPMB. Penulis lulus di Program Studi
Teknologi Hasil Pertanian Departemen Teknologi Pertanian, Fakultas Pertanian.
Selama mengikuti kuliah penulis menjabat sebagai asisten di Laboratorium
Analisa Kimia Bahan Pangan (AKBP). menjadi pengurus IM-THP (Ikatan
Mahasiswa Teknologi Hasil Pertanian), dan anggota di Ikatan Mahasiswa
Simalungun (IMAS-USU).
Penulis telah melaksanakan Praktek Kerja Lapangan (PKL) di Pabrik
KATA PENGANTAR
Puji dan syukur terlebih dahulu penulis panjatkan kepada Tuhan Yang
Maha Esa atas berkat dan anugerah-Nya sehingga skripsi ini dapat selesai. Skripsi
ini berjudul “Pembuatan Pelapis Campuran Larutan Kitosan dengan Emulsi
Lilin”.
Pada kesempatan ini penulis mengucapkan terima kasih yang
sebesar-besarnya kepada Ir. Terip Karo-Karo, MS selaku ketua komisi pembimbing, serta
Ridwansyah, STP, MSi selaku anggota komisi pembimbing yang telah banyak
memberikan bimbingan, pengarahan serta saran-saran dalam menyelesaikan
skripsi ini.
Penulis menyampaikan terima kasih yang sedalam-dalamnya kepada Ayah
saya, bapak J. Sinaga dan Ibu saya, ibu M. br Girsang atas segala doa, dukungan,
perhatian dan kasih sayangnya. Kepada Adek-adek saya yang tercinta Nofrita
Sinaga, Adi Putra Sinaga dan Ronaldo Sinaga.
Penulis juga mengucapkan terima kasih kepada teman – teman
seperjuangan THP’07 yang tidak dapat penulis sebutkan satu persatu yang telah
banyak membantu penulis selama perkuliahan hingga penyelesaian skripsi ini.
Akhir kata penulis mengucapkan terima kasih dan semoga skripsi ini dapat
bermanfaat bagi pihak yang membutuhkan.
Medan, Agustus 2011
Dapot Tua Sinaga: PEMBUATAN PELAPIS CAMPURAN LARUTAN KITOSAN DENGAN EMULSI LILIN LEBAH dibimbing oleh : Terip
Karo-Karo dan Ridwansyah ABSTRAK
Penelitian dilakukan untuk mengetahui adanya pengaruh konsentrasi larutan kitosan dan konsentrasi emulsi lilin lebah terhadap pelapis campuran. Penelitian ini menggunakan rancangan acak lengkap dengan dua faktor, yaitu konsentrasi larutan kitosan (K) : (0%, 15%, 30% dan 45%) dan konsentrasi emulsi lilin lebah (L) : (0%, 15%, 30% dan 45%). Parameter yang dianalisa adalah ukuran partikel, stabilitas relatif emulsi, viskositas, uji organoleptik warna, uji total mikroba dan pH.
Hasil penelitian menunjukkan bahwa konsentrasi larutan kitosan memberi pengaruh berbeda sangat nyata terhadap viskositas dan uji total mikroba, berbeda nyata terhadap stabilitas relatif emulsi dan berbeda tidak nyata terhadap ukuran partikel, uji organoleptik warna dan pH. Konsentrasi emulsi lilin memberi pengaruh berbeda sangat nyata terhadap ukuran partikel, stabilitas relatif emulsi, viskositas, organoleptik warna dan pH, dan berbeda tidak nyata terhadap uji total mikroba. Interaksi antara konsentrasi larutan kitosan dan konsentrasi emulsi lilin memberi pengaruh berbeda sangat nyata terhadap pH Konsentrasi larutan kitosan 45 % dan konsentrasi emulsi lilin 45 %, menghasilkan pelapis campuran yang paling baik.
Kata kunci: Larutan Kitosan, Emulsi Lilin, Pelapis Campuran.
Dapot Tua Sinaga: THE MAKING OF COATING MIXTURE FROM CHITOSAN SOLUTION AND WAX EMULSION Supervised by : Terip
Karo-Karo and Ridwansyah ABSTRACT
The experiment objective was to study the effect of chitosan solution concentration and concentration of wax emulsion on coating mixture. The design of the experiment was completely randomized design with two factors. The first factor was four levels of chitosan solution concentration : 0,15, 30 and 45 % and the second factor was four levels of concentration wax emulsion: 0, 15, 30 and 45 %. Parameters observed were particle size, emulsion relative stability, viscosity, color (organoleptic), microbe activity and pH.
The results showed that chitosan solution concentration had highly significantly affected the viscosity and microbe activity, significantly affected the emulsion relative stability, but did not affected the particle size, color (organoleptic) and pH. The concentration of wax emulsion had highly significantly affected the particle size, emulsion relative stability, viscosity, color (organoleptic) and pH, but did not affected the microbe activity. The interaction of chitosan solution concentration and concentration of wax emulsion had highly significantly affected the pH. The best characteristic of coating mixture was obtained on 45 % chitosan solution concentration and 45 % concentration of wax emulsion.
PENDAHULUAN
Latar belakang
Sarang lebah di Indonesia masih sangat kurang pemanfaatannya. Pada
pemanenan madu biasanya sarangnya tidak dimanfaatkan lebih lanjut oleh para
peternak lebah. Karena lilin yang berasal dari sarang lebah tersebut hanya
dimanfaatkan sebagai bahan pembuat lilin (bahan penerang) saja. Hal ini
mengakibatkan peternak lebah tidak begitu memperhatikannya sehingga sarang
lebah itu dibuang begitu saja. Dengan membuat sarang lebah menjadi emulsi
maka diharapkan daya guna dari sarang lebah ini lebih meningkat.
Lilin yang berasal dari sarang lebah memiliki sifat tidak beracun. Dan
apabila digunakan pada buah maka lilin tersebut dapat memperpanjang masa
simpan buah karena akan menghambat respirasi pada buah, menghambat
penguapan air dan dapat meningkatkan nilai estetika buah.
Kitosan adalah produk terdeasetilasi dari kitin yang merupakan biopolimer
alami kedua terbanyak di alam setelah selulosa, yang banyak terdapat pada
serangga, krustasea, dan fungi. Diperkirakan lebih dari 109-1010 ton kitosan
diproduksi di alam tiap tahun. Sebagai negara maritim, Indonesia sangat
berpotensi menghasilkan kitosan, namun sampai saat ini di Indonesia masih
jarang ditemukan pemanfaatanya terutama dalam bidang pertanian.
Kitosan sangat berpotensi untuk dijadikan sebagai bahan antimikroba,
karena mengandung enzim lysosim dan gugus aminopolysacharida yang dapat
bakteri disebabkan kitosan memiliki polikation bermuatan positif yang mampu
menghambat pertumbuhan bakteri dan kapang.
Pembuatan pelapis campuran emulsi lilin dengan larutan kitosan
dimaksutkan untuk digunakan pada pelapisan buah-buahan yang terdapat di
Indonesia. Pelapis ini diharapkan akan meningkatkan daya simpan dan nilai
estetika buah yang dilapisi.
Kitosan adalah salah satu polisakarida yang digunakan sebagai stabilizer
emulsi. Karena sifat fisiologisnya tersebut, penggunaannya memberikan
kontribusi nilai-tambah yang bermanfaat bagi emulsi akhir yang dihasilkan.
Kitosan memiliki sifat aktivitas permukaan yang dapat meningkatkan baik
pembentukan dan stabilitas emulsi.
Emulsi cair melibatkan dua zat cair yang tercampur, tetapi tidak dapat
saling melarutkan, dapat juga disebut zat cair polar & zat cair non-polar. Biasanya
salah satu zat cair ini adalah air (zat cair polar) dan zat lainnya; minyak (zat cair
non-polar). Emulsi cair itu sendiri dapat digolongkan menjadi 2 jenis, yaitu
emulsi minyak dalam air atau emulsi air dalam minyak.
Dengan mencampurkan emulsi lilin dengan larutan kitosan diharapkan
akan medapatkan kelebihan yang terdapat pada emulsi lilin dan kelebihan yang
terdapat pada larutan kitosan sekaligus meningkatkan pemanfaatan lilin lebah dan
kitosan, sehingga penulis tertarik untuk melakukan penelitian mengenai
Tujuan Penelitian
Tujuan Penelitian ini adalah untuk mengetahui pengaruh perbandingan
konsentrasi larutan kitosan dan konsentrasi emulsi lilin lebah terhadap pelapis
yang dihasilkan.
Kegunaan Penelitian
- Sebagai sumber data di dalam penyusunan skripsi di Departemen
Teknologi Pertanian Fakultas Pertanian Universitas Sumatera Utara,
Medan.
- Sebagai sumber informasi pada pembuatan pelapis campuran larutan
kitosan dengan emulsi lilin lebah.
Hipotesa Penelitian
- Diduga ada konsentrasi larutan kitosan yang paling baik untuk
menghasilkan pelapis campuran yang paling baik.
- Diduga ada konsentrasi emulsi lilin lebah yang paling baik untuk
menghasilkan pelapis campuran yang paling baik.
- Diduga ada perbandingan konsentrasi larutan kitosan dengan
konsentrasi emulsi lilin lebah yang paling baik untuk menghasilkan
TINJAUAN PUSTAKA
Lebah
Lebah madu adalah insekta dimana lebah yang sudah dewasa dan yang
masih muda hidup bersama-sama. Sehingga lebah madu harus memiliki
perbekalan makanan yang banyak dalam bentuk madu. Lebah menghasilkan madu
melebihi yang mereka butuhkan dan inilah yang menjadi surplus bagi peternak
lebah. Lebah madu bukanlah hewan yang jinak seperti hewan yang lainnya.
Peternak lebah menyediakan box sebagai tempat tinggal untuk lebah, namun
demikian binatang ini masih tetap merupakan hewan yang liar (Ree, 1989).
Sistematika lebah madu adalah sebagai berikut:
Kingdom : Animalia
Filum : Arthropoda
Kelas : Insecta
Ordo : Hemenoptera
Famili : Apidae
Genus : Apis
Spesies : Apis andreniformis, Apis cerana, Apis dorsata, Apis florea, Apis
kosehenikovi, Apis laboriosa, Apis mellifera.
(Pusat Perlebahan Apiari Pramuka, 2005).
Menurut taksiran para ahli, untuk mendapatkan 1 kg lilin lebah diperlukan
12 kg nectar/sarang lebah. Lilin dibentuk dalam tubuh melalui proses kimia, lalu
dikeluarkan melalui kelenjar lilin yang terdapat pada segmen abdomen. Dengan
untuk dikunyah dan dibentuk menjadi semacam adonan. Setelah terbentuk, lalu
disiapkan di rahang depan untuk membangun dinding sel sarang. Selanjutnya,
lebah bekerja dengan menggunakan propolis. Propolis adalah bahan yang
dikumpulkan lebah dari kuncup tanaman, yang dibawa ke sarang dalam bakul
sarinya (Sarwono, 2001).
Malam (Lilin Lebah)
Ada tiga jenis lilin yang dikenal di alam, yakni yang berasal dari hewan,
tumbuhan dan petrolium atau mineral. Lilin asal hewan yakni lilin lebah (beewax)
adalah salah satu lilin yang kimianya stabil dan terkenal sepanjang sejarah
perdagangan dunia. Lilin lebah adalah lilin yang paling baik dan dihasilkan oleh
lebah pekerja dari empat pasang kelejar yang terdapat dibagian samping bawah
perut. Puncak sekresi lilin lebah adalah saat lebah pekerja berumur dua minggu.
Satu koloni lebah mengkonsumsi sekitar sepuluh kg madu untuk menghasilakan
satu kg lilin lebah (Sihombing, 1992).
Terdapat dua golongan kualitas malam yaitu:
1. Lilin lebah kualitas pertama, diperoleh dari sarang lebah yang masih baru dan
belum pernah diisi madu atau tepung sari oleh penghuninya. Malam yang
diperoleh dari sarang demikian ini warnanya putih dan bersih.
2. Lilin lebah kualitas kedua yaitu malam yang diperoleh dari sarang lebah yang
telah diisi madu serta telah diambil madunya.
(Sarwono, 2001).
Cara mendapatkan lilin lebah adalah dengan merebus sarang lebah dalam
dibuang. Setelah itu lilin lebah dibersihkan dari segala kotoran kemudian
didinginkan dengan demikian jadilah lilin lebah atau malam (Warisno, 1996).
Lilin lebah yang dipanasi di dalam air yang banyak, maka warna yang
berasal dari tempayak akan hilang dan larut dalam air, tetapi warna yang berasal
dari tepung sari tetap berada di dalam. Warna lilin lebah dari tepung sari
tergantung pada daerah dan waktu pengumpulan. Agar lilin lebah tidak berubah
dan rusak, panaskan lilin lebah dalam air. Lilin lebah yang asli dapat diketahui
dengan mudah, Lilin lebah yang asli warnanya putih, kuning atau orange bersih,
Mudah pecah kalau dingin. Pada suhu 85oF lunak tetapi tidak melekat ditangan
kalau lilin lebah tersebut dipijat. Bau lilin lebah yang khas adalah bau
tanam-tanaman (Sumoprastowo dan Suprapto, 1993).
Lilin lebah merupakan lilin yang kompleks dibentuk dari campuran
beberapa komponen meliputi hidrokarbon 14%, monoester 35%, diester 14%,
triester 3%, hidroksi monoester 4%, hidroksi poliester 8%, asam ester 1%, asam
poliester 2%, asam bebas, alkohol bebas 1%, dan 6% sisanya tidak diketahui.
Komponen utama dari lilin lebah adalah palmitat, palmitoleat, hidroksi palmitat
dan ester oleat yang berantai panjang (C30-C32) dari alkohol aliphatic.
Perbandingan triacontanil palmitat (CH3(CH2)29O-CO-(CH2)14CH3 dengan asam
serotik (CH3(CH2)24COOH, yaitu 6:1 (http://en.wikipedia.org., 2011).
Titik lebur lilin lebah murni berkisar antara 61-690C (142-156oF), indeks
refraksinya 1,44, tahanan dielektrisnya 2,9 dan berat jenis pada suhu 690C adalah
0.96 lebih ringan dari air. Tidak larut dalam air dan sedikit larut dalam alkohol
dingin. Benzen chloroform, karbon disulfida, eter dan beberapa minyak yang
dengan nyala kuning bersih dan mengeluarkan aroma unik. Malam sering
terkontaminasi dengan sedikit polen, propolis, dan madu yang meningkatkan berat
jenis dan warnanya (Sihombing, 1992).
Lilin lebah yang baik adalah lilin lebah yang baik dan murni, bebas dari
bahan campuran lainnya. Lilin lebah yang dibersihkan dengan memanasinya
dalam air, kadang-kadang airnya dicampuri dengan 20 % cuka keras dan 1 %
asam nitrat agar warna malam lebah menarik untuk dipasarkan. Lilin lebah dapat
dicampurkan dengan campuran lilin, tanah, lemak hewan yang keras. Lilin lebah
yang tidak murni tidak baik untuk membuat sarang lebah buatan
(Sumoprastowo dan Suprapto, 1993).
Udang
Udang merupakan jenis ikan konsumsi air payau, badan beruas berjumlah
13 ( 5 ruas kepala dan 8 ruas dada) dan seluruh tubuh ditutupi oleh kerangka luar
yang disebut eksoketelon. Udang dapat kita klasifikasikan sebagai berikut.
Klas : Crustaceae (Binatang berkulit keras)
Sub kelas : Malacostraca (Udang-udangan tingkat tinggi)
Super ordo : Decapoda (Binatang berkaki sepuluh)
Sub ordo : Natantia (kaki digunakan untuk berenang)
Famili : Palaemonidae, Penaeidae
Tubuh udang secara umum terbagi atas tiga bagian besar, yakni kepala dan
dada, badan, serta ekor. Sedangkan persentasinya adalah (36%-49%) bagian
kepala, daging keseluruhan (24%-41%) dan kulit ekor (17%-23%) dari seluruh
Pendayagunaan Limbah Udang
Limbah udang yang mencapai (30-40%) dari produksi udang beku belum
banyak dimanfaatkan. Moelyanto (1979) mengatakan bahwa pemanfaatan limbah
udang menjadi produk udang yang bernilai ekonomis tinggi merupakan contoh
yang sangat baik untuk memperoleh bahan makanan dengan kandungan protein
tinggi. Lebih lanjut dikatakan bahwa limbah udang selain dimanfaatkan sebagai
bahan pangan, dapat juga dipergunaakan untyuk keperluaan industri. Pembuatan
kitosan dari kulit udang dapat dipakai sebagai bahan kimia untuk industri.
Kepala udang yang menyatu dengan jengger udang sebagai limbah industri
udang beku baru sebagian kecil yang dimanfaatkan, yaitu dibuat tepung kepala
udang yang dibuat sebagai pencampur bahan dalam pembuattan pellet untuk
pakan ternak ( Mudjiman, 1982).
Kandungan Kimia Limbah Udang
Susunan kimia limbah udang dapat dilihat pada Tabel 1.
Tabel 1. Kandungan Kimia Limbah Udang (%)
Unsur Kepala udang Jengger udang
Air 78,51 69,30
Protein 12,28 20,70
Lemak 1,27 8,40
Abu 5,34 1,50
Sumber: Juhairi, 1986.
Kulit udang yang terdapat pada kepala, jengger dan tubuh udang
mengandung protein34,9%, kalsium 26,7%, Kitin 18,1% dan unsur lain seperti zat
Kitin dan Kitosan
Kitin
Kitin sebagai prekursor kitosan pertama kali ditemukan pada tahun 1811
oleh henri Braconnot (Prancis) ebagai hasil isolasi dari jamur. Sedangkan kitin
dari kulit serangga ditemukan kemudian ada tahun 1820. Kitin merupakan polimer
kedua terbesar dibumi setelah selulosa. Kitin adalah senyawa amino polisakarida
berbentuk polimer gabungan (Rismana, 2006).
Kitin adalah salah satu polisakarida yang paling banyak terdapat dialam,
khususnya kedua terbanyak, setelah selulosa. Kitin adalah hasil industri melalui
penggunaan bahan kimia atau enzimatik perlakuan limbah cangkang krustasea,
tetapi juga ditemukan di moluska, serangga, jamur dan organisme yang terkait.
Namun utilitasnya terbatas dalam aplikasi industri karena kitin sangat sukar larut,
yang disebabkan oleh kekakuan rantai linearnya (Calero. Et al, 2010).
Struktur kitin dapat dilihat pada Gambar 1.
Gambar 1. Struktur Kitin
(Iranian Polimer Jurnal, 2002)
Kitosan
Kitosan [poli-(b-1 / 4)-2-amino-2-deoksi-D-glukopiranosa] adalah nama
kolektif untuk deasetilasi sebagian atau keseluruhan senyawa kitin. Karena
banyak aplikasi telah ditemukan baik kitosan itu sendiri atau dicampur dengan
polimer alam yang lain (kanji, gelatin, alginat) dalam makanan, farmasi, tekstil,
pertanian, pengolahan air dan industri kosmetik. Aktivitas antimikrobial kitosan
telah terbukti menghambat banyak bakteri, filamen jamur dan juga ragi
(Kong. et al, 2010).
Investigasi sifat antimikroba dari kitosan telah menjadi perjalanan panjang
sampai eksplorasi ilmiah dan pengembangan teknologi. Perjalanan dimulai dari
dua dekade yang lalu, dengan studi tentang biologi fenomena yang timbul dari
jamur patogen makanan dan pertanian (Rabea et al, 2003.). Selanjutnya Bakteri
mendapat perhatian lebih dalam menemukan antimikroba berkhasiat. Penelitian
waktu itu biasanya dilakukan melalui kimia, biokimia, mikrobiologi dan tes medis
kitosan serta turunannya. Antimikroba kitosan dan turunannya tergantung pada
faktor-faktor intrinsik dan ekstrinsik, seperti pH, jenis mikroorganisme, ada atau
tidak adanya kation logam, pKa, Berat molekul (Mw) dan derajat deasetilasi (DD)
kitosan (Kong. et al, 2010).
Kitosan memiliki spektrum yang luas terhadap aktivitas dan tingkat
pembunuhan yang tinggi terhadap Gram-positif dan Gram-negatif bakteri, tetapi
toksinitas yang rendah terhadap sel mamalia (Franklin dan Snow, 1981;
Takemono et al, 1989). Sebelumnya spektrum aktivitas antibakteri kitosan
pertama kali diusulkan oleh Allen (Allan dan Hardwiger, 1979), dan memiliki
potensi untuk dikembangkan. Antimikroba kitosan dan turunannya telah menarik
perhatian besar dari para peneliti (Kong. et al, 2010).
Gambar 2. Struktur Kitosan
(Iranian Polimer Jurnal, 2002)
Sifat-Sifat Kitin dan Kitosan
Kitin dan kitosan merupakan polimer biokompatibel, biodegradable dan
tidak beracun yang memperlihatkan kemampuan untuk berinteraksi dengan ion
logam, pewarna, protein, asam nukleat, lipid, herbisida, pestisida dan asam..
Mereka juga menunjukkan aktivitas antimikroba dan juga dapat digunakan
sebagai film dan coating menghambat pertumbuhan jamur dan bakteri selama
penyimpanan buah-buahan dan sayuran (Abreu dan Sergio, 2008).
Kitin dicirikan oleh sifatnya yang sangat susah larut dalam air dan
beberapa pelarut organik, rendahnya reaktivitas kimia dan sangat hidrofobik.
Ketiga sifat tersebut menyebabkan penggunaan kitin relatif lebih sedikit
dibandingkan kitosan dan derivatnya. Aplikasi kitin yang utama adalah sebagai
senyawa pengkelat logam dalam instalasi pengolahan air bersih atau limbah,
kosmetik, fungisida dan fungistatik penyembuh luka (Rismania, 2006).
Kitosan adalah salah satu polisakarida yang digunakan sebagai stabilizer
emulsi. Karena sifat fisiologisnya tersebut, penggunaannya memberikan
kontribusi nilai-tambah yang bermanfaat bagi emulsi akhir yang dihasilkan.
Kitosan memiliki sifat aktivitas permukaan yang dapat meningkatkan baik
Kitosan Sebagai Antimikroba
Aktivitas kitosan telah diteliti dapat menghambat banyak mikroorganisme
seperti jamur, alga dan beberapa bakteri. Kitosan sebagai anti jamur dan bakteri
dapat dilihat pada Tabel 2 berikut.
Tabel 2. aMIC (Minimum Inhibitor Concentration/Konsentrasi terendah Kitosan yang menghambat pertumbuhan Mikroorganisme).
Bakteri MICa(%)
Proteus mirabilis 0.025
Pseudumonas euroginonsa 0.0125
Proteus mirabilis 0.025
Salmonella enteriditis 0.05
Enterobacter aerogenes 0.05
Escherichia coli 0.025
Staphylococcus aurens 0.05
Corynebacterium 0.025
Enterococcus facalis 0.05
Staphylococcus epidermidis 0.025
Candida albicans/candida parapsilosis 0.1
(Kong. et al, 2010).
Standar Mutu Kitosan
Standar mutu kitosan yang beredar dipasaran dapat dilihat pada Tabel 3.
Tabel 3. Standar Mutu Kitosan
Sifat-sifat Kitosan Mutu yang dikehendaki
Ukuran partikel Butiran Atau Bubuk
Kadar Protein (%) <20
Kadar air (%) <20
Kdar abu (%) <2
Derajat Deasitilasi (%) >70 Sumber: Unhas (2003)
Emulsi
Sistem Emulsi
Emulsi adalah suatu sediaan yang mengandung dua zat cair yang tidak
butir-butir kecil dalam cairan yang lain. Dispersi ini tidak stabil, butir-butir-butir-butir ini akan
bergabung dan membentuk dua lapisan air dan minyak yang terpisah
(Anief, 1999).
Selanjutnya menurut Bird, et al., (1983), emulsi dapat dibedakan atas dua
tipe, yaitu emulsi dengan sistem o/w (oil in water) dan emulsi dengan sistem w/o
(water in oil). Kondisi tergantung dari bagian yang menjadi fase kontinu atau
bagian yang menjadi fase diskontinu. Contoh umum untuk emulsi o/w adalah air
susu dan mayonaise, sedangkan contoh emulsi w/o adalah margarin dan mentega.
Emulsifier
Emulsifier memiliki gugus polar dan gugus non-polar sekaligus dalam satu
molekulnya sehingga pada satu sisi dia akan mengikat minyak yang bersifat
non-polar dan disisi lainnya akan mengikat air yang bersifat non-polar. Selain memiliki
gugus polar dan non-polar dalam satu molekulnya, emulsifier memiliki
kemampuan untuk menurunkan tegangan antar muka dan tegangan permukaan.
Dengan turunnya tegangan antar muka ini akan mengurangi daya kohesi dan
sebaliknya meningkatkan daya adesi. Emulsifier ini membentuk lapisan tipis yang
akan menyelimuti partikel dan akan mencegah partikel tersebut bersatu dengan
partikel sejenisnya (Suryani, dkk., 2002).
Menurut Winarno (1988), daya kerja emulsifier disebabkan oleh bentuk
molekulnya yang dapat terikat baik pada minyak maupun pada air. Bila emulsifier
tersebut lebih terikat pada air atau larut dalam air (polar) maka dapat lebih
membantu terjadinya dispersi minyak dalam air (o/w). Sebaliknya bila emulsifier
lebih larut dalam minyak (non polar) terjadilah emulsi air dalam minyak (w/o).
1. Mengurangi tegangan antarmuka-stabilitas termodinamis.
2. Pembentukan suatu lapisan antar muka yang kaku-pembatas mekanik untuk
penggabungan.
3. Pembentukan lapisan listrik rangkap-penghalang elektrik untuk mendekati
partikel-partikel.
(Lachman, et al., 1994).
Stabilitas Emulsi
Zat aktif permukaan diarahkan pada suatu cara khusus pada antar muka.
Bagian hidrofilik berada dalam fase air sedangkan bagian lipofiliknya berada
dalam fase minyak. Selanjutnya zat aktif permukaan berorientasi pada antarmuka
adalah berkurangnya sedikit demi sedikit tegangan permukaan dengan berjalannya
waktu seiring dengan penambahan zat aktif permukaan sampai dicapai suatu
harga konstan. Sifat ini melukiskan bahwa molekul-molekul zat aktif permukaan
berdifusi melalui air sampai mencapai antarmuka dimana molekul-molekul
tersebut diadsorbsi membentuk sistem yang stabil (Lachman, et al., 1989).
Stabilitas emulsi adalah sifat emulsi tanpa adanya koalesen dari fase
intern, kriming, dan terjaganya rupa yang baik, bau, warna dan sifat-sifat fisis
yang lainnya. Peneliti lain mendefenisikan bahwa ketidakstabilan fisis suatu
emulsi adalah adanya agglomerasi dari fase intern dan terjadi pemisahan produk
(Anief, 1999).
Cukupnya bahan yang membentuk lapisan antar muka penting untuk
melindungi seluruh permukaan dari tiap tetesan dalam fase. Pembentukan emulsi
minyak dalam air atau air dalam minyak tergantung pada derajad kelarutan dari
Creaming adalah proses yang bersifat reversible, berbeda dengan proses
pecahnya emulsi yang bersifat irreversible. Flokul cream dapat mudah didispersi
kembali, dan terjadi campuran homogen bila digocok perlahan-lahan, karena
butir-butir tetesan tetap dilingkupi dengan film pelindung. Sedangkan koalesen,
dengan pengojokan sederhana akan gagal untuk mensuspensi kembali butir-butir
tetesan dalam bentuk emulsi yang stabil, karena film yang meliputi partikel sudah
rusak (Anief, 1999).
Perubahan emulsi o/w menjadi w/o dan sebaliknya disebut dengan istilah
inversi. Terjadinya inversi dipengaruhi oleh beberapa faktor yaitu jenis dan
jumlah pengemulsi, perubahan konsentrasi salah satu fase, dan ion-ion yang
terdapat dalam emulsi (Anief, 1999).
Analisa Sifat Fisik Emulsi
Beberapa sifat fisik yang mempengaruhi emulsi diantaranya adalah ukuran
partikel, stabilitas relatif emulsi, viskositas, dan pH.
1. Ukuran Partikel
Ukuran dan distribusi partikel menentukan kesetabilan suatu emulsi,
semakin baik distribusi ukuran dan semakin kecil diameter droplet, maka akan
stabil suatu emulsi. Ukuran partikel yang besar akan mempercepat gerak partikel.
Akibatnya semakin besar peluang terjadinya tabrakan antar sesama partikel
sehingga partikel cenderung bergabung menjadi partikel yang lebih besar dan
akhirnya menggumpal, dengan kata lain laju pengendapan semakin cepat sehingga
Selanjutnya Budianto dan Ariyanti, (2008) menyatakan bahwa
ukuran dan distribusi partikel sangat menentukan sifat emulsi, seperti sifat aliran
dan kestabilan emulsi.
2. Stabilitas Relatif Emulsi
Prinsip dasar tentang kestabilan emulsi ini adalah keseimbangan antara
gaya tarik menarik dan gaya tolak menolak yang terjadi antar partikel dalam
system emulsi. Apabila kedua gaya ini dapat dipertahankan tetap seimbang dan
terkontrol, maka partikel-partikel dalam sistem emulsi dapat dipertahankan agar
tidak bergabung ( Suryani, dkk., 2002).
Pemisahan fase emulsi dapat diamati dan dapat diukur volume dari fase
yang terpisah. Penting dibedakan antara creaming dan koalesan karena keduanya
berbeda (Anief, 1999).
Semakin tinggi viskositas dari suatu sistem emulsi maka semakin rendah
laju rata-rata pengendapan yang terjadi sehingga kestabilan emulsi juga semakin
tinggi (Suryani, dkk., 2002).
3. Viskositas
Peningkatan rasio minyak/air berarti penurunan fase pendispersi dan
meningkatnya fase terdispersi. Penurunan fase pendispersi ini mengakibatkan
viskositas akan semakin meningkat. Jadi apabila konsentrasi fase terdispersi
ditingkatkan maka akan diikuti oleh peningkatan viskositas yang dihasilkan
(Jost, et al., 1986).
Emulsifier dan lapisan interfacial akan mempengaruhi viskositas melalui
pengaruh terhadap sirkulasi internal droplet. Lapisan interfacial timbul karena
4. pH
pH adalah suatu zat/senyawa yang dipengaruhi oleh sifat dari zat/senyawa
tersebut. Menurut lewis (1924) basa adalah semua senyawa yang dapat
menyumbangkan pasangan elektron (OH-) dan sebaliknya asam adalah semua
senyawa yang dapat menerima pasangan elektron (OH-) ( Pikir, S., 1989).
Penelitian Sebelumnya
Menurut Ginting (1995) pada pembuatan emulsi lilin 12 % sebanyak 1
liter kemudian emulsi lilin ini dapat diencerkan sesuai dengan konsentrasi yang
diinginkan. Sebanyak 120 ml dipanaskan sampai mencair di dalam beaker glass.
Kemudian ke dalam 25 ml air panas ditambahkan 40 ml trietanolamin.
Sebelumnya ke dalam gelas ukur dimasukkan air panas supaya gelas ukur ini
menjadi panas. Setelah gelas ukur panas airnya dibuang. Kemudian ke dalam
gelas ukur tersebut dimasukkan lilin dengan asam oleat (20 ml) yang sudah
dicampur secara perlahan-lahan dan ditambahkan campuran air dengan
trietanolalamin, diaduk sampai terjadi emulsi lilin. Kemudian ditambahkan sisa
air panas sampai sebanyak 1 liter.
Selanjutnya menurut Batubara, (2001) pembuatan emulsi lilin dibuat
dengan melebur 120 g lilin lebah dalam wadah (sampai bersuhu 90-95oC); lalu
ditambahkan 20 ml asam oleat sedikit demi sedikit dan mengaduknya perlahan;
menambahkan 40 ml trietanolamin sambil mengaduk. Pembuatan emulsi
dilanjutkan dengan mengencerkan campuran tersebut dengan air panas (suhu
90-95oC) sampai volume 1000 ml lalu dihomogenisasi dengan mixer selama ± 15
menit dan akhirnya mendinginkannya untuk digunakan lebih lanjut. Hasil akhir
BAHAN DAN METODE PENELITIAN
Waktu dan Tempat Penelitian
Penelitian dilakukan bulan April – Juni 2011 di Laboratorium Analisa
Kimia Bahan Pangan Departemen Teknologi Pertanian Fakultas Pertanian
Universitas Sumatera Utara.
Bahan Penelitian
Kulit udang yang diperoleh dari industri pengolahan udang beku PT.
Centra Windu Sejahtera di kawasan Industri Medan dan sarang lebah yang
diperoleh dari yayasan bina saudara Titikuning Medan
Reagensia
Trietanolamin (TEA), Asam Oleat, Aquadest, NaOH, Asam Asetat, dan
Asam Klorida (HCl).
Alat penelitian
Beaker glass, Timbangan digital, inkubator, jarum hose, Saringan, Hot
plate, Termometer, Stirrer, pH meter, kertas saring, Oven, Labu ukur, Spatula,
Mikroskop optic, Object glass, Deck glass, cawan petrisish, kompor gas,
stopwatch, viskosimeter Ostwald dan Colony counter.
Metode Penelitian
Penelitian ini menggunakan metode Rancangan Acak Lengkap (RAL)
Faktor I : Konsentrasi larutan kitosan pada zat pelapis
K1 = 0 %
K2 = 15 %
K3 = 30 %
K4 = 45 %
Faktor II : Konsentrasi emulsi lilin lebah pada zat pelapis
L1 = 0 %
L2 = 15 %
L3 = 30 %
L4 = 45 %
Banyaknya kombinasi perlakuan (tc) adalah 4 x 4 = 16, Maka jumlah ulangan (n)
adalah sebagai berikut:
Tc (n-1) ≥ 15
16 (n-1) ≥ 15
16n – 16 ≥ 15
16n ≥ 31
n ≥ 1,9 dibulatkan menjadi n = 2
Model Rancangan (Sastrosupadi, 2000).
Rancangan yang digunakan adalah Rancangan Acak Lengkap (RAL) dua
factorial dengan model sebagai berikut:
Yijk = µ + αi + (αβ)ij+ εijk
Dimana:
Yijk : Hasil pengamatan dari faktor K pada taraf ke-I dan faktor P pada taraf
µ : Efek Nilai Tengah
αi : Efek dari faktor K pada taraf ke-i
βj : Efek dari factor P pada taraf ke-j
(αβ)ij : Efek interaksi faktor K pada taraf ke-I dan faktor P pada taraf ke-j
Εijk : Efek galat dari faktor K pada taraf ke-i dan faktor P pada taraf ke-j
dalam ulangan ke-k
Jika diperoleh hasil yang nyata atau sangat nyata kemudian dilanjutkan
dengan uji perbandingan sepasang nilai tengah dengan uji LSR (Least
Significant Range).
Pelaksanaan Penelitian
Pembuatan Kitosan
• Perlakuan Pendahuluan, kulit udang dicuci, dikeringkan dan digiling.
• Deproteinisasi, ditimbang 100 gr kulit udang kemudian dibuat larutan
NaOH 5 % dalam aquadest, kulit udang dimasukkan dalam NaOH dengan
Perbandingan kulit udang dan NaOH adalah 1:6 (berat/volume) kemudian
dipanaskan selama 1 jam dengan suhu 60-700C.
• Penyaringan, Kulit udang yang sudah dipanaskan dicuci dengan air
kemudian disaring.
• Demineralisasi, kulit udang dimasukkan dalam larutan HCl 5% dengan
perbandingan kulit udang dan larutan 1:6 (berat/volume) kemudian
dipanaskan selama 1 jam dengan suhu pemanasan 60-700C.
• Pencucian, bahan dicuci dengan air sampai pH netral
• Deasetilasi, setelah dikeringkan dipanaskan dalam larutan NaOH 60%
dengan perbandingan bahan dan larutan 1:10 (volume/volume) pada suhu
1000C selama 60 menit.
• Pencucian, bahan yang telah selesai dideasetilasi diangkat dan dicuci
dengan air sampai pH netral kemudian ditiriskan.
• Pengeringan, kitosan dikeringkan dalam oven dengan suhu 50-550C
selama 24 jam.
Pembuatan Larutan kitosan 2 % dalam Asam Asetat 2%
• Ditimbang kitosan 2 gr.
• Ditambahkan asam asetat 2 % sampai 100 ml, diaduk dan disaring.
Pengambilan Lilin dari Sarang lebah
Sarang lebah dipanaskan dalam panci perebusan sehingga semua sarang
lebah mencair. Kemudian sarang lebah yang telah mencair tersebut dipindahkan
sambil disaring kedalam wadah. Setelah itu diamkan sampai dingin dan pada
bagian permukaan akan terdapat gumpalan lilin dimana pada lilin itu masih
terdapat kotoran-kotoran sehingga harus dipanaskan kembali dan kemudian
disaring untuk mendapatkan lillin yang baik dan bersih dari kotoran-kotoran.
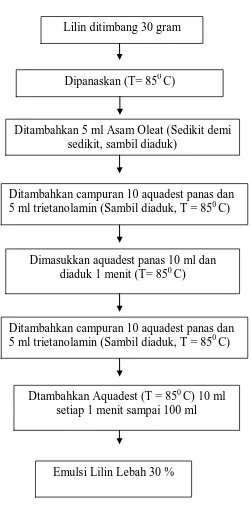
Pembuatan Emulsi Lilin Lebah 30 %
Untuk membuat emulsi lilin 30 %, lilin lebah ditimbang 30 gram,
kemudian dipanaskan di dalam gelas ukur hingga mencair (85oC), setelah
mencair ditambahkan 5 ml asam oleat sedikit demi sedikit dan mengaduknya
perlahan-lahan, kemudian ditambahkan campuran 10 ml aquadest panas dan 5 ml
diaduk selama 1 menit. Kemudian dimasukkan kembali campuran aquadest panas
10 ml dan 5 ml trietanolamin. Seterusnya ditambahkan sebanyak 10 ml aquadest
setiap 1 menit sampai volume 100 ml, sehingga komposisi total 30 gr lilin, asam
oleat 5 ml, Trietanolalamin 10 ml dan air 55 ml.
Pencampuran Emulsi Lilin Lebah dengan Larutan Kitosan
• Diambil larutan kitosan (0 %, 15 %, 30 % dan 45 % ).
• Ditambahkan emulsi lilin lebah (0 %, 15 %, 30 % dan 45 % ) sedikit
demi sedikit sambil diaduk dan dipanaskan dengan suhu 550C.
• Ditambhakan aquadest sambil diaduk sampai volume 100 ml.
• Diaduk selama 30 menit.
• Campuran emulsi lilin lebah dan larutan kitosan dianalisa.
Pengamatan dan Pengukuran Data
Pengamatan dan Pengukuran data dilakukan dengan cara analisa terhadap parameter:
1. Ukuran Partikel (μm)
2. Stabilitas Relatif Emulsi (%)
3. Viskositas (Poise)
4. Uji Organoleptik Warna (Numerik)
5. Uji Total Mikroba (Koloni/ml)
6. pH
Penentuan Ukuran Partikel (Friberg, et al., 1976).
Diambil sampel dengan menggunakan jarum hose dan diteteskan ke
glass telah dipanggang di atas api bunsen sebelumnya. Disiapkan mikroskop optik
(mikroskop cahaya) merk Olympus BH-2 dengan kamera vidio yang telah
disambungkan ke komputer dengan kabel kamera vidio. Diletakkan objeck glass
yang telah berisi sampel di atas meja preparat mikroskop, dilihat dengan
perbesaran 10, 40 atau 100 kali (dilihat dengan perbesaran mana tampilan yang
paling jelas). Setelah didapat ukuran partikel emulsi, lalu emulsi tersebut difoto.
Ditentukan ukuran partikel dengan menjumlahkan ukuran partikel terkecil hingga
terbesar dan merata-ratakannya.
Penentuan Stabilitas Relatif Emulsi (Anief, 1999 dimodifikasi).
Penentuan stabilitas relatif emulsi dilakukan dengan membiarkan sampel di
dalam gelas ukur/tabung reaksi dan dibiarkan selama 3 hari kemudian diamati
berdasarkan kriteria pada Tabel 4.
Tabel 4. Penentuan Stabilitas relatif Emulsi
Skor
Keterangan
0% Terjadi koalesen (kerusakan emulsi yang bersifat irreversible) dan terdapat
pemisahan antara air dan zat pelapis.
25% Terjadi koalesen tetapi tidak terdapat pemisahan antara air dan zat pelapis.
50% Terjadi creaming (kerusakan emulsi yang bersifat reversible), tetapi terdapat pemisahan antara air dan zat pelapis.
75% Terjadi creaming, tetapi tidak terjadi pemisahan antara air dan zat pelapis.
100% Tidak terjadi koalesen dan creaming.
Penentuan Viskositas (Yazid, 2005).
a. Penentuan waktu alir zat pada viskosimeter Oswald (t2)
• Sampel diisap dengan pompa kedalam bola sampai batas tanda yang
terdapat pada alat.
• Sampel dibiarkan mengalir kebawah sampai batas tanda yang terdapat
pada alat.
• Dicatat waktu yang diperlukan dengan menggunakan stopwatch.
b. Penentuan masa jenis zat (d2)
• Diambil 10 ml sampel kemudian diukur beratnya.
• Masa jenis adalah hasil pembagian antara berat zat dengan volume zat.
c. Penghitungan viskositas
Viskositas dihitung dengan menggunakan rumus:
naq/n2 = d1 t1/d2 t2
Dimana :
naq = viskositas aquadest (1.0050 Poise)
n2 = Viskositas zat yang dianalisa
d1 = Masa jenis Aquadest (0.9982)
d2 = Masa jenis zat yang dianalisa
t1 = Waktu alir aquadest pada viskosimeter oswald (120 detik)
t2 = Waktu alir zat yang dianalisa pada viskosimeter Oswald
Uji Organoleptik Warna (Sukarto, 1982 dimodifikasi).
Penentuan warna emulsi ini dapat dilakukan dengan menggunakan nilai
Tabel 5. Nilai Uji Organoleptik Warna
Skor Warna
1 Jernih
2 Putih pucat
3 Putih kekuningan
4 putih seperti susu
Uji Total Mikroba (koloni/ml) (Tim Mikrobiologi, 2011 dimodifikasi)
• Diambil sampel 1 ml dan ditambahkan aquadest sampai 10 ml
(pengenceran 10 kali)
• Diambil sampel dari pengenceran 10 kali sebanyak 1 ml kemudian
ditambahkan aquadest sampai 10 ml (pengenceran 100 kali)
• Diambil sampel dari pengenceran 100 kali sebanyak 1ml kemudian
ditambahkan aquadest sampai 10 ml (Pengenceran 1000 kali)
• Dimasukkan satu tetes suspense 1000 kali pengenceran kedalam cawan
petridish yang telah diisi media agar.
• Dibalik cawan petridish dan diinkubasi selama 24 jam.
• Dihitung jumlah koloni dengan koloni counter.
• Dihitung jumlah mikroorganisme dengan rumus.
Jumlah mikroba (Koloni/ml) = Banyak pengenceran X banyaknya koloni
pH (Derajat Keasaman)
Setelah pH meter dikalibrasi maka pH meter tersebut sudah siap digunakan.
Biasanya kalibrasi disarankan dilakukan setiap 1 kali sehari sebelum digunakan.
Cara pengukurannya adalah sebagai berikut:
• Buka penutup plastik elektroda, bilas dengan aquadest dan keringkan
dengan menggunakan kertas tisu.
• Nyalakan pH meter dan masukkan elektroda kedalam sampel.
• Tekan tombol MEAS untuk memulai pengukuran, pada layar akan muncul
tulisan HOLD yang kelap-kelip, biarkan sampai kelap-kelip berhenti.
• Nilai pH yang ditunjukan pada layar adalah nilai pH sampel yang di check.
Skema Penelitian
Skema proses pembuatan Kitosan ditampilkan pada Gambar 3, skema
pembuatan larutan kitosan 2 % ditampilkan pada Gambar 4, skema proses
pembuatan lilin lebah ditampilkan pada Gambar 5, skema pembuatan emulsi
lilin lebah 30 % ditampilkan pada Gambar 6 dan skema penelitian pembuatan
pelapis campuran larutan kitosan dengan emulsi lilin lebah ditampilkan pada
Gambar 3. Proses Pembuatan Kitosan
Dibersihkan,Dicuci dan dikeringkan
Deproteinisasi dengan NaOH 5 %, pada suhu 60 - 700 C selama satu jam dengan perbandingan 1 : 6
Disaring dan dicuci dengan air
Disaring, Dicuci sampai pH netral dan dikeringkan pada suhu 50 - 550 C, 24 jam
Kitin Digiling
Demineralisasi dengan HCl 5 %, pada suhu 60 - 700 C selama satu jam dengan perbandingan 1 : 6
Deasetilasi dengan NaOH 60 % dengan perbandingan 1 : 10 pada suhu 1000 C selama 60 menit
Disaring, Dicuci Sampai pH netral
Dikeringkan pada suhu 50- 550 C, selama 24 jam
Gambar 4. Proses Pembuatan Larutan Kitosan 2 %
Ditimbang Kitosan 20 gram
Ditambahkan Asam Asetat 2 % sampai 1000 ml
Diaduk dan disaring
Gambar 5. Skema Pembuatan Lilin Lebah
Direbus dengan air hingga semua sel sarang mencair (T = 850 C)
Disaring
Lilin dikeluarkan dari dalam air, dan dikeringkan dibawawah sinar matahari
Diperoleh lilin pada bagian permukaan
Lilin Lebah Sarang Lebah
Lilin direbus kembali hingga mencair (T = 850 C)
Gambar 6. Skema Pembuatan Emulsi Lilin Lebah 30 %
Lilin ditimbang 30 gram
Dipanaskan (T= 850 C)
Ditambahkan 5 ml Asam Oleat (Sedikit demi sedikit, sambil diaduk)
Dtambahkan Aquadest (T = 850 C) 10 ml setiap 1 menit sampai 100 ml
Emulsi Lilin Lebah 30 %
Dimasukkan aquadest panas 10 ml dan diaduk 1 menit (T= 850 C)
Ditambahkan campuran 10 aquadest panas dan 5 ml trietanolamin (Sambil diaduk, T = 850 C)
Gambar 7. Skema Penelitian Pembuatan Pelapis Campuran Larutan Kitosan dengan Emulsi Lilin Lebah
Larutan Kitosan
(K1 = 0%, K2= 15 %, K3 = 30 % dan K4= 45 %)
Ditambahkan Emulsi Lilin Sedikit demi sedikit (T = 550C, sambil diaduk)
(K1 = 0%, K2= 15 %, K3 = 30 % dan K4= 45 %)
Pelapis Campuran Emulsi Lilin dengan Kitosan
- Ukuran Partikel (µm)
- Stabilitas Relatif Emulsi (%) - Viskositas
(Poise)
- Uji Organoleptik Warna
(Numerik) - Uji Total
Mikroba (Koloni/ml) - pH
Ditambahkan Aquadest sampai 100 ml
HASIL DAN PEMBAHASAN
Hasil penelitian menunjukkan bahwa konsentrasi larutan kitosan dan
konsentrasi emulsi lilin lebah pada zat pelapis memberi pengaruh terhadap
parameter yang diamati. Pengaruh konsentrasi larutan kitosan dan konsentrasi
emulsi lilin lebah pada zat pelapis tersebut dapat dilihat sebagai berikut.
Pengaruh Konsentrasi Larutan Kitosan pada Zat Pelapis terhadap Parameter yang diamati
Hasil penelitian menunjukkan bahwa konsentrasi larutan kitosan pada zat
pelapis memberikan pengaruh terhadap ukuran partikel, stabilitas relatif emulsi,
viskositas, uji organoleptik warna, uji total mikroba dan pH dapat dilihat pada
Tabel 6. berikut ini.
Tabel 6. Pengaruh Konsentrasi Larutan Kitosan pada Zat Pelapis terhadap Parameter yang diamati
Keterangan: Data terdiri dari dua ulangan ± Standar deviasi
Tabel 6. menunjukkan bahwa konsentrasi larutan kitosan pada zat pelapis
memberi pengaruh terhadap parameter yang diuji. Ukuran partikel tertinggi
terdapat pada perlakuan K2 yaitu sebesar 2,76 µm dan terkecil pada perlakuan K3
K4 yaitu sebesar 81.25 % dan terendah terdapat pada perlakuan K1 dan K2 yaitu
sebesar 62.50 %. Viskositas tertinggi terdapat pada perlakuan K4 yaitu sebesar
2.030 Centi Poise dan terendah pada perlakuan K1 yaitu sebesar 1.485 Centi
Poise. Uji organoleptik warna tertinggi terdapat pada perlakuan K2 dan K4 yaitu
sebesar 2.83 dan terendah terdapat pada perlakuan K1 yaitu sebesar 2.44. Uji total
mikroba tertinggi terdapat pada perlakuan K1 yaitu 52.1 x 103 koloni/ml dan
terendah terdapat pada perlakuan K4 yaitu sebesar 21.8 x 103 koloni/ml. pH
tertinggi terdapat pada perlakuan K4 dan K1 yaitu sebesar 8.32 dan pH terkecil
pada perlakuan K2 yaitu sebesar 8.26.
Pengaruh Konsentrasi Emulsi Lilin Lebah pada Zat Pelapis terhadap Parameter yang diamati
Hasil penelitian menunjukkan bahwa Konsentrasi emulsi lilin lebah pada
zat pelapis memberikan pengaruh terhadap ukuran partikel, stabilitas relatif
emulsi, viskositas, uji organoleptik warna, uji Total mikroba dan pH dapat dilihat
pada Tabel 7. Berikut ini.
Tabel 7. Pengaruh Konsentrasi Emulsi Lilin Lebah pada Zat Pelapis terhadap Parameter yang diamati
Konsentrasi
Tabel 7. menunjukkan bahwa Konsentrasi emulsi lilin lebah pada zat
pelapis memberi pengaruh terhadap parameter yang diuji. Ukuran partikel
tertinggi terdapat pada perlakuan L2 yaitu sebesar 3.74 µm dan terendah terdapat
pada perlakuan L1 yaitu sebesar 0.43 µ m. Stabilitas relatif emulsi tertinggi terdapat
pada perlakuan L1 yaitu sebesar 100 % dan terendah terdapat pada perlakuan L2
yaitu sebesar 56.25. Viskositas tertinggi terdapat pada perlakuan L4 yaitu sebesar
2.026 Centi Poise dan terendah terdapat pada perlakuan L1 yaitu sebesar 1.437
Centi Poise. Uji organoleptik warna tertinggi terdapat pada perlakuan L4 yaitu
3.43 dan terendah terdapat pada perlakuan L1 yaitu sebesar 1.04. Uji total mikroba
tertinggi pada perlakuan L1 yaitu 35.8 x 103 Koloni/ml dan yang terendah pada
perlakuan L2 yaitu 35.5 x 103 koloni/ml. pH yang tertinggi terdapat pada L4 yaitu
8.75 dan terendah terdapat pada perlakuan L1 yaitu 7.19. Hasil analisis statistik
untuk masing-masing parameter yang diamati dapat dijelaskan sebagai berikut.
Ukuran Partikel
Pengaruh Konsentrasi Larutan Kitosan pada Zat Pelapis terhadap Ukuran Partikel
Daftar analisis sidik ragam (Lampiran 1) menunjukkan bahwa konsentrasi
larutan kitosan pada zat pelapis memberikan pengaruh berbeda tidak nyata
(p>0.05) terhadap ukuran partikel. Sehingga pengujian dengan Least Significant
Range (LSR) tidak dilanjutkan.
Pengaruh Konsentrasi Emulsi Lilin Lebah pada Zat Pelapis terhadap Ukuran Partikel
Daftar analisis sidik ragam (Lampiran 1) menunjukkan bahwa konsentrasi
emulsi lilin lebah pada zat pelapis memberikan pengaruh berbeda sangat nyata
Hasil pengujian dengan Least Significant Range LSR menunjukkan
pengaruh Konsentrasi emulsi lilin lebah pada zat pelapis terhadap ukuran partikel
dapat dilihat pada Tabel 8.
Tabel 8. Uji LSR Efek Utama Pengaruh Konsentrasi Emulsi Lilin Lebah pada Zat Pelapis terhadap Ukuran Partikel
Jarak
LSR Konsentrasi Emulsi Lilin
(%)
Rataan (µm)
Notasi
0.05 0.01 0.05 0.01
- - - L1 = 0 0.43 ±0.301 d D 2 0.220 0.302 L2 = 15 3.74 ±0.012 a A 3 0.231 0.318 L3 = 30 3.31 ±0.163 b B
4 0.236 0.326 L4 = 45 3.04 ±0.046 c C
Keterangan: Notasi huruf yang berbeda antar baris menunjukkan pengaruh yang berbeda nyata pada taraf 5% dan berbeda sangat nyata pada taraf 1%.
Data terdiri dari dua ulangan ± Standar deviasi
Tabel 8 menunjukkan bahwa perlakuan L1 memberi pengaruh berbeda
sangat nyata terhadap L2, L3 dan L4. Perlakuan L2 berbeda sangat nyata terhadap
L3 dan L4. Perlakuan L3 berbeda sangat nyata terhadap L4.
Hubungan antara Konsentrasi emulsi lilin lebah pada zat pelapis terhadap
ukuran partikel dapat dilihat pada Gambar 8.
Gambar 8. menunjukkan bahwa ukuran partikel yang paling rendah
terdapat pada perlakuan L1 yaitu 0,43 µ m. Hal ini disebabkan karena pada
perlakuan ini tidak terdapat penambahan emulsi lilin (hannya larutan kitosan)
dimana ukuran partikel larutan lebih kecil daripada emulsi. Ukuran partikel
selanjutnya meningkat sampai pada perlakuan L2, yang merupakan ukuran
partikel tertinggi yaitu 3.74 µm disebabkan karena perubahan dari bentuk larutan
menjadi campuran larutan dengan emulsi lilin dimana jumlah emulsi lilin yang
ditambahakan merupakan jumlah terendah (berarti Jumlah Emulsifier pada pelapis
juga merupakan jumlah terendah) dan selanjutnya ukuran partikel semakin
menurun sampai titik tertentu disebabkan jumlah emulsi lilin yang ditambahkan
semakin meningkat (berarti jumlah emulsifier pada pelapis juga meningkat).
Suryani, dkk. (2002) menyatakan Emulsifier dapat membentuk lapisan tipis yang
akan menyelimuti partikel dan akan mencegah partikel tersebut bersatu dengan
partikel sejenisnya.
Laju pemisahan antara minyak dan air semakin meningkat dengan
bertambahnya ukuran partikel. Sehingga untuk meningkatkan kestabilan emulsi
ukuran partikel harus sekecil mungkin. Budianto dan Ariyanti (2008) menyatakan
bahwa ukuran dan distribusi partikel sangat menentukan sifat polimer emulsi,
seperti sifat aliran dan kestabilan emulsi.
Pengaruh Interaksi Antara Konsentrasi Larutan Kitosan dan Konsentrasi Emulsi Lilin Lebah pada Zat Pelapis terhadap Ukuran Partikel
Daftar analisis sidik ragam (Lampiran 1) menunjukkan bahwa interaksi
antara Konsentrasi larutan kitosan dalam pelapis dan Konsentrasi emulsi lilin
ukuran partikel (µ m). Sehingga pengujian dengan Least Significant Range (LSR)
tidak dilanjutkan.
Stabilitas Relatif Emulsi
Pengaruh Konsentrasi Larutan Kitosan pada Zat Pelapis terhadap Stabilitas Relatif Emulsi
Daftar analisis sidik ragam (Lampiran 2) menunjukkan bahwa Konsentrasi
larutan kitosan dalam pelapis memberikan pengaruh berbeda nyata (p<0.05)
terhadap stabilitas relatif emulsi.
Uji Least Significant Range (LSR) menunjukkan adanya perbedaan
pengaruh Konsentrasi larutan kitosan pada zat pelapis terhadap stabilitas relatif
emulsi dapat dilihat pada Tabel 9.
Tabel 9. Uji LSR Efek Utama Pengaruh Konsentrasi Larutan Kitosan pada Zat Pelapis terhadap Stabilitas Relatif Emulsi
Jarak LSR
Keterangan: Notasi huruf yang berbeda antar baris menunjukkan pengaruh yang berbeda nyata pada taraf 5% dan berbeda sangat nyata pada taraf 1%.
Data terdiri dari dua ulangan ± Standar deviasi
Tabel 9. menunjukkan bahwa perlakuan K1 memberi pengaruh berbeda
tidak nyata terhadap perlakuan K2, berbeda nyata terhadap perlakuan K3 dan K4.
Perlakuan K2 memberi pengaruh berbeda nyata terhadap K3, dan K4. Perlakuan K3
berbeda nyata terhadap perlakuanK4.
Hubungan Konsentrasi larutan kitosan pada zat pelapis dengan stabilitas
Gambar 9. Hubungan Konsentrasi Larutan Kitosan pada Zat Pelapis terhadap Stabilitas Relatif Emulsi
Gambar 9. menunjukkan bahwa semakin tinggi konsentrasi larutan kitosan
yang ditambahkan maka semakin tinggi stabilitas relatif emulsi yang dihasilkan.
Peningkatan stabilitas relatif emulsi mengikuti garis regresi linier seperti terlihat
pada gambar 9. Konsentrasi tertinggi diperoleh pada perlakuan K4 yaitu 81.25 %
dan terendah pada K1 dan K2 yaitu 62.50 %. Hal ini sesuai dengan pernyataan
Calero, et al (2010) menyatakan bahwa kitosan merupakan salah satu
polisakarida yang dapat digunakan sebagai stabilitas emulsi. Kitosan memberikan
kontribusi nilai-tambah yang bermanfaat bagi emulsi akhir dan memiliki sifat
aktivitas permukaan yang dapat meningkatkan baik pembentukan dan stabilitas
emulsi yang dihasilkan.
Pengaruh Konsentrasi Emulsi Lilin Lebah pada Zat Pelapis terhadap Stabilitas Relatif Emulsi
Daftar analisis sidik ragam (Lampiran 2) menunjukkan bahwa Konsentrasi
emulsi lilin lebah dalam pelapis memberikan pengaruh berbeda sangat nyata
Uji Least Significant Range (LSR) menunjukkan ada perbedaan pengaruh
Konsentrasi emulsi lilin lebah dalam zat pelapis terhadap stabilitas relatif emulsi
dapat dilihat pada Tabel 10.
Tabel 10. Uji LSR Efek Utama Pengaruh Konsentrasi Emulsi Lilin Lebah pada Zat Pelapis terhadap Stabilitas Relatif Emulsi
Jarak LSR
Konsentrasi
Emulsi Rataan
(%)
Notasi
0.05 0.01 Lilin lebah (%) 0.05 0.01
- - - L1 = 0 100.00 ±0.000 a A
2 14.063 19.359 L2 = 15 56.25±0.000 b B 3 14.766 20.344 L3 = 30 59.38±85.84 b B
4 15.141 20.859 L4 = 45 62.50±89.13 b B
Keterangan: Notasi huruf yang berbeda antar baris menunjukkan pengaruh yang berbeda nyata pada taraf 5% dan berbeda sangat nyata pada taraf 1%.
Data terdiri dari dua ulangan ± Standar deviasi
Tabel 10. menunjukkan bahwa perlakuan L1 memberi pengaruh berbeda
sangat nyata terhadap perlakuan L2, L3 dan L4. Perlakuan L2 tidak berbeda nyata
terhadap perlakuan L3 dan L4. Perlakuan L3 tidak berbeda nyata terhadap
perlakuanL4.
Hubungan konsentrasi emulsi lilin lebah pada zat pelapis terhadap
stabilitas relatif emulsi dapat dilihat pada Gambar 10.
Gambar 10. menunjukkan bahwa stabilitas relatif emulsi tertinggi
diperoleh pada L1 yaitu 100 % dan terendah pada L2 yaitu 56.25 %. Perlakuan L1
menghasilkan nilai stabilitas relatif yang paling tinggi yaitu 100 % disebabkan
karena pada perlakuan ini tidak terdapat penambahan emulsi lilin (hannya larutan
kitosan). Selanjutnya terjadi penurunan karena adanya perubahan dari larutan
menjadi campuran larutan dengan emulsi lilin, pada perlakuan L2 merupakan nilai
stabilitas relatif yang paling rendah yaitu 56.25 % hal ini disebabkan karena
adanya penambahan emulsi lilin dengan konsentrasi terendah (berarti jumlah
emulsifier yang terdapat pada pelapis campuran juga merupakan jumlah terendah)
dan selanjutnya stabilitas relatif emulsi semakin meningkat dengan penambahan
konsentrasi emulsi lilin yang semakin banyak sampai titik tertentu (dimana jumlah
emulsifier dalam pelapis merupakan jumlah tertinggi). Suryani, dkk. (2002)
menyatakan emulsifier memiliki kemampuan untuk menurunkan tegangan antar
muka dan tegangan permukaan. Dengan turunnya tegangan antar muka ini akan
mengurangi daya kohesi dan sebaliknya meningkatkan daya adesi.
Pengaruh Interaksi Antara Konsentrasi Larutan Kitosan dan Konsentrasi Emulsi Lilin Lebah pada Zat Pelapis terhadap Stabilitas Relatif Emulsi
Daftar analisis sidik ragam (Lampiran 2) menunjukkan bahwa interaksi
antara Konsentrasi larutan kitosan pada zat pelapis dan Konsentrasi emulsi lilin
lebah pada zat pelapis memberi pengaruh berbeda tidak nyata (p>0.05) terhadap
stabilitas relatif emulsi. Sehingga pengujian dengan Least Significant Range