PEMBUATAN DAN UJI AKTIVITAS ANTIBAKTERI
KRIM MINYAK KELAPA MURNI (VCO/virgin coconut oil) TERHADAP Staphylococcus aureus ATCC 29737 dan Pseudomonas aeruginosa ATCC 25619
SKRIPSI
DELLA PRIANA Br.GINTING NIM : 030814003
FAKULTAS FARMASI
UNIVERSITAS SUMATERA UTARA MEDAN
PEMBUATAN DAN UJI AKTIVITAS ANTIBAKTERI KRIM MINYAK KELAPA MURNI (VCO/virgin coconut oil) TERHADAP Staphylococcus aureus
ATCC 29737 dan Pseudomonas aeruginosa ATCC 25619
SKRIPSI
Diajukan untuk melengkapi salah satu syarat untuk mencapai gelar Sarjana Farmasi pada Fakultas Farmasi
Universitas Sumatera Utara
Oleh:
DELLA PRIANA Br. GINTING NIM 030814003
FAKULTAS FARMASI
UNIVERSITAS SUMATERA UTARA MEDAN
LEMBAR PENGESAHAN SKRIPSI
PEMBUATAN DAN UJI AKTIVITAS ANTIBAKTERI KRIM MINYAK KELAPA MURNI (VCO/virgin coconut oil) TERHADAP Staphylococcus aureus
ATCC 29737 dan Pseudomonas aeruginosa ATCC 25619
Oleh:
DELLA PRIANA Br. GINTING NIM 030814003
Dipertahankan di hadapan Panitia Penguji Skripsi Fakultas Farmasi Universitas Sumatera Utara
Pada Tanggal : Desember 2008
Disetujui Oleh:
Pembimbing I, Panitia Penguji
(Dra. Nazliniwaty, M.Si., Apt.) (Dra. Masfria, MS., Apt.) NIP 131 831 534 NIP 131 569 406
Pembimbing II, (Dra. Nazliniwaty, M.Si., Apt.) NIP 131 831 534
(Dra. Erly Sitompul, M.Si., Apt.) (Dra. Saodah, M.Sc., Apt.) NIP 131 126 695 NIP 130 535 836
(Drs. Immanuel S.Meliala, M.Si., Apt.) NIP 131 383 718
Fakultas Farmasi Universitas Sumatera Utara
Dekan
KATA PENGANTAR
Segala pujian, hormat, dan kemuliaan penulis panjatkan kepada Allah atas segala kasih dan anugerahNya sehingga penulis dapat menyelesaikan penelitian dan penulisan skripsi ini.
Ucapan terima kasih yang tidak terhingga penulis ucapkan kepada almarhum Ayahanda B. Ginting dan Ibunda M. Bangun, serta abang dan kakak saya Natanael
Ginting, Mansur Ginting dan Prestarina Br. Ginting atas kasih sayang, doa serta dukungan dan semangat kepada penulis selama ini.
Penulis juga mengucapkan terima kasih yang sebesar-besarnya kepada Ibu
Dra. Nazliniwaty, M.Si., Apt., dan Ibu Dra. Erly Sitompul, M.Si., Apt selaku dosen pembimbing yang telah banyak memberi petunjuk, serta membimbing penulis mulai
dari penelitian hingga penyusunan skripsi ini.
Penulis juga ingin mengucapkan rasa terima kasih yang sebesar-besarnya kepada : 1. Bapak Dekan Fakultas Farmasi USU yang telah memberikan fasilitas kepada
penulis sehingga dapat menyelesaikan penelitian dan penulisan skripsi ini.
2. Bapak Dra. Azizah Nasution, M.Sc., Apt. selaku dosen wali yang telah
memberikan petunjuk dan bimbingan kepada penulis selama masa pendidikan. 3. Bapak dan Ibu staf penguji yang telah memberikan petunjuk dan bimbingan
kepada penulis sehingga dapat menyelesaikan skripsi ini.
4. Bapak dan Ibu staf Laboratorium Teknologi Formulasi Steril dan Fitokimia yang
5. Bang Ari laboran sebagai Laboratorium Teknologi Formulasi Steril dan Fitokimia
yang telah memberikan bantuan dan masukan kepada penulis selama masa
pendidikan dan penelitian hingga selesai.
6. Kepada rekan-rekan mahasiswa Farmasi yang tidak dapat disebutkan satu persatu
yang selalu memberikan bantuan dan semangat selama ini sehingga penelitian dan
penulisan skripsi ini dapat selesai.
Penulis menyadari sepenuhnya bahwa skripsi ini masih memiliki banyak
kekurangan. Oleh sebab itu dengan segala kerendahan hati penulis mengharapkan kritik dan saran yang bersifat membangun pada skripsi ini. Semoga skripsi ini menjadi sumbangan yang berarti bagi ilmu pengetahuan pada umumnya dan ilmu
farmasi pada khususnya.
Medan, Desember 2008 Penulis
ABSTRAK
Telah dilakukan pembuatan krim tipe emulsi minyak dalam air yang mengandung minyak kelapa murni (VCO/virgin coconut oil) dengan berbagai konsentrasi dan menguji aktivitas antibakteri nya terhadap Staphylococcus aureus dan
Pseudomonas aeruginosa.
Pengujian aktivitas antibakteri dilakukan secara invitro dengan metode difusi
agar mengunakan cincin pencadang.
Hasil pengujian stabilitas fisis sediaan krim minyak kelapa murni (VCO/virgin
coconut oil) yang mengandung nipagin menunjukan bahwa semua formula stabil
selama 12 minggu penyimpanan pada suhu kamar, suhu 4oC, dan suhu 40oC. Hasil pengujian stabilitas fisis sediaan krim tanpa nipagin ternyata kurang stabil, yang
ditunjukkan pada perubahan penampilan setelah 9 minggu penyimpanan pada suhu 40oC.
Hasil pengujian aktivitas antibakteri menunjukkan bahwa krim minyak kelapa
murni tanpa nipagin telah bersifat antibakteri pada konsentrasi 2% dengan diameter hambat sebesar 21,00 mm terhadap Staphylococcus aureus dan 15,93 mm terhadap
ABSTRAC
A making of oil type cream containing virgin coconut oil (VCO) in various concentrations has been done along with test of its antibacterial activity against
Staphylococcus aureus and Pseudomonas aeruginosa.
The test of antibacterial activity was done in vitro with diffusion method so reservoir ring could be used.
The result of physical stability test of virgin coconut oil cream preparations containing nipagine shows that all formulas were stable during 12 weeks of storage in room temperature, 4oC temperature and 40oC temperature. The result of physical
stability test of the cream without nipagine shows a rather un stable result, visible in the change in look after 9 weeks of storage in 40oC temperature.
The result of antibacterial activity test shows that virgin coconut oil cream without nipagine already has antibacterial activity in concentration of 2% with barrier diameter of 21,00mm against Staphylococcus aureus and 15,93mm against
Pseudomonas aeruginosa.
DAFTAR ISI
Halaman
JUDUL... i
LEMBAR PENGESAHAN... iii
KATA PENGANTAR... iv
ABSTRAK... vi
ABSTRACT... vii
DAFTAR ISI... viii
DAFTAR TABEL... xvi
DAFTAR LAMPIRAN... xvii
BAB I. PENDAHULUAN... 1
1.1 Latar Belakang... 1
1.2 Perumusan Masalah... 2
1.3 Hipotesis... 3
1.4 Tujuan Penelitian... 3
1.5 Manfaat... 3
BAB II. TINJAUAN PUSTAKA... 4
2.1 Uraian Kelapa... 4
2.2 Sistematika Tumbuhan... 4
2.3.2 Prinsip Pembuatan Mnyak Kelapa Murni... 6
2.3.3 Kerusakan Minyak... 7
2.4 Krim... 7
2.4.1 Stabilitas Krim... 8
2.4.2 Pembuatan Krim... 10
2.5 Absorbsi Obat Melalui Kulit... 11
2.5.1 Penyakit Dan Kelainan Pada Kulit... 11
2.6 Bakteri... 12
2.6.1 Fase Pertumbuhan Bakteri... 12
2.6.2 Faktor-faktor yang Mempengaruhi Pertumbuhan Mikroorganisme... 13
2.6.3 Obat Antimikroba... 15
2.7 Uji Kepekaan Terhadap Antibakteri Secara In Vitro... 16
2.8 Bakteri Staphylococcus aureus... 16
2.9 Bakteri Pseudomonas aeruginosa... 17
BAB III. METODOLOGI PENELITIAN... 19
3.1 Alat-alat yang digunakan... 20
3.2 Bahan-bahan yang digunakan... 20
3.3 Pengambilan Sampel... 20
3.4 Sterilisasi Alat... 20
3.5 Pembuatan Dasar Krim... 21
3.6 Pemeriksaan Sediaan Krim Minyak Kelapa Murni... 24
3.6.2 Pemeriksaan Homogenitas... 25
3.6.3 Pemeriksaan pH... 25
3.6.4 Pemeriksaan Tipe Emulsi... 25
3.6.5 Pemeriksaan Stabilitas Fisik Sediaan Krim... 25
3.7 Pembuatan Media... 26
3.7.1 Nutrien Agar... 26
3.7.2 Pembuatan Agar Miring... 26
3.8 Pembiakan Bakteri... 27
3.8.1 Pembuatan Stok Kultur... 27
3.8.2 Penyiapan Inokulum... 27
3.9 Pengenceran Minyak Kelapa Murni Berbagai Konsentrasi... 28
3.10 Uji Aktivitas Antibakteri dari Minyak Kelapa Murni (VCO/virgin coconut oil)... 28
3.8.1 Uji Aktivitas Antibakteri dari Minyak Kelapa Murni Terhadap Bakteri Staphylococcus aureus... 28
3.8.2 Uji Aktivitas Antibakteri dari Minyak Kelapa Murni Terhadap Bakteri Pseudomonas aeruginosa... 29
3.11 Uji Aktivitas Antibakteri dari Krim Minyak Kelapa Murni (VCO/virgin coconut oil)... 29
3.8.1 Uji Aktivitas Antibakteri dari Krim Minyak Kelapa Murni Terhadap Bakteri Staphylococcus aureus... 29
3.8.2 Uji Aktivitas Antibakteri dari Krim Minyak Kelapa Murni Terhadap Bakteri Pseudomonas aeruginosa... 30
BAB IV. HASIL DAN PEMBAHASAN... 31
4.1.1 Hasil Pemeriksaan Homogenitas... 31
4.1.2 Hasil Pemeriksaan Organoleptis Sediaan Krim... 31
4.1.3 Hasil Pengukuran pH Krim Minyak Kelapa Murni... 33
4.1.4 Hasil Pemeriksaan Stabilitas Fisis Sediaan Krim... 34
4.2 Hasil Pemeriksaan Aktivitas Antibakteri Minyak Kelapa Murni... 35
BAB V. KESIMPULAN DAN SARAN... 38
5.1 Kesimpulan... 38
5.2 Saran... 38
DAFTAR PUSTAKA... 39
LAMPIRAN... 43
DAFTAR LAMPIRAN
Lampiran Halaman
1. Hasil Pemeriksaan Organoleptis Krim Minyak Kelapa Murni...43
2. Gambar Hasil Pemeriksaan Organoleptis Krim Minyak Kelapa Murni...49
3. Krim VCO dengan penambahan nipagin 0.5% dan tanpa penambahan nipagin...50
4. Gambar Minyak Kelapa Murni Buatan Norman Perangin-angin...51
5. Gambar Hasil Uji Aktivitas Antibakteri Krim Minyak Kelapa Murni...52
DAFTAR TABEL
Halaman Tabel 1. Formula Dasar Krim...22
Tabel 2. Formula Krim dengan Variasi Konsentrasi minyak kelapa murni...22
Tabel 3. Hasil Uji Aktivitas Antibakteri Minyak Kelapa Murni Terhadap
Staphylococcus aureus dan Pseudomonas aeruginosa...35
ABSTRAK
Telah dilakukan pembuatan krim tipe emulsi minyak dalam air yang mengandung minyak kelapa murni (VCO/virgin coconut oil) dengan berbagai konsentrasi dan menguji aktivitas antibakteri nya terhadap Staphylococcus aureus dan
Pseudomonas aeruginosa.
Pengujian aktivitas antibakteri dilakukan secara invitro dengan metode difusi
agar mengunakan cincin pencadang.
Hasil pengujian stabilitas fisis sediaan krim minyak kelapa murni (VCO/virgin
coconut oil) yang mengandung nipagin menunjukan bahwa semua formula stabil
selama 12 minggu penyimpanan pada suhu kamar, suhu 4oC, dan suhu 40oC. Hasil pengujian stabilitas fisis sediaan krim tanpa nipagin ternyata kurang stabil, yang
ditunjukkan pada perubahan penampilan setelah 9 minggu penyimpanan pada suhu 40oC.
Hasil pengujian aktivitas antibakteri menunjukkan bahwa krim minyak kelapa
murni tanpa nipagin telah bersifat antibakteri pada konsentrasi 2% dengan diameter hambat sebesar 21,00 mm terhadap Staphylococcus aureus dan 15,93 mm terhadap
ABSTRAC
A making of oil type cream containing virgin coconut oil (VCO) in various concentrations has been done along with test of its antibacterial activity against
Staphylococcus aureus and Pseudomonas aeruginosa.
The test of antibacterial activity was done in vitro with diffusion method so reservoir ring could be used.
The result of physical stability test of virgin coconut oil cream preparations containing nipagine shows that all formulas were stable during 12 weeks of storage in room temperature, 4oC temperature and 40oC temperature. The result of physical
stability test of the cream without nipagine shows a rather un stable result, visible in the change in look after 9 weeks of storage in 40oC temperature.
The result of antibacterial activity test shows that virgin coconut oil cream without nipagine already has antibacterial activity in concentration of 2% with barrier diameter of 21,00mm against Staphylococcus aureus and 15,93mm against
Pseudomonas aeruginosa.
BAB I
PENDAHULUAN
1.1Latar belakang
Minyak Kelapa Murni (MKM) atau yang sering disebut dengan
VCO/virgin coconut oil adalah minyak yang memiliki kadar air yang rendah
(0,02-0,03%) dan kadar asam lemak bebas yang rendah (0,02%), berwarna
bening, dan berbau harum. Daya simpannya lebih lama dari minyak biasa,
bisa lebih dari 12 bulan (Anonim, 2006)
Minyak kelapa murni (VCO/virgin coconut oil) berkasiat sebagai
antivirus, antibakteri, dan antiprotozoa. Hal tersebut dikarenakan kandungan
asam laurat, asam kaprilat dan asam kaprat didalamnya. Sementara, jenis
minyak lain tidak memiliki sifat antimikroba. Manfaat dari asam laurat
antara lain dapat membunuh berbagai macam jenis mikroba yang membran
sel nya, berasal dari asam lemak (lipid coated microorganism). Sifat asam
laurat dapat melarutkan membran bakteri berupa lipid sehingga akan
mengganggu kekebalan bakteri atau virus. Hal ini akan membuat bakteri
atau virus inaktivasi. Beberapa penyakit yang disebabkan oleh mikroba jenis
ini seperti influenza, Streptococcus sp., Stapilococcus sp., gram positive,
dan gram negative (Sutarmi, 2005).
Berdasarkan hasil analisis Norman Perangin-Angin, 2008, disimpulkan
bahwa minyak kelapa murni olahan pabrik memiliki kemampuan
menurunkan kadar kolesterol dengan tingkat persentase penurunan 31,70%
Menurut Sutarmi, 2005, minyak kelapa murni (VCO/virgin coconut oil)
dapat digunakan untuk mengobati penyakit pada kulit misalnya herpes dan
cacar. Pada dasarnya, dalam mengobati penyakit masyarakat lebih menyukai
pemakaian obat secara praktis misalnya pemakaian topikal, untuk itu
peneliti membuat minyak kelapa murni (VCO/virgin coconut oil) dalam
bentuk sediaan krim tipe minyak dalam air.
Dari sudut pandang terapi bentuk krim tipe minyak dalam air cocok
untuk luka topikal karena mempunyai kemampuan untuk mengabsorbsi
cairan yang keluar dari dalam kulit yang terbuka (Ansel, 1989). Keuntungan
sediaan krim tipe minyak dalam air mudah dicuci, tidak meninggalkan
bekas pada kulit, pakaian, menimbulkan rasa nyaman dan dingin setelah air
menguap pada daerah yang digunakan (Lachman, dkk, 1994).
Berdasarkan hal tersebut, peneliti hendak membuat krim yang
mengandung minyak kelapa murni (VCO/virgin coconut oil) dengan
berbagai konsentrasi dan menguji aktivitas antibakterinya terhadap bakteri
penyebab penyakit pada kulit. Bakteri uji yang digunakan adalah
Staphylococcus aureus ATCC 29737 dan Pseudomonas aeruginosa ATCC
25619.
1.2 Perumusan Masalah
1. Apakah ada perbedaan pada sediaan krim minyak kelapa murni
(VCO/virgin coconut oil) yang mengandung nipagin dan yang tidak
2. Apakah krim minyak kelapa murni (VCO/virgin coconut oil) mempunyai
aktivitas sebagai antibakteri terhadap Staphylococcus aureus dan
Pseudomonas aeruginosa.
1.3 Hipotesis
1. Ada perbedaan yang nyata antara sediaan krim minyak kelapa murni
(VCO/virgin coconut oil) yang mengandung nipagin dan yang tidak
mengandung nipagin terhadap stabilitas krim tersebut.
2. Krim minyak kelapa murni (VCO/virgin coconut oil) mempunyai
aktivitas sebagai antibakteri terhadap Staphylococcus aureus dan
Pseudomonas aeruginosa.
1.4 Tujuan
1. Untuk melihat pengaruh nipagin terhadap stabilitas krim minyak kelapa
murni (VCO/virgin coconut oil)
2. Untuk mengetahui aktivitas antibakteri krim minyak kelapa murni
(VCO/virgin coconut oil) terhadap Staphylococcus aureus dan
Pseudomonas aeruginosa.
1.5 Manfaat
Hasil penelitian ini diharapkan dapat digunakan sebagai krim
BAB II
TINJAUAN PUSTAKA
2.1 Uraian Kelapa
Kelapa termasuk tanaman berkeping satu (monocotyledone), berakar
serabut dan merupakan golongan palem (palmae) (Warisno,2002). Kelapa
terdiri dari batang, sabut, tempurung, daging buah, dan air kelapa. Seluruh
bagian tanaman ini bermanfaat bagi kehidupan sehingga tidak ada yang
terbuang dan dapat dibuat untuk menghasilkan produk industri. Produk
kelapa yang paling berharga adalah minyak kelapa. Minyak kelapa dapat
diperoleh dari daging buah segar (Suhardiyono, 1988).
Buah kelapa terdiri dari bagian-bagian :
- Epicarp, yaitu klit bagian luar yang permukaannya licin, dan agakkeras.
- Mesokarp, yaitu kulit bagian tengah terdiri dari serat-serat keras dengan
ketebalan
3- 5 cm yang dibuat sabut.
- Endocarp, yaitu bagian tempurung yang keras sekali.
- Endosperm, yaitu daging buah yang tebalnya 8-10 mm
2.2 Sistematika Tumbuhan
Divisio : Spermatophyta
Ordo : Palmales
Famili : Palmae
Genus : Cocos
Species : Cocos nucifera (Suhardiman,1999).
2.3 Minyak Kelapa Murni
Minyak kelapa murni atau VCO (virgin coconut oil) merupakan salah
satu olahan dari buah kelapa (Cocos nucifera) (Sutarmi, 2005).
Minyak kelapa trdiri dari 90% asam lemak jenuh dan 10% asam lemak
tidak jenuh. Asam laurat merupakan asam lemak yang paling besar
dibandingkan dengan asam lemak lainnya yaitu sekitar 44-52% (Alamsyah,
2005). Asam laurat ini merupakan asam lemak jenuh dengan rantai sedang
yang lebih dikenal dengan medium chain fatty acids (MCFA) (Rindengan
dan Hengki, 2005).
2.3.1 Manfaat Minyak Kelapa Murni
Minyak kelapa murni atau VCO (virgin coconut oil) mengandung
asam lemak rantai sedang (medium chain fatty acids,MCFA) yang mudah
diurai dalam tubuh. Kandungan asam lemak rantai sedang ini sangat
berperan dalam menjaga kesehatan, misalnya asam laurat. Asam laurat
merupakan suatu monogliceride yang bersifat antibakteri.
Adanya kandungan asam lemak rantai sedang tersebut, maka VCO
1) Membantu mengatasi infeksi bakteri
2) Membunuh jamur yang menyebabkan keputihan
3) Membnatu kulit tetap lembut dan halus
4) Membantu dalam pencegahan sakit jantung, stroke,dan
artherosclerosis
5) Membantu meredakan gejala-gejala dan mengurangi resiko
kesehatan yang dihubungkan dengan diabetes mellitus
6) Membantu mencegah kegemukan ( Bambang, 2006 )
2.3.2 Prinsip Pembuatan Minyak Kelapa Murni
Kandungan kimia minyak yang paling tinggi dalam sebutir kelapa
yaitu air, protein, dan lemak. Ketiga senyawa tersebut tergabung dalam
bentuk emulsi. Emulsi adalah suatu sistem dispersi dimana fase terdispers
terdiri dari bulatan-bulatan kecil zat cair yang terdistribusi ke seluruh
pembawa (fase terdispers) yang tidak saling bercampur (Ansel, 1989).
Sebaliknya yang dimaksud dengan pengemulsi (emulgator) yaiut zat yang
berfungsi untuk mempererat (memperkuat) mencampurnya kedua fase
tersebut. Protein sebagai emulgator akan mengurangi tegangan antar muka
minyak dan air sehingga minyak dan air tidak saling menyatu dan
masing-masing tidak membentuk lapisan sendiri. Emulsi tersebut tidak akan pernah
pecah karena masih ada tegangan muka protein air yang lebih kecil dari
protein minyak. Dngan demikian, air merupakan fase kontinu (terdispers),
sedangkan miyak merupakan fase diskontinu (pendispers). Minyak kelap
murni baru bias keluar dari ikatan emulsi tersebut jika emulgatornya
pemanasan bertahap, enzimatis, tehnik pemancingan, pengasaman dan
sentrifugasi.
2.3.3 Kerusakan Minyak
Bahan makanan berlemak merupakan medium yang baik bagi
pertumbuhan beberapa jenis jamur dan bakteri. Kerusakan lemak di dalam
bahan pangan dapat terjadi selama proses pengolahan dan selama
penyimpanan. Kerusakan lemak ini, menyebabakan bahan pangan berlemak
mempunyai baud an rasa yang tidak enak, sehingga dapat menurunkan mutu
dan nilai gizi bahan pangan ersebut. Tipe penyebab ketengikan dalamlemak
dapat dibagi atas 3 golongan yaitu :
1. ketengikan oleh oksidasi (oxidative rancidity)
2. ketengikan oleh enzim (enzymatic rancidity)
3. ketengikan oleh proses hidrolisa (hidrolitic rancidity)
2.4 Krim
Krim adalah bentuk sediaan setengah padat yang mengandung satu
atau lebih bahan obat terlarut atau terdispersi dalam dasar yang sesuai.
Istilah ini secara tradisional telah digunakan untuk sediaan setengah padat
yang mempunyai konsentrasi relatif cair yang diformulasi sebagai emulsi air
dalam minyak atau minyak dalam air. Sekarang ini batasan tersebut lebih
diarahkan untuk produk yang terdiri dari emulsi minyak dalam air atau
dispersi mikrokristal asam-asam lemak atau alkohol berantai panjang dalam
air, yang dapat dicuci dengan air atau lebih ditujukan untuk penggunaan
Fungsi krim adalah sebagai bahan pembawa substansi obat untuk
pengobatan kulit, sebagai bahan pelumas untuk kulit, dan sebagi pelindung
untuk kulit yaitu mncegah kontak permukaan kulit dengan larutan berair dan
rangsangan kulit ( Anief, 2000).
Syarat-syarat krim yang baik adalah :
- Stabil selama dalam pemakaian pada suhu kamar dan kelembaban
yang ada dalam kamar
- lunak yait semua zat dalam keadaan halus
- seluruh produk homogen
- mudah dipakai
2.4.1 Stabilitas Krim
Pertimbangan yang terpnting bagi sediaan emulsi seperti krim di
bidang farmasi dan kosmetika adalah stabilitas dari produk jadi. Menurut
Anief, 2000, ketidakstabilan emulsi dapat digolongkan menjadi :
a. flokulasi atau creaming
b. Koalesen atau pecahnya emulsi (breaking, cracing)
c. Macam-macam perubahan fisika dan kimia
d. Inverse
Creaming adalah terpisahnya emulsi menjadi dua lapiasan, dimana
lapisan yang satu mengandung butir-butir tetesan (fase terdispers) lebih
bolak-balik, sedangkan pemecahan merupakan proses searah. Krim yang
menggumpal bisa didispersikan kembali dengan mudah, dan dapat terbentuk
kembali suatu campuran yang homogen dari suatu emulsi yang membentuk
krim dengan pengocokan, karena bola-bola minyak masih dikelilingi oleh
suatu lapisan pelindung dari zat pengemulsi. Jika terjadi pemecahan,
pencampuran biasa tidak bisa mensuspensikan kembali bola-bola tersebut
dalam suatu emulsi yang stabil (Martin, 1993).
Inversi adalah peristiwa berubahnya tipe emulsi dari tipe M/A menjadi
A/M atau sebliknya. Inverse dapat dipengaruhi oleh suhu, atau inverse
merupakan fungsi suhu (Anief, 2000).
Faktor-faktor yang dapat memecah emulsi digolongkan dalam:
1. pemecahan emulsi secara kimia, contohnya; penambahan zat yang
dapat menarik air seperti CaCl2 eksikatus dan CaO
2. pecahnya emulsi secara fisika, yaitu;
- Kenaikan suhu, dapat menyebabkan perubahan viskositas,
mengubah sifat emulgator dan menaikkan benturan butir-butir
tetesan.
- Pendingin menyebabkan terpisahnya air dari sistem emulsi
- Penambahan ganul kasar
- Pengenceran emulsi yang berlebihan
- Penyaringan, karena kedua fae melalui pori-pori dan butir-butir
fase intern akan menggumpal menjadi satu
3. Efek elektrolit terhadap stabilitas emulsi, tergantung dari jenis
emulator yang ada. Bila ada reaksi dari elektrolit dengan emulsi
maka emulsi akan pecah (Anief, 2000).
2.4.2 Pembutan Krim
Dalam pembuatan krim dari formula dengan tipe emulsi minyak
dalam air (M/A), metode pembuatan secara umum meliputi proses
peleburan, emulsifikasi dan saponifikasi. Komponen yang tidak berampur
dengan air seperti minyak dan lilin dicairkan di atas penangas air pada
temperature sekitar 70 sampai 75oC. sementara itu, semua larutan berair
yang tahan panas, komponen yang larut dalam air, dibuat dalam sejumlah
air yang dimurnikan, khususnya dalam formula dan dipanaskan pada
temperatur yang sama dengan komponen berlemak. Larutan berair diolah
dalam komponen berlemak yang cair dalam keadaan hangat dengan
pengadukan kontinu sampai campuran membeku/mengental.apabila larutan
berair tidak sama temperaturnya dengan leburan lemak, maka lemak akan
menjadi padat.
2.5Absorbsi Obat Melalui Kulit
Tujuan umum pengunaan obat topikal pada terapi adalah untuk
menghasilkan efek terapetik pada tempat-tempat spesifik di jaringan
epidermis. Daerah yang terkena, umumnya epidermis dan dermis,
sedangkan obat-obat topical tertentu seperti emoliens (pelembab), dan
Faktor-faktor yang mempengaruhi penetrasi kulit sangat
bergantung dari sifat fisika kimia obat dan juga bergantung pada zat
pembawa, pH dan konsentrasi. Perbedaan fisiologis melibatkan kondisi kulit
yaitu apakah kulit dalam keadaan baik atau terluka, umur kulit, perbedaan
spesies dan kelembaban yang dikandung oleh kulit (Lachman, dkk, 1994).
2.5.1 Penyakit dan Kelainan pada Kulit
Penyakit dan kelainan pada kulit diantaranya adalah:
a. Jerawat
Jerawat merupakan penyakit kulit yang sudah dikenal secara luas
dan sering timbul pada wajah, baik wajah para remaja maupun
dewasa. Jerawat terjadi karena adanya peradangan yang disertai
penyumbatan pada saluran kelenjar minyak dalam kulit dan rambut
(Wirakusumah dan Setyowati, 1999).
b. Infeksi pada kulit
Infeksi yang disebabkan oleh bakteri, jamur atau virus ini dapat
berupa bisul, cacar air, kusta atau jamuran. Umumnya infeksi di sela
paha dan telapak kaki (Wirakusumah dan Setyowati, 1999).
c. Penuaan dini pada kulit
Penyebabnya demam yang tinggi dan berkepanjangan atau terkena
sinar matahari yang terlalu lama (Wirakusumah dan
Setyowati,1999).
d. Noda-noda hitam
Kelainan kulit ini disebabkan oleh sinar ultra violet mathari yang
Akibatnya, timbul bercak atau noda hitam pada bagian-bagian kulit
yang sering terkena sinar matahari (Wirakusumah dan
Setyowati,1999).
2.6 Bakteri
Bakteri termasuk kedalam golongan prokariota, ukurannya sangat
kecil dan tidak dapat dilihat secara visual (Tim mikrobiologi FK Unibraw,
2003).
2.6.1 Fase Pertumbuhan Bakteri
Ada empat fase pada pertumbuhan bakteri yaitu :
1. Fase Penyesuaian Diri (Lag Phase)
Kurun waktu ini merupakan penyesuaian bakteri ke suatu
lingkungan baru. Pada fase ini tidak ada kenaikan jumlah sel, melainkan
peningkatan ukuran dan besar sel.
2. Fase Logaritmik (Exponential Phase)
Pada fase ini bakteri berkembang biak, jumlah bakteri meningkat
secara eksponensial. Untuk kebanyakan bakteri, fase ini berlangsung 18-24
jam. Pada pertengahan fase ini pertumbuhan bakteri sangat ideal,
pembelahan terjadi secara teratur, semua bahan dalam sel berada dalam
seimbang (Chatim, 1994).
3. Fase Stasioner (Stationary Phase)
Pada fase ini terjadi penumpukan racun akibat metabolisme sel dan
beberapa sel mati dan yang lainnya tetap tumbuh. Jumlah sel menjadi
konstan.
4. Fase Kematian (Death Phase)
Pada fase ini terjadi akumulasi bahan toksik, zat hara yang
diperlukan oleh bakteri juga berkurang, sehingga bakteri akan memasuki
fase kematian. Fase ini merupakan kebalikan dari fase logaritmik
pertumbuhan. Jumlah sel menurun terus sampai didapatkan jumlah sel yang
konstan untuk beberapa waktu (Roday S., 1999).
2.6.2 Faktor-faktor Yang Mempengaruhi Mikroorganisme
a. Suplai Zat Gizi
Seperti halnya makhluk lain, mikroorganisme juga membutuhkan
suplai makanan yang akan menjadi sumber energi dan menyediakan
unsur-unsur kimia dasar untuk pertumbuhan sel.
b. Waktu
Bila suatu sel mikroorganisme diinokulasi pada nutrient segar,
pertumbuhan yang terlihat mula-mula adalah suatu pembesaran ukuran,
volume dan berat. Ketika ukurannya telah mencapai kira-kira dua kali dari
besar normal, sel tersebut membelah dan menghasilkan empat sel. Selama
kondisi memungkinkan, pertumbuhan dan pembelahan sel berlangsung
terus sampai sejumlah besar populasi sel terbentuk.
Suhu adalah salah satu faktor lingkungan yang terpenting yang
mempengaruhi kehidupan dan pertumbuhan organisme. Suhu dapat
mempengaruhi mikroorganisme dalam dua cara yang berlawanan yaitu :
1. Apabila suhu naik, kecepatan metabolisme naik dan pertumbuhan
dipercepat. Sebaliknya apabila suhu turun, kecepatan metabolisme
juga turun dan pertumbuhan diperlambat.
2. Apabila suhu naik atau turun, tingkat pertumbuhan mungkin
terhenti, komponen sel menjadi tidak aktif dan sel-sel dapat mati.
d. Nilai pH
Setiap organisme mempunyai kisaran nilai pH dimana pertumbuhan
masih memungkinkan dan masing-masing biasanya mempunyai pH
optimum. Kebanyakan mikroorganisme dapat tumbuh pada kisaran pH
6,0-8,0 dan nilai pH diluar kisaran 2,0 sampai 10,0 biasanya bersifat merusak.
Beberapa mikroorganisme dalam bahan pangan tertentu dapat tumbuh
dengan baik pada kisaran nilai pH 3,0-6,0.
e. Aktivitas Air
Semua organisme membutuhkan air untuk kehidupannya. Air
berperan dalam reaksi metabolik dalam sel dan merupakan alat pengangkut
f. Ketersediaan Oksigen (O2)
Tidak seperti bentuk kehidupan lainnya, mikroorganisme berbeda
nyata dalam kebutuhan oksigen guna metabolismenya. Beberapa kelompok
dapat dibedakan atas :
1. Mikroba Aerob, mikroba yang membutuhkan oksigen (O2) didalam
pertumbuhannya.
2. Mikroba Anaerob, mikroba yang tidak membutuhkan oksigen (O2)
didalam pertumbuhannya, bahkan oksigen (O2) ini dapat menjadi
racun bagi mikroba tersebut.
3. Mikroba Anaerob Fakultatif, mikroba yang dapat hidup tumbuh
dengan/tanpa adanya oksigen (O2).
4. Mikroba Mikro-Aerofilik, mikroba yang membutuhkan hanya
sedikit oksigen (O2) dalam pertumbuhannya.
g. Bahan Kimia
Adanya bahan kimia berupa zat pengawet dan bakterisidal dapat
menghambat/mematikan pertumbuhan mikroorganisme, misalnya : fenol,
alkohol, deterjen dan antibiotika (Roday S., 1999).
2.7. Obat Antimikroba
Obat antimikroba dapat berarti terhadap bakteri, jamur dan virus.
Untuk maksud penggunaan secara sistematik diperlukan toksisitas selektif
yang tinggi dari obat antimikroba. Antimikroba dapat digolongkan
berdasarkan kemampuan mematikan (diberi akhiran-sidal) atau hanya
kemampuan mempengaruhi banyaknya jenis bakteri, dikenal antibakteri
berspektrum sempit dan berspektrum luas (Mikrobiologi Tim, 2003).
2.8 Uji Kepekaan Terhadap Antibakteri Secara In Vitro
Aktivitas (potensi) antibakteri dapat ditunjukkan pada kondisi yang
sesuai dengan efek daya hambatnya terhadap bakteri. Ada dua metode
umum yang dapat digunakan yaitu penetapan dengan lempeng silinder atau
”lempeng” dan penetapan dengan cara ”tabung” atau turbidimetri. Metode
pertama berdasarkan difusi antibiotik dari silinder yang dipasang tegak lurus
pada lapisan agar padat dalam cawan petri, sehingga bakteri yang
ditambahkan dihambat pertumbuhannya pada daerah berupa lingkaran atau
”zona” disekeliling silinder yang berisi larutan antibiotik. Metode
turbidimetri berdasarkan atas hambatan pertumbuhan biakan mikroba dalam
larutan serba sama antibiotik dalam media cair yang dapat menumbuhkan
mikroba dengan cepat bila tidak terdapat antibiotik (Ditjen POM, 1995).
2.9 Bakteri Staphylococcus aureus
Sistematika bakteri Staphylococcus aureus menurut Bergey edisi
ke-7 (Dwidjoseputro, 198ke-7) adalah sebagai berikut :
Domain : Bacteria
Phylum : Protophyta
Class : Bacilla
Familia : Staphylococcaceae
Genus : Staphylococcus
Species : Staphylococcus aureus
Staphylococcus aureus merupakan bakteri gram negatif dan mikroba
flora normal yang terdapat pada permukaan tubuh, seperti pada permukaan
kulit, rambut, hidung, mulut dan tenggorokan (Jawetz et all, 2001).
2.10 Bakteri Pseudomonas aeruginosa
Sistematika bakteri Pseudomonas aeruginosa menurut Bergey edisi
ke-7 (Dwidjoseputro, 1987) adalah sebagai berikut :
Domain : Bacteria
Phylum : Protophyta
Class : Schizomycetes
Ordo : Pseudomonadales
Familia : Pseudomonadaceae
Genus : Pseudomonas
Species : Pseudomonas aeruginosa
Kelompok Pseudomonas adalah batang gram negatif dan terlihat
sebagai bakteri tunggal, berpasangan dan kadang-kadang membentuk rantai
yang pendek ; berukuran sekitar 0,6 x 2 μm, bergerak, aerob, ditemukan
°C. Pseudomonas aeruginosa tersebar luas dialam dan biasanya terdapat di
lingkungan yang lembab. Bakteri ini dapat tinggal pada mamalia yang
normal dan menyebabkan penyakit bila pertahanan tubuh inang abnormal
BAB III
METODOLOGI PENELITIAN
Penelitian ini dilakukan di Laboratorium Teknologi Formulasi Steril.
Metode dalam penelitian ini adalah metode penelitian eksperimental
parametrik, meliputi penyiapan bahan, pembuatan krim minyak kelapa
murni (VCO/virgin coconut oil) dengan teknik aseptis, pegujian stabilitas
terhadap krim minyak kelapa murni (VCO/virgin coconut oil) yang
mengandung nipagin dan yang tidak mengandung nipagin, serta uji aktivitas
antibakteri terhadap bakteri Staphylococcus aureus dan Pseudomonas
aeruginosa.
Parameter yang dilihat untuk stabilitas krim minyak kelapa murni
(VCO/virgin coconut oil) meliputi sifat fisik secara organoleptis,
homogenitas, pH, dan tipe emulsi dan parameter untuk aktivitas antibakteri
nya yang diukur adalah zona hambatan pertumbuhan bakteri oleh krim
minyak kelapa murni (VCO/virgin coconut oil) terhadap bakteri
Staphylococcus aureus untuk bakteri gram positif dan Pseudomonas
aeruginosa untuk bakteri gram negatif. Metode yang digunakan adalah
metode difusi agar.
Pada uji aktivitas antibakteri krim minyak kelapa murni (VCO/virgin
coconut oil) yang digunakan adalah dasar krim yang tidak mengandung
3.1 Alat-Alat yang Digunakan
Alat-alat yang digunakan adalah: tabung reaksi (Pyrex), gelas ukur
(Pyrex), gelas ukur (Pyrex), labu tentukur (Pyrex), oven (Memmert),
(Gallenkamp), autoklaf (Fison), inkubator (Fisher Scientific), lemari
pendingin (Uchida), laminar airflow cabinet (Astec HLF 1200 L), neraca
kasar (Ohanus), neraca analitik (Mettler AE 200), jarum ose, lampu bunsen,
mikro pipet, pipet tetes, bola karet, pH meter, alumunium foil, kertas
perkamen, tissu, pencadang logam, cawan petri, kapas steril, jangka sorong,
lumpang, stamfer, spatula.
3.2 Bahan-Bahan yang Digunakan
Bahan-bahan kimia yang digunakan adalah: Etanol proanalis
(Merck), NaCl pro analis (Merck), akuades, bakteri Staphylococcus aureus
(ATCC 29737), bakteri Pseudomonas aeruginosa (ATCC 25619), nutrien
agar (difco), asam stearat (Brataco Chemica), gliserin (Brataco Chemica),
trietanolamin (Brataco Chemica), nipagin (Brataco Chemica), natrium
biborat (Brataco Chemica).
3.3 Pengambilan Sampel
Sampel yang digunakan adalah minyak kelapa murni hasil
pembuatan Norman Perangin-Angin (Norman, 2008).
3.4 Sterilisasi Alat
Bahan-bahan yang tidak rusak bila dipanaskan dengan suhu yang
autoklaf pada suhu 121 °C selama 15 menit dan bahan-bahan dan alat-alat
gelas disterilkan di oven suhu 150-170 °C selama 2 jam (Lay dan Hastowo
S., 1992).
3.5 Pembuatan Dasar Krim
Sediaan krim yang digunakan adalah krim tipe minyak dalam air
berdasarkan formula standart Formularium Indonesia (Ditjen POM, 1984)
dengan dasar vanishing cream yaitu:
R/ Asam stearat 142
Gliserin 100
Natrium bibobarat 2,5
Trietenolamin 10
Air suling 750
Nipagin q.s.
m.f. cream
Sediaan krim yang mengandung minyak kelapa murni (VCO/virgin
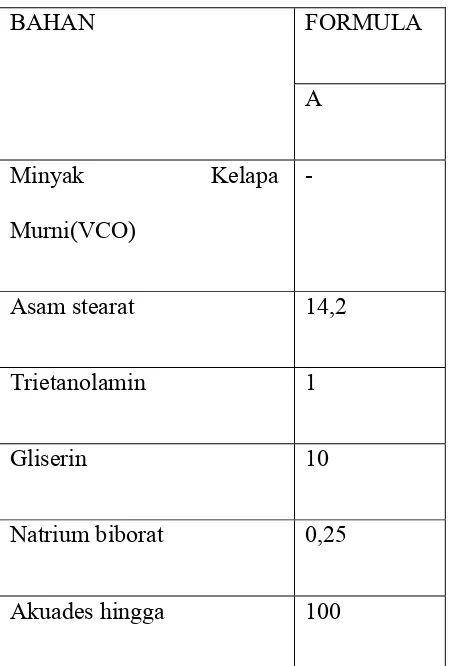
Tabel 1. Formula Dasar Krim
BAHAN FORMULA
A
Minyak Kelapa
Murni(VCO)
-
Asam stearat 14,2
Trietanolamin 1
Gliserin 10
Natrium biborat 0,25
Akuades hingga 100
Tabel 2. Formula Krim dengan Variasi Konsentrasi Minyak Kelapa Murni
Formula B C D E F
Minyak Kelapa Murni(VCO) 2 4 6 8 10
Dasar krim 98 96 94 92 90
Keterangan : Semua bahan dalam satuan % b/b
[image:37.595.110.466.531.645.2]Formula B : Krim minyak kelapa murni (VCO/virgin coconut oil) dengan
kadar minyak kelapa murni (VCO/virgin coconut oil) 2%
Formula C : Krim minyak kelapa murni (VCO/virgin coconut oil) dengan
kadar minyak kelapa murni (VCO/virgin coconut oil) 4%
Formula D : Krim minyak kelapa murni (VCO/virgin coconut oil) dengan
kadar minyak kelapa murni (VCO/virgin coconut oil) 6%
Formula E : Krim minyak kelapa murni (VCO/virgin coconut oil) dengan
kadar minyak kelapa murni (VCO/virgin coconut oil) 8%
Formula F : Krim minyak kelapa murni (VCO/virgin coconut oil) dengan
kadar minyak kelapa murni (VCO/virgin coconut oil) 10%
Cara pembuatan:
Pembuatan krim dilakukan dalam ruang steril yang terdapat kap laminar air
flow dengan teknik aseptik. Langkah – langkah pembuatan krim sebagai
berikut :
a. Pembuatan Krim Minyak Kelapa Murni Tanpa Nipagin
Ditimbang semua bahan yang diperlukan
Asam stearat dalam cawan penguap disterilkan dalam oven suhu
150oC selama 1 jam
Trietanolamin, gliserin, dan natrium biborat masing-masing
dilarutkan dalam air panas kemudian disterilkan dalam autoklaf pada
Asam sterat steril dimasukkan ke dalam lumpang yang telah
disterilkan terlebih dahulu kemudian larutan panas trietanolamin,
gliserin dan natrium biborat ditambahkan sedikit demi sedikit ke
dalamnya dengan pengadukan yang konstan sampai diperoleh massa
krim
Dalam lumpang yang terpisah yang telah disterilkan terlebih dahulu
dasar krim sebanyak yang diperlukan digerus bersama minyak
kelapa murni (VCO/virgin coconut oil) dengan berbagai konsentrasi
dan dimasukkan dengan sudip film dalam wadah tertutup rapat, krim
disimpan di tempat yang terlindung cahaya.
b. Pembuatan Krim Minyak Kelapa Murni Dengan Penambahan
Nipagin
Dalam lumpang yang telah disterilkan terlebih dahulu digerus halus
nipagin kemudian ditambahkan dasar krim sedikit demi sedikit dan
digerus homogen,
3.6. Pemeriksaan Sediaan Krim Minyak Kelapa Murni
3.6.1 Pemeriksaan Organoleptis
Pemeriksaan organoleptis meliputi pemeriksaan warna, bau, dan
penampilan (konsistensi) dari sediaan.
Sediaan dinyatakan stabil apabila warna, bau, dan penampilan tidak berubah
secara visual selama penyimpanan, dan juga secara visual tidak ditumbuhi
3.6.2 Pemeriksaan Homogenitas
Pemeriksaan homogenitas sediaan krim minyak kelapa murni
(VCO/virgin coconut oil) dilakukan dengan cara: Sejumlah tertentu sediaan
diletakkan di atas kaca, kemudian ditutup dengan kaca yang lain lalu
diratakan. Sediaan yang memenuhi persyaratan homogenitas harus
menunjukkan susunan yang homogen dan tidak terlihat adanya butir-butir
yang kasar (Ditjen POM, 1979).
3.6.3 Pengukuran pH
Pemeriksaan pH sediaan dilakukan satu hari setelah pembuatan
sediaan dan setelah penyimpanan pada waktu tertentu. Caranya adalah satu
gram sediaan diencerkan dengan akuades sampai 10 ml di dalam satu
wadah, kemudian pH sediaan diukur dengan menggunakan indikator
universal (Rawlins, 2002).
3.6.4 Pemeriksaan Tipe Emulsi
Pemeriksaan Tipe emulsi dilakukan dengan metode pengenceran,
yaitu sejumlah tertentu sediaan diencerkan dengan akuades. Jika emulsi
tersebut bercampur sempurna dengan air, maka emulsi tersebut bertipe
minyak dalam air, dan bila tidak bercampur sempurna dengan air, maka
emulsi tersebut bertipe air dalam minyak (Martin, 1993).
3.6.5 Pemeriksaan Stabilitas Fisik Sediaan Krim
Pemeriksaan stabilitas fisik sediaan krim dilakukan dengan
setiap 1 minggu selama 12 minggu. Bagian yang diamati meliputi pecah
atau tidaknya emulsi dan pemisahan kedua fase yaitu fase air dan fase
minyak (Lachman, 1994).
3.7 Pembuatan Media
3.7.1 Nutrien Agar
Komposisi: Bacto-beef extract 3 g
Bacto-peptone 5 g
Bacto-agar 15 g
Cara pembuatan :
Ditimbang sebanyak 23 g serbuk nutrien agar kemudian
disuspensikan dengan air suling yang ditambahkan sedikit demi sedikit
dalam erlenmeyer hingga 1000 ml, dipanaskan sampai bahan larut
sempurna. Disterilkan dalam autoklaf pada suhu 121oC selama 15 menit
(Difco, 1977).
3.7.2 Pembuatan Agar Miring
Kedalam tabung reaksi dimasukkan 3 ml media nutrien agar,
didiamkan pada suhu kamar sampai sediaan membeku pada posisi miring,
3.8 Pembiakan Bakteri
3.8.1 Pembuatan Stok Kultur
- Bakteri Staphylococcus aureus
Diambil satu koloni bakteri Staphylococcus aureus dengan
menggunakan jarum ose steril, lalu ditanamkan pada media nutrien agar
miring dengan cara menggores, setelah itu diinkubasi dalam inkubator pada
suhu 35 ± 2oC selama 18-24 jam.
- Bakteri Pseudomonas aeruginosa
Pembuatan stok kultur bakteri Pseudomonas aeruginosa dilakukan
prosedur yang sama dengan pembuatan stok kultur terhadap bakteri
Staphylococcus aureus tetapi yang digunakan adalah Pseudomonas
aeruginosa.
3.8.2 Penyiapan Inokulum
- Bakteri Staphylococcus aureus
Dari stok kultur bakteri Staphylococcus aureus diambil dengan
menggunakan jarum ose steril kemudian disuspensikan dalam tabung yang
berisi 10 ml larutan NaCl 0,9 % steril lalu diinkubasi dalam inkubator pada
suhu 35 ± 2oC selama 3 jam sampai diperoleh transmitan 25 % pada panjang
- Bakteri Pseudomonas aeruginosa
Dari stok kultur bakteri Pseudomonas aeruginosa diambil dengan
menggunakan jarum ose steril kemudian disuspensikan dalam tabung yang
berisi 10 ml larutan NaCl 0,9 % steril lalu diinkubasi dalam inkubator pada
suhu 35 ± 2oC selama 3 jam sampai diperoleh transmitan 25 % pada panjang
gelombang 580 nm, menggunakan spektrofotometer (Ditjen POM, 1995).
3.9 Pengenceran Minyak Kelapa Murni Dengan Berbagai Konsentrasi
Vial dikalibrasi 10 ml. Kemudian sebanyak 1 ml minyak kelapa
murni dimasukkan kedalam vial yang telah dikalibrasi lalu dicukupkan
dengan gliserin hingga batas kalibrasi. Konsentrasi minyak kelapa murni
adalah 10%, kemudian dibuat pengenceran selanjutnya sampai diperoleh
minyak kelapa murni dengan konsentrasi 8%, 6%, 4%, dan 2%.
3.10 Uji Aktivitas Antibakteri dari Minyak Kelapa Murni (VCO/virgin coconut oil)
3.10.1 Uji Aktivitas Antibakteri dari Minyak Kelapa Murni Terhadap Bakteri Staphylococcus aureus
Dipipet sebanyak 0,1 ml suspensi bakteri menggunakan mikropipet
ke dalam cawan petri yang berisi media NA dengan suhu 45-50 °C
sebanyak 15 ml, kemudian cawan digoyang-goyang agar media dan
suspensi bakteri tercampur rata. Pada media yang telah padat ditanam cincin
pencadang logam, dan ditetesi ekstrak sebanyak 0,1 ml dengan berbagai
suhu 35° ± 2 °C selama 18-24 jam. Selanjutnya diameter bening disekitar
cincin pencadang diukur menggunakan jangka sorong. Pekerjaan dilakukan
sebanyak tiga kali. Data dapat dilihat pada tabel 3 halaman 35.
3.10.2 Uji Aktivitas Antibakteri dari Minyak Kelapa Murni Terhadap Bakteri Pseudomonas aeruginosa
Uji aktivitas antibakteri dari sampel terhadap Pseudomonas
aeruginosa dilakukan prosedur yang sama seperti pada bakteri
Staphylococcus aureus hanya bakterinya diganti dengan Pseudomonas
aeruginosa. Dilakukan tiga kali pengulangan.
3.11 Uji Aktivitas Antibakteri Krim Minyak Kelapa Murni (VCO/virgin coconut oil).
3.11.1 Uji Aktivitas Antibakteri Krim Minyak Kelapa Murni Terhadap Bakteri Staphylococcus aureus
Sebanyak 0,1 ml inokulum dimasukkan ke dalam cawan petri steril,
setelah itu dituang media nutrien agar sebanyak 15 ml dengan suhu
45-50o-C. Selanjutnya cawan digoyang di atas permukaan meja, agar media dan
suspensi bakteri tercampur rata. Pada media yang telah padat diletakkan
beberapa pencadang gelas, kemudian krim minyak kelapa murni sebanyak
0,1 g yang ditambah beberapa tetes akuades steril, dimasukkan ke dalam
pencadang dengan berbagai konsentrasi minyak kelapa murni, kemudian
diinkubasi dalam inkubator pada suhu 35±2oC selama 18-24 jam, setelah itu
pencadang dengan menggunakan jangka sorong (Brooks, 1983). Hasil dapat
dilihat pada tabel 4 halaman 36.
3.11.2Uji Aktivitas Antibakteri Krim Minyak Kelapa Murni Terhadap Bakteri Pseudomonas aeruginosa
Uji aktivitas antibakteri dari krim minyak kelapa murni terhadap
Pseudomonas aeruginosa dilakukan prosedur yang sama seperti pada
bakteri Staphylococcus aureus hanya bakterinya diganti dengan
BAB IV
HASIL DAN PEMBAHASAHAN
4.1 Hasil Pemeriksaan Krim
4.1.1 Hasil Pemeriksaan Homogenitas
Hasil pemeriksaan homogenitas diketahui bahwa selama 12 minggu
masing-masing krim yang mengandung nipagin mempunyai konsistensi
yang homogen dan tidak terlihat adanya butir-butir kasar pada objek glass,
sedangkan krim minyak kelapa murni tanpa nipagin pada minggu ke 9 tidak
homogen karena adanya butir-butir kasar pada objek glass. Hal ini
kemungkinan disebabkan karena beberapa faktor yaitu, tidak adanya nipagin
didalam sediaan sehingga dasar krim sendiri tidak mampu mempertahankan
konsistensinya, ketidak seimbangan fase air dan fase minyak dalam sediaan
juga merusak homogenitas sediaan tersebut serta pengaruh dari minyak
kelapa murni yang bersifat asam yang dapat menyebabkan pecahnya emulsi
yang ditandai dengan terbentuknya butir-butir kasar, dimana semakin
banyak jumlah minyak kelapa murni yang terkandung didalam sediaan krim
akan menyebabkan krim tersebut semakin bersifat asam sehingga
mempercepat terbentuknya butir-butir kasar (Data dapat dilihat pada
Lampiran 1 halaman 43).
4.1.2 Hasil Pemeriksaan Organoleptis Sediaan Krim
Pada pemeriksaan penampilan dapat dilihat bahwa formula A (dasar
dan secara visual mempunyai konsistensi yang lunak, berwarna putih, tidak
berbau dan tidak mengalami perubahan penampilan warna dan bau selama
pengamatan (12 minggu). Demikian juga formula B, formula C, formula D,
formula E, dan formula F. Hal ini disebabkan karena didalam sediaan
mengandung bahan gliserin, yang merupakan fase berair yang tidak mudah
menguap, sehingga dapat mempertahankan konsistensi sediaan menjadi
tetap stabil (lunak), selain itu juga mengandung bahan-bahan tambahan
pengawet seperti nipagin sehingga sediaan krim tersebut tidak terurai
dengan adanya mikroba (Anief, 1999). Demikian juga krim minyak kelapa
murni (VCO/virgin coconut oil) yang tidak mengandung nipagin, hal ini
dikarenakan dalam minyak kelapa murni mengandung asam laurat paling
besar dibandingkan dengan asam lemak lainnya. Asam ini merupakan asam
lemak jenuh yang tergolong ke dalam kelompok asam lemak rantai sedang
(MCFA/Medium Chain Faty Acids) yang berfungsi sebagai antibakteri.
Tingginya asam lemak jenuh menyebabkan minyak kelapa tahan terhadap
proses ketengikan akibat oksidasi. MCFA stabil pada suhu tinggi, misalnya
tidak mengental meskipun dalam waktu yang lama digunakan pada suhu
penggorengan (suhu tinggi). Warna MCFA juga tidak berubah akibat
penambahan panas, sehingga krim yang mengandung minyak kelapa murni
(VCO/virgin coconut oil) tetap stabil tidak mengalami perubahan
4.1.3 Hasil Pengukuran pH Krim Minyak Kelapa Murni Mengandung Nipagin Dan Tidak Mengandung Nipagin
Selama pengamatan 12 minggu pH formula A (dasar krim)
mengalami kenaikan menjadi sedikit basa dari pH 7,5 menjadi 7,8 hal ini
disebabkan karena bahan-bahan yang digunakan sebagai dasar krim
mengandung asam stearat dan trietanolamin yang bereaksi membentuk
trietanolaminstearat yaitu suatu sabun yang bersifat basa lemah (Voight,
1994).
Formula B (krim dengan kadar minyak kelapa murni 2%)
mempunyai pH 7,5, setelah pengamatan pada minggu pertama stabil tetapi
pada minggu ke 12 pHnya turun menjadi 6,7. Begitu juga dengan formula C
(krim dengan kadar minyak kelapa murni 4%), formula D (krim dengan
kadar minyak kelapa murni 6%), formula E (krim dengan kadar minyak
kelapa murni 8%), dan formula F (krim dengan kadar minyak kelapa murni
10%) masing-masing mengalami penurunan pH yaitu formula C dari 7,5
menjadi 6,5, formula D dari 7,5 menjadi 6,5 formula E dari 7,5 menjadi 6,5
dan formula F dari 7,5 menjadi 6,4. Penurunan pH yang terjadi pada krim
minyak kelapa murni disebabkan karena banyaknya asam-asam organik
yang terkandung dalam minyak kelapa murni sehingga mempengaruhi
penurunan pH dari krim minyak kelapa murni, dimana semakin besar
konsentrasi minyak kelapa murni dalam sediaan krim maka sediaan tersebut
4.1.4 Hasil Pemeriksaan Stabilitas Fisik Sediaan Krim
Pada pemeriksaan stabilitas sediaan yang mengandung nipagin (data
dapat dilihat pada lampiran 1), formula A, formula B, formula C, formula D,
formula E, dan formula F selama penyimpanan pada suhu kamar, suhu 4oC,
dan suhu 40oC tetap stabil tidak mengalami pemisahan fase, hal ini
disebabkan oleh beberapa hal, yaitu karena adanya nipagin yang
menghambat pertumbuhan mikroorganisme yang berasal dari kontaminasi
udara pada lingkungan penyimpanan sehingga krim minyak kelapa murni
yang mengandung nipagin tidak dapat terurai oleh mikroorganisme dari
udara, dan asam lemak rantai sedang yang terkandung didalam minyak
kelapa murni dimana sesuai dengan teori yang dikemukakan oleh
Alamsyah, A.N, 2005, “Dalam minyak kelapa murni terdapat Medium
Chain Fatty Acids (MCFA). MCFA merupakan komponen asam lemak
rantai sedang. MCFA stabil pada suhu tinggi dan rendah, misalnya tidak
mengental meskipun dalam waktu yang lama digunakan pada suhu
penggorengan (suhu tinggi). Warna MCFA juga tidak berubah hitam akibat
penambahan panas”. Selain itu adanya pengawet seperti nipagin membuat
sediaan krim tersebut tidak terurai dsengan adanya mikroba (Anief, 1999).
Pada sediaan tanpa nipagin terlihat kurang stabil. Pemisahan fase ini
disebabkan karena ketidak seimbangan volume dari fase air dan fase minyak
dalam sediaan sehingga menyebabkan pecahnya sediaan. Perbandingan
volume fase dari suatu emulsi mempunyai pengaruh skunder terhadap
kestabilan produk. Umumnya suatu perbandingan fase volume 50/50
empiris oleh ahli farmasi bertahun-tahun yang lalu, dan emulsi-emulsi obat
umumnya dibuat dengan perbandingan 50 bagian minyak dengan 50 bagian
air (Martin, 1993). Kenaikan temperatur serta tidak adanya nipagin sehingga
mikroorganisme dari udara dapat memacu peruraian zat-zat ataupun
mengoksidasi asam lemak sehingga minyak rusak yang dapat menyebabkan
emulsi pecah karena terjadinya perubahan viskositas dan naiknya
butiran-butiran kasar yang diakibatkan oleh perubahan sifat dari emulgator (Anief,
1999). Data dapat dilihat pada lampiran 1 halaman 47.
4.2 Hasil Pemeriksaan Aktivitas Antibakteri Minyak Kelapa Murni (VCO/virgin coconut oil)
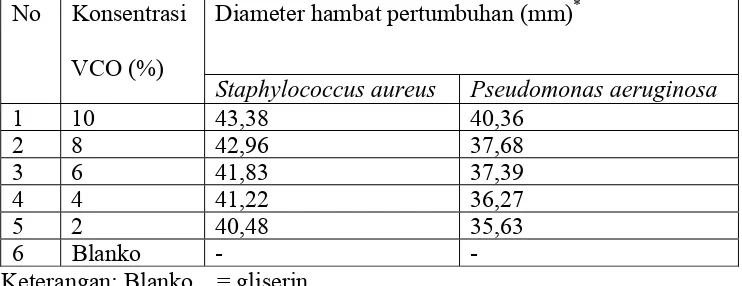
Hasil analisis minyak kelapa (VCO/virgin coconut oil) terhadap
daya aktivitasnya sebagai antibakteri adalah sangat besar karena pada
konsentrasi 2% masih mempunyai daya hambat 40,48 mm terhadap
Staphylococcus aureus dan 35,63 mm untuk Pseudomonas aeruginosa.
[image:50.595.113.484.595.738.2]Data dapat dilihat pada tabel dibawah ini.
Tabel 3. Hasil Uji Aktivitas Antibakteri Minyak Kelapa Murni (VCO/virgin
coconut oil) Terhadap Staphylococcus aureus dan Pseudomonas aeruginosa
Diameter hambat pertumbuhan (mm)* No Konsentrasi
VCO (%)
Staphylococcus aureus Pseudomonas aeruginosa
1 10 43,38 40,36
2 8 42,96 37,68
3 6 41,83 37,39
4 4 41,22 36,27
5 2 40,48 35,63
6 Blanko -
* = Hasil rata-rata tiga kali pangamatan
- = Tidak ada diameter hambatan pertumbuhan bakteri
Hasil Uji Aktivitas Antibakteri Minyak Kelapa Murni dalam Sediaan
Krim Tanpa Nipagin Terhadap Bakteri Staphylococcus aureus dan
Pseudomonas aeruginosa hal ini disebabkan oleh kandungan asam lemak
rantai sedang yang dikenal sebagai Medium Chain Fatty Acids (MCFA).
MCFA merupakan asam lemak khusus yang mempunyai rantai karbon yang
panjang dari C8-C12 yang bersifat jenuh (asam kaprat, kaprilat, dan laurat)
yang bermanfaat sebagai antibakteri, antijamur, antivirus dan antiprotozoa.
Asam lemak dari MCFA yang paling aktif sebagai antibakteri adalah asam
laurat (Ahkam Subroto, 2006). Bagian-bagian tertentu bakteri tersusun dari
lemak, misalnya membrane sel serta bagian tertentu dinding sel nya. Bakteri
memiliki enzim lipase yang dapat memecah lemak menjadi asam lemak dan
[image:51.595.114.486.595.740.2]gliserol (Tim mikribiologi FK Unibraw, 2003).
Tabel 4. Hasil Uji Aktivitas Antibakteri Krim Minyak Kelapa Murni tanpa
Nipagin Terhadap Staphylococcus aureus dan Pseudomonas
aeruginosa
Diameter hambatan pertumbuhan (mm)* No Konsentasi
VCO (%)
Staphylococcus aureus Pseudomonas aeruginosa
1 10 22,96 19,73
2 8 22,43 18,45
3 6 22.00 17,66
4 4 21,20 16,76
5 2 21.00 15,93
6 0 10,58 10.23
= Hasil rata-rata tiga kali pangamatan
Dari tabel diatas terlihat bahwa krim dari minyak kelapa murni
mempunyai daya hambat terhadap pertumbuhan bakteri sangat baik pada
Staphylococcus aureus maupun Pseudomonas aeruginosa.
Kemampuan menghambat pertumbuhan bakteri Staphylococcus
aureus dan Pseudomonas aeruginosa minyak kelapa murni disebabkan
karena bahan-bahan yang digunakan sebagai dasar krim mengandung asam
stearat dan trietanolamin yang bereaksi membentuk trietanolaminstearat
yaitu suatu sabun anionik yang bersifat basa lemah (Voight, 1994) yang
dapat membantu menghambat pertumbuhan bakteri dan juga karena minyak
kelapa murni sendiri mempunyai kandungan asam lemak rantai sedang yang
dikenal sebagai Medium Chain Fatty Acids (MCFA). MCFA merupakan
asam lemak khusus yang mempunyai rantai karbon yang panjang dari
C8-C12 yang bersifat jenuh (asam kaprat, kaprilat, dan laurat) yang bermanfaat
sebagai antibakteri, antijamur, antivirus dan antiprotozoa. Asam lemak dari
MCFA yang paling aktif sebagai antibakteri adalah asam laurat (Ahkam
Subroto, 2006). Bagian-bagian tertentu bakteri tersusun dari lemak,
misalnya membrane sel serta bagian tertentu dinding sel nya. Bakteri
memiliki enzim lipase yang dapat memecah lemak menjadi asam lemak dan
gliserol (Tim mikribiologi FK Unibraw, 2003). Adanya enzim lipase pada
bakteri maka trigleserida minyak kelapa murni dapat diubah menjadi bentuk
BAB V
KESIMPULAN DAN SARAN
5.1 Kesimpulan
Dari penelitian yang dilakukan dapat diambil kesimpulan bahwa
krim minyak kelapa murni (VCO/virgin coconut oil) yang mengandung
nipagin lebih stabil dibandingkan dengan krim minyak kelapa murni
(VCO/virgin coconut oil) yang tidak mengandung nipagin. Krim minyak
kelapa murni (VCO/virgin coconut oil) yang mengandung nipagin tidak
mengalami perubahan penampilan dan warna setelah disimpan selama 12
minggu. Untuk krim minyak kelapa murni (VCO/virgin coconut oil) yang
tidak mengandung nipagin mengalami perubahan penampilan pada minggu
ke 9.
Dari penelitian yang dilakukan, ternyata krim minyak kelapa murni
(VCO/virgin coconut oil) tanpa nipagin sudah bersifat antibakteri pada
konsentrasi 2% dengan diameter daya hambat 40,48 mm untuk
Staphylococcus aureus dan 34,48 mm untuk Pseudomonas aeruginosa.
Penambahan nipagin pada sediaan krim minyak kelapa murni
(VCO/virgin coconut oil) hanya berfungsi sebagai penambah stabilitas
sediaan tersebut.
5.2 Saran
Diharapkan pada peneliti selanjutnya untuk memformulasi minyak
DAFTAR PUSTAKA
Anief, M. (1999). Sistem Dispersi, Formulasi Suspensi dan Emulsi.
Yogyakarta: UGM Press. Hal. 107.
Anief, M. (2000). Farmasetika. Gadjah Mada University Press. Yogyakarta.
Hal. 111, 125-136.
Anonim. (2006). ”Kelapa”. Online. 2007.
http://www.warintek.progressio.or.id/perkebunan/kelapa.htm
Ansel, Howard C. (1989). Pengantar Bentuk Sediaan Farmasi. Edisi ke
empat. Jakarta : Universitas Indonesia Press. Hal : 513-515.
Bambang, S. dan Surip, P. (2006). Membuat VCO Berkualitas Tinggi. Seri
Agritekno. Cetakan Pertama. Jakarta: Penebar Swadaya. Hal. 16-17.
Brooks, G.F. (1983). Biology of Microorganism. Seventh edition. Peaseon
Prentice Hall. Machigan. P. 483-484.
Chatim, A. (1994). Mikrobiologi Kedokteran. Sterilisasi dan Desinfeksi.
Edisi Revisi. Binarupa Aksara. Jakarta. Hal. 42-43
Difco. (1977). Difco of Dehydrate Culture Media Reagent for Microbiology
and Clinical Laboratory Procedures. Ninth edition, Michigan
Detroit : Difco Laboratories. Page : 269-339.
Ditjen POM. (1979). Farmakope Indonesia. Edisi Ketiga. Jakarta:
Ditjen POM. (1984). Formularium Indonesia. Jakarta: Departemen
Kesehatan RI. Hal. 198.
Ditjen POM. (1995). Farmakope Indonesia. Edisi IV. Jakarta. Hal. 891-897.
Dwidjoseputro. (1987). Dasar-Dasar Mikrobiologi. Cetakan ke-9.
Surabaya: Depkes RI. Hal. 116-144.
Jawetz, Melnick, Adelberg’s. (2001). Mikrobiologi Kedokteran. Penerjemah
: Bagian Mikrobiologi Fakultas Kedokteran Universitas Airlangga.
Edisi I. Jakarta. Penerbit Salemba Medika. Hal. 317-326 dan
371-374.
Kabara, J., ”Health oils from the three of life”. Online. 2005
http://www.coconutoil.com/jhon/kabara.pdf
Lachman, L. (1994). Teori dan Praktek Farmasi Industri. Edisi Kedua. Jilid
Kedua. Jakarta: UI Press. Hal. 1098, 1105.
Lay, B.W. dan Hastowo, S. (1992). Mikrobiologi. Bogor : Penerbit Institut
Pertanian Bogor. Hal. 79.
Martin, A.N. dkk. (1993). Farmasi Fisik. Penerjemah : Yoshita. Edisi
Ketiga. Jilid kedua. Jakarta : UI Press. Hal : 1102-1103, 1174-1177.
Norman, P. (2008). Pengaruh Pemberian Minyak Kelapa Murni Olahan
Sendiri dsn Minyak Kelapa Murni Olahan Pabrik Terhadap Kadar
Kolesterol Darah Marmot Dibandingkan Dengan Simvastatin.
Pelczar, Michael J. (1985). Dasar-Dasar Mikrobiologi. Penerjemah : Ratna
Siri Hadioetomo, dkk. Edisi I. Jakarta : UI-Press. Hal. 86 dan 137.
Rawlins, E. (2002). Bentley’s : Textbook of Pharmaceutics. Eightenth
edition. London : Bailliere Tindall. Page : 22, 355.
Rindengan, B. dan Novarianto, H. (2005). Pembuatan dan Pemanfaatan
Minyak Kelapa Murni. Seri Agritekno. Cetakan Keempat. Jakarta:
Penebar Swadaya. Hal. 22-23.
Roday, S., (1999). Hygiene and Sanitation In Food Industry. Tata Mc.
Graw-Hill Publishing Company Limited. New Delhi. P. 13-22.
Sutarmi dan Hartin, R. (2005). Taklukkan Penyakit dengan VCO (Virgin
Coconut Oil). Seri Agrisehat. Cetakan Ketiga. Jakarta: Penebar
Swadaya. Hal. 8-19, 88-92.
Subroto, A. (2006). VCO Dosis Tepat Taklukkan Penyakit. Jakarta: Penebar
Swadaya. Hal. 22-23.
Suhardiman, P. (1999). Bertanam Kelapa Hibrida. Cetakan Kesepuluh.
Jakarta: Penebar Swadaya. Hal. 7-11, 16.
Suhardiyono,l. (1988). Tanaman Kelapa Budidaya dan Pemanfaatannya.
Yogyakarta: Penerbit Kanisus. Hal. 116.
Sonnenwirth, A.C. (1980). Growohl’s Clinical Laboratory Methods and
42
Syah , Andi Nur Alam. (2005). Virgin Coconut Oil. Cetakan Kedua.
Jakarta: Agromedia Pustaka. Hal. 8-19, 88-92.
Tim Mikrobiologi FK Universitas Brawijaya. (2003). Bakteriologik Medik.
Edisi Pertama. Malang: Bayumedia Publishing.
Hal. 12, 139, 197-198.
Voigt, R. (1994). Buku Pelajaran Teknologi Farmasi. Penerjemah:
Soendani Noerono. Edisi Kelima. Yogyakarta : Gajah Mada
University Press. Hal. 436.
Warisno. (1998). Budidaya Kelapa Kopyor. Yogyakarta: Penerbit Kanisius.
Hal. 13.
Wrakusumah, E. S., & Setyowati, R. N. (1999). Cantik Dan Bugar Dengan
Ramuan Nabati. Cetakan Keempat. Penebar Swadaya. Jakarta.
Lampiran 1. Hasil Pemeriksaan Organoleptis Krim Minyak Kelapa Murni (VCO/virgin coconut oil) Jenis pemerik saan Konsentrasi Hari 1 Minggu I Minggu II Minggu III Minggu IV Minggu V Minggu VI Minggu VII Minggu VIII Minggu IX Minggu X Minggu XI Minggu XII Konsist ensi
Dasar Krim SP SP SP SP SP SP SP SP SP SP SP SP SP
2 % SP SP SP SP SP SP SP SP SP - - - -
*2% SP SP SP SP SP SP SP SP SP SP SP SP SP
4 % SP SP SP SP SP SP SP SP SP - - - -
*4% SP SP SP SP SP SP SP SP SP SP SP SP SP
6 % SP SP SP SP SP SP SP SP SP - - - -
*6% SP SP SP SP SP SP SP SP SP SP SP SP SP
8 % SP SP SP SP SP SP SP SP SP - - - -
*8% SP SP SP SP SP SP SP SP SP SP SP SP SP
10% SP SP SP SP SP SP SP SP SP - - - -
*10% SP SP SP SP SP SP SP SP SP SP SP SP SP
Bau Dsr Krim TB TB TB TB TB TB TB TB TB TB TB TB TB
2 % VCO VCO VCO VCO VCO VCO VCO VCO VCO VCO VCO VCO VCO
*2% VCO VCO VCO VCO VCO VCO VCO VCO VCO VCO VCO VCO VCO
4 % VCO VCO VCO VCO VCO VCO VCO VCO VCO VCO VCO VCO VCO
*4% VCO VCO VCO VCO VCO VCO VCO VCO VCO VCO VCO VCO VCO
6 % VCO VCO VCO VCO VCO VCO VCO VCO VCO VCO VCO VCO VCO
*6% VCO VCO VCO VCO VCO VCO VCO VCO VCO VCO VCO VCO VCO
*8% VCO VCO VCO VCO VCO VCO VCO VCO VCO VCO VCO VCO VCO 10% VCO VCO VCO VCO VCO VCO VCO VCO VCO VCO VCO VCO VCO
*10% VCO VCO VCO VCO VCO VCO VCO VCO VCO VCO VCO VCO VCO
Homog enitas
Dsr Krim H H H H H H H H H H H H H
2 % H H H H H H H H H - - - -
*2% H H H H H H H H H H H H H
4 % H H H H H H H H H - - - -
*4% H H H H H H H H H H H H H
6 % H H H H H H H H H - - - -
*6% H H H H H H H H H H H H H
8 % H H H H H H H H H - - - -
*8% H H H H H H H H H H H H H 10% H H H H H H H H H - - - - *10% H H H H H H H H H H H H H Ada/Tid
ak ditumbu
hi Jamur (Visual)
Dsr Krim Tidak Tidak Tidak Tidak Tidak Tidak Tidak Tidak Tidak Tidak Tidak Tidak Tidak
*10% Tidak Tidak Tidak Tidak Tidak Tidak Tidak Tidak Tidak Tidak Tidak Tidak Tidak Pencuci
an
Dsr Krim Dapat dicuci Dapat dicuci Dapat dicuci Dapat dicuci Dapat dicuci Dapat dicuci Dapat dicuci Dapat dicuci Dapat dicuci Dapat dicuci Dapat dicuci Dapat dicuci Dapat dicuci
2 % Dapat
dicuci Dapat dicuci Dapat dicuci Dapat dicuci Dapat dicuci Dapat dicuci Dapat dicuci Dapat dicuci Dapat dicuci Dapat dicuci Dapat dicuci Dapat dicuci Dapat dicuci
*2% Dapat
dicuci Dapat dicuci Dapat dicuci Dapat dicuci Dapat dicuci Dapat dicuci Dapat dicuci Dapat dicuci Dapat dicuci Dapat dicuci Dapat dicuci Dapat dicuci Dapat dicuci
4 % Dapat
dicuci Dapat dicuci Dapat dicuci Dapat dicuci Dapat dicuci Dapat dicuci Dapat dicuci Dapat dicuci Dapat dicuci Dapat dicuci Dapat dicuci Dapat dicuci Dapat dicuci
*4% Dapat
dicuci Dapat dicuci Dapat dicuci Dapat dicuci Dapat dicuci Dapat dicuci Dapat dicuci Dapat dicuci Dapat dicuci Dapat dicuci Dapat dicuci Dapat dicuci Dapat dicuci
6 % Dapat
dicuci Dapat dicuci Dapat dicuci Dapat dicuci Dapat dicuci Dapat dicuci Dapat dicuci Dapat dicuci Dapat dicuci Dapat dicuci Dapat dicuci Dapat dicuci Dapat dicuci
*6% Dapat
dicuci Dapat dicuci Dapat dicuci Dapat dicuci Dapat dicuci Dapat dicuci Dapat dicuci Dapat dicuci Dapat dicuci Dapat dicuci Dapat dicuci Dapat dicuci Dapat dicuci
8 % Dapat
dicuci Dapat dicuci Dapat dicuci Dapat dicuci Dapat dicuci Dapat dicuci Dapat dicuci Dapat dicuci Dapat dicuci Dapat dicuci Dapat dicuci Dapat dicuci Dapat dicuci
*8% Dapat
dicuci Dapat dicuci Dapat dicuci Dapat dicuci Dapat dicuci Dapat dicuci Dapat dicuci Dapat dicuci Dapat dicuci Dapat dicuci Dapat dicuci Dapat dicuci Dapat dicuci
10% Dapat
dicuci Dapat dicuci Dapat dicuci Dapat dicuci Dapat dicuci Dapat dicuci Dapat dicuci Dapat dicuci Dapat dicuci Dapat dicuci Dapat dicuci Dapat dicuci Dapat dicuci
*10% Dapat
dicuci Dapat dicuci Dapat dicuci Dapat dicuci Dapat dicuci Dapat dicuci Dapat dicuci Dapat dicuci Dapat dicuci Dapat dicuci Dapat dicuci Dapat dicuci Dapat dicuci Tipe Emulsi
Dsr Krim M/A M/A M/A M/A M/A M/A M/A M/A M/A M/A M/A M/A M/A
2 % M/A M/A M/A M/A M/A M/A M/A M/A M/A M/A M/A M/A M/A
*2% M/A M/A M/A M/A M/A M/A M/A M/A M/A M/A M/A M/A M/A
4 % M/A M/A M/A M/A M/A M/A M/A M/A M/A M/A M/A M/A M/A
*4% M/A M/A M/A M/A M/A M/A M/A M/A M/A M/A M/A M/A M/A
*6% M/A M/A M/A M/A M/A M/A M/A M/A M/A M/A M/A M/A M/A
8 % M/A M/A M/A M/A M/A M/A M/A M/A M/A M/A M/A M/A M/A
*8% M/A M/A M/A M/A M/A M/A M/A M/A M/A M/A M/A M/A M/A
10% M/A M/A M/A M/A M/A M/A M/A M/A M/A M/A M/A M/A M/A
*10% M/A M/A M/A M/A M/A M/A M/A M/A M/A M/A M/A M/A M/A
pH Dsr Krim 7,5 7,5 7,5 7,5 7,5 7,6 7,6 7,7 7,7 7,7 7,8 7,8 7,8
2 % 7,5 7,5 7,5 7,5 7,5 7,5 7,5 7,5 7,5 7,4 6,8 6,8 6,7
*2% 7,5 7,5 7,5 7,5 7,5 7,5 7,5 7,5 7,5 7,4 6,8 6,8 6,7
4 % 7,5 7,5 7,5 7,5 7,5 7,5 7,5 7,5 7,5 7,3 6,7 6,7 6,7
*4% 7,5 7,5 7,5 7,5 7,5 7,5 7,5 7,5 7,5 7,3 6,7 6,7 6,7
6 % 7,5 7,5 7,5 7,5 7,5 7,5 7,5 7,5 7,4 7,2 6,6 6,6 6,5
*6% 7,5 7,5 7,5 7,5 7,5 7,5 7,5 7,5 7,4 7,2 6,6 6,6 6,5
8 % 7,5 7,5 7,5 7,5 7,5 7,5 7,5 7,4 7,4 7,1 6,6 6,6 6,5
Stabilitas (Suhu Kamar)
Dsr Krim TM TM TM TM TM TM TM TM TM TM TM TM TM
2 % TM TM TM TM TM TM TM TM TM M - - -
*2% TM TM TM TM TM TM TM TM TM TM TM TM TM
4 % TM TM TM TM TM TM TM TM TM M - - -
*4% TM TM TM TM TM TM TM TM TM TM TM TM TM
6 % TM TM TM TM TM TM TM TM TM M - - -
*6% TM TM TM TM TM TM TM TM TM TM TM TM TM
8 % TM TM TM TM TM TM TM TM TM M - - -
*8% TM TM TM TM TM TM TM TM TM TM TM TM TM
10% TM TM TM TM TM TM TM TM TM M - - -
*10% TM TM TM TM TM TM TM TM TM TM TM TM TM
Stabilitas (40oC) Dsr Krim TM TM TM TM TM TM TM TM TM TM TM TM TM
2 % TM TM TM TM TM TM TM TM TM M - - -
*2% TM TM TM TM TM TM TM TM TM TM TM TM TM
4 % TM TM TM TM TM TM TM TM TM M - - -
*4% TM TM TM TM TM TM TM TM TM TM TM TM TM
6 % TM TM TM TM TM T