KARAKTERISTIK FLUKS MEMBRAN KITOSAN
TERMODIFIKASI POLI(VINIL ALKOHOL) DENGAN
VARIASI POLI(ETILENA GLIKOL) SEBAGAI POROGEN
KHOIRUN NISA
DEPARTEMEN KIMIA
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM
INSTITUT PERTANIAN BOGOR
ABSTRAK
KHOIRUN NISA. Karakteristik Fluks Membran Kitosan Termodifikasi Poli(vinil
alkohol) dengan Variasi Poli(etilena glikol) sebagai Porogen. Dibimbing oleh
AHMAD SJAHRIZA dan SRI MULIJANI.
3
ABSTRACT
KHOIRUN NISA. Flux Characteristics of Chitosan Membrane Modified by
Poly(vinyl alcohol) with Variations Poly(ethylene glycol) as Porogen. Supervised
by AHMAD SJAHRIZA and SRI MULIJANI.
KARAKTERISTIK FLUKS MEMBRAN KITOSAN
TERMODIFIKASI POLI(VINIL ALKOHOL) DENGAN
VARIASI POLI(ETILENA GLIKOL) SEBAGAI POROGEN
KHOIRUN NISA
Skripsi
sebagai salah satu syarat untuk memperoleh gelar
Sarjana Sains pada
Departemen Kimia
DEPARTEMEN KIMIA
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM
INSTITUT PERTANIAN BOGOR
5
Judul Skripsi : Karakteristik Fluks Membran Kitosan Termodifikasi Poli(vinil
alkohol) dengan Variasi Poli(etilena glikol) sebagai Porogen
Nama : Khoirun Nisa
NIM : G01400021
Disetujui
Drs. Ahmad Sjahriza Dra. Sri Mulijani, M.S.
Ketua Anggota
Diketahui
Dekan Fakultas Matematika dan Ilmu Pengetahuan Alam
PRAKATA
Puji dan syukur penulis panjatkan kepada Allah SWT atas segala
karunia-Nya sehingga karya ilmiah ini berhasil diselesaikan. Tema yang dipilih dalam
penelitian ini adalah kajian fluks membran hidrogel kitosan-poli(vinil alkohol),
dengan judul Karakteristik Fluks Membran Kitosan Termodifikasi Poli(vinil
alkohol) dengan Variasi Poli(etilena glikol) sebagai Porogen.
Penulis mengucapkan terima kasih kepada Drs. Ahmad Sjahriza dan Dra.
Sri Mulijani, M.S. selaku pembimbing yang telah memberikan bimbingan dan
pengarahan dalam penyusunan karya tulis ini. Ungkapan terima kasih juga
kepada Mimi, Mama, Yayu Wah, Saroh, Aa Maulana, dan Yayang Azhar atas
dukungan, perhatian, dan kasih sayang tulusnya. Penghargaan penulis sampaikan
kepada Bapak Mail, Bapak Nano, Ibu Ai, Pak Pam, Pak Sabur, Mas Toni, serta
staf dosen kimia fisik FMIPA IPB atas bantuannya, juga kepada Fenol, Bu Desi,
Bu Rini, dan rekan-rekan di Laboratorium Teknologi Kimia TIN atas
dukungannya. Selain itu, ucapan terima kasih kepada Dian, Isye, Ulil, selaku
rekan kerja yang mengesankan (
Shrimp family
), Dewi, Nunu, Mila, Tya, Mbak
Retno, Mbak Ain, Deni, Ira rekan Kimia 37, Ade, Yanti, Yayu, Tati, Nican,
Ratna, dan Ucie
the big family of
F-8c dan B-11 atas persahabatan, perhatian,
ilmu, semangat yang diberikan, serta kebersamaan yang indah.
Semoga karya ilmiah ini bermanfaat.
Bogor, Oktober 2005
7
RIWAYAT HIDUP
Penulis dilahirkan di Jatibarang pada tanggal 1 Februari 1982 dari ayah
Drs. M. Rawi dan ibu Fatimah. Penulis merupakan putri kedua dari lima
bersaudara.
Tahun 2000 penulis lulus dari SMU Negeri 6 Cirebon dan pada tahun yang
sama lulus seleksi masuk IPB melalui jalur Undangan Seleksi Masuk IPB
(USMI). Penulis memilih Program Studi Kimia, Departemen Kimia, Fakultas
Matematika dan Ilmu Pengetahuan Alam.
Pemisahan suatu molekul dari molekul-molekul yang lain dalam suatu larutan dapat dilakukan dengan beberapa cara antara lain adalah kromatografi kolom, kromatografi lapis tipis, HPLC, dan elektoforesis. Namun teknik-teknik tersebut memiliki beberapa kekurangan di antaranya adalah tidak sederhana dan memerlukan bahan kimia lain yang tidak sedikit. Saat ini telah banyak digunakan teknik pemisahan yang lebih sederhana, yaitu teknik pemisahan dengan menggunakan membran. Teknologi pemisahan menggunakan membran memiliki beberapa kelebihan, yaitu lebih sederhana, tidak memerlukan bahan kimia tambahan, serta ramah lingkungan (Fadillah 2003).
Membran dapat dibuat dari bahan organik maupun anorganik. Membran organik lebih dikenal dengan membran polimer karena bahan-bahan pembuat membran organik merupakan polimer baik polimer sintetik ataupun alami (Kesting 1971). Membran anorganik dapat dibuat dari beberapa material seperti kaca, keramik, maupun logam (Mulder 1996). Kitosan sebagai salah satu biopolimer yang melimpah di alam dapat juga digunakan sebagai bahan pembuat membran (Aryanto 2002).
Membran kitosan dalam perkembangannya sering dimodifikasi dengan bahan atau polimer lain. Modifikasi tersebut antara lain dapat dilakukan dengan penambahan bahan atau polimer yang dapat membentuk ikatan silang dengan molekul kitosan, seperti penambahan glutaraldehida atau genipin (Jin et al. 2004). Modifikasi juga dapat dilakukan dengan pembentukan jaringan antara molekul kitosan dengan molekul polimer lain seperti poli(etilena oksida) (PEO) (Jin et al. 2004). Modifikasi dapat pula dilakukan dengan melapisi permukaan membran kitosan dengan plasma uap alkana
(petroleum eter) (Wang et al. 2001).
Disamping itu larutan kitosan juga dapat digunakan untuk memodifikasi membran lain dalam hal ini selulosa dengan cara melapisi seluruh permukaan membran selulosa sehingga dihasilkan membran dengan laju alir air yang lebih rendah, ukuran pori-pori yang lebih kecil, dan kemampuan rejeksi makromolekul protein yang lebih tinggi (Yang et al. 2001).
Modifikasi membran kitosan diharapkan dapat menghasilkan membran dengan karakter yang lebih baik seperti peningkatan kestabilan
makromolekul dari suatu larutan oleh membran lebih efektif (Wang et al. 2001).
Membran kitosan yang dimodifikasi dengan agen pertautan silang genipin lebih stabil pada pH 2-4 dibandingkan dengan membran kitosan murni. Penambahan PEO pada campuran kitosan-genipin memberikan karakter hidrogel pada membran yang dihasilkan. Hal itu terjadi karena pembentukan struktur semi-interpenetrating network (semi-IPN) pada membran, akibatnya terjadi pembengkakan membran pada lingkungan dengan pH • 7. Semakin kecil pH maka pembengkakan semakin besar (Jin et al. 2004).
Membran kitosan yang dibuat dalam penelitian ini akan dimodifikasi dengan penambahan bahan pembentuk struktur semi-IPN yaitu poli(vinil alkohol) (PVA) karena sifat mekaniknya yang baik (Hassan & Peppas 2000). Selain penambahan PVA juga dilakukan penambahan glutaraldehida sebagai agen pertautan silang. Untuk pembentukan dan penyeragaman pori-pori membran, dalam hal ini dilakukan penambahan poli(etilena glikol) (PEG) sebagai porogen (Yang et al. 2001).
Penambahan PVA dalam penelitian ini dimaksudkan untuk meningkatkan kekuatan membran kitosan sedangkan penambahan PEG sebagai porogen dilakukan untuk menambah pori-pori yang terbentuk pada membran sehingga dapat meningkatkan fluks. Dalam penelitian ini juga akan dibuktikan terbentuknya struktur hidrogel semi-IPN antara kitosan, PVA dan glutaraldehida yang sensitif terhadap perubahan pH lingkungan.
TINJAUAN PUSTAKA
Kitin dan Kitosan
Kitosan merupakan salah satu produk alam yang merupakan turunan kitin. Kitin adalah sebuah polisakarida yang terbuat dari kulit udang, rajungan dan kepiting. Unit utama dari polimer kitin adalah 2-deoksi-2-(asetilamin) glukosa yang dikombinasikan dengan rantai 1-4 glikosida. Pemutusan gugus asetil dari kitin oleh basa kuat menghasilkan kitosan (Sigma-Aldrich 1999).
9
polikation yang tidak larut dalam air tetapi larut dalam asam organik seperti asam format, asetat, tartat, dan sitrat (Sigma-Aldrich 1999). Gambar 1 menunjukkan struktur kitin dan kitosan.
(a)
(b)
Gambar 1 Struktur molekul Kitin (a) dan Kitosan (b).
Keberadan gugus amina pada kitosan menyebabakan kitosan larut dalam media asam. Pelarutan kitosan dalam asam akan membentuk larutan kental yang dapat digunakan untuk pembuatan gel dalam berbagai variasi seperti butiran, membran, ataupun serat (Jin et al. 2004).
Perbedaan antara kitin dan kitosan terletak pada derajat deasetilasi. Umumnya reaksi pelepasan gugus asetil (deasetilasi) dalam larutan alkali tidak terjadi sepenuhnya walaupun dibawah perlakuan yang ekstrim. Derajat deasetilasi biasanya berkisar antara 70-95%, bergantung pada metode yang digunakan dalam pembuatan kitosan (Li et al. 1992). Derajat deasetilasi kitosan yang dapat digunakan dalam pembuatan membran antara lain 77% dan 85% (Cardenas et al. 2003).
Derajat deasetilasi merupakan salah satu faktor kimia paling penting dalam kitosan. Metode untuk menentukan gugus asetil yang terlepas dari kitosan diantaranya adalah spektroskopi inframerah, titrasi, kromatografi gas, dan absorpsi warna. Menurut Muzzarelli spektrofotometri ultraviolet pada panjang gelombang 199 nm merupakan metode terbaik untuk penentuan derajat deasetilasi secara akurat dan tidak merusak, dengan teknik ini absorbans N-asetilglukosamina bergantung pada konsentrasi dan tidak dipengaruhi oleh keberadaan asam asetat (Li et al. 1992).
Viskositas kitosan dipengaruhi oleh beberapa faktor seperti derajat deasetilasi, berat molekul, konsentrasi pelarut, kekuatan
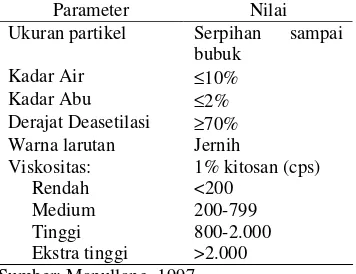
ionik, pH, dan temperatur. Perubahan pH berbanding terbalik dengan viskositas. Semakin tinggi pH maka viskositas semakin rendah (Li et al. 1992). Derajat deasetilasi, kadar abu, kadar air, dan viskositas merupakan parameter penting bagi kitosan seperti terlihat pada Tabel 1.
Optimasi yang dilakukan dalam pembuatan membran kitosan oleh Aryanto (2002) menggunakan pelarut asam asetat, asam sitrat, dan asam formiat dengan konsentrasi 10% pada konsentrasi kitosan 1, 3, 5, dan 7 % memperlihatkan bahwa pelarut dan konsentrasi kitosan terbaik dalam pembuatan membran adalah asam asetat dan konsentrasi 7%. Pembuatan membran kitosan dapat dimodifikasi dengan menggunakan bahan tambahan yang dapat meningkatkan stabilitas dan karakter membran, bahan yang biasa digunakan sebagai penstabil membran antara lain glutaraldehida (Jin et al. 2004) dan genipin (Jin et al. 2004), keduanya merupakan agen pertautan silang pada kitosan. Polimer lain juga dapat ditambahkan pada larutan kitosan untuk pembentukan karakter gel pada membran, polimer tersebut antara lain adalah PVA (Wang et al. 2004) dan PEO (Jin et al. 2004).
Tabel 1 Parameter mutu kitosan.
Parameter Nilai
Ukuran partikel Serpihan sampai
bubuk
Kadar Air ≤10%
Kadar Abu ≤2%
Derajat Deasetilasi ≥70%
Warna larutan Jernih
Viskositas: 1% kitosan (cps)
Rendah <200
Medium 200-799
Tinggi 800-2.000
Ekstra tinggi >2.000 Sumber: Manullang 1997.
Glutaraldehida
Glutaraldehida (Gambar 2) merupakan agen pertautan silang yang sering digunakan dalam polipeptida dan protein karena aktivitasnya yang tinggi dan gugus aldehida yang dapat membentuk basa Schiff´s dengan gugus amino dari protein. Glutaraldehida juga digunakan sebagai agen pertautan silang dengan PVA dan beberapa polisakarida lain seperti heparin, asam hialuronat, dan kitosan (Wang et al. 2004). Glutaraldehida merupakan senyawa dengan fungsi ganda yang umumnya digunakan dalam modifikasi protein dan
O O
HO
CH2OH
NH2
HO
NH2
CH2OH
n
O O
HO
CH2OH
NHAc HO
NHAc CH2OH
H C H2 H2 C C H2 H O O
polimer. Glutaraldehida mempunyai rumus molekul C5H8O2 dengan bobot molekul sebesar 100.1 g/mol, titik didih sebesar 100 ºC, titik lebur -15 ºC, pH 3.2–4.2, berupa larutan yang berwarna kuning, larut dalam air, alkohol, dan benzene (BASF 1999).
Gambar 2 Struktur glutaraldehida.
PVA
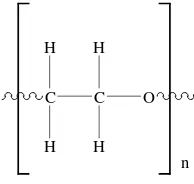
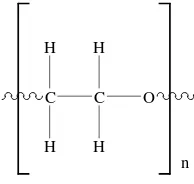
Poli(vinil alkohol) merupakan polimer yang sangat menarik karena memiliki karakter yang sesuai untuk aplikasi dalam bidang farmasi dan biomedis. Sifat mekanik dari PVA merupakan sifat yang menarik terutama dalam preparasi hidrogel. PVA memiliki struktur kimia yang sederhana dengan gugus hidroksil yang tidak beraturan. Monomernya, yaitu vinil alkohol tidak berada dalam bentuk stabil, tetapi berada dalam keadaan tautomer dengan asetaldehida (Wang et al. 2004). Gambar 3 menunjukkan struktur molekul PVA.
PVA dagang biasanya merupakan campuran dari beberapa tipe stereoregular yang berbeda (isotaktik, ataktik, dan sindiotaktik). Mutu PVA dagang yang baik ditentukan oleh derajat hidrolisisnya. Derajat hidrolisis berpengaruh terhadap kelarutan PVA dalam air, semakin tinggi derajat hidrolisisnya maka kelarutannya akan semakin rendah (Hassan & Peppas 2000). PVA dengan derajat hidrolisis 98,5% atau lebih dapat dilarutkan dalam air pada suhu 70°C. Dalam pembuatan hidrogel kitosan-PVA, PVA dilarutkan dalam larutan kitosan pada suhu 80°C selama lima menit (Wang et al. 2004).
Kombinasi Kitosan-PVA dengan glutaraldehida sebagai agen pertautan silang menghasilkan struktur hidrogel semi-IPN. Hidrogel yang terbentuk dari kombinasi tersebut memiliki nisbah pembengkakan dan penyusutan yang tinggi, sensitif terhadap perubahan pH, serta mudah terurai secara alami (Wang et al. 2004).
Gambar 3 Struktur PVA.
PEG
Poli(etilena glikol) adalah molekul sederhana dengan struktur molekul linier atau bercabang. Pada suhu ruang, PEG dengan bobot molekul dibawah 700 berbentuk cair, sedangkan yang memiliki bobot molekul 700-900 berbentuk semi padat, dan PEG dengan bobot molekul 900-1000 atau lebih berbentuk padatan. PEG larut dalam air dan beberapa pelarut organik seperti toluena, aseton, metanol, dan metilklorida tetapi tidak larut dalam heksana dan hidrokarbon alifatik yang sejenis (Fadillah 2003).
PEG secara dagang dibuat dari reaksi antara etilena oksida dengan air atau reaksi antara etilena glikol (HOCH2CH2OH) dengan sejumlah kecil katalis natrium klorida, dan jumlah etilena glikol menentukkan bobot molekul dari PEG. Rumus struktur PEG ditunjukkan oleh Gambar 4 berikut (Stevens 2001).
Menurut hasil penelitian Fadillah (2003), interaksi konsentrasi PEG dengan selulosa asetat menunjukkan adanya pengaruh yang sangat nyata terhadap ukuran pori-pori membran. Fluks membran akan bertambah dengan bertambahnya konsentrasi PEG dan berkurangnya konsentrasi selulosa asetat. Nilai fluks membran komposit selulosa-kitosan semakin meningkat dengan peningkatan konsentrasi PEG (Yang et al. 2001).
Gambar 4 Struktur PEG.
OH
OH OH
n
C C O
H
H H
H
KARAKTERISTIK FLUKS MEMBRAN KITOSAN
TERMODIFIKASI POLI(VINIL ALKOHOL) DENGAN
VARIASI POLI(ETILENA GLIKOL) SEBAGAI POROGEN
KHOIRUN NISA
DEPARTEMEN KIMIA
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM
INSTITUT PERTANIAN BOGOR
ABSTRAK
KHOIRUN NISA. Karakteristik Fluks Membran Kitosan Termodifikasi Poli(vinil
alkohol) dengan Variasi Poli(etilena glikol) sebagai Porogen. Dibimbing oleh
AHMAD SJAHRIZA dan SRI MULIJANI.
3
ABSTRACT
KHOIRUN NISA. Flux Characteristics of Chitosan Membrane Modified by
Poly(vinyl alcohol) with Variations Poly(ethylene glycol) as Porogen. Supervised
by AHMAD SJAHRIZA and SRI MULIJANI.
KARAKTERISTIK FLUKS MEMBRAN KITOSAN
TERMODIFIKASI POLI(VINIL ALKOHOL) DENGAN
VARIASI POLI(ETILENA GLIKOL) SEBAGAI POROGEN
KHOIRUN NISA
Skripsi
sebagai salah satu syarat untuk memperoleh gelar
Sarjana Sains pada
Departemen Kimia
DEPARTEMEN KIMIA
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM
INSTITUT PERTANIAN BOGOR
5
Judul Skripsi : Karakteristik Fluks Membran Kitosan Termodifikasi Poli(vinil
alkohol) dengan Variasi Poli(etilena glikol) sebagai Porogen
Nama : Khoirun Nisa
NIM : G01400021
Disetujui
Drs. Ahmad Sjahriza Dra. Sri Mulijani, M.S.
Ketua Anggota
Diketahui
Dekan Fakultas Matematika dan Ilmu Pengetahuan Alam
PRAKATA
Puji dan syukur penulis panjatkan kepada Allah SWT atas segala
karunia-Nya sehingga karya ilmiah ini berhasil diselesaikan. Tema yang dipilih dalam
penelitian ini adalah kajian fluks membran hidrogel kitosan-poli(vinil alkohol),
dengan judul Karakteristik Fluks Membran Kitosan Termodifikasi Poli(vinil
alkohol) dengan Variasi Poli(etilena glikol) sebagai Porogen.
Penulis mengucapkan terima kasih kepada Drs. Ahmad Sjahriza dan Dra.
Sri Mulijani, M.S. selaku pembimbing yang telah memberikan bimbingan dan
pengarahan dalam penyusunan karya tulis ini. Ungkapan terima kasih juga
kepada Mimi, Mama, Yayu Wah, Saroh, Aa Maulana, dan Yayang Azhar atas
dukungan, perhatian, dan kasih sayang tulusnya. Penghargaan penulis sampaikan
kepada Bapak Mail, Bapak Nano, Ibu Ai, Pak Pam, Pak Sabur, Mas Toni, serta
staf dosen kimia fisik FMIPA IPB atas bantuannya, juga kepada Fenol, Bu Desi,
Bu Rini, dan rekan-rekan di Laboratorium Teknologi Kimia TIN atas
dukungannya. Selain itu, ucapan terima kasih kepada Dian, Isye, Ulil, selaku
rekan kerja yang mengesankan (
Shrimp family
), Dewi, Nunu, Mila, Tya, Mbak
Retno, Mbak Ain, Deni, Ira rekan Kimia 37, Ade, Yanti, Yayu, Tati, Nican,
Ratna, dan Ucie
the big family of
F-8c dan B-11 atas persahabatan, perhatian,
ilmu, semangat yang diberikan, serta kebersamaan yang indah.
Semoga karya ilmiah ini bermanfaat.
Bogor, Oktober 2005
7
RIWAYAT HIDUP
Penulis dilahirkan di Jatibarang pada tanggal 1 Februari 1982 dari ayah
Drs. M. Rawi dan ibu Fatimah. Penulis merupakan putri kedua dari lima
bersaudara.
Tahun 2000 penulis lulus dari SMU Negeri 6 Cirebon dan pada tahun yang
sama lulus seleksi masuk IPB melalui jalur Undangan Seleksi Masuk IPB
(USMI). Penulis memilih Program Studi Kimia, Departemen Kimia, Fakultas
Matematika dan Ilmu Pengetahuan Alam.
Pemisahan suatu molekul dari molekul-molekul yang lain dalam suatu larutan dapat dilakukan dengan beberapa cara antara lain adalah kromatografi kolom, kromatografi lapis tipis, HPLC, dan elektoforesis. Namun teknik-teknik tersebut memiliki beberapa kekurangan di antaranya adalah tidak sederhana dan memerlukan bahan kimia lain yang tidak sedikit. Saat ini telah banyak digunakan teknik pemisahan yang lebih sederhana, yaitu teknik pemisahan dengan menggunakan membran. Teknologi pemisahan menggunakan membran memiliki beberapa kelebihan, yaitu lebih sederhana, tidak memerlukan bahan kimia tambahan, serta ramah lingkungan (Fadillah 2003).
Membran dapat dibuat dari bahan organik maupun anorganik. Membran organik lebih dikenal dengan membran polimer karena bahan-bahan pembuat membran organik merupakan polimer baik polimer sintetik ataupun alami (Kesting 1971). Membran anorganik dapat dibuat dari beberapa material seperti kaca, keramik, maupun logam (Mulder 1996). Kitosan sebagai salah satu biopolimer yang melimpah di alam dapat juga digunakan sebagai bahan pembuat membran (Aryanto 2002).
Membran kitosan dalam perkembangannya sering dimodifikasi dengan bahan atau polimer lain. Modifikasi tersebut antara lain dapat dilakukan dengan penambahan bahan atau polimer yang dapat membentuk ikatan silang dengan molekul kitosan, seperti penambahan glutaraldehida atau genipin (Jin et al. 2004). Modifikasi juga dapat dilakukan dengan pembentukan jaringan antara molekul kitosan dengan molekul polimer lain seperti poli(etilena oksida) (PEO) (Jin et al. 2004). Modifikasi dapat pula dilakukan dengan melapisi permukaan membran kitosan dengan plasma uap alkana
(petroleum eter) (Wang et al. 2001).
Disamping itu larutan kitosan juga dapat digunakan untuk memodifikasi membran lain dalam hal ini selulosa dengan cara melapisi seluruh permukaan membran selulosa sehingga dihasilkan membran dengan laju alir air yang lebih rendah, ukuran pori-pori yang lebih kecil, dan kemampuan rejeksi makromolekul protein yang lebih tinggi (Yang et al. 2001).
Modifikasi membran kitosan diharapkan dapat menghasilkan membran dengan karakter yang lebih baik seperti peningkatan kestabilan
makromolekul dari suatu larutan oleh membran lebih efektif (Wang et al. 2001).
Membran kitosan yang dimodifikasi dengan agen pertautan silang genipin lebih stabil pada pH 2-4 dibandingkan dengan membran kitosan murni. Penambahan PEO pada campuran kitosan-genipin memberikan karakter hidrogel pada membran yang dihasilkan. Hal itu terjadi karena pembentukan struktur semi-interpenetrating network (semi-IPN) pada membran, akibatnya terjadi pembengkakan membran pada lingkungan dengan pH • 7. Semakin kecil pH maka pembengkakan semakin besar (Jin et al. 2004).
Membran kitosan yang dibuat dalam penelitian ini akan dimodifikasi dengan penambahan bahan pembentuk struktur semi-IPN yaitu poli(vinil alkohol) (PVA) karena sifat mekaniknya yang baik (Hassan & Peppas 2000). Selain penambahan PVA juga dilakukan penambahan glutaraldehida sebagai agen pertautan silang. Untuk pembentukan dan penyeragaman pori-pori membran, dalam hal ini dilakukan penambahan poli(etilena glikol) (PEG) sebagai porogen (Yang et al. 2001).
Penambahan PVA dalam penelitian ini dimaksudkan untuk meningkatkan kekuatan membran kitosan sedangkan penambahan PEG sebagai porogen dilakukan untuk menambah pori-pori yang terbentuk pada membran sehingga dapat meningkatkan fluks. Dalam penelitian ini juga akan dibuktikan terbentuknya struktur hidrogel semi-IPN antara kitosan, PVA dan glutaraldehida yang sensitif terhadap perubahan pH lingkungan.
TINJAUAN PUSTAKA
Kitin dan Kitosan
Kitosan merupakan salah satu produk alam yang merupakan turunan kitin. Kitin adalah sebuah polisakarida yang terbuat dari kulit udang, rajungan dan kepiting. Unit utama dari polimer kitin adalah 2-deoksi-2-(asetilamin) glukosa yang dikombinasikan dengan rantai 1-4 glikosida. Pemutusan gugus asetil dari kitin oleh basa kuat menghasilkan kitosan (Sigma-Aldrich 1999).
9
polikation yang tidak larut dalam air tetapi larut dalam asam organik seperti asam format, asetat, tartat, dan sitrat (Sigma-Aldrich 1999). Gambar 1 menunjukkan struktur kitin dan kitosan.
(a)
(b)
Gambar 1 Struktur molekul Kitin (a) dan Kitosan (b).
Keberadan gugus amina pada kitosan menyebabakan kitosan larut dalam media asam. Pelarutan kitosan dalam asam akan membentuk larutan kental yang dapat digunakan untuk pembuatan gel dalam berbagai variasi seperti butiran, membran, ataupun serat (Jin et al. 2004).
Perbedaan antara kitin dan kitosan terletak pada derajat deasetilasi. Umumnya reaksi pelepasan gugus asetil (deasetilasi) dalam larutan alkali tidak terjadi sepenuhnya walaupun dibawah perlakuan yang ekstrim. Derajat deasetilasi biasanya berkisar antara 70-95%, bergantung pada metode yang digunakan dalam pembuatan kitosan (Li et al. 1992). Derajat deasetilasi kitosan yang dapat digunakan dalam pembuatan membran antara lain 77% dan 85% (Cardenas et al. 2003).
Derajat deasetilasi merupakan salah satu faktor kimia paling penting dalam kitosan. Metode untuk menentukan gugus asetil yang terlepas dari kitosan diantaranya adalah spektroskopi inframerah, titrasi, kromatografi gas, dan absorpsi warna. Menurut Muzzarelli spektrofotometri ultraviolet pada panjang gelombang 199 nm merupakan metode terbaik untuk penentuan derajat deasetilasi secara akurat dan tidak merusak, dengan teknik ini absorbans N-asetilglukosamina bergantung pada konsentrasi dan tidak dipengaruhi oleh keberadaan asam asetat (Li et al. 1992).
Viskositas kitosan dipengaruhi oleh beberapa faktor seperti derajat deasetilasi, berat molekul, konsentrasi pelarut, kekuatan
ionik, pH, dan temperatur. Perubahan pH berbanding terbalik dengan viskositas. Semakin tinggi pH maka viskositas semakin rendah (Li et al. 1992). Derajat deasetilasi, kadar abu, kadar air, dan viskositas merupakan parameter penting bagi kitosan seperti terlihat pada Tabel 1.
Optimasi yang dilakukan dalam pembuatan membran kitosan oleh Aryanto (2002) menggunakan pelarut asam asetat, asam sitrat, dan asam formiat dengan konsentrasi 10% pada konsentrasi kitosan 1, 3, 5, dan 7 % memperlihatkan bahwa pelarut dan konsentrasi kitosan terbaik dalam pembuatan membran adalah asam asetat dan konsentrasi 7%. Pembuatan membran kitosan dapat dimodifikasi dengan menggunakan bahan tambahan yang dapat meningkatkan stabilitas dan karakter membran, bahan yang biasa digunakan sebagai penstabil membran antara lain glutaraldehida (Jin et al. 2004) dan genipin (Jin et al. 2004), keduanya merupakan agen pertautan silang pada kitosan. Polimer lain juga dapat ditambahkan pada larutan kitosan untuk pembentukan karakter gel pada membran, polimer tersebut antara lain adalah PVA (Wang et al. 2004) dan PEO (Jin et al. 2004).
Tabel 1 Parameter mutu kitosan.
Parameter Nilai
Ukuran partikel Serpihan sampai
bubuk
Kadar Air ≤10%
Kadar Abu ≤2%
Derajat Deasetilasi ≥70%
Warna larutan Jernih
Viskositas: 1% kitosan (cps)
Rendah <200
Medium 200-799
Tinggi 800-2.000
Ekstra tinggi >2.000 Sumber: Manullang 1997.
Glutaraldehida
Glutaraldehida (Gambar 2) merupakan agen pertautan silang yang sering digunakan dalam polipeptida dan protein karena aktivitasnya yang tinggi dan gugus aldehida yang dapat membentuk basa Schiff´s dengan gugus amino dari protein. Glutaraldehida juga digunakan sebagai agen pertautan silang dengan PVA dan beberapa polisakarida lain seperti heparin, asam hialuronat, dan kitosan (Wang et al. 2004). Glutaraldehida merupakan senyawa dengan fungsi ganda yang umumnya digunakan dalam modifikasi protein dan
O O
HO
CH2OH
NH2
HO
NH2
CH2OH
n
O O
HO
CH2OH
NHAc HO
NHAc CH2OH
H C H2 H2 C C H2 H O O
polimer. Glutaraldehida mempunyai rumus molekul C5H8O2 dengan bobot molekul sebesar 100.1 g/mol, titik didih sebesar 100 ºC, titik lebur -15 ºC, pH 3.2–4.2, berupa larutan yang berwarna kuning, larut dalam air, alkohol, dan benzene (BASF 1999).
Gambar 2 Struktur glutaraldehida.
PVA
Poli(vinil alkohol) merupakan polimer yang sangat menarik karena memiliki karakter yang sesuai untuk aplikasi dalam bidang farmasi dan biomedis. Sifat mekanik dari PVA merupakan sifat yang menarik terutama dalam preparasi hidrogel. PVA memiliki struktur kimia yang sederhana dengan gugus hidroksil yang tidak beraturan. Monomernya, yaitu vinil alkohol tidak berada dalam bentuk stabil, tetapi berada dalam keadaan tautomer dengan asetaldehida (Wang et al. 2004). Gambar 3 menunjukkan struktur molekul PVA.
PVA dagang biasanya merupakan campuran dari beberapa tipe stereoregular yang berbeda (isotaktik, ataktik, dan sindiotaktik). Mutu PVA dagang yang baik ditentukan oleh derajat hidrolisisnya. Derajat hidrolisis berpengaruh terhadap kelarutan PVA dalam air, semakin tinggi derajat hidrolisisnya maka kelarutannya akan semakin rendah (Hassan & Peppas 2000). PVA dengan derajat hidrolisis 98,5% atau lebih dapat dilarutkan dalam air pada suhu 70°C. Dalam pembuatan hidrogel kitosan-PVA, PVA dilarutkan dalam larutan kitosan pada suhu 80°C selama lima menit (Wang et al. 2004).
Kombinasi Kitosan-PVA dengan glutaraldehida sebagai agen pertautan silang menghasilkan struktur hidrogel semi-IPN. Hidrogel yang terbentuk dari kombinasi tersebut memiliki nisbah pembengkakan dan penyusutan yang tinggi, sensitif terhadap perubahan pH, serta mudah terurai secara alami (Wang et al. 2004).
Gambar 3 Struktur PVA.
PEG
Poli(etilena glikol) adalah molekul sederhana dengan struktur molekul linier atau bercabang. Pada suhu ruang, PEG dengan bobot molekul dibawah 700 berbentuk cair, sedangkan yang memiliki bobot molekul 700-900 berbentuk semi padat, dan PEG dengan bobot molekul 900-1000 atau lebih berbentuk padatan. PEG larut dalam air dan beberapa pelarut organik seperti toluena, aseton, metanol, dan metilklorida tetapi tidak larut dalam heksana dan hidrokarbon alifatik yang sejenis (Fadillah 2003).
PEG secara dagang dibuat dari reaksi antara etilena oksida dengan air atau reaksi antara etilena glikol (HOCH2CH2OH) dengan sejumlah kecil katalis natrium klorida, dan jumlah etilena glikol menentukkan bobot molekul dari PEG. Rumus struktur PEG ditunjukkan oleh Gambar 4 berikut (Stevens 2001).
Menurut hasil penelitian Fadillah (2003), interaksi konsentrasi PEG dengan selulosa asetat menunjukkan adanya pengaruh yang sangat nyata terhadap ukuran pori-pori membran. Fluks membran akan bertambah dengan bertambahnya konsentrasi PEG dan berkurangnya konsentrasi selulosa asetat. Nilai fluks membran komposit selulosa-kitosan semakin meningkat dengan peningkatan konsentrasi PEG (Yang et al. 2001).
Gambar 4 Struktur PEG.
OH
OH OH
n
C C O
H
H H
H
11
Membran
Menurut Mulder 1996, membran merupakan batas atau penghalang selektif antara dua fase. Selektif menunjukkan keselektifan membran atau proses yang menggunakan membran tersebut. Membran polimer merupakan semua pembatas atau penghalang polimer yang bersifat semipermeabel (Kesting 1971).
Menurut Mulder 1996, berdasarkan bahan dasarnya membran dibedakan menjadi membran organik dan anorganik, membran organik merupakan membran yang terbuat dari bahan polimer baik polimer alami maupun polimer sintetik, polimer yang biasa digunakan dalam pembuatan membran adalah selulosa beserta turunannya (seperti selulosa asetat), polisulfon, polikarbonat, polipropilena, dan polietilena. Membran anorganik merupakan membran yang terbuat dari bahan-bahan anorganik seperti keramik, kaca, dan logam. Membran keramik antara lain dapat terbuat dari bahan alumina, zirkonia, titania, dan silikon karbida.
Transpor membran dibedakan menjadi transpor aktif dan transpor pasif. Transpor pasif merupakan transpor molekul melewati
membran dengan bantuan gaya dorong seperti perbedaan tekanan (• P), konsentrasi (• C), atau suhu (• T ).
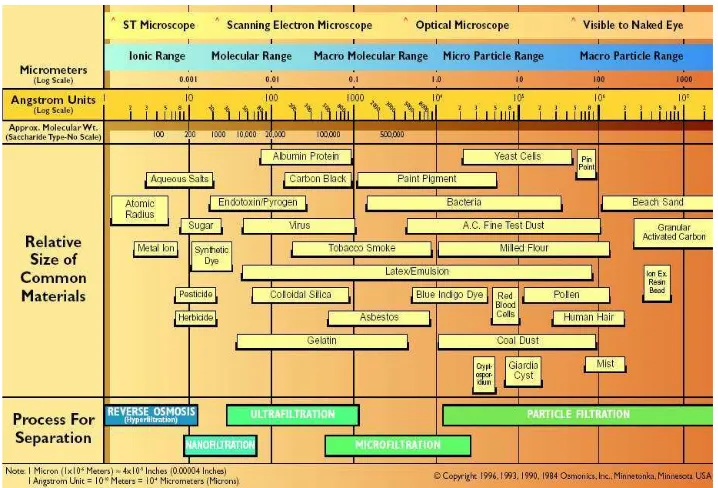
Proses membran dengan gaya dorong • P, dibedakan menjadi mikrofiltrasi, ultrfiltrasi, nanofiltrasi, dan osmosis balik. Gambar 5 berikut menerangkan spektrum teknik pemisahan berdasarkan proses membran dengan gaya dorong • P.
Membran dapat dipreparasi dengan menggunakan beberapa metode antara lain pelelehan, pengepresan, track-etching, dan pembalikan fase. Pembalikan fase adalah proses dimana polimer diubah dari bentuk larutan menjadi bentuk padatan secara terkontrol. Proses pemadatan sangat sering diawali dengan perpindahan polimer dari suatu cairan (pelarut) ke cairan lain (non-pelarut). Fase dengan konsentrasi polimer yang tinggi dalam larutan polimer akan membentuk padatan atau matriks membran, sedangkan fase dengan konsentrasi polimer yang rendah akan membentuk pori-pori (Mulder 1996).
Karakterisasi Membran
Menurut Kesting (1971), membran dapat dikarakterisasi berdasarkan struktur maupun fungsinya. Berdasarkan strukturnya membran dapat dikarakterisasi ketebalan, kandungan air, permeabilitas, ukuran pori, distribusi ukuran pori, densitas pori, dan beberapa sifat fisik dan kimia. Berdasarkan fungsinya karakterisasi membran meliputi adalah koefisien difusi, temperatur, takaran, rejeksi zat terlarut, fluks, potensial membran, jumlah pelarut yang ditransfer melewati membran (permeat), dan volume elektroosmotik.
Fluks. Fluks merupakan aliran fluida yang melewati membran (Minneci dan Paulson 1987). Fluks juga dapat didefinisikan sebagai volume permeat per unit area dan waktu. Menurut Mulder 1996, fluks dapat dinyatakan dengan persamaan berikut:
J = V/ A t
J : Fluks (L/m2 jam) V : Volume permeat (L)
A : Luas membran yang dilalui (m2) t : Waktu (jam)
Fluks membran antara lain dapat dipengaruhi oleh material polimer yang digunakan dalam pembuatan membran, gaya dorong (•P) yang dikenakan pada proses membran, konsentrasi polarisasi, dan fouling (Mulder 1996). Jenis polimer yang digunakan dalam pembuatan membran sangat berpengaruh terhadap pelarut dan non-pelarut yang digunakan, terutama pada membran yang dibuat dengan metode pembalikan fase. Hal tersebut juga akan mempengaruhi struktur dan karakter membran yang terbentuk seperti ukuran pori, distribusi pori, dan respon terhadap fouling. Selain jenis polimernya, konsentrasi polimer yang digunakan sebagai bahan pembuat membran juga sangat berpengaruh, semakin tinggi konsentrasinya maka fluks membran yang dihasilkan akan semakin rendah (Mulder 1996). Gejala tersebut akan diperlihatkan pada Tabel 2.
Tabel 2 Fluks air murni membran polisulfon. Konsentrasi Polimer
(%)
Fluks
(L/m2
jam)
12 200
15 80
17 20
35 0*
Sumber: Mulder 1996.
Gaya dorong (•P) yang dikenakan pada membran akan mempengaruhi laju fluks yang terjadi, semakin tinggi tekanan yang dikenakan maka fluks akan semakin besar (tanpa dipengaruhi faktor polarisasi konsentrasi dan fouling). Pada beberapa jenis
proses membran dengan gaya dorong •P,
perbedaan tekanan yang diberikan akan menghasilkan nilai fluks yang berbeda-beda pula. Hal tersebut ditunjukkan oleh Tabel 3.
Tabel 3 Kisaran nilai fluks dalam variasi tekanan pada proses membran dengan •P sebagai gaya dorong.
Proses Membran Kisaran Tekanan (bar) Kisaran Nilai Fluks (L/m2 jam)
Mikrofiltrasi 0.1-2.0 >50 Ultrafiltrasi 1.0-5.0 10-50 Nanofiltrasi 5.0-20.0 1.40-12
Osmosis Balik
10.0-100.0 0.05-1.40
Sumber: Mulder 1996.
Perilaku membran dapat berubah sangat besar terhadap waktu, sehingga nilai fluks juga berubah terhadap waktu. Semakin lama waktu, nilai fluks yang dihasilkan akan semakin kecil dan berbeda dengan nilai awalnya. Pada umpan suatu larutan hal ini dapat disebabkan oleh polarisasi konsentrasi ataupun fouling. Polarisasi konsentrasi akan menyebabkan terbentuknya beberapa hambatan dalam transpor membran, yaitu diawali dengan peningkatan jumlah zat terlarut pada permukaan membran hingga mencapai konsentrasi tertentu (konsentrasi polarisasi) dan menimbulkan hambatan (Rcp), jika hal ini terus berlanjut akan terbentuk lapisan gel diatas permukaan membran dan menimbulkan hambatan gel (Rg). Hambatan-hambatan lain yang ditimbulkan adalah hambatan adsorpsi (Ra) dan penyumbatan pori oleh zat terlarut (Rpb). Akibatnya nilai fluks turun sampai tercapai keadaan tunak.
13
ultrfiltrasi dan nanofiltrasi kompaksi juga bisa terjadi, yaitu bergantung pada tekanan yang dikenakan dan morfologi membran (Mulder 1996).
Rancangan Sistem. Sistem pemisahan membran dapat dibedakan menjadi beberapa macam sesuai dengan aplikasinya. Dua rancangan sistem yang paling sederhana adalah sistem dead-end dan cross-flow. Pada sistem dead-end, larutan umpan dialirkan secara tegak lurus terhadap membran, akibatnya akumulasi konsentrasi komponen-komponen yang tertahan pada permukaan membran akan cepat terjadi sehingga terjadi
fouling dan menyebabkan penurunan laju
permeat. Pada sistem cross-flow, aliran umpan sejajar (tangensial) terhadap membran sehingga komponen yang tertahan diatas permukaan membran akan dibersihkan oleh aliran tangensial sehingga tidak cepat
terakumulasi dan menyebabkan fouling.
Didalam modul membran aliran umpan dipisahkan menjadi dua aliran, yaitu aliran permeat dan aliran rentetate. Penggambaran dari kedua sistem tersebut ditunjukkan oleh Gambar 6 (Mulder 1996.)
umpan
umpan
rentetate
permeat permeat (a) (b)
Gambar 6 Skema modul operasi dasar Dead-end (a) dan Cross-flow (b)
.
BAHAN DAN METODE
Bahan dan Alat
Bahan-bahan yang digunakan dalam penelitian ini adalah kitosan dengan derajat deasetilasi 77.81% (BM=1579.4 kDa), akuades, asam asetat 1% (v/v), larutan NaOH 1M, PVA (BM=72000), glutaraldehida 25% (v/v), larutan buffer fosfat pH 6, PEG (BM= 400), dan membran dagang (polisulfon dan polikarbonat).
Alat-alat yang digunakan adalah alat-alat kaca, pengaduk magnetik, pH meter, timbangan analitik, pemanas, lempeng kaca, plastik polietilena, alat penyaring cross-flow, dan Fourier Transform Infrared (FTIR Tensor 27-Bruker).
Metode Penelitian
Tahapan yang dilakukan dalam penelitian ini terdiri atas pembuatan larutan kitosan 3% (b/v), pembuatan dope membran yang terdiri dari campuran kitosan 3%, PVA (0.0, 2.5, dan 5.0%), PEG (0.0, 2.5, dan 5.0%), dan glutaraldehida 33.30 µM. Kemudian dilanjutkan dengan pencetakan membran (metode pembalikan fase) dan pengukuran fluks membran dengan umpan akuades dan bufer fosfat pH 6.
Pembuatan larutan kitosan 3%. Sebanyak 3 gram kitosan dilarutkan ke dalam asam asetat 1% (v/v), kemudian diaduk selama 1 jam dengan pengaduk magnetik sampai terbentuk larutan kental jernih kekuningan. Gambar 7a menunjukkan larutan kitosan 3%.
(a) (b)
Gambar 7 Larutan Kitosan 3% (a) Dope (b).
Pembuatan dope. PVA (BM=72000) dimasukkan ke dalam larutan kitosan 3% (b/v) (dengan variasi konsentrasi 0.0, 2.5 dan 5.0% (b/v)) dalam labu erlenmeyer dan diaduk dengan pengaduk magnet di atas pemanas pada suhu 80º C selama lima menit sampai semua PVA larut, selama pemanasan labu erlenmeyer ditutup dengan plastik polietilena. Setelah didinginkan pada suhu ruang dilanjutkan dengan penambahan PEG (BM=400) dengan variasi konsentrasi 0.0, 2.5, dan 5.0% (b/v) ke dalam campuran kitosan-PVA dengan diaduk selama 30 menit sampai semua PEG larut. Tahap terakhir dalam
pembuatan dope (Gambar 7b) adalah
Tabel 4 Komposisi PVA dan PEG setiap jenis membran.
Jenis Membran PVA (%) PEG (%)
R1 0.0 0.0
R2 0.0 2.0
R3 0.0 5.0
R4 2.5 0.0
R5 2.5 2.0
R6 2,5 5.0
R7 5.0 0.0
R8 5.0 2.5
R9 5.0 5.0
Pencetakan membran. Setiap dope yang sudah terbebas dari gelembung-gelembung udara kemudian dicetak di atas permukaan lempeng kaca berukuran 20 x 15 cm dan ditekan dengan batang pengaduk sebagai aplikator sampai diperoleh lapisan tipis yang rata. Cetakan tersebut kemudian diuapkan semalaman lalu dicelupkan ke dalam NaOH 1M dalam wadah berukuran 30 x 20 cm selama 2-3 jam. Membran yang telah tercetak dilepaskan dari permukaan lempeng kaca dan dicuci dengan akuades untuk menghilangkan NaOH. Membran dipotong berbentuk lingkaran dengan diameter 5.5 cm (Gambar 8), kemudian disimpan dalam akuades sampai dilakukan pengukuran fluks. Bagan alir pembuatan membran ditunjukkan pada Lampiran 1.
Gambar 8 Membran kitosan-PVA.
Pengukuran fluks akuades dan bufer fosfat pH 6. Membran yang telah berbentuk lingkaran dimasukkan ke dalam modul pada alat penyaring cross-flow (Lampiran 2) untuk diukur fluksnya. Pengukuran fluks akuades dilakukan pada variasi tekanan (•P) 2.5, 5.0, 7.5, dan 10.0 psi, sedangkan pengukuran fluks bufer fosfat pH 6 dilakukan pada tekanan 2.5 dan 10.0 psi. Pengukuran fluks terhadap fungsi waktu dilakukan sampai tercapai keadaan tunak. Pengukuran fluks juga dilakukan terhadap membran dagang, yaitu membran polisulfon dan polikarbonat.
FTIR. Pengukuran FTIR kitosan dilakukan dengan cara sampel kitosan dihaluskan dengan KBr kemudian dari campuran itu dibentuk pelet lalu diukur pada bilangan
gelombang 400-4000 cm-1. Pengukuran
membran kitosan-PVA dilakukan dengan cara sampel dijepit pada lempeng NaCl lalu diukur pada bilangan gelombang yang sama.
HASIL DAN PEMBAHASAN
Pembentukan Membran Kitosan Termodifikasi
Membran yang terbentuk dari dope
dengan konsentrasi PVA 0.0% (R1, R2, dan R3) sangat rapuh dan tidak dapat dibentuk dalam bentuk lingkaran sehingga tidak dapat diukur fluksnya. Jin et al. (2004) menyatakan, lapisan yang terbuat dari kitosan murni lebih rapuh dibandingkan dengan kitosan yang dimodifikasi oleh PEO. Membran dengan konsentrasi PVA 2.5 dan 5.0% dapat terbentuk dengan baik dan lebih kuat dibandingkan dengan membran yang terbentuk tanpa penambahan PVA sehingga dapat dibentuk dalam bentuk lingkaran dan diukur fluksnya. Hal tersebut membuktikan bahwa sifat mekanik dari PVA mampu menstabilkan membran yang dibentuknya (Hassan & Peppas 2000). Membran yang terbentuk dari dope dengan konsentrasi PVA 2.5 dan 5.0% memiliki ketebalan yang beragam (Tabel 5), hal tersebut dikarenakan perbedaan konsentrasi PEG yang ditambahkan dan proses pencetakan.
Tabel 5 Data pengukuran tebal membran.
Jenis Membran Tebal (µm)
R4 40
R5 99
R6 91
R7 100
R8 74
R9 161
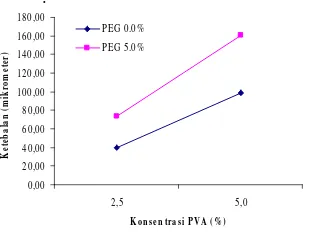
Pengukuran ketebalan membran memperlihatkan bahwa semakin tinggi konsentrasi PVA maka membran yang dihasilkan akan semakin tebal. Hal tersebut terjadi karena semakin tinggi konsentrasi PVA yang ditambahkan maka dope yang terbentuk akan semakin kental sehingga pada saat
pencetakan membran, dope dengan
15
0,00 20,00 40,00 60,00 80,00 100,00 120,00 140,00 160,00 180,00 2,5 5,0K on s e n tra s i P VA (% )
K et eb a la n ( m ik ro m et er) PEG 0.0% PEG 5.0%
teknik pencetakan membran. Membran R8 lebih tipis jika dibandingkan dengan membran R7 dan R9 walaupun ketiganya memiliki konsentrasi PVA yang sama, hal ini disebabkan oleh adanya gangguan dalam pencetakan membran seperti ketidakstabilan tekanan yang diberikan saat pencetakan. Gambar 9 menunjukkan hubungan antara ketebalan membran dan konsentrasi PVA. .
Gambar 9 Hubungan antara ketebalan membran dan konsentrasi PVA.
Nilai Fluks sebagai Fungsi Waktu
Nilai fluks membran berbanding terbalik terhadap fungsi waktu, semakin bertambahnya waktu nilai fluks suatu membran cenderung turun. Penurunan berlangsung terus menerus hingga tercapai keadaan tunak. Gejala tersebut dapat terjadi akibat adanya polarisasi konsentrasi dan atau terjadinya fouling pada permukaan membran yang dilewati oleh suatu larutan. Fluks air murni dalam proses ultrafiltrasi atau mikrofiltrasi biasanya akan mengalami penurunan nilai fluks kurang dari 5% (Mulder 1996).
Pengukuran fluks akuades maupun bufer fosfat pH 6 terhadap membran kitosan yang dihasilkan menunjukkan gejala yang sama, yaitu semakin lama waktu, nilai fluks semakin turun hingga tercapai nilai yang stabil pada keadaan tunak. Gejala ini ditunjukkan oleh Gambar 10.
Gambar 10 Fluks akuades membran R8 pada •P 10.0 psi.
Menurut Mulder (1996) jika gaya dorong yang dikenakan terhadap membran konstan maka nilai fluks membran akan konstan setelah tercapai keadaan tunak. Nilai fluks akuades membran R8 tersebut semakin turun dengan bertambahnya waktu sampai tercapai keadaan tunak (tanda lingkaran). Dari ketiga nilai pada keadaan tunak tersebut diperoleh nilai fluks rata-ratanya adalah 626.13 L/m2 jam. Penurunan nilai fluks dari nilai awalnya yaitu 811.69 L/m2jamtersebut lebih dari 5%, hal ini dapat disebabkan oleh akuades yang digunakan masih mengandung padatan atau pengotor. Gejala penurunan nilai fluks terhadap waktu untuk setiap jenis membran pada variasi tekanan untuk akuades bufer fosfat pH 6 berturut-turut ditunjukkan pada Lampiran 3 dan 4. Nilai fluks rata-rata untuk semua jenis membran yang dihasilkan berkisar antara 527.71 sampai 2558.45 L/m2 jam. Dari nilai tersebut dapat dikatakan bahwa membran kitosan-PVA yang dihasilkan termasuk ke dalam kelompok mikrofiltrasi, hal ini sesuai dengan pernyataan Mulder (1996) bahwa membran mikrofiltrasi memiliki kisaran nilai fluks lebih dari 50 L/m2 jam.
Pengaruh Konsentrasi PVA terhadap Fluks
Konsentrasi polimer pembentuk membran sangat mempengaruhi karakter membran yang terbentuk, semakin tinggi konsentrasi polimer pembentuknya maka membran yang dihasilkan akan semakin padat sehingga fluks membran akan semakin kecil (Mulder 1996). Konsentrasi kitosan dan glutaraldehida pada pembuatan membran dibuat tetap sehingga yang mempengaruhi konsentrsi polimer membran adalah PVA. Hubungan antara konsentrasi PVA dan fluks membran pada tekanan yang berbeda ditunjukkan pada Gambar 11a dan 11b.
0,00 100,00 200,00 300,00 400,00 500,00 600,00 700,00 800,00 900,00
10 15 20 25 30 35 40 45 50 55 60 65
W ak tu (menit)
0,00 200,00 400,00 600,00 800,00 1.000,00 1.200,00 1.400,00 1.600,00 1.800,00 2.000,00
2,5 5,0 7,5 10,0
T e k an a n (psi )
F luk s R a ta -R a ta ( L /j a m m 2 )
R 5 (P V A 2.5% ) R 8 (P V A 5.0% )
0,00 200,00 400,00 600,00 800,00 1.000,00 1.200,00 1.400,00 1.600,00 2,5 10.0 Tekanan (psi) F lu k s R a ta -R a ta ( L /j a m m2 )
R5 (PVA 2.5%)
R8 (PVA 5.0%)
0,00 500,00 1.000,00 1.500,00 2.000,00 2.500,00 3.000,00
2.5 p s i 5.0 p s i 7.5 p s i 10.0 p s i
T e k a n a n (ps i )
F lu k s R a ta -R a ta ( L /j a m m2 )
R7 (PEG 0.0% )
R9 (PEG 5.0% )
0,00 500,00 1.000,00 1.500,00 2.000,00 2.500,00 3.000,00
2.5 p s i 10.0 p s i
T e k a n a n (ps i )
F lu k s R a ta -R a ta ( L /j am m2 )
R 7 (P EG 0.0% )
R 9 (P EG 5.0% ) (a)
(b)
Gambar 11 Hubungan antara fluks dan konsentrasi PVA pada variasi tekanan Akuades (a) dan Bufer fosfat pH 6 (b).
Baik pada umpan akuades maupun bufer
nilai fluks membran turun seiring dengan meningkatnya konsentrasi PVA. Konsentrasi PEG pada dua kondisi tersebut tetap, yaitu 2.5%. Nilai fluks rata-rata untuk semua jenis membran pada variasi tekanan baik untuk akuades maupun bufer fosfat pH 6 ditunjukkan pada Lampiran 5.
Pengaruh Konsentrasi PEG terhadap Fluks
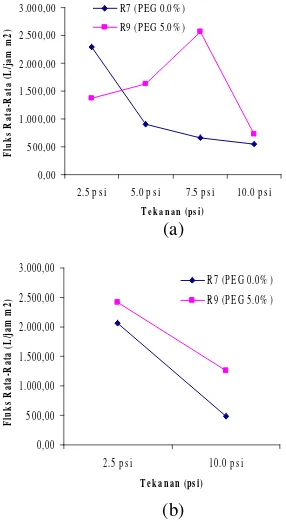
Penggunaan PEG pada penelitian ini dilakukan untuk pembentukan pori-pori membran atau dikenal sebagai porogen (Yang et al. 2001). Pengaruh penambahan PEG pada dope terhadap fluks membran pada variasi tekanan ditunjukkan oleh Gambar 12a dan 12b. Penambahan PEG menyebabkan kenaikan nilai fluks membran baik untuk akuades maupun bufer. Maka terbukti bahwa PEG dapat digunakan sebagai pembentuk pori-pori membran seperti yang dinyatakan oleh Fadillah (2003). Kedua keadaan tersebut terjadi pada konsentrasi PVA yang sama yaitu 5.0%.
(a)
(b)
Gambar 12 Hubungan antara fluks dan konsentrasi PEG pada variasi tekanan Akuades (a) dan Bufer fosfat pH 6 (b).
Karakter Hidrogel Membran dan Pengaruh Perubahan pH Lingkungan
terhadap Fluks Membran
Campuran kitosan dan PVA dengan glutaraldehida sebagai agen pertautan silang menghasilkan struktur jaringan semi-IPN (Wang et al. 2004). Semi-IPN merupakan salah satu jaringan yang dapat membentuk struktur hidrogel. Jaringan semi-IPN tersusun atas dua jenis polimer yang pada salah satu jenis polimernya terjadi ikatan silang antar sesamanya yang dibentuk oleh agen pertautan silang, sedangkan pada polimer yang lain tidak terbentuk ikatan silang oleh agen pertautan silang tersebut. Dalam hal ini polimer yang mengalami ikatan silang oleh glutaraldehida adalah kitosan, sedangkan PVA merupakan polimer yang tidak membentuk ikatan silang.
17
0 5 0 0 1 0 0 0 1 5 0 0 2 0 0 0 2 5 0 0
2 .5 p si 1 0 .0 p si
T e k a n a n (ps i )
F lu k s R at a-R at a ( L /j am m2 )
A k uad es Buffer p H 6
0 5 0 0 1 0 0 0 1 5 0 0 2 0 0 0 2 5 0 0 3 0 0 0
2 .5 p si 1 0 .0 p si
T e k a n a n (ps i )
F lu k s R at a-R at a ( L /j am m2
) A k uad e s
B uffe r p H 6
Menurut Jin et al. (2004), membran
kitosan-PEO dengan bahan pertautan silang genipin membentuk struktur hidrogel yang sensitif terhadap perubahan pH dan suhu lingkungan. Pada bufer pH • 7 terjadi pembengkakan membran hingga mencapai 50-100%, semakin asam lingkungan maka pembengkakan akan semakin besar. Pada lingkungan alkali tidak terjadi pembengkakan membran secara signifikan.
Nilai fluks membran kitosan-PVA dengan bahan pertautan silang glutaraldehida mengalami perubahan dengan adanya perubahan larutan umpan. Nilai fluks membran untuk akuades (pH 7.3) lebih besar jika dibandingkan dengan nilai fluks untuk bufer fosfat pH 6 pada konsentrasi polimer pembentuk membran dan tekanan yang sama. Gambar 13 menunjukkan gejala penurunan nilai fluks membran terhadap perubahan pH larutan umpan.
(a)
(b)
Gambar 13 Hubungan antara fluks dan jenis lautan umpan untuk PVA 2.5% (a) dan PVA
5.0%(b).
Penurunan nilai fluks membran antara lain disebabkan oleh karakter membran yang mengikuti karaktrer hidrogel. Hidrogel merupakan jaringan yang dapat menahan sejumlah air didalam strukturnya tanpa mengalami kelarutan tetapi mengalami
pembengkakan (Wang et al. 2004).
Pembengkakan membran dapat mengakibatkan terjadinya pemampatan pori-pori membran oleh matriks membran yang mengalami pembengkakan sehingga semakin besar pembengkakan yang terjadi pada membran nilai fluksnya akan semakin kecil. Nisbah pembengkakan akan lebih besar pada lingkungan asam dibandingkan pada lingkungan basa sehingga pada perlakuan menggunakan umpan bufer fosfat pH 6 nilai fluks membran yang dihasilkan cenderung lebih kecil daripada penggunaan akuades sebagai umpan dalam proses transpor membran.
Pengaruh Tekanan terhadap Fluks
Nilai fluks air murni pada umumnya berbanding lurus dengan tekanan yang
dikenakan terhadap membran (pressure
dropp) pada transpor membran (Mulder
1996). Kasus tertentu menunjukkan nilai fluks mengalami penurunan seiring dengan naiknya tekanan yang diberikan terhadap transpor membran, gejala ini disebabkan oleh adanya peristiwa kompaksi membran. Menurut Mulder (1996), kompaksi membran merupakan suatu perubahan mekanik pada struktur membran polimer yang terjadi dalam
proses membran dengan gaya dorong •P.
Akibatnya semakin tinggi tekanan yang dikenakan maka kompaksi membran akan berlangsung lebih cepat.
Nilai fluks membran hidrogel yang terbentuk dari kitosan-PVA dan glutraldehida sebagai bahan pertautan silang berbanding terbalik dengan tekanan yang dikenakan pada membran selama proses transpor membran. Hal tersebut terjadi akibat struktur hidrogel membran yang mengalami perubahan bentuk dalam air (umpan) sehingga menyebabkan penyempitan pori-pori membran selama proses berlangsung, terlebih lagi dengan adanya kenaikan tekanan yang dapat mempercepat kompaksi membran. Gejala tersebut digambarkan oleh Gambar 14. Hubungan antara fluks dan tekanan untuk setiap membran terdapat dalam Lampiran 6.
0 ,0 0 5 0 0 ,0 0 1 .0 0 0 ,0 0 1 .5 0 0 ,0 0 2 .0 0 0 ,0 0 2 .5 0 0 ,0 0 3 .0 0 0 ,0 0
2 ,5 5 ,0 7 ,5 1 0 ,0
Te k a n a n ( ps i )
F luk s R a ta -R a ta ( L /j a m m2 )
R 4 (PVA 2,5% )
R 7 (PVA 5.0% )
0,00 1.000,00 2.000,00 3.000,00 4.000,00 5.000,00 6.000,00
2.5 p s i 5.0 p s i 7.5 p s i 10.0 p s i
T e k a n a n (ps i )
F lu k s R at a-R at a ( L /j am m2
) P o likarb on at
P o lis u lfo n
R 4 (P V A 2.5 % )
R 7 (P V A 5.0 % )
Gambar 14 Hubungan antara Fluks dan tekanan.
Perbandingan Nilai Fluks Membran Kitosan-PVA dengan Membran Dagang
Membran dagang yang digunakan sebagai membran pembanding pada penelitian ini adalah membran polisulfon asimetri dengan ketebalan 150 µm dan membran polikarbonat simetri dengan ketebalan 10 µm. Pengukuran fluks membran pembanding menunjukkan gejala yang sama terhadap fungsi waktu, yaitu semakin lama waktu maka nilai fluks semakin turun sampai mencapai nilai yang stabil pada keadaan tunak.
Nilai fluks rata-rata untuk membran polisulfon dan polikarbonat (Lampiran 7) memperlihatkan bahwa semakin besar tekanan yang diberikan dalam proses membran maka nilai fluksnya juga semakin besar. Gejala ini berbeda dengan gejala yang terjadi pada pengukuran fluks membran kitosan-PVA. Hal ini disebabkan karena pada membran dagang tidak terbentuk karakter hidrogel sehingga matriks membran dagang tidak mengalami kompaksi.
Gambar 15 menunjukkan perbandingan nilai fluks rata-rata akuades terhadap fungsi tekanan antara membran R4 dan R7 yang dihasilkan dalam penelitian ini dengan membran-membran pembanding. Membran polikarbonat memiliki nilai fluks paling tinggi diantara keempat membran tersebut, sedangkan membran polisulfon memiliki nilai fluks yang mirip dengan membran kitosan-PVA.
Gambar 15 Kurva perbandingan antara membran kitosan termodifikasi dan membran
dagang.
Kajian Spektrum FTIR Kitosan dan Membran Kitosan
Termodifikasi
Struktur semi-IPN dari campuran kitosan-PVA dengan agen pertautan silang glutaraldehida, terbentuk akibat adanya ikatan silang antar rantai-rantai kitosan sementara pada rantai-rantai PVA tidak terbentuk ikatan silang oleh glutaraldehida. Ikatan kovalen koordinat yang terbentuk pada ikatan silang terjadi antara gugus amino (-NH2) dari rantai kitosan dengan atom karbon pada gugus aldehida dari glutaraldehida (Wang et al. 2004).
Mekanisme pembentukan ikatan silang tersebut ditunjukkan oleh Gambar 16. Pasangan elektron bebas nitrogen pada gug amino (-NH2) dari kitosan menyerang atom karbon tuna elektron akibat penataulangan pada gugus aldehida dari glutaraldehida. Kemudian dalam kondisi asam, reaksi substitusi nukleofilik tersebut melepaskan molekul air sehingga terbentuk ikatan rangkap dua antara atom karbon dengan nitrogen (C=N) yang menunjukkan keberadaan ikatan silang antar rantai kitosan oleh glutaraldehida pada identifikasi FTIR.
19
(a)
(b)
Spektrum FTIR kitosan (Gambar 17a) memperlihatkan puncak pada bilangan
gelombang 895.9 dan 951.4 cm-1 yang
menunjukkan struktur sakarida. Keberadaan gugus amida (N-H) primer dan sekundar dengan vibrasi tekuk pada struktur kitosan ditunjukkan dengan puncak pada panjang gelombang 1596.1 cm-1 dan diperkuat dengan puncak pada 3459.5 cm-1 yang menunjukkan
vibrasi ulur dari amida. Deformasi CH3
ditunjukkan dengan puncak pada 1330.2 cm-1,
sementara puncak pada 2866.1 cm-1
menunjukkan keberadaan gugus C-H ulur. Gugus C-O ulur dan O-H tekuk ditunjukkan dengan puncak-puncak pada 1422.3 dan 1379.0 cm-1.
Spektrum FTIR untuk membran kitosan-PVA (Gambar 17b) menunjukkan beberapa perbedaan pemunculan puncak. Amida primer yang mengalami ionisasi ditunjukkan dengan puncak pada bilangan gelombang 1588.6 cm-1.
Puncak pada 1423.5 cm-1 menunjukkan
keberadaan asam karboksilat pada polimer, yaitu asam yang digunakan untuk melarutkan kitosan, gugus C-H dari asam ditunjukkan dengan puncak pada bilangan gelombang 1332.0 cm-1. Sedangkan puncak yang muncul
pada panjang gelombang 1651.4 cm-1
mengidentifikasikan keberadaan gugus imina (C=N) yang merupakan ikatan kovalen yang terbentuk dari reaksi substitusi nukleofilik (nitrogen dari gugus amina pada rantai kitosan) terhadap gugus aldehida pada glutaraldehida.
SIMPULAN DAN SARAN
Simpulan
Membran yang terbentuk dari dope tanpa penambahan PVA memiliki sifat mekanik yang kurang baik. Hal tersebut ditunjukkan oleh membran yang terbentuk bersifat rapuh. Sebaliknya membran yang terbentuk dari dope dengan penambahan PVA baik 2.5 atau 5.0% memiliki sifat mekanik yang lebih baik. Hal tersebut ditunjukkan oleh membran yang terbentuk kuat dan tidak rapuh sehingga dapat diukur karakter fluksnya.
Penambahan PEG dalam pembuatan membran kitosan dapat meningkatkan jumlah pori-pori membran. Hal ini terlihat dari semakin tinggi konsentrasi PEG yang ditambahkan pada dope, semakin tinggi pula fluks membrannya.
Membran kitosan-PVA dengan glutaraldehida sebagai agen pertautan silang menunjukkan karakter hidrogel semi-IPN, hal
tersebut ditunjukkan oleh keberadaan gugus imina (C=N) pada spktrum FTIR membran. Sensitifitas hidrogel ditunjukkan oleh perubahan nilai fluks terhadap fluida umpan yaitu akuades (pH 7.3) dan bufer fosfat pH 6.0. Fluks lebih kecil pada fluida umpan beffer fosfat dibandingkan pada akuades.
Saran
Karakterisasi membran dalam penelitian ini lebih difokuskan pada nilai fluks, sedangkan masih banyak karakter lain yang harus diketahui diantaranya adalah pengukuran nilai rejeksi dengan berbagai molekul umpan untuk mengetahui bobot molekul terkecil yang dapat
tertahan oleh membran, SEM (Scanning
Electron Microscope) dan TEM (Transmission
Electron Microscope) untuk mengetahui
ukuran dan distribusi pori-pori membran, identifikasi penampang lintang membran, kadar
air membran dan viskositas dope.
Konsentrasi kitosan yang digunakan dalam pembuatan membran perlu divariasikan, sehingga dapat diketahui konsentrasi optimum yang dapat digunakan sebagai pembentuk membran. Untuk mengetahui lebih jauh tentang sensitivitas hidrogel membran kitosan-PVA terhadap pH dan suhu lingkungan perlu dilakukan pengukuran fluks lebih lanjut dengan larutan umpan bufer pH 8 atau lebih (basa) dan bufer pH 5 atau kurang (asam) dengan variasi suhu sehingga dapat lebih dipastikan seberapa jauh sensitivitas membran tersebut terhadap suhu lingkungan.
DAFTAR PUSTAKA
Aisyah IN. 2005. Pembengkakan hidrogel kitosan-PVA [skripsi]. Bogor: Departemen Kimia IPB.
Aryanto AY. 2002. Pemanfaatan kitosan dari limbah kulit udang (crustacea) sebagai bahan untuk pembuatan membran [skripsi]. Bogor: Departemen Teknologi Industri Pertanian IPB.
BASF. 1999. Glutaraldehide-50%. New Jersey: BASF Corporation.
21
Fadillah F. 2003. Pengaruh penambahan PEG terhadap karakterisasi membran selulosa asetat [skripsi]. Bogor: Departemen Teknologi Industri Pertanian IPB.
Hassan CM, Peppas NA. 2000. Structure and aplication of poli(vinyl alcohol) hidrogel produced by conventional crosslinking or by freezing/thawing methodes. Adven Polym Sci 153:37-38.
Jin J, Song M, Hourtston DJ. 2004. Novel chitosan-based films cross-linking by genipin with improved physical properties. Biomacromol 5:162-168.
Kesting R E. 1971. Synthetic Polymeric
Membranes. New York: McGraw-Hill.
Li Q, Dunn ET, Grandmaison EW, Goosen MFA. 1992. Applications and properties of chitosan. Di dalam: Goosen MFA, editor. Applications of Chitin and Chitosan. Lancaster: Technomic. hlm 3-21.
Manullang EH. 1997. Optimasi proses pembuatan kitin dari limbah udang (Penaid sp.) dengan menggunakan bahan teknis [skripsi]. Bogor: Fakultas Teknik Hasil Perikanan, Institut Pertanian Bogor.
Minneci P, Paulson D. 1987. Molecularly-bounded metal microfiltration membrane. http://www.osmonics.com. [17 Sep 2004].
Mulder M. 1996. Basic and Principles of
Membrane Technology. London:
Kluwer.
Sigma-Aldrich. 1999. Search result for: 9012-76-4. http:// www. Sigma-aldrich. com. [16 agustus 2004].
Stevens MP. 2001. Kimia Polimer. Iis sopyan, penerjemah. Jakarta: Pradnya Paramita.
Wang H, Fang Y, Yan Y. 2001. surface modification of chitosan membranes by
alkane vapor plasma. Mater Chem
11:1374-1377.
Wang T, Turhan M, Gunasekaran S. 2004. Selected properties of pH-sensitif, biodegradabel chitosan-poly(vynil alcohol) hidrogel. Pol Int 53:911-918.
Yang L, Hsiao WW, Chen P. 2001. Chitosan-cellulose composite membrane for affinity purifications of biopolymers and
immunoadsorption. J Membr Sci
23
Lampiran 1 Bagan alir pembuatan membran kitosan-PVA
Kitosan (3
gram)
Pelarutan dalam asam asetat
1%(v/v)
Larutan kitosan
3%
PVA (0.0, 2.5 dan
5.0%)
PEG (0.0, 2.5% dan
5%)
glutaraldehida
Dope
membran (variasi jenis
membran)
Pencetakan membran
Perendaman dalam NaOH 1M
Membran
Pencucian membran dengan
akuades
Lampiran 2 Alat sistem penyaringan
cross-flow
Alat penyaring
cross-flow.
25
0,00 500,00 1000,00 1500,00 2000,00 2500,00 3000,00 3500,00 4000,00
10 15 20 25 30 35 40 45 50 55 60 65 70 75
Waktu (menit)
F
luk
s (
L
/j
a
m m2
)
R4 R5 R6 R7 R8 R9
0,00 500,00 1000,00 1500,00 2000,00 2500,00 3000,00
10 15 20 25 30 35 40 45 50 55 60 65 70 75
Waktu (menit)
F
lu
k
s (
L
/j
a
m m
2
)
R4
R5
R6
R7
R8
R9
0,00 500,00 1000,00 1500,00 2000,00 2500,00 3000,00 3500,00
10 15 20 25 30 35 40 45 50 55 60 65 70 75 80 85
Waktu (menit)
F
lu
k
s (
L
/j
a
m m
2
)
R4 R5 R6 R7 R8 R9
Lampiran 3 Kurva penurunan nilai fluks akuades untuk setiap jenis membran pada
variasi tekanan
Kurva hubungan antara fluks dan waktu pada tekanan 2.5 psi.
Kurva hubungan antara fluks dan waktu pada tekanan 5.0 psi.
0,00 500,00 1000,00 1500,00 2000,00 2500,00
10 15 20 25 30 35 40 45 50 55 60 65 70 75 80 85 90 95 10 10 11 11
Waktu (menit)
F
luk
s (
L
/j
a
m m2
)
R4
R5
R6
R7
R8
R9
0,00 500,00 1000,00 1500,00 2000,00 2500,00 3000,00
10 15 20 25 30 35 40 45 50 55 60 65 70 75 80 85 90 95 100
Waktu (menit)
F
luk
s (
L
/j
a
m m
2
)
P 2.5 psi P 5.0 psi P 7.5 psi P 10.0 psi
0,00 1000,00 2000,00 3000,00 4000,00 5000,00 6000,00 7000,00
10 15 20 25 30 35 40 45
Waktu (menit)
F
lu
k
s (
L
/j
m m2
)
P 2.5 psi P 5.0 psi P 7.5 psi P 10.0 psi
Kurva hubungan antara fluks dan waktu pada tekanan 10.0 psi.
Kurva hubungan antara fluks dan waktu pada variasi tekanan membran polisulfon.
27
0,0 0 50 0,0 0 10 00 ,00 15 00 ,00 20 00 ,00 25 00 ,00 30 00 ,00
10 15 20 25 30 35 40 45 50 55 60 65 70 75 80 85 90 95 10 10
W a k tu (m e n i t)
F
lu
k
s (
L
/j
a
m m
R 4 R 5 R 6 R 7 R 8 R 9
0,00 200,00 400,00 600,00 800,00 1000,00 1200,00 1400,00 1600,00 1800,00
10 15 20 25 30 35 40 45 50 55 60 65 70 75 80 85 90 95 10 10
Waktu (menit)
F
lu
k
s (
L
/j
a
m m
2
)
R4 R5 R6 R7 R8 R9
Lampiran 4 Kurva penurunan nilai fluks bufer fosfat pH 6 untuk setiap
jenis membran pada variasi tekanan
Kurva hubungan antara fluks dan waktu pada tekanan 2.5 psi.
Lampiran 5 Nilai fluks rata-rata setiap jenis membran pada variasi tekanan
untuk akuades maupun bufer fosfat pH 6
Data nilai fluks rata-rata untuk setiap jenis membran pada variasi tekanan
Jenis Membran Komposisi Parameter
Tekanan Fluks Rata-Rata Air
Fluks Rata-Rata Bufer fosfat pH 6
(psi) (L/jam m2) (L/jam m2)
R1 A1B1-1 2.5 - -
A1B1-2 5.0 - -
A1B1-3 7.5 - -
A1B1-4 10.0 - -
R2 A1B2-1 2.5 - -
A1B2-2 5.0 - -
A1B2-3 7.5 - -
A1B2-4 10.0 - -
R3 A1B3-1 2.5 - -
A1B3-2 5.0 - -
A1B3-3 7.5 - -
A1B3-4 10.0 - -
R4 A2B1-1 2.5 2487.03 1191.68
A2B1-2 5.0 2284.95 -
A2B1-3 7.5 1215.26 -
A2B1-4 10.0 1164.61 788.50
R5 A2B2-1 2.5 1259.02 1342.30
A2B2-2 5.0 1904.53 -
A2B2-3 7.5 1065.51 -
A2B2-4 10.0 1666.43 572.79
R6 A2B3-1 2.5 942.07 630.53
A2B3-2 5.0 855.43 -
A2B3-3 7.5 807.89 -
A2B3-4 10.0 1252.77 968.45
R7 A3B1-1 2.5 2286.47 2072.09
A3B1-2 5.0 897.13 -
A3B1-3 7.5 655.22 -
A3B1-4 10.0 555.30 491.84
R8 A3B2-1 2.5 989.37 1106.76
A3B2-2 5.0 565.89 -
A3B2-3 7.5 527.71 -
A3B2-4 10.0 626.13 556.23
R9 A3B3-1 2.5 1365.01 2420.38
A3B3-2 5.0 1632.12 -
A3B3-3 7.5 2558.45 -
A3B3-4 10.0 731.06 1255.89
Keterangan:
- : Tidak diukur A1 : Konsentrasi PVA 0.0% Suhu : 26-29º C A2 : Konsentrasi PVA 2.5% Luas permukaan membran : 1.32 x 10-3 m2 A3 : Konsentrasi PVA 5.0%
Volume : 25 x 10-3 B1 : Konsentrasi PEG 0.0%
29
0,00 500,00 1.000,00 1.500,00 2.000,00 2.500,00 3.000,00
2.5 psi 5.0 psi 7.5 psi 10.0 psi
Tekanan (psi)
F
luk
s r
a
ta
-r
a
ta (
L
/j
a
m m2
)
R4
R5
R6
R7
R8
R9
0,00 500,00 1.000,00 1.500,00 2.000,00 2.500,00 3.000,00
2.5 p s i 10.0 p s i
Tek an an (ps i)
fl
u
k
s r
a
ta
-r
a
ta
buf
f (
L
/j
am m2
)
R 4 R 5 R 6 R 7 R 8 R 9
Lampiran 6 Hubungan antara fluks dan tekanan untuk setiap jenis membran
Kurva hubungan antara fluks dan tekanan setiap jenis membran umpan akuades.
Lampiran 7 Data fluks akuades membran dagang
Data fluks akuades membran dagang.
Jenis Membran
Fluks akuades pada variasi tekanan (L/jam m2)