ABSTRAK
PENGARUH VARIASI VOLTASE PROSES ANODISASI PADA
PADUAN ALUMINIUM ADC12 TERHADAP KEKASARAN
PERMUKAAN DAN KANDUNGAN FASA
Oleh :
GANJAR WIDYATMOKO
Dalam pembuatan berbagai bentuk komponen mesin saat ini sudah bukan merupakan suatu hal yang sulit, namun untuk menyempurnakan performa dari suatu material terutama ketahanan terhadap korosi dan memperindah tampilan tanpa mengesampingkan performa dari suatu material diperlukan proses yang sesuai sehingga diperoleh komponen yang tahan lama. Dalam perbaikan performa material, khususnya aluminium dan paduannya, anodisasi adalah salah satu proses yang banyak digunakan untuk mencapai tujuan tersebut.. Anodisasi itu sendiri adalah proses pembentukan lapisan oksida pada logam dengan cara mereaksikan logam terutama aluminium dengan oksigen (O2) dari larutan elektolit.
Penelitian ini menggunakan paduan aluminium ADC12 sebagai logam induk yang akan dilapisi dan asam phospat (H3PO4) sebagai elektrolitnya. Pada logam induk dilakukan anodisasi dengan menggunakan variasi tegangan yaitu 9 volt, 12 volt dan 15 volt dengan kuat arus listrik sebesar 0,2 ampere dan waktu proses anodisasi dilakukan selama 25 menit. Pengujian yang dilakukan meliputi pengujian kekasaran dan kandungan fasa lapisan.
pada permukaan paduan aluminium ADC12. Persentase kandungan fasa yang dihasilkan dalam proses anodisasi paduan aluminium yang menggunakan tegangan masing-masing 9 volt, 12 volt dan 15 volt yang dianodisasi selama 25 menit yaitu Al (76,868 %, 71,223 % dan 88,03 %), AlP (19,678 %, 22,9746 % dan 11,551 %) dan AlN (3,454 %, 5,802 % dan 0,419 %).
ABSTRACT
THE INFLUENCES OF VARYING VOLTAGES
AT ANODIZING PROCESS AT ALUMINUM ALLOY ADC12 TO SURFACE ROUGHNESS AND PHASE CONTENT
By:
GANJAR WIDYATMOKO
It is not a difficult thing to make all machinery components today. However but to perfect performance from a particular material, especially corrosion proof, and to beautify appearance without sacrificing its performance, a particular proper process is required to produce durable components. In improving performance, especially aluminum and its alloy, anodizing is a process to obtain the aforementioned objectives. Anodizing is a process to form oxide coating at metal by making reaction of the metal, especially the aluminum, with oxygen (O2) with electrolyte solution.
This research used aluminum alloy ADC12 as the main metal to coat and phosphate acid (H3PO4) as its electrolyte. Anodizing was applied to the main metal by using varying voltages of 9 volt, 12 volt, and 25 volt with 0.2 Ampere currency strength and 25 minutes duration of anodizing procces. Anodized metal were tested with surface roughness test and phase content coating test.
The research results showed that average higher value for surface roughness test obtained at 12 volt was 0.6756 µm and average lowest value obtained at 15 volt was 0.4044 µm. Anodizing caused phase changes at surface of aluminum alloy ADC12. Percentage of phase content produced in anodizing process at aluminum alloy by using 9 volt, 12 volt, and 15 volt during 25 minute were respectively A1 (76.868%, 71.223% and 88.03%), AlP (19.678%, 22.9746% and 11.551%) and AlN (3.454%, 5.802% and 0.419%).
PENGARUH VARIASI VOLTASE PROSES ANODISASI PADA
PADUAN ALUMINIUM ADC12 TERHADAP KEKASARAN
PERMUKAAN DAN KANDUNGAN FASA
Oleh :
GANJAR WIDYATMOKO
Skripsi
Sebagai Salah Satu Syarat untuk Mencapai Gelar
SARJANA TEKNIK
Pada
Jurusan Teknik Mesin
Fakultas Teknik Universitas Lampung
JURUSAN TEKNIK MESIN
FAKULTAS TEKNIK
UNIVERSITAS LAMPUNG
RIWAYAT HIDUP
Penulis dilahirkan di Bandar Lampung pada tanggal 5
September 1989, sebagai anak ketiga dari lima bersaudara, dari
pasangan Sutikno dan Sumiyah.
Pendidikan di Sekolah Dasar Negeri 7 Sumberejo Kemiling,
Bandar Lampung diselesaikan pada tahun 2001, Sekolah Menengah Pertama Negeri
14 Bandar Lampung diselesaikan pada tahun 2004, Sekolah Menengah Kejuruan
Negeri 2 Bandar Lampung pada tahun 2007, penulis terdaftar sebagai mahasiswa
Teknik Mesin Fakultas Teknik Universitas Lampung melalui jalur Seleksi
Penerimaan Mahasisa Baru (SPMB).
Selama kuliah penulis aktif di Himpunan Mahasiswa Teknik Mesin (Himatem)
Universitas Lampung di bidang Penelitian dan Pengembangan. Selain itu, penulis juga
pernah aktif menjadi anggota Forum Silaturahmi dan Study Islam Fakultas Teknik
(FOSSI-FT).
Penulis melakukan Kerja Praktik di PT. Great Giant Pineapple, Lampung Tengah
Bearing Pada Mesin
Scroll PT. Great Giant Pineapple Terbanggi Besar Lampung
Tengah.
Penulis mengambil konsentrasi mata kuliah pilihan pada bidang material dengan judul
skripsi “Pengaruh Variasi Voltase Proses Anodisasi Pada Paduan Aluminium ADC12
Terhadap Kekasaran Permukaan dan Kandungan Fasa ” dibawah bimbingan
Dengan Kerendahan hati
Dan
Segala usaha untuk mencapai impian
Ku persembahankan karya kecilku ini untuk
Ayahanda dan Ibunda
Ayahanda dan Ibunda
Ayahanda dan Ibunda
Ayahanda dan Ibunda
Atas segala doa, cinta dan kasih sayang yang tak
kan terbalaskan
Kakakku dan adik
Kakakku dan adik
Kakakku dan adik
Kakakku dan adik----adikku
adikku
adikku
adikku
Pemberi semangat dan nasehat
Keluarga Besar Penulis
Keluarga Besar Penulis
Keluarga Besar Penulis
Keluarga Besar Penulis
Teman
Teman
Teman
Motto
Motto
Motto
Motto ::::
”
Do n’t
Do
Do
Do
n’t
n’t
n’t be
be
be afraid
be
afraid
afraid to
afraid
to
to
to move,
move, because
move,
move,
because
because
because the
the
the
the distance
distance
distance
distance of
of
of
of 1000
1000
1000
1000
miles
miles
miles
SANWACANA
Alhamdulillahirabbil’alamin,
puji syukur kehadirat Allah SWT yang telah
memberikan rahmat dan karunia-Nya, sehingga penulis dapat menyelesaikan skripsi
ini. Shalawat serta salam juga disampaikan kepada Nabi Muhammad SAW yang akan
kita tunggu
syafa’at
nya di
yaumil akhir
nanti.
Skripsi dengan judul ”
Pengaruh Variasi Voltase Proses Anodisasi Pada Paduan
Aluminium ADC12 Terhadap Kekasaran dan Kandungan Fasa
” adalah sebagai salah
satu syarat untuk mencapai gelar Sarjana Teknik pada Jurusan Teknik Mesin
Universitas Lampung.
Sebagai rasa syukur, penulis mengucapkan terima kasih kepada:
1. Bapak Prof. Dr. Suharno, M.Sc., selaku Dekan Fakultas Teknik Universitas
Lampung;
2. Ibu Dr. Eng Shirley Savetlana, S.T., M.Met., selaku Ketua Jurusan Teknik Mesin
Universitas Lampung.
3. Harnowo Supriadi, S.T.,M.T., selaku pembimbing utama yang telah memberikan
bimbingan, pengetahuan, dan saran, serta nasehat selama proses penyelesaian
skripsi ini;
4. Bapak Gusri Akhyar, S.T,.M.T.,Ph.D., selaku pembimbing pendamping atas
kesediaanya untuk memberikan bimbingan, masukan, dan saran dalam proses
penyelesaian skripsi ini;
5. Bapak Zulhanif, S.T., M.T. selaku dosen Pembahas yang telah banyak sekali
6. Jorfri Boike Sinaga, S.T.,M.T.., selaku Pembimbing Akademik yang telah
memberikan banyak masukan dan motivasi dalam kegiatan akademik;
7. Novri Tanti, S.T, M.T., selaku Koordinator Tugas Akhir yang telah membantu
kelancaran skripsi ini;
8. Seluruh Dosen Jurusan Teknik Mesin atas ilmu yang telah diberikan selama
penulis melaksanakan studi, baik materi akademik maupun teladan dan motivasi
untuk masa yang akan datang;
9. Orang tua penulis (Bapak dan Ibu), yang telah memberikan banyak pengorbanan,
doa, kasih sayang, motivasi, semangat, harapan, materil dan spiritual, sehingga
penulis dapat merasa aman dan nyaman selama menjalani pendidikan dan
penyelesaian skripsi di Universitas Lampung;
10. Kakak dan adikku tersayang, Mba Iya, Mba Eli, Galuh dan Putra atas doa, kasih
sayang, motivasi dan dukungan selama penulis menjalani pendidikan di
Universitas Lampung;
11. Keluarga besar dan saudara-saudara penulis yang senantiasa memberikan doa,
motivasi dan dukungan;
12. Tanjung, Imem, Arif, Geni, Ponco, Sigit, Anto dan Sofie yang telah memberikan
doa, motivasi, dan dukungan selama penulis menyelesaikan pendidikan;
13. Mas Marta dan Mas Nanang yang telah membantu baik dalam proses seminar;
14. Bapak Tito Prastyo R, M. Si., yang telah membantu dalam pengambilan data di
Nanotech Indonesia.
15. Rekan–rekan Teknik Mesin angkatan 2007 yang telah memberikan semangat,
motivasi dan pandangan dalam penyelesaian skripsi ini, semoga kebersamaan ini
tetap terjaga hingga akhir hayat, salam
Solidarity Forever
;
16. Keluarga Besar Himpunan Mahasiswa Teknik Mesin Universitas Lampung;
17. Semua pihak yang tidak mungkin penulis sebutkan namanya satu persatu, yang
Penulis menyadari bahwa dalam penulisan skripsi ini masih banyak kekurangan. Oleh
sebab itu, penulis mengharapkan saran dan kritik yang bersifat membangun dari
semua pihak. Penulis berharap skripsi ini dapat bermanfaat bagi semua yang
membaca dan bagi penulis sendiri. Amiin.
Bandar Lampung, 22 Desember 2014
Penulis,
DAFTAR ISI
Halaman
ABSTRAK ... i
SANWANCANA ... iii
DAFTAR ISI ... vi
DAFTAR TABEL ... ix
DAFTAR GAMBAR ... x
I. PENDAHULUAN A. Latar Belakang ... 1
B. Tujuan Penelitian ... 3
C. Batasan Masalah ... 3
D. Hipotesa ... 3
E. Sistematika Penulisan ... 4
II. TINJAUAN PUSTAKA A. Aluminium dan Paduannya ... 5
B. Elektrolit ... 10
C. Kerapatan Arus Listrik (Current Density) ... 10
D. Anodisasi ... 11
E. Pembentukan Lapisan Oksida Aluminium ... 16
F. Uji Kekasaran Permukaan... 19
G. Pengujian Fasa ... 21
III. METODE PENELITIAN A. Metoda Penelitian ... 23
B. Variabel Penelitian ... 23
a. Variabel Bebas... 23
vii
C. Tempat dan Waktu Penelitian ... 24
D. Peralatan yang digunakan ... 24
a. Jangka Sorong ... 25
b. Amplas ... 25
c. Gelas Ukur ... 25
d. Stopwatch ... 26
e. Gergaji Besi ... 26
f. Ragum ... 26
g. Alat Pemanas ... 27
h. Instalasi Anodisasi ... 27
i. Masker Hidung ... 28
j. Sarung Tangan ... 28
k. Tang Jepit ... 28
l. Thermometer ... 29
m. SurfaceTtester... 29
n. Kamera Digital ... 29
E. Bahan yang digunakan ... 30
F. Prosedur Penelitian ... 30
a. Studi Literatur... 30
b. Persiapan Bahan dan Alat ... 30
c. Melakukan proses pre-treatment spesimen ... 33
d. Pemberian Kode Spesimen ... 34
e. Proses Anodisasi ... 35
f. Melakukan proses last treatment spesimen ... 35
g. Pengujian Fasa ... 35
h. Pengujian Kekasaran ... 35
i. Analisis Data dan Pembahasan ... 36
j. Pengambilan Kesimpulan ... 36
G. Diagram Alir Penelitian... 36
viii
B. Pembahasan... 40
a. Pengujian Kekasaran Permukaan ... 40
b. Pengujian Fasa ... 43
V. SIMPULAN DAN SARAN
A. Simpulan... 51
B. Saran ... 52
DAFTAR PUSTAKA
LAMPIRAN A
DAFTAR TABEL
Tabel Halaman
1. Daftar seri paduan aluminium tempa ... 7
2. Daftar seri paduan aluminium tuang... 8
3. Komposisi kimia aluminium ADC12-JIS ... 9
4. Tipe anodisasi berdasarkan larutan elektrolitnya ... 12
5. kekasaran permukaan paduan aluminium ADC12 9 volt ... 39
6. kekasaran permukaan paduan aluminium ADC12 12 volt ... 39
7. kekasaran permukaan paduan aluminium ADC12 15 volt ... 39
DAFTAR LAMPIRAN
Halaman LAMPIRAN A ... 54
DAFTAR GAMBAR
Gambar Halaman
1. Skema yang terjadi pada permukaan aluminium... 12
2. Skema pelaksanaan pelapisan anodisasi ... 15
3. Reaksi pembentukan lapisan oksida ... 17
4. Grafik perubahan ketebalan lapisan terhadap current density... 17
5. Mekanisme pembentukan lapisan oksida... 18
6. Alat uji Fasa... 22
7. Jangka Sorong untuk mengukur spesimen uji ... 25
8. Amplas... 25
9. Gelas ukur ... 25
10. Stopwatch ... 26
11. Gergaji besi... 26
12. Ragum ... 26
13. Alat pemanas ... 27
14. Instalasi anodisasi ... 27
15. Masker hidung ... 28
16. Sarung tangan ... 28
17. Tang jepit ... 28
18. Thermometer ... 29
19. Surface tester ... 29
20. Kamera digital ... 29
21. Spesimen paduan aluminium ADC12 ... 30
22. Instalasi alat anodisasi ... 30
23. Asam Phospat (H3PO4) ... 32
24. Dimensi Spesimen ... 34
xi
6
BAB II
TINJAUAN PUSTAKA
A. Aluminium dan paduannya
Aluminium merupakan logam non-ferrous yang paling banyak digunakan di
dunia, dengan pemakaian tahunan sekitar 24 juta ton. Aluminium dengan
densitas 2.7 g/cm3sekitar sepertiga dari densitas baja (8.83 g/cm3), tembaga (8.93
g/cm3), atau kuningan (8.53 g/cm3), mempunyai sifat yang unik, yaitu: ringan,
kuat, dan tahan terhadap korosi pada lingkungan luas termasuk udara, air
(termasuk air garam), petrokimia, dan beberapa sistem kimia.
Pemakaian aluminium dalam dunia industri yang semakin tinggi,
menyebabkan pengembangan sifat dan karakteristik aluminium terus menerus
ditingkatkan. Aluminium dalam bentuk murni memiliki kekuatan yang rendah
dan tidak cukup baik digunakan untuk aplikasi yang membutuhkan
ketahanan deformasi dan patahan, maka dari itu perlu ditambahkan unsur
lain untuk meningkatkan kekuatannya. Aluminium dalam bentuk paduan
yang sering dikenal dengan istilah aluminium alloy merupakan jenis
aluminium yang digunakan cukup besar saat ini.
7
menjadi dua kelompok utama yaitu paduan tempa (wrought) dan paduan tuang
(casting). Jenis paduan aluminium saat ini sangat banyak dan tidak menutup
kemungkinan ditemukannya lagi jenis paduan aluminium baru, oleh
karena itu dibuatlah sistem penamaan sesuai dengan komposisi dan
karakteristik paduan aluminium tersebut untuk memudahkan
pengklasifikasiannya. Salah satu penamaan paduan aluminium adalah
dengan standar AA, seperti pada Tabel 1.
Pada aluminium tempa, seri 1xxx digunakan untuk aluminium murni.
Digit kedua dari seri tersebut menunjukkan komposisi aluminium dengan limit
pengotor alamiahnya, sedangkan dua digit terakhir menunjukkan persentase
minimum dari aluminium tsb. Digit pertama pada seri 2xxx sampai 7xxx
menunjukkan kelompok paduannya berdasarkan unsur yang memiliki
persentase komposisi terbesar dalam paduan.
Tabel 1. Daftar seri paduan aluminium tempa
No. Seri Komposisi Paduan
1xxx Aluminium murni
2xxx Paduan aluminium – tembaga 3xxx Paduan aluminium – mangan 4xxx Paduan aluminium – silicon 5xxx Paduan aluminium – magnesium
6xxx Paduan aluminium - magnesium – silicon 7xxx Paduan aluminium – seng
8xxx Paduan aluminium - timah – litium
9xxx Disiapkan untuk penggunaan di masa depan
(Rahmawati, 2010)
Digit kedua menunjukkan modifikasi dari unsur paduannya, jika digit kedua
8
Jika nilainya 1 - 9, maka paduan tersebut memiliki modifikasi dengan unsur
lainnya. Dua angka terakhir untuk seri 2xxx - 8xxx tidak memiliki arti khusus,
hanya untuk membedakan paduan aluminium tersebut dalam kelompoknya.
Paduan aluminium tuang penamaannya memakai sistem tiga digit diikuti dengan
satu bilangan desimal. Tabel 2 menunjukkan seri paduan aluminium tuang
berdasarkan unsur paduannya.
Tabel 2. Daftar seri paduan aluminium tuang
No. Seri Komposisi Paduan
1xx.x Aluminium murni
2xx.x Paduan aluminium - tembaga
3xx.x Paduan aluminium - silikon – tembaga 4xx.x Paduan aluminium - silicon
5xx.x Paduan aluminium - magnesium 6xx.x Tidak digunakan
7xx.x Paduan aluminium - seng 8xx.x Paduan aluminium - timah 9xx.x Belum digunakan
( Rahmawati, 2010)
Dalam standar AA, angka pertama menunjukkan kelompok paduan. Jadi, untuk
paduan Al-Si-Cu dinyatakan dengan angka 3xx.x, angka kedua dan ketiga
menunjukkan kemurnian minimum untuk aluminium tanpa paduan dan sebagai
nomor identifikasi untuk paduan tersebut, angka keempat menandakan bentuk
produk (.0 = spesifikasi coran, .1 = spesifikasi ingot, .2 = spesifikasi ingot yang
lebih spesifik). ADC12 merupakan paduan aluminium tuang yang
mengikuti tata nama JIS (Japan Industrial Standart). Paduan
9
aluminium 384.0-F, paduan aluminium ini digunakan sebagai bahan untuk
pembuatan piston pada kendaraan bermotor. (ASM Handbook vol.15,1992).
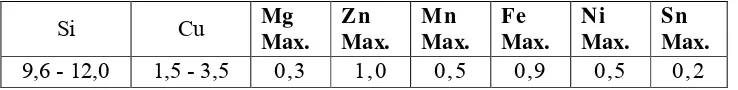
Pada Tabel 3 diperlihatkan komposisi kimia aluminium ADC12-JIS.
Dilihat dari komposisi kimianya, aluminium ADC 12 yang
digunakan pada penelitian ini termasuk paduan aluminium
hipoeutektik.
Tabel 3. Komposisi kimia aluminium ADC12-JIS
Si Cu Mg
Max. Zn Max. Mn Max. Fe Max. Ni Max. Sn Max.
9,6 - 12,0 1,5 - 3,5 0,3 1,0 0,5 0,9 0,5 0,2
(ASM Handbook vol.2, 1992).
Pelapisan aluminium merupakan suatu proses metalurgi yang banyak
melibatkan proses kimia. Pada umumnya korosi yang terjadi pada aluminium
diakibatkan oleh reaksi yang terjadi antara logam dengan oksigen. Jadi prinsip
dari pelapisan ini adalah mencegah oksigen bereaksi dengan logam.
Macam-macam cara pelapisan aluminium dapat dikelompokkan menjadi:
a). Pelapisan aluminium dengan logam lain secara listrik;
b). Pelapisan aluminium dengan logam lain tanpa listrik;
c). Pelapisan aluminium dengan bahan oksida secara listrik;
d). Pelapisan aluminium dengan bahan oksida tanpa listrik
10
B. Elektrolit
Elektrolit adalah komposisi kimia yang akan terpisah menjadi ion-ion apabila
dilarutkan dalam pelarut, hasil dari pemisahan ini berupa ion-ion yang menjadi
penghantar listrik. Fungsi dari larutan elektrolit disini adalah sebagai
penghantar arus dan penambah ion logam pelapis. Daya hantar listrik larutan
elektrolit bergantung pada jenis dan konsentrasinya. Macam-macam larutan
elektrolit diantaranya adalah larutan asam, basa dan garam. Dalam penelitian
ini elektrolit yang digunakan berupa larutan asam phospat (H3PO4).
Elektrolit asam adalah elektrolit yang bila dilarutkan dalam air akan melepas
ion (H+). Elektrolit-elektrolit asam tersebut bila dilarutkan dalam pelarut
(biasanya adalah air) maka akan terurai menjadi ion H+, contoh elektrolit asam
diantaranya adalah asam sulfat (H2SO4). Asam phospat (H3PO4) merupakan
asam triprotik, yaitu asam yang memiliki tiga ion H+ di dalam elektrolit
(Habib, 2012).
C. Kerapatan Arus Listrik (Current Density)
Arus listrik adalah pergerakan muatan-muatan listrik.. Tegangan listrik adalah
beda potensial antara kutub positif (+) dan negatif (-). Jika antara dua titik,
diberi tegangan atau dibuat beda potensial maka akan mengalir arus listrik dari
yang memiliki potensial lebih positif ke arah yang lebih negatif. Jadi intinya
11
Ada dua jenis arus dan tegangan listrik secara garis besar yaitu arus/tegangan
DC (Direct Current atau arus searah) dan arus/tegangan AC (Alternating
Currentatau arus bolak-balik). Arus DC mengalir dari positif ke negatif secara
kontinu (tetap). Sedangkan arus AC mengalir secara bolak-balik dari positif ke
negatif dan sebaliknya dengan frekuensi tertentu, maka pada tegangan AC
tidak ada kutub positif dan negatif karena polaritasnya terus berubah dalam
frekuensi tertentu. Daya dalam fisika adalah laju energi yang dihantarkan atau
kerja yang dilakukan per satuan waktu. Satuan arus listrik adalah Ampere.
Current densityatau kerapatan arus adalah arus yang mengalir per satuan luas
permukaan. Satuan current densityadalah A/dm2. Dengan rumus berikut :
CD = A i
(2.1)
keterangan : CD = current density(A/dm2)
i = arus yang mengalir (A)
A= luas permukaan spesimen (dm2) (Habib, 2012).
D. Anodisasi
Proses anodisasi adalah proses pembentukan lapisan oksida pada logam
dengan cara bereaksikan atau mengkorosikan suatu logam terutama
aluminium dengan oksigen (O2) yang diambil dari larutan elektrolit yang
digunakan sebagai media, sehingga terbentuk lapisan oksida. Proses ini juga
disebut sebagai anodic oxidation yang prinsipnya hampir sama dengan proses
pelapisan dengan cara listrik (elektroplating), tetapi bedanya logam yang akan
12
larutan elektrolit yang digunakan bersifat asam dengan penyearah arus bertipe
(DC) dan ampere tinggi. Proses utama, dalam oksidasi anoda alumunium
memerlukan larutan elektrolit.
Tebal lapisan yang teroksidasi
a. Permukaan alumunium sebelum proses oksidasi anoda
t tebal lapisan
b. Permukaan anodisasi alumunium yang menunjukkan lapisan oksida
t Oksida 2 kali
Gambar 1. Skema yang terjadi pada permukaan aluminium
(Newman, Ron, 2008)
Selama proses oksidasi anoda permukaan alumunium dirubah menjadi oksida
alumunium. Dimana reaksi kimia yang terjadi adalah:
4Al + 3O2 2Al2O3 (2.2)
Tipe anodisasi berdasarkan jenis larutan elektrolit yang digunakan
diperlihatkan pada tabel berikut ini :
Tabel 4. Tipe anodisasi berdasarkan larutan elektrolitnya
Electrolyte composition Curre nt densit y (A/d
m2)
Volta ge (V DC) Temp e rature
(0C)
Treat ment time (min) Film thick ness ( m) Application Bengough
Stuart (Chromic 0,1 - 0 – 40 40 – 2 –
13
acid) Process CrO3: 2,5-3,0%
0,5 40 60 15 organic coating
Phosphoric acid Process H3PO4: 10 - 12%
0,3 -1,8 10 – 20 15 – 30 15 – 30
2 – 5
Pre-treatment prior to adhesive bond, Accelarated Chromic acid Process
CrO3: 5 - 10 %
0,15 -0,3
0 – 40
35 20 – 30
2 – 3
For protection
Sulphuric acid Process
H2SO4: 10-20% 1,0 -2,0 10 – 20 20 – 30 10 – 30 5 – 35 For protection, Good base for dyes.
Oxalic acid Process (COOH)2: 3-10% 1,0 – 3,0 40 – 65 20 – 35 30 – 60 10 – 65 Protective and decorative Boric acid Process H3BO3: 9 -15% 1,0 – 3,0 50– 500 0 – 95 20 – 60 0,25 -7,5 Thin dielectric film for electrolytic condensers Hard Anodize Mixed electrolyte H2SO4: 10 -20% (COOH)2: 0,5-1%
3,0 – 4,0
20 – 90
-5 – 5 20 – 80
40 – 80
Hard and thick abrasion resistant coating
E-matal Process (COOH)2+ Ti or Zr or Ti salt
0,2 – 0,3
120 50 – 70 20 – 60 10 – 20 Protective and decorative for non metallic appearance Micro-Arc Oxidation (alkali- silicate electrolyte) 0,2 – 0,3 A/sq. cm 1000 – 1100 AC 30 – 35 25 – 30 45 – 50
Wear & corrosion resistance, Insulation
(Juhl, 2005).
Salah satu proses anodisasi pada paduan aluminium yang cukup dikenal adalah
Phosphoric Acid Anodizing (PAA) atau anodisasi asam phospat. Pada
umumnya, yang perlu dikontrol saat proses anodisasi berlangsung adalah :
a). Tingkat konsentrasi dari larutan asam phospat yaitu 10 -12%.
14
c). Lamanya pencelupan material pada proses PAA yaitu 15 - 30 menit.
Anodisasi asam phospat atau PAA adalah suatu proses yang cairan
elektrolitnya menggunakan larutan asam phospat (H3PO4). Sebagai katoda
(kutub negatif) digunakan tembaga atau aluminium murni. Sedangkan anoda
(kutub positif) yaitu spesimen itu sendiri. Tahapan reaksi kimia yang terjadi
pada saat proses anodisasi adalah :
H3PO4+ 3H2O 3H3O++ PO43- (2.3)
Pada katoda terjadi : 2e + 2H3O+ 2H2O + H2 (g) (2.4)
Pada anoda terjadi : Al + 6H2O 4H3O++ O2+ Al3++ 7e (2.5)
Dari Reaksi (2.4) dan (2.5) setelah diselesaikan, maka didapatkan :
2Al + 6H3O+ 2Al3++ 6H2O3 + 3H2 (2.6)
Seterusnya,
Al3++ PO43- Al PO4(Kristal alumina) (2.7)
Dan
4Al + 3PO2 2 Al2PO3 (lapisan oksida alumina) (2.8)
Peralatan utama pada proses anodisasi sama seperti yang digunakan pada
proses lapis secara listrik yaitu penyearah arus (rectifier), elektroda non katoda
dan anoda, rak serta bak. Pada proses anodisasi tidak menggunakan sistem
barrel dan alat pemanas, tetapi menggunakan alat pendingin (thermostat).
Fungsi dari alat-alat tersebut hampir sama yang digunakan pada proses lapis
15
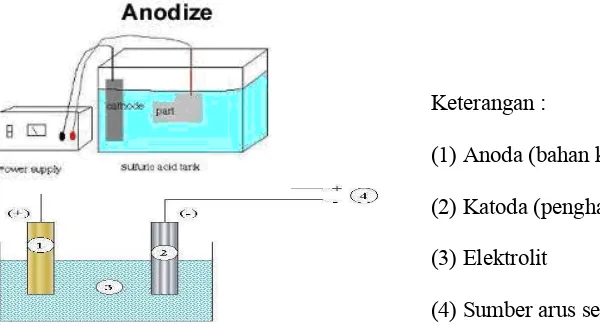
Keterangan :
(1) Anoda (bahan kerja)
(2) Katoda (penghantar)
(3) Elektrolit
[image:32.612.171.471.87.250.2](4) Sumber arus searah
Gambar 2. Skema pelaksanaan pelapisan anodisasi.
(BPPT, 1998).
Pemakaian arus searah akan menghasilkan lapisan yang lebih keras dan tahan
korosi, tetapi lebih bersifat rapuh (brittle). Sifat ketahanan korosi tergantung
pula pada proses pengerjaan akhir terutama pada proses sealing. Proses
pengerjaan akhir lainnya adalah proses pewarnaan. Proses pengerjaan
pewarnaan ini meliputi pewarnaan langsung (integral coloring) dan
pewarnaan dengan bahan pewarnaan organik atau anorganik.
Pewarnaan langsung adalah proses pewarnaan yang langsung terjadi pada saat
proses anodisasi tanpa menambah/mengggunakan bahan pewarna. Hampir
semua alumunium dan paduannya dapat dioksidasi anoda dan diwarnai
sesuai dengan yang diinginkan. Jenis anodik porous dapat diwarnai dengan
obat organik, pigmen anorganik tertentu dan secara lapis listrik pula.
16
E. Pembentukan Lapisan Oksida Aluminium
Jika arus searah mulai dijalankan pada sel anodisasi seperti pada gambar 2.5.1
dengan larutan elektrolit asam phospat maka katoda akan bermuatan negatif
dan anoda akan bermuatan positif. Asam phospat akan terurai menjadi kation
H+ dan ion PO42-. Kation – kation H+akan bergerak menuju katoda dan di sisi
lain akan dinetralkan oleh elektron – elektron katoda sehingga akan terbentuk
gas H2.
6H+ + 6e ־ → 3H2(g) (2.9)
Al pada anoda akan terurai menjadi ion Al3+dan bergerak ke katoda.
2Al → 2Al3++ 6e- (2.10)
Karena ion positif Al3+tidak tereduksi pada katoda, maka reaksi yang terjadi :
3H2O + 3e-→ 3OH-+ 3/2H2 (g) (2.11)
Demikian juga pada ion PO42-tidak teroksidasi pada anoda, reaksi diganti oleh :
3H2O → 6H++ 3O2- (2.12)
Pada permukaan anoda (antara logam dan lapisan barier) gambar 3, terjadi
reaksi antara ion Al3+ dengan oksida atau hidroksida untuk menghasilkan
aluminium oksida (ion hidrogen akan terlepas menuju larutan dan membentuk
gas H2).
2 Al3++ 3O2 ־→ Al2O3 (2.13)
2 Al3++ 3OH ־→ Al2O3+ 3H+ (2.14)
Sehingga didapatkan reaksi keseluruhan:
Ketebalan lapisan oksida
oleh berbagai faktor, antara
proses anodisasi dan lain
current density (rapat
secara teori peningkatan
kenyataannya peningkatan
dipengaruhi oleh adanya
[image:34.612.203.450.301.442.2]pemakaiancurrent density
Gambar 3. Reaksi
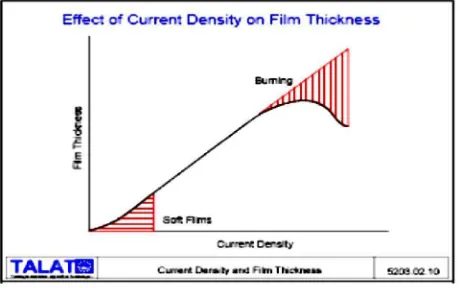
Gambar 4. Grafik p
lapisan oksida yang dihasilkan dari proses anodisasi, dipengaruhi
faktor, antara lain jenis larutan elektrolit, current density
dan lain – lain. Pada gambar 4 dijelaskan tentang
(rapat arus) terhadap pertumbuhan lapisan oksida
peningkatan ketebalan akan terjadi secara konstan sedangkan
peningkatan ketebalan akan semakin berkurang,
oleh adanya peluruhan local Joule’s heating yang disebabkan
current densityyang terlalu besar.
Reaksi pembentukan lapisan oksida (Juhl, 2005).
perubahan ketebalan lapisan terhadap current density
17
, dipengaruhi
density, durasi
tentang pengaruh
oksida dimana
sedangkan pada
berkurang, hal ini
yang disebabkan
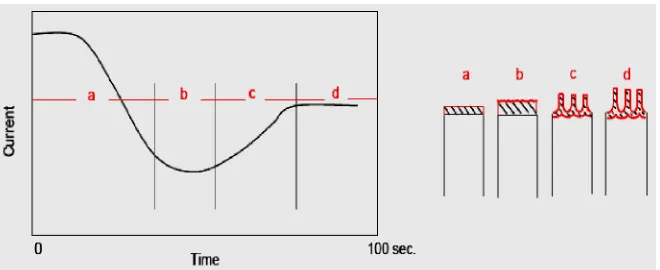
[image:34.612.207.437.529.673.2]Gambar 5. Mekani
Lapisan oksida yang terbentuk
asam phospat akan menghasilkan
Pada mulanya arus yang
melewati logam aluminium.
non porous layer yang
pada permukaan aluminium
daripada aluminium sendiri (pe
lebih tebal oleh karena
arus terus menurun (periode
berdasar pada lapisan
Aliran arus akan lebih
menyebabkan temperatur
daerah ini. Peluruhan
semakin tipis, ini menyebabkan
menyebabkan arus akan
. Mekanisme pembentukan lapisan oksida (Juhl, 2005
yang terbentuk pada hasil anodisasi dengan larutan
akan menghasilkan lapisan yang berpori seperti pada gambar
arus yang melewati elektroda aluminium tinggi karena
m aluminium. Kemudian arus mulai menurun karena barrier
yang rapat dan tipis terbentuk. Lapisan oksida yang terbentuk
permukaan aluminium ini mempunyai hambatan yang lebih
luminium sendiri (periode a). Lapisan oksida yang terbentuk
karena itu hambatan menjadi lebih tinggi yang menyebabkan
menurun (periode b). Kecenderungan kurva keatas pada periode
lapisan oksida yang terbentuk akan kasar pada barier
akan lebih terkonsentrasi pada permukaan yang lebih tipis,
temperatur elektrolit meningkat sehingga terjadi peluruhan
Peluruhan akan terus terjadi yang menyebabkan lapisan
ini menyebabkan resistansi didaerah ini lebih kecil
arus akan meningkat (periode c). Pada tahap ini pembentukan 18
Juhl, 2005).
larutan elektrolit
pada gambar 5.
tinggi karena hanya
barrieratau
oksida yang terbentuk
yang lebih tinggi
rbentuk menjadi
yang menyebabkan
pada periode b
barier layer.
lebih tipis, yang
peluruhan pada
menyebabkan lapisan yang
lebih kecil yang
19
lapisan porousoksida mulai terbentuk dan arus akan stabil, dimana kecepatan
pembentukan dan peluruhan tetap atau stabil (periode d).
Proses peluruhan terjadi karena pemberian energi yang terlalu besar melebihi
energi ikatan Al-O pada Al2O3. Reaksi peluruhan yang terjadi adalah sebagai
berikut:
Al2O3+ 6H+→ 2 Al3+(aq)+ 3H2O (2.16)
Peluruhan yang terjadi ada dua, yaitu peluruhan secara kimia (chemical
dissolution) dan peluruhan karena medan listrik yang terlalu besar dan
terkonsentrasi (field-assisted dissolution). Peluruhan secara kimia karena
tingkat keasaman dari elektrolit. Peluruhan karena medan listrik yang
terkonsentrasi pada barrier layer menyebabkan kenaikan temperatur pada
ketebalan lapisan yang lebih tipis sehingga memicu proses peluruhan, ini
disebut local Joule’s heating. Peluruhan karena medan listrik sangat besar,
yaitu sekitar 300 nm lapisan oksida yang luruh setiap satu menit dan peluruhan
secara kimia lebih lambat, yaitu sekitar 0,1 nm lapisan oksida yang luruh setiap
satu menit.
F. Uji kekasaran Permukaan
Kekasaran Permukaan (Surface Roughness) secara umum dapat dijelaskan
dengan 2 metode: Arithmetic mean value(R), biasanya dilambangkan dengan
AA (Arithmetic Average) atau CLA (Center-Line Average) Root mean square
average (Rq), biasanya disingkat dengan RMS. Satuan yang biasanya
20
atau µin (microinch) dimana 1 µm = 40 µin dan 1 µin = 0.025 µm. Parameter
yang digunakan pada pengukuran kekasaran adalah,
a). Ra (roughness average of the R-curve) : nilai rata-rata aritmatika dari
pengukuran kekasaran permukaan untuk panjang tertentu.
b). Rz (ten points high of irregularities) : pengukuran berdasarkan nilai
rata-rata lima puncak tertinggi dah lima lembah terendah.
c). Rmax (maksimum height of the profile) : jarak antara puncak tertinggi
dengan lembah terendah.
d). Rq : nilai akhir rata-rata kuadrat dari pengukuran kekasaran permukaan
untuk panjang tertentu.
Untuk harga kekasaran Ra di atas 5.0 µm, misalnya permukaan yang
dikerjakan dengan sekrap, perlu diperiksa dengan peralatan yang lebih cocok
karena keterbatasan dari penggunaan peralatan stylus. Salah satu peralatan ukur
yang dikembangkan untuk maksud di atas adalah alat ukur kedalaman kekasaran
(Dial Dept Gauge). Keuntungan dari alat ini adalah dapat dilakukan pengukuran
secara cepat tanpa harus membuat grafik kekasaran permukaan terlebih dulu.
Bentuk pengukur kedalaman kekasaran ini hampir sama dengan
jam ukur, namun perabanya diganti dengan sebuah silinder dari baja atau
diamond yang berfungsi sebagai stylus. Pada bagian stylus ini dilengkapi
dengan dua atau tiga penyentuh data (datum attachment) yang bisa diatur
untuk permukaan yang rata atau bulat.
21
stylus menyentuh alur kekasaran. Kemudian kaki dari datum attachment
ditekankan ke permukaan. Dari sini baru dibaca skala ukurnya. Cara ini
diulang-ulang tiga sampai lima kali, kemudian harga pemeriksaannya di
rata-ratakan. Harga rata-rata ini adalah sama dengan Rz. Harga pembacaan tertinggi
adalah harga Rt.
Bagian dari alat pengukur kekasaran (surface tester) adalah : dial indicator ,
meja datar, skala tekanan, batang gerak, serta display yang terintegrasi yang
dihubungkan dengan printer. Alat ini berfungsi untuk mengukur dan mencatat
kekasaran permukaan suatu benda dengan tingkat ketelitian 0.02 µm. alat ini
sering menggunakan sebuah stylus berbentuk diamond untuk bergerak
sepanjang garis lurus pada permukaan sebagai dial indicator pengukur
kekasaran permukaan benda uji.
(Andriansyah. 2013)
G. Pengujian Fasa
Pengujian Fasa dilakukan untuk mengetahui unsur atau campuran yang
terbentuk pada suatu material dmana pada pengujian kali ini dilakukan pada
material paduan aluminium ADC12.
Jika material dikenai sinar-x, maka intensitas sinar yang ditransmisikan lebih
rendah dari intensitas sinar datang. Hal ini disebabkan adanya penyerapan oleh
material dan juga penghamburan oleh atom-atom dalam material tersebut.
Metode XRD berdasarkan sifar difraksi sinar, yakni hamburan cahaya dengan
22
Gambar 6. Alat uji Fasa (Mahayatra, 2012)
Data yang diperoleh dari metode karakterisasi XRD adalah sudut hamburan
(sudut Bragg) dan intensitas. Berdasarkan teori difraksi, sudut difraksi
bergantung kepada lebar celah kisi sehingga mempengaruhi pola difraksi,
sedangkan intensitas cahaya difraksi bergantung dari berapa banyak kisi Kristal
yang memeliliki orientasi yang sama. Dengan menggunakan metode ini dapat
ditentukan sistem kristal, parameter kisi, derajat kristalinitas dan fase yang
tedapat dalam suatu sampel.
BAB III
METODOLOGI PENELITIAN
A. Metoda Penelitian
Metoda penelitian yang digunakan dalam penelitian ini adalah metoda
penelitian eksperimental nyata (true experimental research). Dalam hal ini
penelitian bertujuan untuk mengetahui pengaruh variasi tegangan listrik
terhadap kekasaran permukaan dan kandungan fasa pada paduan aluminium
ADC12 hasil anodisasi.
Data dan informasi pendukung diperoleh dari kajian buku, artikel dan jurnal
yang diperoleh dari perpustakaan dan internet untuk menambah informasi yang
diperlukan.
B. Variabel Penelitian
Dalam penelitian ini variabel-variabel yang digunakan adalah sebagai berikut:
a). Variabel Bebas
Variabel bebas adalah variabel yang besarnya ditentukan oleh peneliti dan
ditetapkan sebelum melakukan penelitian. Besarnya variabel ini dapat
24
variabel terikatnya. Dalam penelitian ini, variabel bebas yang digunakan
adalah tegangan listrik pada proses anodisasi paduan aluminium ADC12.
Untuk variabel bebas, tegangan listrik yang digunakan adalah : 9 volt, 12
volt, dan 15 volt.
b). Variabel Terikat
Variabel terikat adalah variabel yang besarnya tergantung pada variabel
bebas dan diketahui setelah penelitian itu dilakukan. Besar variabel terikat
dapat berubah-ubah sesuai dengan variabel bebas jika terdapat hubungan
antara keduanya. Dalam penelitian ini, variabel terikatnya adalah
kekasaran permukaan dan kandungan fasa.
C. Tempat dan Waktu Penelitian
Penelitian dilakukan dalam rentang waktu bulan Oktober - Desember 2013 di
Laboratorium Produksi Teknik Mesin Universitas Lampung untuk melakukan
proses anodisasi serta pengujian kekasaran lapisan aluminium dan di Nanotech
Indonesia untuk melakukan pengujian fasa .
D. Peralatan yang Digunakan
25
[image:42.612.265.445.103.224.2]a). Jangka sorong
Gambar 7. Jangka Sorong untuk mengukur spesimen uji
[image:42.612.264.396.287.428.2]b). Amplas
Gambar 8. Amplas untuk menghaluskan dan menghilangkan lapisan oksida
pada permukaan paduan aluminium ADC12.
c). Gelas ukur
[image:42.612.268.392.544.679.2]26
[image:43.612.246.416.103.234.2]d.) Stopwatch
Gambar 10. Stopwatch untuk menghitung waktu pencelupan pada proses
anodisasi.
[image:43.612.234.426.324.467.2]e). Gergaji besi
Gambar 11. Gergaji besi untuk memotong benda kerja.
f). Ragum
[image:43.612.257.402.531.670.2]27
[image:44.612.240.421.105.243.2]g). Alat pemanas
Gambar 13. Alat pemanas untuk memanaskan benda kerja setelah dilakukan
anodisasi.
h). Instalasi anodisasi
Gambar 14. Instalasi anodisasi untuk melakukan proses anodisasi pada
[image:44.612.213.448.333.510.2]28
[image:45.612.219.440.106.227.2]i). Masker hidung
Gambar 15. Masker hidung digunakan untuk mencegah zat kimia masuk
kedalam sistem pernapasan.
[image:45.612.233.428.318.464.2]j). Sarung tangan
Gambar 16. Sarung tangan untuk melindungi kulit tangan dari reaksi zat kimia.
k). Tang jepit
[image:45.612.230.428.527.678.2]29
[image:46.612.201.460.104.233.2]l). Thermometer
Gambar 18. Thermometer untuk mengukur suhu pada proses pre-treatment
dan last-treatment.
[image:46.612.233.427.323.465.2]m). Surface Tester
Gambar 19. Surface testeruntuk menguji kekasaran permukaan specimen yang
telah dianodisasi.
n). Kamera digital
\
[image:46.612.218.424.557.680.2]30
E. Bahan yang Digunakan
[image:47.612.222.436.156.315.2]Spesimen yang digunakan adalah paduan aluminium ADC12.
Gambar 21. Spesimen paduan aluminium ADC12.
F. Prosedur Penelitian
Dalam penelitian ini terdapat beberapa langkah-langkah yang dilakukan untuk
mendapatkan data-data yang diperlukan, yaitu:
a). Studi literatur
b). Persiapan bahan dan alat
1. Persiapan alat anodisasi
[image:47.612.221.420.509.660.2]31
Mengingat bahwa yang akan dianodisasi adalah spesimen berukuran
kecil, maka peralatan yang digunakan dalam penelitian ini adalah
bersifat miniatur. Alat untuk proses anodisasi asam phospat (PAA)
berskala mini menggunakan Power supplay yang sesuai dengan
spesimen uji yang digunakan, dengan katodanya menggunakan
aluminium murni. Untuk mendapatkan kuat arus power supplay yang
sesuai dengan spesimen uji dapat ditentukan dengan menggunakan
persamaan 2.1 yaitu :
CD =
A i
Pada penelitian ini, elektrolit yang digunakan yaitu asam phospat
(H3PO4), maka nilai Current Density(CD) yang sesuai adalah 1,8 A/dm2
(lihat pada tabel 2.4.1). Dan untuk luas permukaan spesimen yang
dianodisasi yaitu 0,1 dm2(lihat pada gambar 3.6.1).
Maka, arus yang sesuai untuk digunakan pada penelitian ini yaitu :
i= A . CD
i = 0,1 dm2. 1,8 A/dm2 = 0,18 Ampere
Untuk mendapatkan power supplaydengan kuat arus 0,18 Ampere cukup
sulit, maka dalam penelitian ini kuat arus power supplayyang digunakan
yaitu 0,2 Ampere, hal ini diharapkan tidak akan mengurangi makna dan
32
Alat ini dikhususkan untuk proses anodisasi asam phospat pada spesimen
dari bahan paduan aluminium ADC12 bentuk sheet. Maka bentuk dan
ukuran dari bak elektrolisis digunakan ukuran yang kecil. Hal ini
semata-mata hanya untuk menghemat cairan dari larutan H3PO4dan lebih
praktis.
[image:49.612.265.374.236.374.2]2. Persiapan elektrolit
Gambar 23. Asam Phospat (H3PO4)
Sebagai cairan elektrolit untuk proses anodasi dalam penelitian ini adalah
larutan asam phospat (H3PO4) yang berkonsentrasi (berkepekatan) 10 %
-12 %. Larutan H3PO4 yang dibeli memiliki konsentrasi yang tinggi yaitu
85 %, dengan menggunakan tabel phosphoric acid diketahui berat
jenisnya yaitu 1,690 gr/ml, yang artinya H3PO4 (85%) =
(85/100).(1,690)(1000) = 1436 gr/liter.
Dari tabel phosphoric acid untuk konsentrasi 10 % harus mempunyai
berat jenis 1,0532 gr/ml, artinya H3PO4 (10%) = (10/100).(1,0532)(1000) =
105,3 gr/liter.
33
1 liter H3PO4 (85%) = (1436/105,3) liter H3PO4 (10%)
= 13,6372 liter H3PO4 (10%)
Jika dikehendaki membuat 1 liter H3PO4 (10%)maka diperlukan :
(1/13,6372) liter H3PO4 (85%)= 0,073329 liter H3PO4 (85%)
= 73,329 ml H3PO4 (85%)
Dengan demikian, tahapan pelaksanaan persiapan elektrolit untuk
keperluan penelitian ini adalah menakar H3PO4 (85%)menggunakan gelas
ukur sebanyak 73,329 ml kemudian ditambah aquades hingga 1 liter
sambil diaduk hingga cairan merata homogen.
c). Melakukan proses pre-treatment spesimen
Langkah-langkah proses pre-treatmentspesimen anodisasi pada penelitian
ini adalah sebagai berikut:
1. Degreasing
Degreasing dilakukan untuk menghilangkan oli atau lemak yang
terdapat pada permukaan aluminium sebelum proses anodisasi.
Pembersihan dilakukan dengan cara direndam kedalam larutan asam
sulfat dengan temperatur antara 400C sampai dengan 700C selama 5 - 15
menit.
34
Etching dilakukan untuk memperhalus permukaan dan menghilangkan
lapisan film oksida aluminium yang terbentuk secara alami pada
permukaan aluminium yang akan dianodisasi. Etchingdilakukan dengan
cara merendam aluminium kedalam larutan soda api dengan temperatur
600C – 750C selama 15 menit.
3. Desmutting
Desmutting adalah proses pembersihan bercak hitam akibat dari proses
etching. Dilakukan dengan cara merendam benda kerja pada larutan
asam nitrat dengan temperatur 250C – 350C selama 10 menit.
Adapun bentuk atau dimensi spesimen yang dibutuhkan dalam penelitian
ini dapat dilihat pada gambar 24 berikut:
Lubang tempat pengait
Ketika proses anodisasi dilakukan
25 mm
3 mm
[image:51.612.202.490.450.598.2]40 mm
Gambar 24. Dimensi spesimen
35
e). Proses anodisasi
Langkah-langkah proses anodisasi pada penelitian ini adalah sebagai
berikut:
1. Persiapan instrumen anodisasi
2. Persiapan larutan elektrolit.
3. Penuangan larutan elektrolit ke dalam bak anodisasi.
4. Melakukan proses anodisasi selama 25 menit.
5. Setelah 25 menit, aluminium diangkat dan dibilas dengan air, untuk
membersihkan sisa-sisa elektrolit.
f). Melakukan proses last treatment spesimen.
Sealing adalah proses yang diperlukan agar pori yang terbentuk di
permukaan menutup. Dilakukan dengan cara merendam benda kerja yang
telah dianodisasi kedalam air mendidih dengan suhu > 90 0 C selama 10
menit.
g). Pengujian fasa permukaan paduan aluminium ADC12 hasil anodisasi
1. Persiapan peralatan pengujian mikroskop metalurgi
2. Melakukan uji fasa
3. Melakukan pengambilan data pada mikroskop metalurgi
4. Pengolahan data hasil penelitian, dimana nantinya data - data hasil
penelitian tersebut akan dimasukkan kedalam tabel untuk selanjutnya
dianalisa.
h). Pengujian kekasaran permukaan paduan aluminium ADC12 hasil anodisasi
1. Persiapan peralatan pengujian kekasaran permukaan
36
3. Pengolahan data hasil penelitian, dimana nantinya data - data hasil
penelitian tersebut akan dimasukkan kedalam tabel untuk selanjutnya
dianalisa.
i). Analisis data dan pembahasan.
j). Pengambilan kesimpulan.
G. Diagram Alir Penelitian
Diagram alir penelitian pada gambar 25 untuk variasi tegangan listrik 9 volt,
37
Gambar 25. Diagram alir penelitian.
Mulai
Pre-treatment
Proses anodisasi selama 25 menit dengan variasi tegangan listrik 9 volt, 12 volt dan 15 volt Pemberian kode spesimen
Studi Literatur
Persiapan Alat dan Bahan
Last treatment
Tidak Benda Hasil
Anodisasi Baik
Pengujian kekasaran
permukaan dan kandungan
Pengolahan data
Analisa dan pembahasan
Kesimpulan
51
BAB V
KESIMPULAN DAN SARAN
A. Kesimpulan
Dari penelitian dan pembahasan data hasil penelitian yang telah dilakukan,
maka dapat diambil kesimpulan sebagai berikut :
a). Nilai kekasaran rata-rata yang dihasilkan dalam proses anodisasi paduan
aluminium yang menggunakan tegangan masing-masing 9 volt, 12 volt
dan 15 volt yang dianodisasi selama 25 menit yaitu 0.6038 µm, 0.6756 µm
dan 0.4044 µm. Variasi tegangan yang digunakan pada proses anodisasi
mempengaruhi kecepatan peluruhan dan pembentukan lapisan pada
permukaan paduan aluminium ADC12 yang menyebabkan terjadinya
perbedaan nilai kekasaran pada permukaan paduan aluminium ADC12.
b). Anodisasi menyebabkan terjadinya perubahan fasa pada permukaan
paduan aluminium ADC12. Persentase kandungan fasa yang dihasilkan
dalam proses anodisasi paduan aluminium yang menggunakan tegangan
masing-masing 9 volt, 12 volt dan 15 volt yang dianodisasi selama 25
menit yaitu Al (76,868 %, 71,223 % dan 88,03 %), AlP (19,678 %,
22,9746 % dan 11,551 %) dan AlN (3,454 %, 5,802 % dan 0,419 %).
52
terjadi pada permukaan paduan aluminium ADC12 terhadap asam phospat
selama proses anodisasi berlangsung.
B. Saran
Saran yang dapat diberikan dari penelitian ini adalah sebagai berikut:
a). Pada penelitian selanjutnya diharapkan lebih dicermati metode yang
digunakan, pencampuran zat kimia dan pengamplasan spesimen untuk
mencegah terjadinya perubahan struktur pada lapisan aluminium.
b). Perlu dilakukan penelitian yang lebih bervariasi terhadap sifat mekanik
lainnya seperti uji kekerasan dan uji korosi.
c). Pada penelitian selanjutnya perlu ditinjau mengenai pengaruh kuat arus dan
waktu proses yang digunakan dalam proses anodisasi.
d). Diperlukan jumlah spesimen yang lebih banyak dalam proses penelitian
untuk mendapatkan hasil yang lebih akurat.
e). Perlu dilakukan penelitian mengenai pengaruh zat kimia pada proses
DAFTAR PUSTAKA
Anominus. Anodizing. www. blog.ub.ac.id/habib2010/files/2012/05/Anodising.doc Diakses
tanggal 1 September 2013
BPPT. 1998.Teknologi Pelapisan Logam Secara Listrik. Program Penerapan IPTEK di
Daerah: Jakarta.
Hartono, J. Anton dan Tomijiro Kaneko. 1992. Mengenal Pelapisan Logam (Elektroplating).
Andi Offset: Yogyakarta.
Juhl, J . 2005. Pulse Anodizing in an Existing Anodizing Line.Http://www.aluconsult.dk/
artikler /pulse_anodizing_in_an_existing_anodizing_line.Pdf. Diakses tanggal 5 September 2013
Kirk-Othmer. Encyclopedia Of Chemical Technology Vol.19 http://stronyinternetowe.home.
pl/autoinstalator/wordpress4/wp-content/uploads/2013/06/book_8592.zip. Diakses
tanggal 10 September 2013
Newman, Ron. Anodizing Aluminum. http://www.focuser.com/atm/anodize/anodize.html.