PENAP
FAKUL
PISAN RIZ
PEMACU
DAN A
LTAS MAT
IN
ZOBAKT
U TUMBU
APLIKASI
AI
DEPART
TEMATIKA
NSTITUT P
TERIA TO
UH TANA
INYA DI R
I KARWAT
TEMEN BIO
A DAN ILM
PERTANIA
BOGOR
2012
OLERAN K
AMAN KE
RUMAH K
TI
OLOGI
MU PENGET
AN BOGOR
KEKERIN
EDELAI
KACA
TAHUAN A
R
NGAN
PENAPISAN RIZOBAKTERIA TOLERAN KEKERINGAN
PEMACU TUMBUH TANAMAN KEDELAI
DAN APLIKASINYA DI RUMAH KACA
AI KARWATI
Skripsi
sebagai salah satu syarat untuk meraih gelar Sarjana Sains
pada Departemen Biologi
DEPARTEMEN BIOLOGI
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM
ISTITUT PERTANIAN BOGOR
BOGOR
Judul : Penapisan Rizobakteria Toleran Kekeringan Pemacu Tumbuh Tanaman
Kedelai dan Aplikasinya di Rumah Kaca
Nama : Ai Karwati
NIM : G34080062
Disetujui
Prof. Dr. Aris Tri Wahyudi, M.Si.
Dr. Edi Husen, M.Sc.
Pembimbing I
Pembimbing II
Diketahui
Dr. Ir. Ence Darmo Jaya Supena, M.Si
Ketua Departemen Biologi
ABSTRAK
AI KARWATI. Penapisan Rizobakteria Toleran Kekeringan Pemacu Tumbuh Tanaman Kedelai dan Aplikasinya di Rumah Kaca. Dibimbing oleh ARIS TRI WAHYUDI dan EDI HUSEN.
Kondisi cekaman kekeringan dapat menurunkan produkivitas tanaman pertanian. Oleh karena itu diperlukan strategi-strategi untuk memacu pertumbuhan tanaman sehingga tanaman dapat tumbuh baik dalam kondisi tercekam kekeringan, salah satu caranya dengan memanfaatkan
Plant Growth Promoting Bacteria (PGPR). Tujuan penelitian ini adalah menapis rizobakteria yang mampu mengendalikan cekaman kekeringan dan mengaplikasikannya pada tanaman kedelai di rumah kaca. Sebanyak 27 rizobakteria yang terdiri atas 14 Pseudomonas sp. (Crb), 11 Bacillus sp. (Cr), dan 2 Bradyrhizobium japonicum. (Bj)ditapis pada kondisi kekeringan menggunakan media yang ditambahkan dengan Polietilen Glikol (PEG) 6000 kemudian produksi eksopolisakarida diuji secara kuantitatif. Bakteri terpilih diuji antagonis satu sama lain sebelum dikombinasikan dalam satu paket formula di dalam gambut. Bakteri ditumbuhkan pada media alternatif susu skim dan molase kemudian diinokulasikan ke dalam 50 g gambut. Formula digunakan untuk uji viabilitas dan uji efektivitas tanaman kedelai pada kondisi cekaman kekeringan di rumah kaca. Sebanyak 17 bakteri berhasil ditapis dan mampu tumbuh pada media bertekanan osmotik rendah (-2 Mpa) dan menghasilkan eksopolisakarida berkisar 1.7-8.0 mg/ml. Berdasarkan produksi eksopolisakarida dan sifat tidak antagonis diperoleh lima paket formula. Viabilitas kelima formula masih stabil sampai masa penyimpanan tiga bulan. Aplikasi lima pada tanaman kedelai, satu formula yaitu F4 memberikan pengaruh yang nyata terhadap tinggi tanaman, berat basah tajuk, berat basah akar dan berat kering akar baik pada kondisi basah maupun kering.
Kata kunci: Rizobakteria, kekeringan, Bacillus, Pseudomonas, Bradyrhizobium japonicum, formulasi, pemacu pertumbuhan, kedelai.
ABSTRACT
AI KARWATI. Screening of Drought Tolerant Rizobacteria to Enhance Soybean Plant Growth and its Aplication in Greenhouse. Under direction of ARIS TRI WAHYUDI and EDI HUSEN.
Drought stress can reduce the productivity of crops. Therefore, strategies to promote growth of plants that can grow well in drought conditions is required. One of the way is by using the plant growth promoting rhizobacteria (PGPR). The aim of this study was to screen rhizobacteria in drought stress and apply them on soybean in greenhouse. A total of 27 rhizobacteria consisted of 14 Pseudomonas sp. (Crb), 11 Bacillus sp. (Cr), and 2 Bradyrhizobium japonicum. (Bj) was screened on drought conditions using media supplemented with Polythylene Glycol (PEG) 6000 then quantitatively tested for exopolysaccharide product. Selected bacteria were tested for antagonistic assay tested before combining them in a package formula in the peat. Bacteria were grown in media skim milk and molasses then inoculated into 50 g of peat soil. The formula were tested for the viability and effectiveness on soybeans in green house. Total of 17 bacteria were successfully screened and all grow well at low osmotic potential (-2 Mpa) medium and produced exopolysaccharide ranging 1.7-8.0 mg/ml. Based on the exopolysaccharide produced and antagonist test, five packages of formula were selected. Viability of five formulas were stable until the three months of storage period. Application of the formulas for soybean in green house, formula F4 showed significant effect on plant height, shoot and root fresh weight and root dry weight in both wet and dry conditions.
Key word: Rhizobacteria, drought, Bacillus, Pseudomonas, Bradyrhizobium japonicum,
v
PRAKATA
Puji dan syukur penulis panjatkan kepada Allah SWT atas segala karunia dan hidayah-Nya sehingga penulis dapat menyelesaikan karya ilmiah ini. Karya ilmiah berjudul “Penapisan Rizobakteria Toleran Kekeringan Pemacu Tumbuh Tanaman Kedelai dan Aplikasinya di Rumah Kaca” dilaksanakan dari bulan Januari sampai Juli 2012 di Laboratorium Mikrobiologi dan rumah kaca Departemen Biologi FMIPA IPB.
Terima kasih penulis ucapkan kepada Prof. Dr. Aris Tri Wahyudi, M.Si dan Dr. Edi Husen, M.Sc selaku pembimbing atas saran dan bimbingannya selama penelitian dan penyusunan karya ilmiah, kepada Prof. Dr.Ir Alex Hartana selaku dosen penguji atas saran dan masukan yang berharga untuk perbaikan karya ilmiah ini. Terima kasih juga kepada Pemerintah Provinsi Jawa Barat yang telah membiayai kuliah dan penelitian selama penulis menimba ilmu di Institut Pertanian Bogor.
Penulis juga mengucapkan terima kasih kepada orang tua dan keluarga atas doa dan kasih sayangnya, kepada Pak Jaka, Ibu Heni, Ibu Rika dan Kakak Meli yang telah membantu selama penelitian.
Semoga karya ilmiah ini dapat bermanfaat.
Bogor, Agustus 2012
RIWAYAT HIDUP
Penulis dilahirkan di Subang pada tanggal 17 Mei 1991 dari ayah Narman dan ibu Anah. Penulis merupakan putri keempat dari empat bersaudara. Penulis lulus SDN Tambakan III Subang tahun 2000 dan lulus MTsN 1 Jalancagak Subang tahun 2003. Tahun 2008 penulis lulus dari MAN 1 Subang dan pada tahun yang sama lulus seleksi masuk IPB melalui jalur Undangan Seleksi Masuk IPB (USMI). Penulis memilih mayor Biologi, Fakultas Matematika dan Ilmu Pengetahuan Alam.
Selama mengikuti perkuliahan, penulis menjadi asisten mata kuliah Fisiologi Prokariot pada tahun ajaran 2010/2011 serta mata kuliah Biologi Dasar dan Mikrobiologi Dasar pada tahun ajaran 2011/2012. Selain itu, penulis juga aktif di lembaga kemahasiswaan Himpunan Mahasiswa Biologi (Himabio) sebagai sekretaris umum II periode 2009/2010 dan sekretaris umum I periode 2010/2011, serta aktif di kepanitiaan BOX, BIONIC, Biologi Interaktif, Revolusi Sains 2, Pesta Sains Nasional. Pada tahun 2010 penulis melakukan studi lapang bersama Rina Rodiana dan Rizqi Ammar di Taman Wahana Alam (TWA) Pangandaran dengan judul “Koleksi dan Identifikasi Avertebrata di Pantai Pangandaran”. Penulis melaksanakan praktik lapang di Balai Laboratorium Kesehatan Yogyakarta tahun 2011 yang berjudul “ Pemeriksaan Mikroskopis, Kultur dan Uji Resistensi M. Tuberculosis di Balai Laboratorium Kesehatan Yogyakarta”.
Bogor, Agustus 2012
DAFTAR ISI
DAFTAR TABEL ... vii
DAFTAR GAMBAR ... vii
DAFTAR LAMPIRAN ... vii
PENDAHULUAN ... 1
Latar Belakang ... 1
Tujuan ... 1
BAHAN DAN METODE ... 1
Bahan dan Alat ... 1
Metode ... 1
Peremajaan Bakteri ... 1
Penyiapan Media dengan Tekanan Osmotik Rendah ... 2
Penapisan Bakteri Toleran Kekeringan ... 2
Uji Kuantitatif Eksopolisakarida ... 2
Uji Antagonistik Bakteri ... 2
Persiapan Gambut sebagai Bahan Pembawa ... 2
Persiapan Inokulan ... 2
Formulasi Inokulan Menggunakan Bahan Pembawa ... 3
Uji Viabilitas ... 3
Uji Efektifitas Inokulan terhadap Pertumbuhan Kedelai dalam Cekaman Kekeringan ... 3
Rancangan Percobaan ... 3
HASIL ... 4
Peremajaan Isolat ... 4
Penapisan Bakteri Toleran Kekeringan ... 4
Uji Kuantitatif Eksopolisakarida ... 4
Uji Antagonistik Bakteri Terpilih ... 5
Formulasi Inokulan menggunakan Bahan Pembawa ... 5
Uji Viabilitas ... 6
Uji Efektivitas Inokulan terhadap Tanaman Kedelai pada Cekaman Kekeringan di Rumah Kaca ... 7
PEMBAHASAN ... 10
SIMPULAN ... 12
vii
DAFTAR TABEL
Halaman 1 Jumlah PEG yang ditambahkan untuk mendapatkan tekanan osmotik tertentu
pada media tumbuh... 2 2 Dosis antibiotikyang digunakan untuk masing-masing bakteri... 3 3 Hasil penapisan toleran kekeringan Hasil penapisan toleran kekeringan bakteri
Pseudomonas sp., Bacillus sp., dan Bradyrhizobium japonicum.... 4 4 Hasil uji kuantitatif eksopolisakarida bakteri Pseudomonas sp. (Crb) dan
Bradyrhizobium japonicu (Bj)... 5 5 Hasil uji antagonistik bakteri Crb dan Bj sebagai bakteri uji terhadap bakteri Cr
sebagai bakteri target... 6 6 Hasil uji antagonistik bakteri Cr dan Bj sebagai bakteri uji terhadap bakteri Crb
sebagai bakteri target... 6 7 Hasil uji antagonistik bakteri Cr dan Crb sebagai bakteri uji terhadap bakteri Bj
sebagai bakteri target... 6 8 Formulasi bakteri yang terdiri atas Pseudomonas sp., Bacillus sp, dan
Bradyrhizobium japonicum...7 9 Viabilitas sel bakteri pada gambut selama masa penyimpanan 1, 2, dan 3 bulan... 7 10 Pengaruh perlakuan formulasi (F0-F5) terhadap tinggi tanaman kedelai ditanam
pada kadar air yang berbeda... 8 11 Pengaruh perlakuan formulasi (F0-F5) terhadap berat basah tajuk (BBT)
tanaman kedelai ditanam pada kadar air yang berbeda... 8 12 Pengaruh perlakuan formulasi (F0-F5) terhadap berat kering tajuk (BKT)
tanaman kedelai ditanam pada kadar air yang berbeda 8 13 Pengaruh perlakuan formulasi (F0-F5) terhadap berat basah akar (BBA)
tanaman kedelai ditanam pada kadar air yang berbeda...8 14 Pengaruh perlakuan formulasi (F0-F5) terhadap berat kering akar (BKA)
tanaman kedelai ditanam pada kadar air yang berbeda... 9 15 Pengaruh perlakuan formulasi (F0-F5) terhadap jumlah bintil akar (JBA)
tanaman kedelai ditanam pada kadar air yang berbeda... 9
DAFTAR GAMBAR
Halaman 1 Isolat Crb82 dan Crb94 sebagai isolat uji menghasilkan zona hambatan terhadap
isolat target Cr28 (ditunjukkan oleh anak panah), sedangkan isolat uji Crb16, Crb17 dan Crb60 tidak menghasilkan zona hambatan; k = kontrol cakram berisi media steril... 5 2 Kemasan formula inokulan dalam gambut... 5 3 Penampilan pertumbuhan tanaman kedelai dengan berbagai pengaruh formulasi
inokulan. K perlakuan kering; B perlakuan basah; F1-F5 perlakuan formulasi
inokulan; F0 kontrol tanpa formulasi inokulan... 9
DAFTAR LAMPIRAN
PENDAHULUAN
Latar Belakang
Kondisi kekurangan air berpotensi menghambat pertumbuhan tanaman. Lahan kering menjadi salah satu lahan kurang produktif karena kondisi kadar air tanah rendah atau berada di bawah kapasitas lapang dan dalam kondisi laju evapotranspirasi melebihi laju absorbsi air (Salisbury & Ross 1995). Cekaman kekeringan menjadi salah satu faktor lingkungan utama yang mempengaruhi produktivitas tanaman pertanian (Manchanda & Garg 2008). Oleh karena itu, diperlukan strategi untuk memanfaatkan lahan kering agar produktivitas tanaman pertanian menjadi optimal, salah satu di antaranya yaitu menggunakan rizobakteria.
Plant Growth Promoting Rhizobacteria
(PGPR)adalah bakteri sekitar perakaran yang dapat memacu pertumbuhan tanaman dan juga merupakan agen pengendali hayati yang menguntungkan bagi tumbuhan. Bakteri ini memiliki kemampuan menyediakan dan memfasilitasi penyerapan berbagai unsur hara diantaranya nitrogen dan fosfat dalam tanah serta mensintesis fitohormon pemacu tumbuh (Kloepper 1992). Beberapa bakteri tanah
Pseudomonas sp. dan Bacillus sp. dilaporkan menghasilkan hormon umbuh IAA, mensekresi siderofor serta memiliki kemampuan biokontrol terhadap fungi patogen akar (Astuti 2008; Widyawati 2008). Bradyrhizobium japonicum diketahui merupakan salah satu bakteri pembentuk bintil akar yang dapat membantu menambat nitrogen pada bintil akar tanaman kedelai (Mubarik et al 2009).
Potensi-potensi PGPR dalam memacu produktivitas tanaman akan menurun seiring dengan penurunan populasinya sepanjang cekaman kekeringan. Namun bakteri tanah tertentu dapat menahan kondisi kekeringan ini dengan memanfaatkan air yang tersimpan dalam mikroporous tanah dan bertahan hidup dengan aktivitas metabolik yang minimum (Alikhani & Mohamadi 2010). Selain itu beberapa bakteri khususnya rizobakteria mampu mensintesis eksopolisakarida untuk mempertahankan hidupnya dalam kondisi tercekam kekeringan (Young & Burns 1993).
Sampai saat ini di laboratorium Mikrobiologi Departemen Biologi FMIPA IPB telah terkoleksi 27 isolat rizobakteria pemacu tumbuh tanaman kedelai, isolat tersebut perlu ditapis yang toleran kering agar dapat dimanfaatkan sebagai inokulan pada lahan kering.
Tujuan
Menapis bakteri pemacu tumbuh tanaman kedelai yang mampu mengendalikan cekaman kekeringan dan mengaplikasikannya pada tanaman kedelai di rumah kaca.
BAHAN DAN METODE
Penelitian dilaksanakan dari bulan Januari sampai dengan Juli 2012 di Laboratorium Mikrobiologi dan Rumah Kaca Departemen Biologi FMIPA IPB.
Bahan dan Alat
Bakteri yang digunakan adalah 14 isolat
Pseudomonas sp. (Crb1, Crb3, Crb8, Crb15, Crb16, Crb17, Crb42, Crb44, Crb60, Crb74, Crb82, Crb93, Crb94, dan Crb95), 11 isolat
Bacillus sp. (Cr22, Cr24, Cr28, Cr31, Cr44, Cr64, Cr66, Cr67, Cr68, Cr69, dan Cr71) (Astuti 2008; Widyawati 2008), dan 2 isolat
Bradyrhizobium japonicum Bj11(wt) (Endarini
et al 1995) (Bj11(19) (Astuti 2006). Media yang digunakan adalah media agar Kings’ B dengan komposisi agar 20 g/l, pepton 20 g/l, K2HPO4 1,5 g/l, MgSO4.7H2O 1,2 g/l, gliserol 1,5 ml, dan aquades 1000 ml dengan pH 7,2 ± 0,2; media agar YMB (Yeast Manitol Broth) dengan komposisi agar 20 g/l, manitol 10 g/l, K2HPO4 0,5 g/l, MgSO4.7H2O 0,2 g/l,
yeast exract 0,2 g/l, dan aquades 1000 ml dengan pH 7,2 ± 0,2; media agar NB (Nutrient Broth) dengan komposisi agar 20 g/l, Nutrient Broth 8 g/l, dan akuades 1000 ml dengan pH pH 7,2 ± 0,2; LB (Luria Bertani) yang dimodifikasi dengan komposisi yeast extract
10 g/l, tripton 10 g/l dan NaCL 1/L dan aquades 1000 ml dengan pH 7,2 ± 0,2; media ATCC no.14 dengan komposisi K2HPO4 0.2
g/l, KH2PO4 0.8 g/l, MgSO4.7H2O 0.2 g/l,
CaSO4.2 H2O 0.1 g/l, FeCl 2.0 mg/l, Na2Mo4.
2H2O (trace), ekstrak khamir 0.5 g/l, sukrosa
20 g/l, bakto agar 15 g/l, dan akuades 1000 ml; susu skim dengan molase, Poly Ethylen Glicol
(PEG) 6000. Bahan pembawa yang digunakan adalah gambut ditambah bahan mineral. Alat-alat yang digunakan adalah cawan petri, erlenmeyer, tabung reaksi dan alat-alat lain yang digunakan di Laboratorium Mikrobiologi Departemen Biologi, FMIPA IPB.
Metode
Peremajaan Bakteri
2
bakteri Bacillus sp. (Cr) pada media agar NB, dan Bradyrhizobium japonicum (Bj) pada media agar YMB. Masing-masing isolat diinkubasi selama 1 sampai 2 hari pada suhu ruang untuk Crb dan Cr serta 7 hari untuk Bj. Penyiapan Media dengan Tekanan Osmotik Rendah
Media NB dan LB yang sudah disterilkan, ketika masih panas ditambahkan dengan PEG untuk menurunkan potensial osmotik mengikuti persamaan menurut Michel & Kaufmann (1973):
φw= -൫1.18 x 10-2 C൯- ቀ൫1.18 x 10-4൯CTቁ + (൫8.39 x 10-7൯x C2Tሻ
Keterangan :
Ψw : potensial osmotik (Mpa)
C : konsentrasi T : suhu (oC)
Potensial osmotik yang diatur adalah -0.73 Mpa, -1 Mpa,-1.5 Mpa, -2 Mpa, -2.5 Mpa. Berdasarkan persamaan diatas, banyaknya PEG 6000 yang ditambahkan ke dalam media untuk masing-masing potensial osmotik tertera pada Tabel 1.
Tabel 1 Jumlah PEG yang ditambahkan untuk mendapatkan tekanan osmotik tertentu pada media tumbuh
Tekanan Osmotik (MPa)
PEG yang ditambahkan (g/L)
- 0.73 249.17
-1.00 295.75
-1.50 367.67 -2.00 428.38 -2.50 481.89
Penapisan Bakteri Toleran Kekeringan Sebanyak 200 µl suspensi Crb, Cr dan Bj yang ditumbuhkan pada media NB (untuk Cr dan Crb) dan LB (untuk Bj) dengan jumlah populasi berkisar 108 diinokulasikan ke dalam 20 ml media NB dan LB yang sudah ditambahkan dengan Polyethylen Glicol (PEG) 6000, diinkubasi pada mesin penggoyang kecepatan 120 rpm pada suhu ruangan selama 24 jam. Pengukuran Optical Density dengan menggunakan spektrofotometer pada panjang gelombang 570 nm.
Uji Kuantitatif Eksopolisakarida
Uji kandungan eksopolisakarida dilakukan melalui penetapan bobot kering eksopolisakarida yang dihasilkan di dalam medium cair ATCC no. 14 dengan menggunakan sumber karbon sukrosa. Bakteri dalam kultur cair dengan populasi 108
ditumbuhkan dalam 50 ml medium cair ATCC no. 14 dan diinkubasi pada temperatur 28oC selama tiga hari di atas mesin pengocok dengan kecepatan 200 rpm. Pada akhir inkubasi, sel dipanen dengan cara menambahkan 1 mM EDTA sebanyak 500 μl, kemudian dikocok sampai homogen lalu disentrifugasi dengan kecepatan 9000 rpm selama 10 menit. Supernatan diambil kemudian ditambah dengan larutan aseton dingin dengan perbandingan 1:3. Selanjutnya dilakukan sentrifugasi kembali dengan kecepatan 12000 rpm selama 30 menit. Endapan biomassa berupa eksopolisakarida selanjutnya dicuci dengan akuades dan dikeringkan pada temperatur 60oC selama 24 jam atau sampai diperoleh bobot kering yang tetap. Nilai bobot kering mg/ml didapat dari selisih bobot effendorf berisi eksopolisakarida dengan bobot effendorf kosong.
Uji Antagonistik Bakteri
Sebanyak 2.5 ml suspensi inokulum Crb yang dikulturkan pada media LB dengan konsentrasi 108 sel/ml, kemudian diinokulasikan ke 50 ml media LA dan dituang ke tiga buah cawan. Kertas cakram steril (d=5 mm) dicelupkan pada masing-masing suspensi inokulum Cr dan Bj yang memiliki konsentrasi sel 108 sel/ml, kemudian diletakkan pada cawan berisi media LA yang telah diinokulasi dengan Crb. Perlakuan serupa dilakukan untuk masing-masing bakteri Cr dan Bj. Sifat antagonistik ditunjukkan dengan ada tidaknya zona bening yang terbentuk. Terbentuknya zona bening merupakan indikator bahwa bakteri-bakteri tersebut saling antagonis, sedangkan tidak terbentuknya zona bening merupakan indikator bahwa bakteri-bakteri tersebut tidak saling antagonis. Bakteri yang tidak antagonis digunakan untuk kombinasi formula di dalam bahan pembawa.
Persiapan Gambut sebagai Bahan Pembawa Bahan pembawa terdiri dari campuran gambut sebanyak 85%, fosfat alam 10%, dan kapur pertanian (kaptan) 5% yang dicampur hingga rata. Sebanyak 50 gr campuran gambut dikemas ke dalam plastik tahan panas dan kemudiaan disterilisasi dua kali pada suhu 121 ºC selama 1 jam dengan tekanan 1 atm. Persiapan Inokulan
3
kemudian ditumbuhkan kembali di dalam media produksi yang mengandung susu skim dan molase pada mesin penggoyang sampai populasi bakteri mencapai berkisar 109. Formulasi Inokulan Menggunakan Bahan Pembawa
Masing-masing suspensi inokulan Crb, Cr, dan Bj dari media produksi yang mengandung susu skim dan molase diinokulasikan ke dalam 50 gram gambut, masing-masing sebanyak 5 ml dengan jumlah populasi berkisar 109 sel/ml suspensi. Tiap kemasan gambut 50 gram diinokulasi dengan campuran tiga bakteri, yaitu Crb, Cr, dan Bj. Dari kombinasi bakteri yang digunakan diperoleh 5 paket inokulan. Tiap set paket inokulan digunakan untuk uji viabilitas dan uji efektivitasnya dalam cekaman kekeringan pada kedelai di rumah kaca.
Uji Viabilitas
Uji viabilitas dilakukan untuk mengetahui pengaruh penyimpanan terhadap penurunan populasi bakteri. Sebanyak 10 gr masing-masing paket inokulan diencerkan dengan 90 ml larutan garam fisiologis. Kemudian dilakukan pengenceran serial 10-1, 10-2, 10-3
dan seterusnya sampai 10-9. Sebanyak 0,1 ml dari pengenceran 107 sampai 109, disebar pada media agar King’s B, agar NB, dan agar YMB yang ditambah antibiotik (Tabel 2) untuk seleksi bakteri dan diinkubasi pada suhu ruang selama 1 sampai 2 hari untuk Crb dan Cr, dan 5 sampai 7 hari untuk Bj. Jumlah koloni bakteri yang tumbuh dihitung dan jumlah populasi ditetapkan per gram bahan pembawa. Masa penyimpanan dilakukan sampai 3 bulan. Tabel 2 Dosis antibiotik yang digunakan untuk
masing-masing bakteri
Isolat bakteri Antibiotik (20μg/ml)
Crb 16 Ampisilin
Crb 17 Ampisilin
Crb 60 Tanpa Antibiotik Crb 82 Tanpa Antibiotik Crb 94 Streptomisin Cr 64 Tanpa Antibiotik
Cr 66 Ampisilin
Cr 67 Tanpa Antibiotik Cr 71 Tanpa Antibiotik Bj 11 (19) Rifampisin Bj 11 (wt) Rifampisin
Uji Efektifitas Inokulan terhadap Pertumbuhan Kedelai dalam Cekaman Kekeringan
Uji dilakukan di rumah kaca dengan menggunakan tanah pH 6 dengan kadar air
yang diatur secara konstan. Perlakuan kadar air yang diberikan yaitu kadar air pada kapasitas lapang (basah) dan kadar air setengah kapasitas lapang (kering). Pengukuran kapasitas lapang dilakukan dengan cara tanah dalam polybag disiram dengan air sampai jenuh kemudian didiamkan selama 3 hari sampai tidak ada air yang menetes. Berat basah dan berat kering tanah ditimbang. Berat basah ditimbang setelah tidak ada air yang menetes dari polybag. Berat kering ditimbang setelah tanah di oven pada suhu 100oC sampai diperoleh berat konstan (Hendriyani dan Setiari 2009). Kadar air kapasitas lapang diukur dengan rumus:
KL=BB-BK
BB x 100 % Ket:
KL : Kadar air kapasitas lapang BB : Berat basah tanah BK : Berat kering tanah
Tanah yang digunakan dimasukkan ke dalam pot ember sebanyak 1 kg dengan volume 1 L. Sebelum digunakan, tanah terlebih dahulu diberi pupuk NPK dengan dosis N, P, dan K berturut-turut 0.025 gram, 0.05 gram dan 0.03 gram. Benih kedelai diinokulasi dengan mencampurkan kedelai lembab dengan inokulan hingga rata kemudian kedelai ditanam pada pot. Setiap pot ditanam dua biji kedelai. Penjarangan dilakukan pada 5 hari setelah tanam (HST) dengan menyisakan satu tanaman setiap pot yang memiliki pertumbuhan relatif seragam. Pengkondisian kekonstanan kadar air setiap harinya dilakukan dengan menyiram tanah sambil ditimbang sehingga mencapai berat tertentu. Tanaman diamati setiap minggu selama satu bulan. Rancangan Percobaan
4
HASIL
Peremajaan Isolat
Semua isolat yang ditumbuhkan pada masing-masing media standar dapat tumbuh dengan baik. Isolat Crb dapat tumbuh baik pada media agar King’s B, isolat Cr tumbuh baik pada media agar NB , isolat Bj tumbuh baik pada media agar YMB. Waktu diinkubasi yang digunakan adalah selama 1 sampai 2 hari untuk Cr dan Crb serta selama 7 hari untuk Bj. Penapisan Bakteri Toleran Kekeringan
Penapisan bakteri toleran kekeringan dilakukan untuk menseleksi bakteri-bakteri yang dapat bertahan dan tumbuh baik dalam kondisi cekaman kekeringan. Bakteri yang memiliki nilai Optical Density (OD) lebih besar dari 0.5 A pada tekanan osmotik tertentu dikategorikan sebagai bakteri yang benar-benar toleran (Alikhani & Mohamadi 2010). Hasil penapisan toleran kekeringan disajikan dalam Tabel 3.
Tabel 3 menunjukkan hasil penapisan toleran kekeringan bakteri Pseudomonas sp. (Crb), Bacillus sp. (Cr), dan Bradyrhizobium japonicum (Bj). Berdasarkan data tersebut, dipilih 7 isolat Crb terbaik dengan nilai OD tertinggi yaitu Crb16, Crb17, Crb60, Crb74, Crb82, Crb94, Crb95. Untuk bakteri Bacillus
sp. dipilih 8 isolat terbaik yaitu Cr22, Cr28, Cr31, Cr44, Cr64, Cr66, Cr67, dan Cr71, sedangkan untuk bakteri Bradyrhizobium japonicum dipilih keduanya yaitu Bj11(wt). dan Bj11(19). Bakteri-bakteri terpilih ini kemudian diuji aktifitas antagonisnya satu sama lain.
Uji Kuantitatif Eksopolisakarida
Uji kuantitatif eksopolisakarida ini ditujukan untuk mengetahui secara kuantitatif kandungan eksopolisakarida yang dihasilkan oleh bakteri Crb dan Bj. Berdasarkan Tabel 4 diketahui bahwa semua isolat menghasilkan eksopolisakarida. Bobot kering ekspolisakarida yang dihasilkan berkisar antara 1.7 mg/ml sampai 8 mg/ml. Isolat Crb17 menghasilkan eksopolisakarida tertinggi yaitu sebesar 8 mg/ml, dan isolat yang menghasilkan eksopolisakarida terendah yaitu Crb3 sebesar 1.7 mg/ml. Semakin tinggi kandungan eksopolisakarida maka diharapkan akan semakin positif korelasinya dengan kemampuan tumbuh baik dalam kondisi cekaman kekeringan dan berfungsi sesuai perannya sebagai bakteri pemacu tumbuh pertumbuhan tanaman.
Tabel 3 Hasil penapisan toleran kekeringan bakteri Pseudomonas sp., Bacillus sp., dan Bradyrhizobium japonicum. Kode
Isolat
Nilai Optical Density (OD) pada Tekanan Osmotik (Mpa) 0 -0.73 -1.0 -1.5 -2.0 -2.5
Pseudomonas sp.
Crb1 1,57 1,24 0,89 0,64 0,54 0,0 Crb3 1,54 0,97 0,79 0,51 0,49 0,0 Crb8 1,60 1,14 0,67 0,66 0,53 0,0 Crb15 1,61 1,25 0,81 0,55 0,42 0,0 Crb16 1,65 1,29 1,06 0,73 0,69 0,28 Crb17 1,52 0,88 0,77 0,74 0,66 0,29 Crb44 1,54 1,33 0,97 0,69 0,50 0,0 Crb47 1,59 1,08 1,03 0,77 0,63 0,0 Crb60 1,62 1,19 1,02 0,88 0,76 0,39 Crb74 1,49 1,27 0,77 0,74 0,56 0,0 Crb82 1,53 0,84 0,80 0,78 0,72 0,51 Crb93 1,54 1,30 0,67 0,57 0,44 0,0 Crb94 1,58 1,16 1,00 0,81 0,75 0,46 Crb95 1,55 1,20 0,89 0,66 0,57 0,0
Bacillus sp.
Cr22 1,10 0,90 0,87 0,61 0,50 0,0 Cr24 1,23 0,82 0,58 0,45 0,34 0,0 Cr28 1,67 1,38 1,20 0,60 0,42 0,0 Cr31 1,53 1,22 1,38 0,64 0,44 0,0 Cr44 1,16 0,73 0,60 0,57 0,46 0,0 Cr64 1,25 0,69 0,68 0,68 0,63 0,0 Cr66 1,54 1,12 0,67 0,64 0,56 0,0 Cr67 1,45 0,98 0,82 0,66 0,45 0,0 Cr68 1,64 1,45 1,28 0,50 0,44 0,0 Cr69 1,65 1,39 1,35 0,50 0,41 0,0 Cr71 1,67 1,42 1,35 0,64 0,54 0,0
Bradyrhizobium japonicum
Bj11
(wt) 1,15 0,81 0,72 0,59 0,29 0,0 Bj11
(19) 1,82 1,48 0,89 0,63 0,39 0,0 Ket : pemilihan isolat terbaik dibatasi sampai tekanan
osmotik -2 Mpa
Tabel 4 Hasil uji kuantitatif eksopolisakari- da bakteri Pseudomonas sp. (Crb) dan
Bradyrhizobium japonicu (Bj)
Kode Isolat
Bobot Kering Eksopolisakarida (mg/ml) Crb1 4.76 Crb3 1.72 Crb8 4.70 Crb15 3.08 Crb16 6.37 Crb17 8.04 Crb44 3.04 Crb60 5.72 Crb74 5.73 Crb82 3.01 Crb84 3.75 Crb93 4.02 Crb94 7.00 Crb95 4.07
Bj 11 (wt) 7.06
5
Uji Antagonistik Bakteri Terpilih
Uji antagonistik dilakukan terhadap bakteri terbaik pada hasil penapisan toleran kekeringan. Tujuan uji ini yaitu untuk mencari isolat-isolat yang tidak memiliki aktivitas antagonis satu sama lain agar bisa dikombinasikan dalam satu paket formulasi. Hasil uji antagonistik antar isolat Crb, Cr dan Bj dimana masing-masing bakteri berperan sebagai isolat uji dan isolat target disajikan dalam Tabel 5, Tabel 6 dan Tabel 7. Isolat target Cr22, Cr66 dan Cr67 tidak dihambat oleh isolat uji manapun, sementara itu isolat Cr28 tidak dihambat oleh isolat uji Crb16, Crb17, Crb74, Crb95 serta isolat Bj11(wt) dan Bj11(19) namun dihambat oleh isolat uji Crb82 dan Crb94 seperti terlihat pada Gambar 1. Selanjutnya isolat target Cr31 tidak dihambat oleh isolat uji Crb16, Crb17, Crb60, Crb74, Crb95, Bj11(wt) dan Bj11(19), serta isolat target Cr71 tidak dihambat oleh Crb16, Crb74, Crb82, Crb95, Bj11(wt) dan Bj11(19) (Tabel 5).
Gambar 1 Isolat Crb82 dan Crb94 sebagai isolat uji menghasilkan zona hambatan terhadap isolat target Cr28 (ditunjukkan oleh anak panah), sedangkan isolat uji Crb16, Crb17 dan Crb60 tidak menghasilkan zona hambatan; k = kontrol cakram berisi media steril. Isolat-isolat Cr dan Bj yang berperan sebagai bakteri uji terhadap isolat target Crb ada yang menghasilkan zona hambatan dan ada pula yang tidak. Isolat target Crb60 tidak dihambat oleh semua isolat uji, isolat target Crb16 hanya dihambat oleh isolat uji Bj11(19), isolat target Crb17 tidak dihambat oleh isolat uji Cr28, Cr631, Cr44, Cr66, Cr67, Cr71, Bj11(wt) dan Bj11(19). Isolat Isolat target Crb74 tidak dihambat oleh Cr22, Cr28, Cr31, Cr44, Cr67, Cr71 dan Bj11(wt), sedangkan Cr82 hanya dihambat oleh isolat uji Cr64.
Crb94 dihambat oleh isolat uji Cr22, Cr64, dan Cr66, isolat target Crb95 dihambat oleh Cr64, Cr66 dan Bj11(19) (Tabel 6). Untuk isolat uji Crb dan Cr terhadap isolat target Bj diperoleh hasil bahwa seluruh isolat uji Crb dan Cr tidak menghasilkan zona hambatan terhadap isolat target Bj11(19). Sedangkan untuk isolat uji Cr64 dan Cr66 menghasilkan zona hambat terhadap isolat target Bj11(wt) (Tabel 7).
Isolat-isolat yang memiliki hubungan tidak antagonis antara ketiga isolat akan dikombinasikan dalam satu formula. Isolat-isolat terpilih ditumbuhkan pada media alternatif susu skim dan molase untuk diinokulasikan di dalam media pembawa. Formulasi Inokulan menggunakan Bahan Pembawa
Inokulan-inokulan dikombinasikan ke dalam formula dengan bahan pembawa. Sebelum diinokulasikan ke dalam bahan pembawa, populasi masing-masing bakteri ditumbuhkan di media alternatif yang mengandung susu skim dan molase. Populasi awal bakteri dihitung menggunakan metode cawan sebar sampai dihasilkan jumlah berkisar antara 108 sampai 1010. Bakteri-bakteri yang akan dikombinasikan dipilih berdasarkan kandungan eksopolisakarida yang tinggi serta sifat tidak antagonistik satu sama lain. Berdasarkan pemilihan tersebut maka terbentuk 5 paket formula yang dihasilkan dari kombinasi tiga jenis bakteri Pseudomonas sp.,
Bacillus sp., dan Bradyrhizobium japonicum. Kombinasi paket formula yang terbentuk disajikan pada Tabel 8. Bentuk paket formulasi adalah serbuk gambut seperti dalam Gambar 2.
6
Tabel 5 Hasil uji antagonistik bakteri Crb dan Bj sebagai bakteri uji terhadap bakteri Cr sebagai bakteri target.
Keterangan : ++ = ada zona hambatan -- = tidak ada zona hambatan
Tabel 6 Hasil uji antagonistik bakteri Cr dan Bj sebagai bakteri uji terhadap bakteri Crb sebagai bakteri target.
Keterangan : ++ = ada zona hambatan -- = tidak ada zona hambatan
Tabel 7 Hasil uji antagonistik bakteri Cr dan Crb sebagai bakteri uji terhadap bakteri Bj sebagai bakteri target.
Keterangan : ++ = ada zona hambatan -- = tidak ada zona hambatan
Uji Viabilitas
Uji viabilitas dilakukan untuk mengetahui kemampuan hidup bakteri selama penyimpanan di dalam bahan pembawa. Setiap
satu bulan sekali populasi bakteri dihitung melalui metode cawan sebar. Jumlah populasi yang terdapat pada paket formulasi disajikanpada tabel 9.
Isolat Target Isolat Uji Crb 16 Crb 17 Crb 60 Crb 74 Crb 82 Crb 94 Crb 95 BJ 11 (wt) BJ 11 (19)
Cr22 -- -- -- -- -- -- -- -- --
Cr28 -- -- -- -- ++ ++ -- -- --
Cr31 -- ++ ++ -- ++ ++ -- -- --
Cr44 -- -- -- -- ++ ++ -- -- --
Cr64 -- -- -- -- ++ -- -- -- --
Cr66 -- -- -- -- -- -- -- -- --
Cr67 -- -- -- -- -- -- -- -- --
Cr71 -- ++ ++ -- -- ++ -- -- --
Isolat Target
Isolat Uji
Cr22 Cr28 Cr31 Cr44 Cr64 Cr66 Cr67 Cr71 BJ 11 (wt)
BJ 11 (19)
Crb16 -- -- -- -- -- -- -- -- -- ++
Crb17 ++ -- -- -- ++ -- -- -- -- --
Crb60 -- -- -- -- -- -- -- -- -- --
Crb74 -- -- -- -- ++ ++ -- -- -- ++
Crb82 -- -- -- -- ++ -- -- -- -- --
Crb94 ++ -- -- -- ++ ++ -- -- -- --
Crb95 -- -- -- -- ++ ++ -- -- -- ++
Isolat Target Isolat Uji Crb 16 Crb 17 Crb 60 Crb 74 Crb 82 Crb 94 Crb 95 Cr 22 Cr 28 Cr 31 Cr 44 Cr 64 Cr 66 Cr 67 Cr 71 BJ 11
(wt) -- -- -- -- -- -- -- -- -- -- -- ++ ++ -- --
BJ 11
7
Tabel 8 Formulasi bakteri yang terdiri atas
Pseudomonas sp., Bacillus sp, dan
Bradyrhizobium japonicum.
Formulasi
Isolat bakteri
Crb Cr Bj
F1 Crb16 Cr64 Bj 11 (wt) F2 Crb17 Cr66 Bj 11 (19) F3 Crb60 Cr64 Bj 11 (wt) F4 Crb82 Cr71 Bj 11 (19) F5 Crb94 Cr67 Bj 11 (19)
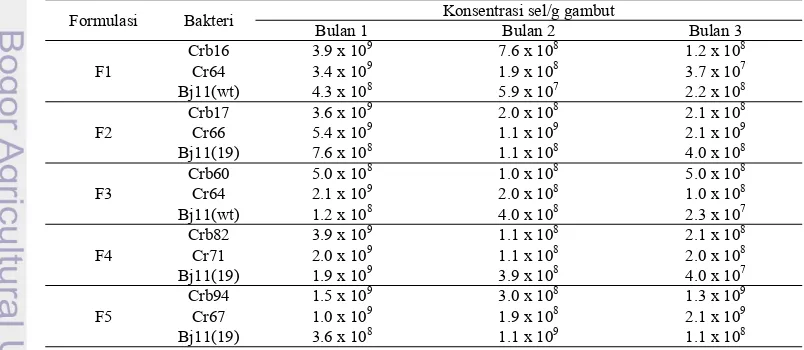
Berdasarkan Tabel 9 diketahui bahwa masing-masing formulasi mengalami pertumbuhan yang fluktuatif setiap bulannya. Pada bulan ke-tiga masing-masing bakteri dalam formula masih bersifat stabil dengan jumlah populasi berkisar 107-109 sel/ml. Uji Efektivitas Inokulan terhadap Tanaman Kedelai pada Cekaman Kekeringan di Rumah Kaca
Uji ini dilakukan dengan menumbuhkan tanaman kedelai yang telah diinokulasi dengan paket formula bakteri dan dikondisikan di dalam cekaman kekeringan. Untuk perlakuan basah, kadar tanah diketahui sebesar 28%. Berdasarkan hasil perhitungan, banyaknya air yang harus ditambahkan untuk mencapai kadar air tersebut yaitu sedemikian rupa sehingga bobot satu perlakuan basah sebesar 1286 gram. Untuk perlakuan kering diketahui kadar air sebesar 20.5%. Banyaknya air yang harus ditambahkan untuk mencapai kadar air tersebut yaitu sedemikian rupa sehingga bobot satu perlakuan kering sebesar 1147 gram. Perhitungan untuk menentukan kadar air dan bobot perlakuan tercantum pada Lampiran 2.
Hasil uji efektifitas formula terhadap pertumbuhan tanaman kedelai pada kadar air
yang berbeda ditunjukkan melalui enam parameter yaitu tinggi tanaman, berat basah tajuk (BBT), berat kering tajuk (BKT), berat basah akar (BBA), berat kering akar (BKA), dan jumlah bintil akar (JBA). Data disajikan dalam Tabel 10-15 mengikuti panduan penyajian tabel berdasarkan Gomez & Gomez (2007). Interaksi antar faktor formula dengan faktor kadar air diketahui terjadi pada parameter BBA dan JBA. Interaksi ini menunjukkan efek pengaruh formula yang bergantung pada kadar air. Untuk parameter BBA dalam keadaan kadar air kering, formula yang signifikan dalam meningkatkan BBA adalah formula F2, F3 dan F4 (ditunjukkan oleh huruf berbeda pada baris). Namun efektivitasnya masih belum dapat menyerupai efek formula pada kadar air basah (ditunjukkan oleh huruf yang berbeda pada lajur) (Tabel 14). Untuk parameter JBA dalam keadaan kering formula F1 dan F2 mampu meningkatkan JBA secara signifikan, namun masih belum menyerupai efektivitas formula pada kadar air basah (Tabel 16).
Untuk parameter tinggi, BBT, BKT dan BKA tidak terjadi interaksi antara formula dan kadar air. Namun pada beberapa parameter terdapat formula yang mampu meningkatkan pertumbuhan tanaman. Untuk parameter tinggi, semua formula mampu meningkatkan tinggi tanaman secara signifikan (Tabel 11). Interpretasi pengaruh parameter tinggi tanaman ditunjukkan oleh Gambar 3. Untuk parameter BBT (Tabel 12) dan BKA (Tabel 13) formula F4 mampu meningkatkan BBT secara signifikan. Pada parameter BKT tidak ada formula yang mampu meningkatkan pertumbuhan tanaman secara signifikan (Tabel 15).
Tabel 9 Viabilitas sel bakteri pada gambut selama masa penyimpanan 1, 2, dan 3 bulan.
Formulasi Bakteri Konsentrasi sel/g gambut
Bulan 1 Bulan 2 Bulan 3
F1
Crb16 3.9 x 109 7.6 x 108 1.2 x 108
Cr64 3.4 x 109 1.9 x 108 3.7 x 107
Bj11(wt) 4.3 x 108 5.9 x 107 2.2 x 108
F2
Crb17 3.6 x 109 2.0 x 108 2.1 x 108
Cr66 5.4 x 109 1.1 x 109 2.1 x 109
Bj11(19) 7.6 x 108 1.1 x 108 4.0 x 108
F3
Crb60 5.0 x 108 1.0 x 108 5.0 x 108
Cr64 2.1 x 109 2.0 x 108 1.0 x 108
Bj11(wt) 1.2 x 108 4.0 x 108 2.3 x 107
F4
Crb82 3.9 x 109 1.1 x 108 2.1 x 108
Cr71 2.0 x 109 1.1 x 108 2.0 x 108
Bj11(19) 1.9 x 109 3.9 x 108 4.0 x 107
F5
Crb94 1.5 x 109 3.0 x 108 1.3 x 109
Cr67 1.0 x 109 1.9 x 108 2.1 x 109
8
Tabel 10 Pengaruh perlakuan formulasi (F0-F5) terhadap tinggi tanaman kedelai ditanam pada kadar air yang berbeda
Kadar Air
Hasil rataan (cm)p
F0* F1 F2 F3 F4 F5 Rata-rataq
Basah 44.8 56.2 57.5 49.8 52.7 54.9 52.65 y
Kering 35.1 32.5 40.2 39.7 42.5 37.4 37.9 x
Rata-rataq 39.9 a 44.3 b 48.8 b 44.7 b 47.6 b 46.1 b p
Rata-rata dari 3 ulangan. *Kontrol tanpa inokulan. q
Dalam satu baris (atau lajur), rataan yang diikuti huruf yang sama tidak berbeda nyata pada taraf 5%
Tabel 11 Pengaruh perlakuan formulasi (F0-F5) terhadap berat basah tajuk (BBT) tanaman kedelai ditanam pada kadar air yang berbeda
Kadar Air
Hasil rataan (g)p
F0* F1 F2 F3 F4 F5 Rata-rataq
Basah 7.55 10.18 10.34 7.36 11.45 9.51 9.40 y
Kering 4.02 2.57 5.58 7.12 6.59 5.05 5.15 x
Rata-rataq 5.78 a 6.38 ab 7.96 ab 7.24 ab 9.02 b 7.28 ab p
Rata-rata dari 3 ulangan. *Kontrol tanpa inokulan. q
Dalam satu baris (atau lajur), rataan yang diikuti huruf yang sama tidak berbeda nyata pada taraf 5%
Tabel 12 Pengaruh perlakuan formulasi (F0-F5) terhadap berat kering tajuk (BKT) tanaman kedelai ditanam pada kadar air yang berbeda
Kadar Air
Hasil rataan (g)p
F0* F1 F2 F3 F4 F5 Rata-rataq
Basah 1.81 2.54 2.03 1.92 2.25 1.90 2.07 y
Kering 0.70 0.54 1.25 1.31 1.45 1.17 1.07 x
Rata-rataq 1.25 a 1.54 a 1.64 a 1.62 a 1.85 a 1.53 a p
Rata-rata dari 3 ulangan. *Kontrol tanpa inokulan.
q Dalam satu baris (atau lajur), rataan yang diikuti huruf yang sama tidak berbeda nyata pada taraf 5%
Tabel 13 Pengaruh perlakuan formulasi (F0-F5) terhadap berat basah akar (BBA) tanaman kedelai ditanam pada kadar air yang berbeda
Kadar Air
Hasil rataan (g)p
F0* F1 F2 F3 F4 F5 Rata-rata
Basah 2.35 a y 3.80 bc y 3.35 abc y 4.05 c y 4.10 c y 2.95 ab y 3.43 Kering 0.50 ab x 0.35 a x 0.90 b x 1.45 c x 2.45 d x 0.30 a x 0.99
Rata-rata 1.43 2.08 2.13 2.75 3.28 1.63
p
Rata-rata dari 3 ulangan. Rataan diidahkan dengan Uji Duncan pda taraf 5 %. *Kontrol tanpa inokulan. a-d membandingkan rataan dalam baris dan x-y membandingkan rataan dalam lajur
Tabel 14 Pengaruh perlakuan formulasi (F0-F5) terhadap berat kering akar (BKA) tanaman kedelai ditanam pada kadar air yang berbeda
Kadar Air
Hasil rataan (g)p
F0* F1 F2 F3 F4 F5 Rata-rataq
Basah 0.28 0.33 0.33 0.30 0.36 0.32 0.32 y
Kering 0.15 0.13 0.18 0.20 0.28 0.12 0.18 x
Rata-rataq 0.22 a 0.23 a 0.25 ab 0.26 ab 0.32 b 0.22 a p
Rata-rata dari 3 ulangan. *Kontrol tanpa inokulan. q
Dalam satu baris (atau lajur), rataan yang diikuti huruf yang sama tidak berbeda nyata pada taraf 5%.
Tabel 15 Pengaruh perlakuan formulasi (F0-F5) terhadap jumlah bintil akar (JBA) tanaman kedelai ditanam pada kadar air yang berbeda
Kadar Air
Hasil rataan (butir)p
F0* F1 F2 F3 F4 F5 Rata-rataq
Basah 6.7 a y 22.3 c y 21.7 c y 28.6 d y 48.3 e y 16.7 b y 24.1 Kering 1.3 a x 6.7 bc x 6.7 bc x 5.3 abc x 5.3 abc x 2.3 ab x 6.5
Rata-rataq 4.0 14.5 14.2 16.9 26.8 9.5
p
Rata-rata dari 3 ulangan. *Kontrol tanpa inokulan. q
9
K/F0
K/F0 K/F0
K/F0
K/F0 B/F0
B/F0 B/F0
B/F0
B/F0 K/F1
B/F5 B/F4
B/F3
B/F2
K/F4 K/F3
K/F2 B/F1
K/F5
PEMBAHASAN
Penapisan rizobakteria pada kondisi cekaman kekeringan bertujuan untuk menseleksi rizobakteria yang toleran terhadap kekeringan. Ketika rizobakteria tersebut mampu bertahan dalam kondisi kekeringan, diharapkan fungsinya sebagai agen hayati dapat diperankan dengan baik dalam kondisi tercekam. Pada penelitian ini, kondisi cekaman kekeringan diatur dengan menambahkan Polietilen Glikol (PEG) 6000 ke dalam media. Senyawa PEG bersifat larut dalam air dan menyebabkan penurunan potensial air. Keadaan seperti ini dimanfaatkan untuk simulasi penurunan potensial air. Potensial air dalam media yang mengandung PEG dapat digunakan untuk meniru besarnya potensial air tanah (Michel and Kaufmann 1973). Berdasarkan data hasil penapisan, sebagian besar rizobakteria mampu bertahan hidup sampai tekanan osmotik -2 Mpa sampai batas OD ≥ 0.5, oleh karena itu pemilihan bakteri dibatasi sampai tekanan osmotik -2 Mpa. Namun demikian, bakteri Crb82 memiliki nilai OD ≥ 0.5 pada tekanan osmotik -2.5 Mpa. Hal ini mengindikasikan bahwa masih terdapat bakteri yang mampu tumbuh baik pada tekanan osmoik yang lebih rendah namun jumlahnya terbatas.
Kemampuan bakteri untuk bertahan dalam kondisi kekeringan berkorelasi positif dengan kemampuannya menghasilkan eksopolisakari- da. Sandhya et al. (2009) melaporkan studi mikroskop scanning elektron yang menunjukkan pembentukan biofilm pada permukaan akar yang diinokulasi dengan bakteri bersamaan dengan struktur tanah yang membaik. Pembentukan biofilm di permukaan akar mampu melindungi akar dari kekeringan. Menurut Hepper (1975) eksopolisakarida dapat menyediakan lingkungan mikro yang mengikat air dan memperlambat dampak cekaman kekeringan dibandingkan dengan lingkungan sekitar diluar lingkungan mikro. Kondisi lingkungan mikro ini dapat melindungi sel tumbuhan dan bakteri perakaran dari kekeringan dengan meningkatkan retensi air sehingga dapat mengatur difusi sumber karbon seperti glukosa ke dalam sel (Roberson & Firestone1992). Oleh karena itu, akumulasi bakteri penghasil eksopolisakarida di zona perakaran memungkinkan untuk mengurangi cekaman kekeringan pada tanaman.
Uji antagonistik diperlukan untuk mengetahui apakah dua atau lebih kelompok bakteri berbeda spesies dapat digabungkan. Hal ini penting untuk mendapatkan hubungan
bakteri yang tidak antagonis antara isolat
Pseudomonas sp. (Crb), Bacillus sp. (Cr) dan
Bradyrhizobium japonicum (Bj) agar dapat digabungkan dalam satu paket formula di dalam bahan pembawa. Penggabungan ketiga isolat dalam satu paket formula ditujukan agar interaksi antara bakteri Crb, Cr dan Bj dapat lebih maksimal dalam memacu pertumbuhan tanaman. Pada penelitian sebelumnya, isolat Crb dan Cr diketahui mampu memacu pertumbuhan tanaman kedelai dengan menghasilkan IAA, mensekresi siderofor serta bersifat antagonis terhadap Rizoctonia solani
(Astuti 2008; Widyawati 2009). Sementara itu, isolat Bj dapat memfiksasi nitrogen melalui pembentukan nodul atau bintil akar karena rhizobium menodulasi tanaman kedelai secara efektif. Dengan demikian, kebutuhan nitrogen tanaman dapat terpenuhi dan tanaman dapat tumbuh lebih baik (Tahar 2008). Ketika ketiga spesies bakteri ini dapat digabungkan, maka peran agen hayati akan semakin optimal.
Isolat Crb, Cr dan Bj umumnya ditumbuhkan pada media standar laboratorium, namun media standar yang relatif mahal dapat digantikan dengan media alternatif dengan bahan-bahan yang lebih ekonomis dan mudah didapat tapi tetap memiliki kualitas yang sama dengan media standar, salah satunya adalah media yang mengandung susu skim dan molase. Susu skim dapat berasal dari susu kadaluarsa, sedangkan molase merupakan hasil sampingan industri gula. Kristin (2009) melaporkan bahwa media alternatif susu skim dan molase menghasilkan pertumbuhan yang baik untuk bakteri Crb, Cr dan Bj dengan populasi sel berkisar 108 sel/ml. Susu skim berperan sebagai sumber nitrogen dan molase berperan sebagai pengganti sumber karbon.
11
pembawa serta kemampuannya untuk dapat bersaing dengan bakteri lain di tanah ketika diaplikasikan.
Kemampuan bakteri untuk tumbuh dan bertahan hidup selama masa penyimpanan dalam gambut diketahui dengan menguji viabilitasnya. Dari uji viabilitas yang dilakukan setiap bulan selama tiga bulan, jumlah bakteri dalam setiap formula dapat dikatakan stabil yaitu berkisar 107- 109 sel/ml (Tabel 9). Beberapa paket inokulan yang masih stabil selama3 bulan yaitu F2, F4 dan F5. Pada F1 dan F3 jumlah populasi mengalami penurunan pada bulan kedua dan ketiga, namun penurunannya tidak terlalu signifikan (populasi bakteri masih dalam kisaran 108). Dengan demikian, dapat dikatakan bahwa semua formula masih layak digunakan sampai masa simpan tiga bulan.
Hasil uji aktivitas formula terhadap pertumbuhan tanaman dalam kondisi kekeringan ditunjukkan melalui enam parameter yaitu tinggi tanaman, bobot basah tajuk (BBT), bobot kering tajuk (BKT), bobot basah akar (BBA), bobot kering akar dan jumlah bintil akar (JBA). Faktor yang diperhatikan dalam uji ini yaitu faktor kadar air (basah dan kering) serta faktor formula (F0-F5), diharapkan terjadi interaksi di antara kedua faktor tersebut. Dua faktor ini dikatakan berinteraksi apabila pengaruh formula berubah pada saat kadar air berubah. Dengan kata lain interaksi ini menunjukkan efek formula yang bergantung pada kondisi kadar air. Berdasarkan hasil uji statistik (Tabel 10-15) diketahui bahwa interaksi antar faktor formula dengan faktor kadar air terjadi pada parameter BBA dan JBA. Oleh karena itu penyajian data difokuskan kepada pengaruh formula pada masing-masing taraf kadar air. Namun demikian, efektivitasnya belum serupa dengan efektivitas pada kadar air basah, terlihat dari nilai yang berbeda antara pengaruh formula pada kadar air basah dan kering.
Pada keadaan kadar air kering, formula F1 dan F2 mampu meningkatkan JBA secara signifikan (Tabel 15). Parameter JBA ini menunjukkan efektivitas Bradyrhizobium
japonicum dalam mengkolonisasi akar
sehingga terbentuk bintil akar. Semakin banyak kolonisasi B. japonicum dalam sistem perakaran tanaman maka fiksasi nitrogen semakin banyak sehingga kebutuhan nitrogen oleh tanaman dapat terpenuhi yang menyebabkan tanaman tumbuh dengan baik. Pada parameter BBA formula F2, F3 dan F4 mampu meningkatkan BBA secara signifikan. Parameter BBA ini menunjukkan status
serapan air oleh akar. Hal ini terkait dengan efektivitas bakteri dalam mensekresi eksopolisakarida. Akumulasi eksopolisakarida di zona perakaran berpotensi meningkatkan retensi air pada tanah di sekitar perakaran sehingga dengan mudah diserap oleh akar.
Parameter tinggi, BBT, BKT dan BKA tidak terjadi interaksi antara formula dan kadar air. Oleh karena itu penyajian data difokuskan kepada pengaruh rata-ratadari setiap formula. Namun demikian, secara umum terdapat formula yang tetap mampu meningkatkan pertumbuhan tanaman. Pada parameter tinggi, semua formulasi mampu meningkatkan tinggi tanaman secara signifikan. Parameter tinggi ini mengindikasikan efektivitas bakteri Bacillus
dan Pseudomonas dalam menghasilkan
hormon indol aceic acid (IAA) yang dapat memacu pertumbuhan tanaman. Pada parameter BBT dan BKA formula F4 mampu menunjukkan peningkatan secara signifikan. Parameter BBT menunjukkan status serapan air pada sel-sel tanaman. Hal ini dapat dikaitkan dengan efektivitas formula dalam membantu tanaman dalam menyerap air terutama dalam kondisi kekeringan. Parameter berat kering (akar dan tajuk) menunjukkan status hara yang diserap oleh tanaman serta laju fotosintesis yang terjadi. Hal ini mengindikasikan efektivitas bakteri
Pseudomonas sp. dan Bacillus sp dalam membantu menyediakan unsur hara bagi tanaman, diantaranya pengikatan unsur Fe melalui sekresi siderofor. Di samping itu, beberapa bakteri dalam paket formulasi memiliki kemampuan melarutkan fosfat serta pensekresi kitinase (Astuti 2008). Pada parameter BKT tidak ada formula yang mampu meningkatkan pertumbuhan tanaman secara signifikan.
Perbedaan pengaruh antar formula terhadap pertumbuhan tanaman diduga akibat perbedaan kemampuan masing-masing bakteri di dalam paket formula. Menurut Iqbal et al.
SIMPULAN
Sebanyak 7 isolat Pseudomonas (Crb16, Crb17, Crb60, Crb74, Crb82, Crb94, Crb95), 8 isolat Bacillus (Cr22, Cr28, Cr31, Cr44, Cr64, Cr66, Cr67, Cr71) dan 2 isolat Bradyrhizobium
japonicum (Bj11(wt), Bj11(19)) mampu
menghasilkan eksopolisakarida. Kombinasi dari isolat Crb, Cr dan Bj menghasilkan lima paket formula dengan gambut sebagai bahan pembawa. Viabilitas kelima formula tersebut masih stabil sampai masa penyimpanan bulan ketiga. Aplikasi formula F4 pada tanaman kedelai meningkatkan tinggi tanaman, berat basah tajuk, berat basah akar dan berat kering akar baik pada kondisi basah maupun kering. Pengujian menggunakan varietas tanaman toleran kekeringan masih diperlukan agar pengaruhnya pada tanaman di lahan kering dapat lebih maksimal.
DAFTAR PUSTAKA
Alikhani HA, Mohamadi L. 2010. Assesing tolerance of rhizobial lentil symbiosis isolates to salinity and drought in dry land farming condition. Di dalam: 19th World
Congress of Soil Science, Soil Solutions for a Changing World; Brisbane, 1-6 Agustus 2010.
Astuti RI. 2008. Rizobakteria Bacillus sp. asal tanah rizosfer kedelai yang berpotensi sebagai pemacu pertumbuhan tanaman [tesis]. Bogor: Sekolah Pascasarjana Institut Pertanian Bogor.
Astuti RI, Wahyudi AT, Mubarik NR. 2006. Cloning of genomic DNA fragment involved in acid-alumunium tolerance in
Bradyrhizobium japonicum through
transposon mutagenesis. Indones J
Microbiol :3 5-39.
Endarini T, Wahyudi AT, Tedja-Irnas. 1995. Seleksi galur-galur Bradyrhizobium japonicumindigenus toleran medium asam-Al. Hayati2: 15-8 1.
Gomez AK, Gomez AA. 2007. Prosedur Statistik Untuk Penelitian Pertanian Edisi Kedua. Sjamsuddin E, Baharsjah JS, penerjemah. Jakarta: UI Press. Terjemahan dari: Statistical Procedures for Agricultural Research.
Hendriyani IS, Setiari N. 2009. Kandungan klorofil dan pertumbuhan kacang panjang (
Vigna sinensis) pada tingkat penyediaan air yan berbeda. J Sains & Math 17: 145-150.
Hepper CM. 1975. Extracellular polysacharides of soil bacteria. Di dalam: Walker N, editor. Soil microbiology, a critical review. New York : Willey.
Iqbal A, Bhatti HN, Nosheen S, Jamil A, Malik MA. 2002. Histochemical and physicoshemical study of bacterial exopolysaccharides. Biotechnol 1:28-33 Kloepper JW. 1992. Plant growth promoting
rhizobacteria as biological control agents. Di dalam: Meeting Jr, editor. Soil Microbial Ecology, Aplications in Agricultural and Environmental Management. New York: Marcel Dekker Inc.
Kristin N. 2009. Formulasi campuran rizobakteria pelarut fosfat dengan
Bradyrhizobium japonicum menggunakan gambut sebagai bahan pembawa [skripsi] Bogor : Fakultas Matematika dan Ilmu Pengetahuan Alam, Institut Pertanian Bogor.
Manchanda I, Garg. 2008. Salinity and its effect on the functional biology of legumes.
J Plant Physiol 7: 1-45.
Michel BE, Kaufmann MR. 1973. The osmotic of polyethylene glycol 6000. J Plant Physiol 51: 914-916.
Mubarik NR, Wahyudi AT, Imas T. 2009. Potensi Bradyrhizobium japonicum toleran asam-aluminium sebagai inokulan pada tanaman kedelai. Di dalam: Prosiding Seminar Hasil – hasil Penelitian IPB.
Bogor: Institut Pertanian Bogor. Hlm 655-665.
Roberson EB, Firestone M. 1992. Relationship between desiccation and exopolysaccharide production in a soil Pseudomonas sp. Appl Environ Microbiol 58: 1284-1291
Sandhya V, Ali SK, Grover M, Reddy G, Venkatcswarlu B. 2009. Alleviation of drought stress effect in sunflower seedlings by the exopolysaccharides producing
Pseudomonas putida strain GAP-P45. Biol Fertil Soil 46: 17-26.
Salisbury FB, Ross CW. 1995. Fisiologi
Tumbuhan Jilid 3. Lukman DR,
Sumaryono, penerjemah. Bandung: ITB Press. Terjemahan dari: Plant Physiology.
13
Tahar. 2009. Rizobakteria Pseudomonas sp. dan Bacillus sp. toleran asam aluminium sebagai pemacu pertumbuhan tanaman dan pengendali fungi patogen akar tanaman kedelai [Tesis] Bogor : Fakultas Matematika dan Ilmu Pengetahuan Alam, Institut Pertanian Bogor.
Widyawati A. 2008. Bacillus sp. asal Rizosfer kedelai yang berpotensi sebagai pemacu pertumbuhan tanaman dan biokontrol fungi pathogen akar. [tesis]. Bogor: Sekolah Pascasarjana IPB.
15
1
DENAH RANCANGAN PERCOBAANKeterangan: P : Pintu A : Keran air M : Meja T : Timbangan K : Perlakuan kadar air kering B : Perlakuan kadar air basah F : Formulasi I, II, III : ulangan 1, 2 dan 3
P
K/F4-I K/F3-II
K/F2-I
B/F1-I
B/F3-I
K/F5-II
B/F5-III
B/F2-III
K/F0-II
B/F4-I
K/F2-III
B/F3-III
B/F2-I
B/F4-III
K/F5-III
K/F2-II
B/F1-II
B/F3-II
K/F1-II
B/F2-II
K/F1-III
B/F5-I
B/F4-II
K/F0-III
K/F1-I
B/F5-III
K/F4-II
K/F0-I
B/F0-II
K/F3-III K/F3-I
B/F0-III
B/F0-III K/F4-III
K/F5-I
B/F1-III
M
A
16
2
PERHITUNGAN KADAR AIR UNTUK UJI KEKERINGAN PADA TANAMAN DI RUMAH KACA1. Perhitungan Kadar Air Awal (tanpa perlakuan apa-apa)
10 gram tanah di oven selama 24 jam (sampai berat keringnya konstan) kemudian ditimbang, dihitung kadar airnya dengan rumus:
KA = BB – BK x 100% KA = kadar air
BB BW = berat wadah BB = berat basah BK = berat kering Tabel 1 Hasil pengukuran kadar air tanah
BW (g) BB (g)
BK-BW
(g) KA (%)
Rata-rata KA
Ulangan 1 0,609 10,000 8,725 12,749
12,997 ~13 % Ulangan 2 0,620 10,000 8,567 14,334
Ulangan 3 0,646 10,000 8,809 11,909
2. Perhitungan Kadar Air Kapasitas Lapang
1 kg/L tanah di dalam ember yang dibolongi bawahnya dijenuhkan dengan air sampai tergenang kemudian didiamkan selama 3 hari sampai tidak ada lagi air yang menetes. Tabel 2 Hasil pengukuran berat tanah pada kapasitas lapang
BE (g) BA BKL+BE
Rata-rata BKL+ BE
BKL-BE
Ulangan 1 72 1000 1282
1285,3 ~1286 g
1214
Ulangan 2 72 1000 1286
Ulangan 3 72 1000 1288
Ket : BE = Berat Ember
BA = Berat tanah awal (sebelum dijenuhkan dengan air) BKL = Berat tanah pada kapasitas lapang
Diketahui :
Kadar Air awal = 13 % Berat Tanah Awal+ Ember = 1000 gram
Berat tanah tanpa air pada tanah awal = 1000 – (13% x 1000) = 1000 – 130 = 870 gram Kadar Air kapasitas Lapang = 1214 gram
Kadar Air Kapasitas Lapang = 1214 – 870 x 100% = 28 % 1214
½ Kapasitas lapang =( Kadar Air kapasitas Lapang – Kadar Air Awal) + Kadar Air Awal 2
= 28 % - 13% = 7.5 % + 13% = 20.5 % 2
Perhitungan berat tanah+air+ember untuk perlakuan setengah kapasita lapang
=Berat tanah tanpa air + 20,25% berat tanah awal = 870 + 20.5% x 1000 = 870 + 205 = 1075 Berat perlakuan setengah kapasitas lapang :
= BK + BE = 1075 + 72 = 1147 Perlakuan :
1. Kapasitas Lapang , ditambahkan air sedemikian rupa sehingga berat tanah+ember+air mencapai 1286 gram dengan estimasi kadar air sebesar 28%