IDENTIFIKASI KERAGAMAN GEN
β
-KASEIN (CSN2) PADA
KAMBING PERANAKAN ETAWAH, SAANEN DAN
PERSILANGANNYA DENGAN
METODE PCR-SSCP
SKRIPSI FERDY SAPUTRA
DEPARTEMEN ILMU PRODUKSI DAN TEKNOLOGI PETERNAKAN FAKULTAS PETERNAKAN
RINGKASAN
Ferdy Saputra. D14070024. 2011. Identifikasi Keragaman Genβ-Kasein (CSN2) pada Kambing Peranakan Etawah, Saanen dan Persilangannya dengan Metode PCR-SSCP. Skripsi. Departemen Ilmu Produksi dan Teknologi Peternakan, Fakultas Peternakan, Institut Pertanian Bogor.
Pembimbing Utama : Ir. Sri Darwati, M.Si
Pembimbing Anggota : Prof. Dr. Ir. Cece Sumantri, M.Agr.Sc
Gen β-kasein secara langsung berkaitan dengan kualitas dan sifat susu. Keragaman gen β-kasein pada kambing perah di Indonesia telah berhasil diidentifikasi dengan metode Polymerase Chain Reaction-Single Strand Conformation Polymorphism (PCR-SSCP). Metode PCR-SSCP merupakan metode yang sensitif dalam mendeteksi adanya keragaman DNA. Metode ini merupakan pemisahan asam nukleat rantai tunggal (single stranded nucleic acids) hasil amplifikasi PCR dengan elektroforesis melalui gel poliakrilamid dan berdasarkan pada perbedaan berat molekul pasangan basa, sehingga dapat menghasilkan perbedaan struktur sekunder gen.
Berdasarkan pola migrasi, kambing PE di lokasi Ciapus ditemukan tiga genotipe, yaitu CC, AA dan CA. Kambing PE di lokasi Cariu dan Elang 45 ditemukan empat genotipe, yaitu CC, AA, CA dan AO. Kambing Saanen di lokasi Cijeruk ditemukan lima genotipe, yaitu CC, AA, OO, CA dan AO. Kambing Saanen di lokasi Cariu dan Taurus ditemukan empat genotipe, yaitu CC, AA, CA dan AO. Kambing PESA di lokasi Cariu ditemukan empat genotipe, yaitu AA, OO, CA dan AO. Kambing PESA di lokasi Balitnak hanya ditemukan dua genotipe, yaitu CC dan CA.
Pada kambing PE ditemukan frekuensi alel tertinggi pada alel C sebesar 0,66 dan frekuensi alel terendah pada alel O sebesar 0,00 keduanya di lokasi Ciapus. Kambing Saanen ditemukan frekuensi alel tertinggi pada alel A sebesar 0,66 di populasi Cijeruk dan frekuensi alel terendah pada alel O sebesar 0,12 di populasi Taurus. Kambing PESA ditemukan frekuensi alel tertinggi pada alel C sebesar 0,83 dan frekuensi alel terendah pada alel O sebesar 0,00 keduanya di lokasi Balitnak.
Keragaman gen β-kasein pada Kambing PE, Saanen dan persilangannya sangat tinggi dengan ditemukannya tiga alel, yaitu C, A dan O. Pada Kambing PE di Cariu dan Elang 45 ditemukan tiga genotipe, yaitu CC, AA, CA dan AO. Kambing Saanen di Cijeruk dan Kambing PESA di Cariu ditemukan lima genotipe, yaitu CC, AA, OO, CA dan AO. Alel A merupakan alel yang frekuensinya tinggi pada kambing PE, Saanen dan PESA yang berada di hampir semua lokasi dalam penelitian ini kecuali pada kambing PE di Ciapus dan kambing PESA di Balitnak.
ABSTRACT
Identification ofβ-Kasein Gene in Local Dairy Goat Using SSCP-PCR Method
Saputra, F., S. Darwati and C. Sumantri
Casein genetic polymorphisms are important and well known due to their effects on quantitative traits and properties of milk. β-kasein gene is directly related to the quality and properties of milk. A protocol for the rapid and simultaneous genotyping of β-kasein alleles was conducted by single strand conformational polymorphism polymerase chain reaction (SSCP-PCR) method in goat. Screening β-kasein gene variability in 3 dairy goat breeds was conducted for Etawah Grade (77 samples), Saanen (67 samples) and PESA (Crossbreed Etawah Grade with Saanen) (29 samples) in Bogor and Sukabumi. The objective of this research was to identify polymorphism of theβ-kasein (CSN2) gene in dairy goat. This research found three alleles of the β-casein gene, ie CSN2*A, CSN2*C, dan CSN2*O. In most breeds, CSN2*O occurred in the lowest frequency. The identification of the CSN2 gene variability in the goat breeds indicated the highly of theAallele. The CSN2*Aallele had a high frequency in Saanen in Cijeruk (0,66); Etawah Grade in Cariu (0,62); and PESA in Cariu (0,54). While the CSN2*C allele had a high frequency in PESA in Balitnak (0,83); Etawah Grade in Ciapus (0,48); and Saanen in Taurus (0.38). Based on the results of chi-square analysis, found that Saanen in Cariu and Taurus were not in Hardy-Weinberg equilibrium.
IDENTIFIKASI KERAGAMAN GEN
β
-KASEIN (CSN2) PADA
KAMBING PERANAKAN ETAWAH, SAANEN DAN
PERSILANGANNYA DENGAN
METODE PCR-SSCP
Ferdy Saputra
D14070024
Skripsi ini merupakan salah satu syarat untuk memperoleh gelar Sarjana Peternakan pada
Fakultas Peternakan Institut Peternakan Bogor
DEPARTEMEN ILMU PRODUKSI DAN TEKNOLOGI PETERNAKAN FAKULTAS PETERNAKAN
Judul : Identifikasi Keragaman Gen β-Kasein pada Kambing Peranakan Etawah, Saanen dan Persilangannya dengan Metode PCR-SSCP Nama : Ferdy Saputra
NIM : D14070024
Menyetujui,
Pembimbing Utama, Pembimbing Anggota,
(Ir. Sri Darwati, M.Si) (Prof. Dr. Ir. Cece Sumantri, M.Agr.Sc) NIP: 19631003 198903 2 001 NIP: 19591212 198603 1 004
Mengetahui, Ketua Departemen
Ilmu Produksi dan Teknologi Peternakan
RIWAYAT HIDUP
Penulis dilahirkan pada tanggal 18 Maret 1990 di Rangkasbitung, Banten. Penulis adalah anak pertama dari tiga bersaudara dari pasangan Bapak Jap Soey Liong dan Ibu Mimih Riyati.
Penulis mengawali pendidikan dasar pada tahun 1995 di Sekolah Dasar Mardi Yuana Rangkasbitung dan diselesaikan pada tahun 2001. Pendidikan lanjutan tingkat pertama dimulai pada tahun 2001 dan diselesaikan pada tahun 2004 di Sekolah Lanjutan Tingkat Pertama Mardi Yuana Rangkasbitung. Penulis melanjutkan pendidikan di Sekolah Menengah Atas Negeri 3 Rangkasbitung pada tahun 2004 dan diselesaikan pada tahun 2007.
KATA PENGANTAR
Puji dan syukur Penulis panjatkan kepada Tuhan yang Maha Esa, atas rahmat dan karunia yang diberikan-Nya sehingga Penulis dapat menyelesaikan studi, penelitian dan penulisan skripsi ini. Skripsi ini berjudul Identifikasi Keragaman Gen
β-Kasein pada Kambing Peranakan Etawah, Saanen dan Persilangannya dengan Metode PCR-SSCP.
Kambing merupakan ternak yang banyak digunakan sebagai ternak penghasil daging dan susu (dwiguna). Kambing dapat hidup di daerah kering dan dapat memanfaatkan hijauan pakan secara efisien. Ternak kambing mempunyai potensi untuk berkembang karena mempunyai kemampuan beradaptasi cukup tinggi. Konsumsi susu dan impor susu akan terus meningkat, sehingga perlu peningkatan populasi ternak perah, efisiensi produksi susu dan diversifikasi ternak perah. Pemeliharaan kambing perah merupakan salah satu alternatif upaya diversifikasi ternak perah dan peningkatan produksi susu. Indonesia memiliki beberapa jenis ternak kambing perah, yaitu kambing Saanen, Peranakan Etawah dan PESA (Persilangan Peranakan Etawah dan Saanen).
Tujuan dari penelitian ini adalah untuk mengidentifikasi keragaman gen
β-kasein (CSN2) pada kambing Peranakan Etawah, Saanen dan PESA (Persilangan Peranakan Etawah dan Saanen) dengan menggunakan metode Polymerase Chain Reaction-Single Strand Conformation Polymorphism(PCR-SSCP). Penulis berharap, semoga skripsi ini dapat memberikan sumbangan yang berarti bagi kemajuan dunia peternakan Indonesia. Amin.
Bogor, 11 Mei 2011
DAFTAR ISI
Kambing Lokal Indonesia ... 3
Kambing Peranakan Etawah ... 5
Kambing Saanen ... 5
Kambing PESA (Persilangan Peranakan Etawah dengan Saanen)... 6
Protein Susu ... 6
β-Kasein ... 7
Keragaman Genβ-Kasein ... Polymerase Chain Reaction-Single Strand Conformation Polymorphism (PCR-SSCP) ... 9
Pewarnaan Perak (Silver Staining) ... 10
Hukum Keseimbangan Hardy-Weinberg ... 11
MATERI DAN METODE ... 12
Lokasi dan Waktu ... 12
Materi Sampel Darah dan Bahan Ekstraksi DNA ... 12
Polymerase Chain Reaction(PCR) ... 12
Polymerase Chain Reaction-Single Strand Conformation Polymorphism(PCR-SSCP) ... 13
Formamida Dye ... 13
Pewarnaan Perak (Silver Staining) ... 13
Prosedur ... 14
Pengambilan Sampel Darah ... 14
Ekstraksi DNA ... 14
Amplifikasi DNA ... 14
Pendeteksian Keragaman Genβ-Kasein dengan Metode (PCR-SSCP) ... 14
Pewarnaan Perak ... 14
Penentuan Genotipe ... 15
Analisis Data ... 15
Frekuensi Genotipe ... 15
Frekuensi Alel ... 16
Hukum Keseimbangan Hardy-Weinberg ... 16
Heterozigositas ... 17
HASIL DAN PEMBAHASAN ... 18
Amplifikasi Genβ-Kasein ... 18
Keragaman Genβ-Kasein ... 18
Frekuensi Genotipe, Alel dan Heterozigositas ... 20
Keseimbangan Hardy-Weinberg ... 23
KESIMPULAN DAN SARAN ... 25
Kesimpulan ... 25
Saran ... 25
UCAPAN TERIMAKASIH ... 26
DAFTAR PUSTAKA ... 27
DAFTAR TABEL
Nomor Halaman
1. Komposisi Protein Susu Ternak Ruminansia ... 7 2. Hasil Frekuensi Alel GenCSN2dengan Metode SSCP ... 8 3. Identitas Sampel Darah ... 12 4. Frekuensi Genotipe Gen β-Kasein pada Kambing PE, Saanen dan
PESA ... 20 5. Frekuensi Alel dan Heterozigositas Genβ-Kasein pada Kambing
DAFTAR GAMBAR
Nomor Halaman
1. Rekonstruksi Struktur Gen β-Kasein Berdasarkan Sekuens Gen
β-Kasein diGenBank (Kode Akses AF409096) ... 9 2. Sekuens Primer GenCSN2pada Kambing ... 13 3. Diagram Elektroforesis (Zymogram) untuk Alel CSN2*A,CSN2*C
danCSN2*0’pada Genβ-Kasein ... 15 4. Hasil Amplifikasi Genβ-Kasein Menggunakan Metode PCR pada
Gel Poliakrilamida 6% ... 18 5. Visualisasi Pola Pita Genβ-Kasein pada Gel Poliakrilamida 10%
dengan Metode PCR-SSCP ... 19 6. Rekonstruksi Pola Pita Genβ-Kasein pada Kambing PE, Saanen
DAFTAR LAMPIRAN
Nomor Halaman
1. Modifikasi Metode Ekstraksi DNA Menggunakan Metode
Sambrook ... 31 2. Informasi Sekuen Genβ-Kasein pada Ternak Kambing ... 32 3. Jumlah Genotipe Gen β-Kasein pada Kambing PE, Saanen dan PESA
PENDAHULUAN
Latar Belakang
Kambing perah merupakan salah satu ternak alternatif yang banyak digunakan sebagai ternak penghasil susu selain sapi perah. Kambing dapat hidup di daerah kering dan dapat memanfaatkan hijauan pakan secara efisien. Ternak kambing mempunyai potensi untuk berkembang karena mempunyai kemampuan beradaptasi cukup tinggi.
Jumlah produksi susu segar di Indonesia sebanyak 647 ton pada tahun 2008 (Direktorat Jenderal Peternakan, 2008). Impor produk susu pada tahun 2008 di Indonesia sebesar 665.159,5 ton (Badan Pusat Statistika, 2008). Dari data tersebut, produksi susu nasional belum mampu memenuhi seluruh kebutuhan konsumsi nasional. Konsumsi susu dan impor susu akan terus meningkat, sehingga perlu peningkatan populasi ternak perah, efisiensi produksi susu dan diversifikasi ternak perah.
Populasi kambing di Indonesia pada tahun 2008 berjumlah sekitar 15.147.432 ekor (Direktorat Jenderal Peternakan, 2008). Data tersebut merupakan jumlah seluruh bangsa kambing yang ada di Indonesia. Jadi, kemungkinan jumlah kambing perah di Indonesia tidak terlalu banyak. Untuk itu, perlu peningkatan jumlah kambing perah di Indonesia. Pemeliharaan kambing perah juga merupakan salah satu alternatif upaya diversifikasi ternak perah dan peningkatan produksi susu. Indonesia memiliki beberapa jenis ternak kambing perah, yaitu kambing Saanen, Peranakan Etawah dan Persilangan Peranakan Etawah dan Saanen (PESA).
2 (PCR-SSCP). Keragaman gen β-kasein pada kambing perah di Indonesia telah berhasil diidentifikasi dengan metode PCR-SSCP. Polymerase Chain Reaction-Single Strand Conformation Polymorphism merupakan metode yang sensitif dalam mendeteksi adanya keragaman DNA.
Tujuan
TINJAUAN PUSTAKA
Klasifikasi Kambing
Kambing diklasifikasikan kedalam kingdom Animalia; phylum Chordata; subphylum Vertebrata; class Mamalia; ordo Artiodactyla; sub-ordo Ruminantia;
family Bovidae; sub family Caprinae dan genus Capra (Mileski, 2004). Kambing (Capra hircus) memiliki 60 kromosom (30 pasang kromosom) yang terdiri dari 29 pasang kromosom autosom dan sepasang kromosom kelamin (Gall, 1981).
Penyebaran kambing sangat luas dan hampir menyebar di seluruh dunia. Hal ini disebabkan, kambing memiliki daya adaptasi yang baik terhadap berbagai iklim dan kemampuannya bertahan hidup pada daerah dengan hijauan terbatas (Gall, 1981). Kambing merupakan ternak yang dapat hidup di daerah kering dan daerah dengan hijauan pakan yang mungkin tidak disukai oleh ternak lain, serta dapat memanfaatkan hijauan pakan secara efisien (Devendra dan Burns, 1994).
Kambing Lokal Indonesia
Kambing Marica yang terdapat di Propinsi Sulawesi Selatan merupakan salah satu genotipe kambing asli Indonesia yang menurut laporan FAO sudah termasuk kategori langka dan hampir punah (endangered). Kambing Marica mempunyai potensi genetik yang mampu beradaptasi baik di daerah agro-ekosistem lahan kering, yaitu daerah dengan curah hujan sepanjang tahun sangat rendah. Kambing Marica dapat bertahan hidup pada musim kemarau walau hanya memakan rumput-rumput kering di daerah tanah berbatu-batu (Pamungkas et al., 2009).
4 Kambing Muara dijumpai di daerah Kecamatan Muara, Kabupaten Tapanuli Utara di Propinsi Sumatera Utara. Penampilan kambing ini gagah, tubuh kompak dan sebaran warna rambut bervariasi antara warna rambut coklat kemerahan, putih dan ada juga yang berwarna rambut hitam. Bobot kambing Muara lebih besar dibandingkan dengan kambing Kacang dan diduga kambing prolifik (Pamungkas et al., 2009).
Kambing Kosta terdapat di sekitar Jakarta dan Propinsi Banten (Setiadi dan Sutama, 1987). Kambing ini dilaporkan mempunyai bentuk tubuh sedang, hidung rata dan kadang-kadang ada yang melengkung, tanduk pendek dan berambut pendek. Kambing ini diduga terbentuk dari persilangan kambing Kacang dengan salah satu rumpun kambing impor (Khasmir/Angora/Etawah) (Pamungkaset al., 2009).
Kambing Gembrong terdapat di daerah kawasan Timur Pulau Bali terutama di Kabupaten Karangasem. Ciri khas dari kambing ini adalah berambut panjang. Panjang rambut berkisar 15-25 cm, bahkan rambut pada bagian kepala sampai menutupi muka dan telinga. Rambut panjang terdapat pada kambing jantan, sedangkan kambing Gembrong betina berambut pendek berkisar 2-3 cm (Pamungkas
et al., 2009).
Kambing Kacang merupakan kambing asli Indonesia juga didapati di Malaysia dan Filipina. Kambing Kacang sangat cepat berkembangbiak, pada umur 15-18 bulan sudah bisa menghasilkan keturunan. Kambing ini cocok sebagai penghasil daging dan kulit, bersifat prolifik, tahan terhadap berbagai kondisi dan mampu beradaptasi dengan baik di berbagai lingkungan yang berbeda termasuk dalam kondisi pemeliharaan yang sangat sederhana. Ciri-ciri kambing Kacang adalah antara lain rambut pendek dan berwarna tunggal (putih, hitam dan coklat) (Pamungkaset al., 2009).
Kambing Peranakan Etawah (PE)
Salah satu jenis kambing perah di daerah tropis khususnya di Indonesia adalah kambing Peranakan Etawah. Kambing PE merupakan hasil persilangan antara kambing Etawah dan kambing lokal Indonesia. Disamping sebagai ternak penghasil susu, pejantan kambing PE juga dapat dimanfaatkan untuk meningkatkan potensi produksi susu kambing lokal Indonesia lainnya dengan inseminasi buatan (IB) (Souhokaet al., 2009). Diharapkan dengan persilangan tersebut akan dihasilkan kambing yang mampu memproduksi susu dan daging cukup tinggi (dual purpose).
Kambing PE dapat menghasilkan daging dan susu (kambing tipe dwiguna). Kambing PE betina memiliki kemampuan menghasilkan susu yang cukup baik. Menurut Atabanyet al. (2001), produksi susu kambing PE adalah 0,99 kg/ekor/hari. Rataan bobot lahir kambing PE kelahiran tunggal betina 3,2 kg, jantan 3,7 kg (Setiadi dan Sutama, 1997).
Ciri khas kambing PE antara lain bentuk muka cembung melengkung dan dagu berjanggut, terdapat gelambir di bawah leher yang tumbuh berawal dari sudut janggut, telinga panjang, lembek menggantung dan ujungnya agak berlipat, ujung tanduk agak melengkung, tubuh tinggi, pipih, bentuk garis punggung mengombak ke belakang, rambut tumbuh panjang di bagian leher, pundak, punggung dan paha, bulu paha panjang dan tebal. Warna rambut ada yang tunggal; putih, hitam dan coklat, tetapi jarang ditemukan. Kebanyakan terdiri dari dua atau tiga pola warna, yaitu belang hitam, belang coklat dan putih bertotol hitam (Pamungkaset al., 2009).
Kambing Saanen
Kambing Saanen berasal dari Swiss Barat. Kambing ini berwarna putih, krem pucat atau coklat muda dengan bercak hitam pada hidung, telinga dan ambing. Kambing ini berambut pendek dan telinganya agak tegak serta mengarah ke depan. Kambing Saanen memiliki rataan produksi susu tertinggi dibanding bangsa kambing lainnya (Devendra dan Burns, 1994). Kambing Saanen memiliki rataan produksi susu 216 kg dengan panjang laktasi 275 hari (Gall, 1981). Menurut Devendra dan Burns (1994), kambing Saanen memiliki rataan hasil susu harian sebanyak 1,06 kg/ekor/hari. Kambing Saanen biasanya dipelihara dan diberi pakan dalam kandang.
6 merupakan kambing yang tidak memiliki tanduk. Kambing Saanen memiliki tubuh dengan konformasi tipe perah yang baik dan ambing yang berkembang baik pula. Jumlah anak lahir seperindukan 1,80 ekor (Devendra dan Burns, 1994). Rataan berat badan kambing betina dan jantan Saanen adalah 65 dan 75 kg (Devendra dan McLeroy, 1982).
Kambing PESA (Persilangan Peranakan Etawah dengan Saanen)
Kambing PESA merupakan kambing hasil persilangan antara kambing Peranakan Etawah (PE) betina dengan kambing Saanen jantan. Kambing PESA memiliki produksi susu harian yang lebih baik daripada Peranakan Etawah tetapi produksinya lebih rendah daripada kambing Saanen. Hal ini dibuktikan dengan produksi susu harian dari kambing Saanen (F1) dan PESA di PT. Taurus Dairy Farm masing-masing sebanyak 1,19 dan 1,12 kg/ekor/hari (Ruhimat, 2003).
Protein Susu
Susu merupakan sumber makanan alami bagi hewan mamalia yang baru dilahirkan. Produksi susu merupakan salah satu dari sifat kuantitatif yang dikendalikan oleh banyak pasangan gen yang aksinya bersifat aditif (Velmalaet al., 1999). Produksi susu dalam satu spesies sangat dipengaruhi oleh bangsa, umur, nutrisi, kesehatan, musim dan lain-lain (Fox dan Mc Sweeney, 1998). Susu dari ternak terdiri dari sebagian air yang terlarut pada protein, gula susu (laktosa), mineral dan vitamin-vitamin yang larut dalam air.
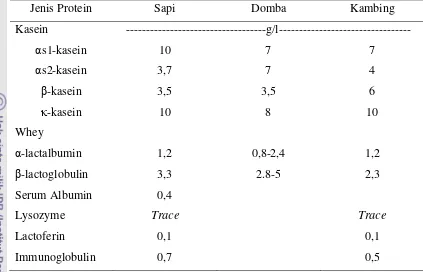
Tabel 1. Komposisi Protein Susu Ternak Ruminansia
Jenis Protein Sapi Domba Kambing
Kasein
---g/l---αs1-kasein 10 7 7
αs2-kasein 3,7 7 4
β-kasein 3,5 3,5 6
κ-kasein 10 8 10
Whey
α-lactalbumin 1,2 0,8-2,4 1,2
β-lactoglobulin 3,3 2.8-5 2,3
Serum Albumin 0,4
Lysozyme Trace Trace
Lactoferin 0,1 0,1
Immunoglobulin 0,7 0,5
Sumber: Martin dan Grosclaude (1993)
β-Kasein
β-kasein adalah bagian yang paling hidrofobik dari kasein dan mengandung sejumlah besar prolin residu, memiliki ujung terminal hidrofilik C dan akhir terminal hidrofobik N (Creamer, 2003). β-kasein terdiri dari 209 asam amino (Martin et al., 2003), dan memiliki massa molekul 24,0 kDa (kilo Dalton) (Creamer, 2003); mengandung lima kelompok phosphoseryl. β-kasein terkandung sekitar 60% dari total kasein dalam susu kambing (Trujilloet al., 1997).
Keragaman Genβ-Kasein
Gen β-kasein merupakan gen yang berpengaruh terhadap produksi susu, persentase protein dan hasil protein (Bovenhuis et al., 1992). Gen β-kasein secara langsung berkaitan dengan kualitas dan sifat susu (Sztankóováet al., 2005). Namun, dalam penelitian Moatsouet al. (2008), genotipeβ-kasein tidak berhubungan dengan kandunganβ-kasein dalam susu.
-8 (2006), gen protein susu terdiri αs1-kasein (CSN1S1), β-kasein (CSN2), κ-kasein (CSN3) dan β-lactoglobulin (LGB). Polimorfisme gen-gen kasein yang tinggi berpengaruh langsung terhadap produksi dan komposisi susu sapi perah (Ng-Kwai-Hanget al., 1986).
Menurut Bovenhuiset al. (1992), genotipeβ-kasein sapi adalah A1A1, A1A2, A2 A2, A1 B, B B, A1 A3, A2 A3, dan A3 B. Selanjutnya Chessa et al. (2005) mengemukakan bahwa variasi genetik β-kasein kambing pada ekson 7 adalah
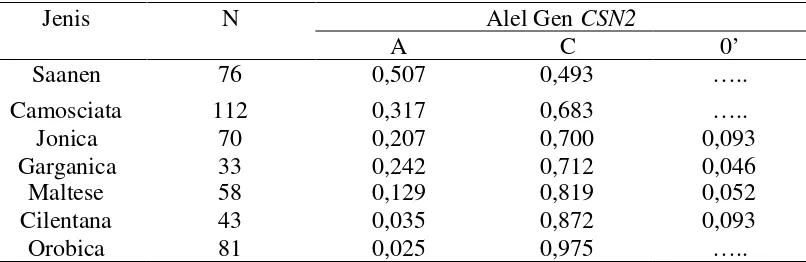
CSN2*A, CSN2*C dan CSN2*0’. Hasil frekuensi alel gen CSN2 menurut Chessa et al. (2005) disajikan dalam Tabel 2.
Tabel 2. Hasil Frekuensi Alel GenCSN2dengan Metode SSCP
Jenis N Alel Gen CSN2
A C 0’
Saanen 76 0,507 0,493 …..
Camosciata 112 0,317 0,683 …..
Jonica 70 0,207 0,700 0,093
Garganica 33 0,242 0,712 0,046
Maltese 58 0,129 0,819 0,052
Cilentana 43 0,035 0,872 0,093
Orobica 81 0,025 0,975 …..
Sumber: Chessaet al. (2005)
I1 I2 I3 I4 I5 I6 I7 I8
E1 E2 E3 E4 E5 E6 E7 E8 E9
Flanking region 5’ flanking region 3’
Keterangan :
Lokus = AF409096
Panjang = 13671 bp
Gen = 4546-4593, 6588-6650, 7384-7410, 7523-7549, 9896-9919, 10016-10057, 11387 -11881, 12464-12505, 13233-13555
Sekuen depan = 4545 = 4545 bp
Ekson 1 (E1) = 4546-4593 = 47 bp Intron 1 (I1) = 4594 -6587 = 1993 bp
Gambar 1. Rekonstruksi Struktur Genβ-Kasein Berdasarkan Sekuens Genβ-Kasein diGenBank (Kode Akses AF409096)
Sumber: Wanget al. (2001)
Polymerase Chain Reaction-Single Strand Conformation Polymorphism
(PCR-SSCP)
Metode ini merupakan pemisahan asam nukleat rantai tunggal (single stranded nucleic acids) hasil amplifikasi PCR dengan elektroforesis melalui gel poliakrilamid dan berdasarkan pada perbedaan berat model pasangan basa, sehingga dapat menghasilkan perbedaan struktur sekunder gen. Suatu metode sederhana yang dapat digunakan untuk mendeteksi mutasi DNA yang disebut dengan PCR-SSCP (Oritaet al., 1989).
10 elektroforesis dalam gel poliakrilamida nondenaturasi (Natarajet al., 1999 ; Hidayat
et al., 2010).
Faktor-faktor yang mempengaruhi sensitivitas SSCP yaitu: (1) Komposisi gel, ukuran fragmen DNA, konsentrasi DNA, dan kandungan basa G dan C dalam fragmen DNA (Nataraj et al., 1999); (2) Komposisi buffer (termasuk kekuatan ion dan derajat keasaman,bufferaditif seperti gliserol dan suhu pada saat elektroforesis (Sheffieldet al., 1993 dan Natarajet al., 1999); (3) Persentase Akrilamida dan rasio
bis (Sheffield et al., 1993); (4) Lokasi mutasi pada fragmen DNA (Baroso et al., 1999); dan (5) Kelebihan dNTP dan primer dalam reaksi PCR.
Kelebihan metode PCR-SSCP dibanding metode lain yaitu: (1) sederhana dan tidak memerlukan peralatan yang rumit dan khusus (Bastos et al., 2001; Nataraj et al., 1999), (2) dapat mendeteksi adanya mutasi pada fragmen DNA (Baroso et al., 1999) sehingga dapat dibedakan dengan yang normal (Nataraj et al., 1999), (3) visualisasi tidak perlu menggunakan bahan radioaktif (Nataraj et al., 1999), dan (4) dapat dikerjakan di laboratorium biasa dan tidak terlalu mahal (Bastoset al.,2001).
Kekurangan PCR-SSCP yaitu ukuran fragmen DNA yang dapat dianalisis terbatas, butuh kondisi yang beragam untuk mendeteksi semua kemungkinan mutasi, kadang-kadang sulit untuk menginterpretasikan pita-pita yang dihasilkan dan tidak efisien untuk fragmen DNA yang tidak diketahui urutan nukloetidanya (Nataraj et al., 1999).
Menurut Gasser et al. (2006), konformasi dalam metode SSCP dipengaruhi oleh panjang fragmen, urutan, lokasi, dan jumlah wilayah pasangan basa. Oleh karena itu, mutasi pada posisi nukleotida tertentu dalam urutan primer dapat mengubah konformasi molekul. Ketika dipisahkan dalam gel non-denaturing, molekul berbeda dengan nukleotida tunggal bisa dilihat, mengingat perubahan dalam mobilitas.
Pewarnaan Perak (Silver Staining)
alkali. Pewarnaan perak terhadap asam nukleat secara luas digunakan untuk mendeteksi DNA dalam metode PCR-SSCP (Byunet al., 2009).
Hukum Keseimbangan Hardy-Weinberg
MATERI DAN METODE
Lokasi dan Waktu
Penelitian ini dilaksanakan selama enam bulan, yaitu mulai bulan November 2010 sampai April 2011. Penelitian ini dilaksanakan di Laboratorium Genetika Molekuler Ternak, Bagian Pemuliaan dan Genetika Ternak, Departemen Ilmu Produksi dan Teknologi Peternakan, Fakultas Peternakan, Institut Pertanian Bogor.
Materi
Sampel Darah dan Bahan Ekstraksi DNA
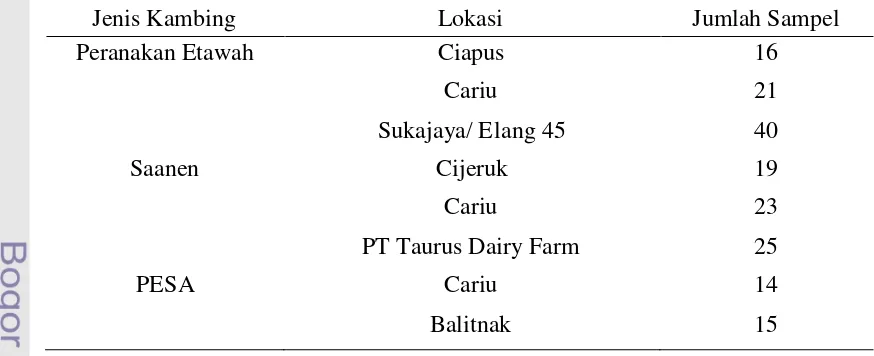
Sampel darah kambing betina yang digunakan berjumlah 173 sampel terdiri dari kambing Saanen (77 sampel), kambing PE (67 sampel) dan kambing PESA (Persilangan kambing PE dan Saanen) (29 sampel). Sampel tersebut merupakan sampel darah koleksi Laboratorium Genetika Molekuler Ternak. Bahan-bahan yang digunakan untuk mengekstraksi DNA adalah TE (Tris EDTA), STE (Sodium Tris-EDTA), NaCl, SDS, CIAA (kloroform isoamil alkohol) dan etanol. Identitas sampel darah serta rincian sampel per lokasi disajikan pada Tabel 3.
Tabel 3. Identitas Sampel Darah
Jenis Kambing Lokasi Jumlah Sampel
Peranakan Etawah Ciapus 16
Cariu 21
Sukajaya/ Elang 45 40
Saanen Cijeruk 19
Cariu 23
PT Taurus Dairy Farm 25
PESA Cariu 14
Balitnak 15
Polymerase Chain Reaction(PCR)
(Gambar 2). Polymerase Chain Reaction (PCR) menggunakan mesinthermocycler, tabung PCR, mikropipet, vortex dan alat sentrifugasi.
11521 ccttcagcct gaaataatgg gagtccccaa agtgaaggag actatggttc ctaagcacaa
11581 agaaatgccc ttccctaaat atccagttga gccctttact gaaagccaga gcctgactct
11641 cactgatgtt gaaaagctgc accttcctct gcctctggtc cagtcttgga tgcaccagcc
11701 tccccagcct ctttctccaa ccgtcatgtt tcctcctcag tccgtgctgt ccctttctca
11761 gcccaaagtt ctgcctgttc cccagaaagt agtgccccag agagatatgc ccatccaggc
11821 ctttctgctg taccaggagc ctgtacttgg tcctgtccgg ggacccttcc ctattcttgt
11881 aagtctaaat ttactaactg tgctgtttaa cttctgatgt ttgtatgata tttgagtaat
Keterangan: huruf tebal dan garis bawah merupakan situs primer
Gambar 2. Sekuens Primer GenCSN2pada Kambing Sumber: Wanget al. (2001)
Polymerase Chain Reaction-Single Strand Conformation Polymorphism
(PCR-SSCP)
Bahan-bahan yang diperlukan dalam Polymerase Chain Reaction-Single Strand Conformation Polymorphism (PCR-SSCP) adalah produk PCR dan
formamida dye. Alat yang digunakan adalah water bath, ice bath, refrigerator, Bio-Rad dan sentrifuse .
Formamida Dye
Komponenformamida dyeterdiri dari 80%formamida solution, 10 µl EDTA, 1 mg/mlbromthymol blue dan 1 mg/mlxylene cyanol.
Polyacrilamide Gel Elektroforesis(PAGE) 10%
Komponen Gel Polyakrilamida 10% terdiri dari 8,3 ml larutan 30% akrilamida (acrylamide : bisacrylamide =29 : 1); 2,5 ml larutan 5 x TBE (tris boric acid-EDTA); 15 µl TEMED (N,N,N’,N’-tetramethylethylenediamine); 150 µl 10% APS (ammonium peroxodisulfat) dan 14 ml air destilasi. Alat-alat yang digunakan adalah plat kaca cetakan gel berukuran 20 x 20 cm2, pipet mikro dan makro.
Pewarnaan Perak (Silver Staining)
Bahan-bahan yang digunakan dalam pewarnaan perak adalah AgNO3, NaOH,
14
Prosedur
Pengambilan Sampel Darah
Sampel darah diambil dari kambing pada vena jugularis di leher menggunakan tabungvaccutainer yang mengandung antikoagulan. Sampel tersebut kemudian disimpan dalam termos es dan suhunya dipertahankan sekitar 4oC.
Ekstraksi DNA
Ekstraksi DNA dilakukan dengan metode Sambrooket al. (1989) yang telah dimodifikasi (Lampiran 2).
Amplifikasi DNA
Campuran untuk mengamplifikasi DNA dalam mesin PCR terdiri dari 1 µl sampel DNA; 0,1 μl Primer; 0,1μl dNTP; 1 μl MgCl2; 1,25 μl DreamTaq Buffer;
0,05 μl Taq dan 8,5 μl air destilasi untuk volume akhir 12 µl. Proses amplifikasi terjadi dalam 30 siklus terdiri dari denaturasi awal pada suhu 94oC selama 5 menit, denaturasi akhir pada suhu 94oC selama 30 detik, penempelan primer (anneling) pada suhu 60 oC selama 45 detik, pemanjangan DNA (ekstensi awal) pada suhu 72 oC selama 1 menit dan ekstensi akhir pada suhu 72 oC selama 5 menit. Hasil amplifikasi DNA dianalisis dengan elektroforesis.
Pendeteksian Keragaman Genβ-Kasein dengan Metode PCR-SSCP
Produk PCR gen β-kasein sebanyak 5 µl disuspensikan dalam larutan
formamida dye sebanyak 5 µl, kemudian diinkubasi dalam water bath pada suhu 95 oC selama 7 menit. Setelah itu, segera didinginkan dengan ice bath selama 2 menit. Konformasi untai DNA dideteksi menggunakan PAGE 10%. Alat elektroforesis diatur pada tegangan 350 V selama 20 jam pada suhu 4oC. Perbedaan konformasi disebabkan oleh adanya mutasi minimal satu basa sehingga terjadi perbedaan migrasi pada pita DNA.
Pewarnaan Perak
Pewarnaan perak dilakukan dengan cara merendam gel dalam larutan A (200 ml air destilasi, 0,20 g AgNO3, 80 µl 10 N NaOH dan 800 µl amonia) selama 8 menit
selanjutnya menggunakan larutan B (6 g NaOH, 200 ml air destilasi dan 200 µl formaldehid dipanaskan pada suhu 60 oC) sampai pita muncul. Bila muncul pita, larutan B dibuang kemudian gel direndam dalam larutan asam asetat (100 ml air destilasi dan 100 µl asam asetat) untuk menghentikan reduksi perak.
Penentuan Genotipe
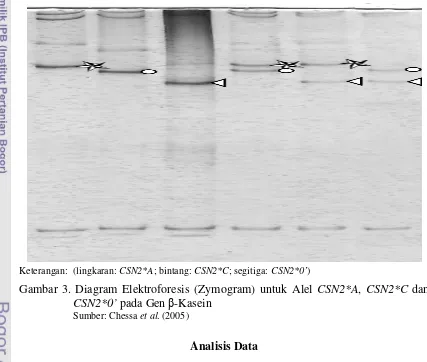
Keragaman genotipe masing-masing individu ditentukan dari migrasi pita-pita DNA yang muncul pada gel poliakrilamida. Penentuan genotipe Kambing PE, Saanen dan PESA berdasarkan Chessa et al. (2005) yang dapat dilihat pada Gambar 3.
Analisis Data
Keterangan: (lingkaran:CSN2*A; bintang:CSN2*C; segitiga:CSN2*0’)
Gambar 3. Diagram Elektroforesis (Zymogram) untuk Alel CSN2*A, CSN2*C dan
CSN2*0’pada Genβ-Kasein Sumber: Chessaet al. (2005)
Analisis Data
Frekuensi Genotipe
16 Keterangan:
= frekuensi genotipe ke ii = jumlah sampel bergenotipe ii N = jumlah seluruh sampel
Frekuensi Alel
Frekuensi alel merupakan rasio relatif suatu alel terhadap keseluruhan alel pada suatu lokus dalam populasi. Masing-masing sampel dibandingkan berdasarkan ukuran (marker) yang sama dan pita-pita DNA hasil SSCP diidentifikasi kemudian hasil identifikasi dihitung frekuensi alelnya dengan merujuk pada rumus (Nei dan Kumar, 2000):
Keterangan:
Xi = frekuensi alel kei
nii= jumlah sampel yang bergenotipeii
nij= jumlah sampel yang bergenotipeij N = jumlah seluruh sampel
Hukum Keseimbangan Hardy-Weinberg
Pengujian nilai genotipe antara hasil pengamatan dan nilai harapan dapat diukur dengan menggunakan uji Chi-Kuadrat (Nei dan Kumar, 2000):
Keterangan:
χ2
= chi-kuadrat O = nilai pengamatan E = nilai harapan
∑ = sigma (jumlah dari nilai-nilai)
Suatu populasi dikatakan seimbang jika nilai χ2 yang didapatkan lebih kecil
Heterozigositas
Tingkat keragaman genetik dalam sebuah populasi biasanya diukur dari rataan keanekaragaman gen, yang sering disebut rataan heterozigositas(Weir, 1996). Keragaman gen pada lokus dapat dilambangkan sebagai berikut:
Keterangan:
H = nilai heterozigositas
N1ij= jumlah individu heterozigot pada lokus ke-1
HASIL DAN PEMBAHASAN
Amplifikasi Genβ-Kasein
Amplifikasi gen β-kasein ekson tujuh pada kambing PE, Saanen dan PESA (Persilangan PE dan Saanen) dilakukan menggunakan metode PCR dengan mesin
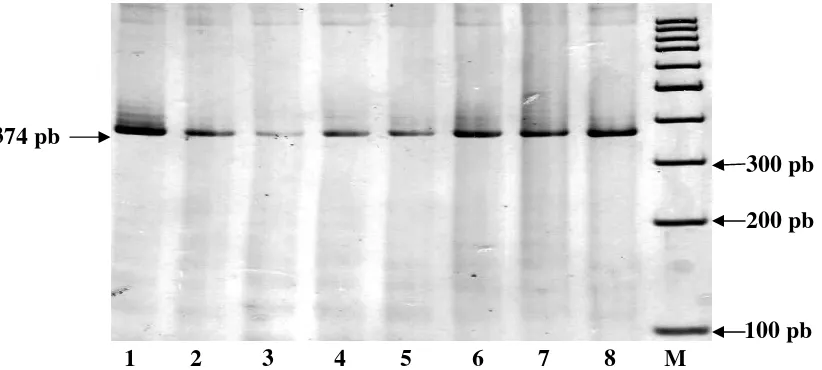
thermocycler (AB System). Pasangan primer yang digunakan mengikuti Cheesaet al. (2005). Suhu annealing adalah suhu yang memungkinkan terjadinya penempelan primer pada sekuen DNA sampel. Suhu anneling menjadi sangat penting dalam proses amplifikasi, hal itu disebabkan proses perpanjangan DNA baru dimulai dari primer. Suhu anneling yang digunakan dalam penelitian ini adalah 60 oC. Hasil amplifikasi genβ-kasein pada gel poliakrilamida 6% disajikan pada Gambar 4.
374 pb
300 pb
200 pb
100 pb
1 2 3 4 5 6 7 8 M
Gambar 4. Hasil Amplifikasi Genβ-Kasein Menggunakan Metode PCR pada Gel Poliakrilamida 6% (M: Marker 100 pb)
Panjang fragmen gen β-kasein ekson tujuh hasil amplifikasi adalah 374 pb (Cheesaet al., 2005). Panjang fragmen hasil amplifikasi dapat diketahui dengan cara mencocokkan situs penempelan primer pada sekuen gen β-kasein ekson tujuh (GenBank No. Acc. AF409096).
Keragaman Genβ-Kasein
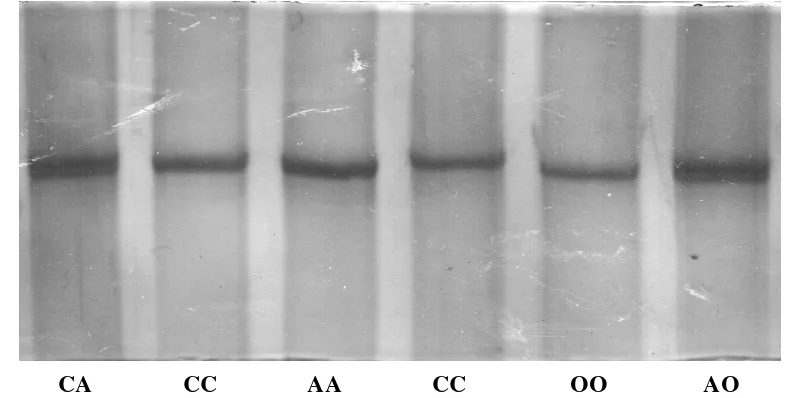
nukleotida yang akan mempengaruhi bentuk dari fragmen DNA untai tunggal (Bastoset al., 2001) akan menyebabkan pola migrasi pada saat elektroforesis dalam gel poliakrilamida (Baroso et al., 1999) walaupun perbedaannya hanya satu nukleotida saja (Nataraj et al., 1999). Hasil pendeteksian keragaman gen β-kasein menggunakan metode PCR-SSCP pada gel poliakrilamida 10% divisualisasikan pada Gambar 5 dengan Genotipe CA, CC, AA, OO dan AO yang direkonstruksi pada Gambar 6.
CA CC AA CC OO AO
Gambar 5. Visualisasi Pola Pita Gen β-Kasein pada Gel Poliakrilamida 10% dengan Metode PCR-SSCP
CA CC AA CC OO AO
20 Perbedaan hasil pendeteksian keragaman dengan metode PCR-SSCP sangat bergantung kepada perubahan bentuk dari ikatan utas tunggal DNA. Bentuk dari utas tunggal DNA dalam gel dipengaruhi oleh beberapa faktor, diantaranya adalah panjang fragmen, pemilihan matriks gel, suhu, konsentrasi ion dan konsentrasi larutan dalam gel (Hayashi, 1991). Menurut Gasser et al. (2006), konformasi dalam metode SSCP dipengaruhi oleh panjang fragmen, urutan, lokasi dan jumlah wilayah pasangan basa. Oleh karena itu, mutasi pada posisi nukleotida tertentu dalam urutan primer dapat mengubah konformasi molekul. Ketika dipisahkan dalam gel non-denaturing, molekul berbeda dengan nukleotida tunggal bisa diidentifikasi berdasarkan perubahan dalam mobilitas.
Frekuensi Genotipe, Alel dan Heterozigositas
Pola migrasi utas tunggal DNA gen β-kasein pada gel poliakrilamida dalam penelitian ini polimorfik (beragam). Hal ini sesuai dengan pernyataan Nei dan Kumar (2000) yang menyatakan jika terdapat dua alel atau lebih dengan nilai frekuensi relatif dalam populasi lebih dari 1% maka disebut beragam (polimorfik). Hasil frekuensi genotipe genβ-kasein disajikan pada Tabel 4.
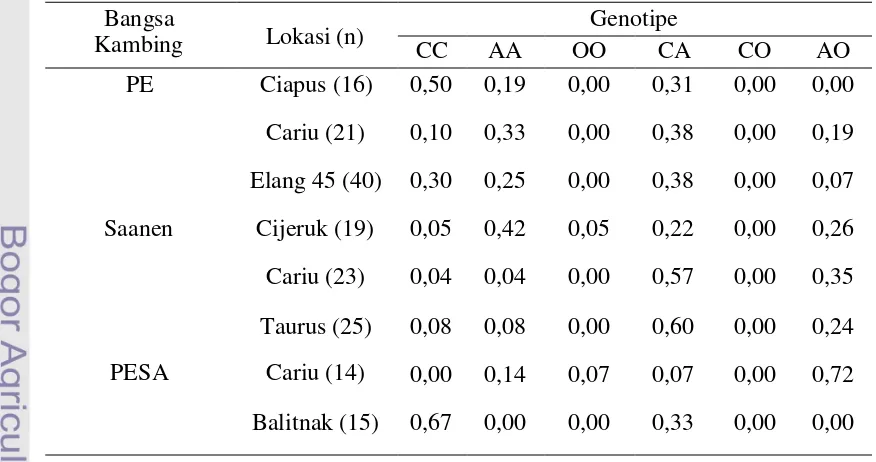
Tabel 4. Frekuensi Genotipe Genβ-Kasein pada Kambing PE, Saanen, dan PESA
Bangsa
Kambing Lokasi (n)
Genotipe
CC AA OO CA CO AO
PE Ciapus (16) 0,50 0,19 0,00 0,31 0,00 0,00
Cariu (21) 0,10 0,33 0,00 0,38 0,00 0,19
Elang 45 (40) 0,30 0,25 0,00 0,38 0,00 0,07
Saanen Cijeruk (19) 0,05 0,42 0,05 0,22 0,00 0,26
Cariu (23) 0,04 0,04 0,00 0,57 0,00 0,35
Taurus (25) 0,08 0,08 0,00 0,60 0,00 0,24
PESA Cariu (14) 0,00 0,14 0,07 0,07 0,00 0,72
Balitnak (15) 0,67 0,00 0,00 0,33 0,00 0,00
dari yang tertinggi ke rendah adalah CC (0,50); CA (0,31); dan AA (0,19). Di lokasi Cariu ditemukan empat genotipe, yaitu CC, AA, CA dan AO. Adapun urutan frekuensi genotipe berturut-turut dari yang tertinggi ke rendah adalah CA (0,38); AA (0,33); AO (0,19); dan CC (0,10). Kambing PE di lokasi Elang 45 ditemukan empat genotipe, yaitu CC, AA, CA dan AO. Adapun urutan frekuensi genotipe berturut-turut dari yang tertinggi ke rendah adalah CA (0,38); CC (0,30); AA (0,25); dan AO (0,07).
Kambing Saanen di lokasi Cijeruk ditemukan lima genotipe, yaitu CC, AA, OO, CA dan AO. Adapun urutan frekuensi genotipe berturut-turut dari yang tertinggi ke rendah adalah AA (0,42); AO (0,26); CA (0,22); CC (0,05); dan OO (0,05). Kambing Saanen di lokasi Cariu ditemukan empat genotipe, yaitu CC, AA, CA dan AO. Adapun urutan frekuensi genotipe berturut-turut dari yang tertinggi ke rendah adalah CA (0,57); AO (0,35); CC (0,04); dan AA (0,04). Kambing Saanen di lokasi Taurus ditemukan empat genotipe, yaitu CC, AA, CA dan AO. Adapun urutan frekuensi genotipe berturut-turut dari yang tertinggi ke rendah adalah CA (0,60); AO (0,24); CC (0,08); dan AA (0,08).
Kambing PESA di Cariu ditemukan empat genotipe, yaitu AA, OO, CA dan AO. Adapun urutan frekuensi genotipe berturut-turut dari yang tertinggi ke rendah adalah AO (0,72); AA (0,14); OO (0,07); dan CA (0,07). Kambing PESA di lokasi Balitnak ditemukan dua genotipe, yaitu CC dan CA masing-masing dengan frekuensi genotipe (0,67) dan (0,33).
Genotipe yang ditemukan pada penelitian ini sesuai dalam penelitian Chessa
et al. (2005) ditemukan lima genotipe, yaitu AC, CO, CC, AA dan AO pada bangsa-bangsa kambing yang berada di Italia. Pada penelitian Chessa et al. (2005) dilaporkan tidak ada bangsa-bangsa kambing Italia yang memiliki genotipe OO. Namun dalam penelitian ini ditemukan individu dari ketiga bangsa kambing yang diteliti yang memiliki genotipe OO dan tidak ditemukan genotipe CO. Genotipe CA dan CC merupakan genotipe yang umum dari kambing PE, Saanen dan PESA hampir di semua lokasi yang diteliti, kecuali kambing PESA di Cariu yang memiliki genotipe AO.
22 yang luas pada frekuensi dan efek dari varian tersebut masih harus dilakukan (Moioli
et al., 2007). Dalam penelitian Moatsou et al. (2008), genotipe β-kasein tidak berhubungan dengan kandungan β-kasein dalam susu. Bonfatti et al. (2010) mengemukakan bahwa pada susu sapi Simmental, gen β-kasein berpengaruh terhadap penurunan Rennet Coagulation Time (RCT) dan meningkatkan Curd Firmness(a30).
Heterozigositas menggambarkan adanya variasi genetik pada suatu populasi. Semakin tinggi nilai heterozigositas dalam suatu populasi maka semakin tinggi pula variasi genetik pada populasi tersebut (Ferguson, 1980). Hasil frekuensi alel dan heterozigositas gen β-kasein pada kambing PE, Saanen dan PESA tersaji pada Tabel 5.
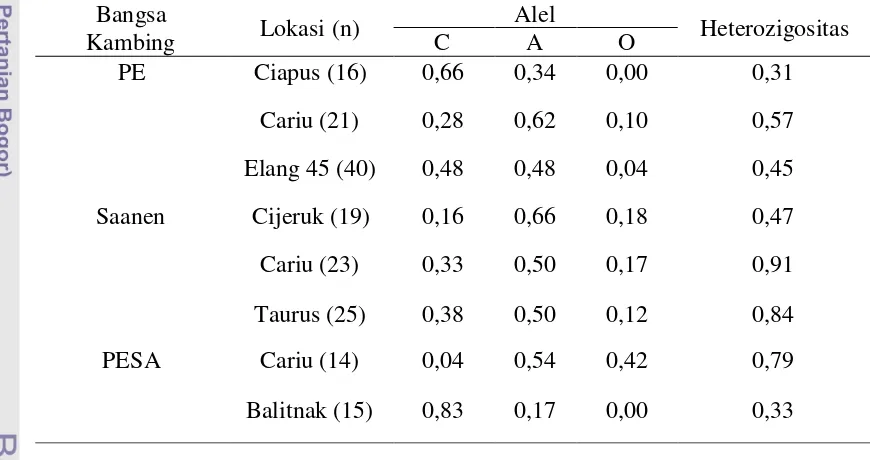
Tabel 5. Frekuensi Alel dan Heterozigositas Gen β-Kasein pada Kambing PE, Saanen dan PESA
Bangsa
Kambing Lokasi (n)
Alel
Heterozigositas
C A O
PE Ciapus (16) 0,66 0,34 0,00 0,31
Cariu (21) 0,28 0,62 0,10 0,57
Elang 45 (40) 0,48 0,48 0,04 0,45
Saanen Cijeruk (19) 0,16 0,66 0,18 0,47
Cariu (23) 0,33 0,50 0,17 0,91
Taurus (25) 0,38 0,50 0,12 0,84
PESA Cariu (14) 0,04 0,54 0,42 0,79
Balitnak (15) 0,83 0,17 0,00 0,33
Tabel 5 menunjukkan bahwa nilai heterozigositas tertinggi berturut-turut terdapat pada kambing Saanen di Cariu (0,91), kambing Saanen di Taurus (0,84), dan kambing PESA di Cariu (0,79). Pendugaan nilai heterozigositas dihitung untuk menggambarkan keragaman genetik dalam populasi yang dapat digunakan untuk membantu program seleksi pada ternak yang akan digunakan sebagai sumber genetik pada generasi berikutnya (Marsonet al., 2005). Frekuensi alel O sangat rendah pada ketiga bangsa kambing pada semua lokasi yang diamati dalam penelitian ini, hal ini sesuai dalam hasil penelitian Chessa et al. (2005) yang menyatakan bahwa bangsa-bangsa kambing yang berada di Italia memiliki frekuensi alel O yang rendah. Menurut Sacchi et al. (2005), alel O berhubungan dengan tingkat kasein yang rendah. Alel A merupakan alel yang frekuensinya tinggi pada kambing PE, Saanen dan PESA yang berada di hampir semua lokasi dalam penelitian ini kecuali pada kambing PE di Ciapus dan kambing PESA di Balitnak. Berdasarkan hasil penelitian Sacchiet al. (2005), alel A merupakan alel yang berhubungan dengan kandunganβ -kasein normal.
Keseimbangan Hardy-Weinberg
Hukum Hardy-Weinberg menggambarkan keseimbangan suatu lokus dalam populasi diploid mengalami perkawinan secara acak dari faktor yang berpengaruh terhadap terjadinya proses evolusi seperti mutasi, migrasi dan pergeseran genetik (Gillespie, 1998). Hasil pengujian keseimbangan populasi kambing PE, Saanen dan PESA disajikan pada Tabel 6.
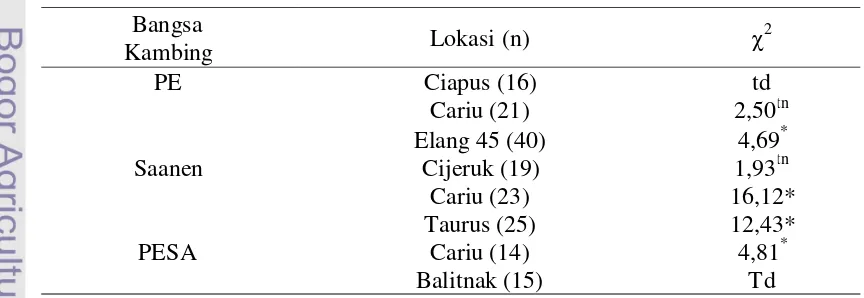
Tabel 6. Hasil Uji χ2 Terhadap Populasi Kambing PE, Saanen dan PESA
Bangsa
Saanen Cijeruk (19) 1,93tn
Cariu (23) 16,12*
Taurus (25) 12,43*
PESA Cariu (14) 4,81*
Balitnak (15) Td
24 Tabel 6 memperlihatkan bahwa kambing PE di lokasi Cariu berada dalam keseimbangan dengan nilai χ2 sebesar 2,50 karena lebih kecil daripada nilai
χ2
tabel(1) kecuali Elang 45 dengan nilai χ2sebesar 4,69 dan di lokasi Ciapus tidak dapat dianalisa karena derajat bebasnya nol. Kambing Saanen di lokasi Cijeruk berada dalam keseimbangan dengan nilai χ2 sebesar 1,93 lebih kecil daripada nilai
χ2
tabel(2), kecuali di lokasi Cariu dengan nilai χ2 sebesar 16,12 dan Taurus dengan nilaiχ2sebesar 12,43 karena lebih besar daripada nilaiχ2tabel(1). Kambing PESA di lokasi Cariu tidak berada dalam keseimbangan dengan nilai χ2 sebesar 4,81 karena lebih besar daripada nilai χ2 tabel(1) sedangkan pada lokasi Balitnak tidak dapat dianalisis karena derajat bebasnya minus satu.
KESIMPULAN DAN SARAN
Kesimpulan
Keragaman gen β-kasein pada Kambing PE, Saanen dan persilangannya sangat tinggi dengan ditemukannya tiga alel, yaitu C, A dan O. Pada Kambing PE di Cariu dan Elang 45 ditemukan tiga genotipe, yaitu CC, AA, CA dan AO. Kambing Saanen di Cijeruk dan Kambing PESA di Cariu ditemukan lima genotipe, yaitu CC, AA, OO, CA dan AO. Alel A merupakan alel yang frekuensinya tinggi pada kambing PE, Saanen dan PESA yang berada di hampir semua lokasi dalam penelitian ini kecuali pada kambing PE di Ciapus dan kambing PESA di Balitnak.
Saran
UCAPAN TERIMAKASIH
Puji dan syukur Penulis panjatkan kepada Tuhan Yang Maha Esa, atas limpahan rahmat dan karunia yang telah diberikan-Nya kepada Penulis sehingga Penulis dapat menyelesaikan penulisan skripsi ini. Kepada Ayah dan Ibu tercinta, Bapak Jap Soey Liong dan Ibu Mimih Riyati yang senantiasa memberikan kasih sayang dan pengorbanan yang tak pernah terbalaskan. Kepada adik Penulis yang tersayang, Hendri Saputra dan Maria Putriana yang telah memberikan dukungan dan kasih sayang.
Penulis mengucapkan terima kasih kepada Ir. Andi Murfi, M.Si sebagai Pembimbing Akademik atas segala perhatian, bimbingan dan nasehatnya. Kepada Ir. Sri Darwati, M.Si dan Prof. Dr. Ir. Cece Sumantri, M.Agr.Sc sebagai Pembimbing Skripsi atas segala bimbingan, perhatian, motivasi dan arahan bagi penulis. Terima kasih Penulis ucapkan kepada Prof. Dr. Ir. Pollung H. Siagian, MS dan Ir. Lilis Khotijah, M.Si sebagai Penguji atas masukan dan arahan terhadap skripsi Penulis. Terima kasih Penulis ucapkan kepada M. Baihaqi, S.Pt, M.Sc sebagai Panitia Ujian atas masukan terhadap skripsi Penulis.
Penulis mengucapkan terima kasih kepada keluarga besar Laboratorium Genetika Molekuler (Kak Eryk, Kak Surya, Kak Restu, Pak Andi, Pak Ihsan, Pak Tafaul, Kak Kia, Kak Mira, Kak Asri, Pris, Paulina, Lenny, Irene, Icha, Dini, Desi, Gina, Gabby, Tifanny, Erwin dan Kak Asep). Penulis juga mengucapkan terima kasih kepada Yesua, Vania, Cintya, Kade, Debora, Siddiq, Furqan, Roceyana, serta teman-teman IPTP 44 atas kerjasama, keceriaan dan kekeluargaannya selama ini.
Bogor, 11 Mei 2011
DAFTAR PUSTAKA
Atabany, A., I. K. Abdulgani, A. Sudono, & K. Mudikjo. 2001. Performa produksi, reproduksi dan nilai ekonomis kambing Peranakan Etawah di Peternakan Barokah. Med. Pet. 24: 1-7.
Badan Pusat Statistik. 2008. Statistik Peternakan 2008. Jakarta: Direktorat Jenderal Peternakan Departemen Pertanian RI. http://www.ditjennak.go.id/ [17 Agustus 2010].
Baroso, A., S. Dunner, & J. Canon. 1999. Technical note: use of PCR-single strand conformation polymorphism analysis for detection of bovineβ-casein variants A1, A2,
A3and B. J. Anim Sci. 77: 2629-2632.
Bastos, E., A. Crvador, J. Azevedo, & H. G. Pinto. 2001. Single strand conformation polymorphism (SSCP) detection in six genes in Portuguese indigenous sheep breed “CHurra da Terra Quente”. Biotechnol. Agron. Soc. Environ. 5: 7-15.
Bonfatti, V., G. Di Martino, A. Cecchinato,L. Degano, & P. Carnier. 2010. Effects of β-κ -casein (CSN2-CSN3) haplotypes, β-lactoglobulin (BLG) genotypes, and detailed protein composition on coagulation properties of individual milk of Simmental cows. J. Dairy Sci. 93: 3809-3817.
Bovenhuis, H., A. M. Johan, V. Arendonk, & S. Korver. 1992. Associations between milk protein polymorphisms and milk production traits of swiss brown cattle. J. Dairy Sci. 75: 2549-2559.
Braunschweig, M. H. 2008. Associations between 2 parental casein hapolotypes and milk yield traits of swiss fleckvieh cattle. J. Appl Genet 49: 69-74.
Brown, T.A. 1999. Genome. Bios Scientific Publishers Ltd. 9 Newtec Place. Magdalen Road. Oxford Ox4 IRE. United Kingdom.
Buckle, K. A., R. A. Edwards, G. H. Fleet, & M. Wootton. 1987. Ilmu Pangan. Terjemahan: H. Purnomo dan Adiono. UI Press, Jakarta.
Byun, S. O., Q. Fang, H. Zhou, & J. G. H. Hickford. 2008. An effective method for silver-staining DNA in large numbers of polyacrylamide gels. Anal. Biochem. 385: 174– 175.
Chessa, S., E. Budelli, F. Chiatti, A. M. Cito, P. Bola, & A. Caroli. 2005. Short communication: predominance ofβ-kasein (CSN2) C allele in goat breeds reared in Italy. J. Dairy Sci. 88: 1878-1881.
Creamer, L.K. 2003. Casein nomenclature, structure and association properties. In:
Encyclopedia of Dairy Sciences. Academic Press, Amsterdam.
Devendra, C. & G. B. McLeroy. 1982. Goat and Sheep Production in The Tropics. Intermediate Tropical Agriculture Series. Longman, London and New York.
Devendra, C. & M. Burns. 1994. Produksi Kambing di Daerah Tropis. Terjemahan: Harya Putra. Penerbit Institut Teknologi Bandung, Bandung.
28 Ferguson, A. 1980. Biochemical Systematics and Evolution Lecturer in Zoology. The
Queens University of Belfast. London.
Fox, P. F. & P. L. H. Mc Sweeney. 1998. Dairy Chemistry and Biochemistry. Blackie Academic & Professional an Imprint of Chapman and Hall, London.
Gall, C. 1981. Goat Production. Academic Press Inc, New York.
Gasser, R. B., Min Hu, N. B. Chilton, B. E. Campbell, A. J. Jex, D. Otranto, C. Cafarchia, I. Beveridge, & X. Zhu. 2006. Single-strand conformation polymorphism (SSCP) for the analysis of genetic variation. Nature Publishing Group. 1: 6.
Gillespie, J. H. 1998. Population Genetics, A Concies Guide. The Johns Hopkins University Press. London.
Hayashi, K. 1991. PCR-SSCP: a simple and sensitive method for detection of mutations in the genomic DNA. PCR Methods Appl. 1:34-38.
Hidayat, T & A. Pancoro. 2010. Single strand conformation polymorphism method for initial detection DNA sequences homogeneity. J. Biosci. 17: 50-52.
Kucerova, J., A. Matejicek, O. M. Jandurova, P. Sorensen, E. Nemcova, M. Stipkova, T. Kott, J. Bouska, & J. Frelich. 2006. Milk protein genesCSN1S1,CSN2, CSN3,LGB
and their relation to genetic values of milk production parameters in Czech Fleckvieh. J. Anim. Sci. 51: 241-247.
Marson, E. P., J. B. S. Ferraz, F. V. Meirelles, J. C. C. Balieiro, J. P. Eler, L. G. G. Figuerido, & G. B. Mourao. 2005. Genetic characterization of European-Zebu composite bovine using RFLP markers. Genet. Mol. Res. 4: 496-505.
Martin, P & F. Grosclaude. 1993. Improvement of milk protein quality by gene technology. J Livest Prod Sci 35: 95-115.
Martin, P., M. Szymanowska, L. Zwierzchowski, & C. Leroux. 2002. The impact of genetic polymorphisms on the protein composition of ruminants milks. Reprod. Nutr. Dev. 42:433–459.
Martin, P., P. Ferranti, C. Leroux, and F. Addeo. 2003. Non-bovine caseins: qualitative variability and molecular diversity. In: Advanced Dairy Chemistry, Volume 1: Proteins, 3rded. Kluwer Academic/Plenum Publishers, New York.
Mileski, A. & P. Myers. 2004. "Capra hircus" (On-line), Animal Diversity Web.
http://animaldiversity.ummz.umich.edu/site/accounts/information/Capra_hircus.html
[17 Agustus 2010].
Moatsou, G., E. Moschopoulou, D. Molle´, V. Gagnaire, I. Kandarakis, & J. Le´onil. 2008. Comparative study of the protein fraction of goat milk from the Indigenous Greek breed and from international breeds. Food Chem. 106: 509-520.
Moioli, B ., M. D’Andrea, & F. Pilla. 2007. Candidate genes affecting sheep and goat milk quality. Small Rum. Res. 68:179–192.
Muladno. 2002. Seputar Teknologi Rekayasa Genetika. Pustaka Wirausaha Muda dan USESE Foundation. Bogor.
Ng-Kwai-Hang, K. F., J. F. Hayes, J. E. Moxley, & H. G. Monardes. 1986. Relationships between milk protein polymorphism and major milk constituents in holstein-friesian cows. J. Dairy Sci. 69: 22-26.
Nei, M. & Kumar S. 2000. Molecular Evolution and Phylogenetics. Oxford University Press. New York.
Nicholas, F.W. 1996. Inntroduction to Veterinary Genetics. Oxford University Press, Inc. New York.
Noor, R.R. 2008. Genetika Ternak. Penebar Swadaya. Jakarta.
Orita, M., Y. Suzuki, T. Sekiya, & K. Hayashi. 1989. Rapid and sensitive detection of point mutations and DNA polymorphisms using the polymerase chain reaction. Genomics 5: 874-879.
Pamungkas, F. A., A. Batubara, M. Doloksaribu, & E. Sihite. 2009. Petunjuk Teknis Potensi Beberapa Plasma Nutfah Kambing Lokal Indonesia. Pusat Penelitian dan Pengembangan Peternakan, Sumatera Utara.
Rahman, A., S. Fardiaz, W. P. Rahaju, Suliantari, & C. C. Nurwitri. 1992. Teknologi Fermentasi Susu. Pusat antar Universitas Pangan dan Gizi. Institut Pertanian Bogor, Bogor.
Ruhimat, A. 2003. Produktivitas kambing persilangan Peranakan Etawah betina dengan Saanen jantan (PESA) di PT. Taurus Dairy Farm. Skripsi. Fakultas peternakan. Institut Pertanian Bogor, Bogor.
Sacchi, P., S. Chessa, E. Budelli, P. Bolla, G. Ceriotti, D. Soglia, R. Rasero, E. Cauvin, & A. Caroli. 2005. Casein haplotype structure in five Italian goat breeds. J. Dairy Sci. 88:1561-1568.
Sambrook, J., F. Fritsch, & T. Miniatis. 1989. Molecular Cloning Laboratory manual. 3rd ed. Cold Spring Harbor Laboratory Press, New York.
Setiadi, B. & I. K. Sutama. 1997. Kambing PE, Kambing Perah Indonesia. Balai Penelitian Ternak, Bogor.
Sheffield, V. C., J. S. Beck, A. E. Kwitek, D. W. Sandstorm, & E. M. Stone. 1993. The sensitivity of single-strand conformation polymorphism for detection of single base substitution. Genomics. 16: 325-332.
Souhoka D. F., M. J. Matatula., W. M. M. Nalley, & M. Rizal. 2009. Laktosa mempertahankan daya hidup spermatozoa kambing Peranakan Etawah. J. Veteriner 10: 135-142.
Sztankóová Z., C. Senese., V. Czerneková, G. Dudková, T. Kott, V. Mátlová, & J. Soldát. 2005. Genomic analysis of the CSN2 and CSN3 loci in two Czech goat breeds. Anim. Sci. 23:67-70.
Trujillo, A. J., B. Guamis, & C. Carretero. 1997. Hydrolysis of Caprineβ-casein by plasmin. J. Dairy Sci. 80: 2258-2263.
30 Wang, Q., Z. Huang, M. J. Chen, S. Z. Huang, & Y. T. Zeng. 2001. GenBank Accession no. AF409096 [Capra hircus β-casein precursor (csn2) gene, complete cds].
http://www.ncbi.nlm.nih.gov//[17 Agustus 2010].
Lampiran 1. Modifikasi Metode Ekstraksi DNA Menggunakan Metode Sambrook
200 µl sampel darah
+ 1000 µl air destilasi
Vorteks ± 5 menit
Sentrifuse 8000 rpm ± 5 menit Buang supernatan
+ 40 µl SDS 20% + 10 µl Prot K + 1 x STE sampai 400 µl
Inkubasi 55oC 2 jam
+ 400 µl fenol + 400 µl CIAA + 40 µl 5M NaCl
Sentrifuse 12000 rpm 5 menit
Bagian DNA (bening)
Tabung 1,5 ml
+ 800 µl EtoH + 40 µl 5M NaCl
Freezing Over Night
Sentrifuse 12000rpm 5 menit Buang supernatan
+ 800 µl EtoH
Sentrifuse 12000rpm 5 menit Buang supernatan
Diamkan dlm keadaan terbuka
32
Lampiran 2. Informasi Sekuen Genβ-Kasein pada Ternak Kambing
LOCUS AF409096 13671 bp DNA linear MAM
04-SEP-2001
DEFINITION Capra hircus beta-casein precursor (csn2) gene, complete cds. ACCESSION AF409096
VERSION AF409096.1 GI:15425979 KEYWORDS .
SOURCE Capra hircus (goat) ORGANISM Capra hircus
Eukaryota; Metazoa; Chordata; Craniata; Vertebrata; Euteleostomi; Mammalia; Eutheria; Laurasiatheria; Cetartiodactyla; Ruminantia; Pecora; Bovidae; Caprinae; Capra.
REFERENCE 1 (bases 1 to 13671)
AUTHORS Wang,Q., Huang,Z., Chen,M.J., Huang,S.Z. and Zeng,Y.T. TITLE Direct Submission
JOURNAL Submitted (09-AUG -2001) Department of Molecular Biology, Shanghai Institute of Medical Genetics, 24/1400 Beijing Western Road,
Shanghai 200040, China
/experiment="experimental evidence, no additional details recorded"
/experiment="experimental evidence, no additional details recorded"
QPPQPLSPTVMFPPQSVLSLSQPKVLPVPQKVVPQRDMPIQAFLLYQEPVLGPVRGPF
12361 caaaatactg aagatgctta tttcaatact cagggaaaat tttcttgcca aaaggcaaga 12421 attgtataat tcattcactt attttatttt tttaattttt aaggtctaag aggatttcaa 12481 agtgaatgcc ccctcctcac ttttggtaag ctttaggaga ttggaggcag actgatcatt 12541 tttatagtta atatctttta catttcatct tcctggataa gccccaatag tagcaatttc 12601 tatcagtata ccagcgtaaa gattagtttt aaatatattt tcagtgattg actgttattt 12661 actgacctga aattatgtat ctgttatatt tcaaataatg caaaactgta tatatatggt 12721 gttgacagat ttgattggtt ttctttcaat tgcctatatc cttattattg attgtaatca 12781 tttatagaaa aaacaaaata atttcttata cttttatgta aacctgttag agcttatttt 12841 aaagatcaac tgcattcaca tttctaatct agtcattatg agcttcaatt gttttatctc 12901 acttaaaatt tatatattgt cttttaattc atgagtcaaa atacaatctc acagtccaga 12961 tatgggactt aaaaggggaa tagcatatag ttttgatatt cttaaagaaa tacatctttt 13021 tgtgatcatg attcagcaga cattttaata aaacaattcc aagtgagccg acacttggtc 13081 ctagaggaat ttttataatc ttaaggtaag gcacagcatg gtgtttttgt aataagattt 13141 cttttatgaa aaagtcacac caaaattgga aatggggtga gatgaagagt tataacatat 13201 aactaaatgg acatttgttc tctattccac agaattgact gcgactggaa atatggcaac 13261 ttttcaatcc ttgcatcatg ctactaagat aatttttaaa tgagtataca tggaacaaaa 13321 aatgaaactt tattccttta tttattttat gctttttcat cttaatttga atttgagtca 13381 taaaccatat actttcaaaa tgttaattca acattagcat aaaagttcaa ttttaacttg 13441 gaaatatcat gaacatatca aattatgtat aaaaataatt tctggaattg tgattattat 13501 ttctttaaga atctatttcc taaccagtca tttcaataaa ttaaccctta ggcatattta 13561 agttttcttg tctttattat atttttaaaa atgaaattgg tctctttatt gttaacttaa 13621 atttatcttt gatgttaaaa atagctgtgg aaaattaaaa ttggatagaa t
38
Lampiran 3. Jumlah Genotipe Genβ-Kasein pada Kambing PE, Saanen dan PESA (Persilangan PE dengan Saanen)
Bangsa
Kambing Lokasi (n)
Genotipe
Total
CC AA OO CA CO AO
PE Ciapus (01) 8 3 0 5 0 0 16
Cariu (02) 2 7 0 8 0 4 21
Elang 45 (03) 12 10 0 15 0 3 40
Saanen Cijeruk (01) 1 8 1 4 0 5 19
Cariu (02) 1 1 0 13 0 8 23
Taurus (03) 2 2 0 15 0 6 25
PESA Cariu (02) 0 2 1 1 0 10 14
Balitnak (03) 10 0 0 5 0 0 15
Total 36 33 2 66 0 36 173
Lampiran 4. Nilai Harapan untuk Uji Chi-Kuadrat
Bangsa
Kambing Lokasi (n)
Genotipe
Total
CC AA OO CA CO AO
PE Ciapus (16) 6,89 1,89 0,00 7,22 0,00 0,00 16,00
Cariu (19) 1,71 8,05 0,19 7,43 1,14 2,48 21,00
Elang 45 (37) 9,51 9,03 0,06 18,53 1,46 1,43 40,00
Saanen Cijeruk (19) 0,47 8,22 0,64 3,95 1,11 4,61 19,00
Cariu (17) 2,45 5,75 0,70 7,50 2,61 4,00 23,00
Taurus (25) 3,61 6,25 0,36 9,50 2,28 3,00 25,00
PESA Cariu (10) 0,02 4,02 2,57 0,54 0,43 6,43 14,00
Balitnak (15) 10,42 0,42 0,00 4,17 0,00 0,00 15,00
IDENTIFIKASI KERAGAMAN GEN
β
-KASEIN (CSN2) PADA
KAMBING PERANAKAN ETAWAH, SAANEN DAN
PERSILANGANNYA DENGAN
METODE PCR-SSCP
SKRIPSI FERDY SAPUTRA
DEPARTEMEN ILMU PRODUKSI DAN TEKNOLOGI PETERNAKAN FAKULTAS PETERNAKAN
RINGKASAN
Ferdy Saputra. D14070024. 2011. Identifikasi Keragaman Genβ-Kasein (CSN2) pada Kambing Peranakan Etawah, Saanen dan Persilangannya dengan Metode PCR-SSCP. Skripsi. Departemen Ilmu Produksi dan Teknologi Peternakan, Fakultas Peternakan, Institut Pertanian Bogor.
Pembimbing Utama : Ir. Sri Darwati, M.Si
Pembimbing Anggota : Prof. Dr. Ir. Cece Sumantri, M.Agr.Sc
Gen β-kasein secara langsung berkaitan dengan kualitas dan sifat susu. Keragaman gen β-kasein pada kambing perah di Indonesia telah berhasil diidentifikasi dengan metode Polymerase Chain Reaction-Single Strand Conformation Polymorphism (PCR-SSCP). Metode PCR-SSCP merupakan metode yang sensitif dalam mendeteksi adanya keragaman DNA. Metode ini merupakan pemisahan asam nukleat rantai tunggal (single stranded nucleic acids) hasil amplifikasi PCR dengan elektroforesis melalui gel poliakrilamid dan berdasarkan pada perbedaan berat molekul pasangan basa, sehingga dapat menghasilkan perbedaan struktur sekunder gen.
Berdasarkan pola migrasi, kambing PE di lokasi Ciapus ditemukan tiga genotipe, yaitu CC, AA dan CA. Kambing PE di lokasi Cariu dan Elang 45 ditemukan empat genotipe, yaitu CC, AA, CA dan AO. Kambing Saanen di lokasi Cijeruk ditemukan lima genotipe, yaitu CC, AA, OO, CA dan AO. Kambing Saanen di lokasi Cariu dan Taurus ditemukan empat genotipe, yaitu CC, AA, CA dan AO. Kambing PESA di lokasi Cariu ditemukan empat genotipe, yaitu AA, OO, CA dan AO. Kambing PESA di lokasi Balitnak hanya ditemukan dua genotipe, yaitu CC dan CA.
Pada kambing PE ditemukan frekuensi alel tertinggi pada alel C sebesar 0,66 dan frekuensi alel terendah pada alel O sebesar 0,00 keduanya di lokasi Ciapus. Kambing Saanen ditemukan frekuensi alel tertinggi pada alel A sebesar 0,66 di populasi Cijeruk dan frekuensi alel terendah pada alel O sebesar 0,12 di populasi Taurus. Kambing PESA ditemukan frekuensi alel tertinggi pada alel C sebesar 0,83 dan frekuensi alel terendah pada alel O sebesar 0,00 keduanya di lokasi Balitnak.
Keragaman gen β-kasein pada Kambing PE, Saanen dan persilangannya sangat tinggi dengan ditemukannya tiga alel, yaitu C, A dan O. Pada Kambing PE di Cariu dan Elang 45 ditemukan tiga genotipe, yaitu CC, AA, CA dan AO. Kambing Saanen di Cijeruk dan Kambing PESA di Cariu ditemukan lima genotipe, yaitu CC, AA, OO, CA dan AO. Alel A merupakan alel yang frekuensinya tinggi pada kambing PE, Saanen dan PESA yang berada di hampir semua lokasi dalam penelitian ini kecuali pada kambing PE di Ciapus dan kambing PESA di Balitnak.
ABSTRACT
Identification ofβ-Kasein Gene in Local Dairy Goat Using SSCP-PCR Method
Saputra, F., S. Darwati and C. Sumantri
Casein genetic polymorphisms are important and well known due to their effects on quantitative traits and properties of milk. β-kasein gene is directly related to the quality and properties of milk. A protocol for the rapid and simultaneous genotyping of β-kasein alleles was conducted by single strand conformational polymorphism polymerase chain reaction (SSCP-PCR) method in goat. Screening β-kasein gene variability in 3 dairy goat breeds was conducted for Etawah Grade (77 samples), Saanen (67 samples) and PESA (Crossbreed Etawah Grade with Saanen) (29 samples) in Bogor and Sukabumi. The objective of this research was to identify polymorphism of theβ-kasein (CSN2) gene in dairy goat. This research found three alleles of the β-casein gene, ie CSN2*A, CSN2*C, dan CSN2*O. In most breeds, CSN2*O occurred in the lowest frequency. The identification of the CSN2 gene variability in the goat breeds indicated the highly of theAallele. The CSN2*Aallele had a high frequency in Saanen in Cijeruk (0,66); Etawah Grade in Cariu (0,62); and PESA in Cariu (0,54). While the CSN2*C allele had a high frequency in PESA in Balitnak (0,83); Etawah Grade in Ciapus (0,48); and Saanen in Taurus (0.38). Based on the results of chi-square analysis, found that Saanen in Cariu and Taurus were not in Hardy-Weinberg equilibrium.
PENDAHULUAN
Latar Belakang
Kambing perah merupakan salah satu ternak alternatif yang banyak digunakan sebagai ternak penghasil susu selain sapi perah. Kambing dapat hidup di daerah kering dan dapat memanfaatkan hijauan pakan secara efisien. Ternak kambing mempunyai potensi untuk berkembang karena mempunyai kemampuan beradaptasi cukup tinggi.
Jumlah produksi susu segar di Indonesia sebanyak 647 ton pada tahun 2008 (Direktorat Jenderal Peternakan, 2008). Impor produk susu pada tahun 2008 di Indonesia sebesar 665.159,5 ton (Badan Pusat Statistika, 2008). Dari data tersebut, produksi susu nasional belum mampu memenuhi seluruh kebutuhan konsumsi nasional. Konsumsi susu dan impor susu akan terus meningkat, sehingga perlu peningkatan populasi ternak perah, efisiensi produksi susu dan diversifikasi ternak perah.
Populasi kambing di Indonesia pada tahun 2008 berjumlah sekitar 15.147.432 ekor (Direktorat Jenderal Peternakan, 2008). Data tersebut merupakan jumlah seluruh bangsa kambing yang ada di Indonesia. Jadi, kemungkinan jumlah kambing perah di Indonesia tidak terlalu banyak. Untuk itu, perlu peningkatan jumlah kambing perah di Indonesia. Pemeliharaan kambing perah juga merupakan salah satu alternatif upaya diversifikasi ternak perah dan peningkatan produksi susu. Indonesia memiliki beberapa jenis ternak kambing perah, yaitu kambing Saanen, Peranakan Etawah dan Persilangan Peranakan Etawah dan Saanen (PESA).
(PCR-SSCP). Keragaman gen β-kasein pada kambing perah di Indonesia telah berhasil diidentifikasi dengan metode PCR-SSCP. Polymerase Chain Reaction-Single Strand Conformation Polymorphism merupakan metode yang sensitif dalam mendeteksi adanya keragaman DNA.
Tujuan
TINJAUAN PUSTAKA
Klasifikasi Kambing
Kambing diklasifikasikan kedalam kingdom Animalia; phylum Chordata; subphylum Vertebrata; class Mamalia; ordo Artiodactyla; sub-ordo Ruminantia;
family Bovidae; sub family Caprinae dan genus Capra (Mileski, 2004). Kambing (Capra hircus) memiliki 60 kromosom (30 pasang kromosom) yang terdiri dari 29 pasang kromosom autosom dan sepasang kromosom kelamin (Gall, 1981).
Penyebaran kambing sangat luas dan hampir menyebar di seluruh dunia. Hal ini disebabkan, kambing memiliki daya adaptasi yang baik terhadap berbagai iklim dan kemampuannya bertahan hidup pada daerah dengan hijauan terbatas (Gall, 1981). Kambing merupakan ternak yang dapat hidup di daerah kering dan daerah dengan hijauan pakan yang mungkin tidak disukai oleh ternak lain, serta dapat memanfaatkan hijauan pakan secara efisien (Devendra dan Burns, 1994).
Kambing Lokal Indonesia
Kambing Marica yang terdapat di Propinsi Sulawesi Selatan merupakan salah satu genotipe kambing asli Indonesia yang menurut laporan FAO sudah termasuk kategori langka dan hampir punah (endangered). Kambing Marica mempunyai potensi genetik yang mampu beradaptasi baik di daerah agro-ekosistem lahan kering, yaitu daerah dengan curah hujan sepanjang tahun sangat rendah. Kambing Marica dapat bertahan hidup pada musim kemarau walau hanya memakan rumput-rumput kering di daerah tanah berbatu-batu (Pamungkas et al., 2009).
Kambing Muara dijumpai di daerah Kecamatan Muara, Kabupaten Tapanuli Utara di Propinsi Sumatera Utara. Penampilan kambing ini gagah, tubuh kompak dan sebaran warna rambut bervariasi antara warna rambut coklat kemerahan, putih dan ada juga yang berwarna rambut hitam. Bobot kambing Muara lebih besar dibandingkan dengan kambing Kacang dan diduga kambing prolifik (Pamungkas et al., 2009).
Kambing Kosta terdapat di sekitar Jakarta dan Propinsi Banten (Setiadi dan Sutama, 1987). Kambing ini dilaporkan mempunyai bentuk tubuh sedang, hidung rata dan kadang-kadang ada yang melengkung, tanduk pendek dan berambut pendek. Kambing ini diduga terbentuk dari persilangan kambing Kacang dengan salah satu rumpun kambing impor (Khasmir/Angora/Etawah) (Pamungkaset al., 2009).
Kambing Gembrong terdapat di daerah kawasan Timur Pulau Bali terutama di Kabupaten Karangasem. Ciri khas dari kambing ini adalah berambut panjang. Panjang rambut berkisar 15-25 cm, bahkan rambut pada bagian kepala sampai menutupi muka dan telinga. Rambut panjang terdapat pada kambing jantan, sedangkan kambing Gembrong betina berambut pendek berkisar 2-3 cm (Pamungkas
et al., 2009).
Kambing Kacang merupakan kambing asli Indonesia juga didapati di Malaysia dan Filipina. Kambing Kacang sangat cepat berkembangbiak, pada umur 15-18 bulan sudah bisa menghasilkan keturunan. Kambing ini cocok sebagai penghasil daging dan kulit, bersifat prolifik, tahan terhadap berbagai kondisi dan mampu beradaptasi dengan baik di berbagai lingkungan yang berbeda termasuk dalam kondisi pemeliharaan yang sangat sederhana. Ciri-ciri kambing Kacang adalah antara lain rambut pendek dan berwarna tunggal (putih, hitam dan coklat) (Pamungkaset al., 2009).
5
Kambing Peranakan Etawah (PE)
Salah satu jenis kambing perah di daerah tropis khususnya di Indonesia adalah kambing Peranakan Etawah. Kambing PE merupakan hasil persilangan antara kambing Etawah dan kambing lokal Indonesia. Disamping sebagai ternak penghasil susu, pejantan kambing PE juga dapat dimanfaatkan untuk meningkatkan potensi produksi susu kambing lokal Indonesia lainnya dengan inseminasi buatan (IB) (Souhokaet al., 2009). Diharapkan dengan persilangan tersebut akan dihasilkan kambing yang mampu memproduksi susu dan daging cukup tinggi (dual purpose).
Kambing PE dapat menghasilkan daging dan susu (kambing tipe dwiguna). Kambing PE betina memiliki kemampuan menghasilkan susu yang cukup baik. Menurut Atabanyet al. (2001), produksi susu kambing PE adalah 0,99 kg/ekor/hari. Rataan bobot lahir kambing PE kelahiran tunggal betina 3,2 kg, jantan 3,7 kg (Setiadi dan Sutama, 1997).
Ciri khas kambing PE antara lain bentuk muka cembung melengkung dan dagu berjanggut, terdapat gelambir di bawah leher yang tumbuh berawal dari sudut janggut, telinga panjang, lembek menggantung dan ujungnya agak berlipat, ujung tanduk agak melengkung, tubuh tinggi, pipih, bentuk garis punggung mengombak ke belakang, rambut tumbuh panjang di bagian leher, pundak, punggung dan paha, bulu paha panjang dan tebal. Warna rambut ada yang tunggal; putih, hitam dan coklat, tetapi jarang ditemukan. Kebanyakan terdiri dari dua atau tiga pola warna, yaitu belang hitam, belang coklat dan putih bertotol hitam (Pamungkaset al., 2009).
Kambing Saanen
Kambing Saanen berasal dari Swiss Barat. Kambing ini berwarna putih, krem pucat atau coklat muda dengan bercak hitam pada hidung, telinga dan ambing. Kambing ini berambut pendek dan telinganya agak tegak serta mengarah ke depan. Kambing Saanen memiliki rataan produksi susu tertinggi dibanding bangsa kambing lainnya (Devendra dan Burns, 1994). Kambing Saanen memiliki rataan produksi susu 216 kg dengan panjang laktasi 275 hari (Gall, 1981). Menurut Devendra dan Burns (1994), kambing Saanen memiliki rataan hasil susu harian sebanyak 1,06 kg/ekor/hari. Kambing Saanen biasanya dipelihara dan diberi pakan dalam kandang.
merupakan kambing yang tidak memiliki tanduk. Kambing Saanen memiliki tubuh dengan konformasi tipe perah yang baik dan ambing yang berkembang baik pula. Jumlah anak lahir seperindukan 1,80 ekor (Devendra dan Burns, 1994). Rataan berat badan kambing betina dan jantan Saanen adalah 65 dan 75 kg (Devendra dan McLeroy, 1982).
Kambing PESA (Persilangan Peranakan Etawah dengan Saanen)
Kambing PESA merupakan kambing hasil persilangan antara kambing Peranakan Etawah (PE) betina dengan kambing Saanen jantan. Kambing PESA memiliki produksi susu harian yang lebih baik daripada Peranakan Etawah tetapi produksinya lebih rendah daripada kambing Saanen. Hal ini dibuktikan dengan produksi susu harian dari kambing Saanen (F1) dan PESA di PT. Taurus Dairy Farm masing-masing sebanyak 1,19 dan 1,12 kg/ekor/hari (Ruhimat, 2003).
Protein Susu
Susu merupakan sumber makanan alami bagi hewan mamalia yang baru dilahirkan. Produksi susu merupakan salah satu dari sifat kuantitatif yang dikendalikan oleh banyak pasangan gen yang aksinya bersifat aditif (Velmalaet al., 1999). Produksi susu dalam satu spesies sangat dipengaruhi oleh bangsa, umur, nutrisi, kesehatan, musim dan lain-lain (Fox dan Mc Sweeney, 1998). Susu dari ternak terdiri dari sebagian air yang terlarut pada protein, gula susu (laktosa), mineral dan vitamin-vitamin yang larut dalam air.
7 Tabel 1. Komposisi Protein Susu Ternak Ruminansia
Jenis Protein Sapi Domba Kambing
Kasein
---g/l---αs1-kasein 10 7 7
αs2-kasein 3,7 7 4
β-kasein 3,5 3,5 6
κ-kasein 10 8 10
Whey
α-lactalbumin 1,2 0,8-2,4 1,2
β-lactoglobulin 3,3 2.8-5 2,3
Serum Albumin 0,4
Lysozyme Trace Trace
Lactoferin 0,1 0,1
Immunoglobulin 0,7 0,5
Sumber: Martin dan Grosclaude (1993)
β-Kasein
β-kasein adalah bagian yang paling hidrofobik dari kasein dan mengandung sejumlah besar prolin residu, memiliki ujung terminal hidrofilik C dan akhir terminal hidrofobik N (Creamer, 2003). β-kasein terdiri dari 209 asam amino (Martin et al., 2003), dan memiliki massa molekul 24,0 kDa (kilo Dalton) (Creamer, 2003); mengandung lima kelompok phosphoseryl. β-kasein terkandung sekitar 60% dari total kasein dalam susu kambing (Trujilloet al., 1997).
Keragaman Genβ-Kasein
Gen β-kasein merupakan gen yang berpengaruh terhadap produksi susu, persentase protein dan hasil protein (Bovenhuis et al., 1992). Gen β-kasein secara langsung berkaitan dengan kualitas dan sifat susu (Sztankóováet al., 2005). Namun, dalam penelitian Moatsouet al. (2008), genotipeβ-kasein tidak berhubungan dengan kandunganβ-kasein dalam susu.
(2006), gen protein susu terdiri αs1-kasein (CSN1S1), β-kasein (CSN2), κ-kasein (CSN3) dan β-lactoglobulin (LGB). Polimorfisme gen-gen kasein yang tinggi berpengaruh langsung terhadap produksi dan komposisi susu sapi perah (Ng-Kwai-Hanget al., 1986).
Menurut Bovenhuiset al. (1992), genotipeβ-kasein sapi adalah A1A1, A1A2, A2 A2, A1 B, B B, A1 A3, A2 A3, dan A3 B. Selanjutnya Chessa et al. (2005) mengemukakan bahwa variasi genetik β-kasein kambing pada ekson 7 adalah
CSN2*A, CSN2*C dan CSN2*0’. Hasil frekuensi alel gen CSN2 menurut Chessa et al. (2005) disajikan dalam Tabel 2.
Tabel 2. Hasil Frekuensi Alel GenCSN2dengan Metode SSCP
Jenis N Alel Gen CSN2
A C 0’
Saanen 76 0,507 0,493 …..
Camosciata 112 0,317 0,683 …..
Jonica 70 0,207 0,700 0,093
Garganica 33 0,242 0,712 0,046
Maltese 58 0,129 0,819 0,052
Cilentana 43 0,035 0,872 0,093
Orobica 81 0,025 0,975 …..
Sumber: Chessaet al. (2005)