PENJERNIHAN EKSTRAK DAUN STEVIA (Stevia rebaudianaBertoni
)
DENGAN ULTRAFILTRASI ALIRAN SILANGOleh : Fifi Isdianti
F 34102078
PENJERNIHAN EKSTRAK DAUN STEVIA (Stevia rebaudianaBertoni
)
DENGAN ULTRAFILTRASI ALIRAN SILANGSKRIPSI
Sebagai salah satu syarat untuk mendapatkan gelar SARJANA TEKNOLOGI PERTANIAN Pada Departemen Teknologi Industri Pertanian
Fakultas Teknologi Pertanian Institut Pertanian Bogor
Oleh : Fifi Isdianti
F 34102078
2007
FAKULTAS TEKNOLOGI PERTANIAN INSTITUT PERTANIAN BOGOR
INSTITUT PERTANIAN BOGOR
FAKULTAS TEKNOLOGI PERTANIAN
PENJERNIHAN EKSTRAK DAUN STEVIA (Stevia rebaudianaBertoni
)
DENGAN ULTRAFILTRASI ALIRAN SILANGSKRIPSI
Sebagai salah satu syarat untuk memperoleh gelar SARJANA TEKNOLOGI PERTANIAN
Pada Departemen TEKNOLOGI INDUSTRI PERTANIAN Fakultas Teknologi Pertanian
Institut Pertanian Bogor
Oleh : Fifi Isdianti
F 34102078
Dilahirkan pada tanggal 30 Desember 1983 di Jambi
Tanggal lulus : Mei 2007
SURAT PERNYATAAN
Saya menyatakan dengan sebenar-benarnya bahwa skripsi dengan judul “Penjernihan Ekstrak Daun Stevia (Stevia rebaudiana Bertoni) Dengan Ultrafiltrasi Aliran Silang” adalah karya asli saya sendiri, dengan arahan dosen pembimbing akademik, kecuali dengan jelas rujukannya.
Bogor, Mei 2007
Yang Menyatakan Pernyataan
Fifi Isdianti. F 34102078. Penjernihan Ekstrak Daun Stevia (Stevia rebaudiana
Bertoni) Dengan Ultrafiltrasi Aliran Silang. Dibawah bimbingan Erliza Noor. 2007.
RINGKASAN
Industri makanan, minuman dan suplemen menggunakan bahan pemanis sebagai penambah cita rasa pada produk mereka. Bahan pemanis terbagi atas dua macam yaitu pemanis alami dan pemanis buatan. Bahan pemanis alami yang biasa digunakan adalah gula sukrosa atau gula tebu. Namun gula tebu/gula sukrosa memiliki kelemahan yaitu memiliki nilai kalori tinggi sehingga dapat menyebabkan kegemukan dan diabetes. Industri melirik ke pemanis buatan karena memiliki tingkat kemanisan tinggi dan rendah kalori. Namun pemanis buatan memiliki bersifat karsinogenik. Untuk itu dicari alternatif penggunaan pemanis alami yang memiliki tingkat kemanisan tinggi, rendah kalori, non-karsinogenik. Salah satu pemanis alami tersebut adalah pemanis stevia dari daun tanaman stevia.
Pemanis stevia diperoleh dari ekstrak daun stevia menggunakan pelarut polar seperti metanol, etanol, dan spiritus. Proses kedua yaitu pemurnian atau penjernihan umumnya dilakukan dengan cara pertukaran ion, menggunakan kolom absorbsi kromatografi, atau penjernihan dengan pelarut. Penggunaan pelarut kimia dikhawatirkan masih menyisakan pelarut pada produk. Untuk itu digunakan alternatif pelarut polar yang aman seperti air untuk mengesktraksi daun stevia. Penjernihan ekstrak daun stevia dilakukan dengan menggunakan membran ultrafiltrasi karena tidak adanya penambahan bahan kimia.
Penelitian bertujuan untuk mempelajari penjernihan ekstrak daun stevia dengan ultrafiltrasi aliran silang. Modul tubular yang dilengkapi dengan membran polietersulfon MWCO 20000 Dalton. Penelitian melihat pengaruh tekanan transmembran, kecepatan alir dan konsentrasi umpan terhadap fluksi, dan rejeksi membran dalam penjernihan pemanis stevia (steviosida)
Produksi pemanis stevia dilakukan dengan dua tahap. Tahap pertama yaitu penentuan suhu pengeringan dan suhu ekstraksi berdasarkan dengan pengukuran konsentrasi steviosida. Suhu pengeringan daun stevia yaitu 60oC, 80oC, dan 100oC dan suhu ekstraksi daun stevia dengan pelarut air yaitu 25oC, 40oC, 60oC, dan 100oC. Tahap kedua penjernihan dengan menggunakan membran ultrafiltrasi aliran silang. Pengamatan yang dilakukan antara lain pengaruh tekanan transmembran (1.49 bar, 1.61 bar, 1.65 bar, dan 1.87 bar), kecepatan alir (0.0029 m/s, 0.011 m/s, dan 0.02 m/s), dan konsentrasi umpan (20.4 g/L dan 28.7 g/L) terhadap fluksi, tingkat rejeksi membran terhadap steviosida, kenaikan konsentrasi larutan stevia dan karakteristik hasil larutan stevia.
Pada tahap pertama, konsentrasi steviosida tertinggi (8.9 g/L) diperoleh pada suhu pengeringan daun dan suhu mengekstrak daun yang digunakan adalah suhu
62%. Pada kecepatan alir yang rendah (0.0029 m/s dengan tekanan transmembran 1.61 bar), persen kejernihan meningkat sebesar 60% dan penurunan kadar abu sebesar 59%.
Fifi Isdianti. F34102078. Clarification of the Extract of Stevia Leaves (Stevia rebaudiana Bertoni) using Cross Flow Ultrafiltration. Supervised by Erliza Noor. 2007.
SUMMARY
Industry of food, beverage and food supplement use sweetener to improve the flavor of their products. Sweeteners are categorized into two kinds, namely natural sweetener and artificial sweetener. Natural sweeteners which are commonly used are sucrose sugar or cane sugar. However, cane sugar/sucrose sugar has weakness, namely high content of calories, which can cause obesity and diabetes. Industries try to study the possibility of using artificial sweetener because of its high level of sweetness and low calories. However, artificial sweetener is carcinogenic. Therefore, the use of alternative natural sweetener which has the properties of high level of sweetness, low calories and non carcinogenic, is sought after. One such natural sweetener is stevia sweetener, derived from stevia plant leaves.
Stevia sweetener is obtained from the extraction of stevia leaves using polar solvent such as methanol, ethanol and methylated spirit. The second process is purification or clarification which is usually conducted by ion exchange process, using chromatography absorption column, or clarification using solvent. It is worrying that the use of chemical solvent could leave residue on the product. Therefore it is necessary to use alternative safe polar solvent, such as water for extracting the stevia leaves. Clarification of the stevia leaf extract is conducted by using ultrafiltration membrane due to absence of chemicals addition.
The objective of this research was learning the clarification of the stevia leaf extract using cross flow ultrafiltration. Tubular module is equipped with polyethersulfone MWCO 20000 Dalton. This research observed the effect of transmembrane pressure, cross flow velocity and feed concentration, on flux and membrane rejection in clarifying the stevia sweetener (stevioside).
membrane pressure (1.87 bar and cross flow velocity of 0.02 m/s), percentage of clarity increased by 64% and ash content decrease was 62%. At low cross flow velocity (0.0029 m/s and transmembrane pressure of 1.61 bar) percentage of clarity increased by 60% and ash content decrease was 59%.
KATA PENGANTAR
Alhamdulillahirabbil’alamin, Puji dan syukur penulis kepada Allah SWT, karena atas rahmat dan karunia-Nya penulis mampu menyelesaikan penelitian dan menyusun skripsi dengan judul Penjernihan Ekstrak Daun Stevia (Stevia rebaudiana Bertoni) Dengan Ultrafiltrasi Aliran Silang dengan baik. Pada kesempatan ini penulis ingin menyampaikan terima kasih yang tulus atas bantuan dan dukungan yang telah diberikan oleh berbagai pihak selama penulis melakukan penelitian hingga penyusunan skripsi. Rasa terima kasih penulis sampaikan kepada :
1. Kedua orang tua penulis yang tercinta atas doa yaitu Zulfiati dan Zulpan Munir, nasihat dan kasih sayang yang tak pernah terputus serta adik – adik (Hendra dan Dafit) penulis atas semangat dan doa yang telah diberikan kepada penulis.
2. Dr. Ir. Erliza Noor sebagai dosen pembimbing akademik atas dorongan dan saran yang diberikan mulai dari persiapan penelitian hingga terselesaikannya skripsi ini.
3. Dr. Ir. Suprihatin selaku dosen penguji atas saran, kritik, dan fasilitas yang telah diberikan.
4. Ir. Indah Yuliasih, MSi. selaku dosen penguji atas saran, kritik dan kesediaan untuk meluangkan waktu.
5. Fitri, Harti, Eva, Yoga, Santo dan Vico terima kasih atas semangat dan kebersamaannya.
6. Beny Budiansyah atas doa, semangat, saran dan kritiknya.
7. Yeni dan Fatma yang bersedia membantu penulis selama penelitian.
8. Ibu Rini, Pak Gunawan, Pak Sugiardi dan para laboran di laboratorium TIN. 9. Rekan – rekan TIN angkatan 39 seperjuangan.
DAFTAR ISI
II. TINJAUAN PUSTAKA ...A. TANAMAN STEVIA ... B. STEVIA SEBAGAI PEMANIS ALAMI ... C. EKSTRAKSI PEMANIS STEVIA ... D. TEKNOLOGI MEMBRAN ... 1. Filtrasi Membran ... 2. Bahan Membran ... 3. Jenis Modul Membran ... E. MEMBRAN ULTRAFILTRASI ... F. KONDISI PROSES FILTRASI MEMBRAN ... G. PENJERNIHAN PEMANIS STEVIA ...
3 B. PROSEDUR PENELITIAN ...
19 19 20 IV.HASIL DAN PEMBAHASAN ...
A. Penentuan suhu pengeringan dan suhu ekstraksi daun stevia ... B. Penjernihan Larutan stevia dengan Ultrafiltrasi... 1. Fluksi Air ... 2. Kondisi Tunak Fluksi Larutan Stevia ... 3. Pengaruh Tekanan Transmembran Terhadap Fluksi... 4. Pengaruh Kecepatan Alir Terhadap Fluksi... 5. Pengaruh Konsentrasi Larutan Stevia Terhadap Fluksi...
PENJERNIHAN EKSTRAK DAUN STEVIA (Stevia rebaudianaBertoni
)
DENGAN ULTRAFILTRASI ALIRAN SILANGOleh : Fifi Isdianti
F 34102078
PENJERNIHAN EKSTRAK DAUN STEVIA (Stevia rebaudianaBertoni
)
DENGAN ULTRAFILTRASI ALIRAN SILANGSKRIPSI
Sebagai salah satu syarat untuk mendapatkan gelar SARJANA TEKNOLOGI PERTANIAN Pada Departemen Teknologi Industri Pertanian
Fakultas Teknologi Pertanian Institut Pertanian Bogor
Oleh : Fifi Isdianti
F 34102078
2007
FAKULTAS TEKNOLOGI PERTANIAN INSTITUT PERTANIAN BOGOR
INSTITUT PERTANIAN BOGOR
FAKULTAS TEKNOLOGI PERTANIAN
PENJERNIHAN EKSTRAK DAUN STEVIA (Stevia rebaudianaBertoni
)
DENGAN ULTRAFILTRASI ALIRAN SILANGSKRIPSI
Sebagai salah satu syarat untuk memperoleh gelar SARJANA TEKNOLOGI PERTANIAN
Pada Departemen TEKNOLOGI INDUSTRI PERTANIAN Fakultas Teknologi Pertanian
Institut Pertanian Bogor
Oleh : Fifi Isdianti
F 34102078
Dilahirkan pada tanggal 30 Desember 1983 di Jambi
Tanggal lulus : Mei 2007
SURAT PERNYATAAN
Saya menyatakan dengan sebenar-benarnya bahwa skripsi dengan judul “Penjernihan Ekstrak Daun Stevia (Stevia rebaudiana Bertoni) Dengan Ultrafiltrasi Aliran Silang” adalah karya asli saya sendiri, dengan arahan dosen pembimbing akademik, kecuali dengan jelas rujukannya.
Bogor, Mei 2007
Yang Menyatakan Pernyataan
Fifi Isdianti. F 34102078. Penjernihan Ekstrak Daun Stevia (Stevia rebaudiana
Bertoni) Dengan Ultrafiltrasi Aliran Silang. Dibawah bimbingan Erliza Noor. 2007.
RINGKASAN
Industri makanan, minuman dan suplemen menggunakan bahan pemanis sebagai penambah cita rasa pada produk mereka. Bahan pemanis terbagi atas dua macam yaitu pemanis alami dan pemanis buatan. Bahan pemanis alami yang biasa digunakan adalah gula sukrosa atau gula tebu. Namun gula tebu/gula sukrosa memiliki kelemahan yaitu memiliki nilai kalori tinggi sehingga dapat menyebabkan kegemukan dan diabetes. Industri melirik ke pemanis buatan karena memiliki tingkat kemanisan tinggi dan rendah kalori. Namun pemanis buatan memiliki bersifat karsinogenik. Untuk itu dicari alternatif penggunaan pemanis alami yang memiliki tingkat kemanisan tinggi, rendah kalori, non-karsinogenik. Salah satu pemanis alami tersebut adalah pemanis stevia dari daun tanaman stevia.
Pemanis stevia diperoleh dari ekstrak daun stevia menggunakan pelarut polar seperti metanol, etanol, dan spiritus. Proses kedua yaitu pemurnian atau penjernihan umumnya dilakukan dengan cara pertukaran ion, menggunakan kolom absorbsi kromatografi, atau penjernihan dengan pelarut. Penggunaan pelarut kimia dikhawatirkan masih menyisakan pelarut pada produk. Untuk itu digunakan alternatif pelarut polar yang aman seperti air untuk mengesktraksi daun stevia. Penjernihan ekstrak daun stevia dilakukan dengan menggunakan membran ultrafiltrasi karena tidak adanya penambahan bahan kimia.
Penelitian bertujuan untuk mempelajari penjernihan ekstrak daun stevia dengan ultrafiltrasi aliran silang. Modul tubular yang dilengkapi dengan membran polietersulfon MWCO 20000 Dalton. Penelitian melihat pengaruh tekanan transmembran, kecepatan alir dan konsentrasi umpan terhadap fluksi, dan rejeksi membran dalam penjernihan pemanis stevia (steviosida)
Produksi pemanis stevia dilakukan dengan dua tahap. Tahap pertama yaitu penentuan suhu pengeringan dan suhu ekstraksi berdasarkan dengan pengukuran konsentrasi steviosida. Suhu pengeringan daun stevia yaitu 60oC, 80oC, dan 100oC dan suhu ekstraksi daun stevia dengan pelarut air yaitu 25oC, 40oC, 60oC, dan 100oC. Tahap kedua penjernihan dengan menggunakan membran ultrafiltrasi aliran silang. Pengamatan yang dilakukan antara lain pengaruh tekanan transmembran (1.49 bar, 1.61 bar, 1.65 bar, dan 1.87 bar), kecepatan alir (0.0029 m/s, 0.011 m/s, dan 0.02 m/s), dan konsentrasi umpan (20.4 g/L dan 28.7 g/L) terhadap fluksi, tingkat rejeksi membran terhadap steviosida, kenaikan konsentrasi larutan stevia dan karakteristik hasil larutan stevia.
Pada tahap pertama, konsentrasi steviosida tertinggi (8.9 g/L) diperoleh pada suhu pengeringan daun dan suhu mengekstrak daun yang digunakan adalah suhu
62%. Pada kecepatan alir yang rendah (0.0029 m/s dengan tekanan transmembran 1.61 bar), persen kejernihan meningkat sebesar 60% dan penurunan kadar abu sebesar 59%.
Fifi Isdianti. F34102078. Clarification of the Extract of Stevia Leaves (Stevia rebaudiana Bertoni) using Cross Flow Ultrafiltration. Supervised by Erliza Noor. 2007.
SUMMARY
Industry of food, beverage and food supplement use sweetener to improve the flavor of their products. Sweeteners are categorized into two kinds, namely natural sweetener and artificial sweetener. Natural sweeteners which are commonly used are sucrose sugar or cane sugar. However, cane sugar/sucrose sugar has weakness, namely high content of calories, which can cause obesity and diabetes. Industries try to study the possibility of using artificial sweetener because of its high level of sweetness and low calories. However, artificial sweetener is carcinogenic. Therefore, the use of alternative natural sweetener which has the properties of high level of sweetness, low calories and non carcinogenic, is sought after. One such natural sweetener is stevia sweetener, derived from stevia plant leaves.
Stevia sweetener is obtained from the extraction of stevia leaves using polar solvent such as methanol, ethanol and methylated spirit. The second process is purification or clarification which is usually conducted by ion exchange process, using chromatography absorption column, or clarification using solvent. It is worrying that the use of chemical solvent could leave residue on the product. Therefore it is necessary to use alternative safe polar solvent, such as water for extracting the stevia leaves. Clarification of the stevia leaf extract is conducted by using ultrafiltration membrane due to absence of chemicals addition.
The objective of this research was learning the clarification of the stevia leaf extract using cross flow ultrafiltration. Tubular module is equipped with polyethersulfone MWCO 20000 Dalton. This research observed the effect of transmembrane pressure, cross flow velocity and feed concentration, on flux and membrane rejection in clarifying the stevia sweetener (stevioside).
membrane pressure (1.87 bar and cross flow velocity of 0.02 m/s), percentage of clarity increased by 64% and ash content decrease was 62%. At low cross flow velocity (0.0029 m/s and transmembrane pressure of 1.61 bar) percentage of clarity increased by 60% and ash content decrease was 59%.
KATA PENGANTAR
Alhamdulillahirabbil’alamin, Puji dan syukur penulis kepada Allah SWT, karena atas rahmat dan karunia-Nya penulis mampu menyelesaikan penelitian dan menyusun skripsi dengan judul Penjernihan Ekstrak Daun Stevia (Stevia rebaudiana Bertoni) Dengan Ultrafiltrasi Aliran Silang dengan baik. Pada kesempatan ini penulis ingin menyampaikan terima kasih yang tulus atas bantuan dan dukungan yang telah diberikan oleh berbagai pihak selama penulis melakukan penelitian hingga penyusunan skripsi. Rasa terima kasih penulis sampaikan kepada :
1. Kedua orang tua penulis yang tercinta atas doa yaitu Zulfiati dan Zulpan Munir, nasihat dan kasih sayang yang tak pernah terputus serta adik – adik (Hendra dan Dafit) penulis atas semangat dan doa yang telah diberikan kepada penulis.
2. Dr. Ir. Erliza Noor sebagai dosen pembimbing akademik atas dorongan dan saran yang diberikan mulai dari persiapan penelitian hingga terselesaikannya skripsi ini.
3. Dr. Ir. Suprihatin selaku dosen penguji atas saran, kritik, dan fasilitas yang telah diberikan.
4. Ir. Indah Yuliasih, MSi. selaku dosen penguji atas saran, kritik dan kesediaan untuk meluangkan waktu.
5. Fitri, Harti, Eva, Yoga, Santo dan Vico terima kasih atas semangat dan kebersamaannya.
6. Beny Budiansyah atas doa, semangat, saran dan kritiknya.
7. Yeni dan Fatma yang bersedia membantu penulis selama penelitian.
8. Ibu Rini, Pak Gunawan, Pak Sugiardi dan para laboran di laboratorium TIN. 9. Rekan – rekan TIN angkatan 39 seperjuangan.
DAFTAR ISI
II. TINJAUAN PUSTAKA ...A. TANAMAN STEVIA ... B. STEVIA SEBAGAI PEMANIS ALAMI ... C. EKSTRAKSI PEMANIS STEVIA ... D. TEKNOLOGI MEMBRAN ... 1. Filtrasi Membran ... 2. Bahan Membran ... 3. Jenis Modul Membran ... E. MEMBRAN ULTRAFILTRASI ... F. KONDISI PROSES FILTRASI MEMBRAN ... G. PENJERNIHAN PEMANIS STEVIA ...
3 B. PROSEDUR PENELITIAN ...
19 19 20 IV.HASIL DAN PEMBAHASAN ...
A. Penentuan suhu pengeringan dan suhu ekstraksi daun stevia ... B. Penjernihan Larutan stevia dengan Ultrafiltrasi... 1. Fluksi Air ... 2. Kondisi Tunak Fluksi Larutan Stevia ... 3. Pengaruh Tekanan Transmembran Terhadap Fluksi... 4. Pengaruh Kecepatan Alir Terhadap Fluksi... 5. Pengaruh Konsentrasi Larutan Stevia Terhadap Fluksi...
6. Tingkat Rejeksi Membran dan kenaikan konsentrasi... C. Karakteristik Larutan Stevia ... D. PEMBAHASAN UMUM...
34 35 45 V. KESIMPULAN DAN SARAN ...
A. KESIMPULAN ... B. SARAN ...
DAFTAR GAMBAR Gambar 7. Karakteristik proses membran... 15 Gambar 8. Sistem Aliran Umpan Pada Membran... 17 Gambar 9. Diagram alir proses filtrasi dengan membran Ultrafiltrasi ... 19 Gambar 10. Kadar air daun selama pengeringan ... 23 Gambar 11. Larutan stevia setelah ekstraksi... 24 Gambar 12. Konsentrasi steviosida larutan stevia pada berbagai suhu
pengeringan dan suhu ekstraksi ... 26 Gambar 13. Kadar gula total larutan stevia pada berbagai
kondisi suhu pengeringan dan ekstraksi... 27 Gambar 14. Hubungan antara lama filtrasi dengan fluksi pada air
destilata pada tekanan 1.87 bar, kecepatan alir 0.04 m/s ... 28 Gambar 15. Grafik hubungan antara lama filtrasi larutan stevia dengan
fluksi pada kecepatan 0.02 m/s dan tekanan 1.23 bar ... 29 Gambar 16. Grafik hubungan antara tekanan transmembran terhadap
fluksi pada beberapa konsentrasi dan kecepatan alir
0.02 m/s ... 30 Gambar 17. Hubungan tekanan transmembran dengan fluksi pada
air destilata dan kecepatan alir 0.04 m/s ... 31 Gambar 18. Grafik hubungan antara kecepatan alir dengan nilai
fluksi pada berbagai konsentrasi dan tekanan transmembran
1.61 bar... 32 Gambar 19. Grafik hubungan antara konsentrasi larutan stevia dengan
nilai fluksi pada tekanan transmembran 1.61 bar, kecepatan alir 0.02 m/s... 33 Gambar 20. Perubahan pH pada berbagai konsentrasi umpan steviosida
dan tekanan... 36 Gambar 21. Perubahan pH pada berbagai konsentrasi umpan
Gambar 22. Perubahan konsentrasi steviosida pada berbagai
konsentrasi umpan steviosida dan tekanan ... 37 Gambar 23. Perubahan konsentrasi steviosida pada berbagai
konsentrasi umpan steviosida dan kecepatan alir... 38 Gambar 24. Perubahan kadar gula total pada berbagai konsentrasi
umpan steviosida dan tekanan... 39 Gambar 25. Perubahan kadar gula total pada berbagai konsentrasi
umpan steviosida dan tekanan... 40 Gambar 26. Perbandingan nilai tingkat kejernihan sebelum (umpan) dan
setelah (permeat) filtrasi oleh membran pada berbagai
tekanan ... 41 Gambar 27. Perbandingan nilai tingkat kejernihan sebelum (umpan)
dan setelah (permeat) filtrasi oleh membran pada berbagai
kecepatan alir ... 41 Gambar 28. Hasil pemurnian larutan stevia (a) umpan, permeat pada (b)
tekanan 1.49 bar, (c) tekanan 1.65 bar, (d) tekanan 1.87 bar 42 Gambar 29. Nilai kadar abu sebelum dan sesudah filtrasi pada
konsentrasi larutan stevia dan tekanan... 43 Gambar 30. Nilai kadar abu sebelum dan sesudah filtrasi pada
DAFTAR TABEL
DAFTAR LAMPIRAN
Halaman Lampiran 1. Perangkat Alat Percobaan ... 52 Lampiran 2. Spesifikasi Teknik Unit Ultrafiltrasi ... 53 Lampiran 3. Diagram alir penentuan suhu pengeringan dan suhu
ekstraksi ... 54 Lampiran 4. Diagram alir pembuatan larutan stevia pada berbagai
konsentrasi untuk proses penjernihan ... 55 Lampiran 5. Data perhitungan konsentrasi steviosida dengan
spektrofotometer UV (λ=210 nm)... 56 Lampiran 6. Prosedur Analisis Sebelum dan Sesudah Filtrasi
membran polyethersulfone (membran Ultrafiltrasi) ... 58 Lampiran 7. Hasil Analisa Fitokimia Daun Stevia... 60 Lampiran 8. Hasil Analisa Tahap Pertama ... 61 Lampiran 9. Data Fluksi Air Hasil Penyaringan Dengan Menggunakan
Membran (P=1.87 bar; v=0.04 m/s)... 62 Lampiran 10. Data Penentuan Kondisi Tunak Larutan Stevia
(P= 1.23 bar; T= 40oC; CFV= 0.02 m/s dan C=28.7 g/L... 64 Lampiran 11. Data Hasil Filtrasi Dengan Membran Ultrafiltrasi... 65 Lampiran 12. Data Analisis hasil pemurnian larutan stevia dengan
membran ultrafiltrasi... 66 Lampiran 13. Hasil Uji High Performance Liquid Chromatography
I. PENDAHULUAN
A. LATAR BELAKANG
Industri makanan, minuman, dan suplemen menggunakan pemanis sebagai penambah cita rasa pada produknya. Bahan pemanis terbagi atas dua macam yaitu pemanis alami dan pemanis buatan. Bahan pemanis alami yang biasa digunakan adalah gula sukrosa atau gula tebu. Namun gula tersebut memiliki beberapa kelemahan yaitu memiliki nilai kalori tinggi yang dapat menyebabkan kegemukan dan diabetes. Industri makanan, minuman, dan suplemen menggunakan pemanis buatan karena memiliki tingkat kemanisan yang tinggi dan rendah kalori. Namun pemanis buatan memiliki sifat yang karsinogenik yaitu penyebab kanker. Untuk itu dicari alternatif pemanis alami yang memiliki tingkat kemanisan yang tinggi, rendah kalori dan tidak bersifat karsinogenik. Salah satu pemanis alami tersebut adalah pemanis stevia dari daun tanaman stevia. Gula sukrosa termasuk ke dalam pemanis nutritif dimana pemanis tersebut menghasilkan kalori sebesar 4 kalori/gram. Stevia termasuk pemanis yang kalorinya tidak ada sama sekali (Anonim, 2007).
Pemanis stevia diperoleh dengan mengekstraksi daun stevia menggunakan pelarut polar yaitu metanol, etanol, atau spiritus. Penggunaan pelarut kimia dikhawatirkan masih menyisakan pelarut pada produk. Untuk itu digunakan pelarut polar yang aman untuk mengekstraksi daun stevia yaitu air.
Proses penjernihan dengan membran adalah proses pemisahan pengotor–pengotor bukan pemanis dari larutan stevia. Pengotor–pengotor yang memiliki bobot molekul lebih besar dari MWCO membran 20000 Dalton seperti senyawa yang menyebabkan warna (pigmen), makromolekul dan protein dapat tertahan sedangkan molekul air dan molekul pemanis stevia dapat lolos berdasarkan bobot molekul tertentu. Kelebihan penjernihan menggunakan membran ultrafiltrasi adalah tidak adanya penambahan bahan kimia selama proses.
Proses penjernihan dengan membran ultrafiltrasi memiliki kelemahan yaitu terjadi rejeksi yang menyebabkan sebagian solut tertahan pada membran. Selain itu juga kelemahannya terdapat pada umur pakai membran yang tidak lama dan harga membran yang tinggi. Penelitian ini mengkaji pengaruh tekanan transmembran, kecepatan alir, dan konsentrasi umpan terhadap fluksi pada membran ultrafiltrasi serta rejeksi membran terhadap pemanis stevia.
B. TUJUAN
Tujuan Penelitian ini antara lain:
1. Mempelajari penjernihan ekstrak daun stevia dengan ultrafiltrasi aliran silang,
2. Mempelajari pengaruh tekanan transmembran, konsentrasi umpan, dan kecepatan alir terhadap fluksi,
II. TINJAUAN PUSTAKA
A. TANAMAN STEVIA
Stevia merupakan tanaman berbentuk perdu (semak), tingginya antara 60 - 90 cm dengan panjang daun 3 - 7 cm dan memiliki banyak cabang. Batang stevia bentuknya lonjong, ditumbuhi oleh bulu-bulu yang halus. Demikian pula tepi daunnya yang bergerigi tampak halus. Bentuk daun stevia lonjong, langsing dan duduk berhadapan. Tanaman stevia dapat tumbuh dengan baik di tanah latosol yang berwarna merah pada ketinggian 500 - 1500 m dari permukaan laut (Lutony (1993), Sudarmaji (1982)).
Gambar 1. Tanaman Stevia rebaudiana Bertoni M
Menurut Lutony (1993) stevia memiliki sistem pengakaran serabut dan terbagi menjadi dua bagian yakni perakaran halus dan perakaran tebal. Bunganya hermaprodite dengan mahkota yang khas berbentuk seperti tabung. Salah satu kelebihan tanaman ini adalah daya regenerasinya yang kuat sehingga tahan terhadap pemangkasan.
sembung-sembungan. Tanaman ini dapat diperbanyak melalui stek, biji, anakan, dan kultur jaringan yang termasuk pada divisi Spermatophyta, kelas
Dicotyledone, dan ordo Campanulatae (Lutony, 1993). Klasifikasi tanaman
Steviarebaudiana B.dapat dilihat pada Tabel 1.
Tabel1.Klasifikasi tanaman Stevia rebaudiana Bertoni. Famili Asteraceae
Genus Stevia Spesies rebaudiana
Sinonim Eupatorium rebaudianum Nama Umum Stevia
Bagian yang digunakan
daun
Sumber : Taylor, 2005
Tanaman stevia dikenal pertama kali di Indonesia sekitar tahun 1977, dan telah dicoba pembudidayaannya dibeberapa daerah seperti Tawangmangu, Sukabumi, Garut, dan Bengkulu dengan ketinggian sekitar 1000 meter di atas permukaan laut. Berdasarkan penelitian Atmoko (2001) bahwa pemberian gambut tanah latosol berpengaruh nyata terhadap jumlah daun, sedangkan terhadap tinggi tanaman, bobot basah dan kering tajuk dan akar tidak berpengaruh nyata. Media tanah gambut 100 % dapat meningkatkan kandungan gula (10.06 %) pada daun stevia, dibandingkan dengan 0 % gambut (7.91 %).
B. STEVIA SEBAGAI PEMANIS ALAMI
1. Rebaudiosida A
Sifat–sifat yang dimiliki senyawa ini adalah titik lebur 235 – 237 oC, berbentuk kristal menyerupai jarum, [α]D = - 15.3o (dalam metanol).
2. Rebaudiosida B
Sifat-sifat yang dimiliki senyawa ini adalah titik lebur 193 – 195oC, berbentuk kristal menyerupai jarum, [α]D = - 45.4o (dalam metanol).
Senyawa ini selain terdapat didalam daun stevia juga dapat diperoleh dari hasil hidrolisis alkalis maupun enzimatis rebaudiosida A.
3. Rebaudiosida C
Sifat–sifat yang dimiliki senyawa ini titik lebur 235 – 238 oC, berbentuk kristal menyerupai jarum, [α]D = - 28.7o (dalam metanol).
4. Rebaudiosida D
Apabila senyawa ini dihidrolisis dengan asam sulfat akan mengakibatkan terputusnya ikatan monosakarida yang terikat, sedangkan hidrolisis oleh alkali dan enzim hanya mampu memutuskan sebagian monosakarida. 5. Rebaudiosida E
Rebaudiosida E tersusun atas empat molekul glukosa dan satu molekul aglikon. Keempat molekul glukosa tersebut dua molekul membentuk disakarida yang terikat pada atom C13 molekul aglikon, sedangkan dua
molekul yang lain membentuk disakarida terikat pada atom C18.
6. Dulkosida A
Sifat–sifat senyawa ini adalah titik lebur 193 – 195 oC, berbentuk kristal menyerupai jarum, [α]D = - 46.7o (dalam metanol).
7. Steviolibiosida
Sifat–sifat yang dimiliki senyawa ini adalah titik lebur 188 – 199 oC, berbentuk kristal menyerupai jarum, [α]D = - 37.4o (dalam metanol).
8. Steviosida
Steviosida memiliki rumus molekul C38H60O18 yang terdiri dari 56.7%
unsur C, 7.51% unsur H, dan 35.78% unsur O dengan berat molekul 804.90. Titik lebur senyawa ini adalah 198oC, [α]D = - 39.3o (dalam air).
disebabkan steviosida masih memiliki rasa sepat dan langu. Rasa sepat dan langu ternyata tidak terdapat pada senyawa yang lainnya. Jika rebaudiosida A, D dan E digabungkan maka campurannya akan memiliki tingkat kemanisan yang setara dengan steviosida (Lutony, 1993).
Glikosida merupakan senyawa organik yang mengandung senyawa gula (glycone) dan bukan gula (aglycone). Glycone terdiri dari unsur pokok yaitu rhamnose, fruktosa, glukosa, xylosa, arabinosa. Sedangkan yang lainnya terdiri dari senyawa kimia yaitu sterol, tanin, dan karotenoid. Selain itu juga stevia mengandung protein, karbohidrat, fosfor, besi, kalsium, potasium, sodium, flavonoid, zinc, vitamin C dan vitamin A (Elkins, 1997). Struktur kimia steviosida dapat dilhat pada Gambar 2.
Gambar 2. Struktur molekul stevioside (Geuns, 2003)
produk makanan dan minuman (Sudarmaji, 1982). Glikosida bila dikristalkan akan terbentuk serbuk putih yang tidak berbau dan tingkat kemanisan dari glikosida pada daun stevia dapat terlihat pada Tabel 2.
Tabel 2. Komposisi glikosida di dalam daun stevia
No.
Jenis senyawa R1 R2 Potensi kemanisan
(sukrosa = 1)
Stevia merupakan sumber alternatif yang berpotensial untuk menggantikan pemanis buatan seperti sakarin, aspartam, asulfam dan lain-lain. Stevioside tidak seperti pemanis rendah kalori yang lain, karena bersifat stabil terhadap suhu dan memiliki pH antara 3 - 9. Industri makanan mulai meluncurkan produk yang menggunakan stevia (Anonim, 2004).
Ekstrak dari daun stevia dapat digunakan sebagai bahan tambahan seperti penyedap makanan atau bahan pemanis pada suplemen, tapi stevia bukan seperti pemanis–pemanis yang tersedia di pertokoan. Zoltan P. Rona, M. D. menulis tentang stevia di terbitan Health Naturally mengatakan bahwa stevia merupakan tumbuhan perdu yang ekstraknya aman dikonsumsi. Selama berabad-abad bangsa Paraguay dan Brazil mengkonsumsi pemanis alami ini. Stevia termasuk pemanis yang bebas kalori, dapat mencegah gigi berlubang, dan tidak memicu gula darah meningkat. Sebagaimana diketahui bahwa pemanis ini dapat membantu penderita diabetes karena berperan dalam proses metabolisme gula (Martini, 1998).
Menurut Acton (1976) pemanis nirkalori yang ideal memiliki sifat, larut dalam air, stabil terhadap panas/kimiawi, tidak beracun, mamiliki rasa tunggal (pure of flavor), dan intensitas rasa manisnya tinggi. Steviosida telah memenuhi beberapa persyaratan diatas. Kandungan beberapa senyawa dapat pada daun tanaman stevia dilihat pada Tabel 3.
Tabel 3. Kandungan beberapa senyawa pada daun tanaman stevia Komponen Kandungan *(%) Rendemen** (%)
Steviosida 5-15 2.52
Rebaudiosida 3-6 1.40
Rebaudiosida B Sedikit sekali 0.04 Steviolbiosida Sedikit sekali 0.04
Bridel dan Lavielle (1931) melakukan ekstraksi daun stevia dengan menggunakan alkohol dan menghasilkan glikosida berbentuk kristal dan tidak memiliki atom nitrogen, glikosida ini dinamakan “stevioside”. Kristal stevioside yang terkandung di dalam daun stevia menyebabkan rasa manis.
Cara ekstraksi daun stevia untuk mengeluarkan komponen pemanis dari daun ada tiga macam yaitu ekstraksi dengan pelarut air yang merupakan modifikasi prosedur Wood et al. (1955), ekstraksi dengan pelarut menguap seperti metanol teknik menurut prosedur Kohda et al. (1976) dan ekstraksi dengan pengepresan hidraulik. Penelitian ini menggunakan pelarut air untuk memperoleh pemanis glikosida pada daun stevia.
Pelarut yang sesuai digunakan untuk ekstraksi daun stevia adalah pelarut polar antara lain air dan alkohol. Pelarut yang baik harus mempunyai sifat: daya larut dan selektivitas terhadap glikosida tinggi, tak bereaksi (merusak) senyawa yang diinginkan, setelah proses ekstraksi dapat dipisahkan dengan mudah. Disamping itu harus tidak mempunyai efek racun, mudah didapat serta murah harganya (Anwar, 1982). Urutan polaritas pelarut menurun sebagai berikut: air, metanol, etanol, n-propanol, aseton, etil asetat, etil eter, kloroform, diklorometan, benzen (Anonim, 2006). Sifat-sifat yang hasil ekstraksi pemanis stevia dengan pelarut metanol dan air dapat dilihat pada Tabel 4.
Tabel 4. Sifat-sifat hasil ekstraksi pemanis stevia Jenis pelarut Sifat-sifat hasil ekstraksi
Metanol Air
Bentuk Bubuk Kasar Cairan kental
Warna Putih kehijauan Coklat
Rendemen 4.4 % ---
Kadar air 4.5 % ---
Rasa Manis Manis
Sumber : Muhammad (1983)
dan setelah dilakukan proses kristalisasi, ternyata tidak terbentuk kristal pemanis stevia (Muhammad, 1983).
Kumar (2000) mengembangkan proses ekstraksi dan penjernihan ekstrak daun stevia dengan mengurangi jumlah unit operasi dan mengurangi dan atau menghilangkan penggunaan kimia termasuk pelarut organik. Operasi tersebut adalah menggunakan membran ultrafiltrasi dan mikrofiltrasi. Kumar menyatakan bahwa air efektif untuk mengekstraksi glikosida dengan pemilihan pH dan suhu.
Zairisman (1984) mengatakan bahwa penentuan kadar stevioside dan rebaudioside-A telah dilakukan oleh beberapa peneliti melalui beberapa cara, yaitu thin layer densitometry, cara droplet counter-current chromatography,
cara High Performance Liquid Chromatography cara dual wavelength thin layer chromatography scanner dan cara two dimentional thin layer chromatography.
D. TEKNOLOGI MEMBRAN 1. Filtrasi Membran
Menurut Cheryan (1998) bahwa filtrasi didefinisikan sebagai pemisahan dua atau lebih komponen yag bersifat cairan atau gas berdasarkan ukuran molekul dengan mengalirkan umpan melalui membran. Sedangkan untuk membran diartikan sebagai selaput
semipermeable yang melewatkan spesi tertentu dan menahan spesi yang lain berdasarkan ukuran spesi yang akan dipisahkan. Spesi yang berukuran besar akan tertahan dan yang ukurannya lebih kecil akan dilewatkan (Mulder, 1996).
1. Proses dapat dilakukan pada suhu kamar, sehingga cocok untuk pemisahan komponen yang tidak tahan pada suhu tinggi.
2. Tidak terjadi perubahan fase komponen
3. Penggunaan energi lebih rendah karena energi yang digunakan hanya untuk menggerakkan pompa.
4. Proses dapat terjadi secara simultan.
2. Bahan Membran
Menurut Mulder (1996), membran dapat dibuat dari berbagai material. Material yang digunakan terbagi ke dalam dua kelas yaitu membran sintetik dan membran biologi. Membran sintetik terbagi menjadi membran organik dan anorganik. Membran biologi dibutuhkan oleh makhluk hidup di muka bumi untuk kelangsungan hidupnya. Industri pada umumnya menggunakan membran dengan bahan polimer. Material membran yang biasa digunakan adalah selulosa asetat, selulosa triasetat, poliakrilonitril, poliamida, polisulfon, polietersulfon, dan poliolefin (Wenten, 1999).
Pemilihan polimer sebagai bahan baku pembuatan membran berdasarkan faktor struktural. Faktor struktural akan menentukan sifat termal, kimia dan mekanik. Setiap faktor tersebut akan mempengaruhi sifat intrinsik polimer yaitu permeabilitas. Kinerja membran ditunjukkan oleh fluksi dan selektivitasnya, dimana selektivitas merupakan parameter utama dari membran ultrafiltrasi (Wenten, 1999). Material membran yang digunakan dalam penelitian ini adalah polietersulfon (PES).
Polisulfone (PSF) adalah hasil reaksi polimerik antara garam natrium bisphenol-A dan garam natrium di-p-dicholorodiphenyl sulfone. PSF memiliki nilai Tg = 195oC sedangkan polietersulfon (PES) memiliki Tg = 230oC, sehingga memberikan stabilitas termal dan stabilitas oksidatif yang baik, kekuatan dan fleksibilitasnya tinggi, tahan terhadap pH yang ekstrim
SO2
cukup baik, dan mudah untuk membran pabrikasi dalam konfigurasi variasi yang luas (Wenten, 1999).
3. Jenis Modul Membran
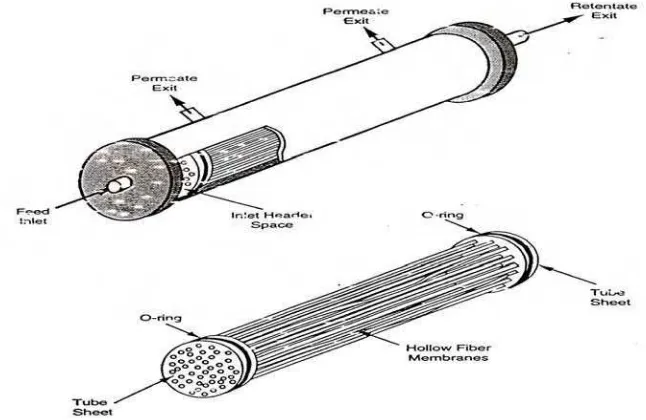
Berbagai bentuk membran biasa disebut modul. Menurut Zeman (1996) bahwa modul membran ada empat macam yaitu hollow fiber,
tubular devices, flate plate, dan spiral wound. Hollow fiber merupakan unit yang dikembangkan untuk ultrafiltrasi dam mikrofiltrasi. Oleh amicon dan ramicon pada tahun 1970. Hollow fiber berbentuk silinder dengan membran yang dapat diletakkan dibagian luar, dalam atau bahkan pada kedua permukaan. Diameter fibernya antara 200-2500 µm, jumlah fiber dalam satu bundelan sekitar 50 – 10.000 fiber (Gambar 4).
Gambar 4. Modul membran hollow fiber (Zeman, 1996)
Gambar 5. Modul membran tubular (Zeman, 1996)
Modul flate-and-frame menggunakan membran multi flate sheet
dengan susunan seperti sandwich/lapisan – lapisan (gambar 6a). Sedangkan modul wound spiral seperti flate sheet yang dibentuk seperti
catridge dan bagian tengah terdapat saluran untuk mengeluarkan permeat (gambar 6b).
a. Spiral wound b. Flat Plate
Gambar 6. Modul Membran (Zeman,1996)
E. MEMBRAN ULTRAFILTRASI
membran tersebut dibedakan berdasarkan ukuran pori. Perbedaan membran tersebut dapat dilihat pada Tabel 5.
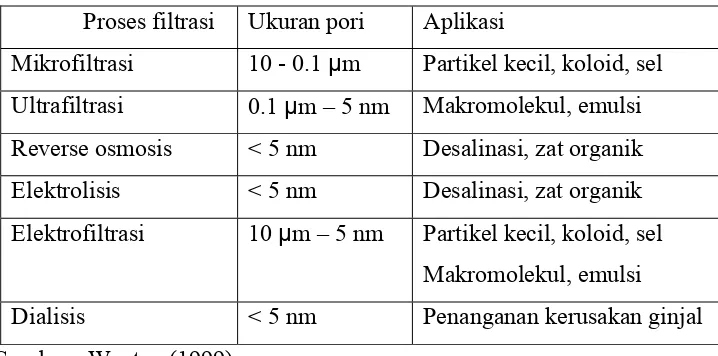
Tabel 5. Klasifikasi membran berdasarkan perbedaan ukuran pori Proses filtrasi Ukuran pori Aplikasi
Mikrofiltrasi 10 - 0.1 µm Partikel kecil, koloid, sel Ultrafiltrasi 0.1 µm – 5 nm Makromolekul, emulsi Reverse osmosis < 5 nm Desalinasi, zat organik Elektrolisis < 5 nm Desalinasi, zat organik Elektrofiltrasi 10 µm – 5 nm Partikel kecil, koloid, sel
Makromolekul, emulsi Dialisis < 5 nm Penanganan kerusakan ginjal Sumber : Wenten (1999)
Membran ultrafiltrasi merupakan proses filtrasi antara nanofiltrasi dan mikrofiltrasi. Membran ultrafiltrasi mempunyai porositas tinggi dan dapat menahan makromolekul bertekanan rendah sehingga “solut” yang kecil dapat lewat bersama air, tekanan yang dibutuhkan untuk proses yaitu berkisar 1 – 10 bar (Mulder, 1996).
Karakteristik cutoff dari membran ultrafiltrasi umumnya dikenal dengan
molecular weight cutoff. Membran ultrafiltrasi tidak akan melewatkan molekul yang memiliki berat molekul lebih dari MWCO.
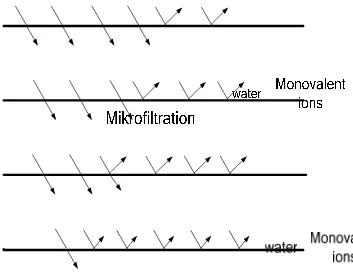
Gambar 7. karakteristik proses membran (www.kochmembran.com)
Membran ultrafiltrasi akan menahan protein dan senyawa koloid yaitu komponen yang memiliki molekul terbesar dan melewatkan komponen atau senyawa yang memiliki berat molekul yang kecil (Gambar 7).
Nanofiltrasi memiliki ukuran pori sekitar 1 nanometer. Membran nanofiltrasi banyak diaplikasi pada pemisahan garam bervalensi dua dari air dan fraksinasi molekul yang kecil di berbagai industri (Gambar 7). Kinerja membran nanofiltrasi dipengaruhi oleh karakterisrik membran yang mencakup fluksi, rejeksi dan Molecular Weight Cut-Off (Mulder, 1996). Hasil penelitian Kumar (2000) menunjukkan bahwa dengan pemisahan nanofiltrasi diakhir operasi dapat mengurangi rasa pahit pada komponen pemanis stevia karena senyawa tersebut ikut tercuci.
F. KONDISI PROSES FILTRASI MEMBRAN
transmembran, kecepatan crossflow dan konsentrasi larutan. Dipertegas pula oleh Cheryan (1986) bahwa faktor penting yang dapat mempengaruhi fluksi pada proses ultrafiltrasi yaitu tekanan transmembran, konsentrasi larutan umpan, suhu dan laju alir serta jenis aliran bahan.
Menurut Pritchard, et al (1995), menyatakan bahwa kecepatan crossflow
dapat mempengaruhi nilai fluksi, dengan semakin tinggi kecepatan crossflow
yang digunakan maka semakin besar fluksi yang dihasilkan. Hal tersebut disebabkan karena semakin banyaknya partikel dipermukaan membran yang bisa digerakkan oleh aliran umpan.
Performansi dan efisiensi membran ditentukan oleh dua parameter yaitu
fluks dan selektifitas. Fluksi adalah jumlah volume permeat yang diperoleh pada operasi membran per satuan waktu per luas permukaan membran (Wenten, 1999).
Fluksi volume (Mulder, 1996)
t
Pada proses filtrasi, di atas permukaan membran maupun di dalam pori– pori membran akan terdapat partikel–partikel yang tertahan. Hal tersebut menunjukkan bahwa membran memiliki nilai rejeksi terhadap larutan umpan. Nilai rejeksi dihitung dengan mengetahui konsentrasi umpan
Umpan
Permeat
Faktor yang menyebabkan keterbatasan penggunaan membran berpori adalah terjadinya peristiwa fouling dan polarisasi konsentrasi. Fouling adalah suatu peristiwa penurunan nilai fluksi akibat terakumulasinya komponen-komponen disekitar membran yang menutupi pori–pori membran. Polarisasi konsentrasi adalah terbentuknya lapisan kedua (second layer) pada permukaan membran yang dapat meningkatkan resistensi membran. Peristiwa fouling
identik dengan penurunan fluksi permeat dan perubahan selektivitas pada membran. Fouling terjadi akibat interaksi spesifik secara fisik dan kimia antara berbagai padatan terlarut dengan membran. Fouling dihilangkan dengan melakukan backflushing, penggunaan laju alir silang yang tinggi atau pembersihan secara kimiawi. Penurunan fluksi secara cepat pada awal filtrasi akibat pengaruh dari polarisasi konsentrasi, tetapi pada penurunan fluksi dalam jangka waktu yang panjang merupakan kontribusi dari terjadinya
fouling pada membran (Wenten, 1999).
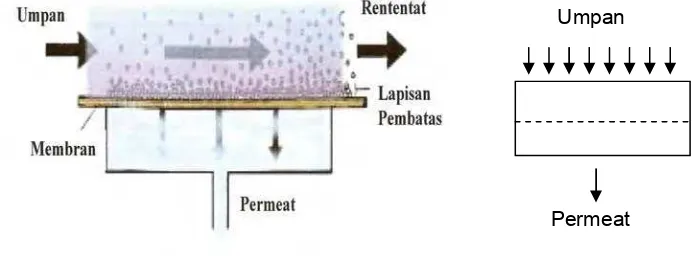
Menurut Mulder (1996) sistem membran terbagi menjadi empat yaitu : (i) dead–end, (ii) crossflow, (iii) hybrid dead–end/crossflow dan (iv) cascade. Sistem crossflow (aliran silang) dapat memperkecil terjadinya fouling karena pembentukan cake yang sangat lambat akibat gaya geser. Sistem crossflow
menurut Noor (2003) yaitu mengalirkan umpan sejajar dengan permukaan membran sehingga solut yang terejeksi dipermukaan membran akan tersapu oleh aliran tersebut. Padatan yang terakumulasi dipermukaan membran dan membentuk lapisan, proses ini disebut dead–end system. Gambar aliran umpan secara dead–end dan crossflow (aliran silang) dapat dilihat pada Gambar 8.
(a) Sistem aliran silang (crossflow) (b) Sistem dead-end
Pada air murni semakin tinggi tekanan yang diberikan, maka fluksi air juga akan semakin tinggi. Fenomena yang terjadi pada larutan, ketika tekanan dinaikkan pada batas tertentu akan menaikkan fluksi tetapi setelah mencapai tekanan tertentu maka fluksi tidak meningkat walaupun tekanan dinaikan, maksimum fluksi ini disebut limiting flux (Wenten, 1999).
G. PENJERNIHAN EKSTRAK DAUN STEVIA
Penjernihan ekstrak daun stevia bertujuan untuk menghilangkan atau membuang semaksimal mungkin bagian bukan pemanis stevia yang terkandung di dalam ekstrak stevia. Hasil ekstraksi daun stevia menggunakan pelarut air masih dalam bentuk ekstrak kasar. Jika ekstrak kasar tidak jernihkan maka tidak dapat dikomersialkan karena rasanya masih sepat, dan warnanya gelap. Kotoran dalam ekstrak kasar terdiri dari pigmen organik dan garam inorganik (Wang, 2002).
Beberapa proses telah dikembangkan dalam penjernihan dan pemurnian pemanis stevia yaitu ekstraksi dengan pelarut, flokulasi dan prespitasi, ion exchange, adsorpsi dengan menggunakan adsorben polimer, adsorpsi dengan menggunakan adsorben inorganik, pemisahan dengan kolom kromatografi, ultrafiltrasi dan pemisahan membran, dan ekstraksi dengan supercritical gas. Pemurnian diatas telah dipelajari untuk pemurnian glikosida stevia (Wang, 2002).
III. METODOLOGI PENELITIAN
A. BAHAN DAN ALAT 1. Bahan
Bahan yang digunakan untuk ekstraksi adalah daun stevia (Stevia rebaudiana Bertoni) yang diperoleh dari kebun Percobaan milik BUMN Perkebunan di Ciomas, air destilata pH 7, membran polyethersulfone
(PES) MWCO 20000 Dalton. Bahan untuk analisa antara lain fenol 5%, H2SO4 PA, NaOH 0.1% untuk membersihkan membran.
2. Alat
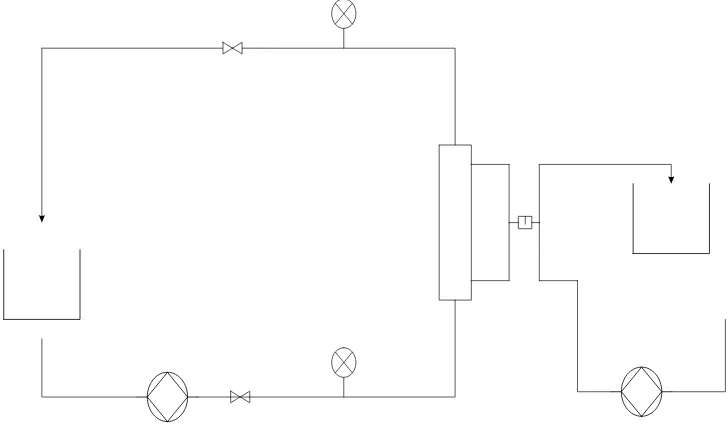
Peralatan yang digunakan adalah oven kipas, waterbatch, gelas piala, termometer, saringan 65 mesh, timbangan analitik, cawan porselen, desikator, alat HPLC merk Waters dari USA, spektrofotometer UV merk Thermospectronic V4.60, gelas ukur, labu takar, pipet mohr, penangas, vortex, pompa dengan sistem modul aliran silang (gambar peralatan dapat dilihat pada Lampiran 1), modul membran ultrafiltrasi yang berbentuk
hollow fiber. Spesifikasi alat ultrafiltrasi dapat dilihat pada Lampiran 2. Diagram alir ditunjukkan pada Gambar 9.
B. PROSEDUR PENELITIAN
1. Tahap Pertama : Penentuan suhu pengeringan dan suhu ekstraksi a. Pengeringan daun stevia
Daun stevia basah dikeringkan dengan menggunakan oven kipas pada suhu 60oC, 80oC, 100oC. Pada setiap setengah jam sekali bahan diambil, kemudian dianalisa kandungan air (kadar air), pengeringan dihentikan jika kadar air bahan telah mencapai maksimum 10% (pengeringan berlangsung selama ± 2 - 4 jam). Daun yang telah kering dihaluskan dengan menggunakan blender kering, kemudian disaring dengan saringan 65 mesh. Daun yang telah halus dikemas di dalam plastik dan disimpan di dalam lemari pendingin suhu 4oC.
b. Proses ekstraksi daun stevia pada berbagai suhu pemanasan
Daun stevia diekstraksi dengan pelarut air (pH 7). Untuk pemilihan suhu ekstraksi, masing-masing daun bubuk yang telah dikeringkan pada suhu 60oC, 80oC, 100oC ditimbang sebanyak 1 gram dalam 20 ml air. Proses ekstraksi dilakukan dengan metode Food Sanitation Association Food Research Laboratory (Zairisman, 1985). Larutan stevia dipanaskan pada suhu yang bervariasi yaitu 250C, 400C, 600C, 1000C. Pemanasan dilakukan selama 1 jam kecuali pada suhu 250C dibiarkan selama semalam. Kemudian disaring dengan kertas saring. Filtrat dipisahkan dan residu dicuci dengan air panas beberapa kali. Filtrat dan air cucian dikumpulkan, kemudian ditambahkan air sehingga volume menjadi tepat 100 ml. Hasil ekstraksi daun stevia diukur konsentrasi steviosida dan kadar gula total. Diagram alir dapat dilihat pada Lampiran 3.
Penjernihan ekstrak daun stevia dilakukan dengan membran ultrafiltrasi. Pada ultrafiltrasi diamati nilai fluksi permeat dan rejeksi dengan parameter tekanan transmembran, kecepatan alir (kecepatan
crossflow) dan konsentrasi umpan (konsentrasi steviosida dalam larutan stevia).
Tata cara proses ultrafiltrasi adalah sebagai berikut: a) Penentuan fluksi air
Penentuan fluksi air bertujuan untuk mengetahui kondisi membran baik sebelum digunakan maupun setelah digunakan. Air disirkulasikan selama 30 menit pada suhu 40oC dengan tekanan transmembran 1.87 bar dan kecepatan alir 0.04 m/s.
b) Penentuan kondisi tunak fluksi larutan stevia
Percobaan dilakukan dengan mengoperasikan proses ultrafiltrasi selama 30 menit hingga keadaan tunak dicapai. Waktu ketika fluksi mulai mengalami kondisi tunak, maka dapat digunakan untuk mengetahui pengaruh ketiga peubah yang akan diamati. Proses dilakukan pada suhu 40oC pada tekanan transmembran 1.23 bar, kecepatan alir 0.02 m/s dan konsentrasi larutan umpan stevia 28.7 g/L. c) Pengamatan pengaruh tekanan transmembran terhadap fluksi larutan
stevia
Proses penjernihan larutan stevia dilakukan pada berbagai tekanan transmembran yaitu 1.49 bar, 1.61 bar, 1.65 bar, 1.87 bar dengan kecepatan alir 0.02 m/s, pada konsentrasi larutan umpan stevia 20.4 g/L dan 28.7 g/L.
d) Pengamatan pengaruh kecepatan alir terhadap fluksi larutan stevia Proses penjernihan dilakukan dengan proses ultrafiltrasi pada berbagai kecepatan alir yaitu antara 0.0029 sampai 0.02 m/s.
e) Pengamatan pengaruh konsentrasi umpan terhadap fluksi
Percobaan dilakukan dengan mengoperasikan proses ultrafiltrasi pada berbagai konsentrasi larutan umpan stevia yaitu 20.4 g/L, 28.7 g/L dengan kecepatan alir 0.02 m/s dan tekanan 1.61 bar.
4. Tahap Ketiga : Analisa Hasil Filtrasi Dengan Ultrafiltrasi
Analisa untuk mengetahui sebelum dan sesudah ultrafiltrasi pada ekstrak daun stevia adalah analisa pH, konsentrasi steviosida, kadar gula total, persen kejernihan (%T), kadar abu dan analisa HPLC. Prosedur analisa dapat dilihat pada Lampiran 6
IV. HASIL DAN PEMBAHASAN
A. Penentuan suhu pengeringan dan suhu ekstraksi daun stevia
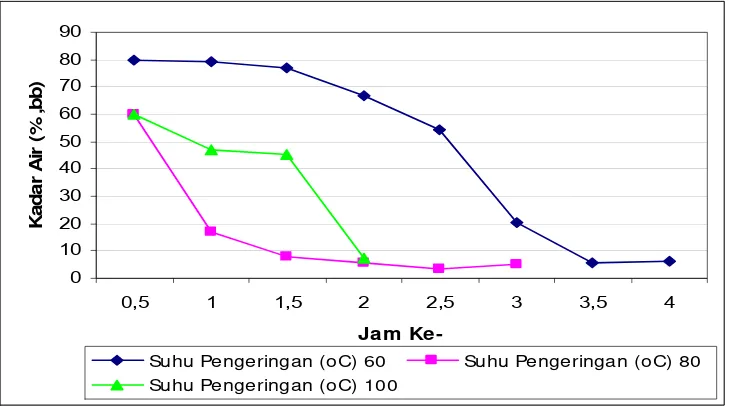
Daun stevia sebelum diekstraksi terlebih dahulu dikeringkan menggunakan oven dengan kipas. Pengeringan daun stevia berkaitan dengan kandungan air dalam daun (kadar air). Sebelum dilakukan proses ekstraksi, bahan baku disimpan dan kandungan air dalam daun diatur, sehingga mikroorganisme, jamur serta enzim tidak berkembang. Hubungan kadar air dengan suhu pengeringan ditunjukkan pada Gambar 10.
0
Suhu Pengeringan (oC) 60 Suhu Pengeringan (oC) 80
Suhu Pengeringan (oC) 100
Gambar 10. Kadar air daun selama pengeringan
Pada gambar terlihat bahwa proses pengeringan daun berlangsung dengan cepat seiring meningkatnya suhu pengeringan. Hal ini disebabkan karena dengan meningkatnya suhu maka penguapan air dalam bahan akan lebih cepat. Kadar air pada daun diharapkan maksimum 10 persen. Adapun tujuan pengeringan adalah untuk memperpanjang daya simpan dan menghindari kerusakan akibat aktifitas serangga, jamur, dan enzim.
pereduksi dengan asam amino. Kemungkinan lain adalah terbentuknya senyawa pheophytin akibat reaksi antara klorofil dengan semua asam yang menguap pada waktu proses pengeringan. Untuk mendapatkan daun yang masih berwarna hijau dan kadar steviosida tidak berubah. maka pengeringan dilakukan pada suhu 60oC.
Ekstraksi daun stevia dilakukan dengan menggunakan pelarut polar yaitu air karena senyawa glikosida bersifat polar sehingga dapat larut dalam air. Daun stevia pada pengeringan 60oC, 80oC, dan 100oC yang telah dicampur dengan pelarut air dipanaskan pada suhu 25oC, 40oC, 60oC dan 100oC untuk mendapatkan suhu ekstraksi yang akan digunakan pada proses selanjutnya.
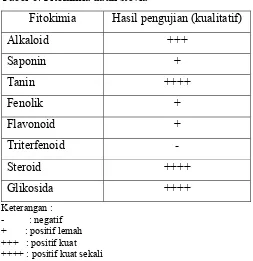
terkandung di dalam daun stevia dapat dilihat pada Tabel 6. Data lengkap fitokimia dapat dilihat pada Lampiran 7.
Tabel 6. Fitokimia daun stevia
Fitokimia Hasil pengujian (kualitatif)
Alkaloid +++
Pemilihan kondisi suhu ekstraksi daun stevia pada berbagai suhu pengeringan berdasarkan pengukuran konsentrasi steviosida dan kadar gula total. Data hasil pengukuran konsentrasi steviosida dan kadar gula total dapat dilihat pada Lampiran 8.
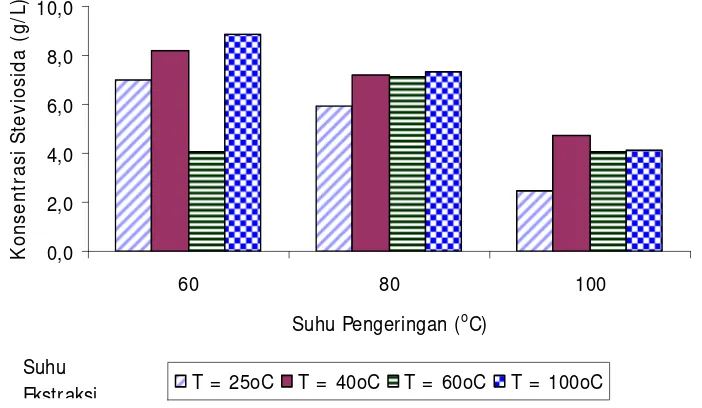
1. Konsentrasi Steviosida
0,0
Suhu Pengeringan (oC)
K
Gambar 12. Konsentrasi steviosida larutan stevia pada berbagai suhu pengeringan dan suhu ekstraksi
Secara umum semakin tinggi suhu ekstraksi maka konsentrasi steviosida yang diperoleh tinggi. Air memiliki titik didih 100oC sehingga pada suhu ini air menjadi lebih efektif dalam melarutkan senyawa-senyawa pemanis stevia. Hal ini sesuai dengan hasil penelitian Marsono (1984) yaitu semakin tinggi suhu ekstraksi (100oC) maka perolehan zat padat terlarut semakin besar dan rasa larutan semakin manis. Larutan stevia yang dihasilkan berwarna kecoklatan dan rasanya manis dengan sedikit rasa sepat.
2. Kadar Gula Total
0,00
Suhu Pengeringan Daun (oC)
K
T ekstraksi 25oC T ekstraksi 40oC T ekstraksi 60oC T ekstraksi 100oC
Gambar 13. Kadar gula total larutan stevia pada berbagai kondisi suhu pengeringan dan ekstraksi
Berdasarkan Gambar 13. kadar gula total yang dihasilkan berkisar 1.43 – 2.48 g/L. Kadar gula yang terukur merupakan molekul gula (glukosa), dimana senyawa glikosida mengandung molekul glukosa yang berikatan dengan aglikon. Steviosida dapat terhidrolisa menjadi steviol dan glukosa dan hal tersebut dapat disebabkan oleh fermentasi oleh mikroorganisme. Kemanisan larutan stevia tidak ditentukan oleh kandungan gula, tetapi lebih ditentukan oleh senyawa–senyawa pemanis yang ada di dalamnya (Steviosida). Penelitian Marsono menunjukkan kadar gula total sebesar 3.6 10-3 % memiliki tingkat kemanisan setara 20 – 25 % gula.
Suhu pengeringan dan suhu ekstraksi yang digunakan untuk penelitian selanjutnya adalah suhu 60oC dan suhu 100oC. Air memiliki titik didih 100oC, sehingga air dapat mengekstrak lebih baik.
B. Penjernihan Ekstrak Daun Stevia dengan Ultrafiltrasi
Pada tahap ini diamati (1) pengaruh tekanan transmembran terhadap fluksi; (2) pengaruh laju alir tehadap fluksi; (3) konsentrasi larutan umpan stevia terhadap fluksi; (4) rejeksi membran dan kenaikan konsentrasi.
1. Fluksi Air
Pengamatan fluksi air dilakukan dengan mensirkulasikan air destilata pada suhu 40oC selama 30 menit. Proses sirkulasi air destilata dilakukan sebelum dan setelah membran digunakan. Tekanan yang digunakan adalah 1.87 bar dan dengan kecepatan alir 0.04 m/s.
Hasil pengukuran fluksi air menunjukkan nilai fluksi belum konstan pada awal filtrasi. Setelah menit ke-10 nilai fluksi mulai konstan, yaitu pada kisaran fluksi 225 L/m2.jam. Grafik hubungan waktu filtrasi dengan fluksi dapat dilihat pada Gambar 14. Data lengkap fluksi air dapat dilihat pada Lampiran 9.
Gambar 14. Hubungan antara lama filtrasi dengan fluksi pada air destilata pada tekanan 1.87 bar, kecepatan alir 0.04 m/s
pada Gambar 15. Data yang berhubungan dengan waktu filtrasi terhadap fluksi dapat dilihat pada Lampiran 10.
0,00
0,00 5,00 10,00 15,00 20,00 25,00 30,00 35,00
Lama Filtrasi (menit)
Gambar 15. Grafik hubungan antara lama filtrasi larutan stevia dengan fluksi pada kecepatan 0.02 m/s dan tekanan 1.49 bar
Kondisi tunak larutan stevia tercapai setelah menit ke-10 dengan nilai fluksi berkisar antara 36.00 – 37.89 L/m2.jam. Fluksi mulai menurun pada saat awal operasi dikarenakan telah terjadi pembentukan lapisan cake pada permukaan membran yang disebut polarisasi konsentrasi. Pada saat lapisan
cake telah terbentuk secara konstan maka nilai fluksi relatif konstan terhadap waktu.
3. Pengaruh Tekanan Transmembran Terhadap Fluksi
0,00
Gambar 16. Grafik hubungan antara tekanan transmembran terhadap fluksi pada beberapa konsentrasi dan kecepatan alir 0.02 m/s
Grafik ini menunjukkan bahwa semakin tinggi tekanan, nilai fluksi yang dihasilkan semakin tinggi. Nilai fluksi tertinggi diperoleh pada konsentrasi steviosida pada larutan umpan 20.4 g/L dengan tekanan 1.87 bar sebesar 60.00 L/m2.jam. Operasi filtrasi larutan stevia dengan membran ultrafiltrasi yang dilakukan pada tekanan tinggi, pada titik tertentu nilai fluksi tidak dipengaruhi oleh tekanan transmembran walaupun tekanan ditingkatkan. Pada tekanan 1.61 bar telah menunjukkan kecenderungan konstan. Peningkatan nilai fluksi yang seiring dengan peningkatan tekanan, dikarenakan tekanan yang semakin tinggi akan meningkatkan gaya dorong larutan menuju membran.
stevia. Hal ini disebabkan karena air tidak mengalami polarisasi konsentrasi sehingga tidak ada hambatan air untuk melewati membran. Data fluksi air dengan berbagai tekanan dapat dilihat pada Lampiran 11a.
1.23 bar
Gambar 17. Hubungan tekanan transmembran dengan fluksi air dengan kecepatan alir 0.04 m/s
Fenomena yang terjadi pada larutan stevia, ketika tekanan dinaikkan akan menaikkan fluksi tetapi setelah mencapai tekanan batas tertentu maka fluksi tidak meningkat walaupun tekanan dinaikkan.
4. Pengaruh Kecepatan alir Terhadap Fluksi
0,00
0 0,005 0,01 0,015 0,02 0,025
Kecepatan alir (m/s)
Gambar 18. Grafik hubungan antara kecepatan alir dengan nilai fluksi pada berbagai konsentrasi dan tekanan transmembran 1.61 bar
Dari Gambar diatas diamati bahwa peningkatan nilai fluksi permeat pada konsentrasi umpan 20.4 g/L berkisar 51.43 – 55.38 L/m2.jam. Semakin besar kecepatan alir yang diberikan maka nilai fluksi semakin besar. Namun pada kecepatan alir 0.011 m/s dan 0.02 m/s fluksi menunjukkan kecenderungan yang konstan. Hal itu disebabkan semakin banyak partikel–partikel besar dipermukaan membran yang dapat digeser sedangkan partikel–partikel yang memiliki ukuran lebih kecil atau mendekati ukuran pori membran akan lebih cepat menimbulkan penyumbatan daripada partikel yang lebih besar. Hal tersebut yang dapat menyebabkan terjadinya fouling dan penurunan fluksi. Namun semakin tinggi konsentrasi umpan akan menyebabkan kecepatan alir larutan berkurang dan fluksi menurun, karena viskositas larutan umpan yang tinggi dan pergerakan partikel keluar dari membran akan menurun.
5. Pengaruh Konsentasi Larutan Umpan Stevia Terhadap Fluksi
Konsentrasi larutan umpan stevia adalah 20.4 g/L dan 28.7 g/L. Grafik hubungan antara konsentrasi larutan stevia dengan fluksi dapat dilihat pada Gambar 19.
Konsentrasi steviosida larutan stevia (g/L)
Flu
Gambar 19. Grafik hubungan antara konsentrasi larutan umpan stevia dengan nilai fluksi pada tekanan transmembran 1.61 bar berbagai kecepatan alir.
6. Tingkat rejeksi membran dan kenaikan konsentrasi larutan stevia Proses penjernihan ekstrak daun stevia dengan membran ultrafiltrasi diharapkan seluruh solut yang mengandung pemanis stevia dapat lolos melewati membran sehingga rejeksi yang diperoleh 0% karena Molecular Weight CutOff (MWCO) membran yang digunakan untuk menjernihkan ekstrak daun stevia ini adalah 20000 Dalton, sedangkan bobot molekul senyawa pemanis stevia berkisar 318.44 – 804.90. Tingkat rejeksi membran terhadap larutan stevia diperlihatkan pada Tabel 7.
Tabel 7. Tingkat rejeksi membran pada berbagai tekanan transmembran dengan kecepatan alir 0.02 m/s
Tekanan
Kenaikan konsentrasi dari larutan umpan dapat diketahui dengan mengetahui konsentrasi retentat dan dapat dihitung dengan rumus:
Kenaikan konsentrasi = x 100 %
Tabel 8. Kenaikan konsentrasi larutan stevia setelah penjernihan pada berbagai tekanan transmembran (kecepatan alir 0.02 m/s)
P (bar) Cf 1.49 0.0204 0.0079 0.0214 100 7.143 92.857 4.7 1.61 0.0204 0.0099 0.0213 100 7.692 92.308 4.3 1.87 0.0204 0.0129 0.0217 100 10.000 90.000 6.3
1.49 0.0287 0.0088 0.0301 100 6.667 93.333 5.0 1.65 0.0287 0.0095 0.0302 100 7.143 92.857 5.1
Berdasarkan Tabel 8. kenaikan konsentrasi steviosida pada larutan retentat adalah sekitar 4.3 – 6.6 persen. Semakin tinggi konsentrasi umpan, semakin banyak pula partikel terlarut yang dapat menghalangi laju difusi larutan ke membran sehingga produk yang diinginkan sulit lolos melewati membran.
C. Karakteristik Larutan Stevia
Uji karakteristik yang dilakukan pada ekstrak daun stevia sebelum dan sesudah filtrasi terhadap tiap tekanan dan kecepatan alir adalah pH, konsentrasi steviosida, kadar gula total, kejernihan dan kadar abu. Data lengkap hasil analisa larutan stevia pada berbagai tekanan dapat dilihat pada Lampiran 12.
a). pH
pH merupakan salah satu pengukuran asam atau basa suatu larutan. Larutan stevia memiliki pH diatas 5.00. Pemanis stevia tidak akan berubah jika dipanaskan pada suhu 100oC selama 1 jam dan stabil pada pH 3 – pH
9 (Anonim. 2004). pH sebelum dan sesudah filtrasi larutan stevia dapat dilihat pada Gambar 20.
5,20
Konsent rasi st eviosida sebelum masuk membran ( KSSM)
p
H
Umpan Tekanan 1,49 bar Tekanan 1,61 bar
Tekanan 1,65 bar Tekanan 1,87 bar
Gambar 20. Perubahan pH pada berbagai konsentrasi umpan steviosida dan tekanan (CFV=0.02 m/s).
5,35
Konsent rasi st eviosida sebelum masuk membran ( KSSM)
p
H
Umpan CFV 0,0029 m/ s CFV 0,011 m/ s CFV 0,016 m/ s
tentang kajian pemurnian nira tebu dengan membran filtrasi dengan sistem aliran silang menghasilkan pH nira sebesar 5.41 dan terjadi penurunan pH setelah proses filtrasi dengan membran.
b). Konsentrasi steviosida
Pemanis stevia yang paling utama pada tanaman Stevia rebaudiana
adalah steviosida. Steviosida jumlahnya lebih banyak dibandingkan dengan pemanis lainnya yang terkandung di dalam tanaman stevia. Kandungan steviosida di dalam daun stevia adalah 5 – 15% dan rebaudiosida A adalah 3 – 6%, sedangkan untuk glikosida yang lain jumlahnya sangat sedikit (Tanaka, 1979). Setelah pemisahan dengan membran pada berbagai tekanan dan kecepatan alir, terjadi penurunan konsentrasi steviosida pada permeat seperti yang ditunjukkan pada Gambar 22 dan Gambar 23.
0, 0
Konsent rasi st eviosida sebelum masuk membran (KSSM)
K
Tekanan 1, 49 bar Tekanan 1, 61 bar Tekanan 1, 65 bar Tekanan 1, 87 bar
0, 0
Konsent rasi st eviosida sebelum masuk membran (KSSM)
K
Gambar 23. Perubahan konsentrasi steviosida pada konsentrasi umpan steviosida dan kecepatan alir (ΔP=1.61 bar).
Pada Gambar 22, tekanan yang tinggi akan menghasilkan konsentrasi steviosida sesudah keluar membran berkisar antara 7.9 g/L – 12.9 g/L sedangkan pada berbagai kecepatan alir konsentrasi steviosida berkisar 6.9 g/L – 10.0 g/L yang dapat dilihat pada Gambar 23. Konsentrasi steviosida setelah difiltrasi dengan membran mengalami penurunan pada konsentrasi 20.4 g/L sebesar 36.76% - 61.27%, sedangkan konsentrasi 28.7 penurunannya sebesar 65.51% – 73.17%. Konsentrasi steviosida mengalami penurunan dikarenakan telah terjadinya fermentasi selama proses filtrasi sehingga steviosida terhidrolisa menjadi steviol dan glukosa, disamping itu juga larutan memiliki sifat sedikit asam sehingga ada kemungkinan terjadi penguraian senyawa di dalam larutan tersebut.
c). Kadar gula total
0, 000
Konsentrasi st eviosida sebelum masuk membran (KSSM)
K
Umpan Tekanan 1,49 bar Tekanan 1,61 bar Tekanan 1,65 bar Tekanan 1,87 bar
Gambar 24. Perubahan kadar gula total pada berbagai konsentrasi umpan steviosida dan tekanan (CFV=0.02 m/s).
0,000
Konsentrasi steviosida sebelum masuk membran (KSSM)
K
Umpan CFV 0,0029 m/s CFV 0,011 m/s CFV 0,02 m/s
Gambar 25. Perubahan kadar gula total pada berbagai konsentrasi umpan steviosida dan kecepatan alir (ΔP=1.61 bar).
Pada kecepatan alir yang bervariasi menunjukkan kadar gula total yang fluktuatif sehingga tidak diketahui kecenderungannya. Namun kadar gula total yang menurun menunjukkan bahwa gula selain gula stevia ada yang tertahan dipermukaan membran. Kadar gula total setelah keluar dari membran pada berbagai kecepatan alir dapat dilihat pada Gambar 25.
d). Persen kejernihan (%T)
Menurut Moerdokusumo (1993), kejernihan merupakan perbandingan antara cahaya yang dipantulkan oleh suatu lapisan gula dan cahaya standar yang sama dipantulkan oleh lapisan magnesia. Kejernihan larutan diukur dengan menggunakan spektrofotometer pada panjang gelombang 490 nm dengan pengenceran 10 kali.
sesudah filtrasi pada berbagai tekanan dan berbagai kecepatan alir dapat dilihat pada Gambar 26 dan Gambar 27.
0 Konsent rasi st eviosida sebelum masuk membran (KSSM)
K
Umpan Tekanan 1, 49 bar Tekanan 1, 61 bar Tekanan 1, 65 bar Tekanan 1, 87 bar
Gambar 26. Perbandingan nilai persen kejernihan sebelum (umpan) dan setelah (permeat) filtrasi oleh membran pada berbagai tekanan (CFV=0.02 m/s).
Konsent rasi st eviosida sebelum masuk membran (KSSM)
K
Gambar 27. Perbandingan nilai persen kejernihan sebelum (umpan) dan setelah (permeat) filtrasi oleh membran pada berbagai kecepatan alir (ΔP=1.61 bar).
kejernihan terdapat pada kecepatan alir rendah (0.0029 m/s) sebesar 60%. Larutan ekstrak daun stevia sebelum difiltrasi masih memiliki warna yang keruh (coklat) dan mengandung pengotor-pengotor. Pengotor yang terkandung di dalam ekstrak daun stevia berupa klorofil, partikel-partikel besar yang menghasilkan pigmen, tanin dan senyawa inorganik. Hasil penjernihan ekstrak daun stevia dapat dilihat pada Gambar 27. Data lengkap persen kejernihan dapat dilihat pada Lampiran 12.
Gambar 28. Hasil penjernihan ekstrak daun stevia (a) umpan. permeat pada (b) tekanan 1.49 bar. (c) tekanan 1.65 bar. (d) tekanan 1.87 bar.
e). Kadar Abu
Larutan ekstrak daun stevia sebelum difiltrasi memiliki kadar abu yang tinggi yaitu sebesar (0.073%). Namun setelah difiltrasi dengan membran, larutan ekstrak daun stevia menghasilkan kadar abu yang lebih rendah. Nilai kadar abu sebelum dan sesudah filtrasi pada
(a) (b)
0,000
Konsentrasi steviosida sebelum masuk membran (KSSM)
K
Umpan Tekanan 1,49 bar Tekanan 1,61 bar Tekanan 1,65 bar Tekanan 1,87 bar
0, 000
Konsent rasi st eviosida sebelum masuk membran (KSSM)
K
Gambar 30. Nilai Nilai kadar abu sebelum dan sesudah filtrasi pada konsentrasi larutan stevia dan kecepatan alir (ΔP=1.61 bar).
f. Analisa larutan stevia dengan High Performance Liquid Chromatography (HPLC)
Larutan stevia yang diekstraksi dengan air destilata sebelum dijernihkan dengan menggunakan membran dianalisa dengan HPLC untuk membuktikan ada tidaknya kandungan steviosida di dalam ekstrak daun stevia menggunakan pelarut air. Larutan ekstrak daun stevia terbukti mengandung senyawa glikosida yang utama yaitu steviosida dan rebaudiosida A. Pada standar steviosida waktu retensinya 3.14 dan standar rebaudiosida A waktu retensinya 5.26. Larutan stevia sebelum jernihkan diketahui adanya steviosida dimana menghasilkan waktu retensi 3.10 (pada puncak kromatogram no. 4) dan 5.20 pada rebaudiosida A (puncak kromatogram no. 8). dapat dilihat pada Lampiran 13.
stevia. Keberhasilan dalam penjernihan ekstrak daun stevia belum dapat dikatakan berhasil karena standar yang digunakan hanya pemanis stevia yaitu steviosida dan rebaudiosida A, sehingga pengotor yang terkandung di dalam hasil ekstrak daun tidak dapat diketahui.
D. PEMBAHASAN UMUM
Membran ultrafiltrasi aliran silang (MWCO 20000 Dalton) mampu menjernihkan larutan stevia dari pengotornya. Pengotor–pengotor yang terkandung di dalam larutan stevia berupa klorofil, tanin, partikel-partikel besar (protein dan koloid) yang menghasilkan pigmen dan senyawa inorganik. Namun proses penjernihan dengan ultrafiltrasi masih memberikan tingkat rejeksi yang tinggi sehingga konsentrasi steviosida yang diperoleh masih rendah. Hal itu dikarenakan larutan masih banyak mengandung partikel– partikel besar yang dapat mempercepat terakumulasinya partikel di atas permukaan membran sehingga pemanis stevia ikut tertahan.
Larutan stevia yang telah difiltrasi diukur kadar abu dan persen kejernihannya (%T) serta melihat nilai fluksi dan tingkat rejeksi pada berbagai kondisi membran untuk melihat tingkat keberhasilan membran dalam menjernihkan ekstrak daun stevia. Larutan stevia yang jernih diindikasikan dengan persen kejernihan yang tinggi dan kadar abu yang rendah. Kondisi yang demikian dapat diperoleh pada tekanan transmembran yang tinggi (1.87 bar dengan kecepatan alir 0.02 m/s) dan kecepatan alir yang rendah (0.0029 m/s dengan tekanan transmembran 1.61 bar). Pada tekanan yang tinggi (1.87 bar) diperoleh peningkatan kejernihan larutan stevia setelah difiltrasi sebesar 64 % dengan penurunan kadar abu sebesar 62%. Kecepatan alir yang rendah (0.0029 m/s) diperoleh peningkatan kejernihan larutan stevia sebesar 60% dengan penurunan kadar abu sebesar 59%. Fluksi tertinggi didapatkan pada tekanan transmembran 1.87 bar dengan kecepatan alir 0.02 m/s dan konsentrasi 20.4 g/L. Hasil analisa dengan HPLC (High Performance Liquid Chromatography) membuktikan bahwa larutan ekstrak daun stevia mengandung pemanis stevia yaitu steviosida sedangkan kandungan lainnya tidak dapat diketahui karena standar yang digunakan hanya pemanis stevia.
V. KESIMPULAN DAN SARAN
A. KESIMPULAN
Peningkatan kejernihan larutan ekstrak daun stevia dapat dilakukan dengan menggunakan membran ultrafiltrasi aliran silang pada kondisi tekanan transmembran yang tinggi dan kecepatan alir yang rendah. Peningkatan kejernihan tertinggi diperoleh sebesar 64% pada kondisi tekanan transmembran yang tinggi (1.87 bar dengan kecepatan alir 0.02 m/s) dan kecepatan alir umpan yang rendah (0.0029 m/s dengan tekanan transmembran 1.61 bar) diperoleh peningkatan kejernihan larutan ekstrak daun stevia sebesar 60%.
Penggunaan kondisi tekanan 1.87 bar dengan kecepatan alir 0.02 m/s selain dapat meningkatkan kejernihan, juga menghasilkan nilai rejeksi yang rendah (36.7%) dan fluksi yang tertinggi (60.00 L/m2.jam).
B. SARAN