MULTI
DRUG
RESISTANCE
TUBERCULOSIS
(MDR
TB)
DISUSUN
OLEH
RINA
YUNITA
NIP.
19790624
200312
2
003
DEPARTEMEN
MIKROBIOLOGI
FAKULTAS
KEDOKTERAN
UNIVERSITAS
SUMATERA
UTARA
DAFTAR
ISI
bstrak
A
.
Pendahuluan
)
).
)
Definisi
)).
)
Patogenesa MDR‐TB
)V.
Mekanisme Molekuler Resistensi Obat Antituberkulosis OAT
. )soniazid
. Rifampisin
. Pirazinamid
. Ethambutol
V.
Metode Deteksi Resistensi Obat Antituberkulosis
. Metode Fenotiping
. . Metode Konvensional
Metode Proporsi
Metode Konsentrasi Absolut
esiste si
Metode Rasio R
n
. . Metode Modern
Metode Radiometri BACTEC
Metode Mycobacterial Growth )ndicator Tube MG)T
. Metode Genotiping
).
Terapi MDR‐TB
V
V)). Kesimpulan
))). Daftar Pustaka
V
aftar
D
Tabel
Tabel . Obat antituberkulosis dan berbagai gen yang terlibat
Dalam mekanisme resistensi
po si ug/ml
Tabel . Konsentrasi kritis antibiotik pada metode pro r
tama
Tabel . Dosis yan dianjurkan untuk OAT lini per
abel
T
. Dosis harian dan tingkat toksisitas dari
obat antituberkulosis lini kedua
Anjuran pengobatan pasien dengan MDR‐TB
Tabel .
Daftar Gambar
amba
G
r .
M.
tuberculosis
dalam pewarnaan tahan asam
kiri dan melalui mikroskop elektron kanan . CDC
amba
h
G
r . Resistensi didapat terjadi karena seleksi alamia
tuhan
akibat pengobatan inefektif dan ketidakpa
s
Gambar . Medium Lowenstein‐Jensen serta koloni
M.tuberculosi
Gambar . Tabung MG)T menunjukkan reaksi positif dan negatif
MULTI
DRUG
RESISTANCE
TUBERCULOSIS
(MDR
TB)
Rina
Yunita
Departemen
Mikrobiologi
Fakultas
Kedokteran
USU
Abstrak
Multiple Drug Resistance Tuberculosis MDR‐TB adalah suatu keadan dimana M.
tuberculosis telah resisten terhadap )N( dan rifampisin saja atau resisten terhadap )N( dan
rifampisin serta OAT lini pertama lainnya. Tuberkulosis TB adalah suatu penyakit infeksi yang
menular, disebabkan oleh kuman Mycobacterium tuberculosis. Sumber penularan adalah dahak
yang mengandung kuman TB. Estimasi global terhadap insidensi MDR‐TB pada tahun
adalah sebesar . atau sekitar , % dari jumlah total estimasi insidens tuberkulosis TB
di negara pada tahun . . . Resistensi obat pada kasus TB adalah masalah
yang mendapat perhatian besar dalam program penanggulangan TB oleh karena beberapa strain MDR‐TB yang sulit diobati. Prevalensi resistensi OAT diantara pasien baru merupakan
indikator yang sangat penting dalam program p engendali n TB.a
Kejadian resistensi M. tubercolosis terhadap OAT adalah akibat mutasi alami.
Penyebaran selanjutnya disebabkan oleh kesalahan pengelolaan penyakit seperti : Kesalahan pengelolaan OAT, kesalahan manajemen kasus TB, kesalahan proses penyampaian OAT kepada pasien, kesalahan hasil uji sensitifitas obat, pemakaian OAT dengan mutu rendah serta kurangnya keteraturan pengobatan atau pengobatan yang tidak selesai. Resistensi terhadap
OAT lini pertama berhubungan dengan adanya mutasi sedikitnya pada gen, yaitu katG, inhA,
ahpC, kasA and ndh untuk resistensi terhadap )N(; rpoB untuk resistensi terhadap R)F, embB
untuk resistensi terhadap EMB; pncA untuk resistensi terhadap PZA serta rpsL dan rrs untuk
resistensi terhadap streptomisin
Metode untuk mendeteksi resistensi OAT diantaranya dengan metode fenotiping yang
dapat dilakukan denagn metode proporsi, konsentrasi absolut, rasio resistensi dan dengan cara otomatis menggunakan Bactec serta MG)T. Selain itu dapat juga dilakukan genotiping untuk
elihat keberadaan gen resistensi. m
Kata Kunci : MDRTB, Tuberkulosis, obat antituberkulosis lini kedua, gen resistensi OAT
I.
PENDAHULUAN
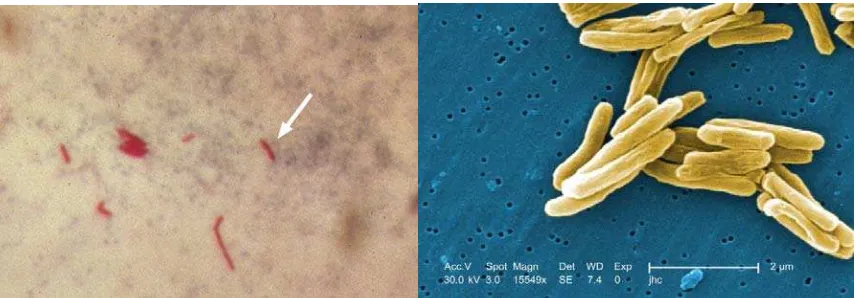
Tuberkulosis TB adalah suatu penyakit infeksi yang menular, disebabkan oleh kuman
Mycobacterium tuberculosis gambar . Sumber penularan adalah dahak yang mengandung
kuman TB. Gejala umum TB paru pada orang dewasa adalah batuk yang terus‐menerus dan berdahak, selama tiga minggu atau lebih. Bila tidak diobati penyakit dapat berkembang
menjadi fatal.
Estimasi global terhadap insidensi MDR‐TB pada tahun adalah sebesar .
atau sekitar , % dari jumlah total estimasi insidens tuberkulosis TB di negara pada
tahun . . . Dua negara penyumbang kasus terbesar adalah China dan )ndia, yang
diperkirakan menyumbang sekitar % dari seluruh kasus MDR‐TB dan diikuti oleh Rusia
sekitar %.
Gambar . M. tuberculosis dalam pewarnaan tahan asam kiri dan melalui mikroskop elektron kanan .
CDC
Resistensi obat pada kasus TB adalah masalah yang mendapat perhatian besar dalam program penanggulangan TB oleh karena beberapa strain MDR‐TB yang sulit diobati. Strain ini mendapat perhatian oleh karena dapat menyebar di seluruh dunia, menekankan perlunya peningkatan program kontrol, seperti metode diagnostik baru, obat‐obatan yang lebih efektif
dan penemuan vaksin yang lebih efektif. Pasien dengan MDR-TB membutuhkan pengobatan lebih
lama dengan obat yang sebenarnya kurang efektif namun lebih toksik. Oleh karena itu sangat penting untuk membedakan diagnosis MDR-TB dengan resistensi lain dengan melakukan kultur mikobakterial dan u i sensitifitas karena implikasi terapi ang berbeda.j y 4
kembali merupakan kelompok heterogen yang terdiri dari pasien kronik yang merupakan kasus gagal pengobatan, kasus relaps, dan pasien yang kembali setelah putus berobat. Dalam beberapa kasus, dari populasi ini lebih dari % menunjukkan hasil smear positif. Kasus kronik dan pengobatan yang gagal memiliki resiko yang lebih besar mendapatkan resistensi dan MDR‐
TB.
Terdapat bukti yang menunjukkan hubungan antara TB dan ()V. Namun meskipun kejadian kasus TB resisten OAT diantara pasien ()V positif secara nosokomial sudah secara luas diketahui, masih sedikit informasi yang didapat tentang hubungan ()V dan resistensi OAT dalam tingkat populasi. Ada dua alasan utama kenapa TB resisten OAT dapat dikaitkan dengan ()V. Pertama adalah terdapatnya resistensi rifampisin diantara pasien TB dengan ()V dan dalam pengobatan TB, meskipun hal ini berkaitan dengan pengobatan yang terputus‐putus. Malabsorbsi OAT juga telah berhasil dibuktikan dalam penelitian kohort pada kelompok dengan prevalensi ()V yang tinggi, yang menunjukkan pasien TB dengan ()V kemungkinan memiliki risiko yang lebih tinggi untuk mendapatkan resistensi. Alasan kedua berhubungan dengan paparan, faktor risikonya adalah riwayat dirawat di rumah sakit yang berarti pasien TB dengan
()V memiliki risiko yang tinggi terpapar kuman yang resisten.
II.
DEFENISI
Multiple Drug Resistance Tuberculosis MDR‐TB adalah suatu keadan dimana M.
tuberculosis telah resisten terhadap )N( dan rifampisin saja atau resisten terhadap )N( dan
rifampisin serta OAT lini pertama lainnya. ,
Drug Resistance TB dikonfirmasi melalui uji laboratorium yang menunjukkan bahwa isolat
Mycobacterium tuberculosis dapat tumbuh secara invitro meskipun dengan adanya satu atau
lebih obat antituberkulosis OAT . Empat kategori resistensi OAT dapat dibedakan atas , :
Monoresistance : resistensi terhadap salah satu dari OAT
Poly‐resistance : resistensi terhadap lebih dari satu OAT, selain isoniazid )N( dan
a a rifampisin secara bers m an
Multidrug‐resistance : resisten terhadap sekurang‐kurangnya )N( beserta
rifampisin
Extensive drug‐resistance : Multidrug‐resistance ditambah resistensi terhadap salah
satu golongan fluoroquinolon, dan sedikitnya satu dari tiga jenis obat lini kedua injeksi kapreomisin, kanamisin dan amikasin
Berdasarkan kategori diagnostik TB oleh W(O yang berimplikasi pada perbedaan regimen pengobatan yang direkomendasikan, kasus MDR‐TB tergolong dalam kategori )V. Kategori diagnostik )V mencakup :
o MDR‐TB yang sudah terkonfirmasi
o Dugaan MDR‐TB. Kelompok ini memerlukan wewenang medis yang relevan yang
merekomendasikan bahwa pasien perlu mendapatkan pengobatan Kategori )V. Pasien dapat dicatat dan memulai pengobatan kategori )V sebelum adanya
konfirmasi MDR‐TB hanya jika adanya survey resistensi obat yang representatif
atau data epidemiologik lain yang mengindikasikan kemungkinan besar kasus tersebut MDR‐TB
o Polyresistant TB. Beberapa kasus poly‐resistant TB membutuhkan pengobatan
kategori )V. Pasien‐pasien ini membutuhkan pengobatan dengan OAT lini pertama
yang lebih lama bulan atau lebih diombinasikan dengan dua atau lebih obat lini
kedua dan dicatat sebagai kelompok kategori )V.
III.
PATOGENESA
MDR
TB
Kejadian resistensi M. Tubercolosis terhadap OAT adalah akibat mutasi alami. Amplifikasi
M. tuberculosis yang resisten selanjutnya terjadi akibat kesalahan manusia seperti :
Kesalahan pengelolaan OAT
Kesalahan manajemen kasus TB
Kesalahan proses penyampaian OAT kepada pasien
Kesalahan hasil uji DST
Pemakaian OAT dengan mutu rendah
Kurangnya keteraturan pengobatan atau pengobatan yang tidak selesai
TB yang rentan OAT dan TB yang resisten menular dengan cara yang sama yaitu melalui droplet saluran nafas yang menyebar di udara. Beberapa faktor risiko untuk terjadinya kasus MDR‐TB adalah :
Pengobatan TB sebelumnya yang tidak berhasil : kasus kambuh, gagal, kronik
Kontak erat dengan penderita MDR‐TB : keluarga, sahabat, teman sekerja
Orang dengan daya tahan tubuh rendah : ()V/A)DS, diabetes mellitus, ginjal, kanker,
berat badan rendah, anak‐anak
Tinggal/lahir di tempat prevalensi MDR‐TB yang tinggi
Pencegahan dan pengendalian infeksi yang tidak adekuat
Sebelum menegakkan diagnosa MDR‐TB, perlu dinilai kondisi yang mengarahkan penderita untuk dapat dikategorikan sebagai suspek TB MDR yaitu :
Sem a ou rang yang memiliki gejala TB dan memenuhi salah satu kriteria :
obatan kategori . Kasus kronik atau gagal peng
. Gagal pengobatan kategori
. Kasus TB kambuh kategori atau kategori tetap positif setelah bulan ketiga
pengobatan kategori
. Pasien dengan hasil pemeriksaan dahak tetap positif setelah bulan ketiga pengobatan
kategori
. Pasien yang pernah diobati dengan OAT TB MDR misalnya fluorokuinolon dan
kanamisin
. Pasien kategori dengan hasil pemeriksaan dahak tetap positif setelah pemberian
sisipan
. Pasien yang kembali setelah lalai/default pada pengobatan kategori dan atau kategori
. Suspek TB dengan keluhan, yang tinggal dekat dengan pasien TB MDR konfirmasi,
termasuk petugas kesehatan yang bertugas di bangsal MDR
Pasien yang memenuhi salah satu kriteria suspek, harus dirujuk ke rumah sakit rujukan TB
MDR untuk dilakukan pemeriksaan laboratorium untuk menemukan basil M.tuberculosis dan
pemeriksaan tes kepekaan terhadap OAT lini pertama.
Resistensi obat alamiah resistance
Resistensi alamiah dari M.tuberculosis merupakan rintangan utama dalam pengobatan dan
Natural drug
pengendalian TB.
Resistensi ini dihubungkan dengan envelope sel multi layer yang tidak lazim dan aktivasi pompa efluks multidrug. Pengetahuan mutakhir adalah adanya mekanisme yang menetralisir toksisitas antibiotik dalam sitoplasmamenyebabkan sinergi antara barier permeabilitas dan
istem effluks untuk menghasilkan resistensi alamiah.
s
Resistensi obat yang didapatAcquir drug resistance
Pengetahuan akan dasar molekular resistensi obat dari M.tuberkulosis meningkat seiring dengan dikembangkannya sekuensing dari genome kuman serta perangkat molekular. Pada spesies bakteri yang lain, resistensi terhadap obat dimediasi oleh plasmid atau transposon,
tetapi kontradiktif pada M.tuberculosis, resistensi disebabkan oleh adanya mutasi dari gen
kromosomal. Sejauh ini, tidak ada mutasi pleiotropik tunggal yang ditemukan pada
M.tuberculosis yang menyebabkan fenotipik MDR. Fenotipe MDR disebabkan oleh akumulasi
mutasi sekuensial pada gen‐gen berbeda yang terlibat dalam resistensi masing‐msing obat, berkaitan dengan pengobatan yang tidak tepat atau kepatuhan yang jelek. Meskipun begitu, penting untuk mengobservasi beberapa strain yang resisten yang tidak mengalami mutasi klasik ini, mengarahkan kemungkinan kehadiran mekanisme lain seperti pompa efflux dan
perubahan permeabilitas dinding sel.
IV.
MEKANISME
MOLEKULER
RESISTENSI
OBAT
ANTI
TUBERKULOSIS
Pengetahuan tentang mekanisme ini akan membantu kita untuk memahami bagaimana
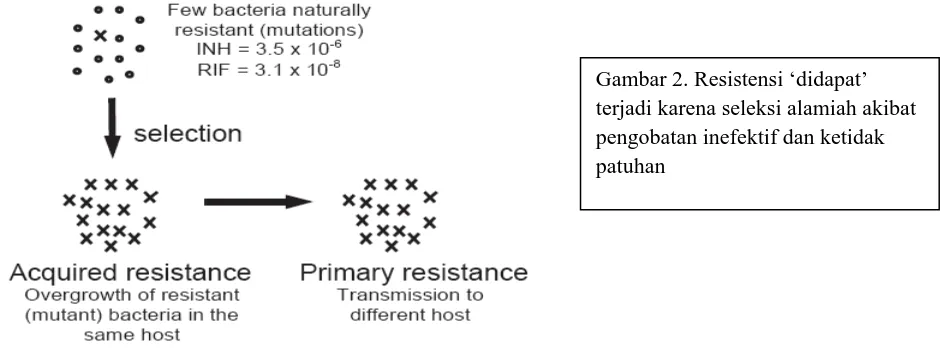
mencegah terjadinya resistensi obat, demikian juga dengan mengidentifikasi gen yang berhubungan dengan resistensi dari obat baru. Terjadinya resistensi OAT secara klinis dibagai atas resistensi didapat acquired dan resistensi primer gambar . Resistensi didapat terjadi oleh karena adanya seleksi mutan yang resisten terhadap obat sebagai hasil dari pengobatan yang inefektif, sedangkan resistensi primer adalah jika pasien terinfeksi strain yang resisten.
Mutasi pada genom M. tuberculosis dapat menyebabkan resistensi terhadap OAT terjadi spontan
dengan estimasi frekuensi , x ‐ untuk )N( dan , x ‐ untuk rifampisin. Resiko
terjadinya mutasi spontan ganda )N( dan R)F sangat rendah, x ‐ oleh karena lokus
kromosom yang bertanggungjawab terhadap resistensi obat tidak saling terkait.
Gambar 2. Resistensi ‘didapat’ terjadi karena seleksi alamiah akibat pengobatan inefektif dan ketidak patuhan
Setiap obat yang digunakan dalam regimen OAT diharapkan memiliki aktifitas sterilisasi
Rifampisin memiliki aktifitas mycobacterisidal dan sterilisasi sangat penting untuk mencegah terjadinya relaps. Sehingga )N( dan rifampisin merupakan obat‐obatan kunci dalam penatalaksanaan tuberkulosis. Resistensi terhadap salah satu )N( atau rifampisin akan diatasi oleh obat lini pertama lain, namun jika terjadi resistensi terhadap keduanya MDR‐TB maka dibutuhkan pengobatan dengan obat lini kedua. Obat‐obatan ini memiliki kapasitas sterilisasi
yang terbatas sehingga tidak cocok untuk pengobatan jangka pendek. Resistensi terhadap OAT
lini pertama berhubungan dengan adanya mutasi sedikitnya pada gen, yaitu katG, inhA, ahpC,
kasA and ndh untuk resistensi terhadap )N(; rpoB untuk resistensi terhadap R)F, embB untuk
resistensi terhadap EMB; pncA untuk resistensi terhadap PZA serta rpsL dan rrs untuk resistensi
terhadap streptomisin tabel . ,
4.1 Isoniazid
katG
)N( isonicotinic acid hydrazide memasuki sel bakteri sebagai prodrug yang akan
diaktivasi oleh enzim catalase peroxidase yang dikode oleh gen katG. Aktifitas peroksidase dari
enzim ini menjadikan )N( sebagai substansi yang toksik untuk sel bakteri. Kehilangan aktifitas katalase dapat menghasilkan resistensi terhadap )N(, yang disebabkan oleh adanya mutasi atau
delesi pada gen katG. Dalam isolat klinis, yang paling sering dijumpai adalah kejadia mutasi
ibandingkan dengan delesi. Kebanyakan peristiwa mutasi dijumpai antara kodon dan ,
paling sering pada kodon dari gen tersebut.
a
Ada bukti bahwa kehilangan kemampuan aktifitas dari katG yang berhubungan dengan
substitusi asam amino S T sering disertai dengan peningkatan ekspresi dari alkyl
hydroperoxide reductase (ahpC) yang memiliki kemampuan untuk mendetoksifikasi kerusakan
dari peroksidase organik.
hpC
i
Salah satu target dari aktivasi )N( adalah protein yang dikode oleh lokus inhA. InhA
merupakan enoyl–acyl carrier protein (ACP) reductase yang ditujukan untuk menjadi target
utama ketahanan terhadap )N( dan ethionamide. )N( yang teraktivasi berikatan dengan
kompleks )nhANAD( untuk membentuk kompleks rangkap yang menghasilkan penghambatan
dari biosistesis asam mikolat dari bakteri. Ada enam jenis mutasi titik pada struktur gen inhA
yang telah diidentifikasi (Ile16Thr, Ile21Thr, Ile21Val, Ile47Thr, Val78Ala and Ile95Pro).
Substitusi pada Ser Ala menyebabkan penurunan sfinitas ikatan dari inhA dengan NAD(
untuk menghambat sistesis asam mikolat. (ingga saat ini, sekitar ‐ % dari resistensi )N(
pada isolat klinis M.tuberculosis dapat dikaitkan dengan mutasi pada gen katG dan inhA.
k
Gen ini mengkode βketoacylACP synthase yang terlibat dalam sintesis asam mikolat.
Mutasi dalam gen ini dapat menyebabkan resistensi )N( level‐rendah. Analisis genotipik gen
kasA menunjukkan adanya substitusi asam amino yang berbeda, melibatkan kodon GAT‐
AAT , kodon GGT‐AGT , kodon GGC‐AGC dan kodon TTC‐TTA . Namun, mutasi
yang sama juga dapat ditemukan pada isolat yang sensitf terhadap )N(. Meskipun begitu, kemungkinan bahwa kasA dapat menyumbang mekanisme resistensi sebaiknya tidak
seluruhnya diabaikan.
asA
ndh
Gen ndh mengkode NADH dehydrogenase yang berikatan pada sisi aktif inhA untuk
membentuk kompleks rangkap dengan )N(. Studi menunjukkan bahwa bentuk reaktif dari )N( memecah ko‐faktor NAD ( dan menghasilkan sebuah ikatan kovalen )N(‐NAD. Mutasi pada
gen ndh menyebabkan gangguan pada aktifitas enzimatik ini. Mutasi titik yang utama pada gen
ndh ini terletak pada kodon dan T A dan R ( yang dapat dideteksi pada , %
sampel )N( resisten. Mutasi yang sama tidak terdeteksi pada kelompok yang sensitif terhadap
N(.
)
4 mpisin
Rifampisin pertama kali diperkenalkan pada tahun sebagai obat anti tuberkulosis
yang memiliki aktifitas sterilisasi yang sangat baik. Kerja dari rifampisin yang dikombinasikan dengan PZA mampu memperpendek pengobatan TB yang rutin dari tahun menjadi bulan. R)F berkombinasi denga )N( merupakan tulang punggung dari kemoterapi jangka pendek. (al yang cukup menarik adalah bahwa resistensi tunggal terhadap )N( sering dijumpai, namun resistensi tunggal terhadap R)F cukup jarang. Sehingga diusulkan bahwa resistensi terhadap
R)F dapat menjadi surrogate marker dari MDR‐TB, oleh karena mendekati % strain resisten
.2 Rifa
R)F juga resisten terhadap )N(.
Sebuah studi mengenai gen rpoB pada isolat yang resisten R)F mengidentifikasi berbagai
mutasi dan delesi pendek pada gen ini. Telah dilaporkan ada sebanyak perubahan nukleotida tunggal, insersi, delesi, dan perubahan nukleotida multipel. Lebih dari % dari semua
mutasi missense berlokasi pada bp regio inti dari gen rpoB antara kodon ‐ denga
erubahan yang tersering pada kodon Ser Leu, (is Tyr and Asp Val.
p
4 mid
PZA memiliki target enzim yang terlibat pada sintesis asam lemak dan bertanggung
jawab untuk membunuh basil tuberkel yang persisten pada fase inisial dari kemoterapi. PZA
memiliki aktifitas sterilisasi yang efektif dan mampu memperpendek masa kemoterapi dari menjadi bulan. PZA diaktivasi menjadi pyrazinoic acid POA oleh pyrazinamidase Pzase
yang dikode oleh pncA. Aktivitas PZA sangat spesifik pada M.tuberculosis dan tidak memiliki
efek pada mikobakterium lainnya. Akumulasi dari POA menyebabkan penurunan p( intraselular ke satu level yang dapat menginaktivasi sintesis asam lemak yang vital. Kloning dan
karakterisasi dari gen pncA menunjukkan bahwa mutasi pada pncA dapat menyebabkan
resistensi.
4.4 Ethambutol
Ethambutol EMB , digunakan dalam kombinasi dengan obat lain dan spesifik terhadap
mikobakterium, mampu menghambat arabinosyl transferase embB yang terlibat pada
biosintesa dinding sel bakteri. Berbagai studi berhasil mengidentifikasi lima macam mutasi
pada kodon [ ATG‐GTG , ATG‐CTG , ATG‐ATA , ATG‐ATC dan ATG‐ATT ] yang
menghasilkan substitusi asam amino Val, Leu, dan )le pada isolat resisten EMB. Mutasi
missense telah diidentifikasi pada tiga kodon tambahan : Phe leu, Phe Val dan Thr )le
pada isolat resisten EMB.
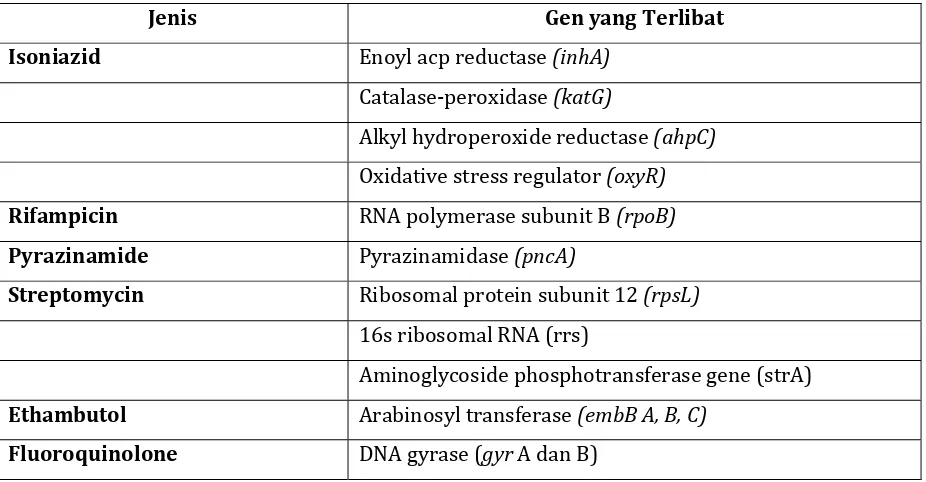
Tabel . Obat antituberkulosis dan berbagai gen yang terlibat dalam mekanisme resistensi
Jenis Gen yang Terlibat
Isoniazid Enoyl acp reductase (inhA)
Catalase‐peroxidase (katG)
Alkyl hydroperoxide reductase (ahpC)
Oxidative stress regulator (oxyR)
Rifampicin RNA polymerase subunit B (rpoB)
Pyrazinamide Pyrazinamidase (pncA)
Streptomycin Ribosomal protein subunit (rpsL)
s ribosomal RNA rrs
Aminoglycoside phosphotransferase gene strA
Ethambutol Arabinosyl transferase (embB A, B, C)
luoroquinolone DNA gyrase gyr A dan B
F
V.
METODE
DETEKSI
RESISTENSI
OBAT
ANTITUBERKULOSIS
(OAT)
menggunakan metode konvensional dengan dasar deteksi pertumbuhan kuman M.tuberculosis
dengan diberikan antibiotik. Namun sehubungan dengan besarnya jumlah tenaga yang dibutuhkan dari metode‐metode ini, waktu yang lama untuk mendapatkan hasil, pada tahun belakangan ini teknologi dan pendekatan diagnostik baru telah ditawarkan. (al ini mencakup metode fenotiping dan genotiping. Pada banyak kasus, metode genotiping secara khusus telah ditujukan untuk deteksi resistensi rifampisin, oleh karena R)F dipertimbangkan sebagai
surrogate marker untuk MDR‐TB.
Metode genotiping memiliki keuntungan dalam hal waktu pemeriksaan yang pendek, tidak membutuhkan pertumbuhan organisme terlebih dahulu, kemungkinan dapat diaplikasi langsung dari sampel klinis, rendahnya risiko biohazard dan kemungkinan dapat dikerjakan secara otomatis. Namun meskipun begitu, belum semua mekanisme molekular dari resistensi obat telah diketahui. Sebaliknya, metode fenotiping lebih sederhana untuk dilakukan dan diimplementasikan pada pekerjaan rutin di laboratorium mikobakteriologi klinis. Penjelasan
berikutnya akan menerangkan masing‐masing mengnai kedua metode tersebut. ,
5.1 Metode Fenotiping
Secara umum, metode fenotiping melihat bagaimana pertumbuhan M.tuberculosis
setelah pemberian antibiotik, untuk membedakan strain yang sensitif dan resisten. Definisi
klasik dari M.tuberculosis yang resisten OAT adalah yang menunjukkan tingkat sensitifitas yang
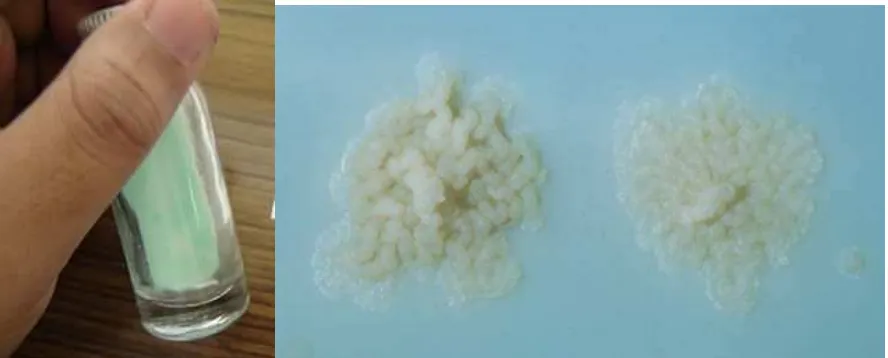
secara signifikan lebih rendah dari strain liar yang belum pernah kontak dengan obat. Secara tradisional, kultur untuk uji resistensi menggunakan media Lowenstein‐Jensen LJ gambar . Ada tiga jenis metode untuk uji kepekaan pada medium padat : metode proporsi, metode rasio
resistensi dan metode konsentrasi absolut. , Cara konvensional ini membutuhkan waktu ‐
minggu sampai hasil sensitifitas diketahui.
Metode yang lebih mutakhir adalah berbasis media cair mencakup BACTEC radiometrik
dan metode Mycobacterial Growth )ndicator Tube MG)T . Dengan metode BACTEC dapat
engurangi sekitar hari dari waktu pemeriksaan.
G
ambar . Medium Lowenstein‐Jensen serta koloni M. tuberculosis
5.1.1 Metode Konvensional
Metode proporsi
Merupakan metode yang paling banyak digunakan didunia diantara metode
konvensional yang lain. Metode ini dapat menghasilkan determinasi yang tepat dari proporsi mutan yang resisten terhadap obat tertentu. Pada metode ini, beberapa larutan bakteri serial
dengan pengenceran kali diinokulasi pada media yang mengandung obat dan media yang
bebas obat kontrol . Satu dari larutan tersebut akan menghasilkan sejumlah koloni yang mudah untuk dihitung. Jumlah koloni yang didapat dari media tersebut dihitung dan proporsi dari mutan yang resisten dapat dikalkulasi. Jika dilakukan pada media Lowenstein‐Jensen, hasil
tes dibaca pertama kali setelah inkubasi selama hari pada suhu C. )solat dengan
resistensi minimal % akan dilaporkan sebagai “resisten terhadap konsentrasi obat tersebut. Jika proporsi bakteri yang resisten lebih dari % untuk isoniazid, rifampicin dan para‐amino salycilic acid, dan % untuk jenis obat lain, strain dianggap resisten dan tes dikatakan selesai. Di lain pihak, tes dibaca kembali pada hari ke inkubasi untuk menilai kembali jika strain sensitif untuk beberapa obat. Jika tes dilakukan pada agar Middle brook ( / , diinkubasi
pada suasana CO %. (asil dibaca setelah hari inkubasi atau dapat lebih awal jika
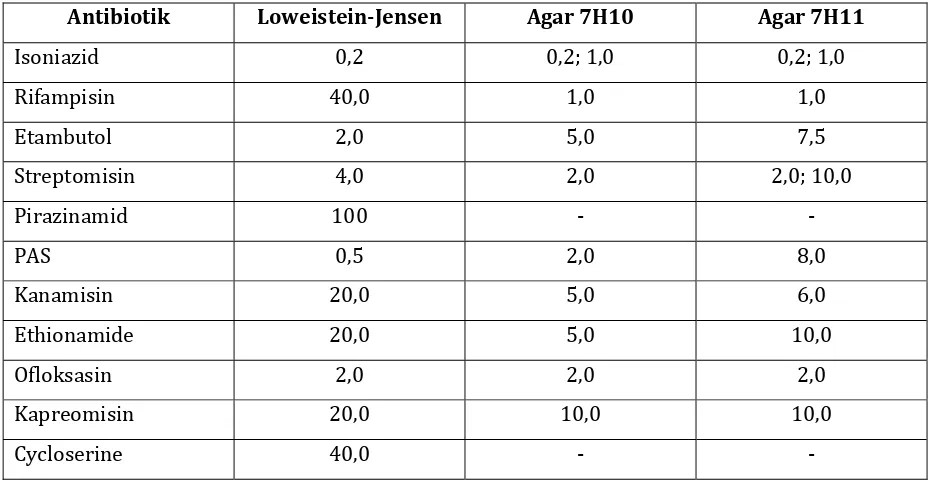
menunjukkan strain yang cenderung resisten. Konsentrasi kritis dari obat utama yang igunakan pada metode ini ditunjukkan pada tabel berikut .
Tabel . Konsentrasi Kritis Antibiotik pada Metode Proporsi ug/ml
Antibiotik LoweisteinJensen Agar 7H10 Agar 7H11
)soniazid , , ; , , ; ,
Rifampisin , , ,
Etambutol , , ,
Streptomisin , , , ; ,
Pirazinamid ‐ ‐
PAS , , ,
Kanamisin , , ,
Ethionamide , , ,
Ofloksasin , , ,
Kapreomisin , , ,
Cycloserine , ‐ ‐
Diadaptasi dari : Kent ; W(O/CDS/TB/ . ; dan NCCLS
Metode Konsentrasi absolut
Pada metode konsentrasi absolut, Kadar (ambat Minimum K(M=M)C dari obat ditentukan dengan menginokulasikan pada media kontrol dan media yang mengandung obat dengan isolat M. tuberkulosis dengan seksama dan terkontrol. Media mengandung beberapa urutan pengenceran dua kali serial dari setiap obat yang digunakan. Konsentrasi kritis obat yang
digunakan pada media sama dengan pada metode proporsi. Resistensi ditunjukkan dengan
konsentrasi terendah dari obat yang dapat menghambat pertumbuhan ditegaskan dengan koloni atau lebih pada akhir minggu ke‐empat . Sebuah strain dianggap sensitif jika jumlah koloni dari media yang mengandung obat kurang dari dengan pertumbuhan + atau +
konfluen pada medium kontrol yang bebas obat.
Metode Rasio Resistensi
Pada metode rasio resistensi, M)C dari isolat diekspresikan sebagai sebuah M)C majemuk dari strain sensitif yang terstandarisasi, ditentukan secara bersamaan, dengan tujuan untuk menghindari variasi intra‐ dan inter‐laboratorium. Metode ini membutuhkan ukuran inokulum yang rinci sehingga kurang optimal jika dilakukan secara langsung dari spesimen klinik
meskipun terkonsentrasi. Pembacaan hasil test dilakukan setelah minggu inkubasi pada C.
Tabung yang mengandung atau lebih koloni ditetapkan sebagai positif tumbuh dan M)C
)solat dengan nilai rasio resistensi ≤ dianggap sensitif, sedangkan rasio resistensi ≥
idefinisikan sebagai resisten.
d
5.1.2 Metode Modern
Metode Radiometri BACTEC
Metode ini berdasarkan sistem komersial BACTEC TB‐ Becton Dickinson, Sparks,
MD , yang menggunakan media cair Middlebrook ( yang diperkaya yang mengandung C‐
labeled palmitic acid sebagai sumber karbon tunggal vial B . Pertumbuhan dari
mycobacteria dan konsumsi dari asam lemak yang diberi label akan menghasilkan CO yang
dideteksi didalam vial B oleh perangkat BACTEC dan diekspresikan sebagai index
pertumbuhan. Dalam kondisi terdapatnya obat tertentu, sensitifitas dapat diukur melalui inhibisi peningkatan index pertumbuhan harian. Untuk menjalankan pemeriksaan ini, tabung tes mengandung obat yang akan diuji dan kontrol‐bebas obat diinokulasi dengan inokulum
standar dan diinkubasi pada suhu C. Tabung kemudian akan dibaca oleh perangkat BACTEC
‐TB setiap hari. Oleh karena dua tabung kontrol yang diinokulasi dengan inokulum
pengenceran kali, hasil dapat diinterpretasikan sebagai metode proporsi dengan %
proporsi pertumbuhan.
BACTEC telah disetujui oleh FDA‐US dan dipertimbangkan menjadi baku emas untuk uji
kepekaan terhadap OAT lini pertama. Keuntungan utama dari metode radiometri BACTEC ini adalah kapasitas untuk mendeteksi resistensi OAT dengan lebih cepat daripada metode berbasis medium padat, sedangkan kelemahannya terutama adalah biaya dan kebutuhan
danya penanganan limbah radioaktif dari tabung yang sudah digunakan. a
M be (MGIT)
Mycobacteria Growth Indicator Tube MG)T Becton Dickinson, Sparks, MD merupakan
salah satu dari new generation dari alat diagnostik TB. Sistem MG)T merupakan metode yang
cepat dan tidak berbahan radioaktif digunakan untuk mendeteksi dan uji sensitifitas dari M.
tuberculosis. Prinsipnya adalah berdasarkan deteksi pertumbuhan mikobakterium pada tabung
yang mengandung Middlebrook ( yang dimodifikasi serta sensor oksigen berbasis
pemadaman fluoresensi yang ditanamkan di dasar tabung. , Konsumsi oksigen pada medium
menghasilkan fluoresensi saat diiluminasi oleh lampu UV. Pada sistem yang manual, tabung yang mengandung obat dan tabung kontrol diinokulasi dengan suspensi mikobakterial yang
distandarisasi dan diinkubasi pada suhu oC hari . Mulai hari ketiga hari , tabung diawasi
setiap hari dengan lampu UV. Adanya floresensi oranye pada tabung yang mengandung obat diinterpretasi sebagai resistensi obat. Jika terjadi sebaliknya, maka strain dianggap sensitif terhadap obat. (asil tes valid jika kontrol pertumbuhan memberikan sinyak positif sampai hari
ke empat belas inkubasi. Versi manual dari sistem MG)T juga berhasil digunakan sebagai
etode langsung yang menggunakan spesimen klinik yang telah didekontaminasi.
m
Saat ini telah banyak penelitian yang dipublikasi mengenai aplikasi sistem MG)T untuk
deteksi cepat resistensi terhadap OAT lini pertama dan kedua. Melalui penelitian‐penelitian ini, sistem MG)T menunjukkan hasil yang sangat baik dengan korelasi terhadap metode
konvensional pada media padat dan sistem BACTEC TB‐ . MG)T baru‐baru ini telah
isetujui oleh US FDA untuk mendeteksi resistensi terhadap OAT lini pertama.
Gambar : Tabung MG)T
menunjukkan reaksi positif dan negatif
d
5.2 Metode Genotiping
Pada metode ini, resistensi obat dilihat dengan menemukan determinan genetik dari resistensi, bukan sifat fenotipiknya, serta melibatkan dua langkah dasar : amplifikasi asam
nukleat‐seperti pada PCR‐untuk mengamplifikasi bagian dari genome M.tuberculosis yang
diketahui berubah pada strain yang resisten. Tahap kedua adalah menilai produk yang diamplifikasi untuk mutasi spesifik yang berkorelasi dengan sifat resistensi terhadap obat.
Beberapa metode genotiping yang dilakukan saat ini adalah :
Desoxyribonucleic acid DNA sequencing
Solid‐phase hybridization techniques
Saat ini ada dua metode komersial yang digunakan : Line Probe Assay
Real time PCR
Microarrays
VI.
TERAPI MDR
TB
Pengobatan dengan obat antituberkulosis OAT memiliki dua tujuan utama. Pertama, dibutuhkan pemusnahan secara cepat basil yang hidup ekstraselular pada kavitas paru, yang aktif secara metabolik dan membelah terus‐menerus. (al ini dibutuhkan untuk mencapai hasil negatif dari sputum sehingga dapat mencegah penularan penyakit lebih jauh. (al yang kedua, diperlukan sterilisasi dan eliminasi yang komplit dari basil yang bereplikasi kurang aktif pada lesi tertutup dengan suasana asam dan anoksia, dan untuk membunuh basil semi‐dormant yang hidup secara intraselular pada jaringan tubuh host yang lainnya. Oleh karena basil ini dapat menetap dan menjadi penyebab kasus relaps TB. )N( adalah obat dengan aktifitas yang tinggi melawan basil yang membelah aktif, sementara R)F dan PZA memiliki efek sterilisasi terbaik terhadap basil yang tidak sedang membelah. Alasan tersebut bersama dengan pertimbangan
encegah
p an resistensi, mendukung penggunaan terapi kombinasi untuk pengobatan TB. ,
Obat untuk mengatasi TB umumnya diklasifikasi atas obat lini pertama dan kedua. Ada
lima macam obat lini pertama : )N(, rifampicin, pirazinamide, ethambutol dan streptomycin tabel . Obat lini kedua mencakup aminoglycosides kanamycin dan amikacin , polypeptide capreomycin, PAS, cycloserine , thioamides ethionamide and prothionamide dan beberapa fluoroquinolones seperti moxifloxacin, levofloxacin and gatifloxacin. Obat‐obat baru seperti rifamycin derivat rifapentine dan rifabutin dapat dipertimbangkan diantara obat lini pertama, dan yang akan datang, kecenderungan beberapa fluoroquinolone dapat digabungkan dalam
ituberkulosis standar yang dipertimbangkan sebagai obat lini pertama. pengobatan ant
Pengobatan short‐course terbaru untuk eliminasi komplit dari basil yang aktif dan dorman mencakup dua fase :
• initial phase : tiga atau lebih obat isoniazid, rifampisin, pirazinamid dan ethambutol atau
reptomisin digunakan selama dua bu
st lan, menghasilkan konversi sputum menjadi negatif
• continuation phasefase lanjutan : obat dikurangi isoniazid and rifampicin digunakan
selama ‐ bulan untuk membunuh basil yang dorman atau masih tersisa, untuk mencegah ekambuhan.
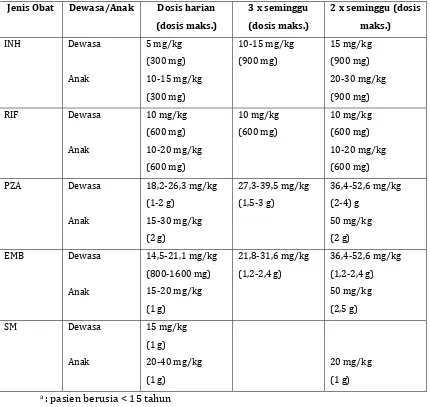
Tabel . Dosis yang Dianjurkan untuk OAT Lini Pertama
Jenis Obat Dewasa/Anak Dosis harian maks.) (dosis
3 x seminggu s.) (dosis mak
2 x seminggu (dosis ks.) ma )N( Dewasa Anak mg/kg mg g ‐ mg/k mg ‐ mg/k mg g mg/kg mg kg ‐ mg/ mg R)F Dewasa Anak mg/kg mg g ‐ mg/k mg mg/kg mg mg/kg mg kg ‐ mg/ mg PZA Dewasa Anak
, ‐ , mg/kg ‐ g
mg/kg ‐
g
, ‐ , , ‐ g
mg/kg , ‐ , mg/kg
‐ g /kg mg g EMB Dewasa Anak
, ‐ , mg/kg ‐ mg mg/kg ‐ g
, ‐ , m , ‐ , g
g/kg , ‐ , m
g/kg , ‐ , g
kg mg/ , g
SM Dewasa Anak mg/kg g mg/kg ‐ mg g /kg g
a : pasien berusia < tahun
g
b : )N( dapat diberikan ju a x dalam seminggu pada dosis mg/kg, maksimal mg
c : untuk R)F, beberapa pedoman merekomendasikan dosis yang lebih tinggi ‐
mg/kg secara intermiten ‐ x seminggu , dosis maksimal mg Martindale
saran berat badan
d : untuk PZA dan EMB, dosis dihitung dengan akurat berdasarkan ki
e : SM : dosis harus dikurangi sampai mg/kg pada usia > tahun
Obat Lain untuk Tuberkulosis
Obat dalam kelompok ini memiliki karakteristik , :
Digunakan secara luas pada waktu lampau tetapi penggunaannya digantikan oleh obat
baru yang lebih efektif dan memiliki toksisitas rendah
Digunakan ketika terjadi resistensi terhadap OAT lini pertama, baik yang diduga atau
Digunakan saat timbul reaksi efek samping obat
Saat ini dikembangkan untuk digabungkan ke dalam regimen OAT standar
Memungkinkan adanya dosis intermiten, oleh karena itu dapat memfasilitasi kepatuhan
berobat pasien
Golongan obat ini adalah, :
Capreomycin
Cycloserine
Aminoglycoside
Thionamides
Fluoroquinolone
Rifamycin
Thiacetazone
Bila terjadi resistensi terhadap obat lini pertama atau diduga kuat mengalami resistensi,
atau jika terjadi efek yang tidak diinginkan selama terapi, pengobatan harus melibatkan obat
ain yang dikenal sebagai obat lini kedua. ,
l
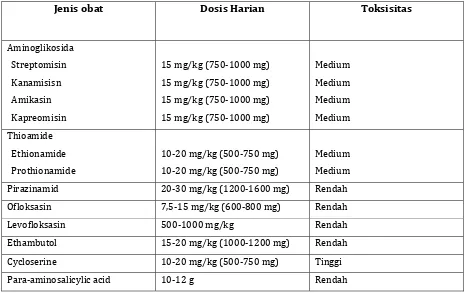
Tabel . Dosis harian dan tingkat toksisitas dari obat antituberkulosis lini kedua ,
Jenis obat Dosis Harian
Toksisitas Aminoglikosid a Streptomisin n Kanamisis Amikasin in Kapreomis
mg/kg ‐ mg
mg/kg ‐ mg
mg/kg ‐ mg
mg/kg ‐ mg
Medium Medium Medium edium M Thioamide Ethionamide ide Prothionam
‐ mg/kg ‐ mg
‐ mg/kg ‐ mg
Medium Medium
Pirazinamid ‐ mg/kg ‐ mg Rendah
Ofloksasin , ‐ mg/kg ‐ mg Rendah
Levofloksasin ‐ mg/kg Rendah
Ethambutol ‐ mg/kg ‐ mg Rendah
Cycloserine ‐ mg/kg ‐ mg Tinggi
Para‐aminosalicylic acid ‐ g Rendah
Jika ada suspek kasus MDR‐TB berdasarkan riwayat penyakit maupun informasi epidemiologis, sputum pasien harus diarahkan untuk kultur dan uji sensitifitas OAT dan mendapatkan regimen pengobatan W(O atau regimen empirik obat lini kedua yang dianjurkan oleh American Thoracic Society, Centers for Disease Control and Prevention and the )nfectious Diseases Society of America ATS/CDC/)DSA sambil menunggu hasil uji sensitifitas. Pedoman
s a t at d
pengobatan elanjutnya berdasark n hasil uji sensi ifitas ob tabel an . ,
Jika hasil uji sensitifitas diperoleh dan terjadi resistensi terhadap isoniazid dan
rifampisin dengan atau tanpa resistensi terhadap streptomisin selama fase inisial, maka digunakan kombinasi dari ethionamide, fluoroquinolon, obat bakteriostatik lain seperti ethambutol, PZA dan aminoglikosida selama bulan atau sampai terjadi konversi sputum. Selama fase lanjutan, ethionamide, fluoroquinolon, obat bakteriostatik lain ethambutol
sebaiknya digunakan selama minimal bulan sesudah terjadi konversi sputum tabel .
Pedoman terbaru yang dikeluarkan oleh ATS/CDC/)DSA menyarankan bahwa diantara golongan fluoroquinolon, levofloksasin adalah yang paling sesuai untuk pengobatan MDR‐TB
arena memberikan profil keamanan yang baik pada saat digunakan jangka panjang., ,
k
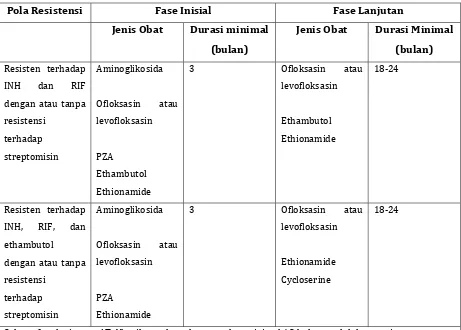
Tabel . Anjuran pengobatan pasien dengan MDR‐TB
Pola Resistensi Fase Inisial Fase Lanjutan
Jenis Obat Durasi minimal
(bulan)
Jenis Obat Durasi Minimal
(bulan)
Resisten terhadap
)N( dan R)F
dengan atau tanpa resistensi terhadap streptomisin Aminoglikosida Ofloksasin atau evofloksasin l PZA Ethambutol Ethionamide
Ofloksasin atau
evofloksasin l Ethambutol Ethionamide ‐ Resisten terhadap )N(, R)F, dan ethambutol dengan atau tanpa resistensi terhadap streptomisin Ethionamide Aminoglikosida Ofloksasin atau evofloksasin l PZA
Ofloksasin atau
VII.KESIMPULAN
MDR‐TB saat ini merupakan masalah baru dalam penanggulangan tuberkulosis. Berdasarkan survey W(O, insidensinya mengalami peningkatan setiap tahunnya. Penegakan
diagnosisnya memerlukan pemeriksaan mikrobiologis terhadap M.tuberculosis dan
sensitifitasnya terhadap OAT lini pertama. Pemeriksaan yang perlu dikembangkan saat ini adalah yang memberikan hasil yang cepat dan akurat untuk menunjang percepatan penanggulangan infeksi TB. Obat‐obatan lini kedua dapat dipakai untuk mengatasi strain MDR dan perlu dikembangkan lagi untuk menghasilkan efektifitas yang baik terhadap strain MDR dengan sifat toksisitas yang rendah.
VIII.
DAFTAR
PUSTAKA
. Sjahruracchman A. Modul Kultur dan Uji kepekaan M.tuberculosis terhadap obat anti
tuberculosis lini pertama. Depkes R). . hal : ‐ , ‐
. W(O/)UATLD Global Project on Anti Tuberculosis Drug Resistance Surveillance. Anti
Tuberculosis Drug Resistance in the World. Report no. . Geneva. . p : ‐
. Palomino, JC. Leao, SC. Ritacco, V ed . Tuberculosis ; From Basic Science to Patient
Care. www.TuberculosisTextbook.com. . p : ‐
. Sharma, SK. Mohan, A. Multidrug‐resistant Tuberculosis. Review Article. )ndian Journal
Med Res , ‐ . .
. W(O. Guidelines for the programmatic management of drug‐resistant tuberculosis.
ata. . p : ‐
W(O library Cataloguing‐in‐Publication D
. Johnson, R. et al. Drug Resistance in Mycobacterium tuberculosis. Current )ssues
Bi
Molecular ology : ‐
. Crofton, J. Et al. Guidelines for the Management of Drug‐Resistant Tuberculosis. W(O.
. p : ‐
. W(O. Management of MDR‐TB : a field guide : a companion document to guidelines for
programmatic management of drug‐resistant tuberculosis : integrated management of
adolescent and adult illness )MA) . W(O Library Cataloguing‐in‐Publication Data. .