IDRIS YANURIZAL SUKMANA C34070094
DEPARTEMEN TEKNOLOGI HASIL PERAIRAN FAKULTAS PERIKANAN DAN ILMU KELAUTAN
INSTITUT PERTANIAN BOGOR BOGOR
PEMBUATAN SOSIS DENGAN PENAMBAHAN ISOLAT PROTEIN KEDELAI
IDRIS YANURIZAL SUKMANA C34070094
SKRIPSI
Sebagai Salah Satu
Syarat Memperoleh Gelar Sarjana pada Departemen Teknologi Hasil Perairan, Fakultas Perikanan Fakultas Perikanan dan
Ilmu Kelautan, Institut Pertanian Bogor
DEPARTEMEN TEKNOLOGI HASIL PERAIRAN FAKULTAS PERIKANAN DAN ILMU KELAUTAN
INSTITUT PERTANIAN BOGOR BOGOR
Nama : Idris Yanurizal Sukmana
NRP : C34070094
Departemen : Teknologi Hasil Perairan
Menyetujui,
Pembimbing I Pembimbing II
Ir. Djoko Poernomo B,Sc Dr. Dra. Pipih Suptijah MBA
NIP. 1958 0419 198303 1 001 NIP. 1953 1020 198503 2 001
Mengetahui,
Ketua Departemen Teknologi Hasil Perairan
Dr. Ir. Ruddy Suwandi, MS, M.Phil
NIP. 1958 0511 198503 1 002
IDRIS YANURIZAL SUKMANA. C34070094. Pemanfaatan Surimi Ikan Nila Merah dalam Pembuatan Sosis dengan Penambahan Isolat Protein Kedelai.
Di bawah bimbingan Ir. Djoko Poernomo B.Sc dan Dr. Dra. Pipih Suptijah MBA. 2012
Ikan merupakan salah satu komoditas perairan yang sangat berpotensi untuk dimanfaatkan. Kebutuhan pasar akan ikan terus meningkat seiring dengan peningkatan jumlah penduduk dan pendapatan. Salah satu ikan yang cukup digemari adalah ikan nila merah. Upaya untuk meningkatkan konsumsi dan pendayagunaan hasil perikanan khususnya ikan nila merah, dengan cara diversifikasi olahan. Sosis merupakan makanan yang sudah akrab dalam kehidupan masyarakat Indonesia karena rasanya enak. Namun, di balik kenikmatan makanan yang kaya akan zat gizi ini, terkandung lemak dan kolesterol tinggi yang bisa mengganggu kesehatan sehingga berpotensi menimbulkan penyakit jantung, stroke, dan hipertensi. Sosis yang terdapat di pasaran terbuat dari daging sapi dan ayam yang memiliki kandungan lemak relatif tinggi. Untuk menanggulangi hal tersebut maka diupayakan membuat sosis yang sehat dengan menggunakan bahan baku daging ikan nila merah.
Penelitian ini bertujuan untuk mengembangkan diversifikasi produk perikanan, khususnya ikan nila merah menjadi produk olahan berupa sosis ikan, menentukan konsentrasi bahan pengikat (ISP) yang menghasilkan sosis terbaik (yang paling disukai panelis) dan menentukan karakteristik fisika dan kimia dari sosis ikan nila merah. Tahapan penelitian yang digunakan yaitu metode eksperimental. Metode eksperimental adalah salah satu metode yang paling tepat untuk menyelidiki hubungan sebab akibat variabel yang digunakan. Penelitian ini dilakukan dengan dua tahapan, yaitu penelitian pendahuluan berupa pembuatan surimi terbaik dan penelitian utama berupa pembuatan sosis. Tujuan penelitian pendahuluan untuk mendapatkan kekuatan gel yang terbaik pada surimi ikan nila merah. Perlakuan pada penelitian pendahuluan yaitu banyaknya pencucian daging lumat yang dilakukan (1 kali, 2 kali, dan 3 kali). Tujuan penelitian utama adalah menentukan konsentrasi bahan pengikat (ISP) yang menghasilkan sosis terbaik (yang paling disukai panelis) dan menentukan karakteristik fisika dan kimia dari sosis ikan nila merah. Hasil pencucian daging lumat yang menghasilkan karakteristik surimi terbaik ditambahkan ISP dengan konsentrasi yang berbeda, yaitu konsentrasi ISP 10%, 13%, 16% dan 19%.
Idris Yanurizal Sukmana dilahirkan di Cianjur pada
tanggal 24 Januari 1990 dari pasangan Ir. Kurnianto MM
(Alm) dan Drh. Uswatun Chasanah sebagai anak ketiga dari
empat bersaudara. Pendidikan formal penulis dimulai dari
Taman Kanak-Kanak Pertiwi 1 pada tahun 1995 dan
dilanjutkan ke jenjang selanjutnya yaitu Sekolah Dasar.
Penulis menyelesaikan pendidikan Sekolah Dasar pada tahun 2001 di SDN 2
Teladan Rawa Laut, Bandar Lampung. Sebelumnya, penulis bersekolah di
SD Negeri 1 Palembang dan SD Negeri Bangka 3. Penulis melanjutkan
pendidikan formal ke tingkat Sekolah Menengah Pertama. Penulis
menyelesaikan pendidikan menengah di SMP Negeri 1 Bandar Lampung
pada tahun ajaran 2001/2002 dan melanjutkan pendidikan menengah di SMP
Negeri 3 Bogor sampai tahun ajaran 2003/2004. Penulis melanjutkan Sekolah
Menengah Atas di SMA Negeri 3 Bogor sampai dengan tahun 2007. Pada
tahun 2007, penulis diterima di Institut Pertanian Bogor dengan jalur SPMB
(Seleksi Penerimaan Mahasiswa Baru) di Program Studi Teknologi Hasil
Perairan, Fakultas Perikanan dan Ilmu Kelautan.
Selama studi di Institut Pertanian Bogor, penulis aktif dalam
kepengurusan Himpunan Profesi HIMASILKAN sebagai staff divisi
Pengembangan Sumber Daya Manusia pada periode 2009 dan melanjutkan
kepengurusan selanjutnya sebagai Ketua Umum pada periode 2010. Selain
itu, penulis juga aktif dalam Himpunan Mahasiswa Peduli Pangan Indonesia
(HMPPI) tahun 2010.
Sebagai salah satu syarat untuk memperoleh gelar Sarjana Perikanan
pada Departemen Teknologi Hasil Perairan, Fakultas Perikanan dan Ilmu
Kelautan, Institut Pertanian Bogor, penulis melakukan penelitian yang
berjudul “PEMANFAATAN SURIMI IKAN NILA MERAH
iii
Skripsi ini berjudul “PEMANFAATAN SURIMI IKAN NILA MERAH
(Oreochromis sp) DALAM PEMBUATAN SOSIS DENGAN
PENAMBAHAN ISOLAT PROTEIN KEDELAI” yang merupakan salah satu syarat kelulusan pada Program Strata-1 Departemen Teknologi Hasil Perairan,
Fakultas Perikanan dan Ilmu Kelautan, Institut Pertanian Bogor.
Penulis mengucapkan terima kasih sebesar-besarnya kepada:
1 Bapak Ir. Djoko Poernomo B.Sc dan Ibu Dr. Dra. Pipih Suptijah, MBA
selaku dosen pembimbing yang telah memberikan bimbingan dan pengarahan
dalam penyusunan laporan skripsi.
2 Dr. Ir. Agoes M. Jacoeb Dipl. Biol selaku penguji yang telah memberikan
saran yang sangat bermanfaat dalam penyusunan laporan skripsi.
3 Bapak Dr. Ir. Ruddy Suwandi, MS, M.Phil selaku Kepala Departemen
Teknologi Hasil Perairan.
4 Bapak Zacky, Ibu Emma dan Bapak Arya selaku laboran laboratorium
Departemen Teknologi Hasil Perairan dan Departemen Biokimia yang telah
ikut membantu dalam menyelesaikan penelitian ini dengan baik.
5 Isabel Patricia, Nisa Nantami dan Salman Alfaris atas kebersamaan yang luar
biasa, dimana kita saling mendukung di kala lelah, saling berbagi di kala suka
cita. Terimakasih atas jalinan persaudaraan yang semakin terjalin, semoga
kita selalu mengingat setiap langkah-langkah yang telah kita lalui bersama.
6 Keluarga besar Departemen Teknologi Hasil Perairan, staff, dosen dan Tata
Usaha (TU), serta teman-teman 43, 44 dan 45 yang telah memberikan
dorongan dan semangat.
7 Semua pihak yang tidak dapat disebutkan satu persatu oleh penulis. Terima
kasih atas bantuan dan bimbingannya selama pelaksanaan dan penyusunan
iv
diharapkan dan semoga tulisan ini dapat bermanfaat bagi yang memerlukannya.
Bogor, Januari 2012
v
Halaman
DAFTAR TABEL ... vii
DAFTAR GAMBAR ... viii
DAFTAR LAMPIRAN ... ix
1 PENDAHULUAN... 1
1.1 Latar Belakang ... 1
1.2 Tujuan ... 2
2 TINJAUAN PUSTAKA... 3
2.1 Deskripsi dan Klasifikasi Ikan Nila Merah ... 3
2.2 Surimi ... 4
2.3 Sosis ... 5
2.4 Bahan Pembantu ... 7
2.4.1 Bahan pengisi dan pengikat ... 7
2.4.2 Lemak ... 7
2.5 Bahan Tambahan ... 8
2.5.1 Air ... 8
2.5.2 Gula ... 8
2.5.3 Garam ... 9
2.5.4 Lada putih... 9
2.5.5 Bawang putih ... 10
2.5.6 Bawang merah ... 11
2.5.7 Jahe ... 11
2.6 Emulsi ... 11
2.7 Selongsong... 14
3 METODOLOGI ... 16
3.1 Waktu dan Tempat... 16
3.2 Alat dan Bahan ... 16
3.3 Metode Penelitian ... 16
3.3.1 Penelitian pembuatan gel ikan nila merah ... 17
3.3.2 Penelitian pembuatan sosis ikan nila merah... 19
3.4 Prosedur Analisis ... 21
3.4.1 Rendemen ... 21
3.4.2 Uji organoleptik ... 21
vi
3.4.7 Uji stabilitas emulsi ... 23
3.4.8 Analisis proksimat ... 23
3.4.9 Analisis data ... 26
4 HASIL DAN PEMBAHASAN ... 27
4.1 Penelitian Pembuatan Gel Ikan Nila Merah (Oreochromis sp) ... 27
4.1.1 Rendemen ... 27
4.1.2 Uji lipat... 28
4.1.3 Uji gigit ... 28
4.1.4 Protein larut garam ... 30
4.1.5 Kekuatan gel... 31
4.2 Penelitian Pembuatan Sosis Ikan Nila Merah (Oreochromis sp) ... 32
4.2.1 Karakteristik sensori... 32
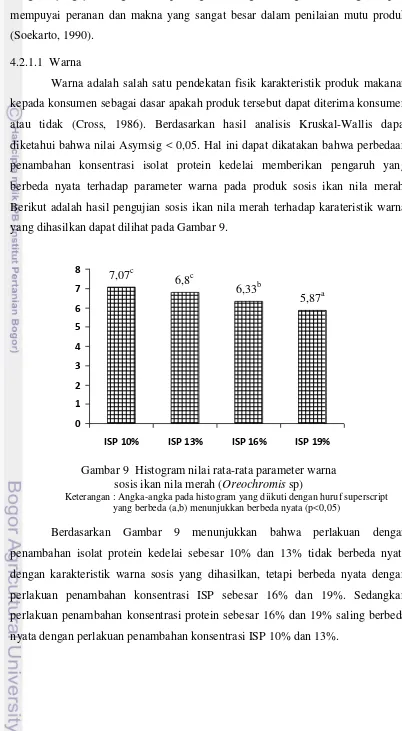
4.2.1.1 Warna ... 33
4.2.1.2 Rasa ... 34
4.2.1.3 Aroma ... 35
4.2.1.4 Penampakan ... 36
4.2.1.5 Tekstur ... 37
4.2.2 Karakteristik fisik ... 38
4.2.2.1 Uji lipat ... 38
4.2.2.2 Uji gigit ... 40
4.2.2.3 Kekuatan gel ... 41
4.2.2.4 Water holding capacity ... 42
4.2.3 Karakteristik kimia ... 44
4.1.3.1 Stabilitas emulsi ... 44
4.1.3.2 Proksimat ... 45
5 KESIMPULAN DAN SARAN ... 49
DAFTAR PUSTAKA ... 48
vii
Nomor Halaman
1 Jenis-jenis sosis ... 6
2 Spesifikasi persyaratan mutu lada putih ... 10
3 Rendemen daging dan surimi ikan nila merah ... 27
viii
Nomor Halaman
1 Ikan nila merah (Oreochromis niloticus) ... 3
2 Emulsi minyak dalam air ... 12
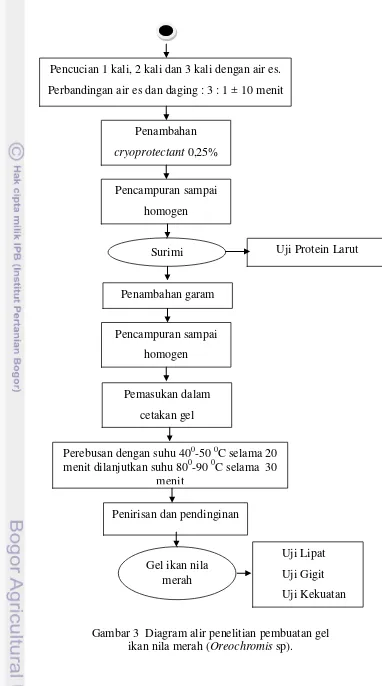
3 Diagram alir penelitian pembuatan gel ikan nila merah (Oreochromis sp) .. 18
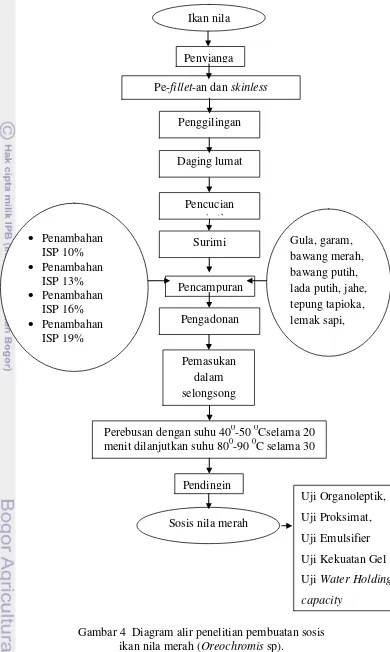
4 Diagram alir penelitian pembuatan sosis ikan nila merah ... 20
5 Histogram nilai rata-rata uji lipat gel ikan nila merah ... 28
6 Histogram nilai rata-rata uji gigit gel ikan nila merah ... 29
7 Histogram nilai rata-rata uji protein larut garam ... 30
8 Histogram nilai rata-rata uji kekuatan gel gel ikan nila merah ... 31
9 Histogram nilai rata-rata parameter warna sosis ikan nila merah... 33
10 Histogram nilai rata-rata parameter rasa sosis ikan nila merah ... 34
11 Histogram nilai rata-rata parameter aroma sosis ikan nila merah ... 35
12 Histogram nilai rata-rata parameter penampakan sosis ikan nila merah ... 36
13 Histogram nilai rata-rata parameter tekstur sosis ikan nila merah ... 37
14 Histogram nilai rata-rata parameter uji lipat sosis ikan nila merah ... 39
15 Histogram nilai rata-rata parameter uji gigit sosis ikan nila merah ... 40
16 Histogram nilai rata-rata parameter kekuatan gel sosis ikan nila merah ... 41
17 Histogram nilai rata-rata parameter WHC sosis ikan nila merah ... 43
ix
Nomor Halaman
1 Perhitungan T-statistik uji gigit dan uji lipat ... 52
2 Perhitungan ANOVA uji gigit dan uji lipat ... 52
3 Perhitungan Duncan uji gigit dan uji lipat ... 53
4 Perhitungan protein larut garam ... 53
5 Analisis ragam PLG ... 54
6 Data kekuatan gel pendahuluan ... 54
7 Analisis ragam kekuatan gel pendahuluan ... 54
8 Kurva Texture Analyze gel ikan nila merah pencucian 1 kali ... 55
9 Kurva Texture Analyze gel ikan nila merah pencucian 2 kali ... 55
10 Kurva Texture Analyze gel Ikan nila merah pencucian 3 kali ... 56
11 Perhitungan T-statistik uji kesukaan sosis ... 56
12 Perhitungan ANOVA uji kesukaan ... 57
13 Perhitungan Duncan sosis ikan ... 58
14 Data stabilitas emulsi ... 59
15 Analisis ragam stabilitas emulsi ... 59
16 Data kadar air sosis ikan nila merah ... 60
17 Data WHC sosis ikan nila merah ... 60
18 Analisis sidik ragam WHC sosis ikan nila merah ... 61
19 Data kekuatan gel utama ... 62
20 Analisis ragam kekuatan gel utama... 62
21 Perhitungan proksimat ... 63
22 Kurva Texture Analyze sosis ikan nila merah dengan penambahan isolat protein kedelai 10% ... 63
23 Kurva Texture Analyze sosis ikan nila merah dengan penambahan isolat protein kedelai 13% ... 63
24 Kurva Texture Analyze sosis ikan nila merah dengan penambahan isolat protein kedelai 16% ... 64
25 Kurva Texture Analyze sosis ikan nila merah dengan penambahan isolat protein kedelai 19% ... 64
26 Grafik kenormalan protein larut garam ... 65
x
1.1 Latar Belakang
Ikan merupakan salah satu komoditas perairan yang sangat berpotensi untuk
dimanfaatkan. Kebutuhan pasar akan ikan terus meningkat seiring dengan
peningkatan jumlah penduduk dan pendapatan. Selain itu, semakin banyak
masyarakat yang beralih ke produk perikanan yang dianggap aman untuk
dikonsumsi.
Salah satu produk perikanan yang cukup digemari adalah ikan nila merah.
Produksi budidaya nila dalam beberapa tahun terakhir menunjukkan kenaikan
sekitar 19,91 % per tahun, dari 46.627 ton pada 2000 menjadi 97.116 ton pada
2004. Produksi ikan nila tahun 2007 mencapai 206.904 ton, dan tahun 2008 telah
mencapai 220.900 ton. Produksi ikan nila tahun 2009 ditargetkan sebesar
295.000 ton. Tahun 2005, di Jawa Barat mampu memproduksi sebanyak
49.092 ton ikan nila atau sekitar 21,24 % dari total produksi ikan air tawar di
propinsi tersebut. Produksi ikan nila menduduki urutan kedua dari 13 jenis ikan
yang dibudidayakan. Permintaan ikan nila dalam setahun bisa mencapai
200.000 ton (Poernomo 2009).
Seiring perkembangan aktivitas dan kesibukan saat ini, makanan cepat saji
sangat diminati oleh masyarakat luas. Sosis merupakan bahan makanan yang
dikenal sejak 500 tahun sebelum masehi, terutama di kawasan jepang. Istilah
sausage (sosis) berasal dari bahasa latin salsus yang berarti digarami atau lebih
jelasnya pengawetan dengan garam. Sosis merupakan produk emulsi daging ikan
giling yang digarami, ditambah bahan pengisi dan minyak serta bumbu-bumbu,
bersifat kenyal dengan bentuk silinder berukuran seragam dengan menggunakan
pembungkus khusus (Price, 1986).
Sosis dibuat dikarenakan berbagai hal, yaitu melihat aktivitas masyarakat saat
ini yang begitu sibuk sehingga ingin mengkonsumsi makanan yang praktis. Sosis
merupakan makanan asing yang sudah akrab dalam kehidupan masyarakat
Indonesia karena rasanya enak. Namun, di balik kenikmatan makanan yang kaya
akan zat gizi ini, terkandung lemak dan kolesterol tinggi yang bisa mengganggu
hipertensi jika dikonsumsi berlebihan. Sosis yang terdapat di pasaran terbuat dari
daging sapi dan ayam yang memiliki kandungan lemak relatif tinggi
(Suratmo, 2008).
Untuk menanggulangi hal tersebut maka diupayakan membuat sosis yang
sehat dengan menggunakan daging olahan ikan. Ikan merupakan sumber protein
hewani dan juga memiliki kandungan gizi yang tinggi di antaranya mengandung
mineral, vitamin, dan lemak tak jenuh. Protein dibutuhkan tubuh untuk
pertumbuhan dan pengganti sel-sel tubuh kita yang telah rusak. Selain itu, protein
merupakan bagian utama dari susunan (komposisi) tubuh kita. Protein dalam ikan
berguna untuk mempercepat pertumbuhan badan (baik tinggi maupun berat),
meningkatkan daya tahan tubuh, mencerdaskan otak atau mempertajam pikiran
dan meningkatkan generasi/keturunan yang baik. Ikan memiliki kadar protein
yang tinggi yaitu sekitar 20 %. Di samping itu protein yang terkandung dalam
ikan mempunyai mutu yang baik, sebab sedikit mengandung kolesterol dan
sedikit lemak.
Oleh karena itu, upaya pengembangan produk olahan ikan perlu ditingkatkan,
melihat kegemaran masyarakat saat ini lebih menyukai makanan yang praktis.
Selain itu, juga meningkatkan daya terima masyarakat terhadap ikan nila merah
dan meningkatkan konsumsi masyarakat terhadap produk olahan perikanan
khususnya produk olahan ikan nila merah.
1.2 Tujuan
Tujuan dari penelitian ini antara lain mengembangkan diversifikasi produk
perikanan, khususnya ikan nila merah menjadi produk olahan berupa sosis ikan,
menentukan konsentrasi bahan emulsifier (ISP) yang menghasilkan sosis terbaik
(yang paling disukai panelis) dan menentukan karakteristik fisika dan kimia dari
2 TINJAUAN PUSTAKA
2.1 Deskripsi dan Klasifikasi Ikan Nila Merah
Ikan nila merah (Oreochromis sp) berasal dari Sungai Nil dan danau-danau
sekitarnya. Ikan ini diintroduksi dari Afrika untuk didatangkan ke Indonesia oleh
Balai Penelitian Perikanan Air Tawar (BPPAT) pada tahun 1969 dan menjadi ikan
peliharaan populer di kolam air tawar serta beberapa waduk di Indonesia. Nila
merah merupakan nama khas yang diberikan oleh Pemerintah melalui Direktorat
Jenderal Perikanan. Ikan nila merah potensial untuk dikembangkan karena
pertumbuhannya yang cepat, disukai masyarakat karena enak dagingnya. Ikan ini,
juga merupakan jenis ikan yang mempunyai nilai ekonomis tinggi dan merupakan
komoditas penting dalam bisnis ikan air tawar dunia (Suyanto, 1994).
Klasifikasi ikan nila (Anonim, 2008) adalah sebagai berikut :
Filum : Chordata
Sub-filum : Vertebrata
Kelas : Osteichtyes
Su-kelas : Acanthopterigii
Ordo : Perchomorphi
Famili : Cichilidae
Genus : Oreochromis
Spesies : Oreochromis sp
Gambar ikan nila dapat dilihat pada Gambar 1.
2.2 Surimi
Surimi merupakan produk antara atau produk intermediate yang terbuat dari
hasil pencucian daging ikan. Terdapat dua perbedaan antara surimi dan daging
lumat yaitu, kapasitas pembentukan gel untuk membentuk tekstur yang diinginkan
dan daya tahan dalam penyimpanan beku yang dapat ditambahkan gula sebagai
cryoprotectants (Sonu, 1986). Setelah menjadi daging lumat, daging lumat dicuci
dengan air tawar. Hal ini bertujuan untuk menghilangkan bahan-bahan yang larut
air seperti protein sarkoplasmik, enzim pencernaan, bahan organik low-molekuler
seperti trimetilamin oxide serta lemak dan darah untuk meningkatkan warna,
aroma serta meningkatkan kekuatan gel surimi (Toyoda, 1992). Surimi
merupakan bahan utama dari berbagai variasi pangan olahan seperti kamaboko,
chikuwa, satsumage, sosis ikan dan bola ikan (bakso), berkontribusi lebih 50%
dari total bahan produksi yang digunakan. Kualitas dari produk akhir bergantung
pada kualitas surimi yang digunakan. Gel merupakan karakteristik utama dari
produk berbasis surimi (Nopianti, 2011).
Proses pencucian merupakan tahapan yang penting dalam pembuatan surimi.
Frekuensi pencucian dapat memengaruhi kekuatan gel. Proses pencucian sangat
diperlukan dalam tahapan pembuatan surimi untuk mencegah protein miofibril
terdenaturasi selama penyimpanan beku. Efektifitas pencucian dapat ditentukan
oleh kandungan ion garam inorganik, protein larut air serta komponen non protein
yang hilang dari jaringan otot atau surimi tersebut (Matsumoto, 1992).
Pembentukan protein gel ada beberapa tipe atau macam yang dibentuk
oleh ikatan polipeptida. Pemanasan menyebabkan molekul saling tidak berikatan
dan interaksi antara intermolecular membentuk suatu matriks seperti gelasi.
Matriks ini mempunyai system yang cukup kompleks meliputi tipe-tipe protein,
lemak dan bahan-bahan lainnya seperti garam, nitrit, gula. Ada tiga tipe
multi-komponen gel yaitu, filled, mixed dan kompleks. Untuk filled gel, satu
makromolekul membentuk gel matriks ketika molekul lainnya berperan sebagai
pengisi pada ruang interstitial. Molekul yang sudah terisi dapat mempengaruhi
tekstur dan daya ikat air. Pada kompleks gel, matriks protein dapat dibentuk
akibat interaksi lebih dari satu komponen. Sebagai contoh, fibrinogen berinteraksi
ditambahkan pada daging olahan. Sedangkan mixed gels terbentuk akibat proses
gelasi dengan perbedaan fraksi dari protein daging atau penambahan gelling agent
(Foegeding, 1988).
2.3 Sosis
Sosis merupakan bahan makanan yang dikenal sejak 500 tahun sebelum
masehi, terutama di kawasan jepang. Istilah sausage (sosis) berasal dari bahasa
latin salsus yang berarti digarami atau lebih jelasnya pengawetan dengan garam.
Pembuatan sosis dimulani dengan proses yang sederhana yaitu proses
penggaraman dan pengeringan (Price, 1986). Berikut adalah cara pembuatan
sosis:
1) Bahan baku yang akan digunakan dalam pembuatan sosis harus dalam
keadaan segar dan mempunyai mutu yang baik. Selanjutnya dilakukan
penyiangan. Setelah itu daging dicuci bersih.
2) Daging ikan yang didapat kemudian digiling sehingga menghasilkan daging
lumat halus. Dengan menggunakan mixer, daging lumat tersebut dicampur
dengan bahan tambahan seperti tepung sebagai bahan pengisi dan minyak
sebagai fase diskontinyu yang melembutkan tekstur. Dapat juga ditambahkan
emulsifier seperti soy protein/lesitin atau protein yang lain serta bumbu yang
sudah disiapkan. Penambahan bumbu/bahan dilakukan berturut-turut dan
sedikit demi sedikit sampai adonan tercampur homogen.
3) Adonan yang sudah homogen dimasukkan kedalam stuffer, kemudian
dimasukkan kedalam casing/selongsong sosis serta diikat sesuai keinginan.
4) Selanjutnya dimasak dengan air pada suhu 400-50 0C selama 20 menit
kemudian perebusan dilanjutkan dengan suhu 800-90 0C sampai matang
selama 30 menit.
5) Sosis yang sudah matang digunting dari ikatan benangnya, kemudian
disimpan dalam tempat yang dingin.
Sosis dibagi atas enam kategori berdasarkan atas metode pembuatannya
yaitu, sosis segar, sosis asap tidak dimasak, sosis asap dimasak, sosis masak, sosis
tidak dimasak tetapi diasap dan bola daging (Price, 1986). Berikut adalah
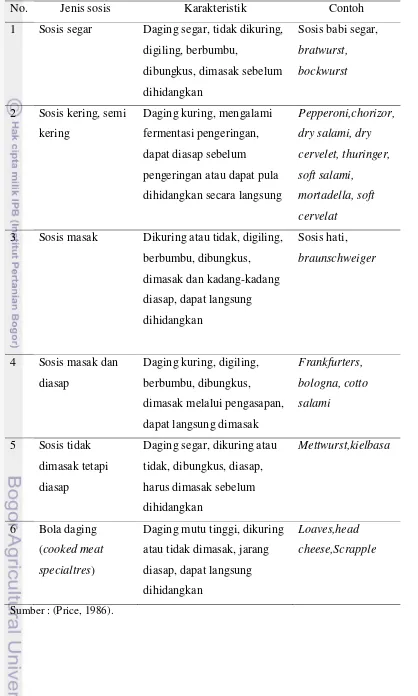
Tabel 1 Jenis-jenis sosis
No. Jenis sosis Karakteristik Contoh
1 Sosis segar Daging segar, tidak dikuring,
digiling, berbumbu,
3 Sosis masak Dikuring atau tidak, digiling,
2.4 Bahan Pembantu
Bahan pembantu adalah bahan yang sengaja ditambahkan dengan maksud
tertentu, misalnya untuk meningkatkan konsistensi, nilai gizi, citarasa untuk
mengendalikan keasaman, kebasaan, memantapkan bentuk dan rupa. Bahan
pembantu yang digunakan adalah bahan pengisi, bahan pengikat, lemak dan bahan
tambahan lainnya.
2.4.1 Bahan pengisi dan pengikat
Bahan pengisi yang umum digunakan dalam sosis adalah tepung,
biji-bijian dan pati yang diekstraksi dari tepung-tepungan, salah satunya tepung
tapioka. Pati terdiri dari dua fraksi yang dapat dipisahkan dengan air panas. Fraksi
terlarut disebut amilosa dan fraksi tidak terlarut disebut amilopektin. Fraksi
amilopektin bertanggung jawab atas keteguhan gel. Perbandingan kandungan
antara amilosa dan amilopektin berperan dalam produk olahan. Semakin besar
kandungan amilopektin atau semakin kecil kandungan amilosa bahan yang
digunakan maka semakin lekat produk olahannya (Winarno, 1997).
Tepung tapioka atau tepung kanji adalah tepung yang terbuat dari ubi kayu
atau singkong. Pembuatan dilakukan dengan cara diparut, diperas, dicuci,
diendapkan, diambil sari patinya, lalu dijemur/keringkan. Sifat tepung kanji,
apabila dicampur dengan air panas akan menjadi liat/seperti lem. Tepung tapioka
disebut juga tepung kanji atau tepung sagu (sagu singkong). Tepung tapioka akan
memiliki perlakuan berbeda untuk setiap jenis kue karena sifat yang dimiliki
tepung tersebut. Adapun sifat fisikimia pati tapioka adalah sebagai berikut, rasio
amilosa dan amilopektin adalah 17% amilosa dan 83% amilopektin, bentuk
granula semi bulat dengan salah satu bagian ujungnya mengerucut, ukuran
5-35 µm, suhu gelatinisasi berkisar antara 52-64 oC, kristalisasi 38%, kekuatan
pembengkakan sebesar 42 µm, kelarutan 31% (Nita, 2011).
2.4.2 Lemak
Sumber-sumber lemak dan minyak dapat dibagi menjadi dua bagian yaitu
sumber dari tumbuh-tumbuhan yang meliputi biji-bijian dari tanaman tahunan
seperti kedelai, biji kapas, kacang tanah, rape seed dan bunga matahari serta
zaitun dan minyak kelapa. Sumber lainnya adalah sumber hewani meliputi babi,
sapi, sardine, ikan herring (Buckle et al. 1978).
Perbedaan utama antara lemak nabati dan lemak hewani adalah kandungan
sterolnya, dimana lemak nabati mengandung fitosterol dan lebih banyak
mengandung asam lemak tak jenuh sehingga umumnya berbentuk cair
sedangkan lemak hewani mengandung kolesterol (Winarno, 1997).
Lemak dan minyak adalah bahan-bahan yang tidak larut dalam air yang
berasal dari tumbuh-tumbuhan dan hewan. Lemak dan minyak yang digunakan
dalam makanan sebagian besar adalah trigliserida merupakan ester dari gliserol
dan berbagai asam lemak. Komponen-komponen lain yang mungkin terdapat,
meliputi fosfolipid, sterol, vitamin dan zat warna yang larut dalam lemak seperti
klorofil dan karotenoid. Peran daripada lemak dalam makanan manusia dapat
merupakan zat gizi yang menyediakan nafsu makan atau dapat membantu
memperbaiki tekstur dari bahan yang diolah. Istilah lemak biasanya digunakan
untuk campuran trigliserida yang berbentuk padat pada suhu ruangan sedangkan
minyak berarti campuran trigliserida cair pada suhu ruangan
(Buckle et al. 1978).
2.5 Bahan Tambahan
Bahan tambahan lain yang digunakan dalam penelitian pembuatan sosis ikan
ini antara lain garam, jahe, gula, air, lada putih, bawang putih, bawang merah,
ISP.
2.5.1 Air
Air merupakan suatu kebutuhan yang tak dapat ditinggalkan dalam proses
pembuatan pangan. Dalam pengolahan dibutuhkan air yang bermutu lebih tinggi
dibandingkan dengan kebutuhan air minum untuk meminimalisir kontaminan
dan semua bahan-bahan di dalam air yang mungkin dapat mempengaruhi
penampakan, rasa dan stabilitas hasil akhir, penyesuaian pH pada tingkat yang
diinginkan, dan mutu air yang konsisten (Buckle et al. 1978).
2.5.2 Gula
Pemberian gula akan mempengaruhi citarasa yaitu meningkatkan rasa
menetralisir garam yang berlebihan serta penambahan energi. Selain itu, gula
juga memiliki daya larut yang sangat tinggi, kemampuan mengurangi
keseimbangan kelembaban relatif (ERH) dan meningkatkan air sehingga dapat
berfungsi sebagai pengawet. Adanya glukosa, sukrosa, pati dan lain-lain dapat
meningkatkan citarasa pada makanan. Penambahan gula akan juga akan
mempengaruhi pelepasan gas karena lepasnya gas CO2 dalam
gelembung-gelembung besar (Buckle et al. 1978).
2.5.3 Garam
Garam merupakan bumbu yang biasanya ditambahkan pada pembuatan
suatu produk. Pemakaian garam NaCl biasanya lebih banyak diatur oleh rasa,
kebiasaan, dan tradisi daripada keperluan. Makanan yang mengandung garam
kurang dari 0,3% akan terasa hambar sehingga kurang disenangi
(Winarno, 1997). Selain itu, garam juga berfungsi sebagai pengawet karena
garam berperan sebagai penghambat selektif terhadap mikroorganisme pencemar
tertentu. Garam mempengaruhi aktifitas air (Aw) dari bahan, sehingga dapat
mengendalikan pertumbuhan mikroorganisme dengan suatu metode yang bebas
dari pengaruh racunnya. Penambahan garam akan menyebabkan kondisi
anaerobic yang terbentuk (Buckle et al. 1978).
2.5.4 Lada putih
Lada atau merica merupakan rempah-rempah yang sering digunakan
dalam pengolahan makanan. Lada sering ditambahkan pada saat memasak ikan
atau daging. Lada mempunyai peranan dalam dehidrasi sehingga dapat berfungsi
sebagai penghambat pertumbuhan mikroba dalam bahan pangan. Lada sangat
digemari karena memiliki dua sifat penting yaitu rasanya yang pedas dan
aromanya yang khas. Kedua sifat tersebut disebabkan kandungan bahan-bahan
kimia organik yang terdapat pada lada. Rasa pedas lada disebabkan oleh adanya
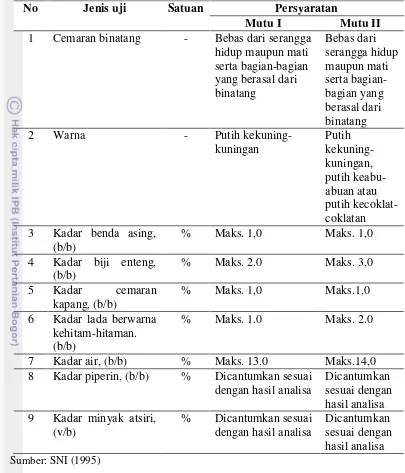
zat piperin dan piperanin serta hapisin. Persyaratan mutu lada putih menurut
Tabel 2 Spesifikasi persyaratan mutu lada putih
Sumber: SNI (1995)
2.5.5 Bawang putih (Allium sativum)
Bawang putih berfungsi sebagai penambah aroma dan untuk meningkatkan
citarasa produk yang dihasilkan. Bawang putih mengandung senyawa allisin,
yang dapat menentukan bau khas bawang putih. Bawang putih juga mengandung
beberapa vitamin seperti thiamin, niasin, riboflavin, asam askorbat, vitamin B, vitamin C. Namun mengandung β-karoten yang merupakan bentuk vitamin A dalam jumlah yang sedikit (Wibowo, 1999).
No Jenis uji Satuan Persyaratan
2.5.6 Bawang merah (Allium ascalonicum L.)
Bawang merah umumnya digunakan sebagai bumbu masak. Bawang
merah memiliki kandungan kimia sebagian besar terdiri dari air sekitar 80-85%,
protein sebesar 1,5%, lemak sebesar 0,3% dan karbohidrat sebesar 9,2%. Selain
itu, umbi bawang merah juga terdapat suatu senyawa yang mengandung ikatan
asam amino yang tidak berbau, tidak berwarna dan dapat larut dalam air. Ikatan
asam amino ini disebut dengan allin yang karena sesuatu hal berubah menjadi
allicin (Wibowo, 1999).
2.5.7 Jahe (Zingiber officinale)
Jahe dapat digunakan sebagai sebagai bumbu masak, pemberi aroma
berbagai makanan dan minuman serta bahan obat-obatan tradisional. dan aneka
keperluan lainnya. Kegunaan jahe antara lain dapat merangsang kelenjar
pencernaan, baik untuk membangkitkan nafsu makan dan pencernaan. Sifat khas
jahe disebabkan terdapatnya kandungan minyak atsiri dan oleoresin jahe.
Minyak atsiri menyebabkan aroma harum jahe, sedangkan oleoresin
menyebabkan rasa pedas. Kandungan minyak atsiri dalam jahe kering sekitar
1-3%. Komponen utama minyak atsiri jahe yang menyebabkan bau harum
adalah zingiberen dan zingiberol. Oleoresin jahe banyak mengandung komponen
pembentuk rasa pedas yang tidak menguap. Komponen dalam oleoresin jahe
terdiri atas gingerol dan zingiberen, shagaol, minyak atsiri dan resin. Pemberi
rasa pedas dalam jahe yang utama adalah zingerol. Bagian tumbuhan jahe yang
digunakan adalah rimpang. Kandungan kimia dari rimpang jahe yaitu minyak
atsiri yang terdiri dari senyawa-senyawa seskuiterpen, zingiberen, zingeron, oleoresin, kamfena, limonen, borneol, sineol, sitral, zingiberal, felandren.
Disamping itu terdapat juga pati, damar, asam-asam organik seperti asam malat
dan asam oksalat, Vitamin A, B, dan C, serta senyawa flavonoid dan polifenol
(Matondang, 2008).
2.6 Emulsi
Emulsi adalah suatu disperse atau suspense cairan dalam cairan yang lain
dengan molekul-molekul kedua cairan tersebut tidak saling berbaur tetapi saling
antagonistik. Pada suatu emulsi terdapat tiga bagian utama, yaitu bagian yang
fase diskontinu, bagian kedua disebut media pendispersi dikenal sebagai fase
kontinu yang biasanya terdiri dari air dan bagian ketiga adalah emulsifier yang
berfungsi menjaga agar butir minyak tadi tetap tersuspensi di dalam air. Senyawa
ini molekulnya mempunyai afinitas terhadap kedua cairan tersebut
(Winarno, 1997).
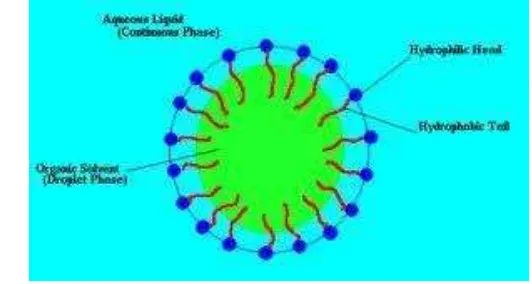
Pada perkembangannya memang diketahui bahwa sosis merupakan emulsi
minyak dalam air (o/w). Dalam emulsi sosis, lemak atau minyak berperan sebagai
fase diskontinyu sedangkan air berperan sebagai fase kontinyu dan protein sebagai
emulsifier. Kriteria terpenting dalam pembuatan sosis adalah kestabilan emulsi.
Suatu emulsi dikatakan stabil apabila partikel-partikel yang terdispersi tidak atau
sedikit mempunyai kecenderungan untuk bersatu lagi sehingga terbentuk lapisan
yang terpisah (Wilson, 1981).
Daya kerja emulsifier terutama disebabkan oleh bentuk molekulnya yang
dapat terikat baik pada minyak maupun air. Bila emulsifier tersebut lebih terikat
pada air atau lebih larut dalam air maka dapat lebih membantu terjadinya disperse
minyak dalam air. Sebaliknya bila emulsifier lebih larut dalam minyak terjadilah
emulsi air dalam minyak. Cara kerja dari emulsifier yakni bila butir-butir lemak
telah terpisah karena adanya tenaga mekanik (pengocokan), maka butir-butir
lemak yang terdispersi tersebut segera terselubungi oleh selaput tipis emulsifier.
Bagian molekul emulsifier yang non polar larut dalam lapisan luar butir-butir
lemak sedangkan bagian yang polar menghadap kepelarutan (air)
(Winarno, 1997). Berikut adalah gambar emulsi minyak dalam air dapat dilihat
pada Gambar 2.
Partikel lemak biasanya berukuran subselular yang tersuspensi dalam protein.
Hal ini dapat terjadi karena adanya ikatan hidrophilik yang saling berikatan dalam
air dan ikatan lipophilik yang saling berikatan dalam lemak. Protein sarkoplasma
dan myofibril dapat membentuk emulsifikasi. Protein myofibril akan lebih dahulu
diserap ke dalam permukaan lemak atau air. Protein myofibril, myosin, akan
terpisah dari aktin di dalam protein yang siap untuk diserap. Ketika protein
myofibril terlibat dalam proses emulsifikasi, protein tersebut akan kehilangan
kemampuan untuk mengikat air. Ketika partikel lemak tersebut diselubungi oleh
protein maka emulsi tersebut sudah terbentuk, emulsi ini akan stabil ketika terjadi
denaturasi protein pada saat pemasakan. Protein myofibril akan membentuk gel
yang kompak sedangkan protein sarkoplasmik akan membentuk gel yang lemah.
Oleh karena itu, protein sarkoplasmik tidak berkontribusi dalam kestabilan produk
(Price, 1986).
Protein myofibril berfungsi untuk mengikat air dalam pembesaran struktur
protein. Kemampuan mengikat air akan meningkat dengan meningkatnya jumlah
muatan negative seperti meningkatnya pH di bawah titik isoelektik. Penambahan
garam dan alkali phosphates akan meningkatkan pembesaran struktur protein.
Gerakan mekanikal selama meningkatnya pembesaran struktur protein akan
membantu ekstraksi protein terlarut yang membentuk permukaan lemak.
Pembesaran dan eksrtraksi protein akan lebih efektif pada temperature dingin
sekitar 30C (Rust, 1986).
Salah satu bahan pengemulsi adalah isolat soy protein (ISP) atau isolat
protein kedelai adalah produk dari protein kedelai bebas lemak atau berlemak
rendah yang diolah sedemikian rupa sehingga kandunan proteinnya tinggi.
Menurut definisinya, kandungan protein pada isolat protein kedelai minimum 95
%. Isolat protein kedelai sangat dibutuhkan dalam industi pangan, karena banyak
sekali digunakan untuk formulasi berbagai jenis makanan. Yang diinginkan dari
isolat protein kedelai adalah sifat fungsional proteinnya. Sifat ini menentukan
pemakaian atau fungsi produk tersebut dalam biaya, nutrisi dan proses. Isolat
soy protein memberikan emulsifikasi dan viskositas yang tinggi serta stabil pada
konsentrasi garam yang tinggi dalam proses brining. Selain itu, isolat soy
pengikat lemak dan air, menstabilkan emulsi dan menjaga struktur protein pada
masakan daging isolat soy protein mengandung pengikat air dan lemak sebagai
pembentuk tekstur produk emulsi (Young, 1980).
Struktur isolat soy protein mengandung sedikitnya 80% protein yang
terdiri dari globulin, conglycinin dan glycinin. Conglycinin merupakan kuartener
trimerik glycoprotein dengan berat molekuler 141 sampai 171 kdaltons, tersusun
dari tiga subunit yang terikat oleh interaksi hydrophobic. Conglycin memiliki
dua rangkaian intramolekular disulfide dan mengandung 5% karbohidrat.
Dengan demikian, conglycinin mengandung amphiphilik untuk membentuk
aktivitas permukaan dan ikatan rasa yang baik. Glicinin terdiri dari dua unit,
6-hydrophobical yang berasosiasi dengan bagian rantai acidic disulfide dan
subunit dasar. Amidasi dari jumlah residu aspartic dan glutamic untuk tingkat
kelarutan alkali dari subunits dasar. Subunit acidic mempunyai rata-rata satu
sampai tiga ikatan disulfide pel mole dan lebih stabil terhadap panas daripada
subunit dasar serta mempunyai satu sampai dua residu cystein. Glicinin
mengandung dua unsur, gugus thiol bebas yang terdapat pada permukaan dan
dapat dilibatkan dalam pertukaran thiol-disulfida. Contohnya, dalam gelatin
formasi dari intermolekuler-disulfida menghasilkan ikatan yang meningkat, tapi
menyebabkan polimerisasi dan mengurangi kemampuan ekstraksi dan kelarutan
(Kinsella, 1979).
2.7 Selongsong
Selongsong (casing) merupakan pembungkus yang digunakan untuk
membungkus dan membentuk sosis. Terdapat tiga jenis selongsong (casing) yang
sering digunakan dalam pembuatan sosis, yaitu alami, kolagen, serta selulosa.
Selongsong alami biasanya terbuat dari usus alami hewan. Casing ini mempunyai
keuntungan dapat dimakan, bergizi tinggi, dan melekat pada produk. Kerugian
penggunaan casing ini adalah produk tidak awet, contohnya adalah casing usus
sapi ataupun usus kerbau. Casing kolagen biasanya dibuat dari regenerasi lapisan
corium kulit jangat daging sapi. Keuntungan dari penggunaan selongsong ini
adalah dapat diwarnai, bisa dimakan, dan melekat pada produk. Casing selulosa
biasanya berbahan baku pulp. Keuntungan casing selulosa adalah dapat dicetak
dimakan. Saat ini telah dikembangkan polyamid casing, yaitu selongsong yang
terbuat dari plastik. Casing jenis ini tidak bisa dimakan, dapat dibuat berpori atau
tidak, bentuk dan ukurannya dapat diatur, tahan terhadap panas, dan dapat dicetak
(Astawan, 2008).
Selongsong diperlukan sebagai wadah pembentuk sosis dan menentukan
bentuk serta ukuran sosis yang diperlukan. Selongsong atau casing yang
digunakan dalam pembuatan sosis ada beberapa macam, yaitu selongsong alami
dan selongsong artificial atau buatan. Selongsong alami dibuat dari kolagen.
Selongsong alami dibuat dari saluran pencernaan hewan antara lain, sapi, domba
atau kambing. Selongsong alami mudah mengalami kerusakan sehingga
penyimpanan dilakukan dalam perendaman air garam dan direndam selama sehari
penuh dalam refrigerator. Hal ini menyebabkan selongsong lebih lembut dan
mudah untuk diisi. Setelah pengisian, selongsong sebaiknya dikemas dengan air
garam dan disimpan. Selongsong buatan terdiri dari selongsong kolagen, plastik
atau selulosa dan sintetik fibrosa. Selongsong kolagen bersifat alami, dapat
dimakan dan memiliki kekuatan elastisitas yang lebih besar. Penggunaan
selongsong kolagen digunakan untuk meningkatkan pendapatan dan produksi
dalam waktu yang lebih singkat. Selongsong plastik atau selulosa mempunyai
elastisitas yang kuat tetapi tidak dapat dimakan. Selongsong sintetik mempunyai
kekuatan elastisitas tinggi dan cukup mahal. Selongsong ini dapat diisi tanpa
3.1 Waktu dan Tempat
Penelitian ini dilaksanakan pada bulan Juli 2011 sampai Agustus 2011
bertempat di Laboratorium Preservasi dan Pengolahan Hasil Perairan,
Laboratorium Biokimia Hasil Perairan, Departemen Teknologi Hasil Perairan,
Fakultas Perikanan dan Ilmu Kelautan, Laboratorium Pengolahan Pangan dan
Laboratorium PAU (Pusat Antar Universitas), Departemen Ilmu dan Teknologi
Pangan, Fakultas Teknologi Pertanian, Laboratorium Biokimia, Departemen
Biokimia, Fakultas Metematika dan Ilmu Pengetahuan Alam, Institut Pertanian
Bogor.
3.2 Alat dan Bahan
Alat yang digunakan dalam penelitian ini antara lain pisau, talenan, baskom,
kain blacu, termometer, mortar, timbangan digital, food processor, grinder,
stuffer, cawan porselen, oven, desikator, tabung reaksi, gelas erlenmeyer, tabung
Kjeldahl, destilator, tabung sokhlet, pemanas, tanur, sentrifuse dingin, syringe,
selongsong lemak, labu lemak dan kondensor, homogenizer, pipet, autoclave,
texture analyzer, kertas Whatman no.1.
Bahan yang digunakan meliputi ikan nila merah (Oreochromis sp) yang
didapatkan dari kolam Budidaya Perairan Darmaga dengan ukuran size 4 dan
harga RP. 16.000/kg, gula, garam, bawang merah, bawang putih, lada putih,
lemak sapi, air es, jahe, STPP 0,25%; H2SO4 pekat, NaOH 40%, N2S2O3 5%,
asam borat (H3BO3) 4%, HCL 0,02 N.
3.3 Metode Penelitian
Tahapan penelitian yang digunakan yaitu metode eksperimental. Metode
eksperimental adalah salah satu metode yang paling tepat untuk menyelidiki
hubungan sebab akibat variabel yang digunakan. Penelitian ini dilakukan dengan
3.3.1 Penelitian pembuatan gel ikan nila merah
Tujuan penelitian pendahuluan untuk mendapatkan kekuatan gel yang
terbaik pada surimi ikan nila merah. Perlakuan pada penelitian pendahuluan yaitu
banyaknya pencucian daging lumat yang dilakukan (1 kali, 2 kali, dan 3 kali)
dengan penambahan cryoprotectant berupa STPP 0,25% untuk tiap perlakuan.
Analisis yang dilakukan untuk mengetahui hasil terbaik yaitu dengan pengujian
uji lipat, uji gigit, protein larut garam dan kekuatan gel. Selanjutnya akan
dianalisis lebih lanjut pada penelitian utama.
Prosedur penelitian pendahuluan sebagai berikut, pertama-tama ikan nila
merah disiangi dengan menghilangkan sisiknya dan dicuci bersih. Selanjutnya
ikan di-fillet untuk mendapatkan slice daging yang diteruskan dengan skinless
atau penghilangan kulit. Daging fillet yang didapatkan selanjutnya digiling dengan
menggunakan meat grinder. Untuk mendapatkan surimi, daging lumat dicuci
dengan air es dengan perbandingan daging lumat dan air es, 1 : 3. Frekuensi
pencucian adalah sebanyak 1 kali, 2 kali dan 3 kali sebagai perlakuan
pendahuluan. Selanjutnya setiap perlakuan pencucian ditambahkan cryoprotectant
berupa STPP 0,25% dari bobot daging dan dilanjutkan dengan pencampuran
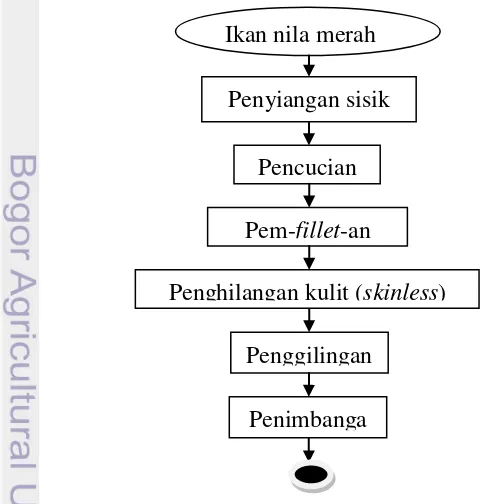
menggunakan food processor dan didapatkan surimi yang siap diuji. Diagram alir
penelitian pendahuluan berupa pembuatan gel ikan nila merah dapat dilihat pada
Gambar 3.
Ikan nila merah
Pem-fillet-an Penyiangan sisik
Penggilingan Pencucian
Penghilangan kulit (skinless)
Gambar 3 Diagram alir penelitian pembuatan gel ikan nila merah (Oreochromis sp).
Pencucian 1 kali, 2 kali dan 3 kali dengan air es.
Perbandingan air es dan daging : 3 : 1 ± 10 menit
Penambahan
cryoprotectant 0,25%
Surimi Uji Protein Larut
Pencampuran sampai
homogen
Penambahan garam
Pencampuran sampai
homogen
Pemasukan dalam
cetakan gel
Perebusan dengan suhu 400-50 0C selama 20 menit dilanjutkan suhu 800-90 0C selama 30
menit
Penirisan dan pendinginan
Gel ikan nila merah
Uji Lipat
Uji Gigit
3.3.2 Penelitian pembuatan sosis ikan nila merah
Tujuan penelitian utama adalah menentukan konsentrasi bahan pengemulsi
(ISP) yang menghasilkan sosis terbaik (yang paling disukai panelis) dan
menentukan karakteristik fisika dan kimia dari sosis ikan nila merah. Hasil
pencucian daging lumat yang menghasilkan karakteristik surimi terbaik
ditambahkan ISP dengan konsentrasi yang berbeda, yaitu konsentrasi ISP 10%,
13%, 16% dan 19%. Prosedur penelitiannya adalah pertama-tama ikan nila merah
disiangi dengan menghilangkan sisiknya dan dicuci bersih. Selanjutnya ikan
di-fillet untuk mendapatkan slice daging yang diteruskan dengan skinless atau
penghilangan kulit. Daging fillet yang didapatkan selanjutnya digiling dengan
menggunakan meat grinder. Untuk mendapatkan surimi, daging lumat tersebut
dicuci dengan air es dengan perbandingan daging lumat dan air es, 1 : 3 selama
10 menit. Frekuensi pencucian menggunakan perlakuan pencucian terbaik dalam
penelitian pendahuluan Selanjutnya ditambahkan cryoprotectant berupa STPP
0,25% dari bobot daging dan dilanjutkan dengan pencampuran menggunakan food
processor dan didapatkan surimi.
Dilanjutkan dengan pencampuran bumbu-bumbu seperti gula halus,
garam, bawang merah, bawang putih, lada, jahe, tepung tapioka, lemak sapi dan
ISP sebagai perlakuan. Bahan-bahan diadon dan dimasukkan dalam stuffer untuk
dicetak. Selanjutnya, adonan yang telah dicetak direbus dengan suhu 400-50 0C
selama 20 menit dan dilanjutkan dengan perebusan kedua dengan suhu 800-90 0C
selama 30 menit. Sosis yang sudah masak selanjutnya didinginkan dan ditiriskan.
Sosis ikan nila merah siap untuk diuji.
Selanjutnya dilakukan analisis fisik untuk menentukan konsentrasi ISP
(Isolat Soy Protein) terbaik yaitu dengan pengujian sensori (warna, rasa, aroma,
tekstur, penampakan), uji lipat dan uji gigit. Selain itu, dilakukan pula analisis
kimia untuk mengetahui proksimat dari sosis ikan terbaik yang dihasilkan
meliputi kadar air, kadar abu, protein, lemak dan karbohidrat serta uji emulsi,
WHC dan kekuatan gel. Diagram alir pembuatan sosis ikan pada penelitian utama
Gambar 4 Diagram alir penelitian pembuatan sosis ikan nila merah (Oreochromis sp).
Pencampuran Ikan nila
Penyianga
Pe-fillet-an dan skinless
Penggilingan
3.4 Prosedur Analisis
Teknik pengujian ada dua cara, yaitu secara subyektif dan secara obyektif.
Analisis obyektif yang dilakukan meliputi analisis kimia dan analisis fisik.
Analisis kimia meliputi analisis proksimat dilakukan untuk sosis daging ayam
(pembanding), sosis nila merah dengan hasil penerimaan panelis terbaik yang
dihasilkan meliputi kadar air, kadar abu, kadar lemak, kadar protein, dan kadar
karbohidrat. Sedangkan analisis secara subyektif dengan cara uji organoleptik.
3.4.1 Rendemen
Rendemen dihitung sebagai persentasi bobot bagian tubuh ikan nila dari
bobot awal. Adapun perumusan matematik adalah sebagai berikut:
Rendemen daging (%) = bobot daging x 100%
bobot total
3.4.2 Uji organoleptik (Rahayu 1998)
Uji organoleptik yang dilakukan adalah uji kesukaan, panelis diminta
untuk memberikan tanggapan tentang tingkat kesukaan atau ketidaksukaan.
Tingkatan-tingkatannya disebut skala hedonik, dalam analisisnya
ditransformasikan menjadi skala numerik dengan angka menaik menurut tingkat
kesukaannya. Dalam penelitian ini digunakan sembilan skala hedonik yang
menunjukkan tingkat kesukaan. Pelaksanaan uji dilakukan dengan uji
perbandingan berpasangan yaitu dengan cara menyajikan sosis ikan yang
dihasilkan dengan sosis daging yang komersial dengan pemberian kode
(menggunakan bilangan acak) dan panelis diminta untuk memberikan penilaian
pada score sheet yang telah disediakan. Panelis yang dibutuhkan sebanyak 30
panelis semi terlatih. Parameter uji meliputi rasa, warna, aroma, tekstur dan daya
oles. Parameter rasa dinilai pada saat memakan sosis. Parameter warna dan aroma
dinilai dengan melihat dan mencium aroma sosis. Parameter tekstur dinilai dengan
perabaan oleh lidah pada saat selai dimakan, dan uji lipat dilakukan dengan
melipat sosis dan diamati kondisinya.
3.4.3 Daya mengikat air (DMA) (Hamm 1972 diacu dalam Wahyuni 1992)
Daya ikat air dapat diukur dengan menggunakan alat carverpress. Sampel
yaitu diantara dua plat jepitan berkekuatan 35 kg/cm2 selama 5 menit. Kertas
saring yang digunakan yaitu Whatman 1 no 40. Luas area basah yaitu luas air
yang diserap kertas saring akibat penjepitan, dengan kata lain selisih luas antara
lingkaran luar dan dalam kertas saring. Bobot air bebas (jumlah air dalam sosis
yang terlepas) dapat dihitung dengan rumus sebagai berikut:
Berat air : Luas area basah 8,0
0,0948
3.4.4 Kekuatan gel (White dan Englar diacu dalam Alpis 2002)
Kekuatan gel dapat diukur dengan alat Reoner RE-3305 dengan luatan
amatan 400 x 0,01 mm; sensitifitas 0,5 v; kecepatan putar mesin 0,5 mm/s dan
kecepatan mencetak grafik 40 mm/min. Kekuatan gel memiliki satuan gramforce
(gf). Nilai konversi yang digunakan sebesar 25 gf.
3.4.5 Analisis protein larut garam (PLG) (Wahyuni 1992)
Sampel sebanyak 5 gram ditambahkan 50 ml larutan NaCl 5% kemudian
dihomogenkan dengan waring blender selama 2-3 menit, suhu dijaga agar tetap
rendah (5-8 0C). Setelah itu disentrifugasi pada 3400 x G selama 30 menit dengan
suhu 10 0C. Selanjutnya disaring menggunakan kertas saring Whatman no.1.
Filtrat ditampung dalam erlenmeyer dan disimpan pada suhu 4 0C. sebanyak 1 ml
filtrat dianalisis kandungan proteinnya dengan menggunakan metode mikro
Kjeldahl.
Kadar PLG (%) =
Keterangan:
A = Volume titrasi HCl sampel (ml) B = Volume titrasi HCl blanko (ml) fp = faktor pengenceran
3.4.6 Uji lipat dan uji gigit (Shaviklo 2006)
Pengujian ini dilakukan untuk mengetahui tingkat elastisitas sosis. Uji
Lipat dan uji gigit dapat dilakukan dengan tangan dan gigitan menggunakan gigi
depan. Uji lipat dilakukan dengan melipat contoh irisan dengan tebal ± 5 mm
secara perlahan sampai terlihat retakan-retakan. Hasil irisan tersebut dilipat
dengan tangan, diantara ibu jari dan telunjuk, kemudian dilipat untuk diamati
sheet yang telah disediakan. Uji gigit dapat dilakukan dengan menggigit contoh
dengan gigi depan untuk mengevaluasi elastisitas contoh. Hasil pengamatan pada
bagian gigitan dikonversikan dengan score sheet yang telah disediakan.
3.4.7 Uji emulsi ( Sathe dan Salunkhe 1981 diacu dalam Wahyuni 1992)
Uji emulsi ini dilakukan untuk mengetahui aktivitas dan stabilitas panas
emulsi. Sampel sebanyak 10 gram disuspensikan ke dalam 50 ml air. Tambahkan
minyak, aduk-aduk di dalam ruang waring blender berkecepatan tinggi selama 2
menit. Emulsi dituangkan ke dalam tabung-tabung sentrifuse. Kemudian tabung
sentrifuse ditempatkan dalam penangas air 25 °C selama 30 menit, sebelum
disentrifus. Selanjutnya tabung-tabung sentrifuse selama 20 menit dengan
kecepatan 145 rpm. Stabilitas emulsi dilakukan dengan cara suspense yang telah
diaduk dalam waring blender (seperti pada pengukuran aktivitas emulsi)
dituangkan ke dalam dua tabung sentrifuse. Emulsi tersebut dipanaskan pada suhu
80 °C selama 30 menit, lalu didinginkan dalam penangas air 25 °C, sebelum
disentrifus. Sentrifus dilakukan selama 30 menit. Aktifitas emulsi dinyatakan
dalam %. Stabilitas emulsi dinyatakan dalam % campuran emulsi setelah
pemanasan.
3.4.8 Analisis proksimat
Analisis proksimat yang dilakukan terhadap ikan patin meliputi: kadar air,
abu, protein dan lemak.
1) Analisis kadar air (AOAC 1995)
Tahap pertama yang dilakukan untuk menganalisis kadar air adalah
mengeringkan cawan porselen dalam oven pada suhu 1020-105 0C selama
30 menit. Cawan tersebut diletakkan ke dalam desikator (kurang lebih 30 menit)
hingga dingin dan ditimbang hingga beratnya konstan. Kemudian cawan dan
sampel seberat 1-2 gram ditimbang setelah terlebih dahulu dihomogenkan. Cawan
dimasukkan ke dalam oven dengan suhu 1020-105 0C selama 6 jam. Cawan
tersebut dimasukkan ke dalam desikator dan dibiarkan hingga dingin kemudian
ditimbang.
Perhitungan kadar air:
Keterangan: A = Berat cawan kosong (gram)
B = Berat cawan dengan sampel (gram)
C = Berat cawan dengan sampel setelah dikeringkan (gram)
2) Analisis kadar abu (AOAC 1995)
Tahap yang dilakuakan adalah cawan abu porselen dikeringkan di dalam
oven selama 30 menit dengan suhu 105 0C, lalu didinginkan dalam desikator
kemudian ditimbang. Sampel sebanyak 1-2 gram yang telah dihomomogenkan
dimasukkan ke dalam cawan abu porselen. Cawan abu porselen dipijarkan dalam
tungku pengabuan bersuhu sekitar 105 0C sampai tidak berasap. Selanjutnya
cawan tersebut dimasukkan ke dalam tanur pada suhu 600 0C selama 2-3 jam.
Proses pengabuan dilakukan sampai abu berwarna putih. Setelah itu cawan abu
porselen didinginkan dalam desikator selama 30 menit, kemudian ditimbang
beratnya.
Perhitungan kadar abu:
% Kadar abu: x 100%
Keterangan: A = Berat cawan abu porselen kosong (gram)
B = Berat cawan abu porselen dengan sampel (gram)
C = Berat cawan abu porselen dengan sampel setelah dikeringkan
(gram)
3) Analisis kadar protein (AOAC 1995)
Prinsip dari analisis protein, yaitu untuk mengetahui kandungan protein
kasar (crude protein) pada suatu bahan. Tahap-tahap yang dilakukan dalam
analisis protein terdiri dari tiga tahap, yaitu destruksi, destilasi dan titrasi.
(1) Tahap destruksi
Sampel ditimbang seberat 0,5 gram, kemudian dimasukkan ke dalam
tabung Kjeltec. Satu butir Kjeltab dimasukkan ke dalam tabung tersebut dan
ditambahkan 10 ml H2SO4. Tabung yang berisi larutan tersebut dimasukkan ke
dalam alat pemanas dengan suhu 410 0C ditambahkan 10 ml air. Proses destruksi
(2) Tahap destilasi
Isi labu dituangkan ke dalam labu destilasi, lalu ditambahkan dengan
aquades (50 ml). Air bilasan juga dimasukkan ke dalam alat destilasi dan
ditambahkan larutan NaOH 40% sebanyak 20 ml.
Cairan dalam ujung tabung kondensor ditampung dalam erlenmeyer 125
ml berisi larutan H3BO3 dan 3 tetes indikator (cairan methyl red dan brom cresol
green) yang ada di bawah kondensor. Destilasi dilakukan sampai diperolah 200
ml destilat yang bercampur dengan H3BO3 dan indikator dalam erlenmeyer.
Perhitungan jumlah nitrogen dalam bahan:
% Nitrogen = x 100%
% Kadar protein = % Nitrogen x faktor konversi (6,25)
4) Analisis kadar lemak (AOAC 1995)
Sampel seberat 2 gram (W1) dimasukkan ke dalam kertas saring dan
dimasukkan ke dalam selongsong lemak, kemudian dimasukkan ke dalam labu
lemak yang sudah ditimbang berat tetapnya (W2) dan disambungkan dengan
tabung soxhlet. Selongsong lemak dimasukkan ke dalam ruang ekstraktor tabung
soxhlet dan disiram dengan pelarut lemak. Tabung ekstraksi dipasang pada alat
destilasi soxhlet, lalu dipanaskan pada suhu 40 0C dengan menggunakan pemanas
listrik selama 16 jam. Pelarut lemak yang ada dalam labu lemak didestilasi hingga
semua pelarut lemak menguap. Pada saat destilasi pelarut akan tertampung di
ruang ekstraktor, pelarut dikeluarkan sehingga tidak kembali ke dalam labu
lemak, selanjutnya labu lemak dikeringkan dalam oven pada suhu 105 0C, setelah
itu labu didinginkan dalam desikator sampai beratnya konstan (W3).
Perhitungan kadar lemak:
% Kadar lemak = x 100%
Keterangan: W1 = Berat sampel (gram)
W2 = Berat labu lemak tanpa lemak (gram)
3.4.9 Analisis Data (Steel and Torrie 1980)
Rancangan percobaan yang digunakan untuk menganalisis konsentrasi
Isolat Soybean Protein adalah analisis Kruskal-Wallis. Pengolahan data dilakukan
dengan menggunakan perangkat lunak Statistical Package For Social Science
(SPSS) pada komputer.
Model Rancangan : Yij = µ + Ai + Ɛij
Keterangan :
Yij : Respon pengaruh A taraf ke-i pada ulangan ke-k
µ : Nilai tengah umum/rataan
Ai : Pengaruh faktor A pada taraf ke-i
Ɛij : Pengaruh galat percobaan
Bentuk hipotesis yang diuji adalah sebagai berikut :
H0 : Perbedaan konsentrasi ISP tidak memberikan pengaruh terhadap mutu sosis
ikan nila merah yang dihasilkan
H1 : Perbedaan konsentrasi ISP memberikan pengaruh terhadap mutu sosis ikan
nila merah yang dihasilkan
Analisis data dilakukan dengan menggunakan analisis ragam. Jika hasil
analisis ragam berbeda nyata, dilanjutkan dengan uji lanjut. Data hasil diuji di
analisa menggunakan statistik nonparametrik Kruskal Wallis. Apabila hasil
analisis menunjukkan adanya pengaruh nyata maka dilanjtkan dengan uji Multiple
Comparison yang bertujuan untuk mengetahui perlakuan mana saja yang
4.1 Penelitian Pembuatan Gel Ikan Nila Merah (Oreochromis sp)
Penelitian pendahuluan bertujuan untuk mendapatkan frekuensi pencucian
terbaik pada surimi ikan nila merah. Penelitian ini berupa perhitungan rendemen,
uji lipat, uji gigit, pengujian protein larut garam dan kekuatan gel. Perlakuan pada
penelitian pendahuluan yaitu banyaknya pencucian daging lumat yang dilakukan
(1 kali, 2 kali, dan 3 kali) dengan penambahan cryoprotectant berupa STPP 0,25%
untuk tiap perlakuan.
4.1.1 Rendemen
Rendemen merupakan bagian yang dapat dimanfaatkan dari suatu individu
atau biota. Semakin tinggi rendemennya maka nilai ekonomisnya pun akan
semakin tinggi pula. Hasil perhitungan rendemen daging dan surimi ikan nila
merah yang digunakan dapat dilihat pada Tabel 3.
Tabel 3 Rendemen daging dan surimi ikan nila merah (Oreochromis sp)
Bobot (gr) Rendemen
daging (%)
Bobot daging lumat dibagi 3 (gr)
Bobot surimi Ikan
utuh
daging (fillet)
Frekuensi pencucian
6000 1500 25 1 2 3 1 2 3
500 500 500 389 378 367
Rendemen Surimi (%) 19,45 18,9 18,35
Berdasarkan Tabel 3 dapat dilihat bahwa rendemen daging ikan nila merah
sebesar 25%, sedangkan rendemen surimi ikan nila yang dihasilkan berturut-turut
sebesar 19,45%; 18,9%; 18,35%. Rendemen daging lebih kecil jika dibandingkan
dengan hasil penelitian Filho (2010) sebesar 30%-35%. Hal ini dapat disebabkan
oleh habitat atau lingkungan dan cara makan. Setelah pencucian, rendemen akan
semakin berkurang akibat pelepasan atau hilangnya komponen-komponen lain
seperti darah, lemak, serta protein larut air. Semakin banyak frekuensi pencucian
4.1.2 Uji lipat
Uji lipat merupakan salah satu pengujian sensori awal bertujuan untuk
menentukan serta memastikan kekuatan gel dan elastisitas surimi oleh para
panelis (Shaviklo, 2006). Berdasarkan hasil analisis Kruskal Wallis dapat
diketahui nilai Asymsig > 0,05 Hal ini dapat dikatakan bahwa perbedaan
frekuensi pencucian tidak memberikan pengaruh berbeda nyata terhadap nilai
pengujian uji lipat. Berikut adalah hasil pengujian uji lipat dapat dilihat pada
Gambar 5.
4,67
4,57
4,73
4,45 4,5 4,55 4,6 4,65 4,7 4,75
Pencucian 1 kali Pencucian 2 kali Pencucian 3 kali
Gambar 5 Histogram nilai rata-rata uji lipat gel ikan nila merah (Oreochromis sp)
Gambar 5 menunjukkan bahwa nilai frekuensi pencucian 2 kali
menunjukkan nilai uji lipat yang terbesar yaitu, 4,73 sedangkan nilai terkecil
ditunjukkan oleh frekuensi pencucian 1 kali sebesar 4,57. Berdasarkan Gambar 5.
dapat dilihat bahwa tendensi penilaian uji lipat terhadap produk gel ikan
mengalami kenaikan seiring dengan bertambahnya frekuensi pencucian. Uji lipat
dapat dikaitkan dengan kemampuan elastisitas produk. Elastisitas produk sosis
atau produk berbasis gel dapat disebabkan oleh kandungan protein myofibril yaitu
aktin dan miosin, kualitas air cucian, pH daging, temperatur air, kadar air,
kekuatan ionik dan tendensi hidrophilik (Sonu, 1986).
4.1.3 Uji gigit
Uji gigit merupakan salah satu pengujian sensori awal bertujuan untuk
dengan cara menggigit bagian contoh yang memiliki ketebalan ± 5 mm dengan
menggunakan gigi bagian depan dan dikonversikan ke dalam tabel yang telah
disediakan (Shaviklo, 2006). Berdasarkan hasil analisis Kruskal Wallis dapat
diketahui nilai Asymsig < 0,05 Hal ini dapat dikatakan bahwa perbedaan
frekuensi pencucian memberikan pengaruh berbeda nyata terhadap nilai pengujian
uji gigit. Berikut adalah hasil pengujian uji lipat dapat dilihat pada Gambar 6.
8,47b
Pencucian 1 kali Pencucian 2 kali Pencucian 3 kali
Gambar 6 Histogram nilai rata-rata uji gigit gel ikan nila merah (Oreochromis sp)
Keterangan : Angka-angka pada histogram yang diikuti dengan huruf superscript yang berbeda (a,b) menunjukkan berbeda nyata (p<0,05)
Gambar 6 menunjukkan surimi dengan frekuensi pencucian 2 kali berbeda
nyata dengan surimi frekuensi 1 kali dan 3 kali. Nilai frekuensi pencucian 2 kali
menunjukkan nilai uji gigit yang terbesar yaitu, 8,47 sedangkan nilai terkecil
ditunjukkan oleh frekuensi pencucian 1 kali sebesar 7,27. Menurut Cross (1986)
mengatakan bahwa prinsip pengujian atau evaluasi yang berkaitan dengan tekstur
atau keempukan dapat dianalisis atau dieliminasi oleh para panelis yang dapat
dievaluasi saat itu juga. Panelis cenderung menyukai perlakuan pencucian kedua
dengan nilai tertinggi uji gigit sebesar 8,47 yang tidak terlalu keras maupun tidak
terlalu lunak. Kondisi produk seperti ini dapat terjadi karena perbedaan jumlah
jaringan daging, jumlah simpanan lemak, temperatur contoh dan lama waktu
4.1.4 Protein larut garam
Protein larut garam adalah protein yang akan larut dalam larutan garam
tertentu berupa protein miofibril. Berdasarkan hasil sidik ragam dapat diketaihui
nilai Asymsig > 0,05 Hal ini dapat dikatakan bahwa perbedaan frekuensi
pencucian tidak memberikan pengaruh berbeda nyata terhadap nilai pengujian
protein larut garam. Berikut adalah hasil pengujian protein larut garam dapat
dilihat pada Gambar 7.
5,13 6,67
6,92
0 1 2 3 4 5 6 7 8
Pencucian 1 kali Pencucian 2 kali Pencucian 3 kali
Gambar 7 Histogram nilai rata-rata uji protein larut garam surimi ikan nila merah (Oreochromis sp)
Gambar 7 menunjukkan bahwa nilai frekuensi pencucian 1 kali
menunjukkan nilai uji lipat yang terbesar yaitu, 6,92 sedangkan nilai terkecil
ditunjukkan oleh frekuensi pencucian 3 kali sebesar 5,13. Kandungan protein larut
garam atau myofibril dapat dipengaruhi oleh beberapa faktor yaitu kualitas air
pencucian antara lain kekuatan ionik atau konsentrasi garam inorganik, pH dan
temperature. Kekuatan ionik air pencucian dapat menyebabkan daging akan
cenderung mengembang. Jika kekuatan ionik air tersebut kecil maka sel-sel
daging akan mengembang sehingga sulit mengeluarkan air dari surimi akan
menyebabkan kandungan air surimi yang relatif tinggi (Toyoda, 1992). Hal itulah
yang diduga menyebabkan semakin banyak frekuensi pencucian akan
menurunkan protein larut garam pada surimi tersebut. Menurut Hossain (2004)
mengatakan bahwa pada proses pencucian yang berlebihan setelah protein
menyebabkan kehilangan lebih lanjut protein myofibril dari daging. Oleh karena
itu, akan meningkatkan penggunaan air cucian dan treatment buangan air cucian
serta kehilangan protein myofibril lebih lanjut.
4.1.5 Kekuatan gel
Kekuatan gel merupakan salah satu indeks kualitas produk yang dapat
diukur berdasarkan spesies, musim dan perlakuan lainnya dengan satuan gf atau g
force (Kongpun, 1999). Berdasarkan hasil sidik ragam dapat diketahui nilai
Asymsig < 0,05 Hal ini dapat dikatakan bahwa perbedaan frekuensi pencucian
memberikan pengaruh berbeda nyata terhadap nilai pengujian kekuatan gel.
Berikut adalah hasil pengujian gel ikan terhadap kekuatan gel yang dihasilkan
dapat dilihat pada Gambar 8.
638,13a
Pencucian 1 kali Pencucian 2 kali Pencucian 3 kali
Gambar 8 Histogram nilai rata-rata uji kekuatan gel gel ikan nila merah (Oreochromis sp)
Keterangan : Angka-angka pada histogram yang diikuti dengan huruf superscript yang berbeda (a,b) menunjukkan berbeda nyata (p<0,05)
Gambar 8 menunjukkan kekuatan gel surimi dengan frekuensi pencucian 3
kali berbeda nyata dengan surimi frekuensi 1 kali dan 2 kali, sedangkan kekuatan
gel dengan pencucian 1 kali dan 2 kali tidak berbeda nyata terhadap kekuatan gel.
Nilai frekuensi pencucian 2 kali menunjukkan nilai kekuatan gel yang terbesar
yaitu, 948,03 sedangkan nilai terkecil ditunjukkan oleh frekuensi pencucian 3 kali