44 Lampiran 2. Tumbuhan dan daun ketepeng
45
Tumbuhan ketepeng
Daun ketepeng
Lampiran 3.Gambarsimplisia dan serbuk simplisia daun ketepeng
46
Simplisia daun ketepeng
Serbuk simplisia daun ketepeng
Lampiran 4. Hasil pemeriksaan mikroskopik serbuk simplisia daun ketepeng
47 Keterangan:
A = Stomata parasitik B = Kristal bentuk prisma C = Trikoma multiseluler
D = Pembuluh dengan penebalan spiral
48 Serbuk Simplisia Lampiran 5.Bagan kerja penelitian
Dicuci di air mengali Ditiriskan
Ditimbang berat basahnya Dikeringkan
Ditimbang berat keringnya
Dihaluskan dengan blender Disimpan
Dimaserasi dengan etanol 80%
Difraksinasi Daun Ketepeng
Simplisia
Karakterisasi Skrining Fitokimia Pembuatan ekstrak
•Makroskopik
•Mikroskopik
•Penetapan Kadar Air
•Penetapan Kadar Sari yang Larut Air
•Penetapan Kadar Sari yang Larut Etanol
•Penetapan Kadar Abu Total
•Penetapan Kadar Abu yang Tidak Larut Asam
Uji Aktivitas Antibakteri
49
Lampiran 6.Bagan pembuatan ekstrak etanol daun ketepeng (Senna alata (L.)Roxb.)
Dimasukkan ke dalam bejana
Dimasukkan etanol 80% sampai simplisia terendam sempurna
Dibiarkan selama 5 hari terlindung dari cahaya, sambil sesekali diaduk
Disaring
Dimaserasi kembali dengan etanol 80 %
Di enap tuang
Diuapkan dengan penguap penguap vakum Diuapkan diatas penangas air
Maserat
Ekstrak kental (72,5 g)
500 g serbuk simplisia
Ampas
Ampas Maserat
50
Lampiran 7. Bagan pembuatan fraksi n-heksana dan fraksi etilasetat daun ketepeng
Ditambahkan 120 ml etanol dan 300 ml akuades
Dihomogenkan
Dimasukkan dalam corong pisah Diekstraksi dengan 150 ml n-heksana
Dikocok dan didiamkan sampai terbentuk dua lapisan dan dipisahkan
Diekstraksi dengan 150 ml Dikumpulkan etil asetat
Dipekatkan dengan penguap vakum Diuapkan diatas penangas air Dikocok dan didiamkan
sampai terbentuk dua lapisan dan dipisahkan
Dikumpulkan
Dipekatkan dengan penguap vakum
Diuapkan diatas penangas air Ekstrak etanol daun ketepeng (30 g)
Fraksi n-heksana
Fraksi etilasetat pekat (2,41 g)
51
Lampiran 8. Bagan pengujian aktivitas antibakteri
← Diambil dengan jarum ose steril
← Ditanam pada media nutrient agar miring
← Diinkubasi pada suhu 37oC selama 24 jam
← Disuspensikan dalam 10 ml media nutrient
broth steril
←disesuaikan kekeruhan dengan standar 0,5 Mc. Farland
← Dimasukkan 0,1 ml inokulum ke dalam cawan petri
← Ditambahkan 15 ml media nutrient agar ke dalam cawan petri
← Dihomogenkan dan dibiarkan hingga memadat
← Diletakkan pencadang kertas yang telah direndam ke dalam larutan uji ekstrak /fraksi dengan berbagai konsentrasi dan pelarut DMSO sebagai blanko
← Diinkubasi pada suhu 37oC selama 18- 24 jam
← Diukur diameter daerah hambatan di sekitar pencadang kertas dengan menggunakan jangka sorong
Biakan murni bakteri
Stok kultur bakteri
Inokulum bakteri
Media Padat
Hasil
52
Lampiran9.Perhitungan Karakterisasi Simplisia Daun Ketepeng
1. Penetapan kadar air
a. Berat sampel = 5,046 g Volume I = 3,5 ml Volume II = 3,8 ml
Kadar air = 3,8-3,5
5,046x 100 % = 5,9453% b. Berat sampel = 5,064 g
Volume I = 3,8 ml Volume II = 4,2 ml
Kadar air = 4,2-3,8
5,064 x 100% = 7,9776% c. Berat sampel = 5,045 g
Volume I = 0,7 ml Volume II = 1,0 ml
Kadar air = 1,0-0,7
5,045x 100% = 5,9464%
Kadar air rata-rata = (5,9453+7,9776+5,9464)%
3
=
6,6231%2. Perhitungan penetapankadar sari larutdalam etanol
a. Berat sampel = 5,0336 g
Kadar air
=
volume II-volume Iberat sampel
�
100 %Kadar sari= berat sari berat sampel x
100
20 ×100%
53 Lampiran 9. (lanjutan)
Berat sari = 0,1565 g
Kadar sari rata-rata = 15,0536+15,0536+15,6271%
3 = 15,4087%
3. Perhitungan penetapankadar sarilarutdalam air
a. Berat sampel = 5,0026 g
Kadar sari = berat sari berat sampel x
100
20 × 100%
54 Lampiran 9. (lanjutan)
Berat sari = 0,1988 g
Kadar sari =0,1988 5,0013
x
100
20
x
100% = 19,8748%Kadar sari rata-rata = (20,0995+21,4228+19,8748 )%
3 = 20,4657%
4. Perhitungan penetapankadarabu total simplisia
a. Berat sampel = 2,0160 g Berat abu = 0,0898 g
Kadar abu =0,0898
2,0160x 100 % = 4,4543 % b. Berat sampel = 2,0850 g
Berat abu = 0,0786 g
Kadar abu = 0,0786
2,0850 x 100% = 3,7697% c. Berat sampel = 2,0900 g
Berat abu = 0,0880 g
Kadar abu = 0,0880
2,0900 x 100% = 4,2105%
Kadar abu total rata-rata = (4,4543+3,7697+4,2105)%
3 = 4,1448%
5. Perhitungan penetapankadarabu tidaklarutdalamasam Kadar abu total = berat abu
berat sampel× 100%
Kadar abu yang tidaklarutdalamasam
=
berat abuberat sampel
x
100%55 Lampiran 9.(lanjutan)
Sampel I Berat sampel = 2,0160 g Berat abu = 0,0060 g
Kadar abu = 0,0060
2,0160 x 100% = 0,2976 % Sampel II Berat sampel = 2,0850 g
Berat abu = 0,0080 g
Kadar abu = 0,0080
2,0850 x 100% = 0,3836% Sampel III Berat sampel = 2,0900 g
Berat abu = 0,0090 g
Kadar abu = 0,0090
2,0900x 100%= 0,4306 %
Kadar abu yang tidaklarutasam rata-rata = 0,2976%+0,3836%+0,4306%
3 = 0,3706%
56
Lampiran 10. Data hasil uji aktivitas antibakteri ekstrak etanol daun ketepeng terhadap bakteri Staphylococcus aureus, Staphylococcus
epidermidis dan Pseudomonas aeruginosa
No
Konsen- trasi (mg/ml)
Diameter Daerah Hambat (mm)
Staphylococcus aureus
Staphylococcus
epidermidis Pseudomonas aeruginosa
D1 D2 D3 D* D1 D2 D3 D* D1 D2 D3 D*
D = Diameter daerah hambatan pertumbuhan bakteri 1,2,3 = Pengulangan
D* = Diameter rata- rata daerah hambatan pertumbuhan bakteri - = Tidak terdapat daerah hambatan pertumbuhan bakteri
57
Lampiran 11. Data hasil uji aktivitas antibakteri fraksi n- heksanadaun ketepeng terhadap bakteri Staphylococcus aureus, Staphylococcus
epidermidis dan Pseudomonas aeruginosa
No
Konsen- trasi (mg/ml)
Diameter Daerah Hambat (mm)
Staphylococcus aureus
Staphylococcus
epidermidis Pseudomonas aeruginosa
D1 D2 D3 D* D1 D2 D3 D* D1 D2 D3 D*
D = Diameter daerah hambatan pertumbuhan bakteri 1,2,3 = Pengulangan
D* = Diameter rata- rata daerah hambatan pertumbuhan bakteri - = Tidak terdapat daerah hambatan pertumbuhan bakteri
58
Lampiran 12. Data hasil uji aktivitas antibakteri fraksi etil asetatdaun ketepeng terhadap bakteri Staphylococcus aureus, Staphylococcus
epidermidis dan Pseudomonas aeruginosa
No
Konsen- trasi (mg/ml)
Diameter Daerah Hambat (mm)
Staphylococcus Aureus
Staphylococcus
epidermidis Pseudomonas aeruginosa
D1 D2 D3 D* D1 D2 D3 D* D1 D2 D3 D*
D = Diameter daerah hambatan pertumbuhan bakteri 1,2,3 = Pengulangan
D* = Diameter rata- rata daerah hambatan pertumbuhan bakteri - = Tidak terdapat daerah hambatan pertumbuhan bakteri
59
Lampiran 13. Gambar pengujian aktivitas antibakteri ekstrak etanol daun ketepeng
Pengujian terhadap Pseudomonas aeruginosa A Pengujian terhadap Staphylococcus aureus
A
Pengujian terdahapStaphylococcus epidermidis
60
Lampiran 14. Gambar hasil uji aktivitas antibakteri fraksi n-heksana daun ketepeng
Pengujian terhadap Staphylococcus aureus A
Pengujian terhadap Staphylococcus epidermidis A
61
Lampiran 15. Gambar pengujian aktivitas antibakteri fraksi etilasetat daun ketepeng
Pengujian terhadap Staphylococcus aureus
A
Pengujian terhadap Staphylococcus epidermidis A
Pengujian terhadap Pseudomonas aeruginosa
41
DAFTAR PUSTAKA
Anonim, (2016). Sistematika Tumbuhan Ketepeng (Cassia alata L.). 2016.
Breed, R.S., Murray, E.G., dan Smith N.R. (1957).Bergeys Manual of
Determinative Bacteriology.Edisi ke-7. USA: The Williams and Wilkins
Company.
Cowan, M.M. (1999). Plant Products as Antimicrobial Agents.Clinical
Microbiology Reviews.12: 564 – 582.
Depkes RI. (1986). Sediaan Galenik. Jakarta: Departemen Kesehatan Republik Indonesia.
Depkes RI. (1995). Materia Medika Indonesia. Jilid V. Jakarta: Departemen Kesehatan RI.
Depkes RI. (1995). Materia Medika Indonesia. Jilid VI. Jakarta: Departemen Kesehatan RI.
Ditjen POM RI. (2000). Parameter Standar Umum Ekstrak Tumbuhan Obat. Jakarta: Departemen Republik Indonesia.
Ditjen POM RI.(1979). Farmakope Indonesia. Edisi III. Jakarta: Departemen Kesehatan Republik Indonesia.
Ditjen POM RI.(1995). Farmakope Indonesia. Edisi IV. Jakarta: Departemen Kesehatan RI.
Doughari, J.H., dan Okafor, B. (2007)Antimicrobial Activity of Senna alata Linn.
East and Central African Journal of Pharmaceutical Sciences Vol. 10.17-21.
Dwidjoseputro.(1990). Dasar-Dasar Mikrobiologi. Jakarta: Djambatan.
Farnsworth, N.R. (1996). Biological and Phytochemical Screening of Plants.Journal of Pharmaceutical Science.55 (3): 225-276.
Gibson, J.M. (1996) Mikrobiologi dan Patologi Modern.Jakarta; Penerbit Buku
Kedokteran EGC.
Gillespie, S., dan Kathlenn B. (2008).At A Glance Mikrobiologi Medis dan
Infeksi. Terjemahan: Stella Tinia H. Edisi ke-3. Jakarta: Penerbit Erlangga.
Gunawan, D., dan Mulyani, S., (2004).Ilmu Obat Alam. Bogor: Penebar Swadaya. Harborne, J.B. (1987). Metode Fitokimia. Edisi kedua.Penerjemah: Kosasih Padmawinata dan Iwang Soediro. Bandung: Penerbit ITB.
Hariana, A. (2011). Tumbuhan Obat dan Khasiatnya 3. Jakarta: Swadaya.
42
Holt, G.J., Kneg, N.R., Sneath, A.H., Starley, T.J, Witirams, T.S. (1988). 9th edition.Bergey’s Manual Od Determinative Bacteriology. London: Williams & Wilkins Company.
Jawetz, Melnick, dan Adelberg
,
s. (2007). Mikrobiologi Kedokteran. Edisi I. Jakarta: Salemba Medika.
Lay, B.W., dan Sugiyo.(1994). Analisis Mikroba di Laboratorium.Jakarta : PT. Raja Grafindo Persada.
Markham, KR., (1998). Cara Mengidentifikasi Flavonoid. Terjemahan Kosasih, P. Bandung: Penerbit ITB.
Merck.(2005). Merck Microbiology Manual.Edisi ke-12.Berlin; Merck.
Muhlisah, F., (2001).Tanaman Obat Keluarga. Edisi ke-7. Penerbit Penebar Swadaya, 7-12. Jakarta.
Naim, R. (2004). Senyawa Antimikroba dari Tumbuhan. Bogor: FKH dan Sekolah Pascasarjana IPB.
Odugbemi, T. (2008).A Textbook of Medicinal Plants from Nigeria. Nigeria: University of Lagos Press.
Owoyale, J A., Olatunji, G A., dan Oguntoye, S O. (2005). Antifungal and Antibacterial Activities of an Alcoholic Extract of Senna alata Leaves. Journal of
Applied Science and Environment Mgt. Vol. 9 (3) 105 – 107.
Pelczar, Michael, J., Chan, E.C.S.. (1988). Dasar – Dasar Mikrobiologi, Jakarta; UI Press.
Pratiwi, S. T. (2008).Mikrobiologi Farmasi. Jakarta: Erlangga.
Robinson, T. (1995).The Organic Constituents of Hight Plant.Edisi ke-4. New York: University of Massachusetts. Terjemahan: Kosasih Padmawinata. Kandungan Organik Tumbuhan Tinggi.Edisi keempat. Bandung: ITB.
Soebagio.(2005). Kimia Analitik II. Malang: Universitas Negeri Malang (UM-PRESS).
Supardi, I. dan Sukamto.(1999). Mikrobiologi Dalam Pengolahan dan Pengolahan.Pangan. Bandung: Penerbit Alumni.
Tim Mikrobiologi FK Brawijaya. (2003). Bakteriologi Medik. Cetakan Pertama. Malang: Bayu Media Publishing.
Titin, Yuniarti. (2008). Ensiklopedi Tanaman Obat Tradisional. Jakarta: Medpress.
43
Venn, R.F. (2008). Principles and Practices of Bioanalysis.Edisi ke-2. Boca Raton: Taylor and Francis Group.
Volk, W.A., dan Wheeler, M.F. (1993). Mikrobiologi Dasar. Jilid I. Alih Bahasa: Markam. Jakarta: Erlangga.
Warsa.(1994). Buku Ajar Mikrobiologi Kedokteran.Fakultas Kedokteran Universitas Indonesia; Jakarta.
World Health Organization. (1998). Quality Control Methods For Medicinal
Plant Material. Switherland: WHO.
Yacob T., dan Endriani R. (2010) Daya Antibakteri Ekstrak Etanol Ketepeng Cina (Senna alata) terhadap Staphylococcus aureus dan Escherichia coli secara In Vitro. Jurnal Natur Indonesia 13(1).63-66.
Lampiran 1. Hasil identifikasi tumbuhan
20 BAB III
METODE PENELITIAN
Penelitian ini dilakukan dengan menggunakan metode eksperimental di Laboratorium Mikrobiologi dan Laboratorium Fitokimia Fakultas Farmasi Universitas Sumatera Utara Medan meliputi pengumpulan dan pengolahan sampel, skrining fitokimia, pemeriksaan karakteristik simplisia, pembuatan ekstrak etanol daun ketepeng. Fraksinasi dengan pelarut n-heksana dan etilasetat.Pengujian aktivitas antibakteri dengan metode difusi agar menggunakan cakram kertas terhadap bakteri Staphylococcus aureus, Staphylococcus
epidermidis, dan Pseudomonas aeruginosa.
3.1 Alat-alat
Alat- alat yang digunakan dalam penelitian ini adalah alat- alat gelas, aluminium foil, alat tanur, blender (Philips), cakram kertas (Oxoid), cawan petri, inkubator (Fiber Scientific), jangka sorong, jarum ose, kaca objek, kamera (Lenovo), Laminar Air Flow Cabinet (Astec HLF I200 L), lampu Bunsen, lemari pendingin (Toshiba), lemari pengering, mikroskop cahaya, otoklaf (Fisons), oven (Memmert), penangas air, penguap vakum (Haake D), pinset, pipet mikro (Eppendorf), dan timbangan analitik (Mettler Toledo).
3.2 Bahan-bahan
Bahan tumbuhan yang digunakan dalam penelitian ini adalah daun ketepeng (Senna alata (L.)Roxb.). Bahan kimia yang digunakan kecuali dinyatakan lain berkualitas proanalisa (E.Merck): amil alkohol, asam asetat
21
anhidrat, asam klorida pekat, asam nitrat pekat, asam sulfat pekat, benzena, besi (III) klorida, bismuth (III) nitrat, dimetilsulfoksida (DMSO), etanol, etilasetat, iodium,isopropanol,kalium iodida, kloroform,metanol,natrium hidroksida, natrium klorida, n-heksana, raksa (II) klorida,serbuk magnesium, timbal (II) asetat, toluene, α-naftol, serta air suling, nutrient agar dan nutrient broth. Bakteri yang digunakan adalah bakteri Staphylococcus aureus, Staphylococcus epidermidis, dan Pseudomonas aeruginosa.
3.3 Pembuatan Larutan Pereaksi dan Media 3.3.1 Pembuatan larutan pereaksi
3.3.1.1 Pereaksi Mayer
Sebanyak 2,266 g raksa (II) klorida dilarutkan dalam air suling hingga 100 mL. Pada wadah lain, 50 g kalium iodida dilarutkan dalam 100 mL air suling. Kemudian 60 mL larutan I dicampurkan dengan 10 mL larutan II dan ditambahkan air suling hingga 100 mL (Depkes, RI., 1989).
3.3.1.2 Pereaksi Bouchardhat
Sebanyak 4 g Kalium Iodida ditimbang kemudian dilarutkan dalam air suling secukupnya sampai KI larut dengan sempurna, lalu ditambahkan 2 g iodium sedikit demi sedikit. Setelah semuanya larut, dicukupkan dengan air suling hingga volume 100 mL (Depkes, RI., 1989).
3.3.1.3 Pereaksi natrium hidroksida 2 N
Sebanyak 8,002 g Natrium hidroksida ditimbang, kemudian dilarutkan dalam air suling hingga 100 mL (Ditjen, POM., 1979).
3.3.1.4 Pereaksi Dragendorff
Sebanyak 8,0 g bismuth (II) nitrat dilarutkan dalam 20 mL asam nitrat dan
22
dilarutkan27,2 g kalium iodida dalam 50 mL air suling. Campur kedua larutan dan dicukupkan dengan air suling hingga 100 mL (Depkes, RI., 1989).
3.3.1.5 Pereaksi besi (III) klorida 1%
Sebanyak 1 g besi (III) klorida ditimbang, kemudian dilarutkan dalam air suling hingga 100 mL, lalu disaring (Ditjen, POM., 1979).
3.3.1.6 Pereaksi asam klorida 2 N
Asam klorida pekat sebanyak 16,6 mL ditambahkan air suling sampai 100 mL (Ditjen, POM., 1979).
3.3.1.7 Pereaksi timbal (II) asetat 0,4 M
Sebanyak 15,17 g timbal asetat ditimbang, kemudian dilarutkan dalam air suling bebas karbon dioksida hingga 100 mL (Depkes, RI., 1989).
3.3.1.8 Pereaksi Liebermann-Burchard
Sebanyak sepuluh tetes asam asetat anhidrat dicampurkan dengan satu tetes asam sulfat pekat. Larutan harus selalu dibuat baru saat akan digunakan.(Depkes, RI., 1989).
3.3.1.9 Pereaksi Molisch
Sebanyak 3 g alfa naftol dilarutkan dalam 15 mL etanol 95 % ditambahkan dengan asam nitrat 0,5 N secukupnya hingga diperoleh larutan 100 mL (Depkes, RI., 1989).
3.3.2 Pembuatan Media 3.3.2.1 Media nutrient agar
Komposisi nutrient agar adalah 5 g Peptone from meat, 3 g Meat extract, 12 g agar, dan air suling ad 1 L. Cara pembuatan: Sebanyak 20 g nutrient agar ditimbang, disuspensikan ke dalam air suling sebanyak 1000 mL, lalu dipanaskan sampai bahan larut sempurna. Disterilkan didalam autoklaf pada suhu 121oC
23 selama 15 menit (Merck, 2005).
3.3.2.2 Media nutrient broth
Komposisi nutrient broth adalah 5 g Peptone, 3 g Meat extract, air suling ad 1 L. Cara pembuatan:Sebanyak 8 g media nutrient broth (NB) dilarutkan dalam air suling steril sedikit demi sedikit kemudian volumenya dicukupkan hingga 1 L dengan bantuan pemanasan sampai semua bahan larut sempurna, kemudian disterilkan dalam autoklaf pada suhu 121oC selama 15 menit (Merck, 2005).
3.3.2.3 Pembuatan agar miring
Sebanyak 3 mL media nutrient agar cair, dimasukkan ke dalam tabung reaksi dan diletakkan pada sudut kemiringan 30-45o dan dibiarkan memadat, kemudian disimpan di lemari pendingin (Lay, 1994).
3.4 Sterilisasi Alat dan Bahan
Alat dan bahan yang digunakan dalam uji aktivitas antibakteri ini disterilkan lebih dahulu sebelum dipakai. Media pertumbuhan disterilkan di otoklaf pada suhu 121oC selama 15 menit dan alat- alat gelas di oven pada suhu 160-170oC selama 1-2 jam, sedangkanjarum ose dan pinset dengan cara dibakar dengan nyala bunsen (Lay, 1994).
3.5 Pengumpulan dan Pengolahan Bahan Tumbuhan 3.5.1 Pengumpulan bahan tumbuhan
Pengambilan bahan tumbuhan dilakukan secara purposif yaitu tanpa membandingkan tumbuhan yang sama dengan daerah lain. Bahan tumbuhan yang digunakan adalah daun ketepeng (Senna alata (L.)Roxb.)diambil dari Kelurahan
24
Padang Bulan Selayang II Kecamatan Medan Selayang, Kota Medan Provinsi Sumatera Utara.
3.5.2 Identifikasi tumbuhan
Identifikasi tumbuhan dilakukan di Herbarium Bogoriense Bidang Botani Pusat Penelitian dan Pengembangan Biologi LIPI Bogor.
3.5.3 Pembuatan simplisia
Daun ketepeng (Senna alata (L.)Roxb.)dicuci bersih dari kotoran dengan air sampai bersih dan ditiriskan.Kemudian diangin-anginkan atau dibiarkan diruangan terbuka tanpa terkena cahaya matahari langsung.Daun ketepeng dianggap kering apabila sudah rapuh atau dapat dipatahkan dengan cara diremas. Kemudian simplisia daun ketepengyang telah kering dihaluskan menggunakan blender sehingga menjadi serbuk simplisia, dan disimpan dalam wadah plastik yang tertutup rapat.
3.6 Karakterisasi Simplisia 3.6.1 Pemeriksaan makroskopik
Pemeriksaan makroskopik dilakukan terhadap serbuk simplisia daun ketepeng (Senna alata (L.)Roxb.)dengan mengamati bentuk, bau, rasa, dan warna. 3.6.2 Pemeriksaan mikroskopik
Pemeriksaan mikroskopik dilakukan terhadap serbuk simplisia daun ketepeng (Senna alata (L.)Roxb.).Serbuk simplisia ditaburkan di atas kaca objek yang telah ditetesi dengan larutan kloralhidrat dan ditutup dengan kaca penutup, kemudian diamati di bawah mikroskop.Selain itu, pemeriksaan mikroskopik juga dilakukan dengan menggunakan media akuades.
3.6.3 Penetapan kadar air
25 a. Penjenuhan toluen
Toluen sebanyak 200 mL dimasukkan ke dalam labu alas bulat, lalu ditambahkan 2 mL air suling, kemudian alat dipasang dan dilakukan destilasi selama 2 jam. Destilasi dihentikan dan dibiarkan dingin selama ± 30 menit, kemudian volume air dalam tabung penerima dibaca dengan ketelitian 0,1 mL. b. Penetapan kadar air simplisia
Labu berisi toluen tersebut dimasukkan 5 g serbuk simplisia yang telah ditimbang seksama, dipanaskan hati-hati selama 15 menit.Setelah toluen mendidih, kecepatan toluen diatur 2 tetes per detik sampai sebagian besar air terdestilasi, kemudian kecepatan destilasi dinaikkan sampai 4 tetes per detik.Setelah semua air terdestilasi, bagian dalam pendingin dibilas dengan toluen.Destilasi dilanjutkan selama 5 menit, tabung penerima dibiarkan mendingin pada suhu kamar. Setelah air dan toluen memisah sempurna, volume air dibaca dengan ketelitian 0,1 mL. Selisih kedua volume air yang dibaca sesuai dengan kadar air yang terdapat dalam bahan yang diperiksa. Kadar air dihitung dalam persen (WHO, 1998).
3.6.4 Penetapan kadar sari larut dalam air
Sebanyak 5 g serbuk simplisia dimaserasi selama 24 jam dalam 100 mL air-kloroform (2,5 ml kloroform dalam aquadest sampai 1 L) dengan menggunakan botol bersumbat sambil sekali-kali dikocok selama 6 jam pertama, kemudian dibiarkan selama 18-24 jam dan disaring. Sebanyak 20 mL filtrat pertama diuapkan hingga kering dalam cawan yang berdasar rata yang telah dipanaskan dan ditara. Residu dipanaskan dalam oven pada suhu 105oC sampai diperoleh bobot tetap. Kadar sari yang larut dalam air dihitung terhadap bahan yang telah dikeringkan (Depkes, RI., 1995).
26 3.6.5 Penetapan kadar sari larut dalam etanol
Sebanyak 5 g serbuk simplisia dimaserasi selama 24 jam dalam 100 mL etanol 96% dengan menggunakan botol bersumbat sambil sekali-kali dikocok selama 6 jam pertama, kemudian dibiarkan selama 18-24 jam dan disaring. Sebanyak 20 mL filtrat pertama diuapkan hingga kering dalam cawan yang berdasar rata yang telah dipanaskan dan ditara.Residu dipanaskan dalam oven pada suhu 105oC sampai diperoleh bobot tetap.Kadar sari yang larut dalam air dihitung terhadap bahan yang telah dikeringkan (Depkes, RI., 1995).
3.6.6 Penetapan kadar abu total
Sebanyak 2,5 g serbuk simplisia yang telah digerus dan ditimbang seksama, dimasukkan ke dalam krus porselin yang telah dipijar dan ditara, kemudian diratakan. Krus porselin bersama isinya dipijarkan perlahan hingga arang habis, dinginkan, ditimbang sampai diperoleh bobot yang tetap.Kadar abu dihitung terhadap bahan yang telah dikeringkan di udara (Depkes, RI., 1995). 3.6.7 Penetapan kadar abu yang tidak larut asam
Abu yang diperoleh pada penetapan kadar abu total dididihkan dengan 25 mL asam klorida encer selama 5 menit, bagian yang tidak larut asam dikumpulkan, disaring dengan kertas saring, lalu cuci dengan air panas. Kemudian residu dan kertas saring dipijarkan sampai diperoleh bobot yang tetap, dinginkan, dan ditimbang beratnya.Kadar abu yang tidak larut asam dihitung terhadap bahan yang telah dikeringkan di udara (Depkes, RI., 1995).
3.7 Skrining Fitokimia
Skrining Fitokimia dari serbuk simplisia, ekstrak etanol, fraksi n-hesana dan etilasetat meliputi pemeriksaan golongan senyawa alkaloida, flavonoida, saponin, tanin, glikosida, glikosida antrakinon dan steroida/triterpenoida.
27 3.7.1 Pemeriksaan alkaloida
Serbuk simplisiaditimbang sebanyak 0,5 g kemudian ditambahkan 1 mL asam klorida 2 N dan 9 mL air suling, dipanasakan di atas penangas air selama 2 menit. Didinginkan dan disaring. Filtrat dipakai untuk percobaan sebagai berikut: a. Filtrat sebayak 3 tetes ditambah dengan 2 tetes larutan pereaksi Meyer, akan
terbentuk endapan menggumpal bewarna putih atau kuning.
b. Filtrat sebanyak 3 tetes ditambah dengan 2 tetes larutan pereaksi Bouchardat, akan terbentuk endapan berwarna coklat sampai hitam.
c. Filtrat sebanyak 3 tetes ditambah dengan 2 tetes larutan pereaksi Dragendorff, akan terbentuk endapan merah atau jingga.
Alkaloida positif jika terjadi endapan atau kekeruham paling sedikit dua dari tiga percobaan (Depkes, RI., 1995).
3.7.2 Pemeriksaan flavonoida
Sebanyak 0,5 g serbuk simplisia ditambahkan 20 mL air panas, dididihkan selama 10 menit dan disaring dalam keadaan panas, ke dalam 5 mL filtrat ditambahkan 0,1 g serbuk magneasium dan 1 mL asam klorida pekat dan 2 mL amil alkohol, dikocok dan dibiarkan memisah. Flavonoida positif jika terjadi warna merah, kuning, jingga pada lapisan amil alkohol (Depkes, RI., 1995).
3.7.3 Pemeriksaan saponin
Sebanyak 0,5 g serbuk simplisiadimasukkan ke dalam tabung reaksi, ditambahkan 10 mL air panas, didinginkan kemudian dikocok selama 10 detik, jika terbentuk busa setinggi 1 sampai 10 cm yang stabil tidak kurang dari 10 menit dan tidak hilang dengan penambahan 1 tetes asam klorida 2 N menunjukkan adanya saponin (Depkes, RI., 1995).
3.7.4 Pemeriksaan glikosida
28
Sebanyak 3 g serbuk simplisiadisari dengan 30 mL campuran etanol 95% dengan air suling (7:3) dan 10 mL asam sulfat 2 N, direfluks selama 1 jam, didinginkan dan disaring.Pada 20 mL filtrat ditambahkan 25 ml air suling dan 25 ml timbal (II) asetat 0.4 M, dikocok, didiamkan 5 menit lalu disaring.Filtrat disari dengan 20 mL campuran isopropanol dan kloroform (2:3), dilakukan berulang sebanyak 3 kali.Kumpulan sari air diuapkan dengan temperatur tidak lebih dari50oC.Sisanya dilarutkan dalam 2 mL metanol. Larutan sisa dipakai untuk percobaan berikut:
a. Larutan sisa dimasukkan ke dalam tabung reaksi dan diuapkan di atas penangas air, pada sisa tambahkan 2 ml air dan 5 tetes pereaksi molish. Tambahkan hati-hati 2 mL asam sulfat pekat pada dinding tabung, terbentuk cincin ungu pada batas kedua cairan, menunjukkan adanya glikosida.
b. Larutan percobaan diuapkan di atas penangas air. Larutkan sisa dalam 5 mL asam asetat anhidrat. Tambahkan 10 tetes asam sulfat pekat, akan terjadi warna biru atau hijau, menunjukkan adanya glikosida (Depkes, RI., 1995). 3.7.5 Pemeriksaan tanin
Sebanyak 0,5 g serbuk simplisia disari dengan 10 mL air suling lalu disaring, filtratnya diencerkan dengan air sampai tidak berwarna. Larutan diambil sebanyak 2 mL dan ditambahkan 1 sampai 2 tetes pereaksi besi (III) klorida 1%.Jika terjadi warna hijau, biru, atau kehitaman menunjukkan adanya tanin (Harborne, 1987).
3.7.6 Pemeriksaan steroida/triterpenoida
Sebanyak 1 g serbuk simplisia dimaserasi dengan 20 mLeter selama 2 jam, disaring, filtrate diuapkan dalam cawan penguap, danpada sisanya
29
ditambahkan 10 tetes asam asetat anhidrat dan 1 tetes asam sulfat pekat (pereaksi Liebermann – Burchard). Apabila pengujian terbentuk warna ungu atau merah yang berubah menjadi biru hijau menunjukkan adanya steroida/triterpenoida (Harborne, 1987).
3.7.7 Pemeriksaan glikosida antrakinon
Sebanyak 0,2 g serbuk simplisia ditambah 5 mL asam sulfat 2 N, dipanaskan sebentar, setelah dingin ditambahkan 10 mL benzena, dikocok dan didiamkan. Lapisan benzena dipisahkan dan disaring.Kocok lapisan benzena dengan 2 mL NaOH 2 N, didiamkan. Lapisan air berwarna merah dan lapisan benzena tidak berwarna menunjukkan adanya glikosida antrakinon (Depkes, RI., 1989).
3.8 Pembuatan Ekstrak
Ekstrak dibuat dengan metode maserasi.Sebanyak 500 g serbuk simplisia dimaserasi dengan 7,5 bagian pelarut(3750 mL) etanol 80%, dimasukkan ke dalam bejana bertutup serta dibiarkan pada suhu kamar selama 5 hari terlindung dari cahaya lansung sambil sering diaduk, kemudian setelah 5 hari hasil maserasi disaring dan diperas. Ampas ditambah dengan cairan penyari (remaserasi) sampai diperoleh seluruh maserat sebanyak 5 liter kemudiandibiarkan di tempat sejuk dan terlindung dari cahaya selama 2 hari dan dienaptuangkan. Seluruh maserat digabungkan menjadi satu kemudian di uapkan dengan menggunakan alat penguap vakum pada temperatur kurang lebih 40o C dan diuapkan kembali menggunakan cawan penguap diatas penangas air sehingga diperoleh ekstrak etanol kental (Ditjen POM RI, 1979).
30
3.9 Pembuatan Fraksi n- Heksana dan Fraksi Etilasetat
Pembuatan fraksi-fraksi dilakukan secara ekstraksi cair-cair (ECC) menggunakan pelarut n-heksana dan etilasetat. Sebanyak 5 g ekstrak etanol ditambahkan etanol dan 10 mL air suling, lalu dimasukkan kadalam corong pisah, kemudian ditambahkan 40 mL heksana, dikocok, didiamkan sampai 2 lapisan n-heksana (lapisan atas) diambil dengan cara dekantasi dan fraksinasi dilakukan sampai warna lapisan n-heksana jernih, kemudian ditambahkan 50 mL etilasetat pada lapisan air, dikocok, didiamkan sampai terdapat 2 lapisan yang terpisah, lapisan etilasetat (lapisan atas) diambil dengan cara dekantasi, dan fraksinasi dilakukan sampai warna lapisan etilasetat jernih, dan Fraksi air (fraksi sisa) diambil dan semua fraksi yang diperoleh diuapkan menggunakan cawan penguap diatas penangas air sampai diperoleh massa fraksi kental.
3.10 Pembuatan Larutan Uji dengan Berbagai Konsentrasi
Ekstrak etanol simplisia daun ketepeng (Senna alata (L.)Roxb.)ditimbang 1 g kemudian dilarutkan dengan pelarut DMSO hingga 2 mL maka konsentrasi ekstrak adalah 500 mg/mL. Kemudian dibuat pengenceran. Selanjutnya larutan tersebut diencerkan kembali dengan pelarut DMSO sehingga didapat konsentrasi 400; 300; 200; 100; 50; l 25; 12,5; dan 6,25 mg/ml. Dilakukan prosedur yang sama untuk fraksi n- heksana dan fraksi etilasetat.
3.11 Pembiakan Bakteri
3.11.1 Pembuatan stok kultur bakteri
Diambil satu kolonibakteridengan menggunakan jarum ose steril, kemudian ditanamkan pada media nutrient agaryang telah disterilkan dengan cara
31
menggores, setelah itu diinkubasi dalam inkubator pada suhu 36 ± 1oC selama 18-24 jam.
3.11.2 Penyiapan inokulum bakteri
Dari stok kulturbakteri yang telah tumbuh diambil dengan jarum ose steril lalu disuspensikan dalam tabung yang berisi 10 mL larutan nutrient broth. Kemudian dibandingkan kekeruhan suspensi mikroba dengan standar 0,5Mc
Farland secara visual.
3.12 Uji Aktivitas Antibakteri
Sebanyak 0,1 mL inokulum dimasukkan ke dalam cawan petri steril, setelah itu dituang media Nutrient Agar sebanyak 15 mL dengan suhu 45o – 50oC.Selanjutnya cawan digoyang di atas permukaan meja, agar media dan suspensi bakteri tercampur rata dan dibiarkan memadat.Dilakukan pengujian aktivitas antibakteri dengan metode difusi cakram kertas yaitu dengan meletakkan cakram kertas yang telah direndam dalam beberapa konsentrasi larutan uji ekstrak etanol di atas media padat yang telah diinokulasi bakteri.Dibiarkan 15 menit, kemudian diinkubasi dalam inkubator pada suhu 36 ± 1oC selama 18-24 jam, setelah itu diukur diameter daerah hambatan (zona jernih) pertumbuhan di sekitar cakram dengan menggunakan jangka sorong. Uji aktivitas antibakteri fraksi n-heksana dan fraksi etilasetatdilakukan cara yang sama.
32 BAB IV
HASIL DAN PEMBAHASAN
4.1 Hasil Identifikasi Tumbuhan
Identifikasi tumbuhan dilakukan di Pusat Penelitian dan Pengembangan LIPI Bogor.Hasil menunjukkan bahwa tumbuhan yang diteliti adalah Senna alata (L.)Roxb.suku Leguminosae.Hasil identifikasi dapat dilihat pada Lampiran 1 halaman 42.
4.2 Hasil Pemeriksaan Karakterisasi
Hasil pemeriksaan makroskopik simplisia daun ketepeng yaitu simplisia berbau khas, lemah, mula-mula tidak berasa, lama-lama agak kelat. Serbuk simplisia terlihat berserat dengan patahan-patahan tulang daun sepanjang 2 sampai 5 mm. Pemeriksaan mikroskopik menunjukkan adanya kristal bentuk prisma, trikoma multiseluler, stomata tipe parasitik, dan berkas pembuluh angkut dengan penebalan spiral. Hasil pemeriksaan karakterisasi simplisiadapat dilihat pada Tabel 4.1.
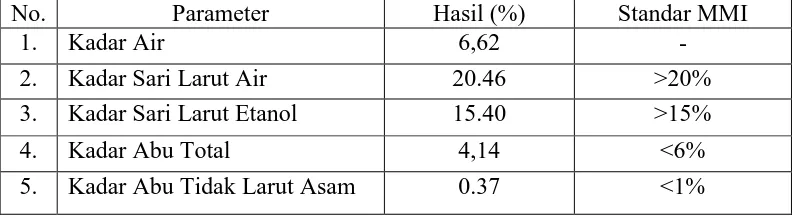
Tabel 4.1 Hasil pemeriksaan karakterisasi serbuk simplisia daun ketepeng
No. Parameter Hasil (%) Standar MMI
1. Kadar Air 6,62 -
2. Kadar Sari Larut Air 20.46 >20%
3. Kadar Sari Larut Etanol 15.40 >15%
4. Kadar Abu Total 4,14 <6%
5. Kadar Abu Tidak Larut Asam 0.37 <1%
Penetapan kadar air pada simplisia dilakukan untuk mengetahui jumlah air yang terkandung dalam simplisia yang digunakan. Kadar air simplisia ditetapkan untuk menjaga kualitas simplisia karena kadar air berkaitan dengan kemungkinan
33
pertumbuhan jamur/kapang. Hasil penetapan kadar air diperoleh lebih kecil dari 10% yaitu 6,62 %. Kadar air yang melebihi 10% dapat menjadi media yang baik untuk pertumbuhan mikroba, keberadaan jamur atau serangga, serta mendorong kerusakan mutu simplisia (WHO, 1998).
Penetapan kadar sari dilakukan menggunakan dua pelarut, yaitu air dan etanol. Penetapan kadar sari larut air adalah untuk mengetahui kadar senyawa kimia bersifat polar yang terkandung di dalam simplisia, sedangkan kadar sari larut dalam etanol dilakukan untuk mengetahui kadar senyawa larut dalam etanol, baik senyawa polar maupun non polar.
Hasil karakterisasi simplisia daun ketepeng menunjukkan kadar sari yang larut dalam air sebesar 20,46%; sedangkan kadar sari yang larut dalam etanol sebesar 15,40%. Hasil penetapan kadar sari menunjukkan bahwa sari yang larut dalam air lebih besar daripada dalam etanol. Senyawa-senyawa yang dapat larut dalam etanol adalah glikosida, antrakinon, steroida, flavonoida, klorofil, dan dalam jumlah sedikit yang larut yaitu lemak dan saponin (Depkes RI, 1986).
Penetapan kadar abu dimaksudkan untuk mengetahui kandungan “abu fisiologis” yaitu yang berasal dari jaringan tanaman itu sendiri dan “abu non-fisiologis” yang berasal dari luar atau lengket di permukaan tumbuhan. Kadar abu tidak larut asam untuk menunjukkan jumlah silikat, khususnya pasir yang ada pada simplisia dengan cara melarutkan abu total dalam asam klorida (WHO, 1998). Penetapan kadar abu pada simplisia daun ketepeng menunjukkan kadar abu total sebesar 4.14% dan kadar abu tidak larut dalam asam sebesar 0,37%.
Karakteristik simplisia daun ketepeng yang diperoleh dibandingkan dengan syarat pada Materia Medika Indonesia Edisi V dan menunjukkan simplisia yang digunakan telah memenuhi persyaratan simplisia daun ketepeng.Hasil
34
perhitungan karakterisasi simplisia daun ketepeng meliputi penetapan kadar air, kadar sari larut air, kadar sari larut etanol, kadar abu dan kadar abu tidak larut asam dapat dilihat pada Lampiran 9, halaman 50-53.
4.3 Hasil Skrining Fitokimia
Penentuan golongan senyawa kimia simplisia, ekstrak etanol, fraksi n-heksan etilasetat dilakukan untuk mengetahui golongan senyawa yang terdapat di dalamnya.Adapun pemeriksaan yang dilakukanadalah pemeriksaan golongan senyawa alkaloid, glikosida, glikosida antrakinon,steroid/triterpenoid, flavonoid, tanin dan saponin.Hasil skrining fitokimia dapat dilihat pada Tabel 4.2.
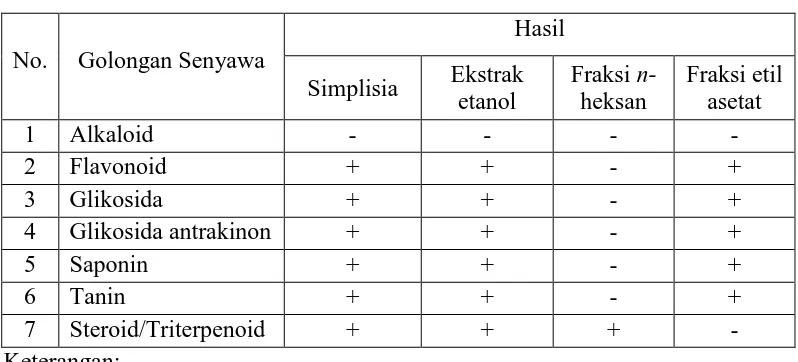
Tabel 4.2 Hasil skrining fitokimia serbuk simplisia
No. Golongan Senyawa
Hasil Simplisia Ekstrak
etanol
(+) positif : mengandung golongan senyawa (-) negatif : tidak mengandung golongan senyawa
Hasil skrining serbuk simplisia dan ekstrak etanol menunjukkan hasil postitif pada golongan senyawa flavonoid, glikosida, glikosida antrakinon, saponin, tanin, dan steroid/triterpenoid.Sedangkan fraksi n-heksan hanya positif untuk steroid/triterpenoid dan fraksi etil asetat menunjukkan hasil sama dengan esktrak etanol kecuali untuk steroid/triterpenoid negatif.
35
Menurut Robinson (1995), senyawa flavonoida, saponin, dan steroida/triterpenoid merupakan senyawa kimia yang memiliki potensi sebagai antibakteri dan antivirus.
4.4 Hasil Ekstraksi dan Fraksinasi
Hasil ekstraksi 500 g simplisia daun ketepeng dengan cara maserasi menggunakan pelarut etanol 80% diperoleh ekstrak etanol daun ketepeng sebanyak 72,5g. Kemudian dilakukan fraksinasi menggunakan pelarut n-heksana dan air, dari 30 g ekstrak diperoleh fraksi n-heksana 3,51 g, selanjutnya fraksi air di fraksinasi dengan etilasetat sehingga diperoleh fraksi etilasetat 2,41 g. Ekstrak etanol, fraksi n-heksana dan etilasetat yang diperoleh diuji aktivitas antibakteri.
4.5 Hasil Uji Aktivitas Antibakteri Ekstrak Etanol, Fraksi n-Heksana, Fraksi etilasetatDaun Ketepeng
Hasil pengujian aktivitas antibakteri ekstrak etanol, fraksi n-heksan dan fraksi etilasetat dapat dilihat pada tabel berikut ini.
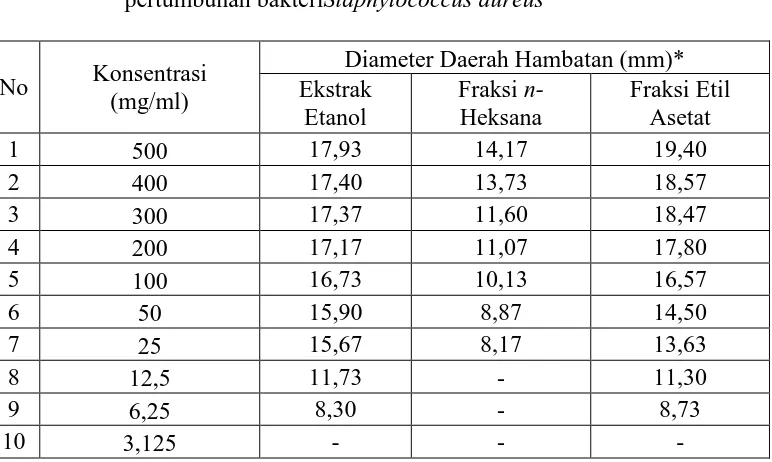
Tabel 4.3 Data hasil pengukuran diameter rata-rata daerah hambatan pertumbuhan bakteriStaphylococcus aureus
No Konsentrasi (mg/ml)
36
Tabel 4.4 Data hasil pengukuran diameter rata-rata daerah hambatan pertumbuhan bakteri Staphylococcus epidermidis
No Konsentrasi (mg/ml)
Diameter Daerah Hambatan (mm)* Ekstrak
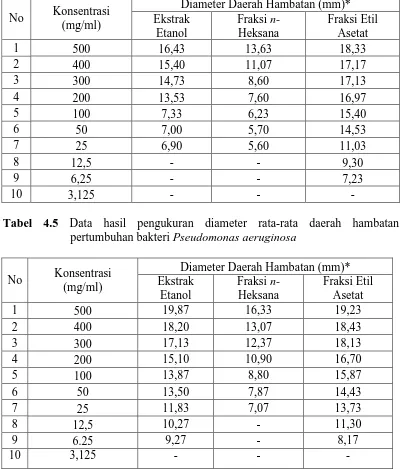
Tabel 4.5 Data hasil pengukuran diameter rata-rata daerah hambatan pertumbuhan bakteri Pseudomonas aeruginosa
No Konsentrasi (mg/ml)
Diameter Daerah Hambatan (mm)* Ekstrak Hasil uji aktivitas antibakteri menunjukkan ekstrak etanol, fraksi n-heksana,dan fraksi etil asetat daun ketepeng dapat menghambat pertumbuhan bakteri Staphylococcus aureus, Staphylococcus epidermidisdanPseudomonas
aeruginosa.Aktivitas suatu zat antimikroba dalam menghambat pertumbuhan atau
37
antimikroba tersebut (Tim Mikrobiologi FK Brawijaya, 2003).Hasil pengukuran dapat dilhat pada Lampiran 10-12, halaman 54-56.
Berdasarkan hasil pengukuran diameter daerah hambatan pada bakteri
Staphylococcus aureus, konsentrasi hambat minimum (KHM) ekstrak etanol dan
fraksi etilasetat daun ketepeng adalah 6,25 mg/mL dengan diameter daerah hambat 8,30 mm dan 8,77 mm; sedangkan untuk fraksi n-heksana adalah 25 mg/mL dengan diameter daerah hambat 8,13 mm.
Hasil pengukuran terhadap bakteri Staphylococcus epidermidis menunjukkan bahwa konsentrasi hambat minimum (KHM) ekstrak etanol dan fraksi n-heksana daun ketepeng adalah 25 mg/mL dengan diameter daerah hambat 6,90 mm dan 5,90 mm, sedangkan KHM fraksi etilasetat daun ketepeng adalah 6,25 mg/mL dengan diameter daerah hambat 7,23 mm.
Hasil pengukuran terhadap bakteri Pseudomonas aeruginosa, menunjukkan bahwa Konsentrasi Hambat Minimum ekstrak etanol dan fraksi etilasetat daun ketepeng adalah 6,25 mg/mL dengan diameter daerah hambat 9,27 mm dan 8,17 mm, sedangkan KHM fraksi n-heksana adalah 25 mg/mL dengan diameter daerah hambat 7,07 mm.
Dari hasil pengamatan menunjukkan bahwa fraksi etil asetat daun ketepeng adalah yang paling tinggi aktivitas antibakteri terhadap ketiga bakteri, konsentrasi hambat minimum (KHM) sebesar 6,25 mg/ml terhadap ketiga bakteri.Pelarut etilasetat dapat mengekstraksi alkaloid, flavonoid, saponin, tanin dan polifenol, serta triterpenoid.Berdasarkan hasil skrining fitokimia, fraksi etilasetat daun ketepeng mengandung flavonoid, saponin, tanin, glikosida, dan glikosida antrakinon.
38
Menurut hasil penelitian yang dilakukan Lumbessy (2013) menunjukkan bahwa kandungan flavonoid didalam daun ketepeng adalah sebesar 26,86 mg/mL, paling tinggi dibandingkan dengan beberapa tanaman obat yang diperiksa pada penelitian tersebut.Flavonoid merupakan kelompok senyawa fenol yang mempunyai kecenderungan untuk mengikat protein, sehingga menganggu proses metabolisme bakteri, selain itu flavonoid juga berfungsi sebagai antibakteri dengan cara membentuk senyawa kompleks terhadap protein ekstraseluler yang mengganggu integritas membran sel bakteri. Polifenol pada kadar tinggi dapat menyebabkan koagulasi protein dan menyebabkan sel membran mengalami lisis. Saponin digunakan sebagai antimikroba pada beberapa tahun terakhir.Mekanisme kerja saponin sebagai antibakteri adalah menurunkan tegangan permukaan sehingga mengakibatkan naiknya permeabilitas atau kebocoran sel dan mengakibatkan senyawa intraseluler akan keluar (Robinson, 1995).
Mekanisme kerja tanin sebagai antibakteri adalah menghambat enzim
reverse transkriptase dan DNA topoisomerase sehingga sel bakteri tidak dapat
terbentuk (Robinson, 1995). Tanin memiliki aktifitas antibakteri yang berhubungan dengan kemampuannya untuk menginaktifkan adhesin sel mikroba juga menginaktifkan enzim, dan menggangu transport protein pada pada lapisan dalam sel (Cowan, 1994). Menurut Naim (2004), tanin juga mempunyai target pada polipeptida dinding sel sehingga pembentukan dinding sel menjadi kurang sempurna. Hal ini menyebabkan sel bakteri menjadi lisis karena tekanan osmotik maupun fisik sehingga sel bakteri akan mati.
Ekstrak etanol dan fraksi n- heksana memberikan diameter daerah hambat yang lebih kecil bila dibandingkan dengan fraksi etilasetat.Sedangkan senyawa yang tersari didalam etanol lebih banyak daripada fraksi etil asetat.Hal ini
39
mungkin disebabkan karena adanya kerja yang tidak sinergis antara senyawa metabolit sekunder dalam ekstrak etanol dalam peranannya sebagai antibakteri.
Hasil uji aktivitas antibakteri fraksi n-heksana daun ketepeng merupakan aktivitas antibakteri yang terlemah bila dibandingkan dengan ekstrak etanol dan fraksi etilasetat.Ini disebabkan berdasarkanhasil skrining fitokimia, golongan senyawa yang tersari pada fraksi n-heksan hanya steroid/triterpenoid.
40 BAB V
KESIMPULAN DAN SARAN
5.1 Kesimpulan
Hasil penelitian yang dilakukan terhadap daun ketepeng (Senna alata (L.)Roxb.)diperoleh kesimpulan:
1. Simplisia daun ketepeng memiliki karakteristik berbentuk serbuk dengan serat pendek, warna hijau kecoklatan, berbau khas lemah dan rasa agak kelat, serta diperoleh kadar air 6,62%, kadar sari larut air 20,46%, kadar sari larut etanol 15,40%, kadar abu total 4,14 % dan kadar abu tidak larut dalam asam 0,37%.
2. Simplisia dan ekstrak etanol daun ketepeng mengandung senyawa golongan flavonoid, glikosida, glikosida antrakinon,saponin, tanin, saponin dan steroid/triterpenoid.
3. Ekstrak etanol, fraksi n-heksan dan fraksi etilasetat daun ketepeng memiliki aktivitas antibakteri terhadap Staphylococcus aureus, Staphylococcus
epidermidis, dan Pseudomonas aeruginosa, dimana fraksi etil asetat
menunjukkan aktivitas terbaik dibandingkan dengan ekstrak etanol dan fraksi
n-heksana.
5.2 Saran
Disarankan kepada peneliti selanjutnya untuk melakukan analisis danisolasi senyawa aktif yang berkhasiat sebagai antibakteri.
5 BAB II
TINJAUAN PUSTAKA
2.1 Uraian Tumbuhan
Uraian tumbuhan meliputi morfologi tumbuhan, sistematika, nama daerah dan nama asing, sinonim, manfaat, dan kandungan kimia.
2.1.1 Morfologi
Tumbuhan ketepeng merupakan perdu dengan tinggi ± 5 m. Batang berkayu, bulat, percabangan simpodial, coklat kotor. Daun majemuk berwarna hijau, menyirip genap, anak daun delapan sampai dua puluh empat pasang, bentuk bulat panjang, ujung tumpul, tepi rata, pangkal membulat, panjang 3,5-15 cm, lebar 2,5-9 cm, pertulangan menyirip, tangkai pendek. Bunga majemuk berbentuk tandan dengan kelopak berbagi lima, benang sari tiga, daun pelindung pendek berwarna jingga, mahkota berbentuk kupu-kupu. Buah polong panjang bersegi empat, panjang ± 18 cm dan lebar ± 2,5 cm, masih muda berwarna hijau setelah tua hitam kecoklatan. Biji berbentuk segitiga lancip, pipih, masih muda hijau setelah tua berwarna hitam.Akar tunggang bercabang, bulat dan kehitaman (Anonim, 2016).
2.1.2 Sistematika
Tumbuhan ketepeng (Senna alata (L.)Roxb.)diklasifikasikan sebagai berikut:
Kingdom : Plantae
Divisi : Spermatophyta Bangsa : Fabales
Suku : Fabaceae / Leguminosae
6 Marga : Senna / Cassia
Spesies : Senna alata (L.) Roxb.(Anonim, 2016). 2.1.3 Nama daerah dan nama asing
Ketepeng kebo (Jawa), ketepeng china (Indonesia), ketepeng badak (Sunda), acon-aconan (Madura), sajamera (Halmahera), kupang-kupang (Ternate), tabankun (Tidore), daun kupang, daun kurap, gelenggang, uru’kap (Sumatera),
seven golden candlestick (Inggris), akapulko (Filipina) (Titin, 2008).
2.1.4 Sinonim
Sinonim :Cassia alata L.; Cassia bracteata L.f.; Cassia herpetica Jacq.;
Cassia rumphiana (DC.) Bojer; Herpetica alata (L.)Raf. (Anonim, 2008)
2.1.5 Manfaat
Daun ketepeng digunakan sebagai obat panu, kurap, kudis, sembelit, cacingan, dan sariawan (Titin, 2008).
2.1.6 Kandungan kimia
Daun ketepeng mengandung rein aloe-emodina, rein aloe-emodina-daintron, rein, aloe emodina, asam krisofanat, dihidroksimetilanthraquinone, tanin (Titin, 2008).
2.2 Uraian Kandungan Kimia 2.2.1 Glikosida
Glikosida merupakan suatu senyawa yang biladihidrolisis akan terurai menjadi gula (glikon) dan senyawa lain (aglikon atau genin). Glikosida dibagi atas 4 tipe berdasarkan atom penghubung glikon dan aglikon, yaitu:
a. Tipe O-heterosida atau O-glikosida, jika glikon dan aglikonnya dihubungkan oleh atom O, contohnya : salisin.
7
b. Tipe S-heterosida atau S-glikosida, jika glikon dan aglikonnya dihubungkan oleh atom S, contohnya : sinigrin.
c. Tipe N-heterosida atau N-glikosida, jika glikon dan aglikonnya dihubungkan oleh atom N, contohnya nikleosidin dan kronotosidin.
d. Tipe C-heterosida atau C-glikosida, jika glikon dan aglikonnya dihubungkan oleh atom C, contohnya aloin dan viteksin (Fransworth, 1996).
2.2.2 Flavonoid
Flavonoid merupakan salah satu golongan fenol alam yag terbesar mengandung 15 atom karbon dalam inti dasarnya, yang tersusun dalam konfigurasi C6-C3-C6, yaitu dua cincin aromatis yang dihubungkan oleh satuan
tiga karbon yang dapat atau tidak dapat membentuk cincin ketiga (Markham, 1998).
Flavonoida sering terdapat sebagai glikosida.Flavonoida merupakan kandungan khas tumbuhan hijau yang terdapat pada bagian tumbuhan termasuk daun, akar, kayu, kulit, tepung sari, nectar, bunga, buah buni dan biji.Flavonoida bersifat polar karena mengandung sejumlah hidroksil yang tersulih atau suatu gula (Markham, 1998).
2.2.3 Steroid/triterpenoid
Steroid adalah triterpena yang kerangka dasarnya sistem cincin siklo pentana perhidrofenantren.Triterpenoid adalah senyawa yang kerangka karbonya berasal dari enam satuan isoprena dan secara biosintesis diturunkan dari hidrokarbon C30 asiklik, yaitu skualena.Uji yang biasa digunakan adalah reaksi
Liebermann-Burchard yang dengan kebanyakan triterpen dan steroida memberikan warna hijau-biru.Senyawa triterpenoid dan steroid berstruktur siklik dengan berbagai gugus fungsi yang melekat padanya, seperti gugus alcohol
8
aldehid atau asam karboksilat. Mereka berupa senyawa tidak berwarna, berbentuk kristal, sering kali memiliki titik leleh tinggi dan bersifat aktif optik Triterpenoid dapat dipilah menjadi sekurang-kurangnya empat golongan senyawa : triterpenasebenarnya, steroid, saponin, dan glikosida jantung. Triterpena tertentu menjadi terkenal karena rasanya, terutama kepahitannya (Harborne, 1987).
2.2.4 Saponin
Saponin merupakan senyawa glikosida triterpenoida ataupun glikosida steroida yang merupakan senyawa aktif permukaan dan bersifat seperti sabun serta dapat dideteksi berdasarkan kemampuannya membentuk busa dan menghemolisa sel darah merah (Harborne, 1987).
2.2.5 Tanin
Tanin adalah senyawa yang mampu mengubah kulit hewan yang mentah menjadi kulit siap pakai karena kemampuannya menyambung silang proteina.Tanin tumbuhan dibagi menjadi dua golongan, yaitu tanin terkondensasi dan tanin terhidrolisis.Kadar tanin yang tinggi mempunyai arti penting bagi tumbuhan yakni pertahanan bagi tumbuhan dan membantu mengusir hewan pemakan tumbuhan.Tanin terkondensasi terdapat pada paku-pakuan, gimnospermae, dan angiospermae, sedangkan tanin terhidrolisis penyebarannya terbatas pada tumbuhan berkeping dua.Beberapa tanin terbukti mempunyai antioksidan dan menghambat pertumbuhan tumor (Harborne, 1987).
2.2.6. Glikosida antrakinon
Glikosida antrakinon, golongan glikosida ini aglikonnya adalah sekerabat dengan antrasena yang memiliki gugus karbonil pada kedua atom C yang berseberangan (atom C9dan C10) atau hanya C9 (antron) dan C9 ada gugus
hidroksil (antranol) (Gunawan dan Mulyani, 2004).
9
Senyawa antrakinon dan turunannya seringkali bewarna kuning sampai merah sindur (oranye), larut dalam air panas atau alkohol encer. Untuk identifikasi digunakan reaksi Borntraeger.Antrakuinon yang mengandung gugus karboksilat (rein) dapat diekstraksi dengan penambahan basa, misalnya dengan natrium bikarbonat.Hasil reduksi antrakinon adalah antron dan antranol, terdapat bebas di alam atau sebagai glikosida.Antron bewarna kuning pucat, tidak menunjukkan fluoresensi dan tidak larut dalam alkali, sedangkan isomemya, yaitu antranol bewarna kuning kecoklatan dan dengan alkali membentuk larutan berpendar (berfluoresensi) kuat.Oksantron merupakan zat antara (intermediate) antara antrakinon dan antranol. Reaksi Borntraeger modifikasi Fairbairn, yaitu dengan menambahkan hydrogen peroksida akan menujukkan reaksi positif. Senyawa ini terdapat dalam Frangulae cortex.Diantron adalah senyawa dimer tunggal atau campuran dari molekul antron, hasil oksidasi antron (Gunawan dan Mulyani, 2004).
Antrakuinon termasuk senyawa yang tidak berbahaya, tidak menimbulkan ketagihan, kebiasaan, ataupun tidak menimbulkan toleransi terhadap manusia.Antanol dan antron memiliki sifat reduksi yang kuat.Sifat ini sering dijadikan sebagai pelengkap ramuan dari obat-obat antiseptik tertentu untuk beberapa penyakit kulit, misalnya pemakaian krisarobin dalam psoriasis, eksim kering dan penyakit kulit karena berbagai jamur, juga pemakaian aloe sebagai antiseptik untuk luka pada pengobatan veteriner (Gunawan dan Mulyani, 2004).
10 2.3Ekstrak
2.3.1 Pengertian ekstrak
Ekstrak adalah sediaan pekat yang diperoleh dengan mengekstraksi zat aktif dari simplisia nabati atau simplisia hewani menggunakan pelarut yang sesuai, kemudian semua atau hamper semua pelarut diuapkan dan massa atau serbuk yang tersisa diperlakukan sedemikian hingga memenuhi baku yang telah ditetapkan (Depkes, RI., 1995). Ekstraksi adalah suatu proses yang dilakukan untuk memperoleh kandungan senyawa kimia dari jaringan tumbuhan maupun hewan (Depkes, RI., 1979).
2.3.2 Metode ekstraksi
Menurut Ditjen POM RI (2000), beberapa metode ekstraksi yaitu: 1. Cara dingin
a. Maserasi, adalah proses penyarian simplisia dengan cara perendaman menggunakan pelarut dengan sesekali pengadukan pada suhu kamar. Maserasi yang dilakukan dengan pengadukan secara terus menerus disebut dengan maserasi kinetik, sedangkan yang dilakukan pengulangan penambahan pelarut setelah dilakukan penyaringan terhadap maserat pertama dan seterusnya disebut remaserasi.
b. Perkolasi, adalah proses penyarian simplisia dengan pelarut yang selalu baru sampai terjadi penyarian sempurna yang umumnya dilakukan pada temperatur kamar. Proses perkolasi terdiri dari tahap pengembangan bahan, tahap maserasi antara, tahap perkolasi sebenarnya (penetesan/ penampungan ekstrak) terus menerus sampai diperoleh perkolat.
2. Cara panas
a. Refluks, adalah proses penyarian simplisia dengan menggunakan alat pada
11
temperatur titik didihnya, selama waktu tertentu dan jumlah pelarut terbatas yang relatif konstan dengan adanya pendingin balik.
b. Digesti,adalahproses penyarian dengan pengadukan kontinu pada temperaturelebih tinggi dari temperatur ruangan, yaitu secara umum dilakukan pada temperatur 40-50oC.
c. Sokletasi, adalah proses penyarian dengan menggunakan pelarut yang selalu baru, dilakukan menggunakan alat soklet sehingga terjadi ekstraksi kontinu dengan pelarut relatif konstan dengan adanya pendingin balik.
d. Infudansi, adalah proses penyarian dengan menggunakan pelarut air pada temperatur 90oC selama 15 menit.
e. Dekoktasi, adalah proses penyarian dengan menggunakan pelarut air pada temperatur 90oC selama 30 menit.
2.4 Fraksinasi
Fraksinasi adalah suatu metode pemisahan senyawa organik berdasarkan kelarutan senyawa-senyawa tersebut dalam dua pelarut yang tidak saling bercampur, biasanya antara pelarut air dan pelarut organik (Soebagio, 2005).
Teknik pemisahan ekstraksi cair-cair ini dilakukan dengan menggunakan corong pisah.Kedua pelarut yang saling tidak bercampur tersebut dimasukkan ke dalam corong pisah, kemudian digojok dan didiamkan.Senyawa organik akan terdistribusi ke dalam fasenya masing-masing bergantung pada kelarutannya terhadap fase tersebut dan kemudian akan terbentuk dua lapisan yang dapat dipisahkan dengan membuka kunci pipa corong pisah (Odugbemi, 2008).
Ekstrak dipartisi dengan menggunakan peningkatan polaritas pelarut seperti petroleum eter, n-heksana, kloroform, etilasetat dan etanol. Pemilihan
12
pelarut pada ekstraksi bergantung pada sifat analitnya dimana pelarut dan analit harus memiliki sifat yang sama, contohnya analit yang sifat lipofilitasnya tinggi akan terekstraksipada pelarut yang relatif nonpolar seperti n-heksana sedangkan analit yang semipolar terlarut pada pelarut yang semipolar (Venn, 2008).
2.5 Bakteri
Bakteri adalah mikroorganisme bersel satu, berbentuk bola, batang atau spiral berdiameter sekitar 0,5-1,0 µm dan panjangnya 1,5-2,5 µm (Dwijoseputro, 1994). Nama bakteri berasal dari kata “bakterion” dari bahasa Yunani yang berarti tongkat atau batang. Sekarang nama itu dipakai untuk menyebut sekelompok mikroorganisme yang bersel satu, tidak berklorofil, berkembangbiak dengan pembelahan diri, serta demikian kecilnya sehingga hanya tampak dengan mikroskop. (Gibson, 1996).
Pertumbuhan dan perkembangan bakteri dipengaruhi oleh: 1. Zat makanan (nutrisi)
Sumber zat makanan bagi bakteri diperoleh dari senyawa karbon, nitrogen, sulfur, fosfor, unsur logam (natrium, kalsium, magnesium, mangan, besi, tembaga dan kobalt), vitamin dan air untuk fungsi metabolik dan pertumbuhannya.
2. Keasaman dan kebasaan (pH)
Kebanyakan bakteri tumbuh optimum pada pH antara 6,5 - 7,5. Namun, beberapa spesies dapat tumbuh dalam keadaan sangat asam atau basa.
3. Temperatur
Proses pertumbuhan bakteri tergantungpada reaksi kimiawi dan laju reaksi kimia yang dipengaruhi oleh temperatur. Maka diklasifikasikan menjadi:
a. Bakteri psikrofil, yaitu bakteri yang dapat hidup pada temperatur 0 - 30oC,
13
dengan temperatur optimum adalah 10 - 20oC.
b. Bakteri mesofil, yaitu bakteri yang dapat hidup pada temperatur 5 - 60oC, temperatur optimum adalah 25 - 40oC.
c. Bakteri termofil, yaitu bakteri yang dapat hidup pada temperatur optimumadalah 55 - 65oC.
4. Oksigen
a. Aerobik, yaitu bakteri yang butuh oksigen dalam pertumbuhannya. b. Anaerobik, yaitu bakteri yang dapat tumbuh tanpa oksigen.
c. Anaerobik fakultatif, yaitu bakteri yang dapat tumbuh dengan oksigen ataupun tanpa oksigen.
d. Mikroaerofilik, yaitu bakteri yang dapat tumbuh baik dengan adanya sedikit oksigen.
5. Tekanan osmosa
Medium yang baik bagi pertumbuhan bakteri adalah medium isotonis terhadap isi sel bakteri.
6. Kelembaban
Secara umum bakteri tumbuh dan berkembang biak dengan baik pada lingkungan yang lembap. Kebutuhan akan air tergantung dari jenis bakterinya (Pelczar, et al.,1988)
2.5.1 Morfologi bakteri
Berdasarkan morfologinya bakteri dapat dibedakan atas tiga bagian yaitu: Bentuk basil
Bakteri yangmempunyai bentuk batang atau silinder, membelah dalam satu bidang, berpasangan ataupun bentuk rantai pendek atau panjang. Bakteri bentuk basil dapat dibedakan atas:
14
a. Monobasil yaitu basil yang terlepas satu sama lain dengan kedua ujung tumpul.
b. Diplobasil yaitu basil yang bergandeng dua dan kedua ujungnya tumpul. c. Streptobasil yaitu basil yang bergandengan panjang dengan kedua ujung
tajam.
Contoh bakteri dengan bentuk basil adalahEschericia coli, Bacillus
anthracis, Salmonella typhimurium dan Shigella dysentriae.
Bentuk kokus
Merupakan bakteri yang bentuknya seperti bola-bola kecil, ada yang hidup sendiri dan ada yang berpasang-pasangan. Bakteri bentuk kokus dapat dibedakan atas:
a. Diplokokus yaitu kokus yang bergandeng dua. b. Tetrakokus yaitu kokus yang mengelompok empat.
c. Stafilokokus yaitu kokus yang mengelompok dan membentuk anggur. d. Streptokokus yaitu kokus yang bergandengan panjang menyerupai rantai. e. Sarsina yaitu kokus yang mengelompok seperti kubus.
Contoh bakteri dengan bentuk kokus adalahStaphylococcus aureus,
Sarcina luten, Diplococcus pneumonia dan Streptococcus lactis.
Bentuk spiral
Dibedakan atas:
a. Spiral yaitu menyerupai spiral atau lilitan.
b. Vibrio yaitu bentuk batang yang melengkung berupa koma.
c. Spirochaeta yaitu menyerupai bentuk spiral, bedanya dengan spiral dalam kemampuannya melenturkan tubuhnya sambil bergerak.
Contoh bakteri dengan bentuk spiral adalah Vibrio cholera dan
15
Spirochaeta palida (Volk dan Wheeler, 1989).
2.5.2Staphylococcus aureus
Staphylococcus aureusmerupakan bakteri gram positif, aerob dan anaerob
fakultatif berbentuk bola atau kokus berkelompok tidak teratur, diameter 0,8 – 1,0 µm, tidak membentuk spora atau tidak bergerak, koloni berwarna kuning. Bakteri ini tumbuh pada suhu 37oC tetapi paling baik membentuk pigmen pada suhu 20-25oC.Koloni pada pembenihan padat berbentuk bulat halus, menonjol, dan berkilau membentuk berbagai pigmen.Bakteri ini terdapat pada kulit, selaput lendir, bisul, dan luka. Dapat menimbulkan penyakit melalui kemampuannya berkembang biak dan menyebar luas dalam jaringan (Jawetz, et al., 2007).
Staphylococcus aureushidup sebagai saprofit di dalam saluran-saluran
pengeluaran lendir dari tubuh manusia dan hewan seperti hidung, mulut, tenggorokan dan dapat pula dikeluarkan pada waktu batuk atau bersin.Selain dapat menyebabkan intoksikasi, bakteri ini juga dapat menyebabkan berbagai macam infeksi seperti jerawat, bisul, meningitis, osteomielitis, pneumonia, dan mastitis pada manusia dan hewan (Supardi dan Sukamto, 1999).Adapun sistematika dari bakteri Staphylococcus aureus yaitu:
Divisi : Schizophyta Kelas : Schizomycetes Bangsa :Eubacteriales Suku : Micrococcaceae Marga : Staphylococcus
Spesies : Staphylococcus aureus(Holt, et al., 1988).
2.5.3Staphylococcus epidermidis
16
Merupakan bakteri gram positif, aerob atau anaerob fakultatif berbentuk bola atau kokus berkelompok tidak teratur, diameter 0,8 – 1,0 um tidak membentuk spora dan tidak bergerak, koloni berwarna putih bakteri ini tumbuh cepat pada suhu 37C tetapi paling baik membentuk pigmen pada suhu kamar 20C. koloni pada pembenihan padat berbentuk bulat halus, menonjol, berkilau, tidak menghasilkan pigmen, berwarna putih porselen sehingga Staphylococcus
epidermidis disebut Staphylococcus albus, koagulasi negatif dan tidak meragi
manitol. Staphylococcus epidermidis terdapat pada kulit, selaput lendir, bisul dan luka. Dapat menimbulkan penyakit melalui kemampuannya berkembang biak dan menyebar luas dalam jaringan(Jawetz, et al., 2007). Adapun sistematika
Staphylococcus epidermidis adalah (Breed, 1957):
Divisi : Bacteriophyta Kelas : Schizomycetes Bangsa : Eubacteriales Suku : Microciccaceae Marga : Staphylococcus
Jenis : Staphylococcus epidermidis 2.5.4 Pseudomonas aeruginosa
Organisme ini merupakan basilus gram-negatif yang motil dan hidup dalam suasana aerob.Bakteri ini terdapat dimana-mana pada lingkungan, tetapi jarang pada flora orang sehat.Jumlah pembawa meningkat dengan perawatan inap rumah sakit. Lingkungan yang lembap merupakan habitat Pseudomonas
aeruginosa, seperti bak cuci dan keran air (Gillespie dan Bamford, 2008)
Pseudomonas aeruginosa memproduksi sitotoksin dan protease (misalnya
17
eksotoksin A dan S, hemolisis, dan etalase). Luka bakar dapat terkoloni menyebabkan septikemia sekunder akibat Pseudomonas aeruginosa.Septikemia dengan mortalitas tinggi merupakan anacaman tersendiri bagi pasien neutropenia (Gillespie dan Bamford, 2008). Sistematika Pseudomonas aeruginosa adalah (Breed, 1957):
Divisi : Eukariota Kelas : Schizomycetes Bangsa : Pseudomonadales Suku : Pseudomonadaceae Marga : Pseudomonas
Jenis : Pseudomonas aeruginosa
2.6 Fase Pertumbuhan Mikroorganisme
Ada empat macam fase pertumbuhan mikroorganisme, yaitu fase lag, fase log (fase esksponensial), fase stasioner dan fase kematian.
a. Fase lag
Fase lag merupakan fase adaptasi, yaitu fase penyesuaian mikroorganisme pada suatu lingkungan baru. Ciri fase lag adalah tidak adanya peningkatan jumlah sel, yang ada hanyalah peningkatan ukuran sel. Lama fase lag tergantung pada kondisi dan jumlah awal mikroorganisme dan media pertumbuhan. Bila sel- sel mikroorganisme diambil dari kultur yang sama sekali berlainan, maka yang sering terjadi adalah mikroorganisme tersebut tidak mampu tumbuh dalam kultur.
b. Fase log (fase esksponensial)
Fase ini merupakan fase dimana mikroorganisme tumbuh dan membelah pada kecepatan maksimum, namun tergantung pada genetika mikroorganisme,
18
sifat media, dan kondisi pertumbuhan. Sel baru terbentuk dengan laju konstan dan massa yang bertambah secara eksponensial. Hal atau keadaan yang dapat menghambat laju pertumbuhan adalah bila satu atau lebih nutrisi dalam kultur habis, sehingga hasil metabolisme yang bersifat racun akan tertimbun dan menghambat pertumbuhan.
c. Fase stationer
Fase ini merupakan fase dimana pertumbuhan mikroorganisme terhenti dan terjadi keseimbangan antara jumlah sel yang membelah dengan jumlah sel yang mati. Terdapat kehilangan sel yang lambat karena kematian diimbangi oleh pembentukan sel-sel baru melalui pertumbuhan dan pembelahan dengan nutrisi yang dilepaskan oleh sel-sel yang mati karena mengalami lisis. d. Fase kematian
Fase ini merupakan fase dimana jumlah sel yang mati meningkat.Faktor penyebabnya adalah ketidaktersediaan nutrisi dan akumulasi produk buangan yang toksik (Pratiwi, 2008).
2.6 Pengukuran Aktivitas Antibakteri
Penentuan kepekaan bakteri patogen terhadap agen antibakteri tertentu dapat dilakukan beberapa metode berikut ini, dimana setiap metode memiliki kelebihan dan kekurangannya masing-masing.
a. Metode dilusi
Metode ini digunakan untuk mengukur kadar hambat minimum (KHM) dan kadar bunuh minimum (KBM). Cara yang dilakukan yaitu dengan membuat seri pengenceran agen antimikroba pada media yang telah ditambahkan dengan mikroba uji. Larutan uji agen antimkroba pada kadar terkecil yang terlihat jernih
19
tanpa adanya pertumbuhan mikroba uji ditetapkan sebagai KHM. Larutan yang ditetapkan sebagai KHM tersebut selanjutnya dikultur ulang pada media tanpa penambahan mikroba uji ataupun agen antimikroba, dan diinkubasi selama 18 – 24 jam.Media yang tetap terlihat jernih setelah diinkubasi ditetapkan sebagai KBM (Pratiwi, 2008).
b. Metode difusi agar
Metode yang paling sering digunakan dan biasanya menggunakan cakram. Ada beberapa jenis cakram yaitu cakram kertas, cakram silinder dan punch hole. Cakram tersebut yang berisi sejumlah tertentu obat ditempatkan pada permukaan medium padat yang sebelumnya telah diinokulasi bakteri uji pada permukaannnya.Setelah diinkubasi, diameter zona hambatan sekitar cakram dipergunakan untuk mengukur kekuatan hambatan obat terhadap mikroorganisme yang uji (Pratiwi, 2008).
c. Metode Bioautografi
Metode bioautografi merupakan metode spesifik untuk mendeteksi bercak pada kromatogram hasil KLT (kromatografi lapis tipis) yang mempunyai aktivitas antibakteri, antifungi, dan antivirus.Keuntungan metode ini adalah sifatnya yang efisien untuk mendeteksi senyawa antimikroba karena letak bercak dapat ditentukan walaupun berada dalam campuran yang kompleks sehingga memungkinkan untuk mengisolasi senyawa aktif tersebut.Kerugiannya adalah metoda ini tidak dapat digunakan untuk menentukan KHM dan KBM (Pratiwi, 2008).
1 BAB I PENDAHULUAN 1.1 Latar Belakang
Dewasa ini, penggunaan tanaman obat semakin diperhatikan dengan berbagai alasan. Diantaranya karena biaya pengobatan secara medis yang semakin mahal, adanya efek samping untuk pemakaian obat kimiawi jangka panjang, maupun kesembuhan melalui cara medis yang tidak 100% khususnya untuk penyakit kronis (Hariana, 2011). Khasiat tanaman obat di Indonesia masih banyak berdasarkan data empiris, sehingga perlu dibuktikan secara ilmiah.Bukti-bukti ilmiah akan lebih meyakinkan masyarakat dalam menggunakan obat tradisional (Muhlisah, 2001).
Salah satu tanaman obat yang sering digunakan untuk pengobatan tradisional adalah ketepeng (Senna alata (L.)Roxb.)termasuk ke dalam suku Leguminosae. Bagian dari tanaman ini yang digunakan sebagai obat adalah daunnya untuk mengobati sembelit, sariawan, dan infeksi bakteri seperti ulkus kulit, sifilis, bronkitis, infeksi jamur seperti panu, kurap, dan eksim (Yacob, 2009). Secara tradisional masyakarat pesisir Riau menggunakan daun ketepeng untuk mengobati infeksi kulit terutama penyakit kudis dengan mengambil ± 10 gram daun segar, dicuci lalu ditumbuk sampai lumat dan ditempelkan pada lokasi infeksi (Anonim, 2016). Penelitian menunjukkan bahwa aktifitas antibakteri daun ketepeng dikarenakan adanya senyawa-senyawa kimia seperti fenol, tanin, saponin, steroid, flavonoid, dan karbohidrat (Owoyale, 2005).
Beberapa bakteri yang dapat menyebabkan penyakit infeksi pada kulit antara lain bakteri Staphylococcus aureus, Staphylococcus epidermidis, danPseudomonas aeruginosa.Staphylococcus aureus merupakan salah satu
2
bakteri patogen utama pada manusia.Sumber utama infeksi ini adalah pada luka-luka yang terbuka, benda-benda yang terkontaminasi luka-luka, serta saluran napas dan kulit manusia (Jawetz, 2007).Sedangkan Staphylococcus epidermidis merupakan bakteri penyebab infeksi kulit yang ringan yang disertai pembentukan abses.Pseudomonas aeruginosa merupakan bakteri penyebab 10-20% infeksi nosokomial.Sering diisolasi dari penderita dengan neoplastik, luka, dan luka bakar yang berat.Bakteri ini juga dapat menyebabkan infeksi pada saluran pernapasan bagian bawah, saluran kemih, mata, dan lain-lainnya (Warsa, 1994).
Penelitian sebelumnya menunjukkan bahwa ekstrak metanol daun ketepeng efektif menghambat pertumbuhan bakteri Staphylococcus aureus dan
Pseudomonas aeruginosa secara invitro dengan konsentrasi hambat minimum
masing-masing 12 mg/ml dan 20 mg/ml (Doughari, 2007), akan tetapi pada penelitian tersebut tidak menggunakan pelarut etanol dan belum sampai pada tahap fraksinasi. Fraksinasi adalah suatu metode pemisahan senyawa organik berdasarkan kelarutan senyawa-senyawa tersebut dalam dua pelarut yang tidak saling bercampur, biasanya antara pelarut air dan pelarut organik.(Soebagio, 2005).
Berdasarkan hal tersebut di atas penulis melakukan pengujian aktivitas antibakteri ekstrak serta fraksi n-heksan dan etilasetat daun ketepeng (Senna alata (L.)Roxb.)terhadap bakteri Staphylococcus aureus, Staphylococcus epidermidis, dan Pseudomonas aeruginosa yang merupakan beberapa bakteri yang menyebabkan infeksi pada kulit. Untuk mengetahui golongan senyawa kimia yang dikandung, dilakukan skirining fitokimia terhadap simplisia, ekstrak, fraksi n-heksan dan fraksi etil asetat daun ketepeng serta dilakukan karakterisasi simplisia daun ketepeng.
3 1.2 Perumusan Masalah
Berdasarkan latar belakang diatas, maka permasalahannya adalah:
a. golongan senyawa kimia apa yang terdapat dalam simplisia daun ketepeng?
b. bagaimana karakteristik dari simplisia daun ketepeng?
c. apakah ekstrak etanol, fraksi n-heksana dan fraksi etilasetat daun ketepeng memiliki aktivitas antibakteri terhadap Staphylococcus aureus,
Staphylococcus epidermidis, dan Pseudomonas aeruginosa.
1.3 Hipotesis
Berdasarkan permasalahan diatas, maka hipotesis penelitian ini adalah: a. golongan senyawa kimia yang ada didalam simplisia daun ketepeng adalah
tanin, saponin, glikosida, flavonoid, dan fenol.
b. karakteristik simplisia daun ketepeng memenuhi persyaratan MMI.
c. ekstrak etanol, fraksi n-heksana dan fraksi etilasetat daun ketepeng mempunyai aktivitas antibakteri terhadap bakteri Staphylococcus aureus,
Staphylococcus epidermidis, dan Pseudomonas aeruginosa.
1.4 Tujuan Penelitian
Adapun tujuan penelitian ini untuk:
a. mengetahui golongan senyawa kimia pada simplisia daun ketepeng. b. mengetahui karakteristik dari simplisia daun ketepeng.
c. mengetahui adanya aktivitas antibakteri ekstrak etanol, fraksi n-heksana danfraksietilasetatdaunketepengterhadapbakteriStaphylococcusaureus,
Staphylococcus epidermidis, dan Pseudomonas aeruginosa.