UJI STABILITAS ASPIRIN PADA CANGKANG KAPSUL ALGINAT YANG DITAMBAHKAN BAHAN PEMBURAM TITANIUM DIOKSIDA
DAN DIKEMAS DENGAN ALUMINIUM FOIL SEBAGAI SEDIAAN LEPAS TUNDA
SKRIPSI
OLEH:
RUDI YANTO ANTONO NIM 081501004
PROGRAM STUDI SARJANA FARMASI FAKULTAS FARMASI
UNIVERSITAS SUMATERA UTARA MEDAN
UJI STABILITAS ASPIRIN PADA CANGKANG KAPSUL ALGINAT YANG DITAMBAHKAN BAHAN PEMBURAM TITANIUM DIOKSIDA
DAN DIKEMAS DENGAN ALUMINIUM FOIL SEBAGAI SEDIAAN LEPAS TUNDA
SKRIPSI
Diajukan untuk melengkapi salah satu syarat untuk memperoleh
Gelar Sarjana Farmasi pada Fakultas Farmasi
Universitas Sumatera Utara
OLEH:
RUDI YANTO ANTONO NIM 081501004
PROGRAM STUDI SARJANA FARMASI FAKULTAS FARMASI
UNIVERSITAS SUMATERA UTARA MEDAN
PENGESAHAN SKRIPSI
UJI STABILITAS ASPIRIN PADA CANGKANG KAPSUL ALGINAT YANG DITAMBAHKAN BAHAN PEMBURAM TITANIUM DIOKSIDA
DAN DIKEMAS DENGAN ALUMINIUM FOIL SEBAGAI SEDIAAN LEPAS TUNDA
OLEH:
RUDI YANTO ANTONO NIM 081501004
Dipertahankan di Hadapan Panitia Penguji Skripsi Fakultas Farmasi Universitas Sumatera Utara
Pada Tanggal: Juni 2012
Disetujui Oleh:
Pembimbing I, Panitia Penguji,
Prof. Dr. Hakim Bangun, Apt. Prof. Dr. Karsono, Apt.
NIP 195201171980031002 NIP 195404121987012001
Pembimbing II, Prof. Dr. Hakim Bangun, Apt.
NIP 195201171980031002
Dra. Anayanti Arianto, M.Si., Apt. Dra. Saodah, M.Sc., Apt.
NIP 195306251986012001 NIP 194901131976032001
Dra. Lely Sari Lubis, M.Si., Apt.
NIP 195404121987012001
Medan, Juni 2012
Fakultas Farmasi Universitas Sumatera Utara
Dekan,
KATA PENGANTAR
Puji syukur kehadirat Tuhan Yang Maha Kuasa yang telah melimpahkan rahmat dan karunia-Nya, sehingga penulis dapat menyelesaikan skripsi dengan judul “Uji Stabilitas Aspirin Pada Cangkang Kapsul Alginat Yang Ditambahkan Bahan Pemburam Titanium Dioksida dan Dikemas Dengan Aluminium Foil Sebagai Sediaan Lepas Tunda”.
Skripsi ini diajukan sebagai salah satu syarat guna memperoleh gelar Sarjana Farmasi dari Fakultas Farmasi Universitas Sumatera Utara. Pada kesempatan ini dengan segala kerendahan hati, penulis mengucapkan terima kasih yang sebesar-besarnya kepada:
1. Bapak Prof. Dr. Sumadio Hadisahputra, Apt., selaku Dekan Fakultas Farmasi yang telah memberikan izin fasilitas sehingga penulis dapat menyelesaikan pendidikan.
2. Bapak Prof. Dr. Hakim Bangun Apt., dan Ibu Dra. Anayanti Arianto, M.Si., Apt., yang telah membimbing dan memberikan petunjuk serta saran-saran selama penelitian hingga selesainya skripsi ini.
3. Bapak Prof. Dr. Karsono, Apt., Ibu Dra. Leli Sari Lubis, M.Si., Apt., dan Ibu Dra. Saodah, M.Sc., Apt., selaku penguji yang telah memberi kritik dan saran demi kesempurnaan skripsi ini.
4. Bapak Drs. David Sinurat, M.Si., Apt., selaku Kepala Laboratorium Farmasi Fisik Fakultas Farmasi Universitas Sumatera Utara Medan yang telah memberikan izin dan fasilitas untuk penulis sehingga dapat mengerjakan dan menyelesaikan penelitian.
5. Ibu Dra. Fat Aminah, M.Sc., Apt., selaku Kepala Laboratorium Formulasi Sediaan Solid Fakultas Farmasi Universitas Sumatera Utara Medan yang telah memberikan izin dan fasilitas untuk penulis sehingga dapat mengerjakan dan menyelesaikan penelitian.
Utara Medan dan Kak Mustika Furi dan Bang Abdi selaku Operator Laboratorium Penelitian Fakultas Farmasi Universitas Sumatera Utara yang telah memberikan fasilitas kepada penulis selama pelaksanaan penelitian.
7. Ayah Ahmad Joni Antono dan Ibu Juliana yang telah memberikan cinta, kasih sayang, dan doa yang tulus serta pengorbanan baik materi maupun non-materi.
8. Saudari Leny dan seluruh teman-teman Farmasi USU stambuk 2008 yang tidak dapat disebutkan namanya satu per satu, atas segala dorongan motivasi dan bantuannya kepada penulis hingga selesainya penulisan skripsi ini.
Penulis menyadari sepenuhnya bahwa dalam penulisan skripsi ini masih jauh dari kesempurnaan. Oleh karena itu dengan segala kerendahan hati, penulis menerima kritik dan saran demi kesempurnaan skripsi ini.
Akhirnya, penulis berharap semoga skripsi ini dapat memberi manfaat bagi kita semua.
Medan, 25 Juni 2012 Penulis,
Rudi Yanto Antono
Uji Stabilitas Aspirin pada Cangkang Kapsul Alginat yang Ditambahkan Bahan Pemburam Titanium Dioksida dan Dikemas Dengan Aluminium Foil
Sebagai Sediaan Lepas Tunda
Abstrak
Aspirin merupakan bahan yang mudah terhidrolisis. Aspirin yang disimpan dalam cangkang kapsul alginat tanpa menggunakan bahan pemburam Titanium dioksida (TiO2) tidak stabil selama penyimpanan. Oleh karena itu, perlu perhatian khusus pada proses penyimpanan dan formulasi cangkang kapsul sehingga stabilitas dalam kapsul menjadi lebih baik. Tujuan utama penelitian ini adalah untuk mengetahui pengaruh penyimpanan terhadap stabilitas kimia dan fisika Aspirin dan stabilitas fisik cangkang kapsul alginat yang mengandung TiO2 dengan menggunakan pengemas aluminium foil (strip).
Pengujian stabilitas kimia Aspirin dalam kapsul alginat yang mengandung TiO2 dilakukan dengan penetapan kadar Aspirin setelah penyimpanan selama 3 bulan secara spektrofotometer ultraviolet yang diukur pada panjang gelombang 296,3 nm. Stabilitas fisik Aspirin dalam cangkang kapsul alginat yang mengandung TiO2 meliputi pengamatan warna, kerapuhan, waktu hancur dan laju pelepasan. Warna diamati secara visual, kerapuhan kapsul diuji dengan capsule shell impact tester
Hasil penelitian pada pengujian terhadap stabilitas kimia Aspirin dalam kapsul alginat yang menggunakan TiO
, waktu hancur diuji dengan alat desintegration tester, dan uji pelepasan dilakukan dengan menggunakan alat disolusi metode dayung dalam medium pH berganti kemudian diukur dengan spektrofotometer ultraviolet pada panjang gelombang 237 nm pada medium pH 1,2 dan 296,3 nm pada medium 6,8.
2 dalam pengemas aluminium foil selama 3 bulan menunjukkan adanya perbedaan kadar Aspirin dengan sebelum penyimpanan. Pada penyimpanan suhu 30°C, RH (Relative Humidity) 70% selama 3 bulan kadar Aspirin masih memenuhi persyaratan (98,60%), tetapi pada penyimpanan suhu 40°C, RH 75% kadar Aspirin menjadi tidak memenuhi persyaratan (91,67%). Pada pengujian stabilitas fisik Aspirin dalam kapsul alginat dengan pengamatan secara visual, warna serbuk Aspirin tidak mengalami perubahan, warna cangkang kapsul tidak berubah selama penyimpanan suhu 30°C, RH 70% sementara pada suhu 40°C, RH 75% warna cangkang kapsul mulai kecoklatan dan keseluruhan kapsul tidak menunjukkan kerapuhan. Pelepasan Aspirin juga dipengaruhi oleh penyimpanan di mana pada suhu 40°C, RH 75% memiliki perbedaan dengan pelepasan Aspirin sebelum penyimpanan, yaitu dibuktikan dengan uji statistik independent t-test. Dapat disimpulkan bahwa penyimpanan mempengaruhi stabilitas kimia Aspirin dimana kadar Aspirin mengalami penurunan setelah penyimpanan dan stabilitas fisik berupa warna serbuk Aspirin tidak berubah, warna cangkang kapsul berubah dan kapsul tidak rapuh, dan pelepasan Aspirin menunjukkan perbedaan dengan sebelum penyimpanan, yaitu pelepasannya menjadi semakin lambat.
The Stability Test of Aspirin in Alginate Capsule Shell Used Titanium Dioxide as Opacifying Agent and Packaged Using Aluminium Foil As
Delayed Release Dossage Form
Abstract
Aspirins is an easily hydrolyzed material. Aspirin which was encapsulated in alginate capsule shell without using Titanium dioxide (TiO2) as opacifying agent was not stable during storage. Therefore, it is needed a special attention in storage and the formulation of the capsules shell so that the stability of the capsules are better. The main objective of this study was to examine the effect of storage condition on chemical and physical stability of Aspirin loaded into alginate capsule containing TiO2
The chemical stability test of Aspirin encapsulated in alginate capsule containing TiO
that packaged with aluminium foil.
2 was done by determining Aspirin content after 3 months storage using UV spectrofotometer at wavelength 296,3 nm. The physical stability of Aspirin encapsulated in alginate capsule shell containing TiO2
The results of chemical stability test of Aspirin encapsulated in alginate capsules containing TiO
included observations of colour, brittleness, desintegration time and the release rate. Colour was observed visually, the brittleness of the capsule was tested using capsule shell impact tester, desintegration time was tested using the desintegration tester, and release rate was tested by using a paddle method dissolution in changing pH medium and measured by UV-spectrophotometer at wavelength of 237.0 nm in pH 1.2 medium and 296.3 nm in pH 6.8 medium. Storage performed at a temperature of 30°C, 70% RH and a temperature of 40°C, 75% RH for 3 months.
2 an packaged with aluminum foil for 3 months showed that there was a difference in Aspirin content before and after storage. When stored at 30°C, RH 70% for 3 months, Aspirin content still fulfill the requirement (98.60%), but when stored at 40°C, RH 75%, Aspirin content did not fulfill the requirement (91.67%). The physical stability test showed that there was no effect of storage on the brittleness of the storage for 3 months at a temperature of 30°C RH 70%, and 40°C RH 75%. Colour of Aspirin and capsules shell had no change when stored at 30°C RH 70%, but when stored at 40°C RH 75%, capsules shell become brownish. The release of Aspirin in storage for 3 months at a temperature of 40°C, RH 75% showed a difference in the release rate of Aspirin prior to storage which the release was slower than prior. It can be concluded that the physical stability during storage alginate capsule shell using TiO2
Key words: Aspirin, stability, packaging
with aluminum
DAFTAR ISI
Halaman
HALAMAN JUDUL ... i
HALAMAN PENGESAHAN ... iii
KATA PENGANTAR ... iv
ABSTRAK ... vi
ABSTRACT ... vii
DAFTAR ISI ... viii
DAFTAR TABEL ... xv
DAFTAR GAMBAR ... xvi
DAFTAR LAMPIRAN ... xviii
BAB I PENDAHULUAN ... 1
1.1 Latar Belakang ... 1
1.2 Kerangka Pikir Penelitian ... 3
1.3 Perumusan Masalah ... 4
1.4 Hipotesis Penelitian ... 5
1.5 Tujuan Penelitian ... 6
1.6 Manfaat Penelitian ... 7
BAB II TINJAUAN PUSTAKA ... 8
2.1 Aspirin ... 8
2.1.2 Farmakologi Aspirin ... 9
2.1.2.1 Aspirin Sebagai Anti Inflamasi ... 9
2.1.2.2 Aspirin Sebagai Analgesik ... 9
2.1.2.3 Aspirin Sebagai Antipiretik ... 9
2.1.2.4 Aspirin Sebagai Anti Agregasi Platelet ... 9
2.1.3 Efek Samping Aspirin ... 10
2.2 Kapsul ... 10
2.3 Natrium Alginat ... 12
2.4 Titanium Dioksida ... 14
2.5 Polimer ... 15
2.5.1 Polietilen Glikol (PEG) ... 15
2.6 Stabilitas Fisik Cangkang Kapsul Gelatin dan HPMC ... 16
2.6.1 Warna ... 16
2.6.2 Kerapuhan ... 17
2.6.3 Waktu Hancur ... 19
2.7 Viskositas ... 19
2.8 Studi Stabilitas ... 20
2.8.1 Uji Dipercepat ... 20
2.8.2 Pengujian Jangka Panjang atau Waktu Nyata ... 20
2.8.3 Pengujian Pasca Pemasaran ... 20
2.9 Pengujian Stabilitas ... 20
2.9.2 Kerapuhan ... 21
2.9.3 Disolusi ... 21
2.10 Pengemasan ... 24
2.11 Pengukuran Hasil Disolusi Aspirin Menggunakan Spektrofotometer UV ... 24
BAB III METODE PENELITIAN ... 26
3.1 Alat-Alat ... 26
3.2 Bahan-Bahan ... 26
3.3 Prosedur Penelitian ... 27
3.3.1 Pembuatan Pereaksi ... 27
3.3.1.1 Larutan Natrium Hidroksida 0,2 N ... 27
3.3.1.2 Larutan Natrium Hidroksida 1 N ... 27
3.3.1.3 Larutan Asam Klorida 1 N ... 27
3.3.1.4 Larutan Kalium Biftalat 0,2 M ... 27
3.3.1.5 Larutan Kalsium Klorida 0,15 M ... 27
3.3.1.6 Medium Cairan Lambung Buatan Tanpa Enzim (pH 1,2) ... 27
3.3.1.7 Medium Cairan Lambung Buatan Tanpa Enzim (pH 3,0) ... 28
3.3.1.9 Medium Cairan Lambung Buatan Tanpa
Enzim (pH 5,0) ... 28
3.3.1.10 Medium Cairan Usus Buatan Tanpa Enzim (pH 6,8) ... 28
3.3.1.11 Medium Cairan Usus Buatan Tanpa Enzim (pH 7,0) ... 28
3.3.2 Pembuatan Kurva Serapan dan Kurva Kalibrasi Larutan Asam Salisilat dalam Medium Cairan Lambung Buatan (pH 1,2) ... 29
3.3.2.1 Pembuatan Larutan Induk Baku Asam Salisilat 29
3.3.2.2 Pembuatan Kurva Serapan Larutan Asam Salisilat ... 29
3.3.2.3 Pembuatan Kurva Kalibrasi Asam Salisilat ... 29
3.3.3 Pembuatan Kurva Serapan dan Kurva Kalibrasi Larutan Asam Salisilat dalam Medium Cairan Usus Buatan (pH 6,8) ... 29
3.3.3.1 Pembuatan Larutan Induk Baku Asam Salisilat... 29
3.3.3.2 Pembuatan Kurva Serapan Larutan Asam Salisilat ... 30
3.3.3.3 Pembuatan Kurva Kalibrasi Asam Salisilat... 30
3.3.4 Pembuatan Cangkang Kapsul Alginat ... 30
3.3.4.1 Pembuatan Larutan Natrium Alginat ... 31
3.3.4.2 Pengukuran Viskositas Larutan Natrium Alginat 34
3.3.4.4 Pembuatan Tutup Cangkang Kapsul Alginat ... 35
3.3.4.5 Pengeringan Cangkang Kapsul Alginat ... 35
3.3.4.6 Penentuan Spesifikasi Cangkang Kapsul ... 36
3.3.4.6.1 Pengukuran Panjang dan Diameter
Cangkang Kapsul ... 36
3.3.4.6.2 Pengukuran Ketebalan Cangkang
Kapsul ... ... 36
3.3.4.6.3 Penimbangan Berat Cangkang Kapsul ... 36
3.3.4.6 4 Pengamatan Warna Cangkang Kapsul ... 36
3.3.4.6.5 Pengukuran Volume Cangkang Kapsul .... 36
3.3.4.6.6 Pengisian Aspirin dalam Kapsul Alginat .. 36
3.4 Penyimpanan Cangkang Kapsul Alginat Yang Berisi Aspirin ... 37
3.4.1 Penyimpanan pada Suhu 300
3.4.2 Penyimpanan pada Suhu 40
C, RH 70% ……….. 37
0
3.5 Pengujian ... 37 C, RH 75% ... 37
3.5.1 Pengaruh penyimpanan ... 37
3.5.1.1 Pengujian Stabilitas Kimia Aspirin dalam Kapsul Alginat 4,5% yang Menggunakan Bahan Pemburam TiO2
Pengemas Aluminium Foil ... 37
yang Disimpan Selama 3 Bulan Dalam
3.5.1.1.1 Penetapan Kadar Aspirin dalam Kapsul ... 37
3.5.1.2 Pengujian Stabilitas Fisik Aspirin dalam Kapsul
Alginat ... 38
3.5.1.2.1 Pengamatan Warna Cangkang Kapsul dan
Warna Bahan Obat Aspirin dalam Kapsul Alginat ... 38
3.5.1.2.2 Uji Kerapuhan ... 38
3.5.1.2.2.1 Cangkang Kapsul Kosong ... 38
3.5.1.2.2.2 Cangkang Kapsul Berisi (Uji Ketahanan terhadap Tekanan) ... 39
3.5.1.2.3 Waktu Hancur ... 39
3.5.1.2.4 Uji Disolusi Medium pH Berganti ... 39
2.5.1.2.4.1 Prosedur ... 40
3.5.2 Pengaruh Penggunaan Titanium Dioksida (TiO2 Pelepasan Aspirin dalam Kapsul Alginat ... 41
) Pada 3.5.2.1 Uji Pelepasan ... 41
3.5.2.2 Prosedur ... 41
3.5.3 Pengaruh Penggunaan PEG 2% Pada Pelepasan Aspirin dalam Kapsul Alginat ... 41
3.5.3.1 Uji Pelepasan ... 41
3.5.3.2 Prosedur ... 42
3.6 Uji Delayed Release Cangkang Kapsul ... 42
3.6.1 Uji Pelepasan ... 42
3.7 Uji Profil Pelepasan Tablet Salut Enterik Ascardia ... 44
3.7.1 Uji Pelepasan ... 44
3.7.2 Prosedur ... 44
3.8 Uji Pengaruh pH Lambung Terhadap Waktu Hancur Cangkang Kapsul Alginat ... 45
3.8.1 Uji Waktu Hancur ... 45
BAB IV HASIL DAN PEMBAHASAN ... 46
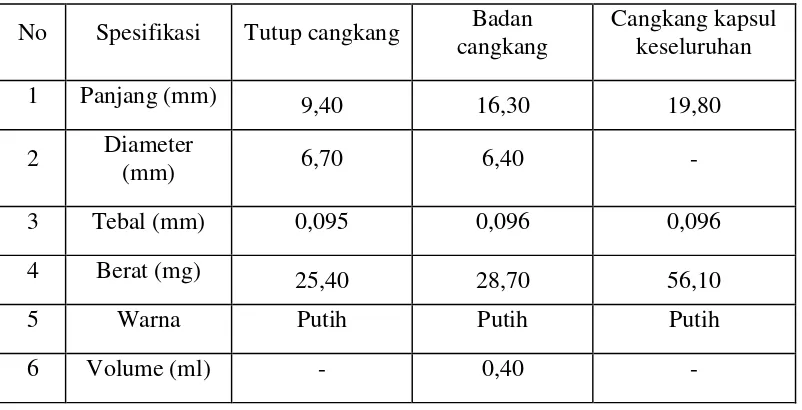
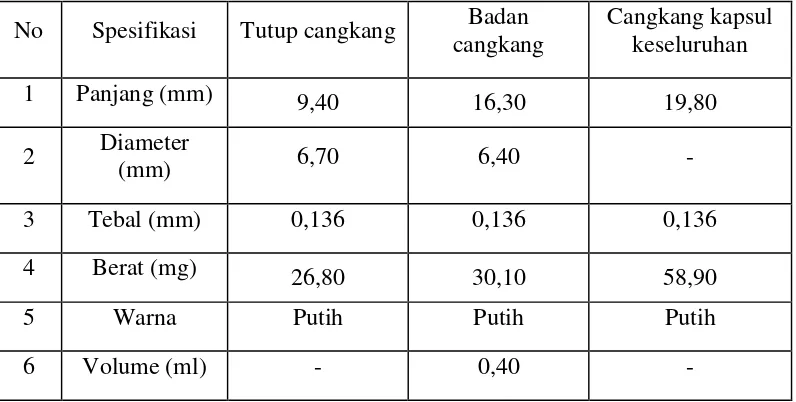
4.1 Pembuatan Cangkang kapsul Alginat ... 46
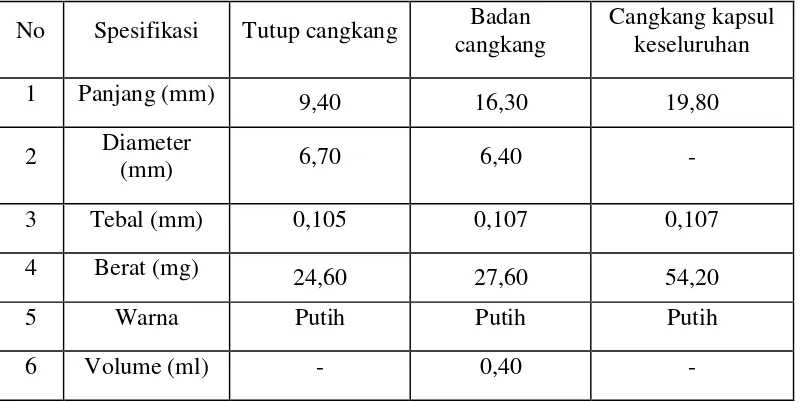
4.1.2 Spesifikasi Cangkang Kapsul Alginat ... 46
4.2 Pengujian Stabilitas Fisik Aspirin Dalam Kapsul Alginat ... 51
4.2.1 Pengamatan Warna ... 51
4.2.1.1 Pengamatan Warna Terhadap Cangkang Kapsul Alginat ... ... ... 51
4.2.1.2 Pengamatan Warna Bahan Obat Dalam Cangkang
Kapsul Alginat ... 52
4.2.1.3 Uji Kerapuhan ... 54
4.2.1.3.1 Cangkang Kapsul Kosong ... 54
4.2.1.3.2 Cangkang Kapsul Berisi (Uji Ketahanan Terhadap Tekanan) ... 55
4.2.1.4 Uji Waktu Hancur (Disintegrasi) ... 57
4.2.1.5 Uji Pelepasan Aspirin dalam Kapsul Alginat ... 59
4.2.1.5.1 Uji Pelepasan Aspirin dalam Kapsul Alginat Yang Menggunakan TiO2
Pengemas Aluminium Foil ... 59 Dalam
4.2.1.5.1.1 Laju Pelepasan Aspirin dalam Kapsul Alginat Sebelum
Penyimpanan dan Setelah Penyimpanan 3 Bulan pada Suhu 300
4.2.1.5.1.2 Laju Pelepasan Aspirin dalam C,RH 70% .. ... 60
Kapsul Alginat Sebelum Penyimpanan dan Setelah Penyimpanan 3 Bulan pada Suhu 400
4.2.1.5.1.3 Laju Pelepasan Aspirin dalam C,RH 75% ... . 61
Kapsul Alginat Setelah Penyimpanan Selama 3 Bulan Pada Suhu 300
dan Suhu 40
C, RH 70%, 0
C, RH 75% ... 63
4.2.1.5,2 Pengaruh Penggunaan TiO2 Pelepasan Aspirin dalam Kapsul
pada
4.2.1.5.2.1Laju Pelepasn Aspirin dalam Cangkang Kapsul Alginat yang Menggunakan TiO2 dan Tanpa Menggunakan
TiO2
4.2.1.5.3 Pengaruh Penggunaan PEG 2% pada ... ... 65
Pelepasan Aspirin dalam Kapsul
Alginat ... 66
4.2.1.5.23.1Laju Pelepasn Aspirin dalam Cangkang Kapsul Alginat yang Menggunakan PEG 2% dan yang Tanpa
Menggunakan PEG ... . 66
4.2.1.5.4Perbandingan Pelepasan Aspirin Dalam Cangkang Kapsul Alginat Dengan Tablet Salut Enterik ... 68
4.2.1.5.4.1 Laju Pelepasan Aspirin Dalam Cangkang Kapsul Alginat Dengan Tablet Salut Enterik 68
4.2.1.6 Penetapan Kadar Aspirin dalam Kapsul Alginat ... 69
4.2.2 Uji Delayed Release dari Beberapa Formula Cangkang Kapsul Alginat ... 71
4.2.2.1 Pengaruh Perbedaan Konsentrasi Na Alginat yang Digunakan Pada Proses Pembuatan Cangkang Kapsul Alginat ... 71
4.2.2.1.1 Laju Pelepasan Aspirin Dalam Cangkang Kapsul Alginat 300-400 cp Dengan
Konsentrasi Na Alginat 4 % dan 4,5% …….. 71 4.2.2.1.2 Laju Pelepasan Aspirin Dalam Cangkang
Kapsul Alginat 300-400 cp Dengan Konsentrasi Na Alginat 4,5 % Tanpa dan
Dengan Penambahan PEG ………. 72
4.2.3 Uji Pengaruh pH Lambung Pada Pelepasan Aspirin Dari
Cangkang Kapsul Alginat ... 74
4.2.3.1 Uji Waktu Hancur (Disintegrasi) ... 74
5.1 Kesimpulan ... 80
5.2 Saran ... 81
DAFTAR PUSTAKA ... 82
DAFTAR TABEL
Tabel Halaman
4.1Spesifikasi Cangkang Kapsul Alginat 80-120 cp dengan konsentrasi Na alginat 4,5% yang menggunakan TiO2
4.2Spesifikasi Cangkang Kapsul Alginat dengan konsentrasi
... 47
Na alginat 4,5% tanpa menggunakan TiO2 ...
4.3Spesifikasi Cangkang Kapsul Alginat 80-120 cp dengan konsentrasi
47
Na alginat 4,5% yang menggunakan PEG 2% ... 48
4.4 Spesifikasi Cangkang Kapsul Alginat 300-400 cp dengan konsentrasi
Na alginat 4 % yang menggunakan TiO2 ...
4.5 Spesifikasi Cangkang Kapsul Alginat 300-400 cp dengan konsentrasi 48
Na alginat 4,5 % yang menggunakan TiO2 ...
4.6 Spesifikasi Cangkang Kapsul Alginat 300-400 cp dengan konsentrasi 49
Na alginat 4,5 % yang menggunakan TiO2 dan PEG 2% ...
4.7 Spesifikasi Cangkang Kapsul Alginat 300-400 cp dengan konsentrasi 49
Na alginat 4,5 % yang menggunakan TiO2 dan PEG 3% ...
4.8 Spesifikasi cangkang kapsul ukuran No. 1 menurut Pfizer Inc.Capsugel 50
Division ... 50
4.9 Sifat fisik cangkang kapsul alginat yang menggunakan
TiO2
4.10 Waktu hancur cangkang kapsul alginat dan tablet salut enterik
dan strip (aluminium foil) sebagai bahan pengemas ... 52
Ascardia ………. 59
4.11 Hasil Penetapan Kadar Ferosulfat dalam cangkang kapsul
alginat sebelum penyimpan dan setelah penyimpanan selama 3 bulan
pada suhu 300C, RH 70%, dan suhu 400
4.13 Uji Delayed Release Dari Berbagai Formula Cangkang Kapsul
Alginat ………...………. 74
4.14 Uji Pengaruh pH Lambung Pada Waktu Hancur Dari Cangkang
DAFTAR GAMBAR
Gambar Halaman
1.1 Kerangka Pikir Penelitian ... 3
2.1 Rumus Bangun Aspirin ... 8
2.2 Struktur G: α- L asam guluronat dan M: β- D asam mannuronat ... 12
2.3 Struktur Alginat ... 12
2.4 Pembentukan khelat alginat dan kalsium ... 13
2.5 Kelembaban Relatif (RH), Kandungan Uap Air Gelatin dan Sifat Kapsul Gelatin Keras ... 18
4.1 Warna cangkang kapsul alginat yang menggunakan TiO2 disimpan dalam bahan pengemas berupa aluminium foil ……… 51
dan 4.2 Warna bahan obat dalam cangkang kapsul alginat yang menggunakan TiO2 berupa aluminium foil ... 53
dan disimpan dalam bahan pengemas 4.3 Uji Kerapuhan cangkang Kapsul kosong penyimpanan 3 bulan pada suhu 300 4.4 Uji Kerapuhan cangkang kapsul kosong penyimpanan 3 bulan C, RH 70% ... 54
pada suhu 400 4.5 Uji Kerapuhan cangkang kapsul berisi penyimpanan 3 bulan C, RH 75 % ... 55
Suhu 300 4.6 Uji Kerapuhan cangkang kapsul berisi penyimpanan 3 bulan C, RH 70% ... 56
Suhu 400 4.7 Pengamatan Cangkang Kapsul pada Uji Waktu Hancur ... 58
C, RH 75% ... 56
4.9 Pengaruh penyimpanan terhadap pelepasan Aspirin dalam kapsul alginat sebelum penyimpanan dan setelah penyimpanan selama 3
bulan pada suhu 400 C ,RH 75% ... 62
4.10 Pengaruh penyimpanan terhadap pelepasan Aspirindalam kapsul alginat disimpan selama 3 bulan pada suhu 300
suhu 40
C,RH 70% , dan pada 0
4.11 Pengaruh bahan pemburan TiO
C ,RH 75% ... 63 2
kapsul alginat yang menggunakan TiO
terhadap pelepasan Aspirin dalam 2
TiO
dan tanpa menggunakan 2
4.12 Pengaruh PEG
... 65
menggunakan PEG 2% dan tanpa menggunakan PEG ... 67 terhadap pelepasan Aspirin dalam kapsul alginat yang
4.13 Perbandingan pelepasan Aspirin dalam kapsul alginat dengan tablet
DAFTAR LAMPIRAN
Lampiran Halaman
1. Pengukuran Viskositas Larutan Alginat ... 85
2. Penentuan Spesifikasi Cangkang Kapsul ... 86
3. Cangkang Kapsul Alginat ... 98
4. Cangkang Kapsul Yang Dikemas Dalam Pengemas Aluminium Foil .. 99
5. Data Hasil Penetapan Kadar Aspirin Dalam Kapsul Alginat ... 100
6. Alat Pencetak Kapsul dan Lemari Pengering Kapsul ... 101
7. Alat-alat untuk Disolusi ... 103
8. Alat Uji Kerapuhan ……… ... 105
9. Alat Uji Viskositas ……….... ... 107
10. Alat Uji Spesifikasi Kapsul .……… ... 108
11. Alat Uji Waktu Hancur (desintegration tester) ... 109
12. Data Uji Waktu Hancur ... 110
13. Kurva Serapan Larutan Aspirin dalam Medium pH 1,2 ... 121
14. Kurva Kalibrasi Larutan Aspirin dalam Medium pH 1,2 ... 122
15. Kurva Serapan Larutan Aspirin dalam Medium pH 6,8 ... 124
16. Kurva Kalibrasi Larutan Aspirin dalam Medium pH 6,8 ... 125
17. Contoh Perhitungan % Kumulatif Pelepasan Aspirin ... 127
18. Data % Kumulatif Rata-Rata dan Standar Deviasi Disolusi Kapsul Alginat 80-120 cp dengan TiO2 19. Data % Kumulatif Rata-Rata dan Standar Deviasi Disolusi Kapsul ... 128
20. Data % Kumulatif Rata-Rata dan Standar Deviasi Disolusi Kapsul
Alginat 80-120 cp dengan TiO2
21. Data % Kumulatif Rata-Rata dan Standar Deviasi Disolusi Kapsul
dan PEG 2% ... 130
Alginat 80-120 cp dengan TiO2
Suhu 30
Setelah Penyimpanan 3 Bulan Pada
o
22. Data % Kumulatif Rata-Rata dan Standar Deviasi Disolusi Kapsul
C, RH 70% ... 131
Alginat 80-120 cp dengan TiO2
Suhu 40
Setelah Penyimpanan 3 Bulan Pada
o
23. Data % Kumulatif Rata-Rata dan Standar Deviasi Disolusi Tablet
C, RH 75% ... 132
Salut Enterik Ascardia ... 133
24. Data AUC Disolusi Aspirin Dalam Kapsul Alginat 80-120 cp ... 134
25. Uji Statistika Waktu Hancur ... 140
26. Uji Statistika Disolusi Aspirin Dari Cangkang Kapsul Alginat ... 146
Uji Stabilitas Aspirin pada Cangkang Kapsul Alginat yang Ditambahkan Bahan Pemburam Titanium Dioksida dan Dikemas Dengan Aluminium Foil
Sebagai Sediaan Lepas Tunda
Abstrak
Aspirin merupakan bahan yang mudah terhidrolisis. Aspirin yang disimpan dalam cangkang kapsul alginat tanpa menggunakan bahan pemburam Titanium dioksida (TiO2) tidak stabil selama penyimpanan. Oleh karena itu, perlu perhatian khusus pada proses penyimpanan dan formulasi cangkang kapsul sehingga stabilitas dalam kapsul menjadi lebih baik. Tujuan utama penelitian ini adalah untuk mengetahui pengaruh penyimpanan terhadap stabilitas kimia dan fisika Aspirin dan stabilitas fisik cangkang kapsul alginat yang mengandung TiO2 dengan menggunakan pengemas aluminium foil (strip).
Pengujian stabilitas kimia Aspirin dalam kapsul alginat yang mengandung TiO2 dilakukan dengan penetapan kadar Aspirin setelah penyimpanan selama 3 bulan secara spektrofotometer ultraviolet yang diukur pada panjang gelombang 296,3 nm. Stabilitas fisik Aspirin dalam cangkang kapsul alginat yang mengandung TiO2 meliputi pengamatan warna, kerapuhan, waktu hancur dan laju pelepasan. Warna diamati secara visual, kerapuhan kapsul diuji dengan capsule shell impact tester
Hasil penelitian pada pengujian terhadap stabilitas kimia Aspirin dalam kapsul alginat yang menggunakan TiO
, waktu hancur diuji dengan alat desintegration tester, dan uji pelepasan dilakukan dengan menggunakan alat disolusi metode dayung dalam medium pH berganti kemudian diukur dengan spektrofotometer ultraviolet pada panjang gelombang 237 nm pada medium pH 1,2 dan 296,3 nm pada medium 6,8.
2 dalam pengemas aluminium foil selama 3 bulan menunjukkan adanya perbedaan kadar Aspirin dengan sebelum penyimpanan. Pada penyimpanan suhu 30°C, RH (Relative Humidity) 70% selama 3 bulan kadar Aspirin masih memenuhi persyaratan (98,60%), tetapi pada penyimpanan suhu 40°C, RH 75% kadar Aspirin menjadi tidak memenuhi persyaratan (91,67%). Pada pengujian stabilitas fisik Aspirin dalam kapsul alginat dengan pengamatan secara visual, warna serbuk Aspirin tidak mengalami perubahan, warna cangkang kapsul tidak berubah selama penyimpanan suhu 30°C, RH 70% sementara pada suhu 40°C, RH 75% warna cangkang kapsul mulai kecoklatan dan keseluruhan kapsul tidak menunjukkan kerapuhan. Pelepasan Aspirin juga dipengaruhi oleh penyimpanan di mana pada suhu 40°C, RH 75% memiliki perbedaan dengan pelepasan Aspirin sebelum penyimpanan, yaitu dibuktikan dengan uji statistik independent t-test. Dapat disimpulkan bahwa penyimpanan mempengaruhi stabilitas kimia Aspirin dimana kadar Aspirin mengalami penurunan setelah penyimpanan dan stabilitas fisik berupa warna serbuk Aspirin tidak berubah, warna cangkang kapsul berubah dan kapsul tidak rapuh, dan pelepasan Aspirin menunjukkan perbedaan dengan sebelum penyimpanan, yaitu pelepasannya menjadi semakin lambat.
The Stability Test of Aspirin in Alginate Capsule Shell Used Titanium Dioxide as Opacifying Agent and Packaged Using Aluminium Foil As
Delayed Release Dossage Form
Abstract
Aspirins is an easily hydrolyzed material. Aspirin which was encapsulated in alginate capsule shell without using Titanium dioxide (TiO2) as opacifying agent was not stable during storage. Therefore, it is needed a special attention in storage and the formulation of the capsules shell so that the stability of the capsules are better. The main objective of this study was to examine the effect of storage condition on chemical and physical stability of Aspirin loaded into alginate capsule containing TiO2
The chemical stability test of Aspirin encapsulated in alginate capsule containing TiO
that packaged with aluminium foil.
2 was done by determining Aspirin content after 3 months storage using UV spectrofotometer at wavelength 296,3 nm. The physical stability of Aspirin encapsulated in alginate capsule shell containing TiO2
The results of chemical stability test of Aspirin encapsulated in alginate capsules containing TiO
included observations of colour, brittleness, desintegration time and the release rate. Colour was observed visually, the brittleness of the capsule was tested using capsule shell impact tester, desintegration time was tested using the desintegration tester, and release rate was tested by using a paddle method dissolution in changing pH medium and measured by UV-spectrophotometer at wavelength of 237.0 nm in pH 1.2 medium and 296.3 nm in pH 6.8 medium. Storage performed at a temperature of 30°C, 70% RH and a temperature of 40°C, 75% RH for 3 months.
2 an packaged with aluminum foil for 3 months showed that there was a difference in Aspirin content before and after storage. When stored at 30°C, RH 70% for 3 months, Aspirin content still fulfill the requirement (98.60%), but when stored at 40°C, RH 75%, Aspirin content did not fulfill the requirement (91.67%). The physical stability test showed that there was no effect of storage on the brittleness of the storage for 3 months at a temperature of 30°C RH 70%, and 40°C RH 75%. Colour of Aspirin and capsules shell had no change when stored at 30°C RH 70%, but when stored at 40°C RH 75%, capsules shell become brownish. The release of Aspirin in storage for 3 months at a temperature of 40°C, RH 75% showed a difference in the release rate of Aspirin prior to storage which the release was slower than prior. It can be concluded that the physical stability during storage alginate capsule shell using TiO2
Key words: Aspirin, stability, packaging
with aluminum
BAB I
PENDAHULUAN
1.1 Latar Belakang
Aspirin merupakan salah satu obat anti inflamasi non steroid (AINS) yang
memiliki efek analgetik, antipiretik, anti inflamasi, dan dalam dosis rendah dapat
menghambat agregasi platelet sehingga dapat digunakan untuk mengurangi infark
miokard. Akan tetapi penggunaan dari aspirin dapat menyebabkan gangguan
saluran cerna, mual, dan muntah. Selain itu juga dapat menyebabkan ulser pada
lambung, pendarahan saluran cerna, dan pengikisan pada dinding lambung
(Gilman, et al., 1996). Untuk mengurangi efek samping aspirin, maka pada saat
sekarang ini umumnya aspirin dibuat dalam bentuk sediaan tablet salut enterik.
Pada penelitian ini akan dibuat formulasi sistem delayed release dalam bentuk sediaan kapsul. Kapsul delayed release adalah kapsul keras ataupun lunak yang disiapkan sedemikian rupa sehingga baik cangkang maupun isi kapsul tahan
terhadap cairan lambung tetapi akan melepaskan bahan aktif dengan adanya
cairan usus (WHO, 2011).
Di Laboratorium Farmasi Fisik Fakultas Farmasi USU telah dilakukan
penelitian tentang pembuatan cangkang kapsul alginat. Ditemukan bahwa
cangkang kapsul alginat terbukti tahan atau tidak pecah oleh cairan lambung
buatan (pH 1,2). Kapsul mengembang dan pecah dalam cairan usus buatan (pH
4,5 dan pH 6,8). Jika kapsul direndam dalam medium pH berganti, di mana
mula-mula dalam medium pH 1,2, lalu medium diganti dengan pH 4,5, maka kapsul
dapat mencegah efek iritasi lokal FeSO4 pada mukosa lambung kelinci (Bangun,
dkk., 2007). Selain FeSO4
Beberapa penelitian telah dilakukan untuk mengatasi efek samping
penggunaan obat AINS. Shiraisi (1991), membuat sediaan dispersi alginat yang
mengandung indometasin dan hasilnya menunjukkan pengurangan luka lambung.
Adeyeye, et al., (1996) melaporkan bahwa enkapsulasi ibuprofen dengan parafin
dapat menunjukkan pengurangan luka lambung pada tikus percobaan.Selanjutnya
Bangun (2002) menginformasikan bahwa enkapsulasi indometasin dengan gel
alginat yakni bentuk butir-butir gel yang mengandung indometasin setelah
dilakukan uji iritasi akut dan kronis terhadap tikus percobaan terbukti dapat
mencegah efek samping penggunaan obat. Pada penelitian sebelumnya (Halim,
2012) melakukan pengujian natrium diklofenak dalam cangkang kapsul alginat
sebagai sediaan delayed-release, namun pelepasannya belum dapat memenuhi persyaratan USP XXX (2007) untuk sediaan delayed release.
, kapsul alginat dapat juga mencegah efek iritasi lokal
aspirin pada mukosa lambung kelinci (Bangun, dkk., 2007).
Berdasarkan uraian di atas, maka penulis tertarik untuk membuat
berbagai formula cangkang kapsul alginat ,yaitu tanpa dan dengan penambahan
TiO2 ,dan dengan penambahan PEG 2% yang berisi Aspirin, untuk dibuat dalam
bentuk sediaan kapsul enterik dengan sistem penghantaran delayed release sebagai metode pemberian terhadap obat-obatan yang mengiritasi mukosa
lambung. Selain itu, diperhatikan pula pengaruh penyimpanan Aspirin dalam
cangkang kapsul alginat yang mengandung TiO2 dan dikemas dengan strip
(aluminium foil) terhadap stabilitas kimia Aspirin dan stabilitas fisik cangkang
visual, kerapuhan kapsul, uji waktu hancur, uji disolusi, dan dibandingkan
pelepasannya dengan tablet yang ada di pasaran, yaitu Ascardia.
1.2 Kerangka Pikir Penelitian
Variabel bebas Variabel Terikat Parameter
Gambar 1.1 Kerangka pikir penelitian Aspirin dalam
kapsul alginat
Pengaruh penyimpanan pada suhu 300C, dan suhu 400C selama 3 bulan
Pengaruh penambahan
Pemburam TiO2 dalam
cangkang kapsul
Pengaruh penambahan PEG 2% dalam cangkang kapsul
Pengaruh alginat 300-400 cp dengan konsentrasi 4% dan 4,5%
Stabilitas Kimia Aspirin
Stabilitas Fisik
Aspirin dalam
cangkang kapsul
Kadar Aspirin
-Warna -Kerapuhan -Waktu hancur -Laju pelepasan Aspirin
Pelepasan
Laju pelepasan Aspirin dalam kapsul alginat
Pengaruh alginat 300-400 cp dengan konsentrasi 4,5% dengann penambahan PEG 2% dan 3% dalam cangkang kapsul
1.3 Perumusan Masalah
Berdasarkan uraian diatas, maka rumusan masalah dalam penelitian ini
adalah sebagai berikut:
a. Apakah penyimpanan suhu 30°C, RH (Relative Humidity) 70% dan suhu 40°C, RH 75% selama 3 bulan berpengaruh terhadap stabilitas kimia
Aspirin yaitu kadar Aspirin dalam kapsul alginat yang menggunakan
pemburam TiO2
b. Apakah penyimpanan suhu 30°C, RH 70% dan suhu 40°C, RH 75%
selama 3 bulan berpengaruh terhadap stabilitas fisik cangkang kapsul
alginat berisi Aspirin yaitu warna, kerapuhan, dan pelepasan Aspirin yang
menggunakan pemburam TiO
dalam pengemas aluminium foil?
2
c. Apakah penggunaan TiO ?
2
d. Apakah penggunaan PEG 2% di dalam pembuatan cangkang kapsul
berpengaruh terhadap pelepasan Aspirin dari kapsul alginat?
di dalam pembuatan cangkang kapsul
berpengaruh terhadap pelepasan Aspirin dari kapsul alginat?
e. Apakah penggunaan alginat 300-400cp dengan perbedaan konsentrasi
Natrium alginat 4% dan 4,5% yang menggunakan pemburam TiO2
f. Apakah penggunaan alginat 300-400cp dengan konsentrasi Natrium
alginat 4,5% yang menggunakan pemburam TiO
dapat
memenuhi persyaratan sediaan delayed release?
2
g. Apakah terdapat kesamaan laju pelepasan aspirin pada kapsul alginat
dengan tablet salut enterik Ascardia?
dan penambahan PEG
2% dan 3% pada pembuatan cangkang kapsul dapat memenuhi
1.4 Hipotesis Penelitian
Berdasarkan perumusan masalah diatas maka hipotesis penelitian ini
adalah sebagai berikut:
a. Penyimpanan suhu 30°C, RH 70% dan suhu 40°C, RH 75% selama 3
bulan berpengaruh terhadap stabilitas kimia Aspirin yaitu kadar Aspirin
dalam kapsul alginat yang menggunakan pemburam TiO2
b. Penyimpanan suhu 30°C, RH 70% dan suhu 40°C, RH 75% selama 3
bulan berpengaruh terhadap stabilitas fisik cangkang kapsul alginat berisi
Aspirin yaitu warna, kerapuhan, dan pelepasan Aspirin yang
menggunakan pemburam TiO
dalam
pengemas aluminium foil.
2
c. Penggunaan TiO
dalam pengemas aluminium foil.
2
d. Penggunaan PEG 2% di dalam pembuatan cangkang kapsul berpengaruh
terhadap pelepasan Aspirin dari kapsul alginat.
di dalam pembuatan cangkang kapsul berpengaruh
terhadap pelepasan Aspirin dari kapsul alginat.
e. Penggunaan alginat 300-400cp dengan perbedaan konsentrasi Natrium
alginat 4% dan 4,5% yang menggunakan pemburam TiO2
f. Penggunaan alginat 300-400cp dengan konsentrasi Natrium alginat 4,5%
yang menggunakan pemburam TiO
dapat
memenuhi persyaratan sediaan delayed release.
2
g. Terdapat kesamaan laju pelepasan aspirin pada kapsul alginat dengan
tablet salut enterik Ascardia.
dan penambahan PEG 2% dan 3%
pada pembuatan cangkang kapsul dapat memenuhi persyaratan sediaan
1.5 Tujuan Penelitian
Tujuan penelitian ini adalah:
a. Mengetahui pengaruh penyimpanan suhu 30°C, RH 70% dan suhu 40°C,
RH 75% selama 3 bulan terhadap stabilitas kimia Aspirin yaitu kadar
Aspirin dalam kapsul alginat yang menggunakan pemburam TiO2
b. Mengetahui pengaruh penyimpanan suhu 30°C, RH 70% dan suhu 40°C,
RH 75% selama 3 bulan terhadap stabilitas fisik cangkang kapsul alginat
berisi Aspirin yaitu warna, kerapuhan, dan pelepasan Aspirin yang
menggunakan pemburam TiO
dalam
pengemas aluminium foil.
2
c. Mengetahui pengaruh penggunaan TiO
dalam pengemas aluminium foil.
2
d. Mengetahui pengaruh penggunaan PEG 2% di dalam pembuatan cangkang
kapsul terhadap pelepasan Aspirin dari kapsul alginat
di dalam pembuatan cangkang
kapsul terhadap pelepasan Aspirin dari kapsul alginat.
e. Mengetahui penggunaan alginat 300-400cp dengan perbedaan konsentrasi
Natrium alginat 4% dan 4,5% yang menggunakan pemburam TiO2
f. Mengetahui penggunaan alginat 300-400cp dengan konsentrasi Natrium
alginat 4,5% yang menggunakan pemburam TiO
dapat
memenuhi persyaratan sediaan delayed release.
2
g. Mengetahui kesamaan laju pelepasan aspirin pada kapsul alginat dengan
tablet salut enterik Ascardia.
dan penambahan PEG
2% dan 3% pada pembuatan cangkang kapsul dapat memenuhi
1.6 Manfaat Penelitian
Penelitian ini bertujuan untuk mengetahui pengaruh penyimpanan
terhadap terhadap stabilitas kimia Aspirin yaitu kadar Aspirin dalam kapsul
selama penyimpanan dan stabilitas fisik Aspirin dalam kapsul alginat yaitu warna,
kerapuhan, dan pelepasan Aspirin yang disimpan selama 3 bulan dengan bahan
pemburam TiO2 dan untuk mengetahui kemampuan strip sebagai bahan pengemas
dalam melindungi bahan aktif yang cenderung mudah terhidrolisis yang terdapat
BAB II
TINJAUAN PUSTAKA
2.1 Aspirin
2.1.1 Uraian Umum Aspirin (Ditjen POM, 1995)
Rumus Bangun :
Gambar 2.1 Rumus Bangun Aspirin
Rumus Molekul : C9H8O
Berat Molekul : 180,16 4
Pemerian : Hablur putih, umumnya seperti jarum atau
lempengan tersusun, atau serbuk hablur putih;
tidak berbau atau berbau lemah. Stabil di udara
kering; di dalam udara
lembab secara bertahap terhidrolisa menjadi asam
salisilat dan asam asetat.
Kelarutan : Sukar larut dalam air, mudah larut dalam etanol,
larut dalam kloroform dan dalam eter.
2.1.2 Farmakologi Aspirin
Asam asetil salisilat yang lebih dikenal sebagai asetosal atau aspirin adalah analgesik, antipiretik, dan anti-inflamasi yang banyak digunakan sebagai golongan obat bebas (Wilmana, 1995).
Dosis oral aspirin untuk memperoleh efek analgesik dan antipiretik pada manusia adalah 325 – 650 mg empat kali sehari,konsentrasi dalam plasmanya 100 – 300 mcg/ml. Untuk memperoleh efek antiinflamasi adalah 4 – 6 gram secara oral per hari, dan untuk mendapatkan efek anti agregasi platelet adalah 60 – 80 mg sacara oral per hari (Mycek, et al., 2001).
2.1.2.1 Aspirin Sebagai Anti Inflamasi
Aspirin menghambat aktivitas siklooksigenase, sehingga aspirin mengurangi pembentukan prostaglandin dan juga memodulasi beberapa aspek inflamasi pada arthritis, tetapi tidak menghentikan progresivitas penyakit maupun menginduksi remisi (Mycek, et al., 2001).
2.1.2.2 Aspirin Sebagai Analgesik
Aspirin menghambat sintesa prostaglandin E2
2.1.2.3 Aspirin Sebagai Antipiretik
dengan menginhibisi enzim siklooksigenase (Mycek, et al., 2001).
2.1.2.4 Aspirin Sebagai Anti Agregasi Platelet
Tromboksan A2 bersifat vasokonstriktor dan juga merangsang platelet menempel di endothelium jaringan yang rusak (adhesi-platelet). Aspirin menghambat sintesis tomboksan A2
2.1.3 Efek Samping Aspirin
sehingga terjadi penghambatan agregasi trombosit dan perpanjangan waktu pendarahan. Efek hemostatik dapat kembali normal kira-kira 36 jam setelah pemberian dosis obat yang terakhir. (Mycek, et al., 2001).
a. Saluran cerna : efek aspirin terhadap saluran cerna yang paling umum adalah distress epigastrum, mual, dan muntah. Pendarahan mikroskopik saluran cerna hamper umum terjadi pada penderita yang mendapatkan pengobatan aspirin. Aspirin bersifat asam, pada pH lambung tidak dibebaskan, akibatnya mudah menembus sel mukosa dan aspirin mengalami ionisasi (menjadi bermuatan negatif), dan terperangkap, jadi berpotensi menyebabkan kerusakan sel secara langsung.
b. Darah : asetilasi irreversibel siklooksigenase trombosit menurunkan kadar tomboksan A2
c. Pernafasan : pada dosis toksis,aspirin menimbulkan depresi pernafasan dan suatu kombinasi pernafasan yang tidak terkompensasi dan asidosis metabolic.
, mengakibatkan penghambatan agregasi trombosit dan perpanjangan waktu pendarahan.
d. Proses metabolik : dosis besar aspirin melepaskan fosforilasi oksidatif. Energi yang dikeluarkan untuk menghasilkan ATP secara normal dikeluarkan sebagai panas, yang menyebabkan terjadinya hipertemia.
2.2 Kapsul
Kapsul dapat didefinisikan sebagai bentuk sediaan padat, dimana satu macam obat atau lebih dan/atau bahan inert lainnya yang dimasukkan ke dalam cangkang atau wadah kecil yang dapat larut dalam air. Pada umumnya cangkang kapsul terbuat dari gelatin. Tergantung pada formulasinya kapsul dapat berupa kapsul gelatin lunak atau keras. Bagaimana pun, gelatin mempunyai beberapa kekurangan, seperti mudah mengalami peruraian oleh mikroba bila menjadi lembab atau bila disimpan dalam larutan berair (Ansel, 2005).
Kapsul tidak berasa, mudah pemberiannya, mudah pengisiannya tanpa persiapan atau dalam jumlah yang besar secara komersil. Didalam praktek peresepan, penggunaan kapsul gelatin keras diperbolehkan sebagai pilihan dalam meresepkan obat tunggal atau kombinasi obat pada perhitungan dosis yang dianggap baik untuk pasien secara individual. Fleksibilitasnya lebih menguntungkan daripada tablet. Beberapa pasien menyatakan lebih mudah menelan kapsul daripada tablet, oleh karena itu lebih disukai bentuk kapsul bila memungkinkan. Pilihan ini telah mendorong pabrik farmasi untuk memproduksi sediaan kapsul dan di pasarkan, walaupun produknya sudah ada dalam bentuk sediaan tablet (Gennaro, 2000).
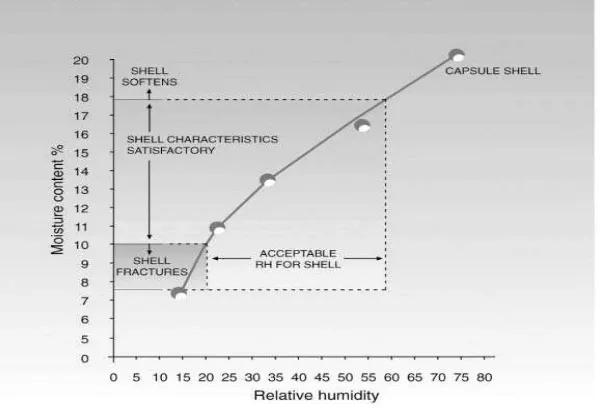
Stabilitas disolusi dari sediaan kapsul gelatin keras terutama ditentukan oleh kandungan uap lembab dari cangkang, yang kemudian dihubungkan dengan kondisi penyimpanan. Normalnya cangkang kapsul gelatin mengandung air 13-16% dan aman disimpan dengan kelembapan 30-60% kelembapan relatif (KR). Kandungan air di bawah 12%, cangkang menjadi rapuh dan mudah pecah. Di atas 18% uap air, cangkang akan menjadi lembab, lembut dan menyimpang cenderung memindahkan lembabnya ke dalam isi kapsul jika isi kapsulnya bersifat higroskopik.
diperoleh dari alga coklat (Phaeophyceae) (Belitz, dkk., 1987). Pada penelitian sebelumnya diperoleh bahwa cangkang kapsul alginat mengandung kadar air 20-25% dan disimpan pada suhu kamar dengan kelembapan relatif 75-90% (Hendra, 2011).
Kapsul delayed-release
Kapsul dapat disalut, atau, lebih umumnya, granul yang dienkaspulasi dapat disalut untuk menahan pelepasan obat dalam cairan lambung dimana suatu penundaan penting untuk mengurangi masalah yang mungkin terjadi pada inaktifasi obat atapun iritasi mukosa lambung. Istilah “delayed-release” digunakan pada monografi Farmakope pada kapsul salut enterik yang ditujukan untuk menunda pelepasan dari bahan obat hingga kapsul melewati lambung (USP XXXII, 2009).
2.3 Natrium Alginat
Natrium alginat merupakan produk pemurnian karbohidrat yang diekstraksi dari alga coklat (Phaeophyceae) dengan menggunakan basa lemah. Natrium alginat larut dengan lambat dalam air, membentuk larutan kental, tidak larut dalam etanol dan eter. Alginat ini diperoleh dari spesies Macrocystis pyrifera, Laminaria, Ascophyllum dan Sargassum (Belitz, dkk., 1987).
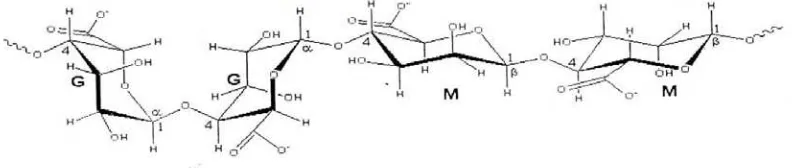
[image:36.595.134.490.482.546.2] [image:36.595.113.509.611.695.2]Gambar 2.2 Struktur G: α- L asam guluronat dan M: β- D asam mannuronat
Asam alginat adalah kopolimer biner yang terdiri dari residu β -D-mannuronat (M) dan α-L-asam guluronat (G) yang tersusun dalam blok-blok yang membentuk rantai linear (Grasdalen, dkk., 1979). Kedua unit tersebut berikatan pada atom C1 dan C4 dengan susunan homopolimer dari masing-masing residu (MM dan GG) dan suatu blok heteropolimer dari dua residu (MG) (Thom, dkk., 1980).
Asam alginat tidak larut dalam air, karena itu yang digunakan dalam industri adalah dalam bentuk garam natrium dan garam kalium. Salah satu sifat dari natrium alginat adalah mempunyai kemampuan membentuk gel dengan penambahan larutan garam-garam kalsium seperti kalsium glukonat, kalsium tartrat dan kalsium sitrat (Thom, dkk., 1980). Pembentukan gel alginat dengan ion kalsium, disebabkan oleh adanya ikatan silang membentuk khelat antara ion kalsium dan anion karboksilat pada blok G-G melalui mekanisme antar rantai. Natrium alginat mempunyai rantai poliguluronat menunjukkan sifat pengikatan ion kalsium yang lebih besar (Morris, et al., 1980).
Untuk kepentingan farmasetik digunakan natrium alginat, dimana larutannya dalam air bereaksi netral sampai asam lemah. Sediaan alginat paling stabil pada daerah pH 6-7, pada pH 4,5 asam bebasnya akan mengendap. Pemanasan yang kuat dan lama, terutama >70o
Di Laboratorium Farmasi Fisik Fakultas Farmasi USU dalam beberapa tahun terakhir telah dikembangkan kapsul yang tahan terhadap asam lambung. Cangkang kapsul ini dibuat dari natrium alginat dengan kalsium klorida menggunakan cetakan. Telah terbukti bahwa cangkang kapsul alginat tahan atau tidak pecah dalam cairan lambung buatan (pH 1,2). Kapsul mengembang dan pecah dalam cairan usus buatan yaitu pH 4,5 dan pH 6,8 (Bangun, dkk., 2005)
C dihindari, karena akan mengalami kehilangan viskositas akibat terjadinya polimerisasi. Sediaan disimpan dingin dan dilindungi dari cahaya dalam wadah tertutup baik (Voight, 1995).
terperangkap dalam kapsul dan terikat dengan manuronat saja. Hal itu berarti kalsium guluronat yang bertanggung jawab terhadap keutuhan kapsul di dalam medium pH 1,2 (Bangun, dkk., 2005).
Cangkang kapsul kalsium alginat dapat mengembang dan pecah di dalam medium pH 4,5 dan 6,8 (cairan usus buatan). Hal ini disebabkan terjadi pertukaran ion kalsium dari kalsium alginat (kalsium guluronat) dengan ion natrium yang terdapat pada cairan usus buatan, sehingga terbentuk natrium alginat (natrium guluronat). Pembentukan natrium alginat pada kapsul dapat menyebabkan kapsul bersifat hidrofilik, sehingga mudah menyerap air, mengembang dan pecah (Bangun, dkk. 2005).
2.4Titanium Dioksida
Titanium dioksida berwarna putih dan dapat menyebabkan warna menjadi opak. Titanium dioksida telah banyak digunakan dalam industri manisan (permen), makanan, kosmetik, plastik dan dalam bidang farmasi untuk pembuatan sediaan oral dan topikal sebagai pigmen pemutih. Karena indeks bias yang tinggi, titanium dioksida mempunyai sifat yang dapat memancarkan cahaya dalam penggunaannya sebagai pigmen pemutih atau pengopak (Rowe, dkk., 2003). Titanium dioksida merupakan senyawa yang tidak mengiritasi dan tidak bersifat toksik. Penelitian yang dilakukan terhadap beberapa spesies hewan, termasuk manusia, menunjukkan tidak terjadi penyerapan yang signifikan terhadap konsumsi titanium dioksida dan juga tidak tersimpan didalam jaringan (Rowe, dkk., 2003).
Dalam bidang farmasi, titanium dioksida digunakan sebagai zat pemutih dalam suspensi salut film, tablet salut gula dan kapsul gelatin. Titanium dioksida dapat juga dicampurkan dengan zat warna yang lain (Rowe, dkk., 2003).
Titanium dioksida sangat stabil pada temperatur tinggi, berwarna putih,amorf, tidak berasa dan tidak higroskopis. Tidak larut dalam H2SO4 encer, HCL, HNO3 pelarut-pelarut organik dan air, tetapi larut dalam asam hidrofluoric dan H2SO4
2.5 Polimer
panas (Rowe, dkk., 2003).
2.5.1 Polietilen Glikol (PEG)
Nama lain dari basis ini adalah Carbowax, Carbowax Sentry, Lipoxol, Lutrol E dan Phenol E (Raymond, 2006). Polietilenglikol merupakan polimer dari etilen oksida dan air. Pemberian nomor menunjukan berat molekul rata-rata dari masing-masing polimer. Polietilenglikol yang memiliki berat rata-rata 200, 400, dan 600 berupa cairan bening tidak berwarna dan yang memiliki berat molekul rata-rata lebih dari 1000 berupa lilin putih, padat, dan kepadatannya bertambah dengan bertambahnya berat molekul. Polietilenglikol memiliki beberapa keuntungan karena sifatnya yang inert, tidak mudah terhidrolisis, tidak membantu pertumbuhan jamur dan dapat dikombinasikan berdasarkan bobot molekulnya sehingga didapatkan suatu basis supositoria yang dikehendaki (Rowe, dkk., 2003).
Polietilenglikol 400 adalah polietilenglikol H(O-CH2-CH2)n OH dimana harga n antara 8,2 dan 9,1.Pemerian : cairan kental jernih, tidak berwarna atau praktis tidak berwarna,bau khas lemah, agak higroskopik. Kelarutan : larut dalam air, dalam etanol (95%) P, dalam aseton P, dalam glikol lain dan dalam hidrokarbon aromatik, praktis tidak larut dalam eter P dan dalam hidrokarbon alifatik. Bobot molekul rata-rata : 380-420, Kandungan Lembab : Sangat higroskopis walaupun higroskopis turun dengan meningkatnya bobot molekul, titik beku 4-8 0
Salah satu polimer yang umum digunakan pada pembuatan dispersi padat adalah polietilen glikol (PEG). Polietilenglikol (PEG) disebut juga makrogol,
merupakan polimer sintetik dari oksietilen dengan rumusstruktur H(OCH2CH2)nOH, dimana n adalah jumlah rata-rata gugus oksietilen. PEG umumnya memiliki bobot molekul antara 200–300000. Penamaan PEG umumnya ditentukan dengan bilangan yang menunjukkan bobot molekul rata-rata. Konsistensinya sangat dipengaruhi oleh bobot molekul. PEG dengan bobot molekul 200-600 (PEG 200-600) berbentuk cair, PEG 1500 semi padat, dan PEG 3000-20000 atau lebih berupa padatan semi kristalin, dan PEG dengan bobot molekul lebih besar dari 100000 berbentuk seperti resin pada suhu kamar. Umumnya PEG dengan bobot molekul 1500-20000 yang digunakan untuk pembuatan dispersi padat (Leuner and Dressman, 2000; Weller, 2003). Polimer ini mudah larut dalam berbagai pelarut, titik leleh dan toksisitasnya rendah, berada dalam bentuk semi kristalin (Craig, 1990). Kebanyakan PEG yang digunakan memiliki bobot molekul antara 4000 dan 20000, khususnya PEG 4000 dan 6000. Proses pembuatan dispersi padat dengan PEG 4000, umumnya menggunakan metode peleburan, karena lebih mudah dan murah (Rowe, dkk., 2003).
PEG (polietilen glikol) merupakan salah satu jenis bahan pembawa yang sering digunakan sebagai bahan tambahan dalam suatu formulasi untuk meningkatkan pelarutan obat yang sukar larut. Bahan ini merupakan salah satu jenis polimer yang dapat membentuk komplek polimer pada molekul organik apabila ditambahkan dalam formulasi untuk meningkatkan kecepatan pelarutan yang dapat membentuk komplek dengan berbagai obat. Cangkang kapsul dengan menggunakan basis polietilenglikol memiliki beberapa keuntungan karena sifatnya yang inert, tidak mudah terhidrolisis, tidak membantu pertumbuhan jamur (Martin, 1993).
2.6 Stabilitas Fisik Cangkang Kapsul Gelatin dan HPMC
2.6.1 Warna
Temperatur dan kadar uap air yang relatif tinggi selama proses pengolahan dan penyimpanan yang berkepanjangan merupakan salah satu faktor utama yang menyebabkan terjadinya reaksi pengcoklatan (enzimatik dan non-enzimatik) (Labuza, 1972).
Reaksi pengcoklatan adalah suatu reaksi dimana suatu bahan berubah menjadi coklat, baik melalui proses enzimatik maupun non-enzimatik. Pengcoklatan enzimatik ini melibatkan polifenol oksidase atau enzim lain yang menghasilkan melanin, sehingga menimbulkan warna coklat. Sedangkan pengcoklatan non-enzimatik dapat menimbulkan warna coklat tanpa adanya aktivitas enzim (Marshall, dkk., 2000).
Ogura dkk (1998) mengisi cangkang kapsul gelatin dan HPMC dengan asam askorbat dan membungkusnya dalam botol polietilen tanpa desikan dan menyimpannya pada suu 400
Reaksi Maillard merupakan suatu reaksi kimia pengcoklatan non-enzimatik antara gula pereduksi dengan protein atau asam amino. Tergantung pada jenis bahan dan jalannya reaksi, perubahan warna yang terjadi bisa dari kuning lemah sampai coklat gelap. Banyak faktor yang mempengaruhi reaksi Maillard, seperti temperatur, aktivitas air, pH, kadar uap air dan komposisi kimia suatu bahan (Morales, dkk., 1998).
C/RH 75% selama 2 bulan. Cangkang kapsul gelatin menjadi berwarna coklat, sedangkan cangkang kapsul HPMC tidak mengalami perubahan warna. Hal ini menandakan bahwa perubahan warna yang terjadi merupakan reaksi antara asam askorbat dan cangkang kapsul gelatin (dikenal dengan reaksi Maillard) (Honkanen, 2004).
2.6.2 Kerapuhan
Laju pengeringan kapsul juga mempengaruhi kekerasan dan kerapuhan kapsul, kemampuan pelarutan, dan kecenderungan untuk melekat satu sama lain.. Kadar uap air yang rendah pada kapsul dapat menghambat pertumbuhan mikroba. Jika kadar uap air pada kapsul gelatin kurang dari 10%, kapsul cenderung menjadi rapuh, dan sebaliknya jika kadar air lebih tinggi dari 18% kapsul gelatin melunak. Kondisi penyimpanan yang direkomendasikan untuk bentuk sediaan kapsul gelatin berkisar 15-300
Perubahan kerapuhan kapsul oleh kelembaban relatif telah dipelajari oleh Kontny dan Mulski. Pemantauan terhadap karakteristik kapsul yang disimpan pada kelembaban yang bervariasi membuktikan bahwa kelembaban merupakan salah satu parameter yang penting dalam pembuatan dan penyimpanan kapsul. Kriteria yang diterima bahwa kerapuhan kapsul yang signifikan tidak boleh terdeteksi pada kapsul yang disimpan pada kelembaban relatif 30% dan 50% selama 4 minggu (Kontny dan Mulski, 1989
[image:42.595.170.470.435.640.2]C dan 30%-60% kelembaban relatif (RH). (Margareth, dkk., 2009).
2.6.3 Waktu Hancur
Chiwele dkk. (2000) telah meneliti mengenai waktu hancur cangkang kapsul gelatin kosong dan kapsul HPMC (Hydroxypropyl Methylcellulose) setelah penyimpanan selama 24 jam pada kondisi tropis lembab (suhu 370
Hasil ini tidak jauh berbeda dengan yang dilaporkan Ogura (1998) bahwa cangkang kapsul HPMC yang telah diisi dengan spiramisin dan disimpan pada suhu 60
C, RH 75%) dan pada temperatur kamar. Dalam metode ini, mereka menggunakan bola besi sebagai bahan pengisi dalam kapsul. Pada penyimpanan kondisi tropis lembab, cangkang kapsul gelatin tidak mengalami perubahan waktu hancur dalam medium apapun, sedangkan waktu hancur kapsul HPMC tidak berubah hanya dalam medium cairan lambung buatan (Honkanen, 2004).
0
C, RH 75% selama 10 hari tidak mengalami perubahan sifat waktu hancur. Tetapi, mereka menggunakan prosedur standar uji waktu hancur dalam farmakope, yang tidak dapat menentukan waktu hancur cangkang kapsul dan bahan obat secara terpisah. Sedangkan dalam metode yang digunakan Chiwele dkk. (2000), bola besi yang digunakan tidak mempengaruhi waktu hancur (Honkanen, 2004).
2.7 Viskositas
2.8 Studi Stabilitas
Waktu nyata dan studi dipercepat dilaksanakan pada bets primer atau bets yang ditetapkan sesuai protocol uji stabilitas untuk menetapkan atau memastikan masa uji ulang dari suatu zat aktif dengan masa simpan atau edar suatu produk.
2.8.1 Uji Dipercepat
Studi didesain untuk meningkatkan derajat degradasi kimiawi atau perubahan fisis dari zat aktif atau produk dengan menggunakan kondisi penyimpanan “berlebihan” sebagai bagian dari studi stabilitas formal. Data yang diperoleh dari studi ini, dapat digunakan untuk menilai efek kimiawi jangka panjang pada kondisi yang tidak dipercepat. Uji dipercepat dilakukan selama 3-6 bulan.
2.8.2 Pengujian Jangka Panjang atau Waktu Nyata.
Pengujian jangka panjang biasanya dilaksakan setiap 3 bulan selama tahun pertama, setiap 6 bulan selama tahun ke 2 dan selanjutnya tiap tahun selama masa simpan atau edar pada paling sedikit 3 bets primer. Studi stabilitas lanjutan atau jangka panjang dilakukan selama 3, 6, 9, 12, 18, 24, 36 dan seterusnya akan dilaksanakan sesuai panduan uji stabilitas setempat dan ASEAN.
2.8.3 Pengujian Pasca Pemasaran
Studi stabilitas hendaknya dilakukan tiap tahun terhadap produk yang dipasarkan. Studi tersebut hendaknya dilaksanakan pada 1 bets dari tiap produk/tahun dan meliputi paling sedikit selama 12 bulan untuk jangka waktu yang cukup mencakup masa simpan/edar yang diusulkan (Balai POM, 2009).
2.9 Pengujian Stabilitas
Parameter pengujian stabilitas adalah : a. Pemerian
b. Identifikasi sesuai dengan monografinya c. Uji disolusi
e. Degradasi
Sebagai contoh, untuk sediaan tablet parameter pemeriksaan selama proses yang dapat dikurangi antara lain keseragaman bobot, kekerasan, kerenyahan dan waktu hancur (Balai POM, 2009)
2.9.1 Warna
Warna merupakan salah satu aspek yang mempengaruhi penilaian konsumen terhadap kualitas produk. Stabilitas formulasi obat dapat dideteksi dalam beberapa hal dengan suatu perubahan fisik, warna, bau dan tekstur dari formulasi tersebut. Temperatur, pH, kekuatan ion, intensitas cahaya dapat mempengaruhi perubahan kestabilan pada obat (Ansel, 2005).
2.9.2 Kerapuhan
Perlu diketahui bahwa cangkang kapsul bukan tidak reaktif, secara fisika atau kimia. Perubahan kondisi penyimpanan seperti temperatur dan kelembaban dapat mempengaruhi sifat kapsul. Dengan terjadinya kenaikan temperatur dan kelembaban dapat menyebabkan kapsul mengikat atau melepaskan uap air. Sebagai akibatnya kapsul dapat menjadi rapuh atau lunak (Margareth, dkk., 2009).
Laju pengeringan kapsul juga mempengaruhi kekerasan dan kerapuhan kapsul, kemampuan pelarutan, dan kecenderungan untuk melekat satu sama lain. Kadar air yang rendah pada kapsul dapat menghambat pertumbuhan mikroba. Jika kadar air pada kapsul kurang dari 10%, kapsul cenderung menjadi rapuh, dan sebaliknya jika kadar air lebih tinggi dari 18% kapsul melunak. Kondisi penyimpanan yang direkomendasikan untuk bentuk sediaan kapsul berkisar 15-300
Perubahan kerapuhan kapsul oleh kelembaban relatif telah dipelajari oleh Kontny dan Mulski. Pemantauan terhadap karakteristik kapsul yang disimpan pada kelembaban yang bervariasi membuktikan bahwa kelembaban merupakan salah satu parameter yang penting dalam pembuatan dan penyimpanan kapsul. Kriteria yang diterima bahwa kerapuhan kapsul yang signifikan tidak boleh
terdeteksi pada kapsul yang disimpan pada kelembaban relatif 30% dan 50% selama 4 minggu (Kontny dan Mulski, 1989).
2.9.3 Disolusi
Proses melarutnya suatu obat disebut disolusi (Ansel, 1989). Uji disolusi yaitu uji pelarutan invitro mengukur laju dan jumlah pelarutan obat dalam suatu media aqueous dengan adanya satu atau lebih bahan tambahan yang terkandung dalam produk obat. Pelarutan obat merupakan bagian penting sebelum kondisi absorbsi sistemik (Shargel dan Andrew, 1988).
Faktor-faktor yang mempengaruhi disolusi dibagi atas 3 kategori yaitu:
a. Faktor-faktor yang berhubungan dengan sifat fisikokimia obat, meliputi: i. Efek kelarutan obat. Kelarutan obat dalam air merupakan faktor utama
dalam menentukan laju disolusi. Kelarutan yang besar menghasilkan laju disolusi yang cepat.
ii. Efek ukuran partikel. Ukuran partikel berkurang dapat memperbesar luas permukaan obat yang berhubungan dengan medium, sehingga laju disolusi meningkat.
b. Faktor-faktor yang berhubungan dengan sediaan obat, meliputi:
i. Efek formulasi. Laju disolusi suatu bahan obat dapat dipengaruhi bila dicampur dengan bahan tambahan. Bahan pengisi, pengikat dan penghancur yang bersifat hidrofil dapat memberikan sifat hidrofil pada bahan obat yang hidrofob, oleh karena itu disolusi bertambah, sedangkan bahan tambahan yang hidrofob dapat mengurangi laju disolusi.
ii. Efek faktor pembuatan sediaan. Metode granulasi dapat mempercepat laju disolusi obat-obat yang kurang larut. Penggunaan bahan pengisi yang bersifat hidrofil seperti laktosa dapat menambah hidrofilisitas bahan aktif dan menambah laju disolusi.
i. Tegangan permukaan medium disolusi. Tegangan permukaan mempunyai pengaruh nyata terhadap laju disolusi bahan obat. Surfaktan dapat menurunkan sudut kontak, oleh karena itu dapat meningkatkan proses penetrasi medium disolusi ke matriks. Formulasi tablet dan kapsul konvensional juga menunjukkan penambahan laju disolusi obat-obat yang sukar larut dengan penambahan surfaktan kedalam medium disolusi.
ii. Viskositas medium. Semakin tinggi viskositas medium, semakin kecil laju disolusi bahan obat.
iii. pH medium disolusi. Larutan asam cenderung memecah tablet sedikit lebih cepat dibandingkan dengan air, oleh karena itu mempercepat laju disolusi (Gennaro, 2000). Obat-obat asam lemah disolusinya kecil dalam medium asam, karena bersifat nonionik, tetapi disolusinya besar pada medium basa karena terionisasi dan pembentukan garam yang larut (Martin, dkk., 1993).
United States Pharmacopeia (USP) XXXII memberi beberapa metode resmi untuk melaksanakan uji pelarutan yaitu:
a. Metode Keranjang (Basket)
Metode keranjang terdiri atas keranjang silindrik yang ditahan oleh tangkai motor. Keranjang menahan cuplikan dan berputar dalam suatu labu bulat yang berisi media pelarutan. Keseluruhan labu tercelup dalam suatu bak yang bersuhu konstan 37o
b. Metode Dayung (Paddle)
C. Kecepatan berputar dan posisi keranjang harus memenuhi rangkaian syarat khusus dalam USP yang terakhir beredar. Tersedia standar kalibrasi pelarutan untuk meyakinkan bahwa syarat secara mekanik dan syarat operasi telah dipenuhi.
ditempatkan dalam suatu bak air yang bersuhu konstan, seperti pada metode basket dipertahankan pada 37o
c. Metode Disintegrasi yang Dimodifikasi
C. Posisi dan kesejajaran dayung ditetapkan dalam USP. Metode dayung sangat peka terhadap kemiringan dayung. Pada beberapa produk obat, kesejajaran dayung yang tidak tepat secara drastis dapat mempengaruhi hasil pelarutan. Standar kalibrasi pelarutan yang sama digunakan untuk memeriksa peralatan sebelum uji dilaksanakan.
Metode ini dasarnya memakai disintegrasi USP ”basket and rack” dirakit untuk uji pelarutan. Bila alat ini dipakai untuk pelarutan maka cakram dihilangkan. Saringan keranjang juga diubah sehingga selama pelarutan partikel tidak akan jatuh melalui saringan. Metode ini jarang digunakan dan dimasukkan dalam USP untuk suatu formulasi obat lama. Jumlah pengadukan dan getaran membuat metode ini kurang sesuai untuk uji pelarutan yang tepat (Shargel dan Andrew, 1988).
2.10 Pengemasan
Pada penelitian sebelumnya dilakukan pengujian stabilitas kapsul alginat yang disimpat dalam botol dan ditambahkan silika gel, diperoleh hasil bahwa kapsul alginat tidak stabil, ditandai dengan adanya perubahan warna pada cangkang kapsul, yaitu menjadi warna coklat (Hendra, 2011).
2.11 Pengukuran Hasil Disolusi Aspirin Menggunakan Spektrofotometer UV
Spektrofotometri serapan adalah pengukuran serapan radiasi elektromagnit panjang gelombang tertentu yang sempit, mendekati monokromatik yang diserap zat. Pengukuran serapan dapat dilakukan pada daerah ultraviolet (panjang gelombang 200 nm-400 nm).
Penetapan kadar Aspirin bisa dilakukan dengan Spektrofotometri UV, High Perfomance Liquid Chromatography (HPLC), Infra-red Spectrum dan Massa Spectrum. Untuk Uji disolusi Aspirin menggunakan spekrofotomertri UV dengan panjang gelombang pada suasana asam yaitu 237,0 nm dan suasana basa yaitu 275,0 nm (Moffats, 2005).
BAB III
METODE PENELITIAN
3.1 Alat-alat
Alat disolusi metoda dayung (Yamato), spektrofotometer (UV-1800
Shimadzu Spectrophotometer), neraca analitik (Boeco), pH meter (Hanna),
viskometer Thomas-Stomer (Haake), termometer, climatic chamber (Memmeth), alat uji waktu hancur (Copley), anak timbangan 50 g dan 2 kg, jangka sorong
(Tricle), mikrometer (Delta), alat pencetak kapsul yang terbuat dari batang
stainless steel berbentuk silindris dengan panjang 10 cm serta berdiameter 6,0 mm
untuk bagian badan cangkang kapsul dan 6,2 mm untuk bagian tutup cangkang
kapsul, bola besi berbahan stainless steel bediameter 1,44 mm dan berat 9 mg (sebagai pengisi untuk uji waktu hancur), cincin disolusi, stopwatch, kamera
digital, labu tentukur 1000 ml (Pyrex), labu tentukur 25 ml (Pyrex), beaker glass
(Pyrex), pipet volume 5 ml (Pyrex), gelas ukur (Pyrex), pipet tetes, bola karet,
botol dan alat-alat laboratorium yang biasa digunakan.
3.2 Bahan-bahan
Natrium alginat 80-120 cP dan natrium alginat 300-400 cP adalah produk
Wako Pure Chemical Industries, Ltd. Japan, Titanium dioksida, PEG, natrium
meta-bisulfit, acetosal, kalium dihidrogen fosfat, natrium hidroksida, asam klorida
(Merck), kalsium klorida anhidrat (Wako Pure Chemical Industries, Ltd Japan),
Gliserin, dan laktosa.
3.3`Prosedur
3.3.1.1Larutan Natrium Hidroksida 0,2 N
Natrim hidroksida sebanyak 8 gram dilarutkan dalam akuades bebas CO2
3.3.1.2Larutan Natrium Hidroksida 1N sampai 1000 ml (Ditjen POM, 1995).
Natrim hidroksida sebanyak 40,01 gram dilarutkan dalam akuades bebas
CO2
3.3.1.3Larutan Asam Klorida 1N sampai 1000 ml (Ditjen POM, 1995).
Asam klorida pekat sebanyak 85 ml dilarutkan dalam akuades sampai
1000 ml.
3.3.1.4 Larutan Kalium Biftalat 0,2 M
Kalium biftalat sebanyak 40,85 gram dilarutkan dalam akuades sampai
1000 ml.
3.3.1.5Larutan Kalsium Klorida 0,15M
Kalsium klorida dihidrat (CaCl2.2H2
3.3.1.6 Medium Cairan Lambung Buatan Tanpa Enzim (Medium pH 1,2) O) sebanyak 22,05 gram dilarutkan
dalam akuades hingga 1000 ml.
Natrium klorida sebanyak 2 gram dilarutkan dalam akuades secukupnya
lalu ditambahkan 7 ml asam klorida pekat dan dicukupkan dengan akuades
3.3.1.7Medium Cairan Lambung Buatan Tanpa Enzim (Medium pH 3,0)
Kalium biftalat sebanyak 50 ml dimasukkan ke dalam labu tentukur 200
ml, kemudian ditambahkan HCl 0,2 M sebanyak 22,3 ml lalu dicukupkan hingga
garis tanda.
3.3.1.8Medium Cairan Lambung Buatan Tanpa Enzim (Medium pH 4,0)
Kalium biftalat sebanyak 50 ml dimasukkan ke dalam labu tentukur 200
ml, kemudian ditambahkan HCl 0,2 M sebanyak 0,1 ml lalu dicukupkan hingga
garis tanda.
3.3.1.9Medium Cairan Lambung Buatan Tanpa Enzim (Medium pH 5,0)
Kalium biftalat sebanyak 50 ml dimasukkan ke dalam labu tentukur 200
ml, kemudian ditambahkan natrium hidroksida 0,2 M sebanyak 22,6 ml lalu
dicukupkan hingga garis tanda.
2.3.1.10 Medium Cairan Usus Buatan Tanpa Enzim (Medium pH 6,8)
Kalium dihidrogen fosfat sebanyak 6,8 gram dilarutkan dalam 250 air
suling bebas CO2, lalu ditambahkan natrium hidroksida 0,2 N sebanyak 112
ml,lalu ditambahkan air suling bebas CO2
2.3.1.11 Medium Cairan Usus Buatan Tanpa Enzim (Medium pH 7,0)
hingga volumenya 1000 ml (Ditjen
POM, 1995).
Kalium dihidrogen fosfat sebanyak 6,8 gram dilarutkan dalam 250 air
suling bebas CO2,lalu ditambahkan natrium hidroksida 0,2 N sebanyak 146
ml,lalu ditambahkan air suling bebas CO2 hingga volumenya 1000 ml (Ditjen
3.3.2 Pembuatan Kurva Serapan dan Kurva Kalibrasi Larutan Asam Salisilat dalam Medium Cairan Lambung Buatan (pH 1,2)
3.3.2.1 Pembuatan Larutan Induk Baku Asam Salisilat
Ditimbang 62,5 mg asam salisilat dan dimasukkan ke dalam labu tentukur
250 ml, ditambahkan 5 ml etanol hingga larut. Kemudian dicukupkan dengan
cairan lambung buatan hingga 250 ml. (Konsentrasi LIB = 250 ppm).
3.3.2.2Pembuatan Kurva Serapan Larutan Asam Salisilat
Larutan induk baku dipipet 0,6 ml, dimasukkan ke dalam labu tentukur 25
ml, dicukupkan dengan cairan lambung buatan sampai garis tanda, dikocok
sampai homogen. Diukur s