EFEKTIVITAS EKSTRAK KULIT BUAH DELIMA
(Punica granatum L.) TERHADAP BAKTERI
Porphyromonas gingivalis
SECARA IN VITRO
SKRIPSI
Diajukan untuk memenuhi tugas dan melengkapi
syarat guna memperoleh gelar Sarjana Kedokteran Gigi
Oleh :
SHINTA
NIM: 100600038
FAKULTAS KEDOKTERAN GIGI
UNIVERSITAS SUMATERA UTARA
Fakultas Kedokteran Gigi
Departemen Ilmu Periodonsia
Tahun 2014
Shinta
Efektivitas Ekstrak Kulit Buah Delima (Punica granatum L.) terhadap Bakteri
Porphyromonas gingivalis secara in vitro
x + 50 halaman
Porphyromonas gingivalis merupakan salah satu bakteri yang paling banyak ditemukan pada penyakit periodontal. Penggunaan antimikroba sintetis sebagai
perawatan penyakit periodontal memiliki banyak efek samping. Potensi bahan alami
dari tumbuhan untuk profilaksis oral menjadi perlu dipertimbangkan. Buah delima
(Punica granatum L) telah dikenal selama ratusan tahun untuk manfaat kesehatan manusia, termasuk aktifitas antimikroba. Delima kaya akan kandungan phenolic, flavonoid, tanin, dan antosianin. Kandungan tersebut lebih tinggi pada kulit daripada
jus buahnya. Tujuan dari penelitian ini adalah untuk mengetahui efektivitas ekstrak
kulit buah delima terhadap bakteri P. gingivalis secara in vitro dengan mencari
Konsentrasi Hambat Minimum (KHM) dan Konsentrasi Bunuh Minimum (KBM).
Penelitian ini dimulai dengan melakukan ekstraksi kulit buah delima dengan metode
perkolasi dengan pelarut etanol hingga menghasilkan ekstrak kental kulit buah
6,25%, 3,125%, 1,6125% dan 0,8%. Masing-masing konsentrasi kemudian diuji nilai
efektivitasnya terhadap P.gingivalis pada media Tryptic Soy Agar dengan metode
Drop plates Miles Mesra. Hasil penelitian menunjukkan bahwa pada konsentrasi
25%, 12,5%, 6,25%, 3,125%, 1,6125% dijumpai tidak adanya pertumbuhan bakteri
yang senilai dengan 0 CFU/ml, sedangkan pada konsentrasi 0,8% dijumpai
pertumbuhan bakteri dengan rata-rata jumlah pada tiap pengulangan adalah 4,56 x
102 CFU/ml. Kesimpulan dari penelitian, ekstrak kulit buah delima memiliki
efektivitas terhadap P. gingivalis dengan nilai KBM 1,6125%. Nilai KHM tidak diketahui karena tidak bisa dibedakan kekeruhan yang terjadi.
Kata Kunci : Kulit buah delima, antibakteri, Porphyromonas gingivalis
Faculty of Dentistry
Department of Periodonsia
In 2014
Shinta
Effectiveness of Pomegranate Peel Extract ( Punica granatum L. ) against bacteria
Porphyromonas gingivalis in vitro
x + 50 pages
Porphyromonas gingivalis is one of the most commonly bacteria that found in periodontal disease. The use of a synthetic antimicrobial treatment of periodontal
disease has many side effects. The potential of natural ingredients from plants for oral
prophylaxis should be considered. Pomegranate (Punica granatum L) has been
known for hundreds of years for the benefit of human health, including antimicrobial
activity. Pomegranate rich in phenolic, flavonoids, tannins, and anthocyanin. The
content was higher in the peel than fruit juice. The purpose of this study was to
determine the effectiveness of pomegranate peel extract against bacteria P. gingivalis in vitro by finding the Minimum Inhibitory Concentration (MIC) and Minimum
Bactericidal Concentration (MBC). The study began with pomegranate peel extract
by percolation method with ethanol to produce a thick rind of pomegranate extract.
The extract was then diluted to obtain a concentration of 25 %, 12.5 %, 6.25 %, 3.125
against P.gingivalis cultured in medium with Tryptic Soy Agar with Droplet Miles Mesra method. The results showed that at a concentration of 25 %, 12.5 %, 6.25 %,
3.125 %, 1.6125 % found no bacterial growth amounting to 0 CFU/ml, whereas at a
concentration of 0.8 % found with the bacterial growth rate the average amount of
each repetition is 4.56 x 102 CFU/ml. In conclusion, pomegranate peel extract has
efficacy against P. gingivalis with MBC value of 1.6125%. MIC value is unknown because it can not be distinguished turbidity occurs.
Keywords : Pomegranate peel, antibacterial, Porphyromonas gingivalis
EFEKTIVITAS EKSTRAK KULIT BUAH DELIMA
(Punica granatum L.) TERHADAP BAKTERI
Porphyromonas gingivalis
SECARA IN VITRO
SKRIPSI
Diajukan untuk memenuhi tugas dan melengkapi
syarat guna memperoleh gelar Sarjana Kedokteran Gigi
Oleh :
SHINTA
NIM: 100600038
FAKULTAS KEDOKTERAN GIGI
UNIVERSITAS SUMATERA UTARA
PERNYATAAN PERSETUJUAN
Skripsi ini telah disetujui untuk dipertahankan
di hadapan tim penguji skripsi
Medan, 23 Januari 2014
Pembimbing: Tanda Tangan
Irma Ervina.,drg.,Sp.Perio (K)
TIM PENGUJI SKRIPSI
Skripsi ini telah dipertahankan di hadapan tim penguji
pada tanggal 23 Januari 2014
TIM PENGUJI
Tanda Tangan
KETUA : Irma Ervina.,drg.,Sp.Perio (K) ………..
ANGGOTA : 1. Zulkarnain, drg., M.Kes ………..
2.Aini Hariyani Nasution, drg., Sp. Perio ………..
Mengetahui,
KETUA DEPARTEMEN
Irmansyah Rangkuti, drg., Ph.D ………..
KATA PENGANTAR
Puji syukur penulis panjatkan kepada Tuhan Yang Maha Esa yang telah
memberikan rahmat dan karunia-Nya, sehingga penulis dapat menyelesaikan skripsi
ini sebagai salah satu syarat untuk memperoleh gelar Sarjana Kedokteran Gigi.
Rasa terima kasih yang tak terhingga penulis sampaikan kepada kedua orang
tua tercinta, Ayahanda Sudarmi dan Ibunda Ernawati, serta Abang tersayang Ridwan
S.P yang senantiasa menyayangi, mendoakan dan mendukung penulis sehingga
penulis dapat mengecap masa pendidikan hingga selesai di Fakultas Kedokteran Gigi
Universitas Sumatera Utara Medan.
Dalam penulisan skripsi ini, penulis juga telah banyak mendapat bimbingan,
bantuan, motivasi, saran-saran serta doa dari berbagai pihak. Oleh karena itu, dengan
kerendahan hati serta penghargaan yang tulus penulis mengucapkan terima kasih
kepada :
1. Prof. Nazaruddin, drg., C.Ort., PhD., Sp.Ort selaku Dekan Fakultas
Kedokteran Gigi Universitas Sumatera Utara.
2. Irmansyah R, drg., PhD selaku Ketua Departemen Periodonsia Fakultas
Kedokteran Gigi Universitas Sumatera Utara.
3. Irma Ervina, drg., Sp.Perio(K) selaku dosen pembimbing skripsi yang telah
banyak meluangkan waktu, tenaga dan pikirannya dalam memberikan bimbingan,
masukan dan semangat kepada penulis dalam menyelesaikan skripsi ini.
4. Dosen penguji skripsi (Zulkarnain, drg., M.Kes dan Aini Haryani Nasution,
drg., Sp.Perio) atas saran dan masukan sehingga skripsi ini dapat lebih baik.
5. Ariyani, drg selaku dosen pembimbing akademik yang telah memberikan
perhatian dan motivasi kepada penulis selama menjalani pendidikan di FKG USU.
6. Seluruh staf pengajar di Departemen Periodonsia FKG USU yang telah
7. Drs. Awaluddin Saragih, M.Si., Apt selaku kepala Laboratorium Obat Tradisional Fakultas Farmasi USU; Abang Bagus, Abang Ari, dan Abang Angga yang telah banyak membantu dalam kegiatan ekstraksi.
8. Wahyu Hidayahtiningsih, S.Si., M.Kes selaku kepala Laboratorium Rumah Sakit Penyakit Tropik Infeksi UNAIR yang membantu dalam kegiatan di laboratorium.
9. Terima kasih penulis sampaikan kepada teman-teman seperjuangan skripsi
di Departemen Periodonsia, Wita, Gebby, Widi, Hazwani, Nazim, Yolanda, Brian,
Shelly, Nastiti, Afiqah dan Ayu.
11. Para sahabat penulis, Rangga, Naro, Cindy, Monica, Wanda, Wahyu,
May, Ummi, Elsa, Mila, Mala, dan Yudha yang telah memberikan saran, semangat,
doa dan dukungan selama studi dan penelitian ini.
Penulis menyadari penulisan skripsi ini masih jauh dari sempurna karena ada
kelemahan dan keterbatasan ilmu yang penulis miliki, namun penulis mengharapkan
kiranya hasil karya sederhana ini dapat memberikan sumbangan pikiran yang berguna
bagi fakultas, pengembangan ilmu dan masyarakat.
Medan, 23 Januari 2014
Penulis
...
( Shinta )
DAFTAR ISI
Halaman
HALAMAN JUDUL ... i
HALAMAN PERSETUJUAN ... ii
HALAMAN TIM PENGUJI SKRIPSI ... iii
KATA PENGANTAR ... iv
2.2Etiologi dan Patogenesis Penyakit Periodontal ... 5
2.3Bakteri Porphyromonas gingivalis ... 7
2.3.1 Faktor Virulensi Bakteri dan Metode Invasi Pada Jaringan. 8
2.4Perawatan Penyakit Periodontal ... 9
2.4.1 Pembersihan Mekanis ... 10
2.4.2 Terapi Farmakologikal ... 10
2.6Nilai Farmakologis Buah Delima ... 13
2.7Efek Ekstrak Kulit Buah Delima Terhadap Bakteri Periodontal 15 2.8Keamanan Ekstrak Delima ... 16
2.9Kerangka Teori ... 17
2.10Kerangka Konsep ... 18
BAB 3 METODOLOGI PENELITIAN 3.1.Jenis dan Rancangan Penelitian ... 19
3.2.Tempat dan Waktu Penelitian ... 19
3.3.Sampel dan Besar Sampel Penelitian ... 20
3.4.Variabel Penelitian ... 21
3.5.Defenisi Operasional ... 21
3.6.Bahan dan Alat Penelitian ... 22
3.7.Proses Pengambilan dan Pengumpulan Data ... 23
3.8.Alur Penelitian ... 31
3.9.Analisis Data ... 31
BAB 4 HASIL PENELITIAN ... 32
BAB 5 PEMBAHASAN ... 37
BAB 6 KESIMPULAN DAN SARAN 6.1. Kesimpulan ... 41
6.2. Saran ... 41
DAFTAR PUSTAKA ... 42
DAFTAR TABEL
Tabel Halaman
1. Daya antibakteri ekstrak kulit buah delima pada penentuan terhadap
DAFTAR GAMBAR
5. Kulit delima dikeringkan di lemari pengering ... 24
6. Kulit delima yang telah kering ... 24
7. Penimbangan kulit delima kering ... 25
8. Pemblenderan kulit delima ... 25
9. Serbuk simplisia ditimbang ... 25
10.Maserasi serbuk simplisia disertai pengadukan ... 25
11.Serbuk kulit delima yang direndam etanol di perkolator ... 26
12.Proses penguapan etanol dan air dalam vacum rotary evaporator 26
13.Ekstrak kental kulit buah delima ... 26
14.Penimbangan dan pelarutan bubuk Triptic Soy Agar ... 27
15.Media disterilkan menggunakan autoklaf ... 28
16.Media Tryptic Soy Agar yang telah selesai dibuat ... 28
17.P.gingivalis ATCC 33277 yang telah dibiakkan pada TSA ... 29
18.Bakteri P.gingivalis yang telah dikultur pada media TSA... 32
19.Bakteri P.gingivalis dilihat dari mikroskop ... 32
20.Kejernihan pada tabung percobaan tidak dapat diamati karena warna ekstrak yang sangat coklat ... 33
21.Pengujian efek anti bakteri pada konsentrasi 1,6125 %, 3,125% dan 6,25% menunjukkan tidak adanya pertumbuhan bakteri ... 35
22.Pengujian efek antibakteri pada konsentrasi 12,5% dan 25% menunjukkan tidak adanya pertumbuhan bakteri (steril) ... 35
DAFTAR LAMPIRAN
1. Data Hasil Uji Ekstrak Kulit buah Delima (Punica granatum L) terhadap
Porphyromonas gingivalis
2. Hasil Identifikasi / Determinasi Tumbuhan
Fakultas Kedokteran Gigi
Departemen Ilmu Periodonsia
Tahun 2014
Shinta
Efektivitas Ekstrak Kulit Buah Delima (Punica granatum L.) terhadap Bakteri
Porphyromonas gingivalis secara in vitro
x + 50 halaman
Porphyromonas gingivalis merupakan salah satu bakteri yang paling banyak ditemukan pada penyakit periodontal. Penggunaan antimikroba sintetis sebagai
perawatan penyakit periodontal memiliki banyak efek samping. Potensi bahan alami
dari tumbuhan untuk profilaksis oral menjadi perlu dipertimbangkan. Buah delima
(Punica granatum L) telah dikenal selama ratusan tahun untuk manfaat kesehatan manusia, termasuk aktifitas antimikroba. Delima kaya akan kandungan phenolic, flavonoid, tanin, dan antosianin. Kandungan tersebut lebih tinggi pada kulit daripada
jus buahnya. Tujuan dari penelitian ini adalah untuk mengetahui efektivitas ekstrak
kulit buah delima terhadap bakteri P. gingivalis secara in vitro dengan mencari
Konsentrasi Hambat Minimum (KHM) dan Konsentrasi Bunuh Minimum (KBM).
Penelitian ini dimulai dengan melakukan ekstraksi kulit buah delima dengan metode
perkolasi dengan pelarut etanol hingga menghasilkan ekstrak kental kulit buah
6,25%, 3,125%, 1,6125% dan 0,8%. Masing-masing konsentrasi kemudian diuji nilai
efektivitasnya terhadap P.gingivalis pada media Tryptic Soy Agar dengan metode
Drop plates Miles Mesra. Hasil penelitian menunjukkan bahwa pada konsentrasi
25%, 12,5%, 6,25%, 3,125%, 1,6125% dijumpai tidak adanya pertumbuhan bakteri
yang senilai dengan 0 CFU/ml, sedangkan pada konsentrasi 0,8% dijumpai
pertumbuhan bakteri dengan rata-rata jumlah pada tiap pengulangan adalah 4,56 x
102 CFU/ml. Kesimpulan dari penelitian, ekstrak kulit buah delima memiliki
efektivitas terhadap P. gingivalis dengan nilai KBM 1,6125%. Nilai KHM tidak diketahui karena tidak bisa dibedakan kekeruhan yang terjadi.
Kata Kunci : Kulit buah delima, antibakteri, Porphyromonas gingivalis
Faculty of Dentistry
Department of Periodonsia
In 2014
Shinta
Effectiveness of Pomegranate Peel Extract ( Punica granatum L. ) against bacteria
Porphyromonas gingivalis in vitro
x + 50 pages
Porphyromonas gingivalis is one of the most commonly bacteria that found in periodontal disease. The use of a synthetic antimicrobial treatment of periodontal
disease has many side effects. The potential of natural ingredients from plants for oral
prophylaxis should be considered. Pomegranate (Punica granatum L) has been
known for hundreds of years for the benefit of human health, including antimicrobial
activity. Pomegranate rich in phenolic, flavonoids, tannins, and anthocyanin. The
content was higher in the peel than fruit juice. The purpose of this study was to
determine the effectiveness of pomegranate peel extract against bacteria P. gingivalis in vitro by finding the Minimum Inhibitory Concentration (MIC) and Minimum
Bactericidal Concentration (MBC). The study began with pomegranate peel extract
by percolation method with ethanol to produce a thick rind of pomegranate extract.
The extract was then diluted to obtain a concentration of 25 %, 12.5 %, 6.25 %, 3.125
against P.gingivalis cultured in medium with Tryptic Soy Agar with Droplet Miles Mesra method. The results showed that at a concentration of 25 %, 12.5 %, 6.25 %,
3.125 %, 1.6125 % found no bacterial growth amounting to 0 CFU/ml, whereas at a
concentration of 0.8 % found with the bacterial growth rate the average amount of
each repetition is 4.56 x 102 CFU/ml. In conclusion, pomegranate peel extract has
efficacy against P. gingivalis with MBC value of 1.6125%. MIC value is unknown because it can not be distinguished turbidity occurs.
Keywords : Pomegranate peel, antibacterial, Porphyromonas gingivalis
BAB 1
PENDAHULUAN
1.1 Latar Belakang
Penyakit periodontal merupakan penyakit inflamasi kronis pada jaringan
gingiva dan jaringan pendukung gigi.1 Penyakit ini diawali dengan inflamasi pada
gingiva yang kemudian dapat berlanjut menjadi penyakit periodontal yang lebih
parah dan dapat menyebabkan kehilangan gigi.2,3
Bakteri merupakan penyebab utama terjadinya penyakit periodontal.4
Penelitian mikrobiologi telah mengungkapkan bahwa infeksi pada poket periodontal
merupakan infeksi multibakterial. Peningkatan spesifik terjadi pada spesies bakteri
Agregatibacter actinomycetemcomitans (A. actinomycetemcomitans), Porphyromonas gingivalis (P. gingivalis), Prevotella intermedia (P. intermedia) dan
Treponema denticola (T. denticola) yang merupakan agen etiologi utama pada penyakit periodontal destruktif.5
P. gingivalis merupakan spesies bakteri anaerob negatif Gramm dan merupakan salah satu jenis dari black-pigmented bacterioides. P. gingivalis
ditemukan pada pasien penderita periodontitis kronis ringan pada orang dewasa dan
remaja. Selain itu, P. gingivalis juga merupakan spesies utama yang terkait dengan periodontitis kronis sedang dan berat pada orang dewasa disamping P. intermedia dan
A. actinomycetemcomitans.5 Stingu melaporkan bahwa prevalensi P. gingivalis
terdeteksi sebanyak 51% pada pasien periodontitis kronis,6 sedangkan Kamma
melaporkan prevalensinya adalah sebesar 89,4% pada periodontitis agresif.7
Selanjutnya, P. gingivalis memiliki proporsi jauh lebih tinggi pada poket yang dalam dibanding dari poket periodontal yang dangkal.5
Perawatan dasar penyakit periodontal yang utama adalah menghilangkan plak
dengan cara mekanis seperti menyikat gigi dan pembuangan deposit lainnya di
dalam praktek sehari-hari oleh banyak individu.9 Pembersihan patogen periodontal
dengan skeling dan root planing juga tidak maksimal, karena terdapat bagian yang tidak dapat diakses oleh alat skeling dan root planing, sehingga pemberian antimikroba dianjurkan untuk meningkatkan hasil terapi.10
Sejumlah bahan kimia antimikroba telah banyak diproduksi, namun tidak
satupun yang tanpa kekurangan. Klorheksidin selama ini digunakan sebagai gold standard, namun tidak dapat diberikan untuk waktu yang lama karena menyebabkan pewarnaan gigi, rasa yang tidak menyenangkan dan iritasi mukosa mulut. Selain
klorheksidin, penggunaan minyak esensial dari tanaman telah dievaluasi secara
ekstensif dan kemudian terbukti memiliki nilai tambah untuk prosedur profilaksis
oral. Upaya untuk menemukan agen antiplak dan antigingivitis yang dapat digunakan
dalam jangka panjang, ideal, dan aman pun berlanjut. Masalah meningkatnya
resistensi terhadap antimikroba sintetik juga telah mendorong mencari produk alami
alternatif. Sehingga, potensi bahan alami dari tumbuhan untuk profilaksis oral
menjadi perlu dipertimbangkan.9
Buah delima (Punica granatum Linn) telah dikenal selama ratusan tahun untuk manfaat kesehatan manusia, termasuk aktifitas antimikroba. Penelitian
menunjukkan bahwa buah delima dan ekstraknya dapat berfungsi sebagai alternatif
alami karena potensinya terhadap berbagai patogen bakteri dan virus. Hampir setiap
bagian dari tanaman delima telah diuji untuk aktifitas antimikroba, termasuk jus
buah, kulit buah, bunga, dan kulit batang. Banyak penelitian telah memanfaatkan
kulit delima dengan sukses.11 Delima memiliki kandungan polifenol, flavonoid, asam
tanin (asam ellagic), dan antosianin yang merupakan antioksidan yang kuat.12,13 Kandungan tersebut lebih tinggi pada kulit daripadajus buahnya.14 Kadar antioksidan
pada delima hampir menyamai teh hijau dan lebih tinggi daripada anggur merah.
Antioksidan ini dapat menghambat pembentukan matriks polisakarida pada plak,
menghambat perlekatan bakteri, dan mencegah terbentuknya asam. Selain itu,
penelitian menunjukkan bahwa ekstrak buah delima dapat menguatkan kembali gigi
yang goyang dan mengurangi tanda-tanda klinis periodontitis kronis.13 Kandungan
yang tinggi. Flavonoid memiliki daya hambat tehadap Aspergillus niger, Bacillus subtillis, Candida albicans, Escherichia coli, Saccaromyces sereviceae, Staphylococcus aureus dan Staphylococcus epidermidis.14
Penelitian Abdollahzadeh menunjukkan bahwa, ekstrak kulit buah delima
memiliki efek antibakteri yang signifikan terhadap Staphylococcus aureus, Staphylococcus epidermidis, Lactobacillus acidophilus, Streptococcus mutans dan
Streptococcus salivarius.15 Menurut Vasconcelous, gel yang mengandung ekstrak buah delima memiliki efisiensi yang lebih besar dalam menghambat perlekatan
mikroba Streptococcus mitis, Streptococcus mutans dan Candida albicans
dibandingkan dengan antibiotik miconazole gel.16 Bhadbhade menyatakan bahwa
ekstrak buah delima efektif dalam menghambat pertumbuhan bakteri periodontitis,
yaitu menghambat P. intermedia pada konsentrasi 16,125 mg/ml, menghambat P. gingivalis pada konsentrasi 31,25 mg/ml, dan menghambat A. acetemcomytans pada konsentrasi 62,5 mg/ml.9
Berdasarkan latar belakang yang telah diuraikan tersebut, peneliti tertarik
untuk meneliti lebih lanjut mengenai efektivitas ekstrak kulit buah delima (Punica granatum) terhadap bakteri P. gingivalis secara in vitro.
1.2 Rumusan Masalah
1. Apakah ekstrak kulit buah delima memiliki efektivitas terhadap bakteri P. gingivalis secara in vitro?
2. Berapakah Konsentrasi Hambat Minimum (KHM) dan Konsentrasi Bunuh
Minimum (KBM) ekstrak kulit buah delima terhadap bakteri P. gingivalis?
1.3 Tujuan Penelitian
1. Untuk mengetahui efektivitas ekstrak kulit buah delima terhadap bakteri P. gingivalis secara in vitro
2. Untuk mengetahui Konsentrasi Hambat Minimum (KHM) dan Konsentrasi
1.4 Hipotesis Penelitian
Ekstrak kulit buah delima efektif dalam menghambat dan membunuh bakteri
P. gingivalissecara in vitro.
1.5 Manfaat Penelitian
1. Sebagai dasar penelitian lebih lanjut pengembangan ekstrak kulit buah
delima sebagai bahan antibakteri dalam perawatan penyakit periodontal
2. Sebagai informasi bagi dokter gigi tentang efek antibakteri dari ekstrak
kulit buah delima
3. Pengembangan material kedokteran gigi yang berasal dari alam dan bersifat
lebih biokompatibel dan harga terjangkau dalam rangka meningkatkan pelayanan
BAB 2
TINJAUAN PUSTAKA
2.1 Penyakit Periodontal
Penyakit periodontal merupakan istilah yang menjelaskan mengenai penyakit
inflamasi pada jaringan yang mengelilingi gigi, meliputi penyakit gingiva dan
penyakit jaringan pendukung gigi.3 Gingivitis dan periodontitis adalah dua bentuk
utama penyakit inflamasi pada periodontal.8 Gingivitis merupakan inflamasi pada
gingiva yang disebabkan oleh bakteri dengan tanda-tanda klinis perubahan warna
lebih merah dari normal, bengkak dan berdarah pada tekanan ringan, namun tidak ada
kehilangan perlekatan antara jaringan ikat dengan gigi.2 Sedangkan, periodontitis
merupakan inflamasi yang sudah sampai ke jaringan pendukung gigi yang meliputi
ligamen periodontal, sementum, dan tulang alveolar. Pada periodontitis, terjadi
kehilangan perlekatan antara jaringan ikat dengan sementum dan akar gigi.
Selanjutnya, periodontitis dapat menyebabkan kehilangan tulang, resesi, maupun
keduanya.3
Penyakit periodontal merupakan salah satu penyakit gigi utama pada populasi
manusia di dunia dengan tingkat prevalensi yang tinggi. WHO melaporkan bahwa
10-15% penduduk dunia menderita periodontitis yang parah.17 Menurut laporan Centers for Disease Control and Prevention of America, prevalensi penyakit periodontal di Amerika tahun 2009 dan 2010 diperkirakan 47,2% atau 64,7 juta orang dewasa
Amerika memiliki periodontitis ringan, sedang atau berat. Pada orang dewasa 65
tahun keatas, tingkat prevalensi meningkat menjadi 70,1%.1 Sedangkan, penelitian
oleh Situmorang, di kota Medan, prevalensi penyakit periodontal pada semua umur
mencapai 96%.18
2.2 Etiologi dan Patogenesis Penyakit Periodontal
Penyebab utama penyakit periodontal adalah iritasi plak bakteri.4 Plak atau
yang terdapat pada permukaan gigi yang dikelilingi oleh matriks ekstraselular yang
dikenal dengan glikokaliks.20 Sejumlah kecil plak dapat terdapat pada gingiva dan
periodontal yang sehat.4 Pada keadaan jaringan periodontal yang sehat, plak terdapat
pada supragingiva dan didominasi oleh bakteri gram positif, diantaranya adalah
Streptococcus sp (Streptococcus sanguis, S. oralis dan S. mitis menjadi spesies perintis), Neiseria, Nocardia dan Actinomyces.20 Plak kemudian berkembang dan matang selama beberapa minggu dan mengalami perubahan dari predominan bakteri
positif Gramm menjadi negatif Gramm, dari spesies fakultatif anaerob menjadi
spesies anaerob dan dengan lebih banyak kehadiran bakteri motil.22 Awalnya,
peningkatan terjadi pada bakteri filamen seperti Actinomyces. Setelah itu, Veilonella
dan bakteri batang negatif Gramm anaerob, seperti Fusobacterium dan P. intermedia
meningkat, dan bakteri batang motil dan spirokaeta muncul. Inflamasi gingiva dapat
diawali oleh berbagai bakteri ini jika mereka hadir dalam jumlah yang banyak karena
rendahnya higiene oral.23
Perkembangan berkelanjutan dari bakteri plak patogenik menyebabkan proses
inflamasi meluas ke ligamen periodontal, sementum, dan tulang alveolar, dan memicu
hilangnya perlekatan gingiva ke gigi serta hilangnya tulang pendukung. Pada tahap
awal periodontitis, bakteri pada celah gingiva sama dengan gingivitis, namun ketika
penyakit berkembang, bakteri menjadi lebih kompleks. Bermacam-macam spesies
mikroba, dimana predominannya adalah spesies bakteri negatif Gramm terlibat
sebagai etiologi dari periodontitis. P.gingivalis tampaknya merupakan patogen periodontal paling penting berdasarkan jumlah kehadirannya dan faktor virulensi
dinding selnya.23 Periodontitis kronis ringan dikaitkan dengan bakteri P.gingivalis
2.3 Bakteri Porphyromonas gingivalis
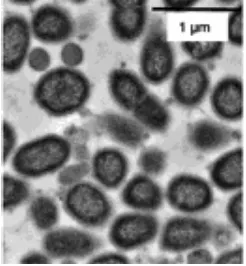
Bakteri Porphyromonas gingivalis (P.gingivalis) merupakan bakteri anaerob negatif Gramm, berpigmen hitam, non motil, assacharolytic dan terlihat berbentuk kokus sampai berbentuk batang pendek.24 Secara taksonomi, bakteri ini
diklasifikasikan sebagai berikut :26
Kingdom : Bacteria
Filum : Bacterioedetes
Kelas : Bacterioedes
Ordo : Bacteriodales
Famili : Porphyromonadaceae
Genus : Porphyromonas
Spesies : Porphyromonas gingivalis
Gambar 1. Porphyromonas gingivalis26
Habitat utama P. gingivalis adalah pada plak subgingiva di dalam sulkus gingiva atau poket periodontal. Namun, juga dapat ditemui pada lidah subjek dengan
periodontal sehat dan sakit. Kolonisasi P. gingivalis pada sulkus gingiva merupakan langkah pertama dalam perkembangan periodontitis kronis, meskipun P. gingivalis
juga dapat ditemui pada gingiva subjek yang sehat dalam jumlah yang lebih rendah.
melaporkan prevalensinya adalah sebesar 89,4%.7 Selain itu, dilaporkan bahwa P. gingivalis lebih banyak terdapat pada poket yang dalam dibanding poket yang dangkal,24 dan jumlahnya berkorelasi signifikan dengan jumlah gigi yang memiliki
kedalaman poket ≥ 4mm. Hal ini menegaskan bahwa, P. gingivalis terdapat pada sulkus gingiva dan lidah pada individu yang memiliki gigi. Sehingga, kehilangan gigi
atau dengan kata lain kehilangan sulkus gingiva dapat mempengaruhi populasi
mikroflora yang menghasilkan penurunan signifikan jumlah P. gingivalis pada rongga mulut.28
2.3.1 Faktor Virulensi Bakteri dan Metode Invasi Pada Jaringan
P.gingivalis memiliki faktor virulensi fimbria, lipopolisakarida (LPS), proteinase, kapsul, hemaglutinin, vesikel membran dan metabolit organik seperti
asam butirik serta berbagai enzim seperti arginin, lisin-gingipain, kolagenase,
gelatinase dan hialuronidase, yang dapat berkontribusi dalam menginduksi
periodontitis kronis dengan berbagai cara. P. gingivalis dapat membentuk koloni pada sulkus gingiva oleh karena peran fimbria.28 Fimbria atau pili merupakan protein,
filamen yang menonjol keluar dari permukaan sel bakteri dan memainkan peran
penting dalam virulensi dengan merangsang perlekatan bakteri dengan sel epitel atau
jaringan pejamu.24 Selain sel epitel, fimbria juga memiliki kemampuan yang kuat
dalam berinteraksi dengan proteinpejamu seperti protein saliva, protein ekstraselular
matriks dan fibroblas.28 Selanjutnya, faktor virulensi LPS berperan sebagai agen
sitotoksin dari bakteri yang dapat memicu respon inflamasi sel dan berbagai sinyal
kemokin dari pejamu.24 Rangsangan oleh LPS ini dapat mengakibatkan rentetan
peristiwa inflamasi dan pertahanan pejamu.27 LPS bersama fimbria, proteinase dan
hemaglutinin berperan bersama-sama sebagai agen adheren terhadap rongga mulut.24
Faktor virulensi proteinase dihasilkan oleh P. gingivalis untuk menghasilkan nutrisi untuk tumbuh. P. gingivalis membutuhkan asam amino, peptida dan hemin untuk tumbuh. Setidaknya, delapan proteinase yang disekresikan, kini telah
permukaan sel dan penyediaan substrat untuk adhesi sel bakteri. Proteinase terlibat
langsung dalam invasi dan pengrusakan jaringan oleh bakteri, dan modulasi respon
imun pejamu.24
Enzim proteolitik gingipain dan kolagenase yang dihasilkan P. gingivalis
dapat berperan secara langsung dan tidak langsung dalam merusak jaringan
periodontal. Disamping itu, metabolit organik seperti amonia, propionat dan butirat
juga menunjukkan kemampuan mengganggu sistem imun pejamu dan menunjukkan
toksisitas terhadap epitel gingiva.28
P. gingivalis telah mengembangkan strategi adaptif untuk menyerang sel-sel epitel gingiva dan mengatasi mekanisme pertahanan pelindung sel epitel. P. gingivalis melekat dan menyerang sel-sel epitel dengan menargetkan reseptor spesifik pejamu, memodulasi sinyal dan menderegulasi jaringan sitokin pejamu. Interaksi
antara P. gingivalis dan sel epitel menyebabkan aktivasi beberapa sinyal kaskade yang kompleks, yang akhirnya mengatur transkripsi gen target yang mengkode
efektor dan regulator dari respon kekebalan. Efektor dari sistem kekebalan bawaan,
sitokin proinflamasi, kemokin, MMPs (matriks metalloproteinases) dan peptida
antimikroba diregulasi dan mungkin memiliki dampak langsung pada perkembangan
penyakit dan proses peradangan, yang dapat berkontribusi terhadap kekebalan bakteri
dan perkembangan manifestasi penyakit periodontal kronis.24
2.4 Perawatan Penyakit Periodontal
Seperti yang telah dijelaskan, plak bakteri adalah etiologi utama penyakit
periodontal.4 Sehingga, tujuan kunci perawatan periodontal adalah menyingkirkan
bakteri patogenik plak, mengoreksi faktor resiko dan mencegah rekolonisasi bakteri.8
Terdapat berbagai cara yang digunakan untuk menyingkirkan plak bakteri,
diantaranya adalah dengan pembersihan mekanis dengan menggunakan sikat gigi,
2.4.1 Pembersihan Mekanis
Pembersihan plak menggunakan sikat gigi telah diterima secara luas sebagai
metode preventif penyakit periodontal. Inovasi bentuk sikat gigi semakin
berkembang, begitupun metode penggunaannya.29 Namun, penelitian menunjukkan
bahwa aktifitas menyikat gigi yang efektif hanya dapat membersihkan plak sekitar
65%, dan tidak dapat membersihkan plak interproksimal, sehingga diperlukan
pembersihan yang menggunakan sikat gigi interdental atau benang gigi (dental floss).21
Pembersihan mekanis sehari-hari menggunakan sikat gigi dan benang gigi
tidak cukup untuk mengatasi penyakit periodontal kronis. Skeling dan root planing
yang dikombinasikan dengan kontrol plak sehari-hari terbukti dapat menjadi pilihan
perawatan, tampak dalam pengurangan inflamasi, pergeseran komposisi mikroba
menjadi flora dengan patogenitas lebih rendah, penurunan kedalaman poket dan
penurunan perluasan penyakit. Namun, ada beberapa faktor yang dapat membatasi
keberhasilan dari perawatan menggunakan alat skeling dan root planing, faktor tersebut antara lain adalah bentuk anatomi dari akar gigi, furkasi dan kedalaman
poket periodontal.Oleh karena itu, dibutuhkan agen farmakologikal dalam perawatan
penyakit periodontal.8 Hal ini juga dibutuhkan karena beberapa keadaan seperti
dalam penyembuhan inflamasi akut, setelah bedah periodontal, dan pasien
kompromis medis.21
2.4.2 Terapi Farmakologikal
Agen farmakoterapeutik dikelompokkan berdasarkan rute pemberiannya,
yaitu secara lokal dan sistemik. Sejumlah penelitian telah dilakukan untuk menilai
kegunaan dari antibiotik sistemik untuk menghentikan atau memperlambat
perkembangan periodontitis atau untuk meningkatkan status periodontal. Penggunaan
antibiotik sistemik tambahan diindikasikan jika dijumpai kondisi pasien yang
penyakitnya tidak responsif terhadap debridemen secara mekanis, infeksi akut,
mengikuti prinsip yaitu, jika memungkinkan terlebih dahulu mengidentifikasi
organisme patogenik dan tes sensitifitas antibiotik.8
Penggunaan agen kemoterapeutik secara lokal dan langsung pada poket
periodontal dapat mengubah komposisi flora patogenik dan meningkatkan
penyembuhan kondisi klinis periodontitis. Obat yang diberikan secara langsung
memberikan beberapa keuntungan, yaitu, obat dengan konsentrasi bakterisidal dapat
dihantarkan langsung pada sisi yang memiliki aktifitas penyakit dan dapat digunakan
dalam waktu yang lama.8
Food and Drug Administration of United State (FDA) telah menyetujui penggunaan etilena vinil asetat yang mengandung serat tetrasiklin, chip gelatin yang
berisi klorheksidin dan formulasi minosiklin polimer sebagai tambahan untuk skeling
dan root planing. FDA juga telah menyetujui doksisiklin hyclat dalam gel polimer
bioabsorable sebagai terapi yang berdiri sendiri untuk pengurangan kedalaman probing, perdarahan saat probing, dan peningkatan level perlekatan. Sistem obat
secara lokal memiliki keterbatasan dan keunggulan. Keunggulannya antara lain,
kemudahan aplikasi, penggunaan langsung pada sisi berpenyakit yang tidak responsif
terhadap terapi konvensional, dan hasil pengobatan bisa ditingkatkan di sisi
berpenyakit tersebut. Modalitas pemberian secara lokal telah menunjukkan perbaikan
klinis menguntungkan berkaitan dengan pengurangan kedalaman probing dan
keuntungan dalam level perlekatan klinis.8 Penggunaan antimikroba sintetik dengan
cara pemberian secara lokal adalah kontraindikasi jika digunakan sebagai monoterapi,
masalah yang terkait dapat mencakup reaksi alergi, kemungkinan ketidakmampuan
untuk melepaskan ikatan biofilm, dan kegagalan untuk menghilangkan kalkulus.8
Penggunaan antimikroba sintetik juga tidak diperbolehkan selama kehamilan dan
menyusui.30
Penggunaan bahan herbal alami belakangan ini banyak menjadi perhatian
beberapa peneliti. Hal ini disebabkan karena efek samping penggunaan herbal
kebanyakan lebih sedikit dibanding bahan sintetik serta efek resistensi dari
2.5 Buah Delima
Punica granatum atau yang dikenal dengan nama delima berasal dari timur tengah. Delima tersebar di daerah subtropik sampai tropik, dari dataran rendah
sampai di bawah 1.000 m dpl. Tumbuhan delima ini menyukai tanah gembur yang
tidak terendam air, dengan air tanah yang tidak dalam. Di Indonesia, delima sering
ditanam di pekarangan rumah sebagai tanaman hias sekaligus untuk dimakan.12,31
Delima sering disebutkan di beberapa kitab suci sebagai buah yang memiliki
berbagai khasiat bagi manusia, diantaranya tertulis dalam Alquran, terdapat juga pada
bibel perjanjian lama, jewish torah, dan kitab babylonian talmud. Delima dipercaya
dalam mitologi Yunani, Mesir serta di China dianggap sebagai lambang kesuburan.32
Pohon delima berupa perdu dengan tinggi 2-5 m. Batang berkayu,
percabangan banyak, berduri pada ketiak daunnya, coklat ketika masih muda, dan
hijau kotor setelah tua. Daun tunggal, berbentuk lonjong dan pertulangan menyirip.
Bunga tunggal bertangkai pendek, biasanya terdapat satu sampai lima bunga
berwarna merah, putih atau ungu dan berbunga sepanjang tahun.31
Buah delima berbentuk bulat dengan diameter 5-12 cm. Bijinya banyak,
kecil-kecil, bentuknya bulat panjang yang bersegi-segi agak pipih, keras, tersusun tidak
beraturan, berwarna merah, merah jambu, atau putih. Dikenal tiga macam buah
delima, yaitu delima putih, delima merah, dan delima ungu.31
Di daerah Sumatera, delima biasanya dikenal dengan nama glima (aceh),
dalimo (batak), sedangkan di daerah Jawa dikenal dengan nama gangsalan dan
dhalima.13
Berdasarkan taksonominya, delima diklasifikasikan sebagai berikut :34
Kingdom : Plantae
Subkingdom : Tracheobionta
Superdivisi : Spermatophyta
Spesies : Punica granatum L
Pemanfaatan delima secara tradisional telah digunakan sebagai obat cacingan,
diare, prolaps rektum, perdarahan seperti muntah darah dan perdarahan rahim, radang
tenggorokan, radang telinga, keputihan, batuk, radang gusi, bronkhitis, sariawan,
rematik, perut kembung, keracunan, nyeri lambung dan hipertensi. Bagian tanaman
yang biasa digunakan sebagai obat adalah kulit kayu, kulit akar, kulit buah, daun, biji
dan bunganya.31
2.6 Nilai Farmakologis Buah Delima
Lebih dari satu dekade belakangan ini, terjadi peningkatan yang signifikan
dalam penelitian mekanisme farmakologi dari buah delima dan bahan didalamnya
yang berhubungan dengan hal tersebut. Beberapa penelitian melaporkan bahwa
batang, akar, daun dan buah dari delima memiliki nilai farmakologis yang penting
untuk kesehatan.32 Nilai farmakologis tersebut antara lain: aktifitas antimikroba
(bakterisidal), antioksidan, antikanker, antijamur, antiviral, laksatif, diuretik,
Penelitian beberapa tahun terakhir menunjukan ketertarikan yang tinggi
terhadap efek terapeutik ekstrak delima.42 Percobaan klinis juga telah banyak
dilakukan, sehingga diketahui bahwa delima memiliki efek terhadap kanker prostat,
prostat hiperplasia, diabetes millitus, limfoma, atherosklerosis, serta penyakit arteri
koroner.32
Efek terapeutik delima erat hubungannya dengan senyawa kimia yang
terkandung di dalamnya. Penelitian terkini mengungkapkan bahwa bahan yang paling
memiliki nilai terapeutik di dalam delima adalah senyawa polifenol atau phenolic13. Selain itu, senyawa kimia lain yang berperan yaitu asam ellagic, tannin ellagic atau
hydrolyzable (termasuk punicalagin), antosianidin, antosianin, asam punicic, flavonoid, dan estyrogenic flavonols dan flavon.30
Phenolic adalah senyawa yang paling penting dalam aktifitas terhadap bakteri, contohnya adalah asam gallic yang diidentifikasi sebagai senyawa yang paling aktif untuk uji penghambatan bakteri. Efek penghambatan senyawa phenolic dapat dijelaskan oleh adsorpsi ke membran sel, interaksi dengan enzim substrat dan
mengurangi komposisi ion logam bakteri.33
Flavonoid dilaporkan menunjukkan kemampuan aktifitas anti-inflamasi,
oestrogenic, enzim inhibition, antimikroba, antialergi, antioksidan, dan aktifitas sitotoksis antitumor. Ekstrak flavonoid dari tanaman ini telah banyak digunakan
dalam penelitian efek terhadap berbagai bakteri secara in vitro.35 Flovanoid memiliki mekanisme antibakteri dengan berbagai aktifitas, diantaranya dengan menghambat
sintesis dari asam nukleat bakteri, menghambat fungsi membran sitoplasmik bakteri,
dan menghambat metabolisme energi bakteri.35
Senyawa tanin seperti punicalagin merupakan agen antimikrobial. Aktifitas tanin dalam melawan bakteri dan jamur dapat dilihat dari hubungan struktur molekul
dan toksisitasnya serta aktifitas astringennya. Efek tanin sebagai antimikroba nampak
dari kemampuan melewati dinding sel bakteri yang terdiri dari polisakarida dan
protein dan berikatan dengan permukaanya.13
antikarsinogenik dan antioksidan yang tinggi.32 Sedangkan, antosianin merupakan
salah satu antioksidan tumbuhan yang kuat yang mampu mencegah berbagai
kerusakan sel.13
2.7 Efek Ekstrak Kulit Buah Delima Terhadap Bakteri Periodontal
Kulit buah delima merupakan 50% dari berat keseluruhan buah dan sering
dijadikan sampah buangan. Padahal, kulit buah delima memiliki kadar polifenol
seperti ellagic tannins, flavonol, antosianin, asam ellagic, dan asam gallic yang lebih tinggi dibanding jus buahnya, sehingga memiliki aktifitas antimikroba dan
antioksidan yang kuat.14,35
Efek ekstrak buah delima terhadap penyakit periodontal telah banyak
dilaporkan. Ekstrak buah delima dapat menguatkan gingiva, menguatkan kembali
gigi yang goyang dan mengurangi tanda-tanda klinis periodontitis kronis.13 Penelitian
Sastravaha pada tahun 2003 menunjukkan dengan menyisipkan chip yang
mengandung ekstrak delima dan pegagan, dapat menyebabkan kedalaman probing
dan tanda klinis periodontitis menjadi berkurang.36
Ekstrak kulit buah delima memiliki kemampuan untuk menurunkan jumlah
bakteri oral. Kote melaporkan bahwa ekstrak delima telah menunjukkan aktifitas
melawan berbagai bakteri dirongga mulut terhadap berbagai spesies Streptococcus dan Lactobacillus.13 Abdollazadeh menambahkan bahwa ekstrak kulit buah delima konsentrasi 4-12 mg/ml efektif dalam melawan bakteri Staphylococcus aureus,
sedangkan terhadap Lactobacillus achidophilus, Streptococcus mutans dan Streptococcus salivarius efektif dengan konsentrasi 8 dan 12 mg/ml.15
Penelitian Bhadbhade pada tahun 2011 menunjukkan tidak ada berbedaan
signifikan antara berkumur dengan klorheksidin dengan berkumur menggunakan
konsentrasi 16,125 mg/ml, sedangkan terhadap Agregatibacter actinomycetecomitans
membutuhkan KHM sebesar 62,5 mg/ml.9
2.8 Keamanan ekstrak delima
Delima dan unsur yang terkandung di dalamnya telah aman dikonsumsi
selama berabad-abad tanpa efek samping.32 Penelitian mengenai efek kandungan
buah delima pada hewan dengan konsentrasi yang umumnya digunakan manusia dan
pada obat tradisional menunjukkan tidak adanya efek toksik.32,37 Toksisitas
antioksidan polifenol punicalagin, yang banyak terdapat pada jus delima telah dievaluasi pada tikus. Tidak ada efek toksik atau perbedaan signifikan yang diamati
dalam kelompok pengobatan dibandingkan dengan kontrol, yang dikonfirmasi
melalui analisis histopatologi organ tikus.32,38 Penelitian lain pada 10 pasien dengan
stenosis arteri karotis menunjukkan konsumsi jus delima (121 mg/L) selama tiga
tahun tidak memiliki efek toksik dalam analisis kimia darah, fungsi ginjal, hati, dan
2.10 Kerangka konsep
Variabel Bebas :
Ektrak kulit buah delima dengan
konsentrasi 25%, 12,5%, 6,25%,
3,125 %, 1,6125 %, dan 0,8%.
Variabel Tergantung :
Pertumbuhan bakteri
Porphyromonas gingivalis pada media Tryptic Soy Agar
Variabel Tak Terkendali :
− Lama penyimpanan buah delima
− Lama penyimpanan, pengiriman,
dan suhu saat pengiriman ektrak
kulit buah delima ke
laboratorium. Variabel Terkendali :
− Asal buah delima
− Konsentrasi etanol
− Suspensi bakteri P.gingivalis
− Media pertumbuhan bakteri
− Suhu inkubasi
BAB 3
METODOLOGI PENELITIAN
3.1 Rancangan Penelitian
Rancangan penelitian ini merupakan penelitian Post Test Only Control Group Design dengan jenis penelitian eksperimental laboratorium.
3.2 Tempat dan Waktu Penelitian
Penelitian dilakukan di Laboratorium Obat Tradisional Fakultas Farmasi
Universitas Sumatera Utara (USU) untuk pembuatan ekstrak kulit buah delima dan di
Laboratorium Rumah Sakit Penyakit Tropik Infeksi Universitas Airlangga (UNAIR)
untuk pengujian efektivitas antibakteri.
Waktu penelitian adalah pada bulan September 2013-Desember 2013
3.3 Sampel dan Besar Sampel
3.3.1 Sampel Penelitian
Sampel penelitian adalah koloni Porphyromonas gingivalis ATCC 33277 yang telah diisolasi dan dibiakkan dalam media Tryptic Soy Agar.
3.3.2 Besar Sampel Penelitian
Adapun penentuan besar sampel dilakukan berdasarkan standar Laboratorium
Pusat Penyakit Tropis Universitas Airlangga. Jumlah pengulangan yang dilakukan
pada penelitian ini menggunakan rumus Federer, yaitu:
(t-1) (r-1) ≥ 15
t : jumlah perlakuan dalam penelitian
Jumlah perlakuan ulang (r) yang digunakan dalam penelitian ini adalah 4 kali
pengulangan.
a. Penentuan nilai KHM
Bahan coba dibagi kedalam 6 kelompok dengan 2 kontrol, yaitu :
− Kelompok I : ekstrak dengan konsentrasi 25 % = 4 sampel
− Kelompok II : ekstrak dengan konsentrasi 12,5 % = 4 sampel
− Kelompok III : ekstrak dengan konsentrasi 6,25 % = 4 sampel
− Kelompok IV : ekstrak dengan konsentrasi 3,125 % = 4 sampel
− Kelompok V : ekstrak dengan konsentrasi 1,625 % = 4 sampel
− Kelompok VI : ekstrak dengan konsentrasi 0,8 % = 4 sampel
− Kelompok VII : kontrol Mc Farland = 1 sampel
− Kelompok VIII: kontrol negatif (ektrak kulit buah delima tanpa suspensi
P.gingivalis = 1 sampel Jumlah sampel = 26 sampel
Dari masing-masing konsentrasi dilakukan dilusi (pengenceran) untuk
mendapatkan konsentrasi minimal yang dapat menghambat pertumbuhan bakteri.
b. Penentuan nilai KBM
Dari hasil penentuan nilai KHM diperoleh beberapa kelompok yang
dilanjutkan dengan perhitungan jumlah koloni bakteri dengan metode Drop Plate Miles Mesra.
− Kelompok I : ekstrak dengan konsentrasi 25 % = 4 sampel
− Kelompok II : ekstrak dengan konsentrasi 12,5 % = 4 sampel
− Kelompok III : ekstrak dengan konsentrasi 6,25 % = 4 sampel
− Kelompok IV : ekstrak dengan konsentrasi 3,125 % = 4 sampel
− Kelompok V : ekstrak dengan konsentrasi 1,625 % = 4 sampel
− Kelompok VI : ekstrak dengan konsentrasi 0,8 % = 4 sampel
− Kelompok VIII: kontrol negatif (ektrak kulit buah delima tanpa suspensi
P.gingivalis = 1 sampel Jumlah sampel = 26 sampel
3.4 Variabel Penelitian
Variabel Bebas
− Ekstrak kulit buah delima dengan konsentrasi 25%, 12,5%, 6,25%, 3,125 %,
1,625 %, dan 0,8%.
Variabel Tergantung
− Pertumbuhan bakteri P.gingivalis pada media Tryptic Soy Agar dengan pengukuran nilai KHM dan KBM
Variabel Terkendali
− Asal buah delima (Kota Sawahlunto)
− Konsentrasi etanol yang dipakai (70%)
− Suspensi P. gingivalis ATCC 33277
− Jenis media pembiakan bakteri Tryptic Soy Agar
− Suhu inkubasi P. gingivalis (37o C)
− Waktu yang digunakan untuk mengamati pertumbuhan atau pembiakan P. gingivalis yaitu 24 jam
Variabel Tak Terkendali
− Lama penyimpanan buah delima
− Lama penyimpanan, pengiriman, dan suhu saat pengiriman bahan coba
(ektrak kulit buah delima) ke laboratorium.
3.5 Definisi Operasional
− Ekstrak kulit buah delima adalah ekstrak yang diperoleh dengan melakukan ekstraksi kulit buah delima yang telah diperkolasi dengan pelarut etanol 70%
− Koloni Porphyromonas gingivalis adalah bakteri yang berasal dari stem cell P. gingivalis ATCC 33277 dan kemudian dikultur pada media Tryptic Soy Agar
dalam suasana anaerob
− Konsentrasi Hambat Minimum (KHM) adalah konsentrasi minimal bahan
coba yang mampu menghambat pertumbuhan bakteri setelah diinkubasi
selama 24 jam dan tidak tumbuh koloni bakteri pada media perbenihan
dengan menggunakan metode dilusi.
− Konsentrasi Bunuh Minimum (KBM) adalah konsentrasi minimal bahan coba
yang dapat membunuh 99,9% atau 100% bakteri setelah dilakukan uji dilusi
selama 24 jam, dengan menghitung jumlah koloni bakteri pada media padat
menggunakan metode Drop Plate Miles Mesra.
3.6 Bahan dan Alat Penelitian
3.6.1 Bahan Penelitian
− Buah delima sebanyak 5000 gram
− Pelarut etanol 70% sebanyak 5 liter (Kimia Farma, Indonesia)
− Suspensi Porphyromonas gingivalis ATCC 33277
− Media Tryptic Soy Agar (Difco, USA)
− Tryptic Soy Broth
− NaCl 0,9% 1 liter (Kimia Farma, Indonesia)
− Aquadest 1 liter
3.6.2 Alat Penelitian
− Lemari pengering
− Kertas perkamen
− Vaccum Rotary Evaporator (Heidolph VV 2000, Germany)
− Perkolator
− Kapas (Bio Panca, Indonesia)
− Alumunium foil 1 gulungan
− Destilator
− Lemari penyimpan petri
− Piring petri (Pyrex, Japan)
− Blender (Panasonic, Japan)
− Kertas saring (Whatman no.42, England)
− Autoklaf (Tomy, Japan)
− Inkubator Co2 (Sanyo, Japan)
− Electronic Balance (Ohyo JP2 6000, Japan)
− Vortex/whirli mixer (Iwaki model TM 100, Japan)
− Pipet mikro dan tips (Gilson, France)
− Kaca pembesar (Ootsuka ENV-CL, Japan)
− Ose
− Spiritus
3.7 Prosedur Pengambilan dan Pengumpulan Data
3.7.1 Prosedur Pembuatan Ekstrak Kulit Buah Delima
Buah yang dipakai adalah buah yang segar, berwarna hijau kemerahan.
(gambar 3). Bahan baku berupa buah delima sebanyak 5000 gram dicuci bersih,
dibuang bijinya, dan diiris halus. (gambar 4) Kulit yang telah diiris ditimbang,
didapat beratnya adalah 2170 gram. Selanjutnya kulit buah delima dikeringkan di
lemari pengering selama 10 hari sampai dapat dipatahkan dengan rapuh ( gambar 5).
Sampel yang telah kering kemudian ditimbang kembali dan didapatkan berat
630 gram (gambar 6 dan 7), kemudian diblender sampai menjadi serbuk simplisia
(gambar 8). Diayak dan ditimbang kembali dan didapatkan berat 250 gram (gambar
9). Simplisia kemudian dimasukkan ke dalam wadah dan dimaserasi selama 3 jam
dengan pelarut etanol 70% dan diaduk sesekali (gambar 10). Setelah itu, dimasukkan
ke dalam perkolator yang ditutup alumunium foil dan dibiarkan selama 24 jam
dengan keadaan etanol cukup merendam sampel. Bagian ujung alat perkulator
perkulator yang juga disambungkan pada tabung untuk menampung cairan dapat
dibuka dengan kecepatan tetesan ±20 tetes/menit (gambar 11). Sampel pada tabung
perkulator tetap dijaga dalam kondisi terendam etanol selama dilakukan
penampungan perkolat. Prosedur penampungan perkolat dilakukan sampai perkolat
yang dihasilkan jernih. Semua perkolat digabung dan disaring, lalu diuapkan dengan
menggunakan Vaccum Rotary Evaporator pada tekanan < 1 ATM dengan temperatur ≤ 550
C. (gambar 12) Hasil akhir yang didapat adalah ekstrak kental kulit buah delima
sebanyak 135 gram.(gambar 13)
Gambar 3. Buah delima segar Gambar 4. Kulit buah delima diiris
Gambar 5. Kulit delima dikeringkan Gambar 6. Kulit delima yang telah kering
Gambar 8.Pemblenderan kulit delima
Gambar 10. Maserasi serbuk simplisia disertai pengadukan Gambar 9. Serbuk simplisia
ditimbang
Gambar 7. Penimbangan kulit
Gambar 13. Ekstrak kental kulit buah delima
3.7.2 Pengenceran Bahan Coba
Ekstrak kulit delima ditimbang menggunakan Electronic balance dan massanya disesuaikan dengan konsentrasi yang diinginkan dengan cara dilarutkan
dengan media Tryptic Soy Broth (TSB). Disediakan 6 buah tabung, pada tabung pertama diisi 1,25 gram ekstrak kulit buah delima dan dilarutkan dengan TSB hingga mencapai volume 5 ml. Kemudian dicampur dengan menggunakan vorteks sehingga Gambar 11. Serbuk kulit delima
yang direndam etanol di perkolator
Gambar 12. Proses penguapan etanol
diperoleh ekstrak kulit buah delima dengan konsentrasi 25%. Lima buah tabung yang
lainnya kemudian diisi masing-masing 2,5 ml TSB. Selanjutnya dilakukan pengenceran dengan cara mengambil setengah dari ekstrak kulit buah delima
konsentrasi 25% menggunakan mikropipet dan diletakkan pada tabung ke-2 untuk
mendapatkan ekstrak kulit buah delima 12,5% (pengenceran ganda). Demikian
seterusnya sampai didapatkan konsentrasi 6,25%, 3,125 %, 1,6125 %, dan 0,8%.
Tabung-tabung tersebut kemudian diberi label sesuai konsentrasinya.
3.7.3 Pembuatan Media Bakteri
Sebelum spesimen dibiakkan, dibuat media dengan melarutkan bubuk Tryptic Soy Agar sebanyak 20 gram ke dalam 500 ml aquadest untuk 40 petri (20 ml/petri). (gambar 14) Kemudian media disterilkan di dalam autoklaf selama 15-20 menit dengan tekanan udara 2 ATM, suhu 121o C. (gambar 15) Setelah disterilkan, media
disimpan di dalam lemari pendingin. (gambar 16)
Gambar 15. Media disterilkan menggunakan autoklaf
Gambar 16. Media Tryptic Soy Agar yang telah selesai dibuat
3.7.4 Pembuatan Suspensi Bakteri
Kegiatan pembuatan suspensi bakteri menggunakan P. gingivalis ATCC 33277 yang telah dibiakkan secara murni pada media Tryptic Soy Agar (TSA) dalam suasana anaerob (gambar 17). Sebanyak 1-2 ose dari biakan murni bakteri uji yang telah dikultur dan tumbuh dengan subur disuspensikan dengan menggunakan larutan
Gambar 17. P.gingivalis ATCC 33277 yang telah dibiakkan pada TSA
3.7.5 Pembuatan Kontrol Positif
Kontrol positif yang digunakan adalah suspensi bakteri yang telah disiapkan
pada prosedur sebelumnya. Suspensi bakteri tersebut diambil sebanyak 2 ml dengan
menggunakan mikropipet dan dimasukkan ke dalam microplate.
3.7.6 Pembuatan Kontrol Negatif
Kontrol negatif yang digunakan adalah ekstrak kulit buah delima tanpa
suspensi bakteri. Ekstrak ini diambil sebanyak 2 ml dengan menggunakan mikropipet
dan dimasukkan ke dalam microplate.
3.7.8 Penentuan KHM Bahan Coba
Bahan coba ekstrak kulit buah delima yang dipakai terdiri dari konsentrasi
25%, 12,5%, 6,25%, 3,125 %, 1,6125 %, dan 0,8%. Dari masing-masing konsentrasi
tersebut diambil sebanyak 1 ml lalu dimasukkan ke dalam microplate reaksi kemudian diberi label sesuai konsentrasinya. Selanjutnya ambil 1 ml suspensi bakteri
yang telah dipersiapkan sebelumnya dengan menggunakan mikropipet lalu
dimasukkan ke dalam masing-masing microplate bahan coba yang telah diberi label kemudian dihomogenkan. Lalu tabung-tabung tersebut diinkubasi pada suhu 37o C
selama 24 jam pada inkubator CO2 dan diamati kekeruhan yang terjadi dengan
KHM dari masing-masing bahan coba. Tabung dengan kekeruhan yang mulai tampak
jernih untuk setiap kelompok perlakuan merupakan KHM yaitu konsentrasi minimal
ekstrak atau bahan uji apapun yang mampu menghambat pertumbuhan P.gingivalis
dalam media perbenihan setelah diinkubasi 24 jam dan tidak tumbuh koloni kuman
dalam perbenihan tersebut.
3.7.9 Penentuan KBM Bahan Coba
Hasil prosedur penentuan nilai KHM, tidak terlihat larutan yang mulai tampak
jernih, sehingga semua kelompok larutan dilanjutkan dengan perhitungan jumlah
koloni bakteri, yaitu pada konsentrasi 25%, 12,5%, 6,25%, 3,125 %, 1,6125 %, dan
0,8% dengan metode Drop Plate Miles Mesra. Bahan coba dengan konsentrasi tersebut masing-masing dihomogenkan dan diambil 50 µl untuk tiap konsentrasi lalu
diteteskan ke dalam media padat Tryptic Soy Agar, dan direplikasi 4 petri, diamkan selama 15-20 menit sampai mengering dan diinkubasi dalam inkubator CO2 dengan
suhu 37o C selama 24 jam. Perhitungan jumlah koloni bakteri dilakukan
menggunakan kaca pembesar dengan prinsip satu sel bakteri hidup bila dibiakkan
pada media padat akan tumbuh menjadi 1 koloni bakteri. Perhitungannya adalah bila
bentuk koloni melebar dianggap berasal dari 1 koloni, bila bentuknya 2 koloni
bersinggungan dianggap sebagai 2 koloni. Satuan yang dipakai adalah CFU (Colony Forming Unit) / ml cairan (suspensi).
Setelah dihitung jumlah koloni pada masing-masing tetesan, kemudian dibuat
jumlah rata-ratanya dan dikalikan dengan faktor pengenceran dan faktor pengali.
Oleh karena konsentrasi yang dilakukan perhitungan jumlah koloni bakteri
merupakan konsentrasi awal (sebelum dilakukan dilusi) maka faktor pengenceran x 1,
selain itu karena pada penetesan suspensi bahan coba dan bakteri pada media padat
sebanyak 50 µl, maka hasil perhitungan harus dikali dengan faktor pengali 20 untuk
mendapatkan hasil sesuai satuan standar (CFU/ml).
Contoh cara perhitungan koloni pada metode Drop Plate Miles Mesra :
a) Pada media padat ditetesi sebanyak 50 µl suspensi bahan coba dengan
b) Kemudian dihitung jumlah koloni yang ada dengan menggunakan kaca
pembesar dan didapatlah 5 koloni
c) Jadi jumlah bakteri pada bahan coba tersebut adalah : 5 x 1 (faktor
pengenceran) x 20 (faktor pengali) = 100 CFU/ml
3.8 Alur Penelitian
3.8 Analisis Data
Data hasil penelitian diperoleh dari penghitungan jumlah bakteri yang telah
diberi perlakuan dengan ekstrak kulit buah delima dengan konsentrasi 25 %, 12,5%,
6,25%, 3,125%, 1,6125% dan 0,8% pada media Tryptic Soy Agar.
Pembuatan ekstrak kulit buah delima
Pengenceran bahan coba
Pembuatan media bakteri
Pembuatan suspensi bakteri
Pembuatan kontrol positif
Penentuan KBM bahan coba Pembuatan kontrol negatif
Penentuan KHM bahan coba
BAB 4
HASIL PENELITIAN
Setelah diperoleh ekstrak kental kulit buah delima, dilakukan uji aktivitas
antibakteri untuk menentukan nilai Konsentrasi Hambat Minimum (KHM) dan
Konsentrasi Bunuh Minimum (KBM). Pengujian aktivitas antibakteri ekstrak dengan
konsentrasi 25%, 12,5%, 6,25%, 3,125 %, 1,6125 % dan 0,8% ini dilakukan pada
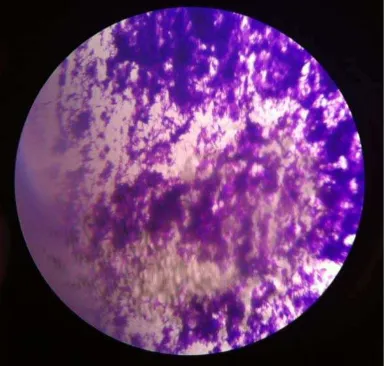
bakteri P.ginggivalis yang telah dikultur pada media Tryptic Soy Agar.(gambar 18 dan 19)
Gambar 18. Bakteri P.gingivalis yang telah dikultur pada media TSA
Pada penelitian ini, penentuan nilai KHM tidak dapat dilakukan karena
ekstrak kental kulit buah delima memiliki warna yang sangat coklat yang
mempengaruhi kekeruhan ketika dilakukannya metode dilusi. Sehingga pada tabung
percobaan, tidak satu tabung pun yang terlihat jernih walaupun ekstrak kulit delima
mungkin efektif menghambat bakteri P. gingivalis. (gambar 20)
Gambar 20. Kejernihan pada tabung percobaan tidak dapat diamati karena
warna ekstrak yang sangat coklat.
Oleh karena penentuan KHM tidak dapat dilakukan, maka uji aktivitas
antibakteri dilanjutkan dengan penentuan nilai KBM. Penentuan nilai KBM
dilakukan dengan penghitungan jumlah koloni bakteri dengan metode Drop Plate Miles Mesra pada media Tryptic Soy Agar, yang bertujuan untuk membuktikan adanya kemampuan untuk membunuh bakteri pada konsentrasi terkecil sebesar 99% -
Tabel 1. Daya Antibakteri Ekstrak Kulit Buah Delima Pada Penentuan KBM
Terhadap Pertumbuhan Porphyromonas gingivalis
Konsentrasi
Ekstrak
Pengulangan Kontrol Mc
Farland
Keterangan : 0 CFU/ml : Steril, tidak dijumpai pertumbuhan bakteri TBUD : Tidak bisa dihitung (> 300 koloni yang tumbuh) CFU/ml : Colony Forming Unit per ml
* : Sudah dikali dengan 20 (faktor pengali)
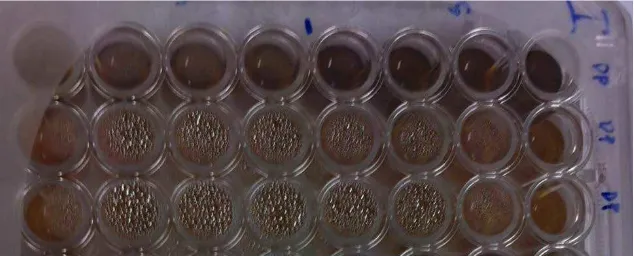
Pada konsentrasi 25%, 12,5%, 6,25%, 3,125 %, dan 1,6125 % dijumpai warna
bening pada medai TSA seperti warna tetesan bahan coba. Hal ini menunjukkan bahwa tidak ada terjadi pertumbuhan bakteri atau seluruh bakteri mati.(gambar 21
Gambar 21. Pengujian efek antibakteri pada konsentrasi 1,6125 %, 3,125% dan
6,25% menunjukkan tidak adanya pertumbuhan bakteri (steril)
Gambar 22. Pengujian efek antibakteri pada konsentrasi 12,5% dan 25%
menunjukkan tidak adanya pertumbuhan bakteri (steril)
Pada konsentrasi 0,8 % dijumpai adanya pertumbuhan bakteri dengan
Gambar 23. Pengujian efek antibakteri pada konsentrasi 0,8% menunjukkan
adanya pertumbuhan bakteri
Dari hasil tersebut dapat ditetapkan bahwa nilai KBM ekstrak kulit buah
BAB 5
PEMBAHASAN
Hasil penelitian eksperimental laboratorium secara in vitro ekstrak kulit buah delima terhadap bakteri Porphyromonas gingivalis menunjukkan bahwa ekstrak memiliki efektivitas dalam membunuh bakteri P.gingivalis. Penelitian ini mendapatkan nilai KBM dengan menghitung jumlah koloni bakteri pada media
Tryptic Soy Agar menggunakan teknik Drop Plate Miles Mesra.
Untuk mendapatkan efek maksimal dari zat aktif yang terdapat pada kulit
buah delima, dilakukan metode ekstraksi etanol. Metode ini berdasarkan pada
penelitian yang dilakukan oleh Voravuthikunchai pada tahun 2005, yang melakukan
penelitian efek antibakteri dengan beberapa metode ekstraksi kulit buah delima
terhadap Escherichia coli. Dari penelitiannya didapatkan hasil bahwa metode ekstraksi etanol kulit buah delima menunjukkan efek yang paling baik dalam
menghambat pertumbuhan Escherechia coli apabila dibandingkan dengan menggunakan metode ekstraksi dengan air mendidih maupun ekstraksi dengan
menggunakan kloroform.40
Konsentrasi ekstrak yang digunakan adalah 25%, 12,5%, 6,25%, 3,125 %,
1,6125 %, dan 0,8%. Konsentrasi ini digunakan merujuk kepada penelitian Badbhade
pada tahun 2011 yang menyatakan bahwa konsentrasi hambat minimum ektrak buah
delima terhadap P.gingivalis adalah 3,125%.10 Kemungkinan besar konsentrasi minimum ekstrak kulit buah delima untuk menghambat dan membunuh bakteri
P.gingivalis adalah konsentrasi dibawah atau diatasnya. Sehingga, pengujian dilakukan tidak dimulai dari konsentrasi 100% tapi cukup dimulai dari konsentrasi
25% sampai 0,8%.
Hasil penelitian menunjukkan bahwa nilai KHM tidak dapat ditentukan
karena warna ekstrak yang berwarna coklat gelap. Warna larutan yang gelap
mempersulit dalam mengamati kejernihan tabung-tabung yang merupakan campuran
ekstrak tersebut kemungkinan disebabkan karena banyaknyakandungan tanin pada
kulit buah delima, dimana Voravuthikunchai menyatakan bahwa kandungan tanin
pada kulit buah delima mencapai 25%.40 Hasil yang sama juga didapatkan pada
penelitian yang dilakukan oleh Seeram pada tahun 2004, untuk mendapatkan ekstrak
murni tanin dari kulit buah delima. Pada penelitiannya tersebut didapatkan hasil
ekstrak berupa serbuk tanin yang berwarna coklat gelap41. Sehingga untuk
mengetahui kadar hambat minimum dari ekstrak kulit buah Delima terhadap
P.gingivalis sebaiknya digunakan metode lain, seperti metode difusi cakram.42
Hasil penelitian menunjukkan ekstrak kulit buah delima memiliki efektivitas
terhadap bakteri P. gingivalis dengan nilai KBM 1,6125 %. Hasil penelitian ini sesuai dengan penelitian sebelumnya oleh Bhadbadhe yang menyatakan bahwa buah
delima (whole fruit) efektif terhadap berbagai bakteri rongga mulut seperti P. intermedia, A. actinomycetemcomytans dan P. gingivalis. Namun, pada penelitian ini ekstrak kulit buah delima berhasil membunuh bakteri P.ginggivalis pada konsentrasi 3,125% sedangkan Bhadbadhe menyatakan bahwa ekstrak buah delima (whole fruit)
dapat menghambat pertumbuhan bakteri P.gingivalis pada konsentrasi 3,125%.10 Hal ini dapat disebabkan karena dalam penelitian Badbhade menggunakan buah delima
secara keseluruhan termasuk biji buahnya, sehingga konsentrasi yang menghambat
pertumbuhan bakteri P.ginggivalis lebih tinggi. Selain itu, perbedaan juga dapat disebabkan karena bedanya asal tanaman yang digunakan.
Pengaruh ekstrak kulit buah delima terhadap kematian bakteri P.gingivalis
disebabkan oleh efek senyawa aktif antibakteri yang ditimbulkan kulit buah delima.
Penelitian menunjukkan bahwa kulit buah delima merupakan sumber buah yang kaya
akan senyawa aktif yang berkhasiat sebagai antibakteri seperti flavonoid, phenolic
dan tanin.13,30,33
Menurut penelitian Chusine pada tahun 2005, flovanoid memiliki mekanisme
antibakteri dengan berbagai aktifitas, diantaranya dengan menghambat sintesis dari
asam nukleat bakteri, menghambat fungsi membran sitoplasmik bakteri, dan
membran sel bakteri, berinteraksi dengan enzim substrat dan mengurangi komposisi
ion logam bakteri.33
Senyawa tanin seperti punicalagin merupakan agen antimikrobial yang memiliki kemampuan melewati dinding sel bakteri yang terdiri dari polisakarida dan
protein dan berikatan dengan permukaannya.14 Tanin mencegah pertumbuhan bakteri
dan aktivitas protease dengan merusak dinding sel dan sitoplasma sehingga
mengakibatkan kerusakan struktur bakteri yang cepat.13 Menurut penelitian yang
dilakukan oleh Sung pada tahun 2012 di Korea menunjukkan bahwa efek
antimikrobial tanin yaitu dengan menginaktivasi adhesin mikroba dan enzim
hidrolitik seperti protease dan karbohidrolase dan sel transpot protein bakteri.43
Penelitian yang dilakukan oleh Doss pada tahun 2009 juga menunjukkan bahwa tanin
melekat pada dinding sel bakteri dan menyebabkan desintegrasi koloni bakteri.44
Penelitian yang sama seperti sebelumnya dilakukan oleh Bele pada tahun
2010 di India mengenai efek antimikrobial tanin. Hasil penelitian tersebut
menunjukkan bahwa tanin memiliki kemampuan untuk berikatan dengan dinding sel
bakteri, polisakarida, karbohidrat dan enzim yang terdapat dalam rongga mulut.45
Penggunaan hanya kulit delima dapat memberikan hasil uji yang berbeda
dengan penggunaan buah delima secara keseluruhan. Hal ini sesuai dengan penelitian
Dahham pada tahun 2010, yang membandingkan efek antibakterial dan antifungal
antara kulit, biji, jus dan keseluruhan dari buah delima. Penelitian tersebut
menunjukkan bahwa ekstrak kulit buah delima adalah bagian yang paling tinggi
aktifitas antimikrobanya dibandingkan dengan ekstrak bagian yang lain.46 Sedangkan
berdasarkan senyawa aktifnya, Yunfeng li pada tahun 2006 menunjukkan bahwa
kandungan polifenol pada kulit buah delima lebih besar daripada biji dan pulpnya.47 Penelitian yang sama juga dilakukan oleh Gozlecki, pada tahun 2011 yang
menunjukkan bahwa total senyawa phenolic pada buah delima terdapat tertinggi pada kulit buahnya dibanding dengan jus dan biji delima.48
Asal buah delima yang berbeda kemungkinan akan memberikan hasil uji yang
berbeda pula. Keadaan geografis dari masing-masing daerah yang berbeda-beda
tanaman tidak sama satu sama lainnya. Delima yang digunakan pada penelitian ini
bersal dari Kota Sawah Lunto, Indonesia, sedangkan pada penelitian Bhadbadhe
BAB 6
KESIMPULAN DAN SARAN
6.1 Kesimpulan
Dari penelitian eksperimental yang telah dilakukan maka dapat disimpulkan
bahwa ekstrak kulit buah delima memiliki efek antibakteri terhadap Porphyromonas gingivalis dengan nilai KBM sebesar 1,6125 %. Hasil dari penentuan nilai KHM dalam penelitian ini tidak representatif sehingga ttidak dapat diketahui nilainya.
6.2 Saran
Perlu dilakukan penelitian lebih lanjut untuk mengetahui :
1. Efektivitas bahan ini terhadap bakteri patogen periodontal yang lain.
2. Nilai KHM dari ekstrak kulit delima dengan menggunakan metode lain
yaitu metode difusi.
3. Zat aktif yang mana dari kulit delima yang memiliki efek antibakteri yang
paling besar
4. Toksisitas ekstrak kulit buah delima untuk mengetahui pengaruhnya
terhadap sel.
5. Keefektifan ekstrak kulit delima sebagai alternatif bahan medikamen
periodontal secara in vivo sebagai lanjutan penelitian ini sehingga bahan ini dapat digunakan secara klinis.