ABSTRACT
EFFECT OF ORAL HERBICIDE PARAQUAT DICHLORIDE TO HEPATOCYTE SWELLING AND SINUSOIDAL CONGESTION IN LIVER OF MALE RATS (Rattus norvegicus) Sprague dawley STRAIN
By
YOLANDA FRATIWI
The use of herbicide paraquat dichloride by farmers, is one of effort to increase the production in agricultural sector. Herbicide paraquat dichloride often used by farmers carelessly and there was caution ignorance. Herbicide cause much adverse effect to organs, especially in liver through oral. The purpose of this study is to determine the effect of oral herbicide paraquat dichloride to hepatocyte swelling and sinusoidal congestion in liver of male rats (Rattus novergicus) Sprague dawley strain.
In this experimental study, 25 male rats (Rattus novergicus) Sprague dawley strain are divided randomly into 5 group and treated for 2 days. K1 is group of controlled, K2, K3, K4, K5 are given herbicide paraquat dichloride 25 mg/kgBW, 50 mg/kgBW, 100 mg/kgBW, and 200 mg/kgBW.
The results showed that the average number of hepatocyte swelling and sinusoidal congestion in liver was increasing. In Kruskal Wallis test and Post Hoc Mann Whitney test found significant difference p=0.000 (p<0.005). There are significant effect of oral paraquat dichloride to hepatocyte swelling and sinusoidal congestion in liver of male rats (Rattus novergicus) Sprague dawley strain.
ABSTRAK
PENGARUH PEMBERIAN HERBISIDA PARAQUAT DIKLORIDA ORAL TERHADAP PEMBENGKAKAN HEPATOSIT DAN KONGESTI SINUSOID HATI PADA TIKUS PUTIH (Rattus norvegicus)
JANTAN GALUR Sprague dawley
Oleh
YOLANDA FRATIWI
Penggunaan herbisida paraquat diklorida oleh para petani sebagai salah satu upaya untuk meningkatkan hasil produksi pada sektor pertanian. Herbisida paraquat diklorida sering digunakan secara sembarangan dan tidak memperhatikan label peringatan. Herbisida yang masuk ke dalam tubuh melalui oral dapat menyebabkan kerusakan berbagai organ, salah satunya adalah hati. Penelitian ini bertujuan untuk mengetahui pengaruh pemberian herbisida paraquat diklorida per−oral terhadap pembengkakan hepatosit dan kongesti sinusoid hati.
Penelitian ini bersifat eksperimental dengan menggunakan 25 ekor tikus putih jantan galur Sprague dawley yang dibagi menjadi 5 kelompok. Masing-masing kelompok terdiri dari 5 ekor tikus yang diberi perlakuan selama 2 hari dengan dosis yang berbeda, yaitu K1 merupakan kelompok kontrol, K2, K3, K4, dan K5 diberi herbisida paraquat diklorida 25 mg/kgBB, 50 mg/kgBB, 100 mg/kgBB, dan 200 mg/kgBB.
Hasil penelitian menunjukkan rerata skor pembengkakan hepatosit dan kongesti sinusoid mengalami peningkatan. Hasil uji Kruskal Wallis yang dilanjutkan uji Post Hoc Mann Whitney menunjukkan perbedaan yang bermakna antar kelompok perlakuan p=0,000 (p<0,05). Pemberian herbisida paraquat diklorida per−oral dapat menyebabkan pembengkakan hepatosit dan kongesti sinusoid hati tikus.
RIWAYAT HIDUP
Penulis dilahirkan di Muara Enim, Sumatera Selatan pada tanggal 29 Juni 1993,
sebagai anak kedua dari tiga bersaudara, dari Bapak Fatahullah dan Ibu Holyati.
Pendidikan penulis dimulai dari pendidikan Taman Kanak-kanak (TK) Pembina
Muara Enim diselesaikan pada tahun 1999, Sekolah Dasar (SD) diselesaikan di
SDN 20 Muara Enim pada tahun 2005, Sekolah Menengah Pertama (SMP)
diselesaikan di SMP Negeri 1 Muara Enim pada tahun 2008, dan Sekolah
Menengah Atas (SMA) diselesaikan di SMA Negeri 1 Muara Enim pada tahun
2011.
Tahun 2011, penulis terdaftar sebagai mahasiswa Fakultas Kedokteran
Universitas Lampung melalui jalur Seleksi Nasional Masuk Perguruan Tinggi
Negeri (SNMPTN) Undangan. Selama menjadi mahasiswa, penulis pernah aktif
pada organisasi Forum Studi Islam (FSI) Ibnu Sina FK Unila sebagai Kardiak FSI
pada tahun 2011 dan anggota bidang Kaderisasi pada tahun 2012, Badan
Eksekutif Mahasiswa (BEM) FK Unila sebagai EA BEM pada tahun 2011 dan
Staff Ahli Dinas Pengembangan Sumber Daya Manusia dan Organisasi (PSDMO)
pada tahun 2012, serta Perhimpunan Mahasiswa Pecinta Alam dan Tanggap
pernah menjadi Asisten Dosen bidang Patologi Anatomi FK Unila periode 2013
“Dengan Nama ALLAH Yang Maha
Pengasih, Maha Penyayang”
(Q.S. Al-Fatihah: 1)
“Ingatlah, hanya dengan mengingat
ALLAH hati menjadi tentram” (Q.S.
Ar-
Ra’d: 28)
Persembahan sederhana teruntuk
Ibu, Bapak, Kakak, dan Adik
atas segala doa dan kasih sayang
yang terus menguatkan dalam LELAH
dan mengubahnya menjadi LILLAH,
Semoga Allah selalu melindungi dan
SANWACANA
Alhamdulillahirobbil’alamin, puji syukur penulis haturkan kehadirat ALLAH
SWT, karena atas rahmat dan hidayah-Nya skripsi ini dapat terselesaikan.
Shalawat serta salam senantiasa tercurahkan kepada Nabi Muhammad SAW.
Skripsi dengan judul “Pengaruh Pemberian Herbisida Paraquat Diklorida
Per−oral terhadap Pembengkakan Hepatosit dan Kongesti Sinusoid Hati pada Tikus Putih (Rattus norvegicus) Jantan Galur Sprague dawley” adalah salah satu syarat untuk memperoleh gelar Sarjana Kedokteran di Universitas Lampung.
Dalam kesempatan ini penulis mengucapkan terima kasih kepada:
1. Bapak Prof. Dr. Ir. Sugeng P. Harianto, M.S., selaku Rektor Universitas
Lampung;
2. Bapak Dr. Sutyarso, M.Biomed., selaku Dekan Fakultas Kedokteran
Universitas Lampung;
3. dr. Indri Windari, Sp.PA., selaku Pembimbing Utama yang telah
meluangkan waktu diantara kesibukannya untuk tetap membantu dan
membimbing, sabar dalam menghadapi pertanyaan-pertanyaan, bersedia
membagi ilmunya, memberikan kritik, saran, serta nasihat yang sangat
4. dr. Muhartono, M.Kes, Sp.PA., selaku Pembimbing Kedua atas
kesediaannya untuk meluangkan waktu diantara kesibukannya untuk tetap
sabar memberikan bimbingan, saran, kritik, nasihat, serta motivasi yang
sangat tinggi untuk menyelesaikan skripsi tepat waktu;
5. dr. Susianti, M.Sc., selaku Dosen Penguji Utama. Terima kasih atas
bimbingan, waktu, ilmu, kritikan, dan saran yang telah diberikan;
6. dr. Diana Mayasari, dr. Risal Wintoko, dan dr. Oktadoni Saputra, M Med
Ed selaku Pembimbing Akademik sejak semester awal hingga akhir yang
telah memberikan bimbingan selama menjalani pendidikan di Fakultas
Kedokteran Universitas Lampung;
7. dr. Tiwuk Susantiningsih, M.Biomed. dan dr. Maya Ganda Ratna yang
telah memberikan saran dan ilmu yang sangat membantu dalam proses
penyelesaian skripsi ini;
8. Ibunda tercinta Holyati, Am.Kep yang selalu mendoakan, membimbing,
menguatkan, dan memberikan kasih sayang yang tak terhingga serta tidak
pernah lupa mengingatkan untuk selalu mengingat Allah SWT. Semoga
Allah selalu melindungi dan menjadikan ladang pahala di akhirat kelak;
9. Bapak IPDA Fatahullah tercinta, yang selalu mendoakan, membimbing,
menguatkan, memberikan kasih sayang, dan menjadi motivator terbaik
yang telah mengajarkan untuk selalu bangkit setiap kali terjatuh. Semoga
Allah selalu melindungi dan menjadikan ladang pahala di akhirat kelak;
10.Kakak Juliandi Franata dan Adik tersayang Triyola Febriani, yang selalu
memberikan doa sepenuh hati, dukungan dan semangat untuk selalu
Selatan yang selalu memberikan doa dan dukungan;
11.Seluruh staf pengajar Program Studi Pendidikan Dokter Fakultas
Kedokteran Universitas Lampung atas ilmu yang telah diberikan kepada
penulis untuk menambah wawasan yang menjadi landasan untuk mencapai
cita-cita;
12.Seluruh Staf Tata Usaha, Akademik, pegawai, dan karyawan FK Unila
yang turut membantu dalam proses penelitian dan penyusunan skripsi ini.
Terima kasih yang sedalam-dalamnya kepada Mbak Luthfi dan Mbak Lisa
yang selalu membantu memudahkan jalan untuk bertemu dr. Muhartono,
M.Kes, Sp.PA. Terima kasih kepada Pak Makmun, Mbak Qori, Mbak Ida,
Mbak Yulis yang selalu memberi saran untuk segala proses pengurusan
kelengkapan surat, Mas Heri, Pak Iskandar, Pak Syahrudin, Mbak
Romiana, dan civitas akademik lainnya yang telah memberikan doa,
semangat, motivasi, dan nasihat selama pembelajaran di FK Unila;
13.Mas Bayu, yang sangat sabar mengajari, membantu, dan membimbing
mengenai prosedur selama proses penelitian dan penyusunan skripsi;
14.Teman-teman Tim Skripsi Paraquat, Diah Septia Liantari, I Gede Eka
Widayana, dan Wayan Ferly Aryana, terima kasih atas kerja sama, bantuan,
suka, duka, pengalaman merawat tikus-tikus penelitian, dan banyak hal
15.Terima kasih untuk drh. Aulia Andi M, M.Si, abang Alias Zulkipli, dan
Om Adi yang telah banyak membantu dalam proses transportasi
tikus-tikus penelitian;
16.Terima kasih yang tak terhingga kepada Diah Septia Liantari, Ferina Dwi
Marinda, Sakinah, dan Tiara Anggraini, untuk semua kebersamaan,
kerjasama, selalu mengingatkan dalam kebaikan, cerita, canda tawa, suka,
duka, diam, marah, dan semua hal lain yang tidak bisa digantikan;
17.Teman-teman CUPS, Bela Riski Dinanti, Desta Eko Indrawan, Diah Anis
Naomi, Diah Septia Liantari, Felicya Rosari, Ferina Dwi Marinda, I Gede
Eka Widayana, Pradila Desty Sari, Putu Filla, Rifka Humaida, Ririn
Rahayu, Rizky Bayu Ajie, Robby Pardiansyah, Rr Agatha Rhana, Sakinah,
dan Wayan Ferly Aryana, terima kasih untuk semua cerita, canda, tawa,
marah, diam, perhatian, melakukan perjalanan, bantuan, nasihat, semangat,
dan semua pelajaran berharga yang tidak akan terlupakan;
18.Teman-teman propti kelompok 2, Ferina Dwi Marinda, Sakinah, Nur Ayu
Virginia, Asih Sulistiyani, Dessy Eva, Putri Fitriana, Zuryati Toiyiba,
Magista Vivi Annisa, Mba Nurul, Robby Pardiansyah, Wayan Ferly
Aryana, Gilang Yoghi Pratama, dan I Gede Eka Widayana, terima kasih
untuk semua awal perjalanan dan perjuangan yang sangat berkesan;
19.Sahabat−sahabat Trinanos, Uni Syefni Jumnaria, Nindia Dinanti, Tria
Yolanda Ariska, Sartika Apriyani, Tia Ambaranti, Reza Dina Astuti, dan
Nadia Laora Ariska, terima kasih sudah menemani dari kecil hingga
20.Sahabat-sahabat Sawit Yowit, Bela Riski Dinanti, Emilia Dwi Sepdaleni,
Giani, Heny Puspita Sari, Mentari Indah Sari, Mutia Milidiah, Norinda
Kasuarina, Priske Pramadima Putri, Putri Mayang Sari, Susan Afrina, dan
Zara Alviometha Putri, terima kasih untuk semua canda, tawa, cerita, suka,
duka, kasih sayang, kebersamaan dan saling mendoakan disetiap keadaan;
21.Teman-teman KKN Tematik Unila 2014, Yuli Widayati, Yoan Martian
Sari, Yunita Dwi Setia Winarni, Yuniawati Eka Putri, Yuni Septi, Zuliani,
Priangga Tri Atmaja, dan Yudi Apriansyah, terima kasih untuk semua
cerita, kesederhanaan, kebersamaan, dan pengalaman luar biasa selama 40
hari bersama di Pesisir Barat serta untuk semua dukungan dan doa yang
telah diberikan;
22.Keluarga Patologi Anatomi FK Unila, dr. Muhartono, M.Kes, Sp.PA., dr.
Indri Windarti, Sp.PA., dr. Heru Sigit, Mas Bayu, dan teman-teman
Asisten Dosen PA, Diah Septia Liantari, Fadia Nadila, I Gede Eka
Widayana, Muflikha Sofiana, Rizky Bayu Ajie, Tiara Anggraini, dan
Yuda Ayu Kusuwa. Terima kasih atas kerja sama, keceriaan, motivasi, dan
ilmunya;
23.Teman sejawat Fakultas Kedokteran Universitas Lampung angkatan 2011,
Ara, Adit, Ane, Dila, Rozi, Aulia, Fatwa, Purin, Likha, Jeanna, Caca,
Ratih, Tanti, Nurul, Rama, Felis, Filla, Gede, Vandy, Sugma, Novita, Lian,
Stevan, Pau, Robby, Angga, Wayan, Lala, Tryvanie, Fadil, Olin, Belda,
Gita, Gita Dewita, Danar, Gulbud, Ferina, Giok, Belinda, Marizka, Hein,
Jaya, Anwar, Fitri, Asih, Azatu, Diah, Nor, Diano, Syafiq, Neola, Cici,
Andina, Ayu Aprilia, Ayu Lestari, Melly, Kartika, Mirdes, Ika, Dika, Imay,
Nayuv, Okta, Bian, Anya, Fabella, Erot, Karimah, Niluh, Ani, Tegar,
Bulan, Naomi, Lina, Dea, Ario, Resty, Berta, Pufit, Yuda, Agung, Fariz,
Fini, Lita, Gilang, Sakinah, Bono, Rifka, Tata, Aryati, Ririn, Ega, Zuy,
Restyana, Tiwi Aminah, Taufiq, Baji, Raissa, Tagor, Gista, Fira, Desta,
Mahe, Yusi, Vivi, Budiman, Satria, Yudo, Mirna, Rizqun, Dessy, Tiwi,
Nyimas, Jihan, dan Mardi. Terima kasih atas segala suka duka, motivasi,
keriuhan, dan kebersamaan yang terjalin selama 3,5 tahun ini;
24.Keluarga besar FSI IBNU SINA, BEM, dan PMPATD PAKIS RESCUE
TEAM FK UNILA periode 2011−2014, terima kasih untuk semua ilmu
dan pengalaman luar biasa dalam setiap kegiatannya;
25.Terima kasih kepada ibu, bapak, dan teman-teman Kost Arbenta yang
telah memberikan banyak bantuan selama merantau di Bandar Lampung;
26.Teman-teman alumni SMAN 1 Muara Enim, Wira, Agus, Hendy, Kris,
Elrizky, Mbak Lupi, Lis Anreni, Anita, Zahara, Haini, dan teman-teman
alumni tembesu lainnya yang telah memberikan doa dan dukungan;
27.Kakak-kakak dan adik-adik tingkat angkatan 2002−2014 (Kak Nora, Kak
Shinta, Mbak Nyimas, Mbak Nida, Mbak Meta, Desti, Zahra Zettira, Dani
Kartika, Devita, Dara, Natasyah, Wulan, Triola, dan adik-adik angkatan
2012−2014 lainnya) yang sudah memberikan semangat kebersamaan
Akan tetapi, sedikit harapan semoga skripsi yang sederhana ini dapat berguna dan
bermanfaat bagi kita semua. Amin.
Bandar Lampung, Desember 2014 Penulis
DAFTAR ISI
A.Herbisida Paraquat Diklorida... 1. Deskripsi Herbisida Paraquat Diklorida... 2. Kandungan Herbisida Paraquat Diklorida... 3. Mekanisme Toksisitas Herbisida Paraquat Diklorida………..
B.Hati…………...
1. Anatomi Hati ...
2. Histologi Hati ...
3. Fisiologi Hati ...
4. Histopatologi Hati ...
C.Radikal Bebas dan Stres Oksidatif...
1. Radikal Bebas…...
2. Stres Oksidatif...
D.Tikus Putih (Rattus norvegicus) Galur Sprague dawley... 1. Klasifikasi Tikus Putih...
2. Jenis Tikus Putih...
3. Biologi Tikus Putih ...
III. METODE PENELITIAN ...
A.Desain Penelitian ...
B.Tempat dan Waktu ...
C.Populasi dan Sampel ...
D.Bahan dan Alat Penelitian ...
E. Prosedur Penelitian ...
F. Identifikasi Variabel dan Definisi Operasional Variabel ...
V. KESIMPULAN DAN SARAN...
A.KESIMPULAN...
B.SARAN...
DAFTAR PUSTAKA
LAMPIRAN
73
73
DAFTAR TABEL
Tabel Halaman
1. Kelas Bahaya Herbisida Menurut WHO……….
2. Data biologi tikus putih (Rattus norvegicus) ... 3. Definisi operasional variabel ...
4. Skor pembengkakan hepatosit...
5. Skor kongesti sinusoid...
6. Analisis Shapiro-Wilk pembengkakan hepatosit... 7. Analisis Shapiro-Wilk kongesti sinusoid... 8. Analisis Uji Mann Whitney pembengkakan hepatosit ... 9. Analisis Uji Mann Whitney kongesti sinusoid...
14
33
50
60
62
64
64
65
DAFTAR GAMBAR
Gambar Halaman
1. Kerangka Teori………...
2. Kerangka Konsep ...
3. Paraquat Diklorida...
4. Gambaran makroskopik hati manusia dilihat dari anterior...
5. Gambaran makroskopik hati manusia dilihat dari posterior...
6. Histologi hati normal………...
7. Gambaran mikroskopis hati manusia...
8. Reduksi oksigen………...
9. Diagram alur penelitian ...
10.Histopatologi hati tikus kelompok 1...
11.Histopatologi hati tikus kelompok 2...
12.Histopatologi hati tikus kelompok 3...
13.Histopatologi hati tikus kelompok 4...
14.Histopatologi hati tikus kelompok 5...
15.Grafik perbandingan rerata skor pembengkakan hepatosit...
16.Grafik perbandingan rerata skoring kongesti sinusoid ...
DAFTAR LAMPIRAN
Lampiran 1
Lampiran 2
Lampiran 3 :
:
:
Uji Statistik
Dokumentasi Kegiatan
BAB I PENDAHULUAN
A. Latar Belakang
Petani merupakan kelompok kerja terbesar di berbagai negara di dunia
termasuk di Indonesia. Walaupun terdapat kecenderungan yang semakin
menurun, angkatan kerja yang bekerja pada sektor pertanian masih berjumlah
sekitar 40% dari seluruh angkatan kerja. Banyak wilayah kabupaten di
Indonesia yang mengandalkan pertanian, termasuk perkebunan sebagai
sumber penghasilan utama daerah. Untuk meningkatkan hasil pertanian yang
optimal, dalam paket intensifikasi pertanian diterapkan berbagai teknologi,
salah satunya adalah dengan penggunan agrokimia. Penggunaan agrokimia
diperkenalkan secara besar-besaran menggantikan teknologi lama baik dalam
hal pengendalian hama maupun pemupukan tanaman. Salah satu pola
penggunaan agrokimia yang digunakan adalah pestisida (Prijanto, 2009).
Pestisida merupakan bahan kimia yang telah secara luas digunakan untuk
tujuan memberantas hama dan penyakit tanaman dalam bidang pertanian dan
bidang kesehatan masyarakat. Di bidang pertanian, penggunaan pestisida
memungkinkan petani untuk meningkatkan produktivitas lahan pertaniannya
serta mampu melindungi petani dari kerugian pasca panen. Sedangkan di
bidang kesehatan masyarakat, penggunaan pestisida telah berhasil mengendalikan vektor−vektor penyakit menular tertentu, sehingga mampu
menurunkan prevalensi penyakit seperti malaria, schistosomiasis, filariasis, demam berdarah dengue, dan penyakit pes (Saftarina, 2011). Laporan
Organisasi Pangan Perserikatan Bangsa−Bangsa (PBB) menyatakan bahwa
lebih dari 70.000 pestisida beredar di seluruh dunia dan dipergunakan secara
aktif oleh para petani. Salah satu jenis pestisida yang mengalami peningkatan
dalam penggunaannya di dunia adalah herbisida yaitu dari 20% pada tahun
1960 menjadi 48% pada tahun 2005 (Zhang et al., 2011).
Herbisida merupakan suatu bahan atau senyawa kimia yang digunakan untuk
menghambat pertumbuhan atau mematikan tumbuhan. Herbisida ini dapat
mempengaruhi satu atau lebih proses-proses pertumbuhan seperti pada proses
pembelahan sel, perkembangan jaringan, pembentukan klorofil, fotosintesis,
respirasi, metabolisme nitrogen, dan aktivitas enzim yang sangat diperlukan
tumbuhan untuk mempertahankan kelangsungan hidupnya. Herbisida bersifat
racun terhadap gulma atau tumbuhan penganggu juga terhadap tanaman yang
dibudidayakan. Herbisida yang diaplikasikan dengan konsentrasi tinggi akan
mematikan seluruh bagian dan jenis tumbuhan. Pada dosis yang lebih rendah,
herbisida akan membunuh tumbuhan dan tidak merusak tumbuhan yang
Herbisida yang banyak digunakan pada bidang pertanian dan perkebunan
adalah jenis herbisida paraquat (1,1−dimethyl,4,4−bipyridylium) (Viaiudiana, 2013). Paraquat(1,1−dimethyl,4,4−bipyridylium) merupakan salah satu bahan aktif herbisida jenis gramoxone yang telah lama dan sampai saat ini paling banyak digunakan dalam budidaya tanaman di seluruh dunia, termasuk di
Indonesia. Dipicu oleh semakin langkanya tenaga kerja dan tersedianya
herbisida yang relatif mudah dan murah, peningkatan penggunaan pestisida di
Indonesia, khususnya herbisida, semakin terlihat nyata pada 20 tahun terakhir
(Sriyani & Salam, 2008). Tingginya intensitas aplikasi dan jumlah herbisida
yang diaplikasikan menimbulkan kekhawatiran yang cukup besar mengenai
bahaya pencemaran yang berasal dari residu herbisida yang tertinggal di
lingkungan, khususnya dalam tanah dan air. Residu herbisida dalam tanah dan
air dikhawatirkan akan menimbulkan gangguan kesehatan bagi manusia
(Sriyani & Salam, 2008).
Di negara berkembang, paraquat sering digunakan dengan sembarangan atau
tidak memperhatikan bahaya serta tidak memperhatikan label peringatan
sehingga dapat menyebabkan angka keterpaparan yang tinggi. Hanya dengan
sedikit sendok teh paraquat, maka dapat menyebabkan kematian. Kematian
dikarenakan kegagalan pernafasan, dan mungkin bisa dijumpai dalam
beberapa hari setelah keracunan bahkan sampai beberapa bulan kemudian.
Selain dapat menyebabkan kematian, paparan herbisida baik secara inhalasi
Data keracunan akibat herbisida di Amerika Serikat adalah 4,14% dari seluruh
kasus keracunan yang disebabkan oleh semua jenis pestisida. Sebanyak 0,78%
dari kasus keracunan herbisida tersebut berakibat fatal serta 27,7%
mengakibatkan korban menderita sakit. Keracunan herbisida tidak hanya
menjadi permasalahan di Amerika Serikat (Sembodo, 2010). Di negara
berkembang, keracunan herbisida merupakan permasalahan kesehatan
masyarakat dengan perkiraan sekitar 300.000 kematian di regio asia pasifik
sendiri. Sebagai contoh, di Sri Lanka ada sekitar 3−400 kasus keracunan
herbisida per 100.000 populasi setiap tahun. Paraquat merupakan agen
penyebab kematian utama di Sri Lanka dengan angka fatalitas yang tinggi
(>50%) (Ginting et al., 2012). Sedangkan data di Indonesia memperlihatkan sekitar 0,3% kasus keracunan disebabkan oleh paparan herbisida. Salah satu
jenis herbisida yang pernah dilaporkan menimbulkan keracunan pada manusia
adalah golongan paraquat (Sembodo, 2010).
Penggunaan paraquat dengan sembarangan dapat merusak berbagai macam organ diantaranya adalah jantung, ginjal, paru−paru, otot, limfa, kelenjar
suprarenal, susunan saraf pusat dan juga dapat merusak hati (Moon & Chun,
2011). Hati merupakan organ target primer dari toksisitas paraquat baik akut
maupun kronik khususnya yang masuk ke dalam tubuh secara ingesti. Hal ini
dikarenakan hati merupakan organ tubuh yang penting untuk mendetoksifikasi
zat kimia yang tidak berguna atau merugikan tubuh, termasuk herbisida
paraquat. Hati merupakan organ yang mempunyai kemampuan untuk
Proses terjadinya kerusakan pada organ hati sebagai organ yang
mendetoksifikasi zat kimia seperti herbisida paraquat, dapat terjadi akibat
toksisitas langsung atau melalui konversi zat kimia yang terkandung dalam
herbisida paraquatmenjadi toksin aktif oleh hati sehingga dapat menyebabkan
timbulnya beberapa kelainan pada hati seperti pembengkakan hepatosit,
kongesti sinusoid hati, fibrosis, sirosis, dan nekrosis (Malekinejad et al., 2013).
Dari uraian diatas, maka penulis tertarik untuk melakukan penelitian tentang pengaruh pemberian herbisida paraquat diklorida per−oral terhadap
pembengkakan hepatosit dan kongesti sinusoid hati pada tikus putih jantan
galur Sprague dawley.
B. Perumusan Masalah
Berdasarkan latar belakang yang telah dijelaskan, dapat dirumuskan masalah
penelitian, yaitu:
1. Apakah terdapat pengaruh pemberian herbisida paraquat diklorida per−oral terhadap pembengkakan hepatosit pada tikus putih jantan galur
Sprague dawley?
2. Apakah terdapat pengaruh pemberian herbisida paraquat diklorida per−oral terhadap kongesti sinusoid hati pada tikus putih jantan galur
C. Tujuan Penelitian
Adapun tujuan penelitian ini antara lain:
1. Untuk mengetahui pengaruh pemberian herbisida paraquat diklorida per−oral terhadap pembengkakan hepatosit pada tikus putih jantan galur
Sprague dawley.
2. Untuk mengetahui pengaruh pemberian herbisida paraquat diklorida per−oral terhadap kongesti sinusoid hati pada tikus putih jantan galur
Sprague dawley.
D. Manfaat Penelitian
Manfaat Teoritis:
Penelitian ini dapat digunakan untuk pengembangan Ilmu Patologi Anatomi
dan Agromedicine khususnya di bidang Toksikologi.
Manfaat Praktis:
1. Bagi penulis
Penelitian ini dapat mengembangkan ide dan menambah pengetahuan
mengenai pengaruh pemberian herbisida paraquat dikloridaper−oral.
2. Bagi penulis lain
Hasil penelitian ini dapat digunakan sebagai landasan untuk penelitian
yang lebih lanjut yang berhubungan dengan pengaruh pemberian herbisida
3. Bagi masyarakat
Penelitian ini diharapkan dapat memberikan pengetahuan mengenai
kandungan herbisida paraquat diklorida serta bahayanya bagi kesehatan
dan organ tubuh.
4. Bagi pemerintah
Hasil penelitian ini diharapkan dapat memberikan pengetahuan mengenai
pengaruh pemberian herbisida paraquat dikloridaper−oral, sehingga dapat
menjadi perhatian terutama dalam pengendalian masyarakat khususnya
para petani terhadap penggunaan herbisida paraquat diklorida.
E. Kerangka Teori
Paraquat merupakan herbisida yang paling umum digunakan dari golongan
bipyridylium. Golongan ini memiliki komposisi kimia C12H14N2. Menurut WHO'sClassification of Pesticides by Hazard, bahan aktif paraquat termasuk golongan II (moderately hazardous) dimana absorbsi paraquat mempunyai efek serius dalam jangka panjang, dengan dosis rendah paraquat relatif
berbahaya dan fatal jika termakan.Paraquat (1,1−dimethyl,4,4'−bipyridylium), sangat cepat diabsorbsi melalui usus setelah tertelan. Absorpsi setelah intake oral sekitar 10% (Ginting et al., 2012).
Paraquat dapat menyebabkan induksi toksisitas dalam tubuh dikarenakan
kemampuannya untuk mempengaruhi siklus redoks dan membentuk ROS. Di
NADPH−Cytochrome p450 reductase, Xantin oksidase, NADH, ubiquinone oxidoreductase, dan nitric oxide synthase. Metabolisme paraquat melalui sistem enzim ini menyebabkan terbentuknya PQ+ di dalam sel. Kemudian PQ+
secara cepat di reoksidasi menjadi PQ2+ dan proses ini mencetuskan
terbentuknya O2-. Atom O2 bertindak sebagai reseptor elektron dan NADP
bertindak sebagai donor elektron pada reaksi ini. Reaksi ini lebih jauh
membentuk HO. Kombinasi antara NO dengan O2 membentuk ONOO- yang
merupakan oksidan yang sangat kuat. Nitrite Oxide secara enzimatis diproduksi dari L−arginine oleh NO synthase, dan paraquat juga secara langsung atau tidak langsung menginduksi NO synthase yang memediasi produksi nitrite oxide. Oksigen reaktif dan nitrit yang terbentuk akan menyebabkan toksisitas pada kebanyakan organ. Paraquat merupakan bahan
reduksi alternatif dan reoksidasi berulang akan menyebabkan terbentuknya
oksigen free radicals, seperti superoxide, hidrogen peroksida, dan hidroksil radikal, yang menyebabkan kerusakan oksidatif pada lemak, protein, dan
DNA (Indika & Buckley, 2011).
Paraquat juga meningkatkan permeabilitas membran mitokondria bagian
dalam dikarenakan lipid peroksida, sehingga menyebabkan depolarisasi
membran, dan pembengkakan matriks mitokondria, khusunya pada hati yang
memiliki peran sebagai detoksifikasi paraquat yang masuk ke dalam tubuh
(Indika & Buckley, 2011). Selain pada hati, pemberian herbisida paraquat diklorida per−oral juga berpengaruh ke organ-organ lain seperti esofagus,
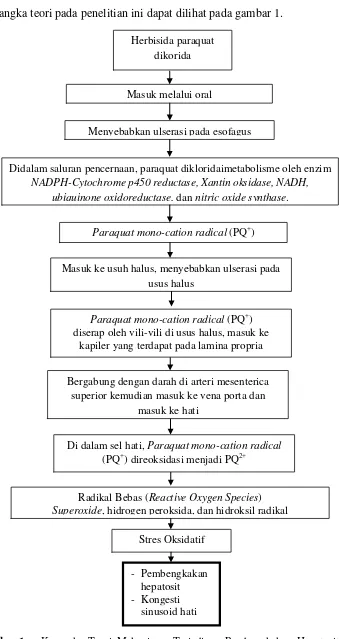
Kerangka teori pada penelitian ini dapat dilihat pada gambar 1.
Gambar 1. Kerangka Teori Mekanisme Terjadinya Pembengkakan Hepatosit dan Kongesti Sinusoid Hati yang disebabkan oleh Pemberian Herbisida Paraquat Diklorida Per−oral.
Herbisida paraquat dikorida
Paraquat mono-cation radical (PQ+)
Didalam saluran pencernaan, paraquat dikloridaimetabolisme oleh enzim
NADPH-Cytochrome p450 reductase, Xantin oksidase, NADH, ubiquinone oxidoreductase, dan nitric oxide synthase.
Masuk melalui oral
Radikal Bebas (Reactive Oxygen Species)
Superoxide, hidrogen peroksida, dan hidroksil radikal Stres Oksidatif
Bergabung dengan darah di arteri mesenterica superior kemudian masuk ke vena porta dan
masuk ke hati
Di dalam sel hati, Paraquat mono-cation radical
(PQ+) direoksidasi menjadi PQ2+
Masuk ke usuh halus, menyebabkan ulserasi pada usus halus
Paraquat mono-cation radical (PQ+) diserap oleh vili-vili di usus halus, masuk ke
F. Kerangka Konsep
Adapun kerangka konsep pada penelitian ini dapat dilihat pada gambar 2.
Gambar 2. Kerangka Konsep Pengaruh Pemberian Herbisida Paraquat Diklorida Per−oral terhadap Pembengkakan Hepatosit dan Konesti Sinusoid Hati Tikus Putih Jantan Galur Sprague dawley.
G. Hipotesis
1. Terdapat pengaruh pemberian herbisida paraquat diklorida per−oral
terhadap pembengkakan hepatosit pada tikus putih jantan galur Sprague dawley.
2. Terdapat pengaruh pemberian herbisida paraquat diklorida per−oral
BAB II
TINJAUAN PUSTAKA
A. Herbisida Paraquat Diklorida
1. Deskripsi Herbisida Paraquat Diklorida
Paraquat (1,1−dimethyl,4,4−bipyridylium) merupakan suatu herbisida golongan bipyridylium. Herbisida yang termasuk dalam golongan ini umumnya merupakan herbisida pasca tumbuh, tidak aktif apabila
diaplikasikan lewat tanah dan bersifat tidak selektif. Herbisida paraquat
diklorida memiliki efek toksisitas terhadap organisme eukariotik (Suntres,
2002).
Karakteristik dari paraquat adalah tidak dapat diserap oleh bagian
tanaman yang tidak hijau seperti batang dan akar serta tidak aktif di
tanah. Ketidakaktifan tersebut disebabkan adanya reaksi antara dua
muatan ion positif pada paraquat dan ion negatif mineral tanah sehingga
molekul positif paraquat terabsorbsi kuat dengan lapisan tanah dan tidak
aktif lagi. Penetrasi paraquat terjadi melalui daun. Aplikasi paraquat
akan menghasilkan hidrogen peroksida yang merusak membran sel.
Cara kerja paraquat yaitu menghambat proses dalam fotosistem I, yaitu
mengikat elektron bebas hasil fotosistem dan mengubahnya menjadi
elektron radikal bebas. Radikal bebas yang terbentuk akan diikat oleh
oksigen membentuk superoksida yang bersifat sangat aktif. Superoksida
tersebut mudah bereaksi dengan komponen asam lemak tak jenuh dari
membran sel, sehingga akan menyebabkan rusaknya membran sel dan
jaringan tanaman (Pusat Informasi Paraquat, 2006).
2. Kandungan Herbisida Paraquat Diklorida
Paraquat merupakan herbisida yang paling umum digunakan dari
golongan bipyridylium. Komposisi kimia dari paraquat adalah C12H14N2. Angka kematian akibat toksisitas dari paraquat sangat tinggi dikarenakan
toksisitasnya secara langsung dan belum adanya pengobatan yang efektif
(Indika & Buckley, 2011). Struktur kimia paraquat dikloridatersaji pada
gambar 3.
Daya toksisitas dari kandungan herbisida biasanya ditunjukkan oleh
angka toksisitas akut hasil uji laboratorium dengan hewan percobaan
(umumnya menggunakan tikus). Studi toksisitas akut pada hewan
menghasiklan LD50. Berdasarkan nilai LD50 WHO menyusun kelas
bahaya suatu herbisida seperti tercantum pada tabel 1.
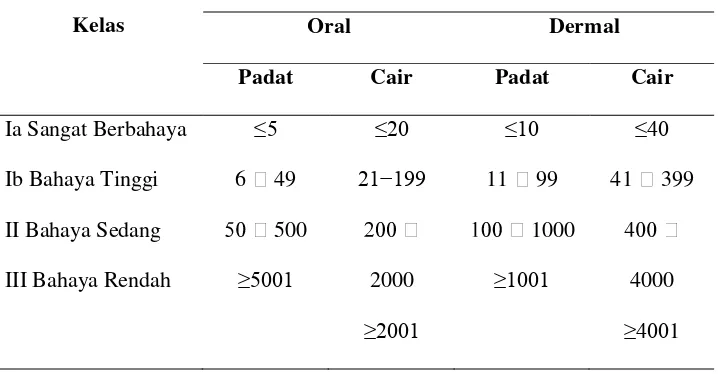
Tabel 1. Kelas Bahaya Herbisida Menurut WHO
Kelas
LD50 akut (tikus) formulasi (mg/kg)
Oral Dermal
Menurut WHO's Classification of Pesticides by Hazard, bahan aktif paraquat termasuk golongan II (moderately hazardous) dimana absorbsi paraquat mempunyai efek serius dalam jangka panjang, dengan dosis
rendah paraquat relatif berbahaya dan fatal jika termakan atau mengenai
kulit secara langsung. Selain itu herbisida paraquat dapat mempengaruhi
kesehatan manusia lewat tanah dan air yang tercemar sehingga produk
makanan manusia maupun hewan ikut tercemar herbisida paraquat
3. Mekanisme Toksisitas Herbisida Paraquat Diklorida
Paraquat (1,1−dimethyl,4,4−bipyridylium), sangat cepat diabsorbsi dengan inhalasi dan melalui usus setelah tertelan. Absorbsi setelah intake oral sekitar 10%. Tempat absorbsi utama dari paraquat adalah di usus
halus, sedangkan penyerapan melalui lambung sangatlah sedikit.
Walaupun absorpsi hanya 10%, sifat korosif dari paraquat akan
menyebabkan erosi dari mukosa saluran cerna, sehingga paraquat akan
semakin banyak diabsorbsi hingga 90%. Hanya sekitar 10−30% paraquat
yang tidak diabsorbsi. Sistem absorpsinya menggunakan carrier-mediated transport system pada brush border membrane (Ginting et al., 2012).
Paraquat dapat menyebabkan induksi toksisitas dalam tubuh dikarenakan
kemampuannya untuk mempengaruhi siklus redoks dan membentuk
Reactive Oxygen species (ROS). Di dalam tubuh, paraquat dimetabolisme oleh beberapa sistem enzim seperti Nikotinamide adenine dinukleotide phosphate oxidase (NADPH)−Cytochrome p450 reductase, Xantin oksidase, Nikotinamide adenosin dinukleotide hidrogen (NADH), ubiquinone oxidoreductase, dan nitrite oxide synthase. Metabolisme paraquat melalui system enzim ini menyebabkan terbentuknya paraquat
sebagai donor elektron pada reaksi ini. Reaksi ini lebih jauh membentuk
Hydroxyl free radical (HO). Nitrite Oxide (NO) kombinasi dengan O2 membentuk peroxinitrite (ONOO-) yang merupakan oksidan yang sangat kuat. Nitrite Oxide secara enzimatis diproduksi dari L−arginine oleh NO synthase, dan paraquat juga secara langsung atau tidak langsung menginduksi NO synthase yang memediasi produksi nitrite oxide. Oksigen reaktif dan nitrit yang terbentuk akan menyebabkan toksisitas
pada organ tubuh. Paraquat merupakan bahan reduksi alternatif dan
reoksidasi berulang akan menyebabkan terbentuknya oksigen free radicals, seperti superoxide, hidrogen peroksida, dan hidroksil radikal, yang menyebabkan kerusakan oksidatif pada lemak, protein, dan DNA
(Indika & Buckley, 2011).
Paraquat terbukti dapat menginduksi lipid peroksidase. Lipid peroksidase
menyebabkan gangguan fungsi sel membran dan dapat mencetuskan
apoptoptosis. Lipid peroksidase juga dianggap sebagai salah satu kunci
utama proses patofisiologi pertama kali pada intoksikasi paraquat.
Perubahan struktur dan fungsi sel lipid dan protein menyebabkan
hilangnya regulasi intra seluler oleh kalsium adenosin trifosfatase (Ca2+
ATPase). Hilangnya regulasi ini dapat menyebabkan kematian sel, sehingga menyebabkan kerusakan lokal dan disfungsi organ. Salah satu
organ primer yang dapat mengalami kerusakan dan kematian sel akibat
karena hati memegang peranan penting dalam proses metabolisme lemak
dan detoksifikasi paparan paraquat (Indika & Buckley, 2011).
Selain dapat menyebabkan kerusakan lokal dan disfungsi organ akibat
hilangnya regulasi intra seluler Ca2+, hasil metabolisme dari paraquat oleh
oleh berbagai enzim seperti NADPH akan menyebabkan terjadinya
toksisitas mitokondria. Toksisitas mitokondria disebabkan karena
berkurangnya kompleks NADH−ubiquinone oxidoreductase di mitokondria sehingga mencetuskan terbentuknya superoxide. Paraquat juga meningkatkan permeabilitas membran mitokondria bagian dalam
dikarenakan lipid peroksida sehingga menyebabkan depolarisasi
membran, dan pembengkakan matriks mitokondria, khususnya pada hati
yang memiliki peran sebagai detoksifikasi paraquat (Indika & Buckley,
2011).
Selain dapat menyebabkan kerusakan pada hati, resiko kontak langsung
dapat mengakibatkan keracunan akut yang ditandai dengan timbulnya
gejala seperti sakit kepala, mual, muntah, iritasi kulit, dan kebutaan, serta
dapat menimbulkan keracunan kronis. Pada keracunan kronis gejala dan
tanda yang timbul tidak selalu mudah dideteksi karena efeknya tidak
segera dirasakan dalam waktu yang relatif singkat, walaupun akhirnya
dapat menimbulkan gangguan kesehatan (Saftarina, 2011). Pemberian
lain seperti esofagus, lambung, usus halus, jantung, ginjal, otot, dan otak
(Dinis Oliveira, 2008).
B. Hati
1. Anatomi Hati
Hati adalah kelenjar paling besar dalam tubuh, dan setelah kulit,
merupakan satu-satunya organ yang paling besar. Berat organ hati adalah
sekitar 1500 gram dan mencakup 2,5% berat tubuh orang dewasa. Hati
terletak dalam kuadran kanan atas abdomen yang tersembunyi dan
terlindungi oleh tulang rangka toraks dan diafragma. Hati normal terletak
di sebelah d XI pada sisi kanan dan menyilang
garis tengah ke arah puting kiri. Hati mengisi hampir semua
hypochondrium kanan dan epigastrium. Hati memanjang ke dalam hypochondrium kiri, disebelah inferior diafragma, yang memisahkannya dari pleura, paru, pericardium, dan jantung (Moore et al., 2013).
Berdasarkan refleksi peritoneum dari permukaannya, fissura yang
terbentuk sehubungan dengan refleksinya, dan pembuluh yang melayani
hati dan vesica biliaris, hati dibagi menjadi dua lobus anatomis dan dua
lobus tambahan. Lobus anatomis terdiri dari lobus dekstra dan lobus
sinistra. Sedangkan lobus tambahan terdiri dari lobus quadrates dianterior
dan inferior serta lobus kaudatus di posterior dan superior, kedua lobus
Hati menerima darah dari dua sumber yaitu arteri hepatika propria (30%)
dan vena portae hepatis (70%). Arteri hepatika propria membawa darah
yang kaya akan oksigen dari aorta, dan vena portae hepatis mengantarkan
darah yang miskin oksigen dari saluran cerna. Darah yang berasal dari
arteri dan vena tersebut berjalan di antara sel-sel hati melalui sinusoid dan
dialirkan ke vena centralis. Vena centralis pada masing-masing lobulus
bermuara ke vena hepatika. Dalam ruangan antar lobulus-lobulus terdapat
kanalis hepatis yang berisi cabang-cabang arteria hepatika, vena portae
hepatis, dan sebuah cabang ductus choledochus (Sloane, 2004).
Persarafan pada hati berasal dari plexus hepaticus, yang merupakan
derivat terbesar pada plexus coeliacus. Plexus hepaticus menyertai
cabang-cabang arteria hepatica dan vena porta ke hati. Plexus terdiri dari
serat simpatis dari plexus coeliacus dan serat parasimpastis dari truncus
Gambar 4. Makroskopis hati manusia dilihat dari anterior (Sumber: Putz & Pabst, 2007).
Gambar 5. Makroskopis hati manusia dilihat dari posterior (Sumber: Putz & Pabst, 2007).
2. Histologi Hati
Hati terdiri atas unit-unit heksagonal yaitu lobulus hepaticus. Di bagian
tengah setiap lobulus terdapat sebuah vena sentralis, yang dikelilingi
secara radial oleh lempeng sel hati (lamina hepatocytica), yaitu hepatosit,
dan sinusoid ke arah perifer. Pada manusia, dapat ditemukan tiga sampai
enam daerah porta setiap lobulus. Darah arteri dan darah vena dari daerah
porta perifer mula-mula bercampur di sinusoid hati saat mengalir ke arah
vena sentralis. Dari sini, darah masuk ke sirkulasi umum melalui vena
hepatika yang keluar dari hati dan masuk ke vena kava inferior
(Eroschenko, 2010).
Hepatosit pada lobus hati tersusun radier. Lempeng sel ini tersusun dari
struktur yang menyerupai labirin dan busa, celah diantara lempeng ini
mengandung kapiler, yaitu sinusoid hati. Kapiler sinusoid adalah
pembuluh lebar yang tak teratur, dan hanya terdiri atas lapisan tak utuh
dari sel endotel berfenestra (Junqueira et al., 2007). Sel-sel endotel pada hati dipisahkan dari hepatosit oleh suatu celah subendotel yang dikenal
sebagai celah disse yang mengandung mikrovili hepatosit, sel penyimpan
lemak (sel Ito) dan serat retikulin yang halus (Gartner & Hiatt, 2012).
Selain sel-sel endotel, sinusoid juga mengandung makrofag yang dikenal
sebagai sel Kupffer. Sel-sel ini ditemukan pada permukaan luminal
sel-sel endotel. Fungsi utamanya adalah memetabolisme eritrosit tua,
mencerna hemoglobin, mensekresi protein yang berhubungan dengan
proses imunologis dan menghancurkan bakteri yang berhasil masuk ke
darah portal melalui usus besar. Kebanyakan sel tersebut berada di daerah
periportal di lobulus hati, tempat berlangsungnya fagositosis yang sangat
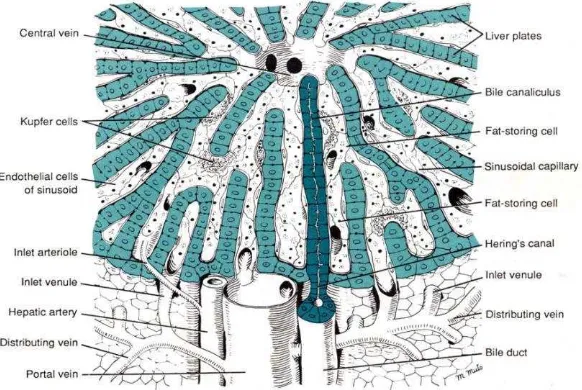
Gambar 6. Histologi hati normal (Sumber: Junqueira et al., 2007). Hepatosit berbentuk polihedral, dengan enam atau lebih permukaan, dan
berdiameter 20−30 µm. Permukaan masing-masing hepatosit berkontak
dengan dinding sinusoid, melalui celah Disse, dan dengan permukaan
hepatosit lain. Di tempat dua hepatosit berkontak, terbentuk suatu celah
tubular di antara kedua sel yang disebut kanalikulus biliaris (Junqueira et al., 2007).
Hepatosit memiliki satu atau dua inti bulat dengan satu atau dua anak inti.
Sebagian intinya poliploid, yaitu mengandung perkalian genap dari
jumlah kromosom haploid. Hepatosit memiliki banyak retikulum
endoplasma, baik halus maupun kasar. Pada hepatosit retikulum
endoplasma kasar membentuk agregat yang tersebar dalam sitoplasma,
agregat ini sering kali disebut badan basofilik. Beberapa protein misalnya,
albumin darah, fibrinogen disintesis pada poliribosom di struktur ini.
Beberapa proses penting berlangsung di dalam retikulum endoplasma
halus, yang tersebar secara difus di dalam sitoplasma. Organel ini
bertanggung jawab atas proses oksidasi, metilasi, dan konjugasi yang
diperlukan untuk menonaktifkan atau mendetoksifikasi berbagai zat
sebelum diekskresi dari tubuh. Retikulum endoplasma halus merupakan
sistem labil yang segera bereaksi terhadap molekul yang diterima
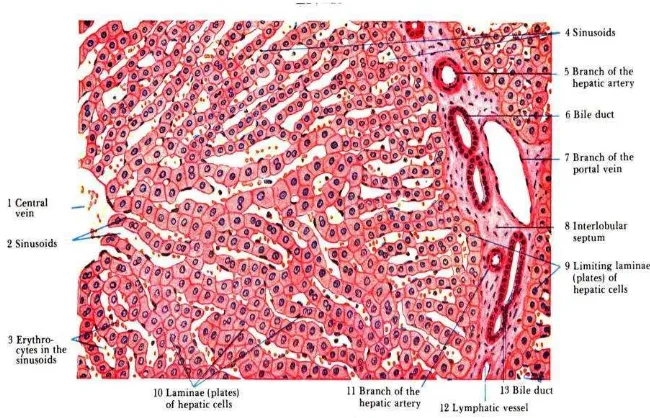
Gambar 7. Gambaran mikroskopis hati normal. Perbesaran 30 kali (Sumber: Eroschenko, 2010).
3. Fisiologi Hati
Menurut Guyton dan Hall (2008), hati mempunyai beberapa fungsi yang
berkaitan dengan pencernaan, antara lain:
a. Metabolisme karbohidrat
Fungsi hati dalam metabolisme karbohidrat adalah menyimpan
glikogen dalam jumlah besar, mengkonversi galaktosa dan fruktosa
menjadi glukosa, glukoneogenesis, dan membentuk banyak senyawa
kimia yang penting dari hasil perantara metabolisme karbohidrat.
b. Metabolisme lemak
Fungsi hati yang berkaitan dengan metabolisme lemak, antara lain
untuk mengoksidasi asam lemak untuk menyuplai energi bagi fungsi
tubuh yang lain, membentuk sebagian besar kolesterol, fosfolipid dan
c. Metabolisme protein
Fungsi hati dalam metabolisme protein adalah deaminasi asam amino,
pembentukan ureum untuk mengeluarkan amonia dari cairan tubuh,
pembentukan protein plasma, dan interkonversi beragam asam amino
dan membentuk senyawa lain dari asam amino.
Hati juga melakukan beberapa fungsi yang tidak berkaitan dengan
pencernaan, antara lain:
a. Mendetoksifikasi atau menguraikan zat sisa tubuh dan hormon serta
obat dan senyawa asing lain.
b. Membentuk protein plasma, termasuk protein yang dibutuhkan untuk
pembekuan darah dan yang untuk mengangkut hormon steroid dan
tiroid serta kolesterol dalam darah.
c. Menyimpan glikogen, lemak, besi, tembaga, dan banyak vitamin.
d. Mengaktifkan vitamin D, yang dilakukan bersama dengan ginjal.
e. Mengeluarkan bakteri dan sel darah merah tua, berkat adanya
makrofag residennya.
f. Mengekskresikan kolesterol dan bilirubin, bilirubin adalah produk
penguraian yang berasal dari destruksi sel darah merah tua
(Sherwood, 2011).
4. Histopatologi Hati
Dari sudut pandang patologi, hati adalah organ yang secara inheren
Respon awal terjadinya cedera yang disebabkan oleh gangguan aliran
darah pada organ hati ditandai dengan adanya kongesti. Kongesti
merupakan terbendungnya pembuluh darah, sehingga terjadi akumulasi
darah dalam organ yang diakibatkan oleh adanya gangguan sirkulasi
pada pembuluh darah. Pada kondisi vena yang terbendung, terjadi
peningkatan tekanan hidrostatik intravaskular yang merupakan tekanan
yang mendorong darah mengalir di dalam vaskular oleh kerja pompa
jantung. Peningkatan tekanan hidrostatik tersebut dapat menimbulkan
perembesan cairan plasma ke dalam ruang interstitium. Cairan plasma ini
akan mengisi pada sela−sela jaringan ikat longgar dan rongga badan
sehingga dapat menyebabkan timbulnya pembengkakan dan penumpukan
sel−sel radang (Wulandari, 2006).
Kongesti yang terjadi pada hati dibedakan menjadi kongesti hepatik akut
dan kronis. Pada kongesti hepatik akut, vena sentralis dan sinusoid akan
menggelembung oleh darah bahkan dapat terjadi degenerasi hepatosit
sentral. Sedangkan pada kongesti hepatik pasif kronis, secara
mikroskopis dapat terlihat nekrosis sentrilobular disertai dengan
hilangnya hepatosit dan terjadi perdarahan (Kumar et al., 2007).
Berdasarkan sifatnya, respon umum hati terhadap cidera dapat
a. Jejas reversibel
1) Peradangan
Cedera hepatosit yang menyebabkan influks sel radang akut
atau kronis ke hati disebut hepatitis. Serangan terhadap hepatosit
hidup yang mengekspresikan antigen oleh sel T yang telah
tersensitisasi merupakan penyebab umum kerusakan hati.
Peradangan mungkin terbatas di saluran porta atau mungkin
meluas ke parenkim (Kumar et al., 2007).
2) Pembengkakan sel
Pembengkakan sel merupakan manifestasi klinis yang muncul
sebagai akibat ketidakmampuan sel dalam mepertahankan
homeostasis ionik dan cairan. Secara mikroskopiks,
pembengkakan sel ditandai dengan vakuola kecil, jernih di
dalam sitoplasma. Vakuola tersebut menggambarkan segmen
retikulum endoplasma yang berdistensi dan menekuk (Kumar et al., 2007).
3) Perlemakan
Terjadi pada jejas hipoksik dan berbagai bentuk jejas toksik atau
metabolik. Secara mikroskopis ditandai dengan adanya vakuola
lipid dalam sitoplasma. Dapat disebut dengan degenerasi lemak
b. Jejas Ireversibel
1) Nekrosis
Nekrosis merupakan kematian sel yang terjadi di lingkungan
cedera eksogen ireversibel. Nekrosis sel dapat terjadi langsung
atau dapat mengikuti degenerasi sel. Gambaran mikroskopis dari
nekrosis dapat berupa gambaran piknosis, karioreksis, dan
kariolisis (Chandrasoma & Taylor, 2005).
2) Fibrosis
Fibrosis merupakan akumulasi matriks ekstraseluler yang
merupakan respon dari cedera akut atau kronik pada hati. Pada
tahap awal, fibrosis terbentuk di dalam atau di sekitar saluran
porta atau vena sentralis atau mungkin mengendap langsung di
dalam sinusoid. Hal ini merupakan reaksi penyembuhan terhadap
cedera. Cedera pada hepatosit akan mengakibatkan pelepasan
sitokin dan faktor solubel lainnya oleh sel kupffer serta sel tipe lainnya yang akan mengaktivasi sel stelat yang akan mensintesis
sejumlah besar komponen matriks ekstraseluler (Kumar et al., 2007).
3) Sirosis
Berlanjutnya fibrosis dan cedera parenkim menyebabkan hati
terbagi–bagi menjadi nodus hepatosit yang mengalami regenerasi
C. Radikal Bebas dan Stres Oksidatif
1. Radikal Bebas
a. Definisi Radikal Bebas
Radikal bebas adalah suatu atom atau molekul yang tidak stabil dan
sangat reaktif karena memiliki satu atau lebih elektron yang tidak
berpasangan pada orbit terluarnya. Untuk mencapai kestabilan atom
atau molekul, radikal bebas akan bereaksi dengan molekul di
sekitarnya untuk memperoleh pasangan elektron. Reaksi ini akan
berlangsung terus menerus di dalam tubuh dan apabila tidak dihentikan
akan menimbulkan berbagai penyakit (Waji & Sugrani, 2009).
Radikal bebas yang diproduksi di dalam tubuh normal akan dinetralisir
oleh antioksidan yang ada di dalam tubuh. Bila kadar radikal bebas
terlalu tinggi maka kemampuan dari antioksidan endogen tidak
memadai untuk menetralisir radikal bebas sehingga terjadi keadaan
yang tidak seimbang antara radikal bebas dengan antioksidan
(Harjanto, 2004).
b. Definisi Reactive Oxygen Species (ROS)
Salah satu elemen kimia yang sering terlibat dalam pembentukan
radikal bebas adalah oksigen. Oksigen (O2) sangat penting bagi
kehidupan manusia namun juga dapat bersifat toksik. Atom O2 adalah
orbital yang berbeda. Kedua elektron ini tidak dapat melintasi orbital
yang sama karena memiliki putaran paralel, yakni berputar dengan
arah yang sama (Wu & Cederbaum, 2004).
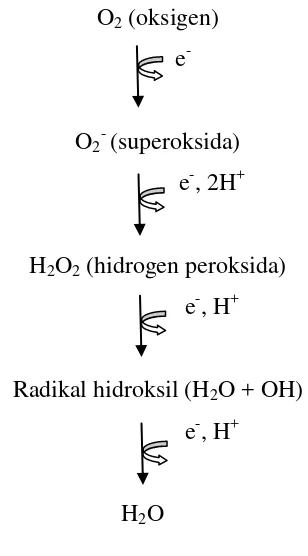
Atom O2 mampu menerima 4 elektron, yang akan direduksi menjadi 2
molekul air. Ketika O2 menerima 1 elektron, superoksida terbentuk.
Superoksida masih menjadi radikal karena masih mempunyai 1
elektron yang tidak berpasangan. Ketika superoksida menerima 1
elektron, superoksida tereduksi menjadi hidrogen peroksida. Hidrogen
peroksida (H2O2) kemudian tereduksi menjadi radikal hidroksil.
Produk akhir dari proses ini adalah H2O. Berikut ini adalah gambar
proses terbentuknya H2O dari O2 (Smith et al., 2005).
O2 (oksigen) e
-O2- (superoksida) e-, 2H+
H2O2 (hidrogen peroksida) e-, H+
Radikal hidroksil (H2O + OH) e-, H+
H2O
Superoksida, peroksida, dan radikal hidroksil dikategorikan sebagai
Reactive Oxygen Species (ROS). Reactive Oxygen Species adalah senyawa yang mengandung O2, termasuk ke dalam radikal bebas yang
sangat reaktif, atau senyawa yang siap dikonversi menjadi radikal
bebas O2 dalam sel (Wu & Cederbaum, 2003). Reactive Oxygen Species dibutuhkan untuk menjalankan fungsi fisiologis tubuh, tetapi apabila berlebihan akan menimbulkan stres oksidatif yang dapat
menimbulkan respons inflamasi yang berbeda manifestasinya pada
setiap individu (Fandika, 2013).
c. Pengaruh ROS terhadap Sel
Tiga reaksi yang berkaitan dengan jejas sel diperantarai ROS adalah
(Kumar et al., 2007):
1) Peroksidasi membran lipid
Ikatan ganda pada lemak tak jenuh membran mudah terkena
serangan ROS. Interaksi ROS lemak menghasilkan peroksida
yang tidak stabil dan reaktif serta terjadi reaksi rantai autokatalitik.
2) Fragmentasi Deoxyribo Nuecleic Acid (DNA)
Reaksi ROS dengan timin pada DNA mitokondria dan nuklear
menimbulkan kerusakan untai tunggal. Kerusakan DNA tersebut
menyebabkan kematian sel dan perubahan sel menjadi ganas.
3) Ikatan silang protein
degradasi atau hilangnya aktivitas enzimatik. Reaksi ROS juga
dapat secara langsung menyebabkan fragmentasi polipeptida.
2. Stres Oksidatif
Stres oksidatif adalah keadaan yang tidak seimbang antara antioksidan
yang ada dalam tubuh dengan produksi ROS. Stres oksidatif dapat
menyebabkan terjadinya reaksi peroksidasi lipid, protein termasuk enzim
dan DNA, yang dapat menyebabkan terjadinya kerusakan oksidatif,
apabila hal tersebut berlanjut dapat menyebabkan terjadinya kerusakan
dan kematian sel (Mahdi et al., 2007). Mekanisme protektif untuk mencegah pembentukan ROS atau untuk mendetoksifikasi ROS di dalam
tubuh melibatkan molekul yang disebut antioksidan. Keadaan terjadinya
gangguan keseimbangan antara produksi ROS dan pembuangan ROS
disebut stres oksidatif. Gangguan keseimbangan ini dapat terjadi dari
kurangnya kapasitas antioksidan karena gangguan dalam produksi dan
distribusinya, atau dari jumlah ROS yang berlebihan (Wu & Cederbaum,
2004).
D. Tikus Putih (Rattus norvegicus) Galur Sprague dawley
1. Klasifikasi Tikus Putih Klasifikasi tikus putih adalah:
Kelas : Mamalia Ordo : Rodentai Subordo : Odontoceti Familia : Muridae Genus : Rattus
Spesies : Rattus norvegicus (Narendra, 2007).
2. Jenis Tikus Putih
Tikus putih atau tikus albino galur outbred lebih sering digunakan untuk penelitian di laboratorium dibandingkan galur inbred. Beberapa contoh jenis tikus putih galur outbred adalah Wistar, Sprague dawley, dan Long Evans. Sprague dawley merupakan galur yang lebih cepat tumbuh dibandingkan tikus Wistar. Sedangkan Long Evans merupakan galur yang lebih kecil dibandingkan tikus Wistar atau Sprague dawley. Galur Fisher 344 dan Lewis adalah tikus putih galur inbred yang paling banyak digunakan dalam penelitian (Animal Care Program, 2011).
3. Biologi Tikus Putih
Tikus putih merupakan hewan yang lebih cepat menjadi dewasa dan lebih
mudah berkembang biak dibandingkan dengan tikus liar. Berat badan tikus
putih lebih ringan dibandingkan berat badan tikus liar. Berat tikus putih
pada umur 4 minggu mencapai 35−40 gram dan berat dewasa rata-rata
Tabel 2. Data Biologi Tikus Putih (Rattus norvegicus)
Kematangan seksual 65−110 hari Siklus estrus 4−5 hari Gestasi 20−22 hari Penyapihan 21 hari
Fisiologi
Suhu tubuh 35,90−37,50 C Denyut jantung 250−600 kali/menit Laju nafas 66−144 kali/menit Tekanan darah diastole 60−90 mmHg Tekanan darah sistol 75−120 mmHg
Feses Padat, berwarna coklat tua, bentuk memanjang dengan ujung membulat Urin Jernih dan berwarna kuning
Konsumsi makan dan air
Konsumsi makan 15–30 gr/hari atau 5–6 gr/100 grBB Konsumsi air 24–60 ml/hari atau 10−12 ml/100 grBB
(Sumber: Isroi, 2010)
Tikus putih (Rattus norvegicus) sering digunakan sebagai hewan percobaan karena tikus merupakan hewan yang mewakili kelas mamalia
sehingga kelengkapan organ, kebutuhan nutrisi, metabolisme biokimia,
sistem reproduksi, pernafasan, peredaran darah, serta ekskresinya
menyerupai manusia. Tikus juga dapat secara alami menderita suatu
penyakit, seperti hipertensi dan diabetes, dan juga sering dipakai dalam
studi nutrisi, tingkah laku, kerja obat, dan toksikologi (Animal Care Program, 2011).
dipelihara dalam jumlah banyak, lebih tenang, dan ukurannya lebih besar
daripada mencit. Tikus putih galur Sprague dawley juga memiliki ciri-ciri albino, kepala kecil, ekor yang lebih panjang dibandingkan badannya,
pertumbuhannya cepat, temperamennya baik, kemampuan laktasi tinggi,
BAB III
METODE PENELITIAN
A. Desain Penelitian
Penelitian ini merupakan penelitian eksperimental laboratorik yang
menggunakan metode rancangan acak terkontrol dengan pola post test only control group design. Sebanyak 25 ekor tikus putih (Rattus norvegicus) jantan galur Sprague dawley berumur 10 minggu yang dipilih secara acak, dan dibagi menjadi 5 kelompok digunakan sebagai subjek penelitian.
B. Tempat dan Waktu
Pemeliharaan dan pemberian perlakuan terhadap tikus putih (Rattus norvegicus) jantan galur Sprague dawley pada penelitian ini dilakukan di animal house Fakultas Kedokteran Universitas Lampung. Pembedahan tikus dilaksanakan di Balai Penyidikan dan Pengujian Veteriner Bandar Lampung.
Pembuatan preparat dan pengamatannya dilakukan di Laboratorium Patologi
Anatomi Fakultas Kedokteran Universitas Lampung. Penelitian ini
C. Populasi dan Sampel
Populasi penelitian ini adalah tikus putih (Rattus norvegicus) jantan galur Sprague dawley berumur 8−10 minggu yang diperoleh dari Unit Pengelola Hewan Laboratorium Fakultas Kedokteran Hewan Institut Pertanian Bogor.
Sampel penelitian sebanyak 25 ekor yang dipilih secara acak yang dibagi
dalam 5 kelompok. Menurut Federer (1967), rumus penentuan sampel untuk
uji eksperimental adalah:
(t−1)(n−1)≥15
Dimana t adalah jumlah kelompok percobaan dan n merupakan jumlah
sampel tiap kelompok. Penelitian ini akan menggunakan 5 kelompok
perlakuan sehingga penghitungan sampel menjadi:
(t−1)(5−1)≥15
5t–t–5+1≥15
4t–4≥15
4t≥19
t≥4,75
Jadi, sampel yang digunakan tiap kelompok percobaan minimal sebanyak 5
ekor (n≥4,75) dan jumlah kelompok yang digunakan adalah 5 kelompok
Adapun kelima kelompok tikus ini terdiri dari:
1. Kelompok 1 merupakan kelompok tikus putih yang tidak diberi herbisida
paraquat diklorida per−oral. Kelompok ini digunakan sebagai kelompok
kontrol.
2. Kelompok 2 merupakan kelompok tikus putih yang diberi herbisida
paraquat diklorida per−oral dengan dosis 25 mg/kgBB selama 2 hari.
3. Kelompok 3 merupakan kelompok tikus putih yang diberi herbisida
paraquat diklorida per−oral dengan dosis 50 mg/kgBB selama 2 hari.
4. Kelompok 4 merupakan kelompok tikus putih yang diberi herbisida
paraquat diklorida per−oral dengan dosis 100 mg/kgBB selama 2 hari.
5. Kelompok 5 merupakan kelompok tikus putih yang diberi herbisida
paraquat diklorida per−oral dengan dosis 200 mg/kgBB selama 2 hari.
Adapun tikus yang digunakan pada penelitian ini memenuhi kriteria
inklusi sebagai berikut:
1. Tikus putih galur Sprague dawley 2. Berjenis kelamin jantan
3. Berat badan sekitar 150 gram
4. Berusia kurang lebih 8–10 minggu
5. Terdapat penampakan keadaan rambut tidak kusam, rontok, atau botak,
dan bergerak aktif
6. Tingkah laku dan aktivitas normal
Kriteria ekslusi pada penelitian ini antara lain:
1. Terdapat penampakan rambut kusam, rontok atau botak dan aktivitas
kurang atau tidak aktif, keluarnya eksudat yang tidak normal dari mata,
mulut, anus dan genital
2. Terdapat penurunan berat badan lebih dari 10% setelah masa adaptasi di
laboraturium
3. Mati selama masa pemberian perlakuan
D. Bahan dan Alat Penelitian
1. Bahan Penelitian
Bahan penelitian yang digunakan meliputi herbisida paraquat diklorida
dengan dosis 25 mg/kgBB, 50 mg/kgBB, 100 mg/kgBB, dan 200
mg/kgBB, tikus putih jantan, pakan dan minum tikus.
2. Bahan Kimia
Bahan yang digunakan untuk pembuatan preparat histopatologi dengan
3. Alat Penelitian
Alat penelitian yang digunakan dalam penelitian ini antara lain:
1. Neraca analitik Metler Toleda dengan tingkat ketelitian 0,01 gram, untuk menimbang berat tikus
2. Sonde oral
3. Minor Set, membedah tikus untuk mengidentifikasi hati
4. Kapas dan alkohol
5. Kandang tikus dan botol minum tikus
6. Alat Pembuatan Preparat Histopatologi meliputi object glass, deck glass, tissue cassette, rotarymicrotome, oven, water bath, latening table, autotechnicom processor, staining jar, staining rak, kertas saring, histoplast, dan paraffin dispenser
7. Alat pemeriksaan mikroskopis yang terdiri dari mikroskop, gelas
objek, dan cairan emersi
8. Kamera digital
E. Prosedur Penelitian
1. Perawatan Hewan Coba
Tikus putih (Rattus norvegicus) jantan galur Sprague dawley berumur 8– 10 minggu yang diperoleh dari Unit Pengelola Hewan Laboratorium
Fakultas Kedokteran Hewan Institut Pertanian Bogor dimasukkan ke
dalam kandang yang telah disiapkan dan diadaptasikan selama tujuh hari.
dan pasir hidrolit, dan ditutupi dengan bedding kawat. Kandang tikus dibersihkan seminggu sekali dengan memberikan desinfektan pada
lantainya. Setiap hari makanan dan minuman diberikan secara ad libitum.
2. Prosedur Pemberian Dosis Herbisida Paraquat diklorida
Dosis herbisida paraquat diklorida yang digunakan pada penelitian ini
adalah 25 mg/kgBB untuk kelompok 2, 50 mg/kgBB untuk kelompok 3,
100 mg/kgBB untuk kelompok 4, dan 200 mg/kgBB untuk kelompok 5.
Kelompok 1 merupakan kelompok kontrol sehingga tidak diberikan
herbisida paraquat diklorida per−oral. Berat rata-rata tikus putih jantan yang digunakan sebagai hewan coba pada penelitian ini adalah 100 gram
atau 0,1 kg. Berdasarkan berat rata-rata tikus putih jantan tersebut akan
dihitung dosis herbisida paraquat diklorida yang akan diberikan per-oral
pada tikus putih jantan dalam satuan mg/100gBB.
Herbisida paraquat diklorida yang digunakan pada penelitian ini adalah
herbisida dalam bentuk cair, sehingga dosis dalam satuan mg/100gBB
akan dikonversikan dalam satuan mililiter (ml) berdasarkan dosis
herbisida paraquat diklorida yang terdapat pada label kemasan yaitu 276
SL atau sama dengan 276 mg/ml. Hasil perhitungan dosis dalam satuan
ml akan dilarutkan dengan air sesuai dengan dosis masing−masing
kelompok sehingga mendapatkan jumlah sebanyak 1 ml cairan yang
Perhitungan dosis herbisida paraquat diklorida yang akan diberikan per-oral
untuk masing-masing tikus pada setiap kelompok adalah sebagai berikut.
1) Dosis untuk setiap tikus kelompok 2
Dosis tikus (100 g) = 25 mg/kgBB x 0,1 kg
= 2,5 mg/100gBB
Dosis herbisida dalam bentuk cairan 276 mg = 2,5 mg/100gBB
1 ml x
x = 2,5 mg/100gBB 276 mg
x = 0,009 ml dibulatkan menjadi 0,01 ml
Dosis herbisida paraquat dikloridayang diberikan per−oral adalah
0,01 ml herbisida paraquat diklorida + 0,99 ml air = 1 ml
2) Dosis untuk setiap tikus kelompok 3
Dosis tikus (100 g) = 50 mg/kgBB x 0,1 kg
= 5 mg/100gBB
Dosis herbisida dalam bentuk cairan 276 mg = 5 mg/100gBB
1 ml x x = 5 mg/100gBB
276 mg
x = 0,0018 ml dibulatkan menjadi 0,02 ml
Dosis herbisida paraquat dikloridayang diberikan per−oral adalah
3) Dosis untuk setiap tikus kelompok 4
Dosis tikus (100 g) = 100 mg/kgBB x 0,1 kg
= 10 mg/100gBB
Dosis herbisida dalam bentuk cairan 276 mg = 10 mg/100gBB
1 ml x
x = 10 mg/100gBB 276 mg
x = 0,036 ml dibulatkan menjadi 0,04 ml
Dosis herbisida paraquat dikloridayang diberikan per−oral adalah
0,04 ml herbisida paraquat diklorida + 0,96 ml air = 1 ml
4) Dosis untuk setiap tikus kelompok 5
Dosis tikus (200 g) = 200 mg/kgBB x 0,1 kg
= 20 mg/100gBB
Dosis herbisida dalam bentuk cairan 276 mg = 20 mg/100gBB
1 ml x
x = 20 mg/100gBB 276 mg
x = 0,072 ml dibulatkan menjadi 0,07 ml
Dosis herbisida paraquat dikloridayang diberikan per−oral adalah
Pemberian herbisida paraquat diklorida dengan dosis yang berbeda untuk
masing−masing kelompok tersebut dilakukan selama 2 hari dengan
menggunakan sonde oral.
3. Prosedur Pengelolaan Hewan Coba Pasca Penelitian
Sebelum dilakukan pembedahan untuk mengambil organ hati pada tikus,
di akhir perlakuan terlebih dahulu tikus akan dianastesi dengan
menggunakan ketamine−xylazine dengan dosis 75−100 mg/kg ditambah 5−10 mg/kg secara intraperitoneal dengan selama 10−30 menit. Setelah
dianastesi, tikus diterminasi dengan cara melakukan dislokasi servikal
(AVMA, 2013).
4. Prosedur Pengambilan Organ Hati
Dilakukan laparotomi kemudian hati tikus diambil untuk pembuatan
sediaan mikroskopis. Setelah itu sample hati difiksasi dengan formalin
10% selama 3 jam. Lalu sampel tersebut dibuat dalam bentuk sedian
mikroskopis dengan menggunakan metode parrafin dan pewarnaan
Hematoksiklin Eosin (HE).
5. Prosedur Operasional Pembuatan Slide
Metode teknik pembuatan preparat histopatologi menurut bagian
Patologi Anatomi Fakultas Kedokteran Universitas Lampung antara lain
a. Fixation
1) Spesimen berupan potongan organ telah dipotong
secara representatif kemudian segera difiksasi dengan
formalin 10% selama 3 jam.
2) Dicuci dengan air mengalir sebanyak 3−5 kali.
b. Trimming
1) Organ dikecilkan hingga ukuran ±3 mm.
2) Potongan organ hati tersebut dimasukkan kedalam tissue casette. c. Dehidrasi
1) Mengeringkan air dengan meletakkan tissue casette pada kertas tisu.
2) Dehidrasi dengan:
a) Alkohol 70% selama 0,5 jam
b) Alkohol 96% selama 0,5 jam
c) Alkohol 96% selama 0,5 jam
d) Alkohol 96% selama 0,5 jam
e) Alkohol absolut selama 1 jam
f) Alkohol absolut selama 1 jam
g) Alkohol absolut selama 1 jam
h) Alkohol xylol 1:1 selama 0,5 jam d. Clearing