ANWAR HASAN
SEKOLAH PASCASARJANA
INSTITUT PERTANIAN BOGOR
PERNYATAAN MENGENAI SUMBER TESIS DAN SUMBER INFORMASI
Dengan ini saya menyatakan bahwa tesis dengan judul Ko-infeksi Infectious Myonecrosis Virus (IMNV) dan Vibrio harveyi pada Udang Vaname (Litopenaeus vannamei) adalah karya saya dengan arahan dari komisi pembimbing dan belum diajukan dalam bentuk apa pun kepada perguruan tinggi mana pun. Sumber informasi yang berasal atau dikutip dari karya yang diterbitkan maupun tidak diterbitkan dari penulis lain telah disebutkan dalam teks dan dicantumkan dalam Daftar Pustaka di bagian akhir tesis ini.
Bogor, Desember 2011
Vibrio harveyi in Pacific White Shrimp (Litopenaeus vannamei). Under direction of SUKENDA and WIDANARNI.
L. vannamei production in Indonesia was growing intensively. In 2006, IMN (infectious myonecrosis) disease was confirmed spread to Indonesia shrimp farm and declined shrimp production. The study was conducted to investigate effect of dose of V. harveyi on co-infection with IMNV in L. vannamei as well as development of viral infection. Shrimps juvenile were oral infected with IMNV infected shrimps 10 % feeding rate during 3 days and co-infected with 106, 107 and 108 cfu/ml V. harveyi. Mortality rate was 0 % in control and single infection of V. harveyi except 108 cfu/ml treatment. Mortality pattern demonstrated on co-infection was faster and higher than single IMNV co-infection in 14 days observation. The density of green colony Vibrio in hepatopancreas of co-infected shrimps collected in 2, 4, 6, 8 and 10 days post infection were higher than V. harveyi single infected (significantly in 10 days post infection). There were no difference of IMN disease development between co-infection and IMNV single infection. It was confirmed by visual gross sign appeared, tissue and lymphoid organ histophatology, organ abnormality, and PCR test. In conclusion, IMN diseasecaused higher and faster mortality on co-infection with V. harveyi, but not affect to IMN disease development.
RINGKASAN
ANWAR HASAN. Ko-infeksi Infectious Myonecrosis Virus (IMNV) dan Vibrio harveyi pada Udang Vaname (Litopenaeus vannamei). Dibimbing oleh SUKENDA dan WIDANARNI.
Penyakit IMN (infectious myonecrosis) adalah penyakit terkini yang menyerang udang Litopenaeus vannamei. Saat ini mortalitas udang akibat penyakit IMN bisa mencapai 70% dan udang yang mengalami kematian tidak menampakkan gejala klinis tingkat lanjut, yaitu sebagian abdomen sampai ekor menjadi merah. Konsep ko-infeksi belum banyak dipelajari di bidang akuakultur, padahal banyak kasus patogen tidak hanya menyerang sebagai infeksi tunggal. Penelitian ini dilakukan untuk menginvestigasi dampak ko-infeksi infectious myonecrosis virus (IMNV) dan Vibrio harveyi pada udang L. vannamei, serta mengamati perkembangan gejala klinis penyakit IMN yang terjadi.
Penelitian ini dilakukan pada Januari-Mei 2011 di Laboratorium Kesehatan Ikan, Departemen Budidaya Perairan, Fakultas Perikanan dan Ilmu Kelautan, Institut Pertanian Bogor. Udang uji diperoleh dengan memelihara benih udang vaname SPF (specific pathogen free) sejak PL (post larvae) 10 hingga berukuran minimal 2 gram. Stok virus adalah udang hidup yang diinfeksi virus IMNV, dan digunakan sebagai sumber infeksi setelah menampakkan symptom penyakit IMN dan diverifikasi dengan PCR (polymerase chain reaction). Sedangkan isolat V. harveyi merupakan koleksi Laboratorium Kesehatan Ikan, Departemen Budidaya Perairan, Institut Pertanian Bogor.
Penelitian ini dibagi menjadi dua percobaan. Percobaan 1 yaitu mengetahui dampak ko-infeksi IMNV dengan berbagai dosis V. harveyi. Juvenil udang vaname dengan bobot rata-rata 2.71±0.395 g sebanyak 8 ekor tiap wadah perlakuan dipelihara di akuarium dengan volume 10 liter. Udang uji diberi perlakuan infeksi oral dengan udang yang terinfeksi virus IMNV dengan feeding rate 10% selama 3 hari. Perlakuan terdiri dari infeksi tunggal V. harveyi (106, 107 and 108 cfu/ml), ko-infeksi IMNV dengan
V. harveyi (106, 107 and 108 cfu/ml), infeksi tunggal IMNV dan kontrol. Pada perlakuan ko-infeksi, sesaat setelah proses infeksi IMNV, udang uji diinfeksi dengan bakteri V. harveyi 106, 107 and 108
Pada percobaan 2, dilakukan pengamatan terhadap 4 perlakuan yaitu infeksi tunggal V. harveyi 10
cfu/ml dengan metode imersi. Selanjutnya udang uji dipelihara dan diamati selama 14 hari setelah infeksi. Parameter yang diamati pada Percobaan 1 yaitu mortalitas udang uji. Berdasarkan hasil Percobaan 1, dosis tertinggi infeksi tunggal V. harveyi yang tidak mematikan pada infeksi tunggal namun mematikan pada ko-infeksi dengan IMNV digunakan pada Percobaan 2.
7 cfu/ml, ko-infeksi IMNV
Densitas Vibrio koloni hijau di hepatopankreas udang yang diisolasi pada hari ke-2, 4, 6, 8, dan 10 pasca infeksi dari perlakuan ko-infeksi IMNV dan V. harveyi 10
Sedangkan pada perlakuan ko-infeksi virus IMNV dengan berbagai dosis V. harveyi diperlihatkan adanya mortalitas pada semua perlakuan dengan awal mortalitas yang lebih cepat dan nilai yang lebih tinggi dibandingkan infeksi tunggal IMNV selama pengamatan 14 hari.
7 cfu/ml selalu lebih tinggi dibandingkan dengan infeksi tunggal
V. harveyi 107 cfu/ml. Bahkan pada hari ke-10 pasca infeksi densitas Vibrio koloni hijau di hepatopankreas pada perlakuan ko-infeksi mencapai 108x105 ± 27,06x105 cfu/ml, signifikan lebih tinggi (P<0.05) dibandingkan infeksi tunggal 2x105 ± 1x105 cfu/ml. Sedangkan jumlah total
Vibrio di hepatopankreas mencapai 139,67x105 ± 5,69x105 cfu/ml, sangat signifikan lebih tinggi (P<0.01) dibandingkan infeksi tunggal 53,67x105 ± 6.81x105 cfu/ml. Tidak ada perbedaan perkembangan gejala klinis penyakit IMN antara perlakuan infeksi tunggal virus IMNV dan ko-infeksi IMNV dengan V. harveyi 107
Dapat dikonfirmasi bahwa gejala klinis berupa perubahan visual transparansi tubuh akibat nekrosis, histopatologi jaringan otot, histopatologi organ limfoid, abnormalitas organ limfoid dan usus serta pengujian dengan polymerase chain reaction (PCR) menunjukkan hasil yang mirip antara infeksi tunggal IMNV dengan ko-infeksi. Gejala klinis awal terlihat pada hari ke-6 pasca infeksi di kedua perlakuan. Sehingga dapat disimpulkan, bahwa penyakit IMN dapat menyebabkan mortalitas yang lebih cepat dan lebih tinggi pada ko-infeksi dengan bakteri patogen V. harveyi, namun tidak berdampak pada perkembangan gejala klinis penyakit IMN.
cfu/ml.
© Hak Cipta milik IPB, Tahun 2011 Hak Cipta dilindungi Undang-undang
Dilarang mengutip sebagian atau seluruh karya tulis ini tanpa mencantumkan atau menyebutkan sumbernya. Pengutipan hanya untuk kepentingan pendidikan, penelitian, penulisan karya ilmiah, penyusunan laporan, penulisan kritik, atau tinjauan suatu masalah; dan pengutipan tersebut tidak merugikan kepentingan yang wajar IPB
DAN
Vibrio harveyi
PADA UDANG VANAME
(
Litopenaeus vannamei
)
ANWAR HASAN
Tesis
Sebagai salah satu syarat untuk memperoleh gelar Magister Sains pada
Program Studi Ilmu Akuakultur
SEKOLAH PASCASARJANA
INSTITUT PERTANIAN BOGOR
Nama : Anwar Hasan NIM : C151090301
Disetujui, Komisi Pembimbing
Dr. Ir. Sukenda, M.Sc
Ketua Anggota
Dr. Ir. Widanarni, M.Si
Diketahui,
Ketua Program Studi Dekan Sekolah Pascasarjana Ilmu Akuakultur
Prof. Dr. Enang Harris, M.S Dr. Ir. Dahrul Syah, M.Sc. Agr
PRAKATA
Syukur Alhamdulillah kepada Allah SWT atas rahmat dan karunia-Nya, penulis dapat menyelesaikan penelitian dan penulisan tesis ini dengan baik. Tema penelitian yang penulis pilih adalah penyakit pada udang vaname yaitu mengenai perkembangan penyakit viral infectious myonecrosis (IMN) dan dampak ko-infeksinya dengan bakteri oportunis. Penulis memilih tema tersebut karena penulis berfikir perlu menambah khasanah literatur mengenai penyakit IMN yang telah mewabah dan menyebabkan penurunan produksi udang di Indonesia, sehingga bisa menjadi salah satu dasar alternatif penanggulangannya. Tema tersebut diterjemahkan dalam judul tesis Ko-infeksi Infectious Myonecrosis Virus (IMNV) dan Vibrio harveyi pada Udang Vaname (Litopenaeus vannamei).
Pada kesempatan ini penulis mengucapkan terima kasih kepada komisi pembimbing yaitu Dr. Sukenda (ketua) dan Dr. Widanarni (anggota) yang telah memberikan bimbingan dan arahannya selama penelitian dan penyusunan tesis ini. Ucapan terima kasih juga penulis sampaikan kepada Dr. Mia Setiawati selaku penguji luar komisi atas saran dan masukannya untuk kesempurnaan tesis ini. Kepada ketua program studi Ilmu Akuakultur IPB Prof. Dr. Enang Harris beserta jajaran staf pengajar yang telah mengajarkan ilmunya selama penulis menempuh pendidikan pascasarjana. Kepada Dr. Sri-Nhonghang Supornchai (DuPont Thailand), dan Bapak George Hadi Santoso serta Ibu Secuandra Elania (DuPont Indonesia) yang telah memberikan izin kepada penulis untuk melanjutkan studi di Sekolah Pascasarjana IPB.
Selanjutnya terima kasih saya persembahkan kepada ayahanda Syofyan Rahim (alm) dan Ibunda Yohana atas didikan dan kasih sayangnya. Keluarga tercinta, Dewi Eka Prasetyati dan ananda Oryza Al Ghiffari serta Syofia Sakura Fajriani.
Semoga tesis ini dapat bermanfaat bagi bidang akuakultur.
Bogor, Desember 2011
tanggal 25 Februari 1982 sebagai putra pertama dari lima bersaudara pasangan Bapak Syofyan Rahim (alm) dan Ibu Yohana. Jenjang pendidikan penulis dimulai di SDN 3 Kalianda pada tahun 1988-1994, kemudian melanjutkan ke SLTPN 1 Kalianda tahun 1994-1997. Penulis menempuh pendidikan menengah atas di SMUN 1 Kalianda pada tahun 1997-2000. Pada tahun 2000, penulis diterima sebagai mahasiswa Jurusan Budidaya Perairan, Fakultas Perikanan dan Ilmu Kelautan, Institut Pertanian Bogor, dan kemudian memperoleh gelar sarjana strata 1 (S1) pada tahun 2005. Penulis melanjutkan pendidikan di Sekolah Pascasarjana IPB pada tahun 2009 pada Program Studi Ilmu Akuakultur.
DAFTAR ISI
Halaman
HALAMAN JUDUL... i
ABSTRACT... iii
RINGKASAN... iv
LEMBAR PENGESAHAN... viii
PRAKATA... ix
RIWAYAT HIDUP... x
DAFTAR ISI... xi
DAFTAR TABEL... xii
DAFTAR GAMBAR... xiii
DAFTAR LAMPIRAN... xiv
I. PENDAHULUAN... 1
1.1 Latar Belakang... 1
1.2 Perumusan Masalah... 3
1.3 Tujuan dan Manfaat... 3
1.4 Hipotesis... 3
II. TINJAUAN PUSTAKA... 4
2.1 Infectious Myonecrosis Virus... 4
2.2 Bakteri Vibrio harveyi 8 2.3 Ko-infeksi Patogen pada Udang Vaname... 9
III. METODE PENELITIAN... 11
3.1 Waktu dan Tempat... 11
3.2 Organisme Uji... 11
3.3 Stok Virus dan Bakteri... 11
3.4 Desain Penelitian... 12
3.4.1 Percobaan 1. Dampak Ko-Infeksi IMNV dan Berbagai Dosis V. harveyi terhadap Mortalitas Udang Uji... 12
3.4.2 Percobaan 2. Penghitungan Jumlah Bakteri Vibrio, Perkembangan Gejala Klinis Penyakit IMN dan Konfirmasi Virus IMNV di Tubuh Udang Uji dengan Polymerase Chain Reaction (PCR)... 13
3.5 Pengukuran Parameter... 14
3.6 Analisis Data... 16
IV. HASIL DAN PEMBAHASAN... 17
4.1 Hasil... 17
4.1.1 Percobaan 1. Dampak Ko-Infeksi IMNV dan Berbagai Dosis V. harveyi terhadap Mortalitas Udang Uji... 17
4.1.2 Percobaan 2. Penghitungan Jumlah Bakteri Vibrio, Perkembangan Gejala Klinis Penyakit IMN dan Konfirmasi Virus IMNV di Tubuh Udang Uji dengan PCR... 18
4.1.2.1 Penghitungan jumlah bakteri Vibrio... 18
4.1.2.2 Perkembangan klinis penyakit IMN... 21
4.2 Pembahasan... 29
V. KESIMPULAN DAN SARAN... 35
5.1 Kesimpulan... 35
5.2 Saran... 35
DAFTAR PUSTAKA... 36
DAFTAR TABEL
Halaman 1. Desain percobaan 1, dampak ko-infeksi virus IMNV dan berbagai
dosis bakteri V. harveyi terhadap mortalitas udang uji ……... 12 2. Desain Percobaan 2, penghitungan densitas bakteri Vibrio,
pengamatan gejala klinis, histopatologi dan uji PCR IMNV.…………... 13 3. Pengamatan gejala klinis dan histopatologi... 14 4. Parameter pengamatan gejala klinis (symptom) Penyakit
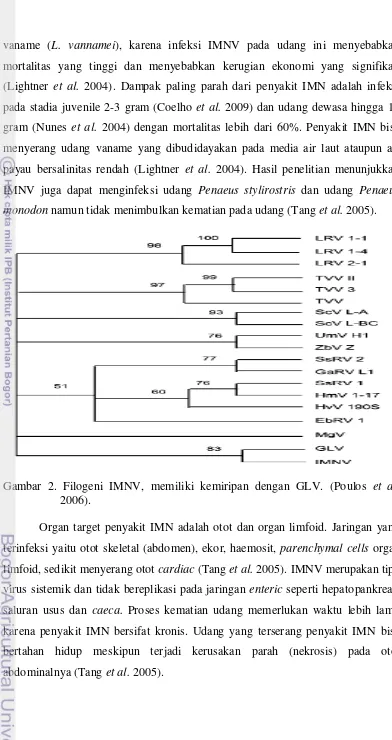
2. Filogeni IMNV, memiliki kemiripan dengan GLV. (Poulos et al.
2006)... 5
3. Gejala klinis penyakit IMN. (Poulos et al. 2006). ... 6
4. Histologi jaringan otot udang yang terinfeksi penyakit IMN dengan pewarnaan haematoxylin – eosin dari berbagai sumber. ... 7
5. Histologi organ limfoid udang. (Andrade et al. 2008)..,... 7
6. Mortalitas udang uji pasca infeksi dengan IMNV dan berbagai dosis V. harveyi... 17
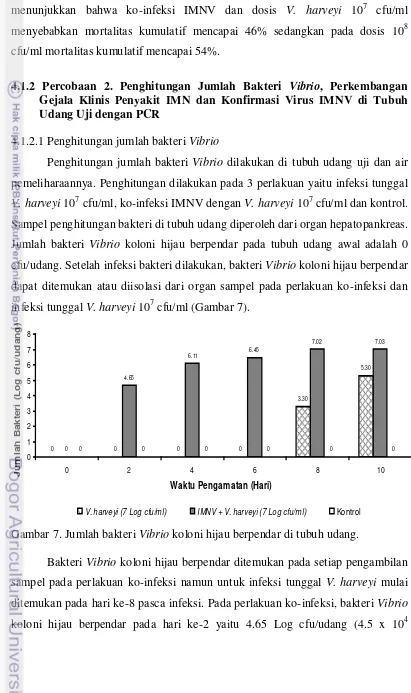
7. Jumlah bakteri Vibrio koloni hijau berpendar di tubuh udang... 18
8. Jumlah bakteri Vibrio koloni hijau berpendar di air pemeliharaan... 19
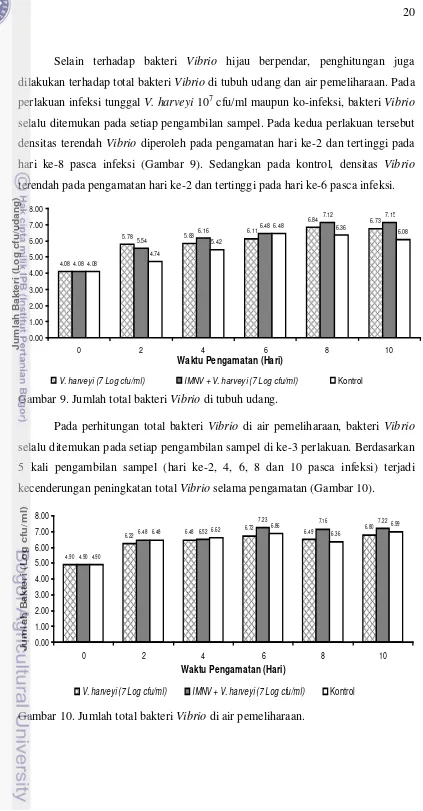
9. Jumlah total bakteri Vibrio di tubuh udang... 20
10. Jumlah total bakteri Vibrio di air pemeliharaan... 20
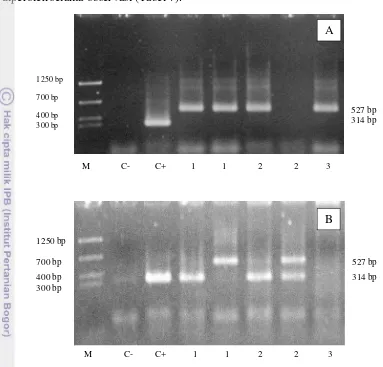
11. Hasil pengujian PCR udang uji menggunakan kit PCR Nugen-IMNV... 23
12. Sampel udang pada hari ke-14 dengan gejala klinis nekrosis level 3. 24 13. Abnormalitas organ limfoid dan usus dengan observasi visual... 25
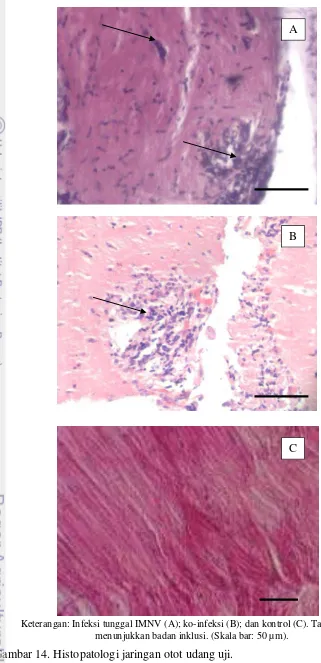
14. Histopatologi jaringan otot udang uji... 27
DAFTAR LAMPIRAN
Halaman 1. Pembuatan media bakteri (SWC dan TCBS)... 39 2. Prosedur pembuatan preparat histologi jaringan... 40 3. Penghitungan mortality rate (MR) pada Percobaan 1……...………... 44 4. Penghitungan bakteri Vibrio di tubuh udang... 45 5. Penghitungan bakteri Vibrio di air pemeliharaan... 46 6. Hasil analisis uji T (MINITAB 16) jumlah bakteri Vibrio hijau
berpendar dan total Vibrio pada perlakuan infeksi tunggal V. harveyi 107 cfu/ml dan ko-infeksi IMNV dengan
I. PENDAHULUAN
1.1Latar Belakang
Udang vaname (Litopenaeus vannamei) merupakan udang yang
dibudidayakan secara global. Lebih dari 90% produksi udang di Amerika Latin adalah udang vaname (Wurmann et al. 2004). Negara produsen udang di Asia
juga beralih membudidayakan udang vaname. Budidaya vaname intensif di Asia menggantikan Penaeus monodon dilakukan sejak tahun 2002, dan 2004 mayoritas
sudah membudidayakan udang vaname (Flegel 2006).
Penyakit sering menjadi masalah utama dalam budidaya udang. Penyakit pada budidaya udang berdampak negatif terhadap ekonomi di beberapa Negara di Asia, Amerika Selatan dan Amerika yang banyak memiliki industri budidaya udang (Liu et al. 2009). Penyakit yang menyerang udang antara lain penyakit
viral IHHN (infectious hypodermal and hematopoietic necrosis), YH (yellow head), WSS (white spot syndrome), TS (taura syndrome) dan penyakit bakterial
vibriosis. Penyakit IMN (infectious myonecrosis) adalah penyakit terkini yang
menyerang udang vaname (Walker dan Winton 2010). Penyakit IMN ditemukan di Brazil tahun 2002 dan menyebabkan dampak kerugian ekonomi yang signifikan (Costa et al. 2009). Wabah IMNV menyebar ke Indonesia dengan gejala klinis
mirip dengan wabah di Brazil pada tahun 2006 (Senapin et al. 2007).
Karakteristik virus IMNV diidentifikasi sebagai dsRNA virus dari famili Totiviridae (Poulos et al. 2006; Tang et al. 2008). IMNV merupakan non-envelop
virus dan virion berbentuk icosahedral dengan ukuran 40 nm (Senapin et al.
2007). Gejala klinis penyakit IMN yaitu hilangnya transparansi pada jaringan otot akibat nekrosis. Pada stadia infeksi lanjutan, warna putih pada distal abdomen dan ekor akibat nekrosis akan berubah menjadi merah dan dapat menyebabkan mortalitas mencapai 70% (Tang et al. 2008).
2
Vibriosis adalah penyakit bakterial pada udang penaeid, dan Vibrio spp.
merupakan agen penyakit ini. V. harveyi bersifat patogen pada udang windu,
bahkan strain V. harveyi yang virulen dengan kepadatan 102 cfu/ml dapat
mematikan udang windu 100% pada stadia larva (Lavilla-Pitogo et al. 1990),
sedangkan pada udang juvenil V. harveyi dapat mematikan udang vaname hingga
80% pada dosis 106 cfu/ml saat ko-infeksi dengan virus WSSV dalam waktu 144 jam (Phuoc et al. 2009). Vibrio spp. bisa bertindak sebagai patogen primer ketika
kualitas air buruk (Vandenberghe et al. 1998) namun dapat menjadi patogen
sekunder karena Vibrio spp. bersifat oportunis (Saulnier et al. 2000).
Banyak kasus patogen tidak hanya menyerang udang sebagai infeksi tunggal. Kejadian ko-infeksi yang sudah dilaporkan antara lain ko-infeksi beberapa virus pada udang vaname seperti WSSV-TSV (Tsai et al. 2002),
WSSV-IHHNV (Yeh et al. 2009), TSV-IHHNV (Tan et al. 2009), TSV-IHHNV-WSSV
(Tan et al. 2009), dan ko-infeksi virus dengan bakteri seperti WSSV-Vibrio campbelli (Phuoc et al. 2009) serta WSSV-V. harveyi (Phuoc et al. 2009).
Ko-infeksi antar patogen dapat terjadi karena patogen-patogen tersebut merupakan agen penyebab penyakit dengan inang yang sama yaitu udang penaeid.
Sifat patogen oportunis Vibrio spp. akan muncul akibat adanya stres
lingkungan atau infeksi primer patogen lain. Infeksi primer WSSV dapat menyebabkan udang menjadi lemah dan meningkatkan infeksi bakteri. Pada udang yang terkena wabah penyakit WSS ternyata ditemukan strain V. alginolyticus yang virulen (Manilal et al. 2010). Investigasi Gomez-Gil et al.
(1998) menunjukkan bahwa V. alginolyticus, V. vulnificus, V. parahaemolyticus, V. damsela, Vibrio sp. dapat dideteksi pada udang sehat tanpa gejala klinis
vibriosis. Flegel et al. (2004) juga menemukan infeksi WSSV tanpa gejala klinis luar dan kerusakan jaringan. Infeksi sekunder Vibrio spp. pun mempercepat kematian udang yang terinfeksi virus (WSSV) tanpa gejala klinis penyakit WSS maupun vibriosis (Phouc et al. 2009).
1.2Perumusan Masalah
Berdasarkan kejadian penyakit IMN pada budidaya udang di Indonesia maka ada dugaan peran ko-infeksi IMNV dan patogen lain, sehingga menyebabkan mortalitas udang di tambak yang terinfeksi penyakit IMN semakin tinggi. Vibrio spp. terutama Vibrio harveyi sebagai bakteri oportunistik
memungkinkan untuk berperan lebih besar dalam mortalitas udang karena kondisi udang yang lemah akibat penyakit yang dialami.
1.3Tujuan dan Manfaat
Penelitian ini bertujuan untuk mengetahui dampak ko-infeksi IMNV dengan bakteri V. harveyi yang dipengaruhi oleh berbagai dosis infeksi V. harveyi
dan menganalisa perkembangan gejala klinis penyakit IMN pada infeksi tunggal serta ko-infeksi.
Penelitian ini diharapkan dapat menghasilkan informasi penting mengenai ko-infeksi virus IMNV dengan V.harveyi dan perkembangan klinis penyakit IMN
pada udang vaname.
1.4Hipotesis
Hipotesis dari penelitian ini yaitu ko-infeksi virus IMNV dengan bakteri V. harveyi dapat menyebabkan dampak kematian yang lebih tinggi dan lebih cepat
4
II. TINJAUAN PUSTAKA
2.1 Infectious Myonecrosis Virus
Virus IMNV (infectious myonecrosis virus) adalah agen penyebab
penyakit IMN. Virus ini memiliki genom tunggal dsRNA yang tidak bersegmen dengan molekul 7560 bp. Partikel IMNV berbentuk icosahedral dengan diameter 40 nm. IMNV memiliki capsid isometrik dengan protein penyusun 901-asam amino (Tang et al. 2008). Tang et al. (2008) juga melaporkan bentuk virion
IMNV dengan cryomicrograph dan rekonstruksi 3-dimensinya (Gambar 1).
Keterangan: (A) Cryomicrograph virion IMNV yang telah dimurnikan dari sampel kepala udang. Tanda panah adalah contoh protrusi pada permukaan virus. (B) Rekonstruksi 3-dimensi virion
IMNV dengan resolusi 8.0-Å. Gambar 1. Virion IMNV. (Tang et al. 2008).
Analisis filogeni IMNV telah dilakukan berdasarkan RDA-dependent dari
gen RNA polimerase (RdRp), hasilnya IMNV memiliki kemiripan dengan
Giardia lamblia virus (GLV) (Gambar 2) yang merupakan bagian dari famili
Totiviridae (Poulos et al. 2006). Sebagian besar anggota famili Totiviridae
memiliki kekurangan dalam mentransmisikan (menyebarkan) virion melalui media ekstraseluler dalam siklus hidupnya (Lightner et al. 2004). Kebanyakan,
penyebaran melalui cara vertikal di dalam sel atau horizontal dengan hyphal anastomiasis kecuali GLV dan IMNV. Sebagai tambahan, IMNV juga merupakan satu-satunya virus dari famili Totiviridae yang diketahui menyebabkan penyakit pada inangnya (Tang et al. 2008).
Inang virus IMNV adalah krustase terutama menyerang udang-udang penaeid. Pada prinsipnya inang paling utama dari penyakit IMN adalah udang
vaname (L. vannamei), karena infeksi IMNV pada udang ini menyebabkan
mortalitas yang tinggi dan menyebabkan kerugian ekonomi yang signifikan (Lightner et al. 2004). Dampak paling parah dari penyakit IMN adalah infeksi
pada stadia juvenile 2-3 gram (Coelho et al. 2009) dan udang dewasa hingga 12
gram (Nunes et al. 2004) dengan mortalitas lebih dari 60%. Penyakit IMN bisa
menyerang udang vaname yang dibudidayakan pada media air laut ataupun air payau bersalinitas rendah (Lightner et al. 2004). Hasil penelitian menunjukkan
IMNV juga dapat menginfeksi udang Penaeus stylirostris dan udang Penaeus monodon namun tidak menimbulkan kematian pada udang (Tang et al. 2005).
Gambar 2. Filogeni IMNV, memiliki kemiripan dengan GLV. (Poulos et al.
2006).
Organ target penyakit IMN adalah otot dan organ limfoid. Jaringan yang terinfeksi yaitu otot skeletal (abdomen), ekor, haemosit, parenchymal cells organ
limfoid, sedikit menyerang otot cardiac (Tang et al. 2005). IMNV merupakan tipe
virus sistemik dan tidak bereplikasi pada jaringan enteric seperti hepatopankreas,
saluran usus dan caeca. Proses kematian udang memerlukan waktu lebih lama
6
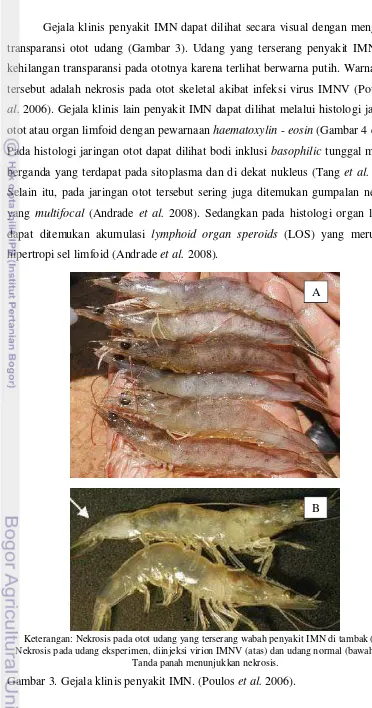
Gejala klinis penyakit IMN dapat dilihat secara visual dengan mengamati transparansi otot udang (Gambar 3). Udang yang terserang penyakit IMN akan kehilangan transparansi pada ototnya karena terlihat berwarna putih. Warna putih tersebut adalah nekrosis pada otot skeletal akibat infeksi virus IMNV (Poulos et al. 2006). Gejala klinis lain penyakit IMN dapat dilihat melalui histologi jaringan
otot atau organ limfoid dengan pewarnaan haematoxylin - eosin (Gambar 4 dan 5).
Pada histologi jaringan otot dapat dilihat bodi inklusi basophilic tunggal maupun
berganda yang terdapat pada sitoplasma dan di dekat nukleus (Tang et al. 2005).
Selain itu, pada jaringan otot tersebut sering juga ditemukan gumpalan nekrosis yang multifocal (Andrade et al. 2008). Sedangkan pada histologi organ limfoid
dapat ditemukan akumulasi lymphoid organ speroids (LOS) yang merupakan
hipertropi sel limfoid (Andrade et al. 2008).
Keterangan: Nekrosis pada otot udang yang terserang wabah penyakit IMN di tambak (A). Nekrosis pada udang eksperimen, diinjeksi virion IMNV (atas) dan udang normal (bawah) (B).
Tanda panah menunjukkan nekrosis. Gambar 3. Gejala klinis penyakit IMN. (Poulos et al. 2006).
A
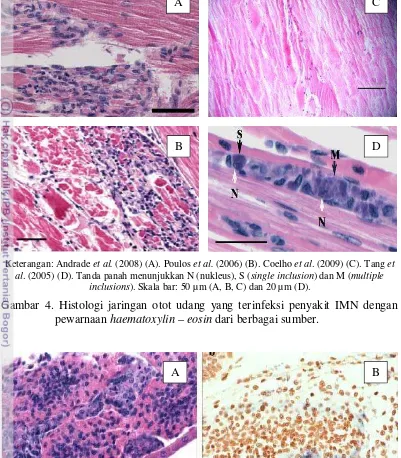
Keterangan: Andrade et al. (2008) (A). Poulos et al. (2006) (B). Coelho et al. (2009) (C). Tang et al. (2005) (D). Tanda panah menunjukkan N (nukleus), S (single inclusion) dan M (multiple
inclusions). Skala bar: 50 µm (A, B, C) dan 20 µm (D).
Gambar 4. Histologi jaringan otot udang yang terinfeksi penyakit IMN dengan pewarnaan haematoxylin – eosin dari berbagai sumber.
Keterangan: Pewarnaan haematoxylin - eosin (A). Pengamatan organ limfoid udang dengan in situ hybridization (ISH) (B). Tanda panah menunjukkan probe penanda positif terinfeksi virus IMNV.
Skala bar: 50 µm.
Gambar 5. Histologi organ limfoid udang. (Andrade et al. 2008).
A
B
C
D
8
2.2 Bakteri Vibrio harveyi
Vibrio harveyi tergolong dalam divisi Bacteria, klas Shyzomycetes, ordo
Eubacteria, famili Vibrionaceae dan genus Vibrio. Bakteri Vibrio memiliki
karakteristik Gram negatif, sel tunggal, berbentuk batang pendek yang bengkok (koma) atau lurus, bersifat motile, ukuran sel 1-4 mikron, berpendar dan mempunyai flagella di salah satu kutubnya (Kreig dan Peter 1984).
Sifat biokimia Vibrio ini yaitu oksidase positif, fermentatif terhadap
glukosa, DNA genomnya mengandung 51% mol guanin dan sitosin (Logan 1994), tidak membentuk gas pada produksi asam dari glukosa dan dapat menggunakan sukrosa sebagai sumber energi. Bakteri V. harveyi menghasilkan lysine
dekarboksilase, nitrat reduktase dan sitokrom oksidase serta enzim amilase, chitinase dan lipase (Lavilla-Pitogo et al. 1990). Protease, phospolipase,
haemolysin atau eksotoksin merupakan faktor patogenitas penting V. harveyi
(Zhang dan Austin 2000).
V. harveyi akan terlihat berpendar jika diamati di ruang gelap dan
pendarannya dapat bertahan 2-3 hari pada media Thiosulphate Citrate Bile-Salt
Sucrose (TCBS). Kemampuan berpendar merupakan hasil aktivitas enzim
luciferase yang dapat berfungsi sebagai katalisator dalam proses oksidasi reduksi. Proses oksidasi melibatkan flavin mononukleotida dan aldehid alifatik rantai panjang sebagai substratnya. Senyawa-senyawa tersebut masing-masing diubah menjadi flavin mononukelotida dan asam lemak disertai dengan pelepasan emisi cahaya dengan panjang gelombang 490 nm (Lavilla-Pitogo et al. 1990).
Pada umumnya V. harveyi bersifat patogen oportunistik, yaitu organisme
yang dalam keadaan normal ada di lingkungan pemeliharaan dan bersifat saprofitik serta berkembang patogenik jika kondisi lingkungan dan inangnya memburuk. Bakteri ini tumbuh secara optimal pada suhu 300
Habitat utama bakteri V. harveyi adalah air laut di daerah tropis, sedimen
pantai, dan saluran pencernaan organisme laut. Bakteri Vibrio merupakan patogen
oleh V. harveyi adalah penyakit bakterial paling utama pada budidaya udang
penaeid.
Penyakit vibriosis pada budidaya udang terjadi pada stadia larva sampai dewasa. Penyakit vibriosis yang disebabkan bakteri berpendar bersifat akut dan ganas. Udang windu stadia dewasa yang terserang bakteri Vibrio menyebabkan
bercak coklat pada karapasnya. Udang yang terserang bakteri Vibrio sering
ditemukan berenang di pinggir tanggul, dengan tanda-tanda kulit rusak dan berwarna coklat, nekrosis, organ limfoid berwarna hitam, bagian ekor dan kaki renangnya berwarna kemerahan, insang berwarna coklat, otot atau daging berwarna kecoklatan, ususnya kosong dan gerakannya lemah serta menyentak (Rukyani 1993). Pada uji tantang 3 strain V. harveyi terhadap Penaeus monodon
dan P. vannamei menunjukkan gejala lesi pada kutikula, terutama di apendik dan
uropod atau kipas ekor (Intaraprasong et al. 2009).
Pada stadia larva, infeksi V. harveyi menyebabkan penyakit
kunang-kunang, bercak merah pada dasar bak pemeliharaan, perubahan warna tubuh menjadi coklat kehitaman dan terjadi penyusutan hepatopankreas (Roza et al.
1997). Pada dosis tinggi (107 cfu/udang) semua udang mati dalam 12 jam setelah diinjeksi V. harveyi, sedangkan lethal doses 50% (LD50) salah satu strain V.
harveyi 102 cfu/udang (Intaraprasong et al. 2009). Sedangkan pada udang vaname,
virulensi V. harveyi tidak setinggi ketika menginfeksi udang windu. Pada udang
vaname yang terinfeksi V. harveyi, tingkah laku udang tidak berenang menyentak
seperti pada udang windu. Pada infeksi V. harveyi 105 cfu/ml, menyebabkan
udang windu mengalami moulting 43% sedangkan pada udang vaname moulting
hanya 10% (Intaraprasong et al. 2009). Bahkan V. harveyi strain BB120 tidak
menimbulkan kematian ketika diinfeksi 106
Beberapa penelitian telah menunjukkan adanya ko-infeksi atau infeksi bersama beberapa patogen pada udang vaname. Ko-infeksi tersebut bisa disebabkan oleh 2 atau lebih patogen viral dan patogen bakterial. Dilaporkan hasil penelitian yang dilakukan pada 2006 di Taiwan bahwa 75% udang sampel yang dikoleksi dari tambak yang terserang infeksi berat white spot syndrome virus
cfu/udang (Phuoc et al. 2009).
10
(WSSV) juga terinfeksi virus infectious hypodermal and hematopoietic necrosis virus (IHHNV) dengan level infeksi berat, medium dan ringan masing-masing
34%, 25% dan 16% (Yeh et al. 2009). Masih di Taiwan, penelitian Tsai et al.
(2002) menunjukkan adanya ko-infeksi virus WSSV dan TSV yang dapat dideteksi menggunakan PCR. Ko-infeksi beberapa virus juga dideteksi dari sampel udang vaname yang diambil dari Provinsi Hainan, China. Sebanyak 59.8% sampel terdeteksi mengalami ko-infeksi virus taura syndrome virus (TSV) dan
IHHNV, 42.7% sampel terdeteksi ko-infeksi WSSV dan IHHNV, serta ko-infeksi 3 virus WSSV, IHHNV dan TSV diperoleh dari 42.7% sampel (Tan et al. 2009).
Ko-infeksi patogen viral dan bakterial juga berdampak negatif pada udang vaname. Ko-infeksi WSSV dan bakteri Vibrio campbellii 104 cfu/udang
menyebabkan kematian 100% pada 84 hpi (hours post infection), padahal infeksi
tunggal V. campbellii 104 cfu/udang tidak menyebabkan kematian dan infeksi
tunggal WSSV menyebabkan mortalitas 100% pada 156 hpi (Phuoc et al. 2009).
Sedangkan ko-infeksi WSSV dengan V. harveyi strain BB120 106 cfu/udang
menyebabkan mortalitas 80% dalam 360 hpi, dan infeksi tunggal V. harveyi strain
BB120 tidak menyebabkan mortalitas pada dosis injeksi 106 cfu/udang (Phuoc et al. 2009).
Strain V. alginolyticus yang tidak patogen pada udang bisa menjadi virulen
pada udang yang terserang virus WSSV, ini dideteksi dari tambak yang terserang wabah penyakit WSS seperti dilaporkan oleh Manilal et al. (2010). Serangan
ko-infeksi juga bisa terjadi antar bakteri Vibrio spp., misalnya bakteri V. parahaemolyicus dan V. harveyi yang menyebabkan red disease syndrome
III. METODE PENELITIAN
3.1 Waktu dan Tempat
Penelitian ini dilakukan pada Januari sampai Mei 2011 bertempat di Laboratorium Kesehatan Ikan, Departemen Budidaya Perairan, Fakultas Perikanan dan Ilmu Kelautan, Institut Pertanian Bogor.
3.2 Organisme Uji
Organisme uji adalah udang Litopenaeus vannamei SPF (specific pathogen free) yang diperoleh dari hatchery komersial di Anyer, Banten. Benur (post larvae) dipelihara pada kondisi terkontrol untuk mencegah peluang infeksi IMNV
dari lingkungan.
Sebagai langkah biosecurity maka air pemeliharaan didisinfeksi
menggunakan desinfektan kuat. Desinfeksi ganda dilakukan untuk mengurangi keberadaan patogen di air yang akan digunakan untuk penelitian. Desinfeksi ganda tersebut menggunakan kalsium hipoklorit (kaporit) 10 ppm dan kalium mono-persulfat (KMPS) dengan dosis 2 ppm.
3.3 Stok Virus dan Bakteri
Stok virus diperoleh dari udang yang terinfeksi virus IMNV, yakni udang dengan symptom penyakit IMN. Verifikasi dilakukan dengan menguji ke
laboratorium PCR (kit komersial Nugen-IMNV). Udang terinfeksi dipelihara sebagai stok virus untuk bahan infeksi oral dalam penelitian ini. Otot udang tersebut dicacah dan segera diinfeksikan secara oral.
Jenis bakteri yang digunakan pada penelitian ini adalah Vibrio harveyi.
Isolat V. harveyi merupakan koleksi Laboratorium Kesehatan Ikan, Departemen
12
3.4 Desain Penelitian
3.4.1 Percobaan 1. Dampak Ko-Infeksi IMNV dan Berbagai Dosis V. harveyi
terhadap Mortalitas Udang Uji
Uji ini dilakukan untuk mengetahui pengaruh ko-infeksi virus IMNV dengan berbagai dosis V. harveyi terhadap mortalitas udang (Tabel 1). Udang uji
dengan bobot rata-rata 2.71±0.395 g sebanyak 8 ekor tiap wadah perlakuan dipelihara pada akuarium dengan volume air 10 liter. Bobot rata-rata tersebut dipilih berdasarkan penelitian ko-infeksi skala laboratorium yang dilakukan oleh Phuoc et al. (2009). Administrasi infeksi IMNV dilakukan secara oral dengan
modifikasi feeding rate 10% per hari dari bobot biomassa udang uji. Udang diberi
pakan otot udang yang terinfeksi penyakit IMN selama 3 hari, kemudian selanjutnya diberi pakan komersial (Coelho et al., 2009). Bakteri diinfeksikan
dengan metode imersi pada hari ke-3 setelah infeksi oral IMNV yang pertama. Pemeliharaan dan pengamatan dilakukan selama 14 hari mengacu pada informasi Tang et al. (2005) bahwa udang vaname yang diinfeksi virus IMNV
memerlukan waktu 9-13 hari untuk menyebabkan kematian. Data yang dianalisa adalah tingkat mortalitas udang tiap perlakuan, sehingga diperoleh dosis tertinggi infeksi V. harveyi yang tidak mematikan pada infeksi tunggal namun mematikan
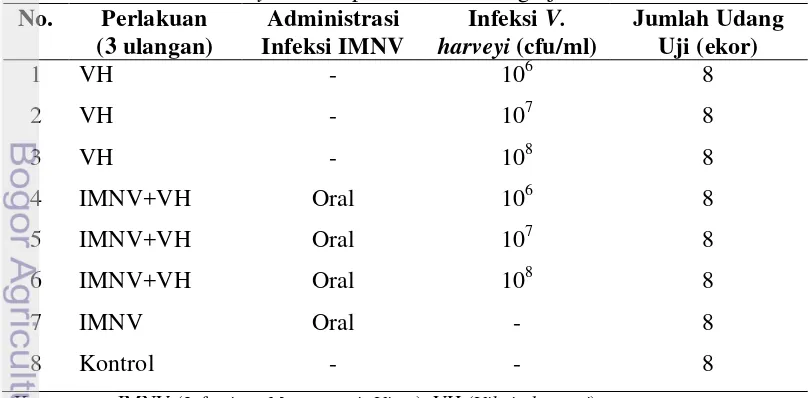
pada ko-infeksi dengan IMNV. Dosis tersebut akan digunakan pada Percobaan 2. Tabel 1. Desain percobaan 1, dampak ko-infeksi virus IMNV dan berbagai dosis
bakteri V. harveyi terhadap mortalitas udang uji.
No. Perlakuan (3 ulangan)
Administrasi Infeksi IMNV
Infeksi V.
harveyi (cfu/ml)
Jumlah Udang Uji (ekor) 1 2 3 4 5 6 7 8 VH VH VH IMNV+VH IMNV+VH IMNV+VH IMNV Kontrol - - - Oral Oral Oral Oral - 106 107 108 106 107 10 8 8 8 8 8 8 8 8 8 - -
3.4.2 Percobaan 2. Penghitungan Jumlah Bakteri Vibrio, Perkembangan Gejala Klinis Penyakit IMN dan Konfirmasi Virus IMNV di Tubuh Udang Uji dengan Polymerase Chain Reaction (PCR)
Pada percobaan ini dilakukan penghitungan densitas Vibrio pada
perlakuan infeksi tunggal V. harveyi, ko-infeksi dan kontrol (Tabel 2). Udang uji
dengan bobot rata-rata 2.91±0.312 g sebanyak 15 ekor tiap wadah perlakuan dipelihara pada akuarium dengan volume air 25 liter. Dosis infeksi diperoleh dari percobaan 1 yaitu V. harveyi 107
No.
cfu/ml. Dosis tersebut adalah dosis perlakuan yang menghasilkan respon kematian pada ko-infeksi IMNV dan V. harveyi namun
tidak berpengaruh terhadap mortalitas ketika diinfeksi V. harveyi saja.
Penghitungan bakteri berdasarkan ciri warna koloni Vibrio di media TCBS.
Koloni Vibrio tersebut digolongkan menjadi Vibrio hijau (berpendar) dan Vibrio
kuning. Penghitungan dilakukan di tubuh udang dan air. Organ sampel tubuh udang yaitu hepatopankreas. Penghitungan dilakukan pada hari ke 2, 4, 6, 8, dan 10 setelah infeksi bakteri.
Tabel 2. Desain Percobaan 2, penghitungan densitas bakteri Vibrio, pengamatan
gejala klinis, histopatologi dan uji PCR IMNV. Perlakuan Pengujian Infeksi
IMNVa
Penghitungan Bakteri (hari)
b
, Gejala Klinisc, Histopatologid (hari) 1
2 3 4
VHe
IMNVf+VHe IMNV
- 2 dan 10 2 dan 10 2 atau 10
f
Kontrol
0, 2, 4, 6, 8, 10 0, 2, 4, 6, 8, 10
-
0, 2, 4, 6, 8, 10
Keterangan: Uji PCR (a), sampel air dan hepatopankreas (b), sampel udang uji (c), sampel otot dan organ limfoid (d), dosis berdasarkan Percobaan 1 (e), infeksi oral (f).
14
yaitu jaringan otot dan organ limfoid. Pengambilan sampel untuk pengujian histopatologi dilakukan pada hari ke- 0, 2, 4, 6, 8, dan 10 pasca infeksi. Kemudian dibandingkan infeksi virus pada infeksi tunggal IMNV dengan ko-infeksi IMNV dan V. harveyi. Konfirmasi IMNV dilakukan dengan analisis PCR menggunakan
kit komersial Nugen-IMNV (hari ke-2 dan 10 setelah infeksi). Tabel 3. Pengamatan gejala klinis dan histopatologi.
No Parameter Pengamatan
Waktu Pengamatan (hari)
Sampel
1 Gejala Klinis 0, 2, 4, 6, 8, 10 Udang uji 2 Histopatologi 0, 2, 4, 6, 8, 10 Otot dan limfoid
3.5 Pengukuran Parameter 3.5.1 Penghitungan Bakteri Vibrio
Penghitungan bakteri Vibrio dilakukan dengan metode hitungan cawan
menggunakan media spesifik TCBS agar. Penghitungan Vibrio dilakukan pada
Percobaan 2. Vibrio hijau berpendar diamati minimal 8 jam setelah kultivasi. Pada
penelitian ini pengamatan dilakukan antara 16-20 jam setelah kultivasi. Untuk sampel dari tubuh udang, sampel hepatopankreas digerus dalam tube ependorf dan
ditambahkan phosphat buffer saline (PBS) steril hingga 1 ml. Selanjutnya
dilakukan pengenceran bertingkat sampai 4. Untuk sampel air pemeliharaan, sebanyak 1 ml air pemeliharaan dimasukkan ke dalam tube ependorf. Selanjutnya
dilakukan pengenceran bertingkat seperti dilakukan pada sampel tubuh udang (hepatopankreas). Inokulasi bakteri juga dilakukan pada pengenceran pertama dan ke-3 atau ke-4. Inokulasi dilakukan dengan mengambil 0.1 ml sampel dari pengenceran tersebut dan disebar pada media TCBS.
3.5.2 Histopatologi
dipotong dengan mikrotom rotary dengan ketebalan 3 – 5 µm dan diletakkan pada
gelas objek. Setelah proses tersebut, dilakukan pewarnaan dengan menggunakan
haematoxylin-eosin. Preparat diamati di bawah mikroskop untuk mengamati
perubahan jaringan yang mungkin terjadi. Histopatologi dilakukan dengan tujuan untuk mengetahui tingkat kerusakan organ akibat infeksi IMNV.
3.5.3 Gejala Klinis Penyakit IMN
Pengamatan gejala klinis dilakukan pada Percobaan 2. Pengamatan gejala klinis dari sampel meliputi beberapa stadia. Gejala-gejala klinis tersebut diamati untuk menentukan waktu awal udang menampakkan gejala klinis IMNV dan melihat perkembangan stadia gejala klinis tersebut. Pengamatan harian dilakukan secara visual pada udang uji.
Parameter gejala klinis ditentukan berdasarkan modifikasi dari pengelompokan gejala klinis menurut Costa et al. (2009). Tingkat gejala klinis
dapat dilihat pada Tabel 4.
Tabel 4. Parameter pengamatan gejala klinis (symptom) Penyakit IMN.
Level Stadia Gejala Klinis/ Symptom Simbol Tingkat Infeksi
1 Terinfeksi tanpa symptom + Ringan
2 Sedikit warna put ih lebam di dalam jaringan di beberapa segmen abdomen
++ Menengah
3 Sebagian besar jaringan
abdomen berwarna putih lebam +++ Berat 4 Bagian abdomen dari arah ekor
berwarna merah (jaringan mati)
++++ Berat
3.5.4 Mortalitas Udang
Mortalitas udang diukur pada Percobaan 1 dan 2. Perhitungan mortalitas udang menggunakan persamaan sebagai berikut:
% 100
x No
Nt
MR=
Keterangan :
16
3.6 Analisis Data
Analisis statistik untuk mengetahui perbedaan densitas bakteri Vibrio hijau
dan total Vibrio di tubuh udang antar perlakuan dievaluasi dengan t-test analysis
menggunakan software MINITAB (versi 16 untuk windows). Hasil pengamatan
0 10 20 30 40 50 60
1 2 3 4 5 6 7 8 9 10 11 12 13 14
Waktu Pengamatan (Hari)
M
o
rta
li
ta
s
(%
)
V. harveyi 6 Log cfu/ml V. harveyi 7 Log cfu/ml V. harveyi 8 Log cfu/ml
IMNV IMNV-V. harveyi 6 Log cfu/ml IMNV-V. harveyi 7 Log cfu/ml
IMNV-V. harveyi 8 Log cfu/ml Kontrol
IV. HASIL DAN PEMBAHASAN
4.1 Hasil
4.1.1 Percobaan 1. Dampak Ko-Infeksi IMNV dan Berbagai Dosis V. harveyi
terhadap Mortalitas Udang Uji
Pada penelitian ini, udang uji yang diinfeksi tunggal dengan V. harveyi 106
dan 107 cfu/ml tidak mengalami mortalitas. Pada dosis infeksi yang lebih tinggi (V. harveyi 108 cfu/ml) diperoleh hasil bahwa infeksi tunggal V. harveyi
menyebabkan awal mortalitas pada pengamatan hari ke-6 setelah infeksi sebesar 13%. Namun setelah hari ke-6 tidak ditemukan adanya mortalitas udang tambahan hingga akhir pengamatan pada hari ke-14 pasca infeksi (Gambar 6). Hasil pengamatan infeksi tunggal IMNV pada Percobaan 1 menunjukkan bahwa mortalitas mulai terjadi pada hari ke-9 pasca infeksi sebesar 4.2% dan mortalitas kumulatif pada akhir pengamatan (hari ke-14) sebesar 38%. Hasil akhir pengamatan mortalitas tersebut identik dengan hasil perlakuan ko-infeksi IMNV dan V. harveyi dosis 106
Mortalitas udang yang lebih tinggi dan lebih cepat diperoleh dari pengamatan perlakuan ko-infeksi IMNV dengan V. harveyi pada dosis 10
cfu/ml.
Gambar 6. Mortalitas udang uji pasca infeksi dengan IMNV dan berbagai dosis V. harveyi.
7 dan 108
cfu/ml. Pada ko-infeksi IMNV dan V. harveyi 107 cfu/ml, mortalitas mulai
18
0 0 0 0
3.30 5.30 0 4.65 6.11 6.45 7.02 7.03
0 0 0 0 0 0
0 1 2 3 4 5 6 7 8
0 2 4 6 8 10
Waktu Pengamatan (Hari)
J u m la h B a k te r i ( L o g c fu /u d a n g )
V. harveyi (7 Log cfu/ml) IMNV + V. harveyi (7 Log cfu/ml) Kontrol
untuk dosis V. harveyi 108 cfu/ml mortalitas awal terjadi pada pengamatan hari
ke-3 pasca infeksi sebesar 4.2%. Hasil akhir pengamatan pada hari ke-14 menunjukkan bahwa ko-infeksi IMNV dan dosis V. harveyi 107 cfu/ml
menyebabkan mortalitas kumulatif mencapai 46% sedangkan pada dosis 108
Penghitungan jumlah bakteri Vibrio dilakukan di tubuh udang uji dan air
pemeliharaannya. Penghitungan dilakukan pada 3 perlakuan yaitu infeksi tunggal
V. harveyi 10
cfu/ml mortalitas kumulatif mencapai 54%.
4.1.2 Percobaan 2. Penghitungan Jumlah Bakteri Vibrio, Perkembangan Gejala Klinis Penyakit IMN dan Konfirmasi Virus IMNV di Tubuh Udang Uji dengan PCR
4.1.2.1 Penghitungan jumlah bakteri Vibrio
7 cfu/ml, ko-infeksi IMNV dengan
V. harveyi 107 cfu/ml dan kontrol.
Sampel penghitungan bakteri di tubuh udang diperoleh dari organ hepatopankreas. Jumlah bakteri Vibrio koloni hijau berpendar pada tubuh udang awal adalah 0
cfu/udang. Setelah infeksi bakteri dilakukan, bakteri Vibrio koloni hijau berpendar
dapat ditemukan atau diisolasi dari organ sampel pada perlakuan ko-infeksi dan infeksi tunggal V. harveyi 107
Bakteri Vibrio koloni hijau berpendar ditemukan pada setiap pengambilan
sampel pada perlakuan ko-infeksi namun untuk infeksi tunggal V. harveyi mulai
ditemukan pada hari ke-8 pasca infeksi. Pada perlakuan ko-infeksi, bakteri Vibrio
[image:34.595.102.513.123.816.2]koloni hijau berpendar pada hari ke-2 yaitu 4.65 Log cfu/udang (4.5 x 10 cfu/ml (Gambar 7).
Gambar 7. Jumlah bakteri Vibrio koloni hijau berpendar di tubuh udang.
0 6.05 6.39 5.00 5.67 5.43 0 6.37 6.48
7.00 6.81 6.94
0 0 0 0 0 0
0 1 2 3 4 5 6 7 8
0 2 4 6 8 10
Waktu Pengamatan (Hari)
Ju m lah B akt er i ( L o g cf u /m l)
V. harveyi (7 Log cfu/ml) IMNV + V. harveyi (7 Log cfu/ml) Kontrol
cfu/udang). Koloni bakteri Vibrio hijau berpendar cenderung bertambah tinggi
pada pengambilan sampel berikutnya, dan koloni bakteri tersebut paling tinggi ditemukan pada hari ke-10 pasca infeksi yaitu 7.03 Log cfu/udang (1.08 x 107
cfu/udang). Vibrio koloni hijau berpendar hanya ditemukan 2 kali pada perlakuan
infeksi tunggal V. harveyi 107cfu/ml dan tidak ditemukan pada perlakuan kontrol.
Bakteri Vibrio koloni hijau berpendar pada perlakuan infeksi tunggal V. harveyi
107 cfu/ml diisolasi dari hari ke-8 (3.30 Log cfu/udang atau 2 x 103 cfu/udang) dan hari ke-10 (5.30 Log cfu/udang atau 2 x 105 cfu/udang) pasca infeksi.
Penghitungan bakteri Vibrio koloni hijau berpendar juga dilakukan di air
pemeliharaan. Jumlah bakteri Vibrio koloni hijau berpendar pada perlakuan
ko-infeksi IMNV dan V. harveyi 107 cfu/ml yang diperoleh dari 5 waktu pengambilan
sampel selalu lebih tinggi dari 6 Log cfu/ml atau 106 cfu/ml (Gambar 8). Jumlah terkecil yang ditemukan yaitu pada hari ke-2 sebesar 6.37 Log cfu/ml (2.33 x 106 cfu/ml), dan terbesar pada hari ke-6 sebesar 7 Log cfu/ml (1.01 x 107
Untuk perlakuan infeksi tunggal V. harveyi 10
cfu/ml).
7 cfu/ml, jumlah
Vibrio
koloni hijau berpendar yang ditemukan cenderung mengalami penurunan. Pada dua pengamatan pertama yaitu hari ke-2 dan 4 pasca infeksi, jumlah Vibrio hijau
berpendar yang ditemukan di atas 6 Log cfu/ml (106 cfu/ml). Namun pada
pengamatan selanjutnya (hari ke- 4, 6 dan 10 pasca infeksi) bakteri Vibrio koloni
hijau berpendar yang ditemukan antara 5 Log cfu/ml sampai 6 Log cfu/ml (105–
106 cfu/ml). Sedangkan pada kontrol, koloni Vibrio hijau berpendar tidak
ditemukan.
20
4.08
5.78 5.83 6.11
6.84 6.73 4.08 5.54 6.16 6.48 7.12 7.15 4.08 4.74 5.42 6.48 6.36 6.08 0.00 1.00 2.00 3.00 4.00 5.00 6.00 7.00 8.00
0 2 4 6 8 10
Waktu Pengamatan (Hari)
J u m la h B a k te ri ( L o g c fu /u d a n g )
V. harveyi (7 Log cfu/ml) IMNV + V. harveyi (7 Log cfu/ml) Kontrol
4.90 6.22 6.48 6.72 6.49 6.80 4.90 6.48 6.52
7.23 7.16 7.22
4.90 6.48 6.62 6.86 6.36 6.99 0.00 1.00 2.00 3.00 4.00 5.00 6.00 7.00 8.00
0 2 4 6 8 10
Waktu Pengamatan (Hari)
Ju m lah B akt er i ( L o g cf u /m l)
V. harveyi (7 Log cfu/ml) IMNV + V. harveyi (7 Log cfu/ml) Kontrol
Selain terhadap bakteri Vibrio hijau berpendar, penghitungan juga
dilakukan terhadap total bakteri Vibrio di tubuh udang dan air pemeliharaan. Pada
perlakuan infeksi tunggal V. harveyi 107
Pada perhitungan total bakteri Vibrio di air pemeliharaan, bakteri Vibrio
selalu ditemukan pada setiap pengambilan sampel di ke-3 perlakuan. Berdasarkan 5 kali pengambilan sampel (hari ke-2, 4, 6, 8 dan 10 pasca infeksi) terjadi kecenderungan peningkatan total Vibrio selama pengamatan (Gambar 10).
Gambar 10. Jumlah total bakteri Vibrio di air pemeliharaan.
cfu/ml maupun ko-infeksi, bakteri Vibrio
selalu ditemukan pada setiap pengambilan sampel. Pada kedua perlakuan tersebut densitas terendah Vibrio diperoleh pada pengamatan hari ke-2 dan tertinggi pada
hari ke-8 pasca infeksi (Gambar 9). Sedangkan pada kontrol, densitas Vibrio
[image:36.595.95.518.31.842.2]terendah pada pengamatan hari ke-2 dan tertinggi pada hari ke-6 pasca infeksi.
Analisis statistik dengan uji T dilakukan untuk membandingkan jumlah bakteri Vibrio yang ditemukan di tubuh udang pada hari ke-10 pasca infeksi. Pada
perlakuan infeksi tunggal Vibrio harveyi jumlah Vibrio hijau berpendar yang
diisolasi pada hari ke-10 pasca infeksi yaitu 2x105 ± 1x105 cfu/ml. Nilai tersebut
berbeda signifikan (P<0.05) jika dibandingkan dengan jumlah Vibrio hijau
berpendar di tubuh udang pada perlakuan ko-infeksi yaitu sebesar 108x105 ± 27,06x105 cfu/ml (Tabel 5). Perbedaan sangat signifikan diperoleh pada analisis jumlah total bakteri Vibrio yang diisolasi pada perlakuan infeksi tunggal dan
ko-infeksi (P<0.01). Pada infeksi tunggal diperoleh densitas total Vibrio 53,67x105 ±
6.81x105 cfu/ml sedangkan pada ko-infeksi 139,67x105 ± 5,69x105
Perlakuan
cfu/ml. Tabel 5. Jumlah bakteri Vibrio (rataan±SD) pada hari ke-10 pasca infeksi.
Vibrio Hijau Berpendar
(cfu/udang)*
Total Vibrio
(cfu/udang)** Infeksi tunggal V. harveyi 2x105 ± 1x105a 53,67x105 ± 6.81x105a
Ko-infeksi 108x105 ± 27,06x105 b 139,67x105 ± 5,69x105b
Keterangan: hp=hepatopankreas. )*=berbeda nyata antara 2 perlakuan (P<0.05). )**=berbeda nyata antara 2 perlakuan (P<0.01).
4.1.2.2 Perkembangan klinis penyakit IMN
Perkembangan klinis penyakit IMN diamati pada perlakuan infeksi tunggal IMNV, ko-infeksi IMNV dengan V. harveyi 107
Perlakuan
cfu/ml dan kontrol untuk mengetahui awal munculnya gejala klinis, mortalitas awal dan total mortalitas pada akhir pengamatan (Tabel 6).
Tabel 6. Observasi gejala klinis dan mortalitas udang uji. Gejala Klinis # (Hari) Mortalitas (Hari) Mortalitas kumulatif (%) Konfirmasi PCR Hari ke-2 Hari ke-10
IMNV 6 10 13.33 2 sampel:
semua (-) (+) dan (-) 2 sampel:
Ko-infeksi 6 4)*
10)**
40 2 sampel:
semua (-) semua (+) 2 sampel:
Kontrol Tidak ada Tidak ada 0 1 sampel:
(-) 1 sampel: (-) Keterangan: )* mortalitas akibat infeksi V. harveyi; )**kematian awal akibat infeksi virus IMNV;
)# nekrosis/ lebam putih pada otot
22
lebam pada jaringan otot pertama kali terlihat pada hari ke-6 pasca infeksi. Namun untuk perlakuan kontrol, tidak ditemukan adanya gejala klinis selama dilakukannya pengamatan.
Mortalitas yang diamati adalah mortalitas awal dan mortalitas kumulatif setelah 14 hari pengamatan. Mortalitas awal perlakuan infeksi tunggal IMNV didapat pada hari ke-10 pasca infeksi dan mortalitas kumulatif sebesar 13.33 %. Sedangkan pada perlakuan ko-infeksi IMNV dan V. harveyi 107 cfu/ml mortalitas
dengan gejala klinis penyakit IMN diperoleh pada hari ke-10 pasca infeksi. Sebelumnya pada perlakuan ko-infeksi ditemukan juga mortalitas pada hari ke-4 pasca infeksi, namun mortalitas tersebut belum ditemukan gejala klinis penyakit IMN sehingga diduga kematian udang lebih disebabkan oleh infeksi V. harveyi.
Mortalitas kumulatif (hari ke-14 pasca infeksi) pada perlakuan ko-infeksi adalah 40 %. Pada perlakuan kontrol tidak ditemukan mortalitas maupun gejala klinis penyakit IMN pada udang uji. Pengamatan akhir perlakuan kontrol di hari ke-14, menunjukkan nilai mortalitas kumulatif sebesar 0 %.
Konfirmasi keberadaan virus IMNV di tubuh udang uji dilakukan dengan mengirimkan sampel ke laboratorium PCR. Pengujian PCR dilakukan pada 3 perlakuan yaitu infeksi tunggal IMNV, ko-infeksi IMNV dengan Vibrio harveyi
107 cfu/ml dan kontrol. Pengujian dilakukan pada pengamatan hari ke-2 dan 10
pasca infeksi. Hasil uji PCR menggunakan kit komersial Nugen-IMNV menunjukkan bahwa pada sampel hari ke-2 setelah infeksi, ke-3 perlakuan menunjukkan IMNV negatif (Tabel 6 dan Gambar 11). Berarti udang uji tidak atau belum terinfeksi oleh virus IMNV atau terinfeksi namun densitas virus masih rendah sehingga tidak bisa dideteksi oleh kit PCR Nugen-IMNV. Pengujian yang dilakukan pada hari ke-10 pasca infeksi, perlakuan infeksi tunggal menunjukkan hasil 1 sampel positif terinfeksi IMNV dan 1 sampel lainnya negatif. Perlakuan ko-infeksi IMNV dan V. harveyi 107
Observasi perkembangan gejala klinis dilakukan setiap 2 hari setelah infeksi terhadap parameter seperti gejala klinis visual lebam putih atau nekrosis,
histopatologi organ limfoid dan jaringan otot, serta gejala-gejala klinis lain yang diperoleh selama observasi (Tabel 7).
Keterangan: Sampel hari ke-2 (A) dan 10 (B) pasca infeksi. Marker (M), kontrol positif (C+), kontrol negatif (C-), perlakuan infeksi tunggal IMNV (1), perlakuan ko-infeksi IMNV dan V. harveyi 107
Seperti disebutkan pada Tabel 6, gejala klinis awal berupa munculnya nekrosis dengan bentuk visual berwarna putih (tidak transparan) pada otot muncul pertama kali pada hari ke-6 pasca infeksi. Gejala klinis tersebut muncul bersamaan baik pada perlakuan infeksi tunggal IMNV maupun ko-infeksi IMNV dan V. harveyi. Gejala klinis tersebut termasuk level 2 berdasarkan Costa et al.
(2009), yaitu terdapat sedikit nekrosis pada abdomen udang. Pada ke-2 perlakuan sampai hari ke-10 setelah infeksi IMNV gejala klinis visual tersebut tetap pada level 2. Namun pada hari ke-12 dan 14 pasca infeksi, pada ko-infeksi ditemukan udang pada level 3 yaitu hampir seluruh otot mengalami nekrosis (Gambar 12).
[image:39.595.111.494.116.483.2]cfu/ml (2) dan kontrol (3). Adanya pita pada 314 bp menunjukkan sampel positif terinfeksi IMNV.
Gambar 11. Hasil pengujian PCR udang uji menggunakan kit PCR Nugen-IMNV.
M C- C+ 1 1 2 2 3
527 bp 314 bp
1250 bp
700 bp
400 bp 300 bp
527 bp 314 bp
M C- C+ 1 1 2 2 3 1250 bp
700 bp 400 bp 300 bp
A
24
Tabel 7. Perkembangan gejala klinis luar (visual) dan histopatologi.
No Gejala Klinis Infeksi Tunggal IMNV (Hari) Ko-infeksi IMNV dan V. harveyi (Hari)
2 4 6 8 10 12 14 2 4 6 8 10 12 14
1 Gejala klinis luar (visual) - - ++ ++ ++ ++ +++ - - ++ ++ ++ +++ +++
2 Histopatologi otot n n n n BI NA NA n n n BI BI NA NA
3 Gejala klinis organ limfoid (visual)
- ukuran n n n n n n n n n n n n n n
- warna n n n n n Mrh Mrh n n n n n n Mrh
4 Histologi organ limfoid n n n Ab Ab NA NA n n n Ab Ab NA NA
5 Pengamatan visual organ lain (usus) n n n n n n n n n n n n n Ab Keterangan: ++ (sedikit nekrosis/ lebam putih pada otot); +++ (nekrosis/ lebam putih tampak jelas di otot udang); BI (badan inklusi); Mrh (merah); Ab (abnormal); n
(normal); NA (not available/ tidak diamati).
Keterangan: Sampel udang infeksi tunggal (A); sampel udang ko-infeksi (B); dan udang normal (C). Gambar 12. Sampel udang pada hari ke-14 dengan gejala klinis nekrosis level 3.
B
[image:40.842.132.680.353.472.2]Pada pengamatan gejala klinis berupa abnormalitas secara visual diperoleh juga abnormalitas pada organ limfoid dan organ usus (Tabel 7 dan Gambar 13). Abnormalitas pada organ limfoid berupa perbedaan warna visual organ limfoid dengan udang normal. Organ limfoid tersebut berwarna kemerahan dan terjadi pada kedua perlakuan. Abnormalitas juga terjadi pada organ usus namun hanya ditemukan pada ko-infeksi. Masing-masing abnormalitas tersebut tidak ditemukan di awal pengamatan setelah infeksi. Abnormalitas warna organ limfoid dan usus ditemukan pada pengamatan hari ke-12 dan 14 pasca infeksi.
Keterangan: Warna organ limfoid pada udang normal (A); warna organ limfoid pada udang perlakuan infeksi tunggal IMNV (B); abnormalitas bentuk usus dan warna organ limfoid udang
[image:41.595.111.489.104.687.2]perlakuan ko-infeksi (C). Tanda panah menunjukkan organ limfoid dan usus. Gambar 13. Abnormalitas organ limfoid dan usus dengan observasi visual.
A B
26
Keterangan: Infeksi tunggal IMNV (A); ko-infeksi (B); dan kontrol (C). Tanda panah menunjukkan badan inklusi. (Skala bar: 50 µm).
Gambar 14. Histopatologi jaringan otot udang uji.
A
28
[image:44.595.121.448.89.737.2]Keterangan: Infeksi tunggal IMNV (A); ko-infeksi (B); dan kontrol (C). (Skala bar: 50 µm). Gambar 15. Histopatologi organ limfoid udang uji.
A
4.2 Pembahasan
Penyakit IMN saat ini masih memerlukan penelitian yang lebih mendalam. Beberapa penelitian penyakit IMN yang telah dilakukan umumnya mengenai biomolekuler virus IMNV (Tang et al. 2005; Poulos et al. 2006; Andrade et al.
2007; Andrade et al. 2008; Tang et al. 2008). Penelitian juga dilakukan untuk
mengkonfirmasi virus IMNV di wilayah yang terkena wabah seperti di Brazil (Pinheiro et al. 2007; Costa et al. 2009) dan Indonesia (Senapin et al. 2007).
Berdasarkan hasil penelitian (Gambar 6), infeksi tunggal bakteri V. harveyi dengan dosis 106 cfu/ml dan 107 cfu/ml menggunakan metode
perendaman (imersi) tidak menyebabkan udang uji mengalami kematian (mortalitas). Kematian dapat terjadi pada dosis infeksi tunggal 108 cfu/ml yaitu
pada saat pengamatan hari ke-6. Hasil berbeda diperoleh Phuoc et al. (2009), yang
melaporkan bahwa infeksi tunggal V. campbellii dengan perendaman pada
berbagai dosis (106, 107 dan 108
Ko-infeksi penyakit virus dan bakteri pada udang juga belum banyak dilaporkan, terutama virus IMNV. Penelitian ko-infeksi virus-bakteri yang telah dilaporkan yaitu WSSV-bakteri Vibrio di tambak udang (Manilal et al. 2010) dan
WSSV-bakteri Vibrio (V. campbelli dan V. harveyi) skala eksperimen (Phuoc et
cfu/ml) pada 6 hari pengamatan setelah dilakukan infeksi tidak menyebabkan mortalitas. Melalui hasil tersebut, Phuoc et al. (2009)
menduga bahwa dosis-dosis V. campbelli tersebut tidak cukup untuk menyerang
udang vaname hingga menyebabkan wabah atau kematian. Jika mengandaikan dengan kondisi alamiah di tambak udang, maka wabah penyakit bakterial dapat terjadi akibat dari interaksi yang komplek (Phuoc et al. 2009).
Namun perbedaan hasil tersebut diduga disebabkan oleh perbedaan padat tebar per akuarium atau wadah uji. Pada penelitian ini padat tebar udang per akuarium adalah 8 ekor (bobot rata-rata= 2.71±0.395 g) per 10 liter air laut, sedangkan Phuoc et al. (2009) menggunakan 6 ekor udang (bobot rata-rata=
2.41±0.65 g) per 10 liter air laut. Seperti diketahui, bahwa disamping status inang (kesehatan atau genetik), kejadian penyakit ditentukan juga oleh beberapa faktor lain seperti: stressor fisik dan patogen lain yang membuat portal entry. Bentuk stressor fisik antara lain fluktuasi di air (oksigen, salinitas, temperatur) dan padat
30
al. 2008; Phuoc et al. 2009). Informasi lain mengenai ko-infeksi IPV (infectious pancreaticnecrosis) - Vibrio pada ikan kerapu (Lee et al. 1999). Umumnya
ko-infeksi pada penelitian-penelitian tersebut menyebabkan peningkatan mortalitas terhadap udang.
Pada penelitian ini yang menggunakan ko-infeksi virus IMNV dan bakteri
V. harveyi, udang uji dengan perlakuan ko-infeksi mengalami mortalitas lebih
cepat jika dibandingkan dengan kontrol. Beberapa dosis V. harveyi yang tidak
menyebabkan kematian pada infeksi tunggal bahkan menghasilkan mortalitas yang lebih tinggi dibandingkan dengan infeksi tunggal IMNV (gambar 6). Costa
et al. (2009) melaporkan dampak infeksi IMNV terhadap nilai kekebalan tubuh
udang vaname. Seperti yang terjadi pada infeksi WSSV, virus IMNV juga menyebabkan penurunan total hemocyte. Penurunan total hemocyte akibat infeksi
IMNV sebesar 30%, bahkan aktivitas antimikrobial pada hemocyte tidak mampu
meningkat ketika ada infeksi bakteri Vibrio harveyi (Costa et al. 2009).
Dilaporkan juga bahwa, pada infeksi virus IMNV dapat menyebabkan peningkatan persentase apoptosis (Costa et al. 2009). Hal ini diduga bahwa
fenomena meningkatnya mortalitas dan percepatan kejadian mortalitas awal udang uji pada penelitian ini terjadi karena penurunan aktivitas antimikrobial dan level hemocyte serta aktivitas kekebalan tubuh udang yang lain. Penurunan
aktivitas kekebalan tubuh tersebut dimanfaatkan oleh V. harveyi ketika
menginfeksi udang. Sehingga pada penelitian ini ditemukan kematian udang sebelum munculnya gejala klinis penyakit IMN pada perlakuan ko-infeksi (Tabel 6). Faktanya, pada kondisi infeksi tunggal V. harveyi 107 cfu/ml tidak ditemukan
mortalitas pada udang uji. Sebagaimana dilaporkan, bahwa udang memiliki kemampuan untuk mengeliminasi jumlah bakteri Vibrio dari dalam tubuhnya
dengan cepat. Bahkan hanya dalam 2 jam pasca injeksi bakteri Vibrio, udang
dapat mengeliminasi Vibrio dari haemolymp hingga mencapai 97% (Van de Braak et al. 2002). Diduga hal ini yang menyebabkan infeksi tunggal V. harveyi pada
penelitian ini memerlukan dosis yang tinggi untuk menyebabkan mortalitas udang uji yaitu 108
Penghitungan Vibrio di tubuh udang dilakukan untuk mengetahui
pada bakteri Vibrio hijau berpendar yang menjadi ciri V. harveyi yang digunakan. V. harveyi pada infeksi tunggal pada penelitian ini ditemukan mulai hari ke-8
pasca infeksi (Gambar 7). Sedangkan bakteri Vibrio hijau berpendar pada
perlakuan ko-infeksi virus IMNV dan V. harveyi 107
Jumlah total Vibrio meningkat secara signifikan pada perlakuan ko-infeksi
dalam penelitian ini. Menurut Rodriguez et al. (2010) ada kemungkinan infeksi
lain (terutama dari golongan virus seperti WSSV, IHHNV dan TSV) yang menyebabkan peningkatan densitas Vibrio di tubuh udang pada kasus wabah
vibriosis di tambak dibandingkan dengan densitas Vibrio pada udang normal. Saat
ini di lapangan belum dapat dikonfirmasi bahwa bakteri Vibrio lain termasuk
koloni berwarna kuning dapat menjadi virulen pada kondisi wabah penyakit IMN. Namun pada saat terjadi wabah penyakit WSS, telah dikonfirmasi bahwa terdapat
V. alginolyticus yang virulen dari tambak yang terkena wabah penyakit WSS
(Manilal et al. 2010). Sedangkan pada skala penelitian laboratorium juga telah
dilaporkan oleh Phuoc et al. (2009). Dalam penelitiannya Rodriguez et al. (2010)
melaporkan bahwa rata-rata jumlah bakteri Vibrio yang diisolasi dari
cfu/ml selalu ditemukan sejak awal pengambilan sampel (hari ke-2) hingga hari ke-10 pasca infeksi. Pada hari ke-10 pasca infeksi densitas Vibrio hijau berbeda signifikan antara perlakuan
infeksi tunggal V. harveyi dan ko-infeksi (P<0.05). Selain itu perbedaan terlihat
juga pada jumlah total Vibrio di tubuh udang pada kedua perlakuan (P<0.01).
Percepatan peningkatan jumlah Vibrio di tubuh udang menyebabkan percepatan
kematian udang uji.
Dengan demikian mekanisme yang terjadi dalam penelitian ini adalah bakteri Vibrio bertindak sebagai patogen sekunder yang diduga menyebabkan
percepatan dan peningkatan mortalitas pada udang yang terinfeksi virus IMNV. Sedangkan virus IMNV bertindak sebagai agen penyakit primer (IMNV sebagai infeksi primer). Hal ini terkait dengan karakteristik bakteri V. harveyi yang
merupakan mikroflora alam di perairan laut atau pantai (Chrisolite et al. 2008)
32
hepatopankreas udang vaname pada saat wabah vibriosis adalah 105 cfu/g. Pada udang sehat dilaporkan bahwa rata-rata Vibrio di hepatopankreas udang vaname
1.3x104 cfu/g (Gomes-Gil et al. 1998). Dalam penelitian ini, mortalitas awal
perlakuan ko-infeksi terjadi pada hari ke-4 tanpa adanya gejala klinis luar penyakit IMN. Pada hari tersebut jumlah bakteri Vibrio yang diisolasi adalah
1.45x106 cfu/hp, densitas tersebut sangat berbeda jika dibandingkan dengan
isolasi dari perlakuan kontrol pada hari yang sama (2.65x105 cfu/hp) maupun pada
udang sehat yang dilaporkan oleh Gomez-Gil et al. (1998).
Pada penelitian ini, tidak ada perbedaan awal ditemukannya gejala klinis nekrosis antara perlakuan infeksi tunggal IMNV dan ko-infeksi. Gejala awal ditemukan pada hari ke-6, sedangkan mortalitas awal diperoleh pada hari ke-10. Mortalitas awal ke-2 perlakuan tersebut juga identik. Hasil penelitian lain yang dilakukan Tang et al. (2005) melaporkan bahwa udang vaname yang diinfeksi
oleh IMNV menampakkan gejala klinis pertama kali pada hari ke 6 setelah infeksi dan mengalami mortalitas pertama kali pada hari ke-13. Mortalitas total udang vaname pada pengujian tersebut 33.33%, mortalitas tersebut lebih tinggi dibandingkan infeksi tunggal IMNV penelitian ini yang hanya 13.33%. Namun pada perlakuan ko-infeksi mortalitas kumulatif pada hari ke-14 pasca infeksi bisa mencapai 40%, walaupun dosis V. harveyi yang diinfeksikan tidak menyebabkan
mortalitas pada infeksi tunggal. Penelitian lain menunjukkan, bahwa udang vaname mengalami mortalitas pertama kali pada hari ke-8, dan mortalitas mencapai 100 % pada hari ke-52 setelah infeksi (Andrade et al. 2007).
Untuk mengkonfirmasi bahwa udang perlakuan terinfeksi oleh virus IMNV, maka dilakukan pengujian PCR dengan menggunakan kit komersial (Nugen-IMNV). Pengujian PCR saat hari ke-2 pasca infeksi pada perlakuan infeksi IMNV dan ko-infeksi belum menunjukkan udang terinfeksi positif IMNV. Namun pada hari ke-10, sampel dapat dikonfirmasi positif IMNV. Coelho et al.
Perkembangan gejala klinis penyakit IMN juga diamati pada perlakuan infeksi tunggal IMNV dan ko-infeksi. Secara umum tidak ada perbedaan gejala klinis penyakit IMN yang diobservasi dari 2 perlakuan tersebut. Pada pengamatan visual diketahui, bahwa gejala klinis nekrosis muncul pertama kali pada hari ke-6 pada level nekrosis ringan, sedangkan pada hari ke-14 setelah infeksi mulai ditemukan udang dengan gejala nekrosis di seluruh otot abdomen (level moderat). Hasil ini identik dengan penelitian yang dilakukan oleh Tang et al. (2005). Pada
penelitian lain, gejala klinis nekrosis pertama kali dapat dilihat pada hari ke-3 setelah infeksi IMNV (Poulos et al. 2006).
Beberapa gejala abnormalitas yang diperoleh selama observasi 14 hari yaitu abnormalitas warna organ limfoid dan abnormalitas bentuk usus. Gejala tersebut belum dapat dikonfirmasi apakah disebabkan oleh IMNV atau oleh patogen lain. Namun sebagai gambaran bahwa organ limfoid merupakan organ prinsip sebagai sampel untuk pengujian molekuler pada infeksi kronis (OIE 2009). Berarti organ limfoid diduga merupakan organ target dari penyakit IMN.
Selain organ limfoid, otot merupakan jaringan yang umum digunakan sebagai sampel untuk pengujian skala sel maupun molekuler (Andrade et al.
2007). Hasil pengamatan histopatologi terhadap organ limfoid dan jaringan otot udang uji pada penelitian ini tidak menampakkan perbedaan pada perlakuan infeksi tunggal IMNV dan ko-infeksi. Pada pengamatan histologi, udang yang terserang infeksi IMNV sering menampakkan koagulasi/penggumpalan nekrosis pada jaringan otot namun tidak selalu (Andrade et al. 2008). Sampel yang
diperoleh dari hari ke-10 menampakkan adanya badan inklusi pada histologi jaringan otot. Selain itu terdapat juga penggumpalan jaringan otot seperti nekrosis (Gambar 14). Secara umum udang yang terinfeksi virus IMNV menunjukkan lesi pada otot skeletal, koagulasi nekrosis termasuk nekrosis multifocal, kongesti pada
hemocyte, inflamasi fibrocytic, fagositosis dan bodi inklusi sitoplasma serta
infiltrasi hemocyte (Tang et al. 2005; Poulos et al. 2006; Andrade et al. 2007;
Coelho et al. 2009).
34
inklusi virus dan degradulasi granul hemocyte. Akumulasi dari LOS dapat
dijadikan indikasi infeksi IMNV (Tang et al. 2005; Andrade et al. 2008).
V. KESIMPULAN DAN SARAN
5.1 Kesimpulan
Ko-infeksi IMNV dengan berbagai dosis Vibrio harveyi (106, 107 dan 108
cfu/ml) dapat mempercepat awal mortalitas dan meningkatkan mortalitas dibandingkan dengan infeksi tunggal IMNV. Infeksi V. harveyi 107 cfu/ml tidak
menyebabkan mortalitas, dan infeksi tunggal IMNV menyebabkan mortalitas diawali pada hari ke-10 pasca infeksi dengan kumulatif 13.33%. Sedangkan ko-infeksi virus IMNV dan V. harveyi 107 cfu/ml menyebabkan awal mortalitas
udang lebih cepat (hari ke-4 pasca infeksi) dengan kumulatif lebih tinggi yaitu 40%. Ko-infeksi juga mempercepat pertumbuhan Vibrio koloni berwarna hijau
berpendar di tubuh udang, dengan densitas mencapai 108x105 ± 27,06x105 cfu/ml pada hari ke-10 pasca infeksi.
Tidak ada perbedaan perkembangan gejala klinis visual maupun histopatologi antara infeksi tunggal IMNV dan ko-infeksi IMNV dengan V. harveyi. Infeksi IMNV menunjukkan beberapa gejala yang nampak yaitu nekrosis
(lebam putih), abnormalitas organ limfoid, terlihat badan inklusi pada sel otot, dan konfirmasi PCR di tubuh udang.
5.2 Saran
Perlu dilakukan penelitian lanjutan untuk mengetahui dampak penanggulangan penyakit IMN melalui pengendalian bakteri Vibrio, misalnya
penggunaan bakteri sebagai biokontrol Vibrio. Perlu juga dilakukan kuantifikasi
36
DAFTAR PUSTAKA
Alapide-Tendencia EV, Dureza LA. 1997. Isolation of Vibrio spp. from Penaeus monodon (Fabricius) with red disease syndrome. Aquaculture 154:107– 114.
Andrade TPD, Srisuvan T, Tang KFJ, Lightner DV. 2007. Real-time reverse transcription polymerase chain reaction assay using TaqMan probe for detection and quantification of Infectious myonecrosis virus (IMNV).
Aquaculture