PENENTUAN KANDUNGAN KARBOHIDRAT DAN PROTEIN
DARI UBI KAYU (
Manihot utilissima)
KUKUS SEBELUM
DAN SESUDAH DIFERMENTASI
SKRIPSI
NURUL FITRIANI
080802006
DEPARTEMEN KIMIA
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM
UNIVERSITAS SUMATERA UTARA
PENENTUAN KANDUNGAN KARBOHIDRAT DAN PROTEIN
DARI UBI KAYU (
Manihot utilissima)
KUKUS SEBELUM
DAN SESUDAH DIFERMENTASI
SKRIPSI
Diajukan untuk melengkapi tugas dan memenuhi syarat mencapai gelar sarjana Sains
NURUL FITRIANI
080802006
DEPARTEMEN KIMIA
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM
UNIVERSITAS SUMATERA UTARA
PERSETUJUAN
Judul : PENENTUAN KANDUNGAN KARBOHIDRAT
DAN PROTEIN DARI UBI KAYU (Manihot
Utilissima) KUKUS SEBELUM DAN SESUDAH
DIFERMENTASI
Kategori : SKRIPSI
Nama : NURUL FITRIANI
Nomor Induk Mahasiswa : 080802006
Program Studi : SARJANA (S1) KIMIA
Departemen : KIMIA
Fakultas : MATEMATIKA DAN ILMU PENGETAHUAN
ALAM (FMIPA) UNIVERSITAS SUMATERA UTARA
Disetujui di
Medan, Juli 2012
Komisi Pembimbing :
Pembimbing 2 Pembimbing 1
Prof. DR. Pina Barus, MS Drs.Ahmad Darwin Bangun,M.Sc
NIP. 194506041980021001 NIP. 19521116198003001
Diketahui/Disetujui oleh :
Departemen Kimia FMIPA USU Ketua,
PERNYATAAN
PENENTUAN KANDUNGAN KARBOHIDRAT DAN PROTEIN
DARI UBI KAYU (
Manihot utilissima)
KUKUS SEBELUM
DAN SESUDAH DIFERMENTASI
SKRIPSI
Saya mengakui bahwa skripsi ini adalah hasil karya saya sendiri, kecuali beberapa kutipan dan ringkasan yang masing-masing disebutkan sumbernya.
Medan, Juli 2012
PENGHARGAAN
Bismillahirrahmanirrahim,
Alhamdulillah, segala puji syukur selalu terucap kepada Allah SWT yang sampai detik ini
selalu melimpahkan rahmatNya kepada saya sehingga skripsi ini dapat saya selesaikan
sebagai salah satu persyaratan untuk meraih gelar Sarjana Sains jurusan Kimia pada
Fakultas Matematika dan Ilmu Pengetahuan Alam Universitas Sumatera Utara. Serta
shalawat dan salam saya sampaikan kepada Rasulullah, Muhammad SAW, semoga kelak
mendapat syafaat Beliau. Amin.
Saya menyampaikan penghargaan dan cinta kasih yang terdalam dan tulus kepada
Ibunda tercinta Nuriah, S. Pd, Ek, sumber semangat dan inspirasi luar biasa untuk saya
meraih impian dan Ayahanda tersayang Safrul Ruslizar (Alm), yang dengan kasih sayang
selalu memberikan yang terbaik untuk saya. Dan yang selalu saya rindukan, adik-adik
tercinta Nurhajryenni dan Very Munandar, semoga kita bisa meraih impian kedua orang
tua kita. Serta seluruh keluarga yang telah memberikan dukungan.
Dengan segala kerendahan hati, saya mengucapkan terima kasih kepada :
1. Drs. Ahmad Darwin Bangun, M. Sc selaku dosen pembimbing 1 dan Prof. DR. Pina
Barus, MS selaku dosen pembimbing 2 yang telah memberikan pengarahan dan
bimbingan hingga terselesaikannya skripsi ini.
2. DR. Rumondang Bulan Nst, MS dan Drs. Albert Pasaribu, M. Sc selaku Ketua dan
Sekretaris Departemen Kimia FMIPA USU.
3. Drs. Barita Lumban Tobing selaku dosen wali saya.
4. Bapak dan Ibu dosen yang telah memberikan ilmunya selama masa studi saya di
5. Kepala, staf, dan teman-teman asisten Laboratorium Kimia Dasar LIDA USU
Medan, Arif, Andre, Novi, Desy, Salmi, terima kasih untuk kesan indah bersama
kalian, bang Sony, bang Rivan, bang Hendi, Ilman, Irwan, Icha, Rina, Indah, Ayu,
Dwi, Eli, Meyrina, Nirmala, Nami, Zulfa, Yuni dan kak Ayu selaku Analis
Laboratorium yang telah memberikan saya fasilitas selama saya melakukan
penelitian.
6. Teman-teman seperjuangan di Departemen Kimia FMIPA USU, teristimewa untuk
stambuk 2008 terima kasih untuk kesan indah persahabatan dengan kalian.
7. Sahabat-sahabat saya, Wimpy, Novi, Emi, Wilda, Elisa, Kak Aida, Sumariah, Dara,
terima kasih untuk persahabatannya, sungguh bahagia bisa mengenal kalian. Dan Feri,
terima kasih untuk dukungan dan bantuannya.
8. Segala pihak yang telah membantu saya menyelesaikan skripsi ini.
Saya menyadari bahwa skripsi ini masih jauh dari sempurna, karena keterbatasan saya
baik dalam literatur maupun pengetahuan. Oleh karena itu, saya mengharapkan saran dan
ABSTRAK
Telah dilakukan penelitian tentang kandungan karbohidrat dan protein dari ubi kayu
(Manihot utilissima) kukus sebelum dan sesudah difermentasi. Sampel berupa ubi kayu yang diambil dari pajak sore Padang Bulan, Medan. Analisa kandungan karbohidrat
dilakukan dengan menghidrolisa sampel menggunakan HCl 3% kemudian menentukan
kadar glukosa menggunakan metode Luff Schoorl, glukosa yang diperoleh dikalikan
dengan faktor konversi 0,9 dan analisa kandungan protein ditentukan dengan metode
Kjeldahl. Dari hasil percobaan menunjukkan adanya pengaruh fermentasi terhadap
penurunan kandungan karbohidrat dan peningkatan kandungan protein dari ubi kayu.
Kandungan karbohidrat ubi kukus sebesar 32,71% setelah fermentasi menjadi 30,78%
DETERMINATION OF CARBOHYDRATES AND PROTEIN
CONTENT OF CASSAVA (
Manihot utilissima )
STEAMED BEFORE
AND AFTER FERMENTED
ABSTRACT
Determination on carbohydrate and protein content of Cassava (Manihot utilissima) steamed before and after fermented has been studied. Sample of Cassava was taken from
Pajak Sore Padang Bulan, Medan. Carbohydrate content analysis performed by hydrolysis
sample using HCl 3% then determining glucose levels in advance using the Luff Schoorl
method, glucose obtained multiplied by conversion factor of 0.9 and analysis of protein
content was determined by the Kjeldahl method. From the experimental results show the
influence of fermentation of reduction content of Cassava of carbohydrate and increasing
protein. Steamed Cassava carbohydrate content of 32.71% to 30.78% after fermentation
DAFTAR ISI
Halaman
Persetujuan i
Pernyataan ii
Penghargaan iii
Abstrak v
Abstract vi
Daftar Isi vii
Daftar Lampiran ix
Bab 1 Pendahuluan 1
1.1 Latar Belakang 1
1.2 Permasalahan 2
1.3 Pembatasan Masalah 2 1.4 Tujuan Penelitian 3 1.5 Manfaat Penelitian 3 1.6 Lokasi Penelitian 3 1.7 Metodologi Penelitian 3
Bab 2 Tinjauan Pustaka 4
2.1 Tanaman Ubi Kayu 4
2.2 Analisa Titrimetri 5 2.2.1 Larutan Baku ( standar ) 6
2.3 Karbohidrat 6
2.3.1 Penentuan Karbohidrat 9 2.3.1.1 Cara Luff Schoorl 9 2.3.1.2 Prinsip Penentuan Kandungan Karbohidrat 10
2.4 Protein 10
2.4.1 Sifat-sifat Fisikokimia asam amino dan protein 11 2.4.2 Analisa Kandungan Protein 11 2.4.3 Jumlah Protein Total 12 2.4.4 Prinsip Penentuan Kandungan Protein 13 2.4.5 Tahap Destruksi 14 2.4.6 Tahap Destilasi 14
2.4.7 Tahap Titrasi 14
2.5 Tape 15
2.6 Fermentasi 15
Bab 3 Metodologi Penelitian 18
3.3.2 Fermentasi Ubi Kayu 23 3.3.2.1 Preparasi sampel sebelum difermentasi 23 3.3.2.2 Preparasi sampel fermentasi 23 3.3.3 Perlakuan Sampel 24 3.3.3.1 Penentuan Kandungan Karbohidrat 24 3.3.3.2 Penentuan Kandungan Protein 24
3.4 Bagan Penelitian 26
3.4.1 Penentuan Kandungan Karbohidrat 26 3.4.2 Penentuan Kandungan Protein 27
Bab 4 Hasil dan Pembahasan 28
4.1 Hasil Penelitian 28
4.1.1 Data Penelitian 28
4.1.2 Pengolahan Data 29
4.2 Pembahasan 40
Bab 5 Kesimpulan dan Saran 41
5.1 Kesimpulan 41
5.2 Saran 41
Daftar Pustaka 42
DAFTAR LAMPIRAN
Halaman
ABSTRAK
Telah dilakukan penelitian tentang kandungan karbohidrat dan protein dari ubi kayu
(Manihot utilissima) kukus sebelum dan sesudah difermentasi. Sampel berupa ubi kayu yang diambil dari pajak sore Padang Bulan, Medan. Analisa kandungan karbohidrat
dilakukan dengan menghidrolisa sampel menggunakan HCl 3% kemudian menentukan
kadar glukosa menggunakan metode Luff Schoorl, glukosa yang diperoleh dikalikan
dengan faktor konversi 0,9 dan analisa kandungan protein ditentukan dengan metode
Kjeldahl. Dari hasil percobaan menunjukkan adanya pengaruh fermentasi terhadap
penurunan kandungan karbohidrat dan peningkatan kandungan protein dari ubi kayu.
Kandungan karbohidrat ubi kukus sebesar 32,71% setelah fermentasi menjadi 30,78%
DETERMINATION OF CARBOHYDRATES AND PROTEIN
CONTENT OF CASSAVA (
Manihot utilissima )
STEAMED BEFORE
AND AFTER FERMENTED
ABSTRACT
Determination on carbohydrate and protein content of Cassava (Manihot utilissima) steamed before and after fermented has been studied. Sample of Cassava was taken from
Pajak Sore Padang Bulan, Medan. Carbohydrate content analysis performed by hydrolysis
sample using HCl 3% then determining glucose levels in advance using the Luff Schoorl
method, glucose obtained multiplied by conversion factor of 0.9 and analysis of protein
content was determined by the Kjeldahl method. From the experimental results show the
influence of fermentation of reduction content of Cassava of carbohydrate and increasing
protein. Steamed Cassava carbohydrate content of 32.71% to 30.78% after fermentation
BAB 1
PENDAHULUAN
1.1Latar Belakang
Singkong/ubi kayu merupakan komoditas hasil pertanian yang banyak ditanam di
Indonesia. Di samping sebagai bahan makanan, ubi kayu juga dapat digunakan sebagai
bahan baku industri dan pakan ternak.
Produksi singkong dunia diperkirakan mencapai 184 juta ton pada tahun 2002.
Sebagian besar produksi dihasilkan di Afrika 99,1 juta ton dan 33,2 juta ton di
Ubinya mengandung pati 25-35%, serta protein 1,2
%,Ubi kayu merupakan sumber energi yang lebih tinggi dibanding padi, jagung, ubi jalar,
dan sorgum.
Singkong/ubi kayu dapat disajikan dalam bentuk tape melalui proses fermentasi,
dimana pada proses tersebut terjadi perubahan bahan-bahan organik dari
senyawa-senyawa komplek menjadi senyawa-senyawa - senyawa-senyawa yang lebih sederhana oleh kerja enzim
Tape yang baik dan bermutu apabila harum, enak, legit, dan tidak menyengat
karena terlalu tinggi kadar alkoholnya (Tarigan, 1998).
Fermentasi merupakan disimilasi anaerobik senyawa-senyawa organik yang
disebabkan oleh aktivitas mikroorganisme atau ekstrak dari sel-sel tersebut. Disimilasi
tingkat energinya lebih rendah sehingga energi dibebaskan dalam proses ini
(Gumbiro, 1987).
Fermentasi adalah suatu oksidasi karbohidrat anaerob dan aerob sebagian dan
merupakan suatu kegiatan penguraian bahan-bahan karbohidrat (Desrosier, 1988).
Fermentasi ubi kayu dapat meningkatkan kandungan protein. Produk fermentasi
selanjutnya dapat digunakan sebagai bahan atau suplemen produk pangan atau pakan
Dari latar belakang diatas, maka Penulis tertarik untuk meneliti kandungan
karbohidrat dan protein pada ubi kayu sebelum dan sesudah difermentasi sehingga
diperoleh gambaran tentang jumlah kandungan karbohidrat dan protein yang terkandung
pada ubi kayu sebelum dan sesudah difermentasi.
1.2Permasalahan
Apakah ada perbedaan kandungan karbohidrat dan protein pada ubi kayu kukus sebelum
dan sesudah difermentasi.
1.3Pembatasan Masalah
Dalam penelitian ini permasalahan dibatasi pada penentuan karbohidrat dan protein pada
1.4Tujuan Penelitian
Untuk mengetahui kandungan karbohidrat dan protein pada ubi kayu kukus sebelum dan
sesudah difermentasi.
1.5Manfaat Penelitian
1. Dari hasil penelitian ini diharapkan dapat memberikan informasi kepada masyarakat
tentang kandungan karbohidrat dan protein pada ubi kayu kukus sebelum dan
sesudah difermentasi.
2. Hasil fermentasi ( tape ubi kayu ) dapat dimanfaatkan sebagai bahan tambahan pakan
ternak, apabila tape tersebut tidak habis terjual.
1.6Lokasi Penelitian
Penelitian ini dilakukan di Laboratorium Kimia Dasar LIDA Universitas Sumatera Utara
dan dilakukan di Laboratorium Biokimia Fakultas Matematika dan Ilmu Pengetahuan
Alam ( FMIPA ) Universitas Sumatera Utara.
1.7Metodologi Penelitian
1. Penelitian ini merupakan penelitian laboratorium
2. Sampel yang digunakan adalah ubi kayu
3. Pengambilan sampel dilakukan secara acak di sekitar Pajak sore Padang Bulan
4. Sampel terlebih dahulu dihaluskan dan dihidrolisa dengan HCl 3%
5. Penentuan kandungan karbohidrat dilakukan dengan menentukan kadar glukosa
terlebih dahulu dengan menggunakan metode Luff Schoorl kemudian dikalikan
dengan faktor konversi 0,9
6. Pada penentuan kandungan protein sampel didestruksi dengan H2SO
BAB 2
TINJAUAN PUSTAKA
2.1 Tanaman Ubi Kayu
Ubi kayu dikenal dengan nama Cassava (Inggris), Kasapen, sampeu, kowi dangdeur
(Sunda); Ubi kayu, singkong, ketela pohon (Indonesia); Pohon, bodin, ketela bodin, tela
jendral, tela kaspo (Jawa).
Tanaman ubi kayu menurut Steenis (1998) merupakan tanaman yang memiliki
klasifikasi sebagai berikut :
Divisio : Spermatophyta
Sub Divisio : Angiospermae
Classis : Dicotyledoneae
Ordo : Euphorbiales
Familia : Euphorbiaceae
Genus : Manihot
Species : Manihot utilissima
Ubi kayu merupakan batang berkayu yang tumbuh tegak, beruas-ruas,
semacam gabus yang berwarna putih. Daunnya serupa tangan manusia dengan jari-jari
( helaian daun terbelah dalam-dalam ). Umbi akar berukuran besar, memanjang dengan
kulit luar berwarna coklat suram
2.2 Analisis Titrimetri
Analisis titrimetri mengacu pada analisis kimia kuantitatif yang dilakukan dengan
menetapkan volume suatu larutan yang konsentrasinya diketahui dengan tepat. Larutan
dengan kekuatan ( konsentrasi ) yang diketahui dengan tepat itu disebut larutan standar.
Larutan standar biasanya ditambahkan dari dalam sebuat buret. Proses penambahan
larutan standar sampai reaksi tepat lengkap disebut titrasi (Vogel, 1994).
Semua metode volumetri syaratnya sama, yaitu reaksi analit dengan pentitrasi
harus diketahui, berlangsung cepat, stoikiometri, dan ada cara untuk menunjukkan saat
sudah terjadi reaksi kuantitatif yang disebut titik akhir titrasi (Satiadarma, K, 2004).
Metode volumetri/titrimetri secara garis besar dapat diklasifikasikan dalam
empat kategori sebagai berikut :
a. Titrasi asam basa yang meliputi reaksi asam dan basa baik kuat ataupun lemah.
b. Titrasi redoks adalah titrasi yang meliputi hampir semua reaksi oksidasi reduksi.
c. Titrasi pengendapan adalah titrasi yang meliputi pembentukan endapan, seperti
titrasi Ag atau Zn dengan K4Fe(CN)6
d. Titrasi kompleksometri sebagian besar meliputi titrasi EDTA seperti titrasi
spesifik dan juga dapat digunakan untuk melihat perbedaan pH pada
pengkompleksan (Khopkar, S. M, 2008).
dengan indikator pengadsorpsi.
Titrasi asidimetri-alkalimetri, yaitu titrasi yang menyangkut asam atau basa.
Reaksi-reaksi yang terjadi dalam titrasi ini adalah :
- Asam dengan basa (reaksi penetralan), agar kuantitatif, maka asam atau basa yang
- Asam dengan garam (reaksi pembentukan asam lemah), agar kuantitatif, asam
harus kuat dan garam itu harus terbentuk dari asam lemah sekali
Contohnya : HCl + Na2CO3 NaHCO3
2HCl + Na
+ NaCl
2CO3 H2O + CO2
HCl + NH
+ 2NaCl
4BO2 HBO2 + NH4 - Basa dengan garam, agar kuantitatif, basa harus kuat dan garam harus terbentuk
dari basa lemah sekali, jadi berdasar pembentukan basa lemah tersebut
(Harjadi, W, 1990).
Cl
1.2.1 larutan baku ( standar )
Semua perhitungan dalam titrimetri didasarkan pada konsentrasi titran sehingga
konsentrasi titran harus dibuat secara teliti. Titran semacam ini disebut dengan larutan
baku ( standar ). Konsetrasi larutan dapat dinyatakan dengan normalitas, molaritas, atau
bobot per volume.
Larutan standar ada dua macam yaitu larutan baku primer dan larutan baku
sekunder. Larutan baku primer mempunyai kemurnian yang tinggi. Larutan baku
sekunder harus dibakukan dengan larutan baku primer. Suatu proses yang mana larutan
baku sekunder dibakukan dengan larutan baku primer disebut dengan standarisasi
(Rohman, A, 2007).
2.3 Karbohidrat
Karbohidrat banyak terdapat di alam, diantaranya dalam bentuk pati, kapas, gula pasir,
dan kayu. Karbohidrat adalah polihidroksi dari aldehida atau keton. Karbohidrat yang
sederhana yang tidak terikat pada karbohidrat lain dinamakan gula sederhana atau
Karbohidrat merupakan sumber kalori utama bagi hampir seluruh penduduk
dunia, khususnya bagi penduduk negara yang sedang berkembang. Walaupun jumlah
kalori yang dapat dihasilkan oleh 1 gram karbohidrat hanya 4 Kal (kkal), karbohidrat
merupakan sumber kalori yang murah. Selain itu beberapa golongan karbohidrat
menghasilkan serat-serat yang berguna bagi pencernaan.
Karbohidrat juga mempunyai peranan penting dalam menentukan karakteristik
bahan makanan, misalnya rasa, warna, tekstur, dan lain-lain. Sedangkan dalam tubuh,
karbohidrat berguna untuk mencegah timbulnya ketosis, pemecahan protein tubuh yang
berlebihan, kehilangan mineral. Sebagian besar karbohidrat didapatkan dari bahan
makanan yang dimakan sehari-hari, terutama bahan makanan yang berasal dari
tumbuh-tumbuhan (Winarno, F. G, 1992).
Karbohidrat secara umum terdapat dalam jaringan makhluk hidup dan sangat
penting dalam metabolisme. Karbohidrat memiliki formula umum CX(H2O)y
a. Monosakarida : misalnya glukosa
dan dapat
diklasifikasikan sebagai berikut :
b. Di – dan tri- sakarida : misalnya maltosa
c. Polisakarida : misalnya pati
Semua mono- ,di- dan tri- sakarida larut dalam air (Allen, S. E, 1974).
Monosakarida adalah karbohidrat yang tidak dapat dihidrolisis menjadi
karbohidrat yang lebih sederhana. Disakarida adalah produk kondensasi dua unit
monosakarida, contohnya maltosa dan sukrosa. Oligosakarida adalah produk kondensasi
tiga sampai sepuluh monosakarida, sebagian besar oligosakarida tidak dicerna oleh enzim
dalam tubuh manusia. Polisakarida adalah produk kondensasi lebih dari sepuluh unit
monosakarida, contohnya pati dan dekstrin yang mungkin merupakan polimer linear atau
Gambar : Glukosa
Pati adalah bentuk polimer simpanan glukosa pada tumbuhan dan merupakan sumber
energi utama dalam makanan (Murray, R, 2006).
Untuk penentuan kadar pati dalam suatu bahan dapat dikerjakan dengan
menghidrolisa pati dengan asam atau enzim sehingga diperoleh gula reduksi.
C6H10O5 + H2O C6H12O
Pati glukosa 6
BM = 162 BM = 180
Setelah diketahui jumlah gula reduksi hasil hidrolisa pati tersebut maka dapat dihitung
jumlah pati yaitu dengan mengalikan dengan suatu faktor konversi sebesar 0,90. Faktor
konversi ini diperoleh dari perbandingan berat molekul pati dengan jumlah berat molekul
gula reduksi yang dihasilkan.
Faktor konversi = �������������������
=
162
180
=
0,90 (Sudarmadji, S, 1987).Jika pati dipanaskan dengan asam akan terurai menjadi molekul-molekul yang
lebih kecil secara berurutan, dan hasil akhirnya adalah glukosa. Molekul-molekul pati
mula-mula pecah menjadi unit-unit rantai glukosa yang lebih pendek yang disebut
dextrin. Dextrin ini dipecah lebih jauh menjadi maltosa (dua unit glukosa) dan akhirnya
Pati dextrin maltosa glukosa
Hidrolisis pati dapat juga dilakukan oleh kegiatan enzim. Dalam pencernaan,
enzim amilase memecah pati menjadi maltosa. Amilase juga terdapat pada tepung dan biji
berkecambah. Pada produk-produk tersebut enzim ini biasanya dikenal dengan nama
diastase. Diastase penting pada pembuatan roti dan pembuatan bir karena enzim ini dapat
menghasilkan gula (maltosa) yang seterusnya oleh enzim yang dihasilkan khamir akan
dipecah lebih lanjut menjadi alkohol dan karbon dioksida (Gaman, P. M, 1981).
2.3.1 Penentuan karbohidrat
Penentuan karbohidrat dalam suatu bahan dapat dibedakan menjadi dua yaitu uji
kualitatif dan uji kuantitatif. Banyak cara yang dapat digunakan untuk menentukan
banyaknya karbohidrat dalam suatu bahan yaitu antara lain dengan cara kimia, secara
fisik, cara enzimatik atau biokimia dan cara kromatrografi. Penentuan yang termasuk
polisakarida maupun oligosakarida memerlukan perlakuan pendahuluan yaitu hidrolisa
terlebih dahulu sehingga diperoleh monosakarisa. Bahan dihidrolisa dengan asam atau
enzim pada suatu keadaan yang tertentu. Penentuan monosakarida yang dihasilkan dapat
dengan salah satu cara berikut :
2.3.1.1 Cara Luff Schoorl
Pada penentuan gula secara Luff Schoorl, yang ditentukan bukan kuprooksida yang
mengendap tetapi dengan menentukan kuprioksida dalam larutan sebelum direaksikan
dengan gula reduksi ( titrasi blanko ) dan sesudah direaksikan dengan sampel gula
reduksi ( titrasi sampel ). Penentuannya dengan titrasi menggunakan Na-tiosulfat. Reaksi
yang terjadi selama penentuan karbohidrat dengan cara ini mula-mula kuprioksida yang
ada dalam reagen akan membebaskan iod dari garam K-iodida. Banyaknya iod dapat
diketahui dengan titrasi menggunakan Na-tiosulfat. Untuk mengetahui apakah titrasi
biru menjadi putih berarti titrasi sudah selesai. Agar perubahan warna biru menjadi putih
dapat tepat maka penambahan amilum diberikan pada saat titrasi hampir selesai.
Reaksi yang terjadi dalam penentuan gula cara Luff dapat dituliskan sebagai
berikut :
R-COH + 2CuO Cu2
H
O + R-COOH
2SO4 + CuO CuSO4 + H2
CuSO
O
4 + 2 KI CuI2 + K2SO
2CuI
4
2 Cu 2I2 + I
I
2
2 + 2Na2S2O3 Na2S4O6
I
+ 2NaI
2
Metode Luff Schoorl menggunakan suatu reagen alkalin yang terdiri dari cupri
sitrat, setelah dipanaskan dengan suatu larutan yang terdiri dari gula reduksi, potassium
iodida dan asam ditambahkan setelah pendinginan dan pembebasan iodin, yang mana
ekuivalen terhadap copper yang tidak tereduksi, dititrasi dengan sodium tiosulfat
(Egan, H, 1981).
+ amilum : biru (Sudarmadji, S , 1987).
2.3.1.2 Prinsip Penentuan Kandungan Karbohidrat
Hidolisis karbohidrat menjadi monosakarida yang dapat mereduksikan Cu2+ menjadi Cu+.
Kelebihan Cu2+ dapat dititrasi secara iodometri (SNI 01-2891-1992).
2.4 Protein
Protein merupakan suatu zat makanan yang amat penting bagi tubuh, karena zat ini
disamping berfungsi sebagai bahan bakar dalam tubuh juga berfungsi sebagai zat
unsur-unsur C,H,O dan N yang tidak dimiliki oleh lemak dan karbohidrat. Fungsi utama
protein bagi tubuh ialah untuk membentuk jaringan baru dan mempertahankan jaringan
yang telah ada. Didalam tubuh manusia terjadi suatu siklus protein, artinya protein
dipecah menjadi komponen-komponen yang lebih kecil yaitu asam-asam amino atau
peptida.
2.4.1 Sifat-sifat fisikokimia asam amino dan protein
Sifat fisikokimia setiap protein tidak sama, tergantung pada jumlah dan jenis asam
aminonya. Ada protein yang larut dalam air dan ada pula yang tidak larut dalam air, tetapi
semua protein tidak larut dalam pelarut lemak seperti etil eter. Bila suatu larutan protein
ditambahkan garam, daya larut protein akan berkurang, akibatnya protein akan terpisah sebagai endapan. Bila garam netral yang ditambahkan berkonsentrasi tinggi, maka
protein akan mengendap (Winarno, F. G, 1992).
2.4.2 Analisa kandungan protein
Dengan adanya pemanasan, protein dalam bahan makanan akan mengalami perubahan
dan membentuk persenyawaan dengan bahan lain. Misalnya antara asam amino hasil
perubahan protein dengan gula-gula reduksi akan membentuk senyawa rasa dan aroma
makanan. Protein murni dalam keadaan tidak dipanaskan hanya memiliki rasa dan aroma
yang tidak berarti.
Berdasarkan uraian diatas, maka tujuan analisa protein dalam bahan makanan adalah:
a. Menera jumlah kandungan protein dalam bahan makanan
b. Menentukan tingkat kualitas protein dipandang dari sudut gizi
c. Menelaah protein sebagai salah satu bahan kimia misalnya secara
2.4.3 Jumlah Protein Total
Peneraan jumlah protein secara empiris yang umum dilakukan adalah dengan menentukan
jumlah nitrogen ( N ) yang dikandung oleh suatu bahan. Cara penentuan ini
dikembangkan oleh Kjeldahl, seorang ahli ilmu kimia dari Denmark pada tahun 1883.
Dalam penentuan protein seharusnya hanya nitrogen yang berasal dari protein saja yang
ditentukan. Akan tetapi secara teknis hal ini sulit sekali dilakukan dan mengingat jumlah
kandungan senyawa lain selain protein dalam bahan biasanya sangat sedikit. Maka
penentuan jumlah N total ini tetap dilakukan untuk mewakili jumlah protein yang ada.
Kadar protein yang ditentukan berdasarkan cara kjedahl ini dengan demikian sering
disebut sebagai kadar protein kasar.
Dasar perhitungan penentuan protein menurut Kjedahl ini adalah hasil penelitian
dan pengamatan yang menyatakan bahwa umumnya protein alamiah mengandung unsur
N rata-rata 16% ( dalam protein murni ). Untuk senyawa-senyawa protein tertentu yang
telah diketahui kadar unsur N nya, maka angka yang lebih tepat dapat dipakai.
Apabila jumlah unsur N dalam bahan telah diketahui ( dengan berbagai cara )
maka jumlah protein dapat diperhitungkan dengan :
Jumlah N x 100/16 atau
Jumlah N x 6,25
Untuk campuran senyawa-senyawa protein atau yang belum diketahui komposisi
unsur-unsur penyusunnya secara pasti, maka faktor perkalian 6,25 inilah yang dipakai.
Sedangkan untuk protein - protein tertentu yang telah diketahui komposisinya yang
lebih tepat maka faktor perkalian yang lebih tepatlah yang dipakai. Misalnya faktor
perkalian yang telah diketahui adalah :
5,70 untuk protein gandum
6,38 untuk protein susu
2.4.4 Prinsip Penentuan Kandungan Protein
Senyawa nitrogen diubah menjadi amonium sulfat oleh H2SO4
Analisis protein cara kjeldahl pada dasarnya dapat dibagi menjadi tiga
tahapan, yaitu proses destruksi, proses destilasi dan tahap titrasi.
pekat. Amonium sulfat
yang terbentuk diuraikan dengan NaOH. Amoniak yang dibebaskan diikat dengan asam
borat dan kemudian dititrasi dengan larutan baku asam (SNI 01-2891-1992).
2.4.5 Tahap Destruksi
Pada tahapan ini sampel dipanaskan dalam asam sulfat pekat sehingga terjadi destruksi
menjadi unsur-unsurnya. Elemen karbon, hidrogen teroksidasi menjadi CO, CO2, H2O.
Sedangkan Nitrogen (N) akan berubah menjadi (NH4)2SO4. Asam sulfat yang digunakan
untuk destruksi diperhitungkan adanya bahan protein lemak dan karbohidrat. Untuk
mempercepat proses destruksi sering ditambahkan katalisator berupa campuran Na2SO4
dan HgO (20 : 1). Dengan penambahan bahan katalisator tersebut titik didih asam sulfat
akan dipertinggi sehingga destruksi berjalan lebih cepat. Suhu destruksi berkisar antara
370 – 4100
Penggunaan selenium lebih reaktif dibandingkan merkuri dan kupri sulfat tetapi
Se mempunyai kelemahan yaitu karena sangat cepatnya oksidasi maka nitrogennya justru
mungkin ikut hilang. Proses destruksi sudah selesai apabila larutan menjadi jernih atau
tidak berwarna. Agar supaya analisa lebih tepat maka tahap destruksi ini dilakukan pula
perlakuan blanko yaitu untuk koreksi adanya senyawa N yang berasal dari reagensia yang
digunakan.
C. Selain katalisator yang telah disebutkan tadi, kadang-kadang juga diberikan
selenium. Selenium dapat mempercepat proses oksidasi karena zat tersebut selain
menaikkan titik didih juga mudah mengadakan perubahan dari valensi tinggi ke valensi
2.4.6 Tahap Destilasi
Amonium sulfat dipecah menjadi ammonia (NH3) dengan penambahan NaOH sampai
alkalis dan dipanaskan. Agar selama destilasi tidak terjadi superheating ataupun
pemercikan cairan atau timbulnya gelembung gas yang besar, maka dapat ditambahkan
logam zink (Zn). Amonia yang dibebaskan selanjutnya akan ditangkap oleh larutan asam
standar. Asam standar yang digunakan adalah asam klorida atau asam borat dalam jumlah
yang berlebihan. Untuk mengetahui asam dalam keadaan berlebihan maka akan diberi
indikator misalnya BCG + MR atau PP destilasi diakhiri bila sudah semua ammonia
terdestilasi sempurna dengan ditandai destilat tidak bereaksi basis.
2.4.7 Tahap Titrasi
Apabila penampung destilat digunakan asam borat maka banyaknya asam borat yang
bereaksi dengan ammonia dapat diketahui dengan titrasi menggunakan asam klorida 0,1
N dengan indikator (BCG + MR). Akhir titrasi ditandai dengan perubahan warna larutan
dari biru menjadi merah muda. Selisih jumlah titrasi sampel dan blanko merupakan
jumlah ekivalen nitrogen.
% �=����� ( ������ − ������)
�����������(�)����� ��������,�������
Setelah diperoleh % N, selanjutnya dihitung kadar proteinnya dengan
mengalikan suatu faktor. Besarnya faktor perkalian N menjadi protein ini tergantung pada
persentase N yang menyusun protein dalam suatu bahan.
% Protein = % N x faktor konversi (Sudarmadji, S, 1992).
Dalam modifikasi Winkler, NH3 ( destilat ) ditangkap dalam larutan asam borat
yang tidak perlu diukur tepat jumlahnya. Garam amonium borat yang terbentuk itulah
Reaksi- reaksi :
a. Sampel + destruksi → NH4+ + CO2 + H2
b. NH
O + dan lain-lain (digestion)
4+ + OH- → H2O + NH3 c. NH
(destilasi)
3 + HBO2 → NH4BO2
d. NH
(penampungan)
4BO2 + HCl → HBO2 + NH4 (Harjadi, W, 1990).
Cl (titrasi)
2.5 Tape
Aneka bahan pangan yang mengandung karbohidrat dapat diolah menjadi makanan khas
yang disebut tape. Bahan pangan yang umumnya dibuat tape adalah ubi kayu (singkong ),
beras ketan putih maupun beras ketan hitam serta sorgum.
Tape mempunyai tekstur lunak, rasa asam manis dan sedikit mengandung alkohol.
Selama fermentasi, tape mengalami perubahan – perubahan biokimia akibat aktivitas
mikroorganisme. Pada dasarnya semua bahan pangan yang kaya akan karbohidrat dapat
diolah menjadi tape. Dewasa ini yang paling popular adalah tape singkong dan tape ketan.
Tape merupakan salah satu jenis makanan dari hasil fermentasi bahan baku yang
diberi ragi sebagai sumber mikrobanya.
2.6Fermentasi
Fermentasi telah dikenal sejak zaman dahulu, dengan kecenderungan terhadap
keberlanjutan lingkungan hidup, dan pengembangan sumber daya yang dapat
diperbaharui. Fermentasi mulai menjadi ilmu pada tahun 1857 ketika Louis Pasteur
menemukan bahwa fermentasi merupakan sebuah hasil dari sebuah aksi mikroorganisme
Dalam arti umum menurut Tarigan (1988) fermentasi dapat didefinisikan sebagai
proses metabolisme dimana terjadi perubahan – perubahan kimia dalam substrat organik,
kegiatan atau aktivitas mikroba yang membusukkan bahan-bahan yang difermentasi.
Perubahan kimia tadi tergantung pada macam bahan, macam mikroba, pH, suhu , adanya
aerasi atau usaha lain yang berbeda dengan faktor-faktor diatas misalnya penambahan-
penambahan bahan tertentu untuk menggiatkan fermentasi.
Fermentasi berarti disimilisasi anaerobik senyawa-senyawa organik yang
disebabkan oleh aktivitas mikroorganisme atau ekstrak dari sel-sel tersebut. Disimilasi
yaitu proses pengubahan senyawa didalam sel seperti glikogen dan ATP menjadi
senyawa yang tingkat energinya lebih rendah sedemikian rupa sehingga energi
dibebaskan dalam proses ini. Disimilasi berlangsung didalam sel dan produk-produknya
dikeluarkan ke media sekitarnya. Disimilasi terutama menghasilkan senyawa organik,
senyawa anorganik dan beberapa unsur, contohnya karbohidrat, glikosida, alkohol, asam
keto, hidrokarbon, asam amino dan amina, sejumlah garam Fe, Mn, dan As, unsur-unsur
karbon, belerang dan lain-lain (Gumbiro, 1987).
Ada beberapa faktor yang mempengaruhi proses fermentasi, antara lain adalah
sebagai berikut :
a. pH
b. suhu
c. oksigen
d. substrat (Desrosier, 1988)
Menurut Winarno (1989), proses fermentasi gula oleh ragi misalnya
Saccharomyces cerevisiae dapat menghasilkan etanol (etil alkohol) dan karbon dioksida melalui reaksi sebagai berikut :
C6H12O6 → 2C2H5OH + 2CO
Menurut Astawan (2004) , proses fermentasi yang terjadi selama pembuatan tape
pada dasarnya meliputi empat tahap penguraian , antara lain sebagai berikut :
a. molekul-molekul pati terpecah menjadi dekstrin dan gula-gula sederhana, proses
ini disebut hidrolisis enzimatis
b. gula yang terbentuk akan diubah menjadi alkohol
c. alkohol akan diubah menjadi asam-asam organik oleh bakteri Pediococcus dan Acetobacter melaui proses oksidasi alkohol
d. sebagian asam organik akan bereaksi dengan alkohol membentuk ester yang
memberi cita rasa pada tape
Lama fermentasi yang dibutuhkan dalam proses fermentasi adalah 2-3 hari.
Pengubahan glukosa menjadi etanol berlangsung beberapa tahap yang masing-masing
tahapnya dikatalisa oleh enzim. Pemecahan glukosa melalui jalur fermentasi alkohol,
etanol sebagai hasil akhir perubahan ini masih banyak mengandung energi
(Martoharsono, S, 1997).
Kandungan karbohidrat dan protein pada penelitian ditentukan pada saat dingin
setelah pengukusan dan fermentasi selama 3 hari 2 malam (lebih kurang 48 jam).
Kandungan karbohidrat menurun disebabkan oleh pemecahan karbohidrat dengan
bantuan enzim pada proses fermentasi yang akan berubah menjadi maltosa kemudian
pemecahan maltosa menjadi glukosa, hasil-hasil akhir proses fermentasi adalah karbon
dioksida, fermentasi dapat meningkatkan kandungan protein karena adanya
mikroorganisme pada ragi yang mempunyai kandungan protein sel tunggal
BAB 3
METODOLOGI PENELITIAN
3.1 Alat- alat Penelitian
− Labu Kjeldahl 100 ml Pyrex − Labu alas datar 500 ml Pyrex − Gelas ukur 50 ml Pyrex
− Labu takar Pyrex
− Buret 50 ml Pyrex
− Labu Erlenmeyer 500 ml Pyrex − Beaker glass 250 ml pyrex
− Neraca analitik Metler
− Corong Pyrex
− Kertas saring No.42 whatman − Pipet volume 5 ml, 10 ml pyrex
− Pipet skala 5 ml pyrex
− Karet penghisap − Pipet tetes − Spatula
− Hotplate Gallenkamp
− Statif dan klem − Dandang − Wadah tape − Pemanas − Alat refluks − Stopwatch
3.2 Bahan-bahan
− SeO2
− H
p.a ( E.Merck )
2SO4 − NaOH
96% p.a ( E.Merck )
(s)
− H
p.a ( E.Merck )
3BO3(s)
− Indikator bromocresol green p.a ( E.Merck ) p.a ( E.Merck )
− Indicator metil merah p.a ( E.Merck )
− HCl 37% p.a ( E.Merck )
− H2O − Na
(aq)
2CO3(s) − KIO
p.a ( E.Merck )
3(s) − KI
p.a ( E.Merck )
(s) − CH
p.a ( E.Merck )
3COOH − HgI
glasial p.a ( E.Merck )
(s) − CuSO
p.a ( E.Merck )
4.5 H2O(s) − Na
p.a ( E.Merck )
2CO3.10 H2O(s) − CuSO
p.a ( E.Merck )
− Asam sitrat 4(l)
− Ubi kayu − Ragi tape
− Pati(s) − C
2H5
3.3 Prosedur Penelitian
OH 96% p.a ( E.Merck )
3.3.1 Pembuatan Pereaksi
3.3.1.1 Larutan Indikator campuran
Disiapkan larutan bromocresol green 0,1% dan larutan merah metil 0,1% dalam alkohol
95% secara terpisah. Campur 500 ml asam borat dengan 5 ml indikator didalam beaker
glass.
3.3.1.2 Larutan Indikator metil merah 0,02%
Ditimbang kristal sebanyak 50 mg dimasukkan kedalam labu takar 250 ml, ditambahkan
dengan 150 ml alkohol 96% dan diencerkan dengan akuades sampai garis tanda.
3.3.1.3Larutan NaOH 30%
Ditimbang 30 g kristal NaOH kemudian dimasukkan kedalam labu takar 100 ml,
diencerkan dengan akuades sampai garis tanda.
3.3.1.4 Larutan H3BO3
Ditimbang 10 g H
2%
3BO3(s) dimasukkan kedalam labu takar 500 ml, diencerkan dengan akuades sampai garis tanda.
25 g CuSO4.5H2O sejauh mungkin bebas besi ,dilarutkan dalam 100 ml akuades, 50 g
asam sitrat dilarutkan dalam 50 ml akuades dan 388 g soda murni ( Na2CO3.10H2O)
dilarutkan dalam 300-400 ml akuades mendidih. Larutan asam sitratnya dituangkan
dalam larutan soda sambil dikocok, selanjutnya ditambahkan larutan CuSO4
3.3.1.6 Larutan HCl 0,1 N
, sesudah
dingin ditambahkan akuades sampai 1 liter.
Sebanyak 8,89 ml HCl 37% dipipet ke dalam labu takar 1000 ml, diencerkan hingga
garis tanda dengan akuades, dan dihomogenkan.
Standarisasi HCl 0,1 N
- Ditimbang 0,1 g Natrium tetraborat murni
- Dimasukkan kedalam erlenmeyer
- Dilarutkan dengan 50 ml aquades
- Ditambahkan 3 tetes indikator metil merah
- Dititrasi dengan HCl sampai warna merah rose
- Dicatat volume HCl yang terpakai
- Dihitung konsentrasi HCl
- Dilakukan hal yang sama sebanyak 3 kali.
3.3.1.7Larutan Na2S2O3
12.5 g Na
0,1 N
2S2O3. 5 H2
Standarisasi larutan Na
O dimasukkan kedalam labu takar 500 ml dan diencerkan dengan
akuades sampai garis tanda.
2S2O
- Dikeringkan K
3
2Cr2O7 dalam oven selama 1 jam pada suhu 110o
- Dikeluarkan dari oven dan didinginkan dalam desikator
C
- Ditimbang 0,1 gram K2Cr2O7
- Ditambahkan 5 mL HCl
- Ditambahkan 20 mL KI 20 % (p)
- Didiamkan selama 5 menit
- Ditambahkan 100 mL akuades
- Dititrasi dengan Na2S2O3 hingga kuning pucat, kemudian ditambahkan indikator
amilum dan dititrasi kembali dengan Na2S2O3
- Dicatat volume Na
hingga berubah warna menjadi
hijau
2S2O3
- Dihitung konsentrasi Na
yang terpakai
2S2O
- Diulangi sebanyak 3 kali 3
3.3.1.8Larutan pati
10 g pati yang dapat larut dicampur dengan 10 mg HgI dan 30 ml akuades, ditambahkan
pada 1 liter akuades yang sedang mendidih didalam beaker glass.
3.3.1.9 HCl 3%
Dipipet 40,6 ml larutan HCl(p) kemudian dimasukkan kedalam labu takar 500 ml,
diencerkan dengan akuades sampai garis tanda.
3.3.1.10CH3
Dipipet 1,5 ml larutan CH
COOH 3%
3COOH glasial kemudian dimasukkan kedalam labu takar 50 ml, diencerkan dengan akuades sampai garis tanda.
3.3.1.11KI 20%
Ditimbang 20 g KI(S) kemudian dimasukkan kedalam labu takar 100 ml, diencerkan
3.3.1.12H2SO4
Dipipet 26,1 ml larutan H
25%
2SO4(p) kemudian dimasukkan kedalam labu takar 100 ml yang telah berisi akuades dan diencerkan dengan akuades sampai garis tanda.
3.3.2 Fermentasi ubi kayu
3.3.2.1 Preparasi sampel sebelum difermentasi
- Dikupas kulit luar ubi kayu sampai bersih
- Dicuci ubi yang telah dikupas kulitnya dengan air sampai bersih
- Dipotong kecil-kecil ubi kayu yang telah dibersihkan
- Dimasukkan ubi kayu yang telah dipotong ke dalam dandang yang berisi air
- Dikukus ubi hingga lunak
- Diangkat ubi kayu yang telah lunak dan ditiriskan
- Didinginkan
3.3.2.2 Preparasi sampel fermentasi
- Ditaburi ragi yang telah dihancurkan sebanyak 1,5470 g secara merata pada ubi kayu
kukus yang sudah didinginkan
- Dimasukkan ke dalam wadah penyimpanan
- Ditutup wadah dengan rapat tanpa aliran udara
3.3.3 Perlakuan Sampel
3.3.3.1 Penentuan kandungan Karbohidrat
- Dimasukkan 3,1533 g ubi kayu yang telah dikukus kedalam labu alas datar 500 ml
- Ditambahkan 200 ml larutan HCl 3%
- Dididihkan selama 3 jam diatas hotplate dengan menghubungkan pada alat refluks
- Didinginkan dan dinetralkan dengan larutan NaOH 30%
- Ditambahkan sedikit CH3
- Dimasukkan larutan kedalam labu takar 500 ml dan diencerkan dengan akudes COOH 3%
- Disaring
- Dimasukkan 10 ml filtrat kedalam erlenmeyer
- Ditambahkan 25 ml larutan Luff Schoorl
- Ditambahkan beberapa batu didih
- Ditambahkan 15 ml akuades
- Dipanaskan campuran sampai mendidih
- Didinginkan
- Ditambahkan 15 ml larutan KI 20%
- Ditambahkan 25 ml H2SO4 25 % secara perlahan-lahan
- Dititrasi dengan larutan Na2S2O3
- Ditambahkan indikator amilum sebanyak 3 tetes
0,1007 N sampai larutan berwarna kuning pucat
- Dititrasi kembali sampai warna biru hilang
Note : dilakukan perlakuan yang sama untuk sampel yang telah difermentasi dan blanko
3.3.3.2 Penentuan kandungan Protein
- Ditambahkan 5 g selenium dan 25 mL H2SO
- Dipanaskan diatas pemanas listrik/ api pembakar sampai mendidih dan larutan
menjadi jernih
4(p)
- Ditunggu sampai larutan dingin
- Dimasukkan kedalam labu ukur 250 ml dan diencerkan dengan akuades
- Dipipet 50 ml larutan yang telah diencerkan dan dimasukkan kedalam alat destilasi
- Ditambahkan batu didih
- Ditambahkan 50 ml NaOH 30%
- Dicelupkan selang aliran destilat kedalam larutan penampung
- Didestilasi selama lebih kurang 1,5 jam
- Ditampung destilat didalam 25 ml larutan asam borat 2% dan 3 tetes indikator
campuran
- Dibilas ujung pendingin dengan akuades
- Dititrasi dengan larutan HCl 0,0969 N
- Dihitung % N
3.4.Bagan Penelitian
3.4.1 Penentuan kandungan Karbohidrat
Dimasukkan kedalam labu alas datar 500 ml
Ditambahkan 200 ml larutan HCl 3%
Dididihkan selama 3 jam diatas hotplate dengan
menghubungkan pada alat refluks
Didinginkan dan dinetralkan dengan larutan NaOH 30%
Ditambahkan sedikit CH3
Dimasukkan larutan kedalam labu takar 500 ml dan
diencerkan dengan akuades
COOH 3%
Disaring
Dimasukkan 10 ml kedalam erlenmeyer
Ditambahkan 25 ml larutan Luff Schoorl
Ditambahkan beberapa batu didih
Ditambahkan 15 ml akuades
Dipanaskan campuran sampai mendidih
Didinginkan
Ditambahkan 15 ml larutan KI 20%
Ditambahkan 25 ml H2SO4 25 % secara perlahan-lahan
Dititrasi dengan larutan Na
2S2O3
Ditambahkan indikator amilum sebanyak 3 tetes
0,1007 N sampai warna kuning
pucat 3,1533 g ubi kayu yang telah dikukus
Dititrasi kembali sampai warna biru hilang
Note : dilakukan perlakuan yang sama untuk sampel yang telah difermentasi dan blanko
3.4.2 Penentuan kandungan Protein
Dimasukkan kedalam labu Kjeldahl 100 ml
Ditambahkan 5 g selenium dan 25 mL H2SO
Dipanaskan diatas pemanas listrik/ api pembakar sampai
mendidih dan larutan menjadi jernih
4(p)
Ditunggu sampai larutan dingin
Dimasukkan kedalam labu ukur 250 ml dan diencerkan
dengan akuades
Dipipet 50 ml larutan yang telah diencerkan dan
dimasukkan kedalam alat destilasi
Ditambahkan batu didih
Ditambahkan 50 ml NaOH 30%
Dicelupkan selang aliran destilat kedalam larutan
penampung
Didestilasi selama lebih kurang 1,5 jam
Ditampung destilat didalam 25 ml larutan asam borat 2%
dan 3 tetes indikator campuran
Dibilas ujung pendingin dengan akuades
Dititrasi dengan larutan HCl 0,0969 N
Dihitung % N 3,1210 g ubi kayu yang telah dikukus
Larutan hijau bening
Destilat dalam asam borat 2%
Note : dilakukan perlakuan yang sama untuk sampel yang telah difermentasi dan blanko
BAB 4
HASIL DAN PEMBAHASAN
4.1 Hasil Penelitian
4.1.1 Data Penelitian
Dari hasil penelitian secara umum dapat dinyatakan bahwa kandungan karbohidrat pada
ubi kayu yang difermentasi mengalami penurunan daripada ubi kayu kukus dan
kandungan protein pada ubi kayu yang difermentasi mengalami peningkatan daripada ubi
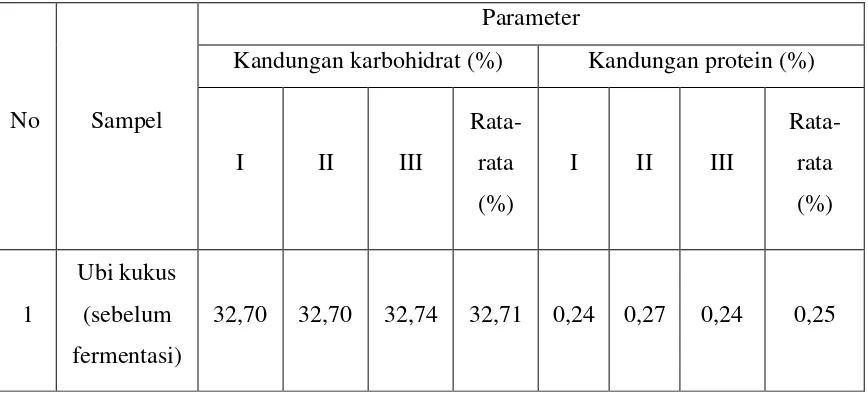
[image:41.612.108.542.511.708.2]kayu kukus. Hal ini dapat dilihat pada tabel berikut ini :
Tabel 4.1 Data hasil pengukuran kandungan karbohidrat dan kandungan protein pada ubi kayu kukus sebelum dan sesudah difermentasi
No Sampel
Parameter
Kandungan karbohidrat (%) Kandungan protein (%)
I II III
Rata-rata
(%)
I II III
Rata-rata
(%)
1
Ubi kukus
(sebelum
fermentasi)
2 Ubi setelah
fermentasi 30,78 30,78 30,78 30,78 0,81 0,81 0,81 0,81
4.1.2. Pengolahan Data
4.1.2.1. Perhitungan Kandungan Karbohidrat
Penentuan kandungan karbohidrat pada ubi kayu kukus dan ubi kayu fermentasi dapat
dihitung sebagai berikut:
Kadar karbohidrat
=
fp × mgglukosa ×0,90Beratsampel ×1000
× 100%
Dimana:
fp = faktor pengenceran
mg glukosa = ml Na2S2O3
ml Na
( tabel penetapan Gula menurut Luff
Schoorl)
2S2O3 = Volume blanko – volume titrant
Perhitungan kandungan karbohidrat pada ubi kayu kukus :
Berat sampel ubi kayu kukus = 3,1533 g
Volume Na2S2O3 0,1007 N
Volume blanko = 24,30 ml = 15,10 ml
Fp =
(
497ml Na2S2O3
= 9,2
0,1007 N = 24,30 – 15,10
Dilihat dari tabel penetapan gula menurut Luff Schoorl untuk 9 ml Na2S2O3
Jadi untuk 9,2 ml Na
0,1 N
jumlah glukosa adalah 22,4 mg
2S2O3
mg glukosa = 9,2 ��
9ml × 22,4
0,1 N, maka jumlah glukosanya adalah :
= 22,8977
Kadar karbohidrat ubi kayu kukus
=
497ml
10ml ×22,8977mg ×0,90
3,1533 ×1000 ×100 %
= 32,48 %
Karena pada tabel penetapan gula menurut Luff Schoorl dipakai Na2S2O3 0,1 N
sedangkan pada penelitian dipakai Na2S2O3
Kadar karbohidrat ubi kayu kukus
=
32,48% ×0,1007N0,1N
0,1007 N maka kadar karbohidrat pada ubi
kayu kukus adalah :
= 32,70 %
Kadar karbohidrat ubi kayu kukus II = 32,70 %
Kadar karbohidrat ubi kayu kukus III = 32,74 %
Kadar karbohidrat rata-rata =32,71 %
Perhitungan kandungan karbohidrat pada ubi kayu fermentasi :
Volume Na2S2O3
Volume blanko = 24,30 ml 0,1007 N = 15,70 ml
Fp =
(
49710
)
mlml Na2S2O3
= 8,6
= 24,30 – 15,70
Dilihat dari tabel penetapan gula menurut Luff Schoorl untuk 8 ml Na2S2O3
Jadi untuk 8,6 ml Na
0,1 N
jumlah glukosa adalah 19,8 mg.
2S2O3
mg glukosa = 8,6��
8ml
x 19,8
0,1 N, maka jumlah glukosanya adalah :
= 21,2850
Kadar karbohidrat ubi kayu fermentasi =
497ml
10ml ×21,2850mg ×0,90
3,1139 ×1000
×
100 %= 30,57%
Karena pada tabel penetapan gula menurut Luff Schoorl dipakai Na2S2O3 0,1 N
sedangkan pada penelitian dipakai Na2S2O3
Kadar karbohidrat ubi kayu fermentasi =
30,57 % ×0,1007N
0,1N
0,1007 N maka kadar karbohidrat pada ubi
kayu fermentasi adalah :
= 30,78 %
Kadar karbohidrat ubi kayu fermentasi II = 30,78 %
Kadar karbohidrat ubi kayu fermentasi III = 30.78 %
Maka banyak karbohidrat yang tidak terfermentasi adalah :
Banyak karbohidrat yang tidak terfermentasi= karbohidrat ubi kukus - karbohidrat ubi fermentasi
= 32,71 % - 30,78 %
= 1,93 %
4.1.2.2 Perhitungan Kandungan Protein
Penentuan Kandungan Protein pada ubi kayu kukus dan ubi kayu fermentasi dapat
dihitung sebagai berikut :
Kadar protein = (b−c)×NHCl ×14,008 ×6,25 ×fp
Beratsampel ×1000
×
100 %Dimana :
b = volume titran sampel (ml)
c = volume titran blanko
6,25 = faktor konversi
Fp = faktor pengenceran
Perhitungan kandungan protein pada ubi kayu kukus :
Berat ubi kayu kukus = 3,1210 g
Volume titran sampel = 0,30 ml
Volume blanko = 0,12 ml
Fp = 250 ml
Kadar protein ubi kayu kukus = (0,30−0,12ml )×0,0968N ×14,008 ×6,25 ×
250ml 50ml
3,1210 ×1000 × 100 % = 0,24 %
Kadar protein ubi kayu kukus II = 0,27%
Kadar protein ubi kayu kukus III= 0,24 %
Kadar protein rata–rata = 0,25 %
Kandungan protein pada ubi kayu fermentasi :
Berat ubi kayu fermentasi = 3,0547 g
Volume titran sampel = 0,70 ml
Volume blanko = 0,12 ml
Fp = 250 ml
50 ml
Kadar protein ubi fermentasi =
(0,70ml−0,12ml)×0,0969N ×14,008 ×6,25 ×250ml
50ml
3,0547 ×1000 x 100% = 0,81 ml
Kadar protein ubi kayu fermentasi II = 0,81 %
Kadar protein ubi kayu fermentasi III = 0,81 %
4.1.2.3 Perhitungan Standarisasi Larutan
4.1.2.3.1 Standarisasi Larutan HCl 0,1
Berat Na2B4O7
Berat Na
I = 0,1022 g Volume HCl I = 5,50 ml
2B4O7
Berat Na
II = 0,1015 g Volume HCl II = 5,50 ml
2B4O7
N HCl = berat ( mg)
VolumeHCl ×MrNa2B4O7 .10H2O
III = 0,1014 g Volume HCl III = 5,50 ml
N HCl = 102,2mg
5,50ml ×190,6
N HCl = 0,0974
Normalitas HCl II = 0,0968
Normalitas HCl III = 0,0967
Normalitas HCl rata-rata = 0,0969
4.1.2.3.2 Standarisasi Larutan Na2S2O3
Berat K
0,1 N
2Cr2O7 I = 0,0997 g Volume Na2S2O3
Berat K
I = 20,20 ml
2Cr2O7 II = 0,0997 g Volume Na2S2O3
Berat K
II = 20,20 ml
2Cr2O7 III = 0,0996 g Volume Na2S2O3
N Na
III = 20,20 ml
2S2O3 =
����� (��)
N Na2S2O3
N Na
= 99,7mg
20,20ml ×49
2S2O3
Normalitas Na
= 0,1007
2S2O3
Normalitas Na
II = 0,1007
2S2O3
Normalitas Na
III = 0,1006
2S2O3 rata-rata = 0,1007
4.1.2.4 Menghitung rata-rata pengukuran kandungan karbohidrat pada ubi kayu kukus dan ubi kayu fermentasi
Untuk mengukur rata-rata data pengukuran kandungan karbohidrat pada ubi kayu kukus
dan ubi kayu fermentasi maka dapat diolah secara statistik yaitu secara deviasi standar
(S),
Dengan menggunakan rumus :
S =
�
∑(Xi−X�)2n−1
Dimana :
Xi = Kandungan karbohidrat
X = Kandungan karbohidrat rata-rata
N = Jumlah perlakuan
Untuk ubi kayu kukus diperoleh data pengukuran karbohidrat :
X1
X
= 32,70 %
X3
Dengan demikian karbohidrat pada ubi kayu kukus adalah : = 32,74 %
�̅
= ∑��
�
= 32,70+32,70+32,74
3
= 32,71 %
(�� − ��)2 = (32,70−32,71)2 = 0,0001
(�� − ��)2 = (32,70−32,71)2 = 0,0001
(�� − ��)2 = (32,74−32,71)2 = 0,0009
∑(�� − ��)2 = 0,0011
Maka : S =
�
∑(��−��)2
�−1
=
�
0,0011
3−1
= 0,0234
Dari harga deviasi (S) yang di peroleh diatas dapat dihitung kandungan karbohidrat ubi
kayu kukus dengan batas kepercayaan melalui rumus berikut :
µ = (
�̅
) ±
��√�
dimna :
µ = populasi rata-rata
�̅ = kandungan karbohidrat rata-rata
t = harga t distribusi ( lihat tabel pada daftar lampiran 5)
S = deviasi standar
dari data distribusi t student untuk n=3, derajat kepercayaan (dk) = n-1 = 2
untuk derajat kepercayaan 95% (P = 0,05), nilai t = 4,30
sehingga diperoleh :
µ = 32,71 ± 4,30(0,0234)
√3
= 32,71 ± 0,0580 %
Dilakukan dengan cara yang sama untuk menghitung rata-rata kandungan karbohidrat
[image:50.612.102.543.353.445.2]pada ubi kayu fermentasi.
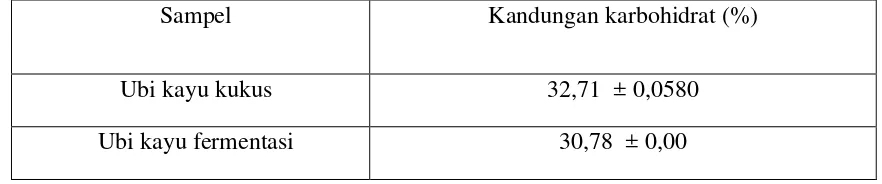
Tabel 4.1.1 Data hasil perhitungan rata-rata kandungan karbohidrat pada ubi kayu kukus
Dan ubi kayu fermentasi
Sampel Kandungan karbohidrat (%)
Ubi kayu kukus 32,71 ± 0,0580
Ubi kayu fermentasi 30,78 ± 0,00
4.1.2.5 Menghitung rata-rata data pengukuran kandungan protein pada ubi kayu kukus dan ubi kayu fermentasi
Untuk mengukur rata-rata data pengukuran kandungan protein pada ubi kayu kukus dan
ubi kayu fermentasi maka dapat diolah secara statistik yaitu secara deviasi standar (S),
dengan menggunakan rumus :
S =
�
∑(��−��)2
�−1
Dimana :
X = Kandungan protein rata-rata
N = Jumlah perlakuan
Untuk ubi kayu kukus diperoleh data pengukuran protein :
X1
X
= 0,24 %
2
X
= 0,27 %
3
Dengan demikian protein pada ubi kayu kukus adalah : = 0,24 %
�̅
= ∑��
�
= 0,24+0,27+0,24
3
= 0,25 %
(�� − ��)2 = (0,24−0,25)2 = 0,0001
(��− ��)2 = (0,27−0,25)2 = 0,0004
(�� − ��)2 = (0,24−0,25)2 = 0,0001
∑(�� − ��)2 = 0,0006
Maka : S =
�
∑(��−��)2
�−1
=
�
0,0006
3−1
= 0,0173
Dari harga deviasi (S) yang diperoleh diatas dapat dihitung kandungan protein ubi kayu
kukus dengan batas kepercayaan melalui rumus berikut :
µ = (
�̅
) ±
��dimana :
µ = populasi rata-rata
�̅ = kandungan protein rata-rata
t = harga t distribusi ( lihat tabel pada daftar lampiran )
S = deviasi standar
n = jumlah perlakuan
dari data distribusi t student untuk n=3, derajat kepercayaan (dk) = n-1 = 2
untuk derajat kepercayaan 95% (P = 0,05), nilai t = 4,30
sehingga diperoleh :
µ = 0,25 ± 4,30(0,0173)
√3
= 0,25 ± 0,0429 %
Dilakukan dengan cara yang sama untuk menghitung rata-rata kandungan protein pada
ubi kayu fermentasi.
Tabel 4.1.2 Data hasil perhitungan rata-rata kandungan protein pada ubi kayu kukus dan
Ubi kayu fermentasi
Sampel Kandungan protein (%)
Ubi kayu kukus 0,25 ± 0,0429
4.2. Pembahasan
Penentuan kandungan karbohidrat dan protein dari Ubi kayu kukus dan Ubi kayu
fermentasi dilakukan dengan menghaluskan sampel Ubi kayu kukus dan Ubi kayu
fermentasi terlebih dahulu. Analisa kandungan karbohidrat dilakukan dengan
menghidrolisa sampel kemudian diukur glukosa hasil hidrolisa menggunakan metode
Luff Schoorl, hasil yang diperoleh dikonversikan kedalam bentuk karbohidrat. Analisa
kandungan protein dilakukan dengan mendestruksi sampel kemudian didestilasi,
penentuannya dilakukan dengan menggunakan metode Kjeldahl.
Dari hasil penelitian yang dilakukan diperoleh hasil bahwa terjadi penurunan
kandungan karbohidrat dan peningkatan kandungan protein pada ubi kayu yang
difermentasi yaitu kandungan karbohidrat ubi kukus sebesar 32,71% setelah fermentasi
menjadi 30,78% dan kandungan protein ubi kukus sebesar 0,25% setelah fermentasi
menjadi 0,81%.
Penurunan kandungan karbohidrat pada ubi kayu selama fermentasi disebabkan
oleh adanya aktifitas mikroba yang terdapat pada ragi. Molekul pati dipecah menjadi gula
yang sederhana sehingga kadar awal menjadi berkurang setelah fermentasi. Fermentasi
merupakan disimilasi anaerobik senyawa-senyawa organik yang disebabkan oleh aktivitas
mikroorganisme atau ekstrak dari sel-sel tersebut. Pemecahan karbohidrat menjadi
monosakarida dapat mereduksikan Cu2+ dalam larutan Luff Schoorl menjadi Cu+,
kelebihan Cu2+
Peningkatan kandungan protein pada ubi kayu selama fermentasi juga disebabkan
oleh adanya aktifitas mikroba yang ada pada ragi dan adanya mikroba dalam ragi yang
memiliki protein sel tunggal memberikan penambahan protein pada ubi kayu. Reaksi
yang terjadi dalam penentuan protein dengan metode Kjeldahl adalah sebagai berikut: dapat dititrasi secara iodometri.
b. (NH4)2SO4 + 2NaOH → Na2SO4 + 2H2O + 2NH3
c. 2NH
3 + 4H3BO3 → (NH4)2B4O7 + 5H2O d. (NH
4)2B4O7 + 2HCl → H2B4O7 + 2NH4Cl .
BAB 5
KESIMPULAN DAN SARAN
5.1. Kesimpulan
Dari data dan hasil penelitian yang dilakukan, terjadi penurunan kandungan karbohidrat
dan peningkatan kandungan protein pada ubi kayu setelah fermentasi, untuk kandungan
karbohidrat diperoleh hasil penurunan dari 32,71 % menjadi 30,78 % setelah fermentasi
dan untuk kandungan protein diperoleh hasil peningkatan dari 0,25% menjadi 0,81%
setelah fermentasi.
5.2. Saran
Perlu dilakukan penelitian lebih lanjut untuk mengetahui pada fermentasi hari keberapa
DAFTAR PUSTAKA
Allen, S. W. 1989 . Chemical Analysis Of Ecological Material . Second Edition. London : Blackweel Scientific Publications
Desrosier, N. W. 1987. Teknologi Pengawetan Pangan . Jakarta : UI Press
Egan, H. 1981. Pearson’s Chemical Analysis Of Foods . Eight edition . New york : Churchill livingstone
Gaman, P. M. 1981. Pengantar Ilmu Pangan Nutrisi Dan Mikrobilologi. Yogyakarta : Gadjah Mada University Press
Gumbiro, S. 1987. Bio Industri Penerapan Teknologi Fermentasi. Jakarta : Mediyatama Sarana Perkasa
Harjadi, W. 1990. Ilmu Kimia AnalitikDasar. Jakarta : PT.Gramedia
Khopkar, S. M. 2003 . Konsep Dasar Kimia Analitik . Jakarta : UI-Press
Martoharsono, S. 1997 . Biokimia . Jilid II . Yogyakarta : Gadjah Mada University Press Riadi, L. 2003 . Teknologi Fermentasi . Jakarta : Graha ilmu
Rohman, A. 2007 . Kimia Farmasi Analisis . Yogyakarta : Pustaka Pelajar
Satiadarma, K. 2004 . Asas Pengembangan Prosedur Analisis . Edisi Pertama . Surabaya : Airlangga University Press
Tarigan, J. 1988. Pengantar Bioteknologi . Jakarta : Departemen Pendidikan dan Kebudayaan Direktorat Jendral Perguruan Tinggi.
Vogel. 1994 . Kimia Analisis Kuantitatif Anorganik . Jakarta : EGC
Wilbraham, A. C. 1992 . Pengantar Kimia Organik Dan Hayati . Bandung : ITB- Press Winarno, F. G. 1997. Kimia Pangan Dan Gizi . Jakarta : PT.Gramedia PustakaUtama
Lampiran 2. Tabel penetapan Gula menurut Luff Schoorl
Na2S2O3 ml
0,1 N
Glukosa,Fruktosa, Gula inversi
mg
Laktosa
mg
Maltosa
1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 17 18 19 20 21 22 23 2,4 4,8 7,2 9,7 12,2 14,7 17,2 19,8 22,4 25,0 27,6 30,3 33,0 35,7 38,5 41,3 44,2 47,1 50,0 53,0 56,0 59,1 62,2 3,6 7,3 11,0 14,7 18,4 22,1 25,8 29,5 33,2 37,0 40,8 44,6 48,4 52,2 56,0 59,9 63,8 67,7 71,1 75,1 79,8 83,9 88,0 3,9 7,8 11,7 15,6 19,6 23,5 27,5 31,5 35,5 39,5 43,5 47,5 51,6 55,7 59,8 63,9 68,0 72,2 76,5 80,9 85,4 90,0 94,6
Lampiran 3. Tabel Daftar harga Distribusi t-Student
Kebebasan
(n-1) 90% 95% 98% 99%