ADITYA HIKMAT NUGRAHA
SKRIPSI
DEPARTEMEN ILMU DAN TEKNOLOGI KELAUTAN FAKULTAS PERIKANAN DAN ILMU KELAUTAN
Dengan ini Saya menyatakan bahwa Skripsi yang berjudul :
PEMANFAATAN GAS KARBONDIOKSIDA (CO2) PADA
KULTIVASI OUTDOOR MIKROALGA Nannochloropsis sp.
adalah benar merupakan hasil karya sendiri dan belum diajukan dalam bentuk apa pun kepada perguruan tinggi mana pun. Semua sumber data dan informasi yang berasal atau dikutip dari karya yang diterbitkan maupun tidak diterbitkan dari penulis lain telah disebutkan dalam teks dan dicantumkan dalam Daftar Pustaka di bagian akhir Skripsi ini.Bogor, Desember 2012
ADITYA HIKMAT NUGRAHA. Pemanfaatan Gas Karbondioksida (CO2) pada Kultivasi Outdoor Mikroalga Nannochloropsis sp. Dibimbing oleh MUJIZAT KAWAROE dan ADRIANI SUNUDDIN
Karbondioksida merupakan gas yang bersifat polutif yang banyak dihasilkan oleh kegiatan industri dan penggunaan kendaraan bermotor. Pencemaran yang berasal dari gas karbondioksida dapat meningkatkan akumulasi gas karbondioksida di atmosfer yang dapat menyebabkan terjadinya pemanasan global. Solusi yang tepat dan murah dibutuhkan dalam memanfaatkan gas karbondioksida diantaranya melalui pendekatan bioteknologi. Penelitian ini menggunakan gas karbondioksida dalam proses kultivasi mikroalga Nannochloropsis sp. Karbondioksida merupakan salah satu bahan utama dalam proses fotosintesis, sehingga pemberian gas
karbondioksida terhadap media kultivasi mikroalga dapat membantu mikroalga dalam berfotosintesis sekaligus mengurangi dampak pencemaran gas
karbondoksida di atmosfer. Penelitian ini berlangsung dari bulan Januari sampai bulan Juni 2012 bertempat di Laboratorium Kultivasi Mikroalga Pusat Penelitian Surfaktan dan Bioenergi (SBRC) LPPM –IPB.
Penelitian ini terdiri dari tiga perlakuan yaitu : Perlakuan kontrol dengan memberikan aerasi, perlakuan dengan pemberian gas karbondioksida sebesar 1 cc x100/ menit selama 120 menit/hari (P1) dan perlakuan dengan pemberian gas karbondioksida karbondioksida sebesar 1,5 cc x100/ menit selama 120 menit/hari (P2). Kultivasi mikroalga Nannochloropsis sp. dengan perlakuan P1 memiliki pertumbuhan yang paling tinggi dengan kelimpahan maksimum mencapai 14,52 x 106 sel/ml pada kultivasi hari ke-5 dengan laju pertumbuhan maksimum µ = 0,46 dan biomassa sebesar 0,45 gr/L. Secara rata-rata P1 mampu meningkatkan kelimpahan sel hingga 59% dan biomassa sebesar 31%.
© Hak Cipta milik IPB, tahun 2012
Hak Cipta dilindungi Undang Undang
Dilarang mengutip sebagian atau seluruh karya tulis ini tanpa mencantumkan atau menyebutkan sumbernya. Pengutipan hanya untuk kepentingan pendidikan, penelitian, penulisan karya ilmiah, penyusunan laporan, penulisan kritik atau tinjauan suatu masalah; dan pengutipan tersebut tidak merugikan kepentingan yang wajar IPB
ADITYA HIKMAT NUGRAHA
SKRIPSI
Sebagai salah satu syarat memperoleh gelar Sarjana Ilmu Kelautan pada
Departemen Ilmu dan Teknologi Kelautan
DEPARTEMEN ILMU DAN TEKNOLOGI KELAUTAN FAKULTAS PERIKANAN DAN ILMU KELAUTAN
Judul Skripsi: PEMANFAATAN GAS KARBONDIOKSIDA
(CO
2)
PADA KULTIVASI OUTDOOR MIKROALGA Nannochloropsis sp.Nama Mahasiswa: Aditya Hikmat Nugraha
Nomor Pokok: C54080049
Departemen: Ilmu dan Teknologi Kelautan
Menyetujui, Dosen Pembimbing
Utama Anggota
Dr. Ir. Mujizat Kawaroe, M.Si. Adriani Sunuddin, S.Pi, M.Si. NIP. 19651213 199403 2 002 NIP. 19790206 200604 2 013
Mengetahui,
Ketua Departemen Ilmu dan Teknologi Kelautan
Prof. Dr. Ir. Setyo Budi Susilo, M.Sc. NIP. 19580909 198303 1 003
vii
Puji dan rasa syukur penulis panjatkan kehadirat Allah SWT, karena atas rahmat dan karunia-Nya, penulis dapat menyelesaikan skripsi ini. Dalam penulisannya, Penulis banyak mendapat bantuan dari berbagai pihak. Untuk itu penulis mengucapkan banyak terima kasih kepada :
1. Ayah, Ibu, dan seluruh keluarga atas dukungannya baik secara moril maupun materil selama penyusunan skripsi ini.
2. Dr.Ir. Mujizat Kawaroe, M.Si dan Adriani Sunuddin S.Pi, M.Si selaku dosen pembimbing yang telah memberikan arahan dan bimbinganya selama ini.
3. Dr.Ir. Tri Prartono, M.Sc Selaku dosen penguji ujian akhir skripsi 4. Seluruh Dosen dan Staff Departemen Ilmu dan Teknologi Kelautan
terimakasih atas ilmu dan pelayanan yang diberikan selama penulis melakukan perkuliahan.
5. Surfactan Bionergy Research Centre Khususnya Divisi Alga yang telah membantu penulis dalam melaksanakan penelitian.
6. Tim penelitian SBRC 2012 Anma, Dea Fauzia, Hari Aditia, Rizky, Dodi, Misep, Yuni, Syibli, Teguh, Berlian, Raka dan Inggit atas suka dan duka yang telah diberikan selama penelitian di SBRC.
7. Indah Mustika Putri, S.Pi terima kasih atas dukungan dan semangat yang telah diberikan.
8. Keluarga besar ITK 45 atas persahabatan dan suka duka yang telah terbangun selama ini.
Penulis menyadari skripsi ini jauh dari kesempurnaan, namun demikian penulis berharap agar skripsi ini dapat berguna bagi diri sendiri maupun pembaca dapat dikembangkan melalui penelitian selanjutnya.
Bogor, Desember 2012
ix
Nannochloropsis sp. Perlakuan P1 ... 26
4.2.3 Biomassa dan Laju Pertumbuhan Biomassa Nannochloropsis sp. Perlakuan P2 ... 27
4.3 Kualitas Air Media Kultur ... 28
4.3.1 Salinitas ... 28
4.3.2 Suhu ... 29
4.3.4 Derajat Keasaman (pH) ... 31
4.4 Parameter Karbondioksida ... 33
4.4.1 Karbondioksida Terlarut dalam Media Kultivasi ... 33
4.4.2 Konsentrasi Karbondioksida Tersisa ... 35
5. KESIMPULAN DAN SARAN ... 37
5.1 Kesimpulan ... 37
5.2 Saran ... 37
DAFTAR PUSTAKA ... 38
ix
Halaman
1. Alat dan bahan yang digunakan dalam penelitian ... 11
2. Kelimpahan sel (×106 sel/mL) dan laju pertumbuhan spesifik
Nannochloropsis sp. ... 19
3. Biomassa (gr/l) dan laju pertumbuhan biomassa (μ)
Nannochloropsis sp. ... 24
x
Halaman
1. Nannochloropsis sp. ... 4
2. Fase pertumbuhan mikroalga ... 7
3. Desain penelitian kultivasi Nannochloropsis sp. skala outdoor ... 14
4. Grafik nilai salinitas media kultivasi selama penelitian ... 28
5. Grafik nilai suhu media kultivasi selama penelitian ... 30
6. Grafik karbondioksida terlarut selama penelitian………. ... 33
xi
Halaman
1. Perhitungan kelimpahan sel Nannochloropsis sp. ... 41
2. Perhitungan laju pertumbuhan spesifik (µ) kelimpahan sel dan biomassa Nannochloropsis sp. ... 42
3. Deskripsi dan mekanisme operasional Orsat ... 44
4. Kelimpahan sel dan laju pertumbuhan kelimpahan sel Nannochloropsis sp ... 49
5. Biomassa dan laju pertumbuhan biomassa Nannochloropsis sp. ... 51
6. Kualitas air media kultivasi Nannochloropsis sp. ... 53
7. Kandungan karbondioksida terlarut dalam kultivasi Nannochloropsis sp. .……….. ... 56
8. Konsentrasi karbondioksida tersisa dalam kultivasi Nannochloropsis sp. ………... ... 57
9. Analisis statistik rancangan acak kelompok………... ... 58
10. Analisis statistik Uji Tukey……… 60
11. Dokumentasi alat dan bahan penelitian………. . 62
1. PENDAHULUAN
1.1 Latar Belakang
Karbondioksida merupakan gas yang bersifat polutif dan banyak dihasilkan
oleh kegiatan industri dan penggunaan kendaraan bermotor. Semakin banyaknya
aktivitas industri dan penggunaan kendaraan bermotor seperti saat ini telah
menyebabkan pencemaran karbondioksida di atmosfer berlangsung setiap waktu.
Hal tersebut berdampak terhadap semakin tingginya akumulasi gas
karbondioksida di atmosfer dan dapat berdampak terhadap terjadinya pemanasan
global yang dapat menyebabkan terjadinya kenaikan suhu permukaan bumi dan
perubahan iklim.
Dibutuhkan sebuah solusi yang tepat dalam mengurangi tingkat akumulasi
gas karbondioksida di atmosfer yang berasal dari pencemaran gas karbondioksida
buangan industri dan penggunaan kendaraan bermotor, salah satu caranya
melalui pendekatan bioteknologi. Pemanfaatan gas karbondioksida yang berasal
dari aktivitas industri dapat dilakukan dengan cara memanfaatkan gas
karbondioksida sebagai bahan pada proses fotosintesis. Sebagaimana diketahui
gas karbondioksida merupakan salah satu bahan utama dalam proses fotosintesis.
Proses pemanfaatan gas karbondioksida oleh organisme yang mampu melakukan
aktivitas fotosintesis dapat dilakukan dengan memberikan gas karbondioksida
secara langsung terhadap organisme tersebut. Salah satu organisme yang dapat
memanfaatkan gas karbondioksida untuk proses fotosintesis adalah mikroalga.
Mikroalga merupakan salah satu organisme tingkat rendah yang termasuk
ke dalam Kingdom Protista yang memiliki kemampuan untuk berfotosintesis.
Selama ini mikroalga banyak digunakanan sebagai bahan farmasi, kosmetik,
pakan alami ikan dan biofuel. Proses produksi biomassa mikroalga dilakukan
dengan proses kultivasi. Pemanfaatan gas karbondioksida dalam proses kultivasi
mikroalga dapat meningkatkan produktivitas mikroalga. Menurut Khoo et al.
(2011) mikroalga dapat mengkonversi cahaya dan karbondioksida menjadi
biomassa secara effisien hal tersebut dikarenakan struktur seluler mikroalga lebih
sederhana dibandingkan dengan tumbuhan tingkat tinggi. Oleh karena itu
mikroalga memiliki potensi untuk mengurangi pemanasan global yang disebabkan
oleh akumulasi gas karbondioksida di atmosfer.
Kultivasi mikroalga dalam penelitian ini dilakukan dengan cara memberikan
gas karbondiokisda murni pada kultivasi di luar ruangan (outdoor). Sistem
kultivasi mikroalga dengan memanfaatkan gas karbondioksida dilakukan terhadap
mikroalga Nannochloropsis sp. Mikroalga jenis Nannochloropsis sp. memimiliki
komposisi asam lemak yang tinggi yang dapat digunakan sebagai bahan pembuatan
biofuel sebagai bentuk solusi dalam mengatasi krisis sumberdaya minyak yang
berasal dari bahan fosil (Kawaroe et al., 2010). Oleh karena itu, penelitian ini
dilakukan untuk mengetahui kemampuan tumbuh mikroalga Nannochloropsis sp.
dalam kultivasi dengan pemanfaatan gas karbondioksida .
1.2 Tujuan
Tujuan dari penelitian ini adalah mengkaji pengaruh pemberian gas
karbondioksida dalam kultivasi outdoorNannochloropsis sp. terhadap laju
2. TINJAUAN PUSTAKA
2.1 Biologi Nannochloropsis sp
Mikroalga adalah tumbuhan tingkat rendah yang memiliki klorofil, yang
dapat digunakan untuk melakukan proses fotosintesis. Mikroalga tidak memiliki
akar, batang dan daun yang terdiferensiasi. Umumnya mikroalga ditemukan di
seluruh habitat di permukaan bumi terutama di ekosistem perairan selain itu dapat
ditemukan juga di atas permukaan tanah yang bersimbiosis dengan berbagai
organisme lainnya (Tomaselli, 2004 :3).
Nannochloropsis sp. merupakan salah satu spesies dari mikroalga laut
yang memiliki sel berwarna kehijauan, pergerakannya tidak motil dan tidak pula
berflagel. Selnya berbentuk bola berukuran kecil dengan diameter 4-6 µm.
Susunan klasifikasi Nannochloropsis sp. yang termasuk ke dalam kelas alga hijau
menurut Adehoog dan Simon (2001) dalam Anon et al. (2009) adalah sebagai
berikut:
Kingdom: Chromista
Filum: Ochrophyta
Kelas: Eustigmatophyceae
Ordo: Eustigmatales
Famili: Eustigmataceae
Genus: Nannochloropsis
Spesies : Nannochloropsis sp.
Nannochloropsis sp memiliki kandungan nutrisi yang terdiri dari
karbohidrat (16 %), lemak (27,64%), protein (52,11%), vitamin C (0,85%) serta
terdiri dari pigmen klorofil-a (Anon et al., 2009). Selain pigmen klorofil-a
Nannochloropsis sp dilengkapi pigmen tambahan violaxanthin yang berfungsi
untuk membantu penyerapan cahaya (Graham dan Wilcox, 2000), astaxanthin dan
canthaxanthin (Hu dan Gao, 2006). Kandungan lipid dari Nannochloropsis sp
cukup tinggi berada pada kisaran 3-68 % (Kawaroe et al., 2010).
Gambar 1. Nannochloropsis sp
Nannochloropsis sp dapat tumbuh optimum pada salinitas 25-35 psu, suhu
25-30 oC , pH 8-9,5 dan intensitas cahaya 100-10000 lux (Anon, 2009).
Nannochloropsis sp memiliki pertumbuhan yang lebih baik dengan aerasi
karbondioksida dibandingkan dengan pemberian aerasi biasa(Chiu et al., 2008).
2.2 Kultivasi Mikroalga
Proses produksi biomassa mikroalga dilakukan dengan cara melakukan
kultivasi. Proses kultivasi mikroalga terdiri dari beberapa tingkatan yaitu;
kultivasi skala laboratorium (5 ml-3 liter), kultivasi skala semi masal (60-100
liter) dan kultivasi skala masal ( > 1 ton) (Isnansetyo et al., 1995). Produktivitas
eksternal (lingkungan). Faktor eksternal yang mempengaruhi kultivasi mikroalga
terdiri dari :
1. Cahaya
Bagi organisme yang melakukan proses fotosintesis seperti mikroalga cahaya
merupakan salah satu faktor penting yang mempengaruhi faktor produktivitas
mikroalga (Wagenen et al., 2012). Intensitas cahaya tinggi menyebabkan laju
fotosintesis yang tinggi begitu pula apabila intensitas cahaya rendah menyebabkan
laju fotosintesis rendah . Nannochloropsis sp dapat tumbuh optimum pada kisaran
intensitas cahaya 100-1000 lux (Anon, 2009).
2. Derajat Keasaman (pH)
Derajat keasaman atau pH menggambarkan variasi ion hidrogen.
Keberagaman nilai hidrogen dalam media kultivasi dapat mempengaruhi
metabolisme dan pertumbuhan mikroalga. Kisaran pH optimum untuk kultivasi
mikroalga Nannochloropsis sp berkisar antara 8,5–9,5 (Anon, 2009)
3. Karbondioksida
Karbondioksida merupakan salah satu bahan utama dalam proses
fotosintesis yang selanjutnya akan diubah menjadi glukosa sebagai asupan
makanan bagi organisme tersebut. Kisaran karbondioksida yang optimum dalam
proses kultivasi mikroalga sebesar 1% sampai 2% dari volume kultivasi.
Kadar karbondioksida yang berlebihan menyebabkan nilai pH rendah yang
akan berdampak terhadap pertumbuhan mikroalga, karena karbondioksida terlarut
dalam air akan membentuk reaksi asam. Pemberian karbondioksida dengan
konsentrasi yang berbeda pada kultivasi mikroalga menghasilkan laju pertumbuhan
4. Nutrien
Nutrien dalam proses kultivasi mikroalga sangat penting bagi pertumbuhan
mikroalga. Kebutuhan nutrien bagi mikroalga yang hidup di alam dapat berasal
dari air sebagai salah satu media tumbuh mikroalga. Kultivasi mikroalga dengan
tujuan pengambilan biomassa mikroalga membutuhkan pertumbuhan yang sangat
baik. Pertumbuhan yang sangat baik dapat dicapai dengan memberikan nutrien
buatan terhadap media kultivasi mikroalga.
Nutrien terdiri atas unsur makro nutrien dan mikro nutrien. Unsur makro
nutrien terdiri atas N (nitrat), F (fosfat), dan C (karbon). Unsur mikro nutrien
terdiri atas Fe (besi), Zn (seng), Cu (tembaga), Mg (magnesium), Mo (molybdate),
Co (kobalt), B (boron), dan lainnya (Cahyaningsih, 2009).
5. Salinitas
Salinitas adalah total kandungan garam yang terlarut dalam air. Menurut Hu
dan Gao (2006) salinitas yang optimum digunakan dalam proses kultivasi mikroalga
Nannochloropsis sp yaitu sebesar 31 psu akan tetapi mikroalga Nannochloropsis sp
masih dapat berkembang pada kisaran salinitas 21-49 psu. Proses pengaturan nilai
salinitas dalam media kultivasi dapat dilakukan dengan melakukan proses
pengenceran dengan menggunakan air tawar.
6. Suhu
Suhu merupakan salah satu bagian parameter fisik perairan yang dapat
mempengaruhi proses fisiologis organisme. Dalam suatu ekosistem perairan,
suhu biasanya dipengaruhi oleh berbagai hal seperti intensitas cahaya matahari,
pertukaran panas antara air dan udara sekelilingnya dan juga faktor kanopi. Suhu
Kisaran suhu optimal dalam proses kultivasi Nannochloropsis sp adalah 25 ± 5°C
(Rocha et al., 2003).
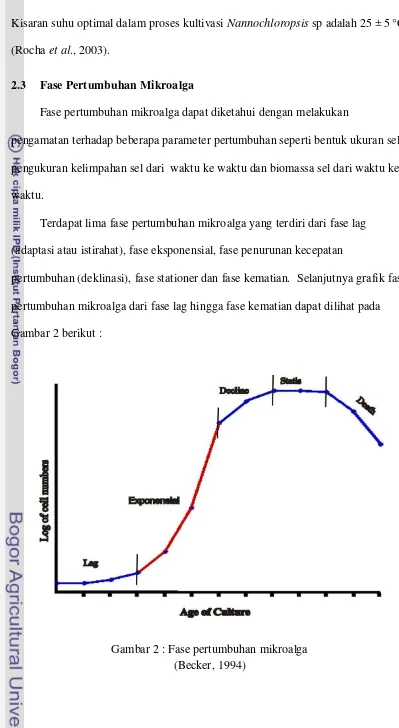
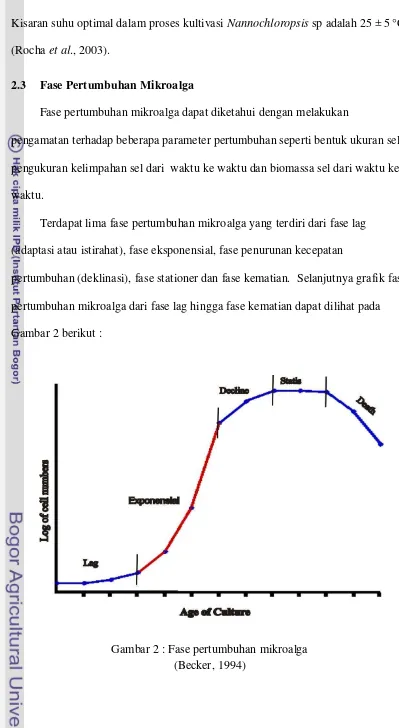
2.3 Fase Pertumbuhan Mikroalga
Fase pertumbuhan mikroalga dapat diketahui dengan melakukan
pengamatan terhadap beberapa parameter pertumbuhan seperti bentuk ukuran sel,
pengukuran kelimpahan sel dari waktu ke waktu dan biomassa sel dari waktu ke
waktu.
Terdapat lima fase pertumbuhan mikroalga yang terdiri dari fase lag
(adaptasi atau istirahat), fase eksponensial, fase penurunan kecepatan
pertumbuhan (deklinasi), fase stationer dan fase kematian. Selanjutnya grafik fase
pertumbuhan mikroalga dari fase lag hingga fase kematian dapat dilihat pada
Gambar 2 berikut :
1. Fase Lag
Fase ini dimulai setelah penambahan inokulan ke dalam media kultivasi
sampai beberapa saat waktu. Pada fase ini mikroalga masih mengalami proses
adaptasi sehingga belum terjadi proses pembalahan sel.
2. Fase Eksponensial (Logaritmik)
Fase ini dimulai dengan pembelahan sel dengan laju pertumbuhan yang
meningkat secara intensif. Bila kondisi kultivasi optimum maka laju pertumbuhan
pada fase ini dapat mencapai nilai maksimum.
3. Fase Deklinasi
Fase ini ditandai oleh pembelahan sel tetap terjadi, namun tidak seintensif
pada fase sebelumnya sehingga laju pertumbuhannya pun menjadi menurun
dibandingkan fase sebelumnya.
4. Fase Stationer
Fase ini ditandai oleh laju reproduksi dan laju kematian relatif sama
sehingga peningkatan jumlah sel tidak lagi terjadi atau tetap sama dengan
sebelumnya (stasioner). Kurva kelimpahan yang dihasilkan dari fase ini adalah
membentuk suatu garis datar, garis ini menandai laju produksi dan laju kematian
sebanding.
5. Fase Kematian
Fase ini ditandai dengan angka kematian yang lebih besar dari pada angka
pertumbuhannya sehingga terjadilah penurunan jumlah kelimpahan sel dalam
wadah kultivasi. Fase ini ditandai dengan perubahan kondisi media seperti warna,
2.4 Pemanfaatan Karbondioksida oleh Mikroalga
Pemanfaatan gas karbondioksida dalam proses kultivasi mikroalga
merupakan salah satu bentuk usaha mitigasi pencemaran gas karbondioksida di
atmosfer. Menurut Benemann (1997), penggunaan karbondioksida pada kultivasi
mikroalga memiliki beberapa keuntungan, karena mikroalga tumbuh di air serta
lebih mudah diamati pertumbuhannya daripada tumbuhan tingkat tinggi, selain itu
mikroalga dapat tumbuh sangat cepat dan mikroalga tidak membutuhkan tempat
atau lahan yang sangat luas untuk tumbuh. Karbondioksida merupakan faktor yang
penting yang dapat mempengaruhi pertumbuhan dan metabolisme mikroalga
(Hoshida et al.,2005).
Gas karbondioksida yang diinjeksikan ke dalam media kultivasi selanjutnya
akan bereaksi dengan air dalam media kultivasi membentuk senyawa asam
karbonat. Asam karbonat selanjutnya akan digunakan sebagai sumber karbon
anorganik dalam proses fotosintesis mikroalga. Pada proses fotosintesis
mikroalga, sumber karbon anorganik yang berasal dari senyawa asam karbonat
dapat dikonversi menjadi biomassa secara efesien, dikarenakan mikroalga memiliki
struktur penyusun tubuh yang lebih sederhana dibandingkan dengan tumbuhan
tingkat tinggi (Khoo et al., 2011).
Pemberian gas karbondioksida berdampak terhadap produktivitas mikroalga,
hal tersebut berdasarkan penelitian yang dilakukan oleh Chiu et al (2008) terhadap
mikroalga spesies Nannochloropsisoculata dan Chlorella vulgaris pemberian gas
karbondioksida dalam konsentrasi (v/v) yang sangat kecil mampu meningkatkan
produktivitas biomassa mikroalga. Selain dapat meningkatkan biomassa
menigkatkan konsentrasi senyawa organik yang dikandung oleh mikroalga seperti
senyawa karbohidrat dan lemak.
Konsentrasi karbondioksida yang dapat dimanfaatkan oleh mikroalga
dengan baik berada pada kisaran 1% - 2% dari total volume kultivasi, pemberian
gas karbondioksida dalam konsentrasi yang berlebih dapat menurunkan
produktivitas mikroalga baik kelimpahan sel maupun biomassa. Menurut Boyd
(1982) konsentrasi karbondioksida terlarut yang telah melebihi nilai 60 mg/L
3.
BAHAN DAN METODE
3.1 Waktu dan Tempat Penelitian
Penelitian ini dilaksanakan pada bulan Januari hingga bulan Juni 2012
bertempat di Laboratorium Kultivasi Mikroalga di Pusat Penelitian Surfaktan dan
Bioenergi (SBRC), Lembaga Penelitian dan Pengabdian kepada Masyarakat,
Institut Pertanian Bogor.
3.2 Alat dan Bahan Penelitian
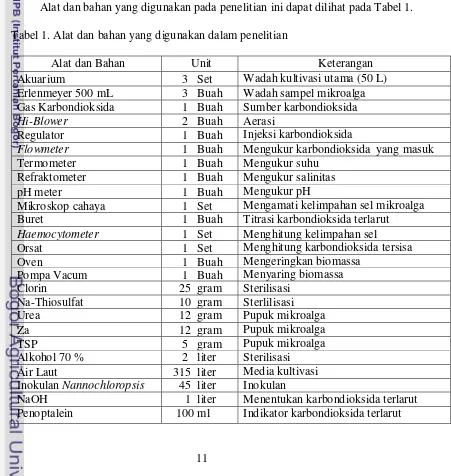
Alat dan bahan yang digunakan pada penelitian ini dapat dilihat pada Tabel 1.
Tabel 1. Alat dan bahan yang digunakan dalam penelitian
Alat dan Bahan Unit Keterangan Penoptalein 100 ml Indikator karbondioksida terlarut
3.3 Persiapan Penelitian
Tahap persiapan penelitian meliputi sterillisasi alat dan bahan, persiapan
inokulan Nannochloropsis sp dan persiapan pupuk.
3.3.1 Sterillisasi
Sebelum melakukan kultivasi mikroalga dilakukan terlebih dahulu
kegiatan sterilisasi terhadap alat dan bahan yang akan digunakan dalam kegiatan
kultivasi. Tujuan dari kegiatan sterilisasi ini adalah untuk membunuh
mikroorganisme yang dapat mengancam keberlangsungan hidup mikroalga
selama proses kultivasi. Pada penelitian ini kegiatan sterilisasi terbagi menjadi
dua yaitu sterilisasi alat dan sterilisasi bahan.
Proses sterilisasi alat kultivasi seperti erlenmeyer, pipet tetes dan alat kaca
lainya dilakukan dengan menggunakan klorin 150 mg/Liter selama 12-24 jam,
kemudian dinetralkan dengan menggunakan NaOH 40-50 mg/Liter dan
selanjutnya dibilas dengan menggunakan air tawar (Isnansetyo et al., 1995).
Setelah dibilas dengan menggunakan air tawar peralatan yang akan digunakan
terlebih dahulu disemprot dengan menggunakan alkohol 70%.
Sterilisasi bahan dilakukan terhadap air laut sebagai media kultur. Air
laut terlebih dahulu disaring dengan menggunakan kain saring, kemudian air hasil
saringan disterilkan dengan menggunakan klorin sebesar 60 ppm. Akhirnya
media air laut diaerasi selama 24 jam, sebelum dinetralkan menggunakan natrium
thiosulfat sebesar 20 ppm (Isnansetyo et al., 1995).
3.3.2 Persiapan Inokulan Nannochloropsis sp
Inokulan Nannochloropsis sp yang digunakan di dalam penelitian ini
dan Bioenergi(SBRC), Lembaga Penelitian dan Pengabdian kepada Masyarakat,
Kampus IPB Baranangsiang. Selanjutnya inokulan tersebut diperbanyak dengan
cara dikultivasi sebagai inokulan yang akan digunakan pada penelitian utama.
Inokulan yang digunakan pada masing-masing ulangan dalam setiap perlakuan
sebanyak 5 Liter.
3.3.3 Persiapan Pupuk
Pupuk bersifat sebagai sumber nutrien bagi pertumbuhan mikroalga. Pada
kultivasi mikroalga skala outdoor pupuk yang digunakan adalah jenis Urea, ZA
dan TSP dengan konsentrasi masing-masing sebesar 30 ppm Urea , 30 ppm ZA,
dan 12 ppm untuk pupuk TSP.
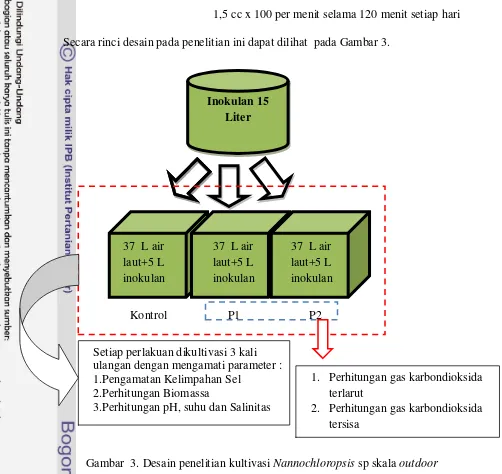
3.4 Desain Penelitian
Kultivasi mikroalga pada skala outdoor merupakan bagian utama dari
penelitian ini. Kultivasi skala outdoor dilakukan pada akuarium berukuran 100 cm x
50 cm x 100 cm. Kultivasi dilakukan selama 9 hari pada volume 42 liter. Kultivasi
pada skala outdoor ini menggunakan rancangan percobaan rancangan acak
kelompok yang terdiri atas 3 perlakuan sebanyak 3 kali ulangan, dengan rincian
sebagai berikut :
1. Kontrol (K) :Perlakuan dengan memberikan
aerasi ke dalam media kultivasi Nannochloropsis sp
selama 24 jam.
2. Perlakuan 1 (P1) :Perlakuan dengan memberikan gas karbondioksida
ke dalam media kultivasi Nannochloropsis sp
dengan konsentrasi 1 cc x 100 per menit selama
3. Perlakuan 2 (P2) :Perlakuan dengan memberikan gas
karbondioksida ke dalam media kultivasi
Nannochloropsis sp dengan konsentrasi sebesar
1,5 cc x 100 per menit selama 120 menit setiap hari Secara rinci desain pada penelitian ini dapat dilihat pada Gambar 3.
Gambar 3. Desain penelitian kultivasi Nannochloropsis sp skala outdoor
3.5 Pengamatan Pertumbuhan Nannochloropsis sp. 3.5.1 Kelimpahan Sel
Kelimpahan sel Nannocloropsis sp. dari setiap ulangan pada setiap
perlakuan dihitung setiap hari dengan menggunakan Haemocytometer dan
Kontrol P1 P2
Setiap perlakuan dikultivasi 3 kali ulangan dengan mengamati parameter : 1.Pengamatan Kelimpahan Sel
2.Perhitungan Biomassa
3.Perhitungan pH, suhu dan Salinitas
1. Perhitungan gas karbondioksida terlarut
mikroskop. Sel yang tercacah selanjutnya dihitung dengan menggunakan formula
ImprovedNeubaeur Haemocytometer sebagai berikut :
Keterangan :
n = Jumlah sel yang teramati
Contoh perhitungan kelimpahan sel yang tercacah selanjutnya terdapat pada
Lampiran 1.
3.5.2Biomassa
Biomassa Nannochloropsis sp dihitung setiap hari dengan menggunakan
metode gravimetrik (Banse et al.,1963). Sebanyak 500 ml sampel air yang berisi
Nannochloropsis sp., sebelumnya diberi tawas sebanyak 250 ppm yang bertujuan
untuk mengendapkan sel Nannochloropsis sp.. Setelah sel Nannochloropsis sp.
mengendap air yang berisi sel Nannochloropsis sp. tersebut disaring dengan
menggunakan kertas saring berdiameter 90 mm yang telah diketahui bobot
awalnya. Proses penyaringan dilakukan dengan menggunakan pompa vakum.
Setelah proses penyaringan selesai kertas saring dikeringkan dalam oven selama 2
jam dengan suhu 60 °C. Setelah proses pengeringan selesai kertas saring
selanjutnya ditimbang. Biomassa mikroalga yang tersaring dihitung dengan
menggunakan persamaan berikut (Lin et al., 2012) :
Biomassa (gr/L) = − 1000
ml sampel ………(2) Keterangan :
= Bobot kertas saring setelah dilakukan penyaringan (gr)
= Bobot kertas saring sebelum dilakukan penyaringan (gr) Kelimpahan sel (sel/ml) = n x 25
5 x10
3.5.3Pengukuran Kualitas Air
Parameter kualitas air yang diamati terdiri dari salinitas, suhu dan pH.
Pengambilan data salinitas dilakukan menggunakan hand refraktometer ,
pengambilan data suhu dilakukan menggunakan thermometer dan pH dilakukan
dengan menggunakan pH meter.
3.5.4 Karbondioksida terlarut dalam media kultivasi
Kandungan karbondioksida yang terlarut di dalam air dapat dihitung dengan
menggunakan metode titrasi (titrimetri) (Boyd,1982). Sebanyak 50 ml sampel air
mikroalga yang akan dianalisis kandungan karbondioksida terlarut diberi indikator
penoptalein untuk menentukan adanya gas karbondioksida yang terlarut.
Sampel air dikatakan mengandung gas karbondioksida terlarut, jika setelah
ditetesi penoptalein tidak mengalami perubahan warna. Selanjutnya sampel air
yang mengandung karbondioksida terlarut dititrasi dengan menggunakan larutan
NaOH 0,0227 N sampai terjadi perubahan warna menjadi merah muda, lalu catat
banyak titran yang digunakan. Nilai konsentrasi karbondioksida terlarut dihitung
dengan rumus (Boyd,1982)
ml titran = Volume titran NaOH yang terpakai (ml)
N titrant = Nilai konstanta (0,0227) N
3.5.3 Konsentrasi Karbondioksida Tersisa
Pada proses kultivasi mikroalga dengan menggunakan gas karbondioksida,
gas karbondioksida yang diberikan tidak semuanya terserap. Tentunya terdapat gas
karbondioksida yang tidak terserap, selanjutnya gas karbondioksida yang tidak
terserap ini dapat dikarakan sebagai gas karbondioksida tersisa.
Setiap akuarium dihubungkan dengan selang yang telah terhubung ke dalam
kantong plastik. Kantong plastik ini berfungsi sebagai tempat menampung gas
karbondioksida yang tidak digunakan dalam proses kultivasi mikroalga. Gas
karbondioksida yang ada didalam kantong plastik tersebut selanjutnya akan
dihitung dengan menggunakan alat bantu bernama orsat. Prosedur penentuan
karbondioksida yang tersisa dengan menggunakan orsat terdapat pada
Lampiran 3. Penggunaan alat bantu orsat ini akan menghasilkan nilai kandungan
gas karbondioksida yang tersisa dalam bentuk persen sesuai dengan angka yang
ditunjukan pada skala dalam salah satu tabung yang terdapat pada orsat.
3.6 Analisis Data
3.6.1 Laju Pertumbuhan Spesifik
Laju pertumbuhan spesifik kelimpahan sel Nannocloropsis sp dihitung
dengan menggunakan persamaan berikut (Krichnavaruk et al.,2004) :
Dimana :
µ = Laju pertumbuhan kelimpahan sel (sel /ml/hari)
N0 = Kelimpahan sel Nannocloropsis sp. pada awal kultivasi (sel/ml)
Nt = Kelimpahan sel Nannocloropsis sp. padaakhir kultivasi(sel/ml)
t = Selang waktu dari N0 ke Nt (hari)
3.6.2 Laju Pertumbuhan Biomassa
Laju pertumbuhan biomassa Nannocloropsis sp. dihitung dengan
menggunakan persamaan berikut (Chiu et al, 2008):
Dimana :
µ = Laju pertumbuhan biomassa ( gr/l/hari)
W0 = Biomassa sel Nannocloropsis sp. padaawal kultivasi (gr/l)
Wt = Biomassa sel Nannocloropsis sp.padaakhir kultivasi (gr/l)
t = Selang waktu dari W0 ke Wt (hari)
3.6.3 Analisis Statistik
Hasil penelitian ini diuji secara statistik untuk mengetahui pengaruh
perbedaan tiap perlakuan dengan kontrol. Analisis sidik ragam yang digunakan
yaitu metode rancangan acak kelompok (Matjik dan Sumertajaya, 2006)
Yij = a + Pi+βi + єij....(6)
Keterangan
Yij = nilai pengamatan pada perlakuan ke-i, kelompok ke-j
a = rataan umum populasi
Pi = pengaruh aditif perlakukan kontrol
βi = pengaruh aditif perlakuan pemberian gas karbondioksida
Єij = galat percobaan
4. HASIL DAN PEMBAHASAN
4.1 Kelimpahan Sel dan Laju Pertumbuhan Spesifik Nannochloropsis sp.
Kelimpahan sel dan laju pertumbuhan spesifik Nannochloropsis sp. pada
perlakuan kontrol, P1 dan P2 memperlihatkan hasil yang berbeda. Kelimpahan
sel Nannochloropsis sp. pada perlakuan kontrol memiliki kelimpahan awal sel
sebesar 1,98×106 sel/ml, perlakuan P1 memiliki kelimpahan awal sel sebesar
1,47x106 sel/ml dan perlakuan P2 memiliki kelimpahan awal sel sebesar
2,38x106 sel/ml. Data kelimpahan sel dan laju pertumbuhan spesifik
Nannochloropsis sp. dapat dilihat pada Tabel 2.
Tabel 2. Kelimpahan sel (×106 sel/mL) dan laju pertumbuhan spesifik
Nannochloropsis sp.
K : Perlakuan kontrol dengan pemberian aerasi
P1 : Pemberian gas karbondioksida sebesar 1 cc x 100/menit selama 120 menit/ hari P2 : Pemberian gas karbondioksida sebesar 1,5 cc x 100/menit selama 120 menit/ hari
Perbedaan kelimpahan sel pada awal kultivasi dalam setiap perlakuan
dikarenakan inokulan yang dimasukan ke dalam setiap perlakuan berasal dari
kultur inokulan yang berbeda. Hal tersebut dilakukan karena kultivasi pada setiap
perlakuan tidak dilakukan secara bersamaan.
Berdasarkan data pada tabel 2, dapat dilihat bahwasannya kelimpahan laju
pertumbuhan kelimpahan sel Nannochloropsis sp. pada perlakuan kontrol secara
umum memiliki laju pertumbuhan kelimpahan sel yang rendah dibandingkan
dengan perlakuan pemberian gas karbondioksida. Hal tersebut diduga bahwa
karbondioksida yang diberikan berfungsi sebagai bahan utama dalam proses
fotosintesis mikroalga sehingga dapat meningkatkan laju proses fotosintesis yang
mengakibatkan meningkatnya kelimpahan sel Nannochloropsis sp.. Hal tersebut
sesuai dengan hasil penelitian yang dilakukan oleh Chiu et al. (2008) pemberian
gas karbondioksida pada kultivasi Nannochloropsis sp. dengan konsentrasi 5%
(v/v) mampu meningkatkan jumlah kelimpahan sel Nannochloropsis sp. hingga
50 % dibandingkan dengan kelimpahan sel Nannochloropsis sp. yang hanya
diberi perlakuan aerasi.
4.1.1 Kelimpahan Sel dan Laju Pertumbuhan Spesifik Nannochloropsis sp Perlakuan Kontrol
Kelimpahan sel Nannochloropsis sp terus mengalami peningkatan dari
awal kultivasi hingga hari ke-6 kultivasi. Kelimpahan sel Nannochloropsis sp.
pada perlakuan kontrol mencapai puncak kelimpahan sel pada hari ke-6 kultivasi
dengan nilai sebesar 10,23 x 106 sel/ml. Hal tersebut menunjukkan terjadinya
perubahan fase pertumbuhan dari fase lag pada awal kultivasi. Nilai laju
ke-3 kultivasi. Hal tersebut didukung oleh faktor fisika kimia perairan yang
mendukung pertumbuhan mikroalga, dengan suhu rata-rata pada media kultivasi
sebesar 29 oC dan pH rata-rata sekitar 8,5.
Puncak kelimpahan sel pada perlakuan kontrol merupakan puncak
kelimpahan sel terendah dibandingkan dengan puncak kelimpahan sel pada
perlakuan dengan pemberian gas karbondioksida. Puncak kelimpahan sel
Nannochloropsis sp. pada perlakuan P1 memiliki puncak kelimpahan sel sebesar
14,52 x 106 sel/ml pada hari ke-5, sedangkan pada perlakuan P2 memiliki
puncak kelimpahan sel sebesar 11,30 x 106 sel/ml pada hari ke- 5 kultivasi.
Setelah mencapai puncak kelimpahan sel pada hari ke-6, pertumbuhan
mikroalga terus mengalami perlambatan pertumbuhan. Fase stasioner diduga terjadi
kurang dari waktu 24 jam, sehingga setelah mengalami fase perlambatan
pertumbuhan mikroalga selanjutnya mengalami fase kematian. Penurunan
pertumbuhan mikroalga Nannochloropsis sp. diduga akibat semakin menurunnya
jumlah nutrien dalam media kultivasi yang telah habis digunakan pada saat jumlah
Nannochloropsis sp. meningkat. Pemberian nutrien dalam proses kultivasi ini
hanya diberikan satu kali pada masa awal kultivasi. Nutrien merupakan salah satu
faktor penting yang dapat memacu pertumbuhan mikroalga.
4.1.2 Kelimpahan Sel dan Laju Pertumbuhan Spesifik Nannochloropsis sp. Perlakuan P1
Pada kultivasi mikroalga perlakuan P1, kelimpahan sel pada masa awal
kultivasi sebesar 1,47 x 106 sel/ml dan terus mengalami peningkatan kelimpahan
sel hingga mencapai puncak kelimpahan sel pada hari ke-5 kultivasi sebesar
pertumbuhan dari fase lag pada awal kultivasi menjadi fase eksponensial. Nilai
laju pertumbuhan maksimum µ= 1,07 teramati pada hari ke-1 kultivasi. Puncak
kelimpahan sel pada perlakuan ini merupakan puncak kelimpahan sel terbesar
dibandingkan dua perlakuan lainnya.
Setelah mencapai puncak kelimpahan sel pada hari ke-5. Pertumbuhan
mikroalga terus mengalami penurunan dan kemudian mengalami fase kematian.
Penurunan pertumbuhan mikroalga Nannochloropsis sp. diduga disebabkan oleh
semakin menurunnya jumlah nutrien pada media kultivasi karena nutrien hanya
diberikan satu kali di awal kultivasi, selain faktor nutrien kandungan
karbondioksida terlarut yang melebihi nilai 60 mg/L dapat menghambat
pertumbuhan organisme akuatik (Boyd, 1988 dalam Effendi, 2003). Nilai
konsentrasi karbondioksida terlarut telah melebihi kisaran nilai 60 mg/L sejak
hari ke-4 kultivasi. Secara rata-rata kandungan karbondioksida terlarut pada
perlakuan ini berada pada kisaran 58,8 mg/L. Nilai karbondioksida terlarut
mempengaruhi nilai pH media kultivasi, secara umum kisaran pH berada pada
rentang 6,1-7,4.
Pada perlakuan P1 memiliki puncak kelimpahan sel tertinggi dibandingkan
dengan perlakuan lainnya. Hal tersebut diduga karena pada perlakuan P1
mikroalga mampu menyerap gas karbondioksida dengan baik, hal tersebut terbukti
pada konsentrasi gas karbondioksida yang tersisa dari total gas karbondioksida
yang diinjeksikan yaitu pada kisaran 2% - 5%. Suhu merupakan salah satu faktor
yang mempengaruhi proses penyerapan gas karbondioksida oleh suatu organisme
fotosintesis (Salisbury,1995). Pada perlakuan P1 nilai suhu rata-rata kultivasi
organisme yang dapat mengkonversi gas karbondioksida secara efesien (Khoo et
al., 2011). Pemberian gas karbondioksida pada proses kultivasi mikroalga dapat
dijadikan sebagai bahan dalam proses fotosintesis sehingga dapat meningkatkan
pertumbuhan mikroalga (Lin et al.,2012).
4.1.3 Kelimpahan Sel dan Laju Pertumbuhan Spesifik Nannochloropsis sp. Perlakuan P2
Kelimpahan sel Nannochloropsis sp. pada perlakuan P2 di awal kultivasi
yaitu sebesar 2,38 x 106 sel/ml dan terus mengalami peningkatan kelimpahan sel
hingga mencapai puncak kelimpahan sel pada hari ke-5 sebesar 11,30 x 106 sel/ml.
Hal tersebut menunjukkan adanya perubahan fase pertumbuhan dari fase lag di awal
kultivasi menuju fase eksponensial. Nilai laju pertumbuhan maksimum µ= 0,70
pada hari ke-2 kultivasi.
Setelah mencapai puncak kelimpahan sel laju pertumbuhan mikroalga terus
mengalami penurunan dan mengalami fase kematian. Kultivasi pada perlakuan ini
memiliki kelimpahan sel jauh lebih baik dibandingkan dengan perlakuan kontrol
tetapi tidak lebih baik dengan perlakuan P1.
Pada perlakuan P2 menyebabkan konsentrasi gas karbondioksida yang
terlarut jauh lebih besar dibandingkan dengan perlakuan P1. Rata-rata nilai
karbondioksida terlarut selama kultivasi sebesar 74,17 mg/L, nilai konsentrasi
tersebut telah melebihi batas nilai konsentrasi yang dapat ditolerir bagi
pertumbuhan organisme akuatik sebesar 60 mg/L (Boyd, 1988 dalam Effendi,
2003). Hal tersebut diduga menyebabkan pertumbuhan Nannochloropsis sp.
lebih rendah dibandingkan dengan pertumbuhan Nannochloropsis sp. pada
yang rendah memiliki efesiensi lebih baik dalam mendukung pertumbuhan
mikroalga dibandingkan dengan pemberian gas karbondioksida dengan konsentrasi
yang lebih tinggi.
4.2 Biomassa dan Laju Pertumbuhan Biomassa Nannochloropsis sp.
Biomassa Nannochloropsis sp. pada perlakuan kontrol, P1 dan P2
memperlihatkan hasil yang berbeda. Perlakuan kontrol memiliki biomassa awal
sebesar 0,15 gr/L, perlakuan P1 memiliki biomassa awal sebesar 0,20 gr/L dan
perlakuan P2 memiliki biomassa awal sebesar 0,25 gr/L. Grafik biomassa dan laju
pertumbuhan Nannochloropsis sp. dapat dilihat pada Tabel 3
Tabel 3. Biomassa (gr/l) dan laju pertumbuhan biomassa (μ) Nannochloropsis sp.
Hari Kontrol P1 P2
K : Perlakuan kontrol dengan pemberian aerasi
P1 : Pemberian gas karbondioksida sebesar 1 cc x 100/menit selama 120 menit/ hari P2 : Pemberian gas karbondioksida sebesar 1,5 cc x 100/menit selama 120 menit/ hari
Secara umum berdasarkan data pada tabel 3, perlakuan dengan pemberian
dengan perlakuan kontrol. Pemberian gas karbondioksida pada proses kultivasi
mikroalga dapat dijadikan sebagai bahan fotosintesis yang akan difiksasi dan
selanjutnya dikonversi menjadi biomassa (Lin et al., 2012).
4.2.1 Biomassa dan Laju Pertumbuhan Biomassa Nannochloropsis sp. Perlakuan Kontrol
Biomassa Nannochloropsis sp. pada massa awal kultivasi sebesar 0,15 gr/L,
nilai biomassa terus mengalami peningkatan hingga hari ke -4 dengan nilai laju
pertumbuhan terbesar sebesar μ = 0,30 gr/L pada hari ke-4 kultivasi.
Peningakatan biomassa Nannochloropsis sp. dari massa awal kultivasi hingga hari
ke-4 kultivasi telah menunjukkan adanya perubahan fase pertumbuhan dari fase
lag menuju fase eksponensial.
Pada hari ke-5 kultivasi biomassa mikroalga mengalami penurunan sebesar
0,03 gr/L, hal ini diduga menunjukkan mulai terjadinya fase perlambatan
pertumbuhan pada Nannochloropsis sp.. Puncak biomassa mikroalga
Nannochloropsis sp terjadi pada hari ke-6 kultivasi sebesar 0,34 gr/L dengan nilai
laju pertumbuhan biomassa µ= 0,21 gr/L/hari. Fase stasioner dari pertumbuhan
mikroalga ini diduga terjadi dalam waktu kurang dari 24 jam sehingga setelah
mencapai puncak biomassa mikroalga yang terlihat hanya fase perlambatan
pertumbuhan yang bergerak menuju fase kematian. Penurunan biomassa mikroalga
ini tentunya tidak terlepas oleh pengaruh dari kelimpahan sel yang ikut mengalami
penurunan pertumbuhan. Biomassa mikroalga pada massa akhir kultivasi mencapai
4.2.2 Biomassa dan Laju Pertumbuhan Biomassa Nannochloropsis sp. Perlakuan P1
Pada kultivasi mikroalga Nannochloropsis sp. dengan perlakuan P1,
biomassa mikroalga pada masa awal kultivasi sebesar 0,25 gr/L dan terus
mengalami peningkatan biomassa hingga hari ke-5 kultivasi sebesar 0,45 gr/L.
Hal ini menunjukkan adanya perubahan fase pertumbuhan mikroalga
Nannochloropsis sp. dari fase lag menuju fase eksponensial. Nilai laju
pertumbuhan biomassa maksimum sebesar μ = 0,46 gr/L/hari pada hari ke-4
kultivasi. Nilai biomassa maksimum pada perlakuan ini merupakan nilai
biomassa maksimum dari ke-3 perlakuan yang dilakukan, hal ini tidak jauh
berbeda antara kelimpahan sel dimana nilai kelimpahan sel maksimum dari
seluruh perlakuan ada pada perlakuan ini. Secara rata-rata pada perlakuan dengan
pemberian gas karbondioksida sebesar 120 cc/hari mampu meningkatkan
biomassa hingga 31 % dari perlakuan kontrol.
Berdasarkan penelitian yang dilakukan oleh Chiu et al. (2008) perlakuan
pemberian gas karbondioksida pada konsentrasi 2 % (v/v) terhadap
Nannochloropsis sp. memiliki hasil biomassa yang lebih baik dengan nilai
produktivitas biomassa sebesar 0,48 gr/L/hari dibandingkan dengan pemberian
gas karbondioksida pada konsentrasi 5 % (v/v) yang memiliki produktivitas
biomassa sebesar 0,37 gr/L/hari. Hasil penelitian yang dilakukan oleh Chiu et al.
(2008) terhadap mikroalga lain jenis Chorella sp. menunjukkan bahwa dengan
pemberian gas karbondioksida yang terlalu berlebih menghasilkan produktivitas
biomassa yang lebih rendah.
Setelah mencapai puncak biomassa pada hari ke-5, pertumbuhan
kematian. Nilai biomassa pada akhir kultivasi mikroalga sebesar 0,17 gr/L
dengan nilai konstanta laju pertumbuhan biomassa mikroalga mengalami
penurunan sebesar -0,50 gr/L/hari. Penurunan pertumbuhan biomassa mikroalga
Nannochloropsis sp. disebabkan oleh semakin menurunnya kelimpahan sel yang
diduga oleh semakin menurunya jumlah nutrien pada media kultivasi, selain
faktor nutrien kandungan karbondioksida terlarut yang telah melebihi nilai kisaran
60 gr/L dapat menghambat pertumbuhan organisme akuatik ( Boyd , 1988 dalam
Effendi, 2003).
4.2.3 Biomassa dan Laju Pertumbuhan Biomassa Nannochloropsis sp. Perlakuan P2
Biomassa mikroalga Nannochloropsis sp. pada perlakuan P2 di awal
kultivasi yaitu sebesar 0,25 gr/L. Pada hari pertama kultivasi biomassa mikroalga
mengalami penurunan sebesar 0,01 g/L. Hal tersebut sangat mungkin terjadi
dikarenakan mikroalga masih mengalami fase lag di dalam media kultivasi, yang
artinya mikroalga masih beradapatasi dengan kondisi lingkungan sekitar. Pada
hari ke-2 kultivasi mikroalga mengalami peningkatan biomassa menjadi 0,26 gr/L
dan terus mengalami peningkatan biomassa hingga mencapai puncak biomassa
pada hari ke-7 yaitu sebesar 0,40 gr/L dengan nilai laju pertumbuhan maksimum
sebesar μ= 0,14 gr/L/hari pada hari ke-5 kultivasi. Secara rata-rata pada
perlakuan P2 mampu meningkatkan biomassa hingga 27 % dari perlakuan
kontrol.
Setelah mencapai puncak biomassa pada hari ke-6, pertumbuhan biomassa
mikroalga terus mengalami penurunan dan kemudian mengalami fase kematian
konstanta laju pertumbuhan biomassa mikroalga mengalami penurunan sebesar
-0,10 gr/L/hari. Penurunan pertumbuhan biomassa mikroalga Nannochloropsis sp.
diduga disebabkan oleh semakin menurunnya kelimpahan sel yang disebabkan
oleh semakin menurunya jumlah nutrien pada media kultivasi, dan jumlah
konsentrasi karbondioksida yang telah melebihi batas toleransi organisme
terhadap kandungan karbodioksida terlarut sehingga dapat mengganggu
pertumbuhan mikroalga.
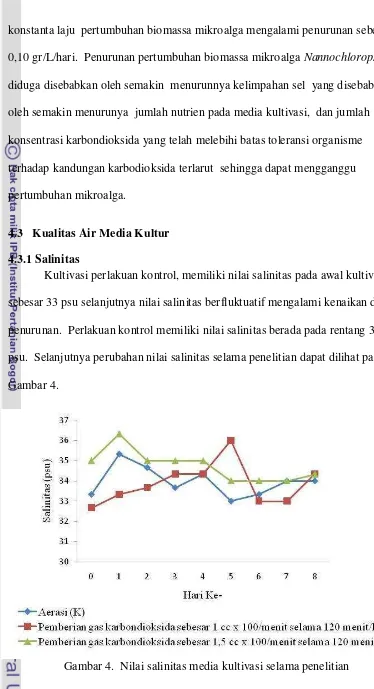
4.3 Kualitas Air Media Kultur 4.3.1 Salinitas
Kultivasi perlakuan kontrol, memiliki nilai salinitas pada awal kultivasi
sebesar 33 psu selanjutnya nilai salinitas berfluktuatif mengalami kenaikan dan
penurunan. Perlakuan kontrol memiliki nilai salinitas berada pada rentang 33-35
psu. Selanjutnya perubahan nilai salinitas selama penelitian dapat dilihat pada
Gambar 4.
Perlakuan P1 memiliki rentang nilai salinitas 32-36 psu dengan nilai
salinitas di awal kultivasi sebesar 33 psu dan terus mengalami peningkatan nilai
salinitas hingga hari ke-5 kultivasi sebesar 36 psu, hal ini diduga mendukung
pertumbuhan mikroalga. Hal tersebut terbukti dengan adanya peningkatan
kelimpahan sel hingga hari ke-5 kultivasi.
Nilai salinitas optimum bagi pertumbuhan mikroalga berada pada kisaran
31 psu dan dapat terus menerus berkembang hingga kisaran salinitas 22-49 psu
(Hu dan Gao, 2006). Kultivasi mikroalga dengan perlakuan P2 memiliki rentang
nilai salinitas 33-36 psu dengan nilai salinitas di awal kultivasi sebesar 35 psu dan
mengalami kenaikan pada hari pertama kultivasi yaitu menjadi 36 psu, setelah itu
nilai salinitas mengalami penurunan.
Secara keseluruhan pada penelitian ini menunjukkan bahwa mikroalga
Nannochloropsis sp mampu hidup pada nilai salinitas yang berfluktuatif.
Fluktuatif nilai salinitas pada media kultivasi mikroalga dipengaruhi oleh
berbagai faktor diantaranya proses metabolisme sel, pengendapan garam dan
nutrient dalam media kultivasi (Rostini, 2007).
4.3.2 Suhu
Besaran nilai suhu di dalam kultivasi mikroalga pada skala outdoor salah
satunya dipengaruhi oleh radiasi yang berasal dari sinar matahari. Perlakuan aerasi
yang bersifat sebagai kontrol memiliki nilai suhu sebesar 29 o C sejak awal kultivasi
hingga hari ke-5, setelah itu nilai suhu mengalami penurunan suhu pada hari ke-6
kultivasi menjadi 26 o C, pada hari selanjutnya suhu menjadi 29 oC dan selanjutnya
27 oC. Fluktuatifnya nilai suhu pada perlakuan kontrol dikarenakan selama masa
kultivasi perlakuan kontrol kondisi cuaca tidak menentu. Secara umum fluktuasi
nilai suhu pada media kultivasi selama penelitian dapat dilihat pada Gambar 5.
Gambar 5. Nilai suhu media kultivasi selama penelitian
Perlakuan P1 memiliki nilai suhu pada kisaran 27-30 oC, secara rata-rata
suhu pada perlakuan ini selama kultivasi sebesar 29 oC. Hal tersebut dikarenakan
sinar matahari pada berlangsungnya perlakuan dengan perlakuan P1 cukup terik di
siang hari. Suhu selama kultivasi pada perlakuan P2 berada pada kisaran 25-30 oC,
secara rata-rata suhu pada perlakuan ini selama kultivasi sebesar 28 oC. Sama halnya
dengan perlakuan kontrol pada kultivasi dengan perlakuan ini kondisi cuaca tidak
menentu, hal ini tentunya menyebabkan nilai suhu memiliki kisaran yang cukup
besar. Secara kesuluruhan kisaran suhu pada media kultivasi Nannochloropsis sp.
berada pada kisaran suhu optimum bagi pertumbuhan Nannochloropsis sp.. Menurut
Rocha et al. (2003) kisaran suhu optimal dalam proses kultivasi mikroalga
4.3.3 Derajat Keasaman (pH)
Selama proses kultivasi perlakuan aerasi memiliki kisaran nilai pH pada
kisaran 8,2-8,9, nilai tersebut menunjukkan bahwa nilai pH berada dalam kondisi basa.
Nilai pH pada kisaran tersebut mendukung bagi pertumbuhan mikroalga, nilai pH
optimum pada bagi pertumbuhan Nannochloropsis sp berada pada kisaran 8,5-9,5
(Anon, 2009). Nilai pH selama kultivasi mikroalga dapat dilihat pada Tabel 4.
Keterangan :
K : Perlakuan kontrol dengan pemberian aerasi
P1 : Pemberian gas karbondioksida sebesar 1 cc x 100/menit selama 120 menit/ hari P2 : Pemberian gas karbondioksida sebesar 1,5 cc x 100/menit selama 120 menit/ hari
Perlakuan dengan pemberian gas karbondioksida pada media kultivasi
menyebabkan terbentuknya asam karbonat setelah gas karbondioksida diberikan. Hal
tersebut terbukti dengan kondisi pH pada perlakuan pemberian gas karbondioksida,
secara umum pH berada dalam kondisi asam pada rentang 5,6 – 7,3. Nilai pH akan
kembali normal kembali di pagi hari sebelum gas karbondioksida diberikan pada
rentang nilai pH 7,90 – 8,37.
P1 P2
Hari Kontrol Sebelum Sesudah Sebelum Sesudah
ke- Diberi CO2 Diberi CO2 Diberi CO2 Diberi CO2
Nilai pH setelah diberikan gas karbondioksida pada perlakuan P1 terdapat
pada rentang 6,1-7,3. Sedangkan nilai pH sebelum diberikan gas karbondioksida
berada pada rentang 7,9-8,3. Fluktuasi nilai pH setelah diberikan gas
karbondioksida dipengaruhi oleh karbondioksida yang dienjeksikan pada media
kultivasi. Semakin banyak konsentrasi karbondioksida terlarut yang digunakan
dalam proses fotosintesis mikroalga, maka nilai pH akan mengalami kenaikan
(Sze, 1993 dalam Prihantini et al., 2005). Pada saat mikroalga Nannochloropsis
sp. mencapai puncak kelimpahan sel, kondisi pH berada dalam kondisi netral
sebesar 7,4 setelah diberikan gas karbondioksida, dan berada pada nilai pH 8,13
sebelum gas karbondioksida diberikan.
Perlakuan P2 memiliki nilai pH media kultivasi sebelum diberi gas
karbondioksida berada pada rentang 7,9-8,3 selanjutnya setelah diberikan gas
karbondioksida berada pada kisaran 5,6- 6,8. Nilai kisaran pH setelah diberikan
gas karbondioksida pada perlakuan ini secara umum berada dalam kondisi yang
jauh lebih asam jika dibandingkan dengan perlakuan P1. Hal tersebut
dikarenakan konsentrasi gas karbondioksida yang diberikan lebih besar, sehingga
pH media kultivasi lebih asam dibandingkan dengan perlakuan P1. Kondisi pH
asam mengakibatkan proses metabolisme sel terganggu sehingga mempengaruhi
kelimpahan sel (Lane, 1981 dalam Prihantini et al., 2005). Hal tersebut diduga
sebagai penyebab kelimpahan sel pada perlakuan P2 tidak lebih baik
4.4 Parameter Karbondioksida
4.4.1 Karbondioksida Terlarut dalam Media Kultivasi
Karbondioksida yang diberikan setiap harinya ke dalam media kultivasi,
selain berasal dari gas karbondioksida yang diberikan sumber karbondioksida
lainnya berasal dari hasil respirasi mikroalga Nannochloropsis sp.. Mikroalga
Nannochloropsis sp. merupakan salah satu spesies mikroalga yang dapat tumbuh
dengan baik pada kultur dengan pemberian gas karbondioksida (Chiu et al., 2008)
Nilai karbondioksida terlarut hanya diukur pada perlakuan pemberian gas
karbondioksida saja.
Nilai karbondioksida terlarut dalam media kultivasi dapat dilihat pada
Gambar 6 :
Gambar 6. Nilai karbondioksida terlarut selama penelitian
Pada perlakuan P1 memiliki nilai karbondioksida terlarut berada pada rentang
11,31- 76 mg/L. Ketika awal masa kultivasi nilai karbondioksida terlarut sebesar
11,31 mg/L nilai tersebut cenderung mengalami kenaikan pada hari-hari
setiap hari, selain itu juga pengaruh dari hasil respirasi mikroalga menyebabkan
nilai karbondioksida terlarut ikut bertambah setiap harinya. Nilai karbondioksida
terlarut pada puncak kelimpahan sel berada pada konsentrasi 69,58 mg/L, nilai
tersebut masih dapat ditolerir bagi pertumbuhan organisme akuatik (Boyd , 1988
dalam Effendi, 2003). Setelah mencapai puncak kelimpahan sel, nilai
karbondioksida terlarut terus mengalami peningkatan. Hal tersebut diduga karena
gas karbondioksida yang diberikan ke dalam media kultivasi tidak termanfaatkan
seluruhnya dalam proses fotosintesis mikroalga, dikarenakan kelimpahan sel
mikroalga yang mengalami penurunan selain itu juga nilai karbondioksida terlarut
dipengaruhi oleh gas karbondioksida hasil respirasi mikroalga.
Pada perlakuan P2, nilai karbondioksida terlarut berada pada rentang 29,43-
77 mg/L Pada awal masa kultivasi nilai karbondioksida terlarut sebesar 29,43
mg/L sama halnya dengan perlakuan pemberian gas karbondioksida dengan
konsentrasi P1, nilai tersebut cenderung mengalami kenaikan pada hari-hari
berikutnya. Hal tersebut dikarenakan pemberian gas karbondioksida dilakukan
setiap hari, selain itu pengaruh dari hasil respirasi mikroalga menyebabkan nilai
karbondioksida terlarut ikut bertambah setiap harinya. Nilai karbondioksida
terlarut pada puncak kelimpahan sel berada pada konsentrasi 54,93 mg/L, nilai
tersebut masih dapat ditolerir bagi pertumbuhan organisme akuatik (Boyd , 1988
dalam Effendi, 2003). Setelah mencapai puncak kelimpahan sel, nilai
karbondioksida terlarut terus mengalami peningkatan. Hal tersebut memicu
terjadinya penurunan kelimpahan sel karena karbondioksida terlarut yang
berlebih dapat mengganggu proses metabolisme sel. Pada massa akhir kultivasi
ditolerir bagi pertumbuhan organisme akuatik, konsentrasi sebesar itu dapat
bersifat toksik bagi organisme akuatik.
4.4.2 Konsentrasi Karbondioksida Tersisa
Konsentrasi gas karbondioksida yang diberikan dalam kultivasi mikroalga
Nannochloropsis sp berasal dari tabung gas karbondioksida, tidak semua
konsentrasi gas karbondioksida yang diberikan terserap, dikarenakan beberapa
konsentrasi gas karbondioksida akan kembali difusi ke udara sehingga tidak
terlarut di dalam media kultivasi.
Konsentrasi karbondioksida yang tersisa dalam kultivasi mikroalga dapat
dilihat pada Gambar 7:
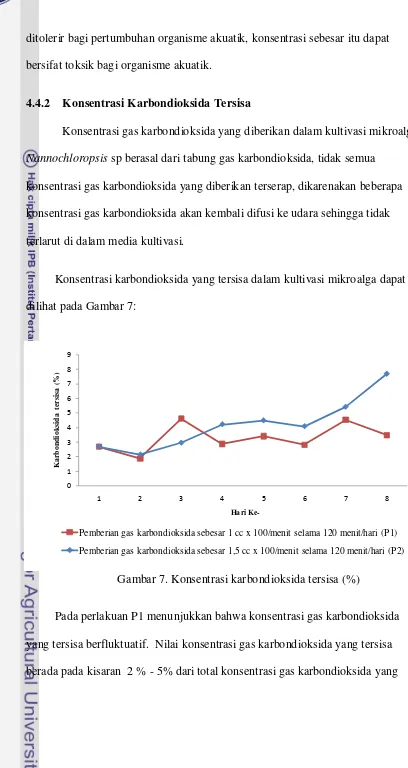
Gambar 7. Konsentrasi karbondioksida tersisa (%)
Pada perlakuan P1 menunjukkan bahwa konsentrasi gas karbondioksida
yang tersisa berfluktuatif. Nilai konsentrasi gas karbondioksida yang tersisa
berada pada kisaran 2 % - 5% dari total konsentrasi gas karbondioksida yang
0
Pemberian gas karbondioksida sebesar 1 cc x 100/menit selama 120 menit/hari (P1)
diberikan pada kultivasi mikroalga. Nilai rata-rata karbondioksida yang tersisa
selama kultivasi berada pada konsentrasi 3 %. Semakin sedikit gas
karbondioksida berarti semakin banyak gas karbondioksida yang terserap.
Konsentrasi nilai gas karbondioksida yang terserap dipengaruhi oleh beberapa
faktor yang terdiri dari faktor internal dan faktor eksternal.
Faktor eksternal meliputi suhu, sedangkan faktor internal meliputi kondisi
fisiologis organisme dan jumlah substrat yang dapat teroksidasi (Salisbury, 1995).
Perlakuan P1 memiliki suhu rata-rata pada media kultivasi sebesar 28,87 oC
lebih tinggi dibandingkan dengan suhu rata-rata pada perlakuan P2. Hal tersebut
berdampak kepada proses respirasi yang dilakukan oleh mikroalga, dimana pada
suhu yang lebih tinggi proses respirasi berjalan lebih cepat. Hal itu dapat dilihat
pada Gambar 11, bahwa pada perlakuan P1 memiliki gas karbondioksida yang
tersisa lebih sedikit dibandingkan dengan perlakuan P2.
Perlakuan P2 memiliki nilai gas karbondioksida yang tersisa pada rentang
2% - 8% dari total gas karbondioksida yang diberikan setiap harinya. Nilai
rata-rata konsentrasi gas karbondioksida yang tersisa sebesar 5% selama proses
kultivasi berlangsung. Pada perlakuan P2 memiliki nilai karbondioksida yang
tersisa lebih tinggi dibandingkan dengan nilai karbondioksida tersisa pada
perlakuan P1, hal ini terjadi diduga karena suhu rata-rata selama kultivasi lebih
rendah dibandingkan dengan perlakuan P1. Nilai suhu rata-rata selama proses
kultivasi pada perlakuan ini sebesar 27,93 oC sehingga hal tersebut menyebabkan
rendahnya proses respirasi yang dilakukan oleh mikroalga tersebut jika
dibandingkan dengan perlakuan P1 yang memiliki suhu media kultivasi lebih
5. KESIMPULAN DAN SARAN
5.1 Kesimpulan
Kultivasi mikroalga Nannochloropsis sp. dengan perlakuan dengan
pemberian gas karbondioksida sebesar 1 cc x 100 /menit selama 120 menit/hari
(P1) memiliki laju pertumbuhan kelimpahan sel dan biomassa terbaik
dibandingkan dengan perlakuan lainnya. Perlakuan P1 memiliki puncak
kelimpahan sel 14,52 x 106 dan puncak biomassa sebesar 0,45 g/L pada hari ke-5.
Nilai karbondioksida terlarut pada kultivasi menggunakan karbondioksida
pada awal kultivasi hingga puncak pertumbuhan kelimpahan sel dan biomassa
masih berada pada kisaran yang cukup baik bagi kehidupan biota perairan.
Konsentrasi gas karbondioksida tersisa pada perlakuan P1 sebesar 3% dan
konsentrasi gas karbondioksida pada perlakuan P2 sebesar 5%. Penggunaan
karbondioksida pada kultivasi mikroalga memberikan pengaruh yang baik bagi
pertumbuhan kelimpahan sel dan pertumbuhan biomassa mikroalga.
5.2 Saran
Saran untuk penelitian selanjutnya agar kondisi kelimpahan sel dan
biomassa pada seluruh perlakuan di awal massa kultivasi dalam kondisi yang
sama selain itu perlu dilakukan pengamatan terhadap konsentrasi kandungan gas
DAFTAR PUSTAKA
Anon Sen MAT, Kocer MTAlp, dan H Erbas. 2009. Studies on Growth Marine Microalgae in Batch Cultures: III. Nannochloropsis oculata
(Eustigmatophyta). Departement of Basic Aquatic Sciences, Faculty of Aquaculture, Firat University, Elazig, Turkey. Asian Jour of Plant Scie 4(6) : 642-644.
Banse K, Falls CP, Hobsons LA.1963. A Gravimetric method for determine suspended matter in seawater using millipore filter. Deep Sea Res.10: 639 -642.
Becker BJ. 1994. Combining significance levels. In H.M. Cooper & L.V.
Hedges (Eds.), The handbook of research synthesis.New York: Russell Sage.
Benemann JR. 1997. CO2 Mitigation with Microalgae Systems. Energy Convers. 38: S475-S479.
Boyd CE. 1982. Water Quality Management for Pond Fish Culture. Amsterdam: Elselvier Science Publisher B.V.
Cahyaningsih S. 2009. Standar Nasional Indonesia Pembenihan Perikanan (Pakan Alami). Pelatihan MPM-CPIB Pembenihan Udang, 16-20 Juni 2009, Situbondo. Balai Budidaya Air Payau Situbondo
Chiu SY, Ya Kao C, Ta Tsai M, Cin Ong S, Hsun Chen C dan Sheng Lin C. 2008. Lipid Accumulation and CO2 Utilization of Nannochloropsis oculata in
Response to CO2 Aeration. Bioresource Tech. 100: 833-838.
Effendi H. 2003. Telaah Kualitas Air bagi Pengelolaan Sumberdaya dan Lingkungan Perairan.Yogyakarta: Kanisius.
Graham LE dan Wilcox LA. 2000. Algae. Prentice Hall, New Jersey. Hoshida H T, Ohira A Minematsu, Akada R, Nishizawa Y. 2005.
Accumulation of Eicosapentaenoic Acid in Nannochloropsis sp. in Response to Elevated CO2 Concentrations, Applied Phycology. 17: 29-34.
Hu H and Gao K. 2006. Response of Growth and Fatty Acid Compositions of
Nannochloropsis sp. to Environmental Factors Under Elevated CO2
Concentration, Biotechnol Lett. 28: 987-992.
Isnansetyo A, Kurniastuty. 1995. Teknik Kultur Phytoplankton dan
Kawaroe M, Prartono T, Sunuddin A, Wulan Sari D, Augustine D. 2010.
Mikroalga Potensi dan Pemanfaatannya untuk Produksi Bio Bahan Bakar. Bogor: IPB Press.
Khoo HH, Sharratt PN, Das P, Balasubramanian RK, Naraharisetti PK, Shaik S. 2011. Life cycle energy and CO2 analysis of microalgae to biodiesel:
Preliminary results and comparisons. Bioresource Tech. 102:5800- 5807.
Krichnavaruk S, Worapanne, Sorawit, dan Prasert. 2004. Optimal Growth Conditions and the Cultivation of Chaetoceros calcitrans in Airlift Photobioreactor. Chemical Engineer. 105: 91-98.
Lavens P dan Sorgeloos P (eds). 1996. Manual on the Production and Use of Live Food for Aquaculture. FAO Fisheries Technical Paper. No. 361. Food and Agriculture Organization of the United Nations. Rome.
Lin Q, Gu N, Li Gang, Lin J, Huang J, Tan L. 2012. Effects of inorganic carbon concentration on carbon formation, nitrate utilization, biomass and oil accumulation of Nannochloropsis oculata CS 179. Bioresource Tech. 111: 353-359.
Mattjik AA. dan Sumertajaya. 2006. Perancangan Percobaan dengan Aplikasi SAS dan Minitab Jilid I. Bogor: IPB Press.
Prihantini NB, Putri, dan Yuniati. 2005. Pertumbuhan Chlorella spp. dalam Medium Ekstrak Tauge (Met) Dengan Variasi pH Awal. Departemen Biologi Fakultas MIPA, Universitas Indonesia. Depok.
Rocha JMS, Gracia Juan EC, Henriques MHF. 2003. Growth aspects of the marine microalga Nannochloropsis gaditana. Biomol Engineer.
20:237-242.
Rostini I. 2007. Karya Ilmiah. Kultur Fitoplankton (Chlorella sp. dan Tetraselmis
sp.) pada Skala Laboratorium di Instalasi Penelitian dan Pengkajian Teknologi Pertanian Bojonegara. Fakultas Perikanan dan Ilmu Kelautan. Universitas Padjajaran. Bandung.
Salisbury.1995. Fisiologi Tumbuhan Jilid 2. Bandung: ITB Press.
Tomaselli L. 2004 . The Microalgal Cell. Di dalam: Amos R, editor. Hand Book of Microalgal Culture:Biotechnology and Applied Phycologyi.Victoria: Blackwell Publishing. hlm:3.
Wagenen JV, Miller TW, Hoobs S, Hook P, Crowe B, Huesemann M. 2012. Effect of Light and Temperature on Fatty Acid Production in
Lampiran 1. Perhitungan kelimpahan sel Nannochloropsis sp.
Kelimpahan sel (ind x106/ml) = n x 25 5 x10
4
Contoh : Pengamatan Nannochloropsis sp. pada perlakuan aerasi di hari ke -1
ulangan 1 diperoleh N = 45
Kelimpahan sel (ind x106/ml) = n x 25 5 x10
4
= 45 x 5 x 104
= 225 x 104
= 2,25 x 106
Lampiran 2. Perhitungan laju pertumbuhan spesifik (μ) kelimpahan sel dan biomassa mikroalga
1. Laju Pertumbuhan Spesifik Kelimpahan Sel (μ) Mikroalga
Laju pertumbuhan spesifik kelimpahan sel Nannocloropsis sp dihitung
dengan menggunakan persamaan berikut
Dimana :
µ = Laju pertumbuhan spesifik kelimpahan sel (sel /ml/hari)
N0 = Kelimpahan sel Nannocloropsis sp.awal (sel/ml)
Nt = Kelimpahan sel Nannocloropsis sp.akhir (sel/ml)
t = Selang waktu dari N0ke Nt (hari)
Laju pertumbuhan spesifik maksimum dihitung dari kelimpahan pada saat awal
kultur hingga puncak kelimpahan maksimum.
Contoh : Nannochloropsis sp. pada perlakuan dengan aerasi memiliki
kelimpahan pada hari ke-0 = 1,98 x106 sel/ml, kelimpahan pada hari ke-1 = 2,45
x106 sel/ml, kelimpahan pada hari ke-2 = 3,70 x106 sel/ml.
Laju pertumbuhan spesifik (µ) kelimpahan sel pada hari ke-1 adalah :
µ = ln (2,45 x106) – ln (1,98 x106)/ (1-0) = 0,21
Laju pertumbuhan spesifik (µ) kelimpahan sel pada hari ke-2 adalah :
Lampiran 2. (Lanjutan)
Laju pertumbuhan biomassa sel Nannocloropsis sp. dihitung dengan
menggunakan persamaan berikut (Chiu et al, 2008) :
Dimana :
µ = Laju pertumbuhan biomasa sel (sel /ml/hari)
w0 = Biomassa sel Nannocloropsis sp.awal (sel/ml)
wt = Biomassa sel Nannocloropsis sp.akhir (sel/ml)
t = Selang waktu dari N0 ke Nt (hari)
Laju pertumbuhan spesifik maksimum dihitung dari kelimpahan pada saat awal
kultur hingga puncak kelimpahan maksimum.
Contoh : Nannochloropsis sp. pada perlakuan dengan aerasi memiliki
biomassa pada hari ke-0 = 0,15 gram/liter, biomassa pada hari ke-1 = 0,18
gram/liter, biomassa pada hari ke-2 = 0,22 gram/liter.
Laju pertumbuhan (µ) biomassa sel pada hari ke-1 adalah :
µ = ln (0,18) –ln (0,15)/ (1-0) = 0,18
Laju pertumbuhan (µ) biomassa sel pada hari ke-2 adalah :
µ = ln (0,22) –ln (0,18)/ (2-1) = 0,20
Lampiran 3. Deskripsi dan mekanisme operasional Orsat
Gambar 1. Peralatan ORSAT
Keterangan Gambar :
A : Valve A, dihubungkan dengan tempat penampungan gas
karbondioksida yang akan dianalisis kandungannya
B : Valve B, dihubungkan ke tabung absorpsi
C : Three-way Valve
D : Tabung Absorpsi
E : Reservoir Gas
Lampiran 3. (Lanjutan)
KETERANGAN PENGISIAN BAHAN KIMIA
Larutan KOH 50% : Diisikan ke dalam Tabung D Fungsinya sebagai
larutan penyerap gas yang akan dianalisis
Larutan NaCl 3% : Diisikan ke dalam Tabung F fungsinya sebagai
larutan pendorong gas yang akan dianalisis
Air : Diisikan ke bagian selubung luar Tabung E
fungsinya sebagai pembias untuk memudahkan
visualisasi/pembacaan skala.
PETUNJUK PENGOPERASIAN PERSIAPAN AWAL
1. Pastikan semua bahan kimia telah berada pada tabung yang tepat.
2. Pastikan juga semua Valve yang tidak digunakan berada pada posisi
tertutup.
3. Buka penutup tabung F.
4. Pastikan level cairan pada tabung D (depan & belakang) berada pada posisi
setara. Jika level cairan tidak setara, atur dengan membuka Valve B dan C,
jika perlu naik turunkan Tabung F. Setelah level cairan setara, kembalikan
Valve B ke posisi tertutup.
5. Mengusir udara atau sisa gas sebelumnya dari Tabung E. Langkah
selanjutnya adalah membuang udara atau sisa gas sebelumnya, sehingga
tidak mengganggu atau menginterferensi analisis yang akan dilakukan.
Lampiran 3. (Lanjutan)
buka Valve C, dan dengan perlahan angkat Tabung F. Perhatikan level
cairan dalam Tabung E, level cairan dalam tabung E akan naik dan udara
atau gas di atasnya akan terusir keluar. Angkat terus Tabung F hingga level
cairan dalam tabung F mencapai pipa horizontal. Jika jumlah udara atau gas
yang terusir keluar sudah dirasa cukup, tutup Valve C.
6. Peralatan ORSAT siap diisi dengan gas baru yang akan dianalisis.
PENGISIAN GAS
1. Pastikan semua kriteria tahapan awal telah telah terpenuhi.
2. Hubungkan kontainer gas ke Valve A.
3. Buka Valve A, pindahkan gas dengan cara memberikan tekanan pada
kontainer gas, atau dengan menurunkan Tabung F.
4. Perhatikan level cairan pada Tabung E, level cairan akhir harus berada pada
skala seratus atau nol pada bagian bawah tabung.
5. Setelah level cairan dalam Tabung E berada pada skala seratus atau nol pada
bagian bawah tabung, tutup Valve A.
6. Peralatan ORSAT siap digunakan untuk keperluan analisis.
TAHAP ANALISIS GAS
1. Pastikan peralatan ORSAT telah siap digunakan untuk analisis.
2. Buka Valve B.
3. Angkat perlahan Tabung F, sehingga gas akan pindah dari tabung E ke
Tabung Absorpsi (Tabung D). Perhatikan level cairan pada Tabung D,
jangan sampai salah satunya menjadi kosong, jika hal ini terjadi maka gas