PEMBUATAN SEL FOTOELEKTROKIMIA PADAT DENGAN
STRUKTUR ITO/CdS/ELEKTROLIT/ITO
HAQQI GUSRA
DEPARTEMEN FISIKA
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM
INSTITUT PERTANIAN BOGOR
ABSTRAK
HAQQI GUSRA.
Pembuatan Sel Fotoelektrokimia Padat dengan Struktur
ITO/CdS/Elektrolit/ITO. Dibimbing oleh
Dr.
AKHIRUDDIN MADDU
dan
Drs. M. NUR INDRO, M.Sc.
Pada penelitian ini, telah dibuat sel fotoelektrokimia padat dengan susunan
ITO/CdS/Elektrolit/ITO. Material sel fotoelektrokimia yang digunakan ialah lapisan
cadmium sulfida di atas substrat kaca ITO. Lapisan CdS berperan sebagai elektroda kerja
pada sel. Elektrolit padat yang digunakan ialah campuran kitosan-PEG-KI/I
2. Konsentrasi
KI/I
2divariasikan dari 0.1/0.01 M hingga 0.5/0.05 M. Arus
–
tegangan keluaran sel
diukur di bawah penyinaran cahaya dari lampu tungsten dan sinar matahari. Tegangan
output didapatkan meningkat sekitar 50 % saat konsentrasi KI/I
2ditingkatkan dari
0.1/0.01 M hingga 0.5/0.05 M. Saat intensitas penyinaran ditingkatkan dari 1,074 mW/m
2ke 4,147 mW/m
2, tegangan Voc meningkat dua kali lipat, arus Isc meningkat tiga kali,
dan efisiensi meningkat dua kalinya pada konsentrasi tetap. Efisiensi sel surya tertinggi
pada pengukuran sel tunggal diperoleh pada konsentrasi KI/I
20.5/0.05 M. Pada rangkaian
yang terdiri dari 4 sel surya, efisiensi dan FF tertinggi dihasilkan pada rangkaian seri.
Kata kunci :
Sel fotoelektrokimia padat, CdS, kitosan, KI-I
2, efisiensi
ABSTRACT
HAQQI GUSRA.
Fabrication of The Photoelectrochemical Solid Cell with
ITO/CdS/Electrolyte/ITO structure. Under direction of
Dr. AKHIRUDDIN MADDU
and
Drs. M. NUR INDRO, M.Sc.
A photoelectrochemical solid cell in ITO/CdS/Electrolyte/ITO structure has been
succesfully composed through this research. The photoelectrochemical cell material is a
layer of cadmium sulfide deposited onto an ITO-covering glass substrate. The CdS layer
is used as a working electrode of the cell. The solid electrolyte used is a combination of
chitosan-PEG-KI/I
2. The concentration of KI/I
2was varied from 0.1/0.01 M to
0.5/0.05 M. The current-voltage output of the cell was measured under a light
illumination of a tungsten lamp and the sun. The output voltage found increases around
50% when the KI/I
2consentration was raised from 0.1/0.01 M to 0.5/0.05 M. When the
radiation intensity increased from 1.074 mW/m
2to 4.147 mW/m
2, V
ocvoltage increased
around threefold, I
sccurrent increased around twice, and power efficiency increased
around twice at a fixed concentration. The highest efficiency of the solar cells (on
single-cell measurements) obtained at the concentrations of 0.5/0.05 M KI/I
2. In a circuit consist
of 4 solar cells, the highest power eficiency and FF produced by the serial circuit.
PEMBUATAN SEL FOTOELEKTROKIMIA PADAT DENGAN
STRUKTUR ITO/CdS/ELEKTROLIT/ITO
HAQQI GUSRA
Skripsi
sebagai salah satu syarat untuk memperoleh gelar
Sarjana Sains pada
Departemen Fisika
DEPARTEMEN FISIKA
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM
INSTITUT PERTANIAN BOGOR
Judul
: Pembuatan Sel Fotoelektrokimia Padat dengan Struktur
ITO/CdS/Elektrolit/ITO
Nama
: Haqqi Gusra
NIM
: G74070065
Disetujui,
Pembimbing 1
Pembimbing 2
Dr. Akhiruddin Maddu, M.Si
NIP. 19660907 199802 1 006
Drs. M. Nur Indro, M.Sc
NIP.
19561015 198703 1 001
Diketahui,
Ketua Departemen Fisika
Institut Pertanian Bogor
Dr. Akhiruddin Maddu, M.Si
NIP. 19660907 199802 1 006
KATA PENGANTAR
Puji dan syukur penulis ucapkan kepada Allah SWT yang hingga saat ini
selalu memberikan nikmat bimbingan-Nya. Dengan izin-Nya pula, penulis dapat
menyelesaikan
penulisan
skripsi
ini
dengan
judul
“
Pembuatan
Sel
Fotoelektrokimia Padat dengan Struktur ITO/CdS/Elektrolit/ITO
”.
Skripsi ini
disusun sebagai salah satu syarat untuk memperoleh gelar Sarjana Sains di
Departemen Fisika, Fakultas Matematika dan Ilmu Pengetahuan Alam, Institut
Pertanian Bogor.
Penyusunan skripsi ini tidak dapat terlaksana dengan baik tanpa adanya
bimbingan dan dukungan dari berbagai pihak. Oleh karena itu, penulis ingin
mengucapkan terima kasih kepada:
Bapak Akhiruddin Maddu, selaku dosen pembimbing yang selalu
memberikan bimbingan dalam menyelesaikan skripsi ini serta motivasi
kepada penulis.
Bapak Nur Indro, selaku dosen pembimbing akademik sekaligus
pembimbing dalam penelitian, yang selalu memberikan motivasi kepada
penulis selama kuliah dan penyusunan skripsi ini.
Teman-teman fisika 43, 44, dan 45 yang selalu bersedia untuk berdiskusi
dan membantu memberikan dukungan.
Bapak dan Mama, Kak Dyan, Anci, Wela, Nisa, Kris dan Nidal, cinta
kalian mengalir menjadi kekuatan untuk menyelesaikan tugas ini.
Akang, dan semua saudara saudari yang tidak pernah berhenti memberikan
doa, semangat dan dukungan serta mengajarkan arti sebuah kesabaran dan
keikhlasan kepada penulis.
Untuknya, syukurku untuk sebuah pandangan yang indah dan sederhana.
Penulis menyadari bahwa tulisan ini masih jauh dari sempurna. Karena itu,
kritik dan saran yang bersifat membangun sangat penulis harapkan untuk hasil
yang lebih baik. Semoga skripsi ini dapat bermanfaat bagi penulis dan para
pembaca.
Bogor, Februari 2013
DAFTAR ISI
Halaman
DAFTAR TABEL... vi
DAFTAR GAMBAR ... vii
DAFTAR LAMPIRAN... viii
PENDAHULUAN ... 1
Latar Belakang ... 1
Rumusan Masalah... 1
Tujuan Penelitian ... 1
Hipotesis ... 1
TINJAUAN PUSTAKA ... 1
Semikonduktor... 1
Kadmium Sulfida (CdS) ... 3
Elektrolit Polimer Padat ... 4
Kitosan ... 4
Sel Surya Fotoelektrokimia... 5
Mekanisme Konversi Sel Fotoelektrokimia... 6
Karakteristik I-V Sel Surya... 7
METODE PENELITIAN... 8
Tempat dan Waktu... 8
Alat dan Bahan... 8
Tahapan Penelitian... 8
Pembuatan Film CdS ... 8
Karakterisasi Film CdS ... 8
Pembuatan Elektrolit Polimer Kitosan dan Karakterisasi ... 9
Pembuatan Sel Fotoelektrokimia Padat ... 9
Karakterisasi Arus-Tegangan (I-V) Sel surya... 9
Model Rangkaian Sel Surya... 10
HASIL DAN PEMBAHASAN... 10
Deposisi Film CdS ... 10
Karakterisasi XRD film CdS ... 11
Karakteristik Optik CdS... 11
Konduktivitas Elektrolit Polimer ... 12
Karakteristik Fotovoltaik Sel CdS/Kitosan+KI/I2 ... 13
Karakteristik Respon Dinamik... 13
Karakteristik Arus-Tegangan (I-V)... 13
KESIMPULAN DAN SARAN... 16
Kesimpulan ... 16
Saran ... 16
DAFTAR PUSTAKA ... 16
DAFTAR TABEL
Halaman
Tabel 1 Kode gel kitosan dengan variasi konsentrasi elektrolit... 9
Tabel 2 Variasi susunan rangkaian pengujian I-V sel surya ... 10
Tabel 3 Karakteristik sel surya pada uji respon dinamik ... 13
Tabel 4 Sampel sel surya pada kondisi tanpa dan dengan penambahan elektrolit... 14
Tabel 5 Nilai karakteristik I-V sel surya untuk kondisi penyinaran yang berbeda ... 15
DAFTAR GAMBAR
Halaman
Gambar 1 Perpindahan elektron dari pita valensi (PV) ke pita konduksi (PK) ... 2
Gambar 2 (a) Struktur kristal silikon (b) Lepasnya elektron dari ikatan kovalen
pada silikon ... 2
Gambar 3 Perubahan keadaan energi gap pada silikon... 2
Gambar 4 (a) Atom pengotor valensi tiga menggantikan posisi salah satu atom
silikon (b) Pita energi semikonduktor tipe-p... 3
Gambar 5 (a) Atom pengotor valensi lima menggantikan posisi salah satu atom
silikon (b) Pita energi semikonduktor tipe-n... 3
Gambar 6 (a) Struktur kristal kubik CdS (b) Struktur kristal hexagonal CdS ... 4
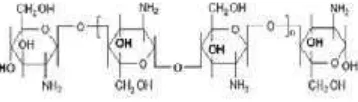
Gambar 7 Struktur kimia dari kitosan... 4
Gambar 8 Sel fotoelektrokimia ... 5
Gambar 9 Tingkat energi pada semikonduktor dan potensial elektrokimia pada
elektrolit ... 6
Gambar 10 (a) Level energi pada persambungan semikonduktor tipe-n dan elektrolit
saat sebelum kontak, dan (b) Sesudah kontak dan setimbang tanpa
disinari ... 6
Gambar 11 Mekanisme aliran elektron pada ... 6
Gambar 12 Kurva karakteristik I-V sel... 7
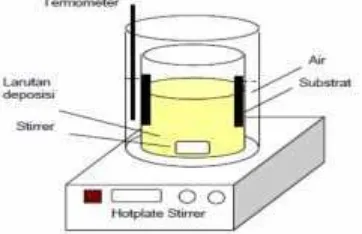
Gambar 13 Metode
CBD
pada deposisi CdS. ... 8
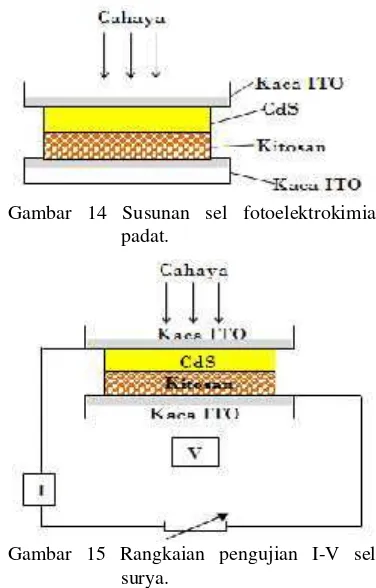
Gambar 14 Susunan sel fotoelektrokimia padat... 9
Gambar 15 Rangkaian pengujian I-V sel surya. ... 9
Gambar 16 Hasil deposisi CdS di atas substrat kaca ITO... 10
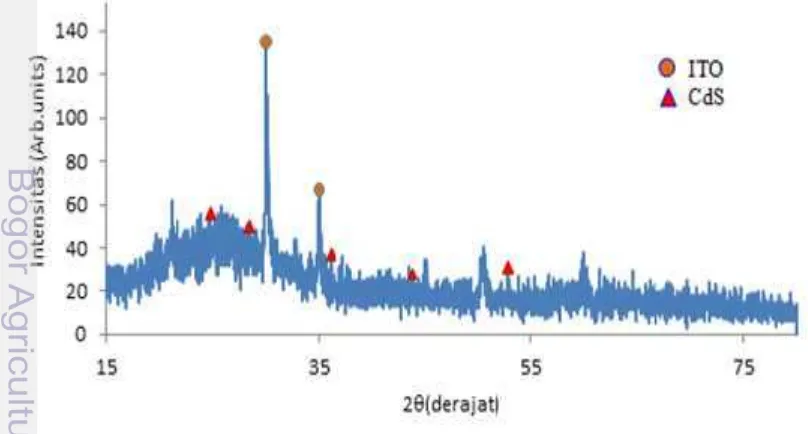
Gambar 17 Pola XRD untuk film CdS... 11
Gambar 18 Kurva absorbansi sampel CdS ... 12
Gambar 19 Gambar 19 Kurva Konduktansi dengan berbagai molaritas KI/I
2... 12
Gambar 20 Grafik respon dinamik untuk sel S1, S2, dan S3... 13
Gambar 21 Kurva I-V sel surya pada 2 kondisi elektrolit polimer yang berbeda... 14
Gambar 22 Kurva I-V dengan intensitas sumber cahaya yang berbeda ... 15
DAFTAR LAMPIRAN
PENDAHULUAN
Latar Belakang
Kebutuhan energi dunia yang semakin meningkat diiringi dengan ketersediaan sumber energi minyak bumi yang semakin menipis menjadikan manusia tertuntut untuk mencari energi baru demi mengatasi terjadinya krisis energi. Sebagian besar energi yang terpakai selama ini bersumber dari minyak bumi. Dalam pemanfaatannya, sumber-sumber energi tersebut menimbulkan beberapa masalah, seperti pencemaran dari zat sisa pembakaran yang dapat membahayakan kelangsungan makhluk hidup. Selain itu, sumber energi minyak bumi merupakan sumber energi yang tidak dapat diperbaharui yang pada akhirnya akan habis.1
Energi radiasi matahari merupakan sumber energi alternatif yang dapat digunakan dalam jangka waktu yang lama. Salah satu cara pemanfaatan energi radiasi matahari dilakukan berdasarkan sistem konversi fotovoltaik melalui suatu piranti optoelektronik yang disebut sel surya (Solar Cell).2 Penelitian tentang efek fotovoltaik pertama kali dilakukan oleh Becquerel pada tahun 1839, dimana Becquerel mendeteksi adanya tegangan listrik ketika sinar matahari mengenai elektroda pada larutan elektrolit.3 Kemudian pada tahun 1954, para peneliti dari Bell Laboratories melakukan pengembangan efek fotovoltaik menjadi sel surya dengan menggunakan material silikon kristal terdifusi, efisiensi konversi sel surya yang diperoleh sekitar 4,5%.4
Piranti sel surya menggunakan bahan semikonduktor sebagai komponen utama. Semikonduktor yang banyak digunakan dalam sel surya saat ini adalah silikon. Pada sel surya terjadi dua proses yang berkelanjutan, yaitu absorbsi cahaya dan pemisahan muatan listrik.5
Sel fotoelektrokimia adalah sistem sel surya yang menggunakan elektroda semikonduktor di dalam sistem elektrokimia. Salah satu semikonduktor yang dapat digunakan sebagai fotoelektroda pada sistem fotoelektrokimia adalah CdS.1
Sel surya fotoelektrokimia merupakan sel surya dengan struktur persambungan semikonduktor-elektrolit.5 Dibandingkan dengan struktur sel surya lainnya, seperti persambungan p-n dan persambungan Schottky, sel surya fotoelektrokimia memiliki kelebihan diantaranya: peralatan yang digunakan lebih sederhana, mudah dalam
pembuatannya, dan biaya produksi yang relatif murah. Sel surya fotoelektrokimia menggunakan elektrolit dalam bentuk cair. Sel surya ini dapat menghasilkan efisiensi hingga 12,4%, tetapi keberadaannya kurang stabil karena elektrolit berupa cairan atau larutan dapat menguap sehingga mengalami degradasi dan menjadi tidak stabil.3
Pada penelitian ini digunakan elektrolit padat dan film semikonduktor CdS sebagai fotoelektroda pada sistem sel fotoelektrokimia. Elektrolit yang digunakan adalah campuran polimer PEG-Kitosan dan elektrolit KI/I2. Jika dibandingkan dengan sel
surya dengan elektrolit cair, sel surya dengan elektrolit padat akan lebih stabil.3Saat ini sel surya fotoelektrokimia padat mencapai tingkat efisiensi konversi energi sekitar 19,6%.6
Rumusan Masalah
Rumusan Masalah dari penelitian ini adalah:
1) Apakah peningkatan konsentrasi elektrolit dari 0,1/0,01 M hingga 0,5/0,05 M pada gel kitosan dapat meningkatkan nilai I-V pada sel surya fotoelektrokimia?
2) Apakah sel fotoelektrokimia padat dengan struktur ITO/CdS/Kitosan/ITO dapat menghasilkan nilai efisiensi tinggi?
Tujuan Penelitian
Tujuan penelitian ini ialah membuat sel fotoelektrokimia ITO/CdS/Kitosan/ITO untuk aplikasi konversi energi cahaya menjadi energi listrik.
Hipotesis
Pada sel surya fotoelektrokimia, variasi komposisi KI dan I2 di dalam larutan
elektrolit dengan kitosan menghasilkan karakteristik I-V yang bervariasi. Efisiensi sel fotoelektrokimia ITO/CdS/Kitosan/ITO dapat ditingkatkan dengan meningkatkan konsentrasi elektrolit pada polimer kitosan.
TINJAUAN PUSTAKA
Semikonduktor
2
energi yang memperbolehkan keberadaan elektron, yaitu pita valensi berenergi rendah yang terisi penuh oleh elektron dan pita konduksi berenergi tinggi yang kosong.8 Celah energi yang memisahkan kedua pita tersebut disebut sebagai pita terlarang atau disebut juga energi gap (Eg). Celah energi
pada material semikonduktor ditunjukkan pada Gambar 1.
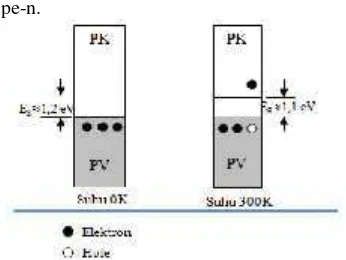
Salah satu sifat penting semikonduktor adalah memiliki celah energi 0,2 – 2,5 eV. Nilai celah energi tersebut lebih kecil dari nilai celah energi isolator.7 Sifat ini memungkinkan suatu elektron memasuki level energi yang lebih tinggi. Beberapa faktor yang mempengaruhi elektron untuk berpindah dari pita valensi ke pita konduksi ialah suhu dan penyinaran.8 Perpindahan elektron terjadi apabila elektron pada pita valensi menyerap energi sama dengan atau lebih besar dari nilai celah energi antara pita valensi dan pita konduksi seperti terlihat pada Gambar 1. Elektron dan hole inilah yang menjadi pembawa muatan listrik pada material semikonduktor.7
Sifat listrik kristal semikonduktor yang mempunyai ikatan kovalen dapat juga diterangkan dengan memperhatikan keadaan ikatannya. Kristal semikonduktor yang murni atau tidak ditambahkan bahan pengotor dalam pembuatannya disebut semikonduktor intrinsik, sedangkan yang ditambahkan bahan pengotor disebut semikonduktor ekstrinsik.9
Semikonduktor intrinsik, pada suhu 0 K semua elektron berada pada ikatan kovalen. Pada suhu tersebut, tidak ada elektron bebas atau tidak ada pembawa muatan sehingga bersifat isolator. Struktur ikatan pada semikonduktor dapat dilihat pada Gambar 2. Saat semikonduktor intrinsik berada pada suhu 300 K, celah energi antara pita valensi dan pita konduksi berkurang sehingga beberapa elektron valensi dapat keluar dari ikatan kovalen menjadi elektron bebas sebagai pembawa muatan negatif.
Gambar 1 Perpindahan elektron dari pita valensi (PV) ke pita konduksi (PK)8
(a)
(b)
Gambar 29(a) Struktur kristal silikon (b) Lepasnya elektron dari ikatan
kovalen pada silikon
Berkurangnya celah energi pada semikonduktor dapat dilihat pada Gambar 3. Munculnya elektron bebas diikuti dengan terbentuknya hole sebagai pembawa muatan positif.10
Semikonduktor ekstrinsik dapat diperoleh dengan menambahkan (doping) atom-atom asing dalam pembuatannya. Tujuan dari pemberian doping ini ialah untuk memperoleh elektron valensi bebas dalam jumlah yang lebih banyak dan permanen dan diharapkan dapat menghantarkan listrik.8 Semikonduktor ekstrinsik terdiri dari dua tipe yaitu semikonduktor tipe-p dan semiknduktor tipe-n.
3
Semikonduktor tipe-p diperoleh dengan menambahkan sejumlah kecil atom pengotor dari golongan IIIA (atom trivalen seperti Aluminium (Al), Boron (B), Galium (G) atau Indium (In)) pada semikonduktor murni, misalnya silikon murni.11 Atom – atom pengotor ini memiliki tiga elektron valensi sehingga dapat membentuk tiga ikatan kovalen. Saat sebuah atom trivalen menempati posisi atom silikon dalam kristal maka hanya ada tiga elektron yang dapat membentuk ikatan kovalen dan tersisa sebuah muatan positif (hole) dari atom silikon yang tidak berpasangan.11 Struktur semikonduktor tipe-p dapat dilihat pada Gambar 4 (a) . Material yang dihasilkan dari proses pengotoran ini dinamakan semikonduktor tipe-p karena menghasilkan pembawa muatan positif pada kristal yang netral. Karena atom pengotor menerima elektron, maka atom pengotor ini disebut atom aseptor.11 Penambahan atom aseptor ini akan menimbulkan tambahan tingkat energi sedikit di atas pita valensi. Peningkatan energi pada semikonduktor tipe-p dapat dilihat pada Gambar 4 (b).10
Semikonduktor tipe-n dapat diperoleh dengan cara yang sama seperti semikonduktor tipe-p, dengan menambahkan atom pengotor pentavalen (golongan VA, seperti arsenik (As), fosfor (P), atau antimon (Sb)) pada silikon murni.
(a)
(b)
Gambar 4 (a) Atom pengotor valensi tiga menggantikan posisi salah satu atom silikon.11
(b) Pita energi semikonduktor tipe-p.12
(a)
(b)
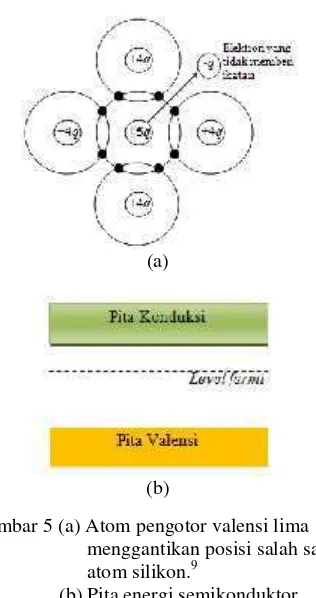
Gambar 5 (a) Atom pengotor valensi lima menggantikan posisi salah satu atom silikon.9
(b) Pita energi semikonduktor tipe-n.12
Atom pentavalen yang menempati posisi atom silikon dalam kristal, lima elektron valensi dari atom pengotor akan membentuk empat ikatan kovalen lengkap dan tersisa satu elektron yang tidak berpasangan. Sisa elektron ini akan menjadi elektron bebas dan menjadi pembawa muatan dalam proses hantaran listirk. Struktur semikonduktor tipe-n dapat dilihat pada Gambar 5 (a).8
Material dari proses pengotoran ini disebut semikonduktor tipe-n karena menghasilkan pembawa muatan negatif. Karena atom pengotor memberikan elektron, maka atom pengotor ini disebut atom donor.11 Penambahan atom donor ini akan menambah satu tingkat energi baru di bawah pita konduksi.10 Penambahan energi pada semikonduktor tipe-n dapat dilihat pada Gambar 5 (b).
Kadmium Sulfida (CdS)
4
(a)
(b)
Gambar 6 (a) Struktur kristal kubik CdS19 (b) Struktur kristal hexagonal
CdS20
Semikonduktor CdS memiliki sifat optik dan listrik yang sesuai untuk aplikasi sel surya. CdS memiliki koefisien penyerapan (absorbansi) yang tinggi sehingga sebagian besar cahaya dapat diserap olehnya. Lapisan tipis CdS sangat efektif untuk sel surya lapisan tipis.13
Semikonduktor CdS banyak diaplikasikan sebagai bahan optoelektronik seperti pada pembuatan sel surya, filter optik, dan fotodetektor.14,15,16 CdS merupakan bahan yang sifat kelistrikannya dapat merespon cahaya sehingga CdS disebut sebagai bahan yang memiliki efek optoelektronik (listrik-optik).17 Efek fotovoltaik pada CdS pertama kali diperkenalkan oleh D. C. Reynolds pada tahun 1954.18
Salah satu teknik deposisi untuk menumbuhkan sifat optik, listrik, dan struktur yang diinginkan dari film CdS ialahchemical deposition.15Pada pembuatan deposisi kimia CdS, ada beberapa jenis garam kadmium yang digunakan sebagai sumber kadmium seperti kadmium asetat, kadmium klorida, dan kadmium sulfat.13,21,22, 23
Elektrolit Polimer Padat
Elektrolit berbasis polimer memiliki potensi untuk aplikasi di bidang teknologi, khususnya dalam sistem elektrokimia karena memiliki sifat mekanis yang baik, dapat membentuk film, kontak yang baik dengan bahan elektroda.
Secara umum, elektrolit polimer dapat diklasifikasikan menjadi tiga kategori: elektrolit polimer kering padatan, elektrolit polimer komposit dan elektrolit polimer-plasticized.24
Elektrolit polimer padat sering digunakan dalam pembuatan sel fotoelektrokimia (PEC) padat. Konfigurasi sel-sel tersebut secara umum adalah elektroda fotoaktif, elektrolit polimer, dan elektroda lawan (counter electrode). Elektrolit polimer pada dasarnya terdiri dari polimer dan garam yang bersama membentuk pasangan redoks. Contohnya polietilen oksida (PEO)-KI-I2,
kitosan-PEO-NH4I-I2, I2-PEONH4I, polyvinylchloride
(PVC)-LiClO4, dan kitosan-PVA-KOH.25,26
Elektrolit polimer padat dapat dikelompokkan sebagai bahan padat yang memiliki kemampuan untuk menghantarkan arus listrik dengan cara pergerakan ion dan memiliki fungsi yang sama seperti larutan elektrolit. Sistem polimer yang memiliki konduktivitas ionik tinggi dapat disiasati dengan memberikan bahan tambahan seperti bahan anorganik ke dalam matriks polimer tersebut.26Konduktivitas ionik suatu polimer bergantung pada kerapatan dan mobilitas ion. Secara fisik, elektrolit polimer terlihat seperti bahan yang berfase padat tetapi di dalamnya memiliki struktur seperti fase cair yang berpengaruh pada perubahan konduktivitas.26
Beberapa ciri yang harus dimiliki oleh suatu polimer agar dapat berfungsi sebagai hostdalam elektrolit polimer adalah:26 i. Memiliki atom atau kumpulan atom yang
cukup untuk mendonorkan elektron sehingga dapat membentuk ikatan koordinasi dengan kation.
ii. Memiliki hambatan yang kecil terhadap pemutaran ikatan sehingga memungkinkan pergerakan ion pada ikatan polimer.
Kitosan
Kitosan merupakan bahan dasar suatu polielektrolit yang mengandung gugus amina dan gugus hidroksil, yang banyak digunakan sebagai bahan molekul transport aktif suatu
5
anion dalam kitosan.8 Kitosan berbentuk padatan amorf dan dapat larut dalam asam organik seperti asam asetat.27 Kitosan merupakan polimer alam yang memiliki sifat mudah terdegradasi, tidak beracun, dan biokompatibel.8,27Struktur kimia dari kitosan dapat dilihat pada Gambar 7. Sifat – sifat kitosan dihubungkan dengan adanya gugus amina dan kardoksil yang terikat. Adanya gugus tersebut menyebabkan kitosan memiliki reaktivitas kimia yang baik dan penyumbang sifat elektrolit kation.8
Sel Surya Fotoelektrokimia
Sel surya fotoelektrokimia bekerja berdasarkan proses yang diakibatkan adanya persambungan antara semikonduktor dan elektrolit untuk mengkonversi energi cahaya menjadi listrik. Komponen utama pada sel fotoelektrokimia ialah elektroda semikonduktor dan elektrolit cairan maupun padatan. Sel fotoelektrokimia dengan elektrolit cair dirancang sangat sederhana menggunakan dua elektroda yang terdiri dari bahan logam dan semikonduktor. Kedua elektroda tersebut dicelupkan ke dalam larutan elektrolit yang mengandung kopel redoks. Sel fotoelektrokimia dapat dilihat pada Gambar 8. Larutan yang digunakan mengandung kompleks-kompleks redoks seperti Sulfida, Selenida, Iodida, Tellurida dan sebagainya.1
Elektroda kerja (working electrode) dari bahan semikonduktor berperan sebagai fotoelektroda atau fotoanoda yang berfungsi menyerap energi foton sedangkan elektroda lawan (counter electrode) dari bahan logam, misalnya ITO, sebagai katoda. Kedua elektroda tersebut dihubungkan dengan rangkaian luar. Elektroda kerja dapat berupa bahan bulk semikonduktor atau bentuk lapisan tipis yang dideposisikan pada substrat gelas konduktif transparan (ITO).1
Sifat antarmuka semikonduktor-elektrolit berkaitan dengan tingkat energi semikonduktor dan potensial elektrokimia dalam elektrolit. Pada semikonduktor, potensial elektrokimia ditunjukkan oleh
Gambar 8 Sel fotoelektrokimia28
level Fermi yang mengacu pada energi referensi. Pada elektrolit yang mengandung kopel redoks, potensial elektrokimia (Eredoks)
dari elektrolit ditentukan oleh potensial redoks. Hal ini diberikan oleh persamaan Nerst:1
E
redoks= E
0 redoks+
(aox
ared) (1)
Biasanya konsentrasi dinyatakan sebagai pengganti aktivitas ditunjukkan oleh a=γc dimana γ adalah koefisien aktivitas. Potensial elektrokimia dari sistem redoks mengacu pada NHE (Normal Hydrogen Electrode) sebagai referensi. Proses yang terjadi pada sel fotoelektrokimia secara kuantitatif adalah level Fermi dari semikonduktor dan elektrolit ditempatkan pada skala energi. Penggunaan skala energi absolut, energi dari kopel redoks (EF, redoks) diberikan oleh Persamaan (2):
1
E
F, redoks=
E
refE
redoks (2)Nilai dari Erefuntuk NHE biasanya adalah
-4,5 eV dimana interval pengukurannya (-4,54,7) eV, sehingga Persamaan (2) dapat ditulis sebagai berikut:
E
F, redoks=
-4,5 - E
redoks (3)dengan mengacu pada level vakum. Perbandingan tingkat energi pada semikonduktor dan potensial elektrokimia dalam elektrolit diperlihatkan pada Gambar 9.1
Prinsip dasar sel fotoelektrokimia ialah (a) Ketika foton diserap oleh elektroda semikonduktor, elektron tereksitasi ke tingkat energi yang lebih tinggi.3 (b) Akibat gaya tolak dari ruang muatan negatif di antarmuka elektrolit-semikonduktor, elektron tersebut bergerak meninggalkan semikonduktor melalui rangkaian luar dan kemudian diinjeksikan pada elektroda lawan untuk menghasilkan reaksi reduksi.3,28(d) Akseptor A direduksi menjadi donor A-yang kemudian bergerak menuju elektroda semikonduktor untuk mendonasikan elektron kepada hole melalui proses oksidasi.3,28(e) Pada saat yang sama, pita valensi terbentuk hole yang berdifusi ke daerah deplesi, kemudian berekombinasi dengan elektron yang didonasikan oleh ion donor dari elektrolit. Karena elektron dan hole bergerak dalam arah yang berlawanan, arus akan mengalir secara berkelanjutan selama sel disinari dan tersambung dengan rangkaian luar.3,28
6
Gambar 9 Tingkat energi pada
semikonduktor dan potensial elektrokimia pada elektrolit.1
melalui pembangkitan elektron oleh cahaya dalam kisaran cahaya tampak. Cahaya yang dibutuhkan untuk transisi tersebut harus memiliki energi foton yang lebih besar atau sama dengan selisih energi antara dua keadaan (hv ≥ Eg).1 Jika foton yang diserap memiliki energi lebih besar dari celah pita energi maka foton mampu membuat elektron berpindah dari pita valensi ke pita konduksi.1
Mekanisme Konversi Sel
Fotoelektrokimia
Mekanisme konversi sel surya fotoelektrokimia memanfaatkan efek fotovoltaik yang dihasilkan dari persambungan semikonduktor-elektrolit. Persambungan semikonduktor-elektrolit identik dengan persambungan logam-semikonduktor atau dioda Schottky.1
Ketika terjadi kontak antara semikonduktor tipe-n dengan elektrolit, maka terjadi pertukaran elektron denga cepat antara jenis redoks dan elektroda yang disebabkan oleh perbedaan potensial elektrokimia.28Jika level Fermi awal (potensial elektrokimia) pada semikonduktor diatas level Fermi awal pada elektrolit maka akan terjadi pertukaran elektron dari semikonduktor ke elektrolit.1 Proses ini berhenti ketika potensial elektrokimia kedua fase sama pada saat mencapai kondisi kesetimbangan.28Pada kondisi kesetimbangan tersebut dihasilkan daerah lapisan muatan positif pada semikonduktor yang dinamakan daerah deplesi, dan daerah muatan negatif pada elektrolit yang disebut daerah Helmholtz.1,28
Sebagai hasilnya, pita konduksi dan pita valensi meningkat untuk menghasilkan potensial barrier yang melawan pertukaran elektron ke dalam elektrolit.28Kondisi energi pada persambungan semikonduktor tipe-n dan elektrolit saat sebelum dan sesudah kontak dapat dilihat pada Gambar 10 (a) dan (b).
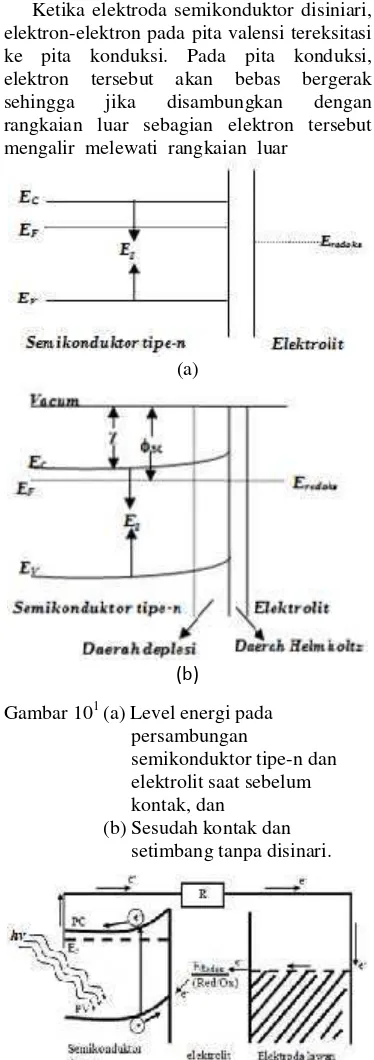
Ketika elektroda semikonduktor disiniari, elektron-elektron pada pita valensi tereksitasi ke pita konduksi. Pada pita konduksi, elektron tersebut akan bebas bergerak sehingga jika disambungkan dengan rangkaian luar sebagian elektron tersebut mengalir melewati rangkaian luar
(a)
(b)
Gambar 101(a) Level energi pada persambungan
semikonduktor tipe-n dan elektrolit saat sebelum kontak, dan
(b) Sesudah kontak dan setimbang tanpa disinari.
Gambar 11 Mekanisme aliran elektron pada sel fotoelektrokimia
7
menuju katoda dan melintasi elektrolit yang mengandung kompleks-kompleks redoks menuju pita valensi semikonduktor dan berekombinasi dengan hole. Arah aliran elektron bebas danhole pada semikonduktor tipe-n terlihat seperti pada Gambar 11.1
Karakteristik I-V Sel Surya
Karakterisasi arus tegangan sel surya pada persambungan semikonduktor-elektrolit identik dengan persambungan logam-semikonduktor (dioda Schottky). Pada kondisi tidak disinari (dark condition), hubungan arus-tegangan sebuah dioda ideal dinyatakan dalalam Persamaan (4) sebagai berikut:29
=
I
01
(4)Ketika sel surya disinari, akan dihasilkan arus yang disebut dengan arus foto (photocurrent) akibat pembangkitan arus oleh cahaya, sehingga persamaan (4) dapat ditulis menjadi:1
=
I
phI
01
(5)dengan Iph adalah arus foto, I0 adalah arus saturasi pada kesetimbangan, dan V adalah tegangan bias. UntukIph>I0maka Persamaan (5) dapat ditulis menjadi:1
I
phI
0 (6)Pada rangkaian terbuka (open circuit),I = 0, sehingga diperoleh
V
oc=
Iph
I0
(7)
sedangkan pada rangkaian pendek (short circuit), V = 0, sehingga diperoleh Iph = I0 dengan I0 disebut arus rangkaian pendek (I0= Isc).1,29
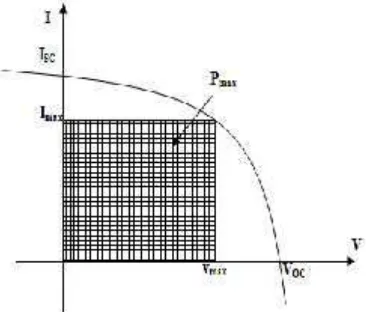
Berdasarkan pengukuran-pengukuran yang dilakukan maka karakteristik sel surya dapat digambarkan seperti pada Gambar 12, dimana VOC adalah tegangan rangkaian
terbuka sel surya dan ISC adalah arus
rangkaian pendek pada sel surya. Pada kurva I-V sel surya, ISC merupakan perpotongan
kurva dengan sumbu arus (V=0) dan VOC
adalah perpotongan kurva dengan sumbu tegangan (I=0).4
Dari gambar kurva di bawah terlihat titik pengoperasian terletak di sepanjang kurva. Terdapat titik khusus yang merupakan daya output sel surya maksimum, yaitu pada titik (Vmax, Imax). Daya output akan maksimum
jika letak (Vmax, Imax) pada kurva mempunyai
luasan yang lebih besar pada persegi panjang yang diarsir tersebut. Titik (Vmax, Imax) akan
dipergunakan untuk mendefinisikan parameter sel surya yaitu pengisian (Fill Factor).4 Fill Factor merupakan perbandingan antara daya maksimum dengan hasil kali tegangan terbuka dan arus rangkaian singkat pada sel surya. Secara matematis dapat ditulis sebagai berikut:4,29
=
V
maxI
maxV
ocI
sc(8)
Efisiensi konversi merupakan ukuran kemampuan sel surya mengkonversi energi cahaya menjadi listrik yang ditentukan melalui hubungan arus-tegangan keluaran yang dihasilkan sebuah sel surya saat disinari dengan energi foton yang sesuai. Secara matematis dapat dituliskan sebagai berikut:29
=
P
outP
in(9)
dengan Pout adalah daya output sel surya (watt) dan Pin adalah daya input sel surya (watt).
Efisiensi maksimum sel surya adalah:
=
PmaxPin
× 100%
(10)Pmaxadalah daya maksimum yang dihasilkan.
Pmaxdihasilkan dari Persamaan (11):
P
max =V
maxx I
max= V
ocx I
scx FF
(11)Pinadalah daya energi cahaya yang menyinari permukaan sel surya. Pin ditentukan dengan menggunakan Persamaan (12):
P
in =I
inx A
(12)dengan Iin adalah intensitas sumber cahaya danAadalah luas sel surya yang disinari.29
METODE PENELITIAN
Tempat dan Waktu
Penelitian ini dilaksanakan di laboratorium Biofisika Material dan Membran Departemen Fisika FMIPA-IPB, LIPI BATAN. Penelitian dilaksanakan pada bulan Oktober 2011 sampai dengan September 2012.
Alat dan Bahan
Bahan yang digunakan dalam penelitian ini adalah kaca ITO (Indium Tin Oxide), cadmium klorida (CdCl2), thiourea (CN2H4S),
trietanolamina (TEA), ammonium hidroksida (NH4OH), kitosan padat, asam asetat
(CH3COOH) 1%, padatan KI, padatan kristal
I2, polietilen glikol (PEG), dan aquades.
Alat yang digunakan adalah statip, hotplate, pengaduk magnetik, gelas kimia, neraca analitik, multimeter, furnace, LCR-meter, Spektrofotometer UV-Vis GenesysTM 10 Series, X-Ray Diffractometer, Lampu Tungsten 160 Watt, Potensiometer 100 k dan 500 k, sensor tegangan.
Tahapan Penelitian
Pembuatan Film CdS
Pembuatan film CdS menggunakan metode Chemical Bath Deposition (CBD). Melalui metode ini, film terdeposisi di atas substrat kaca ITO dengan cara mencelupkan substrat ke dalam larutan prekursor CdS sambil dipanaskan dan diaduk. Metode deposisi CdS diperlihatkan pada Gambar 13. Sebelum digunakan, kaca ITO dicuci menggunakan sabun, dibilas dengan aquades, di rendam dengan ethanol lalu dikeringkan di suhu ruang.
Larutan prekursor CdS dibuat dengan mencampurkan larutan CdCl2sebagai sumber
ion Cd2+(20 ml; 0,1 M) dan Thiourea sebagai ion S2-(20 ml; 1 M). Selain itu, ditambahkan pula NH4OH (10 ml; 96%), dan TEA (5 ml)
ke dalam gelas kimia yang dinding gelas bagian dalamnya telah ditempeli kaca ITO. Gelas tersebut direndam di dalam gelas kimia yang berukuran lebih besar yang berisi air. Larutan diputar di atas hotpalte dengan kecepetan 300 rpm selama 2 jam pada suhu 70oC. Hasil deposisi yang terbentuk diatas substrat ITO diangkat dan dibersihkan.
Penambahan NH4OH di dalam larutan
berperan sebagai larutan buffer untuk mempertahankan pH larutan selama deposisi
berlangsung dan pengontrol kelajuan reaksi. Sedangkan TEA berperan sebagai penghambat terjadinya pengendapan selama deposisi berlangsung. Pembentukan CdS mengggunakan metode CBD dibuat dalam bentuk larutan yanng bersifat basa. Sumber basa yang digunakan adalah NH4OH yang
juga berperan sebagai agen pengkompleks ion cadmium.8,
Pembentukan ion kompleks diawali dengan terbentuknya Cd(OH)2 berupa
endapan dengan reaksi kimianya sebagai berikut.8,30
CdCl2+ NH4OHCd(OH)2+ 2NH4Cl
Selanjutnya endapan ini bereaksi dengan larutan amonium hingga terbentuk ion kompleks [Cd(NH3)4]2+.
Cd(OH)2+ 4NH4OH[Cd(NH3)4](OH)2+
4H2O
[Cd(NH3)4](OH)2[Cd(NH3)4] 2+
+ 2OH
-Ion kompleks yang terurai kembali menjadi [Cd(NH3)4]2+ selanjutnya terdekomposisi di
dalam larutan
[Cd(NH3)4] 2+
Cd2++ 4NH3
Di sisi lain, terjadi hidrolisis thiourea di dalam larutan basa membentuk ion S2-,
(NH2)2CS + 2OH-CH2N2+H2O + S
2-Ion Cd2+ dan S2- yang dihasilkan kemudian bereaksi membentuk CdS.
Cd2++ S2-CdS
Karakterisasi Film CdS
Film CdS yang berhasil terdeposisi selanjutnya dikarakterisasi menggunakan XRD dan spektroskopi UV-Vis. Karakterisasi XRD dilakukan pada sampel untuk memastikan kristal yang tumbuh pada substrat adalah mayoritas CdS dengan cara membandingan sudut difraksi yang
9
dihasilkan sampel dengan literatur berdasarkan rujukan jurnal dan JCPDS.
Uji spektroskopi UV-Vis dilakukan untuk mengetahui sifat optik film CdS. Karakterisasi optik diukur menggunakan alat spektrofotometer dengan kisaran panjang gelombang yang digunakan ialah 300 – 900 nm. Melalui uji optik, dapat ditentukan daerah panjang gelombang serapan maksimum film CdS dari kurva absorbansi yang terbentuk. Dari data panjang gelombang tersebut dapat diperkirakan nilai celah energinya.
Pembuatan Elektrolit Polimer Kitosan
dan Karakterisasi
Polimer kitosan dibuat dengan cara melarutkan 0,15 gram kitosan ke dalam 6 mL asam asetat 1%. Larutan ditambahkan PEG sebanyak 0,15 gram. Proses pencampuran dilakukan di atas hotplate stirrer pada suhu 60oC hingga larutan homogen. Sebelumnya, telah dibuat beberapa larutan KI/I2dengan 5
konsentrasi molar yang berbeda yaitu 0,1/0,01 M; 0,2/0,02 M; 0,3/0,03 M; 0,4/0,04 M; dan 0,5/0,05 M.
Polimer kitosan yang telah homogen ditambahkan 1mL larutan elektrolit KI/I2dan
sambil diaduk hingga homogen dan membentuk gel. Gel yang telah dibuat, diteteskan di atas kaca konduktif dan ditindih dengan kaca konduktif pula lalu didiamkan pada suhu ruang. Dengan cara yang sama, dibuat 5 sampel gel kitosan lainnya dengan konsentrasi elektrolit yang berbeda. Tabel 1 menunjukkan kode gel kitosan yang akan dilakukan pengukuran konduktivitas menggunakan LCR-meter.
Sampel yang telah siap, diuji sifat listriknya menggunakan LCR meter untuk mengetahui nilai konduktivitas dari masing – masing sampel. Selanjutnya, akan dibuat sel surya dengan dua perbandingan keadaan yaitu sel dengan struktur ITO/CdS/Kitosan+PEG dan ITO/CdS/Kitosan+PEG+KI/I2 dengan nilai
konduktivitas yang tertinggi.
Tabel 1 Kode gel kitosan dengan variasi konsentrasi elektrolit
Kode gel Konsentrasi elektrolit KI/I2 pada polimer kitosan (M) 1 2 3 4 5 6 (tanpa elektrolit) 0,1/0,01 0,2/0,02 0,3/0,03 0,4/0,04 0,5/0,05
Pembuatan
Sel
Fotoelektrokimia
Padat
Lapisan CdS pada substrat kaca ITO ditetesi dengan elektrolit gel polimer hingga menutupi permukaan film CdS. Selanjutnya ditutupi dengan kaca ITO sebagai elektroda lawan menyerupai bentuk sandwich, seperti yang terlihat pada Gambar 14, lalu didiamkan selama sehari hingga mengering dan kedua elektroda saling merekat dengan kuat.
Karakterisasi Arus-Tegangan (I-V) Sel
surya
Sel surya yang telah terbentuk selanjutnya dilakukan pengukuran I-V untuk mengetahui performa sel surya yang dihasilkan. Karakterisasi ini diujikan pada dua jenis sel berbeda. Salah satu sel menggunakan elektrolit KI/I2 pada konsentrasi maksimum,
dan lainnya hanya menggunakan kitosan-PEG tanpa penambahan elektrolit KI/I2.
Kedua sel ini diuji pada sumber cahaya matahari. Selanjutnya untuk sel dengan konsentrasi elektrolit KI/I2 0,5/0,05 M diuji
karasteristik I-V dengan perbandingan cahaya matahari dan lampu.
Sel surya dihubungkan dengan amperemeter dan voltmeter seperti yang terlihat pada Gambar 15. Dari pengukuran ini, diperoleh data yang menghasilkan kurva hubungan arus-tegangan (I-V).
Gambar 14 Susunan sel fotoelektrokimia padat.
Dari kurva dapat ditentukan parameter-parameter sel surya yaitu tegangan open-circuit(Voc), arusshort-circuit(Isc), tegangan
maksimum (Vmax), arus maksimum (Imax), dan
daya maksimum (Pmax).
Model Rangkaian Sel Surya
Hasil pengukuran I-V pada salah satu sel dengan nilai efisiensi dan FF tertinggi selanjutnya dibuat beberapa variasi rangkaian. Sel surya PEC sebanyak empat buah sel dihubungkan satu dengan yang lain menggnakan kabel penghubung dan penjepit hingga terbentuk rangkaian seri empat sel surya PEC. Dengan prosedur yang sama, dibentuk pula 2 macam rangkaian sel surya yang berbeda. Model rangkaian yang akan diuji digambarkan pada Tabel 2.
Ketiga jenis rangkaian ini diuji hubungan arus dan tegangannya untuk membandingkan parameter-parameter sel surya yang dihasilkan. Dari data yang diperoleh, dapat ditentukan nilai efisiensi tertinggi dari ketiga jenis rangkaian sel surya.
Tabel 2 Model susunan rangkaian pengujian I-V sel surya
Kode
Rangkaian Gambaran
R1
R2
R3
HASIL DAN PEMBAHASAN
Deposisi Film CdS
Pada penelitian ini, semikonduktor CdS dibentuk dari 20 mL CdCl20,1 M dan 10 mL
NH4OH 96%. Pada pencampuran tersebut
selanjutnya ditambahkan 20 mL Thiourea (NH2)2CS dan diaduk selama 30 menit pada
temperatur 30oC. Proses deposisi dilakukan dengan mencelupkan substrat ke dalam larutan (CdCl2+ NH4OH+(NH2)2CS) pada
temperatur 70oC selama 120 menit diatas hotplateyang diaduk pada 300 rpm.
Melalui metode CBD ini, dihasilkan lapisan CdS berwarna kuning diatas substrat ITO dengan ukuran 1 x 1,5 cm2. Selain itu, terbentuk pula koloid CdS yang mengendap pada larutan bath. Hasil deposisi film CdS dapat dilihat pada Gambar 16.
Terdapat 3 fase pembentukan CdS, yaitu fase awal disebut proses nucleation center, fase pembentukan ion per ion (mekanisme heterogen), dan pembentukan kluster per kluster (mekanisme homogen).8 Proses nucleation center merupakan proses pembentukan ion cadmium dan ion sulfur baik pada permukaan substrat maupun pada larutanbath.8Pada pembentukan CdS ion per ion dapat menghasilkan CdS dengan morfologi yang lebih baik dibandingkan jika yang terjadi adalah kluster per kluster
Dalam penelitian ini, terlihat pembentukan CdS terjadi pada mekanisme homogen yang ditandai dengan banyak terbentuknya koloid berwarna kuning di dalam larutan bath sehingga mempengaruhi struktur kristal CdS yang terbentuk.
Waktu deposisi mempengaruhi karakteristik fisik CdS yang dihasilkan. Jika deposisi dilakukan dalam jangka waktu yang lama akan menghasilkan film yang tebal. Selain itu, jika waktu deposisi cukup lama maka akan semakin banyak kluster CdS yang menempel pada permukaan sampel sehingga menghasilkan morfologi film yang kurang baik. Sebaliknya, jika jangka waktu deposisi terlalu singkat maka film yang dihasilkan sangat tipis.
Gambar 16 Hasil deposisi CdS di atas substrat kaca ITO
11
Temperatur deposisi juga mempengaruhi karakteristik fisik film. Jika deposisi dilakukan pada temperatur yang rendah maka akan membutuhkan waktu yang lama untuk menumbuhkan film pada substrat ITO. Jika temperatur deposisi dinaikkan hingga melebihi 100oC maka film yang dihasilkan tidak merata, hal ini karena lebih banyak koloid yang terbentuk pada larutanbathyang menempel pada permukaan film CdS.8 Pada penelitian ini digunakan waktu deposisi selama 120 menit pada temperatur 70oC.
Karakterisasi XRD film CdS
Karakterisasi XRD sampel CdS dilakukan di Pusat Penelitian dan Pengembangan Ilmu Pengetahuan dan Teknologi Material, Badan Tenaga Nuklir Nasional (BATAN), Serpong. Tangerang. Gambar 17 merupakan hasil karakterisasi XRD sampel CdS yang dideposisi selama 2 jam pada suhu 70oC. Pada Gambar 17 memperlihatkan puncak-puncak CdS berada pada 2= 24,88o; 28,48o; 36,18o; 43,86o; dan 52,92o. Menurut Yani yang mengacu pada data JCPDS No. 80-006 diketahui bahwa pada 2 = 24,929o (100); 28,328o(101); 36,821o(102); 43,905o(110); 53,077o(201) merupakan puncak CdS dengan struktur kristal Wurtzite (hexagonal).8
Berdasarkan data XRD yang dihasilkan menunjukkan bahwa CdS telah tumbuh pada permukaan ITO. Selain puncak CdS, kurva XRD juga menunjukkan puncak 2 pada 30,06o dan 35,02o yang merupakan sudut
difraksi untuk ITO. Munculnya permukaan ITO pada pola XRD disebabkan karena film CdS yang terdeposisi terlalu tipis dan tidak merata. Terbentuknya lapisan film yang tidak merata dapat disebabkan oleh suhu deposisi yang rendah sehingga mengurangi dispersi ion di dalam larutan. Kondisi ini mengakibatkan permukaan film yang terbentuk kasar dan dapat menurunkan kristalinitas film yang dihasilkan.
Puncak-puncak CdS yang teramati pada pola XRD menunjukkan bahwa struktur kristal CdS yang terbentuk adalah polikristal heksagonal pada 2= 15ohingga 80o. Hal ini dapat diamati dengan adanya puncak-puncak yang tidak terindentifikasi yang diakibatkan oleh impuritas-impuritas yang muncul dari bahan-bahan yang digunakan selama proses pembuatan sampel.
Karakteristik Optik CdS
Karakteristik optik film CdS diukur menggunakan alat spektrofotometer UV-Vis. Gambar 18 memperlihatkan spektrum serapan dari film CdS yang dideposisi pada suhu 70oC. Dari gambar terlihat bahwa film CdS menyerap cahaya pada panjang gelombang 300-500 nm. Hasil ini sesuai dengan beberapa literatur yang menunjukkan bahwa pita serapan CdS terjadi pada panjang gelombang 350-500 nm.8,32
12
Gambar 18 Kurva absorbansi sampel CdS
Celah energi pada semikonduktor berpengaruh pada sifat konduktivitasnya. Semakin besar nilai celah energy maka konduktivitasnya semakin menurun.33 Pola absorbansi dapat digunakan untuk memperkirakan nilai celah energi (Eg) yang
dimiliki oleh sampel CdS melalui Persamaan (13):
=
λ (13)
dimana h adalah konstanta Planck, c adalah kecepatan cahaya, dan e adalah panjang
gelombang tepi absorbsi sampel CdS. Berdasarkan kurva absorbansi CdS diketahui nilai e = 506,31 nm dan diperoleh nilai
celah energi (Eg) dari CdS sebesar 2,449 eV.
Nilai Eg ini sesuai dengan beberapa literatur
dengan nilai celah energi CdS sekitar 2,3 – 2,5 eV.13 Pita absorbsi yang landai menunjukkan tingkat kristalinitas film yang rendah.8,33
Konduktivitas Elektrolit Polimer
Gel kitosan pada penelitian ini dibuat dengan melarutkan 0,15 gram kitosan dan 0,15 gram PEG di dalam pelarut asam asetat 1% sebanyak 6 mL. Proses pelarutan dilakukan di atashotplatedengan temperatur 60OC hingga homogen. Pada larutan tersebutselanjutnya ditambahkan larutan KI/I2
sebanyak 1 mL. Penambahan KI/I2dilakukan
sedikit demi sedikit untuk memudahkan pelarutan hingga larutan membentuk gel. Hasil akhir pelarutan ini adalah berupa gel tak berwarna (bening) untuk semua sampel
Gel yang telah terbentuk kemudian diteteskan pada kaca konduktif (ITO) untuk diukur nilai konduktansiya. Pada penelitian ini, pengukuran konduktansi dan impedansi dilakukan dengan memvariasikan nilai frekuensi dari 100 Hz hingga 5 kHz. Dari hasil pengukuran diketahui nilai konduktivitas kitosan-PEG tanpa penambahan KI/I2 (sampel 1) berkisar
antara 2,0703 sampai 21,9541 x 10-8 S/cm pada fungsi frekuensi. Nilai ini menjelaskan bahwa kitosan mampu berfungsi sebagai matriks konduktif bagi larutan elektrolit sehingga dapat melewatkan ion-ion redoks yang dihasilkan pada elektrolit saat sel bekerja.
Nilai konduktivitas meningkat ketika ditambahkan KI/I2ke dalam polimer tersebut.
Peningkatan konduktivitas polimer semakin bertambah ketika molaritas dari elektrolit KI/I2 diperbesar. Konduktivitas tertinggi
diperoleh pada sampel 6 yaitu saat konsentrasi KI/I2 sebesar 0,5/0,05 M yang
berkisar antara 1,46876 x 10-5 hingga 1,20728 x 10-3 S/cm. Secara rinci nilai konduktivitas masing-masing sampel dari hasil pengukuran dapat dilihat pada Lampiran 1 (Tabel B).
Peningkatan nilai konduktivitas disebabkan adanya penambahan molaritas KI/I2 yang berkaitan dengan meningkatnya
jumlah ion I-/I3- sebagai pembawa muatan
dan reaksi ion tersebut di dalam rantai polimer.
Gambar 19 memperlihatkan nilai konduktivitas meningkat ketika konsentrasi KI/I2meningkat pada frekuensi 1 kHz. Hasil
13
Ini berlaku juga ketika gel diuji pada frekuensi 100 Hz, 500 Hz, dan 5 kHz. Peningkatan ini akan berpengaruh pada kinerja sel surya ketika disinari. Artinya saat sel surya dengan konduktivitas tinggi mendapat penyinaran, tegangan keluaran yang dihasilkan akan besar pula.
Karakteristik Fotovoltaik Sel
CdS/Kitosan+KI/I2
Karakteristik Respon Dinamik
Pada sampel S1 hingga S3, dengan karakteristik sel dijelaskan pada Tabel 3, dilakukan uji respon dinamik menggunakan sensor tegangan. Sumber cahaya yang digunakan memiliki intensitas sebesar 24,7 W/m2. Pada Gambar 20 memperlihatkan hasil respon dinamik dari masing-masing sel surya saat kondisi terang dan gelap. Dari grafik terlihat bahwa semua sel surya fotoelektrokimia CdS/Kitosan+KI/I2
merespon cahaya dengan baik. Artinya saat sel dikenai cahaya dengan intensitas tinggi, sel surya menghasilkan tegangan tinggi dan tegangan akan berkurang ketika intensitas cahaya dikurangi.
Pada Gambar 20, setiap sel menunjukkan sensitivitas yang berbeda terhadap cahaya. Perbedaan ini dilihat dari nilai tegangan keluaran yang dihasilkan oleh masing-masing sel. Pada ketiga sampel terlihat bahwa ketika konsentrasi elektrolit KI/I2 dinaikkan,
tegangan rangkaian terbuka (Voc) yang
dihasilkan juga meningkat. Keadaan ini sebanding dengan konduktivitas masing-masing sel. Jika konduktivitas sel tinggi berarti sel memiliki kemampuan yang tinggi
Tabel 3 Penamaan sel surya pada uji respon dinamik
Sampel Variasi elektrolit
S1 S2 S3
KI 0,1 M + I20,01 M
KI 0,3 M + I20,03 M
KI 0,4 M + I20,04 M
pula dalam mobilitas hole-elektron. Selain berfungsi sebagai penyedia level energi bagi elektron, CdS juga memiliki kemampuan yang tinggi untuk mengalirkan elektron-hole di dalam bahan. Keadaan ini berlaku sama untuk setiap sel (S1S3).
Perbedaan nilai Voc tergantung pada molaritas larutan elektrolit. Konsentrasi molar larutan elektrolit mempengaruhi konsentrasi pasangan reduktor-oksidator (kopel redoks) dalam larutan. Kopel redoks sangat berperan dalam proses mobilitas muatan, sehingga sangat mempengaruhi aliran elektron-hole dalam sel secara keseluruhan. Artinya, ketika molaritas elektrolit dinaikkan jumlah kopel redoks di dalam larutan juga meningkat sehingga nilai konduktivitas sel pun meningkat.
Pada penelitian ini, ketebalan polimer saat diteteskan ke tiap sel tidak dapat dipastikan sama. Karena polimer yang digunakan bersifat gel, maka kemungkinan terjadi kebocoran pada tepi lapisan sel. Kebocoran ini menyebabkan terjadinya pengurangan jumlah polimer sehingga jumlah pasangan elektron-hole yang dihasilkan menurun.
Karakteristik Arus-Tegangan (I-V)
a) Pada konsentrasi elektrolit yang berbedaKarakteristik arus–tegangan dilakukan pada prototipe sel surya fotoelektrokimia (PEC) yang dibuat dalam bentuk padat dengan susunan: 1) lapisan CdS yang dideposisi pada substrat kaca ITO. 2) Elektrolit polimer dengan penambahan elektrolit yang mengandung kopel redoks. 3) Kaca ITO yang berperan sebagai kaca konduktif.
. Tabel 4 menunjukkan penamaan polimer yang digunakan pada sel untuk karakterisasi I-V. Kedua sampel diuji pada kondisi penyinaran secara langsung oleh sumber cahaya matahari. Luas permukaan sel surya adalah 0,5625 cm2 untuk sampel S0 dan 0,6 cm2untuk sampel S5.
14
Tabel 4 Sampel sel surya pada kondisi tanpa dan dengan penambahan elektrolit
Sampel Konsentrasi
elektrolit (M) Pin (Watt)
S0 - 33,01 x 10-4
S5 KI 0,5 M + I2
0,05 M 41,47 x 10
-4
Gambar 21 Kurva I-V sel surya pada 2 kondisi elektrolit polimer yang berbeda
Gambar 21 memperlihatkan perbandingan hasil pengujian sel surya antara sampel S0 yang tidak menggunakan elektrolit dan sampel S5 dengan penambahan elektrolit KI/I2 pada konsentrasi (0,5/0,05) M.
Kurva I-V menunjukkan bahwa pada sampel S5 mengalami peningkatan arus dan tegangan dibandingkan sampel S0 ketika sel surya disinari. Nilai VOC, ISC, efisiensi konversi,
dan FF yang dihasilkan oleh sel S0 sebesar 47,8 mV, 0,61 A, 0,4x10-3 %, dan 0,48 secara berturut-turut. Sedangkan pada sampel S5 menghasilkan Nilai VOC, ISC, efisiensi
konversi, dan FF sebesar 225 mV, 5,9 A, 11,7x10-3%, dan 0,368 secara berturut-turut.
Kehadiran elektrolit KI/I2 yang
mengandung kopel redoks di dalam sel surya fotoelektrokimia mempengaruhi nilai arus dan tegangan keluaran yang dihasilkan. Pada sampel S0, pembuatan gel kitosan dilakukan tanpa penambahan elektrolit KI/I2.
Kitosan merupakan biopolimer yang bersifat konduktif sehingga mampu menghantarkan arus melalui pergerakan ion-ion dalam matriks polimernya. Akan tetapi, kemampuan kitosan terbatas pada konduktivitas ionnya yang rendah sehingga arus-tegangan keluaran yang terukur masih rendah.
Peningkatan nilai tegangan yang dihasilkan sampel S5 dipengaruhi oleh konsentrasi elektrolit yang ditambahkan ke dalam gel kitosan. Pada penelitian ini,
prototipe sel surya fotoelektrolit merupakan persambungan semikonduktor dan elektrolit polimer sehingga nilai tegangan yang terukur terjadi karena adanya perbedaan tingkat energi antara semikonduktor (Efermi) dengan
energi dari kopel redoks (EF,redoks). Semakin
besar perbedaan antara Efermi dan EF,redoks
semakin besar pula nilai tegangan yang dihasilkan. Perubahan tingkat energi dapat terjadi baik pada Efermimaupun EF,redoks.
Posisi level Fermi pada semikonduktor CdS saat memperoleh intensitas penyinaran yang lebih tinggi akan meningkat mendekati level pita konduksi. Sedangkan perubahan tingkat Eredoksternyata tidak dipengaruhioleh
intensitas penyinaran, melainkan oleh variasi konsentrasi elektrolit.28,35 Untuk elektrolit KI/I2, konsentrasi KI menghasilkan ion I
-yang kemudian bereaksi dengan I2
membentuk I3-. Ion I-berperan sebagai donor
elektron (oksidator) sedangkan ion I3
-berperan sebagai akseptor elektron (reduktor).
Karena konsentrasi KI lebih besar daripada I2, tidak semua ion I
-yang dihasilkan akan bereaksi dengan I2. Keadaan
ini menyebabkan konsentrasi I- lebih besar dibandingkan dengan konsentrasi I3
-sehingga potensial elektrokimia elektrolit (Eredoks)
menjadi lebih negatif. Berdasarkan persamaan Nerts (persamaan 1, 2, & 3), potensial elektrokimia yang lebih negative akan menghasilkan energi dari kopel redoks (EF,redoks) menjadi lebih positif. Artinya, level
redoks akan turun menjauhi level Fermi. Perubahan level energi ini mengakibatkan jarak antara tingkat energi fermi semikonduktor dengan tingkat energi redoks menjadi lebih besar.
b) Pada intensitas yang berbeda
Daya masukan (Pin) yang diterima oleh sel
bergantung pada besarnya intensitas penyinaran dan luas permukaan sel yang disinari.35 Semakin luas permukaan sel dan intensitas penyinaran yang semakin tinggi maka semakin besar pula nilai Pin yang
15
Tabel 5 Nilai karakteristik I-V sel surya untuk kondisi penyinaran yang berbeda
Parameter Sampel S5
Sumber Cahaya Lampu Tungsten (Ruang tertutup) Cahaya Matahari
Pin(W) 1074 4147
Imax(A) 1,06 3
Vmax(mV) 59,1 163
Pmax(W) 0,06265 0,489
Isc(A) 1,93 5,9
Voc(mV) 89,7 225
Fill Factor 0,361862 0,368361 Efisiensi (%) 0,0058287 0,011791
Gambar 22 Kurva I-V dengan intensitas sumber cahaya yang berbeda
Dari kurva I-V, diperoleh nilai daya keluaran maksimum (Pmax) pada
masing-masing kondisi penyinaran. Seperti yang tertera pada Tabel 5. nilai Pmax sangat
berpengaruh terhadap nilai efisiensi sel surya. Besarnya efisiensi konversi menunjukkan kemampuan sel surya dalam mengkonversi energi cahaya menjadi energi listrik ketika sel disinari dengan daya masukan tertentu.
Dari Gambar 22, dapat dijelaskan bahwa semakin tinggi intensitas penyinaran maka jumlah foton yang masuk ke dalam sel juga semakin banyak. Jumlah foton yang tinggi saat mengenai permukaan sel sebanding dengan jumlah elektron yang lepas menuju pita konduksi. Hal ini sebanding pula dengan arus keluaran yang dihasilkan. Akan tetapi, energi kinetik elektron tidak bergantung pada intensitas cahaya melainkan pada besarnya frekuensi dari sumber cahaya yang digunakan. Perbandingan hasil pada sampel S5 yang menggunakan sumber cahaya berbeda menunjukkan bahwa semua parameter yang terukur mengalami perubahan yang cukup linier terhadap intensitas penyinaran.
c) Karakteristik Rangkaian Sel
Kurva arus-tegangan yang dihasilkan dari variasi rangkaian sel surya fotoelektrokimia diperlihatkan pada Gambar 23 Kurva arus-tegangan yang dihasilkan dipengaruhi oleh susunan sel pada rangkaian tersebut. Untuk meningkatkan nilai tegangan keluaran maka sel surya PEC dihubungkan secara seri, sedangkan untuk meningkatkan nilai arus keluaran maka sel PEC disusun secara paralel.
Sebanyak empat buah sel surya PEC disusun menjadi tiga macam bentuk rangkaian. Dari ketiga macam rangkaian, diperoleh nilai Voc yang paling tinggi dari
rangkaian R1. Pada rangkaian R1, empat sel PEC disusun secara seri sehingga tegangan keluaran totalnya merupakan jumlah semua tegangan dari masing-masing sel surya. Hal ini sesuai dengan sifat rangkaian seri sumber ggl (gaya gerak listrik) yang mana tegangan total rangkaian seri sumber ggl merupakan jumlah tegangan (ggl) dari masing-masing sumber.34 Arus rangkaian pendek terendah (Isc) juga dihasilkan oleh rangkaian R1.
Keadaan ini memenuhi Persamaan (14) yang berlaku untuk rangkaian seri.
= + + = ( + + )(14)
Nilai Isc tertinggi dan Voc terendah diperoleh
dari rangkaian R2. Pada rangkaian R2, sel disusun secara paralel sehingga tegangan pada setiap cabang sel adalah sama. Hal ini sesuai dengan sifat rangkaian paralel sumber ggl, yaitu jumlah total arus di dalam rangkaian merupakan jumlah masing-masing arus yang dihasilkan oleh sumber, seperti yang dituliskan melalui Persamaan (15).34
= + + (15)
Pada rangkaian R3 merupakan kombinasi rangkaian seri dan paralel. Untuk rangkaian R2, saat setiap sel dianggap memiliki hambatan yang sama dan dengan menerapkan Persamaan (14) dan (15) akan diperoleh arus dan tegangan yang nilainya diantara kedua rangkaian. Penerapan kondisi ini sesuai dengan hasil yang diperoleh pada rangkaian R3 yang mana nilai Isc dan Voc-nya berada
diantara nilai R1 dan R2.
16
Gambar 23 Kurva I-V untuk 4 sel surya dengan susunan rangkaian berbeda
Tabel 6 Nilai karakteristik I-V untuk variasi susunan rangkaian sel surya
Parameter Rangkaian Uji (4 sel)
R1 R2 R3
Pin(W) 6560,8 6815 6455,8
Imax(A) 1 2,21 0,66
Vmax(mV) 782 189 380
Pmax(W) 0,782 0,418 0,251
Isc(A) 1,58 3,21 2,31
Voc(mV) 1089 404 450
Fill Factor 0,45449 0,32208 0,24127
Efisiensi (%) 0,01192 0,00613 0,00389
dengan prinsip dioda Schottky. Akan tetapi, nilai efisiensi yang dihasilkan masih sangat rendah. Faktor yang mempengaruhi rendahnya nilai efisiensi dapat disebabkan oleh beberapa hal, seperti adanya impuritas dan cacat kristal. Faktor ini dapat menghambat pembangkitan pasangan elektron-hole karena terjadinya rekombinasi prematur.
KESIMPULAN DAN SARAN
Kesimpulan
Deposisi CdS yang dibuat dengan metode CBD pada suhu 70oC menghasilkan lapisan berwarna kuning di atas subtrat ITO. Pemilihan waktu dan temperatur saat deposisi sangat mempengaruhi sifat morfologi dari film yang dihasilkan. Daerah serapan cahaya dari film CdS berada pada kisaran panjang gelombang 300-500 nm dengan nilai celah energi sebesar 2,449 eV.
Pola XRD menunjukkan bahwa telah terbentuk polikristal CdS dengan struktur hexagonal. Selain itu, terbentuk pula puncak kristal lainnya seperti ITO. Kemunculan
puncak selain CdS dapat dipengaruhi oleh impuritas dan ketebalan film.
Konduktivitas elektrolit polimer tertinggi ialah pada konsentrasi KI/I2 tertinggi
(0,5-0,05 M) sebesar 1,46876 x 10-5 1,20728 x 10-3 S/cm. Konduktivitas polimer meningkat dengan semakin meningkatnya frekuensi dan molaritas elektrolit.
Sel fotoelektrokimia dengan konsentrasi elektrolit yang semakin meningkat menunjukkan sifat sensitivitas yang semakin baik dengan menghasilkan nilai tegangan keluaran yang semakin tinggi. Efisiensi konversi tertinggi dihasilkan oleh sel surya pada konsentrasi (0,5/0,05) M sebesar 0,11791%. Peningkatan nilai karakteristik sel surya terhadap molaritas elektrolitnya berbuhungan dengan peningkatan jumlah pasangan redoks (I-/I3-) yang bekerja pada sel.
Perbedaan nilai intensitas penyinaran menghasilkan nilai arus-tegangan yang berbeda pula.
Dari variasi susunan rangkaian sel surya fotoelektrokimia, diperoleh VOCdan efisiensi
tertinggi pada rangkaian sel surya yang disusun secara seri. Sedangkan ISC tertinggi
diperoleh pada susunan rangkaian paralel.
Saran
Efisiensi sel surya dipengaruhi oleh larutan elektrolit. Untuk mencapai sel yang lebih optimal pada semikonduktor tipe-n, maka disarankan untuk mencoba variasi konsentrasi I2 yang lebih tinggi dibanding
konsentrasi KI. Selain itu, dapat dicoba pula untuk menggunakan larutan elektrolit lainnya. Tidak terkontrolnya kebocoran polimer saat pelapisan mempengaruhi karakteristik persambungan CdS/polimer, maka perlu dilakukan teknik lainnya untuk mencegah hal tersebut.
DAFTAR PUSTAKA
1. Hutauruk, P. T. P. (2000). Efek Fotovoltaik Lapisan Tipis CdS (Cadmium Sulfide) pada Sistem Sel Surya Fotoelektrokimia. [skripsi]. Bogor: Fakultas Matematika dan Ilmu Pengetahuan Alam, Institut Pertanian Bogor
2. Wenas, W. W. “Teknologi Sel Surya: Perkembangan Dewasa Ini dan yang Akan Datang”. 1994. Web. 25
November 2010.
17
3. Strandwitz, N. C., J. Good, J. & Lewis, N. S. “Photoelectrochemistry of Semiconductors”. Electrochemistry Encyclopedia. November 2011. Web.
23 Februari 2012.
<http://electrochem.cwru.edu/encycl/art -p06-photoel.htm>
4. Anonim. 2010. Web. 20 Juli 2011. <http://repository.upi.edu/operator/uplo ad/s_d515_043461_chapter2.pdf> 5. Restuanita, D.P. (2004).Pembuatan dan
Karakterisasi Prototipe Sel Surya Nanokristal TiO2 Tersensitisasi Dye
Menggunakan CuI Sebagai Elektrolit (TiO2/Dye/CuI) [skripsi]. Bogor: Departemen Fisika, Institut Pertanian Bogor
6. Singh, P. K. et al. “Present status of solid state photoelectrochemical solar cells and dye sensitized solar cells using PEO-based polymer electrolytes”. Natural Science. 8 April 2011. Web. 23
Februari 2012.
<http://iopscience.iop.org/2043-6262> 7. Lestari, S. I. (2006). Sintesis dan
Optimalisasi Gel Kitosan-Gom Guar [skripsi]. Bogor: Departemen Kimia, Institut Pertanian Bogor
8. Yani, S. (2011). Efek Fotovoltaik pada Persambungan CdS/P3HT-Kitosan [tesis]. Bogor: Sekolah Pascasarjana Boifisika. Institut Pertanian Bogor 9. Rio, S. R. & Iida, M. (1999).Fisika dan
Teknologi Semikonduktor. Jakarta: Pradnya Paramita
10. Anonim. “Semikonduktor”. 25 April 2010. Web. 12 Oktober 2011. <http://jonioke.blogspot.com/2010/04/se mikonduktor.html>
11. Hamonanga, A. “Prinsip Dasar Semikonduktor”. 18 Januari 2009. Web.
12 Oktober 2011.
<http://www.electroniclab.com/index.ph p?option=com_content&view=article&i d=13:prinsip-dasar-semikonduktor> 12. Iswanto, A. “Prinsip Kerja Sel Surya
P-N”. 22 Juni 2008. Web. 17 Februari 2012. <http://102fm- itb.org/2008/06/22/prinsip-kerja-sel-surya-sambungan-p-n/>
13. Çetinörgü, E., Gümüs, C. & Esen, R. (2006). Effects of Deposition Time and Temperature on the Optical Properties of Air-Annealed Chemical Bath Deposited CdS Films.Thin Solid Films, 515, 1688–1693.
14. Tiwari, S. & Tiwari, S. (2006). Development of CdS Based Stable Thin
Film Photo Electrochemical Solar Cells. Solar Energy Materials & Solar Cells, 90, 1621-1628.
15. Patidar, D. et al. (2006). Optical Properties of CdS Sintered Film. Bull. Mater. Sci., 29, 21–24.
16. Jinxia, XU. (2008). Fabrication and Photoluminescence Property of CdS Nanowire Array by Template Electrodeposition. Jurnal of Wuhan University of Technology-Mater. Sci., 23, 188-120.
17. Tjakrawadi, I. K. (2003). Sifat Optik dan istrik Lapisan Tipis CdS Hasil Deposisi CBD (Chemical Bath Deposition) [skripsi]. Bogor: Fakultas Matematika dan Ilmu Pengetahuan Alam, Institut Pertanian Bogor
18. Hill, E.R. & Keramidas, B.G. (1966). A Model for The CdS Solar Cell. Pyhs.Rev., (3), 189-193.
19. Robinson, P. “Spotlight on Colour:Vermillion and Cadmium Red”. Winsor&Newton. 2003-2011. Web. 28
Januari 2012.
<http://www.winsornewton.com/resourc e-centre/product-articles/vermilion-cadmium-red>
20. Steele, R. B. “Electron-Doped Antifluorites as Superconductors”. Chemexplore. 2004. Web. 23 Februari 2012.
<http://www.chemexplore.net/antifluorit es.htm>
21. Aguilar, J. H.et al. (2006). Influence of the S/Cd Ratio on the Luminescent Properties of Chemical Bath Deposition CdS Films. Solar Energy Materials & Solar Cells, 90, 2305-2306.
22. Altosaar, M. et al. (2005). Comparison of CdS Films Deposited from Chemical Bath Containing Different Doping Impurities. Thin Solid Films,(480–481), 147–150.
23. Oladeji, I. O. & Lee, C. (1997). Optimization of Chemical Bath Deposited Cadmium Sulfide Thin Films. J. Electrochemical Soc., 144, 2342-2346.
24. Muhammad, F. H. et al. (2010). Conductivity and Dielectric Studies on Filler-Doped Hexanoyl Chitosan based Polymer Electrolytes. Solid State Science and Technology,18, 44-52. 25. Buraidah, M. H. et al. (2010).
18
International Journal of Photoenergy, 2010(805836).
26. Putri, R. (2010). Studi Konduktivitas Elektrolit Polimer Kitosan/PVA+KOH . [tesis]. Bogor: Sekolah Pascasarjana Biofisika. Institut Pertanian Bogor. 27. Romawarni, A. (2011).Sintesis dan Uji
In Vitro Hidroksiapatit Berporogen Kitosan dengan Metode Sol Gel. [skripsi]. Bogor: Departemen Kimia, Institut Pertanian Bogor.
28. Herdianto, N. (2002). Pembuatan dan Karakterisasi Sifat-Sifat Fotoelektrokimia Lapisan Semiknduktor Nanokristal TiO2. [skripsi]. Bogor: Jurusan Fisika, Institut Pertanian Bogor. 29. Maddu, A. (2010).Penuntun Praktikum
Eksperimen Fisika II. Laboratorium Fisika Lanjut, Jurusan Fisika, IPB. Bogor.
30. Zhou, X. et al. (2008). Preparation and Formation Mechanism of CdS Nano-Films via Chemical Bath Deposition. Journal of Jilin University (Science Edition), 3, 18-22.
31. Yani, S., Maddu, A. & Irmansyah. (2011). Pengaruh Doping Boron Terhadap Struktur, Morfologi, dan Karakteristik Optik Film CdS Hasil Deposisi dengan Metode CBD. Bogor 32. Devi R, P. Purkayashta, P. K. Kalita, B.
K. Sarma. (2007). Synthesis of Nanocrystalline CdS Thin Film in PVA Matrix.Bull. Mater. Sci.30(2): 123-128 33. Lesmana, T. J. (2009). Pembuatan dan
Karakterisasi Sel Surya Hibrid ITO/CdS/Klorofil/PANI/ITO [tesis]. Bogor: Sekolah Pascasarjana Boifisika. Institut Pertanian Bogor
20
Lampiran 1 Data perhitungan konduktivitas polimer kitosan
Tabel A.
Data konduktansi elektrolit polimer kitosan dengan variasi [elektrolit]
Konsentrasi [M] f (Hz) luas (A) tebal (l) Z (kΩ) G (µS) Z (Ω) G (S)
0
100
7,48E-05 0,00004
258,473 3,8688761 258473 3,86888E-06
500 79,8108 12,529633 79810,8 1,25296E-05
1000 64,908222 15,406369 64908,222 1,54064E-05
5000 24,3744 41,026651 24374,4 4,10267E-05
0,1-0,01
100
7,48E-05 0,00004
146,253 6,8374666 146253 6,83747E-06
500 60,1708 16,619357 60170,8 1,66194E-05
1000 44,086889 22,682481 44086,889 2,26825E-05
5000 7,90744 126,46318 7907,44 0,000126463
0,2-0,02
100
6,83E-05 0,00004
67,1327 14,89587 67132,7 1,48959E-05
500 20,7724 48,140802 20772,4 4,81408E-05
1000 5,5156667 181,30175 5515,6667 0,000181302
5000 2,94795 339,21878 2947,95 0,000339219
0,3-0,03
100
0,000063 0,00004
40,2097 24,869621 40209,7 2,48696E-05
500 10,67887 93,642867 10678,87 9,36429E-05
1000 4,2349111 236,13247 4234,9111 0,000236132
5000 1,67537 596,88308 1675,37 0,000596883
G (mS) Z (Ω) G (S)
0,4-0,04
100
0,000063 0,00004
2,0833507 479,996 0,002083351
500 3,0171219 331,4417 0,003017122
1000 5,2541245 190,32667 0,005254124
5000 9,0884387 110,0299 0,009088439
0,5-0,05
100
0,000063 0,00004
2,3132994 432,283 0,002313299
500 60,38064 16,5616 0,06038064
1000 96,910702 10,318778 0,096910702
5000 190,1466 5,2591 0,190146603
Z
: Impedansi (
)
G
: Koduktansi (S)
A
: Luas penampang bahan (m
2)
l
: tebal bahan (m)
σ
: konduktivitas (S/m)
ρ
: resistivitas (
m)
21
Tabel B.
Data Perhitungan Konduktivitas elektrolit polimer kitosan
Konsentrasi KI-I2[M]
f (Hz) luas (m2) tebal (m) ρ
(Ωm) σ(S/m) σ(S/cm)
0
100
7,48E-05 0,00004
483021,42 2,0703E-06 2,0703E-08
500 149146,43 6,70482E-06 6,70482E-08
1000 121297,24 8,24421E-06 8,24421E-08
5000 45549,66 2,19541E-05 2,19541E-07
0,1-0,01
100
7,48E-05 0,00004
273310,29 3,65884E-06 3,65884E-08
500 112444,18 8,8933E-06 8,8933E-08
1000 82387,374 1,21378E-05 1,21378E-07
5000 14777,029 6,76726E-05 6,76726E-07
0,2-0,02
100
6,83E-05 0,00004
125454,23 7,97103E-06 7,97103E-08
500 38818,423 2,5761E-05 2,5761E-07
1000 10307,402 9,70177E-05 9,70177E-07
5000 5508,9816 0,000181522 1,81522E-06
0,3-0,03
100
0,000063 0,00004
75141,877 1,33082E-05 1,33082E-07
500 19956,138 5,01099E-05 5,01099E-07
1000 7913,9901 0,000126359 1,26359E-06
5000 3130,8477 0,000319402 3,19402E-06
0,4-0,04
100
0,000063 0,00004
755,9937 0,001322762 1,32276E-05
500 522,02068 0,001915633 1,91563E-05
1000 299,7645 0,003335952 3,33595E-05
5000 173,29709 0,005770437 5,77044E-05
Konsentrasi [M] f (Hz) luas (A) tebal (l) ρ(Ωm) σ(S/m) σ(S/cm)
0,5-0,05
100
0,000063 0,00004
680,84573 0,00