LAMPIRAN 1
PERHITUNGAN DAN DATA HASIL PENELITIAN
Pada penelitian ini, dilakukan dua analisa yaitu analisa kadar
selulosa, hemiselulosa, dan lignin terhadap pulp yang dihasilkan pada proses
delignifikasi serta analisa kadar glukosa terhadap kadar glukosa yang di
hasilkan pada proses hidrolisa.
L.1 Tahap Delignifikasi
L.1.1 Perhitungan Kadar Hemiselulosa
Kadar hemiselulosa dihitung dengan rumus:
×
100 %1. Kadar hemiselulosa (blanko 1)
Berat a = 0,9748 gr
Berat b = 0,8940 gr
Kadar hemiselulosa =
×
100 % = 8,08 %2. Kadar hemiselulosa (Run 2)
Berat a = 0,9639 gr
Berat b = 0,8537 gr
Kadar hemiselulosa =
×
100 % = 10,02 %3. Kadar hemiselulosa (Run 5)
Berat a = 0,9519 gr
Berat b = 0,8062 gr
Kadar hemiselulosa =
×
100 % = 14,57 %4. Kadar hemiselulosa (Run 8)
Berat a = 0,9392 gr
Berat b = 0,7811 gr
1.2 Perhitungan Kadar Selulosa
Kadar selulosa dihitung dengan rumus :
×
100 %1. Kadar Selulosa (blanko 1)
Berat b = 0,8940 gr
Berat c = 0,6518 gr
Kadar selulosa
=
×
100 % = 24,22 %2. Kadar Selulosa (Run 2)
Berat b = 0,8537 gr
Berat c = 0,5553 gr
Kadar selulosa =
×
100 % = 29,48 %3. Kadar Selulosa (Run 5)
Berat b = 0,8062 gr
Berat c = 0,4517 gr
Kadar selulosa =
×
100 % = 35,45 %4. Kadar Selulosa (Run 8)
Berat b = 0,7811 gr
Berat c = 0,3887 gr
Kadar selulosa =
×
100 % = 39,24%1.3 Perhitungan Kadar Lignin
Kadar lignin dihitung dengan rumus :
×
100 %1. Kadar lignin (blanko 1)
Berat c = 0,6518 gr
Kadar lignin =
×
100 % = 19,40 %Maka,hasil dari keseluruhan hasil pada proses delignifikasi dapat dilihat
pada tabel L1.1:
Tabel L1.1 Hasil Analisa Kadar Hemiselulosa, Selulosa dan Lignin
5 14,57 35,45 6,52
6 16,09 37,54 5,35
7 12,95 38,76 4,98
8 15,81 39,24 3,77
9 18,59 39,80 3,62
*Larutan blanko adalah larutan yang hanya menggunakan larutan NaOH
2. Tahap Hidrolisa
Pada percobaan ini, dilakukan analisa kadar glukosa menggunakan
metode Luff:
1. Rumus Perhitungan Kadar Glukosa
% Glukosa =
Keterangan :
W1 = Berat glukosa (mg)
Fp = Faktor pengenceran dari volume larutan Luff yang digunakan
W = Bobot contoh (mg)
2. Rumus Perhitungan Volume Na2SO4 Menurut Metode Luff
Volume Na2SO4 = ( Vblanko - Vtio ) x Normalitassesungguhnya/
Normalitascontoh
Wsampel = 2,0271 gr = 2027,1 mg
Vblanko = 24,95 ml
Vtio = 16,85 ml
Ntio = 0,0990 N
Volume Na2SO4 = ( 24,95 ml – 16,85 ml ) x = 8,019 ml
Table L.1.2 Penetapan gula menurut Luff Schoorl berdasarkan SNI
01-2892-1992
Penentuan berat glukosa menurut metode Luff dilakukan dengan
menggunakan interpolasi dari yang tertera pada Table L.1.2.
Dimana :
X (Vol Tio) ml Y (Berat Glukosa) mg
X1 8 Y1 19,8
X 8,019 Y 19,849
X2 9 Y2 22,4
Berat glukosa = 19,8 ml + (0,019 mg x 2,6 mg) = 19,849 mg
Maka kadar glukosa =
Dan untuk run selanjutnya akan dilanjutkan dengan cara seperti di atas.
1. Sampel pada menit 60 dengan cairan ionik 10 %.
Wsampel = 1,9918 gr = 1991,8 mg
Vblanko = 24,95 ml
Vtio = 13,75 ml
Ntio = 0,0990 N
Faktor Pengenceran = 250/10
Volume Na2SO4 = ( 24,95 ml – 13,75 ml ) x = 11,088 ml
Berat Glukosa = 27,6 mg + ( 0,088 mg x 2,7 mg ) = 27,8376 mg
Kadar Glukosa =
2. Sampel pada menit 60 dengan cairan ionik 15 %.
Wsampel = 2,0653 gr = 2065,3 mg
Vblanko = 24,95 ml
Vtio = 13,10 ml
Faktor Pengenceran = 250/10
Volume Na2SO4 = ( 24,95 ml – 13,10 ml ) x = 11,731 ml
Berat Glukosa = 27,6 mg + ( 0,731 mg x 2,7 mg ) = 29,5750 mg
Kadar Glukosa =
3. Sampel pada menit 60 dengan cairan ionik 20 %.
Wsampel = 2,1094 gr = 2109,4 mg
Vblanko = 24,95 ml
Vtio = 12,45 ml
Ntio = 0,0990 N
Faktor Pengenceran = 250/10
Volume Na2SO4 = ( 24,95 ml – 12,45 ml ) x = 12,05 ml
Berat Glukosa = 30,3 mg + ( 0,05 mg x 2,7 mg ) = 30,435 mg
Kadar Glukosa =
Maka hasil dari semua analisa pada proses hidrolisa dapat dilihat pada Tabel
L 1.3.
Run Kadar Glukosa (%)
Blanko 1 (30 menit) 24,48
Blanko 2 (60 menit) 28,13
Blanko 3 (90 menit) 30,87
1 35,3
2 36,1
3 37,4
4 36,7
5 38,6
6 39,4
7 35,9
8 37,3
9 38,3
LAMPIRAN 2
DOKUMENTASI PENELITIAN
L 2.1 Gambar Proses Penggilingan Ampas Tebu
Gambar L 2.1 Penghancuran (penggilingan) Ampas Tebu Menggunakan
Ball Mill
L 2.2 Gambar Proses Pengayakan Serbuk Ampas Tebu
Gambar L 2.2 Pengayakan Serbuk Ampas Tebu Menggunakan Ayakan 60
L 2.3 Gambar Serbuk Ampas Tebu yang Sudah Diayak
Gambar L 2.3 Serbuk Ampas Tebu yang Sudah Diayak
L 2.4 Gambar Hasil Proses Pemasakan Menggunakan ChCl
Gambar L 2.4 Hasil Proses Pemasakan Menggunakan ChCl
L 2.5 Gambar Penyaringan Serbuk Ampas Tebu Hasil Pemasakan
Gambar L 2.5 Proses Penyaringan Serbuk Ampas Tebu Hasil Pemasakan
L 2.6 Gambar Proses Pemasakan dengan Menggunakan Oven
Gambar L 2.6 Proses Pemasakan dengan Menggunakan Oven
L 2.7 Gambar Serbuk Ampas Tebu Hasil Delignifikasi
Gambar L 2.7 Hasil Delignifikasi Gambar L 2.8 Hasil Delignifikasi
DAFTAR PUSTAKA
Abidin, R. 2009. Membuat Bensin dari Ubi. Jakarta : Cipta Prima.
Aden, A., M. Ruth, K. Ibsen, dan J. Jechura, (2002), “Lignocellulosic
Biomass to Ethanol Process Design and Economics Utilizing
Co-Current Dilute Acid Prehydrolysis and Enzymatic Hydrolysis for
Corn Stover”, Report T-P510- 32438. Golden, CO: National Renewable Energy Laboratory.
Al-Baari, A. N, (2013),”Profil Produksi Alkohol dari Fermentasi Whey dan
Ampas Tebu”, Jurnal Aplikasi Teknologi Pangan.
Anggraini, D., Han Roliadi, (2011), “Pembuatan Pulp Dari Tandan Kosong Kelapa Sawit Untuk Karton Pada Skala Usaha Kecil”, Jurnal Penelitian Hasil Hutan Vol. 29 No. 3, September 2011: 211-225.
Anindyawati, Trisanti. 2009. Prospek Enzim dan Limbah Lignoselulosa
untuk Produksi Bioetanol. Pusat Penelitian Bioteknologi-LIPI:
Cibinong.
Anonim. 2007. Sugarcane Bud Chips for Seed Multiplication. Sugarcane
Breeding Institute, Indian.
Artati, Enny, K., Novia, Margareta, dan Widhie, Visia, (2010), “Konstanta
Kecepatan Reaksi Sebagai Fungsi Suhu pada Hidrolisa Selulosa dari
Ampas Tebu dengan Katalisator Asam Sulfat”, Jurnal Teknik Kimia,
Vol. 9. No. 1. Halaman: 1-4, Jurusan Teknik Kimia, Fakultas
Teknik, Universitas Sebelas Maret, Surakarta.
Cheng, Fangchao, Wang, Hui, Chatel, Gregory, Gurau, Gabriel, and Rogers,
Robin, (2014), “Facile pulping of lignocellulosic biomass using choline acetate”, Laboratory of Bio-based Material Science and
Technology of Ministry Education of China, College of Material
Elda Melwita. 2011. Ionic Liquid Sebagai Katalisator Potensial Untuk
Meningkatkan Produksi Bioetanol. Prosiding Seminar Nasional A
VoER ke-3. Palembang
Farmer V, Welton T. 1999. The Oxidation of Alcohols Using Rethonium
Catalysts and Imidazolium Ionic Liquids. International Symposium
on Molten Salts: Electrochemical Society INC.
Gendish, Yoricya. 2015. Proses Delignifikasi Lignoselulosa Tandan Kosong
Kelapa Sawit Menggunakan Cairan Ionik Kolin Klorida.
Departemen Teknik Kimia, Fakultas Teknik Kimia. Medan:
Universitas Sumatera Utara.
Hermiati, Euis, (2009), “ Pemanfaatan Biomassa Lignoselulosa Ampas Tebu untuk Produksi Bioetanol”, Departemen Teknologi Industri
Pertanian, Fakultas Teknologi Pertanian, Institut Pertanian Bogor.
Farid. B. 2003. Perbanyakan Tebu (Saccharum Officinarum L.) Secara In
Vitro pada Berbagai Konsentrasi IBA dan BAP. J. Sains dan
Teknologi. 3: 103-109.
Ida, Bagus, dkk, (2011), “Delignifikasi Ampas Tebu dengan Larutan Natrium Hidroksida sebelum Proses Sakaraifikasi secara Enzimatis
menggunakan Selulase Kasar dari Aspergillus Niger FNU 6018”,
Jurusan Teknologi Industri Pertanian, Fakultas Teknologi Pertanian,
Denpasar, Bali.
Irna, Cicy, dkk, (2013), “Produksi Bioetanol dari Ampas Tebu dengan
Metode Simultan Sakarifasi dan Fermentasi”, Jurnal Kimia, Jurusan
Kimia FMIPA, Universitas Andalas.
Isroi. 2011. Produksi Bioethanol Berbahan Baku Biomassa Lignoselulosa :
Hidrolisis Asam. (online)
(http://isroi.wordpress.com/2008/11/21/produksi-bioethanol-berbahan-baku-biomassa-lignoselulosa-hidrolisis/ diakses pada
Judoamidjojo M, Sa’id EG, Hartoto L. 1989. Biokonversi. Direktorat
Jendral Pendidikan Tinggi. Bogor. Pusat antar Universitas
Bioteknologi Institut Pertanian Bogor.
K. Zhao, Changzhi Li. 2012. Efficient Acid-Catalyzed Hydrolysis of
Cellulose in Ionic Liquid. China: Chinese Academy of Sciences.
Kataren, S. 1986. Minyak dan Lemak Pangan. Jakarta: Universitas
Indonesia.
Krisna, Agustin. 2015. Preatretment Ampas Tebu (Saccharum Oficinarum)
Sebagai Bahan Baku Bioetanol Generasi Kedua. Jurnal Pangan dan
Agroindustri Vol. 3 No. 4 P. 1430-1437. Malang: Universitas
Brawijaya.
Maryudi, (2009), Pembuatan Gula dari Pati Biji Nangka dengan Hidrolisis
Asam Khlorida, Laporan Penelitian, Jurusan Teknik Kimia,
Universitas Ahmad Dahlan, Yogyakarta.
Oktavianus, Ferdin, Martua, Roy S, dan Bustan, Djoni, (2013), “Pembuatan
Bioetanol dari Batang Jarak Menggunakan Metode Hidrolisa dengan
Katalis Asam Sulfat”, Jurnal Teknik Kimia, Jurusan Teknik Kimia,
Fakultas Teknik, Universitas Brawijaya, Palembang.
Risdianto H, Setiadi T, Suhardi SH, Nipoperbowo W. 2007. Pemilihan
spesies jamur dan media amobilisasi untuk produksi enzim lignolitik.
Prosiding seminar nasional rekayasa kimia dan proses. ISSN:
1411-4216.
Samsuri, M. G., Baiquni, M., Hermansyah, A., Wijanarko, A., Prasetya, B.,
Nasikin, M., 2007, Pemanfaatan Selulosa Bagas untuk Produksi
Ethanol Melalui Sakarifasi dan Fermentasi Serentak dengan Enzim
Xylanase. Makara Teknologi 2007, Vol. 11:17-24.
Sastrohamidjojo H, Prawirohatmojo S. 1995. KAYU : Kimia, Ultrastruktur,
Sediawan, W.B., Megawati, Millati, R., and Syamsiah, S., (2007),
Hydrolysis of Lignocellulosic Waste for Ethanol Production,
International Biofuel Conference, Bali, Indonesia.
Sjostrom, E. (1995). Kimia Kayu Dasar-Dasar dan Penggunaan. UGM
Press. Yogyakarta.
Syamsuri I, Sulisestijono, Ibrohim, dan Rahayu, (2007), “IPA Biologi”, jilid
2. Jakarta: Erlangga.
Taherzadeh, M. J. dan Karimi, Keikhosro, (2008), “Pretreatment of
Lignocellulosic Wastes to Improve Ethanol and Biogas production:
A Review”, International Journal of Molecular Sciences, Vol. 9,
Hal. 1621- 1651Ketaren,S. Minyak dan Lemak Pangan. Jakarta :
Universitas Indonesia, 1986.
Tjokroadikoesoemo S. 1986. HFS dan Industri Ubi Kayu Lainnya. Jakarta.
PT. Gramedia.
Vancov T., Alston A., Brown T., McIntosh S. 2014. Use of Ionic Liquids in
Converting Lignocellulosic Material to Biofuels. USA: Energy 45.
Wilkes, Jhon S., Zaworotko, Michael J. 1992. Air and Water Stable
1-ethyl-3-methylimidazolium Based Ionic Liquid. USA: Royal Society of
BAB III
METODOLOGI
3.1 Waktu dan Tempat
Penelitian ini berlangsung selama 2 bulan. Penelitian dilaksanakan di
Laboratorium Penelitian Kimia, Jurusan Teknik Kimia Industri, Fakultas
Teknik, Pendidikan Teknologi Kimia Industri.
3.2 Alat dan Bahan
3.2.1 Alat dan Bahan untuk Delignifikasi
Alat yang digunakan adalah neraca analitik, blender, ayakan mesh,
kertas saring, oven, dan alat-alat gelas (pyrex) yang umum digunakan dalam
laboratorium kimia. Bahan baku yang digunakan dalam penelitian adalah
ampas tebu. Bahan kimia yang digunakan antara lain: aquadest, kolin
klorida, dan natrium hidroksida.
3.2.2 Alat dan Bahan untuk Hidrolisa
Peralatan yang digunakan adalah: magnetic stirrer, dan alat-alat
gelas (pyrex) yang umum digunakan dalam laboratorium kimia. Sedangkan
bahan yang di gunakan adalah selulosa hasil delignifikasi. Bahan kimia
yang digunakan antara lain: aquadest, kolin klorida, dan asam sulfat.
3.3 Rancangan Penelitian
Penelitian ini dirancang menggunakan Rancangan Acak Lengkap
(RAL) yang terdiri dari variabel yaitu variasi waktu dan jumlah cairan ionik
pada proses deliginfikasi terhadap rendemen selulosa, sehingga terdapat 9
unit percobaan. Parameter yang diamati yaitu jumlah lignin, hemiselulosa
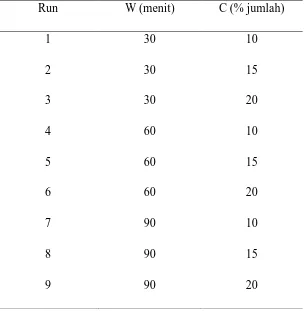
Tabel 3.1 Rancangan Acak Lengkap (RAL) untuk Proses Delignifikasi
Run W (menit) C (% jumlah)
1 30 10
2 30 15
3 30 20
4 60 10
5 60 15
6 60 20
7 90 10
8 90 15
9 90 20
Keterangan untuk proses delignifikasi:
W (Waktu) : = 30 menit, = 60 menit, = 90 menit
C (Jumlah larutan ionik) : = 10 %, = 15 %, = 20 %
Sedangkan untuk proses hidrolisis terdiri dari variabel yaitu variasi
waktu dan jumlah cairan ionik. Parameter yang di amati adalah jumlah
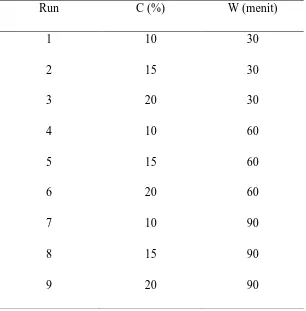
Tabel 3.2 Rancangan Acak Lengkap (RAL) untuk Proses Hidrolisis
Run C (%) W (menit)
1 10 30
2 15 30
3 20 30
4 10 60
5 15 60
6 20 60
7 10 90
8 15 90
9 20 90
Keterangan untuk proses hidrolisis:
W (Waktu) : = 30 menit, = 60 menit, = 90 menit
C (Jumlah larutan ionik) : C1 = 10 %, C2 = 15 %, C3 = 20 %
3.4 Persiapan Bahan Baku
Perlakuan awal terhadap ampas tebu meliputi pencucian,
pengeringan, dan pengayakan. Pencucian dilakukan untuk menghilangkan
bahan-bahan yang terikut dalam ampas tebu seperti kulit dan kotoran lain.
Pengeringan dilakukan dengan menggunakan sinar matahari langsung.
Pengeringan dilakukan untuk memudahkan dalam proses penggilingan serat
ampas tebu, karena pada keadaan lembab ampas tebu sukar untuk
dihancurkan. Tahap penghancuran bertujuan untuk memperkecil ukuran
ampas tebu menggunakan blender. Ampas tebu yang sudah dihancurkan
3.5 Prosedur Tahap Delignifikasi
1. Serbuk ampas tebu ditimbang sebanyak 30 gram, kemudian dimasukkan
ke dalam gelas kimia.
2. Larutan NaOH 1N sebanyak 6% (dari berat ampas tebu) ditambahkan ke
dalam gelas kimia yang berisi serbuk ampas tebu.
3. Kemudian campuran diaduk dengan rata sampai merendam serbuk
ampas tebu.
4. Serbuk ampas tebu yang sudah tercampur rata dicuci 3 kali dengan air
dan dikeringkan pada suhu 105 °C selama 16 jam sebelum digunakan.
5. Lalu serbuk ampas tebu diayak, kemudian dicampurkan dengan cairan
ionik kolin klorida, dipanaskan sampai suhu 130 °C selama waktu yang
sudah ditentukan.
6. Setelah itu serbuk ampas tebu dicuci dengan air untuk menghilangkan
cairan ionik.
7. Kemudian dicuci lagi dengan air sampai pH 7 selanjutnya dikeringkan
pada suhu 30 °C didalam oven.
3.6 Analisis selulosa, hemiselulosa, dan lignin
1. Sebanyak 1 gram serbuk kering ampas tebu hasil delignifikasi (berat
konstan) dimasukkan dalam Erlemmeyer 250 ml dan ditambah aquades
150 ml.
2. Kemudian dipanaskan selama 2 jam di dalam penangas pada suhu
100°C, dan dilakukan penyaringan dan pencucian dengan aquades
sampai volume filtrat 300 ml.
3. Kemudian residu dikeringkan pada oven bersuhu 105 °C hingga
diperoleh berat konstan (a). Residu kering (a) dimasukkan kedalam
Erlenmeyer 250 ml ditambah 150 ml H2SO4 1N, kemudian dipanaskan
4. Kemudian dilakukan penyaringan dan residu dicuci dengan aquades
sampai volume filtrat 300 ml. Residu yang diperoleh kemudian
dikeringkan hingga beratnya konstan dan ditimbang (b).
5. Selanjutnya residu kering (b) dimasukkan ke dalam Erlenmeyer 250 ml
dan ditambahkan H2SO4 72% sebanyak 10 ml. Direndam selama 4 jam
pada suhu kamar kemudian ditambahkan 150 ml H2SO4 1 N (untuk
pengenceran), dipanaskan pada penangas air pada suhu 100 °C selama 2
jam.
6. Kemudian dilakukan penyaringan dan dicuci dengan aquades hingga
volume filtrat 400 ml. Residu dikeringkan hingga beratnya konstan dan
ditimbang (c). Residu (c) tersebut kemudian diabukan selama 6 jam
(600 °C) (Chesson, 1981).
Kadar hemiselulosa, selulosa, dan lignin dapat dihitung dengan
menggunakan rumus:
Kadar hemiselulosa = × 100%
Kadar selulosa = × 100%
Kadar lignin = × 100%
3.7 Prosedur Tahap Hidrolisis
Selulosa yang tidak segera diproses disimpan terlebih dahulu di
lemari es untuk menghindari tumbuhnya jamur dan atau mikroorganisme.
Sedangkan untuk selulosa yang akan digunakan, dikeringkan terlebih dahulu
pada suhu 105oC selama 16 jam selanjutnya disimpan dalam desikator untuk mempertahankan level moisture (Lavarack dkk., 2002). Tahap hidrolisis
dilakukan dengan tahapan sebagai berikut:
1. Selulosa hasil delignifikasi ditimbang sebanyak 10 gram.
3. Masukkan selulosa hasil delignifikasi tersebut ke dalam erlenmeyer dan
di campur dengan cairan ionik sebanyak yang telah ditentukan.
4. Kemudian tutup erlenmeyer tersebut dengan gabus dan dipanaskan
sambil diaduk dengan menggunakan magnetic stirrer selama 30, 60, dan
90 menit.
5. Suhu di dalam erlenmeyer dijaga pada 90 oC.
6. Hasil dari hidrolisa ini kemudian disaring dengan menggunakan kertas
saring.
7. Kemudian dilakukan pengukuran kadar glukosa dengan menggunakan
metode Luff Schoorl.
3.8 Analisa Kadar Glukosa
1. Timbang sebanyak 2 gr sampel dan masukkan kedalam labu ukur 250
ml, ditambahkan 100 ml air dan di homogenkan.
2. Kemudian tambahkan 5 ml pb-asetat.
3. Selanjutnya teteskan 1 tetes larutan (NH4)2HPO4 10%
4. Kemudian goyang dan tepatkan isi labu ukur sampai tanda garis batas
dengan aquades, dihomogenkan dan disaring.
5. Larutan hasil penyaringan dipipet dan dimasukkan kedalam erlenmeyer
500 ml.
6. Setelah itu tambahkan 15 ml aquades dan 25 ml larutan Luff serta
beberapa butir batu didih.
7. Kemudian hubungkan erlenmeyer dengan pendingin tegak, dipanaskan
diatas pemanas listrik sampai mendidih selama 10 menit.
8. Setelah dipanaskan kemudian diangkat dan didinginkan.
9. Setelah dingin ditambah 10 ml larutan KI 20% dan 25 ml larutan H2SO4
25%.
10.Titrasi dengan larutan natrium tio-sulfat 0,0990 N dengan larutan kanji
0,5% sebagai indikator.
11.Selanjutnya buat larutan blanko dengan 25 ml air dan 25 ml larutan luff
dengan cara yang sama tanpa menggunakan larutan sampel
Cara perhitungan: ( Vblanko – Vtio ) ml tio yang dibutuhkan oleh contoh
dijadikan ml 0,1000 N, kemudian dalam daftar table lampiran A cari
beberapa mg glukosa yang tertera untuk ml tio yang dipergunakan
(misalnya W1 mg)
W1 x fp
% Glukosa = ___________ x 100%
W
Dimana:
3.9 Flowchart Percobaan
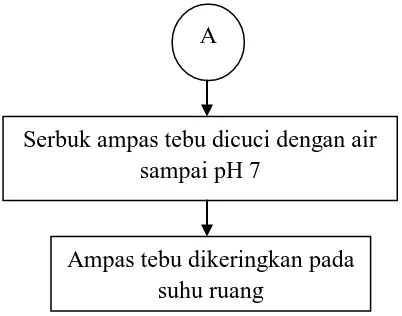
3.9.1 Persiapan Bahan Baku
Gambar 3.1 Persiapan Bahan Baku
Ampas Tebu ditimbang 30 gram
Ampas Tebu dicuci
Pengeringan dengan sinar matahari langsung
Ampas tebu dihancurkan
Ampas tebu diayak
Ampas tebu siap untuk di lanjutkan ke tahap
selanjutnya Mulai
3.9.2 Proses Delignifikasi
Mulai
Serbuk ampas tebu direndam sebanyak 30
gram didalam gelas kimia
Larutan NaOH sebanyak 3% dari
berat ampas tebu
Ampas tebu dicuci 3 kali dengan air
Ampas tebu dikeringkan pada suhu 105°C selama 16 jam
serbuk ampas tebu diayak
Ampas tebu dicampurkan dengan cairan ionik kolin
Ampast tabu dipanaskan sampai suhu 130°C selama waktu yang sudah
ditentukan
Gambar 3.2 Proses Delignifikasi
A
Serbuk ampas tebu dicuci dengan air sampai pH 7
3.9.3 Analisa Selulosa, hemiselulosa, dan lignin
1 gram serbuk kering ampas tebu disiapkan
Ampas tebu dimasukkan ke dalam erlenmeyer 250 ml
Ampas tebu ditambahkan aquades 150 ml
Ampas tebu dipanaskan selama 2
jam pada suhu 100
o
C
Ampas tebu disaring dan dicuci
Ampas tebu dikeringkan pada oven dengan suhu 105 oC dan diperoleh berat konstan (a)
Mulai
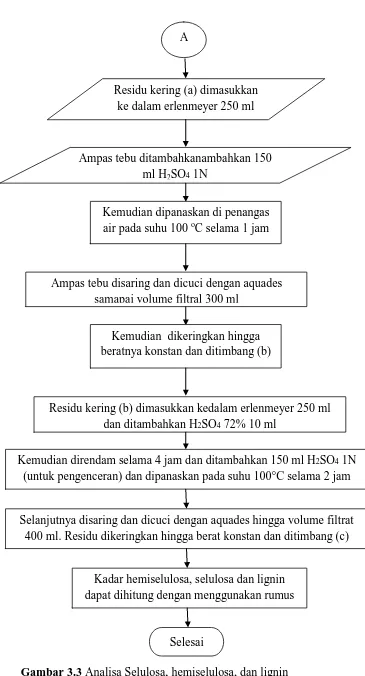
Gambar 3.3 Analisa Selulosa, hemiselulosa, dan lignin
Residu kering (a) dimasukkan ke dalam erlenmeyer 250 ml
Ampas tebu ditambahkanambahkan 150 ml H2SO4 1N
Kemudian dipanaskan di penangas air pada suhu 100 oC selama 1 jam
Ampas tebu disaring dan dicuci dengan aquades samapai volume filtral 300 ml
Kemudian dikeringkan hingga beratnya konstan dan ditimbang (b)
Residu kering (b) dimasukkan kedalam erlenmeyer 250 ml dan ditambahkan H2SO4 72% 10 ml
Kemudian direndam selama 4 jam dan ditambahkan 150 ml H2SO4 1N
(untuk pengenceran) dan dipanaskan pada suhu 100°C selama 2 jam A
Selanjutnya disaring dan dicuci dengan aquades hingga volume filtrat 400 ml. Residu dikeringkan hingga berat konstan dan ditimbang (c)
Kadar hemiselulosa, selulosa dan lignin dapat dihitung dengan menggunakan rumus
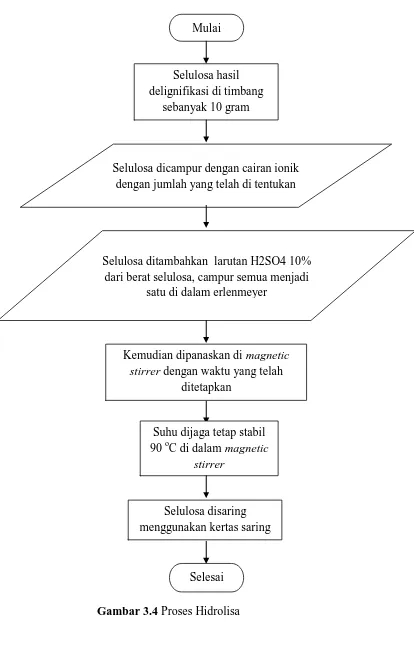
3.9.4 Proses Hidrolisa
Gambar 3.4 Proses Hidrolisa
Mulai
Selulosa hasil delignifikasi di timbang
sebanyak 10 gram
Selulosa dicampur dengan cairan ionik dengan jumlah yang telah di tentukan
Selulosa ditambahkan larutan H2SO4 10% dari berat selulosa, campur semua menjadi
satu di dalam erlenmeyer
Kemudian dipanaskan di magnetic
stirrer dengan waktu yang telah
ditetapkan
Suhu dijaga tetap stabil 90 oC di dalam magnetic
stirrer
Selulosa disaring menggunakan kertas saring
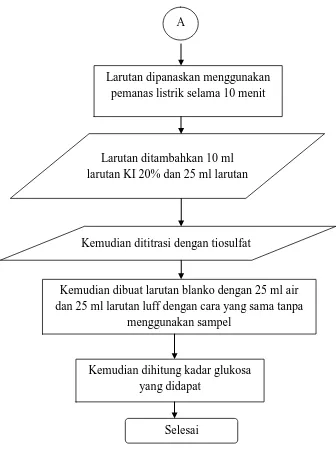
3.9.5 Flowchart Analisa Kadar Glukosa
Tidak
Ya
Mulai
2 gr sampel dimasukkan ke dalam labu ukur 250 ml
Kemudian diteteskan 1 tetes larutan (NH4)2HPO4 10%
Apakah larutan sudah terendapkan seluruhnya?
A
Kemudian ditambahkan 5 ml Pb-asetat
Larutan dikocok 12 kali dan disaring
Larutan hasil penyaringan dipipet 10 ml
Gambar 3.5 Flowchart Analisa Kadar Glukosa
Kemudian dihitung kadar glukosa yang didapat
Selesai A
Larutan dipanaskan menggunakan pemanas listrik selama 10 menit
Larutan ditambahkan 10 ml larutan KI 20% dan 25 ml larutan
Kemudian dititrasi dengan tiosulfat
Kemudian dibuat larutan blanko dengan 25 ml air dan 25 ml larutan luff dengan cara yang sama tanpa
BAB IV
HASIL DAN PEMBAHASAN
4.1 Proses Delignifikasi terhadap Ampas Tebu
Pada penelitian ini dilakukan proses delignifikasi, yaitu proses
pemutusan senyawa lignin dari biomassa. Proses ini dilakukan sebagai
pretreatment sebelum proses hidrolisis, agar kandungan lignin dalam
biomassa pada proses hidrolisis menjadi berkurang dari bahan baku
sehingga mendapatkan selulosa dengan kadar kemurnian yang tinggi.
Delignifikasi ampas tebu ini menggunakan NaOH dalam sistem Kolin
Klorida (ChCl) dan tanpa ChCl.
Pemutusan senyawa lignin menggunakan NaOH dalam sistem cairan
ionik ChCl bekerja ganda untuk memicu terjadinya degradasi gugus basa
dari larutan pemasak (ChCl dan NaOH) yang menyerang alfa dan beta
lignin, sehingga hasil degradasi tidak stabil memicu terjadinya kondensasi.
Kondensasi menyebabkan putusnya ikatan lignin dari hemiselulosa dan
selulosa. ChCl adalah cairan yang bersifat asam. Pada suasana asam, bobot
molekul lignin cenderung bertambah. Peristiwa ini menyebabkan lignin
mengendap, lalu larut dalam air proses pencucian. Sehingga lignin yang
terbuang semakin banyak, berbanding terbalik dengan lignin sisa yang
tertinggal di dalam ampas tebu hasil delignifikasi. Hal tersebut
mengakibatkan kadar selulosa dan hemiselulosa semakin meningkat seiring
bertambahnya waktu pemasakan. Sedangkan mekanisme pemutusan
senyawa lignin menggunakan NaOH tanpa ChCl tidak berbeda dengan
mekanisme menggunakan ChCl. Hanya saja NaOH bekerja sendiri untuk
4.1.1 Perbandingan Kadar Lignin yang Tertinggal di dalam Ampas Tebu Hasil Proses Delignifikasi Tanpa ChCl dan Menggunakan ChCl
Proses delignifikasi ampas tebu dilakukan menggunakan NaOH
dalam sistem cairan ionik kolin klorida (ChCl) dengan berbagai variasi
jumlah ChCl yaitu 10%, 15%, 20% dari berat ampas tebu dan hanya
menggunakan NaOH tanpa ChCl. Gambar 4.1 adalah grafik yang
menunjukkan perbandingan proses delignifikasi dengan jumlah ChCl 15%
dan tanpa ChCl terhadap kadar lignin.
Gambar 4.1 Perbandingan Kadar Lignin yang Tertinggal di dalam
Ampas Tebu Hasil Proses Delignifikasi Tanpa ChCl dan
Menggunakan ChCl 15 %
Dapat dilihat pada Gambar 4.1 bahwa kadar lignin menurun secara
signifikan seiring peningkatan jumlah ChCl dan waktu delignifikasi,
sedangkan kadar lignin tanpa ChCl hanya sedikit menurun. Penurunan
lignin secara signifikan ini disebabkan adanya kerja ganda antara ChCl dan
NaOH yang memutuskan ikatan lignin dari bahan baku untuk meningkatkan
senyawa lignin yang terbuang. Sehingga kadar lignin yang tertinggal di
di dalam Ampas Tebu hasil delignifikasi menggunakan NaOH tanpa ChCl
lebih besar, hal ini disebabkan tanpa adanya bantuan dari ChCl.
Peneliti terdahulu melaporkan delignifikasi kayu menggunakan kolin
asetat ([Cho] [OAc]) menghasilkan kadar lignin sebesar 5% (Cheng et al.,
2014). Namun, pada penelitian ini delignifikasi ampas tebu menggunakan
NaOH (tanpa ChCl) menghasikan kadar lignin sebesar 18,99% dan
delignifikasi menggunakan ChCl sebesar 3,62 %. Hal ini terlihat jelas
bahwa delignifikasi menggunakan NaOH dalam sistem cairan ionik ChCl
menurunkan kadar lignin lebih besar dibandingkan tanpa ChCl.
4.1.2 Perbandingan Proses Delignifikasi Tanpa ChCl dan Menggunakan ChCl Terhadap Kadar Selulosa
Gambar 4.2 menunjukkan pengaruh perbandingan antara jumlah ChCl
15% dan tanpa ChCl terhadap kadar selulosa.
Gambar 4.2 Perbandingan Kadar Selulosa Hasil Proses Delignifikasi Tanpa
ChCl dan dengan Menggunakan ChCl 15 %
Pada proses delignifikasi ampas tebu ini, NaOH dan ChCl bekerja
sama sebagai larutan pemasak untuk memutuskan ikatan lignin. ChCl
membantu NaOH meningkatkan kadar selulosa yang dihasilkan. Dapat
dilihat pada Gambar 4.2 bahwa kadar selulosa meningkat secara signifikan
dengan menggunakan NaOH dalam sistem cairan ionik ChCl, sedangkan
bahkan relatif konstan. Hal ini disebabkan ChCl bersifat asam
mengakibatkan terjadinya degradasi senyawa penyusun lignin sehingga
kadar selulosa yang diperoleh semakin meningkat. Sedangkan kadar
selulosa yang diperoleh tanpa ChCl peningkatannya tidak besar disebabkan
NaOH merupakan basa alkali yang memiliki kemampuan melarutkan
senyawa organik dan anorganik tidak relatif tinggi.
Penelitian terdahulu menyatakan bahwa delignifikasi jerami padi
menggunakan Switchable Ionic Liquids dengan 1-etil-3-metilimidazolium
asetat ([C2mim] OAc) menghasilkan kadar selulosa sebesar 32% (jian Luo,
2013). Pada penelitian ini, kadar selulosa tertinggi yang dihasilkan
menggunakan ChCl sebesar 39,8%, sedangkan kadar selulosa tertinggi yang
dihasilkan tanpa menggunakan ChCl sebesar 24,98%. Sangat terlihat jelas
bahwa delignifikasi menggunakan NaOH dalam sistem cairan ionik ChCl
menghasilkan kadar selulosa yang lebih besar dibandingkan tanpa ChCl.
4.1.3 Perbandingan Proses Delignifikasi Tanpa ChCl dan Menggunakan ChCl Terhadap Kadar Hemiselulosa
Gambar 4.3 menunjukkan pengaruh perbandingan antara jumlah
ChCl 15% dan tanpa ChCl terhadap kadar hemiselulosa.
Gambar 4.3 Perbandingan Kadar Hemiselulosa Hasil Proses
Sama halnya dengan selulosa, ChCl membantu NaOH dalam
meningkatkan kadar hemiselulosa yang dihasilkan. Pada proses delignifikasi
ampas tebu ini, NaOH dan ChCl bekerja sama sebagai larutan pemasak
untuk memutuskan ikatan lignin dari hemiselulosa dan selulosa. Dapat
dilihat pada Gambar 4.3 bahwa kadar hemiselulosa meningkat seiring
peningkatan jumlah ChCl dan waktu delignifikasi, tetapi kadar hemiselulosa
tanpa ChCl meningkat tidak signifikan, bahkan cenderung konstan. Hal ini
disebabkan tanpa adanya bantuan dari ChCl yang membantu memutuskan
ikatan lignin untuk meningkatkan kadar hemiselulosa.
Peneliti sebelumnya menyatakan bahwa delignifikasi kayu pinus
menggunakan cairan ionik Choline Acetate ([Cho][OAc]) menghasilkan
kadar hemiselulosa sebesar 10,2% (Cheng 2014). Pada penelitian ini, kadar
hemiselulosa tertinggi yang dihasilkan menggunakan ChCl sebesar 18,59%,
sedangkan kadar hemiselulosa tertinggi yang dihasilkan tanpa menggunakan
ChCl sebesar 8,25%. Hal ini terlihat jelas bahwa kadar hemiselulosa lebih
besar dihasilkan dengan menggunakan NaOH dalam sistem cairan ionik
ChCl dibandingkan tanpa ChCl.
4.1.4 Pengaruh Jumlah Kolin Klorida (ChCl) dan Waktu Delignifikasi Terhadap Kadar Lignin yang Tertinggal di Dalam Ampas Tebu Hasil Delignifikasi
Proses delignifikasi ampas tebu dilakukan menggunakan NaOH
dalam sistem cairan ionik kolin klorida (ChCl) pada berbagai variasi jumlah
ChCl, yaitu 10%, 15%, dan 20% berat ampas tebu. Hasil penelitian
menunjukkan bahwa jumlah cairan ionik yang berbeda berpengaruh
terhadap lignin yang dihasilkan. Gambar 4.4 menunjukkan hubungan antara
kadar lignin yang tertinggal di dalam Ampas Tebu dengan jumlah ChCl dan
Gambar 4.4 Pengaruh Jumlah Kolin Klorida (ChCl) dan Waktu
Delignifikasi Terhadap Kadar Lignin yang Tertinggal
di dalam Ampas Tebu Hasil Delignifikasi
Pada proses delignifikasi ampas tebu dalam sistem ChCl ini
diharapkan dapat dihasilkan selulosa dengan kandungan lignin yang rendah.
Gambar 4.4 menunjukkan bahwa kadar lignin menurun seiring peningkatan
jumlah ChCl. Penurunan kadar lignin disebabkan waktu pemasakan yang
cukup lama memicu terjadinya degradasi gugus basa dari larutan pemasak
yang menyerang alfa dan beta lignin, sehingga hasil degradasi tidak stabil
memicu terjadinya kondensasi (Hidayati, 2014). Kondensasi menyebabkan
putusnya ikatan lignin dari hemiselulosa dan selulosa. Dan karena ChCl
bersifat asam, pada suasana asam bobot molekul lignin cenderung
bertambah. Peristiwa ini menyebabkan lignin mengendap, lalu larut dalam
air proses pencucian.
Sesuai dengan uraian di atas, bahwa ChCl sebagai larutan pemasak
yang membantu NaOH menyebabkan makin berkurangnya kadar lignin
seiring bertambahnya waktu sampai pada batas waktu tertentu. Peningkatan
jumlah larutan pemasak memudahkan pemutusan ikatan senyawa penyusun
lignin karena kondisi asam menyebabkan perusakan senyawa lignin yang
ikut terlarut pada pelarut. Namun, dengan jumlah ChCl lebih dari 15%
menyebabkan kadar lignin yang tertinggal di dalam Ampas Tebu relatif
yang menyebabkan lignin tidak ikut larut dalam air pencucian (Hidayati,
2014).
Peran ChCl terhadap kadar lignin yang dihasilkan adalah
memutuskan senyawa lignin, sehingga pada saat pengendapan dilakukan
semakin banyak lignin terisolasi. Kandungan lignin di dalam ampas tebu
yaitu sekitar 3 % dari berat ampas tebu.
4.1.5 Pengaruh Jumlah Kolin Klorida (ChCl) dan Waktu Delignifikasi Terhadap Kadar Selulosa
Kadar selulosa merupakan faktor penting dari proses delignifikasi.
Semakin tinggi kadar selulosa yang bisa dihasilkan dari ampas tebu, maka
semakin besar pengaruh untuk proses selanjutnya.
Gambar 4.5 menunjukkan hubungan antara kadar selulosa dengan
jumlah ChCl dan waktu delignifikasi.
Gambar 4.5 Pengaruh Jumlah ChCl dan Waktu Delignifikasi Terhadap
Kadar Selulosa
Dapat dilihat pada Gambar 4.5, bahwa kadar selulosa meningkat
seiring peningkatan jumlah ChCl dan waktu delignifikasi. Peningkatan
selulosa terjadi sampai pada batas waktu tertentu dan diperoleh kadar
yang bersifat selektif, yang khusus menyerang lignin dan menguraikan
selulosa dari ikatan lignin.
Sesuai dengan pernyataan di atas bahwa peningkatan kadar selulosa
disebabkan oleh ikatan lignin yang terputus dari hemiselulosa dan selulosa
akibat degradasi pada alfa dan beta lignin, sehingga selulosa yang dihasilkan
semakin meningkat. Namun, kadar selulosa yang dihasilkan cenderung
konstan pada waktu 90 menit dengan jumlah ChCl lebih dari 15%. Hal ini
disebabkan terjadinya degradasi pada kelompok polisakarida yaitu selulosa
dan hemiselulosa yang terkandung pada bahan baku.
Dilaporkan dari hasil penelitian terdahulu bahwa kadar selulosa dari
hasil delignifikasi yang dilakukan pada ampas tebu menggunakan H2O2
dalam media asam asetat pada konsentrasi H2O2 15% adalah 35,71% pada
suhu 130 °C dengan waktu delignifikasi 3 jam. Penggunaan H2O2 pada
konsentrasi lebih dari 15% menyebabkan terjadinya oksidasi polisakarida
yang pada akhirnya menyebabkan penurunan selulosa akibat reaksi yang
terjadi (Zuidar, 2014).
Peran ChCl terhadap kadar selulosa yang didapatkan adalah sebagai
larutan pemasak yang dapat meningkatkan kadar selulosa yang dihasilkan
dibandingkan tanpa ChCl. ChCl juga meningkatkan porositas sampel
sehingga lebih mudah mendelignifikasi serbuk ampas tebu dengan
meningkatnya waktu delignifikasi. Kandungan selulosa hasil dari
delignifikasi di dalam ampas tebu adalah sekitar 39% dari berat ampas tebu.
4.1.6 Pengaruh Jumlah Kolin Klorida (ChCl) dan Waktu Delignifikasi Terhadap Kadar Hemiselulosa
Gambar 4.6 menunjukkan hubungan antara kadar hemiselulosa
Gambar 4.6 Pengaruh Jumlah ChCl dan Waktu Delignifikasi Terhadap Jumlah Kadar Hemiselulosa
Kadar hemiselulosa meningkat seiring peningkatan jumlah ChCl dan
waktu delignifikasi. Sama halnya dengan selulosa, peningkatan
hemiselulosa disebabkan oleh ikatan lignin yang terputus dari hemiselulosa
dan selulosa akibat degradasi pada alfa dan beta lignin, sehingga
hemiselulosa yang dihasilkan semakin meningkat. Hemiselulosa merupakan
suatu polisakarida yang terdapat dalam tanaman dan tergolong senyawa
organik non-kristalin.
Penelitian terdahulu menyatakan bahwa delignifikasi dapat
menurunkan kadar lignin hingga 16% dari kandungan awal, serta
meningkatkan kadar selulosa hingga 32% dan hemiselulosa hingga tiga kali
lipat. Berdasarkan hasil penelitian tersebut diperoleh perlakuan yang
terbaik, yaitu delignifikasi dengan konsentrasi NaOCl 1% dan lama
perendaman 5 jam (Bagus Ida, 2011). Pada penelitian ini, kandungan
hemiselulosa di dalam ampas tebu adalah 18,59 % dari berat ampas tebu.
4.2 Proses Hidrolisis terhadap Ampas Tebu
4.2.1 Perbandingan Proses Hidrolisis Tanpa Menggunakan Cairan Ionik Dengan Menggunakan Cairan Ionik
Jika dibandingkan antara proses hidrolisis dengan menggunakan
yang lebih besar pada sistem yang menggunakan cairan ionik seperti
ditunjukan pada Gambar 4.2. Kadar glukosa optimum diperoleh pada
kondisi waktu reaksi 60 menit dengan kadar glukosa yang dihasilkan 39,4%
pada konsentrasi kolin klorida 15%. Sedangkan untuk proses hidrolisis
tanpa penggunaan cairan ionik didapat kadar glukosa yang lebih sedikit
pada kondisi waktu yang sama yaitu 90 menit sebesar 30,87%.
Gambar 4.8 Perbandingan Kadar Glukosa Proses Hidrolisis Dengan
Menggunakan Cairan Ionik 15 % dan Tanpa Menggunakan
Cairan Ionik
Dapat dilihat pada Gambar 4.8 bahwa kadar glukosa semakin
meningkat dengan meningkatnya waktu reaksi dan didapat kadar glukosa
tertinggi dengan menggunakan cairan ionik. Waktu reaksi optimum untuk
memeperoleh kadar glukosa tertinggi adalah 60 menit dengan menggunakan
cairan ionik 20%. Dengan menggunakan cairan ionik dapat mengefisienkan
waktu hidrolisisis lebih cepat untuk mendapatkan kadar glukosa terbaik.
Dapat dilihat dari gambar, kadar glukosa lebih sedikit fluktuasi dari
waktu 30 menit sampai waktu 90 menit pada proses hidrolisis dalam sistem
cairan ionik. Jika waktu hidrolisis diperpanjang dengan menggunakan
temperatur yang sama dan kenaikan waktu hidrolisis yang sama, didapat
hasil hidrolisis yang tidak terlalu jauh dengan menggunkan cairan ionik.
Namun, jika tanpa menggunkan cairan ionik akan terjadi kenaikan kadar
perubahan kenaikan yang signifikan sebab di pengaruhi oleh pemanasan
yang dapat merusak rantai polisakarida yang akan menjadi glukosa.
Peneliti sebelumnya merancang penggunaan cairan ionik mampu
mengikat selulosa dan asam serta dapat memecah kristal selulosa dengan
mengikat beberapa gugus hidroksil, meningkatkan kelarutan dan aktivitas
katalitik (Haryanti, 2015).
4.2.2 Pengaruh Perubahan Waktu Reaksi Dan Konsentrasi Kolin Klorida Terhadap Kadar Glukosa
Proses hidrolisis ampas tebu dilakukan dalam sistem cairan ionik kolin
klorida dengan variasi konsentrasi kolin klorida 10%, 15% dan 20% dan
variasi waktu hidrolisis 30, 60, dan 90 menit. Hasil analisis menunjukkan
bahwa jumlah cairan ionik yang berbeda, berpengaruh terhadap kadar
glukosa yang dihasilkan dengan konsentrasi optimum 20% dan waktu reaksi
optimum 60 menit yaitu sebesar 39,4%. Gambar 4.7 menunjukkan
hubungan antara kadar glukosa dengan jumlah kolin klorida dan waktu
hidrolisis.
Gambar 4.7 Pengaruh Waktu Reaksi Dan Konsentrasi Kolin Klorida Terhadap Kadar Glukosa
Dapat dilihat pada Gambar 4.7 bahwa kadar glukosa semakin
kolin klorida. Pada penelitian ini, untuk peningkatan konsentrasi kolin
klorida dari 10% sampai 20% terjadi kenaikan persentase kadar glukosa
yaitu sebesar 2,1% pada waktu 30 menit, 2,7% pada waktu 60 menit, dan
2,4% pada waktu 90 menit. Sedangkan untuk jumlah kolin klorida 20%,
peningkatan waktu hidrolisis dari 60 menit ke 90 menit, didapatkan kadar
glukosa yang menurun.
Semakin bertambahnya waktu reaksi, kadar glukosa yang dihasilkan
semakin bertambah dan sampai pada batas waktu tertentu akan diperoleh
kadar glukosa yang maksimum. Ini disebabkan kontak antara zat–zat yang bereaksi dapat lebih lama dan apabila waktu tersebut diperpanjang
pertambahan kadar glukosa sangat kecil bahkan akan menurun. Jika
semakin lama waktu reaksi, selulosa tidak larut dalam air sehingga
pemecahan rantai polisakarida menjadi glukosa tidak dapat berlangsung
dengan baik. Selain itu pemanasan yang terus-menerus dapat merusak
glukosa.
Kolin klorida mampu meningkatkan konversi selulosa menjadi gula.
Cairan ionik bereaksi dengan air dan dapat membantu mengikat
hemiselulosa agar serat hemiselulosa tidak terikut bersama selulosa dan
dapat membentuk senyawa glukosa dengan baik dan karena sifat cairan
ramah lingkungan maka dapat mengurangi konsentrasi katalis asam sulfat,
sehingga aman bagi lingkungan dan tidak menimbulkan korosi pada alat.
Pada penelitian ini, kadar glukosa optimum sebesar 39,4% diperoleh
pada kondisi waktu reaksi hidrolisis 60 menit dan konsentrasi cairan ionik
20%. Penggunaan cairan ionik yang berbeda sebagai pelarut memiliki
kemampuan melarutkan yang berbeda-beda pula tergantung pada ukuran
BAB V
KESIMPULAN DAN SARAN
5.1 KESIMPULAN
Kesimpulan yang dapat diambil dari penelitian yang telah dilakukan
adalah:
1. Pada proses delignifikasi ampas tebu menggunakan ChCl didapatkan
kadar selulosa terbaik adalah pada penggunaan ChCl sebesar 20 % dan
pada waktu 90 menit dengan hasil kadar selulosa yang didapat mencapai
39,80 %.
2. Penggunaan jumlah ChCl 20% dari berat ampas tebu sudah mencukupi
untuk terjadinya degradasi gugus basa dari larutan pemasak yang
menyerang alfa dan beta lignin, yang menyebabkan kadar selulosa
meningkat.
3. Kadar glukosa tertinggi sebesar 39,4%, diperoleh pada kondisi waktu
hidrolisis 90 menit dengan konsentrasi cairan ionik kolin klorida 15%,
sedangkan tanpa menggunakan cairan ionik kolin klorida diperoleh
kadar glukosa sebesar 30,87%.
5.2 SARAN
Sebaiknya untuk penelitian berikutnya disarankan untuk:
1. Mengkaji pengaruh peningkatan temperatur pada proses delignifikasi
ampas tebu.
2. Menggunakan cairan ionik berbasis kolin dengan anion yang berbeda
untuk melihat pengaruhnya terhadap kadar selulosa, hemiselulosa, dan
lignin yang dihasilkan.
3. Menggunakan alat uv-visible untuk menganalisa kadar glukosa yang
BAB II
TINJAUAN PUSTAKA
2.1 Tebu
Tanaman tebu (Saccharum officinarum) dimanfaatkan sebagai bahan baku utama dalam industri gula. Pengembangan industri gula mempunyai peranan penting bukan saja dalam rangka mendorong pertumbuhan perekonomian di daerah serta penambahan atau penghematan devisa, tetapi juga langsung terkait dengan pemenuhan kebutuhan pokok rakyat dan penyediaan lapangan kerja (Farid, 2003). Bagian lain dari tanaman seperti daunnya dapat pula dimanfaatkan sebagai pakan ternak dan bahan baku pembuatan pupuk hijau atau kompos. Ampas tebu digunakan oleh pabrik gula itu sendiri untuk bahan bakar selain itu biasanya dipakai oleh industri pembuat kertas sebagai campuran pembuat kertas.
Daun tebu yang kering (dalam bahasa Jawa, dadhok) adalah biomassa yang mempunyai nilai kalori cukup tinggi. Di pedesaan dadhok sering dipakai sebagai bahan bakar untuk memasak; selain menghemat minyak tanah yang makin mahal, bahan bakar ini juga cepat panas. Dalam konversi energi pabrik gula, daun tebu dan juga ampas batang tebu digunakan untuk bahan bakar boiler, yang uapnya digunakan untuk proses produksi dan pembangkit listrik (Anonim, 2007). Tanaman tebu dapat dilihat pada Gambar 2.1.
Gambar 2.1 Tanaman Tebu
atau pabrik gula yang menyewa lahan pertanian penduduk dan sekaligus mengupah tenaganya dalam usaha mengembangkan tanaman tebu bagi keperluan memenuhi bahan baku bagi pabriknya (Kartasapoetra, 1988).
Produk utama dari pabrik gula adalah gula putih. Namun ada produk yang merupakan produk samping dari pengolahan tebu menjadi gula. Hasil samping tersebut berupa tetes (molase), pucuk daun tebu, blotong, ampas tebu yang merupakan limbah pabrik. Hasil samping berupa limbah pabrik sering menimbulkan banyak permasalahan sebab menjadi sumber pencemaran lingkungan.
Ampas tebu adalah hasil samping dari proses ekstraksi (pemerahan) cairan tebu. Dari satu pabrik dapat dihasilkan ampas tebu sekitar 35 – 40% dari berat tebu yang digiling. Mengingat begitu banyak jumlahnya, maka ampas tebu akan memberikan nilai tambah untuk pabrik jika diberi perlakuan lebih lanjut (Tim Penulis PS, 1992).
2.2 Ampas Tebu
Ampas tebu adalah suatu residu dari proses penggilingan tanaman tebu (saccharum oficinarum) setelah diekstrak atau dikeluarkan niranya pada Industri pemurnian gula sehingga diperoleh hasil samping sejumlah besar produk limbah berserat yang dikenal sebagai ampas tebu (bagasse). Ampas tebu dapat dilihat pada gambar 2.2.
Gambar 2.2 Ampas Tebu
juta galon (setara dengan 18.819 juta liter) dan pada tahun 2008 meningkat menjadi 17.524 juta galon (setara dengan 66.328 juta liter). (Hermiati, 2009).
Manfaat umum yang dapat diperoleh dari bahan bakar bioetanol antara lain, digunakan untuk bahan baku industri turunan alkohol, campuran minuman keras, industri farmasi, sampai pada bahan baku campuran kendaraan. Tentu saja, pemanfaatan etanol ini harus disesuaikan dengan jenis kebutuhannya. Misalnya, untuk kebutuhan industri diperlukan etanol dengan grade antara 90-96,5%, sedangkan untuk minuman keras dibutuhkan etanol berkadar 99,5-100%, atau etanol yang harus betulbetul kering dan anhydrous supaya tidak korosif (Abidin, 2009).
Pemanfaatan ampas tebu untuk dikonversikan menjadi bioetanol telah banyak diteliti dari dulu hingga saat ini, diantaranya yang pernah memanfaatkan ampas tebu menjadi bioetanol yaitu M.Samsuri dkk (2007) dan Euis Hermiati dkk (2009).
Ampas tebu sebagian besar mengandung lignoselulosa. Panjang seratnya antara1,7 sampai 2 mm dengan diameter sekitar 20 mikro, sehingga ampas tebu ini dapat memenuhi persyaratan untuk diolah menjadi papan-papan buatan. Bagase mengandung air 48 - 52%, gula rata-rata 3,3% dan serat rata-rata 47,7%.
Serat bagase tidak dapat larut dalam air dan sebagian besar terdiri dari jenis selulosa, pentosan dan lignin (Husin, 2007). Menurut Husin (2007) hasil analisis serat bagas adalah seperti dalam Tabel 2.1.
Tabel 2.1 Komposisi kimia ampas tebu
Kandungan Kadar %
Delignifikasi adalah suatu proses pendahuluan penghilangan lignin
selulosa dengan kemurnian yang cukup besar. Delignifikasi selulosa dapat
dilakukan dengan beberapa cara, diantaranya yaitu :
1. Ozonolysis Pretreatment, yaitu delignifikasi menggunakan ozon
dilakukan pada suhu ruangan dan tekanan atmosfer serta dapat
menghancurkan sekitar lignin yang terkandung dalam lignoselulosa.
2. Delignifikasi Pulp menggunakan Hidrogen Peroksida ( dalam
media asam asetat.
3. Delignifikasi Oksigen, yaitu proses untuk mengurangi kandungan
lignin dari pulp coklat (yang belum mengalami proses pemutihan).
Bahan kimia yang dipakai adalah dan alkali.
4. Delignifikasi dengan larutan NaOH.
5. Delignifikasi menggunakan cairan ionik, yaitu delignifikasi
menggunakan garam yang berwujud cair di bawah suhu 100 °C.
Contoh cairan ionik kolin klorida (Trimethyl(2- hydroxyethyl)
ammonium chloride).
Tujuan dari proses delignifikasi yaitu untuk menghilangkan lignin, juga dapat mengurangi kristalinitas selulosa, dan meningkatkan porositas bahan. Selain lignin terdapat juga zat non selulosa lain seperti zat ekstraktif, tanin dan resin yang melekat kuat pada selulosa. Lignin merupakan salah satu bagian yang mengayu dari tanaman seperti janggel, kulit keras, biji, bagian serabut kasar, akar, batang dan daun. Lignin mengandung substansi yang kompleks dan merupakan suatu gabungan beberapa senyawa yaitu karbon, hidrogen dan oksigen. Selain lignin, bagian yang lain dari ampas tebu adalah selulosa. Selulosa merupakan polisakarida yang didalamnya mengandung zat-zat gula. Dalam pembuatan etanol dari ampas tebu yang digunakan adalah selulosanya sehingga lignin dalam kayu harus dihilangkan. Proses pemisahan atau penghilangan lignin dari serat-serat selulosa disebut delignifikasi atau pulping.
2.4 Selulosa
hidroksil pada rantai di sebelahnya. Serat selulosa yang mempunyai kekuatan fisik yang tinggi terbentuk dari fibril-fibril ini, tergulung seperti spiral dengan arah-arah yang berlawan menurut satu sumbu. Selulosa merupakan jenis polisakarida yang paling melimpah pada hampir setiap struktur tanaman. Kandungan selulosa kayu berkisar 48 – 50%, pada bagas berkisar antara 50 – 55% dan pada tandan kosong kelapa sawit sekitar 45%. Selulosa dapat dihidrolisis dengan asam kuat maupun dengan enzim selulase.
Selulosa adalah salah satu komponen utama dari ligniselulosa yang terdiri dari unit monomer D-glukosa yang terikat pada ikatan 1,4-glikosidik. Selulosa cenderung membentuk mikrofibril melalui ikatan inter dan intra molekuler sehingga memberikan struktur yang larut. Mikrofibril selulosa terdiri dari 2 tipe, yaitu kristalin dan amorf (Trisanti Anindyawati, 2009).
Adapun struktur selulosa dapat dilihat dibawah ini :
Gambar 2.3 Struktur Selulosa
Selulosa terdapat pada semua tanaman baik pohon tingkat tinggi hingga organisme primitif seperti rumput laut. Senyawa-senyawa seperti lemak, lilin, protein, dan pektin dapat dihilangkan dengan cara ekstraksi dengan pelarut organik atau alkali encer (Sastrohamidjojo dan Prawirohatmojo, 1995).
2.5 Hemiselulosa
Hemiselulosa termasuk dalam kelompok polisakarida heterogen yang dibentuk melalui biosintesis yang berbeda dari selulosa. Bebbeda dengan selulosa yang merupakan homopolisakarida, hemiselulosa merupakan heteropolisakarida. Derajat polimerisasi hemiselulosa dapat mencapai 200 (Sastrohamidjojo dan Prawirohatmojo, 1995).
air, bersifat plastis, dan mempunyai permukaan kontak antar molekul lebih luas dibandingkan dengan selulosa (Judoamidjojo, et al., 1989; Winarno, 1997). Ikatan di dalam rantai hemiselulosa banyak bercabang karena gugus
β-glukosida di dalam molekul yang satu berkaitan dengan gugus hidroksil , , dan dari molekul yang lain. Hemiselulosa berbentuk amorf,
mempunyai derajat polimerisasi lebih rendah dan mudah larut dalam alkali tetapi struktur larut dalam asam, sedangkan selulosa sebaliknya (Tjokroadikoesoemo, 1986). Struktur hemiselulosa dapat dilihat pada gambar 2.4.
Gambar 2.4 Struktur Hemiselulosa
2.6 Lignin
Lignin adalah polimer aromatik kompleks yang terbentuk melalui polimerisasi tiga dimensi dari sinamil alkohol dengan bobot molekul 11.000 (Krisnawati, 2008). Lignin terbentuk dari fenil propana, unit-unit fenil propana terikat satu dengan lainnya dengan ikatan ester (C-0-C) maupun ikatan karbon-karbon (Sjostrom, 1985).
Gambar 2.5 Struktur molekul lignin
2.7 Hidrolisis
Hidrolisis merupakan proses pemecahan polisakarida dalam biomassa lignoselulosa, yaitu selulosa dan hemiselulosa menjadi monomer gula yang dapat dilakukan secara kimia ataupun enzimatis. Pada hidrolisis sempurna selulosa akan menghasilkan glukosa, sedangkan hemiselulosa menghasilkan beberapa monomer gula pentose (C5) dan heksosa (C6). Hidrolisis dapat dilakukan secara kimia (asam) atau enzimatik (Trisanti, 2010). Hidrolisis ampas tebu adalah representasi dari proses delignifikasi yaitu memisahkan serat (selulosa dan fragmentasinya) yang terdapat dalam kayu dari senyawa lignin.
Pada metode hidrolisis asam, biomassa lignoselulosa dihidrolisa dengan asam pada suhu dan tekanan tertentu selama waktu tertentu, dan menghasilkan monomer gula dari polimer selulosa dan hemiselulosa. Hidrolisis selulosa menjadi glukosa dapat dilakukan menggunakan cara kimiawi dan hayati. Hidrolisis dengan cara kimiawi menggunakan asam kuat, sedangkan dengan cara hayati menggunakan enzim murni atau mikroorganisme penghasil enzim selulase. Kendala yang dihadapi yaitu rendahnya laju hidrolisis karena adanya kandungan lignin dalam bahan lignoselulosa. Oleh karena itu dilakukan proses delignifikasi sebelum dihidrolisis.
Beberapa asam yang umum digunakan untuk hidrolisis asam antara lain adalah asam sulfat (H2SO4), asam perklorat dan HCl. Asam sulfat
merupakan asam yang paling banyak diteliti dan dimanfaatkan untuk hidrolisis asam. Hidrolisis asam dapat dikelompokkan menjadi hidrolisis asam pekat dan hidrolisis asam encer (Isroi, 2008).
hidrolisis asam, antara lain: tidak terjadi degradasi gula hasil hidrolisis, kondisi proses yang lebih rendah (suhu rendah), berpotensi memberikan hasil yang tinggi dan biaya pemeliharaan peralatan relatif rendah karena tidak ada bahan yang korosif. Beberapa kelemahan dari hidrolisis enzimatik antara lain adalah membutuhkan waktu yang lebih lama, dan kerja enzim dihambat oleh produk. Di sisi lain harga enzim saat ini lebih mahal daripada asam sulfat, namun demikian pengembangan terus dilakukan untuk menurunkan biaya dan meningkatkan efisiensi hidrolisis maupun fermentasi (Isroi, 2008).
Hidrolisis dalam suasana asam menghasilkan pemecahan ikatan glikosida dan berlangsung dalam tiga tahap. Tahap pertama proton yang berkelakuan sebagai katalisator asam berinteraksi cepat dengan oksigen glikosida yang menghubungkan dua unit gula, yang akan membentuk asam konjugat. Langkah ini akan diikuti dengan pemecahan yang lambat dari ikatan C-O, dalam kebanyakan hal menghasilkan zat antara kation karbonium siklis. Protonasi dapat juga terjadi pada oksigen cincin , menghasilkan pembukaan cincin dan kation karbonium non siklis. Mekanisme reaksi total hidrolisis selulosa secara asam ditampilkan dibawah ini :
(C6H10O5)n + nH2O katalis asam/enzim nC6H12O6
(selulosa) (glukosa)
2.8 Cairan Ionik (Ionic Liquid)
Air adalah pelarut yang sangat populer di masyarakat. Namun, bila ditanyakan kepada ahli kimia tentang pelarut maka mereka bisa mengatakan banyak tentang benzena, toluen, diklorometan, kloroform dan banyak lagi. Pelarut memang menjadi sangat esensial dalam proses kimia. Banyak pelarut digunakan dengan penyesuaian zat terlarutnya. Itulah yang membuat banyak sekali jenis pelarut yang digunakan dalam proses kimia, baik itu dalam reaksi maupun pemisahan satu zat dari kumpulan zat.
Ada tiga komponen penting dari cairan ionik ini. Pertama, yang bermuatan positif (+) disebut kation. Kedua, yang bermuatan negatif (-) adalah anion. Dan terakhir yang diberi simbol R adalah subtituen alkil yang juga merupakan bagian dari kation. Ketiga komponen itu bisa divariasikan untuk mendapatkan sifat fisika dan kimia yang berbeda pula.
2.8.1 Sifat fisika dan kimia
Sifat fisik dari cairan ionik dapat diatur dengan memvariasikan kation, anion dan subtituen gugus alkilnya. Contohnya, kelarutan dalam air bisa diatur dengan gugus R-nya. Memperpanjang gugus alkil (R) akan menurunkan kelarutan dalam air dengan meningkatkan hidrofobisitas dari kationnya. Sifat kimia dan fisikanya bisa diubah dengan mengatur anionnya, seperti halida, nitrat, asetat, trifluoroasetat, tetrafluoroborat, triflat, heksafluorofosfat dan bis(trifluorometilsulfonil)imida. Contohnya, garam imidazolium dengan anion halida, nitrat dan trifluorofosfat bercampur sempurna dengan air, tapi dengan anion [PF6-] dan [(CF3SO2)2N-] tidak
bercampur dengan air, dan [BF4-] dan [CF3SO3-] bisa bercampur atau tidak
tergantung pada subtituen kationnya.
Titik leleh dari garam yang memiliki anion halida cenderung lebih tinggi bila anion yang digunakan lebih banyak, dan titik leleh umumnya meningkat seiring meningkatnya panjang rantai subtituen. Cairan ionik pertama yang banyak digunakan adalah campuran dari dialkilimidazolium atau alkilpiridinum halida dengan AlCl3 atau AlBr3 (Welton, 1999). Cairan ionik pertama yang stabil terhadap udara dan air yang memiliki titik leleh rendah adalah 1-etil-3-metilimidazolium BF4 dan 1-etil-3-metilimidazolium MeCO2 (Wilkes dan Zaworotko, 1992).
Cairan ionik lebih kental dari pelarut organik biasa. Contohnya, viskositas dari kebanyakan imidazolium berada pada rentang 35 sampai 500 cP dalam suhu ruang (Seddon et al, 2000). Garam dengan anion bis(trifluorometilsulfonil)imida [(CF3SO2)2N-] memiliki viskositas terendah dalam rentang tadi (Bonhote et al., 1996), sama juga seperti garam dengan kation pirolidinium (MacFarlane et al., 1999). Data yang dimiliki bahwa cairan ionik merupakan fluida Newtonian (Brennecke et al., 2001).
2.8.2 Kolin Klorida (Trimethyl(2- hydroxyethyl) ammonium chloride)
Kolin Klorida merupakan salah satu contoh cairan ionik yang berupa garam organik dengan rumus molekul C5H14ClNO dan mempunyai titik
leleh 302 °C (576 °F; 575 K). Dalam laboratorium kolin dapat dibuat dengan metilasi dimetiletanolamina dengan metil klorida.
Kolin klorida diproduksi secara massal dan merupakan aditif penting dalam pakan terutama untuk ayam mempercepat pertumbuhan. Garam kolin komersial lainnya adalah hidroksida kolin dan bitartrat kolin. Dalam bahan makanan senyawa ini sering hadir sebagai fosfatidilkolin. Hal ini juga digunakan sebagai aditif dalam cairan yang digunakan untuk rekah hidrolik. Dan berfungsi untuk menurunkan derajat kristalinitas dan meningkatkan porositas sampel sehingga lebih mudah mendelegnifikasi selulosa. Keuntungan kolin klorid dibandingkan perarut lainnya yaitu lebih mudah larut, harganya ekonomis, dan biodegradable. Struktur kolin klorid dapat dilihat pada gambar 2.6.
BAB I
PENDAHULUAN
1.1 Latar Belakang
Tebu merupakan tanaman yang ditanam untuk bahan
baku gula dan vetsin. Tanaman ini hanya dapat tumbuh di daerah beriklim
tropis. Tanaman ini termasuk jenis rumput-rumputan. Umur tanaman sejak
ditanam sampai bisa dipanen mencapai kurang lebih 1 tahun. Di Indonesia
tebu banyak dibudidayakan di pulau Jawa dan Sumatra. Luas dari
perkebunan tebu di Indonesia mencapai 398.260 ha (BKPM, 2008). Dari
proses pembuatan tebu tersebut akan dihasilkan gula 5%, ampas tebu 90%
dan sisanya berupa tetes (molasse) dan air (Enny, 2010).
Ampas tebu merupakan salah satu bahan baku pembuatan bioetanol yang mengandung selulosa. Disamping itu pemanfaatan ampas tebu masih dalam proses pengembangan, biasanya ampas tebu digunakan untuk bahan bakar, bahan baku untuk kertas, ahan baku industri kanvas rem, industri jamur dan lain-lain. Ampas tebu termasuk biomassa yang mengandung lignoselulosa sangat dimungkinkan untuk dimanfaatkan menjadi sumber energi alternatif seperti bioetanol atau biogas. Ampas tebu memiliki kandungan selulosa 52,7%, hemiselulosa 20,0%, dan lignin 24,2% (Samsuri
et al., 2007).
Bioetanol adalah salah satu bentuk energi terbaharui yang dapat diproduksi dari tumbuhan. Bioetanol dapat dibuat dari tanaman-tanaman yang umum, misalnya tebu, kentang, singkong, dan jagung. Krisis energi yang melanda saat ini merupakan akibat dari penggunaan energi fosil yang terlalu berlebihan sehingga cadangan energi yang tersedia semakin sedikit. Salah satu solusi mengatasinya adalah mengembangkan energi terbarukan yang dihasilkan berasal dari pemanfaatan limbah.
Delignifikasi selulosa dengan menggunakan cairan ionik lebih efektif dibandingkan tanpa cairan ionik. Ionic liquid (IL) atau cairan ionik adalah garam yang pada suhu kamar berbentuk cair. Hal ini disebabkan cairan ionik telah menurunkan derajat kristalinitas dan meningkatkan porositas sampel sehingga lebih mudah mendelegnifikasi selulosa.
Cairan ionik umumnya dapat digunakan pada suhu kamar dan tidak
menghasilkan reaksi samping yang bersifat toksik. Cairan ionik kolin
klorida (Trimethyl(2- hydroxyethyl) ammonium chloride) mempunyai
tingkat toksiksitas yang rendah, biodegradable, dapat dinyatakan sebagai
asam lemah. Riset-riset yang ada saat ini belum melaporkan aplikasi cairan
ionik terhadap lignoselulosa dari ampas tebu. Uraian-uraian diatas menjadi
tantangan untuk mempelajari delignifikasi lignoselulosa ampas tebu
menggunakan cairan ionik. Dapat dilihat pada Tabel 1.1 menunjukkan hasil
penelitian terdahulu tentang delignifikasi menggunakan cairan ionic.
Tabel 1.1 Data hasil penelitian tentang delignifikasi menggunakan cairan
Tabel 1.1 Data hasil penelitian tentang delignifikasi menggunakan cairan ionik (Lanjutan)
No. Bahan/Metode /Produk
Proses Hasil Nama Peneliti
Berdasarkan hasil-hasil penelitian di atas, dapat disimpulkan bahwa SIL MEA-SO2 terbukti lebih efisien dan lebih baik sebagai pelarut untuk
menghilangkan lignin, tapi memiliki harga yang mahal. Kemudian cairan ionik (kolin asetat ([Cho] [OAc]) bersifat biodegradable namun memiliki kekurangan yaitu kurang cepat sebagai bahan pelarut dalam proses delignifikasi. Sedangkan [C2mim] OAc adalah pelarut yang baik untuk
kayu. Kekurangan dari penelitian-penelitian sebelumnya menjadi kelemahan dalam proses delignifikasi, dan akan diperbaiki dalam penelitian ini.
Ampas tebu mempunyai potensi untuk digunakan sebagai sumber glukosa melalui proses hidrolisis dengan asam atau enzim. Larutan gula yang dihasilkan selanjutnya dapat dikonversi menjadi berbagai prosuk seperti alkohol yang mempunyai nilai ekonomis yang jauh lebih tinggi. Hidrolisis lignoselulosa dengan asam encer adalah yang paling umum diaplikasikan untuk mendapatkan gula .
Hidrolisis asam encer dilakukan menggunakan asam mineral seperti H2SO4 dan HCl, pada suhu antara 120-200 oC (Taherzadeh dan Karimi,
2007). Proses hidrolisis berbahan lignoselulosa yang telah dilakukan antara lain hidrolisis biji nangka menggunakan larutan HCl 0,1 N mendapatkan gula 9,84 mg/ml (Maryudi, 2009). Hidrolisis serbuk gergaji menggunakan larutan H2SO4 0,5% mendapatkan gula dengan kadar 11,53 mg/ml
(Sediawan, dkk, 2010). Dari hidrolisis asam memiliki kelemahan antara lain adalah membutuhkan waktu yang lebih lama, rendahnya laju hidrolisis dan jumlah glukosa yang dihasilkan sedikit
Penelitian yang telah dilakukan mengenai aplikasi cairan ionik dalam produksi bioalkohol menunjukkan bahwa cairan ionik berperan sebagai pelarut dalam proses hidrolisa lignoselulosa dan selulosa. Pelarutan selulosa dan lignoselulosa dalam cairan ionik mampu mempercepat reaksi hidrolisa dan meningkatkan konversi selulosa dan lignoselulosa menjadi gula.
Beberapa kajian hidrolisis menggunakan cairan ionik telah dilaporkan seperti ditunjukkan dalam Tabel 1.2.
Tabel 1.2 Data Hasil Penelitian Tentang hidrolisis dengan menggunakan cairan ionik. lebih rendah (dari 63,39% sebelum pengolahan awal menjadi 59 dan 36% setelah pengolahan awal), dan memperkecil ukuran partikel TKKS (dari 63,55 nm sebelum meningkatkan kadar glukosa yang reaksi 8 jam pada temperatur 90°C dan waktu kontak 20 jam
Tabel 1.2 Data Hasil Penelitian Tentang hidrolisis dengan menggunakan cairan ionic (Lanjutan)
No Bahan/Metode
Hasil glukosa selama 48 jam hidrolisis enzimatik sebesar 2,282 mg/ml menggunakan [c-Oim](CH3COO) >1,77 mg/ml
dengan yield glukosa meningkat
Berkaitan dengan hasil penelitian di atas, masih terdapat beberapa kekurangan yang perlu diperbaiki antara lain: cairan ionik 1-butil-3-metil imidazolium bromida dan selulase yang harus di sintesis terlebih dahulu, bersifat toksik dan waktu hirolisis yang cukup lama.
Kelebihan cairan ionik dibanding pelarut lain adalah tidak menguap dan polaritasnya dapat didesain menurut kebutuhan. Hal ini dapat meningkatkan selektifitas cairan ionik sebagai pelarut terhadap alkohol. Berdasarkan latar belakang tersebut, maka peneliti tertarik melakukan penelitian yang berjudul “PROSES DELIGNIFIKASI DAN HIDROLISIS LIGNOSELULOSA AMPAS TEBU MENGGUNAKAN
SISTEM CAIRAN IONIK KOLIN KLORIDA”.
1.2 Rumusan Masalah
1.3 Tujuan Penelitian
Tujuan penelitian ini adalah:
1. Mengetahui bagaimana pengaruh cairan ionik kolin klorida yang
digunakan dalam proses delignifikasi dan hidrolisis ampas tebu.
2. Menentukan kondisi terbaik dari delignifikasi dan hidrolisis ampas
tebu.
1.4 Manfaat Penelitian
Manfaat yang diharapkan dari penelitian delignifikasi ini adalah: 1. Menambah wawasan tentang proses delignifikasi dan hidrolisis
ampas tebu dengan menggunakan cairan ionik kolin klorida.
2. Memanfaatkan limbah ampas tebu untuk dijadikan sesuatu yang
lebih bernilai.
3. Cairan ionik berbasis garam kolin klorida ini diharapkan mampu
melarutkan biomassa dengan lebih baik dan dapat menggantikan
pelarut yang saat ini digunakan. Sehingga dapat mengurangi biaya
produksi dan dapat mengurangi tingkat pencemaran lingkungan.
1.5 Ruang Lingkup Penelitian
Adapun ruang lingkup dari penelitian ini adalah : a. Ampas tebu yang digunakan dari PTPN 2
b. Cairan ionik yang digunakan adalah kolin klorida
c. Jumlah ampas tebu yang digunakan adalah 30 gram
d. Variabel dalam proses delignifikasi yang dilakukan adalah :
1. Jumlah ChCl : 10%, 15% dan 20% (dari berat
komposisi yaitu analisis selulosa, hemiselulosa dan lignin.
g. Variabel dalam proses hidrolisis yang dilakukan adalah :
1. Jumlah ChCl : 10%, 15%, 20% (dari berat selulosa
hasil delignifikasi)
2. Jumlah H2SO4 1N : 10 % (dari berat selulosa hasil
delignifikasi) (Ferdin oktavianus, 2013)
3. Waktu : 30 menit, 60 menit dan 90 menit
4. Temperatur : 105 °C
h. Analisa yang dilakukan analisa kadar glukosa menggunakn