PEMBUATAN ETIL ASETAT DARI HASIL
HIDROLISIS, FERMENTASI DAN ESTERIFIKASI
KULIT PISANG KEPOK (Musa paradisiaca L.)
SKRIPSI
Oleh
RENI SUTRI
100405016
DEPARTEMEN TEKNIK KIMIA
FAKULTAS TEKNIK
UNIVERSITAS SUMATERA UTARA
MEDAN
PEMBUATAN ETIL ASETAT DARI HASIL
HIDROLISIS, FERMENTASI DAN ESTERIFIKASI
KULIT PISANG KEPOK (Musa paradisiaca L.)
SKRIPSI
Oleh
RENI SUTRI
100405016
SKRIPSI INI DIAJUKAN UNTUK MELENGKAPI SEBAGIAN
PERSYARATAN MENJADI SARJANA TEKNIK
DEPARTEMEN TEKNIK KIMIA
FAKULTAS TEKNIK
UNIVERSITAS SUMATERA UTARA
MEDAN
PENGESAHAN
Skripsi dengan judul:
PEMBUATAN ETIL ASETAT DARI HASIL HIDROLISIS, FERMENTASI DAN ESTERIFIKASI KULIT PISANG KEPOK (Musa paradisiaca L.)
dibuat untuk melengkapi persyaratan menjadi Sarjana Teknik pada Departemen Teknik Kimia Fakultas Teknik Universitas Sumatera Utara. Skripsi ini telah diujikan pada sidang ujian skripsi pada 22 Desember 2014 dan dinyatakan memenuhi syarat/sah sebagai skripsi pada Departemen Teknik Kimia Fakultas Teknik Universitas Sumatera Utara.
Medan,
Dosen Pembimbing
DEDIKASI
Penulis mendedikasikan skripsi ini kepada :
1. Kedua orang tua penulis, Kapten Inf. Suherman dan Fitri Agusmainur S.Pd yang tak hentinya memberikan doa dan dukungan baik moral maupun materil kepada penulis dalam menyelesaikan penelitian dan penulisan skripsi ini.
2. Seluruh keluarga besar penulis terutama adikku, Ridwan Sutri serta Amak, Nenek dan Kakek yang tak hentinya memberikan doa kepada penulis dalam menyelesaikan penelitian dan penulisan skripsi ini.
3. Ibu Dr. Ir. Iriany, M.Si dosen pembimbing yang telah banyak memberikan bimbingan, arahan, dan motivasi yang luar biasa dalam menyelesaikan penelitian dan penulisan skripsi ini.
4. Ibu Ir. Renita Manurung, MT selaku koordinator penelitian dan dosen penguji yang telah memberikan saran dan masukan untuk kesempurnaan skripsi ini.
5. Bapak M. Hendra S. Ginting, ST, MT selaku dosen penguji yang telah memberikan saran dan masukan untuk kesempurnaan skripsi ini.
6. Bapak Dr. Eng. Ir. Irvan, MT, selaku Ketua Jurusan Teknik Kimia USU. 7. Ibu Dr. Ir. Fatimah, MT, selaku Sekretaris Jurusan Teknik Kimia USU. 8. Ibu Prof. Dr. Ir. Rosdanelli Hasibuan MT sebagai Dosen Pembimbing
Akademik.
9. Seluruh Dosen/Staf Pengajar dan Pegawai Administrasi Departemen Teknik Kimia yang telah memberikan banyak sekali ilmu yang sangat berharga dan bantuan kepada penulis selama menjalankan perkuliahan. 10.Sari Liza Azura Nst sebagai partner atas kerjasamanya yang luar biasa
selama melakukan penelitian dan penulisan skripsi ini.
11.Sahabat terbaikku Sari Andhika Putri, Najla Annisa, Rahmadia Pratiwi dan Fitri Istislaam Zafmi yang telah banyak memberikan doa dan semangat kepada penulis dalam menyelesaikan skripsi.
yang telah banyak memberikan banyak dukungan, semangat, doa, pembelajaran hidup, dan kenangan tak terlupakan kepada penulis.
13.Seluruh mahasiswa Teknik Kimia Universitas Sumatera Utara baik junior maupun senior yang telah banyak memberi sokongan kepada penulis untuk menyelesaikan skripsi ini.
.RIWAYAT HIDUP PENULIS
Nama : Reni Sutri
NIM : 100405016
Tempat, tanggal lahir :Tanjung Pati, 30 Januari 1993 Nama orang tua : Suherman dan
Fitri Agusmainur Alamat orang tua :
Kompleks SMAN 1 Harau, Tanjung Pati, Kec. Harau, Kab. Limapuluh Kota, Sumatera Barat
Asal Sekolah:
SDN 01 Koto Tuo tahun 1998-2004
SMP Islam Raudhatul Jannah tahun 2004 – 2007
SMAN 1 Payakumbuh 2007 – 2010 Beasiswa yang diperoleh:
Beasiswa PPA tahun 2012 Universitas Sumatera Utara Beasiswa PPA tahun 2013 Universitas Sumatera Utara Beasiswa PT. Gas Negara tahun 2013/2014
Pengalaman Organisasi:
1. Pemerintahan Mahasiswa (PEMA) FT USU periode 2010/2011 sebagai Staff Internal
2. Klub Kegiatan Kreatifitas Mahasiswa Islam (K3MI) Al-Hadiid FT USU periode 2011/2012 sebagai Bendahara Umum
3. Unit Kegiatan Mahasiswa Islam (UKMI) Ad-Dakwah Universitas Sumatera Utara periode 2012 sebagai Staff Lembaga Mentoring Agama Islam (L-MAI)
4. Komisi Pemilihan Umum (KPU) FT USU periode 2012 sebagai Sekretaris Umum
5. Klub Kegiatan Kreatifitas Mahasiswa Islam (K3MI) Al-Hadiid FT USU periode 2012/2013 sebagai Sekretaris Departemen Kaderisasi 6. Covalen Study Grup (CSG) periode 2012/2013 sebagai Ketua Bidang
Keputrian
7. Ikatan Mahasiswa Payakumbuh Limapuluh Kota (IMAPALIKO) periode 2012/2013 sebagai Sekretaris Bidang Keanggotaan
8. Himpunan Mahasiswa Teknik Kimia (HIMATEK) FT USU periode 2013/2014 sebagai Staff Hubungan Masyarakat
9. Ikatan Mahasiswa Payakumbuh Limapuluh Kota (IMAPALIKO) tahun 2010-sekarang sebagai anggota
ABSTRAK
Etil asetat merupakan bahan baku dalam pembuatan essence yang umumnya diperoleh dari hasil reaksi esterifikasi antara etanol dan asam asetat. Etanol dapat dibuat dari kulit pisang yang merupakan limbah melalui proses hidrolisis dan fermentasi. Tujuan dari penelitian ini adalah untuk memanfaatkan limbah kulit kepok pisang untuk menghasilkan etil asetat. Variasi yang dilakukan dalam percobaan ini adalah perbandingan bahan baku dan air 1:4; 1:7; 1:10 dan suhu hidrolisis 50oC, 60oC, 70oC. Limbah kulit pisang ini dikerok, dikeringkan dan dihaluskan untuk membuat tepung kulit pisang. Tepung kulit pisang kepok mempunyai kadar karbohidrat sebesar 84,71% (b/b). Tepung kulit pisang dihidrolisis dengan air dan katalis asam klorida selama 180 menit. Hasil hidrolisis
difermentasi pada suhu ruangan dengan menggunakan ragi instan ‘Fermipan’
selama 24 jam dan selanjutnya didistilasi. Hasil distilasi diesterifikasi dengan asam asetat dan katalis asam klorida selama 15 menit pada suhu 60oC. Pada kondisi terbaik diperoleh yield maksimum dari etil asetat adalah 82,7% yang didapat dengan menggunakan perbandingan bahan baku dan air = 1:10 dan suhu hidrolisis 60oC. Hasil yang diperoleh pada penelitian ini menunjukkan bahwa kulit pisang kepok dapat digunakan sebagai bahan baku berbiaya murah untuk memproduksi etil asetat.
ABSTRACT
Ethyl acetate is a raw material in essence making which is obtained from esterification reaction between ethanol and acetic acid. Ethanol can be produced from banana peel waste through hydrolysis and fermentation process. The
objective of the study was to use ‘kepok’ banana peel waste to produce ethyl
acetate. The variation in this experiment were the ratio of banana powder and water 1:4 ; 1: 7 ; 1:10 and hydrolysis temperature 50, 60 and 70oC. The banana peel waste was scraped, dried and mashed to produce banana peel powder. The
contain of ‘Kepok’ banana peel powder is 84,71% carbohydrate. The banana peel
powder was hydrolyzed by water and chloride acid as catalyst for 180 minutes. The hydrolysis product was fermented in room temperature using instant yeast
‘Fermipan’ for 24 hours and then was distilled. The distillation product was
esterified with acetic acid and chloride acid as catalyst within 15 minutes with temperature 60oC. In the best condition, the maximum yield was obtained 74.21% from the ratio of banana powder and water 1:10 and hydrolysis temperature 60oC. The result from this experiments show that ‘kepok’ banana waste can be used as low cost raw material to produce ethyl acetate.
Keywords: ethyl acetate, ‘kepok’ banana peel, hydrolisys, fermentation,
DAFTAR ISI
Halaman
PERNYATAAN KEASLIAN SKRIPSI i
PENGESAHAN ii
PRAKATA iii
DEDIKASI iv
RIWAYAT HIDUP PENULIS vi
ABSTRAK vii
ABSTRACT viii
DAFTAR ISI ix
DAFTAR GAMBAR xi
DAFTAR TABEL xiv
DAFTAR LAMPIRAN xv
DAFTAR SINGKATAN xvii
DAFTAR SIMBOL xviii
BAB I PENDAHULUAN 1
1.1 LATAR BELAKANG 1
1.2 PERUMUSAN MASALAH 5
1.3 TUJUAN PENELITIAN 5
1.4 MANFAAT PENELITIAN 5
1.5 RUANG LINGKUP PENELITIAN 5
BAB II TINJAUAN PUSTAKA 7
2.1 KULIT PISANG KEPOK (Musa paradisiacal L.) 7
2.2 ETIL ASETAT (CH3COOC2H5) 8
2.2.1 Karakteristik Asam Asetat 8
2.2.2 Kegunaan Etil Asetat 9
2.2.3 Pembuatan Etil Asetat 9
2.3 ETANOL 12
2.3.1 Karakteristik Etanol 13
2.4 ANALISIS EKONOMI 18
BAB III METODOLOGI PENELITIAN 19
3.1 LOKASI DAN WAKTU PENELITIAN 19
3.2 BAHAN 19
3.3 PERALATAN 19
3.4 PROSEDUR 21
3.4.1 Prosedur Penelitian 21
3.4.2 Prosedur Analisis 22
3.5 FLOWCHART 26
3.5.1 Flowchart Penelitian 26
3.5.2 Flowchart Analisis 30
BAB IV HASIL PEMBAHASAN 32
4.1 ANALISIS KARBOHIDRAT TEPUNG KULIT
PISANG KEPOK 33
4.2 PENGARUH VARIABEL PERCOBAAN 34
4.2.1 Pengaruh Perbandingan Bahan Baku Terhadap
Kadar Etil Asetat Terbentuk 34
4.2.2 Pengaruh Perbandingan Bahan Baku Terhadap
Yield Etil Asetat Terbentuk 35 4.2.3 Pengaruh Suhu Hidrolisis Terhadap Yield Etil
Asetat Terbentuk 36
4.3 ETIL ASETAT TERBANYAK 38
BAB V KESIMPULAN DAN SARAN 39
DAFTAR GAMBAR
Halaman
Gambar 2.1 Pisang Kepok 8
Gambar 2.2 Reaksi Esterfikasi 10
Gambar 2.3 Diagram Alir Proses Dehidrogenasi Hidrogen 12
Gambar 2.4 Reaksi Hidrolisis Pati 14
Gambar 2.5 Reaksi Proses Fermentasi 15
Gambar 2.6 Saccharomyces Cerevisiae 17
Gambar 2.7 Reaksi Penguraian Glukosa 17
Gambar 3.1 Flowchart Persiapan Bahan Baku Tepung Kulit Pisang 26 Gambar 3.2 Flowchart Hidrolisis Tepung Kulit Pisang 27
Gambar 3.3 Flowchart Proses Fermentasi 28
Gambar 3.4 Flowchart Proses Esterifikasi 29
Gambar 3.5 Flowchart Analisis Kandungan Karbohidrat dalam
Tepung Kulit Pisang Kepok 30
Gambar 3.6 Flowchart Analisis Densitas 31
Gambar 3.7 Flowchart Analisis Viskositas 32
Gambar 4.1 Hubungan Perbandingan Bahan Baku Terhadap Kadar
Etil Asetat yang Terbentuk 34
Gambar 4.2 Hubungan Perbandingan Bahan Baku Terhadap Yield
Etil Asetat yang Terbentuk 35
Gambar 4.3 Reaksi Hidrolisis Pati dengan Air 36
Gambar 4.4 Hubungan Suhu Terhadap Yield Etil Asetat yang
Terbentuk 36
Gambar L2.1 Hasil Analisis Pati Kulit Pisang Kepok 46 Gambar L2.2 Hasil Analisis Glukosa Pada Hidrolisat 46 Gambar L2.3 Hasil Analisa GC Etanol Pada Distilat Dengan Kondisi
Suhu Hidrolisis 60oC dan Perbandingan Bahan Baku 1:10
47
Hidrolisis 50oC dan Perbandingan Bahan Baku 1:4 Gambar L2.5 Hasil Analisis GC Etil Asetat Pada Kondisi Suhu
Hidrolisis 60oC dan Perbandingan Bahan Baku 1:4 48 Gambar L2.6 Hasil Analisis GC Etil Asetat Pada Kondisi Suhu
Hidrolisis 70oC dan Perbandingan Bahan Baku 1:4 48 Gambar L2.7 Hasil Analisis GC Etil Asetat Pada Kondisi Suhu
Hidrolisis 50oC dan Perbandingan Bahan Baku 1:7 49 Gambar L2.8 Hasil Analisis GC Etil Asetat Pada Kondisi Suhu
Hidrolisis 60oC dan Perbandingan Bahan Baku 1:7 49 Gambar L2.9 Hasil Analisis GC Etil Asetat Pada Kondisi Suhu
Hidrolisis 70oC dan Perbandingan Bahan Baku 1:7 50 Gambar L2.10 Hasil Analisis GC Etil Asetat Pada Kondisi Suhu
Hidrolisis 50oC dan Perbandingan Bahan Baku 1:10 50 Gambar L2.11 Hasil Analisis GC Etil Asetat Pada Kondisi Suhu
Hidrolisis 60oC dan Perbandingan Bahan Baku 1:10 51 Gambar L2.12 Hasil Analisis GC Etil Asetat Pada Kondisi Suhu
Hidrolisis 70oC dan Perbandingan Bahan Baku 1:10 51 Gambar L2.13 Hasil Analisis GC Etil Asetat Standard 52
Gambar L4.1 Foto Kulit Pisang Kepok 57
Gambar L4.2 Foto Kulit Pisang Setelah Dikerok 57
Gambar L4.3 Foto Kulit Pisang Setelah Dikeringkan 57 Gambar L4.4 Foto Kulit Pisang Setelah Diblender 58
Gambar L4.5 Foto Kulit Pisang Setelah Diayak 58
Gambar L4.6 Foto Rangkaian Alat Hidrolisis 58
Gambar L4.7 Foto Proses Penyaringan 59
Gambar L4.8 Foto Hidrolisat Hasil Saringan 59
Gambar L4.9 Foto Pengaturan pH Hidrolisat dengan NaOH 59 Gambar L4.10 Foto Penambahan Ragi Pada Hidrolisat 60
Gambar L4.11 Foto Proses Pengadukan 60
Gambar L4.12 Foto Setelah Proses Pengadukan 60
Gambar L4.13 Foto Rangkaian Alat Esterifikasi 61
Gambar L4.15 Foto Analisis Densitas 62
Gambar L4.16 Foto Analisis Viskositas 62
DAFTAR TABEL
Halaman Tabel 1.1 Penelitian Terdahulu Mengenai Hidrolisis 2
Tabel 2.1 Komposisi Kulit Pisan Kepok 8
Tabel 2.2 Perbandingan Penggunaan Katalis Asam dan Enzim
Dalam Hidolisis 14
Tabel 2.3 Perhitungan Biaya Pembelian Bahan Baku 18 Tabel 2.4 Perhitungan Biaya Kebutuhan Listrik 19
Tabel 3.1 Rancangan Percobaan 20
Tabel 3.2 Program Pengatur GC 23
Tabel L1.1 Data Kemurnian Etil Asetat 44
Tabel L1.2 Data Volume Etil Asetat 44
Tabel L1.3 Data Yield Etil Asetat 45
DAFTAR LAMPIRAN
Halaman LAMPIRAN 1 DATA PERCOBAAN
L1.1 DATA KEMURNIAN ETIL ASETAT 44
L1.2 DATA VOLUME ETIL ASETAT 44
L1.3 DATA YIELD ETIL ASETAT 45
LAMPIRAN 2 HASIL ANALISISI 46
L2.1 HASIL ANALISIS PATI TEPUNG
KULIT PISANG KEPOK 46
L2.2 HASIL ANALISIS GLUKOSA PADA
HIDROLISAT 46
L2.3 HASIL ANALISIS ETANOL PADA
DISTILAT 47
L2.4 HASIL ANALISIS ETIL ASETAT 47
L2.5 HASIL ANALISIS ETIL ASETAT
STANDARD 52
LAMPIRAN 3 CONTOH PERHITUNGAN 53
L3.1 PERHITUNGAN KEBUTUHAN AIR 53
L3.1.1 Untuk Hidrolisis 53
L3.1.2 Untuk Pembuatan Larutan NaOH 53
L3.2 PERHITUNGAN ASAM KLORIDA 53
L3.2.1 Sebagai Katalis Proses Hidrolisis 53 L3.2.2 Sebagai Katalis Proses Esterifikasi 53 L3.3 PERHITUNGAN NATRIUM
HIDROKSIDA 54
L3.4 PERHITUNGAN ASAM ASETAT 54
L3.5 PERHITUNGAN VOLUME ETIL
ASETAT 55
L3.6 PERHITUNGAN YIELD ETIL ASETAT 55
LAMPIRAN 4 DOKUMENTASI PENELITIAN 57 L4.1 FOTO PERLAKUAN AWAL BAHAN
BAKU 57
L4.2 FOTO PROSES HIDROLISIS 58
L4.3 FOTO PROSES FERMENTASI 60
L4.4 FOTO PROSES ESTERIFIKASI 61
DAFTAR SINGKATAN
BM Berat Molekul
BPOM Balai Pengawasan Obat dan Makanan
cP Centipoise
dkk Dan Kawan-Kawan
GC Gas Chromatography
HPLC High Performance Liquid Chromatography
pH Power Of Hydrogen
PPKS Pusat Penelitian Kelapa Sawit
ppm Part Per Million
rpm rotary per minute
DAFTAR SIMBOL
Simbol Keterangan Dimensi
T Suhu oC
M Molaritas Mol/L
V Volume ml
m Berat sampel gram
ρ Massa jenis gr/cm3
µ Viskositas cP
sg Spesific gravity
t Waktu alir s
k Konstanta alir cP/s
k Konstanta laju reaksi L/jam
ABSTRAK
Etil asetat merupakan bahan baku dalam pembuatan essence yang umumnya diperoleh dari hasil reaksi esterifikasi antara etanol dan asam asetat. Etanol dapat dibuat dari kulit pisang yang merupakan limbah melalui proses hidrolisis dan fermentasi. Tujuan dari penelitian ini adalah untuk memanfaatkan limbah kulit kepok pisang untuk menghasilkan etil asetat. Variasi yang dilakukan dalam percobaan ini adalah perbandingan bahan baku dan air 1:4; 1:7; 1:10 dan suhu hidrolisis 50oC, 60oC, 70oC. Limbah kulit pisang ini dikerok, dikeringkan dan dihaluskan untuk membuat tepung kulit pisang. Tepung kulit pisang kepok mempunyai kadar karbohidrat sebesar 84,71% (b/b). Tepung kulit pisang dihidrolisis dengan air dan katalis asam klorida selama 180 menit. Hasil hidrolisis
difermentasi pada suhu ruangan dengan menggunakan ragi instan ‘Fermipan’
selama 24 jam dan selanjutnya didistilasi. Hasil distilasi diesterifikasi dengan asam asetat dan katalis asam klorida selama 15 menit pada suhu 60oC. Pada kondisi terbaik diperoleh yield maksimum dari etil asetat adalah 82,7% yang didapat dengan menggunakan perbandingan bahan baku dan air = 1:10 dan suhu hidrolisis 60oC. Hasil yang diperoleh pada penelitian ini menunjukkan bahwa kulit pisang kepok dapat digunakan sebagai bahan baku berbiaya murah untuk memproduksi etil asetat.
ABSTRACT
Ethyl acetate is a raw material in essence making which is obtained from esterification reaction between ethanol and acetic acid. Ethanol can be produced from banana peel waste through hydrolysis and fermentation process. The
objective of the study was to use ‘kepok’ banana peel waste to produce ethyl
acetate. The variation in this experiment were the ratio of banana powder and water 1:4 ; 1: 7 ; 1:10 and hydrolysis temperature 50, 60 and 70oC. The banana peel waste was scraped, dried and mashed to produce banana peel powder. The
contain of ‘Kepok’ banana peel powder is 84,71% carbohydrate. The banana peel
powder was hydrolyzed by water and chloride acid as catalyst for 180 minutes. The hydrolysis product was fermented in room temperature using instant yeast
‘Fermipan’ for 24 hours and then was distilled. The distillation product was
esterified with acetic acid and chloride acid as catalyst within 15 minutes with temperature 60oC. In the best condition, the maximum yield was obtained 74.21% from the ratio of banana powder and water 1:10 and hydrolysis temperature 60oC. The result from this experiments show that ‘kepok’ banana waste can be used as low cost raw material to produce ethyl acetate.
Keywords: ethyl acetate, ‘kepok’ banana peel, hydrolisys, fermentation,
BAB I
PENDAHULUAN
1.1LATAR BELAKANG
Pisang merupakan buah yang umum ditemui di Indonesia. Badan Pusat statistik mencatat pada tahun 2012 produksi pisang di Indonesia adalah sebanyak 6.189.052 ton. Jumlah produksi pisang menduduki peringkat pertama produksi buah-buahan di Indonesia mengalahkan jumlah produksi mangga yang hanya sebesar 2.376.339 ton [1]. Tingginya jumlah produksi pisang menyebabkan banyaknya limbah kulit pisang. Berat kulit pisang adalah sekitar 30-40% dari total keseluruhan buah pisang [2]. Jika limbah kulit pisang dibuang begitu saja tanpa dimanfaatkan akan sangat disayangkan, karena limbah kulit pisang mengandung komponen bernilai seperti karbohidrat, vitamin C dan nutrien lainnya berpotensi untuk diolah menjadi bahan baku yang berguna dan bernilai lebih. Berdasarkan sifat fisik dan kimianya, limbah kulit pisang sangat berpotensi untuk digunakan sebagai sumber karbon dalam pembuatan alkohol [3].
Kulit pisang dapat diolah menjadi etil asetat dengan tiga proses utama yaitu hidrolis, fermentasi dan esterifikasi. Hidrolisis adalah suatu proses reaksi antara reaktan dengan air agar suatu senyawa pecah atau terurai. Reaksi ini merupakan
reaksi orde satu, karena air yang digunakan berlebih, sehingga perubahan air
dapat diabaikan [4]. Derajat keasaman, suhu hidrolisis dan konsentrasi katalis
yang dipakai sangat mempengaruhi proses hidrolis [5].
Saat ini dikenal dua macam jenis hidrolis yaitu hidrolisis asam dan enzimatik.
Berikut adalah tabel penelitian terdahulu mengenai hidrolisis:
Tabel 1.1 Penelitian Terdahulu Mengenai Hidrolis
No Peneliti Tahun Judul dan Variabel
1. Wahyudi, dkk. [4]
2011 "Pengaruh Suhu Terhadap Kadar Glukosa Terbentuk dan Konstanta Kecepatan Reaksi pada Hidrolisa Kulit Pisang"
Variabel berubah:
- Suhu hidrolisis: 29 oC, 60 oC, 101 oC Variabel tetap:
- Waktu hidrolisis: 180 menit - Bahan baku : air = 1: 10 - Katalis: asam klorida
Optimum suhu hidrolisis 60 oC dengan konsentrasi glukosa 0,292 mol/L
2. Yusak [7] 2004 "Pengaruh Variasi Volume HCl 0,5 N Dan Waktu Hidrolisa Terhadap Mutu Sirup Pada Pembuatan Sirup Glukosa Dari Pati Ubi Jalar (Ipomoea Babatas L, Sin Babatas Edulis Choisy)"
Variabel berubah :
- Volume HCl : 5, 10, 15, 20, 25 ml - Waktu hidrolisi : 2, 4, 6, 8 jam Variabel tetap:
- HCl 0,5 N
Optimum pada penambahan HCl sebanyak 25 ml, waktu hidrolisi 2 jam dan kadar gula yang dihasilkan 44,5%
3. Gusmarwani, dkk. [8]
2010 "Pengaruh Perbandingan Berat Padatan Dan Waktu Reaksi Terhadap Gula Pereduksi Terbentuk Pada Hidrolisis Bonggol Pisang"
Variabel berubah:
- Waktu hidrolisis = 10, 20, 30, 40, 50, 60, 70, 80, 90 menit Variabel tetap :
- Volume asam sulfat 10 ml - Suhu hidrolisis 120 oC
Optimum: waktu hidrolisisi 80 menit, padatan : air = 1: 5, glukosa yg dihasilkan sebanyak 13,08 g/ 100 ml
4. Putri dan Sukandar [9]
2008 "Konversi Pati Ganyong (Canna edulis Ker.) Menjadi Bioetanol melalui Hidrolisis Asam dan Fermentasi"
Variabel berubah :
- Jenis asam : HCl, H2SO4, HNO3
- Konsetrasi asam : 3, 4, 5, 6, 7 % Variabel tetap :
- Suhu hidrolisis 120 oC - Waktu hidrolisis 1 jam
Optimum: asam nitrat dengan konsentrasi 7% jumlah gula 48090 ppm 5. Apriliani dan
Agustinus [3]
2013 "Pembuatan Etanol Dari Kulit Pisang Secara Fermentasi" Variabel berubah:
- Suhu hidrolisis: 50 oC, 60 oC, 70 oC, 80 oC - Jumlah nutrisi : 10 gr/L, 20 g/L, 30 gr/L Variabel tetap :
- Waktu hidrolisis : 1 jam - pH hidrolisis: 1
- Waktu fermentasi: 12 hari - Katalis: asam klorida
Proses fermentasi merupakan proses biokimia dimana terjadi perubahan-perubahan atau reaksi-reksi kimia dengan pertolongan jasad renik penyebab fermentasi tersebut bersentuhan dengan zat makanan yang sesuai dengan pertumbuhannya. Akibat terjadinya fermentasi sebagian atau seluruhnya akan berubah menjadi alkohol setelah beberapa waktu lamanya [10].
Pembuatan alkohol dari kulit pisang dapat dilakukan secara fermentasi dengan bantuan mikroorganisme, sebagai penghasil enzim zimosa yang mengkatalis reaksi biokimia pada perubahan substrat organik. Mikroorganisme yang dapat digunakan untuk fermentasi terdiri dari yeast (ragi), khamir, jamur, dan bakteri [11].
Saccharomyces cereviseae adalah sejenis khamir yang dapat diperoleh dalam
bentuk kultur murni maupun ragi. Saccharomyces cereviseae mampu hidup pada suhu tinggi dan tetap stabil selama proses fermentasi pada pH rendah [12].
Esterifikasi, atau reaksi pembentukan ester, dapat dilakukan dengan mereaksikan asam dan alkohol dengan adanya asam mineral sebagai katalis (metode Esterifikasi Fischer). Prosesnya adalah sebuah keseimbangan. Pencapaian keseimbangan tersebut dipercepat oleh ion hidrogen [13].
Selain proses esterifikasi terdapat beberapa cara lain untuk memproduksi etil asetat. Armstrong et al memproduksi etil asetat dari larutan etanol encer dengan bantuan Candida utilis [14]. Horan et al memproduksi etil asetat dengan cara mereaksikan asam asetat dan etanol dengan katalis asam kuat selanjutnya uap yang dihasilkan dilewatkan melalui zona distilasi, kemudian didinginkan dan dikondensasikan dan kemudian didistilasi untuk kedua kalinya untuk menghasilkan asam asetat dengan sedikit pengotor [15]. Urit et al memproduksi etil asetat dengan bantuan Kluyveromyces marxianus yang terdapat pada whey, dengan mengkonversi laktosa pada whey menjadi asam asetat [16]. Gadewar memproduksi etil asetat dari etanol menggunakan kolom distilasi reaktif dengan penghilangan hidrogen [17].
klorida dan fermentasi oleh Saccharomyces cereviseae dilanjutkan dengan proses esterifikasi dengan asam asetat.
1.2PERUMUSAN MASALAH
Proses hidrolisis merupakan salah satu tahapan penting bagi keberhasilan produksi etil asetat dari kulit pisang. Perbaikan pada proses hidrolis mempengaruhi hasil akhir yang berupa etil asetat. Dalam penelitian ini dilakukan bebererapa variasi dalam proses hidrolisis yaitu variasi pada temperatur hidrolisis dan perbandingan jumlah bahan baku dan air.
1.3TUJUAN PENELITIAN
Adapun tujuan dari penelitian ini yaitu sebagai berikut :
1. Menghasilkan etil asetat dari dari bahan baku kulit pisang kepok (Musa paradisiaca L.) melalui proses hidrolisis, fermentasi dan dilanjutkan dengan reaksi esterifikasi.
2. Mengetahui pengaruh rasio bahan baku : air dan suhu hidrolisis terhadap etil asetat yang dihasilkan dari kulit pisang kepok (Musa paradisiaca).
1.4MANFAAT PENELITIAN
Penelitian ini diharapkan dapat menghasilkan etil asetat yang memiliki banyak kegunaan dalam bidang industri. Selain itu juga dapat mengurangi limbah kulit pisang dan meningkatkan nilai ekonomis dari kulit pisang kepok (Musa paradisiaca) yang merupakan limbah padat.
1.5RUANG LINGKUP PENELITIAN
Adapun ruang lingkup dari penelitian ini adalah :
1. Penelitian ini dilakukan di Laboratorium Operasi Teknik Kimia dan Labratorium Proses Industri Kimia, Departemen Teknik Kimia, Fakultas Teknik Universitas Sumatera Utara, serta Laboratorium Penelitian, Fakultas Farmasi, Universitas Sumatera Utara, Medan.
3. Bahan baku untuk tahap hidrolisis adalah kulit pisang kepok (Musa paradisiaca L.) yang diperoleh secara acak dari penjual goreng pisang di
Medan, air dan asam klorida (HCl). Reaksi hidrolisis kulit pisang kepok (Musa paradisiaca L.) dilangsungkan selama 180 menit. Proses dilakukan dalam labu leher satu yang dilengkapi dengan magnetic stirrer dengan kecepatan 350 rpm dengan memvariasikan tiga variabel seperti berikut : - Rasio bahan baku: air = 1:4 [18]; 1:7; 1:10 [4].
- Suhu hidrolisis: 50oC, 60oC [4] dan 70oC [3]. Sedangkan variabel tetap nya adalah :
- Waktu hidrolisis 180 menit. - pH hidrolisis = 1.
4. Pada tahap fermentasi bahan yang digunakan hidrolisat hasil hidrolisis kulit pisang dan Saccharomyses cerevisiae. Fermentasi pati hasil kulit pisang kepok (Musa paradisiaca) dilangsungkan pada suhu ruangan selama 24 jam dengan kondisi anerobik. Jumlah ragi yang ditambahkan adalah sebanyak 14,29% berat bahan baku [19].
5. Pada tahap esterifikasi bahan yang digunakan adalah etanol hasil fermentasi, asam asetat (CH3COOH) dan asam klorida (HCl) sebagai
katalis. Reaksi esterifikasi etanol dari proses fermentasi dilangsungkan pada suhu 80oC selama 15 menit dengan perbandingan mol etanol : mol asam asetat = 1:1,02 dan katalis 32% [20].
Analisis yang dilakukan adalah :
1. Analisis kadar karbohidrat tepung kulit pisang kepok.
2. Analisis kadar etil asetat dengan menggunakan kromatografi gas. 3. Analisis untuk etil asetat terbaik:
a. Analisis kadar glukosa hasil hidroliss b. Analisis kadar bioetanol hasil fermentassi c. Analisis densitas
BAB II
TINJAUAN PUSTAKA
2.1 KULIT PISANG KEPOK (Musa paradisiaca L.)
Tanaman pisang merupakan buah tropis yang sangat popular di dunia. Hal ini disebabkan rasanya yang lezat, gizi yang tinggi dan harga yang relatif murah. Buah ini biasa dikonsumsi sebagai buah segar dan aneka bahan makanan olahan seperti gorengan, keripik, tepung dan sale pisang serta berbagai olahan lainnya. Tiap industri pengolahan pisang baik skala besar maupun kecil dalam mengolah pisang menjadi aneka ragam makanan olahan akan menghasilkan limbah yang jumlahnya tidak sedikit seperti kulit pisang. Sebagian limbah tersebut dibuang begitu saja sehingga dapat menyebabkan pencemaran lingkungan. Salah satu cara untuk mengatasi pencemaran lingkungan yaitu dengan menggunakan limbah tersebut sebagai bahan baku biofermentasi [21].
Menurut Suyanti dan Supriyadi terdapat tiga jenis umum tanaman pisang yang dibudidayakan di Indonesia [22]:
1. Pisang serat (Noe. Musa texstiles)
Pisang serat adalah tanaman pisang yang tidak diambil buahnya tetapi diambil seratnya, misalnya untuk bahan pakaian.
2. Pisang hias (Heliconia indica Lamk)
Pisang hias juga tidak diambil buahnya. Tumbuhan ini memang bagus sekali di tanam di muka rumah sebagai hiasan.
3. Pisang buah (Musa paradisiaca L.)
Pisang buah dibedakan menjadi empat golongan:
a. Golongan pertama dapat dimakan langsung setelah masak, misalnya pisang susu dan pisang hijau.
b. Golongan kedua dapat dimakan setelah diolah terlebih dahulu, misalnya pisang tanduk.
c. Golongan ketiga dapat dimakan langsung setelah masak maupun diolah terlebih dahulu, misalnya pisang kepok dan pisang raja.
Berikut adalah gambar pisang kepok yang digunakan dalam percobaan:
Gambar 2.1 Pisang Kepok [23]
Komposisi kulit pisang kepok dapat dilihat pada tabel 2.1 Tabel 2.1 Komposisi kulit pisang kepok [24]
No Hasil test kimia laboratorium
Kadar
1 Air 73,60%
2 Protein 2,15%
3 Lemak 1,34%
4 Gula reduksi 7,62%
5 Pati 11,46%
6 Serat kasar 1,52%
7 Abu 1,03%
8 Vitamin
Vitamin C mg/100 gr
36 9 Mineral
Ca, mg/100 gr Fe, mg/100 gr P, mg/100 gr
31 26 63 2.2 ETIL ASETAT (CH3COOC2H5)
Etil asetat adalah senyawa ester dari asam organik. Di dalam skala laboratorium maupun industri, biasanya dibuat dengan cara memanaskan etanol dengan asam asetat dengan penambahan asam sulfat sebagai katalis [20].
2.2.1 Karakteristik Etil Asetat
a. Sifat fisika
Berupa cairan bening
Tidak berwarna
Bau bervariasi,
Berat molekul 88,11 gr/mol
Titik didih 171°F (77°C)
Titik beku -119°F (-84°C) ,
Tekanan uap pada 20°C = 73 mmHg
Kerapatan uap (udara=1) 3,04
Kerapatan relatif (air=1) 0,9003
Nilai ambang batas bau 50 bpj
b. Sifat Kimia
Mudah menguap
Kelarutan dalam air 8,7%
pH netral
Larut dalam alkohol, benzen, eter, aseton, kloroform.
2.2.2 Kegunaan Etil Asetat
Etil asetat di dalam industri biasa digunakan sebagai pelarut tinta, perekat, resin [26]. Selain itu juga digunakan sebagai citarasa buah buatan. Dalam sintesis organik etil asetat dapat digunakan untuk membuat etil asetoasetat [20]. Etil asetat juga dapat digunakan dalam proses coating plastik [25].
2.2.3 Pembuatan Etil Asetat
Esterifikasi
Etil asetat yang merupakan senyawa ester dapat dibuat melalui reaksi asam karboksilat dengan alkohol yang dikenal dengan nama esterifikasi, dan biasanya menggunakan katalis asam. Katalis asam yang biasa digunakan yaitu asam sulfat dan asam klorida [27].
Reaksi antara etil alkohol dan asam asetat menghasilkan etil asetat, juga air. Etil asetat juga dapat dibuat dengan reaksi anhidrida asetat dengan etil alkohol, selama reaksi selain etil asetat juga dihasilkan asam asetat, yang selanjutnya akan diesterifikasi dengan etil alkohol. Esterifikasi adalah reaksi kesetimbangan dan dipercepat oleh kehadiran katalis asam [28].
Proses esterifikasi dapat dilakukan dengan cara memasukkan 50 ml etanol dan 50 ml asam asetat glasial ke dalam labu leher tiga, kemudian ditambahkan 16 ml asam sulfat. Campuran dipanaskan selama 15 menit dengan pemasangan refluks dan air pendingin pada labu. Kemudian peralatan diganti dengan peralatan distilasi. Semua fraksi yang didapat dari distilasi hingga 80 oC dikumpulkan. Distilat direaksikan dengan sodium karbonat 2M di dalam corong pemisah untuk menghilangkan asam. Lapisan yang berminyak pada corong pemisah kemudian di reaksikan dengan kalsium klorida untuk menghilangkan etanol. Produk akhirnya dipisahkan dari kalsium klorida anhidrat dengan distilasi. Fraksi yang terkumpul antara suhu 74-79 oC dikumpulkan [20].
Reaksi estertfikasi dapat dilihat pada gambar berikut:
CH3COOH + CH3OH CH3COOC2H5 + H2O
Asam Asetat Etanol Etil Ester Air Gambar 2.2 Reaksi Esterifikasi [20]
Konversi Larutan Ethanol Encer oleh Candida utilis
Proses ini menggunakan bantuan Candida utilis untuk mengkonversi larutan etanol encer menjadi etanol pekat dan etil asetat. Kinetika akumulasi etanol dan etil asetat dalam perkembangan glukosa Candida utilis menunjukkan bahwa pembentukan ester dihasilkan dari pemanfaatan etanol dibawah kondisi aerasi yang tepat dan dihambat oleh penambahan Fe3+. Candida utilis
mengkonversi etanol menjadi etil asetat paling optimal pada pH 5-7. Proses berlangsung selama lima hari [14].
Konversi Laktosa Pada Whey oleh Kluyveromyces marxianus
Kluyveromyces marxianus mampu mengkonversi laktosa menjadi etil asetat
sebagai salah satu langkah untuk menggunakan membali whey. Pembentukan mikroba etil asetat dalam jumlah besar memerlukan proses aerobik dan kemudian etil asetat yang mudah menguap dilepaskan dari bioreaktor yang teraerasi. Pada proses ini berdasarkan percobaan yang sudah ada, laju stripping dibuat sebanding dengan laju alur gas. Percobaan menunjukkan pembentukan etil asetat hanya terjadi saat pertumbuhan yeast terhambat karena kekurangan makanan. Produksi etil asetat tertinggi yaitu 0,25 gr etil asetat per gr laktosa, hasil ini mendekati 50% teori maksimum [16].
Perbaikan Proses Esterifikasi
Etil asetat dapat dibuat dengan cara mereaksikan asam asetat dan etanol dengan katalis asam kuat selanjutnya uap yang dihasilkan dilewatkan melalui zona distilasi, kemudian didinginkan dan dikondensasikan dan kemudian didistilasi untuk kedua kalinya untuk menghasilkan asam asetat dengan sedikit pengotor. Proses ini menggunakan distilasi azeotrop yang menghasilkan 50 ppm pengotor [15].
Dehidrogenasi Etanol
Gambar 2.3 Diagram Alir Proses Dehidrogenasi Hidrogen [17]
2.3 ETANOL
Etanol adalah senyawa organik yang terdiri dari karbon, hidrogen dan oksigen, sehingga dapat dilihat sebagai turunan senyawa hidrokarbon yang mempunyai gugus hidroksil dengan rumus C2H5OH. Etanol merupakan zat cair,
tidak berwarna, berbau spesifik, mudah terbakar dan menguap, dapat bercampur dalam air dengan segala perbandingan.
Menurut Endah, dkk. dalam industri dikenal 2 macam pembuatan etanol, yaitu [10]:
1. Cara non fermentasi (synthetic)
Suatu proses pembuatan alkohol yang sama sekali tidak menggunakan enzim atau jasad renik.
2. Cara fermentasi
2.3.1 Karakteristik Etanol
Sakhashiri menjelaskan sifat fisika kimia etanol adalah sebagai berikut [29]: a. Sifat fisika
Berupa cairan tidak berwarna
Memiliki bau yang bervariasi
Berat molekul 46,07 gr/mol
Titik didih 78,4 °C
Titik beku -112 °C
Densitas 0,7893 gr/ml
Indeks bias 1,36143 cP
Viskositas pada 20 °C 1,17 cP
Panas Penguapan 200,6 kal/gr
b. Sifat Kimia
Merupakan pelarut yang baik untuk senyawa organik
Mudah menguap dan mudah terbakar
Bila direaksikan dengan asam halida akan membentuk alkil halida dan air
CH3CH2OH + HC=C CH3CH2OCH=CH
Bila direaksikan dengan asam karboksilat akan membentuk ester dan air
CH3CH2OH + CH3COOH CH3COOCH2CH3 + H2O
Dehidrogenasi etanol menghasilkan asetaldehid
Mudah terbakar diudara sehingga menghasilkan lidah api (flame) yang berwarna biru muda dan transparan, dan membentuk H2O dan CO2.
2.3.2 Hidrolisis
bahwa garam yang terbentuk setelah penetralan hasil merupakan garam yang tidak berbahaya yaitu garam dapur [10].
Reaksi hidrolisis pati berlangsung menurut persamaan reaksi sebagai berikut: (C6H10O5)n + nH2O n(C6H12O6)
pati air glukosa Gambar 2.4 Reaksi Hidrolisis Pati [11]
Hidrolisis enzimatik dikatalisasi oleh enzim selulosa. Jika reaksi perubahan selulosa menjadi glukosa dilakukan tanpa bantuan katalis asam maupun enzim, maka reaksi akan berlangsung sangat lama, karena selulosa dilindungi oleh matriks lignin dan hemiselulosa dalam makrofibril. Karena itu, perlakuan awal bahan sangat penting untuk meningkatkan laju hidrolisis selulosa untuk menghasilkan gula yang dapat difermentasi [2].
Menurur Taherzadeh dan Karimi berikut adalah perbandingan hidrolisis menggunakan katalis asam dan enzim [30]:
Tabel 2. 2 Perbandingan penggunaan katalis asam dan enzim dalam hidrolisis Variabel Perbandingan Larutan Asam Enzim
Kondisi hidrolisis mudah Tidak Ya
Yield hidrolisis tinggi Tidak Ya
Produk penghalang selama hidrolisis Tidak Ya Pembentukan produk samping penghalang Ya Tidak
Harga kalalis murah Ya Tidak
Waktu hidrolisis sebentar Ya Tidak
Menurut Sari faktor-faktor yang mempengaruhi proses hidrolisis adalah sebagai berikut [5]:
1. Derajat keasaman
Derajat keasaman mempengaruhi proses hidrolisis sehingga dapat dihasilkan hasil hidrolisis yang sesuai dengan yang diinginkan.
2. Suhu
Suhu mempengaruhi kecepatan reaksi hidrolisis. 3. Konsentrasi
2.3.3 Fermentasi
Fermentasi adalah suatu proses oksidasi karbohidrat anaerob jenuh atau sebagian. Dalam suatu proses fermentasi bahan pangan seperti natrium khlorida bermanfaat untuk membatasi pertumbuhan organisme pembusuk dan mencegah pertumbuhan sebagian besar organisme yang lain. Suatu fermentasi yang gagal biasanya adalah fermentasi yang mengaalami kontaminasi, sedangkan fermentasi yang normal adalah perubahan karbohidrat menjadi alkohol [24].
Proses fermentasi merupakan proses biokimia dimana terjadi perubahan- perubahan atau reaksi- reaksi kimia dengan pertolongan jasad renik penyebab fermentasi tersebut bersentuhan dengan zat makanan yang sesuai dengan pertumbuhannya. Akibat terjadinya fermentasi sebagian atau seluruhnya akan berubah menjadi alkohol setelah beberapa waktu lamanya.
Perubahan yang terjadi selama proses fermentasi adalah sebagai berikut:
C6H12O6 2C2H5OH + 2 CO2
Glukosa etanol
Gambar 2.5 Reaksi Pada Proses Fermentasi [11]
Pati yang terkandung dalam suatu bahan dapat diubah menjadi alkohol, melalui proses biologi dan kimia (biokimia). Fermentasi oleh yeast, misalnya dapat menghasilkan etil alkohol (etanol) dan CO2.
Faktor- faktor yang mempengaruhi proses fermentasi menurut Endah, dkk. [10]:
1. Keasaman (pH) 2. Mikroba
3. Suhu
Suhu fermentasi sangat menentukan macam mikroba yang dominan. Pada suhu 10- 30 oC terbentuk alkohol lebih banyak karena ragi bekerja optimal pada suhu itu
4. Waktu
Laju perbanyakan bakteri bervariasi menurut spesies dan kondisi
Saccharomyces Cerevisiae
perbanyakan bakteri. 5. Makanan (nutrisi)
Semua mikroorganisme memerlukan nutrient yang menyediakan: Energi biasanya diperoleh dari subtansi yang mengandung karbon. Nitrogen, Salah satu contoh sumber nitrogen yang dapat digunakan adalah urea. Mineral, salah satunya adalah asam phospat yang dapat diambil dari pupuk TSP.
Saccharomyses Cervisiae
Produsen etanol yang paling umum digunakan adalah Saccharomyces cerevisiae [31].
Khamir ini bersifat fakultatif anaerobik, tumbuh baik pada suhu 30 oC dan pH 4,0 – 4,5. Produksi etanol dari substrat gula oleh khamir Saccharomyces cereviseae merupakan proses fermentasi dengan kinetika sangat sederhana karena
hanya melibatkan satu fasa pertumbuhan dan produksi. Pada fase tersebut glukosa diubah secara simultan menjadi biomassa, etanol dan CO2. Terdapat dua
parameter yang mengendalikan pertumbuhan dan methabolisme khamir dalam keadaan anaeorobik, yaitu konsentrasi gula dan etanol. Secara kinetik glukosa berperan ganda, pada konsentrasi rendah (kurang dari 1 g/l) merupakan substrat pembatas, sedangkan pada konsentrasi tinggi (lebih dari 300 g/l) akan menjadi penghambat. Pada permulaan proses fermentasi, khamir memerlukan oksigen untuk pertumbuhannya. Setelah terjadi akumulsi CO2 dan reaksi berubah menjadi
Gambar 2. 6 Saccharomyces Cereviciae [33]
Berikut adalah reaksi penguraian glukosa menjadi etanol: C6H12O6 + 2 Pi + 2 ADP 2 C2H5OH + 2 CO2 + 2 ATP + 2 H2O
Glukosa + Asam Piruvat + Energi Etanol + Karbon Dioksida + Energi Gambar 2.7 Reaksi Penguraian Glukosa [34]
Dari persamaan diatas, dapat dihitung yield teoritis adalah 0,511 gr etanol yang dihasilkan dari setiap gram glukosa yang dikonsumsi [34].
Zymomonas mobilis
Zymomonas mobilis merupakan organisme penghasil etanol yang paling efektif walaupun saat ini belum digunakan secara komersial. Mikroorganisme ini dapat memproduksi etanol lebih cepat dibandingkan Saccharomyses cereviseae. Selain itu mikroorganisme ini toleran terhadap kadar etanol yang tinggi dan tidak membutuhkan peralatan aerasi untuk mengoptimalkan proses produksi etanol. Tetapi mikroorganisme ini memerlukan media yang sangat steril untuk dapat menghasilkan yield etanol tinggi [31].
2.4 POTENSI EKONOMI
Kulit pisang merupakan bahan sisa dari buah pisang. Berat kulit pisang adalah sekitar 30-40% dari total keseluruhan buah pisang [2]. Pada tahun 2012 Badan Pusat Statistik mencatat produksi pisang di Indonesia adalah sebanyak 6.189.052 ton [1]. Banyaknya produksi pisang Indonesia berbanding lurus dengan banyaknya limbah kulit pisang yang dihasilkan.
Di Indonesia selain di ekspor dan langsung dikonsumsi, buah pisang biasanya diolah menjadi gorengan, keripik atau produk olahan pisang lainnya. Produsen makanan olahan pisang ini merupakan salah satu sumber limbah kulit pisang terbesar. Limbah kulit pisang ini akan sangat disayangkan jika langsung dibuang ke lingkungan karena kandungan bahan organiknya yang tinggi.
Salah satu produk yang bernilai tambah tinggi yang dapat dibuat dari kulit pisang adalah etil asetat. Etil asetat banyak digunakan sebagai pelarut, perekat, resin dan citarasa buah buatan. Etil asetat sebagai citarasa buah buatan dapat digunakan kembali oleh produsen makanan olahan pisang sebagai penambah cita rasa produk mereka.
BAB III
METODOLOGI PENELITIAN
3.1 LOKASI DAN WAKTU PENELITIAN
Penelitian dilakukan di Laboratorium Operasi Teknik Kimia dan Laboratorium Proses Industri Kimia, Departemen Teknik Kimia, Fakultas Teknik, Universitas Sumatera Utara, Medan serta Laboratorium Penelitian, Fakultas Farmasi, Universitas Sumatera Utara, Medan. Penelitian ini dilakukan selama lebih kurang 6 bulan.
3.2 BAHAN
Pada penelitian ini bahan yang digunakan antara lain: 1. Limbah kulit pisang kepok matang
2. Aquadest 3. Asam klorida 4. Natrium hidroksida 5. Asam asetat
6. Ragi instan ‘Fermipan’
3.3 PERALATAN
Pada penelitian ini peralatan yang digunakan antara lain: 1. Oven
2. Alumunium foil 3. Blender
4. Ayakan 70 mesh 5. Labu leher tiga 6. Gabus
7. Termometer 8. Magnetic Stirrer 9. Hotplate
12.Erlenmeyer 13.Gelas Ukur 14.Timbangan 15.Stopwatch
16.Refluks kondensor 17.Spatula
18.Heating mantle 19.Piknometer
20.Viskosimeter Oswalt 21.Pipet Tetes
22.Statif dan klem 23.pH meter 24.Kertas saring 25.Shaker
3.4 PROSEDUR
3.4.1 Prosedur Penelitian Persiapan Bahan Baku
Prosedur persiapan bahan baku kulit pisang diadopsi dari Retno dan Nuri [11], Wahyudi, dkk. [4] danSeftian, dkk. [38].
1. Kulit pisang dikerok bagian dalamnya.
2.Dikeringkan di dalam oven pada suhu 105oC selama 5 jam.
3.Kulit pisang kering kemudian dihancurkan dengan blender selama 5 menit hingga berbentuk tepung kasar.
4.Tepung kulit pisang kasar tersebut kemudian dihaluskan dengan ball mill selama 9 jam.
5.Tepung kulit pisang yang sudah halus selanjutnya diayak dengan ayakan 70 mesh.
Hidrolisa Tepung Kulit Pisang Kepok
Prosedur hidrolisa kulit pisang dengan menggunakan asam klorida diadopsi dari Wahyudi, dkk. [4], Apriliani dan Agustinus [3], serta Endah, dkk. [10], sebagai berikut:
1. Diambil 50 gram tepung kulit pisang halus dan dimasukkan kedalam labu leher satu.
2. Ditambahkan larutan air dengan perbandingan bahan baku: air = 1: 4; 1:7; 1; 10 (b/v).
3. Ditambahkan asam klorida 37% hingga pH=1.
4. Dipanaskan pada suhu 50, 60, dan 70oC dan diaduk dengan magnetic stirrer selama 180 menit.
5. Didinginkan hingga suhu ruangan.
6. Hasil hidrolisis disaring, sehingga didapat hidrolisat.
Fermentasi Hidrolisat
Prosedur proses fermentasi diadopsi dari Jhonprimen, dkk. [19], sebagai berikut:
1. Hidrolisat dimasukkan ke dalam erlenmeyer.
2. Disterilisasi dengan oven pada suhu 105oC selama 30 menit. 3. Didinginkan hingga suhu ruangan.
4. Ditambahkan ragi instan 'Fermipan' sebanyak 7,14 gram.
5. Dihomogenkan dengan shaker selama 15 menit dengan kecepatan 150 rpm.
6. Difermentasi selama 24 jam.
7. Hasil fermentasi didistilasi dengan rotary evaporator vacuum pada tekanan 0,72 bar dan suhu 70oC.
8. Didapat distilat berupa etanol.
Esterifikasi
Prosedur esterifikasi diadopsi dari Bahl dan Bahl [20], sebagai berikut: 1. Dimasukkan etanol yang didapat ke dalam labu leher tiga.
2. Ditambahkan asam asetat (CH3COOH) glasial dan asam klorida (HCl)
37%. dengan perbandingan mol etanol : mol asam asetat = 1:1,02 dan katalis 32%.
3. Dipanaskan hingga suhu 60 oC dan dipertahankan selama 15 menit. 4. Didinginkan hingga suhu ruangan.
5. Hasil esterifikasi di ambil untuk dianalisis.
3.4.2 Prosedur Analisis
Analisis Kadar Karbohidrat Tepung Kulit Pisang
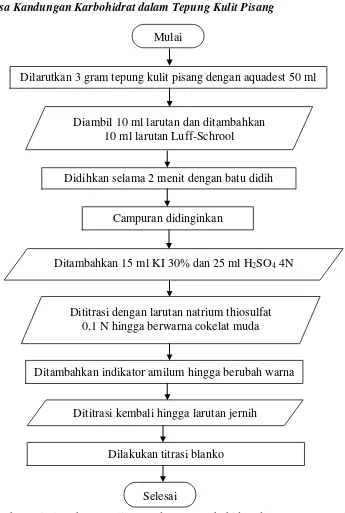
Analisis kadar karbohidrat tepung kulit pisang dilakukan dengan metode Luff-Schrool. Analisis ini dilakukan di Balai Riset dan Standardisasi Industri (BARISTAND) yang bertempat di Jalan Sisingamangaraja, Medan. Prosedur analisa sebagai berikut:
2. Diambil 10 ml larutan dan dimasukkan ke dalam Erlenmeyer kemudian ditambahkan 10 ml larutan Luff-Schrool
3. Dimasukkan beberapa butir batu didih ke dalam campuran, dididihkan selama 2 menit.
4. Selanjutnya campuran didinginkan kemudian ditambah 15 ml KI 30% dan 25 ml H2SO4 4N.
5. Campuran dititrasi dengan natrium thiosulfat 0,1 N hingga berwarna coklat muda.
6. Kemudian ditambahkan indikator amilum hingga berubah warna 7. Dititrasi kembali sampai larutan menjadi jernih.
8. Dibuat pula perlakuan blanko. 9. Dihitung kadar karbohidrat
Kadar karbohidrat mgr karbohidrat faktor pengenceran berat sampel 1 mgr 1 %
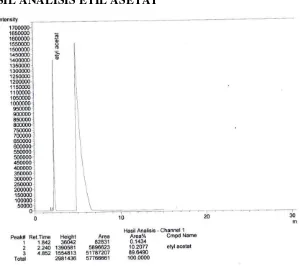
Analisis Kadar Etil Asetat
Analisis kadar etil asetat dilakukan dengan menggunakan kromatografi gas. Analisis kromatografi gas dilakukan dengan menggunakan GC QP 2010 Shimadzu dengan automatic sampling system yang mampu menganalisis 50 scans perdetik. Kolom yang digunakan adalah DB-23. Analisis GC dilakukan dengan menggunakan pelarut aquadest dengan gas pembawa helium dengan kondisi pengaturan temperatur pada alat GC (Colom, Injection) dapat dilihat pada tabel berikut:
Tabel 3.2 Program Pengatur GC
Parameter Nilai Satuan
Temp Oven Kolom 60 0C
Temp Injeksi 200 0C
Tekanan 100 kPa
Kecepatan Aliran 62,3 ml/min
Kecepatan Kolom 1,2 ml/min
Analisis Etil Asetat Optimum
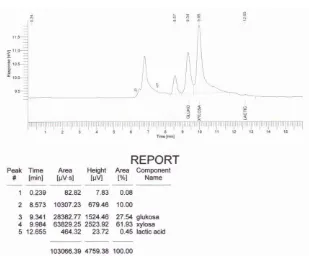
1. Analisis Kadar Glukosa Hasil Hidrolisis
dilakukan di Pusat Penelitian Kelapa Sawit (PPKS) yang terletak di Jalan Bridjen Katamso, Medan. Kolom yang digunakan adalah Hi Plex- H dengan detektor refraktif index dan fase gerak asam sulfat 0,005M. Kondisi operasi dapat dilihat pada tabel di bawah ini
Tabel 3.3 Program Pengatur HPLC
Parameter Nilai Satuan
Temp Kolom 60 0C
Temp Detektor 40 0C
Volume Injek 20 µL
Kecepatan Aliran 0,6 ml/min
2. Analisis Kadar Etanol Hasil Fermentasi
Analisis kadar glukosa hidrolisat dilakukan dengan menggunakan alat Gas Chromatography (GC). Analisis ini dilakukan di Pusat Penelitian Kelapa Sawit (PPKS) yang terletak di Jalan Bridjen Katamso, Medan
3. Analisis Densitas
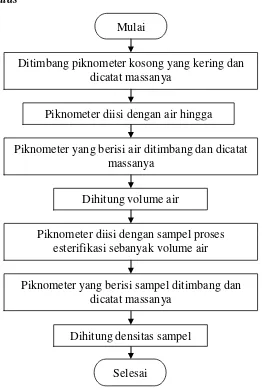
Prosedur analisis densitas diadopsi dari SNI 06-2583-1992 Etil Asetat [25], sebagai berikut:
1. Ditimbang piknometer kosong yang kering dan dicatat massanya. 2. Diisi piknometer 5 ml dengan air hingga penuh.
3. Ditimbang piknometer yang berisi air dan dicatat massanya. Selisih antara massa piknometer kosong dan piknometer yang berisi air merupakan massa air yang diisi ke dalam piknometer.
4. Dihitung volume air dengan rumus:
5. Diisi piknometer dengan sampel sebanyak volume air.
6. Ditimbang piknometer yang berisi sampel dan dicatat massanya. Selisih antara piknometer kosong dan piknometer yang berisi sampel merupakan massa sampel.
7. Dihitung densitas ester dengan persamaan:
4. Analisis Viskositas
Prosedur analisis viskositas diadopsi dari SNI 06-2583-1992 Etil Asetat [25], sebagai berikut:
1. Dilakukan kalibrasi viskosimeter untuk menghitung harga k. Diisi viskosimeter dengan air sebanyak 5 ml.
2. Dihisap air dengan karet penghisap sampai batas garis atas.
3. Ketika air berada pada batas atas, pengukuran waktu dimulai. Waktu alir diukur saat air turun dari batas atas hingga air mencapai batas bawah lalu dicatat waktu alirnya.
4. Dilakukan pengukuran waktu alir sebanyak 3 kali. 5. Dihitung harga k dengan menggunakan rumus:
sgair = 1
6. Air dalam viskosimeter dibuang dan diganti dengan sampel sebanyak 5 ml. 7. Dilakukan pengukuran waktu alir sampel. Pengukuran waktu alir pada
sampel dilakukan seperti halnya pada air dan dilakukan sebanyak 3 kali. 8. Dihitung viskositas sampel dari waktu alir yang diperoleh, dengan rumus:
Viskositas sampel = k x s.g x t Dimana: s.g = densitas sampel / densitas air
3.5 FLOWCHART 3.5.1 Flowchart Penelitian Persiapan Bahan Baku
[image:48.595.148.475.132.421.2]
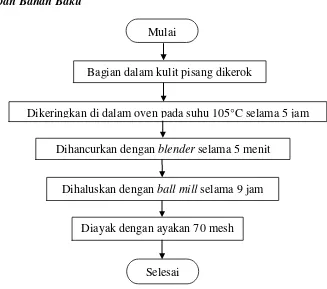
Gambar 3.1 Flowchart Persiapan Bahan Baku Tepung Kulit Pisang Mulai
Bagian dalam kulit pisang dikerok
Dihancurkan dengan blender selama 5 menit
Dikeringkan di dalam oven pada suhu 105°C selama 5 jam
Dihaluskan dengan ball mill selama 9 jam
Diayak dengan ayakan 70 mesh
Hidrolisa Kulit Pisang Kepok
[image:49.595.123.488.76.488.2]
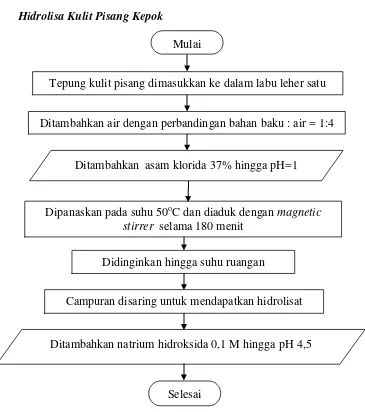
Gambar 3.2 Flowchart Hidrolisis Tepung Kulit Pisang Tepung kulit pisang dimasukkan ke dalam labu leher satu
Ditambahkan air dengan perbandingan bahan baku : air = 1:4
Ditambahkan asam klorida 37% hingga pH=1
Dipanaskan pada suhu 50oC dan diaduk dengan magnetic stirrer selama 180 menit
Didinginkan hingga suhu ruangan
Campuran disaring untuk mendapatkan hidrolisat
Ditambahkan natrium hidroksida 0,1 M hingga pH 4,5
Fermentasi Hidrolisat
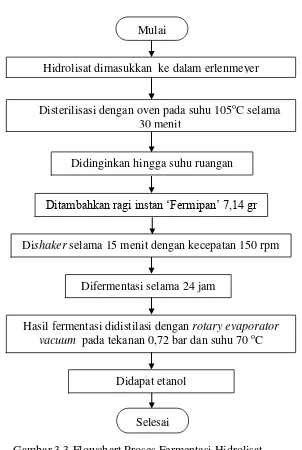
Gambar 3.3 Flowchart Proses Fermentasi Hidrolisat Mulai
Hidrolisat dimasukkan ke dalam erlenmeyer
Disterilisasi dengan oven pada suhu 105oC selama 30 menit
Difermentasi selama 24 jam
Hasil fermentasi didistilasi dengan rotary evaporator vacuum pada tekanan 0,72 bar dan suhu 70 oC
Selesai
Didinginkan hingga suhu ruangan
Ditambahkan ragi instan ‘Fermipan’ 7,14 gr
Dishaker selama 15 menit dengan kecepatan 150 rpm
Esterifikasi
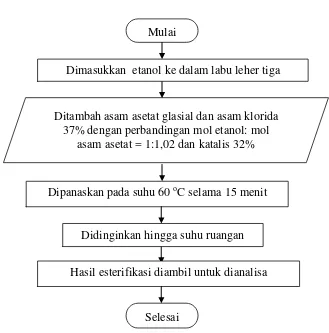
Gambar 3.4 Flowchart Proses Esterifikasi Mulai
Dimasukkan etanol ke dalam labu leher tiga
Ditambah asam asetat glasial dan asam klorida 37% dengan perbandingan mol etanol: mol
asam asetat = 1:1,02 dan katalis 32%
Dipanaskan pada suhu 60 oC selama 15 menit
Didinginkan hingga suhu ruangan
Selesai
3.5.2 Flowchart Analisis
Analisa Kandungan Karbohidrat dalam Tepung Kulit Pisang
[image:52.595.142.487.106.619.2]
Gambar 3.5 Flowchart Analisa Kandungan Karbohidrat dalam Tepung Kulit Pisang
Mulai
Dilarutkan 3 gram tepung kulit pisang dengan aquadest 50 ml
Didihkan selama 2 menit dengan batu didih
Ditambahkan indikator amilum hingga berubah warna Campuran didinginkan
Selesai
Diambil 10 ml larutan dan ditambahkan 10 ml larutan Luff-Schrool
Ditambahkan 15 ml KI 30% dan 25 ml H2SO4 4N
Dititrasi dengan larutan natrium thiosulfat 0,1 N hingga berwarna cokelat muda
Dititrasi kembali hingga larutan jernih
Analisis Densitas
Gambar 3.6 Flowchart Analisis Densitas Mulai
Piknometer diisi dengan air hingga penuh
Selesai
Ditimbang piknometer kosong yang kering dan dicatat massanya
Piknometer yang berisi air ditimbang dan dicatat massanya
Dihitung volume air
Piknometer diisi dengan sampel proses esterifikasi sebanyak volume air
Piknometer yang berisi sampel ditimbang dan dicatat massanya
Analisis Viskositas
[image:54.595.193.457.94.592.2]
Gambar 3.7 Flowchart Analisis Viskositas Mulai
Air dihisap dengan karet hisap hingga melewati batas atas
Viskosimeter diisi dengan air sebanyak 5 ml
Hitung waktu alir air saat melewat batas atas hingga mencapai batas bawah
Pengukuran dilakukan sebanyak 3 kali Dihitung harga k
Viskosimeter diisi dengan sampel sebanyak 5 ml Sampel dihisap dengan karet hisap hingga
melewati batas atas
Hitung waktu alir sampel saat melewat batas atas hingga mencapai batas bawah
Pengukuran dilakukan sebanyak 3 kali Dihitung viskositas sampel
BAB IV
HASIL PEMBAHASAN
4.1 ANALISIS KARBOHIDRAT TEPUNG KULIT PISANG KEPOK. Pada percobaan ini dilakukan beberapa perlakuan untuk meningkatkan kadar karbohidrat dalam kulit pisang. Setelah diberi perlakuan awal hasil analisis kadar karbohidrat tepung kulit pisang dengan metode Luff-Schrool adalah sebesar 84,71%.
Sukowati menyatakan bahwa komposisi kulit pisang mentah berdasarkan analisis dinding sel (% berat kering) yaitu: 37,52% hemiselulosa, 12,06% selulosa, 7,04% lignin. Lignoselulosa terdiri dari selulosa, hemiselulosa, dan lignin [39].
4.2 PENGARUH VARIABEL PERCOBAAN
4.2.1 Pengaruh Perbandingan Bahan Baku Terhadap Kadar Etil Asetat Terbentuk
Hubungan perbandingan bahan baku dan air terhadap kadar etil asetat yang terbentuk ditampilkan pada gambar 4.1 di bawah ini.
Gambar 4.1 Hubungan Perbandingan Bahan Baku Terhadap Kadar Etil Asetat yang Terbentuk
Wahyudi, dkk. menyatakan bahwa proses hidrolisis polisakarida dengan menggunakan asam dipengaruhi oleh ukuran bahan, konsentrasi asam, suhu, waktu, ratio bahan dan pengadukan [4].
Pada gambar 4.1 dapat dilihat bahwa kadar etil asetat yang didapat cenderung menurun dengan bertambahnya rasio perbandingan bahan baku dan air pada proses hidrolisis. Kadar etil asetat tertinggi diperoleh pada perbandingan bahan baku 1:4 suhu 50oC sebesar 10,21% dan terendah pada perbandingan bahan baku 1:10 suhu 70oC sebesar 2,06%.
Penurunan kadar terjadi karena semakin kecil perbandingan bahan baku dan air, semakin banyak jumlah air di dalam campuran. Owen menyatakan bahwa untuk setiap titik didih ada satu campuran ratio yang tepat untuk proses distilasinya. Semakin kecil rasio dari zat yang diuapkan maka titik didih proses akan semakin tinggi. Serta tidak peduli pada konsentrasi campuran distilasi dan
0% 2% 4% 6% 8% 10% 12%
0 1 2 3 4
Kad ar E til A setat
Perbandingan Bahan Baku dan Air
50°C 60°C 70°C
titik didih zat pengotor, zat pengotor akan tetap ada dalam distilat atau ikut menguap selama proses berlangsung [40].
Rendahnya kadar etil asetat pada rasio perbandingan air dan bahan baku yang tinggi dapat disimpulkan karena banyaknya air yang ikut menguap pada proses distilasi etanol.
4.2.2 Pengaruh Perbandingan Bahan Baku Terhadap Yield Etil Asetat Terbentuk
Hubungan perbandingan bahan baku dan air terhadap yield etil asetat yang terbentuk ditampilkan pada gambar 4.2 di bawah ini.
Gambar 4.2 Hubungan Perbandingan Bahan Baku Terhadap Yield Etil Asetat yang Terbentuk
Pada gambar 4.2 yield etil asetat yang dihasilkan semakin bertambah seiring dengan bertambahnya rasio perbandingan bahan baku dan air. Yield etil asetat tertinggi didapat pada perbandingan bahan baku 1:10 dan suhu 60oC yaitu sebesar 82,7%. Sedangkan yield etil asetat terendah didapat pada perbandingan bahan baku 1:4 dan suhu 70oC yaitu sebesar 28%.
Gusmarwani menjelaskan bahwa semakin banyak jumlah air, kontak antara air dengan padatan akan semakin baik sehingga reaksi hidrolisis semakin optimal [8]. Minah menjelaskan bahwa penggunaan air berlebih dapat mengingkatkan
0 10 20 30 40 50 60 70 80 90
0 1 2 3 4
Yiel d Etil A setat (% )
Perbandingan Bahan Baku dan Air
50°C 60°C 70°C
Reaksi hidrolisis polisakarida merupakan proses pemecahan molekul amilum menjadi bagian-bagian penyusunnya yang lebih sederhana seperti dekstrin, isomaltosa, maltosa dan glukosa. Reaksi ini merupakan reaksi orde satu jika digunakan air yang berlebih [41]. Berikut adalah skema reaksi hidrolisis pati dengan air:
Gambar 4.3 Reaksi Hidrolisis Pati Dengan Air [41]
Banyaknya air mengoptimalkan kontak air dengan padatan yang berpengaruh terhadap banyaknya glukosa yang dihasilkan [8][41]. Sehingga, yield etil asetat akan semakin meningkat seiring dengan bertambahnya rsaio perbandingan bahan baku dan air.
4.2.3 Pengaruh Suhu Hidrolisis Terhadap Yield Etil Asetat Terbentuk
Hubungan suhu hidrolisis terhadap yield etil asetat yang terbentuk ditampilkan pada gambar 4.5 di bawah ini.
Gambar 4.4 Hubungan Suhu Hidrolisis Terhadap Yield Etil Asetat yang Terbentuk
10 20 30 40 50 60 70 80 90
40 50 60 70 80
Yiel d Etil A setat (% )
Suhu Hidrolisis (°C)
1:4
1:7
Pada gambar 4.4 dapat dilihat bahwa yield etil asetat yang di dapat cenderung meningkat dengan bertambahnya suhu hidrolisis, namun pada suhu 70oC terjadi penurunan yield.
Berdasarkan percobaan yang dilakukan oleh Apriliani dan Agustinus semakin tinggi suhu hidrolisis, kecepatan hidrolisis akan semakin meningkat, sehingga akan terbentuk produk yang lebih banyak untuk waktu hidrolisis yang sama [3]. Kenaikan kadar glukosa akibat bertambahnya suhu hidrolisis tersebut sesuai dengan persamaan Arrhenius, yaitu [42]:
k = A.e –Ea/RT Dimana:
k = konstanta laju reaksi (s-1) Ea = energi aktivasi (J/mol) T = suhu (oC)
Brandberg dkk. menyimpulkan bahwa peningkatan suhu berperan dalam pemutusan ikatan lignin dan hemiselulosa. Selain itu peningkatan suhu juga dapat menigkatkan laju suatu reaksi hidrolisis. Adanya peningkatan laju reaksi yang dipengaruhi oleh suhu operasi hidrolisis inilah yang menghasilkan gula pereduksi lebih banyak [43].
Dari hasil percobaan diperoleh yield paling tinggi pada setiap perbandingan bahan baku adalah pada suhu 60oC dan mengalami penurunan pada suhu 70oC. Hal ini dikarenakan reaksi hidrolisis merupakan reaksi endotermis sehingga memerlukan panas untuk dapat bereaksi. Tetapi jika suhu terlalu tinggi, maka katalis akan menguap yang mengakibatkan melambatnya reaksi hidrolisis sehingga berakibat pada jumlah glukosa yang diperoleh [4].
Wahyudi, dkk. melakukan penelitian mengenai pengaruh suhu hidrolisis kulit pisang terhadap glukosa yang terbentuk, hasil tertinggi diperoleh pada suhu reaksi 60oC dengan konsentrasi sebesar 0,292 mol/L [4].
Setyawati dan Rahman dari hasil penelitiannya menyatakan tingginya jumlah glukosa yang dihasilkan menyebabkan kenaikan kadar etanol [44].
Hasil penelitian ini sesuai dengan penelitian yang dilakukan oleh Wahyudi dkk., dimana suhu optimum untuk proses hidrolisis kulit pisang adalah 60oC. Suhu hidrolisis yang sesuai menghasilkan glukosa yang lebih banyak. Dengan kadar glukosa yang lebih banyak maka etanol sebagai bahan esterifikasi pun lebih banyak dihasilkan, sehingga volume etil asetat yang dihasilkan juga lebih banyak dan yield yang lebih bagus.
4.3 ETIL ASETAT TERBANYAK
Penentuan etil asetat yang terbaik pada penelitian ini ditentukan berdasarkan yield etil asetat yang diperoleh. Yield etil asetat tertinggi diperoleh pada kondisi perbandingan bahan baku dan air 1 : 10 dan suhu 60oC dengan perolehan yield sebesar 82,7 %. Densitas campuran adalah sebesar 1,017 gr/cm3 dan viskositas campuran sebesar 1,746 cP.
Dari hasil analisis dengan menggunakan HPLC diperoleh kadar glukosa campuran setelah proses hidrolisis sebesar 27,45 %(b/v). Minarni dkk. menyatakan, cake maupun sirup glukosa dapat digunakan sebagai sumber bioetanol karena keduanya memiliki jumlah glukosa yang cukup tinggi dan mampu diubah menjadi etanol oleh mikroba dengan kondisi yang sesuai [45].
Semakin tinggi jumlah glukosa yang dihasilkan maka etanol yang terbentuk semakin banyak, karena bahan yang akan difermentasi menjadi alkohol adalah glukosa [46].
BAB V
KESIMPULAN DAN SARAN
5.1 KESIMPULAN
Adapun kesimpulan yang dapat diambil dari penelitian yang telah dilakukan adalah :
1. Peningkatan rasio perbandingan bahan baku dan air pada proses hidrolisis mengasilkan etil asetat yang lebih banyak karena dengan banyaknya jumlah air yang digunakan kontak antara bahan baku dan air akan semakin baik 2. Suhu hidrolisis terbaik untuk proses pembuatan etil asetat dari tepung kulit
pisang kepok adalah 60oC. Suhu yang tinggi menyebabkan katalis menguap dan suhu yang rendah menyebabkan reaksi kurang sempurna.
3. Pada pembuatan etil asetat dengan proses hidrolisis, fermentasi dan esterifikasi, variabel kondisi terbaik diperoleh pada kondisi suhu hidrolisis 60oC dan perbadingan jumlah bahan baku dan air adalah 1:10 dengan yield sebesar 82,7%.
4. Kulit pisang kepok dapat dijadikan bahan baku pembuatan etil asetat dari proses hidrolisis, fermentasi dan esterifikasi.
5.2 SARAN
Adapun saran yang dapat diberikan dari penelitian yang telah dilakukan untuk penelitian selanjutnya adalah:
DAFTAR PUSTAKA
[1] Badan Pusat Statistik (2013). “Produksi Buah-Buahan di Indonesia 1995-2012”. Diakses pada 12 November 2013 dari bps.go.id.
http://bps.go.id/tab_sub/view.php?tabel=1&daftar=1&id_subyek=55¬ab=5.
[2] Shyam Kumaar, Ganesh Moorthy, Rajeswari, Harikrishnan, “Utilization of Waste Ripe Banana and Peels For Bio Ethanol Production Using Saccharomyces Cerevisiae”, Biosciences Reasearch Journal, 2(2) 2011 : hal 67-71.
[3] Asteria Apriliani, Franky Agustinus, “Pembuatan Etanol Dari Kulit Pisang Secara Fermentasi”, Jurnal Teknologi Kimia dan Industri, 2(2) 2013 : hal. 177-180.
[4] Jatmiko Wahyudi, Wusana A. Wibowo, Yulian A. Rais, Atika Kusumawardani, “Pengaruh Suhu Terhadap Kadar Glukosa Terbentuk Dan Konstanta Kecepatan Reaksi Pada Hidrolisa Kulit Pisang”, Prosiding Seminar Nasional Teknik Kimia Pengembangan Teknologi Kimia untuk Pengolahan Sumber Daya Alam Indonesia, (Februari, 2011), hal. B09-1 – B09-5.
[5] Ketut Ni Sari, “Pembuatan Bioetanol Dari Rumput Gajah Dengan Distilasi Batch”, Jurnal Teknik Kimia Indonesia, 8(3) 2009 : hal. 94-103.
[6] M. Samsuri, M. Gozan, R. Mardias, M. Baiquni, H. Hermansyah, A.
Wijanarko, “Pemanfaatan Sellulosa Bagas Untuk Produksi Etanol Melalui
Sakarifikasi dan Fermentasi Serentak dengan Enzim Xylanase”. Makara Journal of Technology Series, 11(1) 2007 : hal. 17-24
[7] Yuniarti Yusak, ”Pengaruh Variasi Volume HCl 0.5 N dan Waktu Hidrolisa Terhadap Mutu Sirup Pada Pemuatan Sirup Glukosa Dari Pati Ubi Jalar (Ipomea babatas L, Sin babatas edulis choisy)”, Jurnal Sains Kimia, 8(1) 2004 : hal. 21-25
[8] Sri R. Gusmarwani, M.Sri Prasetyo Budi, Wahyu Budi Sediawan, Muslikhin Hidayat, “Pengaruh Perbandingan Berat Padatan Dan Waktu Reaksi Terhadap Gula Pereduksi Terbentuk Pada Hidrolisis Bonggol Pisang”, Jurnal Teknik Kimia Indonesia, 9(3) 2010: hal. 77-82
[9] Lily S. E. Putri, Dede Sukandar, “Konversi Pati Ganyong (Canna edulis Ker.) Menjadi Bioetanol Melalui Hidrolisis Asam dan Fermentasi”, Jurnal Biodiversiti, 9(2) 2008: hal 112-116
[11] Dyah T. Retno, Wasir Nuri, “Pembuatan Bioetanol dari Kulit Pisang”, Prosiding Seminar Nasional Teknik Kimia Pengembangan Teknologi Kimia untuk Pengolahan Sumber Daya Alam Indonesia, (Februari, 2011), hal. E11-1 – E11-7. [12] Isra Dharma Suyandra. “Pemanfaatan Hidrolisat Pati Sagu (Metroxylon sp.) Sebagai Sumber Karbon Pada Fermentasi Etanol Oleh Saccharomyces cerevisiae”. Skripsi, Program Sarjana Fakultas Teknologi Pertanian IPB, Bogor, 2007, hal.7-8
[13] Dwi A. Setyawardhani, Yoenitasari, Sri Wahyuningsih, “Kinetika Reaksi Esterifikasi Asam Formiat Dengan Etanol Pada Variasi Suhu Dan Konsentrasi Katalis”, EKUILIBRIUM, 4(2) 2005 : hal.64-70
[14] David W. Armstrong, Stanley M. Martin, Hiroshi Yamazaki, “Production of Ethyl Acetate from Dilute Ethanol Solutions by Candida utilis”, Biological and Bioengineering, XXVI (Desember, 1983), hal. 1038-1041
[15] Kimberly A. Horan, Carl D. Murphy, Russell M. Stephens, R. J. Warner,
Kenneth A. Windhorst, “Process Impovement For Continuous Ethyl Acetate
Production”, United States Patent, No. US 6,788,021 B2 (Juli, 2004)
[16] Thanet Urit, Christian Loser, Martin Wunderlich, Thomas Bley, “Formation of Ethyl Acetate by Kluyveromyces marxianus on Whey: Studied of the Ester
Stripping”, Bioprocess Biosyst Engineering. 34 2011 : hal 574-559
[17] Sagar B. Gadewar, “Ethyl Acetate Production”, United States Patent, No. US2012/0035390 A1 (Oktober, 2010)
[18] J. P. Essien, E.J. Akpan, E.P Essien, “Studies on Mould Growth and Biomass Production Using Waste Banana Peel”, Bioresource Technology Journal, 96 (13) 2005 : hal. 1451-1456
[19] Jhonprimen H.S, Andreas Turnip, M. Hatta Dahlan, “Pengaruh Massa Ragi,
Jenis Ragi dan Waktu Fermentasi Pada Bioetanol Dari Biji Durian”, Jurnal Teknik Kimia, 2(18) 2012 : hal. 43-51
[20] Arun Bahl, B.S. Bahl , A Textbook of Organic Chemistry. (New Delhi: S. Chand & Company LTD, 2007), hal. 501
[21] Evy Rossy, Usman Pato, S. R. Damanik, “Optimasi Pemberian Ammoium
Sulfat terhadap Produksi Nata de Banana Skin”, Agricultural Science and Technology Journal, 7(2) 2008: hal. 30
[22] Suyanti Satuhu, Ahmad Supriyadi, Pisang, Budidaya, Pengolahan, dan Prospek Pasar, (Bogor: PT Penebar Swadaya, 1999), hal. 15-17
[24] Retno Dewati, Limbah Kulit Pisang Kepok Sebagai Bahan Baku Pembuatan Ethanol (Jawa Timur: UPN Press, 2008), hal. 6
[25] Informasi Keracunan BPOM (2 1 ). “Etil asetat”. Diakses pada 15 Juli 2013 http://ik.pom.go.id/katalog/ETIlLASETAT.pdf.
[26]“Etil Asetat”. SNI Departemen Perindustrian, 1992. [27] Riswiyanto. 2009. Kimia Organik. Erlangga: Jakarta
[28] Jiri Kolena, Jaromir Lederer, Pavel Moravek, Jiri Hanika, Quido Smejkal,
Davis Skala, “Method of Producing Ethyl Acetate and an Equipment for
![Gambar 2.3 Diagram Alir Proses Dehidrogenasi Hidrogen [17]](https://thumb-ap.123doks.com/thumbv2/123dok/306214.27294/34.595.163.509.85.343/gambar-diagram-alir-proses-dehidrogenasi-hidrogen.webp)