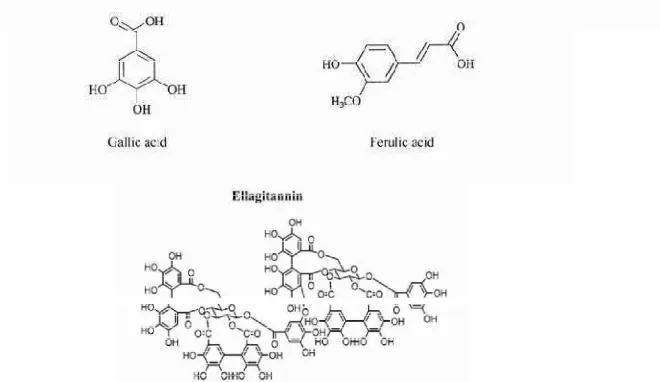
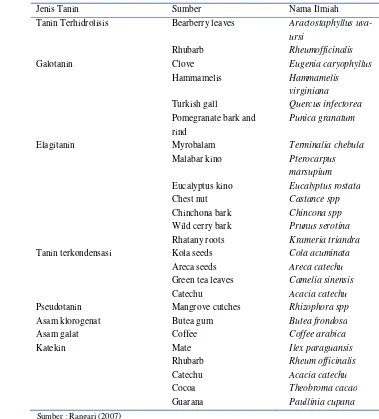
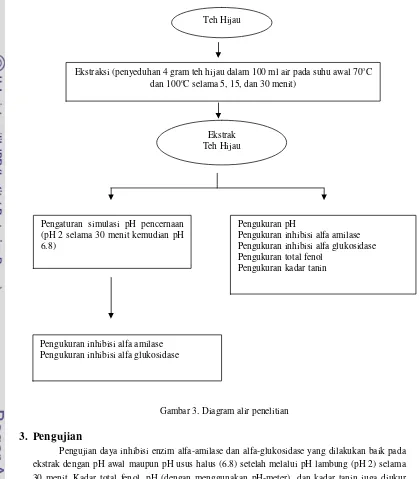
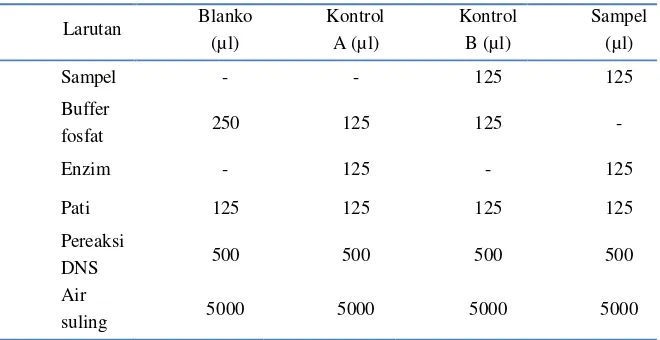
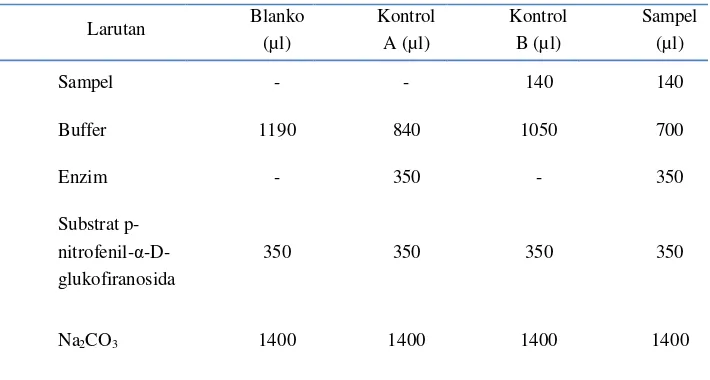
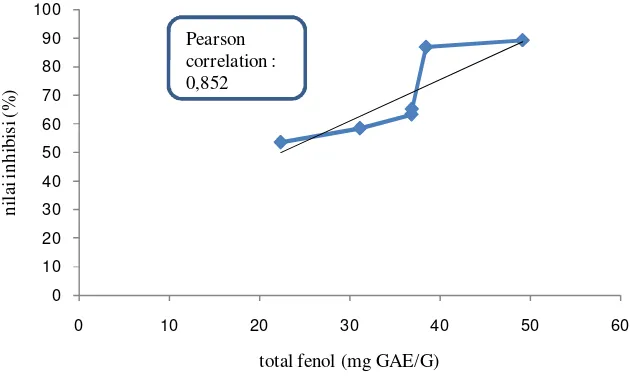
Pengaruh Suhu dan Lama Penyeduhan Teh Hijau (Camellia sinensis) serta Proses Pencernaan secara In vitro terhadap Penghambatan Aktivitas Enzim Alfa Amilase dan Alfa Glukosidase secara In vitro
Teks penuh
Gambar

Dokumen terkait
fisik dan mekanik tanah yang terdiri dari parameter : (a) konsistensi tanah, (b) ltadar air tanah, (c) bulk density tanah, (d) tahanan penetrasi tanah, (e) gaya geser
Pointers: Konsep kelekatan negara dan ekonomi; Arti penting jaringan sosial industri kecil di Taiwan; Negara dan industri besar di Korea.
Hasil dari penelitian ini, penulis telah berhasil membangun sebuah media pembelajaran untuk memperkenalkan bentuk geometri pada anak dengan mengimplementasikan software Adobe
Judul : Hubungan Tingkat Pendidikan Formal Wajib Pajak dengan Tingkat Kesadaran Membayar Iuran Wajib Televisi di Kecamatan Genuk Kodya SemarangC. Program : P3T Tahun : 1988
- Kesediaan merekomendasikan program studi pada institusi perguruan tinggi Sedangkan Zeithaml, Berry, Parasuraman (1996) dalam penelitian pada empat perusahaan yang
Kelompok II SIKMRN Kelompok III SIKMR + Kitosan Blangkas Nano Kelompok IV SIKMRN + Kitosan Blangkas Nano Penanaman sampel gigi P dalam pipa paralon.. Preparasi kavitas
Hasil penelitian menunjukkan bahwa usaha industri kreatif di Bali pada umumnya: (1) sangat tergantung pada kemampuan bekerjasama (sinergisitas) dengan pihak terkait, kemampuan
Ditawarkan” : berarti saham biasa atas nama yang diterbitkan oleh Perseroan masing-masing dengan nilai nominal Rp100 (seratus Rupiah) untuk ditawarkan dan dijual kepada