PENGARUH SUHU DAN KONSENTRASI NaCl TERHADAP
TEGANGAN PERMUKAAN LARUTAN PENCUCI TANGAN
SKRIPSI
ELISA PUTRI KAROLINA
090822041
DEPARTEMEN KIMIA
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM
UNIVERSITAS SUMATERA UTARA
PENGARUH SUHU DAN KONSENTRASI NaCl TERHADAP
TEGANGAN PERMUKAAN LARUTAN PENCUCI TANGAN
SKRIPSI
Diajukan untuk melengkapi tugas dan memenuhi syarat mencapai gelar Sarjana Sains.
ELISA PUTRI KAROLINA 090822041
DEPARTEMEN KIMIA
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM
UNIVERSITAS SUMATERA UTARA
PERSETUJUAN
Judul : PENGARUH SUHU DAN KONSENTRASI NaCl
TERHADAP TEGANGAN PERMUKAAN LARUTAN PENCUCI TANGAN
Kategori : SKRIPSI
Nama : ELISA PUTRI KAROLINA
Nomor Induk Mahasiswa : 090822041
Program Studi : SARJANA (S1)/ KIMIA EKSTENSI
Departemen : KIMIA
Fakultas : MATEMATIKA DAN ILMU PENGETAHUAN ALAM
UNIVERSITAS SUMATERA UTARA
Disetujui di, Medan, September 2011
Komisi Pembimbing
Pembimbing 2 Pembimbing 1
Drs. Abdi Negara Sitompul Dr. Marpongahtun, M.Sc NIP. 194607161974031001 NIP.196111151988032002
Diketahui/ Disetujui oleh:
Departemen Kimia FMIPA USU Ketua,
PERNYATAAN
PENGARUH SUHU DAN KONSENTRASI NaCl TERHADAP
TEGANGAN PERMUKAAN LARUTAN PENCUCI TANGAN
SKRIPSI
Saya mengakui bahwa skripsi ini adalah hasil kerja saya sendiri, kecuali beberapa kutipan dan ringkasan yang masing-masing disebutkan sumbernya.
Medan, september 2011
PENGHARGAAN
Puji dan syukur penulis panjatkan kepada Tuhan Yang Maha Esa atas segala berkat dan penyertaan Nya sehingga penulis dapat menyelesaikan studi, penelitian dan penulisa skripsi ini, dengan judul “Pengaruh Suhu dan Konsentrasi NaCl Terhadap Tegangan Permukaan Larutan Pencuci Tangan”.
Secara khusus penulis ingin mengucapkan terima kasih yang tak terhingga kepada orang tua tercinta, ayahanda S.Purba dan ibunda T.Sembiring yang telah memberikan dukungan moril, spiritual, maupun materil sehingga penulis dapat menyelesaikan studi, penelitian dan penulisan skripsi ini.
Pada kesempatan ini penulis juga ingin mengucapkan terima kasih kepada semua pihak yang telah membantu penulis dalam menyelesaikan tugas akhir ini,antara lain:
1. Ibu Dr. Marpongahtun, M.Sc dan Bapak Drs. Abdi Negara Sitompul selaku dosen Pembimbing I dan Pembimbing II yang telah membimbing dan mengarahkan penulis dalam menyelesaikan skripsi ini.
2. Ibu Dr. Rumondang Bulan, MS dan Bapak Drs. Albert Pasaribu, M.Sc selaku Ketua dan Sekretaris Jurusan Kimia FMIPA USU
3. Kepala dan Staf Laboratorium Kimia Fisika dan Polimer yang telah memberikan bimbingan dan bantuan kepada penulis selama melakukan penelitian.
4. Abang dan adik penulis, Jhon Hendrik dan Jonatan Ricardo yang telah memberikan dukungan dan doanya.
5. Teman-teman semasa D3 (Dina, Domi, Netti, Susi, Dewi, Santi, Helga, Floren, Risna, Mutiara, Widya, Mery, Juli, Lia, Erix,) yang telah memberikan dukungan, semangat dan doa walaupun dari jarak jauh. Bisa mengenal kalian adalah salah satu hal berharga di hidupku.
6. Bang Osbal yang telah mau bekerja sama dan membantu selama penelitian dan penulisan skripsi ini. Juga buat Bang Ian yang telah memberikan bantuan, semangat dan doanya.
7. Teman-teman semasa SMA khususnya Tasya, Fida, Asril, Ayub, Anes, Johan, Meylini, Sulaiman, Cristian yang selalu memberi dukungan, semangat dan doanya.
8. Rekan-rekan seperjuangan Kimia Ekstensi stambuk 2009.
Penulis menyadari bahwa cara penulisan skrispsi ini serta isinya masih jauh dari sempurna. Oleh karena itu dengan kerendahan hati penulis sangat mengharapkan masukan berupa kritikan maupun saran yang bersifat membangun demi kesempurnaan skripsi ini.
Akhir kata dengan segala kerendahan hati, penulis mengharapkan skripsi ini akan bermanfaat bagi kita semua.
Medan, september 2011
ABSTRAK
T
HE EFFECT OF TEMPERATURE AND CONCENTRATION OF NACLTO SURFACE TENSION OF HANDWASHING LIQUID
ABSTRACT
The investigation of The effect of Temperature and concentration of NaCl to Surface Tension of Hand Wash Liquid was carried out. The investigation was done by measuring the surface tension of hand wash liquid with various temperature (300C,
400C, 500C) and various concentration of NaCl (10%, 20%, 30%). The surface
DAFTAR ISI
Halaman
PERSETUJUAN ii
PERNYATAAN iii
PENGHARGAAN iv
ABSTRAK v
ABSTRAC vi
DAFTAR ISI vii
DAFTAR GAMBAR ix
DAFTAR TABEL x
DAFTAR LAMPIRAN xi
BAB 1 PENDAHULUAN
1.1. Latar Belakang 1
1.2. Perumusan Masalah 3
1.3. Pembatasan Masalah 3
1.4. Tujuan Penelitian 3
1.5. Manfaat Penelitian 4
1.6. Metodologi Penelitian 4
1.7. Lokasi Penelitian 4
BAB 2 TINJAUAN PUSTAKA
2.1. Deterjen 5
2.2. Komponen Penyusun Deterjen 7
2.2.1.Builder 8
2.2.2.Filler 8 2.2.2.Aditif 8 2.2.4.Surfaktan 8
2.2.4.1. Pembagian surfaktan 9
2.3.Koloid 10
2.3.1.Pembagian koloid 11
2.4.Kegunaan Koloid pada Bahan Pencuci 11
2.5.Tegangan Permukaan 11
2.5.1.Faktor-faktor yang mempengaruhi tegangan permukaan 11
2.5.2.Pengukuran tegangan permukaan 13
2.5.2.1.Metode kenaikan pipa kapiler 13
2.5.2.2.Metode cincin du NuOy 16
2.5.2.3. Metode tekanan gelembung maksimum 17
BAB 3 BAHAN DAN METODE PENELITIAN
3.1 Bahan – bahan 18
3.2 Alat – alat 18
3.3 Metode Penelitian 19
3.3.1. Populasi 19
3.3.2. Sampling 19
3.3.3. Persiapan 19
3.3.3.1. Pencucian alat 19
3.3.3.3. Kalibrasi piknometer 20
3.3.3.4. Pembuatan larutan 20
3.3.3.4.1. Pembuatan larutan Natrium klorida 10% 21 3.3.3.4.2. Pembuatan larutan Natrium klorida 20% 21 3.3.3.4.3. Pembuatan larutan Natrium klorida 30% 21 3.3.3.4.4. Pembuatan larutan SLES 33,3 % 21 3.3.3.4.5. Pembuatan larutan SLS 33,3 % 21 3.3.3.4.6. Prosedur pembuatan bahan pencuci tangan (1 L) 21
3.3.4. Pengumpulan data 22
3.3.4.1. Penentuan densitas 22
3.3.4.2. Penentuan tegangan permukaan 22
3.4. Pengolahan Data 23
3.4.1. Penentuan kesalahan 23
3.4.1.1. Sumber kesalahan sistematik 23
3.4.1.2. Kesalahan random (Intermediate) 24 3.4.1.3. Kesalahan gabungan dari kesalahan random 24 3.4.2. Penentuan ketidakpastian dalam significant figure 24 3.4.2.1. Perhitungan ketidakpastian persentase NaCl 24 3.4.2.2. Perhitungan ketidakpastian pipet volume 10 mL 25 3.4.2.3. Perhitungan ketidakpastian gelas ukur 10 mL 26 3.4.2.4.Perhitungan ketidakpastian gelas ukur 100 mL 27
3.5. Analisis Data 28
3.5.1. Analisis variansi 28
3.5.2. Analisis regresi 29
3.5.3. Uji hipotesa 30
3.6. Skema Pengambilan Data 32
3.6.1. Skema pembuatan larutan pencuci tangan 32
3.6.2. Skema penentuan densitas 33
3.6.3. Skema penentuan tegangan permukaan 34
BAB 4 HASIL DAN PEMBAHASAN
4.1. Hasil 36
4.2. Pembahasan 37
4.2.1. Hipotesa satu 37
4.2.2. Hipotesa dua 38
BAB 5 KESIMPULAN DAN SARAN
5.1. Kesimpulan 40
5.2. Saran 40
DAFTAR GAMBAR
Halaman
Gambar 2.1. Lambang Umum Surfaktan 9
Gambar 2.2. Struktur Surfaktan Liniear Alkilbenzen Sulfonat 9 Gambar 2.3. Proses kenaikan Cairan pada Pipa Kapiler 15
Gambar 2.4. Tensiometer Du Nuoy 16
Gambar 4.1. Grafik Pengaruh Konsentrasi NaCl Terhadap Nilai 38 Tegangan Permukaan Larutan Pencuci Tangan
DAFTAR TABEL
Halaman
Tabel 4.1. Data Hasil Perhitungan Nilai Tegangan Permukaan 36 Berdasarkan Variasi Konsentrasi NaCl
DAFTAR LAMPIRAN
Halaman Tabel 1. Data Hasil Pengukuran Densitas Larutan Pencuci 43
Tangan dengan Variasi Konsentrasi NaCl dan Suhu Larutan Pencuci Tangan
Tabel 2. Data Statistik Nilai Tegangan Permukaan 44 Berdasarkan Variasi Konsentrasi NaCl
Tabel 3. Hasil Analisis Sidik Ragam Efek Konsentrasi NaCl 44 Terhadap Nilai Tegangan Permukaan Larutan
Pencuci Tangan
Tabel 4. Data Statistik Nilai Tegangan Permukaan 45 Berdasarkan Variasi Suhu
Tabel 5. Hasil Analisis Sidik Ragam Efek Suhu Terhadap Nilai 45 Tegangan Permukaan Larutan Pencuci Tangan
Tabel 6. Data Anaalisis Regresi Efek Konsentrasi NaCl 46 Terhadap Nilai Tegangan Permukaan Larutan
Pencuci Tangan
Tabel 7. Hasil perhitungan analisis regresi untuk nilai 46 Tegangan Permukaan larutan pencuci tangan
berdasarkan efek Konsentrasi NaCl
Gambar1.Grafik analisa regresi untuk nilai Tegangan Permukaan 47 larutan pencuci tangan berdasarkan efek konsentrasi NaCl
Tabel 8. Data Ananlisis Regresi Efek Suhu Larutan Pencuci 47 Tangan Terhadap Nilai Tegangan Permukaan
Larutan Pencuci Tangan
Tabel 9. Hasil perhitungan analisis regresi untuk nilai 48 Tegangan Permukaan larutan pencuci tangan berdasarkan
Efek Suhu larutan Pencuci Tangan
ABSTRAK
T
HE EFFECT OF TEMPERATURE AND CONCENTRATION OF NACLTO SURFACE TENSION OF HANDWASHING LIQUID
ABSTRACT
The investigation of The effect of Temperature and concentration of NaCl to Surface Tension of Hand Wash Liquid was carried out. The investigation was done by measuring the surface tension of hand wash liquid with various temperature (300C,
400C, 500C) and various concentration of NaCl (10%, 20%, 30%). The surface
BAB 1 PENDAHULUAN
1.1 Latar Belakang
Deterjen adalah campuran berbagai bahan, yang digunakan untuk membantu
pembersihan dan terbuat dari bahan-bahan turunan minyak bumi. Dibanding dengan
sabun, deterjen mempunyai keunggulan antara lain mempunyai daya cuci yang lebih
baik serta sifat tidak membentuk endapan dengan ion-ion logam divalen dalam air
sadah. Deterjen merupakan garam natrium dari asam sulfonat.
Deterjen dalam kerjanya dipengaruhi beberapa hal, yang terpenting adalah
jenis kotoran yang akan dihilangkan dan air yang digunakan. Deterjen, khususnya
surfaktannya, memiliki kemampuan yang unik untuk mengangkat kotoran, baik yang
larut dalam air maupun yang tak larut dalam air. Salah satu ujung dari molekul
surfaktan bersifat lebih suka minyak atau tidak suka air, akibatnya bagian ini
menetrasi kotoran yang berminyak. Ujung molekul surfaktan satunya lebih suka air,
bagian inilah yang berperan mengendorkan kotoran dari kain dan mendispersikan
kotoran.1
Bahan baku untuk pembuatan deterjen ini terdiri dari beberapa jenis, yaitu
bahan aktif, bahan pengental (filler), dan bahan tambahan (additif). Bahan aktif yang
digunakan adalah jenis surfaktan yang merupakan bahan utama pembuatan deterjen
karena bahan ini mempunyai kemampuan mengikat dan mengangkat kotoran.
Surfaktan menurunkan tegangan permukaan air dengan mematahkan ikatan-ikatan
hidrogen pada permukaan. Setelah mencapai konsentrasi tertentu, tegangan
permukaan akan konstan walaupun konsentrasi surfaktan ditingkatkan. Filler (pengisi)
adalah bahan tambahan deterjen yang tidak mempunyai kemampuan meningkatkan
daya cuci, pemberian bahan ini berguna untuk memperbanyak atau memperbesar
1
volume, tapi juga berfungsi meningkatkan kekuatan ionik dalam larutan pencuci.
Contoh Sodium sulfat, sodium klorida. Sedangkan bahan tambahan (additif) yang
digunakan hanya bertujuan sebagai komersialisasi produk, misalnya pewangi atau
pewarna.2
Semua cairan memiliki tegangan permukaan, tetapi tegangan permukaan air
lebih tinggi dari yang lainnya. Tegangan permukaan dari air bisa diturunkan dengan
penambahan zat pembasah seperti sabun atau deterjen. Sabun dan deterjen adalah
surfaktan (zat aktif permukaan). Ketika suatu deterjen ditambahkan ke butiran air
dalam permukaan yang berminyak, tegangan permukaan akan menurun,
butiran-butiran akan hancur, dan air akan menyebar. 3
Tegangan permukaan cairan dapat didefinisikan sebagai gaya per satuan
panjang pada permukaan cairan yang melawan ekspansi dari luas permukaan.
Tegangan permukaan cairan γ, berbeda-beda bergantung pada jenis cairan dan suhu. Adanya zat terlarut pada cairan dapat menaikkan atau menurunkan tegangan
permukaan tergantung sifat zat terlarutnya. Makin kecil nilai γ suatu cairan, makin besar kemampuan cairan tersebut membasahi benda. Hubungan ini banyak
dimanfaatkan dalam kehidupan sehari-hari; misalnya untuk menghasilkan cucian
pakaian agar lebih bersih dapat digunakan air panas atau air sabun.4
Penelitian mengenai sifat-sifat deterjen dan dampaknya terhadap perairan yang
telah dilakukan Manik, J.M (1987), yang menyimpulkan bahwa secara fisika deterjen
merupakan zat yang berfungsi menurunkan tegangan permukaan zat cair.
Bhattacharya (2004) telah meneliti tentang studi tegangan permukaan
poly(vinil alcohol) yang dipengaruhi konsentrasi, suhu dan penambahan zat
chaotropic telah dilakukan oleh, yang menyimpulkan bahwa suhu dan konsentrasi
dapat meningkatkan dan menurunkan tegangan permukaan molekul polimer tersebut.
2
http:// wordpress.com/2010/08/28/surfaktant-deterjen-sabun-revisi/.
3
Matta, M.S, 1986. General, Organic & Biological Chemistry. Cuming Publishing Company, Inc.
California
4
Syahra (2004) telah meneliti pengaruh konsentrasi deterjen komersil dan
komposisi linier alkilbenzen sulfonat pada beberapa merek dagang deterjen cair
terhadap tegangan antar permukaan air-minyak tanah.
Lebih lanjut berdasarkan peneliti terdahulu oleh Rangkuti (2010) yang
meneliti pengaruh penambahan NaCl terhadap viskositas bahan pencuci tangan cair,
maka dianggap perlu melakukan penelitian bagaimana pengaruh suhu dan konsentrasi
zat yang terlarut yakni NaCl dapat mempengaruhi tegangan permukaan larutan
pencuci tangan. Hal inilah yang mendorong penulis melakukan penelitian bagaimana
pengaruh suhu dan konsentrasi NaCl dapat mempengaruhi tegangan permukaan
larutan pencuci tangan.
1.2. Perumusan Masalah
1. Adakah pengaruh suhu terhadap tegangan permukaan (γ) larutan pencuci
tangan
2. Adakah pengaruh konsentrasi NaCl terhadap tegangan permukaan (γ) larutan
pencuci tangan
1.3. Pembatasan Masalah
Dalam penelitian ini penulis membatasi masalah penelitian dengan menentukan
tegangan permukaan (γ) larutan pencuci tangan setelah pemasan dan penambahan zat pengental. Tegangan permukaan (γ) larutan pencuci tangan ditentukan dengan menggunakan metode kenaikan pipa kapiler. Variasi suhu yang digunakan adalah
300C, 400C, 500C. Jenis zat pengental yang digunakan adalah Natrium Klorida (NaCl) dengan varisi konsentrai yang digunakan adalah 10%, 20%, 30%.
1. Untuk mengetahui pengaruh suhu terhadap tegangan permukaan (γ) larutan
pencuci tangan
2. Untuk mengetahui pengaruh konsentrasi NaClterhadap tegangan permukaan (γ) larutan pencuci tangan.
1.5. Manfaat Penelitian
Dengan tercapainya tujuan penelitian ini, maka akan diperoleh penjelasan bagaimana
suhu dan konsentrasi NaCl mempengaruhi nilai tegangan permukaan (γ) dari larutan pencuci tangan.
1.6. Metodologi Penelitian
Penelitian ini adalah eksperimen laboratorium dengan melakukan variasi suhu dan
konsentrasi NaCl sebagai zat pengental pada bahan pencuci tangan dengan tujuan
mengetahui pengaruhnya terhadap tegangan permukaan. Variasi suhu yang digunakan
adalah 30oC, 40oC, 50oC. Variasi konsentrasi NaClyang digunakan adalah 10%, 20%, dan 30% (sebagai variabel bebas). Tegangan permukaan larutan pencuci tangan di uji
dengan menggunakan metode kenaikan pipa kapiler menggunakan alat tensiometer
kapiler (sebagai variabel terikat). Faktor yang mempengaruhi yaitu faktor pengadukan
yang menentukan tingkat kehomogenan bahan pencuci tangan (sebagai variabel tetap).
1.7. Lokasi Penelitian
Penelitian dilakukan dilaboratorim Kimia Fisika Fakultas Matematika dan Ilmu
BAB 2
TINJAUAN PUSTAKA
2.1.Deterjen
Suatu deterjen (dari bahasa Latin detergere, menyeka) adalah molekul yang
sama seperti sabun, membentuk missel dalam air dan emulsi lemak dan minyak.
Deterjen sintetis yang biasa sering digunakan adalah natrium alkilbenzenesulfonat,
Deterjen mirip dengan sabun yang memiliki sebuah grup ion dan suatu
hidrokarbon berantai panjang tetapi pasti menguntungkan. Ketidak untungan sabun
muncul bila digunakan dalam air sadah, yang mengandung kation logam-logam
tertentu seperti Ca, Mg, Ba, Fe, dan Fe. Kation-kation tersebut menyebabkan
garam natrium atau kalium dari asam karboksilat yang semula larut menjadi
garam-garam karboksilat yang tidak larut.5
Rantai alkil sebaiknya tidak bercabang. Alkil benzenasulfonat yang bercabang
bersifat tidak dapat didegradasi oleh jasad renik (biodegradable). Deterjen ini
mengakibatkan masalah polusi berat pada tahun 1950-an, yaitu berupa buih pada
unit-unit penjernihan serta di sungai dan danau-danau. Sejak tahun 1965, digunakan alkil
benzenasulfonat yang tidak bercabang. Deterjen jenis ini mudah didegradasi secara
biologis oleh mikroorganisme dan tidak berakumulasi di lingkungan kita.6
Deterjen pertama kali dikenalkan pada tahun 1933 yang dianggap lebih efektif
dalam air sadah. Deterjen memiliki dua kesamaan karakteristik struktur yang
dilakukan oleh sabun:
5
Richey, G.H., 1983. Chemistry. The Pennsylvania State University. New Jersey.
6
1. Memiliki suatu rantai panjang, nonpolar, hidrofobik, hidrokarbon, yang mana
larut dalam lemak dan minyak
2. Mereka memiliki suatu ujung polar dan hidrofilik yang mana larut dalam air.
Sebagian besar deterjen sekarang ini adalah biodegradable. Yang berarti bahwa
deterjen tersebut dapat secara cepat dimetabolisme oleh mikroorganisme dalam suatu
kotoran pembuangan tanaman dan tidak dibebaskan kedalam lingkungan. Untuk
deterjen yang biodegradable, rantai panjang alkil harus diputus. Deterjen yang
digunakan pada tahun 1950-1960an memiliki rantai bercabang yang tidak
biodegradable.7
Sebagian besar kotoran pada pakaian atau kulit melekat menjadi suatu lapisan
tipis dari minyak. Jika lapisan minyak dapat diubah menjadi partikel-partikel kotoran
maka akan mudah dibersihkan. Suatu molekul sabun terdiri dari panjangnya
hidrokarbon dimana rantai atom karbon dengan sifat polar atau grup ionik pada
ujungnya. Rantai karbon adalah lipofilik (mengikat atau larut dalam lemak dan
minyak), dan ujung polarnya adalah hidrofilik (mengikat atau larut dalam air). Ketika
sabun tercampur dengan air, akan terbentuk suatu dispersi koloid. Larutan sabun ini
terdiri dari agregat molekul sabun yang disebut misel. Ujung nonpolar atau hidrofilik
dari molekul secara langsung menuju pusat micelles ujung molekul yang polar atau
hidrofilik membentuk ’permukaan’ dari misel yang hadir pada air. Ekor lipofilik pada
molekul sabun tidak larut dalam minyak. Ujung hidrofilik memperpanjang minyak
jatuh ke dalam air.8
7
Bailey, S.P,. 1985. Organic Chemistry. Third edition. California Polytechnic State
University.
San Luis Obispo.
8
Hart, H., 1991. Organic Chemistry A Short Course. Eight edition. Houghton Mifflin
Company.
Pencucian adalah proses membersihkan suatu permukaan benda padat dengan
bantuan larutan pencuci melalui suatu proses kimia-fisika yang disebut deterjenasi.
Sifat utama dari kerja deterjenasi adalah membasahi permukaan yang kotor kemudian
melepaskan kotoran. Pembasahan berarti penurunan tegangan muka padatan-cair.
Pencucian pada permukaan atau pelepasan kotoran berlangsung dengan jalan
mendispersikan dan mengemulsi kotoran, lalu dengan bantuan aksi mekanik kotoran
menjadi terlepas dari permukaan benda padat. Kotoran padat dapat melekat karena
adanya pengaruh: ikatan minyak, gaya listrik statik, dan ikatan hidrogen. Penambahan
sedikit alkali membantu daya deterjensi dari sabun, tetapi dapat mendorong terjadinya
hidrolisa. Alkali digunakan untuk menjaga pH larutan. Deterjen cair biasanya
menggunakan bahan pelarut organik sebagai pelengkap dan penambah daya
deterjenasi dan diperlukan untuk kotoran-kotoran yang sulit dihilangkan atau
berlemak.9
2.2.Komponen Penyusun Deterjen
Pada umumnya, deterjen mengandung bahan-bahan berikut:
2.2.1.Builder
Builder adalah suatu bahan yang dapat menambah kerja dari bahan penurun
tegangan permukaan dengan cara menonaktifkan mineral penyebab kesadahan air.
Builders digunakan untuk melunakkan air sadah dengan cara mengikat
mineral-mineral yang terlarut, sehingga surfaktan dapat berkonsentrasi pada fungsi utamanya.
Builder juga membantu menciptakan kondisi keasaman yang tepat agar proses
pembersihan dapat berlangsung lebih baik serta membantu mendispersikan dan
mensuspensikan kotoran yang telah lepas.
9
Schwartz, A.M. 1958. Surface Aktive Agents and Detergents. Interscience Publisher,
Dalam pembuatan detergen, builder sering ditambahkan dengan maksud
menambah kekuatan daya cuci dan mencegah mengendapnya kembali
kotoran-kotoran yang terdapat pada pakaian yang akan dicuci. Contohnya: Sodium Tri Poli
Phosphat (STPP), Nitril Tri Acetat (NTA), Ethylene Diamine Tetra Acetate (EDTA)
2.2.2.Filler
Filler (pengisi) adalah bahan tambahan deterjen yang tidak mempunyai
kemampuan meningkatkan daya cuci, tetapi menambah kuantitas Bahan ini berfungsi
sebagai pengisi dari seluruh campuran bahan baku. Pemberian bahan ini berguna
untuk memperbanyak atau memperbesar volume. Keberadaan bahan ini dalam
campuran bahan baku sabun semata-mata ditinjau dari aspek ekonomis. Namun selain
digunakan sebagai pembantu proses, bahan pengisi ini juga berfungsi meningkatkan
kekuatan ionik dalam larutan pencuci. Contoh Sodium sulfat, sodium klorida.
2.2.3.Aditif
Aditif adalah bahan suplemen / tambahan untuk membuat produk lebih
menarik, misalnya pewangi, pelarut, pemutih, pewarna dst, tidak berhubungan
langsung dengan daya cuci deterjen. Additives ditambahkan lebih untuk maksud
komersialisasi produk. Contoh : Enzim, Boraks, Sodium klorida, Carboxy Methyl
Cellulose (CMC).
2.2.4.Surfaktan
Surfaktan (surface active agent) merupakan zat aktif permukaan yang
sekaligus memiliki gugus hidrofilik dan gugus lipofilik sehingga dapat
mempersatukan campuran yang terdiri dari air dan minyak. Aktifitas surfaktan
diperoleh karena sifat ganda dari molekulnya. Molekul surfaktan memiliki bagian
polar yang suka akan air (hidrofilik) dan bagian non polar yang suka akan
minyak/lemak (lipofilik). Bahan aktif ini berfungsi menurunkan tegangan permukaan
air sehingga dapat melepaskan kotoran yang menempel pada permukaan bahan. 10
10
ekor hidrofobik ekor hidrofilik
Gambar.2.1. Lambang umum untuk suatu surfaktan 2.2.4.1. Pembagian Surfaktan
a. Surfaktan anionik
Surfaktan anionik merupakan surfaktan dengan bagian aktif pada permukaannya
mengandung muatan negatif. Contoh dari jenis surfaktan anionik adalah Linier Alkil
Benzene Sulfonat (LAS), Alkohol Sulfat (AS), Alkohol Eter Sulfat (AES), Alpha
Olefin Sulfonat (AOS).
SO3-Na+
Gambar 2.2. Struktur Linier Alkilbenzen Sulfonat
b. Surfaktan kationik
Surfaktan ini merupakan surfaktan dengan bagian aktif pada permukaannya
mengandung muatan positif. Surfaktan ini terionisasi dalam air serta bagian aktif pada
permukaannya adalah bagian kationnya. Contoh jenis surfaktan ini adalah ammonium
kuarterner.
c. Surfaktan nonionik
Surfaktan yang tidak terionisasi di dalam air adalah surfaktan nonionik yaitu surfaktan
dengan bagian aktif permukaanya tidak mengandung muatan apapun, contohnya:
d. Surfaktan ampoterik
Surfaktan ini dapat bersifat sebagai non ionik, kationik, dan anionik di dalam larutan,
jadi surfaktan ini mengandung muatan negatip maupun muatan positip pada bagian
aktif pada permukaannya. Contohnya: Sulfobetain (RN+(CH3)2CH2CH2SO3-.
Surfaktan-surfaktan menurunkan tegangan permukaan air dengan mematahkan
ikatan-ikatan hidrogen pada permukaan. Mereka melakukan ini dengan menaruh
kepala-kepala hidrofiliknya pada permukaan air dengan ekor-ekor hidrofobiknya
terentang menjauhi permukaan air. 11
2.3.Koloid
Koloid merupakan dispersi partikel kecil dari suatu material ke dalam material
lain. “kecil” berarti diameternya kurang dari 500 nm (sekitar panjang gelombang
sinar). Secara umum, partikel itu merupakan kumpulan dari sejumlah atom atau
molekul, tetapi terlalu kecil untuk dilihat dengan mikroskop optik biasa. Partikel ini
melewati kertas saring, tetapi dapat dideteksi dengan hamburan sinar, sedimentasi dan
osmosis.
Nama yang diberikan kepada koloid bergantung pada kedua fasa yang terlibat.
Sol adalah disperse padatan dalam cairan (seperti kumpulan atom panas dalam air)
atau padatan dalam padatan (seperti kaca rubi, yang merupakan sol emas dalam kaca,
dan mendapatkan warnanya karena hamburan). Aerosol merupakam dispersi cairan
dalam gas (seperti kabut) dan padatan dalam gas (seperti asap); partikelnya seringkali
cukup besar untuk dilihat dengan mikroskop. Emulsi merupakan disperi cairan dalalm
cairan (seperti susu).12
11
12
Atkins, P.W. 1996. Kimia Fisik. Jilid 2. Erlangga. Jakarta.
2.3.1.Pembagian Koloid
Berdasarkan cara pembentukannya koloid dibedakan menjadi koloid disperse, koloid
asosiasi dan koloid makromolekul.
1. Koloid Dispersi, yaitu koloid yang terbentuk dari penyebaran (dispersi)
partikel-partikel kecil yang tidak larut dalam medium (fasa pendispersi)
dengan membentuk agregat molekul atau atom yang sangat banyak.
Contohnya: disperse koloid emas (Au) dan Belerang (S)
2. Koloid asosiasi, yaitu kolid yang terbentuk dari gabungan (asosiasi)
molekul-molekul kecil, atom atau ion yang larut dalam medium sehingga membentuk
agregat-agregat molekul yang disebut misel. Contoh: larutan sabun dan
deterjen.
3. Koloid Makromolekul, yaitu koloid yang terbentuk dari molekul tunggal yang sangat besar (makromolekul), contoh: protein dan polimer tinggi sepereti karet
dan plastik.
Partikel-partikel suatu zat senantiasa bergerak. Gerakan tersebut dapat bersifat
acak seperti pada zat cair dan gas, atau hanya bervibrasi di tempat seperti pada zat
padat. Untuk sistem koloid dengan medium pendispersi zat cair atau gas, pergerakan
partikel-partikel akan menghasilkan tumbukan dengan partikel-partikel koloid itu
sendiri. Tumbukan tersebut berlangsung dari segala arah. Oleh karena ukuran partikel
cukup kecil, maka tumbukan yang terjadi cenderung tidak seimbang. Sehingga
terdapat suatu resultan tumbukan yang menyebabkan perubahan arah gerak partikel
sehingga terjadi gerak zigzag atau gerak Brown.
Semakin kecil ukuran partikel koloid, semakin cepat gerak Brown terjadi.
Demikian pula, semakin besar ukuran partikel kolopid, semakin lambat gerak Brown
yang terjadi. Hal ini menjelaskan mengapa gerak Brown sulit diamati dalam larutan
Gerak Brown juga dipengaruhi oleh suhu. Semakin tinggi suhu sistem koloid,
maka semakin besar energi kinetik yang dimiliki partikel-partikel medium
pendispersinya. Akibatnya, gerak Brown dari partikel-partikel fase terdispersinya
semakin cepat. Demikian pula sebaliknya, semakin rendah suhu sistem koloid, maka
gerak Brown semakin lambat
2.4.Kegunaan Koloid pada Bahan Pencuci
Larutan pencuci atau deterjen dapat digunakan untuk membersihkan kotoran
pada pakaian. Fungsi dari zat ini adalah sebagai pengemulsi minyak dalam air. Sabun
akan terionisasi dalam air menjadi Na+ dan anion asam lemak. Bagian ujung lemak yang bermuatan negatip bersifat polar sehingga larut dalam air dan ujung lainnya
bersifat non polar dan cenderung larut dalam minyak. Hal ini menyebabkan kotoran
yang berupa tetesan-tetesan minyak larut dalam air sehingga mudah lepas pada saat
pembilasan.
2.5.Tegangan Permukaan
Permukaan zat cair mempunyai sifat ingin meregang, sehingga permukaannya
seolah-olah ditutupi oleh suatu lapisan yang elastis. Hal ini disebabkan adanya gaya
tarik menarik antara partikel sejenis di dalam zat cair sampai ke permukaan.
Di dalam cairan, tiap molekul ditarik oleh molekul lain yang sejenis di
dekatnya dengan gaya yang sama ke segala arah. Akibatnya tidak terdapat sisa
(resulton) gaya yang bekerja pada masing-masing molekul. Pada permukaan cairan,
tiap molekul ditarik oleh molekul sejenis di dekatnya dengan arah hanya kesamping
dan ke bawah, tetapi tidak ditarik oleh molekul di atasnya karena diatas permukaan
Akibatnya terdapat perbedaan gaya tarik, sehingga ada sisa gaya yang bekerja
pada lapisan atas cairan. Gaya tersebut mengarah ke bawah karena molekul di bawah
permukaan cairan jumlahnya lebih banyak dan jarak antara molekul lebih rapat.
Adanya gaya atau tarikan ke bawah menyebabkan permukaan cairan berkontraksi dan
berada dalam keadaan tegang. Tegangan ini disebut dengan tegangan permukaan.
Adanya tegangan permukaan menyebabkan permukaan cairan sepereti ditutupi
oleh hamaparan selaput yang elastis, sehingga mampu menahan suatu benda untuk
terapung. Selain itu, akibat adanya tegangan permukaan zat cair selalu berusaha untuk
menyusut atau mendapatkan luas permukaan terkecil karena bentuk ini dianggap
mempunyai energi yang paling rendah (paling stabil). Bentuk yang paling memenuhi
keadaan ini adalah bujur telur(sferik). Sifat cenderung untuk memperkecil luas
permukaan inilah yang menyebabkan tetesan-tetesan cairan berbentuk bulat
Fenomena lain yang berhubungan dengan tegangan permukaan adalah
terbentuknya meniscus apabila cairan dimasukkan ke dalam tabung reaksi. Air yang
membasahi dinding kapiler dan akan naik sehingga lebih tinggi daripada permukaan
air sekitarnya, spons yang dapat menyerap air ataupun air yang dapat meresap ke
dalam tanah merupakan beberapa contoh yang menunjukkan bahwa tegangan
permukaan itu memang ada.13
Tegangan permukkan (γ) suatu cairan dapat didefinisikan sebagai banyaknya kerja yang dibutuhkan untuk memperluas permukaan cairan sebanyak satu satuan
luas. Pada satuan cgs, γ dinyatakan dalam erg cm-2 atau dyne cm-1. Dalam satuan SI, γ dinyatakan dalam N m-1. Kedua besaran tadi saling berhubungan berdasarkan hubungan 1 dyne cm-1 = 10-3 N m-1. 14
13
Yazid. E. 2005. Kimia Fisika Untuk Paramedis. Penerbit Andi Offset. Yogyakarta.
14
2.5.1.Faktor-faktor yang Mempengaruhi Tegangan Permukaan
Tegangan permukaan cairan γ, berbeda-beda bergantung pada jenis cairan dan suhu. Pada umumnya cairan yang memiliki gaya tarik antara molekulnya besar seperti
air, maka tegangan permukaannya juga besar. Sebaliknya pada cairan seperti bensin
karena gaya tarik antara molekulnya kecil, maka tegangan permukaannya juga kecil.
Perubahan pada temperatur menyebabkan suatu perubahan dalam tegangan
permukaan suatu cairan. Ketika temperature dinaikkan, ada peningkatan energi kinetic
dari molekul cairan (KE∞T) dimana molekul-molekul cairan bergerak lebih cepat dan pengaruh interaksi antara molekul berkurang sehingga tegangan permukaannya
menurun atau adanya penurunan gaya intermolecular. Ini menghasilkan penurunan
pada fungsi tekanan kedalam pada permukaan dari cairan. Dengan kata lain tegangan
permukaan menurun dengang meningkatnya temperatur.15
Adanya zat terlarut pada cairan dapat menaikkan atau menurunkan tegangan
permukaan tergantung sifat zat teralarutnya. Zat terlarut dengan susunan kimia sama
hampir tidak berpengaruh. Untuk air adanya elektrolit anorganik dan non elektrolit
tertentu seperti sukrosa dan gliserin menaikkan tegangan permukaan. Sedangkan
adanya zat-zat sepereti sabun, detergen dan alcohol adalah efektif dalam menurunkan
tegangan permukaan atau tegangan antara muka. Zat ini sering disebut dengan surface
active agents atau surfaktan.
Penurunan tegangan permukaan oleh sabun menyebabkan perlusan film air
dengan pembentukan gelembung atau busa. Ada hubungan antara besar kecilnya
tegangan permukaan cairan dengan kemampuannya untuk membasahi benda. Makin
kecil nilai γ suatu cairan, makin besar kemampuan cairan tersebut membasahi benda.
.
15
Bahl, B.S., 1994. Essentials of Physical Chemistry. S.Chand & Company LTD.
Hubungan ini banyak dimanfaatkan dalam kehidupan sehari-hari; misalanya unutk
menghasilkan cucian pakaian agar lebihi bersih dapat digunakan air panas atau air
sabun. Keduanya dapat menurunkan γ air,sehingga meningkatkan kemampuapn air membasahi kotoran pakaaian. Akibatnya kotoran mudah larut dan terbawa oleh air
pada saat pembilasan. Alcohol dan antiseptic yang dipakai mengobati luka selain
memiliki daya bunuh kuman yang baik juga memiliki γ yang rendah, sehingga dapat membasahi seluruh permukaan luka.16
2.5.2.Pengukuran Tegangan Permukaan 2.5.2.1.Metode Kenaikan Pipa Kapiler
Tegangan permukaan yang dapat diukur selain antara permukaan cairan dan
gas, juga tegangan permukaan antara suatu cairan dengan cairan lain.
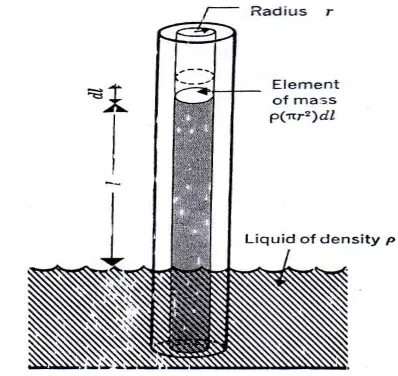
Cara yang paling sederhana dan mudah adalah dengan menggunkan metode
kapiler. Pada metoda ini, sebuah tabung kapiler yang bersih dengan jari-jari
diamasukkan ke dalam cairan yang akan diukur tegangan permukaannya. Permukaan
cairan akan naik sampai gaya gravitasi sama dengan gaya ke atas yang disebabkan
tegangan permukaan.17
Pada gambar 2.4 ditunjukkan suatu pipa kapiler kaca dimasukkan kedalam suatu
wadah berisi air yang akan ditentukan. Semua cairan yang membasahai gelas akan
naik ke dalam pipa, dan inilah kenaikan pipa kapiler yang dapat digunakan untuk
menentukan tegangan permukaaan.
16
Yazid, E, Op Cit. 17
Gambar2.3. Proses Kenaikan Cairan pada Pipa Kapiler
Kenaikan cairan dapat dimengerti jika ini diasumsikan bahwa film tipis
diadsorbsi dari cairan yang ada dalam dinding kapiler. Supanya mengurangi total area
permukaan, cairan manaiki pipa. Kesetimbangan dicapai ketika energi bebas pada
keadaan minimum, dengan kata lain kenaikan dapat mengeluarkan energy bebas yang
berlebih ke dalam kerja yang tersusun pada kolom cairan yang disimpan dengan
penurunan tegangan permukaan.
Penurunan pada area permukaan yang dihasilkan dari kenaikan cairan dengan suatu
jumlah dl adalah 2πr dl, dan hubungan penurunan dalam energy permukaan adalah:
dGenergy permukaan = γ d A
= γ (2 π r ) dl
Pengeluaran energy bebas dalam kenaikan suatu jumlah cairan dengan volume π r2 dl dan densitas ρ terhadap tinggi l adalah:
dGgravitasi = (π r2 dl ρ) gl
ketika kolom cairan telah dinaiki pada kapiler hingga mencapai tinggi yang
γ (2πr) dl = πr2 dl ρgl
dan: γ =
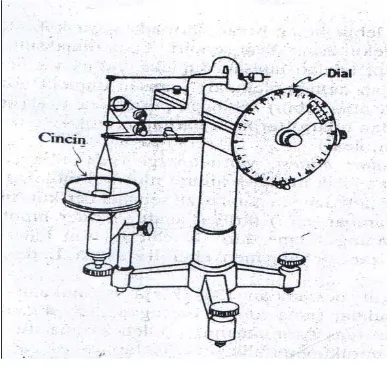
2.5.2.2.Metode Cincin du NuOy
Prinsip dari Metode cincin du Nouy bergantung pada kenyataan bahwa gaya yang
diperlukan untuk melepaskan suatu cincin platina-iridium yang dicelupkan pada
permukaan adalah sebanding dengan tegangan permukaan atau tegangan antarmuka.
Gaya yang diperlukan untuk melepaskan cincin dengan cara ini diberikan oleh suatu
[image:31.595.219.414.341.528.2]kawat spiral dan dicatat dalam suatu dyne pada suatu penunjuk yang dikalibrasi. 19
Gambar 2.4. Tensiometer Du Nuoy
cincin keliling x
dyne dalam dial pembacaan
2
x faktor koreksi
18
Borrow, G.M., 1961. Physical Chemistry. Mc Graw Hill Book Company,Inc. New
York.
19
Martin,A., (1993), Farmasi Fisik, Penerbit Universitas Indonesia, Jakarta
Pertama tekanan dikenakan, jari-jari gelembung sangat besar, sementara
gelembung itu mengembang, jari-jarinya akan semakin kecil sampai mencapai nilai
minimum. Pada keadaan ini jari-jari gelembung sama dengan jari-jari tabung gelas.
Bila tekanan terus dinaikkan, jari-jari gelembung akan membesar kembali sampai
akhirnya gelembung itu lepas dari tabung gelas dan naik ke permukaan cairan.
Tekanan maksimum diperoleh pada saat jari-jari minimum.
Tekanan maksimum ini bukan hanya disebabkan perbedaan tekanan pada
kedua sisi gelembung, tetapi juga disebabkan oleh karena adanya tekanan hidrostatik
(yang bergantung pada ketinggian tabung gelas dalam cairan). Jadi tekanan
maksimum yang terbaca pada manometer:
ΔPmaks = + g h (ρ – ρ0)
Dimana: r : jari-jari tabung
h: jarak ujung tabung gelas dari permukaan cawan
ρ: densitas larutan
ρ0: densitas uap cairan (biasanya diabaikan karena ρ0 << ρ)
20
Danill, F., 1956. Experimental Physical Chemistry. Sixth Edition. McGraw Hill
Book Company,Inc.
BAB 3
BAHAN DAN METODE PENELITIAN
Dalam penelitian ini adapun bahan dan alat-alat yang digunakan adalah sebagai
berikut:
3.1 Bahan – bahan
- Natrium Lauril Eter Sulfat (SLES)
- Natrium Lauril Sulfat (SLS)
- Natrium Klorida (NaCl)
- Etilena Diamina Tetra Acetat (EDTA)
- Zat pewarna kuning sintetik
- Parfum Lemon
- Aquades
3.2 Alat – alat
- Tensiometer Kapiler Fisher
- Piknometer 5 mL (presisi ±0,01 mL) Iwaki
- Gelas ukur
10 mL (presisi ±0,02 mL) Pyrex
- Gelas ukur
100 mL (presisi ±0,05 mL) Pyrex
- Gelas
Beaker 1000 mL (presisi ±0,8 mL) Pyrex
- Gelas
Beaker 250 mL (presisi ±0,2 mL) Pyrex
- Neraca
- Pipet
Volume 10 mL (presisi ±0,02 mL) Pyrex
- Pengaduk (Magnetic Stirer) Fisher
- Botol Aquades
- Thermometer
- Thermostat
3.3. Metode Penelitian 3.3.1. Populasi
Dalam penelitian eksperimen ini yang digunakan sebagai populasi sasaran adalah
bahan pencuci tangan.
3.3.2. Sampling
Berdasarkan sifat kehomogenan dari populasi, maka teknik sampling yang digunakan
adalah teknik rancangan acak lengkap kelompok, dengan dua variabel berubah yaitu
konsentrasi NaCl dan suhu larutan pancuci tangan yang masing-masing variabel
terdiri dari tiga variasi (disain percobaan 2x3) dimana replikasi dilakukan tiga kali
untuk setiap perlakuan dari masing-masing sampel dan eksperimen dilakukan secara
acak dan randomisasi.
3.3.3. Persiapan
3.3.3.1. Pencucian Alat
Larutan pencuci dibuat dari 2,0 g Kalium Bikromat yang dilarutkan dengan 5 ml
aquadest, dipanaskan hingga semua garam larut, kemudian didinginkan. Lalu
ditambahkan 60 ml asam sulfat pekat secara perlahan-lahan sambil diaduk. Alat-alat
kaca diisi dengan larutan tersebut dan dibiarkan selama 15 menit. Kemudian larutan
dikeluarkan dan alat kaca dibilas dengan aquadest paling sedikit 4 kali. Lalu
perhatikan apakah air mengalir tanpa meninggalkan tetesan pada dinding, jika tidak
pembersihan harus diulang.
Alat-alat kaca volumetrik dikalibrasi dengan menghitung berat larutan (biasanya
akuades) yang diisi dalam alat volumetric yang telah diketahui densitas dan
temperaturnya. Data penimbangan terlebih dahulu dikoreksi dengan persamaan:
W1 = W2 + W2
Dimana: W1 = berat sesungguhnya
W2 = berat dari pengukuran
Lalu volume alat pada temperature kalibrasi (T) ditentukan dengan mengalikan
densitas larutan dengan berat yang dikoreksi. Sehingga volume ini dikoreksi terhadap
temperatur standar 200C.
3.3.3.3. Kalibrasi Piknometer
Piknometer kosong dibersihkan dan ditimbang, masanya adalah m0, diisi piknometer
dengan air yang baru didestilasi dan bebas dari udara, dibiarkan piknometer selama 1
jam di dalam oven atau thermostat yang diatur pada temperature antara 50C dari temperature yang akan ditentukan (secara normal 20, 40, atau 600C), disesuaikan level air pada tabel densitas air yang telah ditentukan, dicatat temperature t2 dari yang
ditentukan, yang mendekati 0,10C, ditimbang dan dicatat total massanya sebagai m2.
Volume Vt dari piknometer adalah sebagai berikut:
Dimana: mo adalah massa piknometer kosong (g)
m2 adalah massa piknometer kosong yang telah terisi air (g)
adalah densitas air pada t20C
3.3.3.4. Pembuatan Larutan
3.3.3.4.1. Pembuatan Larutan Natrium Klorida 10%
NaCl ditimbang sebanyak 33,3 g, dimasukkan ke dalam beaker glass 1 L dan
ditambahkan aquades 300 g lalu diaduk hingga homogen.
3.3.3.4.2. Pembuatan Larutan Natrium Klorida 20%
NaCl ditimbang sebanyak 75 g, dimasukkan ke dalam beaker glass 1 L dan
ditambahkan aquades 300 g lalu diaduk hingga homogen.
3.3.3.4.3. Pembuatan Larutan Natrium Klorida 30%
NaCl ditimbang sebanyak 128,57 g, dimasukkan ke dalam beaker glass 1 L dan
ditambahkan aquades 300 g lalu diaduk hingga homogen.
3.3.3.4.4. Pembuatan Larutan SLES 33,3 %
Sodium Lauril Eter Sulfat ditimbang sebanyak 500 g, dimasukkan ke dalam ember 10
L ditambahkan aquades sebanyak 1000 g, kemudian diaduk sampai homogen.
3.3.3.4.5. Pembuatan Larutan SLS 33,3 %
Sodium Lauril Sulfat ditimbang sebanyak 500 g, dimasukkan ke dalam ember 10 L
ditambahkan aquades sebanyak 1000 g, kemudiam diaduk sampai homogen.
3.3.3.4.6. Prosedur Pembuatan Bahan Pencuci Tangan (1 L)
Ke dalam beaker glass 1000 mL, dimasukkan 150 mL larutan Sodium Lauril Eter
Sulfat. Ditambahkan 20 mL sodium lauril sulfat sambil diaduk hingga larutan
homogen. Kedalam larutan homogen ditambahkan 50 mL larutan NaCl 10% dan
diaduk hingga homogen. Ditambahkan 1 ml parfum Lemon dan 2 g zat pewarna
kuning sintetik sambil diaduk. Ditambahkan Etilena Diamina Tetra Acetat sebanyak 2
g dan diaduk hingga homogen dengan kecepatan pengadukan 2000rpm ditambahkan
aquades hingga menunjukkan volume larutan 500 mL sambil diaduk hingga larutan
sama dilakukan pembuatan bahan pencuci tangan untuk variasi konsentrasi NaCl 20%
dan 30%
3.3.4. Pengumpulan data 3.3.4.1. Penentuan Densitas
1. Piknometer 5 mL (kosong) ditimbang pada neraca analitik dan dicatat
massanya
2. Larutan pencuci tangan di pipet 5 mL dan dimasukkan ke dalam piknometer
3. Piknometer berisi ditimbang pada neraca analitik dan dicatat massanya.
4. Perlakuan yang sama dilakukan sebanyak 3 kali
5. Densitasnya dihitung
6. Dilakukan percobaan yang sama dengan larutan pencuci tangan dengan variasi
konsentrasi NaCl 10%, 20% dan 30%
Nilai Densitas dihitung berdasarkan persamaan berikut :
d =
dimana : d = densitas larutan (g/mL)
M = massa (g)
V = volume (mL)
3.3.4.2. Penentuan Tegangan Permukaan a. Pengaruh Suhu
1. Larutan pencuci tangan dipanaskan dalam thermostat sampai suhu 300C 2. Larutan pencuci tangan dipipet sebanyak 10 ml dan dimasukkan ke dalam
tensiometer kapiler
3. Larutan pencuci tangan dihisap perlahan-lahan dan dibiarkan turun sampai
setimbang
5. Perlakuan yang sama dilakukan sebanyak 3 kali
6. Tegangan permukaannya dihitung
7. Dilakukan percobaan yang sama dengan dengan variasi suhu 400C, 500C
b. Pengaruh Konsentrasi NaCl
1. Larutan pencuci tangan dengan konsentrasi NaCl 10% dipipet sebanyak 10
ml dan dimasukkan ke dalam tensiometer kapiler
2. Larutan pencuci tangan dihisap perlahan-lahan dan dibiarkan turun sampai
setimbang
3. Tinggi larutan pencuci tangan dalam kapiler kaca dicatat
4. Perlakuan yang sama dilakukan sebanyak 3 kali
5. Tegangan permukaannya dihitung
6. Dilakukan percobaan yang sama terhadap larutan pencuci tangan dengan
konsentrasi NaCl 20%, 30%.
Tegangan Permukaan dapat dihitung berdasarkan persamaan berikut:
γ
=
dimana : d = densitas
g = gravitasi
h = tinggi larutan dalam kapiler kaca
r = jari-jari kapiler
3.4. Pengolahan Data 3.4.1. Penentuan Kesalahan
a. Kesalahan instrument, yaitu bersumber dari alat atau instrumentnya sendiri,
misalnya penyimpangan nol dalam pembacaan skala. Kesalahan ini dapat
diminimalkan dengan cara kalibrasi atau penggunaan blangko.
b. Kesalahan metode, dalam penelitian ini metode yang digunakan adalah metode
kenaikan pipa kapiler.
c. Kesalahan personal, yaitu kesalahan yang dilakukan seorang peneliti ataupun
karena kesalahan prosedur. Kesalahan ini dapat diminimalkan dengan
maningkatkan ketelitian dan kedisplinan peneliti.
3.4.1.2. Kesalahan Random (Intermediate)
Tipe kesalahan ini disebabkan oleh banyaknya variabel bebas dan pengulangan dalam
setiap pengukuran kimia dan fisika. Kesalahan terjadi ketika sebuah sistem
pengukuran diteruskan hingga kesensifitas maksimumnya. Terdapat banyak
kontributor kesalahan random, namun tidak ada yang dapat diidentifikasi dan di hitung
karena sangat kecil dan tidak dapat di deteksi tersendiri. Kesalahan ini dapat di lihat
dari rata-rata yang merefleksikan ketelitian.
3.4.1.3. Kesalahan Gabungan dari Kesalahan Random
Kebanyakan hasil akhir dalam kimia fisika dihasilkan dari perhitungan
pengukuran-pengukuran yang digabungkan. Hal ini penting untuk memastikan bagaimana
kesalahan pengukuran individual mempengaruhi hasil akhir.
3.4.2. Penentuan ketidakpastian dalam significant figure
Data yang diperoleh ditentukan nilai ketidakpastiannya berdasarkan sumber- sumber
ketidakpastian. Baik pada saat menimbang, pengukuran volume maupun penggunaan
alat untuk setiap penentuan dalam penelitian ini. Kemudian data yang diperoleh
dianalisa secara statistik dengan analisis varians (ANAVA) dan grafik dengan tingkat
signifikansi 5 % untuk menerima atau menolak hipotesa yang diajukan.
3.4.2.1. Perhitungan ketidakpastian persentase NaCl
Parameter yang di ukur adalah persentaselarutan NaClyang tergantung pada berat
Massa ( m NaCl )
Sertifikat kalibrasi timbangan tercantum ± 0,15 mg untuk linieritas. Produsen
timbangan merekomendasikan untuk menggunakan distribusi rektangular untuk
mendapatkan kontribusi linier deviasi standar.
3 15 , 0
= 0,087 mg
u(m NaCl) =
2
087 , 0
2x = 0,123 mg
Kemurnian NaCl
PNaCl = 98% = 100% ± 2,00%
= 1,0 ± 0,02
u(PNaCl) =
3 02 , 0
= 0,0115
Massa Molar Natrium Klorida (MNaCl )
Dari tabel IUPAC, berat atom dan daftar ketidakpastian untuk unsur-unsur
pembentukan natrium klorida adalah atom Na dan Cl.
U(MNaCl) =
2 2
Cl
Na s
s
3.4.2.2. Perhitungan Ketidakpastian Pipet volume 10 mL (VT1)
Ketidakpastian pipet volume 10 mL dengan presisi ± 0,02 mL dapat di hitung dari
penggabungan dua pengaruh utama terhadap volume, yaitu : kalibrasi dan
pengaruh suhu.
a. Kalibrasi
u(V10_cal) =
6 02 , 0
= 0,0081 mL
b. Perbedaan suhu laboratorium dengan suhu kalibrasi
Suhu yang tertera pada alat gelas volumetri adalah 200C, sedangkan suhu laboratorium bervariasi antara ± 100C. Ketidakpastian dapat di hitung dari perbedaan suhu dengan koefisien pemuaian volume air (γ = 2,1 x 10-40C), dan koefisien rektangular di mana akan memberikan
± V x ∆t x γ
± 10 x 10 x 2,1 x 10-4 = 0,021 mL
u(V10_temp) =
3 021 , 0
= 0,0121 mL
ketidakpastian gabungan pipet volume 10 mL
u(V10) =
2 _ 10 2_
10 cal uV temp
V
u
= 0,0146 mL
3.4.2.3. Perhitungan Ketidakpastian gelas ukur 10 mL
a. Kalibrasi
u(V10_cal) = 6 05 , 0
b. Perbedaan suhu laboratorium dengan suhu kalibrasi
± V x ∆t x γ
± 10 x 10 x 2,1 x 10-4 = 0,021 mL
u(V10_temp) = 3 021 , 0
= 0,0121 mL
c. Perulangan
u(V50_rep) = 3 05 , 0
= 0,02886 mL
ketidakpastian gabungan gelas ukur 50 ml
u(V50) =
2 _ 50 2 _ 50 2 _50 cal uV temp uV rep
V
u
= 0,03768 mL
3.4.2.4. Perhitungan Ketidakpastian gelas ukur 100 mL
a. Kalibrasi
u(V100_cal) =
6 5 , 0
= 0,2041 mL
b. Perbedaan suhu laboratorium dengan suhu kalibrasi
± V x ∆t x γ
± 50 x 10 x 2,1 x 10-4 = 0,105 mL
u(V50_temp) =
3 105 , 0
c. Perulangan
u(V50_rep) =
3 5 , 0
= 0,2886 mL
ketidakpastian gabungan gelas ukur 50 ml
u(V50) =
2 _ 50 2 _ 50 2 _50 cal uV temp uV rep
V
u
= 0,3587 mL
3.5. Analisis Data 3.5.1. Analisis Variansi
Dalam menguji hipotesa yang telah diajukan maka di pakai rancangan acak kelompok
sederhana. Dalam rancangan ini tidak terdapat lokal kontrol, sehingga sumber
keragaman yang diamati hanya perlakuan yang di ragam sebanyak kelompok.
a. Analisis jumlah kuadrat untuk nilai Tegangan Permukaan
Analisis jumlah kuadrat untuk nilai tegangan permukaan berdasarkan pengaruh
suhu dan konsentrasi NaCl dapat dihitung melalui persamaan di bawah ini, data
untuk menghitung jumlah kuadrat dapat dilihat dari data statistik pada tabel 2 dan 4
pada lampiran:
1. Jumlah kuadrat total (JKT)
JKT = -
2. Jumlah kuadrat antar kelompok (JKA)
JKA = + + -
JKD = JKT – JKA
4. Rata-rata kuadrat antar kelompok (RKA)
RKA =
5. Rata-rata kuadrat dalam kelompok (RKD)
RKD =
FHitung =
Analisis sidik ragam
Derajat Bebas (dB)
dBa = m – 1
dBT = n – 1
dBd = dBT - dBa
Hasil perhitungan dapat dilihat pada tabel hasil analisa sidik ragam yang terlampir
pada tabel 3 dan 5
3.5.2. Analisis Regresi
Analisis Regresi untuk nilai Tegangan Permukaan berdasarkan pengaruh konsentrasi NaCl
Hasil pengukuran nilai tegangan permukaan diplotkan terhadap konsentrasi NaCl.
Persamaan garis regresi diturunkan dengan metode Least Square, dapat di lihat pada
di mana : X = konsentrasi NaCl
Y = nilai tegangan permukaan
Persamaan garis regresi untuk kurva kalibrasi dapat di hitung dari persamaan berikut ;
Y = aX + b
di mana harga a (slope) dan b (intersep) dapat di hitung dari persamaan :
a =
2 2 i i i i i i X X n Y X Y X nHarga intersep (b) diperoleh dengan mensubtitusikan harga slope (a) ke dalam
persamaan :
b =
2 2 2 i i i i i i i X X n Y X X X Ymaka diperoleh harga intersep (b). Hasil perhitungan dapat dilihat pada tabel 7.
Dengan cara dan rumus yang sama dilakukan perhitungan untuk nilai tegangan permukaan
berdasarkan pengaruh suhu. Hasil yang diperoleh dapat dilihat pada tabel 9
3.5.3. Uji Hipotesa
1) Hipotesa Nol 0 A : H10 i
yang berarti bahwa tidak ada pengaruh konsentrasi NaCl terhadap nilai tegangan
permukaan larutan pencuci tangan
yang berarti bahwa tidak ada pengaruh suhu terhadap nilai tegangan permukaan
larutan pencuci tangan
2) Hipotesa Alternatif
0 A : H11 i
yang berarti bahwa ada pengaruh konsentrasi NaCl terhadap nilai tegangan
permukaan larutan pencuci tangan
0 A : H11 i
yang berarti bahwa ada pengaruh suhu terhadap nilai tegangan permukaan larutan
pencuci tangan
Kriteria Pengujian
Pada batas ketangguhan = 5 % pada daerah kritis pengujian berlaku :
H1 0 ; H
2
0 di terima bila FHitung ≤ F0,05 dan di tolak bila FHitung ≥ F0,05
3.6. Skema Pengambilan Data
3.6.1. Skema Pembuatan Larutan Pencuci Tangan
ditambahkan ditambahkan ditambahkan
aquades 1000 g aquades 1000 g aquades 300 g
diaduk hingga homogen diaduk hingga diaduk hingga
homogen homogen
dimasukkan 150 mL larutan sodium
lauril eter sulfonat ke dalam beaker
gelas 1000 mL
ditambahkan 20 mL larutan sodium
lauril sulfonat sambil diaduk
ditambahkan 50 mL larutan NaCl
dengan variasi konsentrasi 10%, 20%,
30%, sambil diaduk hingga homogen
ditambahkan 2 mL parfum Lemon dan
2 g zat pewarna kuning sintetik sambil
diaduk
Ditambahkan EDTA sebanyak 2 g dan
diaduk hingga homogen dengan
kecepatan pengadukan 2000rpm sambil
ditambahkan aquadest hingga volume Sodium Lauril Eter
Sulfonat 500 g
Natriun Klorida 33,3 g Sodium Lauril Sulfonat
500 g
Larutan Sodium Lauril Eter Sulfonat
Larutan Sodium Lauril Sulfonat
larutan 500 mL
didiamkan larutan selama 24 jam
3.6.2. Skema Penentuan Densitas Larutan Pencuci Tangan
Ditimbang sebagai M(piknometer kosong), dan
dicatat massanya
Dipipet 5 mL Larutan Pencuci Tangan
hingga penuh dan ditutup
Ditimbang sebagai M(piknometer berisi), dan
dicatat massanya.
Perlakuan diulangi sebanyak 3 kali
Dihitung nilai densitas larutan pencuci tangan Larutan Pencuci
Tangan
Piknometer Kosong (5 mL)
Data Massa
3.6.3. Skema Penentuan Tegangan Permukaan Larutan Pencuci Tangan a. Pengaruh Suhu
dipanaskan larutan pencuci tangan di dalam
thermostat sampai suhu 300C
diukur 10 mL, dimasukkan kedalam
tensiometer kapiler
dihisap larutan pencuci tangan perlahan-lahan dan
dibiarkan turun sampai setimbang
dicatat tinggi larutan pencuci tangan dalam kapiler
kaca
perlakuan diulangi sebanyak 3 kali
dihitung nilai tegangan permukaan larutan pencuci
tangan
Dilakukan percobaan yang sama untuk suhu 400 C dan 500 C Larutan Pencuci
Tangan
Data Tinggi Larutan
b. Pengaruh Konsentrasi NaCl
diukur 10 mL, dimasukkan kedalam
tensiometer kapiler
dihisap larutan pencuci tangan perlahan-lahan dan
dibiarkan turun sampai setimbang
dicatat tinggi larutan pencuci tangan dalam kapiler
kaca
perlakuan diulangi sebanyak 3 kali
Dilakukan perlakuan yang sama terhadap larutan pencuci tangan dengan
konsentrasi NaCl 20% dan 30% Larutan Pencuci Tangan
dengan Konsentrasi NaCl 10%
BAB 4
HASIL DAN PEMBAHASAN
4.1. Hasil
Dari hasil penelitian yang telah dilakukan, diperoleh hasil bahwa pengaruh
konsentrasi NaCl sebagai zat pengental dan pengaruh suhu larutan pencuci tangan
memberikan pengaruh yang sangat nyata terhadap perubahan tegangan permukaan
larutan pencuci tangan.
Dari hasil perhitungan yang dilakukan diperoleh data bahwa nilai tegangan
permukaan larutan pencuci tangan semakin menurun dengan bertambah besarnya
konsentrasi NaCl yang terkandung dalam larutan pencuci tangan, hal ini dapat dilihat
[image:51.595.102.530.616.743.2]tabel 4.1:
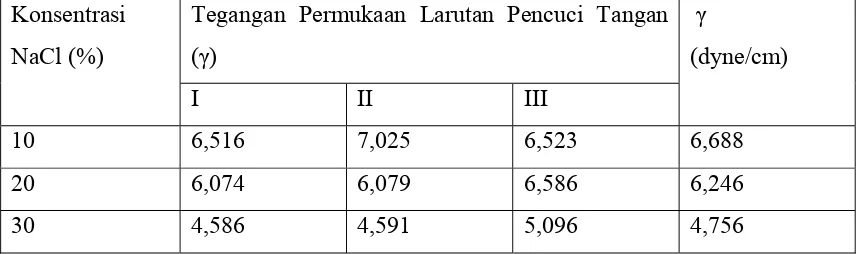
Tabel 4.1. Data Hasil Perhitungan Nilai Tegangan Permukaan Berdasarkan Variasi Konsentrasi NaCl
Konsentrasi
NaCl (%)
Tegangan Permukaan Larutan Pencuci Tangan
(γ)
γ
(dyne/cm)
I II III
10 6,516 7,025 6,523 6,688
20 6,074 6,079 6,586 6,246
Dari hasil perhitungan yang dilakukan diperoleh data bahwa nilai tegangan
permukaan larutan pencuci tangan semakin menurun dengan meningkatnya suhu
[image:52.595.107.531.313.421.2]larutan pencuci tangan, hal ini dapat dilihat dalam tabel 4.2:
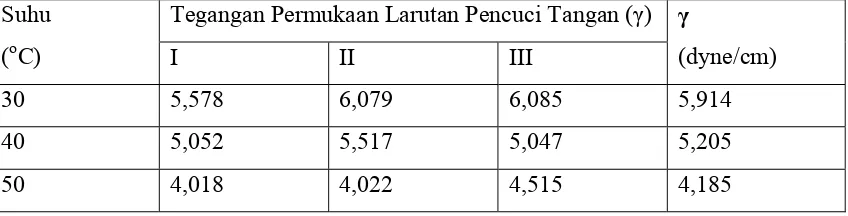
Tabel 4.2. Data Hasil Perhitungan Nilai Tegangan Permukaan Berdasarkan Variasi Suhu
Suhu
(oC)
Tegangan Permukaan Larutan Pencuci Tangan (γ) γ
(dyne/cm) I II III
30 5,578 6,079 6,085 5,914
40 5,052 5,517 5,047 5,205
50 4,018 4,022 4,515 4,185
Contoh perhitungan nilai tegangan permukaan:
Nilai tegangan permukaan untuk pengaruh konsentrasi NaCl 10%, perlakuan I:
Diketahui: d = 1,023 g/cm3 h = 1,3 cm
g = 9,8 m/s2 r = 0,01 cm
Nilai tegangan permukaan dapat dihitung berdasarkan persamaan berikut:
γ
=
=
4.2. Pembahasan 4.2.1. Hipotesa Satu
Diperoleh harga FHitung lebih besar dari pada harga FTabel, maka H11 diterima
dan H10 ditolak, yang berarti ada pengaruh konsentrasi NaCl terhadap nilai tegangan
permukaan larutan pencuci tangan. Bertambah besarnya konsentrasi NaCl sebagai zat
pengental, memberikan pengaruh yang sangat nyata terhadap tegangan permukaan
[image:53.595.110.473.319.537.2]larutan pencuci tangan, seperti yang ditunjukkan pada gambar 4.1:
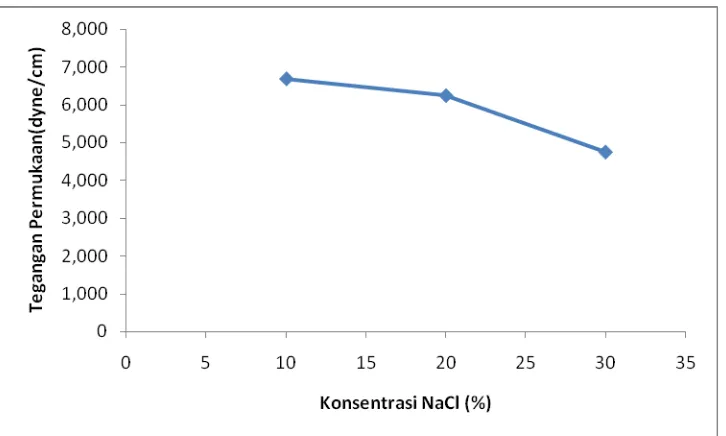
Gambar 4.1. Grafik Pengaruh Konsentrasi NaCl Terhadap Nilai Tegangan
Permukaan Larutan Pencuci Tangan
Dari grafik dapat dijelaskan bahwa nilai tegangan permukaan larutan pencuci tangan
semakin menurun dengan bertambah besarnya konsentrasi NaCl yang terkandung
dalam larutan pencuci tangan. Hal ini dapat dijelaskan bahwa semakin besar
konsentrasi NaCl dalam larutan pencuci tangan, maka jumlah molekul yang larut
semakin banyak sehingga nilai tegangan permukaan dari larutan pencuci tangan
4.2.2. Hipotesa Dua
Diperoleh harga FHitung lebih besar dari pada harga FTabel, maka H12 diterima
dan H20 ditolak, yang berarti adanya pengaruh suhu larutan pencuci tangan terhadap
nilai tegangan permukaan larutan pencuci tangan. Semakin meningkatnya suhu
larutan pencuci tangan tersebut, memberikan pengaruh yang sangat nyata terhadap
[image:54.595.108.490.319.568.2]tegangan permukaan larutan pencuci tangan, hal ini dapat dilihat pada gambar 4.2:
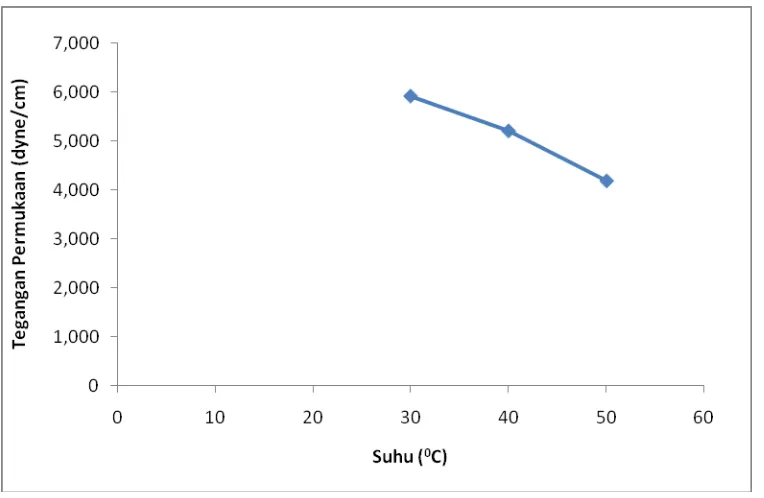
Gambar 4.2. Grafik Pengaruh Suhu Terhadap Nilai Tegangan Permukaan Larutan
Pencuci Tangan
Dari grafik dapat dijelaskan bahwa nilai tegangan permukaan larutan pencuci
tangan semakin menurun dengan bertambah besarnya suhu larutan pencuci tangan.
Hal ini dapat dijelaskan dimana perubahan pada temperatur menyebabkan suatu
perubahan dalam tegangan permukaan suatu cairan. Partikel-partikel suatu zat
atau hanya bervibrasi di tempat seperti pada zat padat. Untuk sistem koloid dengan
medium pendispersi zat cair atau gas, pergerakan partikel-partikel akan menghasilkan
tumbukan dengan partikel-partikel koloid itu sendiri. Tumbukan tersebut berlangsung
dari segala arah. Oleh karena ukuran partikel cukup kecil, maka tumbukan yang
terjadi cenderung tidak seimbang. Sehingga terdapat suatu resultan tumbukan yang
menyebabkan perubahan arah gerak partikel sehingga terjadi gerak zigzag atau gerak
Brown.
Gerak Brown dipengaruhi oleh suhu. Semakin tinggi suhu sistem koloid, maka
semakin besar energi kinetik yang dimiliki partikel-partikel medium pendispersinya.
Akibatnya, gerak Brown dari partikel-partikel fase terdispersinya semakin cepat.
Demikian pula sebaliknya, semakin rendah suhu sistem koloid, maka gerak Brown
semakin lambat. Sehingga ketika temperatur larutan pencuci tangan dinaikkan, ada
peningkatan energi kinetik dari molekul cairan dimana molekul-molekul cairan
bergerak lebih cepat (KE∞T), dan adanya penurunan gaya intermolekular atau pengaruh interaksi antara molekul berkurang sehingga tegangan permukaannya
menurun. Ini menghasilkan penurunan pada fungsi tekanan kedalam pada permukaan
dari cairan. Dengan kata lain tegangan permukaan menurun dengan meningkatnya
BAB 5
KESIMPULAN DAN SARAN
5.1. Kesimpulan
Dari hasil penelitian yang diperoleh dapat diambil kesimpulan sebagai berikut:
1. Semakin besar konsentrasi NaCl yang terkandung dalam larutan pencuci
tangan maka nilai tegangan permukaan larutan pencuci tangan tersebut
semakin menurun, dan semakin kecil konsentrasi NaCl yang terkandung dalam
larutan pencuci tangan maka nilai tegangan permukaan larutan pencuci tangan
semakin besar.
2. Semakin meningkatnya suhu larutan pencuci tangan maka nilai tegangan
permukaan larutan pencuci tangan tersebut semakin menurun, dan semakin
kecil suhu larutan pencuci tangan maka nilai tegangan permukaan larutan
pencuci tangan semakin besar.
5.2. Saran
Diharapkan kepada peneliti selanjutnya untuk melakukan penelitian terhadap
larutan pencuci tangan yang mengandung surfaktan anionik maupun kationik . Serta
melakukan penelitian tentang pengaruh volume dan tekanan terhadap tegangan
DAFTAR PUSTAKA
Atkins, P.W., 1996. Kimia Fisik. Jilid 2. Erlangga. Jakarta.
Bahl, B.S., 1994. Essentials of Physical Chemistry. S.Chand & Company LTD. New Delhi
Bailey, S.P., 1985. Organic Chemistry. Third edition. Polytechnic State University. California
Bird, T., 1985. Kimia Fisik Untuk Universitas. P.T. Gramedia. Jakarta.
Borrow, G.M., 1961. Physical Chemistry. Mc Graw Hill Book Company,Inc. New York.
Danill, F., 1956. Experimental Physical Chemistry. Sixth Edition. McGraw Hill Book Company,Inc. New York
Dogra, S. K., 1990. Kimia Fisik dan Soal-Soal. Cetakan Pertama. UI-Press. Jakarta.
Hart, H., 1991. Organic Chemistry A Short Course. Eight edition. Houghton Mifflin Company. Boston
http:// wordpress.com/2010/08/28/surfaktant-deterjen-sabun-revisi/ Diakses tanggal
6 Desember 2010
http://www.chem-is-try.org/materi_kimia/definisi-detergen/. Diakses tanggal 15 Februari 2011
Martin,A., (1993), Farmasi Fisik, Penerbit Universitas Indonesia, Jakarta
Matta, M.S., 1986. General, Organic & Biological Chemistry. Cuming Publishing
Company, Inc.California
Myers, D., 2006. Surfactant Science and Technology. New Jersey : Jhon Wiley and Son, Inc.New York.
Rangkuti, S.E., 2010. Pengaruh Penambahan NaCl terhadap Perubahan Viskositas Bahan Pencuci Tangan Cair. Skripsi FMIPA USU. Medan
San Luis Obispo.
Schwartz, A.M., 1958. Surface Aktive Agents and Detergents. Interscience Publisher, Inc. New York
Lampiran 1
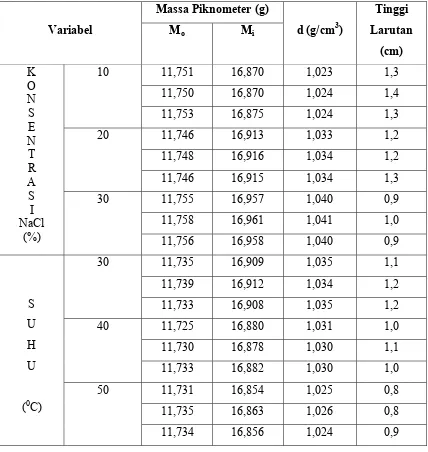
Tabel 1. Data Hasil Pengukuran Densitas Larutan Pencuci Tangan dengan Variasi Konsentrasi NaCl dan Suhu Larutan Pencuci Tangan
Variabel
Massa Piknometer (g)
d (g/cm3)
Tinggi Larutan
(cm)
Mo Mi
K O N S E N T R A S I NaCl (%)
10 11,751 16,870 1,023 1,3
11,750 16,870 1,024 1,4
11,753 16,875 1,024 1,3
20 11,746 16,913 1,033 1,2
11,748 16,916 1,034 1,2
11,746 16,915 1,034 1,3
30 11,755 16,957 1,040 0,9
11,758 16,961 1,041 1,0
11,756 16,958 1,040 0,9
S
U
H
U
(0C)
30 11,735 16,909 1,035 1,1
11,739 16,912 1,034 1,2
11,733 16,908 1,035 1,2
40 11,725 16,880 1,031 1,0
11,730 16,878 1,030 1,1
11,733 16,882 1,030 1,0
50 11,731 16,854 1,025 0,8
11,735 16,863 1,026 0,8
Lampiran 2
Tabel 2. Data Statistik Nilai Tegangan Permukaan Berdasarkan Variasi Konsentrasi NaCl
No 10% 20% 30% Total
1 6,516 6,074 6,523
2 7,025 6,079 6,586
3 6,523 4,586 5,096
ΣXT 20,064 18,739 14,273 53,076
ΣXT2 134,358 117,222 68,077 319,657
Nk 3 3 3 9 (NT)
Tabel 3. Hasil Analisis Sidik Ragam Efek Konsentrasi NaCl Terhadap Nilai Tegangan Permukaan Larutan Pencuci Tangan
Sumber Keragaman
Derajat Bebas
Jumlah Kuadrat
Rata-rata
Kuadrat FHitung
FTabel
(5 %)
Antar kelompok Dalam kelompok
2 6
6,138
0,513 3,069 0,0855
35,895
- 5,14
-
[image:60.595.106.544.452.622.2]Lampiran 3
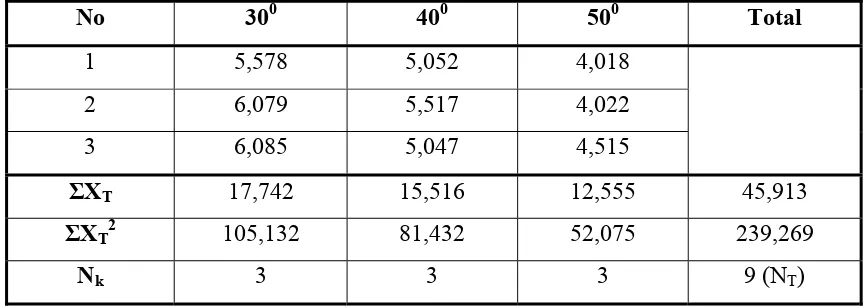
Tabel 4. Data Statistik Nilai Tegangan Permukaan Berdasarkan Variasi Suhu
No 300 400 500 Total
1 5,578 5,052 4,018
2 6,079 5,517 4,022
3 6,085 5,047 4,515
ΣXT 17,742 15,516 12,555 45,913
ΣXT2 105,132 81,432 52,075 239,269
Nk 3 3 3 9 (NT)
Tabel 5. Hasil Analisis Sidik Ragam Efek Suhu Terhadap Nilai Tegangan Permukaan Larutan Pencuci Tangan
Sumber Keragaman
Derajat Bebas
Jumlah Kuadrat
Rata-rata
Kuadrat FHitung
FTabel
(5 %)
Antar kelompok Dalam kelompok
2 6
4,531
0,515 2,2655 0,0858
26,404
- 5,14
-
[image:61.595.108.541.423.605.2]Lampiran 4
Tabel 6. Data Ananlisis Regresi Efek Konsentrasi NaCl Terhadap Nilai Tegangan Permukaan Larutan Pencuci Tangan
No Xi Yi Xi2 Yi2 Xi.Yi
1 10 6,688 100 44,7293 66,88
2 20 6,246 400 39,0125 124,92
3 30 4,758 900 22,6385 142,74
∑ 60 17,692 1400 106,3803 334,54
Tabel 7. Hasil perhitungan analisa regresi untuk nilai Tegangan Permukaan larutan pencuci tangan berdasarkan efek konsentrasi NaCl
Analisa Larutan Pencuci Tangan
Slope (a) -0,0965
Lampiran 5
Gambar 1. Grafik analisa regresi untuk nilai Tegangan Permukaan larutan pencuci tangan berdasarkan efek konsentrasi NaCl
Tabel 8. Data Ananlisis Regresi Efek Suhu Larutan Pencuci Tangan Terhadap Nilai Tegangan Permukaan Larutan Pencuci Tangan
No Xi Yi Xi2 Yi2 Xi.Yi
1 30 5,914 900 34,9753 177,42
2 40 5,205 1600 27,0920 208,2
3 50 4,185 2500 17,5124 209,25
[image:63.595.110.535.569.689.2]Lampiran 6
Tabel 9. Hasil perhitungan analisis regresi untuk nilai Tegangan Permukaan larutan pencuci tangan berdasarkan efek Suhu larutan Pencuci Tangan
Analisa Larutan Pencuci Tangan
Slope (a) -0,08545
[image:64.595.110.513.360.643.2]Intersep (b) 8,5176