PENGGUNAAN DAUN PISANG BATU (MUSA BALBISIANA
COLLA) SEBAGAI ADSORBEN UNTUK MENYERAP
LOGAM CROM (Cr) DAN NIKEL (Ni)
TESIS
Oleh
PENGGUNAAN DAUN PISANG BATU (MUSA BALBISIANA
COLLA) SEBAGAI ADSORBEN UNTUK MENYERAP
LOGAM CROM (Cr) DAN NIKEL (Ni)
TESIS
Diajukan sebagai salah satu syarat untuk memperoleh gelar Magister Sains dalam Program Studi Magister Ilmu Kimia pada Program Pascasarjana
Fakultas MIPA Universitas Sumatera Utara
Oleh
ULFA HANIM
097006023/KIMFAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM UNIVERSITAS SUMATERA UTARA
PENGESAHAN TESIS
Judul Tesis: : PENGGUNAAN DAUN PISANG BATU
(MUSA BALBISIANA COLLA) SEBAGAI ADSORBEN UNTUK MENYERAP LOGAM CROM (Cr) DAN NIKEL (Ni)
Nama Mahasiswa :
Ulfa Hanim
Nomor Induk Mahasiswa : 097006023 Program Studi : Magister Kimia
Fakultas : Matematika dan Ilmu Pengetahuan Alam Universitas Sumatera Utara
Menyetujui Komisi Pembimbing
Prof.Dr.Harry Agusnar,MSc Drs.Chairuddin,MSc
Ketua Anggota
Ketua Program Studi, D e k a n,
PERNYATAAN ORISINALITAS
PENGGUNAAN DAUN PISANG BATU (MUSA BALBISIANA
COLLA) SEBAGAI ADSORBEN UNTUK MENYERAP
LOGAM CROM (Cr) DAN NIKEL (Ni)
TESIS
Dengan ini saya nyatakan bahwa saya mengakui semua karya tesis ini adalah hasil kerja saya sendiri kecuali kutipan dan ringkasan yang tiap satunya telah dijelaskan sumbernya dengan benar.
Medan, 22 Juni 2011
ULFA HANIM
PERNYATAAN PERSETUJUAN PUBLIKASI
Sebagai sivitas akademika Universitas Sumatera Utara, saya yang bertanda tangan :
Nama : Ulfa Hanim
Nim : 097006023
Program Studi : Magister Kimia Jenis Karya Ilmiah : Tesis
Demi pengembangan ilmu pengetahuan, menyetujui untuk memberikan kepada Universitas Sumatera Utara Hak Bebas Royalti Non-Ekslusif ( Non-Exclusive Royalty Free Right) atas Tesis saya yang berjudul :
PENGGUNAAN DAUN PISANG BATU (MUSA
BALBISIANA COLLA) SEBAGAI ADSORBEN UNTUK MENYERAP LOGAM CROM (Cr) DAN NIKEL (Ni)
Beserta perangkat yang ada (jika diperlukan). Dengan Hak Bebas Royalti Non-Ekslusif ini, Universitas Sumatera Utara berhak menyimpan, mengalih media, memformat, mengelola dalam bentuk data-base, merawat dan mempublikasikan Tesis saya tanpa meminta izin dari saya selama tetap mencantumkan nama saya sebagai penulis dan sebagai pemegang dan atau sebagai pemilik hak cipta.
Demikian pernyataan ini dibuat dengan sebenarnya.
Medan, Juni 2011
ULFA HANIM
Telah diuji pada
Tanggal : 22 Juni 2011
PANITIA PENGUJI TESIS
Ketua : Prof.Dr.Harry Agusnar,MSc,M.Phil
Anggota : 1. Drs.Chairuddin,MSc
2. Prof.Basuki Wirjosentono,MS,Ph.D 3. Prof.Dr.Harlem Marpaung
RIWAYAT HIDUP
Ulfa Hanim dilahirkan di Mabar. Pada tanggal 05 Februari 1983, merupakan putri
dari pasangan Kasno dan Nadiah Hasibuan. Mengawali pendidikan dasarnya di SD
Subsidi Tri Bakti I Kecamatan Medan Marelan Kotamadya Medan tahun 1989-1995.
Kemudian melanjutkan ke Sekolah Lanjutan Tingkat Pertama Negeri 39 Medan pada
tahun 1995-1998, SMAK Depkes RI Medan pada tahun 1998-2001 dan pada tahun
2002 penulis diterima sebagai mahasiswa Jurusan Pendidikan Kimia Fakultas
Matematika dan Ilmu Pengetahuan Alam Universitas Negeri Medan. Pada 08
November 2007, penulis berhasil mendapatkan gelar sarjana pendidikan (SPd). Pada
tahun 2009 mengambil Program Studi Ilmu Kimia pada Sekolah Pascasarjana
Universitas Sumatera Utara dan lulus serta memperoleh gelar Magister Sains tahun
KATA PENGANTAR
Pertama-tama kami panjatkan puji dan syukur kehadirat Allah SWT Tuhan
Yang Maha Esa atas segala limpahan rakhmad dan karunia-Nya sehingga tesis ini
dapat diselesaikan.
Dengan selesainya tesis ini, perkenankanlah kami mengucapkan terima kasih
yang sebesar-besarnya kepada :
Rektor Universitas Sumatera Utara, Prof. Dr. dr. Syahril Pasaribu, DTMH&H,
M,Sc (CTM), Sp. AK atas kesempatan yang diberikan kepada kami untuk megikuti
dan menyelesaikan pendidikan Program Magister.
Dekan Fakultas MIPA Universitas Sumatera Utara, Dr. Sutarman, MSc atas
kesempatan menjadi mahasiswa Program Magister pada Program Pascasarjana
FMIPA Universitas Sumatera Utara.
Ketua Program Studi Magister Ilmu Kimia, Prof. Basuki Wirjosentono, MS,
Ph.D. Sekretaris Program Studi Ilmu Kimia, Dr. Hamonangan Nainggolan, MSc
beserta seluruh Staf Pengajar pada Program Studi Magister Ilmu Kimia Program
Pascasarjana Fakultas MIPA Universitas Sumatera Utara.
Terimakasih yang tak terhingga dan penghargaan setinggi-tingginya saya
ucapkan kepada Prof. Dr. Harry Agusnar, MSc, M.Phil selaku Promotor/Pembimbing
Utama yang penuh perhatian dan telah memberikan dorongan, bimbingan dan saran
sehingga penulis dapat meraih predikat magister, demikian juga kepada Drs.
Chairuddin, MSc selaku Co.Promotor/Pembimbing Lapangan yang dengan penuh
Penulis mengucapkan terima kasih kepada Kepala Sekolah SMA PAB 5
Klumpang Bapak Drs. Suprapto, dan Kepala Sekolah SMP PAB 19 Manunggal
Bapak Drs.Adi Rusdianto, MSi yang telah memberi kesempatan dan bantuan moril
kepada penulis untuk mengikuti Program Pascasarjana di Universitas Sumatera Utara.
Kepada Ayah penulis Kasno dan Bunda penulis Nadiah Hasibuan serta
adik-adikku Isnaini Maulida, AMK., SKM; Rakhmat Mutthaqin, ST; Harris Nata Kusuma.
Terima kasih atas segala pengorbanan kalian baik berupa moril maupun material,
budi baik ini tidak dapat dibalas hanya diserahkan kepada Allah SWT, Tuhan Yang
Maha Esa.
Hormat Penulis
PENGGUNAAN DAUN PISANG BATU (MUSA BALBISIANA
COLLA ) SEBAGAI ADSORBEN UNTUK MENYERAP
LOGAM CROM (Cr) DAN NIKEL (Ni)
ABSTRAK
Penelitian berupa penggunaan daun pisang batu (Musa Balbisiana Colla) sebagai adsrorben untuk menyerap logam crom (Cr) dan logam nikel (Ni), telah dilakukan Sampel berupa daun pisang batu kering yang telah dihaluskan dengan ukuran diameter 50 mesh dan dibuburkan dengan NaOH 20%, diaktivasi dengan menggunakan larutan HCl 1N. Dalam penelitian ini dilakukan pengukuran pH terhadap larutan logam crom (Cr) dan logam nikel (Ni) dengan menggunakan alat pH meter dan pengukuraan kadar logam crom (Cr) dan logam nikel (Ni) yang terdapat dalam sampel daun pisang batu kering sebelum diaktivasi dan setelah diaktivasi menggunakan spektrofotometer serapan atom dengan kondisi alat dioptimasi sesuai dengan prosedur yang berlaku. Hasil pengujian pH larutan logam crom (Cr) dan larutan logam nikel (Ni) bersifat asam yaitu 4,045 untuk pH logam crom dan 4,210 untuk pH logam nikel. Dari hasil pengukuran logam crom (Cr) dan logam nikel (Ni) dalam sampel daun pisang batu kering sebelum diaktivasi memiliki nilai absorbansi lebih tinggi dan daya serap (%) lebih rendah terhadap logam crom dan logam nikel dibandingkan dengan pengukuran logam crom (Cr) dan logam nikel (Ni) dalam sampel daun pisang setelah diaktivasi memiliki nilai absorbansi lebih rendah dan daya serap (%) lebih tinggi terhadap logam crom dan logam nikel.
THE USING OF BATU BANANA LEAVES (MUSA BALBISIANA
COLLA) AS ADSORBENT OF CHROME (Cr) AND NICKEL (Ni)
ABSTRACT
A research for the using of batu banana leaves (Musa Balbisiana Colla) as adsorbent of chrome (Cr) and nickel (Ni), has been done. The sample of dried batu banana leaves that had be powdered in the size of 50 mesh and mixed with NaOH 20% activated by using HCl 1 N solution. In this research, the pH is measured on the chrome (Cr) and nickel (Ni) using pH meter and the measurement of chrome (Cr) and nickel (Ni) content in the sample of dried batu banana leaves before activation and after activation using spectrophotometer atomic absorption in the tool condition optimized based on the valid procedure. The results of pH measurement of the chrome (Cr) and nickel (Ni) solution indicate the acidic, i.e. 4.045 chrome pH and 4.210 for nickel pH. The measurement of chrome (Cr) and nickel (Ni) content in the sample of dried batu banana leaves before activation has the higher absorbance value and the lower absorbance value and the lower absorbence to the chrome and nickel compared to the measurement of chrome (Cr) and nickel (Ni) in sample of banana leaves after activation in which the absorbance is lower and absorbance (%) is higher to the chrome and nickel.
DAFTAR ISI
Halaman
KATA PENGANTAR i
ABSTRAK iii
ABSRACT iv
DAFTAR ISI v
DAFTAR TABEL viii
DAFTAR GAMBAR ix
DAFTAR LAMPIRAN x
BAB I PENDAHULUAN 1
1.1.Latar Belakang 1
1.2. Permasalahan 2
1.3. Pembatasan Masalah 2
1.4. Tujuan Penelitian 2
1.5. Manfaat Penelitian 2
BAB II TINJAUAN PUSTAKA 3
2.1. Logam 3
2.1.1. Logam Crom 4
2.2. Adsorben 7
2.2.1. Kriteria Adsorben 8
2.2.2. Mekanisme Adsorben 8
2.2.3. Penggolongan Adsorben 8
2.3. Daun Pisang Batu (Musa Balbisiana Colla) 9
2.4. Spektrofotometer Serapan Atom 11
BAB III METODOLOGI PENELITIAN 17
3.1. Lokasi Penelitian 17
3.2. Sampel dan Cara Pengambilan Sampel 17
3.2.1. Sampel 17
3.2.2. Cara Pengambilan Sampel 17
3.3. Alat yang digunakan 17
3.4. Bahan-bahan yang digunakan 11
3.5. Prosedur Penelitian 18
3.5.1. Pembuatan Bubur Daun pisang Batu 18
3.5.2. Perlakuan dari daun pisang Batu yang tidak diaktivasi 18
3.5.3. Perlakuan dari daun pisang Batu yang diaktivasi 18
3.5.4. Bagan Cara Kerja ion logam penyerap 18
3.6. Bagan Prosedur Penelitian 19
BAB IV HASIL DAN PEMBAHASAN 23
4.1.2. Pengukuran Kandungan Crom 23
4.1.2.1. Penentuan Kurva Kalibrasi dengan Analisis Regresi 24
4.1.2.2. Penentuan Kadar Crom 25
4.1.3. Pengukuran Kandungan Nikel 26
4.1.3.1. Penentuan Kurva Kalibrasi dengan Analisis Regresi 26
4.1.3.2. Penentuan Kadar Nikel 27
4.2.Pembahasan 29
4.2.1. Kandungan Crom dalam sampel daun pisang batu 29
4.2.2. Kandungan Nikel dalam sampel daun pisang batu 31
BAB V KESIMPULAN DAN SARAN 35
DAFTAR PUSTAKA 36
DAFTAR TABEL
Nomor
Tabel
J U D U L
Halaman
4.1
4.2
4.3
4.4
4.5
Data Hasil Pengukuran pH Larutan logam Crom dan logam Nikel
Data Hasil Pengukuran Absorbansi Larutan Standard Crom (Cr)
Data Hasil Pengukuran Absorbansi Larutan Standard Nikel (Ni)
Konsentrasi crom (Cr) yang terserap didalam daun pisang batu kering
Konsentrasi nikel (Ni) yang terserap didalam daun pisang batu kering
30
30
34
37
DAFTAR GAMBAR
Nomor
Gambar
J U D U L
Halaman
4.1 4.2 4.3
4.4
4.5
4.6
Kurva Kalibrasi Larutan Standard Crom (Cr) Kurva Kalibrasi Larutan Standard Nikel (Ni)
Grafik Konsentrasi larutan crom (Cr) setelah ditambahkan daun pisang batu kering
Grafik konsentrasi crom yang terserap didalam daun pisang batu kering
Grafik Konsentrasi larutan nikel (Ni) setelah ditambahkan daun pisang batu kering
Grafik konsentrasi nikel (Ni) yang terserap didalam daun pisang batu kering
31 34 38
39
41
DAFTAR LAMPIRAN
Nomor
Lampiran J U D U L Halaman
A
B
C
D
E
Data Hasil Perhitungan Penurunan Persamaan Garis Regresi
Untuk Crom (Cr)
Data Hasil Perhitungan Penurunan Persamaan Garis Regresi
Untuk Nikel (Ni)
Data Pengukuran logam Crom dalam sampel daun pisang batu
sebelum diaktivasi
Data Pengukuran logam Nikel dalam sampel daun pisang batu
sebelum diaktivasi
Data Pengukuran logam Crom dalam sampel daun pisang batu
yang diaktivasi
Data Pengukuran logam Nikel dalam sampel daun pisang batu
yang diaktivasi
Absorbansi dan hasil perhitungan Konsentrasi crom (Cr) didalam
sampel daun pisang batu
Absorbansi dan hasil perhitungan Konsentrasi nikel (Ni) didalam
sampel daun pisang batu
Dokumentasi Penelitian
38
39
40
41
PENGGUNAAN DAUN PISANG BATU (MUSA BALBISIANA
COLLA ) SEBAGAI ADSORBEN UNTUK MENYERAP
LOGAM CROM (Cr) DAN NIKEL (Ni)
ABSTRAK
Penelitian berupa penggunaan daun pisang batu (Musa Balbisiana Colla) sebagai adsrorben untuk menyerap logam crom (Cr) dan logam nikel (Ni), telah dilakukan Sampel berupa daun pisang batu kering yang telah dihaluskan dengan ukuran diameter 50 mesh dan dibuburkan dengan NaOH 20%, diaktivasi dengan menggunakan larutan HCl 1N. Dalam penelitian ini dilakukan pengukuran pH terhadap larutan logam crom (Cr) dan logam nikel (Ni) dengan menggunakan alat pH meter dan pengukuraan kadar logam crom (Cr) dan logam nikel (Ni) yang terdapat dalam sampel daun pisang batu kering sebelum diaktivasi dan setelah diaktivasi menggunakan spektrofotometer serapan atom dengan kondisi alat dioptimasi sesuai dengan prosedur yang berlaku. Hasil pengujian pH larutan logam crom (Cr) dan larutan logam nikel (Ni) bersifat asam yaitu 4,045 untuk pH logam crom dan 4,210 untuk pH logam nikel. Dari hasil pengukuran logam crom (Cr) dan logam nikel (Ni) dalam sampel daun pisang batu kering sebelum diaktivasi memiliki nilai absorbansi lebih tinggi dan daya serap (%) lebih rendah terhadap logam crom dan logam nikel dibandingkan dengan pengukuran logam crom (Cr) dan logam nikel (Ni) dalam sampel daun pisang setelah diaktivasi memiliki nilai absorbansi lebih rendah dan daya serap (%) lebih tinggi terhadap logam crom dan logam nikel.
THE USING OF BATU BANANA LEAVES (MUSA BALBISIANA
COLLA) AS ADSORBENT OF CHROME (Cr) AND NICKEL (Ni)
ABSTRACT
A research for the using of batu banana leaves (Musa Balbisiana Colla) as adsorbent of chrome (Cr) and nickel (Ni), has been done. The sample of dried batu banana leaves that had be powdered in the size of 50 mesh and mixed with NaOH 20% activated by using HCl 1 N solution. In this research, the pH is measured on the chrome (Cr) and nickel (Ni) using pH meter and the measurement of chrome (Cr) and nickel (Ni) content in the sample of dried batu banana leaves before activation and after activation using spectrophotometer atomic absorption in the tool condition optimized based on the valid procedure. The results of pH measurement of the chrome (Cr) and nickel (Ni) solution indicate the acidic, i.e. 4.045 chrome pH and 4.210 for nickel pH. The measurement of chrome (Cr) and nickel (Ni) content in the sample of dried batu banana leaves before activation has the higher absorbance value and the lower absorbance value and the lower absorbence to the chrome and nickel compared to the measurement of chrome (Cr) and nickel (Ni) in sample of banana leaves after activation in which the absorbance is lower and absorbance (%) is higher to the chrome and nickel.
BAB I
PENDAHULUAN
1.1. Latar Belakang
Seiring dengan meningkatnya kemajuan teknologi dan berkembangnya
kegiatan industri, selain membawa dampak positif juga membawa dampak negatif.
Tumbuh pesatnya industri juga berarti makin banyak limbah yang dikeluarkan dan
mengakibatkan permasalahan yang kompleks bagi lingkungan. Limbah yang sangat
berbahaya dan memiliki daya racun tinggi umumnya berasal dari buangan industri,
terutama industri kimia, termasuk industri logam. Oleh karena itu, proses penanganan
limbah menjadi bagian yang sangat penting dalam industri. Logam berat tergolong
limbah B3 yang pada kadar tertentu dapat membahayakan lingkungan sekitarnya
karena bersifat toksik bagi hewan dan manusia (La Grega, 2001).
Limbah merupakan bahan sisa dan menurut asalnya dapat dibedakan atas 2
macam yaitu limbah domestik dan limbah industri. Limbah dari industri berat yang
mengandung ion logam berat dikatakan beracun apabila dapat langsung meracuni
manusia dan mahkluk hidup lain. Agar tidak mencemari lingkungan, limbah industri
yang akan dibuang harus diolah terlebih dahulu sehingga tidak melewati batas kadar
maksimum yang diperbolehkan oleh regulasi pemerintah (Lampiran PerMenLH No.3
tahun 2010).
Banyak penelitian yang telah dilakukan untuk menurunkan kadar logam berat
tersebut dalam air dan air limbah industri antara lain menggunakan daun dan biji
kelor untuk menurunkan kadar logam Fe pada air sumur bor dan dapat menurunkan
hingga 60% (Mahbubin, 2002). Tongkol jagung telah digunakan sebagai adsorben
untuk menurunkan kadar logam Fe dengan melakukan aktivasi terlebih dahulu
(Utomo,2003). Sisa hasil pertanian juga telah diuji sebagai potensi adsorben yang
tukar dari sisa hasil pertanian tersebut berasal dari senyawa turunan polimer, selulosa,
lignin, pictin dan hemiselulosa.
Pada penelitian ini digunakan daun pisang batu sebagai adsorben untuk
menyerap logam crom dan nikel . Pengaktivasian daun pisang batu dengan asam
sebelum digunakan, dimana komponen utama daun pisang yaitu lignin dan selulosa
meningkatkan efisiensi terhadap ion logam yang diserap (Nada et al, 2002).
1.2. Permasalahan
Apakah daun pisang batu dapat digunakan sebagai adsorben untuk menyerap
logam berat.
1.3. Pembatasan Masalah
Pada penelitian ini permasalahan dibatasi pada logam crom (Cr) dan nikel
(Ni) saja.
1.4. Tujuan Penelitian
1. Penggunaan daun pisang batu sebagai adsorben untuk menyerap logam
crom (Cr) dan nikel (Ni).
2. Mengetahui apakah ada perbedaan penyerapan daun pisang batu sebelum
diaktivasi dan setelah diaktivasi terhadap logam crom (Cr) dan nikel (Ni).
1.5. Manfaat Penelitian
Sebagai sumber informasi tentang penggunaan daun pisang batu sebagai
BAB II
TINJAUAN PUSTAKA
2.1. Logam
Dalam kimia, sebuah logam (bahasa Yunani: Metallon) adalah sebuah unsur
kimia yang siap membentuk ion (kation) dan memiliki ikatan logam, dan kadangkala
dikatakan bahwa ia mirip dengan kation di awan elektron. Metal adalah salah satu
dari tiga kelompok unsur yang dibedakan oleh sifat ionisasi dan ikatan, bersama
dengan metaloid dan nonlogam. Dalam tabel periodik, garis diagonal digambar dari
boron (B) ke polonium (Po) membedakan logam dari nonlogam. Unsur dalam garis
ini adalah metaloid, kadangkala disebut semi-logam; unsur di kiri bawah adalah
logam; unsur ke kanan atas adalah nonlogam. Nonlogam lebih banyak terdapat di
alam daripada logam, tetapi logam banyak terdapat dalam tabel periodik. Beberapa
logam terkenal adalah aluminium, tembaga, emas, besi, timah, perak, titanium,
uranium, dan zink. Alotrop logam cenderung mengkilap, lembek, dan konduktor yang
baik, sementara nonlogam biasanya rapuh (untuk nonlogam padat), tidak mengkilap,
dan insulator. Dalam bidang astronomi, istilah logam seringkali dipakai untuk
menyebut semua unsur yang lebih berat daripada helium. Paduan logam merupakan
pencampuran dari dua jenis logam atau lebih untuk mendapatkan sifat fisik, mekanik,
listrik dan visual yang lebih baik. Contoh paduan logam yang populer adalah baja
tahan karat yang merupakan pencampuran dari besi (Fe) dengan crom (Cr).
Umumnya, logam bermanfaat bagi manusia, karena penggunaannya di bidang
industri, pertanian, dan kedokteran. Contohnya, merkuri yang digunakan dalam
proses klor alkali. Proses klor alkali merupakan proses elektrolisis yang berperan
penting dalam industri manufaktur dan pemurnian zat kimia.Beberapa zat kimia yang
dapat diperoleh dengan proses elektrolisis adalah natrium, kalsium, magnesium,
aluminium, tembaga, seng, perak, hidrogen, klor, fluor, natrium hidroksida, kalium
tersebut merupakan proses klor-alkali. Elektrolisis larutan NaCl menghasilkan
natrium hidroksida di katoda (kutub positif) dan gas klor di anoda (kutub negatif).
Pada industri angkasa luar dan profesi kedokteran dibutuhkan bahan yang kuat, tahan
karat, dan bersifat noniritin, seperti aloi titanium.Sebagian jenis logam merupakan
unsur penting karena dibutuhkan dalam berbagai fungsi biokimiawi. Pada zaman
dahulu, logam tertentu, seperti tembaga, besi, dan timah digunakan untuk membuat
peralatan, perlengkapan mesin, dan senjata (Bondy et al, 1988).
2.1.1. Logam Krom
Limbah cair industri pelapisan logam mengandung asam dan logam berat
berbahaya, salah satunya adalah Crom(VI). Pada umumnya, limbah cair ini diolah
dengan cara pengendapan menggunakan larutan basa. Namun, Crom (VI) sulit
diendapkan dengan basa, sehingga diperlukan proses reduksi menjadi Crom (III).
Seiring dengan meningkatnya kemajuan teknologi dan berkembangnya kegiatan
industri, selain membawa dampak positif juga membawa dampak negatif. Salah satu
contoh adalah industri pelapisan logam. Beberapa komponen logam memerlukan
pelapisan logam yang berperan sebagai pelapis dekoratif-protektif dapat melindungi
besi atau komponen logam lainnya agar lebih menarik penampilannya atau lebih
tahan tehadap korosi dan keausan. Kegiatan pelapisan logam akan menghasilkan
limbah yang berbahaya dan dapat menjadi permasalahan yang kompleks bagi
lingkungan sekitarnya. Limbah industri pelapisan logam yang tidak dikelola dengan
baik dan benar dapat mengakibatkan pencemaran lingkungan. Air limbah industri
pelapisan logam umumnya banyak mengandung logam-logam berat, diantaranya
CrO42-. Limbah industri pelapisan logam yang mengandung Cr(VI) jika langsung
dibuang kelingkungan tanpa pengolahan terlebih dahulu akan menimbulkan dampak
negatif terhadap komponen-komponen lingkungan, sehingga akan menurunkan
kualitas lingkungan. Menurut Peraturan Pemerintah Republik Indonesia Nomor 18
tahun 1999 tentang Pengelolaan Limbah Berbahaya dan Beracun disebutkan bahwa
limbah krom yang dibuang ke lingkungan tidak boleh melebihi batas ambang yang
ditetapkan yaitu 0,5 ppm. Dalam pengolahan limbah, pengendapan merupakan salah
satu metode pengolahan limbah yang banyak digunakan untuk memisahkan logam
krom dari limbah cair tersebut. Namun, banyak kendala dalam pengolahan limbah
tersebut yaitu Cr(VI) ini sulit diendapkan. Oleh karena itu, agar pengendapan dapat
mencapai efisiensi yang tinggi Cr(VI) harus direduksi terlebih dahulu menjadi Cr(III).
Logam krom yang terdapat dalam limbah pelapisan logam berada dalam bentuk ion
CrO4 - sehingga bervalensi 6.
Limbah cair sebagai hasil samping dari aktivitas industri sering menimbulkan
permasalahan bagi lingkungan (Anis Kundari, 2009). Limbah cair tersebut
mengandung bahan-bahan berbahaya dan beracun yang keberadaannya dalam
perairan dapat menghalangi sinar matahari menembus lingkungan akuatik, sehingga
mengganggu proses-proses biologi yang terjadi di dalamnya, di samping itu juga
mengganggu estetika badan perairan akibat munculnya bau busuk. Pencemaran air
oleh logam-logam berat dapat berasal dari proses-proses industri seperti industri
metalurgi, industri penyamakan kulit, industri pembuatan fungisida, industri cat dan
zat warna tekstil (Anis Kundari, 2009). Zat pencemar berupa logam-logam berat
merupakan masalah yang lebih serius dibandingkan dengan polutan organik karena
ion-ion logam berat merupakan racun bagi organisme serta sangat sulit diuraikan
secara biologi maupun kimia. Logam krom (Cr) adalah salah satu jenis polutan logam
berat yang bersifat toksik, dalam tubuh logam krom biasanya berada dalam keadaan
sebagai ion Cr3+. Krom dapat menyebabkan kanker paru-paru, kerusakan hati (liver)
dilakukan untuk mengurangi kadar pencemar pada perairan biasanya dilakukan
melalui kombinasi proses biologi, fisika dan kimia. Pada proses fisika, dilakukan
dengan mengalirkan air yang tercemar ke dalam bak penampung yang telah diisi
campuran pasir, kerikil serta ijuk. Hal ini lebih ditujukan untuk mengurangi atau
menghilangkan kotoran-kotoran kasar dan penyisihan lumpur. Pada proses kimia,
dilakukan dengan menambahkan bahan-bahan kimia untuk mengendapkan zat
pencemar misalnya persenyawaan karbonat. Di samping itu, pengurangan zat
pencemar secara kimia juga sering dilakukan dengan menggunakan bahan-bahan
yang dapat menyerap zat-zat pencemar seperti karbon aktif, biomassa sel, dan
lempung. Lempung dapat digunakan sebagai adsorben untuk menyerap senyawa
fosfat dari air limbah (Masduqi, 2004). Zeolit alam terimpregnasi
2-merkaptobenzotiazol dapat digunakan untuk menyerap ion Cd (II) dan Cr (III).
Beberapa bahan lain yang telah digunakan sebagai penyerap adalah karbon aktif,
lempung, dan batu cadas. Namun, bahan-bahan tersebut relatif sulit diperoleh dan
karbon aktif mempunyai harga yang cukup mahal. Oleh karena itu, penelusuran
terhadap material baru yang lebih murah, mudah didapat serta mempunyai daya
adsorpsi besar sangat perlu diupayakan. Bahan-bahan alam organik yang mempunyai
gugus hidroksil (-OH) dapat dipakai untuk mengadsorpsi ion-ion logam berat.
2.1.2. Logam Nikel
Nikel adalah unsur kimia metalik dalam tabel periodik yang memiliki simbol
Ni dan nomor atom 28. Nikel mempunyai sifat tahan karat. Dalam keadaan murni,
nikel bersifat lembek, tetapi jika dipadukan dengan besi, krom, dan logam lainnya
berat dapat berpengaruh langsung hingga terakumulasi pada rantai makanan. Seperti
halnya sumber-sumber polusi lingkungan lainnya, logam berat tersebut dapat
ditransfer dalam jangkuan yang sangat jauh di lingkungan. Dalam rangka mengatasi
permasalahan akibat konsentrasi nikel yang masih tinggi dan endapan yang
dihasilkan banyak akibat pemakaian kapur, konsentrasi nikel di bawah baku mutu
yang berlaku dan menghasilkan endapan yang sedikit. Nikel dan senyawanya tidak
memiliki karakteristik bau atau rasa. Nikel terdapat di udara, menetap di tanah atau
dikeluarkan dari udara dalam hujan. Sumber utama nikel adalah asap tembakau,
knalpot mobil, pupuk, superfosfat, pengolahan makanan, dihidrogenasi
lemak-minyak, limbah industri, peralatan masak stainless steel, pengujian perangkat nuklir,
baking powder, pembakaran bahan bakar minyak, perawatan gigi dan jembatan. Efek
yang ditimbulkan logam nikel adalah serangan asma, bronkitis kronis, sakit kepala,
pusing, sesak napas, muntah, nyeri dada, batuk, sesak napas, kejang, bahkan kematian
( Indri Hapsari P et al, 2010).
2.2. Adsorben
Adsorben atau kebanyakan zat pengadsorpsi adalah bahan-bahan yang sangat
berpori, dan adsorpsi berlangsung terutama pada dinding-dinding pori atau pada
daerah tertentu di dalam partikel itu. Karena pori-pori adsorben biasanya sangat kecil
maka luas permukaan dalamnya menjadi beberapa kali lebih besar dari permukaan
luar. Adsorben yang telah jenuh dapat diregenerasi agar dapat digunakan kembali
untuk proses adsorpsi. Suatu adsorben dipandang sebagai suatu adsorben yang baik
untuk adsorpsi dilihat dari sisi waktu. Lama operasi terbagi menjadi dua, yaitu waktu
penyerapan hingga komposisi diinginkan dan waktu regenerasi / pengeringan
adsorben. Makin cepat dua varibel tersebut, berarti makin baik unjuk kerja adsorben
2.2.1. Kriteria Adsorben
Kriteria adsorben yang baik adalah :
1. Adsorben-adsorben yang digunakan biasanya dalam wujud butir berbentuk
bola, belakang dan depan, papan hias tembok, atau monolit-monolit dengan
garis tengah yang hidrodiamik antara 5 dan 10 juta.
2. Harus mempunyai hambatan abrasi tinggi.
3. Kemantapan termal tinggi.
4. Diameter pori kecil, yang mengakibatkan luas permukaan yang diunjukkan
yang lebih tinggi dan kapasitas permukaan tingggi karenanya untuk adsorbsi.
5. Adsorben-adsorben itu harus pula mempunyai suatu struktur pori yang
terpisah jelas yang memungkinkan dengan cepat pengangkutan dari uap air
yang berupa gas.
2.2.2. Mekanisme adsorben
Proses adsorpsi dapat digambarkan sebagai proses dimana molekul
meninggalkan larutan dan menempel pada permukaan zat adsorben akibat kimia dan
fisika. Proses adsorpsi tergantung pada sifat zat padat yang mengadsorpsi, sifat antar
molekul yang diserap, konsentrasi, temperatur dan lain-lain.
2.2.3. Penggolongan Adsorben. Adsorben dapat dibedakan menjadi :
1. Berdasarkan Sifatnya Terhadap Air
2. Berdasarkan Bahannya
1.1. Berdasarkan Sifatnya Terhadap Air.
1.2. Berdasarkan Bahannya. Klasifikasi adsorben berdasarkan bahannya dibagi
menjadi dua,yaitu :
Adsorben Organik
Adsorben organik adalah adsorben yang berasal dari bahan-bahan yang
mengandung pati. Adsorben ini sudah mulai digunakan sejak tahun 1979 untuk
mengeringkan berbagai macam senyawa. Beberapa tumbuhan yang biasa digunakan
untuk adsorben diantaranya adalah ganyong, singkong, jagung, dan gandum.
Kelemahan dari adsorben ini adalah sangat bergantung pada kualitas tumbuhan yang
akan dijadikan adsorben. Oleh karena itu, adsorben ini tidak dipilih dalam penelitian
yang akan dilakukan.
Adsorben Anorganik
Adsorben ini mulai dipakai pada awal abad ke-20. Dalam perkembangannya,
pemakaian dan jenis dari adsorben ini semakin beragam dan banyak dipakai orang.
Penggunaan adsorben ini dipilih karena berasal dari bahan-bahan non pangan,
sehingga tidak terpengaruh oleh ketersediaan pangan dan kualitasnya cenderung
sama.
2.3. Daun Pisang Batu (Musa balbisiana colla)
Jika ingin menggunakan daun pisang, pilihlah daun pisang batu. Daunnya
lentur, tidak mudah pecah, warnanya hijau tua menarik, dan permukaannya mengilap
(kompas.com, 2011/06/01).
Pisang (Musa sp.) merupakan tumbuhan yang berasal dari Asia dan tersebar di
Spanyol, Itali, Indonesia, Amerika, dan bagian dunia lainnya. Tanaman ini
dikelompokkan menjadi pisang liar dan pisang budidaya. Pisang liar pada umumnya
ditemukan tumbuh liar di alam, mempunyai banyak biji, dan bersifat diploid.
Sedangkan pisang budidaya pada umumnya tumbuh dipekarangan, bijinya sedikit,
dan bersifat triploid atau kadang diploid. Jenis pisang budidaya inilah yang sering
kita manfaatkan, sedangkan pisang liar tidak banyak dimanfaatkan secara ekonomi
digali. Indonesia merupakan salah satu negara pusat asal-usul pisang-pisangan.
Jumlah jenis pisang liar di Indonesia sangat melimpah. Sebanyak 12 jenis pisang liar
telah ditemukan di Indonesia mulai dari lembah alas (Aceh Tenggara) sampai ke
daerah Papua bagian utara. Salah satu jenis pisang liar adalah Musa balbisiana
Colla. Masyarakat Indonesia mengenalnya secara umum dengan sebutan pisang batu,
pisang biji, atau pisang klutuk. Jenis ini belum pernah dilaporkan, dan ditemukan
tumbuh secara liar di Indonesia. Akan tetapi secara luas telah ditanam di
kebun-kebun Indonesia.
Propinsi Lampung menyumbang lebih dari 30% total produksi nasional (BPS,
2007). Sentra produksi pisang di Lampung ada di daerah Kedondong, Kalianda,
Gading Rejo, Trimurjo, Metro, dan Semulih Raya. Selain jumlahnya yang besar,
Lampung juga mempunyai jenis pisang yang beragam. Hampir semua jenis pisang di
Indonesia tumbuh di sini, namun belum seluruhnya dimanfaatkan khususnya pisang
batu.
Potensi pisang liar di Indonesia belum mempunyai nilai ekonomi yang tinggi.
Selama ini tunas atau bonggol pisang muda diberikan sebagai pakan ternak pengganti
rumput. Daunnya digunakan sebagai pembungkus makanan. Tangkai daun dan serat
upih daun yang kering digunakan sebagai pengikat. Masyarakat Jawa Tengah
menggunakan upih daun kerting sebagai pembungkus daun tembakau, sedangkan di
Sumatera Utara digunakan sebagai pembungkus gula aren. Selain itu upih batang
dapat digunakan sebagai pelindung bibit tanaman. Padahal kalau dikaji lebih jauh
lagi, kegunaan pisang liar tidak hanya terbatas pada hal tersebut. Pisang liar
mempunyai potensi yang luar biasa, diantaranya sebagai sumber plasma nutfah. Musa
pisang-berbentuk tandan setelah masak berwarna kuning. Pisang biji rasanya manis, tetapi
banyak sekali bijinya, dalam 1 buah pisang terdapat ± 50 biji, biji kecil, berwarna
hitam (seperti biji kapuk randu). Habitat tanaman ini tumbuh di dataran rendah
sampai ketinggian ± 2200 m dpl. Tanaman pisang ini menyukai daerah yang panas,
subur atau sedikit berbatu, dekat dengan pembuangan sampah. Pisang batu sudah
dibudidayakan/ditanam di kebun dengan skala kecil (0,5 hektar) sampai skala sedang
(± 2 hektar) di Jawa Timur. Tetapi dijumpai pula tumbuh liar di tepi hutan.
2.4. Spektrofotometer Serapan Atom (SSA)
1. Pengertian Spektrofotometer Serapan Atom (SSA) adalah suatu alat yang
digunakan pada metode analisis untuk penentuan unsur-unsur logam dan metaloid
yang berdasarkan pada penyerapan adsorbsi radiasi oleh atom bebas.
2. Prinsip Dasar
Spektrofotometer serapan atom (SSA) merupakan teknik analisis kuantitafif
dari unsur-unsur yang pemakainnya sangat luas di berbagai bidang karena
prosedurnya selektif, spesifik, biaya analisisnya relatif murah, sensitivitasnya tinggi
(ppm-ppb), dapat dengan mudah membuat matriks yang sesuai dengan standar, waktu
analisis sangat cepat dan mudah dilakukan. SSA pada umumnya digunakan untuk
analisa unsur, spektrofotometer adsorpsi atom juga dikenal sistem single beam dan
double beam layaknya Spektrofotometer UV-VIS. Sebelumnya dikenal fotometer
nyala yang hanya dapat menganalisis unsur yang dapat memancarkan sinar terutama
unsur golongan IA dan IIA. Umumnya lampu yang digunakan adalah lampu katoda
cekung yang mana penggunaanya hanya untuk analisis satu unsur saja. Metode SSA
berprinsip pada adsorbsi cahaya oleh atom. Atom-atom menyerap cahaya tersebut
pada panjang gelombang tertentu, tergantung pada sifat unsurnya. Metode serapan
atom hanya tergantung pada perbandingan dan tidak bergantung pada temperatur.
Setiap alat SSA terdiri atas tiga komponen yaitu unit teratomisasi, sumber radiasi,
sistem pengukur fotometerik. Teknik SSA menjadi alat yang canggih dalam analisis.
yang ditentukan karena kemungkinan penentuan satu unsur dengan kehadiran unsur
lain dapat dilakukan, asalkan katoda berongga yang diperlukan tersedia. SSA dapat
digunakan untuk mengukur logam sebanyak 61 logam. Sumber cahaya pada SSA
adalah sumber cahaya dari lampu katoda yang berasal dari elemen yang sedang
diukur kemudian dilewatkan ke dalam nyala api yang berisi sampel yang telah
teratomisasi, kemudia radiasi tersebut diteruskan ke detektor melalui monokromator.
Chopper digunakan untuk membedakan radiasi yang berasal dari sumber radiasi, dan
radiasi yang berasal dari nyala api. Detektor akan menolak arah searah arus (DC) dari
emisi nyala dan hanya mengukur arus bolak-balik dari sumber radiasi atau sampel.
Atom dari suatu unsur pada keadaan dasar akan dikenai radiasi maka atom tersebut
akan menyerap energi dan mengakibatkan elektron pada kulit terluar naik ke tingkat
energi yang lebih tinggi atau tereksitasi. Jika suatu atom diberi energi, maka energi
tersebut akan mempercepat gerakan elektron sehingga elektron tersebut akan
tereksitasi ke tingkat energi yang lebih tinggi dan dapat kembali ke keadaan semula.
Atom-atom dari sampel akan menyerap sebagian sinar yang dipancarkan oleh sumber
cahaya. Penyerapan energi oleh atom terjadi pada panjang gelombang tertentu sesuai
dengan energi yang dibutuhkan oleh atom tersebut.
3. Bagian-Bagian pada SSA
a. Lampu Katoda
Lampu katoda merupakan sumber cahaya pada SSA. Lampu katoda memiliki
masa pakai atau umur pemakaian selama 1000 jam. Lampu katoda pada setiap unsur
yang akan diuji berbeda-beda tergantung unsur yang akan diuji, seperti lampu katoda
Cu, hanya bisa digunakan untuk pengukuran unsur Cu. Lampu katoda terbagi
berfungsi sebagai sumber cahaya untuk memberikan energi sehingga unsur logam
yang akan diuji, akan mudah tereksitasi. Selotip ditambahkan, agar tidak ada ruang
kosong untuk keluar masuknya gas dari luar dan keluarnya gas dari dalam, karena
bila ada gas yang keluar dari dalam dapat menyebabkan keracunan pada lingkungan
sekitar. Cara pemeliharaan lampu katoda ialah bila setelah selesai digunakan, maka
lampu dilepas dari soket pada main unit SSA, dan lampu diletakkan pada tempat
busanya di dalam kotaknya lagi, dan dus penyimpanan ditutup kembali. Sebaiknya
setelah selesai penggunaan, lamanya waktu pemakaian dicatat.
b. Tabung Gas
Tabung gas pada SSA yang digunakan merupakan tabung gas yang berisi gas
asetilen. Gas asetilen pada SSA memiliki kisaran suhu ± 20000K, dan ada juga
tabung gas yang berisi gas N2O yang lebih panas dari gas asetilen, dengan kisaran
suhu ± 30000K. regulator pada tabung gas asetilen berfungsi untuk pengaturan
banyaknya gas yang akan dikeluarkan, dan gas yang berada di dalam tabung.
Spedometer pada bagian kanan regulator. Merupakan pengatur tekanan yang berada
di dalam tabung. Pengujian untuk pendeteksian bocor atau tidaknya tabung gas
tersebut, yaitu dengan mendekatkan telinga ke dekat regulator gas dan diberi sedikit
air, untuk pengecekkan. Bila terdengar suara atau udara, maka menendakan bahwa
tabung gas bocor, dan ada gas yang keluar. Hal lainnya yang bisa dilakukan yaitu
dengan memberikan sedikit air sabun pada bagian atas regulator dan dilihat apakah
ada gelembung udara yang terbentuk. Bila ada, maka tabung gas tersebut positif
bocor. Sebaiknya pengecekkan kebocoran, jangan menggunakan minyak, karena
minyak akan dapat menyebabkan saluran gas tersumbat. Gas didalam tabung dapat
keluar karena disebabkan di dalam tabung pada bagian dasar tabung berisi aseton
yang dapat membuat gas akan mudah keluar, selain gas juga memiliki tekanan.
c. Ducting
Ducting merupakan bagian cerobong asap untuk menyedot asap atau sisa
lingkungan sekitar. Asap yang dihasilkan dari pembakaran pada SSA, diolah
sedemikian rupa di dalam ducting, agar polusi yang dihasilkan tidak berbahaya. Cara
pemeliharaan ducting, yaitu dengan menutup bagian ducting secara horizontal, agar
bagian atas dapat tertutup rapat, sehingga tidak akan ada serangga atau binatang
lainnya yang dapat masuk ke dalam ducting. Karena bila ada serangga atau binatang
lainnya yang masuk ke dalam ducting , maka dapat menyebabkan ducting tersumbat.
Penggunaan ducting yaitu, menekan bagian kecil pada ducting kearah miring, karena
bila lurus secara horizontal, menandakan ducting tertutup. Ducting berfungsi untuk
menghisap hasil pembakaran yang terjadi pada SSA, dan mengeluarkannya melalui
cerobong asap yang terhubung dengan ducting.
d. Kompresor
Kompresor merupakan alat yang terpisah dengan main unit, karena alat ini
berfungsi untuk mensuplai kebutuhan udara yang akan digunakan oleh SSA, pada
waktu pembakaran atom. Kompresor memiliki 3 tombol pengatur tekanan, dimana
pada bagian yang kotak hitam merupakan tombol ON-OFF, spedo pada bagian tengah
merupakan besar kecilnya udara yang akan dikeluarkan, atau berfungsi sebagai
pengatur tekanan, sedangkan tombol yang kanan merupakan tombol pengaturan
untuk mengatur banyak/sedikitnya udara yang akan disemprotkan ke burner. Bagian
pada belakang kompresor digunakan sebagai tempat penyimpanan udara setelah usai
penggunaan SSA. Alat ini berfungsi untuk menyaring udara dari luar, agar
bersih.posisi ke kanan, merupakan posisi terbuka, dan posisi ke kiri merupakan posisi
tertutup. Uap air yang dikeluarkan, akan memercik kencang dan dapat mengakibatkan
lantai sekitar menjadi basah, oleh karena itu sebaiknya pada saat menekan ke kanan
berada pada burner, merupakan lobang pemantik api, dimana pada lubang inilah awal
dari proses pengatomisasian nyala api. Perawatan burner yaitu setelah selesai
pengukuran dilakukan, selang aspirator dimasukkan ke dalam botol yang berisi
aquabides selama ±15 menit, hal ini merupakan proses pencucian pada aspirator dan
burner setelah selesai pemakaian. Selang aspirator digunakan untuk menghisap atau
menyedot larutan sampel dan standar yang akan diuji. Selang aspirator berada pada
bagian selang yang berwarna oranye di bagian kanan burner. Sedangkan selang yang
kiri merupakan selang untuk mengalirkan gas asetilen. Logam yang akan diuji
merupakan logam yang berupa larutan dan harus dilarutkan terlebih dahulu dengan
menggunakan larutan asam nitrat pekat. Logam yang berada di dalam larutan, akan
mengalami eksitasi dari energi rendah ke energi tinggi. Nilai eksitasi dari setiap
logam memiliki nilai yang berbeda-beda. Warna api yang dihasilkan berbeda-beda
bergantung pada tingkat konsentrasi logam yang diukur. Bila warna api merah, maka
menandakan bahwa terlalu banyaknya gas. Dan warna api paling biru, merupakan
warna api yang paling baik, dan paling panas, dengan konsentrasi.
f. Buangan pada SSA
Buangan pada SSA disimpan di dalam drigen dan diletakkan terpisah pada
SSA. Buangan dihubungkan dengan selang buangan yang dibuat melingkar
sedemikian rupa, agar sisa buangan sebelumnya tidak naik lagi ke atas, karena bila
hal ini terjadi dapat mematikan proses pengatomisasian nyala api pada saat
pengukuran sampel, sehingga kurva yang dihasilkan akan terlihat buruk. Tempat
wadah buangan (drigen) ditempatkan pada papan yang juga dilengkapi dengan lampu
indikator. Bila lampu indikator menyala, menandakan bahwa alat SSA atau api pada
proses pengatomisasian menyala, dan sedang berlangsungnya proses pengatomisasian
nyala api. Selain itu, papan tersebut juga berfungsi agar tempat atau wadah buangan
tidak tersenggol kaki. Bila buangan sudah penuh, isi di dalam wadah jangan dibuat
5. Keuntungan metode SSA
Keuntungan metode SSA dibandingkan dengan spektrofotometer biasa yaitu
spesifik, batas deteksi yang rendah dari larutan yang sama bisa mengukur unsur-unsur
yang berlainan, pengukurannya langsung terhadap contoh, output dapat langsung
dibaca, cukup ekonomis, dapat diaplikasikan pada banyak jenis unsur, batas kadar
penentuan luas (dari ppm sampai %). Sedangkan kelemahannya yaitu pengaruh kimia
dimana SSA tidak mampu menguraikan zat menjadi atom misalnya pengaruh fosfat
terhadap Ca, pengaruh ionisasi yaitu bila atom tereksitasi (tidak hanya disosiasi)
sehingga menimbulkan emisi pada panjang gelombang yang sama, serta pengaruh
BAB III
METODOLOGI PENELITIAN
3.1. Lokasi Penelitian
Penelitian ini dilakukan di Laboratorium Kimia Analitik, Departemen Kimia
Fakultas Matematika Dan Ilmu Pengetahuan Alam Sumatera Utara (FMIPA USU).
3.2. Populasi dan Sampel 3.2.1. Sampel :
Daun pisang batu
Larutan standar logam crom Larutan standar logam nikel
3.2.1. Cara pengambilan sampel :
Pengambilan sampel daun pisang batu di Desa Selemak Hamparan Perak,
sampel daun pisang batu yang diambil adalah daun pisang batu yang telah kering
dipohon.
3.3. Alat yang digunakan :
Spektrofotometer Serapan Atom (SSA)Shimadzu tipe : AA-6300 Mode lampu : BGC-D2
Laju alur gas : 15.0 L/min Gas asetilen
3.4. Bahan-bahan yang digunakan : NaOH 20%
3.5. Prosedur Penelitian
3.5.1. Pembuatan Bubur Daun pisang batu
Sebanyak 282,7 gram daun pisang batu yang telah dihaluskan dengan ukuran
diameter 50 mesh, dibuburkan dengan 2 liter NaOH 20% dan diinkubasi pada
suhu 60 ºC selama 2 jam. Bubur dipisahkan dari cairan hitamnya dengan cara
dicuci dengan air suling sampai cairan hitamnya hilang, dan dikeringkan.
3.5.2. Perlakuan dari bubur daun pisang batu yang tidak diaktivasi.
Sampel bubur daun pisang batu yang sudah dikeringkan, direfluks selama 1
jam dan disaring kemudian dicuci dengan air suling sampai netral. Hasil akhir
dicuci dengan methanol dan dikeringkan pada suhu kamar.
3.5.3. Perlakuan dari bubur daun pisang batu yang diaktivasi.
Sampel bubur daun pisang batu yang sudah dikeringkan ditambahkan HCl 1
N, direfluks selama 1 jam dan disaring kemudian dicuci dengan air suling
sampai netral. Hasil akhir dicuci dengan methanol dan dikeringkan pada suhu
kamar.
3.5.4. Bagan Cara Kerja ion logam penyerap
Sebanyak 100 mL larutan crom 20 ppm dimasukkan dalam 5 beaker glass ukuran 250 mL yang masing-masing berisi sampel daun pisang yang telah
diaktivasi dengan berat 0,2 gram ; 0,4 gram ; 0,6 gram ; 0,8 gram ; dan 1,0
gram. Diaduk dengan waktu kontak selama 30 menit dan disaring. Larutan
crom diukur dengan menggunakan spektrofotometer serapan atom (SSA).
3.6. Bagan Prosedur Penelitian
Bagan Pembuatan Bubur
Daun Pisang
sebanyak 282,7 gram
diinkubasi pada suhu 60°C
didiamkan selama 2 jam
dibuburkan Ditambah 2 liter
NaOH 20%
dicuci dengan air sampai netral bubur
dipisahkan dari cairan hitam
Lignin diendapkan
dicuci dengan air suling
Bagan Perlakuan dari Daun Pisang tidak diaktivasi
ud
Daun pisang
Direfluks 1 jam
disaring
Dicuci dengan air suling
Dicuci dengan metanol
Bagan Perlakuan dari Daun Pisang yang diaktivasi
ud
Daun pisang + HCl 1N
Direfluks 1 jam
disaring
Dicuci dengan air suling
Dicuci dengan metanol
Bagan Cara Kerja Ion Logam Penyerap
Daun pisang kering yang telah diaktivasi
Diaduk dengan waktu kontak selama 30 menit
disaring
0,2 gram 0,4 gram 0,6 gram 0,8 gram 1,0 gram
masing-masing sampel ditambahkan sebanyak 100 mL larutan crom 20 ppm
BAB IV
HASIL DAN PEMBAHASAN
4.1 Hasil Penelitian
4.1.1 Pengukuran pH Larutan Logam Crom dan Larutan Logam Nikel
Keasaman atau standar pH larutan logam nikel dan crom dalam sampel daun
pisang batu (ukuran 50 mesh) yang telah diaktivasi menyebabkan pH larutan logam
crom dan larutan logam nikel bersifat asam. Hasil pengukuran pH terlihat pada Tabel
[image:42.612.171.473.328.390.2]4.1 dibawa ini.
Tabel 4.1 Data Hasil Pengukuran pH Larutan logam Crom dan logam Nikel
No. Larutan Logam pH
1. Larutan Logam crom 4,045
2. Larutan Logam nikel 4,210
4.1.2 Pengukuran Kandungan Crom
Pada pengukuran kandungan crom dalam sampel daun pisang batu yang telah
diaktivasi dimulai dengan pengukuran absorban larutan standard Crom (Cr) dengan
Spektroskopi Serapan Atom (SSA). Data hasil pengukuran absorbansi dari larutan
standard Crom (Cr) diplotkan terhadap konsentrasi larutan standard crom (Cr) tertera
pada tabel 4.2 berikut :
Tabel 4.2 Data Hasil Pengukuran Absorbansi Larutan Standard Crom (Cr)
No. Konsentrasi (ppm) Absorbansi (A)
[image:42.612.186.461.554.703.2]4.1.2.1 Penentuan Kurva Kalibrasi dengan Analisis Regresi
Dari absorbansi yang diperoleh selanjutnya dengan metode Least-Square
diperoleh data yang tertera pada tabel 1 lampiran 1, kemudian dibuat kurva kalibrasi
antara konsentrasi dengan absorban. Berikut ini kurva kalibrasi larutan standard Crom
[image:43.612.160.475.214.401.2](Cr).
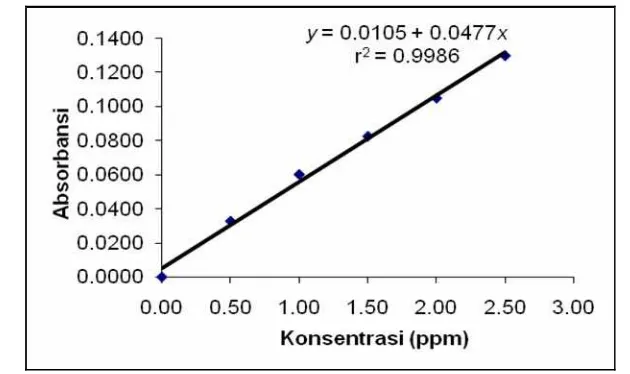
Gambar 4.1 Kurva Kalibrasi Larutan Standard Crom (Cr)
Diperolehnya gambar 4.1 dari formula persamaan garis regresi linier
hubungan antara absorban terhadap konsentrasi larutan standard sebagai berikut : y =
0,0105 + 0,0477x, dimana y = nilai absorban dan x = konsentrasi larutan logam crom
(Cr) dalam sampel daun pisang batu. Nilai koefisien korelasi (r) sebesar 0,9993, hasil
ini menunjukkan bahwa antara kandungan crom (Cr) dalam konsentrasi - absorbansi
berkorelasinya erat (r2 = 0,9986), nilai r2 sebesar 0,9986 berarti kurva pada gambar
4.1. tersebut mempunyai keakuratan dalam menentukan konsentrasi sebesar 99,86%.
4.1.2.2 Penentuan Kadar Crom
Sebagai contoh penentuan kadar crom, berikut disajikan perhitungan kadar
crom sampel daun pisang diperoleh nilai absorbansi :
A1 = 0,1315
A2 = 0,1258
A3 = 0,1166
A4 = 0,1132
A5 = 0,1086
Dengan mensubstitusikan nilai Y (absorbansi) kepersamaan regresi :
y = 0,0105 + 0,0477x. Maka diperoleh :
X1 = 2,54 ppm
X2 = 2,42 ppm
X3 = 2,22 ppm
X4 = 2,15 ppm
X5 = 2,06 ppm
Dengan demikian kadar crom dalam sampel daun pisang batu adalah :
X = ppm
n Xi 28 , 2 5 39 , 11
(X1- X)2 = (2,54 – 2,28)2 = 0,068
(X2-X)2 = (2,42 – 2,28)2 = 0,020
(X3-X)2 = (2,22 – 2,28)2 = 0,004
(X4-X)2 = (2,15 – 2,28)2 = 0,020
(X5-X)2 = (2,06 – 2,28)2 = 0,049 +
2
) (Xi X
= 0,161Maka S =
0,201 5 161 , 0 1 2
Xni XDari data hasil distribusi t student untuk n = 5, derajat kebebasan (dk) = n-1 =
4.Untuk derajat kepercayaan 95% (p=0,05), nilai t = 4,30. Maka d = t (0,05;n-1) Sx.d
= 4,30 x 0,09 = 0,39
Dari data pengukuran crom ( Cr ) dengan menggunakan sampel daun pisang
batu sebagai absorben adalah 2,28 ± 0,39 ppm.
4.1.3 Pengukuran Kandungan Nikel
Pada pengukuran kandungan Nikel dalam sampel daun pisang batu yang telah
diaktivasi dimulai dengan pengukuran absorban larutan standard Nikel (Ni) dengan
Spektroskopi Serapan Atom (SSA). Data hasil pengukuran absorbansi dari larutan
standard nikel (Ni) diplotkan terhadap konsentrasi larutan standard Nikel (Ni) tertera
[image:45.612.207.446.416.543.2]pada tabel 4.3 berikut :
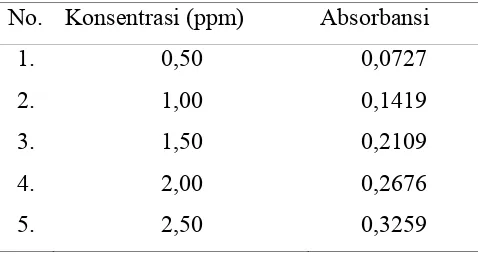
Tabel 4.3 Data Hasil Pengukuran Absorbansi Larutan Standard Nikel (Ni)
No. Konsentrasi (ppm) Absorbansi
1. 0,50 0,0727
2. 1,00 0,1419
3. 1,50 0,2109
4. 2,00 0,2676
5. 2,50 0,3259
4.1.3.1 Penentuan Kurva Kalibrasi dengan Analisis Regresi
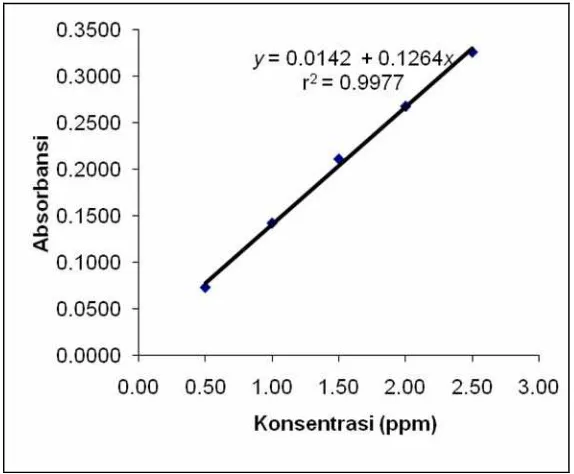
Gambar 4.2 Kurva Kalibrasi Larutan Standard Nikel (Ni)
Diperolehnya gambar 4.2 dari formula persamaan garis regresi linier
hubungan antara absorban terhadap konsentrasi larutan standard sebagai berikut : y =
0,0142 + 0,1264x , dimana Y = nilai absorban dan X = konsentrasi larutan logam
crom (Cr) dalam sampel daun pisang batu. Nilai koefisien korelasi (r) sebesar 0,9988,
hasil ini menunjukkan bahwa antara kandungan nikel (Ni) dalam konsentrasi
-absorbansi berkorelasinya erat (r2 = 0,9977), nilai r2 sebesar 0,9977 berarti kurva
pada gambar 4.2 tersebut mempunyai keakuratan dalam menentukan konsentrasi
sebesar 99,77%. Selanjutnya menentukan kandungan nikel (Ni) dalam sampel daun
pisang batu dilakukan pengukuran absorban. Data Absorban kandungan nikel dalam
sampel daun pisang batu terdapat dalam tabel 6 lampiran 3.
4.1.3.2. Penentuan Kadar Nikel
Kadar Nikel dapat ditentukan dengan menggunakan metode kurva kalibrasi
terhadap garis regresi dan kurva kalibrasi y = 0,0142 + 0,1264x, sehingga diperoleh
konsentrasi nikel.
Untuk sampel daun pisang diperoleh nilai absorbansi :
A1 = 0,2784
A2 = 0,2612
A3 = 0,2220
A4 = 0,1901
A5 = 0,1493
Dengan mensubstitusikan nilai Y (absorbansi) kepersamaan regresi :
y = 0,0142 + 0,1264x. Maka diperoleh :
X1 = 2,09 ppm
X2 = 1,95 ppm
X3 = 1,64 ppm
X4 = 1,39 ppm
X5 = 1,07 ppm
Dengan demikian kadar Nikel dalam sampel daun pisang adalah :
X = ppm
n Xi 63 , 1 5 14 , 8
(X1- X)2 = (2,09 – 1,63)2 = 0,2116
(X2-X)2 = (1,95 – 1,63)2 = 0,1024
(X3-X)2 = (1,64 – 1,63)2 = 0,0001
(X4-X)2 = (1,39 – 1,63)2 = 0,0576
(X5-X)2 = (1,07 –1,63)2 = 0,3136 +
2
) (Xi X
Dari data hasil distribusi t student untuk n = 5, derajat kebebasan (dk) = n-1 =
4.Untuk derajat kepercayaan 95% (p=0,05), nilai t = 4,30. Maka d = t (0,05;n-1) Sx.d
= 4,30 x 0,18 = 0,77
Dari data pengukuran nikel ( Ni ) dengan menggunakan sampel daun pisang
batu sebagai absorben adalah 1,63 ± 0,77 ppm.
4.2 Pembahasan
4.2.1 Kandungan Crom dalam Daun Pisang Batu
Kurva kalibrasi larutan standard crom (Cr) yang diperoleh dengan
memvariasikan konsentrasi larutan crom (Cr) dengan absorbansi dengan persamaan
Least-Square sehingga diperoleh persamaan garis linear : y = 0,0105 + 0,0477x.
[image:48.612.150.491.388.558.2]Dengan persamaan garis linear diperoleh kandungan crom (Cr) sebagai berikut :
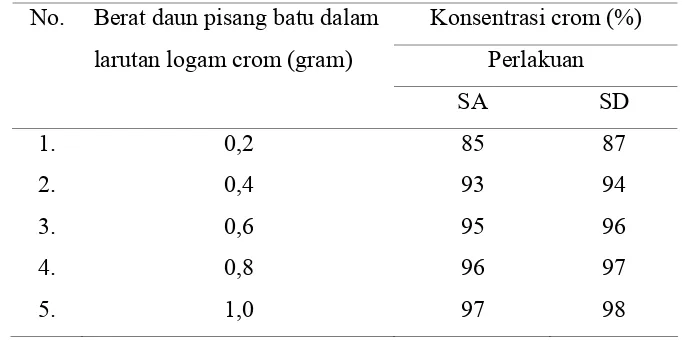
Tabel 4.4 Konsentrasi crom (Cr) yang terserap didalam daun pisang batu
Konsentrasi crom (%)
Perlakuan No. Berat daun pisang batu dalam
larutan logam crom (gram)
SA SD
1. 0,2 85 87
2. 0,4 93 94
3. 0,6 95 96
4. 0,8 96 97
5. 1,0 97 98
Keterangan :
SA : Sebelum aktivasi
SD : Sesudah aktivasi
Berdasarkan pada tabel 4.4 dapat dilihat bahwa nilai absorbansi crom (Cr)
terhadap daun pisang batu sebelum aktivasi lebih tinggi dan memiliki daya serap
terhadap logam crom lebih rendah dibandingkan dengan daun pisang batu sesudah
aktivasi, dengan nilai absorbansi yang lebih rendah tetapi memiliki daya serap
terhadap logam crom lebih tinggi, menunjukkan bahwa daun pisang batu yang telah
diaktivasi dengan HCl 1 N lebih banyak dapat menyerap logam crom. Dimana daun
pisang batu yang berfungsi sebagai adsorben logam dapat benar-benar berfungsi
sebagai adsorben dari logam crom. Dalam bentuk grafik data diatas ditunjukkan
[image:49.612.157.485.298.483.2]dalam grafik 4.3 dan 4.4 dibawah ini.
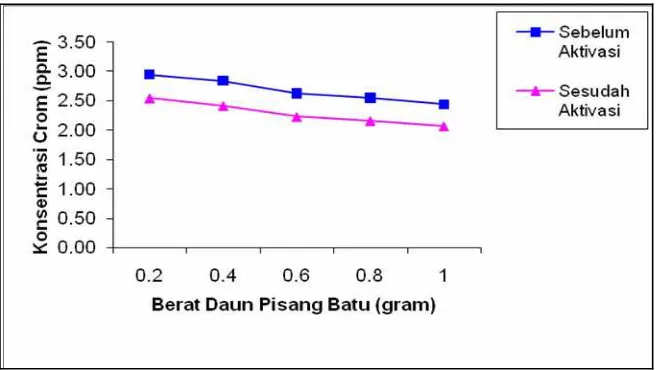
Gambar 4.3 Grafik Konsentrasi larutan crom (Cr) setelah
ditambahkan daun pisang batu
Dari gambar 4.3 konsentrasi larutan crom (Cr) setelah ditambahkan daun
pisang batu. Dari berat sampel daun pisang batu 0,2 gram; 0,4 gram; 0,6 gram; 0,8
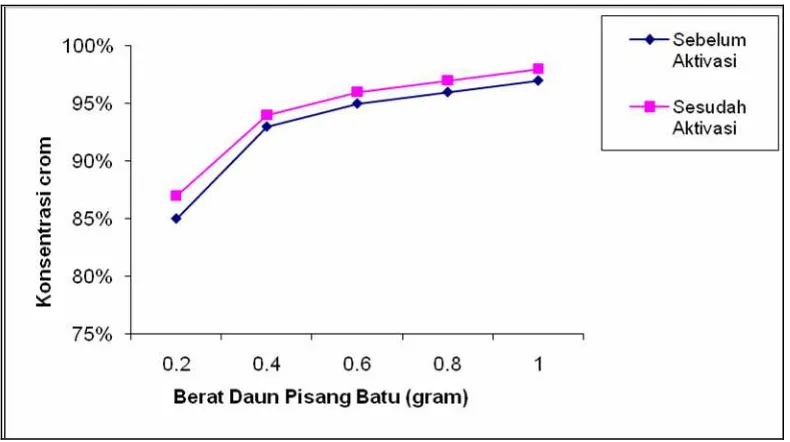
Gambar 4.4. Grafik konsentrasi crom yang terserap
didalam daun pisang batu
Dari gambar 4.4 Grafik konsentrasi crom (Cr) yang terserap didalam daun
pisang batu. Berat sampel daun pisang batu 0,2 gram; 0,4 gram; 0,6 gram; 0,8 gram
sampai 1,0 gram yang tampak pada grafik, semakin banyak berat sampel daun pisang
yang dicampurkan kedalam larutan logam crom (Cr) semakin terjadi kenaikan daya
serap daun pisang batu terhadap logam crom. Menunjukkan sellulosa yang
mempunyai gugus OH yang terdapat dalam daun pisang mampu mengikat logam
crom ( Nada et al, 2010).
4.2.2 Kandungan Nikel dalam Sampel daun Pisang Batu
Kurva kalibrasi larutan standard nikel (Ni) yang diperoleh dengan
memvariasikan konsentrasi larutan Nikel (Ni) dengan absorbansi dengan persamaan
Least-Square sehingga diperoleh persamaan garis linear : y = 0,0142 + 0,1264x.
Tabel 4.5 Konsentrasi nikel (Ni) yang terserap didalam daun pisang batu
Konsentrasi nikel (%)
Perlakuan No. Berat daun pisang batu dalam larutan l
logam nikel (gram)
SA SD
1. 0,2 88 89
2. 0,4 94 95
3. 0,6 97 97
4. 0,8 98 98
5. 1,0 98 99
Keterangan :
SA : Sebelum diaktivasi
SD : Sesudah diaktivasi
* : 100 mL larutan nikel 20 ppm
Berdasarkan pada tabel 4.5 dapat dilihat bahwa nilai absorbansi nikel (Ni)
terhadap sampel daun pisang batu sebelum aktivasi lebih tinggi dan memiliki daya
serap terhadap logam crom lebih rendah dibandingkan dengan daun pisang batu
sesudah aktivasi, dengan nilai absorbansi yang lebih rendah tetapi memiliki daya
serap terhadap logam crom lebih tinggi, menunjukkan bahwa daun pisang batu yang
telah diaktivasi dengan HCl 1 N lebih banyak dapat menyerap logam nikel. Dimana
daun pisang batu yang berfungsi sebagai adsorben logam dapat benar-benar berfungsi
sebagai adsorben dari logam crom. Dalam bentuk grafik data diatas ditunjukkan
Gambar 4.5. Grafik Konsentrasi larutan nikel (Ni) setelah
ditambahkan daun pisang batu
Dari gambar 4.5. konsentrasi larutan nikel (Ni) setelah ditambahkan daun
pisang batu. Dari berat sampel daun pisang batu 0,2 gram; 0,4 gram; 0,6 gram; 0,8
gram sampai 1,0 gram yang tampak pada grafik, semakin banyak berat sampel daun
pisang yang dicampurkan kedalam larutan logam nikel (Ni) semakin terjadi
penurunan konsentrasi nikel (ppm) dalam larutan yang diadsorbsi oleh daun pisang
batu. Menunjukkan sellulosa yang mempunyai gugus OH yang terdapat dalam daun
pisang mampu mengikat logam nikel ( Nada et al, 2010).(Data dapat dilihat pada
lampiran 4).
Gambar 4.6. Grafik konsentrasi nikel (Ni) yang terserap
didalam daun pisang batu
Dari gambar 4.6 Grafik konsentrasi nikel (Ni) yang terserap didalam daun
pisang batu. Berat sampel daun pisang batu 0,2 gram; 0,4 gram; 0,6 gram; 0,8 gram
sampai 1,0 gram yang tampak pada grafik, semakin banyak berat sampel daun pisang
yang dicampurkan kedalam larutan logam nikel (Ni) semakin terjadi kenaikan daya
serap daun pisang batu terhadap logam crom. Menunjukkan sellulosa yang
mempunyai gugus OH yang terdapat dalam daun pisang mampu mengikat logam
BAB V
KESIMPULAN DAN SARAN
5.1. Kesimpulan
Dari hasil analisis penggunaan daun pisang batu yang telah diaktivasi dengan
HCl 1N, terjadi penuruan kadar crom (Cr) dan nikel (Ni).
Dari hasil analisis terhadap larutan logam crom dan nikel dalam sampel daun
pisang batu yang telah diaktivasi dengan berat sampel yang berbeda-beda, semakin
banyak berat sampel daun pisang batu ditambahkan dalam larutan logam crom (Cr)
dan nikel (Ni) semakin terjadi penurunan terhadap kadar crom (Cr) dan nikel (Ni).
Larutan logam crom (Cr) dan nikel (Ni) yang dicampurkan kedalam sampel daun
pisang yang telah diaktivasi dengan waktu kontak 30 menit mempunyai pengukuran
pH yang bersifat asam disekitar 4,04 pada crom dan 4,2 pada nikel.
5.2. Saran
Diharapkan kepada peneliti berikutnya untuk menganalisis kadar logam lain
seperti : Mg, Mn,Zn dengan sampel daun pisang yang berbeda pula, seperti : daun
pisang lilin, daun pisang kepok, daun pisang raja,dsb.
Diharapkan kepada peneliti berikutnya untuk menganalisis kadar logam yang
sama, yaitu crom dan nikel tetapi dengan membuat perbandingan adsorben dua
DAFTAR PUSTAKA
A.M.A. Nada,A.A. El-Gendy*S.H.Mohamed. 2010. Banana leaves as adsorbent for removal of metal ions from waste water.journal homepage : www.elsevier.com/locate/carbpol. National Research Centre,Cellulose & Paper Department, El Buhoth St, Cairo, Dokki 12311,Egypt.
Ali Masduqi. 2004. Teknologi Alamiah Untuk Pengolahan Air Limbah Industri. Jurusan Teknik Lingkungan. Fakultas Teknik Sipil Dan Perencanaan. Institut Teknologi Sepuluh Nopember. Surabaya.
Alwin Parulian. 2009. Monitoring Analisis Kadar Aluminium (Al) dan Besi (Fe) Pada Pengolahan Air Minum PDAM Tirtanadi Sunggal. Sekolah Pasca Sarjana Universitas Sumatera Utara.
Bey Ubay. 2009. Spektrofotometer Serapan Atom. Mozilla firefox.
Djendakita Purba. 1996. Studi Pemakaian Natrium Alginat Untuk Menurunkan Kadar Ion-ion Logam Berat Dalam Air Limbah. Pengelolaan Sumber Daya Alam Dan Lingkungan Program Pasca Sarjana Universitas Sumatera Utara. Medan.
Eke. 2011. Bagian penelitian tepung pisang (http://dududuuuw.blogspot.com/bagian penelitian-eke-dtepung-pisang.html).
Indri Hapsari P,Wiharyanto Oktiawan,Junaidi. 2010. Penurunan Nikel (Ni) Dan Seng (Zn) Dalam Pengolahan Limbah Cair Industri Elektronik Menggunakan Metode Presipitasi Dengan Senyawa Alkali NaOH Dan Na2CO3. Studi Kasus PT. Hartono Istana Teknologi.
Jauhar Maghza Khaeruddin., Edo Catha Putra., Haryo Pandu Winito. 2007. Kerjasama ITB Dengan PT. Rekayasa Industri.
Lampiran PerMenLH No.3 tahun 2010 tentang Baku Mutu Air Limbah Bagi Kawasan Industri. Sumber : www.menlh.go.id (Baku Mutu Air Limbah Kawasan Industri).
…………, Keputusan Menteri Negara Lingkungan Hidup Nomor : Kep-51/MENLH/10/1995.http//www.bapedal.go.id/kepmen.
Marhaeniyanto Eko. 2009. Pemanfaatan Limbah Pisang Sebagai Strategi Pengembangan Ternak Kambing.
Noor Anis Kundari, Nurmaya Arofah, Kartini Megasari. 2009. Seminar Nasional V SDM Teknologi Nuklir : Kinetika Reduksi Krom (VI) Dalam Limbah Cair Industri Pelapisan Logam. Sekolah Tinggi Teknologi Nuklir- BATAN-Yogyakarta.
Nona Faziera Sari. 2010. Monitoring Kadar Mangan (Mn), Zinkum (Zn) Dan Magnesium (Mg) Dalam Air Gambut Setelah Dijernihkan Dengan Metode Elektrokoagulasi. Magister Ilmu Kimia Sekolah Pasca Sarjana Universitas Sumatera Utara.Medan.
Nurul Kasyfita. 2007. Efektifitas Penggunaan Adsorben Kulit Pisang Kepok (Musa Normalis) dalam meningkatkan Kualitas Minyak Goreng Bekas. Jurusan Pendidikan Kimia FKIP Universitas Mulawarman. Jalan Muara Pahu Kamus Gn. Kelua Samarinda 75123.
Palar, H. 1994. Pencemaran Dan Toksikologi Logam Berat. Rineka Cipta. Jakarta.
Lampiran A. Hasil Perhitungan Penurunan Persamaan Garis Regresi
Tabel. 1 Data Hasil Perhitungan Penurunan Persamaan Garis Regresi Untuk Crom (Cr)
No. Xi(ppm) Yi(A) (Xi - X) (Yi-Y) (Xi-X)2 (Yi-Y)2 (Xi-X)(Yi-Y)
1. 2. 3. 4. 5. 6. 0,0000 0,5000 1,0000 1,5000 2,0000 2,5000 0,0000 0,0328 0,0602 0,0826 0,1049 0,1298 -1,25 -0,75 -0,25 0,25 0,75 1,25 -0,0683 -0,0355 -0,0081 0,0143 0,0366 0,0615 1,5625 0,5625 0,0625 0,0625 0,5625 1,5625 0,0046 0,0012 0,0006 0,0002 0,0013 0,0037 0,0853 0,0266 0,0020 0,0035 0,0274 0,0768
∑ 7,5000 0,4103 0 0,0005 4,3750 0,01106 0,2216
Tabel. 2 Data Hasil Perhitungan Penurunan Persamaan Garis Regresi Untuk Nikel (Ni)
No. Xi(ppm) Yi(A) (Xi - X) (Yi-Y) (Xi-X)2 (Yi-Y)2 (Xi-X)(Yi-Y)
1. 2. 3. 4. 5. 6. 0,0000 0,5000 1,0000 1,5000 2,0000 2,5000 0,0000 0,0727 0,1419 0,2109 0,2676 0,3259 -1,25 -0,75 -0,25 0,25 0,75 1,25 -0,1698 -0,0971 -0,0279 0,0411 0,0978 0,1561 1,5625 0,5625 0,0625 0,0625 0,5625 1,5625 0,0288 0,0094 0,0007 0,0016 0,0095 0,0243 0,2122 0,0728 0,0069 0,0102 0,0733 0,1951
∑ 7,5000 1,0190 0 0,0002 4,3750 0,0743 0,5705
Lampiran B. Hasil Pengukuran Absorbansi Logam Crom dan Nikel Sebelum diaktivasi
Tabel. 3 Data Pengukuran logam Crom dalam sampel daun pisang batu
sebelum diaktivasi
No. Sampel daun pisang batu (gram) Absorbansi 1. 2. 3. 4. 5. 0,2 0,4 0,6 0,8 1,0 0,1505 0,1460 0,1356 0,1320 0,1270
Tabel.4 Data Pengukuran logam Nikel dalam sampel daun pisang batu
sebelum diaktivasi
[image:59.612.182.497.476.675.2]Lampiran C. Hasil Pengukuran Absorbansi Logam Crom dan Nikel Setelah diaktivasi
Tabel. 5 Data Pengukuran logam Crom dalam sampel daun pisang batu yang
diaktivasi
No. Sampel daun pisang batu (gram) Absorbansi
[image:60.612.184.498.465.665.2]1. 2. 3. 4. 5. 0,2 0,4 0,6 0,8 1,0 2,5356 0,1258 0,1166 0,1132 0,1086
Tabel. 6 Data Pengukuran logam Nikel dalam sampel daun pisang batu yang
diaktivasi
No. Sampel daun pisang batu (gram) Absorbansi
Lampiran D. Absorbansi dan hasil perhitungan konsentrasi logam didalam sample daun pisang batu
Tabel. 7 Absorbansi dan hasil perhitungan konsentrasi crom (Cr) didalam sampel daun pisang batu
Nilai Absorbansi Konsentrasi (ppm)
Perlakuan Perlakuan No. Berat sampel daun
pisang dalam larutan
logam crom (gram) SA SD SA SD
1. 0,2 gram 0,1505 0,1315 2,94 2,54
2. 0,4 gram 0,1460 0,1258 2,84 2,41
3. 0,6 gram 0,1356 0,1166 2,62 2,22
4. 0,8 gram 0,1320 0,1132 2,55 2,15
5. 1,0 gram 0,1270 0,1086 2,44 2,06
Keterangan :
SA : Sebelum diaktivasi SD : Sesudah diaktivasi
* : Konsentrasi awal larutan crom 20 ppm
Tabel. 8 Absorbansi dan hasil perhitungan konsentrasi nikel (Ni) didalam sampel daun pisang batu
Nilai Absorbansi Konsentrasi (ppm)
Perlakuan Perlakuan No. Berat sampel daun
pisang dalam larutan
logam logam nikel
(gram)
SA SD SA SD
1. 0,2 gram 0,2980 0,2784 2,24 2,09
2. 0,4 gram 0,2810 0,2612 2,11 1,95
3. 0,6 gram 0,2410 0,2220 1,79 1,64
Lampiran E. Gambar Dokumentasi Penelitian
Gambar 1 Serbuk daun pisang batu
[image:62.612.150.491.372.608.2][image:63.612.151.491.410.630.2]
Gambar 5 Pencucian bubur daun pisang dalam larutan NaOH 20% Dengan menggunakan air suling
[image:64.612.151.491.424.628.2]
Gambar 7 Pengaktivasian Bubur daun pisang yang telah dikeringkan dengan menggunakan HCl 1 N
[image:65.612.151.492.435.641.2]Gambar 9 Pembuatan larutan standard logam crom (Cr) dan nikel (Ni)
[image:66.612.152.491.419.670.2]
Gambar 11 Lampu katoda untuk pengukuran larutan standard logam crom (Cr) dan logam nikel (Ni) serta pengukuran sampel daun pisang batu dalam
larutan logam crom dan nikel
[image:67.612.151.491.370.593.2]