PURIFIKASI DAN KARAKTERISASI
INHIBITOR KATEPSIN DARI IKAN BANDENG
(Chanos chanos Forskal) DAN IKAN PATIN (Pangasius sp.)
SEFRI RUSYADI
SEKOLAH PASCASARJANA
INSTITUT PERTANIAN BOGOR
2
PERNYATAAN MENGENAI TESIS DAN SUMBER INFORMASI
Dengan ini saya menyatakan bahwa tesis Purifikasi dan Karakterisasi Inhibitor Katepsin dari Ikan Bandeng (Chanos chanos, Forskal) dan Ikan Patin
(Pangasius sp.) adalah karya saya dengan arahan dari komisi pembimbing dan
belum diajukan dalam bentuk apapun kepada perguruan tinggi mana pun. Sumber informasi yang berasal atau dikutip dari karya yang diterbitkan maupun tidak diterbitkan dari penulis lain telah disebutkan dalam teks dan dicantumkan dalam Daftar Pustaka di bagian akhir tesis ini.
Bogor, Januari 2010
Sefri Rusyadi
3
ABSTRACT
SEFRI RUSYADI. Purification and Characterization of a Chatepsin Inhibitor from Milk fish (Chanos chanos, Forskal) and Catfishes (Pangasius sp.). Supervised by TATI NURHAYATI and RUDDY SUWANDI
Proteolytic enzymes are distributed in all types of organisms including fishes. The cysteine protease is the largest group and includes lysosomal cathepsins were shown to cause softening and degradation of the myofibrillar protein. The action of proteases was regulated with endogenous inhibitors. The purposes of this research were to optimize extraction of protease inhibitor from skin, muscle, and viscera of fishes, to purify chatepsin inhibitor from the selected source, and to study the characteristics of the chatepsin inhibitor. A chatepsin protease inhibitor has been purified to homogeneity from the muscle of milk fish (Chanos chanos, Forskal) and catfishes (Pangasius sp.). Previously, we report the purification and further biochemical characterization of the endogenous chatepsin inhibitor. The purification was carried out by DEAE-Shepadex A-50 and Shepadex G-100. Throughout the purification procedure, chatepsin inhibitory activity was assayed using haemoglobin as substrate. The molecular inhibitor was 16,65 kDa, as estimated by SDS-PAGE and gel filtration. the smaller protein was purified with yield 1,85 % and purity of 16,91 fold. The chatepsin inhibitor was stable in the pH range of 7,0-9,0 with maximum stability at pH 8,0. Inhibitor presented thermal stability at temperature below 60 oC and exhibited maximum activity at temperature of 20-50 oC.
4
RINGKASAN
SEFRI RUSYADI. Purifikasi dan Karakterisasi Inhibitor Katepsin dari Ikan Bandeng (Chanos chanos, Forskal) dan Ikan Patin (Pangasius sp.). Dibimbing oleh TATI NURHAYATI dan RUDDY SUWANDI
Proses penurunan mutu ikan segar terutama diawali dengan proses perombakan oleh aktivitas enzim yang secara alami terdapat di dalam ikan. Salah satu jenis enzim yang berperan penting dalam proses kemunduran mutu ikan adalah enzim-enzim pengurai protein seperti katepsin, calpain dan kolagenase. Enzim proteolitik ini dapat menyebabkan timbulnya akumulasi metabolit, perubahan citarasa, dan pelunakan tekstur, terbentuknya komponen volatil serta peningkatan jumlah bakteri yang akhirnya menimbulkan kebusukan. Katepsin merupakan kelompok dari sistein proteinase diantaranya katepsin B dan L yang dapat menyebabkan terjadinya pelunakan daging (softening) pada ikan. Interaksi antara sistein protease dan inhibitornya telah menjadi tujuan beberapa penelitian pada dua dekade ini. Inhibitor spesifik dari sistein protease yang berupa molekul protein, sangat dibutuhkan untuk mencegah terjadinya proteolisis yang destruktif. Inhibitor protease pada ikan diperkirakan dapat melakukan perlindungan dari mikrooganisme, proses embriogenesis pada regulasi pertumbuhan awal embrio. Saat ini terdapat permintaan yang kuat terhadap protease inhibitor alami yang dapat digunakan untuk mencegah proses kemunduran pada daging ikan dan produk berbasis surimi. Beberapa inhibitor protease telah dicoba ditambahkan ke dalam daging ikan untuk menjelaskan peranan enzim pada proses pelunakan daging saat post mortem.
Tujuan penelitian ini adalah untuk menentukan sumber inhibitor katepsin dari bagian ikan bandeng dan ikan patin, yaitu kulit, daging, dan organ dalam, serta untuk mengetahui dan mendapatkan informasi mengenai metode purifikasi dan karakteristik inhibitor katepsin alami dari ikan. Hasil penelitian ini kedepannya dapat dimanfaatkan sesuai dengan sifat dan karakteristiknya tersebut baik untuk bidang kesehatan maupun untuk mencegah proses kemunduran pada daging ikan dan produk berbasis surimi. Untuk memperoleh inhibitor katepsin yang mempunyai aktivitas yang tinggi, perlu dilakukan proses purifikasi dan karakterisasi. Faktor-faktor yang mempengaruhi keberhasilan purifikasi dan karakterisasi adalah pemilihan sumber inhibitor katepsin, penggunaan substrat enzim dan pemilihan metode yang tepat pada setiap tahapan purifikasi seperti pemilihan metode ekstraksi, pemilihan presipitan pada tahap presipitasi, pemilihan jenis kantong dialisis dan pemilihan jenis gel kromatografi.
5
dan hasil pengendapan dengan ammonium sulfat yang meliputi penentuan suhu optimum, pH optimum, stabilitas panas dan pH, pengaruh ion logam serta penentuan bobot molekul dengan metode SDS-PAGE.
Hasil optimasi sumber inhibitor katepsin terbaik dari bagian kulit, daging dan organ dalam ikan bandeng dan patin diperoleh pada bagian daging yang diekstraksi pada suhu 80 oC dengan aktivitas penghambatan sebesar 87,84% pada ikan bendeng dan 90,28% dari ikan patin. Ekstrak jeroan menunjukkan aktivitas inhibitor yang negatif, sedangkan ekstrak inhibitor dari kulit ikan pada suhu ekstraksi 80 oC menunjukkan aktivitas yang cukup tinggi, yaitu 77,72% pada ikan bandeng dan 77,24% pada kulit ikan patin.
Ekstrak kasar inhibitor katepsin terbaik dari daging ikan bandeng dan patin, dilakukan pengendapan dengan ammonium sulfat. Hasil pengendapan dengan aktivitas penghambatan terbaik pada konsentrasi ammonium sulfat 70% (w/v) pada bagian pelet atau endapan baik pada ikan bandeng maupun ikan patin. Hasil pengendapan inhibitor dari ikan patin merupakan ekstrak terpilih yang selanjutnya digunakan untuk dilakukan dialisis dan dimurnikan dengan penukar ion DEAE Sephadex A-50. Puncak aktivitas inhibitor tertinggi terdapat pada fraksi no. 10 dengan aktivitas 1,98 U/ml. Fraksi tersebut mempunyai konsentrasi protein sebesar 0,1059 mg/ml dan aktivitas spesifik sebesar 18,762 U/mg dengan kelipatan pemurnian 4,65 kali. Fraksi aktif dengan aktivitas tertinggi (fraksi 10) selanjutnya dimurnikan kembali dengan kromatografi filtrasi gel. Hasilnya menunjukkan puncak aktivitas inhibitor berada pada fraksi ke 8 dengan aktivitas sebesar 1,8281 U/ml, konsentrasi protein sebesar 0,0268 mg/ml dan menunjukkan peningkatan aktivitas spesifik yang cukup tinggi menjadi 68,159 U/mg dengan kelipatan kemurnian sebesar 16,91 kali. Fraksi ke 8 dengan aktivitas tertinggi merupakan ekstrak murni inhibitor protease katepsin yang selanjutnya dilakukan karakterisasi bobot molekul dengan elektroforesis (SDS-PAGE)
Karakteristik inhibitor katepsin yang dihasilkan, yaitu mempunyai suhu optimum 40 oC, dan pH optimum 8. Ekstrak inhibitor katepsin relatif stabil pada suhu 10-50 oC dan pada kisaran pH 7-9. Inhibitor ekstrak mempunyai bobot molekul 15,651 kDa. Ion-ion logam menurunkan aktivitas inihibitor protease kecuali ion logam Mn2+ dan Na+ 1 mM.
6
@ Hak cipta milik IPB, tahun 2010 Hak cipta dilindungi Undang-Undang
1. Dilarang mengutip sebagian atau seluruh karya tulis ini tanpa
mencantumkan atau menyatakan sumber :
a. Pengutipan hanya untuk kepentingan pendidikan, penelitian, penulisan
karya ilmiah, penyusunan laporan, penulisan kritik atau tinjauan suatu makalah.
b. Pengutipan tidak merugikan kepentingan yang wajar IPB.
2. Dilarang mengumumkan dan memperbanyak sebagian atau seluruh karya
7
PURIFIKASI DAN KARAKTERISASI INHIBITOR KATEPSIN
DARI IKAN BANDENG (
Chanos chanos,
Forskal) DAN
IKAN PATIN (
Pangasius
sp
.
)
SEFRI RUSYADI
Tesis
Sebagai salah satu syarat untuk memperoleh gelar Magister Sains
pada Program Studi Teknologi Hasil Perairan
SEKOLAH PASCASARJANA
INSTITUT PERTANIAN BOGOR
8
9
HALAMAN PENGESAHAN
Judul Tesis : Purifikasi dan Karakterisasi Inhibitor Katepsin dari Ikan Bandeng (Chanos chanos, Forskal) dan Ikan Patin (Pangasius sp.)
Nama : Sefri Rusyadi NIM : C351070101
Disetujui :
Komisi Pembimbing
Dr. Tati Nurhayati S.Pi, M.Si. Dr. Ir. Ruddy Suwandi, MS, M.Phil
Ketua Anggota
Mengetahui :
Ketua Program Studi Dekan Sekolah Pascasarjana Teknologi Hasil Perairan
Dr. Tati Nurhayati S.Pi, M.Si. Prof. Dr. Ir. Khairil A. Notodiputro, M.S
10
PRAKATA
Puji dan syukur penulis panjatkan kepada Allah SWT atas segala Rahmat dan Karunia-Nya sehingga penulisan tesis ini dapat diselesaikan. Judul tesis ini adalah ”Purifikasi dan Karakterisasi Inhibitor Katepsin dari Ikan Bandeng (Chanos chanos, Forskal) dan Ikan Patin (Pangasius sp.)”.
Terima kasih penulis ucapkan kepada Dr. Tati Nurhayati, S.Pi, M.Si dan Dr Ir. Ruddy Suwandi MS, M.Phil selaku dosen pembimbing yang telah memberikan bimbingan, arahan, dukungan, semangat serta pelajaran tentang berbagai macam hal sehingga penulis dapat menyelesaikan thesis ini. Ucapan terima kasih juga disampaikan kepada Dr. Ir. Sri Purwaningsih, M.Si. serta seluruh dosen pengajar Departemen Teknologi Hasil Perairan, atas panduan ilmu dan saran-sarannya.
Terima kasih disampaikan juga kepada ketua tim penelitian dari Hibah
Bersaing Batch 2 tahun 2009, DP2M-Ditjen Dikti DEPDIKNAS melalui Dr.Tati Nurhayati, S.Pi, M.Si yang telah mendanai penelitian ini.
Hasil karya ini saya persembahkan kepada kedua orang tuaku Bapak Hairuddin S.Ag dan Ibu Siti Kamilah, kakak dan adikku, serta calon istriku Kiki Puspita Amalia S.Pi dan keluarga atas segala pengertian, doa, dukungan dan pengorbanan yang diberikan.
Terima kasih penulis sampaikan kepada semua pihak yang telah
membantu penelitian, khususnya teman seperjuangan Mba Tatty Yuniarti, teman-teman Pascasarjana THP 2006 sampai 2010, Tim Inhibitor Enzim THP 42 (Febri, Ary, Zaenuri, Fahrul). Terimakasih juga kepada Ibu Ika yang telah banyak
membantu dalam kromatografi dan elektroforesis.
Akhirnya, semoga karya ilmiah ini bermanfaat.
Bogor, Februari 2010
11
RIWAYAT HIDUP
Penulis dilahirkan di Pamekasan Madura pada tanggal 26 September 1983 sebagai anak kedua dari empat bersaudara, putra dari pasangan Hairuddin S.Ag dan Siti Kamilah. Penulis mengawali pendidikan di SDN Bulay 1 pada tahun 1990 dan menyelesaikan pendidikan pada tahun 1996. Pada tahun yang sama penulis diterima di SLTPN 1 Pamekasan dan menyelesaikan pendidikannya pada tahun 1999. Kemudian penulis melanjutkan pendidikan di SMAN 1 Pamekasan dan selesai pada tahun 2002.
12
3.4.3 Pengukuran Konsentrasi Protein (Bradford 1976) ... 25
3.4.4 Penentuan Berat Molekul dengan SDS-PAGE ... 26
4 HASIL DAN PEMBAHASAN ... 28
4.1 Optimasi Proses Ekstraksi Inhibitor Katepsin ... 28
4.2 Produksi dan Pemurnian Inhibitor Katepsin ... 30
4.2.1 Ekstraksi Inhibitor Katepsin ... 30
4.2.2 Pemurnian Inhibitor Katepsin dengan Kolom Kromatografi ... 32
13
4.3 Karakteristik Inhibitor Katepsin ... 36
4.3.1 Suhu Optimum ... 36
4.3.2 Penentuan pH Optimum ... 37
4.3.3 Stabilitas terhadap Panas ... 39
4.3.4 Stabilitas terhadap pH ... 40
4.3.5 Pengaruh Ion Logam terhadap Aktivitas Inhibitor... 40
4.3.6 Perbandingan Aktivitas Inhibitor Komersial ... 42
4.3.7 Penentuan Bobot Molekul ... 42
5 KESIMPULAN DAN SARAN ... 46
5.1 Kesimpulan ... 47
5.2 Saran ... 47
DAFTAR PUSTAKA ... 48
14
DAFTAR TABEL
Halaman
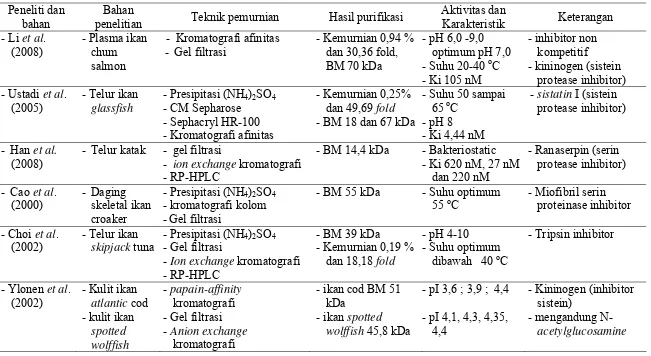
1. Beberapa penelitian mengenai purifikasi inhibitor enzim dari
jaringan hewan ... 11
2. Metode kromatografi untuk faraksinasi protein ... 17
3. Prosedur untuk mengukur aktivitas katepsin ... 23
4. Prosedur pengukuran aktivitas inhibitor katepsin ... 24
5. Pembuatan larutan standar BSA konsentrasi 0,01-0,3 mg/ml ... 26
6. Komposisi gel penahan dan pemisah SDS-PAGE ... 26
7. Peningkatan aktivitas inhibitor katepsin pada berbagai tahap pemurnian ... 35
8. Perbandingan aktivitas inhibitor komersial dengan inhibitor ekstrak patin ... 42
15
DAFTAR GAMBAR
Halaman
1. Ikan bandeng (Chanos chanos, Forskal)... 4
2. Ikan patin (Pangasius sp.) ... 5
3. Reaksi polimerisasi akrilamida dan N,N’-metilen-bis-akrilamida... 16
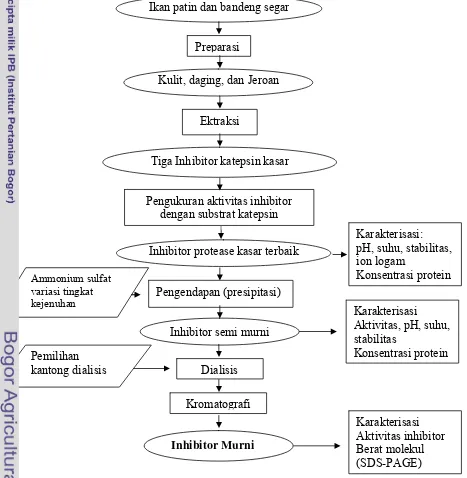
4. Diagram alur kerja penelitian pemurnina inhibitor katepsin ... 19
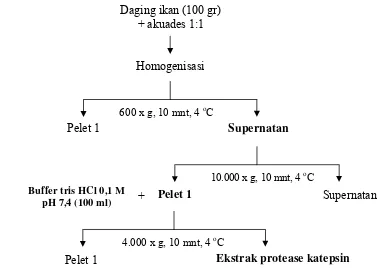
5. Diagram alir proses ekstraksi enzim katepsin dengan teknik differensial sentrifugasi (Dinu et al. 2002) ... 20
6. Diagram alir proses ekstraksi inhibitor enzim katepsin dengan teknik differensial sentrifugasi (An et al. 1995) ... 21
7. Persen (%) penghambatan aktivitas katepsin pada ekstrak inhibitor ikan bandeng (1) dan ikan patin (2), (□) suhu 60 oC, (□) suhu 70 oC, (□) suhu 80 oC ... 28
8. Uji protein pada semua ekstrak kasar inhibitor katepsin (□) inhibitor bandeng, (■) inhibitor patin ... 29
9. Persentase (%) aktivitas penghambatan inhibitor katepsin ikan bandeng setelah pengendapan ammonium sulfat (A) ; konsentrasi protein setelah pengendapan dangan ammonium sulfat (B), —■— endapan, —▲— supernatan ... 31
10. Persentase (%) aktivitas penghambatan inhibitor katepsin ikan patin setelah pengendapan ammonium sulfat (A) ; konsentrasi protein setelah pengendapan dangan ammonium sulfat (B), —■— endapan, —▲— supernatan ... 31
11. Pemurnian inhibitor katepsin menggunakan kromatografi penukar ion DEAE sephadex A-50, –●– konsentrasi protein, –×– aktivitas inhibitor, — gradien NaCl (M). ... 33
12. Pemurnian inhibitor katepsin menggunakan filtrasi gel sephadex G-100, –●– konsentrasi protein, –×– aktivitas inhibitor ... 33
13. Persentase (%) penghambatan inhibitor protease ekstrak kasar ikan patin dan bandeng pada suhu 10-70oC (A); Aktivitas penghambatan inhibitor ekstrak ikan patin setelah pengendapan dangan ammonium sulfat 70 % (B), (□) inhibitor bandeng, (■) inhibitor patin... 36
14. Persentase (%) penghambatan inhibitor protease ikan patin dan bandeng pada pH 3-10 (A); Aktivitas penghambatan inhibitor ekstrak ikan patin setelah pengendapan dangan ammonium sulfat 70% (B), (□) inhibitor bandeng, (■) inhibitor patin ... 38
16
16. Stabilitas inhibitor katepsin pada kisaran pH 3-10,
–●– ekstrak kasar, –▲– hasil pengendapan... 40 17. Pengaruh beberapa jenis logam terhadap aktivitas penghambatan
ekstrak ikan bandeng (A) dan ikan patin (B), (□) 1 mM,
(■) 5 mM ... 41 18. Hasil elektroforesesis: (M) Marker, (1) ekstrak kasar, (2) hasil
pengendapan ammonium sulfat, (3) hasil dialisis, (4) penukar ion,
17
DAFTAR LAMPIRAN
Halaman
1. Bahan bahan untuk ekstraksi katepsin dan inhibitor ... 53 2. Bahan-bahan untuk pengukuran aktivitas katepsin
dan inhibitor katepsin ... 53 3. Kurva standar penentuan konsentrasi protein
menurut metode Bradford ... 54 4 Komposisi gel dan pereaksi untuk elektroforesis ... 55 5 Pereaksi yang digunakan untuk pewarnaan perak dan
1. PENDAHULUAN
1.1 Latar Belakang
Proses penurunan mutu ikan segar terutama diawali dengan proses perombakan oleh aktivitas enzim yang secara alami terdapat di dalam ikan. Salah satu jenis enzim yang berperan penting dalam proses kemunduran mutu ikan adalah enzim-enzim pengurai protein (enzim proteolitis) yang menguraikan protein menjadi pepton, peptida dan asam-asam amino. Hidrolisis protein oleh suatu protease seperti katepsin, calpain dan kolagenase dapat menyebabkan timbulnya akumulasi metabolit, perubahan citarasa, dan pelunakan tekstur, terbentuknya komponen volatil serta peningkatan jumlah bakteri yang akhirnya menimbulkan kebusukan
Aktivitas proteolitik menyebabkan perubahan fungsional dan sifat organoleptik dari daging ikan. Katepsin merupakan kelompok dari sistein protease diantaranya katepsin B dan L yang dapat menyebabkan terjadinya pelunakan daging (softening) pada ikan (Ladrat et al. 2006). Katepsin L ditemukan pada sebagian besar proteinase termasuk penyebab degradasi protein miofibril pada surimi ikan pacific whitening. Penambahan inhibitor protease seperti sistatin pada surimi dapat mengurangi penurunan kekuatan gel melalui penghambatan sistein protease endogenous (Morrissey et al. 1995).
Interaksi antara sistein protease dan inhibitornya telah menjadi tujuan beberapa penelitian pada dua dekade ini. Inhibitor spesifik dari sistein protease sangat dibutuhkan untuk mencegah terjadinya proteolisis yang destruktif dan juga dapat dimanfaatkan pada proses terapi dan pada berbagai bahan penelitian. Pengertian yang mendalam pada interaksi sistein proteinase dan inhibitornya dapat memberikan informasi penting untuk mengkontrol aktivitas proteolitik (Hultman 2003). Inhibitor sistein proteinase yang secara luas tersebar pada jaringan hewan dan cairan tubuh, merupakan suatu molekul protein yang terdiri dari 100 sampai 120 deret asam amino dengan adanya jembatan disulfida dan residu karbohidrat (Otto dan Schirmeister 1997).
2
embrio. Inhibitor seperti sistatin juga dapat berperan sebagai pertahanan melawan protease virus yang dibutuhkan untuk replikasi virus (Ustadi et al. 2005). Inhibitor protease alami telah berhasil dipurifikasi seperti sistatin yang dipurifikasi dari telur ikan glassfish (Ustadi et al. 2005), cairan ovarian ikan nila, telur ikan salmon, kulit ikan atlantik salmon dan ikan cod (Olonen 2004), plasma ikan chum salmon (Li et al. 2008), dan purifikasi inhibitor tripsin dari telur ikan skipjack tuna (Choi et al. 2002)
Ikan bandeng (Chanos chanos, Forskal) dan ikan patin (Pangasius sp.) seperti halnya mahluk hidup lainnya merupakan sumber enzim dan inhibitor alami yang dapat berada dalam sel (intraseluler) dan melekat pada membran atau berada di luar sel (ekstraseluler). Saat ini terdapat permintaan yang kuat terhadap inhibitor protease alami yang dapat digunakan untuk mencegah proses kemunduran pada daging ikan dan produk berbasis surimi (Ustadi et al. 2005). Beberapa inhibitor protease telah dicoba ditambahkan ke dalam daging ikan untuk menjelaskan peranan enzim pada proses pelunakan daging saat post mortem. Berdasarkan penelitian Kubota et al. (2001) menunjukkan bahwa EDTA, pengkelat ion logam dan phenantroline (inhibitor spesifik metalloprotease) dapat menekan terjadinya pelunakan daging ikan flounder.
1.2 Perumusan Masalah
3
1.3 Tujuan dan Manfaat Penelitian
Tujuan dari penelitian tentang purifikasi dan karakterisasi inhibitor katepsin dari ikan bandeng dan ikan patin adalah sebagai berikut:
a. Menentukan sumber inhibitor katepsin terbaik dari bagian ikan bandeng dan ikan patin, yaitu kulit, daging, dan organ dalam;
b. Mendapatkan metode purifikasi inhibitor terbaik yang menghasilkan inhibitor katepsin dengan aktivitas yang tinggi;
c. Menentukan karakteristik inhibitor katepsin yang dihasilkan.
Penelitian ini diharapkan dapat bermanfaat untuk mengetahui dan mendapatkan informasi mengenai metode purifikasi dan karakteristik inhibitor katepsin alami dari ikan sehingga dapat mengaplikasikannya sesuai dengan sifat dan karakterisasinya tersebut baik untuk bidang kesehatan maupun untuk mencegah proses kemunduran pada daging ikan dan produk berbasis surimi
1.4 Hipotesis Penelitian
Hipotesis pada penelitian ini adalah:
a. Salah satu dari tiga bagian ikan bandeng dan ikan patin, yaitu kulit, daging, dan organ dalam diduga dapat menjadi sumber inhibitor katepsin yang terbaik; b. Tingkat kemurnian inhibitor katepsin yang dihasilkan pada tahap purifikasi
2. TINJAUAN PUSTAKA
2.1. Deskripsi dan Identifikasi Ikan Bandeng (Chanos chanos, Forskal)
Bandeng (Chanos chanos, Forskal) merupakan hasil utama budidaya tambak. Berwarna putih keperak-perakan. Sepintas mirip dengan ikan salem, namun dagingnya tidak berwarna merah, melainkan putih susu, sehingga di berbagai negara yang berbahasa Inggris, dikenal sebagai milkfish. Badannya langsing berbentuk torpedo dengan sirip ekor yang bercabang dan merupakan suatu tanda ikan perenang cepat. Panjang badannya bisa mencapai 1 meter, tetapi di tambak ukuran badannya tidak dapat melebihi 50 cm karena pengaruh faktor ruang dan sengaja diambil sebelum menjadi dewasa (Soeseno 1988).
Secara taksonomi, bandeng termasuk dalam Kelas Pisces (bangsa ikan), Subkelas Teleostei (ikan bertulang sejati), Ordo Malacopterygii (ikan berjari-jari sirip lemah), Keluarga Chanidae (bandeng-bandengan), Genus Chanos, spesies
Chanos chanos. Ikan ini dalam bahasa daerah, dikenal juga dengan nama-nama bandeng, bolu, muloh dan ikan agam (Mudjiman 1991). Gambar morfologi bandeng (Chanos chanos Forskal) disajikan pada Gambar 1.
Gambar 1 Ikan bandeng (Chanos chanos, Forskal).
Sumber:http://www.verwijsfish.com/picture content/cms_picture/7.jpg [30 Desember 2008]
5
Ikan bandeng juga bersifat herbivorous dan tanggap terhadap pakan buatan, dengan formulasi pakan buatan relatif mudah, tidak bersifat kanibal, dan mampu hidup dalam kondisi berjejal. Ikan bandeng juga dapat dibudidayakan secara polikultur dengan spesies lainnya, seperti baronang. Ikan bandeng dagingnya bertulang, tetapi rasanya lezat dan di beberapa daerah memiliki tingkat preferensi konsumsi yang tinggi. Ikan bandeng juga dapat digunakan sebagai umpan bagi industri penangkapan tuna (Rachmansyah et al. 1997).
2.2 Deskripsi dan Identifikasi Ikan Patin (Pangasius sp.)
Ikan patin (Pangasius sp.) merupakan ikan konsumsi budidaya ikan air tawar unggulan dari famili pangasidae yang dikenal dengan nama lokal patin, jambal atau pangasius. Ikan patin berbadan panjang, berwarna putih perak dengan punggung berwarna kebiruan-biruan. Daging ikan patin memiliki kandungan kalori dan protein cukup tinggi, rasa dagingnya enak, lezat dan gurih. Gambar ikan patin dapat dilihat pada Gambar 2.
Gambar 2 Ikan patin (Pangasius sp.).
Saanin (1984) mengklasifikasi ikan patin sebagai berikut : Filum : Chordata
Kelas : Pisces Sub Kelas : Teleostei Ordo : Ostariophysi Sub Ordo : Siluroidei Famili : Schilbeidae Genus : Pangasius
6
2.3 Protease pada Ikan
Protease adalah enzim yang mampu menghidrolisis ikatan peptida pada protein. Enzim ini untuk melakukan aktivitasnya membutuhkan air sehingga dikelompokkan dalam kelas hidrolase. Protease berperan dalam sejumlah reaksi biokimia seluler. Selain diperlukan untuk degradasi protein nutrien, enzim protease terlibat dalam sejumlah mekanisme patogenisitas, proses koagulasi darah, proses sporulasi, diferensiasi, sejumlah proses pasca translasi protein, dan mekanisme ekspresi protein ekstra seluler (Rao et al. 1998).
Secara umum protease dapat dibagi dalam dua golongan, yaitu proteinase dan peptidase. Proteinase mengkatalisis hidrolisis molekul protein menjadi fragmen-fragmen besar, sedangkan peptidase mengkatalisis fragmen polipeptida menjadi asam amino (Suhartono 1992). Dilihat dari letak pemutusan ikatan
peptida, protease dibedakan menjadi endopeptidase atau proteinase (EC 3.4.21-99) dan eksopeptidase (EC 3.4.11-21). Endopeptidase memutuskan
ikatan peptida yang berada di dalam rantai protein sehingga dihasilkan peptida dan polipeptida, sedangkan eksopeptidase menguraikan protein dari ujung rantai sehingga dihasilkan satu asam amino dan sisa peptida. Berdasarkan sifat kimia dan sisi aktifnya dikenal empat golongan protease yaitu serin (EC 3.4.21), sistein (EC 3.4.22), aspartat (EC 3.4.23), dan metallo endopeptidase (EC 3.4.24) (Otto dan Schirmeister 1997).
Sistein protease merupakan kelompok besar enzim, termasuk katepsin lisosomal dan calpain. Secara fisiologis, sistein proteinase mempunyai peranan penting pada metabolisme protein dan sebaliknya. Selain itu sistein proteinase juga dihubungkan dengan proses dan aktivasi berbagai prohormon, proenzim, dan peptida (Hultman 2003). Katepsin juga terlibat dalam kemunduran tekstur daging. Katepsin yang berbeda dapat memberikan aksi pada proses autolisis daging ikan (Kolodziejska dan Sikorski 1996).
7
kemungkinan paling penting dalam kemunduran tekstur daging (Aoki et al. 2000; Kolodziejska dan Sikorski 1996). Aktivitasnya berbeda beda tiap fraksi daging dan spesies ikan. Aktivitas optimum dilaporkan pada suhu 40-50 oC dan aktivitasnya menurun dengan penurunan suhu. Katepsin secara umum bekerja pada pH 3-4 dan beberapa katepsin juga mempunyai aktivitas tinggi pada pH 6-6,5 (Aoki et al. 2000; Kolodziejska dan Sikorski 1996).
Aktivitas katepsin sangat berpengaruh terhadap tekstur daging ikan karena katepsin dapat menurunkan fleksibilitas (kekenyalan) sehingga daging ikan menjadi tidak elastis dan jaringan daging ikan melunak (lembek). Pelunakan daging ini merupakan salah satu sumber masalah pada industri surimi karena katepsin dapat menurunkan kemampuan pembentukan gel pada proses pembuatan surimi dari daging ikan akibat degradasi protein miofibril yang dapat mengurangi elastisitas dan kekuatan gel surimi. Jenis katepsin B, D, L dan H telah diketahui memiliki efek gel softening pada proses pembentukan gel surimi (Haard 2000).
Calpain (EC 3.4.22.17) merupakan proteinase netral yang diaktifkan adanya ion kalsium, dan bekerja bersama dengan spesifik inhibitor endogenous (calpastatin) pada kebanyakan hewan mamalia tetapi tidak ditemukan pada tanaman (Otto dan Schirmeister 1997). Calpain mempunyai peran pada post
mortem degradasi daging ikan melalui pemecahan protein miofibrillar. Calpain
adalah sistein endopeptidase netral yang ditemukan pada sarkoplasma daging. Disusun dari dua subunit dan diaktifkan oleh ion kalsium dan komponen thiol, kebanyakan aktif pada pH netral (6,9-7,5) dan suhu 30 oC (Kolodziejska dan Sikorski 1996).
Kolagenase (EC 3.4.24.7) merupakan metalloproteinase yang ditemukan pada daging skeletal (Kolodziejska dan Sikorski 1996). Endogenous kolagenase berperan dalam kerusakan jaringan penghubung daging ikan yang menyebabkan
gaping dan perubahan tekstur yang tidak diinginkan. Selain itu, terjadinya
8
2.4 Inhibitor Protease
Suatu molekul enzim dapat kehilangan aktivitasnya akibat panas, asam atau basa kuat, pelarut organik, atau faktor lain yang dapat menyebabkan denaturasi dan perubahan konformasi protein. Hambatan atau inhibisi pada suatu reaksi yang menggunakan enzim sebagai katalis dapat terjadi apabila penggabungan substrat pada bagian aktif enzim mengalami hambatan. Molekul atau ion yang dapat menghambat reaksi tersebut dinamakan inhibitor (Lehninger 1993).
Inhibitor enzim merupakan suatu komponen yang dapat menurunkan laju rata-rata pengukuran reaksi katalitik enzim (Carreno dan Cortes 2000). Lebih dari 100 jenis inhibitor protein alami telah berhasil diidentifikasi dan lebih banyak lagi jenis yang telah berhasil disintetis. Inhibitor proteinase memiliki berbagai macam bentuk dan sering dikelompokkan berdasarkan mekanisme reaksinya dan kesamaan strukturnya (Creighton 1989 diacu dalam Wijaya 2005). Banyak inhibitor proteinase alami berupa protein dengan ukuran molekul berkisar 3.000-800.000 Da. Inhibitor dari kultur mikroba juga mengandung inhibitor proteinase dengan berat molekul rendah dan biasanya berupa peptida (Nagase dan Salvesen 2001).
Inhibitor enzim, berdasarkan spesifitas kerjanya, dibagi atas inhibitor enzim non spesifik dan spesifik. Inhibitor non spesifik meliputi α2-macroglobulin,
peptida klorometil keton, peptida aldehida, dan metal chelator. α2-macroglobulin
mempunyai bobot molekul tinggi, bersifat irreversible, dapat berikatan dan menghambat kebanyakan endopeptidase (proteinase). Inhibitor jenis peptida aldehida bersifat reversible, terdiri dari leupeptin dan antipain yang mengandung aldehida (Salvesen dan Nagase 2001).
9
nontoksik, mempunyai kecepatan reaksi yang lebih cepat dibandingkan dengan DFP atau PMSF, sehingga merupakan inhibitor yang paling banyak direkomendasikan. Inhibitor proteinase logam berupa peptida inhibitor dan protein inhibitor seperti TIMPs (Salvesen dan Nagase 2001).
2.4.1 Inhibitor Sistein Proteinase
Aktivitas sistein proteinase dapat diatur dan dihambat secara endogenous, melalui inhibitor alami maupun melalui pengikatan sistein pada kondisi lingkungan tertentu seperti pH dan agen pengkelat. Jika sistem kontrol pada lingkungan proteinase tidak seimbang maka akan menyebabkan kerusakan serius. Banyak pathogen mempunyai sendiri sistein proteinase untuk menginvasi inangnya. Mengganggu aktivitas sistein proteinase dan inhibitor alaminya dapat dihubungkan dengan beberapa kondisi patologis seperti arthritis, kekacauan system syaraf, dan kanker (Hultman 2003).
Inhibitor proteinase sistein meliputi peptida diazometana, peptida epoksida, florometil keton, asilometil keton, dan sistatin. Semuanya bersifat
irreversible kecuali sistatin yang bersifat reversible. Mekanisme penghambatan oleh peptida diazometana melalui pembentukan sistin teralkilasi, sedangkan peptida epoksida melalui pembentukan gugus alkil pada sisi aktifnya. Peptida klorometil keton menghambat enzim dengan cara mengikat protein melalui alkilasi pada sisi aktif histidin oleh klorometil (Salvesen dan Nagase 2001).
Inhibitor sistein proteinase dari hewan dan mamalia dapat berupa sistatin yang dibagi kedalam tiga kelompok, yaitu stefin, sistatins, dan kininogens. Pada umumnya, semua inhibitor sistein proteinase mempunyai stabilitas yang besar terhadap suhu tinggi (sampai 100 oC) dan pH yang ekstrim (LMW-CPIs pH 2-12, kininogens pH 5-12) maupun spesifitasnya pada sistein proteinase (Otto dan Schirmeister 1997).
10
stefin, sistatin A, B dan rat cystatin β. Kelompok II sistatin, mempunyai karakteristik dua ikatan disulfida dengan jumlah asam amino 110-120, seperti
human cystatin, chiken cystatin, dan rat cystatin. Kelompok I dan II ini
mempunyai berat molekul 10 sampai 20 kDa. Kelompok III sistatin adalah kininogen yang mempunyai rantai tunggal glikoprotein yang mengandung 3 domain like cystatin dengan berat molekul 68 sampai 120 kDa (Oliviera et al. 2003 ; Ustadi et al. 2005).
Inhibitor endogenous dari sistein proteinase yaitu sistatin telah dilaporkan dapat bereaksi sebagai agen pertahanan melawan bakteri, virus, dan hama. Salah satu sistatin yang ditemukan dari kulit tikus dan juga pada manusia. Lingkungan tempat ikan hidup yang penuh dengan pathogen dapat memungkinkan juga kulit ikan mengandung mekanisme pertahanan nonspesifik (Hultman 2003).
Interaksi antara proteinase sistein dan inhibitornya telah menjadi tujuan beberapa penelitian pada dua dekade ini. Spesifik inhibitor dari sistein protease sangat dibutuhkan untuk mencegah terjadinya proteolisis yang destruktif dan juga dapat dimanfaatkan pada proses terapi dan pada bahan penelitian. Pengertian yang mendalam pada interaksi sistein proteinase dan inhibitornya dapat memberikan informasi penting unutuk mengontrol aktivitas proteolitik (Hultman 2003).
4
Tabel 1 Beberapa penelitian mengenai purifikasi inhibitor enzim dari jaringan hewan
11
Peneliti dan bahan
Bahan
penelitian Teknik pemurnian Hasil purifikasi
Aktivitas dan
- ion exchange kromatografi - RP-HPLC
12
2.4.2 Mekanisme Kerja Inhibitor Protease
Hambatan yang dilakukan oleh inhibitor dapat dibagi menjadi dua jenis, yaitu hambatan tidak dapat balik (irreversible) dan hambatan dapat balik
(reversible). Hambatan tidak dapat balik pada umumnya disebabkan oleh
terjadinya proses destruksi atau modifikasi sebuah gugus atau lebih yang terdapat pada molekul enzim inhibitor (Carreno dan Cortes 2000). Inhibitor tidak dapat balik (irreversible) atau disebut juga inactivator, selalu mengikat enzim secara kovalen (Otto dan Schirmeister 1997).
Hambatan dapat balik (reversible) biasanya merupakan interaksi non kovalen antar enzim dan inhibitor (Otto dan Schirmeister 1997). Hambatan dapat balik terdiri dari hambatan bersaing (kompetitif) dan tidak bersaing (non kompetitif). Hambatan bersaing disebabkan karena ada molekul yang mirip dengan substrat, yang dapat pula membentuk kompleks, yaitu kompleks enzim inhibitor (EI). Pembentukan kompleks EI ini sama dengan pembentukan kompleks ES (enzim substrat), yaitu melalui penggabungan inhibitor dengan enzim pada bagian aktif enzim, sehingga terjadi persaingan antara inhibitor dengan substrat terhadap bagian aktif enzim. Inhibitor bersaing menghalangi terbentuknya kompleks ES dengan cara membentuk kompleks EI. Berbeda dengan kompleks ES, kompleks EI tidak dapat membentuk produk (P). Ciri inhibitor kompetitif ini adalah penghambatan dapat dibalikkan atau diatasi hanya dengan meningkatkan konsentrasi substrat (Lehninger 1993).
13
2.5 Pemurnian Enzim dan Inhibitor Enzim
Pemurnian enzim dan inhibitor endogenous enzim secara umum mempunyai teknik pemurnian yang sama, karena bentuk molekul dari inhibitor (natural protease inhibitor) dapat berupa protein. Inhibitor alami proteinase banyak berupa protein dengan ukuran molekul berkisar 3.000-800.000 Da. (Nagase dan Salvesen 2001). Tujuan utama pemurnian enzim adalah mengisolasi enzim murni dengan aktivitas spesifik yang tinggi dan kemurnian maksimal pada tingkat rendemen maksimal dengan biaya yang efektif (Harris dan Angal 1989 diacu dalam Wijaya 2005). Pemurnian enzim secara umum dapat dibagi menjadi ekstraksi, pemekatan, dan fraksinasi. Pemilihan tahapan pemurnian secara tepat sangat berpengaruh terhadap kriteria enzim murni yang dihasilkan.
Enzim dan inhibitor protease endegenous dari hewan, seperti pada ikan, pada umumnya terletak pada jaringan dan organ-organ khusus atau intraseluler sehingga dibutuhkan teknik tertentu untuk mengekstraknya. Tahap awal untuk ekstraksi enzim intraseluler adalah pemecahan sel melalui proses mekanis (agitasi, sonikator, homogenasi, dan lainnya) atau non mekanik dengan manipulasi lingkungan, kimiawi, dan enzimatis (Suhartono 1989). Aktivitas inhibitor yang terdeteksi terdapat pada ekstrak kasar, selanjutnya dilakukan fraksinasi inhibitor, dengan ammonium sulfat, pelarut organik, fraksinasi dengan polietilen glikol, kromatografi gel filtrasi, atau penukar ion. Proses ini dapat menentukan peningkatan aktivitas spesifik inhibitor setelah fraksinasi (Nagase dan Salvesen 2001).
14
Pemekatan enzim dan inhibitor protease yang berupa protein pada dasarnya sama dengan pemurnian enzim, yaitu dilakukan untuk memisahkan konsentrat protein dari komponen biomolekul lainnya, seperti karbohidrat, lipid, dan asam nukleat. Berbagai metode pemekatan yang lazim digunakan dalam pemurnian enzim, yaitu pelarut organik, presipitasi dengan garam, polimer, dialisis, ultrafiltrasi, dan liofilisasi (Rosenberg 1996).
Pemekatan enzim dan inihibitor protease endogenous dilakukan untuk memisahkan konsentrat protein dari komponen biomolekul lainnya. Beberapa metode pemekatan yang banyak digunakan dalam pemurnian enzim atau inhibitor adalah presipitasi dengan garam. Presipitasi untuk memurnikan enzim antara lain adalah presipitasi dengan pengaturan pH, peningkatan kekuatan ion, penurunan kekuatan ion, dan penggunaan pelarut organik. Presipitasi yang paling banyak digunakan adalah peningkatan kekuatan ion atau lebih dikenal dengan nama salting out (Rosenberg 1996). Presipitasi dengan garam (ammonium sulfat dan natrium sulfat) lebih disukai daripada presipitasi dengan pelarut organik, seperti etanol dan aseton. Ammonium sulfat sering digunakan karena kelarutannya tinggi, harganya murah, dan umumnya tidak mempengaruhi struktur protein atau menstabilkan protein enzim (Suhartono 1989).
Presipitasi protein menggunakan ammonium sulfat dapat menyebabkan dehidrasi lingkungan mikro dari molekul protein. Ion-ion dari garam, seperti ion sulfat (SO42-) akan menarik dan mengikat molekul air dari koloid protein. Pada
konsentrasi rendah, ion-ion ini akan mengisi lingkungan molekul protein sehingga protein melarut yang disebut salting in. Pada konsentrasi tinggi terjadi peningkatan muatan listrik yang akan menarik molekul air dari koloid protein sehingga interaksi hidrofobik diantara sesama molekul protein akan menurunkan kelarutan protein sehingga terjadi salting out yang menyebabkan protein mengendap (Suhartono 1989 ; Rosenberg 1996).
15
2.6. Elektroforesis SDS-PAGE
Elektroforesis merupakan teknik pemisahan senyawa berdasarkan kecepatan migrasi dari senyawa bermuatan listrik dibawah pengaruh medan listrik. Beberapa matriks yang banyak digunakan adalah agarose dan poliakrilamida (Westermeier 2005). Elektroforesis gel poliakrilamida (poly
acrilamide gel electrophoresis) merupakan metode yang sering digunakan dalam
analisis sampel biologis karena kemampuannya dalam memisahkan campuran protein kompleks dengan baik dengan resolusi yang tinggi (Rosenberg 1996).
Molekul-molekul biologis yang bermuatan listrik di dalam larutan akan bergerak ke arah elektroda yang polaritasnya berlawanan dengan muatan molekul. Prinsip inilah yang digunakan untuk memisahkan molekul-molekul dengan muatan berbeda. Beberapa contoh partikel yang bermuatan, yaitu asam amino, protein, asam nukleat, dan ion-ion (Westermeier 2005).
Metode ini menggunakan matriks dari gel yang disusun oleh akrilamida dan N,N’-metilen-bis-akrilamida yang berpolimerisasi melalui mekanisme radikal bebas dengan bantuan katalisator N,N,N’,N’,-tetramethylene-diamine (TEMED) dan inisiator ammonium persulfate (APS) (Rosenberg 1996 ; Westermeier 2005). Poliakrilamida adalah polimer dari monomer akrilamida. Pada saat polimer terbentuk, Poliakrilamida berubah menjadi gel dan digunakan untuk menarik protein melalui gel sehingga keseluruhan proses disebut SDS-PAGE. Gel poliakrilamida tidaklah padat tetapi membentuk saluran labirin yang menghubungkan antar pori fiber. Molekul yang berukuran kecil dapat melewati gel poliakrilamida lebih cepat dibanding molekul besar. Setelah proses dihentikan kemudian dilakukan proses pewarnaan protein (Westermeier 2005).
16
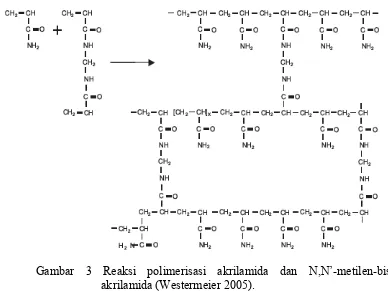
Reaksi polimerisasi akrilamida dan N,N’-metilen-bis-akrilamida dapat dilihat pada Gambar 3.
Gambar 3 Reaksi polimerisasi akrilamida dan N,N’-metilen-bis-akrilamida (Westermeier 2005).
2.7. Kromatografi
Kromatografi merupakan teknik pemisahan dengan mengadakan manipulasi atas dasar perbedaan sifat-sifat fisik dari zat-zat yang menyusun suatu campuran. Kromatografi juga termasuk teknik isolasi komponen dalam suatu campuran menggunakan medium yang mengalir pada liquid atau gas yang disebabkan perbedaan migrasi setiap komponen. Aliran tersebut biasanya menggunakan tekanan atau gravitasi. Teknik kromatografi secara mendasar terdiri dari empat kelompok, yaitu gel filtrasi, ion exchange, interaksi hidrofobik, dan kromatografi afinitas (Rosenberg 1996).
17
Tabel 2 Metode kromatografi untuk fraksinasi protein Sifat protein Teknik pemisahan
Hidrofobik
Ukuran dan bentuk molekul Titik isoelektrik
Muatan
Biospesifik terhadap ligan, inhibitor, reseptor, antibodi dll.
-Interaksi hidrofobik dan fase balik kromatografi -Filtrasi gel
-kromatofokusing
-Ion exchange kromatografi -Kromatografi afinitas
Sumber : APB (2001)
Kromatografi penukar ion (ion exchange chromatography) merupakan teknik pemisahan berdasarkan muatan dengan memanfaatkan sifat amfoter dari protein. Pengisi kolom merupakan senyawa polimer elastik dengan kerangka resin sintetik berupa polistirena yang dikaitkan dengan suatu gugus fungsional yang akan berinteraksi dengan molekul enzim. Dietilaminoetil (DEAE) selulosa merupakan penukar ion yang paling banyak digunakan untuk keperluan fraksinasi enzim dan merupakan penukar anion lemah yang bekerja pada kisaran pH 2-9. Penukar ion paling baik dipergunakan pada tahap awal kromatografi dengan kapasitas yang tinggi (Suhartono 1989; Rosenberg 1996).
3. METODOLOGI
3.1 Waktu dan Tempat Penelitian
Penelitian ini dimulai pada bulan Januari 2009 dan selesai pada bulan November 2009. Penelitian dilakukan di Laboratorium Biokimia dan Bioteknologi II, Departemen Teknologi Hasil Perairan (FPIK-IPB), Laboratorium Immunologi, Fakultas Kedokteran Hewan, Laboratorium Pusat Penelitian Sumberdaya Hayati dan Bioteknologi (PAU) IPB.
3.2 Alat dan Bahan
Bahan utama yang digunakan pada penelitian adalah ikan bandeng (Chanos chanos, Forskal) dan ikan patin (Pangasius sp.). Ikan patin dan ikan bandeng dibawa dalam keadaan hidup ke laboratorium, dimatikan dan dipreparasi untuk diambil bagian daging, kulit, dan jeroan. Bahan-bahan kimia yang digunakan untuk ekstraksi dan analisis adalah tris base (Applichem), asam sitrat (Applichem), ammonium sulfat ((NH4)2SO4), sodium fosfat (Merck), sodium
azida (Merck), 2-merkaptoetanol (Sigma), asam trikloro asetat (TCA) (Merck), tirosin (Applichem), folin (Merck), hemoglobin (Sigma), commasive brilliant blue
R-250 (Sigma), bovine serum albumin (BSA) (Applichem). Logam-logam yang digunakan untuk mengetahui karakterisasi enzim yaitu CaCl2 NaCl, MnCl2 dan
CoCl2 dari Merck. Inhibitor komersial seperti PMSF, EDTA dan pepstatin. Bahan
untuk purifikasi digunakan DEAE sephadex A-50 dan sephadex-G100 (pharmacia). Penentuan berat molekul digunakan SDS poliakrilamida (SDS-PAGE), prestained protein marker dengan berat molekul 175-7 kDa (NE Biolabs) yang terdiri dari MBP (maltose-binding protein) -β-galactosidase (175 kDa), MBP-paramyosin (80 kDa), MBP-CBD (chitin binding domain) (58 kDa),
CBD-Mxe Intein-2CBD (46 kDa), CBD-Mxe Intein (30 kDa), CBD-BmFKBP13 (25 kDa), lysozyme (17 kDa), aprotinin (7 kDa),
19
3.3 Metode Penelitian
Penelitian ini dilakukan melalui beberapa tahapan, yaitu preparasi bahan baku berupa ikan bandeng dan ikan patin yang diambil dari kulit, daging, dan jeroan. Tahapan selanjutnya, yaitu purifikasi inhibitor katepsin yang meliputi ekstraksi inhibitor katepsin, presipitasi, dan dialisis, pemurnian dengan kromatografi, dan karakterisasi inhibitor. Tahapan metode penelitian dapat dilihat pada Gambar 4.
Ammonium sulfat variasi tingkat kejenuhan
Kulit, daging, dan Jeroan
Ektraksi Tiga Inhibitor katepsin kasar
Kromatografi
Ikan patin dan bandeng segar
Preparasi
Pengukuran aktivitas inhibitor dengan substrat katepsin
Pemilihan kantong dialisis
20
3.3.1 Ekstraksi Enzim Katepsin (Dinu et al. 2002)
Ekstraksi dilakukan dengan preparasi sampel untuk memperoleh ekstrak kasar protease katepsin. Proses ekstraksi menggunakan ikan bandeng yang sudah post rigor. Daging ikan diambil dan disuspensikan dalam akuades dengan perbandingan daging ikan dan akuades sebesar 1:1, lalu dihomogenisasi pada suhu 0-4 0C. Skema ekstraksi enzim katepsin dari ikan bandeng dapat dilihat pada Gambar 5.
Daging ikan (100 gr) + akuades 1:1
Homogenisasi
600 x g, 10 mnt, 4 oC
Supernatan
Pelet 1
10.000 x g, 10 mnt, 4 oC
Pelet 1 Supernatan
4.000 x g, 10 mnt, 4 oC
Ekstrak protease katepsin
Pelet 1
Buffer tris HCl 0,1 M pH 7,4 (100 ml) +
Gambar 5 Diagram alir proses ekstraksi enzim katepsin dengan teknik differensial sentrifugasi (Dinu et al. 2002).
21
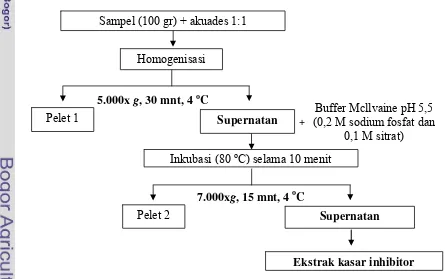
3.3.2 Ekstraksi Inhibitor Katepsin (An et al. 1995)
Ekstraksi dilakukan masing-masing pada bagian kulit, jeroan, dan daging ikan. Preparasi ikan bandeng dan ikan patin dilakukan saat setelah ikan dimatikan. Sebanyak 100 g sampel dihomogenasi dengan 100 ml akuades dingin (dibawah 4 oC), selanjutnya disentrifugasi dingin pada kecepatan 5.000 x g selama 30 menit. Supernatannya diambil dan ditambahkan buffer McIlvaine’s pH 5,5 (dibuat dari 0,2 M sodium fosfat dan 0,1 M asam sitrat (lampiran 1)) dengan jumlah yang sama dengan supernatan.
Campuran diinkubasi selama 10 menit pada suhu 60, 70, dan 80 oC, selanjutnya disentrifugasi kembali pada kecepatan 7.000 x g selama 15 menit. Supernatannya diambil dan disimpan suhu dingin. Hasil ekstraksi berupa ekstrak kasar inhibitor katepsin kemudian dianalisis aktivitasnya dan dipilih aktivitas dengan penghambatan tertinggi dari salah satu ketiga sampel (jeroan, kulit, dan daging) sebagai sumber inhibitor katepsin untuk dimurnikan lagi dengan presipitasi dan dialisis. Proses ekstraksi inhibitor enzim katepsin dapat dilihat pada Gambar 6.
Buffer Mcllvaine pH 5,5 (0,2 M sodium fosfat dan
0,1 M sitrat)
5.000x g, 30 mnt, 4 oC
7.000xg, 15 mnt, 4 oC
+
Sampel (100 gr) + akuades 1:1
Homogenisasi
Supernatan
Pelet 1
Pelet 2 Supernatan
Ekstrak kasar inhibitor
Inkubasi (80 oC) selama 10 menit
22
3.3.3. Presipitasi dan Dialisis (Ustadi et al. 2005)
Inhibitor katepsin ekstrak kasar dipresipitasi atau diendapkan dengan menggunakan ammonium sulfat ((NH4)2SO4) dengan variasi tingkat kejenuhan
30% sampai 80% (w/v). Pengendapan dilakukan dengan menambahkan garam ammonium sulfat ke dalam supernatan (ekstrak kasar inhibitor katepsin) sedikit demi sedikit. Campuran didiamkan selama semalam pada suhu sekitar 4 oC, selanjutnya disentrifugasi pada kecepatan 12.000 x g selama 30 menit.
Hasil pengendapan, yaitu presipitat dilarutkan dalam buffer A (buffer McIlvaine’s pH 5,5 yang dibuat dari 0,2 M sodium fosfat dan 0,1 M asam sitrat). Konsentrasi ammonium sulfat dalam ekstrak dapat dikurangi dengan melakukan proses dialisis menggunakan kantong dialisis dengan ukuran molecular weight cut off (MWCO) yang sesuai (12 kDa). Proses dialisis dilakukan selama 4 jam dengan larutan buffer B yang dibuat dari 20 mM buffer Tris pH 7,5 yang mengandung 10 mM sodium azida dan 10 mM 2-merkaptoetanol. Hasil dialisis, yaitu inhibitor katepsin semi murni kemudian dimurnikan lagi dengan kromatografi.
3.3.4. Pemurnian dengan Kromatografi (Ustadi et al. 2005)
Tahap pemurnian pertama dilakukan dengan kromatografi penukar ion dengan bahan pengelusi buffer B. Sedangkan matriksnya menggunakan kolom DEAE sephadex A-50 (3,0 x 30,0 cm) dengan laju aliran 1 mL/menit. Selain itu juga digunakan NaCl bergradien 0-0,7 M. Jumlah volume tiap fraksi ditampung sebanyak 5 ml. Masing-masing fraksi diuji konsentrasi protein dengan spektrofotometer uv λ=280 nm dan diukur aktivitasnya tiap fraksi dengan metode Dinu et al. (2002).
23
3.3.5. Karakterisasi Inhibitor Katepsin
Karakterisasi inhibitor katepsin dilakukan terhadap ekstrak kasar dan hasil pengendapan dengan ammonium sulfat. Karakterisasi meliputi penentuan suhu optimum, pH optimum, stabilitas panas dan pH, pengaruh ion logam, serta penentuan bobot molekul.
3.4. Prosedur Analisis
Analisis yang dilakukan meliputi aktivitas katepsin, konsentrasi protein, dan aktivitas inhibitor katepsin.
3.4.1 Aktivitas Katepsin (Dinu et al. 2002)
Aktivitas proteolitik dari katepsin diuji menggunakan hemoglobin terdenaturasi asam sebagai substratnya. Sebanyak 8% (w/v) hemoglobin dilarutkan dalam akuades dengan perbandingan 1:3. Kemudian pH dibuat menjadi 2,0 dengan HCl 1 N dan konsentrasi akhir hemoglobin dibuat menjadi 2% (w/v) dengan akuades. Prosedur pengukuran aktivitas katepsin disajikan pada Tabel 3.
Tabel 3 Prosedur untuk mengukur aktivitas protease katepsin
Pereaksi sample (ml) standar (ml) blanko (ml) Buffer tris 0,1 M pH 7,4 0,1 0,1 0,1
Disaring dengan kertas saring
Filtrat 1 1 1
Folin 1 1 1
Didiamkan pada 37 oC, 20 menit Diukur pada spektrofotometer λ 750 nm
Aktivitas enzim katepsin dapat dihitung dengan rumus berikut:
UA = jumlah tirosin yang dihasilkan per ml enzim per menit P = faktor pengenceran
24
Sebanyak 0,5 ml dari larutan substrat diinkubasi dengan 0,1 ml larutan enzim pada 37 ºC selama 10 menit. Reaksi dihentikan dengan penambahan 2 ml TCA 5% (w/v). Campuran disaring dan hasil reaksi yang dapat larut ditambah dengan 1 ml pereaksi folin. Campuran kemudian diukur dengan spektrofotometer pada λ=750 nm. Selain itu, dilakukan pula pengukuran untuk larutan blanko dan larutan standar dengan prosedur yang sama seperti larutan sampel, hanya untuk larutan blanko dan larutan standar enzimnya digantikan dengan akuades dan tirosin. Setiap sampel yang dianalisis harus disertai dengan blanko dan standar.
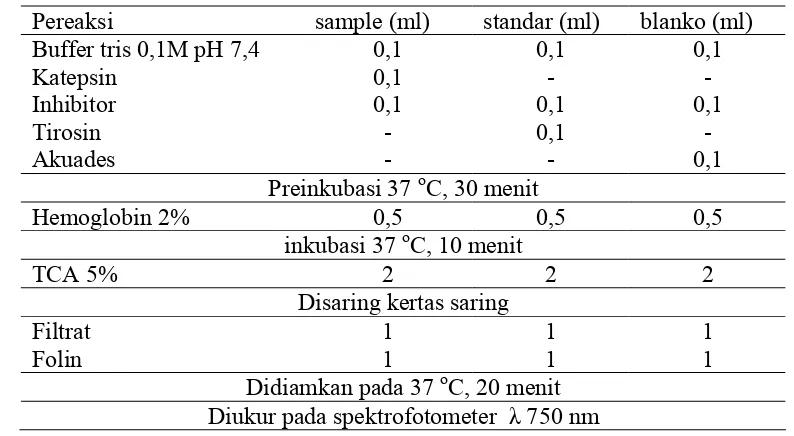
3.4.2 Uji Aktivitas Inhibitor katepsin (Dinu et al. 2002)
Uji ini ditentukan dengan mengukur derajat penghambatan dari aktivitas katepsin menggunakan substrat hemoglobin (lampiran 2). Uji ini di mulai dengan mereaksikan ekstrak inhibitor 0,1 ml dengan katepsin 0,1 ml selama 30 menit pada suhu inkubasi 37 oC. Selanjutnya ditambahkan 0,5 ml dari larutan substrat hemoglobin 2% (w/v) dan diinkubasi kembali pada 37 ºC selama 10 menit. Reaksi dihentikan dengan penambahan 2 ml TCA 5% (w/v). Campuran disaring dan hasil reaksi yang dapat larut ditambah dengan 1 ml pereaksi folin, kemudian campuran diukur dengan spektrofotometer pada λ=750 nm. Prosedur pengukuran inhibitor protese katepsin dapat dilihat pada Tabel 4.
Tabel 4 Prosedur pengukuran aktivitas inhibitor katepsin
25
Selain itu dilakukan pula pengukuran untuk larutan blanko dan larutan standar dengan prosedur yang sama seperti larutan sampel hanya untuk larutan blanko dan larutan standar, enzim katepsin digantikan dengan akuades dan tirosin. Setiap sampel yang dianalisis, harus disertai dengan uji aktivitas katepsin tanpa penambahan inhibitor. Aktivitas inhibitor dihitung berdasarkan perbedaan aktivitas enzim katepsin dengan inhibitor dan yang tanpa inhibitor.
Aktivitas enzim katepsin dapat dihitung dengan rumus berikut:
Satu unit inhibitor katepsin adalah jumlah inhibitor katepsin yang mampu menghambat aktivitas protease katepsin sebesar 50% pada kondisi pengujian.
3.4.3 Pengukuran Konsentrasi Protein (Bradford 1976)
Konsentrasi protein ditentukan menggunakan metode Bradford dengan
bovine serum albumin sebagai standar. Persiapan pereaksi Bradford dilakukan
26
(lampiran 3). Berdasarkan kurva tersebut dapat ditentukan konsentrasi protein dalam sampel. Tabel komposisi volume larutan dengan pembuatan larutan standar dengan konsentrasi 0,01-0,3 mg/ml dari larutan stok BSA konsentrasi 2 mg/ml disajikan pada Tabel 5.
Tabel 5 Pembuatan larutan standar BSA konsentrasi 0,01-0,3 mg/ml Konsentrasi BSA (mg/ml) Volume BSA (ml) Volume akuades (ml)
0,00 0,00 10,00
3.4.4 Penentuan Berat Molekul dengan SDS-PAGE
Metode SDS-PAGE (sodium dodecyl sulphate-polyacrylamide gel electrophoresis) yang dikerjakan dalam penelitian ini menggunakan 4 % stacking gel dan 10% gel akrilamida (lampiran 4). Metode ini menggunakan matriks dari gel yang disusun oleh akrilamida dan N,N’-metilen-bis-akrilamida yang berpolimerisasi melalui mekanisme radikal bebas dengan bantuan katalisator N,N,N’,N’,-tetramethylene-diamine (TEMED) dan inisiator ammonium persulfate (APS) (Rosenberg 1996). Komposisi pembuatan gel penahan dan pemisah SDS-PAGE dapat dilihat pada Tabel 6.
Tabel 6 Komposisi gel penahan dan pemisah SDS-PAGE
Komponen Gel pemisah (8%) Gel penahan (4%) Larutan stok akrilamida 2,66 ml 0,67 ml Buffer gel pemisah 2,50 ml -Buffer gel pengumpul - 1,25 ml
Akuades 3,18 ml 3,00 ml
Ammonium persulfat 10% 50,00 µl 50,00 µl
27
Konsentrasi akrilamida yang digunakan dalam analisis ini adalah 10% (w/v). Pewarnaan yang digunakan adalah pewarnaan perak. Deteksi SDS-PAGE dilakukan dengan melepaskan gel hasil elektroforesis dari cetakan dan diukur jarak migrasi bromphenol blue. Gel tersebut dicelup dan direndam dalam larutan fiksasi (25% methanol + 12% asam asetat) selama 1 jam sambil digoyang konstan. Kemudian direndam dalam 50% (v/v) etanol selama 20 menit, kemudian diganti dengan 30% (v/v) etanol selama 2x20 menit. Larutannya diganti dengan larutan pengembang kemudian dicuci dengan akuabidestilata. Setelah dicuci ditambahkan larutan perak nitrat selama 30 menit kemudian dicuci lagi dengan akuabidestilata 2x20 detik dan ditambahkan larutan campuran Na2CO3 dan
4. HASIL DAN PEMBAHASAN
4.1 Optimasi Proses Ekstraksi Inhibitor Katepsin
Optimasi proses ekstraksi dilakukan untuk mendapatkan inhibitor protease katepsin dengan aktivitas penghambatan yang tinggi. Pada tahap ini dilakukan ekstraksi inhibitor pada tiga bagian ikan, yaitu pada daging, kulit, dan jeroan dengan perlakuan inkubasi ekstraksi pada suhu 60, 70, dan 80 oC. Hasil penelitian menunjukkan bahwa aktivitas terbaik diperoleh pada ekstrak daging pada waktu suhu inkubasi ekstraksi 80 oC baik pada ekstrak ikan bandeng maupun ekstrak ikan patin, sedangkan untuk ekstrak dari jeroan tidak menunjukkan adanya aktivitas penghambatan protease katepsin. Hasil penghambatan ekstrak inhibitor dari ikan bandeng dan ikan patin dapat dilihat pada Gambar 7.
87.84
Gambar 7 Persen (%) penghambatan aktivitas katepsin pada ekstrak inhibitor ikan bandeng (1) dan ikan patin (2). (□) suhu 60 oC, (□) suhu 70 oC, (□) suhu 80 oC.
29
Ekstrak inhibitor dari kulit ikan pada suhu ekstraksi 80 oC, juga menunjukkan aktivitas yang cukup tinggi, yaitu 77,72% pada ikan bandeng dan 77,24% pada kulit ikan patin. Hasil beberapa penelitian lain menunjukkan adanya inhibitor protease pada kulit, yaitu penelitian Ylonen et al. (2002) yang melakukan pemurnian inhibitor dari kulit ikan wolffish dan atlantic cod, serta penelitian Olonen (2004), melakukan pemurnian inhibitor dari kulit ikan salmon. Kedua penelitian tersebut berhasil memurnikan inhibitor protease berupa kininogen yang termasuk inhibitor sistein proteinase. Penelitian Olonen et al.
(2003), juga menemukan inhibitor sistein proteinase tipe baru berupa salarin dari ikan Atlantic salmon (Salmo salar L.) dan ikan Arctic charr (Salvelimus alpinus).
Gambar 8 menunjukkan bahwa ekstrak inhibitor dari daging mengandung protein lebih tinggi dari pada ekstrak inhibitor dari kulit, kecuali pada eksrak inhibitor jeroan ikan bandeng. Hal ini karena bandeng merupakan ikan herbivora sehingga jeroannya masih banyak pengotor dari sisa makanan yang dapat terekstrak. Perlakuan inkubasi dari suhu 60 oC sampai suhu 80 oC selama 10 menit dapat menurunkan konsentrasi protein. Hal ini karena sifat enzim dan protein yang mudah mengalami kerusakan (terdenaturasi) sehingga mengalami pengendapan. Inhibitor endegenous dari kelas inhibitor proteinase sistein mempunyai sifat lebih tahan panas dibandingkan dengan enzim dan protein lainnya, sehingga proses panas ini dapat memisahkan inhibitor dengan protein atau enzim lainnya
30
Beberapa inhibitor protease dapat stabil setelah perlakuan panas pada suhu 95 oC selama 15 menit, seperti TIMPs dan sistatin (Nagase dan Salvesen 2001). Inhibitor sistein proteinase dari hewan dan mamalia berupa sistatin dibagi dalam tiga kelompok yaitu stefin, sistatin dan kininogen, pada umumnya mempunyai stabilitas yang besar terhadap suhu tinggi (sampai 100 oC) (Otto dan Schirmeister 1997).
Hasil penelitian awal dari proses optimasi ekstraksi inhibitor terbaik digunakan sebagai acuan untuk tahap penelitian selanjutnya, yaitu produksi inhibitor protease katepsin dengan ekstraksi dari bagian daging ikan pada suhu ekstraksi 80 oC. Penelitian An et al. (1995) menemukan adanya inhibitor yang berikatan kompleks dengan katepsin L pada daging ikan pacific whitening dan berhasil melakukan pemisahan katepsin dengan inhibitor melalui perlakuan asam, sedangkan penelitian Ustadi et al. (2005) berhasil melakukan pemurnian inhibitor dari telur ikan glassfish pada perlakuan suhu 80 oC pada saat ekstraksi.
4.2 Produksi dan Pemurnian Inhibitor Katepsin
Proses pemurnian yang dilakukan dalam penelitian ini ada beberapa tahapan yang meliputi ekstraksi daging ikan patin sebagai ekstrak kasar inhibitor, presipitasi inhibitor protease menggunakan ammonium sulfat, dilakukan proses dialisis kemudian dilanjutkan dengan pemurnian inhibitor menggunakan kromatografi penukar ion dan gel filtrasi.
4.2.1 Ekstraksi Inhibitor Katepsin
31
disajikan pada Gambar 9 dan Gambar 10. Hasil pengendapan dengan aktivitas penghambatan tertinggi digunakan untuk tahap dialisis.
0.0
Gambar 9 Persentase (%) aktivitas penghambatan inhibitor katepsin ikan bandeng setelah pengendapan ammonium sulfat (A) ; konsentrasi protein setelah pengendapan dangan ammonium sulfat (B). —■— endapan, —▲— supernatan
Berdasarkan Gambar 9 dapat dilihat adanya peningkatan aktivitas penghambatan inhibitor hasil endapan (pelet) pada beberapa tingkat konsentrasi ammonium sulfat. Aktivitas persen penghambatan optimum terdapat pada hasil endapan dengan konsentrasi ammonium sulfat 70%. Hasil supernatan menunjukkan penurunan aktivitas persen (%) penghambatan. Ekstrak dari ikan Patin yang dipresipitasi dengan ammonium sulfat (Gambar 10) menunjukkan peningkatan aktivitas penghambatan pada hasil endapan 70%, dan mengalami penurunan aktivitas pada bagian supernatan.
(B) (B)
32
Hasil presipitasi pada kedua ekstrak inhibitor menyebabkan penurunan kadar protein dalam supernatan, sedangkan pada hasil endapan (pelet) terjadi peningkatan konsentrasi protein. Hasil presipitasi yang mempunyai aktivitas persen penghambatan paling tinggi, digunakan untuk pemurnian tahap selanjutnya. Hasil pengendapan dengan konsentrasi ammonium sulfat 70% bagian pelet merupakan ekstrak terpilih untuk dilakukan proses dialisis.
4.2.2 Pemurnian Inhibitor Katepsin dengan Kolom Kromatografi
Hasil pengendapan kemudian didialisis dengan tujuan untuk menghilangkan sisa-sisa garam yang digunakan saat pemekatan. Proses dialisis juga dapat memisahkan molekul besar dari molekul kecil berdasarkan sifat semi permeabel untuk meloloskan molekul kecil dan menahan molekul-molekul yang berukuran besar. Inhibitor katepsin setelah melalui tahap dialisis kemudian dimurnikan dengan 2 tahap. Tahap pertama dilakukan dengan penukar ion menggunakan matriks sephadex A-50. Tahap kedua kromatografi filtrasi gel menggunakan matrik sephadex G-100.
Tahap pertama pemurnian dilakukan dengan kromatografi penukar ion. kromatografi ini mempunyai matrik sephadex dengan gugus fungsionalnya DEAE (dietilaminoetil) yang merupakan penukar anion dengan kisaran pH 2- 9. Teknik kromatografi penukar ion sangat baik dipergunakan pada tahap awal kromatografi (Rossenberg 1996).
33
Gambar 11 Pemurnian inhibitor katepsin menggunakan kromatografi penukar ion DEAE sephadex A-50. –●– konsentrasi protein, –×– aktivitas inhibitor, — gradien NaCl (M).
Prinsip pemurnian dengan filtrasi gel adalah pemisahan protein berdasarkan ukuran partikel dan sangat baik digunakan pada tahap akhir pemurnian enzim (Rosenberg 1996). Pada tahapan ini digunakan fase bergerak yaitu buffer B yang dibuat dari 20 mM buffer Tris pH 7,5 yang mengandung 10 mM sodium azida dan 10 mM 2-Merkaptoetanol, dan fase diamnya adalah sephadex G-100 (1,5 x 40,0 cm). Hasil pemurnian inhibitor protease katepsin dengan kromatografi filtrasi gel disajikan pada gambar 12.
No. Fraksi
34
Berdasarkan Gambar 12 dapat dilihat adanya puncak aktivitas inhibitor pada fraksi ke 8 dengan aktivitas sebesar 1,8281 U/ml dengan konsentrasi protein sebesar 0,0268 mg/ml. Fraksi tersebut merupakan ekstrak murni inhibitor protease katepsin yang selanjutnya ditentukan bobot molekulnya dengan SDS-PAGE.
4.2.3 Produksi Inhibitor Katepsin
Produksi dilakukan berdasarkan penelitian dari tahap awal yaitu menggunakan ekstrak daging patin, karena mempunyai aktivitas yang lebih tinggi dibandingkan ikan bandeng. Ekstrak kasar inhibitor katepsin yang dihasilkan dari ikan patin mempunyai aktivitas 1,6450 U/ml dengan konsentrasi protein 0,4081 mg/ml sehingga aktivitas spesifiknya sebesar 4,03 U/mg.
Ekstrak kasar selanjutnya diendapkan dengan ammonium sulfat 70% (w/v). Endapan yang dihasilkan dilarutkan dengan buffer pH 5,5. Endapan tersebut mempunyai aktivitas sebesar 1,722 U/ml dengan konsentrasi protein 0,3221 mg/ml sehingga aktivitas spesifiknya adalah 5,3475 U/mg. Kemudian didialisis dan diperoleh kandungan protein 8,1605 mg dengan aktivitas spesifik 5,805 U/mg. Inhibitor katepsin selanjutnya dimurnikan dengan penukar ion DEAE Sephadex A-50. Berdasarkan hasil pemurnian ini didapatkan aktivitas spesifik sebesar 18,762 U/mg dengan kelipatan pemurnian 4,65 kali. Tahap akhir pemurnian adalah filtrasi gel. Hasilnya menunjukkan peningkatan aktivitas spesifik yang cukup tinggi menjadi 68,159 U/mg dengan kelipatan kemurnian sebesar 16,91 kali. Data setiap tahap pemurnian dirangkum pada Tabel 7.
Tahap pemurnian
Volume (ml)
Protein (mg/ml)
Aktivitas inhibitor (U/ml)
Total protein (mg)
Total aktivitas
Aktivitas spesifik (U/mg)
Yield (%)
Kelipatan pemurnian Ekstrak kasar 300 0,4081 1,6450 122,4380 493,506 4,0306 100,00 1,00
Pengendapan 50 0,3221 1,7222 16,1029 86,111 5,3475 17,45 1,33 Dialisis 30 0,2720 1,5794 8,1605 47,381 5,8061 9,60 1,44 Penukar ion 5 0,1059 1,9867 0,5294 9,933 18,7625 2,01 4,65
Gel filtrasi 5 0,0268 1,8281 0,1341 9,141 68,1590 1,85 16,91 Tabel 7 Peningkatan aktivitas inhibitor katepsin pada berbagai tahap pemurnian
36
4.3 Karakterisasi Inhibitor Katepsin
Faktor-faktor utama yang mempengaruhi aktivitas enzim adalah konsentrasi enzim, substrat, produk, senyawa inhibitor dan aktivator, pH, jenis pelarut yang terdapat pada lingkungan, kekuatan ion, dan suhu (Suhartono 1989). Tujuan karakterisasi inhibitor katepsin ini untuk mengetahui kondisi optimum dari kerja inhibitor enzim. Karakterisasi dilakukan pada ekstrak kasar dari ikan bandeng dan ikan patin, dan pada ekstrak inhibitor katepsin setelah pengendapan ammonium sulfat dengan aktivitas penghambatan tertinggi. Karakterisasi yang dilakukan meliputi penentuan suhu dan pH optimum, stabilitas panas dan pH, kemudian dilakukan juga karakterisasi untuk mengetahui pengaruh beberapa ion logam terhadap ekstrak inhibitor katepsin..
4.3.1 Suhu Optimum
Inhibitor protease katepsin memiliki aktivitas maksimum pada suhu tertentu. Aktivitasnya akan meningkat seiring dengan peningkatan suhu sehingga mencapai suhu optimum. Setelah itu kenaikan suhu lebih lanjut akan menyebabkan aktivitas menurun. Suhu optimum inhibitor katepsin baik dari ekstrak kasar ikan patin, ekstrak ikan bandeng, dan ekstrak inhibitor ikan patin hasil pengendapan dengan ammonium sulfat, yaitu 40 oC seperti yang disajikan pada Gambar 13.
37
Ekstrak inhibitor protease katepsin masih mempunyai aktivitas yang cukup tinggi sampai suhu 70 oC. Pada saat suhu dinaikkan, maka akan menyebabkan peningkatan aktivitas inhibitor hinggga mencapai maksimum dan jika dilanjutkan terus naik maka akan menyebabkan penurunan aktivitas inhibitor dengan pola yang berbeda pada setiap bentuk inhibitor. Inhibitor proteinase sistein dapat bersifat thermostabil atau stabil pada suhu tinggi karena adanya asam amino hidrofobik, jembatan disulfida, dan intensitas interaksi elektrostatik. Rantai samping dari asam amino yang bersifat elektrostatik (bermuatan) seperti asam aspartat, asam glutamat, dan arginin menyebabkan struktur enzim dan inhibitor proteinase lebih kaku (rigid), sehingga sangat tahan terhadap perubahan suhu yang cukup tinggi.
Suhu mempengaruhi laju reaksi katalisis inhibitor enzim dengan dua cara. Pertama, kenaikan suhu akan meningkatkan laju reaksi inhibitor enzim sampai batas tertentu. Peningkatan suhu yang berlebih akan berpengaruh terhadap perubahan konformasi substrat (enzim), sehingga sisi aktif substrat (enzim) mengalami hambatan untuk memasuki sisi aktif inhibitor enzim, dan dapat menurunkan aktivitas inhibitor enzim. Kedua, peningkatan energi termal molekul yang membentuk struktur protein inhibitor enzim itu sendiri akan menyebabkan rusaknya interaksi nonkovalen seperti ikatan hidrogen, ikatan van der walls, ikatan hidrofobik, dan interaksi elektrostatik yang menjaga struktur tiga dimensi inhibitor enzim secara bersama-sama, sehingga inhibitor enzim mengalami denaturasi. Denaturasi protein menyebabkan struktur lipatan inhibitor enzim membuka pada bagian permukaannya sehingga sisi aktif inhibitor enzim berubah dan sebagai akibatnya akan terjadi penurunan aktivitas inhibitor enzim (Hames dan Hoper 2000).
4.3.2 Penentuan pH Optimum
38
menyebabkan enzim terdenaturasi yang menyebabkan enzim kehilangan aktivitas biologisnya (Lehninger 1993).
Inhibitor katepsin yang merupakan protein mengikuti sifat-sifat protein yang mempunyai konstanta disosiasi pada gugus asam maupun basa terutama pada gugus residu terminal karboksil dan terminal aminonya. Perubahan aktivitas inhibitor protease dapat terjadi akibat adanya perubahan ionisasi pada gugus ionik inhibitor pada sisi aktifnya maupun sisi lain yang secara tidak langsung mempengaruhi sisi aktif. Gugus ionik berperan dalam menjaga konformasi sisi aktif dalam mengikat substrat (enzim) (Nurhayati 2006). Gugus fungsional pada sisi aktif yang dapat terionisasi, memegang peranan penting pada suatu reaksi katalis enzim. Reaksi pengikatan dan pelepasan ion hidrogen pada gugus fugsional tersebut dapat dianggap sebagai reaksi antara enzim dengan suatu ligan secara umum (logam, asam, atau molekul lain) (Suhartono 1989).
Data mengenai pH optimum inhibitor katepsin disajikan pada Gambar 14. Berdasarkan Gambar 14 dapat dilihat bahwa pH optimum inhibitor protease katepsin dalam bentuk ekstrak kasar maupun setelah pengendapan dengan ammonium sulfat adalah 8. Ekstrak inhibitor dari ikan bandeng maupun ikan patin juga mempunyai pH optimum yang sama, berada pada kisaran pH 7-9. Kisaran pH ini menujukkan bahwa ekstrak inhibitor katepsin termasuk inhibitor protease alkalin atau bersifat basa.
0
39
Penelitian yang lain menunjukkan bahwa inhibitor protease seperti sistatin mempunyai aktivitas penghambatan pada kisaran pH alkalin. Penelitian Ustadi et al. (2005), ekstrak inhibitor protease dari telur ikan glassfish
mempunyai aktivitas yang tinggi pada kisaran pH 7-9 dan optimum pada pH 8. Penelitian oleh Li et al. (2008) inhibitor sistein protease dari plasma ikan chum salmon menujukkan aktivitas pada pH 6,0 -9,0 dan optimum pada pH 7,0.
4.3.3 Stabilitas terhadap Panas
suhu
Analisis dilakukan dengan cara menginkubasi inhibitor protease pada kisaran suhu 10-70 oC selama 10 menit. Selanjutnya dilakukan pengukuran aktivitas inhibitor pada kondisi optimum. Informasi ini diperlukan untuk mengetahui tingkat ketahanan inhibitor protease pada suhu yang lebih tinggi dari suhu optimumnya. Gambar 15 menunjukkan tingkat stabilitas panas inhibitor protease dari bentuk ekstrak kasar dan hasil pengendapan. Hasil penelitian memperlihatkan aktivitas inhibitor yang cukup tinggi sampai suhu 50 oC.
Gambar 15 Stabilitas panas inhibitor katepsin pada suhu 10-70 oC. –●– ekstrak kasar, –▲– hasil pengendapan.
40
4.3.4 Stabilitas terhadap pH
Analisis ini dilakukan dengan cara menyimpan ekstrak inhibitor pada kisaran pH 3-10 selama 10 menit pada suhu 37 oC. Selanjutnya inhibitor tersebut diuji aktivitasnya pada kondisi optimum. Hasil penelitian stabilitas ekstrak kasar dan hasil pengendapan inhibitor diperlihatkan pada Gambar 16. Inhibitor katepsin yang disimpan pada kisaran pH tersebut menunjukkan bahwa inhibitor tersebut tahan dan stabil pada kisaran pH 7-8
pH
Gambar 16 Stabilitas inhibitor katepsin pada kisaran pH 3-10. –●– ekstrak kasar, –▲– hasil pengendapan.
Sistein proteinase inhibitor dari hewan dan mamalia berupa sistatin mempunyai stabilitas yang besar terhadap suhu tinggi (sampai 100 oC) dan pH yang ekstrim (LMW-CPIs pH 2-12, kininogens pH 5-12) maupun spesifitasnya pada sistein protease (Otto dan Schirmeister 1997). Beberapa inhibitor protease dapat stabil setelah perlakuan panas pada suhu 95 oC selama 15 menit, seperti TIMPs dan sistatin (Nagase dan Salvesen 2001).
4.3.5 Pengaruh Ion Logam terhadap Aktivitas Inhibitor