STUDI ST
RE
(STUDI KTATUS F
EHABILIT
KASUS PT
D
IN
UNGI MI
TASI PAS
INCO Tbk
A
DEPARTE
FAKUL
NSTITUT
IKORIZA
CA PENA
k. SOROWARIF SETIA
EMEN SIL
LTAS KEH
T PERTAN
2011
A ARBUSK
AMBANG
AKO, SULAAWAN
LVIKULT
HUTANA
NIAN BOG
KULA DI
GAN NIKE
AWESI SEL
TUR
AN
GOR
STUDI ST
RE
(STUDI KSebag
TATUS F
EHABILIT
KASUS PT
gai salah satu Faku
D
IN
UNGI MI
TASI PAS
INCO Tbk
A
u syarat untu ultas Kehutan
DEPARTE
FAKUL
NSTITUT
IKORIZA
CA PENA
k. SOROWARIF SETIA
Skripsi uk mempero nan Institut P
EMEN SIL
LTAS KEH
T PERTAN
2011
A ARBUSK
AMBANG
AKO, SULAAWAN
oleh gelar Sa Pertanian Bo
LVIKULT
HUTANA
NIAN BOG
KULA DI
GAN NIKE
AWESI SEL
arjana Kehut ogor
TUR
AN
GOR
AREAL
EL
LATAN)
ABSTRAK
ARIF SETIAWAN. E44062636. Studi Status Fungi Mikoriza Arbuskula di Areal Rehabilitasi Pasca Penambangan Nikel (Studi Kasus PT INCO Tbk. Sorowako, Sulawesi Selatan). Dibimbing oleh Dr.Ir. Yadi Setiadi, M. Sc.
PT INCO Tbk. adalah salah satu perusahaan tambang nikel terbesar di Asia-Pasifik dan telah beroperasi secara komersial di Indonesia sejak tahun 1978. Lokasi konsesi PT INCO Tbk. salah satunya berada di daerah Sorowako Sulawesi Selatan dengan luas areal pada saat ini sebesar 218.000 ha.
Proses operasi penambangan yang dilakukan adalah proses penambangan terbuka. Proses penambangan ini berdampak hilangnya vegetasi, hal ini akan meningkatkan erosi, hilangnya keanekaragaman hayati, merusak habitat satwa liar dan degradasi areal penyimpan air, untuk itu perlu dilakukan kegiatan revegetasi (Setiadi 1995).
Revegetasi yang telah dilakukan terkendala dengan kondisi lahan yang marginal dimana struktur tanah rusak dan tanah bersifat laterik. Tanah akan menjerap unsur Phospat (P) yang sangat penting bagi kehidupan tanaman, sehingga tanah akan miskin akan P-tersedia yang dapat diserap oleh tanaman. Oleh sebab itu perlu dilakukan input teknologi yang efektif dan ramah lingkungan, salah satunya dengan bio-teknologi pupuk hayati Fungi Mikoriza Arbuskula (FMA). FMA memiliki berbagai fungsi, salah satunya adalah peningkatan penyerapan hara terutama P. Untuk itu, penelitian tentang status keberadaan mikoriza perlu dilakukan sebagai pendahuluan untuk penelitian dan aplikasi mikoriza di areal rehabilitasi pasca penambangan nikel.
Dari hasil penelitian ini diketahui bahwa FMA berasosiasi dengan seluruh tanaman yang diamati. Beberapa jenis tanaman yang potensial dikembangkan adalah Sengon buto (Enterolobium cyclocarpum), Sengon albizia (Paraserianthes falcataria), Dengen (Dillenia cerrata), Jati (Tectona grandis), Johar (Senna siamea), Kayu angin (Casuarina equisetifolia), Kayu tanduk (Alstonia spectabilis), dan Ekaliptus (Eucalytus urograndis). Beberapa genus yang yang ditemukan adalah Glomus sp; Acaulospora sp; dan Gigaspora sp.
ABSTRACT
ARIF SETIAWAN. E44062636. Study of Arbuscular Mycorrhizal Fungi status at Rehabilitation Post-Nickel Mining Area (Case study at PT INCO Tbk. Sorowako, South Sulawesi). Guided by Dr.Ir. Yadi Setiadi, M. Sc.
PT INCO Tbk. is one of the biggest nickel mining company in the Asia-Pasific region and has been operated commercially in Indonesia since 1978. It is located at Sorowako, South Sulawesi Indonesia with the area up to 218.000 hectares.
The mining operation process is surface mining. It eliminated the existing vegetation, and it will lead to soil erosion, loss of biodiversity, damage of wildlife habitats and degradation of watershed area, considering with these negative impacts a revegetation programme is fully needed (Setiadi 1995).
Revegetation that has been done obstacled by the marginal land conditions where soil structure has been damaged and it has became a lateritic soil. It absorbs elements of phosphate (P), which is essential for plant life. It will be poor of P-available that can be absorbed by plants. Therefore input for more effective technology and environmentally friendly is needed, among others by applying a bio-technology Arbuscular Mycorrhizal Fungi biofertilizer (AMF). It has some functions, one of them is increasing nutrients absorption, especially P. Therefore, research on the existence of mycorrhizal status needs to be done as an introduction for research and application of mycorrhizal in the rehabilitation field of post- nickel mining.
The result of this research is FMA has been associated with all of observed plants. Some potentially plants to be developed are Sengon buto (Enterolobium cyclocarpum), Sengon albizia (Paraserianthes falcataria), Dengen (Dillenia cerrata), Teak (Tectona grandis), Johar (Senna siamea), Kayu angin (Casuarina equisetifolia), Kayu tanduk (Alstonia spectabilis), and Eucalyptus (Eucalytus Urograndis). Several genera that were found are Glomus sp; Acaulospora sp; and Gigaspora sp.
PERNYATAAN
Dengan ini saya menyatakan bahwa skripsi yang berjudul Studi Status Fungi Mikoriza Arbuskula di Areal Rehabilitasi Pasca Penambangan Nikel (Studi Kasus PT INCO Tbk. Sorowako, Sulawesi Selatan) adalah benar-benar hasil karya saya sendiri dengan pembimbing dan belum pernah digunakan sebagai karya ilmiah pada perguruan tinggi atau lembaga manapun. Sumber informasi yang berasal atau dikutip dari karya yang diterbitkan maupun tidak diterbitkan dari penulis lain telah disebut dalam teks dan dicantumkan dalam daftar pustaka di bagian akhir skripsi ini.
Bogor, November 2010
Arif Setiawan
Judul Skripsi : Studi Status Fungi Mikoriza Arbuskula Di Areal Rehabilitasi Pasca Penambangan Nikel (Studi Kasus PT INCO Tbk. Sorowako, Sulawesi Selatan).
Nama Mahasiswa : Arif Setiawan
NRP : E44062636
Menyetujui: Dosen Pembimbing
Dr. Ir. Yadi Setiadi, M. Sc NIP 19551205 198003 1 004
Mengetahui :
Ketua Departemen Silvikultur
Prof. Dr. Ir. Bambang Hero Saharjo, M. Agr NIP 19641110 199002 1 001
KATA PENGANTAR
Segala puji dan syukur tercurah bagi Allah SWT yang telah melimpahkan segala Rahmat, Hidayah dan RidhoNya saya dapat menyelesaikan skripsi ini. Dalam skripsi ini penulis membahas tentang status fungi mikoriza arbuskula di areal rehabilitasi pasca penambangan nikel (studi kasus PT INCO Tbk. Sorowako, Sulawesi Selatan).
Pada kesempatan kali ini penulis ingin mengucapkan terima kasih kepada: 1. Keluarga, Ayah, Ibu, dan adik-adik tercinta yang selalu mendo’akan, memberi
dukungan dan semangat yang tiada henti.
2. Dr. Ir. Yadi Setiadi, M.Sc selaku dosen pembimbing telah memberikan bimbingan, arahan dan ilmu kepada penulis
3. Hafizah Tarigan yang selalu memberikan dukungan dan motivasi kepada penulis.
4. Seluruh staff di bagian Mine Rehabilitation PT INCO Tbk. yang telah banyak membantu dan memfasilitasi dalam pengambilan bahan penelitian.
5. Staff dan pegawai laboratorium Bioteknologi Hutan dan Lingkungan, PPSHB IPB atas fasilitas, bantuan dan arahan hingga terselesaikannya penelitan ini. 6. Teman-teman seperjuangan PKP, teman-teman mahasiswa Silvikultur 43 dan
semua pihak yang telah memberikan bantuan dalam proses penelitian. Semoga skripsi ini dapat bermanfaat.
Bogor, November 2010
RIWAYAT HIDUP
Penulis dilahirkan di Demak, Jawa Tengah pada tanggal 24 Mei 1988, sebagai anak pertama dari tiga bersaudara dari pasangan Sahri Charir dan Suwarni.
Penulis memulai pendidikan dasar di SD Negeri 10 Bintoro Demak tamat pada tahun 2000, kemudian melanjutkan pendidikan di SLTP Negeri 2 Demak dan tamat pada tahun 2003, selanjutnya meneruskan pendidikan di SMA Negeri 1 Demak dan berhasil tamat pada tahun 2006.
Pada tahun 2006, penulis diterima di Institut Pertanian Bogor (IPB) melalui jalur Undangan Seleksi Mahasiswa IPB (USMI). Pada tahun 2007, penulis masuk di Departemen Silvikultur, Fakultas Kehutanan, IPB.
Selama kuliah penulis aktif dalam organisasi kemahasiswaan, yaitu Himpunan profesi Tree Grower Comunity (TGC) sebagai wakil ketua (2007-2008) dan sebagai ketua divisi Informasi dan Komunikasi (2008-2009). Semasa perkuliahan penulis juga dipercaya untuk menjadi asistem praktikum ekologi hutan semester genap tahun ajaran 2009-2010.
Kegiatan praktek yang telah dilakukan oleh penulis dibidang kehutanan yaitu Praktek Pengenalan Ekosistem Hutan (P2EH) di Baturaden dan Cilacap pada tahun 2008, kemudian Praktek Pengelolaan Hutan (P2H) pada tahun 2009 di Hutan Pendidikan Gunung Walat (HPGW), Sukabumi; KPH Tanggeung, Cianjur; dan Taman Nasional Gunung Gede Pangarango (TNGGP). Pada tahun 2010, penulis melakukan Kuliah Kerja Profesi (KKP) di PT. INCO Tbk. Sorowako, Sulawesi Selatan.
DAFTAR ISI
Halaman
KATA PENGANTAR... i
DAFTAR TABEL... ii
DAFTAR GAMBAR... iii
DAFTAR LAMPIRAN... iv
BAB I. PENDAHULUAN 1.1Latar Belakang... 1
1.2Tujuan... 2
1.3Manfaat... 2
BAB II. TINJAUAN PUSTAKA 2.1 Pengertian Mikoriza... 3
2.2 Karakteristik dan Struktur FMA... 3
2.3 Taksonomi FMA... 4
2.4 Penyebaran FMA... 5
2.5 Fungsi FMA... 6
2.6 Faktor-faktor yang Mempengaruhi Infeksi FMA... 7
2.7 Faktor-faktor yang Mempengaruhi Kkolonisasi dan Sporulasi FMA 8 2.8 Kondisi Tanah Pasca Penambangan Nikel... 9
2.9 Peran FMA dalam Proses Rehabilitasi Hutan... 9
BAB III. METODOLOGI PENELITIAN 3.1 Waktu dan Tempat... 11
3.2 Bahan dan Alat... 11
3.3 Prosedur Penelitian... 11
3.3.1 Persiapan Bahan dan Alat... 11
3.3.2 Pengambilan Contoh Tanah dan Akar... 12
3.3.3 Pengamatan Infeksi Akar... 12
3.3.4 Perhitungan Infeksi Akar... 13
3.3.6 Penangkaran (Trapping) Spora FMA... 14
3.3.7 Perhitungan Spora... 15
BAB IV. HASIL DAN PEMBAHASAN 4.1Hasil... 16
4.2Pembahasan... 18
4.2.1. Infeksi FMA... 18
4.2.2. Genus Spora yang Ditemukan... 23
4.2.3. Perkembangan FMA pada Areal Rehabilitasi... 27
4.2.4. Potensi FMA dalam Revegetasi Lahan Pasca Penambangan Nikel... 30
4.2.5. Evaluasi Status FMA... 31
BAB V. KESIMPULAN DAN SARAN 5.1 Kesimpulan... 32
5.2 Saran... 32
DAFTAR PUSTAKA... 33
DAFTAR TABEL
Halaman
Tabel 1 Taksonomi FMA berdasarkan sekuen rDNA... 4
Tabel 2 Status infeksi, miselia dan spora FMA... 16
Tabel 3 Rata-rata kepadatan dan genus spora tiap blok... 17
DAFTAR GAMBAR
Halaman
Gambar 1. Klasifikasi FMA... 5
Gambar 2. Hifa (a), Vesikula (b), Arbuskula (c) ... 18
Gambar 3. Persentase infeksi di blok Petea... 19
Gambar 4. Persentase infeksi di blok Fiona... 19
Gambar 5. Persentase infeksi di blok Konde... 20
Gambar 6. Persentase infeksi di blok Manggali... 20
Gambar 7. Persentase infeksi di blok Debbie... 21
Gambar 8. Persentase infeksi di Nursery... 21
Gambar 9. Rata-rata persentase infeksi seluruh tanaman... 22
Gambar 10. Glomus sp.1... 25
Gambar 11. Glomus sp.2... 25
Gambar 12. Glomus sp.3... 25
Gambar 13. Glomus sp.4... 25
Gambar 14. Glomus sp. pada larutan melzer’s reagent... 25
Gambar 15. Acaulospora sp. ... 26
Gambar 16. Sporiferous Saccule pada Acaulospora sp. ... 26
Gambar 17 Acaulospora sp. pada larutan melzer’s reagent... 26
Gambar 18 Gigaspora sp. ... 26
Gambar 19 Bulbous Suspensor pada Gigaspora sp. ... 26
Gambar 20 Gigaspora sp. pada larutan melzer’s reagent... 27
Gambar 21 Diagram rata-rata kepadatan spora tiap blok... 28
DAFTAR LAMPIRAN
Halaman
BAB I PENDAHULUAN
1.1. Latar belakang
PT INCO Tbk. adalah salah satu perusahaan tambang nikel terbesar di Asia-Pasifik dan telah beroperasi secara komersial di Indonesia sejak tahun 1978. Lokasi konsesi PT INCO Tbk. salah satunya berada di daerah Sorowako Sulawesi Selatan dengan luas areal pada saat ini sebesar 218.000 ha.
Proses operasi penambangan yang dilakukan adalah proses penambangan terbuka, dimana dalam proses ini, mineral tambang diambil dengan membuka lapisan tanah yang ada di atasnya. Proses tersebut mengakibatkan kerusakan lingkungan, seperti rusaknya vegetasi, hewan, tanah dan juga menghilangkan ekosistem yang ada. Dampak negatif dari hilangnya vegetasi antara lain yaitu meningkatnya erosi, hilangnya keanekaragaman hayati, merusak habitat satwa liar, degradasi areal penyimpanan air (Setiadi, 1995), untuk mengurangi dampak negatif yang terjadi maka perlu dilakukan revegetasi.
Di lapangan, proses revegetasi ini tidaklah mudah untuk dilakukan. Area yang akan direvegetasi kondisi tanahnya (fisik, kimia dan biologi) telah rusak (marginal) dan tidak mampu mendukung pertumbuhan tanaman dengan baik. Bibit pohon yang ditanam banyak yang mati, dan untuk pohon yang bertahan hidup pertumbuhannya tidak maksimal (Setiadi, 1995). Hal tersebut disebabkan karena tanah yang masam, defisiensi P, keracunan logam Al, Fe, maupun Mn, rendahnya aktivitas mikroba dan juga mengalami stress air. Dengan demikian perlu dilakukan usaha-usaha dengan menggunakan input teknologi agar dapat menunjang proses revegetasi tersebut.
Salah satu cara yang dilakukan adalah dengan mengaplikasikan peran fungi mikoriza arbuskula (FMA) sebagai inokulum. FMA merupakan komponen esensial yang dibutuhkan untuk membantu meningkatkan daya hidup dan pertumbuhan tanaman, khususnya pada lokasi pasca tambang (Kiernan et al. 1983; Garedner & Malajczuk, 1988; Jasper et al. 1988 dalam Setiadi, 1995)
2
agregat yang stabil dan meningkatkan toleransi terhadap kekeringan dan keracunan logam (Linderman & Pfleger, 1994; Jasper 1994 dalam Setiadi 1995). Sehubungan dengan hal itu, penelitian ini dilakukan sebagai studi awal untuk mempelajari status dan potensi mikoriza di areal tambang.
1.2. Tujuan
Tujuan dari penelitian ini adalah sebagai penelitian pendahuluan untuk mengetahui keberadaan fungi mikoriza arbuskula (FMA) pada berbagai jenis tanaman yang tumbuh di areal rehabilitasi pasca penambangan nikel PT INCO Tbk; serta prospek penggunaannya.
1.3. Manfaat
BAB II
TINJAUAN PUSTAKA
2.1. Pengertian mikoriza
Mikoriza adalah suatu struktur akar yang terbentuk sebagai hasil hubungan simbiosis mutualistik antara akar tumbuhan tingkat tinggi dengan jamur. Mikoriza terdiri dari dua kata yang berasal dari bahasa Yunani, yaitu mykes (cendawan) dan rhiza (akar) Sieverding (1991).
Fungi ini pada umunya terdiri dari benang-benang mikroskopik yang disebut hifa dan secara kolektif membentuk miselium. Hifa tersebut bisa bercabang ke segala arah dengan tebal antara 0,5-100 mikron dan panjangnya bisa mencapai beberapa meter.
2.2. Karakteristik dan struktur FMA
Berdasarkan bentuk dan cara infeksi jamur terhadap pohon inang mikoriza dapat dikelompokan kedalam dua tipe yaitu endomikoriza dan ektomikoriza. Menurut Setiadi (1989), karakteristik yang membedakan antara endomikoriza dengan ektomikoriza adalah endomikoriza mempunyai ; i) perakaran yang terinfeksi tidak membesar; ii) jamur tidak membentuk selubung hifa pada permukaan akar; iii) hifa menginvasi jaringan korteks secara intra dan inter seluler dan iv) terbentuk struktur khusus sistem percabangan hifa yang disebut arbuskula serta pada sub-ordo tertentu juga terbentuk struktur oval yang disebut vesikula. Ditambahkan oleh Brundett et al. (1996) tipe asosiasi mikoriza yaitu endomikoriza, ektomikoriza, ektendomikoriza, orchid mycorrhizas dan ericoid mycorrhizas.
4
Spora adalah struktur FMA yang biasa digunakan untuk bahan identifikasi. Spora yang dihasilkan dari lapangan biasanya jumlahnya relatif sedikit dan sering terserang nematoda. Penangkaran merupakan suatu teknik yang umum digunakan untuk mendapatkan spora FMA yang utuh dan dengan memanipulasi kondisi lingkungan, produksi spora dapat ditingkatkan.
2.3. Taksonomi FMA
Taksonomi FMA terus berkembang, hingga saat ini, keanekaragaman FMA dapat dilihat hingga tingkat DNA sebagai dasar informasi genetik tiap jenis makhluk hidup. Dengan demikian tiap jenis dari FMA dapat diketahui dengan lebih akurat. Taksonomi FMA berdasarkan sekuen rDNA (penanda DNA ribosom) dapat dilihat pada Tabel 1.
Tabel1. Taksonomi FMA berdasarkan sekuen rDNA
Phylum Class Ordo (4) Famili (10) Genus (14) Glomeromycota Glomeromycetes Glomerales Glomeraceae Glomus
Diversisporales Gigasporaceae Gigaspora
Scutellospora
Racocetra
Acaulosporaceae Acaulospora
Entrophosporaceae Entrophospora
Pacisporaceae Pacispora
Diversisporaceae Diversispora
Otospora
Paraglomerales Paraglomeraceae Paraglomus
Archaeosporales Geosiphonaceae Geosiphon
Ambisporaceae Ambispora
Archaeosporaceae Archaeospora
Intraspora
Sumber : http://www.lrz.de/~schuessler/amphylo/ [19 Oktober 2010]
Paraglomus. Sedangkan sub-ordo Gigasporinae hanya memiliki satu family dan dua genus, yaitu Gigasporaceae dengan genus Gigaspora dan Scutellospora. Untuk lebih jelasnya dapat dilihat pada gambar 1.
Gambar 1. Klasifikasi FMA.
Sumber : http://INVAM.caf.wvu.edu/fungi/taxonomy/classification.htm [9 september 2010].
2.4. Penyebaran FMA
FMA terdapat pada berbagai ekosistem. Penyebaran FMA ini sangat luas di seluruh dunia, mulai dari artik sampai daerah tropis, dan tidak hanya pada habitat darat tetapi juga pada habitat air. Laporan pertama tentang Fungi MA di Indonesia (juga yang pertama di daerah tropis), berdasarkan hasil penelitiannya pada sejumlah tanaman di Kebun Raya Cibodas, terdapat kolonisasi mikoriza pada 69 spesies dari 75 yang diperiksanya. Spesies ini termasuk pada 56 famili dari Bryophyta, Pteridophyta, Gymnosperma, dan Angiosperma. (Gerdemann, 1968; Sondergaard and Laegaard, 1977; Janse 1896 dalam Simanungkalit, 1999)
6
pada padang alang-alang 10-11 spesies (Simanungkalit et al. 1999).
Menurut Nusantara (2004), sekalipun asosiasinya tidak bersifat spesifik untuk satu jenis atau beberapa jenis tanaman inang namun menariknya FMA ditemui hampir pada semua ekosistem daratan mulai dari dataran semi gurun, lahan terlantar, gumuk pasir (sand dune), padang rumput, semak-semak, hutan, dan lahan pertanian. Namun demikian FMA jarang ditemui pada hutan yang dikuasai oleh pohon berdaun jarum (conifer).
2.5. Fungsi FMA
Mikoriza mempunyai beberapa fungsi antara lain (Setiadi, 1989): i) penyerapan unsur hara bagi tanaman terutama unsur P dan unsur hara mikro serta berperan dalam siklus hara; ii) peningkatan pertumbuhan tanaman di bawah kondisi tanah yang tidak cocok, tertekan oleh iklim seperti suhu yang tinggi dan kekeringan; iii) pemeliharaan interaksi antara berbagai jenis mikroorganisme tanah dan dapat mengendalikan mikroorganisme tanah yang bersifat patogenik; iv) perbaikan agregasi tanah serta v) pengatur hormon dan zat pengatur tumbuh tanaman.
Selain yang tersebut di atas, Fungi Mikoriza Arbuskula (FMA) juga memiliki potensi yang lain, berikut adalah beberapa potensi biologis dari FMA (Setiadi, 2001) :
a. Perbaikan nutrisi tanaman
Fungi ini mampu berasosiasi dengan hampir 90 % jenis tanaman. FMA menginfeksi sistem perakaran tanaman inang dan memproduksi jalinan hifa secara intensif sehingga tanaman inang yang bermikoriza akan mampu meningkatkan kapasitasnya dalam menyerap unsur hara dan air. Hifa eksternal dari FMA bisa mengirimkan hingga 80% P, 25% N, 10% K, 25% Zn, dan 60 % Cu dari tanaman (Marschner dan Dell, 1994 dalam Setiadi, 1995).
b. Sebagai pelindung hayati (bio-protection)
bermikoriza akan terlindung dari serangan patogen akar karena secara fisik dilindungi oleh hifa dan secara kimiawi akar tanaman yang bermikoriza menghasilkan senyawa yang bersifat anti patogen dan dapat memproduksi hormon dan zat pengatur tumbuh bagi tanaman.
c. Meningkatkan resistensi terhadap kekeringan
Fungi ini mampu meningkatkan resistensi terhadap kekeringan dengan adanya struktur yang dibentuk berupa hifa didalam tanah yang dapat tumbuh panjang sehingga luas bidang penyerapan air juga meningkat. Oleh karena itu penggunaannya sangat efisien untuk membantu pertumbuhan tanaman reboisasi pada areal-areal yang kurang hujan.
d. Siklus biogeokimia
FMA mempercepat terjadinya suksesi pada habitat-habitat yang mendapat gangguan secara ekstrim. Keberadaannya sangat diperlukan karena berperan penting dalam mengefektifkan daur ulang unsur hara sehingga merupakan alat yang sangat efektif untuk memperbaiki stabilitas ekosistem hutan yang terganggu. e. Sinergis dengan mikroorganisme lain
Bagi tanaman legum, FMA sangat diperlukan karena diawal pembentukan bintil akar dan aktivitas penambatan N oleh bakteri rhizobium yang terdapat didalamnya membutuhkan unsur Phospat yang tinggi. Berdasarkan kemampuannya tersebut maka FMA dapat berfungsi meningkatkan biodiversitas mikroba potensial di sekitar perakaran tanaman.
Selain fungsi di atas FMA juga memiliki fungsi untuk mengefisiensikan penggunaan pupuk. Menurut Santoso et al. (2006) Cikal bakal kegiatan RHL (Rehabilitasi Hutan dan Lahan) terletak pada kegiatan produksi bibit tanaman hutan di persemaian.
2.6. Faktor-faktor yang mempengaruhi infeksi FMA
8
Menurut Fakuara (1988) dalam Tuheteru (2003), intensitas infeksi FMA dipengaruhi oleh berbagai macam faktor meliputi pemupukan, nutrisi tanaman, pestisida, intensitas cahaya, musim, kelembaban tanah, pH, kepadatan inokulum dan tingkat kerentanan tanaman.
2.7. Faktor-faktor yang mempengaruhi kolonisasi dan sporulasi FMA
Faktor lingkungan yang mempengaruhi perkembangan dan pertumbuhan hifa diantaranya adalah sebagai berikut :
1. pH
Setiadi (1992) mengatakan bahwa perkembangan spora FMA sangat dipengaruhi oleh pH tanah, sebagai contoh proses infeksi dan proses pertumbuhan hifa terjadi pada tanaman Caprosoma robusta yang diinfeksi dengan Glomus mossea pada pH 5,6-7,0. Sedangkan pH optimum untuk Glomus sp. antara 5,5-9,5 dan Gigaspora sp. berkisar antara 4-6 (Gunawan, 1993 dalam Tuheteru, 2003). Kemampuan kolonisasi Acaulospora leavis pada kondisi alkalin dan netral akan menurun (Mosse, 1981 dalam Tuheteru, 2003).
2. Kandungan hara tanah
Menurut Hepper (1983) dalam Tuheteru (2003) Glomus mossea dan Glomus caledum terhambat perkecambahannya pada konsentrasi P yang tinggi, walupun berkecambah namun mengalami kerusakan dan pertumbuhan saluran kecambah terhambat.
3. Cahaya
Besarnya intensitas cahaya berimplikasi pada banyak sedikitnya pembentukkan FMA. Hal ini disebabkan karena cahaya matahari berperan dalam pembentukkan karbohidrat melalui asimilasi karbon yang selanjutnya FMA akan menggunakan karbon tersebut sebagai sumber energi bagi pertumbuhannya (Fakuara, 1988 dalam Tuheteru, 2003)
4. Suhu
34 oC, sedangkan Glomus sp. Pada suhu 20 oC (Gunawan, 1993; Setiadi, 1990 dalam Tuheteru, 2003)
5. Oksigen
Menurut Setiadi (1992) bahwa penurunan konsentrasi O2 dapat menghambat perkecambahan spora FMA dan kolonisasi akar.
2.8. Kondisi tanah pasca penambangan nikel
Tanah pada lahan bekas penambangan akan mengalami kerusakan (fisik, kimia, biologi) dan lahan menjadi marginal sehingga tidak dapat mendukung pertumbuhan tanaman. Tanah ini juga bersifat lateritik, dimana tanah akan mengikat unsur Phospat (P). Unsur P hanya dapat diserap oleh tanaman dalam bentuk ion H2PO4- atau HPO42-, namun untuk tanah yang mengalami keracunan logam berat (Al3+, Fe2+, Mn2+, Ca2+, ataupun Mg2+) unsur P akan terikat pada logam berat tersebut, sehingga tanah mengalami jenuh P, akibatnya tanah menjadi miskin akan P-tersedia yang dapat dimanfaatkan oleh tanaman.
Menurut Ernita (2004), Unsur P merupakan unsur hara makro bagi tumbuhan. Dimana P berperan dalam proses fotosintesis, metabolisme karbohidrat, dan transfer energi dalam tubuh tanaman. Namun masalah unsur P adalah ketersediaannya yang rendah pada pH rendah (masam) karena terjerap oleh unsur Al3+, Mn2+ maupun Fe2+. Penambahan P dengan pemupukkan kimia akan mengakibatkan tanah jenuh P dan akan mencemari lingkungan dan menjadi tindakan pemborosan.
2.9. Peran FMA dalam proses rehabilitasi hutan
Salah satu peran FMA adalah dapat meningkatkan P-tersedia dan unsur hara mikro lain dalam tanah (Setiadi, 1989), hal ini karena FMA mampu mengkhelat/ memecah P yang terikat oleh unsur Al3+, Mn2+ maupun Fe2+ dengan mengeluarkan asam-asam organik (Ernita, 2004).
10
mampu memperbaiki fisik tanah dimana FMA meningkatkan kestabilan agregat tanah (Setiadi, 1995) sehingga memiliki daya dukung pertumbuhan tanaman.
BAB III
METODE PENELITIAN
3.1. Waktu dan tempat
Penelitian dilaksanakan selama 6 bulan dari bulan Mei sampai Oktober 2010. Pengambilan contoh tanah dan akar tanaman dilakukan di persemaian dan areal rehabilitasi pasca tambang PT INCO Tbk, sedangkan analisis contoh tanah dan akar tanaman dilakukan di laboratorium Bioteknologi Hutan dan Lingkungan, Pusat Penelitian Sumberdaya Hayati dan Bioteknologi (PPSHB) IPB, dan rumah kaca laboratorium Ekologi Hutan, Departemen Silvikultur, Fakultas Kehutanan, IPB.
3.2. Bahan dan alat
Bahan yang digunakan dalam penelitian ini adalah contoh tanah dan akar tanaman dari areal rehabilitasi dan persemaian PT INCO, benih Pueraria javanica, pupuk Hyponex-red, zeolit, Sunclin™, larutan glukosa 60%, KOH 10%, HCL 2%, larutan Trypan Blue 0,05%, melzer’s reagent dan Aquades.
Alat-alat yang digunakan untuk pengambilan contoh tanah dan akar tanaman adalah sekop, kantong plastik, spidol dan kertas label. Sedangkan untuk pengamatan di laboratorium adalah saringan spora (saringan bertingkat dua dengan ukuran 715 µm, dan 45 µm), sentrifuse, pipet plastik, pinset spora, mikroskop, kaca preparat, cover glass, petridish, pipet, timbangan analitik, gunting akar, sprayer dan pot plastik ukuran 200 cc.
3.3. Prosedur kerja
3.3.1. Persiapan bahan dan alat.
12
3.3.2. Pengambilan contoh tanah dan akar.
Pengambilan contoh tanah dan akar serabut beberapa jenis tanaman (Lampiran 1) dilakukan di areal rehabilitasi pasca penambangan dan persemaian PT INCO Tbk. Pengambilan contoh dilakukan pada areal yang dapat mewakili keadaan areal tambang secara umum, pada penelitian ini contoh tanah dan akar diambil dari 5 blok yaitu di blok Manggali, Konde, Fiona, Debbie, dan Petea.
Pengambilan contoh tanah dari lapangan dilakukan dengan cara mengambil tanah dengan sekop sebanyak ± 200 gram untuk setiap contoh. Contoh tanah yang diambil adalah tanah di sekitar akar atau daerah rhizosfer dengan kedalaman 10-20 cm. Sedangkan untuk pengambilan contoh akar, diambil akar serabut dari masing-masing pohon. Kemudian setiap contoh tanah dan akar yang diambil di masukkan ke dalam plastik dan diberi label sesuai dengan jenis pohon dan lokasi pengambilan. Contoh diambil sebanyak dua ulangan tiap tanaman, hal ini dilakukan untuk mempermudah dalam transportasi contoh tanah dan akar dari lokasi pengambilan hingga ke laboratorium Bioteknologi Hutan dan Lingkungan.
Untuk pengambilan contoh tanah dan akar dari persemaian, dilakukan dengan cara, memotong bibit pada leher akar setinggi ± 1 cm dari media, hal ini dilakukan untuk mempermudah dalam pembungkusan contoh media dan akar. Kemudian media dan akar tanaman yang masih berada dalam polybag, dimasukkan ke dalam plastik dan diberi label. Contoh yang diambil sebanyak dua contoh tiap tanaman.
3.3.3. Pengamatan infeksi akar
Untuk dapat melihat infeksi akar, perlu dilakukan pewarnaan akar. Pewarnaan akar dilakukan dengan metode Phillips dan Hyman (1970) yang dimodifikasi. Tahapan pewarnaan tersebut ialah :
1. Contoh akar di lapangan dipotong dan diambil akar serabut pada bagian samping kiri dan samping kanan, dari batang pokok.
2. Pada saat di laboratorium, akar yang akan diamati dicuci dengan air mengalir hingga kotoran dan tanah yang menempel hilang.
4. Akar dibilas dengan air bersih agar KOH-nya hilang.
5. Akar direndam dalam larutan HCl 2% selama ±24 jam. Hal ini dilakukan agar proses pewarnaan yang akan dilakukan dapat terjadi dengan sempurna (berwarna biru), dimana larutan pewarna (stainning) akan menempel dengan baik pada pH normal (akar akan berwarna kemerahan apabila pH terlalu tinggi). Setelah direndam dalam larutan KOH (basa), pH akar menjadi normal bila direndam dalam larutan HCl (asam).
6. Akar dibilas dengan air bersih agar HCl-nya hilang.
7. Akar direndam dengan larutan staining Trypan Blue 0,05% sampai akar berwarna biru
Setelah pewarnaan selesai, maka contoh akar dapat diamati. Untuk pengamatan akar, dilakukan dengan memotong akar yang telah diwarnai sepanjang 1 cm, kemudian akar ditata di atas preparat dan ditutup dengan cover glass, jumlah akar tiap preparat sebanyak 10 potong. Setelah preparat siap, maka langsung diamati di bawah mikroskop. Infeksi akar dapat dilihat melalui adanya vesikula, arbuskula maupun hifa yang menginfeksi akar
3.3.4. Perhitungan infeksi akar
Perhitungan infeksi akar digunakan rumus Giovannety dan Mosse (1980) sebagai berikut :
Akar terinfeksi (%) = ∑contoh akar terinfeksi X 100%
∑contoh seluruh akar yang diamati
3.3.5. Ekstraksi dan identifikasi spora.
14
saringan paling atas dilepas, dan pada saringan kedua tersisa sejumlah tanah yang tertinggal pada saringan terbawah dipindahkan ke dalam tabung sentrifuse.
Setelah didapatkan hasil saringan tanah dalam tabung sentrifuse, langkah selanjutnya adalah tabung tersebut di sentrifuse dengan teknik sentrifugasi dari Brundet et al. (1996). Hasil saringan tanah dalam tabung sentrifuse ditambahkan glukosa 60% sampai 2/3 isi tabung. Tabung sentrifuse ditutup rapat dan di sentrifuse dengan kecepatan 2500 rpm selama 5 menit. Selanjutnya cairan yang bening diambil dan dituangkan ke dalam saringan yang berukuran 45 µm, lalu dicuci dengan air mengalir untuk menghilangkan gulanya. Setelah dicuci, spora yang ada dipindahkan ke dalam cawan petri dan dihitung jumlahnya atau diidentifikasi. Identifikasi menggunakan metode Schenk dan Perez (1990), spora diidentifikasi dengan pengamatan morfologi spora dan preparat slide spora yang diwarnai dengan pewarnaan melzer’s reagent. Berdasarkan keberadaan struktur spora, FMA ditentukan genusnya.
3.3.6. Penangkaran (trapping) spora FMA
Ada kemungkinan spora tidak teramati apabila pengamatan dilakukan dari contoh tanah secara langsung, hal ini karena mikoriza masih dalam bentuk miselia dan belum menghasilkan spora. Trappingatau penangkaran spora dilakukan untuk mengembangbiakan spora dari contoh tanah yang telah diambil, sehingga dapat diketahui keseluruhan jenis spora. Teknik trapping yang digunakan mengikuti metode Brundrett et al. (1996) dengan metode kultur pot terbuka yang dimodifikasi yaitu dengan menggunakan tanaman inang Pueraria javanica dan media yang digunakan untuk trapping adalah batuan zeolit.
1. Penyiapan media
Menurut Setiadi dan Hariangbanga (2009) beberapa media yang telah diuji kelayakannya diantaranya adalah pasir kali, zeolit, dan batuan lunak. Media yang dipakai perlu dicuci bersih dan bebas dari partikel-partikel tanah. Pada penelitian ini digunakan media zeolit.
2. Pemilihan tanaman inang
Tanaman inang yang dapat dipakai adalah tanaman yang terbukti cocok dengan jenis-jenis FMA dan media. Beberapa jenis yang dapat dipakai adalah sorgum, tegetes, ceplukan, pueraria, dan rumput sudan grass (Setiadi dan Hariangbanga, 2009).
Tanaman inang yang digunakan untuk penelitian ini adalah Pueraria javanica. Sebelum benih disemai, terlebih dahulu disterilkan dengan direndam dalam larutan chlorox (SunclinTM) 5% selama 5-10 menit dengan tujuan sterilisasi permukaan, kemudian benih dibilas hingga baunya hilang. Setelah itu benih direndam dengan air hangat selama 24 jam untuk mematahkan dormansi benih. Kemudian benih disemai dalam bak kecambah sampai muncul dua helai daun, setelah itu semai ditanam pada media yang telah disiapkan (Delvian, 2006). 3. Pemeliharaan
Pemeliharaan yang dilakukan adalah penyiraman sebanyak 20 cc setiap dua kali sehari di pagi dan sore hari. Selain itu juga dilakukan pemupukkan setiap dua kali dalam seminggu menggunakan pupuk Hyponex-red (dosis 1 gram dilarutkan dalam 1 liter air) sebanyak 20 ml per pot (Delvian, 2006) .
4. Pengeringan dan Pemanenan Hasil Trapping.
Menurut INVAM (2010), kultur paling tidak berumur empat bulan untuk dapat dipanen. Pada saat kultur berumur 3,5 bulan, penyiraman dan pemupukkan dihentikan dan tanaman dibiarkan mengering perlahan. Setelah kultur berumur 4 bulan dilakukan pemanenan dengan cara memotong batang tanaman inang. Hasil dari trapping berupa inokulum spora yang akan diproses lebih lanjut yaitu ekstraksi dan identifikasi spora.
5. Ekstraksi dan identifikasi spora dari hasil penangkaran (trapping).
Ekstraksi dan identifikasi spora menggunakan teknik yang sama dengan ekstraksi dan identifikasi spora langsung dari contoh tanah, namun pada spora hasil trapping tidak perlu digunakan teknik sentrifugasi.
3.3.7. Perhitungan spora
Perhitungan spora dilakukan untuk mengetahui kepadatan spora. Kepadatan spora tiap 50 gram tanah dihitung dengan rumus :
16
BAB IV
HASIL DAN PEMBAHASAN
4.1. Hasil
Berdasarkan hasil identifikasi spora, miselia dan infeksi FMA, didapatkan hasil status FMA yang disajikan pada tabel 2.
Tabel 2. Status infeksi, miselia dan spora FMA
No Jenis tanaman Nama latin Infeksi Miselia Spora Genus Spora 1 Belulang Stemonurus celebicus +++ ++ + G
2 Betao Calophyllum spp. ++ + + G 3 Bitti Vitex cofassus ++ ++ + G, A 4 Buri Weinmannia blumei ++ + + G 5 Dengen Dillenia cerrata +++ +++ + G, A 6 Ekaliptus Eucalyptus urograndis ++ ++ + G, A, Gi
7 Ficus Ficus spp. +++ + + G, Gi
8 Jambu-jambu Syzygium spp. ++ + + G 9 Jati Tectona grandis +++ +++ ++ G 10 Johar Senna siamea ++ ++ ++ G, A, Gi 11 Kayu angin Casuarina equisetifolia +++ ++ ++ G, A, Gi 12 Kayu tanduk Alstonia spectabilis +++ +++ ++ G, Gi 13 Kolaka Maranthes corymbosa ++ + + G 14 Krei payung Filicium decipiens + + + G 15 Malotus Malotus sp. ++ ++ ++ G, A 16 Nyatoh Palaquium obovatum + + + G 17 Saga Adenanthera pavonina ++ + +++ G 18 Sengon albizia Paraserianthes falcataria +++ ++ ++ G, A, Gi 19 Sengon buto Enterolobium cyclocarpum +++ +++ +++ G, A, Gi 20 Uru Elmerillia tsiampacca + + + G, A
Keterangan: +++ = Banyak, ++ = Sedang, + = Sedikit Genus spora:
G : Glomus sp. A : Acaulospora sp. Gi : Gigaspora sp.
% infeksi :
≥75% : Banyak 51-74% : Sedang ≤50% : Sedikit
Jumlah spora :
Dari hasil rekapitulasi data hasil penelitian tiap blok, diketahui rata-rata kepadatan genus spora / 50 gram pada masing-masing blok. Hasil yang didapatkan disajikan pada tabel 3.
Tabel 3. Rata-rata kepadatan dan genus spora tiap blok
Blok Rata-rata kepadatan
spora / 50 g Genus spora
Fiona 253 Glomus sp; Acaulospora sp; Gigaspora sp. Petea 234 Glomus sp; Acaulospora sp.
Manggali 209 Glomus sp; Acaulospora sp
Konde 122 Glomus sp; Acaulospora sp; Gigaspora sp. Debbie 55 Glomus sp; Acaulospora sp; Gigaspora sp. Nursery 46 Glomus sp; Acaulospora sp.
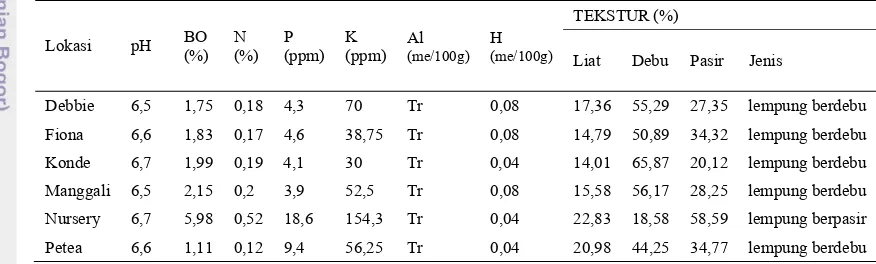
Dalam penelitian ini dilakukan pula analisis tanah. Analisis tanah dilakukan di Departemen Ilmu Tanah dan Sumberdaya Lahan, Fakultas Pertanian, IPB. Hasil analisis dapat dilihat pada tabel 4.
Tabel 4. Analisis tanah
Lokasi pH BO (%)
N (%)
P (ppm)
K (ppm)
Al (me/100g)
H (me/100g)
TEKSTUR (%)
Liat Debu Pasir Jenis
Debbie 6,5 1,75 0,18 4,3 70 Tr 0,08 17,36 55,29 27,35 lempung berdebu
Fiona 6,6 1,83 0,17 4,6 38,75 Tr 0,08 14,79 50,89 34,32 lempung berdebu
Konde 6,7 1,99 0,19 4,1 30 Tr 0,04 14,01 65,87 20,12 lempung berdebu
Manggali 6,5 2,15 0,2 3,9 52,5 Tr 0,08 15,58 56,17 28,25 lempung berdebu
Nursery 6,7 5,98 0,52 18,6 154,3 Tr 0,04 22,83 18,58 58,59 lempung berpasir
Petea 6,6 1,11 0,12 9,4 56,25 Tr 0,04 20,98 44,25 34,77 lempung berdebu
Keterangan : Tr = Tidak terukur
[image:30.612.110.548.371.503.2]18
4.2. Pembahasan
4.2.1. Infeksi FMA
Terjadinya asosiasi antara fungi mikoriza arbuskula (FMA) dapat diketahui dengan ada tidaknya infeksi yang yang terjadi. Infeksi FMA dapat diketahui dengan adanya struktur-struktur yang dihasilkan oleh FMA antara lain, yaitu : hifa, miselia, vesikula, arbuskula, maupun spora. Hifa adalah salah satu struktur dari FMA berbentuk seperti benang-benang halus yang berfungsi sebagai penyerap unsur hara dari luar. Miselia merupakan kumpulan dari hifa. Arbuskula adalah unit kolonisasi yang telah mencapai sel korteks yang lebih dalam letaknya dan menembus dinding sel serta membentuk sistem percabangan hifa yang kompleks, tampak seperti pohon kecil yang mempunyai cabang-cabang, struktur ini berperan sebagai tempat pertukaran unsur hara dan karbon. Vesikula adalah struktur menggelembung yang dibentuk pada hifa-hifa utama, berfungsi sebagai organ penyimpan. Struktur ini juga berfungsi sebagai spora istirahat (Gunawan, 1993; Hudson, 1989; dan Setiadi, 1989 dalam Tuheteru, 2003). Dengan adanya satu atau lebih struktur FMA tersebut, maka dapat dikatakan terjadi infeksi oleh FMA.
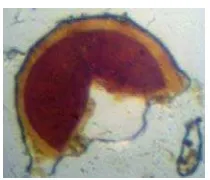
Dari hasil pengamatan, beberapa struktur yang ditemukan dalam contoh akar antara lain, yaitu : hifa, miselia, vesikula dan arbuskula. Untuk lebih jelasnya dapat dilihat pada gambar 2.
[image:31.612.114.508.497.623.2]Gambar 2. Struktur FMA di dalam akar, (a) Hifa, (b) Vesikula, (c) Arbuskula.
Dari hasil pengamatan diketahui bahwa 100% tanaman atau seluruh tanaman telah terinfeksi oleh FMA. Hal ini menunjukkan bahwa asosiasi antara FMA dengan akar tanaman berkembang sangat baik. selain itu dapat dikatakan
(a) (b) (c)
b d s U p d p l m c t ≤ bahwa tanam dapat bertah sebagai pupu Namun Untuk di b persentaase dimana terda persentase in lebih jelasny Gamb Untuk memiliki pe cukup baik tanaman den
≤50 %. Untu
Gamba 0 2 4 6 8 100 0% 20% 40% 60% 80% 100% % man revege han hidup, d
uk hayati san n persentase blok Petea infeksi yang apat 3 jenis nfeksi 51-74 ya dapat dilih
bar 3. Persen k di blok F ersentaase in dimana terd ngan persent uk lebih jela
ar 4. Persent 70% 0% 0% 0% 0% 0% 0% Ekalipt % Infeksi 50% % % % % % % Ekaliptus % Infeksi
tasi areal b dan dari ha ngat prospek e infeksi tia ditemukan g berbeda-be
dengan pers 4%, dan han hat pada gam
ntase infeksi Fiona ditem nfeksi yang dapat 4 jeni tase infeksi snya dapat d
tase infeksi d 100%
us Johar
60%
Johar
ekas penam asil ini dapa
ktif.
ap tanaman 6 jenis tan eda. Infeksi sentase infek nya 1 tanam mbar 3.
i di blok Pet mukan 7 jen
berbeda-bed is dengan pe 51-74%, dan dilihat pada g
di blok Fion 80% Kayu angin 80% 8 Kayu angin K ta mbangan mem at dilihat ba
berbeda sa naman, ma
tanaman pa ksi ≥75 %, 2 man yang ter
ea
nis tanaman da. Infeksi t
ersentase in n hanya 1 ta gambar 4. na 65% Malotus 85% 55% Kayu nduk Malo merlukan F ahwa pemak atu dengan asing-masing da blok ini c 2 jenis tanam rinfeksi ≤50
n dan masi tanaman pad nfeksi ≥75
anaman yang 50% 7 Saga Se b % 90% otus Sengon albizia MA untuk kaian FMA yang lain. g memiliki cukup baik man dengan 0 %. Untuk
ing-masing da blok ini
m c t ≤ m p p j i Di blo memiliki pe cukup baik tanaman den
≤50 %. Untu
Gamba Untuk masing juga pada blok persentase in G Sedang juga memili ini cukup ba
0% 20% 40% 60% 80% 100%
ok Konde ju ersentaase in dimana terd ngan persent uk lebih jela
[image:33.612.182.477.485.634.2]ar 5. Persent k di blok M a memiliki ini sangat nfeksi ≥75 %
Gambar 6. P gkan di blok iki persentaa aik dimana t
95% % % % % % % Dengen 0% 20% 40% 60% 80% 100% uga ditemuk nfeksi yang dapat 3 jeni tase infeksi snya dapat d
tase infeksi d Manggali han
persentaase baik diman %. Untuk leb
Persentase in k Debbie dit ase infeksi y terdapat 4 je
50%
Ekaliptus J
85%
Ekaliptus
kan 7 jenis t berbeda-bed is dengan pe 51-74%, dan dilihat pada g
di blok Kond nya ditemuk
infeksi yan na terdapat bih jelasnya
nfeksi di blok temukan 10 yang berbeda enis dengan 60% 70 Johar Ka an % Infek 75% Kayu angin % Infeks tanaman dan da. Infeksi t
ersentase in n hanya 1 ta gambar 5.
de
kan 4 jenis ng berbeda-b semua jen dapat diliha k Manggali jenis tanam a-beda. Infek persentase i 0% 75% ayu gin Malotu ksi 95% Malotus si n masing-m tanaman pad nfeksi ≥75
anaman yang
tanaman da beda. Infeks nis tanaman at pada gamb
man dan masi ksi tanaman infeksi ≥75
65% us Sengon albizia 100% Sengon buto 20 masing juga da blok ini %, 3 jenis g terinfeksi an masing-si tanaman n memiliki bar 6. ing-masing n pada blok %, 5 jenis
100%
Sengon buto
t ≤ G m p % t G 0% 10% 20% 30% 40% 50% 60% 70% 80% 90% 100% 2 3 4 5 6 7 8 9 10 tanaman den
[image:34.612.109.538.104.354.2]≤50 %. Untu
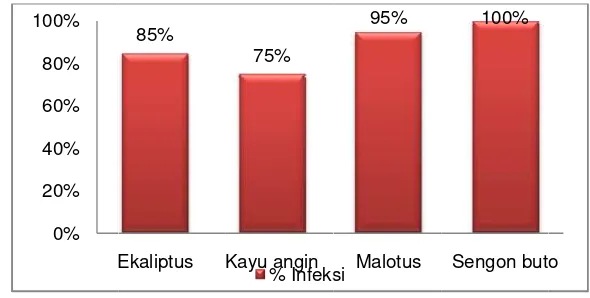
[image:34.612.105.539.489.678.2]Gambar 7. P Terakh masing juga pada blok in %, 4 jenis terinfeksi ≤5
Gambar 8. P 75% % % % % % % % % % % % 70% 0% 10% 20% 30% 40% 50% 60% 70% 80% 90% 00% ngan persent uk lebih jela
Persentase in hir adalah di a memiliki ni sedang dim
tanaman de 50 %. Untuk
Persentase in 60% 75 % 60% tase infeksi snya dapat d
nfeksi di blok i Nursery di
persentaase mana terdapa
engan perse k lebih jelasn
nfeksi di Nur 5%
60%
95%
51-74%, dan dilihat pada g
k Debbie imana ditem
infeksi yan at hanya 2 je entase infek nya dapat dil
rsery 80% % Infeksi 45% 70 % Infeks
n hanya 1 ta gambar 7.
mukan 9 jenis ng berbeda-b enis dengan p si 51-74%, ihat pada ga
90% 65% % 35% si anaman yang
r i i t ( j d g S d y S K Secara rata-rata per Gamba Ketera
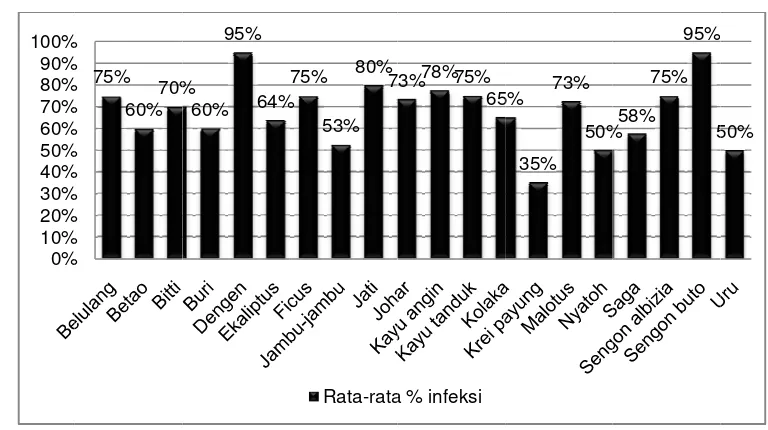
[image:35.612.150.534.113.328.2]Pada t ini kemungk infeksi miko terhadap mi (Setiadi, 199 Secara jenis tanama dan hanya 3 gambar 9 dia
Dari d Sengon buto dengan pers yang digun Sedangkan Kedua jenis 0% 10% 20% 30% 40% 50% 60% 70% 80% 90% 100% a keseluruha rsentase infek
ar 9. Rata-ra angan % infe
tiap-tiap tana kinan diseba
oriza terhad ikoriza, efek 95).
a umum rata an yang teri 3 tanaman y
atas.
diagram diata o (Enterolob sentase infek nakan untuk Dengen me ini sangat p
75% 60% 70% % % % % % % % % % % % an, persentas ksi seperti p
ata persentas eksi : ≥75%
aman memil abkan oleh p
ap tanaman ktifitas isola
a-rata infeks infeksi ≥75% yang terinfek as, rata-rata bium cycloc ksi mencapai k revegetasi erupakan jen otensial untu % 60% 95% 64%
se infeksi se ada gambar
se infeksi se : Banyak; 5
liki persenta erbedaan be , antara lain at, maupun
si yang terja %, 11 jenis ksi ≤50%. Je
persentase i carpum) dan
i 95%. Sen , jenis ini nis lokal y uk dikemban % 75% 53% 80% 7 Rata-rata eluruh tanam 9. eluruh tanam 1-74% : Sed
ase infeksi y eberapa fakto n yaitu : keb kondisi nut
adi cukup ba tanaman den enis-jenis tan
nfeksi tertin n juga Deng ngon buto m
termasuk p yang digunak ngkan denga 73%78%75%
65
a % infeksi
man yang ad
man
dang; ≤50%
yang berbeda or yang mem bergantunga trisi terutam aik, dimana ngan infeksi naman dapa nggi terdapat gen (Dilleni merupakan je pohon cepa kan untuk an mikoriza. 5% 35% 73% 50% 22 da memiliki : Sedikit a-beda, hal mpengaruhi an tanaman ma unsur P
terdapat 8 i 51-74% , at dilihat di
Berdasarkan persentase infeksi dan miselia, selain jenis Sengon buto dan Dengen, juga terdapat beberapa jenis lain yang potensial dikembangkan dengan mikoriza antara lain yaitu : Jati (Tectona grandis), Johar (Senna siamea), Kayu angin (Casuarina equisetifolia), Kayu tanduk (Alstonia spectabilis) dan juga Sengon albizia (Paraserianthes falcataria). Jati terbukti memiliki kompabilitas yang baik terhadap asosiasi FMA di KPH Cepu dan KPH Saradan, hal ini ditunjukkan dengan tingginya persen kolonisasi dan peningkatan pertumbuhan (Nurmalasari, 2009). Habte (2000) mengelompokkan Johar, Sengon buto dan Sengon albizia kedalam kelompok dengan tingkat kebergantungan yang tinggi (Highly dependent) terhadap mikoriza, hal ini menunjukkan bahwa tanaman tersebut memerlukan asosiasi dengan mikoriza untuk dapat tumbuh maksimal.
Walaupun hasil dari pengamatan menunjukkan bahwa seluruh jenis tanaman terinfeksi mikoriza, akan tetapi tidak semua jenis tanaman selalu memberikan respon positif terhadap aplikasi FMA. Hal ini selain ditentukan oleh tingkat efektivitas isolat dan status nutrisi substrat yang dipakai, juga sangat ditentukan oleh ketergantungan tanaman tersebut terhadap mikoriza (Setiadi, 1995).
4.2.2. Genus spora yang ditemukan
Dalam penelitian ini evaluasi status FMA hanya dibatasi hingga tingkat genus. Dari hasil pengamatan, diperoleh tiga genus dari tujuh genus FMA yang ada. Genus terbanyak yang ditemukan antara lain, yaitu: Glomus sp; Acaulospora sp; dan Gigaspora sp. Dari hasil beberapa penelitian ketiga genus tersebut telah teruji efektif dan mampu berkembang dengan baik pada areal revegetasi sehingga dapat dikembangkan sebagai inokulum yang efektif.
24
menunjukkan bahwa perkembangan Gigaspora sp. sangat baik di lahan pantai dengan tekstur pasir >80%.
Dari hasil penelitian diketahui bahwa Glomus sp. berasosiasi dengan semua jenis tanaman yang diamati, sedangkan Acaulospora sp. berasosiasi dengan 9 jenis tanaman, dan Gigaspora sp. hanya berasosiasi dengan 7 jenis tanaman. Dengan demikian diketahui bahwa Gigaspora sp. memiliki kecenderungan lebih spesifik untuk berasosiasi dengan tanaman bila dibadingkan dengan Acaulospora sp. dan Glomus sp.
Apabila dilihat dari genus spora yang berasosiasi, beberapa jenis tanaman yang potensial dikembangkan dengan FMA adalah Ekaliptus (Eucalyptus urograndis), Johar (Senna siamea), Kayu angin (Casuarina equisetifolia), Sengon albizia (Paraserianthes falcataria), dan juga sengon buto (Enterolobium cyclocarpum), dimana jenis-jenis tersebut berasosiasi dengan ketiga genus spora yang ditemukan. Dengan kemampuan jenis-jenis tersebut berasosiasi dengan berbagai genus FMA (multispora), maka semakin besar peluang jenis tersebut berasosiasi dengan FMA. Sehingga dapat meningkatkan kemampuan tanaman untuk bertahan hidup dan tumbuh pada areal pasca penambagan.
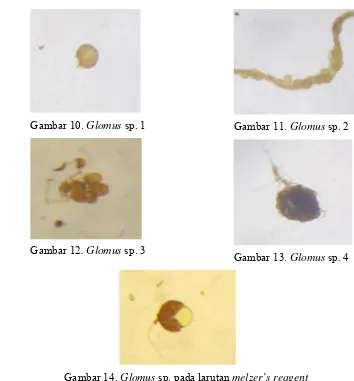
Glomus sp. adalah genus mikoriza dari family glomaceae. Genus ini memiliki keberagaman jenis tertinggi dari yang lain, beberapa ciri khas dari genus ini yaitu spora terbentuk secara tunggal ataupun berpasangan dua pada terminal hifa non-gametangium yang tidak berdiferensiasi dalam sporocarp, pada saat dewasa spora dipisahkan dari hifa pelekat oleh sebuah sekat, spora berbentuk globos sub-globos, ovoid ataupun obovoid dengan dinding spora terdiri dari lebih dari satu lapis, berwarna hyaline sampai kuning, merah kecoklatan, coklat, dan hitam, berukuran antara 20 – 400 µm (Sen dan Hepper, 1986; INVAM, 2010). Selain itu Glomus sp. tidak bereaksi dengan larutan melzer’s reagent (Schenk dan Perez, 1990) untuk lebih jelasnya dapat dilihat pada gambar 14.
Gambar 10. Glomus sp. 1
[image:38.612.129.483.71.452.2]Gambar 12. Glomus sp. 3
Gambar 11. Glomus sp. 2
Gambar 13. Glomus sp. 4
Gambar 14. Glomus sp. pada larutan melzer’s reagent
[image:38.612.362.484.77.322.2]26
[image:39.612.375.493.77.169.2]
Gambar 15. Acaulospora sp. Gambar 16. Sporiferous Saccule pada Acaulospora sp.
Gambar 17. Acaulospora sp. pada larutan melzer’s reagent
Gigaspora sp. adalah genus mikoriza yang termasuk dalam family Gigasporaceae. Genus ini memiliki ciri khas, antara lain yaitu spora dihasilkan secara tunggal didalam tanah, tidak memiliki lapisan dinding spora dalam, terdapat Bulbous Suspensor (gambar 19), berbentuk globos atau sub-globos, berwarna krem hingga kuning, berukuran 125-600 µm (Wilson et al. 1983; INVAM, 2010) (gambar 18). Selain itu ciri khas Gigaspora sp. adalah bereaksi dengan larutan melzer’s reagent (Schenk dan Perez, 1990) untuk lebih jelasnya dapat dilihat pada gambar 20.
[image:39.612.281.386.212.302.2]Gambar 18. Gigaspora sp.
Gambar 19. Bulbous Suspensor pada Gigaspora sp.
Bulbous Suspensor
[image:39.612.361.483.512.641.2]Gambar 20. Gigaspora sp. pada larutan melzer’s reagent
4.2.3. Perkembangan FMA pada areal rehabilitasi
Dari beberapa penelitian diketahui bahwa simbiosis FMA dipengaruhi oleh level P, sumber P, pH, efektifitas isolat FMA dan kebergantungan tanaman inang terhadap mikoriza (Setiadi, 1995).
Dari hasil analisis contoh tanah yang diambil dari tiap blok (tabel 4), diketahui bahwa kondisi lahan diseluruh areal rehabilitasi yang diamati memiliki pH berkisar antara 6,5-6,7 dan kandungan logam Al tidak terukur atau sangat kecil, dan kandungan P rendah hingga sedang, serta tekstur tanah berupa lempung berdebu.
Sifat kimia tanah relatif normal, dimana tanah tersebut memiliki pH netral dan tidak mengalami keracunan logam Al (kandungan Al sangat kecil). Kondisi ini sangat berbeda dari kondisi lahan paska penambangan nikel, dimana lahan biasanya memiliki tanah yang masam (pH rendah), keracunan logam Al, Fe ataupun Mn, rendahnya aktivitas mikroba serta mengalami stress air sehingga lahan menjadi marginal (Setiadi, 1995). Hal ini kemungkinan dikarenakan pada areal rehabilitasi telah dilakukan penimbunan top soil pada saat proses penataan lahan. Sehingga kondisi lahan menjadi lebih mendukung untuk proses revegetasi.
o s G b k t d a ( k l b o m d y p Bebera optimum un sp; 4 - 6 u Gunawan, 1
Gamba
Dari d bahwa perk kepadatan s terdapat di F dilapangan, areal tersebu (2003) bahw konsentrasi lebih baik.
Pada b blok Konde oleh kandun maka akan m
Untuk dikarenakan yang berasa pemupukkan
apa FMA d ntuk perkemb untuk Gigasp 993; Hepper
ar 21. Diagr
diagram rata-kembangan
spora / 50 Fiona, kemu diketahui b ut mengalam wa perkecam
P, sehingga
blok Debbie e, Manggali, ngan K yang
menurunkan k di Nurser n tanaman di al dari pemu n kandunga 0 50 100 150 200 250 300 dapat berkem bangan FMA pora sp. dan r, 1984 dalam
ram rata-rata
-rata kepada spora cukup
g. Untuk a udian Petea, bahwa spora mi defisiens mbahan Glom
makin keci
e memiliki k Petea mau relatif lebih tingkat spor ry, perkemb Nursery me upukkan seba an P dan K
55 2
mbang baik A adalah ber n 4 - 5 untu m Tuheteru,
a kepadatan
atan spora ti p baik, dZm areal rehabi
Manggali, K a berkemban
i P. Menuru mus sp. Akan il konsentras
kepadatan sp upun Fiona. h tinggi dari rulasi FMA. bangan FM endapatkan h agai langkah K meningka 253 122 pada lahan rkisar antara uk Acaulospo 2003)
spora tiap b
ap blok (gam mana dapat ilitasi perke Konde dan t ng baik, hal ut Hepper ( n berkurang si P maka F
pora yang l Hal ini kem blok lainnya
MA relatif l hara yang cu h perawatan at, sehingga
209
n tersebut, d a 5,6 - 7 untu
ora sp. (Set
lok
mbar 21), da t dilihat dar embangan p terakhir Deb ini dikaren 1983) dalam dengan men MA akan be
lebih rendah mungkinan d
a. Dengan tin
lebih sediki ukup terutam n bibit. Deng perkemban 46 234 28 dimana pH uk Glomus iadi, 1992; apat dilihat ri rata-rata paling baik bbie. Untuk nakan pada m Tuheteru ningkatnya erkembang
h dari pada disebabkan ngginya K,
it, hal ini ma P dan K
b t b m t k p d N p d t G K c ( K
berkurang, h terhambat de Apabi bahwa tanah memiliki aer tanah kekur kondisi ini penurunan k dan kolonis Namun dem pori mikro, dalam tanah
[image:42.612.108.529.342.625.2]Dari b tiap jenis tan
Gambar 22. Keterangan: Kepad cyclocarpum
(Adenanther Kemudian d
45 45 0 100 200 300 400 500 600
hal ini sesu engan adany ila ditinjau d h tersebut be
rasi yang bu rangan oks juga meng konsentrasi sasi akar. mikian FMA sehingga ta dapat menin beberapa jeni naman berbe Diagram ke
≤ 100 : Sed datan spora m) dengan k
ra pavonina
diikuti oleh 5 38 21
84
uai dengan D ya pemupukk
dari sifat fisi ertekstur lem uruk terutam igen. Selain ghambat per oksigen dap Oleh karen juga memil anah akan m
ngkat. is tanaman y eda-beda. Ha
epadatan spo dikit; 101 – 1
tertinggi kepadatan me
a) dengan Sengon Alb 4 87 35 23 ke Delvian (200 kan P. ik tanahnya, mpung (kand ma saat terjad n mengham rkembangan pat mengham na itu/s perk
liki hifa ekst memiliki aer
yang diamati asil pengama
ra pada tiap 199 : Sedang terdapat pa encapai 477 kepadatan bizia, Malotu
3
154 15113
epadatan spor
06) perkemb
, dari hasil a dungan liat ti di hujan, hal mbat pertum n FMA. Me mbat perkec kembangan ternal yang a rasi yang ba
i, diketahui b atan dapat di
jenis tanam g; ≥ 200 : Ba ada Sengon 7 spora/50 g
spora seb us, Jati, Joha 32 135
26 2
ra / 50g
bangan mik
analisis tanah inggi). Tana
ini akan me mbuhan akar
enurut Setia cambahan sp FMA akan akan membe aik dan kad
bahwa kepad ilihat pada g
an (/50 g tan anyak n buto (En
tanah kemu besar 232
30
angin, Ekaliptus, Dengen, Belulang, Betao, Uru, Bitti, Ficus, Nyatoh, Krei payung, Kolaka, Jambu-jambu dan paling sedikit adalah Buri.
Dari hasil penelitian ini, dapat dilihat bahwa persentase infeksi tidak berbanding lurus, dimana tingginya persentase infeksi tidak selalu memperbesar kepadatan spora. Menurut Tuheteru (2003) bahwa antara infeksi akar dan jumlah spora yang dihasilkan tidak memiliki korelasi yang erat, sehingga spora yang banyak belum tentu persentase infeksi akar akan tinggi pula.
4.2.4. Potensi FMA dalam revegetasi lahan pasca penambangan nikel
Telah banyak penelitian mengenai potensi dari FMA baik dalam pertanian maupun kehutanan. Dimana kebanyakan hasil penelitian menunjukkan hasil yang membuktikan bahwa FMA dapat meningkatkan pertumbuhan tanaman, meningkatakan penyerapan hara, pelindung hayati (Bio-protector), memperbaiki siklus biogeokimia, meningkatkan resistensi terhadap kekeringan dan keracunan logam berat, serta memperbaiki struktur tanah (Setiadi, 2001)
Masalah yang terjadi dalam program revegetasi antara lain adalah tanaman yang ditanam banyak yang mengalami kematian, apabila tanaman tersebut mampu hidup, biasanya pertumbuhannya buruk (Setiadi, 1995). Untuk itu FMA sangat diperlukan untuk meningkatkan keberhasilan program revegetasi.
4.2.5. Evaluasi status FMA
Dilaporkan oleh Setiadi (1995) bahwa tiga genus yang di uji coba memberikan pengaruh terhadap pertumbuhan Acacia mangium, Paraserianthes falcataria, dan Trichospermum burretii di persemaian, dimana genus yang digunakan merupakan genus eksotik yaitu Glomus sp. (INVAM-FL216) dan Gigaspora sp. (INVAM-FL105), serta genus indigenous yaitu Acaulospora sp. (INCO-1 dan INCO-2).
Dari hasil pengamatan diketahui bahwa genus Glomus sp; Gigaspora sp; dan Acaulospora sp. dapat berkembang baik di persemaian dan di lapangan. Genus- genus indegenous mampu beradaptasi dan berkembang baik pada daerah asalnya, hal ini dibuktikan dengan genus Acaulospora sp. yang ditemukan disetiap blok. Namun tidak menutup kemungkinan bahwa genus-genus eksotik mampu berkembang baik, bahkan lebih baik daripada genus-genus indigenous seperti Glomus sp. yang dapat berkembang sangat baik di semua areal rehabilitasi paska penambangan dan persemaian PT INCO Tbk.
Implementasi FMA dalam rehabilitasi lahan pasca penambangan antara lain yaitu penggunaan isolat indigenous ataupun eksotik yang terbukti efektif untuk kegiatan produksi bibit, menurut Mosse et al. (1981) dalam Delvian (2004) bahwa fase bibit mungkin merupakan fase yang sangat tergantung pada mikoriza, baik untuk tumbuhan tahunan maupun tumbuhan semusim. Sehingga dengan adanya FMA bibit akan memiliki ketahanan terhadap kondisi lahan yang marginal.
32
BAB V
KESIMPULAN DAN SARAN
5.1. Kesimpulan
Dari penelitian ini dapat disimpulkan bahwa dari hasil infeksi, semua tanaman telah bermikoriza sehingga mempunyai potensi untuk beradaptasi dengan tanah lateritik. Beberapa tanaman yang potensial dikembangkan dengan mikoriza antara lain Sengon buto (Enterolobium cyclocarpum), Dengen (Dillenia cerrata), Sengon albizia (Paraserianthes falcataria), ,Jati (Tectona grandis), Johar (Senna siamea), Kayu angin (Casuarina equisetifolia), Kayu tanduk (Alstonia spectabilis), dan Ekaliptus (Eucalytus urograndis).
Terdapat tiga genus FMA yang mendominasi pohon yang tumbuh di areal rehabilitasi pasca penambangan nikel di PT INCO Tbk, yaitu : Glomus sp; Acaulospora sp; dan Gigaspora sp. Genus-genus tersebut terbukti berkembang baik pada areal rehabilitasi dan sangat potensial dikembangkan sebagai inokulum untuk kegiatan rehabilitasi lahan pasca penambangan nikel.
5.2. Saran
Adapun saran yang dapat dilakukan antara lain:
1. Perlu dilakukan penelitian lebih lanjut mengenai status FMA hingga tingkat spesies.
2. Perlu dilakukan penelitian tentang efektivitas isolat dan ketergantungan mikoriza pada tanaman-tanaman lokal untuk revegetasi di areal pasca penambagan nikel.
3. Perlu dilakukan pengembangan dan produksi FMA secara intensif dan kontinyu di persemaian PT INCO Tbk. sebagai langkah awal peningkatan mutu bibit untuk menunjang keberhasilan program rehabilitasi.
DAFTAR PUSTAKA
Achmad, Wilarso S, Mansur I, dan Setiadi Y.1992. Petunjuk Laboratorium Mikrobiologi Tanah Hutan. Bogor. Centre for International Forestry Research.
Brundrett M, Neale B, Bernei D, Tim G dan Nick M. 1996. Working With Mycorrhizas in Forestry and Agriculture. Australian Centre for International Agriculture Research (ACIAR). Canbera: Australia.
Delvian. 2004. Aplikasi Cendawan Mikoriza Arbuskula Dalam Reklamasi Lahan
Kritis Pasca Tambang. [terhubung berkala]. http://repository.usu.ac.id/bitstream/123456789/879/3/hutan-delvian.pdf.txt
Delvian. 2006. Koleksi Isolat Cendawan Mikoriza Arbuskula. [terhubung berkala].
http://repository.usu.ac.id/bitstream/123456789/1048/3/06005280.pdf.txt Ernita. 2004. Pemanfaatan Mikroba Pelarut Phospat dan Mikoriza sebagai
Alternatif Pengganti Pupuk Phospat Pada Tanah Ultisol Kabupaten Langkat Sumatera Utara. Jurnal Penelitian Bidang Pertanian Vol 2 No 3. Desember 2004: 45-55. UMN Al-Washllyah Medan.
Giovannetti M dan Mosse B. 1980. An Evaluation of Techniques for Measuring Vesicular-Arbuscular Mycorrhizal infection in roots. New Phytol. 84 : 489-500.
Gerdemann JW. 1968. Vesicular-Arbuscular Mycorrhiza and Plant Growth. Annu. Rev. Phytopath. 6: 397-418.
Gunawan AW. 1993. Mikoriza Arbuskula. Pusat Antar Universitas Ilmu Hayat. IPB. Bogor.
Habte M. 2000. Mycorrhizal Fungi and Plant Nutrition. College of Tropical Agriculture and Human Resources, University of Hawaii. [terhubung berkala]. http://www.ctahr.hawaii.edu/oc/freepubs/pdf/pnm14.pdf
Hardjowigeno S. 1995. Ilmu Tanah. Edisi revisi. Jakarta : Akademika pressindo. Hudson HJ. 1989. Fungal Biology. Departement of Botany University of
Cambribge.
INVAM. 2010. Classification of Glomeromycota [terhubung berkala]. http://invam.caf.wvu.edu/ [18 Oktober 2010].
Nurmalasari D. 2009. Efektivitas Mycofer® Terhadap Tanaman Kehutanan, Pertanian, Perkebunan, Bioremediasi, dan Pakan Hijau Ternak (Kajian Pustaka).[Skripsi]. Bogor: Program Sarjana, Institut Pertanian Bogor.
Nusantara AD. 2004. Strategi produksi inokulum mikoriza arbuskula bebas patogen. Makalah Pribadi Falsafah Sains (PPS 702). Sekolah pasca sarjana. IPB [terhubung berkala]. http://rudyct.com/PPS702-ipb/08234/abimanyu_dn.htm. [13 November 2009].
Pacioni G. 1992. Wet Sieving and Decanting Techniques for the Extraction of Spores of VA Mycorrizhal Fungi. Di dalam: Methods in Microbiology. San Diego. Academic Press Inc.
34
Santoso E, Turjaman M, dan Irianto R. 2006. Aplikasi Mikoriza Untuk Meningkatkan Kegiatan Rehabilitasi Hutan Dan Areal Terdegradasi. Prosiding Ekspose Hasil-Hasil Penelitian, 2007. Padang.
Schenk NC, Perez Y. 1990. Manual for Identification of VA Mycorrizhal Fungi. Florida. University of Florida.
Setiadi Y. 1989. Pemanfaatan Mikroorganisme Dalam Kehutanan. PAU-IPB. Bogor.
Setiadi Y. 1992. Mikoriza dan Pertumbuhan Tanaman. Departemen Pendidikan dan Kebudayaan, Direktorat Jenderal Pendidikan Tinggi Pusat Antar Universitas IPB. Bogor
Setiadi Y. 1993. Mycorrhiza for reforestation. Makalah presentasi di Biodiversity-Biotechnology Inovation Symposium. British Council. Jakarta, 3 Mei 1993. Setiadi Y. 1995. The Practical Application of Arbuscular Mycorrizhae Fungi for
Reforestation in Indonesia [Thesis]. Kent: Research School of Biosciences, University of Kent.
Setiadi Y. 2001. Peranan Mikoriza Arbuskula dalam Reboisasi Lahan Kritis di Indonesia. Makalah seminar penggunaan CMA dalam sistem pertanian organik dan rehabilitasi lahan. Bandung. 21-23 April 2001.
Setiadi Y dan Hariangbanga G. 2009. Revegetation Techniques for Rehabilitating Degraded Land After Post Mining and Oil/Gas Operation. [tidak dipublikasikan]
Sieverding E. 1991. Vesicular Arbuscular Mychorrizhal Management in Tropical Agrosystems (GTZ). Federal Republic of Germany.
Simanungkalit RDM, Iswandi A, Setiadi Y dan Noordwijk MV. 1999. Microbial Diversity as Affected by Different Land Use Systems in Lampung and Jambi. Di dalam seminar: The International Seminar on Toward Sustainable Agriculture in Humid Tropical Soils Facing the 21st Century. Bandar Lampung (September 26-28, 1999).
Siradz SA dan Kabirun S. 2003. Pengembangan Lahan Marginal Pantai Dengan Bioteknologi Masukan Rendah. Jurusan Tanah, Fakultas Pertanian, Universitas Gadjah Mada, Yogyakarta.
Sondergaard M, Laegaard S. 1977. Vesicular-Arbuscular Mycorrhiza in Some Aquatic Vascular Plants. Nature 268: 232-233.
36
Lampiran 1. Data pohon yang diamati
No Jenis tanaman Nama latin Family
1 Belulang Stemonurus celebicus Icacinaceae
2 Betao Calophyllum spp. Clusiaceae
3 Bitti Vitex cofassus Verbenaceae
4 Buri Weinmannia blumei Cunoniaceae
5 Dengen Dillenia cerrata Dilleniaceae
6 Ekaliptus Eucalyptus urograndis Myrtaceae
7 Ficus Ficus spp. Moraceae
8 Jambu-jambu Syzygium spp. Myrtaceae
9 Jati Tectona grandis Verbenaceae
10 Johar Senna siamea Fabaceae
11 Kayu angin Casuarina equisetifolia Casuarinaceae 12 Kayu tanduk Alstonia spectabilis Apocynaceae 13 Kolaka Maranthes corymbosa Chrysobalanaceae 14 Krei payung Filicium decipiens Sapindaceae
15 Malotus Malotus sp. Euphorbiaceae
16 Nyatoh Palaquium obovatum Sapotaceae
17 Saga Adenanthera pavonina Fabaceae
18 Sengon albizia Paraserianthes falcataria Fabaceae 19 Sengon buto Enterolobium cyclocarpum Fabaceae
Lampiran 2. Tabel kriteria penilaian sifat kimia tanah
Sangat
Masam Masam
Agak
Masam Netral
Agak
Alkalis Alkalis pH H2O < 4,5 4,5 - 5,5 5,6- 6,5 6,6-7,5 7,6-8,5 > 8,5
Sifat Tanah Sangat
Rendah Rendah Sedang Tinggi
Sangat tinggi
C -Organik (%) < 1,00 1,00 - 2,00
2,01 - 3,00
3,01 -
5,00 > 5,00
Nitrogen (%) < 0,10 0,10 - 0,20
0,21 - 0,50
0,51 -
0,75 > 0,75 C/N < 5 5 - 10 11 - 15 16 - 25 > 25 P2O5 HCl (mg/100g) < 10 10 - 20 21 - 40 41 - 60 > 60 P2O5 Bray-1 (ppm) < 10 10 - 15 16 - 25 26 - 35 > 35 P2O5 Olsen (ppm) < 10 10 - 25 26 - 45 46 - 60 > 60 K2O HCl 25%
(mg/100g) < 10 10 - 20 21 - 40 41 - 60 > 60 KTK (me/100g) < 5 5 - 16 17 - 24 25 - 40 > 40
Susunan Kation :
38
Lampiran 3. Rekapitulasi data status FMA hasil pengamatan
No Jenis tanaman Blok %
infeksi Rata-rata % infeksi Kepadatan spora Rata-rata kepadatan spora
Genus Spora Infeksi Miselia Spora
1 Stemonurus celebicus Debbie 75% 75% 45 45 Glomus sp. +++ ++ +
2 Calophyllum spp. Debbie 60% 60% 45 45 Glomus sp. ++ + +
3 Vitex cofassus Nursery 70% 70% 38 38 AcaulosporaGlomus sp; sp. ++ ++ +
4 Weinmannia blumei Nursery 60% 60% 21 21 Glomus sp. ++ + +
5 Dillenia cerrata
Konde 95% 95%
42
84 Glomus sp;
Acaulospora sp. +++ +++ +
Nursery 95% 127
6 Eucalyptus urograndis
Fiona 50%
64%
68
87
Glomus sp;
Acaulospora sp;
Gigaspora sp.
++ ++ +
Konde 50% 21
Manggali 85% 93
Petea 70% 167
7 Ficus spp. Debbie 75% 75% 35 35 Glomus sp;
Gigaspora sp. +++ + +
8 Syzygium spp.
Debbie 60% 53%
21
23 Glomus sp. ++ + ++
Nursery 45% 26
9 Tectona grandis Debbie 80% 80% 154 154 Glomus sp. +++ +++ ++
10 Senna siamea
Fiona 60%
73%
285
151
Glomus sp;
Acaulospora sp;
Gigaspora sp.
++ ++ ++
Konde 60% 100
Petea 100% 68
11 Casuarina equisetifolia
Debbie 90%
78%
71
132
Glomus sp;
Acaulospora sp;
Gigaspora sp.
+++ ++ +
Fiona 80% 318
Konde 70% 74
Manggali 75% 163
Nursery 70%
Petea 80% 156
12 Alstonia spectabilis
Debbie 65% 75%
34
135 GigasporaGlomus sp; sp. +++ +++ +
Fiona 85% 236
13 Maranthes corymbosa Debbie 65% 65% 26 26 Glomus sp. ++ + +
14 Filicium decipiens Nursery 35% 35% 27 27 Glomus sp. + + +
15 Malotus sp.
Fiona 55%
73%
191
156 Glomus sp;
Acaulospora sp. ++ ++ ++
Konde 75% 62
Manggali 95% 79
Petea 65% 290
16 Palaquium obovatum Debbie 50% 50% 33 33 Glomus sp. ++ + +
17 Adenanthera pavonina
Nursery 65% 58%
65
232 Glomus sp. ++ + +++
Petea 50% 400
18 Paraserianthes
falcataria
Debbie 70%
75%
88
188
Glomus sp;
Acaulospora sp;
Gigaspora sp.
+++ ++ ++
Fiona 90% 446
Lanjutan..
No Jenis tanaman Blok %
infeksi
Rata-rata % infeksi
Kepadatan spora
Rata-rata kepadatan spora
Genus Spora Infeksi Miselia Spora
19 Enterolobium
cyclocarpum
Fiona 100%
95%
226
477
Glomus sp;
Acaulospora sp;
Gigaspora sp.
+++ +++ +++
Konde 100% 1618
Manggali 100% 153
Nursery 100% 65
Petea 75% 321
20 Elmerillia tsiampacca Nursery 50% 50% 39 39 Glomus sp;
40
Lampiran 4. Denah lokasi blok pengambilan contoh tanah dan akar
Keterangan :
: Nursery
: Konde
: Manggali
: Debbie
: Fiona
: Petea
![Gambar 1. Klasifikasi FMA. Sumber : http://INVAM.caf.wvu.edu/fungi/taxonomy/classification.htm [9 september 2010]](https://thumb-ap.123doks.com/thumbv2/123dok/810301.375979/18.612.193.474.136.329/gambar-klasifikasi-sumber-invam-fungi-taxonomy-classification-september.webp)