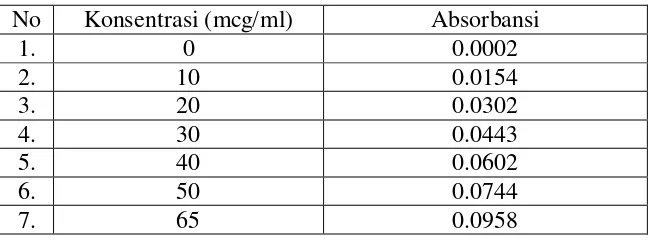
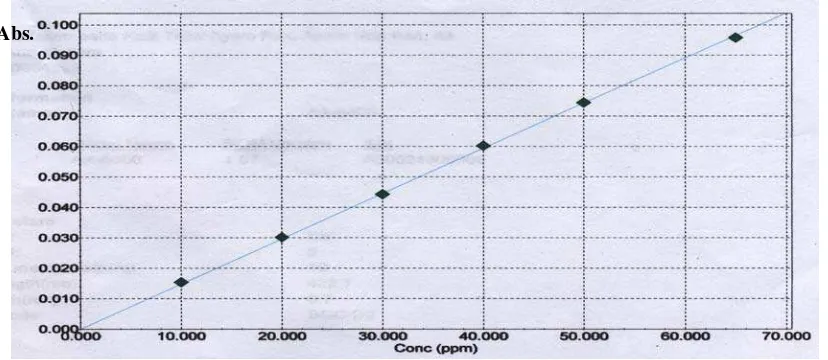
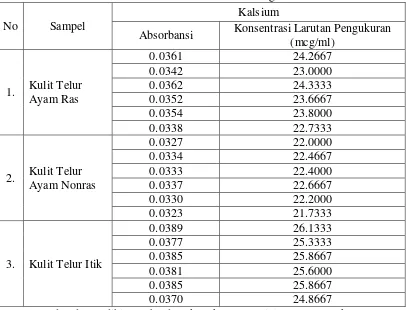
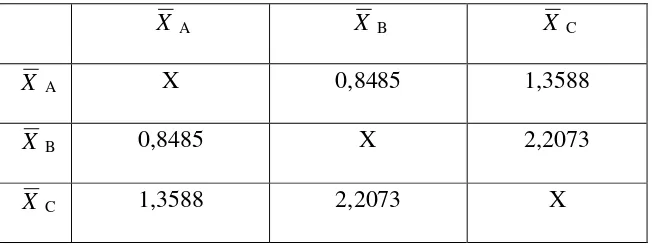
Penetapan Kadar Kalsium Pada Kulit Telur Ayam Ras, Kulit Telur ayam NonRas Dan Kulit Itik Secara Spectrofometri Serapan Atom
Teks penuh
Gambar
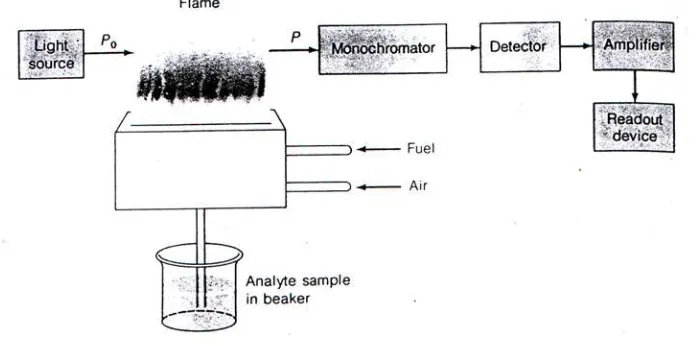
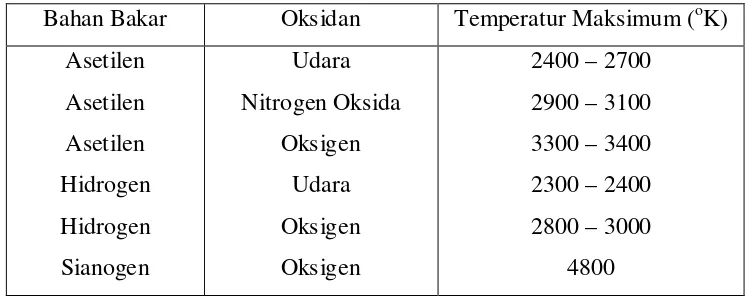
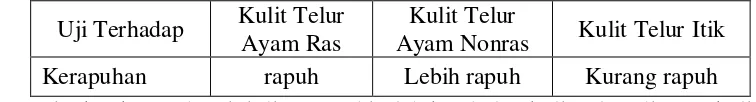

Dokumen terkait
Kajian ini menunjukkan sebahagian daripada pemakai kanta sentuh tidak mempunyai pengetahuan yang cukup mengenai risiko dan bahaya ke atas mata mereka kerana ketidakpatuhan pada
mempengaruhi lingkungan fisik kimiawi, proses dan hasilnya mempengaruhi lingkungan sosial budaya, eksploitasi sumber daya air yang pemanfaatannya berpotensi menimbulkan
Berdasarkan pengkajian ysang dilakukan oleh peneliti didapatkan diagnosa keperawatan yang sama dari responden 1 dan responden 2 yaitu ketidak mampuan ke;luarga untuk
bahwa perubahan tata guna lahan pada daerah hulu, tidak terlalu signifikan, sedangkan pada daerah hilir pada DAS Malalayang terjadi perubahan tata guna lahan yang cukup
Sosialisasi kebijakan merupakan kegiatan untuk memperkenalkan program kerja dari suatu perangkat daerah (PD) dan sosialisasi terkait informasi atau isu serta
Hasil analisis bivariat dengan uji korelasi menunjukkan bahwa ada hubungan antara status gizi menurut IMT/U, persen lemak tubuh, aktivitas fisik, asupan zat besi, dan
Hasil analisa menunujukkan bahwa kapal setelah dimodifikasi memenuhi kriteria IMO, kapal sebelum dimodifikasi memiliki stabilitas lebih baik dari pada kapal setelah
Ciri yang sama juga dapat dilihat pada Gending Rangkung, bahkan pada Gending Rangkung terdapat spesifikasi yang lebih khusus yaitu pada bagian ngelik disajikan dalam irama