ABSTRAK
PROFIL NITRAT ANORGANIK DAN PROTEIN TOTAL INTRASELULER PADA FASE EKSPONENSIAL Nannochloropsis sp.
Oleh
PRATICA FAJRIN
Nitrat anorganik merupakan salah satu sumber nutrien penting dalam kultur Nannochloropsis sp. terutama pada fase eksponensial, dan faktor penentu fluktuasi kepadatan sel dan kandungan protein total intraseluler. Penelitian bertujuan menganalisis pengaruh pengurangan nitrat anorganik sebanyak 50% pada pupuk Conwy terhadap kepadatan dan kandungan protein total intraseluler Nannochloropsis sp. pada fase eksponensial. Hasil penelitian menunjukkan bahwa pengurangan kandungan nitrat anorganik dapat memperpendek fase eksponensial sehingga dapat mempecepat waktu panen mikroalga. Pengurangan nitrat anorganik juga memiliki sisi negatif yaitu penurunan kandungan protein total intraseluler dan kepadatan sel Nannochloropsis sp. Defisiensi nitrat anorganik sebesar 50% cenderung akan menurunkan rasio P/Nt sebesar 19,3% dan menurunkan rasio P/NO3- sebesar 3,26%.
ABSTRACT
THE PROFILE OF INORGANIC NITRATE AND INTRACELLULAR CRUDE PROTEIN ON Nannochloropsis sp. BIOMASS
EXPONENTIAL PHASE
By
PRATICA FAJRIN
Inorganic nitrate is one of the important sources of nutrients in the culture of Nannochloropsis sp. especially in exponential phase, and factor of fluctuations in cell density and intracellular crude protein content. The study aimed to analyze the effect of reduction inorganic nitrate up to 50% in Conwy culture media towards density and intracellular crude protein content Nannochloropsis sp. in exponential phase. The results showed that reduction of inorganic nitrate content can shorten exponential phase so that can accelerate harvest microalgae. Reduction of inorganic nitrate also has a negative side, which was a decrease of intracellular crude protein content and cell density Nannochloropsis sp. Deficiency of inorganic nitrate by 50% inclined to reduce 19,3% of P/Nt ratio and 3,26% of P/NO3- ratio.
RIWAYAT HIDUP
Penulis dilahirkan di Bandar Lampung, pada tanggal 22 November 1992, anak pertama dari dua bersaudara dari pasangan Bapak Wasis Wahyudi dan Ibu Erna Suzmiyanah.
Pendidikan formal penulis diawali dari taman kanak-kanak di TK Kartika II-27 tahun 1997-1998. Pendidikan dasar di SD Kartika II-5 Bandar Lampung tahun 1998-2004. Pendidikan tingkat pertama di SMP Negeri 25 bandar Lampung pada tahun 2004-2007. Pendidikan tingkat atas di SMA Negeri 7 Bandar Lampung tahun 2007-2010. Pada tahun 2010 penulis terdaftar sebagai mahasiswa Program Studi Budidaya Perairan, Fakultas Pertanian, Universitas Lampung melalui jalur Seleksi Nasional Masuk Perguruan Tinggi Negeri (SNMPTN).
Penulis aktif dalam organisasi HIDRILA (Himpunan Mahasiswa Budidaya Perairan Unila) sebagai Sekretaris Bidang Penelitian dan Pengembangan periode 2011/2012 sebagai Sekretaris Umum periode 2012/2013.
Penulis melaksankan Praktik Umum (PU) di Balai Besar Pengembangan Budidaya air Tawar (BBPBAT) Sukabumi, Jawa Barat dengan judul “Pembenihan Ikan Nila Gesit
(Oreochromis niloticus) di Balai Besar Pengembangan Budidaya Air Tawar
Nyata (KKN) Tematik di Desa Panaragan, Kecamatan Tulang Bawang Tengah, Kabupaten Tulang Bawang Barat pada tahun 2014.
Pada tahun 2014, Penulis menyelesaikan tugas akhirnya dengan menulis skripsi yang
Skripsi ini dipersembahkan untuk Allah SWT. yang
selalu memberikan rencana terbaik dari tangan-Nya untuk
masa depan yang penuh harapan,
keluarga tercinta (Ayah, Ibu, Adik),
sahabat-sahabat terbaik
serta seseorang yang selalu memberikan kasihnya yang
terindah di setiap waktu.
Teman angkatan 2010 dan seperjuangan
yang telah bersama - sama memperjuangkan dan menimba ilmu
di program studi
BUDIDAYA PERAIRAN UNILA
serta
Ilmu itu lebih baik daripada harta. Ilmu menjaga engkau
dan engkau menjaga harta. Ilmu itu penghukum (hakim)
dan harta terhukum. Harta itu kurang apabila
dibelanjakan tapi ilmu bertambah bila dibelanjakan.
(Saidina Ali bin Abi Talib)
Barang siapa menempuh satu jalan untuk mendalami ilmu
maka Allah akan permudahkan baginya satu jalan ke surga
(HR. Muslim)
Jika
kau ingin menjadi seseorang dalam hidup…
Jika kau ingin mendapatkan sesuatu…
Jika kau ingin memenangkan sesuatu, selalu dengarkan
kata hatimu,
dan jika itu juga tak memberimu jawaban…
Tutup kedua matamu dan pikirkan kedua orangtuamu,
maka semua rintangan dan halangan akan hancur, dan
engkau akan mendapatkan yang dirimu inginkan.
Kemenangan hanya milikmu dan hanya milikmu.
M o t o :
Pendidikan adalah bekal terbaik untuk hari tua.
Orang yang paling sempurna bukanlah orang dengan otak
yang sempurna, melainkan orang yang dapat
mempergunakan sebaik-baiknya dari bagian otaknya yang
kurang sempurna
(Aristoteles)
Education is not the learning of facts, but the training of the
SANWACANA
Puji syukur penulis panjatkan kehadirat Allah SWT. atas kasih karunia-Nya
sehingga penulis dapat menyelesaikan skripsi ini. Skripsi dengan judul “Profil
Nitrat Anorganik dan Protein Total Intraseluler pada Fase Eksponensial Biomassa
Nannochloropsis sp.” ini disusun sebagai salah satu syarat memperoleh gelar Sarjana Perikanan di Universitas Lampung.
Dalam kesempatan ini penulis menyampaikan ucapan terima kasih kepada:
1. Ayah, Ibu dan adik yang telah memberikan semangat, dukungan, kasih
sayang dan, doa selama penulisan skripsi ini.
2. Bapak Prof. Dr. Ir. Wan Abbas Zakaria, M.S. selaku Dekan Fakultas
Pertanian Universitas Lampung.
3. Ibu Ir. Siti Hudaidah, M.Sc. selaku Ketua Program Studi Budidaya Perairan
Universitas Lampung.
4. Bapak Moh. Muhaemin, S.Pi., M.Si. selaku pembimbing akademik dan
selaku pembimbing pertama yang telah membimbing, membantu serta
memberi masukan, kritik, saran, dukungan, serta motivasi pada penulis dalam
5. Ibu Esti Harpeni, S.T., MAppSc. selaku pembimbing kedua yang telah
membimbing, membantu serta memberi dukungan penulis dalam proses
penyusunan skripsi ini.
6. Bapak Agus Setyawan, S.Pi., M.P. selaku pembahas yang telah memberi
masukan, kritik, dan saran dalam proses penyusunan skripsi ini.
7. Rosi Dona Simatupang atas kerjasama, bantuan dan semangat sebagai patner
selama penelitian hingga akhir skripsi.
8. Oktarinaldi I. yg telah memberikan bantuan, motivasi dan semangat dalam
pennyusunan skripsi.
9. Duma, Jelita, Sera, Tita, dan Angga yang selalu ceria, terima kasih atas
kebersamaan kita, yang telah mendukung selama perkuliahan, proses skripsi
dan masa kompre.
10. Sahabatku Melina dan Fitri terima kasih atas motivasi dan persahabatan dari
sekolah dasar hingga penulis menyelesaikan perkuliahan.
11. Teman-teman SMA Devi, April dan Weni yang selalu memberi semangat dan
motivasi kepada penulis.
12. Teman-teman angkatan 2010 yang terkasih, untuk setiap doa, kehangatan,
keributan, kesatuan, dan kedewasaan yang datang bersama kalian selama
masa-masa kebersamaan yaitu ardi (masangin lampu), shoffan (minjemin
genset), soma (komti), anggi (ketum, udah pinjemin motor), anjar (ableh),
opeh, asry, winda, bg yul, windi, olip, bang dio, septi, aulia, maul, ely, siti,
dwinda, dike, safrina, nyinyi, rima, frisca, dian, ncim, memed, oji, regi,
mpeb, aan, baihaqi, om boci, njum, erwin (bebeb), ali (bos cupang), salsin,
13. Adik asuh Rizky Alfiani yang selalu memberi semangat dan dukungan untuk
penulis.
Serta semua teman dan pihak yang tidak dapat disebutkan satu persatu. Akhir
kata, saya berharap Allah SWT. berkenan membalas segala kebaikan semua pihak
yang telah membantu. Semoga skripsi ini membawa manfaat bagi pengembangan
ilmu khususnya bidang perikanan.
Bandar Lampung, Agustus 2014
Penulis,
xv DAFTAR ISI
Halaman
DAFTAR ISI ………..…………... xv
DAFTAR TABEL ……….….….... xvii
DAFTAR GAMBAR ……….…..... xviii
DAFTAR LAMPIRAN ………... xx
I. PENDAHULUAN 1.1 Latar Belakang ... 1
1.2 Perumusan Masalah ... 4
1.3 Tujuan Penelitian ………. 5
1.4 Manfaat ………. 6
1.5 Hipotesis ………. 6
II. TINJAUAN PUSTAKA 2.1 Biologi Nannochloropsis sp. 2.1.1 Klasifikasi dan Morfologi ………. 7
2.1.2 Pertumbuhan Nannochloropsis sp. ………... 10
2.1.3 Faktor Pembatas ………... 13
2.2 Protein ……….………….. 15 2.3 Nitrogen ……….….. 16
III. METODOLOGI 3.1 Tempat dan Waktu Penelitian ……….………….. 20
3.2 Materi Penelitian 3.2.1 Biota Kultur ………..…. 20
3.2.2 Media Kultur ………... 20
3.3 Alat dan Bahan Penelitian 3.3.1 Alat ………... 21
3.3.2 Bahan ………... 22
3.4 Rancangan Penelitian ………...... 22
3.5 Prosedur Penelitian 3.5.1 Persiapan ……….….. 25
3.5.2 Pelaksanaan Penelitian ……….….. 26
xvi 3.6.1 Uji Proksimat Protein ………..………. 27 3.6.2 Uji Kandungan Nitrat ………..……. 29
3.6.3 Model Regresi Linier ………... 30
3.6.4 Penghitungan Kepadatan Nannochloropsi sp. …...……… 31 3.7 Analisis Data
3.7.1Hubungan Antar Dua Variabel Dependen ………... 32
IV. HASIL DAN PEMBAHASAN
4.1 Hubungan Linier Absorbansi Spektrofotometer (Å) dalam Kepadatan Sel Nannochloropsis sp. (sel/ml) ……….…….. 34 4.2 Pertumbuhan Nannochloropsis sp. ………... 35 4.3 Perubahan Konsentrasi Nitrat Anorganik pada Media Kultur
Nannochloropsis sp. ………... 38 4.4 Kandungan Protein Total Intraseluler pada Nannochloropsis sp. …... 41 4.5 Hubungan Antar Variabel
4.5.1Hubungan Linier antara Kepadatan (Nt) dengan Protein Total Intraseluler Nannochloropsis sp. ………... 43 4.5.2Hubungan Polinomial Kepadatan (Nt) dengan Nitrat Anorganik
pada Media Kultur ………... 46
4.5.3Hubungan Polinomial Nitrat Anorganik dengan Protein Total
Intraseluler ………... 48
V. KESIMPULAN
5. 1 Kesimpulan ………... 51
5. 2 Saran ………... 51
xvii DAFTAR TABEL
Tabel Halaman
1. Komposisi pupuk Conwy skala laboratorium ... 21
xviii DAFTAR GAMBAR
Gambar Halaman
1. Diagram kerangka pikir penelitian ………... 5
2. Koloni Nannochloropsis sp. ………... 8
3. Sel Nannochloropsis sp. ………. 9
4. Morfologi sel Nannochloropsis sp. ………... 9
5. Pola pertumbuhan Fitoplankton ………... 12
6. Proses perombakan nitrat dari luar tubuh menjadi protein dalam tubuh ….. 18
7. Tata letak wadah kultur Nannochloropsis sp. ……... 23
8. Alur penelitian ………... 24
9. Hubungan linier antara absorbansi spektrofotometer dan kepadatan sel Nannochloropsis sp.dengan optical density (OD) 650 nm …………... 35
10. Kepadatan Nannochloropsis sp. pada tiap perlakuan (a) NaNO3 100%; (b) NaNO3 50% ………... 38
11. Perubahan konsentrasi nitrat anorganik pada media kultur Nannochloropsis sp. pada tiap perlakuan (a) NaNO3 100%; (b) NaNO3 50% ………... 40
12. Perubahan konsentrasi protein total intraseluler pada media kultur Nannochloropsis sp. pada tiap perlakuan (a) NaNO3 100%; (b) NaNO3 50% ………...…… 43
xix 14. Hubungan polinomial kepadatan Nannochloropsis sp. (Nt) dengan nitrat anorganik pada media kultur di tiap perlakuan (a) NaNO3 100%; (b) NaNO3
50% ………... 47
15. Hubungan Polinomial Nitrat Anorganik dengan Protein Total Intraseluler Nannochloropsis sp. pada tiap perlakuan (a) NaNO3 100%; (b) NaNO3
xx DAFTAR LAMPIRAN
Lampiran Halaman
1. Uji t kepadatan rata-rata sel Nannochloropsis sp. ... 57
2. Uji t protein total intraseluler Nannochloropsis sp. ... 59
3. Uji t nitrat anorganik pada media kultur Nannochloropsis sp. ... 61
4. Cara penggunaan Spektrofotometer Genesys 20 ... 63
5. Penyimpanan sampel uji setelah pengambilan sampel pengamatan ... 64
1
I. PENDAHULUAN
1.1 Latar Belakang
Mikroalga merupakan organisme air fotoautropik uniseluler atau
multiseluler (Biondi and Tredici, 2011). Mikroalga hidup dengan berkoloni,
berfilamen atau helaian pada kondisi sel tunggal (Stanley, 2000). Secara umum
mikroalga dikenal sebagai organisme mikroskopik yang hidup dari nutrien
anorganik dan produksi zat organik yang berasal dari proses fotosintesis.
Mikroalga dapat mengubah nutrien anorganik menjadi bahan organik sehingga
dapat menghasilkan oksigen yang diperlukan oleh makhluk hidup yang tingkat
tropiknya lebih tinggi, sehingga mikroalga berperan sebagai produsen tingkat
pertama dalam rantai makanan (Isnansetyo dan Kurniastuty, 1995).
Mikroalga memiliki peranan penting dalam proses budidaya sebagai pakan
alami bagi zooplankton dan larva ikan. Harun et.al. (2010) menjelaskan bahwa mikroalga memiliki kandungan protein alami yang tinggi sehingga berpotensi
menghasilkan berbagai macam produk seperti karotenoid, fikobilin, asam lemak,
polisakarida, vitamin, sterol, enzim dan senyawa bioaktif lainnya. Mikroalga
dapat pula dimanfaatkan sebagai penyerap beberapa senyawa yang bersifat racun
bagi larva, mengendalikan kandungan CO2 sehingga dapat meningkatkan oksigen
terlarut, penyangga kualitas air dalam bak larva, anti bakterial imunostimulan, dan
2 1995). Selain itu mikroalga juga memiliki peran sebagai agen bioremediasi logam
berat (Muhaemin, 2009). Bahkan mikroalga juga mampu mengurangi secara
signifikan konsentrasi gas rumah kaca, sehingga memberikan solusi untuk global warming (Harun et.al., 2010). Salah satu mikroalga yang sering dimanfaatkan untuk pakan alami bagi larva ikan adalah Nannochloropsis sp.
Nannochloropsis sp., adalah salah satu jenis Chlorophyta yang dapat melakukan fotosintesis. Nannochloropsis sp. merupakan salah satu jenis mikroalga yang banyak dimanfaatkan sebagai pakan alami, terutama untuk pakan
benih ikan. Beberapa unsur hara makro dan mikro diperlukan Nannochloropsis sp. untuk dapat hidup (Purwitasari et.al, 2012). Secara umum mikroalga membutuhkan nutrien untuk pertumbuhannya diantaranya karbon (dihasilkan dari
CO2 atau HCO3-), nitrogen (seperti NO3-), pospor (berbentuk ortopospat), sulfur
(SO42-), dan elemen tambahan seperti Na, K, Mg, Fe, Co, dan Mo (Stanley, 2000).
Protein memiliki peran penting di dalam tubuh, diantaranya untuk proses
pembentukan sel-sel baru sehingga dapat memperbaiki jaringan tubuh yang rusak.
Nannochloropsis sp. sebagai mikroalga memiliki peran sebagai sumber protein bagi larva ikan. Kandungan gizi pada Nannochloropsis sp. sangat baik untuk pertumbuhan larva karena kandungan proteinnya yang tinggi. Kebanyakan
mikroalga memiliki kandungan protein yang tinggi sekitar 20% dari berat
basahnya (Isnansetyo dan Kurniastuty, 1995).
Populasi Nannochloropsis sp. yang terus meningkat dapat menyebabkan makin berkurangnya nutrien yang dibutuhkan oleh Nannochloropsis sp. untuk terus tumbuh, di mana tingkat pertumbuhan tersebut bergantung pada konsentrasi
3 pertumbuhan fitoplankton di lautan. Nitrogen yang terdapat pada media kultur
biasanya 1.000 kali lebih terkonsentrasi daripada di perairan alami. Fitoplankton
memiliki kemampuan untuk menggunakan asam amino sebagai sumber nitrogen
pada konsentrasi tinggi (Lavens and Sorgeloos, 1996).
Adanya pertumbuhan dalam kultur fitoplankton ditandai dengan
bertambahnya jumlah sel fitoplankton dan bertambah besarnya ukuran sel
(Isnansetyo dan Kurniastuty, 1995). Pertumbuhan fitoplankton dibagi dalam
beberapa fase yaitu fase lag, fase logaritmik atau eksponensial, fase berkurangnya
pertumbuhan relatif, fase stasioner, dan fase kematian (Lavens and Sorgeloos,
1996).
Nannochloropsis sp. yang dikultur skala laboratorium memiliki ukuran 2-3µm dan berada pada kondisi optimal dengan pH 8, suhu 23oC dan salinitas
30 ppt. Kondisi lingkungan mikro, terutama stress nitrogen di ekosistem laut,
menjadi faktor utama yang mempengaruhi pertumbuhan Nannochloropsis sp. Profil nitrat anorganik dan protein total intraseluler pada fase eksponensial
biomassa Nannochloropsis sp. belum banyak dilakukan sehingga perlu adanya penelitian mengenai pengaruh peningkatan dan penurunan kandungan nitrogen
anorganik pada fase eksponensial Nannocholoropsis sp. Pengamatan pada fase eksponensial pada kultur Nannochloropsis sp. penting untuk mempersingkat waktu kultur pada fase pertumbuhan sehingga menyebabkan melandainya waktu
4 1.2 Perumusan Masalah
Mikroalga merupakan sumber produktifitas primer dalam rantai makanan
pada ekosistem perairan karena merupakan organismee autotrof yang dapat
menghasilkan makanannya sendiri melalui proses fotosintesis. Mikroalga
berperan penting sebagai pakan zooplankton dan larva ikan karena memiliki
kandungan protein yang tinggi (Isnansetyo dan Kurniastuty, 1995). Pertumbuhan
mikroalga dalam kultur dapat ditandai dengan bertambah banyaknya jumlah sel
melalui fase pertumbuhan yaitu fase eksponensial. Isnansetyo dan Kurniastuty
(1995) menjelaskan bahwa fase eksponensial merupakan fase pertumbuhan
mikroalga yang ditandai dengan pembelahan sel dengan laju pertumbuhan yang
tetap. Pertumbuhan mikrolaga sangat dipengaruhi oleh kondisi lingkungan,
dimana makin ekstrim kondisi suatu lingkungan akan memperpanjang waktu fase
eksponensial pada mikroalga. Berdasarkan hasil penelitian Muhaemin (2005) fase
eksponensial pada mikroalga dicapai dengan kisaran waktu kultur antara 5-120
jam.
Hudaidah et.al. (2013) mengindikasikan bahwa pengurangan nutrien berupa nitrat anorganik mampu menekan pengaruh lingkungan eksternal sehingga
menyebabkan fluktuasi produksi lipid dan protein pada biomassa mikroalga.
Kemampuan tersebut muncul diduga berkaitan dengan makin melandainya waktu
fase eksponensial pada kurva pertumbuhan. Indikasi tersebut dapat menjadi dasar
untuk mengetahui apakah pengurangan nitrat anorganik juga dapat
mempersingkat fase eksponensial dan meningkatkan kandungan protein pada
5 satunya dengan menyediakan kondisi nutrien yang sesuai bagi pertumbuhannya
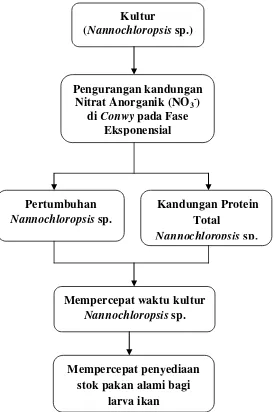
terutama pada fase pertumbuhan (fase eksponensial). Diagram kerangka pikir
penelitian digambarkan dalam Gambar 1.
Gambar 1. Diagram kerangka pikir penelitian
1.3 Tujuan penelitian
Tujuan penelitian antara lain:
a. menganalisis pengaruh konsentrasi nitrat anorganik pada media terhadap
kepadatan Nannochloropsis sp. pada fase eksponensial. Kultur
(Nannochloropsis sp.)
Pengurangan kandungan Nitrat Anorganik (NO3-)
di Conwy pada Fase Eksponensial
Kandungan Protein Total
Nannochloropsis sp. Pertumbuhan
Nannochloropsis sp.
Mempercepat waktu kultur Nannochloropsis sp.
Mempercepat penyediaan stok pakan alami bagi
6 b. menganalisis pengaruh kepadatan terhadap kandungan protein total
intraseluler Nannochloropsis sp. pada fase eksponensial.
c. menganalisis hubungan antara pemanfaatan nitrat anorganik dan kandungan
protein total intraseluler Nannochloropsis sp. pada fase eksponensial
1.4 Manfaat
Penelitian diharapkan dapat memberikan informasi mengenai konsentrasi
nitrat yang mendukung pertumbuhan optimal biomassa Nannochloropsis sp. dan berpengaruh pada protein total intraseluler pada fase eksponensial.
1.5 Hipotesis
Hipotesis yang diuji adalah terdapat pengaruh nitrat anorganik (sebagai
nutrien) terhadap kepadatan dan protein total intraseluler pada fase eksponensial
7 II. TINJAUAN PUSTAKA
2.1 Biologi Nannochloropsis sp. 2.1.1 Klasifikasi dan Morfologi
Mikroalga diartikan berbeda dengan tumbuhan yang biasa dikenal walaupun
secara struktur tubuh keduanya memiliki klorofil sehingga dapat melakukan
fotosintesis (Bold and Wynne, 1985). Fitoplankton Nannochloropsis sp., adalah salah satu jenis mikroalga yang dapat melakukan fotosintesis. Klasifikasi
Nannochloropsis sp. menurut Hibberd (1981) adalah sebagai berikut : Kingdom : Chromista
Super Divisi : Eukaryotes
Divisi : Heterokontophyta
Kelas : Eustigmatophyceae
Ordo : Eustigmatales
Famili : Monodopsidaceae
Genus : Nannochloropsis Spesies : Nannochloropsis sp.
Divisi Eustigmatophyta merupakan kelompok mikroalga dengan 7 genus
dan 12 spesies. Mikroalga divisi Eustigmatophyta meliputi mikroalga laut, air
8 bersifat uniseluler, sel berbentuk coccoid dan dinding sel polisakarida.
Eustigmatophyta mengandung satu kloroplas berwarna hijau kekuninan yang
mengandung klorofil badan pigmen aksesori violaxanthin dan β-karoten dan
merupakan organisme autotrof (Hibberd, 1981). Salah satu spesies mikroalga dari
divisi Eustigmatophyta adalah Nannochloropsis sp.
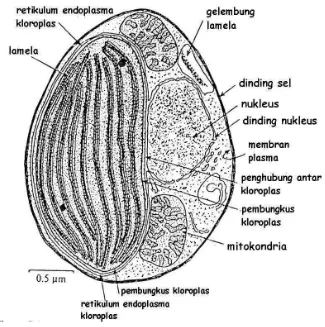
Sel Nannochloropsis sp. bersifat non-motil, berbentuk bulat telur, berdiameter 2-4 m, memiliki pyrenoid dalam kloroplas tunggal dan mengandung
klorofil-a (Biondi, 2011). Sedangkan Hoek et.al. (1998) menjelaskan bahwa Nannochloropsis sp. merupakan fitoplankton berwarna hijau yang berukuran
2-4 m dan tidak memiliki flagel (Gambar 2). Nannochloropsis sp. dapat
melakukan fotosintesis karena memiliki klorofil-a yang terdapat di kloroplas. Tiap
satu sel Nannochloropsis sp. (Gambar 3) hanya memiliki satu kloroplas yang mengandung pyrenoid.
9 Gambar 3. Sel Nannochloropsis sp. (perbesaran 100x)
10 Nannochloropsis sp. dapat hidup di banyak tempat (kecuali tempat yang kritis bagi kehidupannya) sehingga bersifat kosmopolit dan dapat hidup pada
salinitas optimum sekitar 20 – 25 ‰. Nannochloropsis sp. Selain itu fitoplankton ini hidup pada pH 8-9,5; intensitas cahaya 1.000 – 10.000 lux dan suhu 25o-30o C.
Selain itu Nannochloropsis sp. masih dapat bertahan hidup pada suhu 40o C namun pertumbuhannya tidak normal (Balai Budidaya Laut, 2002).
Genus Nannochloropsis meliputi laut dan spesies air tawar, meskipun bioteknologi dari alga ini pada saat ini terbatas pada spesies laut (Biondi, 2011).
Nannochloropsis sp. merupakan salah satu jenis mikroalga yang banyak dimanfaatkan sebagai pakan alami, terutama untuk pakan larva ikan.
Nannochloropsis sp. memerlukan beberapa unsur hara makro dan mikro untuk dapat hidup. Unsur makro yang diperlukan Nannochloropsis sp. seperti N, P, K sedangkan unsur mikro yang dibutuhkan Nannochloropsis sp. diantaranya Mg, Mn, S, Zn dan Cu. Unsur hara makro dapat digunakan dalam media kultur dengan
bentuk yang berbeda misalnya dalam bentuk NO3-, NO2- dan NH4 (Bold and
Wynne, 1985). Nitrogen (N) merupakan unsur makro yang paling dibutuhkan oleh
Nannochloropsis sp. dalam jumlah banyak dibandingkan unsur yang lain karena nitrogen merupakan senyawa yang mudah larut di dalam air sehingga mudah
dimanfaatkan oleh Nannochloropsis sp. sebagai sumber nutrien (Purwitasari et.al, 2012).
2.1.2 Pertumbuhan Nannochloropsis.sp
Adanya pertumbuhan dalam kultur fitoplankton ditandai dengan
11 and Sorgeloos (1996) menjelaskan bahwa pertumbuhan fitoplankton dibagi dalam
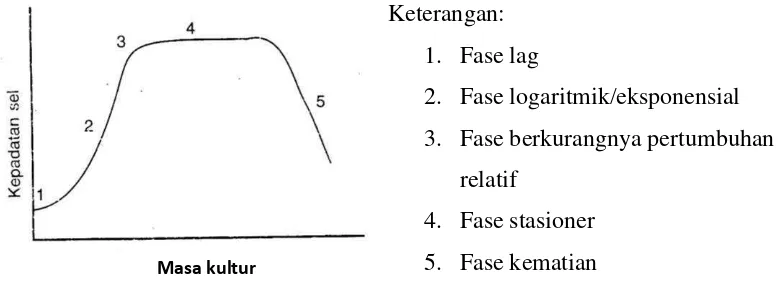
beberapa fase (Gambar 4) yaitu fase lag, fase logaritmik/eksponensial, fase
berkurangnya pertumbuhan relatif, fase stasioner, dan fase kematian.
1. Fase Lag
Pada fase lag belum mengalami perubahan. Pada fase ini pertumbuhan
fitoplankton dikaitkan dengan adaptasi fisiologis metabolisme sel
pertumbuhan fitoplankton, seperti peningkatan kadar enzim dan metabolit
yang terlibat dalam pembelahan sel dan fiksasi karbon.
2. Fase Logaritmik atau Eksponensial
Pada fase eksponensial sel fitoplankton telah mengalami pembelahan sel
dengan laju pertumbuhannya tetap. Pertumbuhan fitoplankton dapat
maksimal tergantung pada spesies alga, nutrien, intensitas cahaya, dan
temperatur.
3. Fase berkurangnya pertumbuhan relatif
Pertumbuhan sel mulai melambat ketika nutrien, cahaya, pH, CO2 atau
faktor kimia dan fisika lain mulai membatasi pertumbuhan.
4. Fase Stasioner
Pada fase keempat faktor pembatas dan tingkat pertumbuhan seimbang.
Laju kematian fitoplankton relatif sama dengan laju pertumbuhannya
sehingga kepadatan fitoplankton pada fase ini relatif konstan.
5. Fase Kematian
Pada fase kematian, kualitas air memburuk dan nutrient habis hingga ke
12 menurun dengan cepat karena laju kematian fitoplankton lebih tinggi
daripada laju pertumbuhannya hingga kultur berakhir.
Keterangan: 1. Fase lag
2. Fase logaritmik/eksponensial 3. Fase berkurangnya pertumbuhan
relatif
[image:32.595.115.504.168.312.2]4. Fase stasioner 5. Fase kematian
Gambar 5. Pola pertumbuhan fitoplankton (Lavens and Sorgeloos, 1996).
Fase eksponensial ditandai dengan cepatnya pertumbuhan sel
Nannochloropsis sp. pada fase tersebut dengan diiringi banyaknya produksi pigmen Nannochloropsis sp (Chalid, 2010). Yanuaris (2012) menjelaskan bahwa pada kultur fitoplankton, fase eksponensial mulai terjadi pada hari pertama hingga
hari kedua karena ketersediaan nutrien untuk Nannochloropsis sp. habis terserap pada hari itu.
Pada fase eksponensial fitoplankton memiliki waktu penggandaan yang
lebih singkat dibanding fase lag apabila lingkungan adaptasinya baik. Cepatnya
pembelahan sel fitoplankton dapat disebabkan oleh kebutuhan nutrien yang
tercukupi (Resmawati et.al, 2012). Muhaemin (2005) menjelaskan bahwa fase eksponensial pada kultur mikroalga berada pada kisaran jam ke 5-120 di mana
fase tersebut ditandai dengan meningkatnya densitas fitoplankton yang signifikan
13 2.1.3 Faktor Pembatas
Kepadatan dan nutrisi pada fitoplankton dipengaruhi oleh beberapa faktor
lingkungan, diantaranya suhu, cahaya, pH air dan jumlah nutrien yang ada
(Isnansetyo dan Kurniastuty, 1995).
1. Suhu
Pertumbuhan sel dalam kultur fitoplankton ditandai dengan bertambah besar
dan bertambah banyaknya ukuran sel. Suhu dalam kultur mempengaruhi
keberhasilan fitoplankton. Suhu air yang optimal bagi pertumbuhan fitoplankton
adalah sekitar 23-25oC pada skala laboratorium dan 30oC pada skala masal dan
semi masal (Sari dan Manan, 2012). Sementara itu menurut Barsanti dan Paulo
(2006) suhu yang sesuai pertumbuhan fitoplankton pada iklim tropis adalah
>20oC, namun biasanya kebanyakan jenis fitoplankton dapat menoleransi suhu
antar 16-27 oC.
2. Cahaya
Pada kultur fitoplankton, cahaya merupakan faktor terpenting karena
fitoplankton membutuhkan cahaya untuk proses fotosintesis (Isnansetyo dan
Kurniastuty, 1995). Cahaya dalam kultur fitoplankton diperoleh dari penyinaran
lampu neon. Penyinaran cahaya haru sesuai untuk kultur, apabila cahaya terlalu
terang akan menghambat proses fotosintesis, durasi pencahayaan buatan minimum
harus 18 jam (Lavens and Sorgeloos, 1996). Sari dan Manan (2012) menjelaskan
bahwa untuk kultur skala laboratorium cahaya didapat dari cahaya lampu TL
14 3. pH Air
Kondisi pH yang baik diperlukan untuk kultur fitoplankton terutama pada
saat panen. Pada saat itu proses koagulasi fitoplankton harus berada pada kondisi
maksimum agar waktu koagulasi fitoplankton lebih singkat dan presentase
tenggelam tinggi. Kondisi tersebut dapat dicapai dengan penambahan NaOH
100 ppm pada pH 8 (Muhaemin dkk, 2006). Sari dan Manan (2012) menjelaskan
bahwa nilai pH diukur dengan menggunakan pH meter. Nilai pH pada kultur
fitoplankton skala laboratorium dan semi masal berkisar antara 7,7 - 7,8.
Sementara itu menurut Barsanti dan Gualtieri (2006) pH yang sesuai untuk kultur
fitoplankton adalah antara 7-8 dengan rentang optimum 8,2-8,7. Rentang pH
untuk kultur kebanyakan spesies alga adalah antara 7-9 dan rentang optimumnya
antara 8,2-8,7 (Lavens and Sorgeloos, 1996).
4. Nutrien
Pada kultur fitoplankton nutrien seperti unsur makro dan mikro sangat
diperlukan untuk makanan fitoplankton. Unsur makro seperti N, P, K, S, Na, Si,
dan Ca serta unsur mikro seperti Fe, Zn, Mn, Cu, Mg, Mo, Co, B, dan lain-lain
masing-masing memiliki fungsi pada pertumbuhan fitoplankton. Dalam
pembentukan protein unsur N, P dan S sangat diperlukan. Selain itu unsur K
berfungsi dalam metabolisme karbohidrat, Fe dan Na berguna dalam
pembentukan protein, sedangkan Si dan Ca berfungsi dalam pembentukan dinding
15 2.2 Protein
Komponen penting dan utama pada sel hewan atau manusia adalah protein,
karena protein berperan sebagai zat utama dalam pembentukan tubuh (Isnansetyo
dan Kurniastuty, 1995). Protein memiliki fungsi biologis yang sangat luas dan
merupakan polipeptida yang terbentuk secara alami. Berat molekul protein dapat
lebih besar dari 5000 (Kuchel and Ralston, 2006).
Protein digolongkan dalam dua golongan, yaitu protein sederhana yang
terdiri atas molekul-molekul asam amino dan protein gabungan yang terdiri atas
protein dan gugus bukan protein. Protein sederhana dapat dibagi menjadi protein
fiber dan protein globular, sedangkan protein gabungan diantaranya mukoprotein,
glikoprotein, lipoprotein, dan nukleoprotein. Di dalam air protein akan
membentuk ion positif dan ion negatif.
Berdasarkan fungsi struktur dan mekanisme kerja protein dibagi dalam
empat kelas utama, yaitu (1) Protein pengubah (Transforming proteins) adalah protein yang mengubah satu jenis energi ke energi yang lain, seperti energi kimia
menjadi energi mekanik (protein otot). Enzim merupakan salah satu contoh
protein dalam protein pengubah karena dapat mengubah energi kimia menjadi
jenis lain dari energi kimia berdasarkan mengubah satu zat kimia menjadi lain. (2)
Protein informasi (Informational proteins), berfungsi dalam transmisi atau pemrosesan informasi. (3) Protein struktural (Structural proteins) berperan sebagai pembentuk blok dalam sel, atau sebagai bagian dari kerangka kerja di luar
16 organisme berbahaya dan termasuk antibodi, protein pembekuan darah dan racun
(Robson and Garnier, 1988)
Protein akan membentuk ion positif apabila dalam suatu perairan dalam
keadaan asam sedangkan apabila kondisi perairan dalam keadaan basa protein
akan membentuk ion negatif. Aktifitas biokimiawi protein dapat berkurang
apabila terdapat perubahan di lingkungan seperti perubahan suhu, pH atau karena
reaksi dengan senyawa lain sehingga konformasi molekulnya berubah. Aktifitas
dan kemampuan protein untuk menunjang aktivitas organ tubuh tertentu akan
berkurang apabila suatu protein mengalami konformasi pada molekulnya
(Poedjiadi, 1994). Kandungan protein per sel fitoplankton yang dianggap sebagai
salah satu faktor yang paling penting untuk menentukan nilai gizi fitoplankton
sebagai pakan dalam budidaya ikan. Kandungan protein untuk Nannochloropsis oculata dalam berat kering adalah sebesar 2,1 pg/cell dengan presentase 35% (Lavens and Sorgeloos, 1996).
2.3 Nitrogen
Pada media pertumbuhan fitoplankton, unsur yang paling penting di fase
pertumbuhan eksponensial adalah konsentrasi N yang tinggi pada NaNO3. Hal itu
disebabkan karena tetap berlangsungnya aktivitas metabolisme sel dalam jangka
waktu optimum sehingga pembelahan sel terus berlangsung di fase eksponensial.
Kandungan nitrogen yang tinggi dalam NaNO3 pada media tumbuh fitoplankton
dapat menghasilkan fitoplankton yang memiliki kandungan protein yang tinggi
(Suminto, 2009). Reynolds (2006) menjelaskan bahwa nitrogen merupakan
17 fitoplankton setelah asam amino. Konsentrasi nitrogen dalam NaNO3 yang rendah
akan mengakibatkan rendahnya jumlah protein dalam fitoplankton, karena dalam
proses sintesis asam amino nitrogen diperlukan sebagai penyusun protein dalam
sel (Colla et al., 2005 dalam Suminto, 2009). Nitrogen yang terdapat pada media tumbuh fitoplankton memiliki peran penting dalam pembentukan protein
(Isnansetyo dan Kurniastuty, 1995).
Nitrogen merupakan senyawa yang berfungsi sebagai penyusun protein dan
klorofil pada tumbuhan dan hewan. Di perairan, nitrogen didapat bukan dalam
bentuk gas namun berupa nitrogen organik dan nitrogen anorganik. Nitrogen
organik berupa protein, asam amino dan urea, sedangkan nitrogen anorganik
terdiri atas ammonia (NH3), ammonium (NH4), Nitrit (NO2), Nitrat (NO3) dan
molekul nitrogen dalam bentuk gas (N). Nitrat yang menjadi sumber nitrogen
untuk penuyusun protein pada tumbuhan diperoleh dari proses konversi. Proses
tersebut dapat dilihat pada persamaan reaksi (Effendi, 2003).
NO3- + CO2 + tumbuhan + cahaya matahari protein
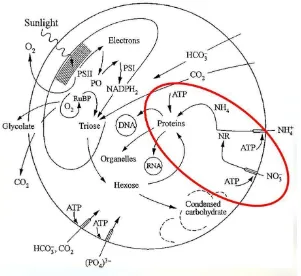
Mikrolaga membentuk protein dalam tubuh dengan mengambil nutrien yang
dibutuhkan untuk pembentukan protein dari luar tubuhnya seperti NO3-
(Reynolds, 2006). Perubahan nitrat menjadi protein dalam tubuh fitoplankton
18 Gambar 6. Proses perombakan nitrat dari luar tubuh menjadi protein dalam tubuh
(lingkaran merah) (Reynolds, 2006)
Salah satu senyawa nitrogen yang penting bagi mikroalga adalah dalam
bentuk senyawa nitrat. Bentuk penting dari kombinasi nitrogen yang dapat
dimanfaatkan oleh fotoautotrof seperti fitoplankton adalah ion nitrat (NO3-), nitrit
(NO2-) dan ammonium (NH4+) meskipun tidak semua jenis fitoplankton dapat
memanfaatkannya (Reynolds, 2006). Sementara itu menurut Edhy dkk (2003)
nitrogen yang dapat dimanfaatkan langsung oleh fitoplankton secara langsung
adalah ammonia bebas (NH3) dan nitrat (NO3-). Nitrat merupakan bentuk dari
nitrogen di perairan yang bersifat mudah larut dalam air dan bersifat stabil. Nitrat
diperoleh dari proses oksidasi sempurna dari senyawa oksigen di perairan
(Effendi, 2003). Nitrat merupakan sumber nitrogen yang sering digunakan dalam
media kultur fitoplankton (Barsanti dan Gualtieri, 2006). Svehla (1985)
19 senyawa yang larut dalam air. Apabila diolah dengan air nitrat dapat
menghasilkan garam basa yang dapat larut dalam nitrat encer. Karena sifatnya
yang mudah larut dalam air, nitrat mudah dimanfaatkan oleh Nannochloropsis sp. untuk pertumbuhan sehingga pertumbuhan fitoplankton lebih cepat (Purwitasari
20
III. METODOLOGI
3.1 Tempat dan Waktu Penelitian
Penelitian dilaksanakan pada tanggal 13-21 Januari 2014 bertempat di
Laboratorium Budidaya Perikanan, Jurusan Budidaya Perairan, Fakultas
Pertanian, Universitas Lampung. Uji protein dilakukan di Laboratorium
Teknologi Hasil Pertanian Politeknik Negeri Lampung, dan uji kandungan nitrat
dilakukan di Laboratorium Kualitas Air Balai Besar Pengembangan Budidaya
Laut (BBPBL), Lampung.
3.2 Materi Penelitian 3.2.1 Biota Kultur
Biota kultur yang digunakan dalam penelitian adalah Nannochloropsis sp. yang dikultur dengan skala laboratorium di Laboratorium Budidaya Perikanan,
Jurusan Budidaya Perairan, Fakultas Pertanian, Universitas Lampung.
3.2.2 Media Kultur
Media yang dipergunakan dalam kultur Nannochloropsis sp. berbentuk cair atau larutan yang tersusun dari senyawa-senyawa kimia (pupuk) yang merupakan
21 Komposisi pupuk Conwy yang digunakan adalah komposisi pupuk standar (Tabel 1) dan komposisi pupuk dengan pengurangan NaNO3 sebanyak 50%.
Tabel 1. Komposisi pupuk Conwy skala laboratorium (BBPBL Lampung)
No Bahan Kimia Takaran Per Liter
1 Aquabides hingga 1 liter
2 EDTA 45 gram
3 FeCl3 1,5 gram
4 H3BO3 33,6 gram
5 NaH2PO4 20 gram
6 MnCl2 0,5 gram
7 NaNO3 100 gram
8 Trace metal solution : 1 cc
a) ZnCl2 2,1 gram
b) CoCl2 2 gram
c) CuSO4 2 gram
d) (NH4)MO7 0,9 gram
e) Distilled 100 ml
Komposisi pupuk Conwy yang kedua hampir sama dengan komposisi pertama, perbedaannya adalah adanya konsentrasi NaNO3 yang dikurangi hingga 50% pada
komposisi pupuk.
3.3 Alat dan Bahan Penelitian 3.3.1 Alat
Penelitian menggunakan beberapa alat untuk mendukung jalannya
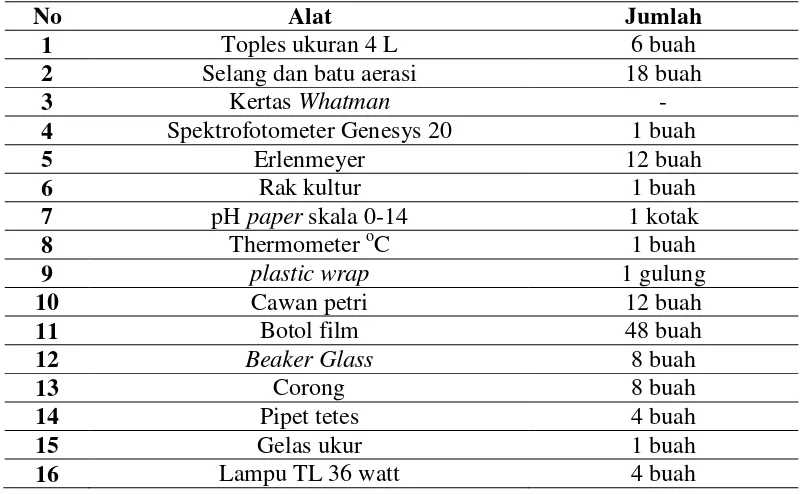
22 Tabel 2. Alat yang digunakan dalam penelitian
No Alat Jumlah
1 Toples ukuran 4 L 6 buah
2 Selang dan batu aerasi 18 buah
3 Kertas Whatman -
4 Spektrofotometer Genesys 20 1 buah
5 Erlenmeyer 12 buah
6 Rak kultur 1 buah
7 pH paper skala 0-14 1 kotak
8 Thermometer oC 1 buah
9 plastic wrap 1 gulung
10 Cawan petri 12 buah
11 Botol film 48 buah
12 Beaker Glass 8 buah
13 Corong 8 buah
14 Pipet tetes 4 buah
15 Gelas ukur 1 buah
16 Lampu TL 36 watt 4 buah
3.3.2 Bahan
Penelitian menggunakan beberapa bahan untuk mendukung jalannya
penelitian. Bahan-bahan yang digunakan dalam penelitian adalah bibit
Nannochloropsis sp., air laut steril, aquades, alkohol, pupuk Conwy (100% & 50%), H2SO4, NaOH, sodium arsenit, asam sulfat, dan brucine.
.
3.4 Rancangan Penelitian
Penelitian terdiri dari 2 perlakuan dan 3 kali ulangan, masing-masing
perlakuan dilakukan 10 kali waktu sampling. Perlakuan tersebut adalah sebagai
berikut :
Perlakuan P1 : kultur Nannochloropsis sp. tanpa pengurangan kandungan nitrat anorganik (NO3-) 100%
23 Waktu pengambilan contoh kepadatan Nannochloropsis sp. dan analisis kandungan nitrat dilakukan pada air laut steril (N-1), saat setelah pupuk
dimasukkan (N0) dan pada jam kultur ke- 10, 12, 18, 24, 30, 36, 42, 48.
Sedangkan pengamatan uji protein dilakukan pada jam kultur ke- 10, 12, 18, 24,
30, 36, 42, 48. Pengamatan pada jam ke-10 adalah sebagai penanda awal fase
eksponensial di mulai.
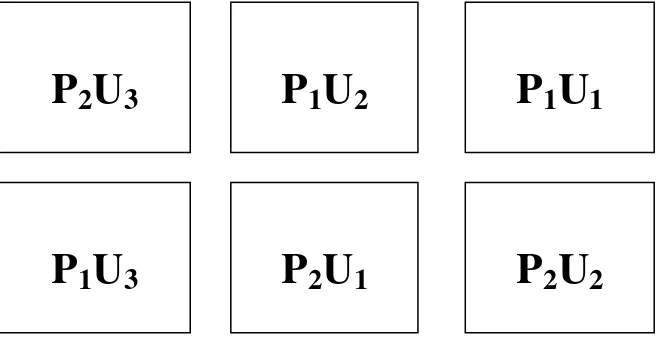
[image:43.595.139.467.309.478.2]Peletakan wadah kultur dilakukan secara acak disajikan pada Gambar 7.
Gambar 7. Tata letak wadah kultur Nannochloropsis sp.
Keterangan:
P1 : Perlakuan pertama dengan penambahan komposisi Pupuk Conwy standar dengan kandungan nitrat anorganik (NO3-) sebanyak 100%
P2 : Perlakuan kedua dengan pengurangan kandungan nitrat anorganik (NO3-)
pada Pupuk Conwy hingga 50%
U1 : Ulangan pertama pada pengambilan sampel
U2 : Ulangan kedua pada pengambilan sampel
U3 : Ulangan ketiga pada pengambilan sampel
P
1
U
1
P
1
U
2
P
2
U
3
P
2
U
2
P
2
U
1
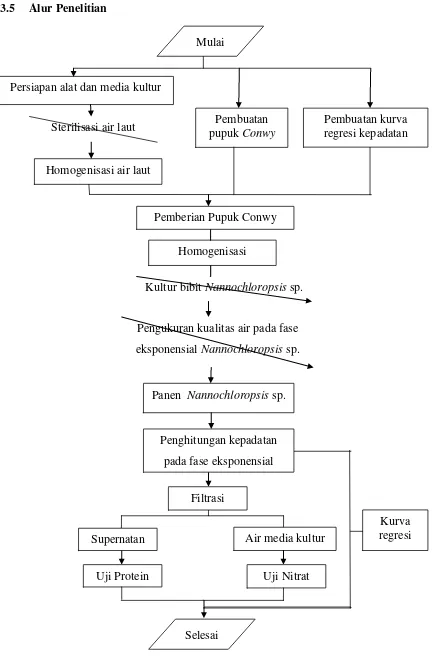
24 3.5 Alur Penelitian
Gambar 8. Tahapan alur penelitian Sterilisasi air laut
Homogenisasi air laut
Pemberian Pupuk Conwy
Homogenisasi
Kultur bibit Nannochloropsis sp.
Pengukuran kualitas air pada fase eksponensial Nannochloropsis sp.
Panen Nannochloropsis sp.
Uji Nitrat Uji Protein
Persiapan alat dan media kultur
Penghitungan kepadatan pada fase eksponensial
Kurva regresi Pembuatan
pupuk Conwy Mulai
Selesai
Pembuatan kurva regresi kepadatan
Filtrasi
25 3.5.1 Persiapan
Tahap awal yang dilakukan adalah persiapan seluruh alat dan bahan yang
akan digunakan dalam penelitian. Alat dan bahan yang digunakan untuk kultur
Nannochloropsis sp. harus dalam keadaan steril agar tidak terjadi kontaminasi dengan organisme lain yang bisa menjadi kompetitor bagi Nannochloropsis sp.
a. Sterilisasi alat
Sterilisasi alat kultur seperti toples dan cawan petri direndam menggunakan
larutan kaporit selam 1 hari dengan konsentrasi 100 ppm. Selanjutnya alat-alat
tersebut dicuci menggunakan sabun pencuci piring, lalu dibilas menggunakan air
tawar. Alat-alat kultur yang telah dibilas disemprot dengan alkohol 70%.
Sedangkan untuk selang dan batu aerasi, setelah, dicuci, dibilas dengan air tawar,
lalu direndam kaporit dan direbus selama 15 menit.
b. Sterilisasi air
Air laut yang akan digunakan disterilisasi dengan cara penyinaran
ultraviolet dan dilakukan ozonisasi. Setelah diberi ozon, air yang akan digunakan
dididihkan 2 kali (masing-masing 30 menit) untuk memastikan tidak ada
organisme kontaminan (terutama protozoa) yang akan mempengaruhi
keberhasilan kultur fitoplankton.
c. Pembuatan stok pupuk Conwy
26 bahan-bahan yang digunakan mencapai 100%. Pemberian pupuk pada kultur yaitu
1 ml/liter untuk sekali kultur. Adapun cara pembuatan pupuk Conwy untuk stok (Muhaemin, 2009) yaitu:
1. Bahan pembuatan pupuk Conwy dipersiapkan dan ditimbang secara berurutan sesuai dengan takaran seperti yang disajikan pada Tabel 1 menggunakan
timbangan digital. Alat seperti, pipet tetes, gelas beaker dan sendok juga disiapkan untuk penelitian.
2. Semua bahan ditimbang, lalu aquabides dimasukkan ke dalam gelas beaker sebanyak 800 ml, kemudian bahan-bahan pupuk Conwy dimasukkan secara berurutan mulai dari EDTA 45 g (Tabel 1. No.2) dimasukkan ke dalam gelas
beaker dan dilarutkan, begitu seterusnya (No.3, No.4, No.5, No. 6) hingga NaNO3 100g/liter (No.7) larut.
3. Trace metal solution (Tabel 1 No.8) dimasukkan ke dalam gelas beaker dan dilarutkan satu persatu masing-masing 1 ml.
4. Setelah semua larut, aquabides ditambahkan lagi ke dalam larutan pupuk
hingga menjadi 1 liter.
3.5.2 Pelaksanaan Penelitian
Penelitian dilakukan untuk memperoleh data dari masing-masing perlakuan
yang akan diteliti. Prosedur kultur yang dilakukan yaitu:
1. Toples kultur disusun pada rak kultur dengan susunan rancangan acak dan
diberi pencahayaan lampu.
2. Air laut steril disiapkan sebanyak 3,5 liter tiap toples kultur
27 4. Pupuk Conwy diberikan sebanyak 1 ml/liter dalam toples kultur
5. Air laut yang diberi pupuk Conwy dihomogenisasi kembali dengan aerasi kuat
6. Bibit Nannochloropsis sp. disiapkan. Bibit diambil dan diencerkan dengan volume air kultur 3,5 liter masing-masing pada 6 (2 perlakuan × 3 ulangan)
buah toples plastik volume 4 liter
7. Kualitas air diukur setelah biota dibiakkan saat mencapai fase akhir lag atau
pada fase awal eksponensial.
8. Pengamatan kepadatan Nannochloropsis sp. dilakukan menggunakan spektrofotometer dengan optical density (OD) 650 nm.
9. Kemudian kultur Nannochloropsis sp. dipanen secara total dengan cara dibuat dan disaring dengan menggunakan kertas whatman sampai didapat sampel plankton segar. Tiap sampel disimpan ke dalam cawan petri dan ditutup
dengan plastic wrap. Sedangkan air dari penyaringan berupa supernatan dimasukkan ke dalam botol film.
10. Langkah terakhir yang dilakukan yaitu sampel yang telah disimpan dalam
cawan petri dibawa untuk dilakukan uji protein dan supernatan dilakukan uji
nitrat.
3.6 Parameter yang Diamati 3.6.1 Uji Proksimat Protein
Uji proksimat protein dilakukan pada jam kultur ke- 10, 12, 18, 30, 42, 48,
28 Negeri Lampung. Uji proksimat protein pada Nannochloropsis sp. dengan menggunakan metoda Gunning.
1. Bahan ditimbang 0,5-1,0 gr lalu dimasukkan ke dalam labu Kjeldahl,
kemudian ditambahkan 10 gr Potasium Sulfida (K2S) atau Natrium Sulfat
(Na2SO4) anhidrat, dan 10-15 ml Asam Sulfat (H2SO4) pekat. Apabila
distruksi sukar dilakukan perlu ditambah 0,1-0,3 gr Tembaga (II) Sulfat
(CuSO4) dan dihomogenkan
2. Larutan kemudian distruksi di atas pemanas listrik dalam lemari asam, mula
mula dengan api kecil, setelah asap hilang api dibesarkan, pemanasan diakhiri
setelah cairan menjadi jernih tak berwarna lagi
3. Kemudian perlakuan blangko dibuat seperti perlakuan di atas tanpa contoh.
4. Aquades 100 ml ditambahkan ke dalam labu kjeldahl setelah sampel dingin,
kemudian larutan Natrium Hidroksida (NaOH) 45% dimasukkan sampai
cairan bersifat basis, lalu labu kjeldahl dipasang dengan segera pada alat
distilasi.
5. Labu Kjeldahl dipanaskan sampai amonia menguap semua, distilat ditampung
dalam erlenmeyer berisi 25 ml Asam Klorida (HCl) 0,1N yang sedang diberi
indikator PhenolPtalein (C20H14O4) 1% beberapa tetes. Distilasi diakhiri
setelah distilat tertampug sebanyak 150 ml atau setelah distilat yang keluar
tak bersifat basis.
6. Kelebihan HCl 0,1 N dalam distilat dititrasi dengan larutan basa standar
29 Perhitungan kandungan protein dalam sampel dihitung menggunakan
rumus:
% Protein = % N × Faktor Konversi Keterangan:
Faktor Konversi = 6,25 (setara dengan 0,16 gram nitrogen per gram protein)
3.6.2 Uji Kandungan Nitrat (NO3-)
a. Pembuatan Reagen
Reagen untuk uji kandungan nitrat dibuat dengan metode dari BBPBL adalah
sebagai berikut:
1) Sodium Arsenit (NaAsO2)
0,5 gram sodium arsenit dilarutkan dengan aquades menjadi 50 ml.
2) Brucine (C23H26N2O)
5 gram brucine dilarutkan dengan asam asetat glacial (C2H4O2) menjadi
100 ml.
3) Asam Sulfat (H2SO4)
125 ml asam sulfat pekat ditambahkan dengan 31,25 ml aquades.
b. Uji Nitrat
Uji kandungan nitrat dalam Nannochloropsis sp. dilakukan pada air laut steril (N-1), saat setelah pupuk dimasukkan (N0) dan pada jam kultur ke- 10, 12,
18, 24, 30, 36, 42, dan 48 dengan menggunakan spektrofotometer. Cara pengujian
30 1. Sampel supernatan disaring dengan menggunakan whatman paper no. 42 lalu diambil sebanyak 5 ml lalu dimasukkan ke dalam beaker glass berukuran 50 ml.
2. Satu tetes sodium arsenit (NaAsO2); 0,25 ml brucine (C23H26N2O) dan 5 ml
asam sulfat (H2SO4) ditambahkan ke dalam sampel.
3. Larutan diaduk dan didiamkan selama 10 menit
4. Setelah 10 menit dalam suhu ruang, sampel diukur dengan menggunakan
spektrofotometer pada optical density (OD) ( ) 410 nm
5. Nilai absorbansi pada tampilan layar spektrofotometer dibaca lalu
dimasukkan dalam persamaan kurva regresi X dan Y
3.6.3 Model Regresi Linier
Perhitungan kepadatan sel Nannochloropsis sp. dibuat dengan menggunakan hubungan regresi linier antara kepadatan Nannochloropsis sp. dan absorbansi yang terbaca pada spektrofotometer. Muhaemin (2008) menyatakan
bahwa optical density (OD) spektofotometer yang optimal dalam pengukuran kepadatan fitoplankton adalah sebesar 650 nm. Cara mencari regresi linier
tersebut adalah sebagai berikut:
1. Sampel bibit kultur diambil sebanyak 50 ml dan dipisahkan dalam 10 wadah
yang berbeda (volume wadah ± 30 ml).
2. Tiap wadah diisi dengan sampel Nannochloropsis sp. dengan volume masing-masing 20, 18, 16, 14, 12, 10, 8, 6, 4, dan 2 ml.
3. Tiap wadah yang telah diisi sampel tersebut selanjutnya diberi aquades
31 4. Setelah pengenceran dilakukan, selanjutnya tingakat absorbansi sampel
diamati dengan menggunakan spektrofotometer. Disaat yang sama dilakukan
pula pengamatan kepadatan pada sampel tersebut dengan menggunakan
mikroskop dan haemocytometer.
5. Prosedur no.4 dilakukan pula pada seluruh sampel yang tersedia dan
masing-masing diulang sebanyak tiga kali.
6. Hasil pengamatan pada prosedur no.5 selanjutnya digambarkan pada kurva
linier untuk dihitung nilai koefisien regresi, korelasi dan determinasinya.
7. Kurva dan persamaan yang diperoleh selanjutnya dapat digunakan sebagai
persamaan untuk mengonversi nilai kepadatan Nannochloropsis sp. berdasarkan hasil pengamatan nilai absorbansi pada spektrofotometer.
3.6.4 Penghitungan Kepadatan Nannochloropsis sp.
Kepadatan fitoplankton dihitung menggunakan spektrofotometer dengan
optical density (OD) 650 nm. Cara menghitung kepadatan Nannochloropsis sp. sebagai berikut:
1. Sampel bibit kultur diambil sebanyak 20 ml
2. Sampel bibit dimasukkan ke dalam spektrofotometer dan dicatat nilai
absorbansinya. Pengukuran diulang sebanyak 3 kali
3. Sampel diambil pada jam kultur ke- 10, 12, 18, 24, 30, 36, 42, dan 48
4. Hasil dari kepadatan pada pengamatan dikonversikan dengan nilai regresi
32 3.6.5 Kualitas air (oksigen terlarut, pH, dan suhu media kultur)
Kualitas air selama peneitian dibuat agar berada pada kondisi yang optimal
untuk pertumbuhan Nannochloropsis sp. Pengukuran pH, dan suhu media menggunakan pH meter, dan termometer. Pengukuran parameter tersebut
dilakukan pada awal kultur (t10) dan pada akhir kultur (t48). Pengukuran kualitas
air dilakukan pada setiap unit sampel. Data kualitas air digunakan sebagai data
pendukung.
3.7 Analisis Data
3.7.1 Hubungan Antar Dua Variabel Dependen
Hubungan antara pemanfaatan nitrat anorganik dengan kandungan protein
total pada Nannochloropsis sp. dianalisis menggunakan model persamaan regresi linier dan polinomial, dengan model persamaan regresi linier Y = aX + b; dan
model persamaan regresi polinomial Y = aX2 + bX + c, koefisien korelasi (r)
Pearson dan koefisien determinasi (R2) (Supangat, 2007), di mana r adalah:
r =
Sedangkan analisis untuk menguji koefisien regresi secara individual adalah
dengan menggunakan uji t (t-test) untuk membandingkan dua nilai tengah contoh
bebas apabila n1 = n2 = n, dengan anggapan bahwa kedua populasi menyebar
normal dan memiliki ragam sama yang tidak diketahui nilainya (Steel dan Torrie,
33 t =
S2 = –
Sx1-x2 = db = 2 (n-1)
Keterangan:
X = variabel independen
Y = variabel dependen
a = kemiringan kurva/slope
b = intercept n = jumlah sampel
t = Koefisien t
= rata-rata sampel
S2 = ragam
S = simpangan baku
34
V. KESIMPULAN
5. 1 Kesimpulan
Berdasarkan penelitian dapat disimpulkan bahwa:
a. Pengurangan kadar NO3- hingga 50% pada pupuk Conwy cenderung menyebabkan penyempitan waktu fase eksponensial sehingga waktu kultur
Nannochloropsis sp. akan berakhir lebih cepat, penurunan kepadatan rata-rata dan maksimum sel, penurunan kandungan protein total intraseluler, serta
belum memberikan respon yang signifikan terhadap perubahan kandungan
nitrat anorganik pada media kultur.
b. Terdapat sisi negatif dari pengurangan nitrat anorganik yaitu penurunan rasio
kepadatan terhadap kandungan protein total intraseluler (P/Nt) sebesar 19,3%
dan menurunkan rasio nitrat anorganik terhadap kandungan protein total
intraseluler (P/NO3-) sebesar 3,26%.
c. Nilai absorbansi spektrofotometer dapat secara representatif digunakan untuk
menghitung kepadatan sel Nannochloropsis sp.
5. 2 Saran
Perlu dilakukan penelitian lanjutan mengenai cara meningkatkan kandungan
52 DAFTAR PUSTAKA
Balai Budidaya Laut. 2002. Budidaya Fitoplankton dan Zooplankton. Direktorat Jendral Perikanan. Departemen Kelautan dan Perikanan. 9: 7-8.
Barsanti, L. and P. Gualtieri. 2006. Algae : Anatomy, Biochemistry, and Biotechnology. CRC Press. United States of America. 301 hal.
Becker, E.W. 1994. Mikroalgae Biotechnology and Microbiology. Cambridge University Press. New York.
Biondi, N. and M. Tredici. 2011. Algae and Aquatic Biomass for a Sustainable Production of 2nd Generation Biofuels. UNIFI. Page 148-150.
Bold, H.C. and M.J. Wynne. 1985. Introduction to the Algae: Structure and Reproduction. Prentice-Hall Inc. United States of America. 718 hal.
Borowitzka, M.A., dan L.J Borowitzka. 1989. Mikro-algal Biotechnology. Cambridge University Press. Cambridge. Hal 257-287.
Chalid, S.Y., S. Amini dan S.D. Lestari. 2010. Kultivasi Chlorella sp. pada Media Tumbuh yang Diperkaya dengan Pupuk Anorganik dan Soil Extract. Jurnal Valensi. Vol. 1 (6): 298-304.
Determann, S., J.M. Lobbes, R. Reuter, dan J. Rullkötter. 1998. Ultraviolet Fluorescence Excitation and Emission Spectroscopy of Marine Algae and Bacteria. Journal Marine Chemistry. Vol. 62: 137-156.
Edhy, W.A., J. Pribadi dan Kurniawan. 2003. Plankton di Lingkungan PT. Central Pertiwi Bahari: Suatu Pendekatan Biologi dan Manajemen Plankton dalam Budidaya Udang. PT. Central Pertiwi Bahari. Tulang Bawang.
Effendi, H. 2003. Telaah Kualitas Air. Penerbit Kanisius. Yogyakarta. hal. 145-155
53 Forján, E., L. Garbayo, C. Casal, dan C. Vílchez. 2007. Enhancement of Carotenoid Production in Nannochloropsis by Phosphate and Sulphur Limitation. Journal Communicating Current Reaserch and Educational Tropics and Trends in Applied Microbiology. Hal 356-364.
Harun, R., M. Singh, G.M. Forde, and M.K. Danquah. 2010. Bioprocess Engineering of Microalgae to Produce a Variety of Consumer Products. Renewable and Sustainable Energy Reviews. Vol. 14: 1037–1047.
Hibberd, D.J. 1981. Notes on the taxonomy and nomenclature of the algal classes Eustigmatophyceae and Tribophyceae (synonym Xanthophyceae). Journal of the Linnean Society of London, Botany. 82 (17): 93-119.
Hoek, C.V.D., D.G. Mann and H.M. Jahns. 1998. Algae: An Introduction to Phycology. Cambridge University Press. Melbourne.
Hu, H. and K. Gao. 2006. Response of Growth and Fatty Acid Compositions of Nannochloropsis sp. to Environmental Factors Under Elevated CO2 Concentration. Journal Biotechnol Lett. Vol. 28: 987-992.
Hudaidah, S., M. Muhaemin dan Rosdinar. 2013. Strategy of Nannochloropsis Againts Environment Starvation: Population Density and Crude Lipid Contents. Maspari Journal. Vol. 5 (2): 64-68.
Isnansetyo, A. dan Kurniastuty. 1995. Teknik Kultur Phytoplankton dan Zooplankton. Kanasius. Yogyakarta. 116 halaman.
Kuchel, P. and G. B. Ralston. 2006. Schaum’s Easy Outlines Biokimia. Erlangga. Jakarta.
Lavens, P. and P. Sorgeloos. 1996. Manual on the Production and Use of Live Food for Aquaculture. FAO Fisheries Technical Paper. Belgium.
Malensang, J.S., H. Komalig dan D. Hatidja. 2012. Pengembangan Model Regresi Polinomial Berganda pada Kasus Data Pemasaran. Jurnal Ilmiah Sains. Vol. 12 (2): 149-152.
Muhaemin, M., R.F. Kaswadji dan T. Prartono. 2006. Kemampuan Pengikatan Metaloprotein Asam Amino Methionin Terhadap Pb pada Dunaliella salina. Jurnal Pertanian Terapan. Vol 6 (2): 160-165.
Muhaemin, M. 2008. The Glutatihione Diurnal Cycling in Dunaliella salina. Journal of Coastal Development. Vol 12 (1): 41-46.
Muhaemin, M. 2009. Cadmium-Peptides Complexes in Dunaliella salina Cells. Journal of Coastal Development. Vol 13 (1): 54-58.
54 Poedjiadi, A. 1994. Dasar-Dasar Biokimia. UI Press. Jakarta.
Purwitasari, A.T., M.A. Alamsjah dan B.S. Rahardja. 2012. Pengaruh Konsentrasi Zat Pengatur Tumbuh (Asam-2,4-Diklorofenoksiasetat) Terhadap Pertumbuhan Nannochloropsis oculata. Journal of Marine and Coastal Science. Vol. 1 (2): 61 – 70
Resmawati, M.B., E.D. Masithah dan L. Sulmartiwi. 2012. Pengaruh Pemberian Pupuk Cair Limbah Ikan Lemuru (Sardinella sp.) Terhadap Kepadatan Populasi Spirulina platensis. Journal of Marine and Coastal Science. Vol 1(1): 22–33
Reynolds, C.S. 2006. Ecology of Phytoplankton. Cambridge University Press. New York. 535 hal.
Robson, B. and J. Garnier. 1988. Introduction to Proteins and Protein Engineering. Elsevier Science Publisher B.V. Amsterdam.
Rudiyanti, S. 2011. Pertumbuhan Skeletonema costatum pada Berbagai Tingkat Salinitas Media. Jurnal Saintek Perikanan.Vol.6 No. 2: 69-76.
Sari, I.P. dan A. Manan. 2012. Pola Pertumbuhan Nannochloropsis oculata pada Kultur Skala Laboratorium, Intermediet, dan Masal. Jurnal Ilmiah Perikanan dan Kelautan. Vol. 4 (2): 123-127.
Steel, R.G.D. dan J.H. Torrie. 1993. Prinsip dan Prosedur Statistika: Suatu Pendekatan Biometrik. PT Gramedia Pustaka Utama. Jakarta.
Suminto. 2009. Penggunaan Jenis Media Kultur Teknis Terhadap Produksi dan Kandungan Nutrisi Sel Spirulina platensis. Jurnal Saintek Perikanan. Vol. 4 (2): 53-61.
Supangat. A. 2007. Statistika. Prenada Media Group. Jakarta. Hal 334-350.
Stanley, M. 2000. Enviromental Chemistry Seventh Edition. CRC Press LLC. USA. hal 149-150
Svehla, G. 1985. Vogel Bagian Satu Buku Teks Analisis Anorganik Kualitatif Makro dan Semi Makro. PT Kalman Media Pustaka. Jakarta.
Walpole, R.E. 1992. Pengantar Statistika Edisi Ketiga. PT. Gramedia Pustaka Utama. Jakarta.
55 Yanuaris, L.M., R. Kusdarwati dan Kismiyati. 2012. Pengaruh Fermentasi Actinobacillus sp. pada Kotoran Sapi Sebagai Pupuk Terhadap Pertumbuhan Nannochloropsis sp. Jurnal Ilmiah Perikanan dan Kelautan. Vol. 4 (1): 21-26.