AKTIVITAS ANTIOKSIDAN EKSTRAK
ETANOL DAUN BANGUN-BANGUN
(Plectranthus amboinicus (Lour.) Spreng.)
SKRIPSI
OLEH:
DEWI SARTIKA
NIM 081501016
PROGRAM STUDI SARJANA FARMASI
FAKULTAS FARMASI
UNIVERSITAS SUMATERA UTARA
MEDAN
AKTIVITAS ANTIOKSIDAN EKSTRAK
ETANOL DAUN BANGUN-BANGUN
(Plectranthus amboinicus (Lour.) Spreng.)
SKRIPSI
Diajukan untuk melengkapi salah satu syarat untuk memperoleh gelar Sarjana Farmasi pada Fakultas Farmasi
Universitas Sumatera Utara
OLEH:
DEWI SARTIKA
NIM 081501016
PROGRAM STUDI SARJANA FARMASI
FAKULTAS FARMASI
UNIVERSITAS SUMATERA UTARA
MEDAN
PENGESAHAN SKRIPSI
Dipertahankan di Hadapan Panitia Penguji Skripsi Fakultas Farmasi Universitas Sumatera Utara
Pada Tanggal: Mei 2013
Disetujui Oleh:
Pembimbing I, Panitia Penguji
Poppy Anjelisa Z. Hsb., S.Si., M.Si., Apt. Prof. Dr. Sumadio Hadisahputra, Apt. NIP 197506102005012003 NIP195311281983031002
Pembimbing II, Poppy Anjelisa Z. Hsb., S.Si., M.Si., Apt.
KATA PENGANTAR
Puji dan syukur kehadirat Tuhan Yang Maha Esa, karena limpahan rahmat, kasih dan karuniaNya, sehingga penulis dapat menyelesaikan skripsi ini
yang berjudul ”Aktivitas Antioksidan Ekstrak Etanol Daun Bangun-bangun (Plectranthus amboinicus (Lour.) Spreng.)”. Skripsi ini diajukan sebagai salah
satu syarat untuk memperoleh gelar sarjana farmasi pada Fakultas Farmasi
Universitas Sumatera Utara.
Pada kesempatan ini penulis mengucapkan terima kasih yang tulus dan ikhlas kepada Bapak Prof. Dr. Sumadio Hadisahputra, Apt., selaku Dekan
Fakultas Farmasi USU Medan yang telah memberikan fasilitas sehingga penulis dapat menyelesaikan pendidikan. Ibu Poppy Anjelisa Z. Hasibuan., S.Si., M.Si.,
Apt., dan Ibu Aminah Dalimunthe, S.Si., M.Si., Apt., selaku pembimbing yang telah memberikan waktu, bimbingan, dan nasehat selama penelitian hingga selesainya penyusunan skripsi ini serta kepada Ibu Dra. Herawati Ginting, M.Si.,
Apt., selaku penasehat akademis yang telah memberikan bimbingan kepada penulis. Bapak Prof. Dr. Sumadio Hadisahputra, Apt., Bapak Drs. Rasmadin
Mukhtar, M.S., Apt., dan Ibu Dra. Suwarti Aris, M.Si., Apt., selaku dosen penguji yang telah memberikan saran dan arahan kepada penulis dalam menyelesaikan skripsi ini. Kepada Bapak dan Ibu staf pengajar Fakultas Farmasi USU yang telah
mendidik selama perkuliahan serta Bapak kepala Laboratorium Penelitian dan yang telah memberikan bantuan dan fasilitas selama penulis melakukan
penelitian.
ikhlas bagi kesuksesan penulis, juga kepada abang saya Faisal Kurniawan, Irvan Syahputra dan adik saya Desy Syahriani yang selalu setia memberi doa, dukungan dan motivasi selama melakukan penelitian.
Penulis menyadari skripsi ini masih belum sempurna, oleh karena itu diharapkan kritik dan saran yang membangun untuk penyempurnaannya. Harapan
penulis semoga skripsi ini dapat bermanfaat bagi ilmu pengetahuan kefarmasian.
Medan, Mei 2013 Penulis
AKTIVITAS ANTIOKSIDAN EKSTRAK ETANOL DAUN BANGUN-BANGUN (Plectranthus amboinicus (Lour.) Spreng.)
ABSTRAK
Daun bangun-bangun banyak mengandung senyawa yang berkhasiat sebagai antioksidan seperti senyawa flavonoid dan turunan polifenol. Peneliti terdahulu menyebutkan bahwa daun bangun-bangun memiliki efek antiinflamasi, hepatoprotektif, radioprotektif dan mampu melindungi kerusakan kromosom. Diduga efek tersebut karena daun bangun-bangun memiliki sifat antioksidan yang mampu mencegah radikal bebas dalam merusak sel-sel di dalam tubuh. Tujuan penelitian ini adalah untuk mengetahui aktivitas antioksidan ekstrak etanol daun bangun-bangun (Plectranthus amboinicus (Lour.) Spreng.).
Ekstrak etanol daun bangun-bangun diuji aktivitas antioksidannya terhadap DPPH (1,1-Diphenyl-2-picrylhydrazyl) sebagai radikal bebas. Daun bangun-bangun diuji dengan variasi konsentrasi 125, 250 dan 500 µg/ml dan sebagai pembanding digunakan vitamin C konsentrasi 20, 40 dan 60 µg/ml. Pengukuran absorbansi dilakukan pada menit ke-60 pada panjang gelombang 516 nm. Kemampuan antioksidan diukur sebagai penurunan absorbansi larutan DPPH setelah penambahan ekstrak.
Hasil analisis yang diperoleh menunjukkan, bahwa ekstrak etanol daun bangun-bangun memiliki aktivitas antioksidan yang mampu meredam radikal bebas DPPH, dengan nilai Inhibitory Concentration (IC50) sebesar 148,58 µg/ml. Kata kunci : Daun bangun-bangun, antioksidan.
ANTIOXIDANT ACTIVITY OF ETHANOLIC EXTRACT OF BANGUN-BANGUN LEAVES (Plectranthus amboinicus (Lour.) Spreng.)
ABSTRACT
Plectranthus amboinicus (Lour.) Spreng. contain potential antioxidants such as flavonoids and polyphenols. The recent studies said that Plectranthus amboinicus (Lour.) Spreng. has anti-inflammatory effect, hepatoprotective, radioprotektive and protect chromosome damage. these effects caused by antioxidant properties that can prevent free radical damage to the body cells. Antioxidant activity of ethanol extracts of Plectranthus amboinicus (Lour.) Spreng.
The antioxidant activity of ethanol extracts of Plectranthus amboinicus (Lour) Spreng. were tested with DPPH (1,1-Diphenyl-2-picrylhydrazyl) as free radical by measuring the DPPH absorbance at 516 nm wave length on 60th minutes after the addition of methanol solvent with variety concentration 125, 250 and 500 µg/ml, vitamin C as a control with variety concentration 20, 40 dan 60 µg/ml. Antioxidant’s ability was measured as the decrease of DPPH solution absorbance after the extracts addition.
The result showed that the ethanol extract of Plectranthus amboinicus (Lour.) Spreng. had a weak antioxidants activity scavenger DPPH free radical, with the Inhibitory Concentration (IC50) values in the amount of 148,58 µg/ml.
3.3.7 Penentuan nilai IC50 ... 22
BAB IV HASIL DAN PEMBAHASAN ... 23
4.1 Hasil Uji Aktivitas Antioksidan EEDBB ... 23
4.2 Hasil Analisis Peredaman Radikal Bebas DPPH ... 24
4.3 Analisis Nilai Inhibitory Concentration (IC50) Sampel Uji .... 26
BAB V KESIMPULAN DAN SARAN ... 27
5.1 Kesimpulan ... 27
5.2 Saran ... 27
DAFTAR PUSTAKA ... 28
LAMPIRAN ... 31
DAFTAR TABEL
Tabel Halaman
4.1 Data Absorbansi dan % Inhibisi EEDBB ... 24 4.2 Data Absorbansi dan % Inhibisi Vitamin C ... 24
DAFTAR GAMBAR
Gambar Halaman
1.1 Kerangka Pikir Penelitian ... 4
2.1 Rumus Bangun Vitamin C ... 13
2.2 Rumus Bangun DPPH ... 15
2.3 Resonansi DPPH ... 15
2.4 Reaksi Antara DPPH dengan Atom H Netral yang Berasal dari Antioksidan ... 16
DAFTAR LAMPIRAN
Lampirkan Halaman
1 Hasil Identifikasi Tumbuhan ... 30
2 Karakteristik EEDBB ... 31
3 Hasil Penentuan Golongan Senyawa Kimia EEDBB ... 32
4 Bagan Kerja Pembuatan EEDBB ... 33
5 Data Absorbansi dan % Inhibisi EEDBB dan Vitamin C Setelah Didiamkan selama 60 Menit ... 34
6 Perhitungan % Inhibisi EEDBB dan Vitamin C Setelah Didiamkan Selama 60 Menit ... 35
AKTIVITAS ANTIOKSIDAN EKSTRAK ETANOL DAUN BANGUN-BANGUN (Plectranthus amboinicus (Lour.) Spreng.)
ABSTRAK
Daun bangun-bangun banyak mengandung senyawa yang berkhasiat sebagai antioksidan seperti senyawa flavonoid dan turunan polifenol. Peneliti terdahulu menyebutkan bahwa daun bangun-bangun memiliki efek antiinflamasi, hepatoprotektif, radioprotektif dan mampu melindungi kerusakan kromosom. Diduga efek tersebut karena daun bangun-bangun memiliki sifat antioksidan yang mampu mencegah radikal bebas dalam merusak sel-sel di dalam tubuh. Tujuan penelitian ini adalah untuk mengetahui aktivitas antioksidan ekstrak etanol daun bangun-bangun (Plectranthus amboinicus (Lour.) Spreng.).
Ekstrak etanol daun bangun-bangun diuji aktivitas antioksidannya terhadap DPPH (1,1-Diphenyl-2-picrylhydrazyl) sebagai radikal bebas. Daun bangun-bangun diuji dengan variasi konsentrasi 125, 250 dan 500 µg/ml dan sebagai pembanding digunakan vitamin C konsentrasi 20, 40 dan 60 µg/ml. Pengukuran absorbansi dilakukan pada menit ke-60 pada panjang gelombang 516 nm. Kemampuan antioksidan diukur sebagai penurunan absorbansi larutan DPPH setelah penambahan ekstrak.
Hasil analisis yang diperoleh menunjukkan, bahwa ekstrak etanol daun bangun-bangun memiliki aktivitas antioksidan yang mampu meredam radikal bebas DPPH, dengan nilai Inhibitory Concentration (IC50) sebesar 148,58 µg/ml. Kata kunci : Daun bangun-bangun, antioksidan.
ANTIOXIDANT ACTIVITY OF ETHANOLIC EXTRACT OF BANGUN-BANGUN LEAVES (Plectranthus amboinicus (Lour.) Spreng.)
ABSTRACT
Plectranthus amboinicus (Lour.) Spreng. contain potential antioxidants such as flavonoids and polyphenols. The recent studies said that Plectranthus amboinicus (Lour.) Spreng. has anti-inflammatory effect, hepatoprotective, radioprotektive and protect chromosome damage. these effects caused by antioxidant properties that can prevent free radical damage to the body cells. Antioxidant activity of ethanol extracts of Plectranthus amboinicus (Lour.) Spreng.
The antioxidant activity of ethanol extracts of Plectranthus amboinicus (Lour) Spreng. were tested with DPPH (1,1-Diphenyl-2-picrylhydrazyl) as free radical by measuring the DPPH absorbance at 516 nm wave length on 60th minutes after the addition of methanol solvent with variety concentration 125, 250 and 500 µg/ml, vitamin C as a control with variety concentration 20, 40 dan 60 µg/ml. Antioxidant’s ability was measured as the decrease of DPPH solution absorbance after the extracts addition.
The result showed that the ethanol extract of Plectranthus amboinicus (Lour.) Spreng. had a weak antioxidants activity scavenger DPPH free radical, with the Inhibitory Concentration (IC50) values in the amount of 148,58 µg/ml.
BAB I
PENDAHULUAN
1.1Latar belakang
Tubuh manusia tanpa disadari akan membentuk radikal bebas melalui
peristiwa metabolisme sel normal, peradangan, kekurangan gizi dan akibat respon terhadap pengaruh dari luar tubuh berupa polusi lingkungan, sinar ultraviolet, asap rokok dan asap kendaraan. Senyawa radikal ini akan menyerang komponen
penyusun organ tubuh manusia dan menyebabkan berbagai penyakit degeneratif seperti katarak, kanker dan jantung. Oleh karena itu tubuh memerlukan suatu
substansi penting yang berfungsi membantu melindungi tubuh dari serangan radikal bebas yang terbentuk yaitu antioksidan. Antioksidan adalah zat yang dapat menetralisir radikal bebas sehingga elektron yang tidak berpasangan pada radikal
bebas mendapat pasangan elektron. Sistem antioksidan sebagai mekanisme pertahanan terhadap serangan radikal bebas, secara alami telah ada dalam tubuh
manusia (Kosasih, 2004).
Radikal bebas selain terdapat diluar tubuh, radikal bebas juga terjadi dalam tubuh. Pembentukan radikal bebas dalam tubuh dan reaksi oksidasi pada
biomolekul akan berlangsung sepanjang hidup. Radikal bebas dalam jumlah kecil masih dapat ditolerin oleh tubuh, namun berbahaya apabila dalam jumlah yang
berlebih. Inilah penyebab utama dari proses penuaan dan berbagai penyakit degeneratif (Silalahi, 2006).
Antioksidan adalah senyawa yang mempunyai struktur molekul yang dapat
komponen makanan yang mengandung senyawa tidak jenuh (mempunyai ikatan rangkap) misalnya minyak dan lemak. Kombinasi beberapa jenis antioksidan memberikan perlindungan yang lebih baik (sinergisme) terhadap oksidasi
dibanding dengan satu jenis antioksidan saja (Kumalaningsih, 2006).
Daun bangun-bangun (Plectranthus amboinicus (Lour.) Spreng.) termasuk
suku Labiateae merupakan salah satu tanaman yang secara turun-temurun digunakan masyarakat Sumatera Utara sebagai menu sayuran sehari-hari bagi ibu-ibu yang baru melahirkan untuk memperlancar ASI. Beberapa penelitian telah
dilakukan terhadap daun bangun-bangun dan diketahui memiliki efek sebagai radioprotektif (Rao, dkk., 2006), melindungi kerusakan kromosom (Shyama, dkk.,
2002) hepatoprotektor (Patel, 2011) antiinflamasi (Chang, dkk., 2007). Skrining fitokimia yang dilakukan oleh Santosa dan Hertiani (2005), menunjukkan bahwa pada ekstrak air daun bangun-bangun mengandung senyawa flavonoid, glikosida
flavonol, polifenol dan minyak atsiri. Flavonoid umumnya terdapat pada tumbuhan sebagai glikosida, gugusan gula yang terdiri dari satu atau lebih gugus
hidroksil fenolik. Flavonoid terdapat pada seluruh bagian tanaman, termasuk pada daun, buah, tepung sari dan akar. Golongan flavonoid diantaranya adalah flavon yang dapat bekerja sebagai diuretik dan antioksidan (Sirait, 2007).
Berdasarkan uraian diatas belum ada diteliti efek antioksidan ekstrak etanol daun bangun-bangun (Plectranthus amboinicus (Lour.) Spreng.) sehingga peneliti
tertarik untuk meneliti aktivitas antioksidan ekstrak etanol daun bangun-bangun (Plectranthus amboinicus (Lour.) Spreng.) dengan menggunakan metode
penangkapan radikal bebas DPPH (1,1-diphenyl-2-picrylhydrazil). Sebagai baku
merupakan metode yang sering digunakan para peneliti untuk memperkirakan efisiensi zat-zat antioksidan.
1.2 Perumusan masalah
Berdasarkan latar belakang diatas, maka perumusan masalah dalam penelitian ini adalah:
a. apakah ekstrak etanol daun bangun-bangun memiliki aktivitas antioksidan. b. apakah ekstrak etanol daun bangun-bangun memiliki aktivitas antioksidan
yang kuat berdasarkan nilai IC50.
1.3 Hipotesis
Berdasarkan perumusan masalah diatas, maka hipotesis penelitian ini adalah:
a. ekstrak etanol daun bangun-bangun memiliki aktivitas antioksidan.
b. ekstrak etanol daun bangun-bangun memiliki aktivitas antioksidan yang kuat berdasarkan nilai IC50.
1.4 Tujuan Penelitian
Tujuan penelitian ini adalah untuk:
a. mengetahui aktivitas antioksidan dari ekstrak etanol daun bangun-bangun. b. menghitung nilai IC50 ekstrak etanol daun bangun-bangun.
1.5 Manfaat Penelitian
1.6 Kerangka Pikir Penelitian
Kerangka pikir penelitian ini adalah sebagai berikut:
Variabel bebas Variabel terikat Parameter
Gambar 1.1 Kerangka Pikir Penelitian Ekstrak Etanol Daun
Bangun-bangun konsentrasi 125 µg/ml, 250 µg/ml
dan 500 µg/ml
Pengujian Antioksidan metode DPPH
BAB II
TINJAUAN PUSTAKA
2.1 Uraian Tumbuhan
Daun bangun-bangun merupakan tanaman daerah tropis yang daunnya memiliki aroma tertentu sehingga dikenal sebagai tanaman aromatik. Tanaman ini
banyak ditemukan di India, Ceylon dan Afrika Selatan (Anonim, 2010; Kaliappan, et al., 2008).
2.1.1 Sistematika Tumbuhan
Menurut Pandey (2003), sistematika tanaman bangun-bangun adalah sebagai berikut:
Kingdom : Plantae
Divisi : Spermatophyta Kelas : Dicotyledonae
Ordo : Solanales Famili : Lamiaceae
Genus : Plectranthus
Spesies : Plectranthus amboinicus (Lour.) Spreng.
2.1.2 Nama Daerah
Menurut Heyne (1987), nama daerah daun bangun-bangun adalah sebagai berikut:
2.1.3 Morfologi Tumbuhan
Daun bangun-bangun merupakan tumbuhan semak menjalar, batangnya berkayu, lunak, beruas-ruas, ruas yang menempel ditanah akan tumbuh akar,
mudah patah, penampang bulat, diameter pangkal ± 15 mm, tengah ± 10 mm, dan ujung ±5 mm, batang yang masih muda berambut kasar dan hijau pucat. Berakar
tunggang, berwarna putih kotor. Daunnya tunggal, mudah patah, bulat telur, tepi beringgit, ujung dan pangkal membulat, berambut, panjang 6,5-7 cm, lebar 5,5-6,5 cm, tangkai panjang 2,4-3 cm, pertulangan menyirip dan berwarna hijau muda.
Bunga nya majemuk, bentuk tandan, berambut halus, kelopak bentuk mangkok, setelah mekar pecah menjadi lima, berwarna hijau keunguan, putik satu,
panjangnya ± 17 mm, kepala putik coklat, benang sari empat, kepala sari kuning, mahkota bentuk mangkok berwarna ungu (Depkes, 1989).
2.1.4 Kandungan Kimia Tumbuhan
Daun bangun-bangun mengandung saponin, flavonoid, polifenol, minyak atsiri, betakaroten, niasin, karvakrol, kalsium, asam-asam lemak, asam oksalat dan
serat (Duke, 2000).
2.1.5 Khasiat Tumbuhan
Senyawa-senyawa yang terkandung dalam daun bangun-bangun
berpotensi terhadap aktivitas biologik yaitu diuretik, analgesik, mencegah kanker, antitumor, antivertigo, immunostimulan, antiradang, antiinfertilitas,
hipokolesterolemik, hipotensif dan antiseptika (Santosa dan Hertiani, 2005). 2.2 Ekstraksi
Ekstraksi adalah suatu proses pemisahan kandungan senyawa kimia dari
bahan-bahan dikeringkan terlebih dahulu kemudian dihaluskan pada derajat kehalusan tertentu (Harborne, 1987).
Menurut Depkes RI (2000), beberapa metode ekstraksi yang sering
digunakan dalam berbagai penelitian antara lain yaitu: A. Cara dingin
1. Maserasi
Maserasi adalah proses penyarian simplisia dengan cara perendaman menggunakan pelarut dengan sesekali pengadukan pada temperatur kamar.
Maserasi yang dilakukan pengadukan secara terus-menerus disebut maserasi kinetik sedangkan yang dilakukan pengulangan panambahan pelarut setelah
dilakukan penyaringan terhadap maserat pertama dan seterusnya disebut remaserasi.
2. Perkolasi
Perkolasi adalah proses penyarian simplisia dengan pelarut yang selalu baru sampai terjadi penyarian sempurna yang umumnya dilakukan pada
temperatur kamar. Proses perkolasi terdiri dari tahap pelembaban bahan, tahap perendaman antara, tahap perkolasi sebenarnya (penetesan/penampungan ekstrak) terus-menerus sampai diperoleh perkolat yang jumlahnya 1-5 kali bahan.
B. Cara panas 1.Refluks
Refluks adalah proses penyarian simplisia dengan pelarut pada temperatur titik didihnya, selama waktu tertentu dan jumlah pelarut terbatas yang relatif konstan dengan adanya pendingin balik.
Digesti adalah proses penyarian dengan pengadukan kontinu pada temperatur lebih tinggi dari pada temperatur ruangan, yaitu secara umum dilakukan pada temperatur 40-50oC.
3. Sokletasi
Sokletasi adalah proses penyarian dengan menggunakan pelarut yang
selalu baru, dilakukan dengan menggunakan alat soklet sehingga terjadi ekstraksi kontinu dengan pelarut relatif konstan dengan adanya pendingin balik.
4. Infundasi
Infundasi adalah proses penyarian dengan menggunakan pelarut air pada temperatur 90oC selama 15 menit.
5. Dekoktasi
Dekoktasi adalah proses penyarian dengan menggunakan pelarut air pada temperatur 90oC selama 30 menit.
2.3 Radikal Bebas
Radikal bebas ialah atom atau molekul dengan susunan elektron tidak
lengkap atau tidak berpasangan misalnya Cl*, CH3*, HO* sehingga bersifat tidak stabil dan kecenderungan kuat untuk berpasangan. Radikal bebas bertendensi kuat memperoleh elektron dari atom lain, sehingga atom lain yang kekurangan satu
elektron ini menjadi radikal bebas pula yang disebut radikal bebas sekunder. Proses ini akan berlangsung berantai dan menyebabkan kerusakan biologik.
Radikal bebas menyebabkan efek samping invivo sehingga terjadi injury sel atau disfungsi dan diikuti inflamasi dan pada akhirnya terjadi penyakit degeneratif. Metabolisme aerobik terjadi karena adanya pengaruh atmosfer yang berisi oksigen
Pembentukan radikal bebas dan reaksi oksidasi pada biomolekul akan berlangsung sepanjang hidup. Inilah penyebab utama dari proses penuaan dan berbagai penyakit degeneratif. Tubuh memiliki mekanisme pertahanan
antioksidan (antioxidant defence) dalam bentuk enzim antioksidan dan zat antioksidan untuk menetralisir radikal bebas. Akan tetapi karena perkembangan
industri yang pesat, manusia berkontak dengan berbagai sumber radikal bebas yang berasal dari lingkungan dan dari kegiatan fisik yang tinggi sehingga sistem pertahan antioksidan dalam tubuh tidak memadai (Silalahi, 2006).
Radikal bebas yang ada didalam tubuh berasal dari hasil metabolisme tubuh dan faktor eksternal seperti asap rokok, hasil penyinaran ultra violet, zat
pemicu radikal dalam makanan dan polutan lain. Contoh penyakit yang sering dihubungkan dengan radikal bebas adalah serangan jantung, kanker, katarak dan menurunnya fungsi ginjal. Tubuh memerlukan antioksidan untuk mencegah atau
mengurangi penyakit kronis yang disebabkan oleh radikal bebas tersebut.
Secara umum tahapan reaksi pembentukan asam lemak menjadi radikal
Tahap inisiasi adalah tahap awal terbentuknya radikal bebas, suatu senyawa turunan asam lemak mengalami kehilangan satu atom. Tahap propogasi adalah tahap perpanjangan radikal berantai, asam lemak bereaksi dengan oksigen
membentuk radikal peroksi, kemudian radikal peroksi lebih lanjut akan menyerang asam lemak lagi membentuk hidroperoksi dan asam lemak baru.
Tahap terminasi adalah tahap akhir, terjadinya pengikatan suatu radikal bebas dengan radikal bebas lain sehingga tidak menjadi reaktif (Kumalaningsih, 2006).
Radikal bebas yang sangat berbahaya dalam makhluk hidup antara lain
adalah golongan hidroksil (OH-), superoksida (O-2), nitrogen monooksida(NO), peroksidal (RO-2), peroksinitrit (ONOO-), asam hipoklorit (HOCl), hydrogen
peroksida (H2O2) (Silalahi, 2006). 2.4 Antioksidan
Antioksidan adalah substansi yang diperlukan tubuh untuk menetralisir
radikal bebas dan mencegah kerusakan yang ditimbulkan oleh radikal bebas terhadap sel normal, protein, dan lemak. Antioksidan menstabilkan radikal bebas
dengan melengkapi kekurangan elektron yang dimiliki radikal bebas, dan menghambat terjadinya reaksi berantai dari pembentukan radikal bebas yang dapat menimbulkan stress oksidatif.
Ternyata di dalam tubuh manusia terdapat mekanisme alami untuk menetralisir radikal bebas yang terbentuk sebagai hasil metabolisme maupun
radikal bebas yang masuk dari luar sebagai radikal bebas eksogen. Menurut Kosasih (2004) antioksidan endogen yang kita ketahui antara lain:
a. Superoksida dismutase (SOD): suatu enzim yang memang berperan dalam
b. Enzim lainnya adalah Glutathion peroxidase yang lebih dikenal sebagai GPx yang menghancurkan lemak peroksida dan hydrogen peroksida. c. Katalase: enzim yang ikut mengontrol hidrogen peroksida.
Antioksidan endogen dalam melakukan tugas Free Radicals Scavenger/ penangkap radikal bebas selalu memanfaatkan antioksidan eksogen yang berasal
dari bahan makanan seperti vitamin E, vitamin C, beta karoten dan senyawa flavonoid seperti isoflavon yang terdapat dalam kedelai
Flavonoid dan komponen yang lebih besar yaitu polipenol memberi warna
pigmen pada buah dan sayur mayur. Sayur mayur mengandung banyak antioksidan berkat kadar vitamin C, vitamin E, betakaroten, likopen, dan
flavonoid. Kuersetin salah satu antioksidan dari kelompok flavonoid, terdapat pada tanaman tingkat tinggi. Berbagai jenis buah, sayuran dan biji-bijian merupakan sumber senyawa flavonoid disamping sebagai sumber vitamin
antioksidan seperti alfa tokoferol, vitamin C dan beta karoten. Kini diketahui hampir 80% dari total antioksidan dalam buah dan sayuran berasal dari flavonoid,
yang dapat berfungsi sebagai penangkap anion superoksida, lipid peroksida radikal, oksigen singlet dan pengkelat logam.
Dari asal terbentuknya, antioksidan dibedakan menjadi dua yakni
intraseluler (di dalam sel/endogen) dan ekstraseluler (di luar sel/ eksogen) ataupun dari makanan sehingga antioksidan dalam tubuh dapat dikelompokkan menjadi 3
yakni:
a. Primary Antioxidant (Antioksidan Utama/ Antioksidan Primer)
Yang termasuk dalam antioksidan ini adalah: Superoksidase Dismutase
Antioksidan primer ini bekerja untuk mencegah terbentuknya senyawa radikal bebas baru. Antioksidan ini mengubah radikal bebas yang ada menjadi molekul yang berkurang dampak negatifnya sebelum radikal bebas ini sempat
bereaksi. Contoh antioksidan ini adalah enzim SOD yang berfungsi sebagai pelindung hancurnya sel-sel dalam tubuh serta mencegah proses peradangan
karena radikal bebas.
b. Secondary Antioxidant (Antioksidan Kedua/ Antioksidan Sekunder)
Antioksidan ini berfungsi menangkap radikal senyawa serta mencegah
terjadinya reaksi berantai. Contoh antioksidan sekunder: vitamin E, vitamin C dan betakaroten.
c. Tertiary Antioxidant (Antioksidan Ketiga/ Antioksidan Tersier)
Antioksidan ini memperbaiki kerusakan sel-sel dan jaringan yang disebabkan radikal bebas. Contoh enzim yang memperbaiki DNA pada inti sel
adalah metionin sulfoksidan reduktase. Adanya enzim-enzim perbaikan DNA ini berguna untuk mencegah penyakit misalnya kanker.
2.4.2 Vitamin C
Vitamin C atau asam askorbat mempunyai berat molekul 176,13 dengan rumus bangun C6H8O6, dengan titik lebur 190-192oC. asam askorbat mengandung
tidak kurang dari 99,0% C6H8O6. Pemerian: serbuk atau hablur putih atau agak kuning, tidak berbau, rasa asam, oleh pengaruh cahaya lambat laun menjadi gelap,
dalam larutan cepat teroksidasi. Kelarutan: mudah larut dalam air, agak sukar larut dalam etanol (95%) P, praktis tidak larut dalam kloroform P, dalam eter P dan dalam benzene P. penyimpanan dalam wadah tertutup rapat, terlindung dari
Gambar 2.1 Rumus Bangun Vitamin C
Vitamin C berperan dalam pencegahan penyakit jantung koroner,
mencegah kanker, meningkatkan sistem kekebalan tubuh terhadap infeksi virus dan bakteri, dan berperan dalam regenerasi vitamin E (Silalahi, 2006).
Vitamin C apabila terkena pengaruh oksigen, zat-zat pengoksidasi lemah, atau oleh pengaruh enzim asam askorbat oksidase, asam askorbat mudah mengalami oksidasi menjadi asam dehidroaskorbat. Karena memiliki sifat mudah
teroksidasi, asam askorbat digunakan sebagai antioksidan (Counsell dan Hornig, 1981; Almatsier, 2004).
2.5 Spektrofotometer Visibel
Prinsip kerja spektrofotometer Visibel adalah diteruskannya sinar/cahaya melewati sebuah wadah (kuvet) yang berisi larutan, yang akan menghasilkan
spektrum. Alat ini menggunakan hukum Lambert Beer sebagai acuan (Ewing, 1975).
Panjang gelombang untuk sinar ultraviolet antara 200-400 nm sedangkan panjang gelombang untuk sinar tampak/visibel antara 400-750 nm (Rohman, 2007).
Spektrofotometri serapan adalah pengukuran serapan radiasi elektromagnetik panjang gelombang tertentu yang sempit, mendekati
sumber sinar monokromator, tempat sel untuk zat yang diperiksa, detektor, penguat arus dan alat ukur atau pencatat. (Depkes RI, 1979).
2.6 Metode DPPH (1,1-Diphenyl-2-Picrylhydrazyl)
Pada tahun 1992, Goldschmidt dan Renn menemukan senyawa berwarna ungu radikal bebas stabil DPPH, yang sekarang digunakan sebagai reagen
kolorimetri. DPPH sangat berguna dalam berbagai penyelidikan seperti inhibisi atau radikal polimerisasi kimia, penentuan sifat antioksidan amina, fenol atau senyawa alami (vitamin, ekstrak tumbuh-tumbuhan, obat-obatan). DPPH
berwarna sangat ungu seperti KMnO4 dan tereduksinya berwarna oranye-kuning (Ionita, 2005). Rumus bangun DPPH dapat dilihat pada Gambar 2.2 sebagai
berikut:
Gambar 2.2 Rumus Bangun DPPH
Metode DPPH adalah metode yang sederhana dapat digunakan untuk menguji kemampuan antioksidan yang terkandung dalam makanan. Prinsipnya
atom hidrogen yang disumbangkan senyawa antioksidan. Perubahan warna ini berdasarkan reaksi kesetimbangan kimia (Prakash, 2001).
DPPH merupakan radikal bebas yang stabil karena resonansi yang
dialaminya. Resonansi juga menyebabkan peningkatan kepekatan warna ungu (Molyneux, 2004). Resonansi DPPH dapat dilihat pada Gambar 2.3 berikut:
Gambar 2.3 Resonansi DPPH
Ketika larutan DPPH dicampurkan dengan senyawa yang dapat
mendonorkan atom hidrogen, akan dihasilkan bentuk tereduksi dari DPPH dan berkurangnya warna ungu (Molyneux, 2004). Reaksi antara DPPH dengan atom H dari senyawa antioksidan dapat dilihat pada Gambar 2.4 berikut:
Parameter yang dipakai untuk menunjukkan aktivitas antioksidan adalah harga konsentrasi efisiensi atau efficient concentration (EC50) atau Inhibitory Concentration (IC50) yaitu konsentrasi suatu zat antioksidan yang dapat
menyebabkan 50% DPPH kehilangan karakter radikal atau konsentrasi suatu zat antioksidan yang memberikan persen peredaman sebesar 50%. Zat yang
mempunyai aktivitas antioksidan tinggi, akan mempunyai harga EC50 atau IC50 yang rendah (Molyneux, 2004).
2.6.1 Pelarut
Metode ini akan bekerja dengan baik menggunakan pelarut methanol atau etanol karena kedua pelarut ini tidak mempengaruhi dalam reaksi antara sampel
uji sebagai antioksidan dengan DPPH sebagai radikal bebas (Molyneux, 2004). 2.6.2 Pengukuran absorbansi-panjang gelombang
Panjang gelombang maksimum (λmaks) yang digunakan dalam pengukuran
sampel uji sangat bervariasi. Menurut beberapa literatur panjang gelombang maksimum untuk DPPH antara lain 515-520 nm. Bagaimanapun dalam praktiknya
hasil pengukuran yang memberikan peak maksimum itulah panjang gelombangnya yaitu sekitar panjang gelombang yang disebutkan diatas. Nilai absorbansi yang mutlak tidaklah penting, karena panjang gelombang dapat diatur
untuk memberikan absorbansi maksimum sesuai dengan alat yang digunakan (Molyneux, 2004).
Ada beberapa alasan mengapa harus menggunakan panjang gelombang maksimal, yaitu: pada panjang gelombang maksimal, kepekaannya juga maksimal karena perubahan absorbansi untuk setiap satuan konsentrasi adalah yang paling
dilakukan pengukuran ulang maka kesalahan yang disebabkan oleh pemasangan ulang panjang gelombang akan kecil sekali (Rohman, 2007).
2.6.3 Waktu Pengukuran
Pada awalnya lama pengukuran menurut beberapa literatur, yang direkomendasikan adalah selama 30 menit dan ini telah dilakukan dalam beberapa
penelitian khususnya belakangan ini, waktu pengerjaan terpendek yaitu 5 menit atau 10 menit. Waktu pengukuran digunakan sebagai parameter untuk mengevaluasi aktivitas antioksidan sampel sebagai rujukan untuk digunakan pada
BAB III
METODE PENELITIAN
Penelitian ini dilakukan dengan metode eksperimental, meliputi pengujian
aktivitas antioksidan ekstrak etanol daun bangun-bangun dengan metode DPPH (1,1-diphenyl-2-picrylhydrazyl).
3.1 Alat dan Bahan
3.1.1 alat-alat
Alat-alat yang digunakan terdiri dari: erlenmeyer, gelas ukur, gelas beaker,
labu tentukur, tabung reaksi, gelas corong, batang pengaduk, kaca arloji neraca listrik (Mettler Toledo), Spektrofotometer ultraviolet-visisibel (UV PharmaSpec
1700 Shimadzu), bola karet, pipet volume, mat pipet, kertas saring, kertas label,
aluminium foil.
3.1.2 Bahan
Bahan-bahan yang digunakan pada penelitian ini adalah ekstrak etanol daun bangun-bangun. Bahan-bahan kimia lainnya berkualitas pro analisis yaitu
DPPH (1,1-diphenyl-2-picrylhydrazyl) (Sigma). Metanol, aseton, akuades dan vitamin C.
3.2 Pembuatan Ekstrak Etanol Daun Bangun-Bangun (EEDBB)
Pembuatan ekstrak dilakukan dengan cara maserasi, dilakukan dengan cara merendam sebanyak 500 g serbuk simplisia dengan 5000 ml etanol 96% dalam
wadah kaca. Selanjutnya dibiarkan selama 5 hari sambil sesekali diaduk. Di enap tuangkan atau disaring. Ditampung maserat pada botol gelap, dan ampasnya di rendam kembali dengan 2000 ml etanol, hal ini dilakukan sebanyak 2 kali. Hasil
evaporator. Kemudian dikeringkan dengan freeze dryer selama lebih kurang 24
jam dan diperoleh eksrak etanol (Kemala, 2012).
3.3 Pengujian Aktivitas Antioksidan EEDBB
3.3.1 Prinsip metode DPPH
Kemampuan sampel uji dalam meredam proses oksidasi DPPH
(1,1-diphenyl-2-picryl-hidrazyl) sebagai radikal bebas dalam larutan metanol (sehingga
terjadi perubahan warna dari ungu menjadi kuning) dengan nilai IC50 (konsentrasi sampel uji yang mampu meredam radikal bebas sebesar 50%) digunakan sebagai
parameter untuk menentukan aktivitas antioksidan sampel uji tersebut. 3.3.2 Pembuatan larutan DPPH 0,5 mM
Timbang 20 mg DPPH kemudian dilarutkan dalam metanol hingga volume 100 ml (Molyneux, 2004).
3.3.3 Pembuatan larutan blanko
Larutan DPPH 0,5 mM dipipet sebanyak 5 ml, kemudian dimasukkan kedalam labu tentukur 25 ml, dicukupkan volumenya dengan metanol sampai
garis tanda untuk mendapatkan konsentrasi 40 ppm (Molyneux, 2004). 3.3.4 Pembuatan larutan induk
Sebanyak 25 mg sampel uji (ekstrak kental) ditimbang, dimasukkan
ke dalam labu tentukur 25 ml dilarutkan dengan metanol lalu volumenya dicukupkan dengan metanol sampai garis tanda (konsentrasi 1000 ppm).
3.3.5 Pengukuran aktivitas antioksidan sampel uji dan vitamin C
Larutan induk dipipet sebanyak 3,12 ml; 6,25 ml; dan 12,5 ml ke dalam labu tentukur 25 ml untuk mendapatkan konsentrasi larutan uji 125 μg/ml, 250
μg/ml dan 500 μg/ml. ke dalam masing-masing labu tentukur ditambahkan 5 ml
tanda, kemudian di diamkan selama 60 menit. Pengukuran dilakukan dengan alat spektrofotometer pada panjang gelombang 516 nm (Rosidah, 2008).
Sebanyak 25 mg vitamin C ditimbang, dimasukkan ke dalam tentukur 25
ml dilarutkan dengan metanol lalu volumenya dicukupkan dengan metanol sampai garis tanda. Dipipet sebanyak 0,5 ml ke dalam labu tentukur 25 ml untuk
mendapatkan konsentrasi larutan uji 20 μg/ml. ke dalam masing-masing labu
tentukur ditambahkan 5 ml larutan DPPH 0,5 mM lalu volumenya dicukupkan dengan metanol sampai garis tanda, kemudian di diamkan selama 60 menit.
Pengukuran dilakukan dengan alat spektrofotometer pada panjang gekombang 516 nm.
3.3.6 Penentuan persen peredaman
Penentuan aktivitas penangkap radikal bebas dari sampel uji menggunakan metode DPPH dengan spektrofotometer panjang gelombang 516 nm. Pengukuran
dilakukan setelah didiamkan selama 60 menit. Nilai serapan larutan DPPH sebelum dan sesudah penambahan ekstrak tersebut dihitung sebagai persen
inhibisi (% inhibisi) dengan rumus sebagai berikut :
% Inhibisi = x 100%
Keterangan : AKontrol = Absorbansi tidak mengandung sampel
Asampel = Absorbansi sampel 3.3.7 Penentuan nilai IC50
Perhitungan yang digunakan dalam penentuan aktivitas penangkap radikal
adalah nilai IC50 (inhibitory concentration 50%). Nilai tersebut menggambarkan besarnya konsentrasi senyawa uji yang dapat menangkap radikal bebas 50%. Hasil
(μg/ml) sebagai absis (sumbu X) dan nilai % inhibisi (antioksidan) sebagai
ordinatnya (sumbu Y).
Secara spesifik, suatu senyawa dikatakan sebagai antioksidan sangat kuat
jika nilai IC50 kurang dari 50 µg/ml, kuat jika IC50 bernilai 50-100 µg/ml, sedang jika nilai IC50 bernilai 100-150 µg/ml dan lemah jika IC50 bernilai 151-200 µg/ml
BAB IV
HASIL DAN PEMBAHASAN
Ekstrak yang digunakan pada penelitian ini berasal dari peneliti
sebelumnya yaitu saudari Senja Kemala (2012), identifikasi tumbuhan, karakterisasi simplisia dan skrining fitokimia telah dilakukannya.
4.1 Hasil Uji Aktivitas Antioksidan Ekstrak Etanol Daun Bangun-bangun (EEDBB)
Pengukuran aktivitas antioksidan terhadap sampel uji dilakukan secara spektrofotometri pada panjang gelombang 516 nm. Larutan DPPH dalam metanol menghasilkan serapan maksimum pada panjang gelombang 516 nm, termasuk
dalam kisaran panjang gelombang sinar tampak (400-700 nm) (Rohman, 2007). Untuk melihat hubungan absorbansi DPPH terhadap penambahan konsentrasi
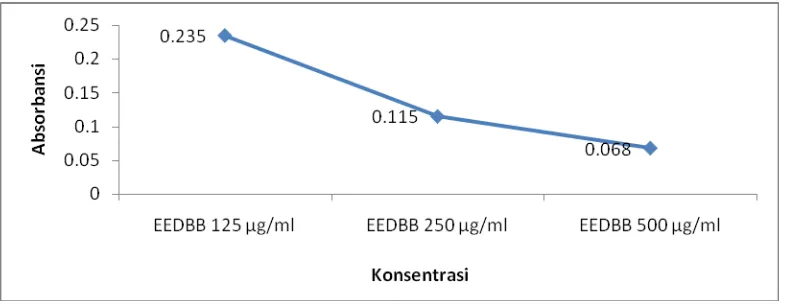
larutan uji dalam menganalisis aktivitas antioksidannya dapat dilihat pada Gambar 4.1 berikut ini:
Gambar 4.1 Hasil analisis aktivitas antioksidan ekstrak etanol daun bangun-bangun
Gambar hasil analisis aktivitas antioksidan sampel ekstrak etanol daun bangun-bangun menunjukkan bahwa adanya penurunan nilai absorbansi DPPH
Penurunan nilai absorbansi ini menunjukkan telah terjadi peredaman radikal bebas DPPH oleh larutan uji sehingga menunjukkan adanya aktivitas antioksidan dari sampel. Interaksi antioksidan dengan DPPH baik secara transfer
elektron atau radikal hidrogen pada DPPH, akan menetralkan radikal bebas dari DPPH.
Jika semua elektron pada radikal bebas DPPH menjadi berpasangan, maka warna larutan berubah dari ungu tua menjadi kuning terang dan absorbansi pada panjang gelombang maksimumnya akan hilang. Perubahan ini dapat diukur secara
stoikiometri sesuai dengan jumlah elektron atau atom hidrogen yang ditangkap oleh molekul DPPH akibat adanya zat antioksidan (Prakash, 2001; Molyneux,
2004).
4.2 Hasil Analisis Peredaman Radikal Bebas DPPH oleh Sampel Uji
Kemampuan antioksidan diukur pada menit ke-60 sebagai penurunan
serapan larutan DPPH (peredaman warna ungu DPPH) akibat adanya penambahan larutan uji. Nilai serapan larutan DPPH sebelum dan sesudah penambahan larutan
uji tersebut dihitung sebagai persen peredaman atau persen inhibisi. Dari analisis yang telah dilakukan, diperoleh nilai persen peredaman pada setiap kenaikan konsentrasi sampel uji dan vitamin C seperti yang terlihat pada Tabel 4.1 dan 4.2
Tabel 4.1 Data absorbansi dan % inhibisi ekstrak etanol daun bangun-bangun Konsentrasi
Larutan Uji
Absorbansi Pengukuran ke- Rata-rata Absorbansi
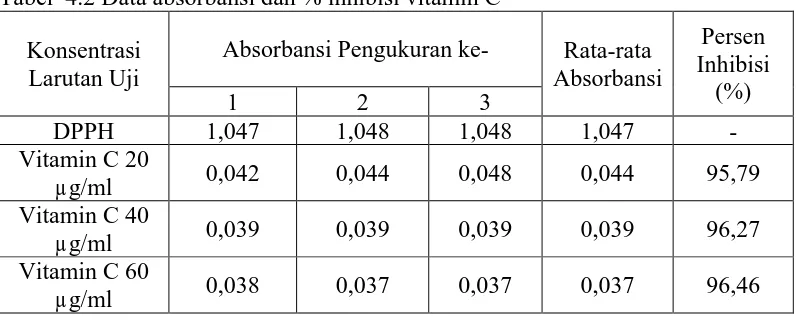
Tabel 4.2 Data absorbansi dan % inhibisi vitamin C Konsentrasi
Larutan Uji
Absorbansi Pengukuran ke- Rata-rata Absorbansi
Tabel 4.1 dan Tabel 4.2 menunjukkan bahwa semakin meningkat
konsentrasi maka semakin meningkat aktivitas peredaman DPPH karena semakin banyak DPPH yang berpasangan dengan atom hidrogen dari ekstrak sehingga serapan DPPH menurun. Hal ini juga dipengaruhi oleh lamanya reaksi antara
DPPH dengan larutan uji ekstrak dan vitamin C. Semakin lama DPPH bereaksi dengan larutan uji ekstrak maka memungkinkan semakin banyak DPPH yang
berikatan dengan atom hidrogen akibatnya serapan DPPH juga menurun. 4.3 Analisis Nilai Inhibitory Concentration (IC50) Sampel Uji
Nilai IC50 diperoleh berdasarkan persamaan regresi linier yang didapatkan
parameter aktivitas antioksidan, dimana konsentrasi larutan uji (ppm) sebagai absis dan nilai persen peredaman sebagai ordinat.
Hasil analisis nilai IC50 yang diperoleh berdasarkan perhitungan
persamaan regresi dapat dilihat pada Tabel 4.3 berikut ini: Tabel 4.3 Hasil analisis nilai IC50
Sampel IC50
Ekstrak etanol daun bangun-bangun 148,58
Vitamin C 11,66
Tabel 4.3 menunjukkan nilai IC50 ekstrak etanol daun bangun-bangun sebesar 148,58 µg/ml dan nilai IC50 vitamin C sebesar 11,66 µg/ml. Menurut
Anonim (2005), jika nilai IC50 berkisar 100-150 µg/ml mengindikasikan bahwa suatu senyawa memiliki aktivitas antioksidan sedang (menengah). Secara
keseluruhan aktivitas antioksidan ekstrak etanol daun bangun-bangun masih dibawah aktivitas antioksidan vitamin C. senyawa golongan fenol, flavonoid dan viamin C yang terdapat pada ekstrak memiliki sifat antioksidan (Ditjen POM,
1995). Pada ekstrak etanol daun bangun-bangun terkandung senyawa flavonoid yang diduga menyebabkan daun bangun-bangun memiliki aktivitas antioksidan
BAB V
KESIMPULAN DAN SARAN
5.1 Kesimpulan
Berdasarkan hasil penelitian yang telah dilakukan dapat disimpulkan bahwa: a. Ekstrak etanol daun bangun-bangun memiliki aktivitas antioksidan.
b. Hasil pemeriksaan aktivitas antioksidan dengan menggunakan spektrofotometer sinar tampak pada panjang gelombang 516 nm diperoleh hasil ekstrak etanol daun bangun-bangun memiliki aktivitas antioksidan
dengan nilai IC50 sebesar 148,58 µg/ml dan vitamin C sebesar 11,66 µg/ml.
5.2 Saran
Disarankan kepada peneliti selanjutnya untuk mengukur aktivitas antioksidan menggunakan fraksi dari daun bangun-bangun dan metode selain
DAFTAR PUSTAKA
Almatsier, S. (2004). Prinsip Dasar Ilmu Gizi. Jakarta: Gramedia Pustaka Utama. Hal. 173-177, 186-187.
Anonim, (2010). Potensi Daun Bangun-bangun Sebagai Laktogogum. Diakses 14 Mei 2012. Artikel. http://www.pdgmi.org/2010/05/potensi-daun-bangun-bangun-coleus.html
Anonim. (2005). Tanaman Obat Indonesia. Diakses 18 Maret 2013. Jurnal. http://www.iptek.go.id
Chandrappa, M.S., Harsha, R., Dinesha, R., dan Gowda, T. (2010). Antibacterial Activity Of Coleus aromaticus Leaves. International Journal of Pharmacy and Pharmaceutical Sciences. 2(3): 63-64.
Chang, J., Cheng, C., Hung, L., Chung, Y., dan Wu, R. (2007). Potential Use of Plectranthus amboinicus in The Treatment of Rheumatoid Arthritis. eCAM. 7(1):115-120.
Caunsel, J.N., dan Hornig, D.H. (1981). Vitamin C (Ascorbic Acid). New Jersey: Applied Science Publisher Ltd. Hal. 144-145.
Depkes. (1979). Materia Medika Indonesia. Jilid III. Jakarta: Departemen Kesehatan RI. Hal. 159, 167-171.
Depkes. (1980). Materia Medika Indonesia. Jilid IV. Jakarta: Departemen Kesehatan RI. Hal. 152.
Depkes. (1984). Farmakope Indonesia. Edisi III. Jakarta: Direktorat Jenderal Pengawasan Obat dan Makanan Departemen Kesehatan RI. Hal. 32-33. Depkes. (1989). Materia Medika Indonesia. Jilid V. Jakarta: Departemen
Kesehatan RI. Hal. 151-154, 537-540.
Depkes. (2000). Parameter Standar Umum Ekstrak Tanaman. Jakarta: Depkes RI. Hal. 10-12.
Ditjen POM. (1989). Farmakope Indonesia. Eisi Ketiga. Jakarta: Depkes RI. Hal. 28-29.
Duke. (2000). Dr.Duke’s Constituens and Ethnobotanical Database. Phytochemical Database, USDA-ARS-NGRL. http://www.ars-grin.gov/cgi-bin/duke/farmacy-scroll3.pl. Accessed Maret 2013.
Harbone, J.B. (1987). Metode Fitokimia, Penuntun Cara Modern Menganalisa Tumbuhan. Terjemahan Kosasih Padmawinata. Edisi II. Bandung: ITB Press. Hal. 47-102, 152-153.
Heyne, K., (1987), Tumbuhan Berguna Indonesia, Jilid 3, Departemen Kehutanan, Jakarta. Hal. 1698.
Ionita, P. (2005). Is DPPH Stable Free Radical a Good Scavenger for Oxygen Species?. Chem. Pap. 59(1): 11-16.
Jaitun, S. (2010). Manfaat Daun Bangun-Bangun. Diakses 14 Mei 2012. Artikel.
Kaliappan, N.D., dan Viswanathan, P.K. (2008). Pharmacognostical Studies on The Leaves of Plectranthus amboinicus (Lour) Spreng. Journal of Medical Research. 2(3): 182-184.
Kemala, S. (2012). Efek Toksisitas Akut Ekstrak Etanol dan Fraksi Daun Bangun-bangun (Plectranthus amboinicus (Lour.) Spreng) Terhadap Larva Atemia salina Leach dengan Metode Brine Shrimp Lethality Test (BSLT). Skripsi. Medan: Fakultas Farmasi Universitas Sumatera Utara. Kosasih, E., dan Setiabudi, T. (2004). Peran Antioksidan pada Lanjut Usia.
Jakarta: Pusat Kajian Nasional Makalah Lanjut Usia. Hal. 42-75.
Kumalaningsih, S. (2006). Antioksidan Alami. Cetakan I. Surabaya: Trubus Agrisarana Surabaya: Hal. 16-25.
Molyneux, P. (2004). The Use Of The Stabil Free Radical Diphenylpicrilhydrazyl (DPPH) For Estimating Antioxidant Activity. Songklanakarin J. Sci. Technol. 26(2): 211-219.
Pandey, B.P. (2003). A Text Book of Botany Angiosperms Taxonomy, Anatomy, Embryology (Including Tissue Culture And Economic Botany). New Delhi: S.Chand & Company LTD. Hal. 349.
Patel, R. (2011). Hepatoprotective Effects of Plectranthus amboinicus (Lour.) Spreng Againts Carbon Tetrachloride-Induced Hepatotoxicity. Journal of Natural Pharmaceuticals. 2(1): 28-35.
Prakash, A. (2001). Antioxidant Activity. Analytical Progress. 19(2): 1-4.
Rao, B. S., Shanboge, R., Upadhya, D., Jagetia, G.C., Adiga, S.K., Kumar, P., Guruprasad, K., dan Gayathri, P. (2006). Antioxidant, Anticlastogenic and Radioprotective Effect of Coleus aromaticus on Chinese Hamster Fibroblast Cells (V79) Exposed to Gamma Radiation. Mutagenesis. 21(4): 237-242.
Rosidah, Yom, M.F., Sadikun, A., dan Asmawi, M.Z. (2008). Antioxidant Potential of Gynura Procumbers. Pharmaceutical Biology. 46(a): 616-625.
Rout, O.P., Rout, K.K., Acharya, R., dan Mishra, S.K. (2010). Preliminary Pharmacognostical and Phytochemical evaluation of Coleus aromaticus Benth. leaf. International Journal of Pharma World Research. 1(4): 2-4.
Santosa, C.M., dan Hertiani, T. (2005). Kandungan Senyawa Kimia dan Efek Ekstrak Air Daun Bangun-Bangun (Coleus amboinicus, L.) Pada Aktivitas Fagositosis Netrofil Tikus Putih (Rattus norvegicus). Majalah Farmasi Indonesia. 16(3): 141–148.
Silalahi, J. (2006). Makanan Fungsional. Yogyakarta: Penerbit Kanisius. Hal. 38-55.
Sirait, M. (2007). Penuntun Fitokimia dalam Farmasi. Bandung: Penerbit ITB. Hal. 129-130.
Shyama, P. S., Naik, P., dan Vijayalaxmi, K. (2002). Efficiency of Coleus Aromaticus Extract in Modifying Cyclophosphamide and Mitomicyn-C induced Clastogenicity in Mouse Bone Marrow Cells. Journal of Experimental Biology. 40(9): 1020-1025.
Shu jing Wu dan Lean Teik Ng. (2007). Antioxidant and Free Radical Scavenging Activities of Wilod Bitter Melon (Momordica charantia Linn. Var.
Lampiran 2. Karakteristik Daun Bangun-Bangun
2.1 Makroskopik Daun Bangun-Bangun (Plectranthus amboinicus (Lour.) Spreng.
Lampiran 3. Data absorbansi dan % inhibisi ekstrak etanol daun bangun-bangun dan vitamin C setelah didiamkan selama 60 menit
1. Data absorbansi dan % inhibisi ekstrak etanol daun bangun-bangun
Konsentrasi Larutan Uji
Absorbansi Pengukuran ke- Rata-rata Absorbansi
2. Data absorbansi dan % inhibisi vitamin C
Konsentrasi Larutan Uji
Lampiran 4. Perhitungan % inhibisi ekstrak etanol daun bangun-bangun dan vitamin C setelah didiamkan selama 60 menit
1. Ekstrak etanol daun bangun-bangun
Konsentrasi 125 µg/ml
% inhibisi
Konsentrasi 250 µg/ml
% inhibisi =
=
= 84,78 % Konsentrasi 500 µg/ml
% inhibisi =
=
= 91 %
2. Vitamin C
Konsentrasi 20 µg/ml
% inhibisi =
=
Konsentrasi 40 µg/ml % inhibisi =
=
= 96,27 % Konsentrasi 60 µg/ml
% inhibisi =
=
Lampiran 5. Perhitungan nilai IC50 ekstrak etanol daun bangun-bangun dan vitamin C selama 60 menit
1.Perhitungan nilai IC50 ekstrak etanol daun bangun-bangun
X Y xy x2
Persamaan garis regresi y = 0,1593 x + 26,33
IC50 = y = 0,1593 x + 26,33 50 = 0,1593 x + 26,33
1.Perhitungan nilai IC50 vitamin C
Persamaan garis regresi y = 1,207x + 35,92 IC50 = y = 1,207x + 35,92
50 = 1,207x + 35,92