LAYU BAKTERI PADA TANAMAN JAHE
(Zingiber officinale Rosc.)
SRI RAHAYUNINGSIH
SEKOLAH PASCASARJANA
INSTITUT PERTANIAN BOGOR
Dengan ini saya menyatakan bahwa tesis Pemanfaatan Bakteri Endofit sebagai Alternatif Pengendalian Penyakit Layu Bakteri pada Tanaman Jahe (Zingiber officinale Rosc.) adalah karya saya sendiri dengan arahan dari komisi pembimbing dan belum diajukan dalam bentuk apapun kepada perguruan tinggi manapun. Sumber informasi yang berasal atau dikutip dari karya yang diterbitkan maupun tidak diterbitkan dari penulis lain telah disebutkan dalam teks dan dicantumkan dalam Daftar Pustaka di bagian akhir tesis ini.
Bogor, Juni 2011
SRI RAHAYUNINGSIH. Endophytic bacteria as alternatives diseases control of bacterial wilt on ginger (Zingiber officinale). Under direction of ABDUL MUNIF, WIDODO and SUPRIADI.
Ginger is cultivated in many tropical and subtropical regions of the world. Growers expressed concern regarding the impact of pathogens on yields in recent years. Similarly, growers expressed concern regarding the effect that pathogen threats will have on the industry in the future. Bacterial wilt disease caused by Ralstonia solanacearum is an important disease on ginger plant (Zingiber officinale Rosc) in Indonesia. The objective of this research was to study the effectiveness of endophytic bacteria in inhibiting the progress of bacterial wilt disease on ginger. Three isolates of endophytic bacteria were selected and tested their antibiosis activity and plant growth promoting rhizobacteria (PGPR) against the bacterial wilt disease (R. solanacearum). The research showed that under greenhouse condition all of the ginger plants treated with the 3 isolates of endophytic bacteria produced symptoms of bacterial wilt disease 7 days after inoculation of R. solanacearum. The 3 isolates of can only inhibit 12 % of severity of bacterial wilt disease on ginger up to 42 days after the inoculation, therefore they are not effective as biocontrol agent. .
SRI RAHAYUNINGSIH. Pemanfaatan Bakteri Endofit sebagai Alternatif Pengendalian Penyakit Layu Bakteri pada Tanaman Jahe (Zingiber officinale). Dibimbing oleh ABDUL MUNIF, WIDODO dan SUPRIADI.
Penyakit layu bakteri yang disebabkan oleh Ralstonia solanacearum pada tanaman jahe (Zingiber officinale Rosc), merupakan penyakit penting di beberapa negara di Asia, Australia, dan Afrika. Di Indonesia, penyakit layu bakteri jahe ditemukan pada tahun 1971 di Kuningan, Jawa Barat. Penyakit ini dapat menurunkan potensi hasil jahe sampai 90 %. Pada kasus tanaman jahe, varietas tahan dengan produksi rimpang yang memenuhi syarat sampai saat ini belum diperoleh di samping itu belum ada cara pengendalian yang efektif untuk penyakit layu bakteri. Alternatif pengendalian yang sedang dikembangkan adalah dengan meningkatkan pertahanan tanaman melalui induksi ketahanan. Penelitian bertujuan untuk mendapatkan isolat-isolat bakteri endofit yang potensial dalam mengendalikan penyakit layu bakteri pada tanaman jahe yang disebabkan oleh bakteri R. solanacearum.
Penelitian dilaksanakan di laboratorium Penyakit dan rumah kaca Balai Penelitian Tanaman Obat dan Aromatik (BALITTRO) Bogor, pada bulan Oktober 2008 – Januari 2010. Eksplorasi bakteri endofit dilakukan di daerah sentra produksi tanaman obat. Isolasi bakteri endofit dilakukan dengan cara mensterilisasi permukaan akar/batang menggunakan larutan NaOCL 10 % dan air steril. Bakteri patogen diisolasi dari tanaman jahe terinfeksi bakteri R. solanacearum di lapang. Isolat bakteri endofit diseleksi berdasarkan kemampuannya memproduksi bakteriosin atau sifat antibiosis. Uji potensi plant growth-promoting rhizobacteria (PGPR) dilakukan dengan menyiram benih mentimun yang telah disterilkan permukaanya dengan suspensi bakteri endofit dan ditumbuhkan dalam bak perkecambahan yang berisi tanah steril. Perlakuan diulang sebanyak 10 kali. Bakteri endofit hasil seleksi dikarakterisasi berdasarkan sifat morfologi koloni dan fisiologinya. Isolat bakteri endofit terpilih diuji potensinya di rumah kaca dengan cara menyiramkan 50 ml suspensi bakteri endofit 108 cfu/ml kedalam polibag yang telah ditanami bibit jahe umur 2 bulan, sebagai kontrol dilakukan penyiraman dengan menggunakan air steril. Satu minggu setelah aplikasi bakteri endofit tanaman diinokulasi R. solanacearum isolat T-954 dengan cara menyiramkan 25 ml ml/tanaman inokulum dengan kerapatan populasi 108 cfu/ml (OD600 = 0,1). Rancangan percobaan menggunakan rancangan acak lengkap (RAL) dengan jumlah perlakuan tiga isolat bakteri endofit yang paling berpotensi dari uji in-vitro diulang tiga kali. Masing-masing unit perlakuan terdiri dari 10 bibit. Peubah yang diamati meliputi Keparahan penyakit, kejadian penyakit, dan indeks penekanan penyakit. Data dianalisis menggunakan Anova dan dilanjutkan dengan uji Tukey pada taraf 5%.
antibiosis paling tinggi berasal dari tanaman jagung (41,03 %), berturut-turut diikuti isolat dari tanaman jahe (28,20), tomat (25,64 %), dan kencur (5,13 %). Pengujian potensi 39 isolat bakteri endofit antibiosis dalam meningkatkan pertumbuhan tanaman secara in vivo pada tanaman mentimun menunjukkan bahwa, terdapat tiga isolat bakteri endofit yang mampu meningkatkan pertumbuhan perakaran tanaman mentimun tertinggi. Ketiga isolat tersebut berasal dari tanaman jahe (EJH6), tomat (ET9), dan jagung (EJG14) yang selanjutnya akan digunakan dalam uji potensi dalam menekan perkembangan penyakit layu bakteri R. solanacearum pada tanaman jahe di rumah kaca.
© Hak Cipta milik IPB, tahun 2011
Hak Cipta dilindungi Undang-Undang
Dilarang mengutip sebagian atau seluruh karya tulis ini tanpa mencantumkan atau menyebutkan sumbernya. Pengutipan hanya untuk kepentingan pendidikan, penelitian, penulisan karya ilmiah, penyusunan laporan, penulisan kritik, atau tinjauan suatu masalah; dan pengutipan tersebut tidak merugikan kepentingan yang wajar IPB.
LAYU BAKTERI PADA TANAMAN JAHE
(Zingiber officinale Rosc.)
SRI RAHAYUNINGSIH
Tesis
Sebagai salah satu syarat untuk memperoleh gelar Magister Sains pada
Program Studi Fitopatologi
SEKOLAH PASCASARJANA
INSTITUT PERTANIAN BOGOR
Puji syukur penulis ucapkan pada Allah SWT atas rahmat dan karunia-Nya sehingga karya ilmiah dengan judul “Pemanfaatan Bakteri Endofit sebagai Alternatif Pengendalian Penyakit Layu Bakteri pada Tanaman Jahe
(Zingiber officinale Rosc)” dapat diselesaikan.
Karya ilmiah ini disusun sebagai salah satu satu syarat kelulusan di Sekolah Pasca Sarjana IPB untuk mendapatkan gelar Magister Sains pada Departemen Hama dan Penyakit
Pada kesempatan ini pula penulis mengucapkan terima kasih kepada Dr. Ir. Abdul Munif, M.Sc. Agr selaku ketua komisi pembimbing, Dr. Ir. Widodo, MS dan Prof. Dr. Ir. Supriadi, M.Sc selaku anggota komisi pembimbing atas segala bimbingan dan arahannya kepada penulis dalam penulisan usulan penelitian ini. Ungkapan terima kasih juga disampaikan kepada ayah (alm), ibu, suami, anak, serta seluruh keluarga atas segala do’a dan dukungannya.
Semoga karya ilmiah ini bermanfaat bermanfaat bagi pihak yang memerlukan.
Bogor, Juni 2011
Sri Rahayuningsih
Penulis lahir di Surabaya, pada tanggal 6 Oktober 1968 dari pasangan ayah (Alm.) H. Soeprapto dan ibu Hj. Rr. Soetartik sebagai putri ke-5 dari enam bersaudara.
Penyakit Layu Bakteri Pada Tanaman Jahe………... Strategi Pengendalian Penyakit Layu Bakteri Jahe ... Induksi KetahananTanaman………...
Tempat dan Waktu Penelitian ………... Tahap dan Metode Penelitian ... Pengamatan ...
15 15 19
HASIL DAN PEMBAHASAN 21
Kelimpahan Bakteri Endofit ... Bakteri Endofit Bersifat Antibiosis ... Bakteri Endofit sebagai Pemacu Pertumbuhan Tanaman ... Karakterisasi Morfologi dan Fisiologi Bakteri Endofit ... Potensi Bakteri Endofit di Rumah Kaca ...
Halaman No
1. Jumlah isolat bakteri endofit yang diisolasi dari tanaman jahe, kencur, tomat, dan jagung ... 21 2. Diameter Zona hambatan isolat bakteri endofit penghasil
bakteriosin ... 25 3. Persentase peningkatan pertumbuhan bibit mentimun pada umur 7
hari setelah diberi perlakuan bakteri endofit ... 28 4. Karakter morfologi dan fisiologi bakteri endofit isolat EJH6, ET9,
dan EJG14 ……… 30
Halaman No
1. Penampilan koloni bakteri endofit hasil isolasi (a) dan koloni bakteri endofit yang sudah dimurnikan (b) pada media TSA 22 2. Persentase bakteri endofit bersifat antibiosis hasil koleksi (a), dari
tanaman jae, kencur, tomat, dan jagung ... 23 3. Zona hambatan bakteri endofit dengan R. solanacearum (a) dan
koloni R. solanacearum pada media TTZA ………. 24 4. Persentase kelompok diameter hambatan bakteri endofit antibiosis
hasil koleksi (a), dari tanaman jahe, kencur, tomat, dan jagung (b) 25 5. Persentase peningkatan pertumbuhan bibit mentimun yang diberi
perlakuan bakteri endofit dibandingkan dengan kontrol …………. 27 6. Ciri pertumbuhan bakteri endofit isolate EJH6 dari tanaman jahe
(a), ET9 dari tomat (b), EJG14 dari jagung (c) ... 31 7. Grafik kejadian penyakit layu bakteri pada tanaman jahe yang
diaplikasi dengan bakteri endofit ... 32 8. Grafik keparahan penyakit layu bakteri pada tanaman jahe yang
PENDAHULUAN
Latar Belakang
Jahe (Zingiber officinale Rosc) adalah tanaman asli dari China Selatan yang juga dibudidayakan di daerah tropis dan sub tropis di dunia. Jahe
merupakan salah satu tanaman obat dengan klaim khasiat paling banyak, di
antaranya sebagai bumbu/penyedap makanan, bahan baku industri jamu, makanan
dan minuman kesehatan, fitofarmaka serta produk kosmetik dan perawatan tubuh
(SPA). Komoditas jahe, saat ini masih menempati urutan teratas dalam
penggunaan, sehingga masih memiliki peluang besar untuk terus dikembangkan.
Menurut data FAO (Camacho dan Brescia 2009), luas lahan dan produksi
jahe di seluruh dunia mengalami peningkatan sejak tahun 1999 dan diperkirakan
kecenderungannya akan terus meningkat di masa mendatang. Produksi jahe
dunia pada tahun 1999 adalah 952.222 ton meningkat menjadi 1.387.445 ton pada
tahun 2007. Hal yang sama terjadi pada luas lahan jahe di dunia yang juga
mengalami peningkatan beberapa tahun terakhir. Total luas lahan jahe dunia pada
tahun 1999 dari 762.318 acre (308.434 Ha) meningkat setiap tahunnya menjadi
1.060.818 acre (429.207 Ha) pada tahun 2007. Dalam beberapa tahun terakhir
China dan India secara terus menerus menempati urutan teratas dalam produksi
jahe segar dunia (lebih dari 50 %), diikuti Indonesia, Nepal and Nigeria. Tahun
1999 Indonesia menempati urutan ke 2 setelah China sebagai negara pengekspor
jahe terbesar di dunia, namun pada tahun 2000 - 2005 produksi jahe Indonesia
terus mengalami penurunan. Penurunan ini disebabkan adanya serangan penyakit
layu bakteri di daerah sentra pengembangan jahe utama di Jawa Barat.
Penyakit layu bakteri yang disebabkan oleh Ralstonia solanacearum (Smith) Yabuuchi et al., merupakan salah satu penyakit penting dan merupakan kendala utama dalam produksi pada tanaman jahe di banyak negara beriklim
tropis dan sub tropis di dunia (Buddenhagen dan Kelman 1964; Hayward 1991).
Di Indonesia, penyakit layu bakteri jahe ditemukan pada tahun 1971 di Kuningan,
Jawa Barat (Sitepu 1991) kemudian menyebar ke daerah Jawa Barat, Jawa
Tengah, Jambi, Lampung, Bengkulu, dan Sumatera Utara. Penyakit ini dapat
Bakteri patogen R. solanacearum ditemukan di seluruh dunia dan memiliki kisaran inang yang luas termasuk dalam ratusan spesies rentan dari
sekitar 50 famili tumbuhan yang berbeda, sehingga sulit dikendalikan (Kelman et al 1994;. Hayward 1991). Strategi pengelolaan konvensional seperti rotasi tanaman, penyesuauan waktu tanam, teknik budaya dan pengelolaan tanah masih
belum efektif (Chellemi et al. 1997).
Pengendalian penyakit layu bakteri harus dilakukan secara terpadu
menggunakan varietas tahan, secara kultur teknis, pemakaian bibit yang sehat dan
secara hayati (Elphinstone dan Aley 1995). Pada kasus tanaman jahe, varietas
tahan dengan produksi rimpang yang memenuhi syarat sampai saat ini belum
diperoleh di samping itu belum ada cara pengendalian yang efektif untuk penyakit
layu bakteri. Oleh karena itu, perlu dicari alternatif lain dalam pengendalian
penyakit layu bakteri jahe. Salah satu diantaranya adalah pengendalian secara
hayati yang mungkin dapat diintegrasikan dengan cara-cara pengendalian lainnya.
Pengendalian hayati terhadap penyakit tanaman yang telah dikembangkan
saat ini umumnya bersifat langsung terhadap patogen, yaitu melalui kompetisi,
antibiosis atau parasit. Aspek lain yang perlu diteliti adalah potensi agen hayati
dalam menginduksi ketahanan tanaman. Menurut Tuzun dan Kuc (1991)
ketahanan tanaman dapat terinduksi dengan menginokulasi agen penginduksi
sehingga dapat melindungi tanaman terhadap patogen dan mekanisme ini dikenal
dengan imunisasi.
Alternatif pengendalian yang sedang dikembangkan adalah dengan
meningkatkan pertahanan tanaman melalui induksi ketahanan. Ketahanan
merupakan suatu kemampuan tanaman untuk mengendalikan pengaruh yang
ditimbulkan patogen atau faktor perusak lainnya secara keseluruhan atau
sebagian. Induksi ketahanan terjadi apabila terdapat agen penginduksi yang dapat
mengakibatkan tanaman mengalami peningkatan ketahanan pada saat diserang
patogen (Agrios 1997). Induksi ketahanan tidak didasarkan pada penekanan
patogen, melainkan pada pengaktifan mekanisme pertahanan tanaman (Steiner &
Schönbeck 1995).
Dasar pemikiran dari induksi ketahanan adalah bahwa gen untuk ketahanan
diekspresikan setelah adanya induksi ketahanan pada tanaman dan biasanya
akan terdeteksi oleh adanya inokulasi challenge (infeksi susulan) pada waktu dan lokasi yang berbeda. Respon ketahanan tanaman yang terinduksi dapat berupa
respon hypersensitive, sintesis, fitoaleksin, pembentukan callose, pembentukan
pathogenesis-related (PR) protein, ß-1-3-glukanase, kitinase, peroksidase dan proteinase inhibitor (Stermer 1995).
Sejumlah komponen diketahui dapat menginduksi ketahanan tanaman
ketika diaplikasikan secara eksogeneous pada tanaman. Komponen tersebut dapat
berupa komponen biotik seperti mikroorganisme patogenik dan non patogenik, ras
inkompatibel, komponen microbial, ekstrak tanaman dan komponen abiotik
seperti senyawa kimia sintetik, radiasi dan CO2 (Oku 1994). Salah satu
komponen yang dapat digunakan dalam induksi ketahanan adalah bakteri endofit.
Pengendalian penyakit tanaman dengan menggunakan bakteri endofitik
merupakan salah satu alternatif pengendalian yang ramah lingkungan,
berkesinambungan dan dapat diintegrasikan dalam program pengendalian hama
terpadu. Beberapa jenis bakteri endofit disamping sebagai agen biokontrol, juga
sebagai pemacu pertumbuhan tanaman, dan mengimunisasi ketahanan tanaman
terhadap patogen (Kloepper et al. 1999).
Bakteri endofit adalah bakteri yang mengkolonisasi jaringan internal
tanaman dan tidak menimbulkan pengaruh yang merugikan bagi tanaman
(Hallmann et al. 1997). Bakteri endofit sudah banyak dilaporkan berpotensi sebagai agens biokontrol untuk mengendalikan beberapa jenis patogen seperti
virus, fungi, bakteri, nematoda, dan beberapa serangga (Van Loon et al. 1998). Bakteri endofit dapat berasal dari biji (Adams dan Kloepper 1996), bahan
vegetatif tanaman (Sturz 1995), dan tanah rhizosfer maupun phylloplane
(Hallmann et al. 1997). Pada umumnya bakteri endofit masuk ke dalam jaringan tanaman melalui stomata, lenti sel, luka (termasuk patahnya trikhom), area yang
rentan pada perakaran tanaman, dan radikel perkecambahan (Huang 2001).
Bakteri endofit saat ini menjadi perhatian para peneliti karena
keberadaannya yang mempengaruhi mekanisme fisiologi tanaman. Terjadinya
penyimpangan mekanisme fisiologi tanaman yang mengarah kepada peningkatan
metabolit sekunder tertentu pada tanaman seperti tanaman obat (jahe) melalui
bakteri endofit. Senyawa yang menginduksi metabolit sekunder, elisitor, dapat
berupa polisakarida, oligosakarida, protein, glikoprotein dan asam lemak.
Komponen tersebut salah satu diantaranya dapat berupa komponen dinding sel
mikroorganisme (Dixon dan Lamb 1990).
Penelitian bertujuan untuk mendapatkan isolat-isolat bakteri endofit yang
potensial dalam mengendalikan penyakit layu bakteri pada jahe yang disebabkan
oleh bakteri Ralstonia solanacearum melalui induksi ketahanan.
Hipotesis
Hipotesis yang dapat diajukan adalah bakteri endofit yang diperoleh dapat
menginduksi ketahanan tanaman jahe terhadap R. solanacearum (EF Smith) Yabuchii et al. penyebab penyakit layu.
Manfaat Penelitian
Manfaat yang diharapkan dari penelitian ini adalah mendapatkan isolat
bakteri endofit yang dapat menginduksi ketahanan tanaman jahe sebagai salah
TINJAUAN PUSTAKA
Tanaman Jahe
Tanaman jahe adalah jenis herba tahunan, yang tumbuh di daerah tropis
dan subtropis di Asia dan Australia. Tanaman ini termasuk genus Zingiber dari famili Zingiberaceae yang terdiri dari sekitar 150 spesies. Zingiberaceae cukup penting sebagai tanaman rempah yang bermanfaat sebagai tanaman obat dan
mempunyai nilai ekonomi. Selain jahe (Z. officinale Rosc.) yang termasuk ke dalam famili Zingiberaceae antara lain bangle (Z. cassumunar) dan lempuyang wangi (Z. aromaticum) (Ravindran et al. 2004).
Tanaman jahe tumbuh merumpun, berakar serabut dan mempunyai batang
semu yang bebentuk bulat dengan tinggi antara 30 – 75 cm. Tumbuh tegak, tidak
bercabang, berwarna hijau muda, sering kemerahan pada bagian pangkal. Setiap
batang umumnya terdiri 8 – 12 helai daun, berdaun sempit memanjang
menyerupai pita dengan panjang 15 – 23 cm dan lebar sekitar 2,5 cm yang
tersusun teratur dua baris berseling. Bunga berupa malai yang tersembul pada
permukaan tanah seperti gada dengan panjang lebih kurang 25 cm. Rimpang jahe
beruas-ruas, gemuk, agak pipih tertanam kuat dalam tanah dan semakin
membesar dengan bertambahnya umur tanaman. Rimpang jahe mengandung
minyak atsiri yang aromatis dan oleoresin khas jahe (Rostiana et al. 1991, Rismunandar 1988).
Rimpang jahe mengandung minyak essensial α zingiberen yang tinggi.
Minyak jahe banyak digunakan dalam industri makanan dan minuman, misalnya
ginger ale, bir jahe, dan berbagai kue maupun makanan penutup. Industri
kosmetik, farmasi,dan parfum juga menggunakannya dalam jumlah kecil. kapsul
Jahe dapat digunakan untuk meredakan kelelahan, membantu pencernaan, dan
untuk mengobati penyakit reumatik.
Di Indonesia famili Zingiberaceae digunakan sebagai obat-obatan,
kosmetik dan bumbu masak. Species penting yang dikomersial adalah jahe,
kunyit, temulawak dan lengkuas. Penggunaan temu-temuan untuk obat-obatan
masih di bawah 20 % dari total temu-temuan (Kuntorini 2005). Industri tanaman
obat tradisional Indonesia mengalami peningkatan yang sangat nyata dari tahun ke
tahun. Jumlah perusahaan obat tradisional pada tahun 1981 mencapai 165 buah
meningkat menjadi 1.023 pada tahun 2003; dan pangsa pasarnya pada tahun 2010
diperkirakan mencapai Rp. 7,2 triliun (Syakir 2007).
Tipe jahe yang banyak di tanam di Indonesia dikenal ada tiga yang
didasarkan atas ukuran dan warna rimpang, yaitu jahe putih besar, jahe putih kecil
dan jahe merah. Jahe putih kecil dan jahe merah sebagian besar dimanfaatkan
dalam industri minuman penyegar dan bahan baku industri obat tradisional, herba
terstandar maupun fitofarmaka (Bermawie et al. 2006). Jahe putih besar banyak digunakan untuk sayur, makanan, minuman, permen dan rempah-rempah
(Januwati 1999). Kontribusi Jahe di dalam perdagangan rempah-rempah dunia
sekitar 90% dibandingkan dengan rempah-rempah lainnya, seperti lada, cengkeh,
kayu manis, pala, dan kapulaga (Nakatani dan Kikuzaki, 2002).
Penyakit Layu Bakteri pada Tanaman Jahe
Penyakit layu bakteri tanaman jahe yang disebabkan oleh R. solanacearum (EF Smith) Yabuuchi et al. (sebelumnya disebut Pseudomonas solanacearum (EF Smith) merupakan kendala budidaya jahe. Penyakit ini sulit sekali ditanggulangi,
antara lain karena patogen ini mampu bertahan dalam tanah dalam waktu yang
cukup lama dan mempunyai sekitar 250 jenis tumbuhan dari 44 famili yang
dilaporkan dapat menjadi inang dari R. solanacearum (Hayward, 1991).
Supriadi (2000), melaporkan ada sekitar 124 jenis tanaman inang dari R. solanacearum adalah tanaman-tanaman yang berkhasiat obat. Beberapa jenis diantaranya merupakan komoditas penting yang banyak digunakan dalam industri
Hayward (1991), Denny dan Hayward (2001) menyebutkan bahwa R. solanacearum bersifat gram negatif, berbentuk batang dengan ukuran 0,5–0,7 x 1,5–2,5 µm, oksidase dan katalase positif, mengakumulasi poly-ß-hydroxibutirat sebagai sumber karbon, dan dapat mereduksi nitrat.
Gejala penyakit layu bakteri jahe yang paling mudah dilihat adalah
tanaman menjadi layu dan mati. Sebelum itu dapat diamati beberapa gejala
seperti daun menguning, pada pangkal batang dekat dengan rimpang ditemukan
bercak-bercak memar. Batang mudah dilepas dari rimpangnya dan kalau dicium
berbau busuk. Rimpang dari tanaman yang terserang menjadi lunak dan berbau
busuk. Bila batang dipotong kemudian direndam ujungnya dalam air jernih maka
bakteri yang ada di dalam jaringan pembuluh kayu akan keluar berupa gumpalan
berwarna putih. Dalam beberapa waktu warna air berubah dari jernih menjadi
keruh (putih susu).
Gejala penyakit di lapang umumnya baru muncul setelah tanaman jahe
berumur 2-3 bulan dan perkembangan gejala berlangsung dengan cepat (2-3
minggu) setelah infeksi (Supriadi, 1994). Berdasarkan kisaran inangnya, R. solanacearum dikelompokkan ke dalam 5 ras berdasarkan perbedaan tanaman inang utamanya, yaitu: ras 1 dengan inang fa mili Solanaceae dan Leguminosae,
ras 2 dengan inang tanaman pisang dan Heliconia spp., ras 3 dengan inang tanaman kentang dan tomat, ras 4 dengan inang tanaman jahe, dan ras 5 dengan
inang tanaman mulberry (Buddenhagen & Kelman 1964; He 1986). Khusus
untuk ras 4 (jahe), juga menyerang beberapa komoditas bernilai ekonomi tinggi,
dan beberapa jenis gulma. Misalnya, dari kelompok terung-terungan adalah
Penyebaran R. solanacearum terutama melalui benih, ras jahe menyebar cukup luas, meliputi Australia, China, Thailand, Malaysia, Hawaii, dan Indonesia
akibat terbawa benih jahe yang sudah terkontaminasi patogen (Hayward 1991;
Supriadi 1999). Penyebaran R. solanacearum di dalam kebun umumnya berlangsung melalui eksudat akar yang keluar dari tanaman sakit, kemudian
menginfeksi akar-akar tanaman sehat disekitarnya (Supriadi et al. 2000). Pegg dan Moffett (1971), menyimpulkan bahwa R. solanacearum strain jahe dapat bertahan hampir 2 tahun di dalam lahan bekas pertanaman jahe di Queensland,
Australia.
Strategi Pengendalian Penyakit Layu bakteri
Berbagai cara pengendalian telah diupayakan untuk menekan
perkembangan penyakit layu bakteri R. solanacearum dengan keberhasilan yang masih terbatas. Penyakit layu bakteri adalah masalah utama dan menjadi salah
satu kendala dalam produksi jahe dan tanaman sayuran lainnya karena sebaran
geografisnya sangat luas, banyak tanaman inangnya, mampu bertahan lama di
dalam tanah, variabilitas genetik, epidemiologi dan cara penularan yang
kompleks.
Strategi pengendalian layu bakteri yang umum dilakukan adalah : pemilihan
rimpang sehat dari daerah bebas penyakit; penentuan lahan yang sebelumnya
tidak memiliki riwayat layu bakteri, perlakuan rimpang dengan aplikasi panas atau
bahan kimia; sanitasi yang ketat di lapangan, termasuk pembatasan gerakan
pekerja pertanian dan air irigasi di lapangan; teknik budidaya dan pengolahan
tanah minimum; rotasi tanaman dengan tanaman bukan inang seperti padi dan
jagung; perlakuan tanah, termasuk agen pengendalian biologis, pengendalian
hama serangga dan nematoda di lapangan (Kumar dan Hayward 2005).
Strategi pengendalian yang dapat diterapkan pada tanaman obat, seperti
jahe adalah pencegahan masuknya patogen pada lahan yang masih sehat. Strategi
ini tergantung pada ketersediaan benih sehat dan informasi sejarah penggunaan
lahan. Pertanaman yang akan dijadikan sebagai sumber benih harus memenuhi
lapangan, untuk itu perlu dilakukan monitoring secara periodik, minimal 2 kali
(Supriadi et al. 2000).
Menurut French (1994) dalam Supriadi (2000), pengendalian penyakit layu bakteri bisa dengan pendekatan ras patogen. Faktor yang harus diperhatikan
untuk mengembangkan strategi pengendalian penyakit layu bakteri yang
disebabkan oleh R. solanacearum ras 1 dan ras 3, diantaranya adalah lahan bebas penyakit, pengendalian nematoda, bibit sehat, tanaman tahan, perlakuan tanah
dengan pemanasan maupun “soil amendments”, rotasi, tumpang sari, dan
pembuangan gulma di kebun.
Strategi untuk menghadapi R. solanacearum pada tanaman obat dapat mengikuti pola pendekatan ras 1. Pemilihan lokasi merupakan salah satu faktor
yang kontribusinya paling penting dalam keberhasilan pengendalian penyakit layu
bakteri pada jahe. Tanah yang tidak memiliki riwayat penyakit layu bakteri akan
menghasilkan tanaman jahe yang sehat jika rimpang yang ditanam bebas dari
patogen. Lahan sawah berpeluang sebagai lahan bebas penyakit, karena tanah
sawah terus menerus dalam keadaan tergenang megakibatkan anaerob R. solanacearum tidak akan bertahan hidup lama (Supriadi 2000). Tindakan pencegahan patogen lebih luas di lapang dapat dilakukan dengan mengeradikasi
tanaman sakit apabila sebaran patogen masih berada pada areal terbatas. Kunci
keberhasilan tidak merebaknya R. solanacearum pada tanaman jahe di Australia karena dilakukannya tindakan eradikasi dan karantina yang ketat pada tahun
1960an sehingga sampai saat ini Australia bebas dari R. solanacearum ras 4 jahe (Hayward 1991).
Bibit jahe tahan nematoda merupakan faktor penting dalam pengendalian
layu bakteri setelah lahan bebas penyakit. Nematoda berperan utama dalam
membuat luka pada sistem perakaran tanaman sehingga mempermudah R. solanacearum masuk/menginfeksi tanaman (Mustika 1996). Menanam varietas tahan adalah cara yang paling efisien, mudah, dan praktis, tetapi tidak mudah
mendapatkan varietas jahe tahan dilakukan melalui pemuliaan inkonvensional
seperti somaklonal dan fusi protoplas, sebagaimana dilakukan oleh Ibrahim
(2009), yang telah mendapatkan somaklonal jahe yang mengindikasikan
ketahanan terhadap toksin yang dihasilkan oleh R. solanacearum.
Keberhasilan agen pengendali hayati yang mampu untuk bersaing dengan
mikroba lain di dalam mikroflora tanah, dengan menghasilkan antibiotik atau
menginduksi tanaman inang dalam meningkatkan pertahanan tanaman untuk
menghambat pertumbuhan R. solanacearum sudah banyak dilaporkan. Bakteri antagonis strain avirulen R. solanacearum efektif dalam mengendalikan layu pada kacang tanah. Bakteri endofit strain liar 358 adalah agen pengendali layu bakteri
yang potensial (Frey et al. 1993).
Induksi Ketahanan Tanaman
Tanaman mempertahankan diri terhadap infeksi patogen dalam bentuk
struktur anatomis dan sistem fisiologis yang diaktifkan oleh suatu sinyal (induksi
ketahanan). Pertahanan dalam bentuk sistem fisiologis ini bersifat laten dan
hanya terjadi apabila ada penginduksi yang tepat (Van Loon 1997), seperti infeksi
patogen non kompatibel atau terserapnya senyawa bioaktif (Sequeira et al. 1977, Dixon & Lamb 1990).
Induksi ketahanan tanaman merupakan aktivitas pertahanan tanaman untuk
melindungi diri dari patogen atau hama melalui pengaktifan mekanisme
ketahanan tanaman (Ouchi 1983). Mekanisme pertahanan tanaman terjadi akibat
perlakuan agens penginduksi ketahanan dan infeksi challenge. Agens penginduksi akan diterima dan dikenali oleh reseptor tanaman yang berada diluar
dan/atau pada membran sel. Agens penginduksi ketahanan bisa berperan sebagai
sinyal itu sendiri atau hanya memicu sintesis sinyal tertentu yang ditransduksikan
ke bagian tanaman lain. Sinyal tersebut diproduksi di satu bagian tanaman dan
berperan di bagian lain. Transduksi sinyal dapat ditransfer secara intraseluler dan
interseluler sehingga menyebabkan perlindungan sistemik. Beberapa sinyal yang
terlibat dalam induksi ketahanan adalah asam salisilat (SA), asam jasmonat,
Pengaktifan reaksi ketahanan ditandai dengan adanya perubahan aktivitas
gen tanaman yang diindikasikan oleh suatu metilasi DNA genom setelah aplikasi
agens penginduksi tertentu. Dalam ketahanan terinduksi terjadi peningkatan
aktivitas enzim dalam lintasan produksi metabolit tertentu dan peningkatan jumlah
produksi gen primer seperti kitinase, β-1,3-glukanase, peroksidase, pathogenesis
related (PR) protein. Sintesis protein-protein ini tampaknya diregulasi pada level
mRNA (Park & Kloepper 2000).
Hoffland et al. 1996, mengemukakan bahwa induksi ketahanan oleh bakteri non-patogenik umumnya tidak menimbulkan dampak bunuh diri
(hypersensitivity/ programmed cell death). Dampak fenotipik yang teramati berupa induksi ketahanan secara sistemik (induced systemic resistance atau ISR). ISR ditujukan pada penekanan perkembangan penyakit tanpa adanya hubungan
langsung antara bakteri penginduksi dengan patogen pada tempat infeksi.
Menurut Sticher et al. (1997), beberapa hal yang membedakan antara mekanisme ISR dengan antagonisme, antara lain : tidak ada pengaruh toksik dari stimulan
terhadap patogen, sifat induksi ketahanan menurun bila inhibitor (aktinomisin D)
diaplikasikan, dan tidak ada korelasi dengan produksi metabolit toksik dari
stimulan.
Mulya et al. (1996) melaporkan adanya kelompok bakteri yang mempunyai habitat pada risosfer tanaman atau disebut dengan risobakteri yang
dapat mengkolonisasi jaringan dan menginduksi ketahanan tanaman. Bakteri
Pseudomonas fluorescens PfG32R dapat hidup dalam jaringan daun tembakau dan menginduksi aktivitas enzim fenilalanin amoniliase. Kemampuan hidup dan
menginduksi ensim tersebut diduga ada kaitannya dengan keberadaan gen yang
memiliki homology dengan gen asal patogen yang mengkode hipersensitivitas dan
patogenesitas, yaitu gen hrp. Risobakteri diaplikasikan melalui pencampuran dengan tanah steril, perendaman akar bibit tanaman atau pelapisan biji (Kloeper
1996).
Faktor-faktor yang menentukan induksi ketahanan oleh risobakteri
meliputi produksi asam salisilat, siderofor, dan lipopolisakarida (LPS). Pada
risosfer tanaman tembakau atau kacang buncis dimana ketersediaan ion besi
asam salisilat. Asam salisilat tersebut menjadi faktor penentu dalam induksi
ketahanan tanaman tembakau terhadap tobacco mosaik virus (TMV) atau
ketahanan kacang buncis terhadap Botrytis cinerea (Sticher et al. 1997).
Bakteri Endofit
Keberadaan mikroorganisme non-patogenik dalam jaringan tanaman tanpa
menimbulkan gejala penyakit telah lama diketahui (Trevet dan Hollis 1948).
Mikroorganisme tersebut dikenal sebagai endophytic microorganisms, termasuk bakteri endofit. Pada tanaman hortikultura musiman populasi bakteri endofit
dalam jaringan tanaman dapat mencapai 107 cfu per gram tanaman, sedangkan
pada tanaman tahunan seperti pinus berkisar antara 105 cfu per gram tanaman.
Berbagai spesies bakteri endofit terisolasi dari berbagai jenis tanaman dan
dapat menginduksi ketahanan tanaman. Kemampuan bakteri untuk hidup dalam
jaringan tanaman, sifat antagonisme terhadap patogen dan kemampuan
menginduksi ketahanan merupakan sifat menonjol dari bakteri endofit (Nejad dan
Johnson 2000). Keberadaan bakteri langsung dalam jaringan tanaman
mengurangi cekaman lingkungan yang sering mempengaruhi efektifitas
pengendalian. Strain bakteri tertentu selain menginduksi ketahanan juga dapat
memperbaiki pertumbuhan tanaman, meningkatkan ketahanan terhadap
kekeringan dan mencegah infeksi nematoda (Chanway 1998).
Bakteri endofit umumnya mengkolonisasi bagian interselluler dari
jaringan tanaman dan hanya sedikit laporan mengenai kolonisasi bakteri endofit
pada daerah intra seluler. Disamping itu bakteri endofit juga dapat
mengkolonisasi sistem pembuluh dan dapat ditranslokasikan secara sistemik ke
seluruh bagian tanaman (Hallmann et al. 1997).
Mekanisme bakteri endofit dalam menginduksi ketahanan tanaman yang
telah dilaporkan adalah menstimulasi akumulasi senyawa antimikrobia yang
merupakan suatu substansi dengan berat molekul rendah seperti fitoaleksin dan
senyawa fenol, pembentukan pathogegenesis-related protein (protein-PR), dan
pembentukan barier sel tanaman baik barier fisik maupun kimiawi dengan
kaya akan hidroxiproline sehingga patogen tidak dapat menyebar ke dalam
jaringan tanaman.
Beberapa spesies bakteri endofit yang telah dilaporkan diantaranya adalah
BAHAN DAN METODE
Tempat dan Waktu
Penelitian dilaksanakan di laboratorium dan rumah kaca Hama dan Penyakit
dan rumah kaca Balai penelitian Tanaman Obat dan Aromatik (BALITTRO),
Bogor; pada bulan Oktober 2008 – Januari 2010.
Kelimpahan bakteri endofit
Eksplorasi bakteri endofit dilakukan di daerah sentra produksi tanaman
obat. Beberapa contoh tanaman obat (jahe, kencur, kunyit) yang tidak
menunjukkan gejala penyakit (tanaman sehat). Bagian tanaman yang diambil
adalah rimpang, akar atau batang. Selanjutnya contoh tanaman diisolasi di
laboratorium bakteri BALITTRO.
Isolasi bakteri endofit dilakukan dengan cara mensterlisasi permukaan
akar/batang menggunakan larutan NaOCL 10 dan air steril. Air cucian yang
terakhir ditumbuhkan pada media 1/10 Tryptic Soy Agar (TSA), kemudian diinkubasikan pada suhu 37oC. Bila pada medium tidak ada mikroorganisme
yang tumbuh menandakan sterilisasi permukaan sudah berhasil. Contoh tanaman
yang telah disterilisasi permukaannya digerus dengan mortar steril sampai halus
dan diencerkan dengan air steril. 0,1 ml suspensi ekstrak tanaman ditumbuhkan
pada medium 1/10 TSA dan diinkubasikan pada suhu 37oC selama 48 jam.
Setelah 48 jam koloni bakteri yang tumbuh dimurnikan dan diperbanyak pada
medium TSA. Isolat bakteri endofit dikoleksi dan disimpan dalam botol berisi air
steril untuk diuji potensinya.
Isolasi bakteri patogen
dimasukkan kedalam tabung reaksi berisi air steril. Setelah 5 menit, suspensi
bakteri yang terbentuk digoreskan pada medium selektif Tryphenyl Tetrazolium Chloride (TTZA) dengan menggunakan jarum ose. Selanjutnya diinkubasikan pada suhu 37oC selama 48 jam. Koloni bakteri virulen yang tumbuh dimurnikan
dan diperbanyak pada medium Sucrose Peptone Agar (SPA). Isolat bakteri murni disimpan dalam botol berisi air steril dan siap untuk digunakan.
Seleksi sifat antibiosis secara in vitro
Isolat bakteri endofit yang diperoleh dari hasil isolasi diseleksi untuk
mendapatkan isolat potensial. Isolat diseleksi berdasarkan kemampuannya
memproduksi bakteriosin. Isolat ditumbuhkan pada medium SPA dalam cawan
petri dengan metode titik dan diinkubasikan pada suhu 37oC selama 48 jam.
Setelah biakan tumbuh dimatikan dengan uap chloroform selama 30 menit
kemudian dituangi dengan suspensi R. solanacearum dengan kerapatan populasi 108 cfu/ml (OD600 = 0,1) dan diinkubasikan lagi selama 24 jam. Pengamatan
dilakukan terhadap zona bening (hambatan) yang terbentuk disekitar koloni
bakteri endofit dan diukur diameternya. Diamater zona hambatan dikelompokkan
menjadi tiga kategori, yaitu lemah (< 8mm), sedang (8 - 16 mm), dan kuat (> 16
mm).
Isolat bakteri endofit yang mampu memproduksi bakteriosin atau bersifat
antibiosis dikoleksi untuk diuji potensinya dalam meningkatkan pertumbuhan
tanaman pada benih dan tanaman mentimun di rumah kaca.
Uji potensi dalam memacu pertumbuhan tanaman
Biakan bakteri endofit berumur 48 jam disuspensikan dengan akuades
steril hingga diperoleh kerapatan 108 cfu/ml. Benih mentimun yang telah
disterilkan permukaanya dengan larutan natrium hipoklorit 1 % kemudian dibilas
dengan akuades selanjutnya ditumbuhkan dalam nampan perkecambahan yang
berisi campuran, pasir, dan pupuk kandang steril dengan perbandingan 2 : 1 : 1
didalam rumah kaca pada suhu kamar. Masing-masing suspensi bakteri endofit
diteteskan akuades steril dengan volume yang sama. Perlakuan diulang sebanyak
10 kali. Pengamatan dilakukan satu minggu setelah perlakuan terhadap panjang
akar dan jumlah akar serabut bibit mentimun. Peningkatan pertumbuhan tanaman
dihitung berdasarkan persentase panjang akar dan jumlah akar serabut bibit
mentimun yang diberi perlakuan bakteri endofit dibandingkan dengan kontrol.
Isolat bakteri endofit antibiosis yang berpotensi meningkatkan
pertumbuhan tanaman dikarakterisasi dan diidentifikasi untuk digunakan dalam
pengujian induksi ketahanan di rumah kaca.
Karakterisasi bakteri endofit
Isolat bakteri endofit bersifat antibiosis yang berpotensi meningkatkan
pertumbuhan tanaman dikarakterisasi berdasarkan sifat morfologi koloni dan
fisiologinya sebagaimana diuraikan dalam Supriadi (1994), Kerr (1980) dan
Schaad et al. (2001). Beberapa tahapan yang dilakukan, antara lain :
Karakter koloni.
Bakteri endofit ditumbuhkan pada medium SPA dan King’s B Agar
(KBA) dan diinkubasikan pada suhu 37oC selama 48 jam. Karakter koloni bakteri
yang tumbuh diamati. Menurut Kerr (1980), pembentukan pigmen fluorescens
ditandai oleh adanya warna kuning kehijauan yang berpendar di bawah cahaya
ultra violet).
Reaksi Gram.
Pada permukaan kaca objek diletakkan 1-2 tetes KOH 3%. Koloni bakteri
dicampur dengan KOH menggunakan jarum ose selama 10 detik. Koloni yang
membentuk lendir dan bila ditarik seperti benang menandakan bereaksi positif
atau termasuk gram negatif, sebaliknya bila tidak berlendir bereaksi negatif atau
Reaksi oksidatif/fermentatif.
Isolat bakteri ditusukkan ke dalam dua tabung reaksi yang berisi medium
oksidatif-fermentatif, satu tabung ditutup dengan parafin cair steril dan satu lagi
dibiarkan terbuka kemudian diinkubasikan selama 7 hari. Medium yang berwarna
kuning pada tabung terbuka dan tertutup menandakan reaksi fermentatif,
sedangkan reaksi oksidatif ditandai terbentuknya warna kuning pada medium
hanya pada tabung yang terbuka (Kerr, 1980).
Hidrolisis arginin.
Isolat bakteri ditusukkan ke dalam tabung reaksi yang berisi medium
arginin dan diinkubasikan selama 7 hari. Terjadinya hidrolisis arginin ditandai
dengan perubahan warna merah pada media (Kerr, 1980).
Reaksi hipersensitif.
Isolat bakteri ditumbuhkan pada medium TSA dan diinkubasikan pada
suhu 37oC selama 48 jam, selanjutnya disuspensikan dalam air steril hingga
diperoleh kerapatan populasi 108 (OD600 = 0,1). Suspensi bakteri diinjeksikan
pada tulang sekunder daun tembakau. Isolat yang bersifat patogen terlihat dari
gejala putih transparan, kematian jaringan daun (collapse) dalam waktu 24 – 48 jam setelah injeksi (Lelliot dan Stead, 1987).
Uji potensi di rumah kaca
Efektifitas isolat bakteri endofit yang bersifat antibiosis kuat dan
berpotensi meningkatkan pertumbuhan tanaman diuji di rumah kaca. Bibit jahe
yang digunakan adalah jahe putih besar. Aplikasi bakteri endofit dengan cara
penyiraman 50 ml suspensi bakteri endofit 108 cfu/ml kedalam polibag yang telah
ditanami bibit jahe umur 2 bulan, sebagai kontrol dilakukan penyiraman dengan
diinokulasi R. solanacearum isolat T-954 dengan cara menyiramkan 25 ml ml/tanaman inokulum dengan kerapatan populasi 108 cfu/ml (OD600 = 0,1).
Rancangan percobaan menggunakan rancangan acak lengkap (RAL)
dengan jumlah perlakuan tiga isolat bakteri endofit yang paling berpotensi dari uji
in-vitro diulang tiga kali. Masing-masing unit perlakuan terdiri dari 10 bibit.
Peubah yang diamati
Kejadian penyakit
Kejadian penyakit dihitung dengan menggunakan rumus :
P = a / b x 100 %
Keterangan : P = Kejadian penyakit layu
a = Jumlah tanaman yang menunjukan gejala layu
b = Jumlah tanaman yang diamati
Keparahan penyakit
Indeks penyakit dihitung menggunakan rumus seperti digunakan oleh
Winstead dan Kelman (1954), Arwiyanto et al. (1994) yang dimodifikasi. Keparahan penyakit dihitung berdasarkan skala :
0 = tidak ada gejala daun menguning
1 = 10 % daun menguning
2 = 20 – 50 % daun menguning
3 = semua daun menguning kecuali daun pucuk
4 = semua daun menguning
Rumus keparahan penyakit (KP) adalah :
(n1 x 1) + (n2 x 2) + (n3 x 3) + n4 x 4) + (n5 x 5)
K P = x 100 % N x 5
n1 …5 = jumlah tanaman dengan skala penyakit tertentu
0, 1, …, 5 = skala penyakit
N = Jumlah tanaman pada tiap perlakuan
Penekanan penyakit
Indeks penekanan penyakit dihitung dengan rumus :
DIc – DIb
Indeks penekanan penyakit = x 100 % DIc
DIc = Indeks penyakit pada kontrol
DIb = indeks penyakit pada perlakuan agens biokontrol
Analisis Data
Data yang diperoleh dianalisis secara statistika dengan dengan menggunakan
HASIL DAN PEMBAHASAN
Kelimpahan bakteri endofit
Hasil eksplorasi dan isolasi bakteri endofit dari akar, rimpang, dan batang
tanaman jahe, kencur, tomat, dan jagung disajikan pada Tabel 1. Bakteri endofit
yang diperoleh sebanyak 222 isolat, paling banyak diperoleh pada bagian akar
dibandingkan pada bagian batang tanaman. Banyaknya isolat bakteri endofit
yang diperoleh menunjukkan bahwa keberadaan bakteri endofit di alam
berlimpah.
Tabel 1 Jumlah isolat bakteri endofit yang diisolasi dari tanaman jahe, kencur, tomat, dan jagung
Tanaman Asal Bagian Isolat
Akar Rimpang/
batang
∑ (%)
Jahe Sukabumi 13 32 45 20,27
Kencur Bogor 21 12 33 14,86
Tomat Lembang 36 24 60 27,03
Jagung Bogor 45 39 84 37,84
Jumlah 222 100
Data Tabel 1 menunjukkan bahwa bakteri endofit bisa ditemukan di dalam
jaringan tanaman pada bagian akar, batang, maupun rimpang temu-temuan seperti
kencur dan jahe. Sebagaimana dikemukakan oleh Adams dan Kloepper (1996),
bahwa bakteri endofit dapat berasal dari biji dan bahan vegetatif tanaman.
Selanjutnya Zinniel et al. (2002), mengemukakan bakteri endofitik dapat diisolasi dari bagian akar, batang, bunga, dan kotiledon. Bakteri dapat masuk melalui
proses perkecambahan biji, akar-akar sekunder stomata, atau melalui kerusakan
yang terjadi pada daun. Di dalam tanaman, bakteri endofitik dapat terlokalisir
pada bagian dimana bakteri tersebut mulai masuk atau menyebar ke bagian
tanaman lainnya. Di dalam jaringan tanaman bakteri berada di dalam sel, diruang
Hasil isolasi bakteri endofit diperoleh jumlah isolat yang bervariasi,
dengan urutan pertama diperoleh dari tanaman jagung (37,84 %), diikuti tanaman
tomat (27,03 %), tanaman jahe (20,27 %), dan terendah dari tanaman kencur
(14,86 %), dengan peluang diperoleh bakteri endofit paling banyak pada bagian
akar. Liang et al. (2003), melakukan pengamatan terhadap kolonisasi bakteri endofit tomat 01-144 pada akar dan batang tanaman tomat. Hasil pengamatan
menunjukkan bahwa bakteri endofit lebih kuat mengkolonisasi akar dibandingkan
batang dan fluktuasi populasi pada bagian akar juga lebih tinggi.
Gambar 1 Penampilan koloni bakteri endofit hasil isolasi (a) dan koloni bakteri endofit yang sudah dimurnikan (b) pada media TSA
Peranan bakteri endofit di dalam jaringan tanaman tomat dan jagung sudah
banyak dilaporkan, diantaranya bakteri endofit yang diisolasi dari tanaman jagung
efektif terhadap Fusarium moniliforme (Bacon 1998), dan bakteri endofit P. fluorescens dari tanaman tomat efektif terhadap R. solanacearum (Trevet dan Hollis 1948). Lebih lanjut dikemukakan oleh Hartman et al. (1992) bahwa P. fluorescens dan P. gladiol dapat menekan pertumbuhan R. solanacearum sebesar 60-90 % pada tanaman tomat.
Sebaliknya peranan bakteri endofit di dalam jaringan tanaman
temu-temuan seperti jahe dan kencur belum banyak diketahui. Studi pustaka dari
berbagai sumber juga menunjukkan belum adanya informasi tentang keberadaan
dan peran bakteri endofit di dalam tanaman jahe dan kencur. Oleh karena itu,
isolat-isolat bakteri endofit yang diperoleh dari kedua tanaman tersebut perlu
dikarakterisasi, khususnya kemungkinan sebagai agens hayati untuk pengendalian
penyakit layu bakteri.
Bakteri endofit bersifat antibiosis
Kemampuan bakteri endofit dalam menghambat pertumbuhan bakteri
patogen R. solanacearum merupakan langkah pertama dalam pemilihan agen biokontrol potensial. Hasil pengujian secara in vitro menunjukkan, dari 222 isolat
bakteri endofit yang diperoleh terdapat 39 atau 18 % di antaranya mampu
memproduksi bakteriosin atau bersifat antibiosis, sedangkan 82 % sisanya tidak
bersifat antibiosis (Gambar 2).
Gambar 2 Persentase bakteri endofit bersifat antibiosis hasil koleksi (a), dari tanaman jahe, kencur, tomat, dan jagung (b)
Terbentuknya zona bening (hambatan) di sekitar koloni bakteri endofit
mengindikasikan adanya senyawa antibiotik yang dikeluarkan oleh bakteri endofit
yang diuji untuk menghambat perkembangan bakteri patogen R. solanacearum penyebab penyakit layu pada tanaman jahe. Hal ini menunjukkan bakteri endofit
tersebut mempunyai mekanisme penekanan secara antibiosis. 82%
18%
Bakteri
endofit
non antibiosis antibiosis
a
0 20 40 60 80 100
Jahe Kencur Tomat Jagung
Endofit Antibiosis
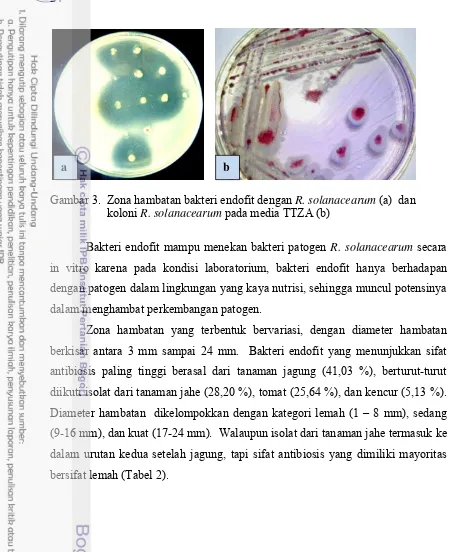
Gambar 3. Zona hambatan bakteri endofit dengan R. solanacearum (a) dan koloni R. solanacearum pada media TTZA (b)
Bakteri endofit mampu menekan bakteri patogen R. solanacearum secara in vitro karena pada kondisi laboratorium, bakteri endofit hanya berhadapan
dengan patogen dalam lingkungan yang kaya nutrisi, sehingga muncul potensinya
dalam menghambat perkembangan patogen.
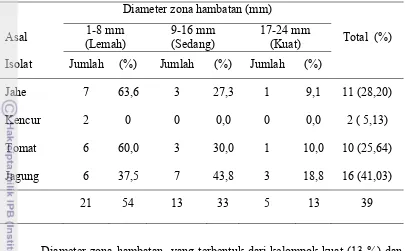
Zona hambatan yang terbentuk bervariasi, dengan diameter hambatan
berkisar antara 3 mm sampai 24 mm. Bakteri endofit yang menunjukkan sifat
antibiosis paling tinggi berasal dari tanaman jagung (41,03 %), berturut-turut
diikuti isolat dari tanaman jahe (28,20 %), tomat (25,64 %), dan kencur (5,13 %).
Diameter hambatan dikelompokkan dengan kategori lemah (1 – 8 mm), sedang
(9-16 mm), dan kuat (17-24 mm). Walaupun isolat dari tanaman jahe termasuk ke
dalam urutan kedua setelah jagung, tapi sifat antibiosis yang dimiliki mayoritas
bersifat lemah (Tabel 2).
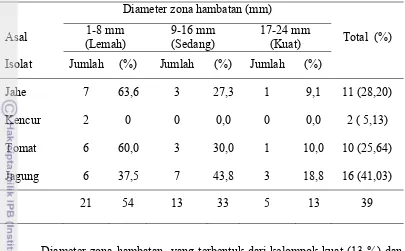
Tabel 2. Diameter zona hambatan isolat bakteri endofit penghasil bakteriosin.
Diameter zona hambatan yang terbentuk dari kelompok kuat (13 %) dan
sedang (33 %) terbanyak dari tanaman jagung, sedangkan kelompok lemah (54 %)
dari tanaman kencur dan jahe (Gambar 4). Sifat menonjol dari bakteri endofit
adalah kemampuannya untuk hidup dalam jaringan tanaman, sifat antagonisme
terhadap patogen dan kemampuan untuk menginduksi ketahanan (Nejad dan
Johnson 2000).
Gambar 4 Persentase kelompok diameter hambatan bakteri endofit antibiosis
hasil koleksi (a) dari tanaman jahe, kencur, tomat, dan jagung (b)
Antibiosis merupakan salah satu mekanisme penghambatan pertumbuhan
patogen oleh agens antagonis dan berperan penting dalam mengendalikan
diisolasi dari tanaman kentang dan jagung dilaporkan dapat mengendalikan
patogen, dengan mekanisme pengendalian menghasilkan senyawa antibiosis
(Hinton dan Bacon 1995).
Antibiotik yang dihasilkan agens antagonis menyebabkan pertumbuhan
patogen terhambat. Antibiotik phenazine-1-1 carboxylate yang dihasilkan P. fluorescens 2-79 dapat aktif pada media yang kekurangan unsur Fe, seperti pada media KBA sehingga dapat menekan pertumbuhan patogen (Thomashow dan
Weller 1998). P. cepacia menghasilkan antibiotik phenazine carboxylic acid juga senyawa pengikat besi cephabactin (Meyer et al. 1989). Bacillus sp strain Ba-118 dan P. putida strain pf-20 telah dilaporkan menunjukkan aktivitas antibiosis secara in vitro terhadap R. solanacearum bakteri patogen penyebab layu pada tanaman tembakau. Kedua bakteri tersebut juga mampu menekan perkembangan
penyakit layu bakteri baik di rumah kaca maupun di lapangan (Arwiyanto dan
Hartana 2001).
Kebaradaan bakteri endofit dalam tanaman jagung sudah banyak diteliti
dan diuji potensinya sebagai agens hayati. Eliza (2004), melaporkan bahwa
peluang terbesar dari bakteri yang diisolasi dari empat jenis tanaman dengan
kemampuan antibiosis tertinggi didapatkan dari bakteri endofit akar jagung yaitu
sebesar (37,9 %).
Bakteri endofit sebagai pemacu pertumbuhan tanaman (PGPR)
Bakteri endofit yang mampu menghambat perkembangan R. solanacearum secara invitroselanjutnyadiseleksi potensinya dalam meningkatkan pertumbuhan
tanaman secara in vivo pada tanaman mentimun di rumah kaca (Gambar 5).
Hasil pengujian 39 isolat bakteri endofit antibiosis dalam meningkatkan
pertumbuhan tanaman secara in vivo pada tanaman mentimun menunjukkan
bahwa, beberapa isolat bakteri endofit mampu meningkatkan pertumbuhan
tanaman. Kemampuan isolat bakteri endofit dalam meningkatkan pertumbuhan
Gambar 5 Pertumbuhan bibit mentimun yang diberi perlakuan bakteri endofit
Hasil pengamatan menunjukkan tidak semua isolat bakteri endofit bersifat
antibiosis yang diuji mampu meningkatkan pertumbuhan tanaman mentimun
dibandingkan dengan tanaman kontrol (yang bernilai minus tidak mampu
meningkatkan pertumbuhan). Peningkatan pertumbuhan tanaman tertinggi
terdapat pada tanaman mentimun yang beri perlakuan isolat bakteri endofit
antibiosis yang berasal dari tanaman jagung, yaitu sebesar 35,96 % diikuti dari
tanaman tomat (33,40 %), dan tanaman jahe (31,34 %). Peningkatan
pertumbuhan ini diduga karena keberadaan bakteri endofit yang menyebabkan
jumlah akar dan panjang akar lateral meningkat dan memacu pertumbuhan
tanaman. Akar lateral dapat memperluas daerah penyerapan unsur hara oleh
tanaman sehingga kebutuhan nutrisi lebih cepat terpenuhi dan mampu
meningkatkan pertumbuhan tanaman (Vasudevan et al. 2002).
Isolat bakteri endofit yang dapat meningkatkan pertumbuhan tanaman
mentimun dengan persentase tertinggi dibandingkan dengan kontrol yang akan
diuji lebih lanjut potensinya sebagai agens hayati terhadap R. solanacearum pada tanaman jahe. Pemilihan tersebut sejalan dengan pendapat Kloepper et al. (1999), bahwa mayoritas agens hayati yang berpotensi memiliki kemampuan dalam
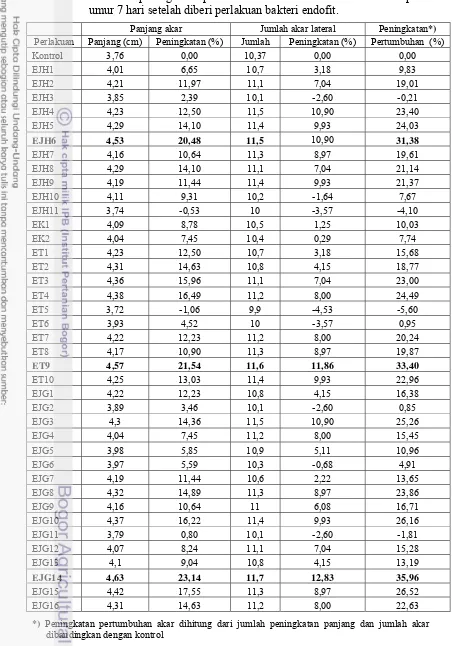
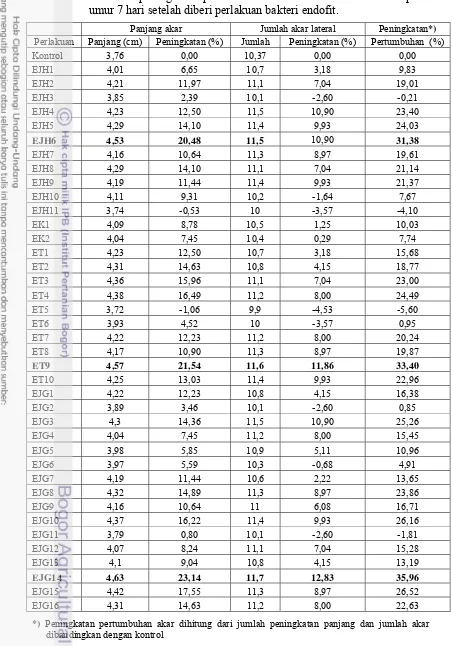
Tabel 3. Persentase peningkatan pertumbuhan bibit mentimun mentimun pada umur 7 hari setelah diberi perlakuan bakteri endofit.
Panjang akar Jumlah akar lateral Peningkatan*)
Perlakuan Panjang (cm) Peningkatan (%) Jumlah Peningkatan (%) Pertumbuhan (%)
Kontrol 3,76 0,00 10,37 0,00 0,00
Hasil seleksi pada Tabel 3 menunjukkan terdapat tiga isolat bakteri endofit
yang mampu meningkatkan pertumbuhan perakaran tanaman mentimun tertinggi.
Ketiga isolat tersebut berasal dari tanaman jahe (EJH6), tomat (ET9), dan
jagung (EJG14) yang selanjutnya akan digunakan dalam uji potensi dalam
menekan perkembangan penyakit layu bakteri R. solanacearum pada tanaman jahe di rumah kaca.
Mekanisme utama peningkatan pertumbuhan adalah mekanisme
penyerapan nutrisi oleh tanaman. Keberadaan bakteri pemacu pertumbuhan
tanaman menyebabkan tanaman mampu menyerap nutrisi makro maupun mikro
lebih baik. Mekanisme lainnya adalah yang berkaitan dengan kemampuan dalam
memproduksi hormon pertumbuhan, siderophore yang dapat mengikat ion Fe dan
membuatnya tersedia bagi perakaran tanaman, serta kemampuan melarutkan
mineral P (Nelson 2004).
Salamone et al. 2001 melaporkan bahwa P. fluorescens dapat menghasilkan hormon pertumbuhan sitokinin, tiga jenis sitokinin yang dihasilkan
adalah sitokinin dihydrozeatin riboside (DHZR), isopentenyladenosine (IPA), dan
trans-zeatin ribose (ZR). Hormon pertumbuhan yang dihasilkan oleh bakteri juga
dapat dimanfaatkan oleh tanaman untuk meningkatkan pertumbuhan tanaman.
Karakterisasi morfologi dan fisiologi bakteri endofit
Isolat bakteri endofit antibiosis yang berpotensi meningkatkan
pertumbuhan tanaman terbaik dikarakterisasi dan diidentifikasi, untuk digunakan
dalam pengujian induksi ketahanan di rumah kaca.
Hasil karakterisasi morfologi dan fisiologi bakteri endofit dari tiga isolat
terpilih hasil seleksi antibiosis dan PGPR yang berasal dari tanaman jahe, tomat
Tabel 4 Karakter morfologi dan fisiologi bakteri endofit isolat EJH6, ET9, dan EJG14
Karakter EJH6 ET9 EJG14
Gram positif negatif negatif
Warna Koloni putih putih kekuningan putih kekuningan
Pigmen fluorescens tidak berpendar berpendar berpendar
Endospora berspora tidak berspora tidak berspora
Uji O/F tidak diuji oksidatif oksidatif
Hidrolisis arginin tidak diuji positif positif
Reaksi Hipersensitif negatif negatif negatif
Hasil pengamatan menunjukkan tiga isolat yang dikarakterisasi terbagi
dalam dua kelompok yang berbeda. Terdapat dua isolat (ET9 dan EJG14)
termasuk kedalam kelompok P. fluorescens dan satu isolat (EJH6) kelompok Bacillus.
Koloni ET9 dan EJG14 berwarna putih kekuningan pada media King’s B
agar, dan berfluorescens dengan warna kuning kehijauan dibawah sinar ultra
violet. Kedua isolat bakteri tersebut termasuk kedalam kelompok bakteri
fluorescens. Sebagaimana dikemukakan oleh Goto (1992), bahwa fluorescensi
dihasilkan oleh pigmen fluoresesns, yaitu senyawa fluoresein atau pioverdin yang
terbentuk apabila bakteri tumbuh pada media yang kekurangan unsur besi, seperti
KBA. Karakter Pseudomonas kelompok fluorescens yang berfluorescensi di bawah cahaya ultra violet memudahkan untuk membedakannya dengan kelompok
bakteri lain.
Koloni EJH6 berwarna putih pada media SPA, tekstur kering tidak
(a) (b) (c)
Gambar 6 Ciri pertumbuhan bakteri endofit isolat EJH6 dari tanaman jahe (a), isolat ET9 dari tomat (b), dan EJG14 dari jagung (c).
Studi yang berfokus untuk mendapatkan bakteri pemacu pertumbuhan
tanaman seringkali berhasil ditemukan pada genus Pseudomonas dan Bacillus. (Merriman et al. 1974.). Viswanathan et al. (2003) melaporkan P. fluorescens berhasil diisolasi dari tebu dan dan dari tanaman kentang Reiter et al. (2002).
Menurut Landa et al. (2002), kelompok bakteri antagonis yang banyak ditemukan di rizosfer dan dalam jaringan akar graminae adalah Bacillus spp, Paenibacillus, Pseudomas, dan Stenotrophomonas spp, dan Pseudomonas kelompok fluorescens (Larkin et al. 1996). Lemaga et al. (2001) melaporkan pada rizofer jagung ditemukan Pseudomonas cepacia yang bersifat antagonis terhadap R. solanacearum yang dapat menurunkan kerapatan populasi bakteri patogen ini.
Potensi bakteri endofit di rumah kaca
Isolat R. solanacearum (T 954) yang digunakan dalam pengujian bakteri endofit mempunyai virulensi yang tinggi, terlihat dari perkembangan gejala
penyakit layu yang cepat pada tanaman jahe yang diinokulasi. Munculnya gejala
awal penyakit layu bakteri, yang ditandai dengan daun menguning sudah terlihat
pada hari ke-6 setelah inokulasi baik pada perlakuan kontrol positif (RS) maupun
tanaman yang diberi perlakuan dengan tiga isolat bakteri endofit (Gambar 7).
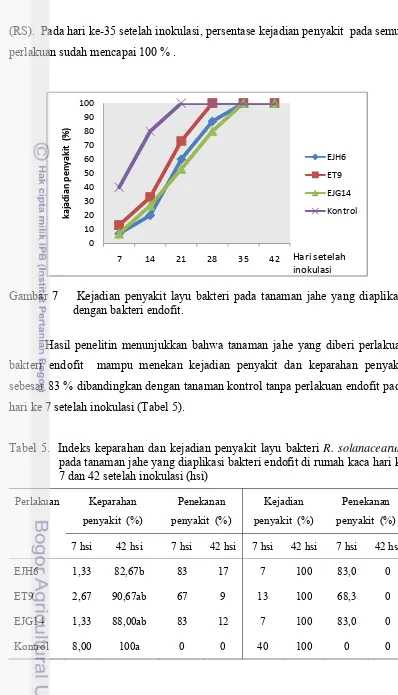
Kejadian penyakit hari ke-7 setelah inokulasi, terendah (1,33 %) pada
(RS). Pada hari ke-35 setelah inokulasi, persentase kejadian penyakit pada semua
perlakuan sudah mencapai 100 % .
Gambar 7 Kejadian penyakit layu bakteri pada tanaman jahe yang diaplikasi dengan bakteri endofit.
Hasil penelitin menunjukkan bahwa tanaman jahe yang diberi perlakuan
bakteri endofit mampu menekan kejadian penyakit dan keparahan penyakit
sebesar 83 % dibandingkan dengan tanaman kontrol tanpa perlakuan endofit pada
hari ke 7 setelah inokulasi (Tabel 5).
Tabel 5. Indeks keparahan dan kejadian penyakit layu bakteri R. solanacearum pada tanaman jahe yang diaplikasi bakteri endofit di rumah kaca hari ke 7 dan 42 setelah inokulasi (hsi)
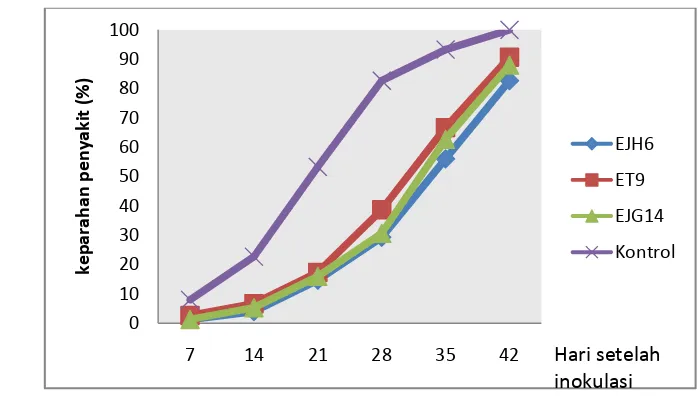
Penekanan keparahan penyakit jahe berangsur-angsur menurun dengan
bertambahnya umur tanaman dari 83 % pada 7 hari setelah inokulasi menjadi
12 % pada hari ke 42 (Gambar 8). Tingkat keparahan penyakit yang meningkat
dengan cepat ini dikarenakan virulensi patogen yang tinggi dan lingkungan yang
mendukung perkembangan patogen. Penekanan ini masih belum signifikan
karena waktu tanam jahe di lapangan dapat mencapai 7 – 9 bulan sebelum panen.
Gambar 8 Grafik keparahan penyakit layu bakteri pada tanaman jahe yang diaplikasi dengan bakteri endofit.
Berkurangnya tingkat keparahan penyakit layu bakteri pada tanaman jahe
disebabkan oleh adanya mekanisme pertahanan tanaman jahe yang terjadi akibat
perlakuan bakteri endofit dan adanya infeksi challenge. Menurut Steiner & Schönbeck 1995, agens penginduksi akan diterima dan dikenali oleh reseptor
tanaman yang berada diluar dan/atau pada membran sel. Agens penginduksi
ketahanan bisa berperan sebagai sinyal itu sendiri atau hanya memicu sintesis
sinyal tertentu yang ditransduksikan ke bagian tanaman lain. Sinyal tersebut
diproduksi di satu bagian tanaman dan berperan di bagian lain. Transduksi sinyal
dapat ditransfer secara intraseluler dan interseluler sehingga menyebabkan
perlindungan sistemik. Beberapa sinyal yang terlibat dalam induksi ketahanan
adalah asam salisilat (SA), asam jasmonat, sistemin, 2,6 dichloro-isonicotinic.
Ada beberapa kemungkinan alasan bakteri endofit belum mampu
perkembangan populasi bakteri patogen lebih cepat dibandingkan dengan populasi
bakteri endofit, sehingga keberadaan bakteri endofit semakin tertekan dan belum
mampu mengkolonisasi akar tanaman jahe. Sebagaimana dikemukakan oleh
Kloepper et al. (1992), bahwa bakteri endofit harus mampu mengkolonisasi perakaran dan memproduksi suatu pemicu atau sinyal untuk menginduksi
ketahanan dan ditranslokasikan secara sistemik sebelum ada infeksi patogen
(challenge).
Alasan kedua adalah, ekspresi peningkatan ketahanan dari perlakuan bakteri
endofit belum muncul pada waktu tanaman jahe diinokulasi R. solanacearum. Hasil penelitian Ibrahim (2009) pada kultur kalus jahe yang diperlakukan dengan
senyawa kimia penginduksi ketahanan (asam salisilat) menunjukkan bahwa
ekspresi ketahanan baru terlihat pada hari ke 30 setelah perlakuan asam salisilat.
Aktivitas antibakteri Bacillus spp dan Pseudomonas fluorescens terhadap R. solanacearum pada skala laboratorium, keberhasilannya pada skala rumah kaca dan lapang tidak konsisten (Supriadi dan Febriyanti 1995; Hartati et al. 1991). Hasil penelitian Mulya et al. (2000), menunjukkan bahwa aplikasi suspensi bakteri antagonis (Bacillus spp dan Pseudomonas fluorescens) belum mampu menekan laju perkembangan penyakit layu bakteri pada tanaman jahe di lapangan.
Chen et al. (1995) melaporkan bahwa aplikasi bakteri endofit yang diinjeksikan pada batang tanaman kapas dapat mengurangi busuk akar yang
disebabkan oleh Rhizoctonia solani dan layu vaskular yang disebabkan oleh Fusarium oxysporum. Bakteri ini bergerak ke atas dan ke bawah membentuk titik aplikasi dan mengkolonisasi jaringan akar internal, dapat menghambat masuknya
patogen dalam jaringan vaskular. Jadi bakteri endofit dapat keluar-berkompetisi
dengan patogen. Dengan demikian, keberadaan populasi bakteri menguntungkan
dalam rhizosphere tampaknya menjadi kunci untuk memperoleh keseimbangan
microfloral dan tanaman sehat. Dalam kondisi lapangan, efektivitas dari agen
biokontrol tergantung pada berbagai faktor seperti waktu aplikasi, umur tanaman,
kekuatan formulasi agen biokontrol, cara penerapan dan berbagai faktor lainnya
(Botelho dan Mendonca-Hagler 2006).
Kemampuan bakteri endofit mengkolonisasi jaringan internal dan dapat
berkembang dengan baik akan menghambat perkembangan patogen lebih optimal.
Mekanisme bakteri endofit dalam mengendalikan penyakit diantaranya dengan
mengkolonisasi relung ekologi patogen, terutama patogen penyebab penyakit pada
jaringan pembuluh (Hallmann 2001).
Bakteri endofit masih berpeluang digunakan sebagai agens pengendalian
hayati walaupun pada penelitian ini efektifitasnya baru pada skala laboratorium
dan memperlambat munculnya gejala penyakit layu bakteri R. solanacearum pada tanaman jahe di rumah kaca. Untuk meningkatkan potensi bakteri endofit dalam
mengendalikan penyakit layu bakteri pada tanaman jahe perlu dicari metode
aplikasinya, seperti cara aplikasi (aplikasi pada benih maupun tanaman), waktu
dan frekuensi aplikasi, dan formulasi yang tepat, sehingga bakteri endofit mampu
mengkolonisasi akar dengan cepat.
KESIMPULAN
Bakteri endofit hasil isolasi dari tanaman tomat, jagung, dan temu-temuan
diperoleh 222 isolat, 39 isolat (18 %) bersifat antibiosis, tiga diantaranya dapat
meningkatkan pertumbuhan tanaman mentimun di atas 30 % dibandingkan
dengan kontrol dan termasuk dalam kelompok Bacillus sp dan P. Fluorescens. Secara umum hasil penelitian menunjukkan bahwa ketiga isolat bakteri endofit
yang diuji dapat memperlambat munculnya gejala penyakit R. solanacearum pada tanaman jahe.
SARAN
Perlu dilakukan penelitian lanjutan, yaitu dengan melakukan pengamatan
kemampuan bakteri endofit dalam mengkolonisasi akar yang akan digunakan
DAFTAR PUSTAKA
Adams PD, Kloepper JW. 1996. Seed-borne bacterial endophytes in different cotton cultivars. Phytopathology 86:S97.
Adhi EM, Supriadi, Febriyanti M, Karyani N. 1998. Patogenisitas tiga isolat Ralstonia solanacearum pada tiga tipe kencur. Prosiding Seminar Nasional IV PFI Komisariat Jateng dan DIY, Surakarta 5 Desember 1998 : 421-425.
Adhi EM, Supriadi, Karyani N. 1998. Penyakit layu bakteri pada tanaman garut (Marantha arundinaceae). Prosiding Seminar Nasional IV PFI Komisariat Jateng dan DIY, Surakarta 5 Desember 1998 : 188-191.
Agrios GN. 1997. Plant Pathology. Fourth Edition. San Diego. Academic Press.
Arwiyanto T, Goto M, Tsuyumu S, Takikawa Y. 1994. Biological control of bacterial wilt of tomato by an avirulent strain of Pseudomonas solanacearum isolated from Strelitzia reginae. Ann. Phytopath. Soc. Japan 60:421-430.
Arwiyanto T, Hartana 2001. Percobaan lapangan pengendalian hayati penyakit layu bakteri tembakau. Media Gama 2:7-14
Bacon CW. 1998. The use of bacillus subtilis as an endophyte for control of corn seedling blight disease caused by Fusarium moniliforme. USDA, ARS:1 pp. Bermawie N, Syahid SF, Ajijah N, Purwiyanti P, Martono B. 2006. Usulan Pelepasan Varietas Jahe. Balai Penelitian Tanaman Rempah dan Obat, Bogor. Tidak dipublikasikan.
Botelho GR, Mendonca-Hagler LC (2006) Fluorescent Pseudomonas associated with the rhizosphere of crops—an overview. Braz J Microbiol 37:401– 416. doi:10.1590/S1517-83822006000400001
Buddenhagen IW, Kelman A. 1964. Biological and physiological aspecs of bacterial wilt caused by P. solanacearum. Ann. Rev. of Phytopathological 2:660 – 664.
Camacho HE, Brescia A. 2009. The Australian ginger industry. Overview of market trends and opportunities. The State of Queensland, Department of Employment, Economic Development and Innovation.
Chanway C. 1998. Bacterial endophytes : ecological and practical implication. Paper No.2.9.4S. International Congress of Plant protection: 2pp.
Chellemi DO, Olson SM, Mitchell DJ, Secker I, McSorley R. 1997. Adaptation of soil solarization to the integrated management of soil-borne pests of tomato under humid conditions. Phytopathology 87:250–258.
Dixon RA, Lamb JC. 1990. Molecular communication in interaction between plants and microbial pathogens. Ann. Rev. Plant Physiology and Plant Molecular Biology 41:339-367
Eliza. 2004. Pengendalian layu Fusarium pada pisang dengan bakteri perakaran graminae (tesis). Bogor: Sekolah Pasca Sarjana, IPB.
Elphinston JG, Aley P. 1995. Integrated control of bacterial wilt of potato in the warm tropics of Peru. Di dalam: Hartman GL, Hayward AC, editor. Bacterial Wilt. ACIAR Proceeding 45:276-283.
Frey P, Prior P, Trigalet-Demery D, and Trigalet A. 1993. Hrp-mutants of Pseudomonas solanacearum for biological control of tomato bacterial wilt. In: Hartman, G.L., and Hayward,A.C. (eds.) Bacterial Wilt. Proceedings of an international symposium, Kaohsiung, Taiwan,ROC, Oct. 29–30, 1992, ACIAR Proceedings 45, 257–260, ACIAR, Canberra.
Germida JJ, de Freitas JR. 1994. Growth promotion of Cabbage, lettuce and anion by flourescent pseudomonads under growth chamber condition. Di dalam: Ryder MH, Stephens PM, Bowen GD, editor. Improving Plant Productivity with Rhizosphere Bacteria. Proceeding of the Third International Workshop on Plant Growth Promoting Rhizobacteria; Adelaide, South Australia, March 7-11 1994. Adelaide: CSIRO 37-79.
Goto M. 1992. Fundamental of Bacterial Plant Pathology. San Diego: Academic Press.
Hallmann J, Quadt-Hallmann A, Mahaffee WF, Kloepper JW. 1997. Bacterial endophytes in agricultural crops. Can. J. Microbiology 43:895-914.
Hallmann J. 2001. Plant interaction with endophytic bacteria di dalam Jeger MJ, Spence NJ, Editors. Biotic Interaction in plant pathogen Associations. Wallingfod:CABI. hlm: 87-119.
Hartati SY, Boa ER, Supriadi, Adhi EM, Karyani N. 1991. Biological control of Sumatra disease bacterium Pseudomonas syzygii with its avirulent strains and Pseudomonas solanacearum. Industrial Crops Research Journal 4 (1): 1-4.
Hartati SY, Supriadi, Adhi EM, Karyani N. 1994. Colonization of Pseudomonas solanacearum in clove seedlings. Journal of Spice and Medicinal Crops 2 (2):24-28.
Hartman GL, Wong WF, Hanudin, Hayward AC. 1992. Potential of biological and chemical control of bacterial wilt. Di dalam: Hartman GL, Hayward AC, editor. Bacterial Wilt. Kaohsiung, 28-30 October 1992. Canbera: ACIAR. hlm 232-237.
Hayward AC. 1991. Biology and epidemiology of bacterial wilt caused by Pseudomonas solanacearum. Ann. Rev. of Phytopathol., 29, 67–87.