iv
EFEK ANTIBAKTERI EKSTRAK ETANOL DAUN AFRIKA
(Vernonia amygdalina) SEBAGAI BAHAN ALTERNATIF
MEDIKAMEN SALURAN AKAR TERHADAP
Porphyromonas gingivalis
(In Vitro)
SKRIPSI
Diajukan untuk memenuhi tugas dan melengkapi
syarat memperoleh gelar Sarjana Kedokteran Gigi
Oleh:
TIURMA SITOMPUL
NIM: 110600115
FAKULTAS KEDOKTERAN GIGI
UNIVERSITAS SUMATERA UTARA
iv
Fakultas Kedokteran Gigi
Departemen Ilmu Konservasi Gigi
Tahun 2015
Tiurma Sitompul
Efek Antibakteri Ekstrak Etanol Daun Afrika (Vernonia amygdalina) sebagai Bahan Alternatif Medikamen Saluran Akar terhadap Porphyromonas gingivalis (In Vitro)
xi + 61 halaman
Perawatan saluran akar memerlukan bahan medikamen untuk mengeliminasi
mikroorganisme yang tidak dapat dicapai dengan teknik preparasi chemo-mechanical. Salah satu bakteri yang sering ditemukan pada infeksi endodontik primer adalah
Porphyromonas gingivalis. Ca(OH2) merupakan bahan medikamen yang umum
digunakan selama ini, namun pada beberapa penelitian menemukan Ca(OH)2 kurang
efektif mengeliminasi Porphyromonas gingivalis. Daun Afrika (Vernonia amygdalina) merupakan salah satu bahan alami yang bersifat antibakteri yang dapat
dijadikan sebagai bahan alternatif medikamen saluran akar. Tujuan penelitian adalah
untuk mengetahui efek antibakteri ekstrak etanol daun Afrika terhadap bakteri
Porphyromonas gingivalis.
Penelitian ini dimulai dengan melakukan ekstraksi daun Afrika sebanyak 2 kg
dengan pelarut etanol 70% hingga diperoleh ekstrak kental. Pengujian efek
antibakteri menggunakan metode dilusi dengan mengencerkan ekstrak etanol daun
Afrika dalam media MHB dimulai dari konsentrasi 100%, 50%, 25%, 12,5%, 6,25%, dan 3,125% yang direplikasi 4 kali. Setiap konsentrasi ditambahkan 1 ml suspensi
bakteri, divorteks, dan diinkubasi 37°C selama 24 jam pada inkubator CO2.
Kekeruhan diamati dan dibandingkan dengan kontrol Mc Farland secara visual. Pada tabung dengan kekeruhan yang mulai tampak jernih merupakan nilai KHM. Setelah
penentuan KHM, dilanjutkan penghitungan jumlah koloni bakteri dengan metode
iv
Berdasarkan hasil penelitian dapat disimpulkan bahwa ekstrak etanol daun
Afrika memiliki efek antibakteri terhadap Porphyromonas gingivalis secara in vitro dengan nilai KBM pada konsentrasi 50% dan nilai KHM tidak representatif sehingga
tidak dapat diketahui hasilnya.
Kata kunci : Porphyromonas gingivalis, medikamen saluran akar, daun Afrika, antibakteri
EFEK ANTIBAKTERI EKSTRAK ETANOL DAUN AFRIKA
(Vernonia amygdalina) SEBAGAI BAHAN ALTERNATIF
MEDIKAMEN SALURAN AKAR TERHADAP
Porphyromonas gingivalis
(In Vitro)
SKRIPSI
Diajukan untuk memenuhi tugas dan melengkapi
syarat memperoleh gelar Sarjana Kedokteran Gigi
Oleh:
TIURMA SITOMPUL
NIM: 110600115
FAKULTAS KEDOKTERAN GIGI
UNIVERSITAS SUMATERA UTARA
iv
KATA PENGANTAR
Puji dan syukur kehadirat Tuhan Yang Maha Esa yang telah memberikan
rahmat dan karunia-Nya yang melimpah sehingga penulis dapat menyelesaikan
skripsi ini sebagai salah satu syarat untuk memperoleh gelar sarjana Kedokteran Gigi
di Universitas Sumatera Utara.
Penulis menyampaikan terimakasih yang sebesar-besarnya kepada orang tua
tercinta, Delimar Sitompul dan Ratna Butarbutar yang telah senantiasa memberikan
kasih sayang, doa, nasehat, motivasi dan dukungan yang tidak dapat terbalaskan.
Penulis tidak lupa juga mengucapkan terimakasih kepada adik-adik tercinta, Shanty,
Ricky, dan Joel serta seluruh keluarga penulis yang selalu memberikan doa,
dukungan dan masukan kepada penulis.
Selama pelaksanaan penelitian dan penulisan skripsi ini, penulis banyak
mendapatkan bantuan, pengarahan dan bimbingan dari berbagai pihak. Untuk itu,
pada kesempatan ini dengan segala kerendahan hati dan penghargaan yang tulus,
penulis ingin mengucapkan terimakasih kepada:
1. Prof. Nazruddin, drg., Sp. Ort, Ph.D selaku Dekan Fakultas Kedokteran
Gigi Universitas Sumatera Utara.
2. Cut Nurliza, drg., M.Kes selaku Ketua Departemen Ilmu Konservasi Gigi
Fakultas Kedokteran Gigi USU dan selaku dosen pembimbing pertama yang telah
meluangkan waktu dan tenaga untuk memberikan arahan, masukan, bimbingan,
penjelasan dan motivasi dalam proses penyusunan skripsi ini sampai dengan selesai.
3. Fitri Yunita Batubara, drg., MDSc selaku dosen pembimbing kedua yang
juga telah meluangkan banyak waktu, tenaga, pemikiran, kesabaran, dukungan dan
bimbingan kepada penulis sehingga skripsi ini dapat diselesaikan.
4. Seluruh staf pengajar dan pegawai FKG USU terutama Departemen Ilmu
Konservasi Gigi Fakultas Kedokteran Gigi USU yang telah membantu penulis
dengan memberikan arahan dan masukan dalam penyelesaian skripsi.
5. Prof. Sondang Pintauli, drg., Ph.D selaku Dosen Pembimbing Akademis
yang telah membimbing dan mengarahkan penulis selama menjalani pendidikan di
6. Drs. Awaluddin Saragih, M.Si., Apt. selaku kepala Laboratorium Obat
Tradisional Farmasi USU dan kepada staf laboratorium yang telah membimbing dan
membantu penulis dalam menjalani kegiatan laboratorium.
7. Wahyu Hidayatiningsih, S.Si, M.Kes selaku penguji dan staf laboran di
Laboratorium Pusat Penyakit Tropis di UNAIR yang telah membantu penulis dalam
kegiatan penelitian.
8. Maya Fitria, SKM, M.Kes yang telah meluangkan waktu dan membantu
penulis dalam konsultasi statistika.
9. Partner tersayang penulis, Sumindak Gultom yang selalu mendoakan,
memberi dukungan dan semangat kepada penulis hingga saat ini.
10. Sahabat-sahabat terbaik penulis yaitu Ellizabeth, Elsi, Rikha dan Yohana,
dan kelompok rohani yaitu kak Ruth, Bella, Mustika, serta teman-teman masa SMA
angkatan XIX yang selalu memberikan doa, semangat dan motivasi setiap saat
sehingga penulis dapat menyelesaikan skripsi ini.
11. Teman-teman seperjuangan skripsi, Hendy, Alvin, Mutiara, Inggrid, Yuki,
Adel, Deasy, Margareth, Dina, Fenny, Cyntia, Eldora, Ong, Hengyan, Ezzati, dan
Shamini serta teman-teman angkatan 2011 Fakultas Kedokteran Gigi USU lainnya,
yang telah banyak memberi dukungan dan bantuan kepada penulis selama pembuatan
skripsi.
Penulis menyadari bahwa dalam penulisan skripsi ini masih terdapat banyak
kekurangan, oleh karena itu penulis memohon maaf yang sebesar-besarnya apabila
terdapat kesalahan selama penyusunan skripsi ini. Dengan segala kerendahan hati,
penulis berharap semoga skripsi ini dapat memberikan sumbangan pikiran yang
berguna bagi fakultas, pengembangan ilmu dan bermanfaat bagi masyarakat.
Medan, 30 April 2015 Penulis,
Tiurma Sitompul
iv
2.2 Porphyromonas gingivalis sebagai Salah Satu Bakteri yang Ter- dapat pada Infeksi Endodontik Primer ... 9
2.4.2 Nilai Farmakologi Daun Afrika (Vernonia amygdalina) .. 21
2.4.3 Aktivitas Antibakteri Daun Afrika (Vernonia amygdalina) 22 2.5 Kerangka Teori ... 23
BAB 3 KERANGKA KONSEP DAN HIPOTESIS PENELITIAN ... 24
3.1 Kerangka Konsep... 24
3.2 Hipotesis Penelitian ... 24
BAB 4 METODOLOGI PENELITIAN... 25
4.1.1 Jenis Penelitian ... 25
4.1.2 Rancangan Penelitian... 25
4.2 Lokasi dan Waktu Penelitian ... 25
4.2.1 Lokasi Penelitian ... 25
4.2.2 Waktu Penelitian ... 25
4.3 Populasi, Sampel dan Besar Sampel Penelitian ... 25
4.3.1 Populasi Penelitian ... 25
4.3.2 Sampel Penelitian ... 25
4.3.3 Besar Sampel Penelitian ... 26
4.4 Variabel dan Definisi Operasional... 28
4.4.1 Variabel Penelitian... 28
4.5 Metode Penatalaksanaan Penelitian ... 32
DAFTAR TABEL
Tabel Halaman
1. Hasil Uji Efektivitas Antibakteri Ekstrak Daun Afrika (Vernonia amygdalina) dalam pelarut etanol 70% terhadap Porphyromonas
DAFTAR GAMBAR
Gambar Halaman
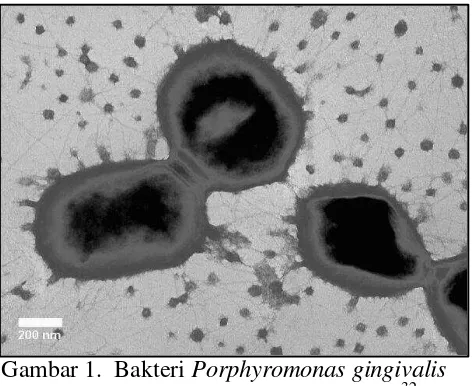
1. Bakteri Porphyromonas gingivalis dibawah electron micrograph ... 11
2. Prevalensi mikroorganisme yang terdeteksi pada gigi dengan infeksi endodontik primer disertai abses apikalis akut dengan metode Poly- merase Chain Reaction ... 15
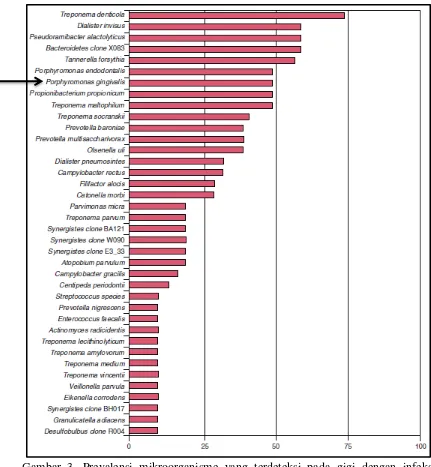
3. Prevalensi mikroorganisme yang terdeteksi pada infeksi saluran akar disertai periodontitis apikal akut dengan metode Polymerase Chain Reaction... 16
4. Daun Afrika (Vernonia amygdalina) ... 19
5. Bunga Vernonia amygdalina ... 19
6. Penimbangan daun Afrika 2 kg ... 35
7. Pengeringan daun Afrika ... 35
8. Daun Afrika yang sudah kering diblender ... 35
9. Simplisia daun Afrika ... 35
10. Proses destilasi etanol 96% ... 36
11. Pengenceran etanol 96% ... 36
12. Proses maserasi ... 36
13. Proses perkolasi ... 36
14. Ekstrak cair daun Afrika ... 36
15. Vacuum rotavapor ... 36
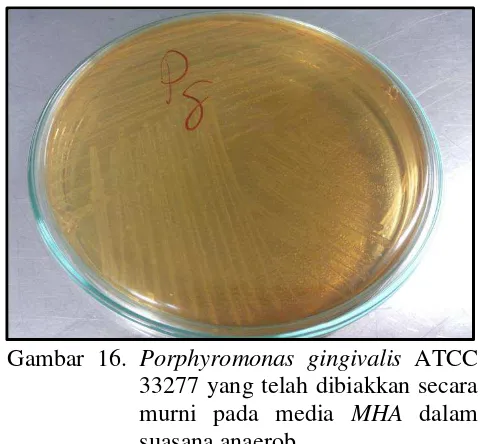
16. Porphyromonas gingivalis ATCC 33277 yang telah dibiakkan ... 38
17. Ekstrak kental daun Afrika... 41
18. Uji antibakteri ekstrak etanol daun Afrika dengan metode dilusi ... 42
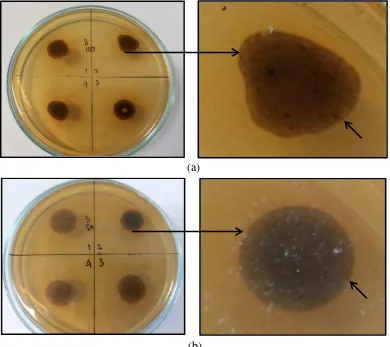
19. Pertumbuhan bakteri pada media MHA dengan konsentrasi 100% dan 50% ... 43
20. Pertumbuhan bakteri pada media MHA dengan konsentrasi 25% dan 12,5% ... 44
22. Pertumbuhan bakteri pada media MHA dengan konsentrasi 6,25%
dan 3,125% ... 46
DAFTAR LAMPIRAN
Lampiran Halaman
1. Skema Alur Pikir ... 62
2. Alur Penelitian ... 65
3. Sertifikat Hasil Uji ... 69
BAB 1
PENDAHULUAN
1.1Latar Belakang
Mikroorganisme memegang peranan sebagai agen etiologi utama dalam
penyakit pulpa dan jaringan periapikal.1 Sekitar 700 spesies bakteri mulut telah diidentifikasi dengan analisis urutan nukleotida subunit 16S rRNA dan kurang dari
50% dari spesies ini tidak bisa dan belum dapat diisolasi dari pulpa terinfeksi.2 Mayoritas bakteri yang diisolasi adalah bakteri obligat anaerob. Pada penelitian
pengkulturan bakteri dari gigi yang utuh dengan infeksi saluran akar ditemukan 91%
bakteri yang terlibat adalah bakteri obligat anaerob.2 Hal ini didukung oleh penelitian Baumgartner (1991) yang mengkultur apeks gigisepanjang 5 mm yang terkena karies
menemukan 67% bakteri obligat anaerob.2,3
Infeksi saluran akar memiliki sifat polimikroba yaitu dimana mikroorganisme
melekat satu sama lain atau pada dinding saluran akar yang membentuk interaksi
antar bakteri.2 Bakteri-bakteri ini tumbuh dan membentuk suatu kesatuan dalam komunitas yang terintegrasi secara metabolik yang disebut dengan biofilm.4 Bakteri dalam bentuk biofilm memiliki virulensi yang lebih tinggi dan cenderung mempunyai tantangan besar dalam mengeliminasi dari dinding saluran akar.2,4 Bakteri obligat anaerob merupakan yang mendominasi pada biofilm yang terbentuk pada infeksi endodontik primer.4,5
Porphyromonas gingivalis merupakan salah satu bakteri obligat anaerob berpigmen hitam gram negatif yang banyak ditemukan pada saluran akar yang
nekrosis.4-6 Berdasarkan penelitian Kipalev et al. (2014), bakteri Porphyromonas gingivalis yang paling sering terdeteksi dengan infeksi endodontik primer dengan menggunakan metode Polymerase Chain Reaction yaitu sebesar 54,2% dibandingkan
infeksi endodontik sekunder.7 Penelitian yang telah dilakukan oleh Tomazinho et al. (2007) juga melaporkan bahwa pada infeksi endodontik primer bakteri
diketahui memiliki faktor virulensi yang besar termasuk diantaranya fimbriae, haemagglutinin, capsule, outer membrane vesicles, powerful hydrolytic enzymes dan
lipopolysaccharide (LPS). Faktor virulensi ini memulai mekanisme pertahanan dengan menimbulkan kerusakan jaringan host.9
Bakteri Porphyromonas gingivalis mempunyai kemampuan untuk
berkolonisasi dengan bakteri lain membentuk microbial biofilm sehingga menimbulkan inflamasi dan lebih patogen.6 Penelitian membuktikan keberadaan
Porphyromonas gingivalis dihubungkan dengan bakteri lainnya pada inflamasi periapikal akan meningkatkan toksisitas dan risiko timbulnya simtom klinis serta
pembentukan abses.2 Pada penelitian Loo et al. (2009) menunjukkan bahwa terjadi infeksi silang antara bakteri Porphyromonas gingivalis dengan Bacteroides forsythus
pada saluran akar yang meningkatkan resiko periodontitis apikalis kronis.11 Selain itu, kombinasi Fusobacterium nucleatum, Prevotella spp., dan Porphyromonas spp. dapat memberikan faktor risiko untuk endodontik flare-up dengan bertindak secara sinergi sehingga meningkatkan intensitas reaksi inflamasi periapikal.11
Perawatan saluran akar merupakan perawatan yang bertujuan untuk
mengeliminasi bakteri beserta produknya dan menciptakan lingkungan dimana
mikroorganisme yang tersisa tidak dapat bertahan hidup. Hal ini menjadi dasar untuk
keberhasilan perawatan saluran akar.5,12 Untuk mengeliminasi bakteri sebanyak mungkin dari seluruh sistem saluran akar dilakukan kombinasi preparasi saluran akar
chemo-mechanical dengan larutan irigasi. Namun, beberapa studi telah menunjukkan bahwa preparasi saluran akar chemo-mechanical dengan irigasi antibakteri hanya akan memberikan 50-70% dari kanal yang terinfeksi bebas dari mikroorganisme.13
Pada penelitian Siquiera et al. (2007) melaporkan bahwa setelah preparasi
chemo-mechanical menggunakan sodium hipoklorit (NaOCl) 2.5% sebagai bahan irigasi menunjukkan sekitar 40-55% pada infeksi endodontik primer dengan lesi
periodontitis apikal masih menghasilkan kultur positif bakteri.12 Hal ini kemungkinan disebabkan karena anatomi pulpa yang kompleks sehingga beberapa mikroorganisme
dapat bermigrasi ke ramifikasi, isthmus, delta saluran akar, dan tubulus dentin setelah
akar.12,13 Adapun syarat dari bahan medikamen saluran akar harus memiliki aktivitas antibakteri, mengeliminasi bakteri saluran akar yang tidak tereliminasi pada proses
preparasi chemo-mechanical, mengurangi inflamasi periapikal, mengurangi rasa sakit pasca perawatan, mampu mencegah infeksi ulang dan bersifat biokompatibel.13,14
Medikamen saluran akar yang digunakan dalam perawatan saluran akar dibagi
atas beberapa kelompok besar yaitu golongan fenol, aldehida, halida, steroid, kalsium
hidroksida, antibiotik, dan kombinasi.14 Salah satu bahan medikamen saluran akar yang banyak digunakan dalam bidang kedokteran gigi sejak tahun 1920 hingga saat
ini adalah kalsium hidroksida (Ca(OH)2).12,15 Ca(OH)2 memiliki efek antimikroba,
dapat mempertahankan aktivitas antimikrobanya dalam waktu yang panjang,
menghidrolisis lipopolisakarida (LPS) dari bakteri gram negatif dan menghilangkan
kemampuan LPS untuk merangsang TNF yang diproduksi monosit darah perifer
sehingga mungkin mengurangi respon inflamasi lokal.13,15,16
Ca(OH)2 juga memiliki efek terhadap jaringan dimana penggunaannya
sebagai medikamen saluran memberikan efek yang kurang baik terhadap jaringan
periodontal. Blomlőf et al. (1988) mengamati hal tersebut disebabkan karena Ca(OH)2 memberikan pengaruh negatif terhadap proses penyembuhan jaringan lunak
dan menghambat proses perlekatan gingival fibroblast.17 Ca(OH)2 juga memberikan
efektivitas antibakteri yang lambat hingga memerlukan waktu minimal satu minggu
dan residu yang sulit dihilangkan.13 Penelitian Saunders juga menemukan bahwa
Ca(OH)2 kurang efektif mengeliminasi Porphyromonas gingivalis dan
Peptostreptococcus micros.3 Akibat dari kelemahan yang dimiliki oleh bahan medikamen tersebut, maka diperlukan pengembangan bahan alami sebagai bahan
alternatif medikamen saluran akar yang memenuhi syarat bahan medikamen saluran
akar.
Menurut WHO, tanaman herbal akan menjadi sumber terbaik untuk
menghasilkan berbagai jenis obat dan telah merekomendasikan penggunaan obat
herbal dalam pemeliharaan kesehatan masyarakat, pencegahan dan pengobatan
obat-obatan berbahan dasar alami.19 Salah satu tanaman herbal yang masih dalam penelitian adalah daun Afrika (Vernonia amygdalina).
Daun Afrika (Vernonia amygdalina) merupakan salah satu alternatif bahan alami yang dapat dikembangkan sebagai bahan medikamen saluran akar. Daun Afrika
yang biasa disebut bitter leaf di Inggris ini sering digunakan secara tradisional mengatasi demam, cegukan, penyakit ginjal diabetes, diare, antimalaria, antimikroba,
antivirus, analgesik, antifungal, antihelmintik, antikanker, antioksidan, dan
antidiabetes.20,21 Daun Afrika (Vernonia amygdalina) memiliki berbagai metabolit sekunder antara lain anthraquinones, tannins, flavonoids, alkaloids, saponins, cardiac glycosides, dan triterpenes.21,22 Oleh karena itu, aktivitas antimikroba dan antifungal yang kuat pada Vernonia amygdalina terjadi karena adanya kandungan bioaktif seperti alkaloid, saponin, tanin, flavonoid dan terpene.20-22
Beberapa penelitian eksperimental Vernonia amygdalina telah melaporkan bahwa tanaman ini memiliki aktivitas antibakteri dan antifungal.20 Hal ini didukung oleh penelitian bahwa ekstrak air batang dan kulit kayu Vernonia amygdalina
menunjukkan aktivitas bakterisida terhadap bakteri anaerob mulut seperti
B. gingivalis, B. asaccharolyticus, B. melaninogenicus, dan B. orali ≤ 10%.20 Ekstrak air dari akar Vernonia amygdalina juga menunjukkan aktivitas antibakteri pada
Steptococcus gordonii, Porphyromonas gingivalis, Porphyromonas nigrescens, Prevotella intermedia, Fusobacterium nucleatum, dan P. aeruginosa dengan kadar hambat minimum 100 mg/ml.21 Pada penelitian Vika (2014) menunjukkan efek antibakteri ekstrak etanol daun Afrika (Vernonia amygdalina) terhadap
Fusobacterium nucleatum dengan nilai konsentrasi bunuh minimum (KBM) sebesar 12,5%.23 Penelitian Jocelyn (2014) juga menunjukkan aktivitas antibakteri ekstrak etanol daun Afrika (Vernonia amygdalina) terhadap Enterococcus faecalis dengan nilai konsentrasi bunuh minimum sebesar 6,25%.24 Penelitian Ilondu et al. (2009) juga menunjukkan bahwa pada ekstrak air daun Afrika (Vernonia amygdalina)
dengan konsentrasi 50 %, 40%, 30%, 20%, 10% memiliki daya hambat terhadap
pertumbuhan jamur.25 Selain itu, penelitian Ibrahim et al. (2011) melakukan penelitian mengenai toksisitas dari ekstrak etanol daun Afrika terhadap tikus dan
Berdasarkan penelitian Ibrahim et al. juga menyimpulkan daun Afrika (Vernonia amygdalina) juga memiliki aktivitas analgesik yang dapat mengatasi sakit gigi, gingivitis, dan rematik.26
Dari uraian diatas, dapat diketahui bahwa daun Afrika (Vernonia amygdalina) dapat dijadikan sebagai bahan alternatif medikamen saluran akar karena memenuhi
beberapa syarat bahan medikamen saluran akar yaitu mempunyai aktivitas
anktibakteri, bersifat biokompatibel dan mengurangi rasa nyeri. Namun hingga saat
ini belum ditemukan penelitian mengenai efek antibakteri ekstrak etanol daun Afrika
(Vernonia amygdalina) terhadap bakteri saluran akar Porphyromonas gingivalis
sebagai salah satu bakteri yang ditemukan pada infeksi endodontik primer. Oleh
karena itu, perlu dilakukan pengujian efek antibakteri ekstrak etanol daun Afrika
(Vernonia amygdalina) terhadap bakteri saluran akar Porphyromonas gingivalis
sebagai alternatif bahan medikamen saluran akar. Penelitian ini menggunakan metode
dilusi untuk menentukan nilai KHM dan KBM yang mempresentasikan efek
antibakteri ekstrak etanol daun Afrika (Vernonia amygdalina) terhadap
Porphyromonas gingivalis. Kultur bakteri diinkubasi pada suhu 37oC selama 24 jam karena pada suhu dan waktu tersebut Porphyromonas gingivalis dapat tumbuh dengan optimal.
1.2 Rumusan Masalah
Berdasarkan uraian diatas, maka dirumuskan permasalahan sebagai berikut:
Apakah ada efek antibakteri ekstrak etanol daun Afrika (Vernonia amygdalina) sebagai bahan alternatif medikamen saluran akar terhadap bakteri
Porphyromonas gingivalis diukur dari nilai konsentrasi hambat minimum (KHM) dan konsentrasi bunuh minimum (KBM) ekstrak etanol daun Afrika (Vernonia amygdalina)?
1.3Tujuan Penelitian
Tujuan dari penelitian ini adalah untuk mengetahui efek antibakteri ekstrak
hambat minimum (KHM) dan konsentrasi bunuh minimum (KBM) ekstrak etanol
daun Afrika (Vernonia amygdalina).
1.4Manfaat Penelitian
1.4.1 Manfaat Teoritis
1. Sebagai dasar untuk penelitian lebih lanjut pengembangan ekstrak etanol
daun Afrika (Vernonia amygdalina) sebagai bahan alternatif untuk medikamen saluran akar.
2. Hasil penelitian diharapkan dapat digunakan sebagai studi/referensi
tambahan tentang bahan medikamen saluran akar dari ekstrak etanol daun Afrika
untuk digunakan dalam perawatan saluran akar bagi bidang ilmu kedokteran gigi
khususnya konservasi.
1.4.2 Manfaat Praktis
1. Menambah informasi dalam bidang kedokteran gigi mengenai efek
antibakteri dari ekstrak etanol daun Afrika (Vernonia amygdalina).
2. Meningkatkan pengembangan bahan kedokteran gigi yang berasal dari
alam, mempunyai sifat biokompatibel yang tinggi, mudah didapat dan harga yang
terjangkau.
3. Meningkatkan pelayanan kesehatan gigi pada masyarakat dengan
BAB 2
TINJAUAN PUSTAKA
Dasar keberhasilan perawatan saluran akar adalah mengeliminasi bakteri dan
produk-produknya. Ca(OH)2 merupakan bahan medikamen saluran akar yang umum
digunakan, namun pada penelitian menemukan bahwa Ca(OH)2 kurang efektif
mengeliminasi Porphyromonas gingivalis. Beberapa penelitian telah melakukan pengembangan bahan alami sebagai alternatif medikamen saluran akar yang telah
dilakukan. Untuk itu, ekstrak etanol daun Afrika diharapkan dapat dikembangkan
sebagai alternatif bahan medikamen saluran akar.
2.1 Bahan Medikamen dalam Perawatan Saluran Akar
Bahan medikamen saluran akar adalah suatu medikamen yang diletakkan
sementara pada saluran akar dengan biokompatibilitas yang baik. Tujuan utama
penggunaan bahan medikamen saluran akar yaitu untuk mengeliminasi bakteri yang
mungkin masih tersisa setelah dilakukannya instrumentasi mekanis maupun irigasi.12 Beberapa studi telah menunjukkan bahwa preparasi saluran akar chemo-mechanical
dengan irigasi antibakteri hanya akan memberikan 50-70% dari kanal yang terinfeksi
bebas dari mikroorganisme.12 Hal ini dapat disebabkan beberapa mikroorganisme dapat bermigrasi ke ramifikasi, isthmus, delta saluran akar, dan tubulus dentin
meskipun sudah dilakukan preparasi chemo-mechanical sehingga perlu dieliminasi dengan medikamen saluran akar.12,13 Oleh karena itu, perawatan saluran akar memerlukan bahan medikamen untuk meningkatkan keberhasilan perawatan.12-14
Syarat dari bahan medikamen saluran akar adalah harus memiliki aktivitas
antibakteri, mengeliminasi bakteri saluran akar yang tidak tereliminasi pada proses
preparasi chemo-mechanical, mengurangi inflamasi periapikal, mengurangi rasa sakit
pasca perawatan, mampu mencegah infeksi ulang dan bersifat biokompatibel.12,13 Selain itu medikamen juga digunakan untuk mengeliminasi eksudat pada daerah
dibagi dalam beberapa kelompok besar yaitu golongan fenol (Eugenol, CMCP,
Parachlorophenol, Camphorated Parachlorophenol, Metakresilasetat, Kresol, Creosote, Timol), golongan aldehid/formaldehida (formokresol dan glutaraldehid), golongan halida (natrium hipoklorit dan iodine-kalium iodida), kalsium hidroksida,
antiobiotik, steroid dan kombinasi. Namun yang paling populer sering digunakan
adalah Ca(OH)2, CMCP, dan formokresol.12,14
Bahan medikamen golongan fenol merupakan bahan kristalin putih
mempunyai bau khas batubara. Fenol adalah racun protoplasma dan menyebabkan
nekrosis jaringan lunak. Selain itu, golongan fenol juga memiliki potensi mutagenik
dan kariogenik dan jika berkontak dengan cairan membuatnya menjadi tidak aktif.
Penggunaan bahan medikamen saluran akar golongan fenol sudah tidak dianjurkan
lagi.14 Bahan medikamen formokresol merupakan suatu medikamen bakterisidal yang tidak spesifik dan sangat efektif terhadap organisme aerobik dan anaerobik yang
ditemukan dalam saluran akar.14 Antibiotik yang paling umum yaitu pasta Ledermix dan Septomixine Forte. Keduanya sama-sama mengandung kortikosteroid sebagai
agen antiinflamasi, namun belum sesuai untuk digunakan pada perawatan saluran
akar karena spektrum kerja kedua jenis antibiotik tersebut kurang luas dan hanya
fokus pada inflamasi.12,14
Ca(OH)2 telah digunakan secara luas di bidang endodontik dan dikenal
sebagai bahan desinfeksi saluran akar yang paling efektif.13,14 Ca(OH)2 pertama kali
diperkenalkan pada tahun 1920 oleh Herman dan sejak itu penggunaannya dalam
perawatan endodontik telah meningkat terutama untuk digunakan sebagai bahan
medikamen saluran akar dan menjadi gold standard dalam perawatan saluran akar.15,16 Ca(OH)2 memberikan efek antibakteri melalui pH yang tinggi yang dapat
mencapai 12,5 yang menyebabkan rusaknya dinding sel bakteri sehingga terjadi
proses denaturasi protein yang menghambat replika DNA dari bakteri dan
menyebabkan terhambatnya pertumbuhan bakteri.3,17 Cara kerja Ca(OH)2 melalui
pelepasan ion Ca2+ yang memiliki peran dalam proses mineralisasi jaringan dan ion OH- yang menghasilkan alkalin yang tinggi sehingga menyebabkan lingkungan yang tidak sesuai bagi mikroorganisme. Ca(OH)2 juga dapat menghambat resorpsi tulang
menghidrolisis LPS dengan menghasilkan asam lemak hidroksi dalam jumlah yang
banyak dan menonaktifkan enzim dalam membran bakteri serta mengganggu
mekanisme transportasi yang mengakibatkan sel keracunan.27
Selain memiliki keunggulan, Ca(OH)2 juga memiliki kelemahan. Penelitian
klinis menunjukkan bahwa pemakaian rutin medikamen ini sebagai medikamen
saluran akar tidak berpengaruh pada pencegahan atau pengurangan rasa sakit.12 Ca(OH)2 merupakan antimikroba yang bekerja lambat dan diperlukan dalam jumlah
yang cukup banyak serta memerlukan waktu minimal satu minggu untuk efektif.27 Kelemahan lainnya adalah sisa residunya sulit dihilangkan dari dinding saluran akar
sehingga akan mengurangi setting time sealer yang berbasis zinc oxide yang digunakan pada pengisian saluran akar.13 Blomlőf et al. (1998) menemukan penggunaan Ca(OH)2 sebagai medikamen saluran akar pada pasien yang juga
melakukan perawatan periodontal memiliki efek yang kurang baik pada jaringan
periodontal. Hal ini disebabkan karena Ca(OH)2 memberikan pengaruh negatif dalam
proses penyembuhan jaringan lunak dan terlihat Ca(OH)2 dapat menghambat proses
perlekatan gingiva fibroblas walaupun tidak secara signifikan.17
2.2 Porphyromonas gingivalis sebagai Salah Satu Bakteri yang Terdapat pada Infeksi Endodontik Primer
Pada saluran akar yang terinfeksi terdapat kumpulan berbagai jenis komunitas
bakteri sehingga disebut sebagai infeksi polimikrobial. Mikroorganisme menginvasi
saluran akar berupa sel tunggal (bentuk planktonik) yang tersebar bebas dalam cairan
pada saluran akar atau melekat satu sama lain atau ke akar dinding saluran atau
keduanya.4,11 Namun yang menjadi faktor penting dalam beberapa tahun terakhir adalah bahwa bakteri dalam saluran akar dapat tumbuh tidak hanya sebagai sel
planktonik atau beragregasi, berkoagregasi, tetapi dapat juga membentuk biofilm
yang terdiri dari jaringan kompleks mikroorganisme yang berbeda. Biofilm
didefinisikan sebagai sebuah lapisan tipis dari komunitas mikroorganisme
multiseluler yang terkondensasi dan melekat secara kuat pada permukaan dan
terperangkap dalam matriks extracellular polymeric substance (EPS) yang terdiri dari
Komunitas biofilm adalah struktur kompleks dan dinamis yang berkumpul melalui kolonisasi beberapa bakteri rongga mulut yang berurutan dan teratur.2,28
Pembentukan biofilm pada infeksi saluran akar diawali beberapa saat setelah terjadinya invasi pada ruang pulpa oleh bakteri planktonik akibat kerusakan jaringan.
Lesi inflamasi yang terus berkembang ini akan menyediakan cairan bagi organisme
planktonik yang menginvasi sehingga mereka dapat bereplikasi dan terus melekat
pada dinding saluran akar. Jaringan nekrotik pulpa menjadi lingkungan yang
menguntungkan bagi proliferasi mikrobial karena adanya residu organik atau nutrisi
yang berperan sebagai substrat atau medium kultur.28
Bakteri yang berada di biofilm dapat berkomunikasi, bertukaran bahan genetik dan juga memperoleh sifat-sifat baru. Komunikasi dalam biofilm terdiri dari dua jenis yaitu komunikasi intraspesies dan komunikasi antar spesies. Quorum sensing adalah komunikasi intraspesies bakteri yang dimediasi oleh molekuler rendah yang berat,
yang dapat mengubah aktivitas metabolisme sel-sel tetangga dan mengkoordinasikan
fungsi sel bakteri yang terdapat dalam biofilm. Quorum sensing juga dapat mengatur properti mikroba seperti faktor virulensi dan penggabungan DNA ekstraseluler.12,28
Pada infeksi endodontik primer, bakteri yang paling banyak diisolasi adalah
obligat anaerob, salah satunya adalah bakteri Porphyromonas gingivalis.2,5,12 Bakteri
Porphyromonas gingivalis yang merupakan golongan Porphyromonas sp., juga merupakan salah satu bakteri yang dapat dijumpai pada biofilm yang terbentuk pada infeksi saluran akar.2 Berdasarkan taksonominya, bakteri Porphyromonas gingivalis
diklasifikasikan sebagai berikut:9
Kingdom : Eubaceria
Filum : Bacteroidates
Classes : Bacteroides
Ordo : Bacteroidales
Famili : Porphyromonadaceae
Genus : Porphyromonas
Spesies : Porphyromonas gingivalis
sel berbentuk batang, berukuran kecil antara 0,5-2 μm, asaccharolytic, pleomorfik, dan berbentuk coccobacilli.2,9,31 Bakteri golongan Porphyromonas sp. memiliki karakteristik khusus yang memancarkan warna merah bata ketika berada di bawah
sinar ultraviolet gelombang panjang dan bewarna coklat hitam ketika dikultur pada
blood-containing media, sehingga bakteri ini juga dapat diidentifikasi sebagai bakteri berpigmen hitam Bacteroides.9,31
Porphyromonas gingivalis tumbuh dalam media kultur membentuk koloni berdiameter 1-2 mm, konveks, halus dan mengkilat, yang bagian tengahnya
menunjukkan gambaran lebih gelap karena memproduksi protoheme, yaitu suatu
substansi yang bertanggung jawab terhadap warna khas koloni ini. Pertumbuhannya
dipengaruhi oleh adanya protein hydrolysates, seperti peptone atau yeast extract. Produk fermentasi Porphyromonas gingivalis yang utama adalah n-butirat dan asam asetat sedangkan sedangkan produk minornya terdiri dari propionic, isobutyric, isovaleric, dan phenilacetic acids.33
2.2.1 Faktor Virulensi Bakteri Porphyromonas gingivalis
Porphyromonas gingivalis memiliki berbagai faktor virulensi yang patogenik
yang berperan dalam menyebabkan penyakit. Faktor virulensi tersebut antara lain
adalah fimbriae, capsule, outer membrane vesicles, hemagglutinin,
lipopolysaccharides (LPS), enzyme activity dan protein antigens. Faktor virulensi tersebut dapat menginisiasi mekanisme pertahanan host yang menyebabkan
kerusakan jaringan. Di antara faktor-faktor ini, LPS adalah faktor yang umumnya
dianggap sebagai faktor virulensi penting dalam bakteri gram negatif.9,15,34
Fimbriae bakteri memiliki peranan penting dalam interaksi bakteri dan sel
host. Fimbriae Porphyromonas gingivalis merupakan komponen filamen pada struktur permukaan sel dengan diameter 5 nm hingga 10 nm.9,11 Fimbriae
Porphyromonas gingivalis memiliki variasi aktivitas biologi termasuk imunogenitas, perlekatan pada berbagai protein host, menstimulasi sitokin dan merangsang terjadinya resopsi tulang. Fimbriaenya juga memiliki perlekatan yang sangat kuat
pada sel host dan memiliki potensi yang besar menjadi virulensi dengan berinteraksi
dengan bakteri lain.11
Kapsul bakteri telah dianggap faktor virulensi utama pada permukaan sel
bakteri.29 Semua bakteri yang termasuk golongan Bacteroides yang salah satunya
Porphyromonas gingivalis memiliki kapsul yang tersusun dari polisakarida pada membran luar sel. Kapsulnya terlibat dalam adhesi atau perlekatan, pembentukan
abses dan melindungi dari proses opsonisasi dan fagositosis sel host. Bakteri yang terselubung dalam kapsul seperti Bacteroides, Fusobacterium, fakultatif kokus gram positif biasanya menyebabkan abses, sedangkan bakteri yang tidak terselubung dalam
kapsul tidak menyebabkan abses.9,34
Lipopolysacharide (LPS) yang juga disebut endotoksin, merupakan komponen yang tidak terpisahkan dari dinding sel bakteri gram negatif.11 Patogenitas yang utama dari bakteri gram negatif disebabkan oleh adanya LPS pada dinding
selnya. LPS adalah komponen utama dari bakteri gram negatif yang tersusun dari
polysaccharide, core polysaccharide dan Lipid A.9,30 LPS memiliki potensi yang kuat sebagai stimulator inflamasi karena LPS mampu menembus ke dalam jaringan
periradikuler dan bertindak sebagai endotoksin dalam organisme host sehingga menyebabkan peradangan dan berlanjut dengan terjadinya kerusakan tulang.
Penelitian menunjukkan bahwa respon radang dimulai saat LPS Porphyromonas gingivalis berikatan dengan lipopolysacharide binding protein (LBP) membentuk
molekul CD14. Molekul ini akan dikenali oleh makrofag melalui reseptor TLR4
Enzim cysteine protease yang dihasilkan Porphyromonas gingivalis yang dinamakan gingipain menjadi salah satu faktor virulensi penting.30 Gingipain
memiliki kemampuan untuk mendegradasi protein pertahanan host untuk menyediakan peptida dan asam amino sebagai sumber karbon dan nitrogen bagi
pertumbuhan bakteri tersebut. Gingipain ini juga berperan dalam 85% aktivitas proteolitik yang dihasilkan oleh bakteri Porphyromonas gingivalis. Gingipain ini sendiri terdiri atas Arg-gingipain (Rgp) dan Lys-gingipain (Kgp).34 Collagenase
merupakan faktor virulensi Porphyromonas gingivalis yang berhubungan dengan penyakit periodontal. Penelitian menyatakan keberadaan collagenase gene (prtC)
yang diperiksa pada 21 strain spesies Porphyromonas dapat diisolasi pada infeksi saluran akar. Porphyromonas gingivalis dari infeksi saluran akar memiliki prtC gen, sedangkan Porphyromonas endodontalis tidak memiliki prtC gen.34
Kemampuan untuk menyerang sel dan jaringan host merupakan faktor virulensi penting dalam bakteri. Masuknya Porphyromonas gingivalis ke sel epitel gingiva prevalensinya sangat tinggi dan cepat, dan bakteri ini berkumpul pada daerah
perinuklear sel. Porphyromonas gingivalis berada di dalam sel selama lebih dari 24 jam dan menghasilkan aktin sitoskeleton bersamaan dengan perubahan ukuran dan
bentuk sel host. Mikroorganisme yang terdapat pada saluran akar yang terinfeksi dapat menyebabkan fokal infeksi pada penyakit kardiovaskuler. Hal ini dibuktikan
dengan kultur primer sel kardiovaskuler.34
Saluran akar yang terinfeksi merupakan infeksi polimikrobial yang
menyebabkan risiko terjadinya virulensi semakin tinggi bila terdapat kombinasi
mikroorganisme dalam jumlah yang besar terutama dari spesies bakteri gram negatif.
Kombinasi Porphyromonas gingivalis dengan Fusobacterium nucleatum dan bakteri berpigmen hitam Prevotella intermedia juga menunjukkan virulensi yang lebih tinggi dan memiliki risiko terjadinya flare up endodonti. Hal ini disebabkan adanya sinergi pada infeksi saluran akar antara bakteri tersebut, sehingga meningkatkan intensitas
terjadinya inflamasi pada jaringan periapikal.11 Selain itu, pada penelitian Loo et al. (2009) juga menunjukkan bahwa terjadi infeksi silang antara bakteri
Bakteri Porphyromonas gingivalis merupakan salah satu bakteri “red complex” (Bacteroides forsythus, Porphyromonas gingivalis dan Treponema denticola) yang paling proteolitik dan patogen dalam golongannya serta bakteri yang paling sering ditemukan pada infeksi endodontik primer.2,6,29 Namun, pada infeksi sekunder bakteri ini masih dapat ditemukan walaupun dalam jumlah yang sedikit. Hal
ini sesuai dengan hasil penelitian Ercan et al. (2006) yaitu bahwa bakteri
Porphyromonas spp. ditemukan memiliki prevalensi yang lebih rendah pada saluran akar dengan infeksi endodontik sekunder dibandingkan infeksi endodontik primer.35
Berdasarkan penelitian Kipalev et al. (2014) melaporkan bahwa bakteri
Porphyromonas gingivalis yang paling sering terdeteksi pada infeksi saluran akar
primer dengan menggunakan metode PCR. Persentase bakteri Porphyromonas gingivalis pada infeksi saluran akar primer sebesar 54,2%.7 Penelitian Tomazinho et al. (2007) juga melaporkan bahwa pada infeksi endodontik primer bakteri
Porphyromonas gingivalis memiliki prevalensi sebesar 27,3% dengan metode kultur dan 43,3% dengan metode Polymerase Chain Reaction.8 Penelitian Saito et al. (2009) mendeteksi bakteri Porphyromonas gingivalis sebesar 28% pada infeksi endodontik primer dengan metode Polymerase Chain Reaction.30 Hal ini didukung juga dari penelitian pada infeksi endodontik primer disertai abses apikal akut yang
menggunakan metode PCR menemukan prevalensi sekitar 55% dari jumlah sampel
dan pada infeksi endodontik primer disertai periodontitis apikal akut menggunakan
metode PCR dengan prevalensi sekitar 48% dari jumlah sampel.36
Pada infeksi endodontik primer maupun sekunder, bakteri Porphyromonas gingivalis diketahui sering ditemukan dengan bakteri Porphyromonas endodontalis.
Namun, prevalensi bakteri Porphyromonas gingivalis lebih tinggi ditemukan dibandingkan bakteri Porphyromonas endodontalis. Penelitian Kipalev et al. (2014) menemukan prevalensi Porphyromonas endodontalis 48,6%7 pada infeksi endodontik primer dan penelitian Tomazinho et al. (2007) menemukan prevalensi sebesar 43,3%
2.3 Penggunaan Bahan Alami dalam Bidang Endodontik
Produk herbal telah digunakan sejak dahulu sebagai obat secara tradisi di
masyarakat Timur dan Barat. Banyak tanaman dengan sifat biologis dan antimikroba
diteliti sejak ribuan tahun lalu dalam kedokteran gigi yang digunakan sebagai
anti-inflamasi, antibiotik, analgesik dan agen obat penenang. Akibat sering terjadinya
medikamen saluran akar untuk mengeliminasi bakteri di tubulus dentin, maka dalam
bidang endodontik mulai dikembangkan beberapa bahan medikamen yang berasal
dari komponen biologis tanaman herbal.37
Beberapa penelitian telah dilakukan di Indonesia mengenai penggunaan bahan
alami dalam bidang endodontik. Penelitian yang dilakukan Kawilang dkk. (2014)
menyimpulkan bahwa ekstrak kulit manggis memiliki aktivitas antibakteri terhadap
biofilm Porphyromonas gingivalis dengan nilai KHM dan KBM yang diperoleh adalah 25% dan 50%.38 Penelitian yang dilakukan Vivi Leontara dan Nevi Yanti (2014) menunjukkan bahwa ekstrak lerak mempunyai antibakteri terhadap
Porphyromonas gingivalis dengan diperolehnya nilai KBM pada konsentrasi 25%.39 Penelitian Sarah Amalia (2012) juga menunjukkan bahwa ekstrak pegagan memiliki
daya antibakteri terhadap bakteri Porphyromonas gingivalis dengan diperolehnya nilai KBM sebesar 25% sehingga ekstrak pegagan dapat dikembangkan sebagai
bahan alternatif medikamen saluran akar.40
2.4 Daun Afrika (Vernonia amygdalina)
Vernonia amygdalina adalah tanaman tropis yang termasuk dalam genus
Vernonia dan digunakan secara luas sebagai sayuran dan tanaman obat.20 Genus
Vernonia memiliki sekitar 1000 spesies dan lebih dari 500 tanaman Vernonia ini dapat ditemukan di Afrika dan Asia, sekitar 300 di Meksiko, dan sekitar 16
ditemukan di Amerika Serikat.20,21 Penelitian yang telah dilakukan ditemukan sebanyak 109 spesies Vernonia menunjukkan adanya kandungan sebagai medikamen. Seratus lima dari spesies tersebut dihubungkan kepada perawatan atau manajemen
dari 44 penyakit atau kondisi kesehatan manusia, sementara dua spesies digunakan
sebagai medikasi pada simpanse dan gorila. Penelitian secara in vitro dan in vivo
melaporkan validasi adanya kandungan medikasi dari beberapa spesies. Seratus tiga
senyawa bioaktif juga diisolasi dari berbagai spesies Vernonia dan Vernonia amygdalina diidentifikasi yang paling sering digunakan dari genus Vernonia.21
Vernonia amygdalina atau Gymnanthemum amygdalinum yang secara umum
berdiameter sekitar 6 mm (Gambar 4).20,21 Vernonia amygdalina memiliki daun berwarna hijau gelap dengan bau yang khas dan rasanya yang pahit. Tanaman ini
tidak menghasilkan benih sehingga untuk memperbanyak tanaman tersebut dapat
dilakukan dengan cara stek batang. Selain itu beberapa penelitian menemukan bahwa
Vernonia amygdalina juga memiliki bunga yang akan tumbuh pada lingkungan tertentu, berwarna putih, harum dan menarik kedatangan lebah (Gambar 5).20,21
Berdasarkan taksonominya Vernonia amygdalina diklasifikasikan sebagai berikut:21
Synonym : Gymnanthemum amygdalinum
Kingdom : Plantae
Division : Angiosperma
Classes : Dicotyledons
Order : Asterales
Family : Compositae
Genus : Vernonia
Species : V. amygdalina
Botanical Name : Vernonia amygdalina
Vernonia amygdalina memiliki sebutan yang berbeda oleh setiap suku di seluruh dunia. Di Indonesia dikenal dengan sebutan daun Afrika, di Inggris disebut
bitter leaf, di Malaysia disebut South Africa leaf, dan dalam bahasa lokal bangsa Nigeria disebut sebagai ewuro (Yoruba), etidot (Efik), uzi (Ebira), shikawa (Hausa), dan onugbu (Igbo). Di tempat lain di Afrika disebut muop atau ndole (Cameroon),
tuntwono (Tanzania), dan mululuza (Uganda) sedangkan beberapa negara lain disebut
Chrysanthemum tonsils (China), Olulusia dan South Africa leaf (Kenya), Buzut
(Ethiopia), Musikavakadzi (Zimababwe), Umubilizi (Rwanda), dan liNyatselo
Vernonia amygdalina tumbuh di daerah ekologi di Afrika termasuk Zimbabwe dan Nigeria yang beriklim tropis dan dapat tumbuh secara liar ataupun
ditanam di sepanjang Sub-saharan Afrika.41,42 Di Nigeria, Ghana dan Kamerun tanaman ini ditanam di kebun dan di sekitar perumahan untuk persediaan dan sebagai
tanaman pagar dan pot.42 Daun Vernonia amygdalina juga dapat dijadikan sebagai sayuran dan dikonsumsi setelah melalui proses penghilangan rasa pahit melalui
perendaman atau perebusan untuk menghilangkan komponen astringent yang terkandung di dalamnya.20,42
Gambar 4. Daun Afrika (Vernonia amygdalina)20
2.4.1 Senyawa Fitokimia Daun Afrika (Vernonia amygdalina) sebagai Antibakteri
Berdasarkan penelitian Asaolu et al. (2010) melaporkan analisis fitokimia daun Afrika (Vernonia amygdalina) adalah anthraquinones (0.08 ± 0.001), tannins
(1.55 ± 0.81), flavonoids (0.17 ± 0.004), alkaloids (2.95 ± 0.40), saponins (2.85 ± 0.39), cardiac glycosides (1.10 ± 0.03), dan triterpenes (0.54 ± 0.02). Luteolin, luteolin 7-0-beta-glukuronoside, dan luteolin 7-0-beta glukoside yang merupakan 3 jenis dari flavonoid yang juga terdapat pada daun Afrika (Vernonia amygdalina) memiliki aktivitas antioksidan dan berguna untuk mencegah kanker, serta dapat
melindungi dari diabetes dan arterosklerosis. Selain itu, ditemukan pula kandungan
antioksidan vitamin C yang tinggi pada Vernonia amygdalina.20,21 Kandungan bioaktif alkaloids, saponins, tannin, flavonoids dan terpenoids sebagai metabolit sekunder dari ekstrak daun Afrika (Vernonia amygdalina) memiliki peran sebagai antibakteri dengan mekanisme yang berbeda sebagai berikut:
a. Saponins merupakan zat yang mempunyai sifat seperti sabun yang dapat melarutkan kotoran. Secara kimia, saponin adalah glikosida berat molekul tinggi
dimana bagian triterpen atau steroid aglycone terikat dengan gula. Senyawa saponin dapat bekerja sebagai antibakteri adalah dengan membentuk senyawa kompleks
dengan membran sel bakteri melalui ikatan hidrogen yang kemudian dapat
menghancurkan permeabilitas dinding sel bakteri yang mengakibatkan kematian sel.43 b. Flavonoids adalah senyawa fenolik yang mengandung satu gugus karbonil dengan mekanisme kerja sebagai antibakteri adalah dengan membentuk senyawa
kompleks dengan protein ekstraseluler dan protein yang terlarut sehingga dapat
merusak dinding sel bakteri serta bersifat lipofilik yang dapat merusak lapisan lipid
pada membran bakteri.43
c. Alkaloids adalah senyawa nitrogen heterosiklik yang sudah digunakan berabad-abad dalam bidang medis karena dapat melawan sel asing melalui ikatan
dengan DNA sel sehingga mengganggu fungsi sel.43
d. Terpenes atau terpenoids aktif terhadap bakteri, jamur, virus, dan protozoa. Mekanisme kerja dari terpenoid tidak sepenuhnya dimengerti tetapi diduga
e. Tannins adalah senyawa fenolik polimer yang larut dalam air, gliserol, metanol, hidroalkoholik, dan propilena glikol, tetapi tidak dapat larut dalam benzene,
kloroform, eter, pretoleum eter, dan karbon disulfida. Tannin mempunyai rasa sepat
dan juga bersifat sebagai antibakteri dan astringent (bersifat menciutkan). Mekanisme penghambatan bakteri pada tannin adalah dengan cara bereaksi dengan membran sel,
inaktivasi enzim-enzim esensial dan destruksi fungsi material.43
f. Anthraquinones merupakan senyawa fenol yang bekerja sebagai antibakteri mirip dengan sifat-sifat fenol lainnya, yaitu menghambat bakteri dengan cara
mendenaturasi protein.43
2.4.2 Nilai Farmakologi Daun Afrika (Vernonia amygdalina)
Penggunaan Vernonia amygdalina sebagai tanaman obat dimulai ketika farmasi kebun binatang memberikan batang Vernonia amygdalina pada simpanse yang sakit. Berdasarkan laporan tersebut, banyak peneliti yang melakukan penelitian
ilmiah tentang manfaat medis ekstrak yang berbeda dari tanaman ini.20 Daun Afrika (Vernonia amygdalina) memiliki aktivitas biologis yaitu sebagai antibakteri, antijamur, antivirus, antiinflamasi, analgesik, antioksidan, antimalaria, antidiabetes,
dan antikanker. Ekstrak akar tanaman Vernonia amygdalina juga dapat digunakan untuk mengobati malaria dan penyakit saluran pencernaan. Tanaman Vernonia amygdalina juga dapat digunakan sebagai chewing stick dan digunakan secara tradisional untuk menjaga kesehatan mulut dengan dengan berkontribusi terhadap
penyembuhan gingiva, menyingkirkan mikroorganisme kariogenik, menghambat
pembentukan plak, dan berefek mengurangi karies gigi. 20
Berdasarkan laporan Aregheore et al. (1998) dan Igile et al. (1995) bahwa terdapat kandungan fitokimia yang mempunyai toksin dan menunjukkan terjadinya
hepatotoksisitas pada tikus.44 Namun, Ojiako dan Nwanjo (2006) melaporkan bahwa daun Afrika (Vernonia amygdalina) mungkin beracun (seperti beberapa sayuran
lainnya) jika dikonsumsi dalam jumlah yang sangat besar, tetapi bahaya yang
ditimbulkan tidak lebih parah dibandingkan sayuran umum lainnya yang rutin
bahkan menjadi lebih terorganisir dengan baik pada hewan yang diteliti dibandingkan
hewan kontrol.44
2.4.3 Aktivitas Antibakteri Daun Afrika (Vernonia amygdalina)
Banyak penelitian eksperimental Vernonia amygdalina telah melaporkan bahwa tanaman ini memiliki aktivitas antibakteri. Setiap bagian dari Vernonia amygdalina memiliki aktivitas antibakteri. Di Nigeria, batang dan akar Vernonia amygdalina digunakan sebagai chewing stick. Hasil penelitian menunjukkan bahwa ekstrak dari batang dan akar Vernonia amygdalina yang digunakan sebagai chewing stick menunjukkan aktivitas antibakteri terhadap bakteri anaerob rongga mulut seperti
Bacteroides gingivalis, Bacteroides asaccharolyticus, Bacteroides melaninogenicus,
dan Bacteroides Oralis pada konsentasi KHM 100 mg/ml.20 Penelitian Taiwo et al (1999), ekstrak air dari akar Vernonia amygdalina juga menunjukkan aktivitas antibakteri terhadap bakteri Streptococcus gordoni, Porphyromonas nigrescens, Porphyromonas gingivalis, Provotella intermedia, Fusobacterium nucleatum, dan
Pseudomanas aeruginosa dengan KHM 100 mg/ml.20
Aktivitas antibakteri dari ekstrak daun Vernonia amygdalina secara signifikan lebih tinggi dibandingkan ekstrak batang dan akar Vernonia amygdalina. Pada penelitian Oboh dan Masodje (2009) menunjukkan bahwa ekstrak air daun Afrika
(Vernonia amygdalina) dapat menghambat pertumbuhan Staphylococcus aureus dan
2.5 Kerangka Teori
Ekstrak etanol daun Afrika (Vernonia amygdalina)
BAB 3
KERANGKA KONSEP DAN HIPOTESIS PENELITIAN
3.1 Kerangka Konsep
Penelitian ini dilakukan dengan menguji efek antibakteri ekstrak etanol daun
Afrika (Vernonia amygdalina) sebagai bahan alternatif medikamen saluran akar terhadap bakteri Porphyromonas gingivalis dengan penentuan nilai Kadar Hambat Minimum (KHM) dan nilai Kadar Bunuh Minimum (KBM).
3.2 Hipotesis Penelitian
Ada efek antibakteri ekstrak etanol daun Afrika (Vernonia amygdalina) sebagai bahan alternatif medikamen saluran akar terhadap bakteri Porphyromonas gingivalis dengan mencari konsentrasi hambat minimum (KHM) dan konsentrasi bunuh minimum (KBM).
Ekstrak etanol daun Afrika
(Vernonia amygdalina) dengan konsentrasi 100%, 50%, 25%,
12,5%, 6,25% dan 3,125%.
Pertumbuhan bakteri Porphyromonas gingivalis pada media MHB dan
MHA dengan penentuan nilai KHM dan KBM
BAB 4
METODE PENELITIAN
4.1 Rancangan Penelitian
4.1.1 Jenis Penelitian
Jenis penelitian yang digunakan dalam penelitian ini adalah eksperimental
laboratorium.
4.1.2 Rancangan Penelitian
Rancangan penelitian yang digunakan dalam penelitian ini adalah posttest only control group design.
4.2 Lokasi dan Waktu Penelitian
4.2.1 Lokasi Penelitian
Lokasi penelitian yang digunakan pada penelitian ini adalah:
1. Laboratorium Obat Tradisional Fakultas Farmasi USU
2. Laboratorium Rumah Sakit Khusus Infeksi UNAIR
4.2.2 Waktu Penelitian
Waktu penelitian adalah 3 bulan (Januari 2015-Maret 2015)
4.3 Populasi, Sampel dan Besar Sampel
4.3.1 Populasi
Populasi dalam penelitian ini adalah bakteri Porphyromonas gingivalis.
4.3.2 Sampel
Sampel yang digunakan dalam penelitian ini adalah koloni bakteri
Keterangan:
t = jumlah perlakuan dalam penelitian r = jumlah perlakuan ulang (sampel)
4.3.3 Besar Sampel Penelitian
Penentuan besar sampel sesuai dengan SOP (Standard Operational Prosedur)
yang ada di Laboratorium Rumah Sakit Khusus Infeksi, Universitas Airlangga, yaitu
dengan menggunakan rumus:
(t-1) (r-1) ≥ 15
(t-1) (r-1) ≥ 15
(6-1) (r-1) ≥ 15 5r –5 ≥ 15
5r ≥ 20
r ≥ 4
Jumlah perlakuan ulang (r) yang dapat digunakan dalam penelitian ini adalah 4 kali
pengulangan.
Adapun penentuan besar sampel dilakukan sebagai berikut:
a. Penentuan nilai Kadar Hambat Minimum (KHM)
Bahan coba dibagi ke dalam 6 kelompok dengan 2 kontrol, yaitu:
Kelompok 1 : ekstrak etanol daun Afrika 100% = 4 sampel
Kelompok 2 : ekstrak etanol daun Afrika 50% = 4 sampel
Kelompok 3 : ekstrak etanol daun Afrika 25% = 4 sampel
Kelompok 4 : ekstrak etanol daun Afrika 12,5% = 4 sampel
Kelompok 5 : ekstrak etanol daun Afrika 6,25% = 4 sampel
Kelompok 6 : ekstrak etanol daun Afrika 3,125% = 4 sampel
Kelompok 7 : kontrol Mc Farland = 4 sampel
Kelompok 8 : kontrol negatif (ekstrak etanol daun Afrika
b. Penentuan nilai Kadar Bunuh Minimum (KBM)
Kelompok yang dilanjutkan perhitungan koloni bakteri dengan Drop Plate Miles Misra, adalah:
Kelompok 1 : ekstrak etanol daun Afrika 100% = 4 sampel
Kelompok 2 : ekstrak etanol daun Afrika 50% = 4 sampel
Kelompok 3 : ekstrak etanol daun Afrika 25% = 4 sampel
Kelompok 4 : ekstrak etanol daun Afrika 12,5% = 4 sampel
Kelompok 5 : ekstrak etanol daun Afrika 6,25% = 4 sampel
Kelompok 6 : ekstrak etanol daun Afrika 3,125% = 4 sampel
Kelompok 7 : kontrol Mc Farland = 4 sampel
Kelompok 8 : kontrol negatif (ekstrak etanol daun Afrika
4.4 Variabel dan Definisi Operasional
4.4.1 Variabel Penelitian
Variabel bebas
Ekstrak etanol daun Afrika (Vernonia amygdalina) dengan konsentrasi 100%, 50%, 25%, 12,5%, 6,25% dan
c. Lama pengeringan daun Afrika (± 6 hari) d. Suhu pengeringan daun Afrika (40oC) e. Volume etanol yang dipakai 6 liter f. Konsentrasi etanol yang dipakai (70%) g. Waktu perendaman daun Afrika (15 menit) h. Waktu perkolasi (2 minggu)
i. Nomor kertas saring yang dipakai (Whatman No.42)
j. Jumlah kertas saring saat perkolasi (3 lapis) k. Kecepatan tetes cairan dalam perkolator (20 tetes/menit)
l. Suhu penguapan rotavapor (40oC)
m.Media pertumbuhan bakteri yaitu MHA dan MHB
n. Sterilisasi alat, bahan coba, dan media o. Porphyromonas gingivalis ATCC 33277
p. Jumlah bahan coba yang diteteskan ke MHA dan MHB (MHA=50µl, MHB=1 ml)
q. Suhu inkubasi (37oC)
r. Teknik pembiakan Porphyromonas gingivalis
s. Waktu pembiakan Porphyromonas gingivalis (24 jam)
c. Perlakuan terhadap daun Afrika selama tumbuh
4.4.2 Variabel Bebas
Variabel bebas pada penelitian ini adalah ekstrak etanol daun Afrika
(Vernonia amygdalina) dengan konsentrasi 100%, 50%, 25%, 12,5%, 6,25% dan 3,125%.
4.4.3 Variabel Tergantung
Variabel tergantung pada penelitian ini adalah pertumbuhan bakteri
Porphyromonas gingivalis pada media MHA dengan pengukuran nilai KHM dan KBM.
4.4.4 Variabel Terkendali
Variabel terkendali pada penelitian ini terdiri atas:
a. Jenis dan asal daun Afrika (Vernonia amygdalina) (Kelurahan Hamdan, Medan)
b. Berat daun Afrika (Vernonia amygdalina) sebelum pengeringan (2 kg) dan setelah pengeringan (300 gram)
c. Lama pengeringan daun Afrika (± 6 hari)
d. Suhu pengeringan daun Afrika (Vernonia amygdalina) (40oC) e. Volume etanol yang dipakai 6 liter
f. Konsentrasi etanol yang dipakai (70%)
g. Waktu perendaman daun Afrika (Vernonia amygdalina) (15 menit) h. Waktu perkolasi (2 minggu)
i. Nomor kertas saring yang dipakai (Whatman No.42)
j. Jumlah kertas saring saat perkolasi (3 lapis)
k. Kecepatan tetes cairan dalam perkolator (20 tetes/menit)
l. Suhu penguapan rotavapor (40oC)
m. Media pertumbuhan bakteri yaitu Mueller Hinton Broth (MHB) dan
Mueller Hinton Agar (MHA)
n. Sterilisasi alat, bahan coba, dan media
p. Jumlah bahan coba yang diteteskan ke MHA dan MHB (MHA=50µl, MHB=1 ml)
q. Suhu inkubasi (37oC)
r. Teknik pembiakan Porphyromonas gingivalis
s. Waktu pembiakan Porphyromonas gingivalis (24 jam) t. Waktu pengamatan (24 jam)
u. Keterampilan operator
4.4.5 Variabel Tidak Terkendali
Variabel yang tidak terkendali pada penelitian ini terdiri atas:
a. Lingkungan (kondisi tanah dan iklim) tempat tumbuh daun Afrika
(Vernonia amygdalina)
b. Usia daun Afrika (Vernonia amygdalina)
c. Perlakuan terhadap daun Afrika (Vernonia amygdalina) selama tumbuh d. Lama penyimpanan daun Afrika (Vernonia amygdalina) sampai proses ekstraksi
e. Suhu penyimpanan daun Afrika (Vernonia amygdalina) sampai proses ekstraksi
f. Lama bahan coba sampai ke Laboratorium Rumah Sakit Khusus Infeksi
UNAIR
g. Suhu saat pengiriman dari bahan coba sampai ke Laboratorium Rumah
4.4.6 Definisi Operasional
Variabel Bebas
No Variabel Defenisi Operasional Satuan
Variabel Tergantung
No Variabel Defenisi Operasional Satuan Ukur Skala
Ukur
4.5 Metode Penatalaksanaan Penelitian
4.5.1 Bahan Penelitian
Bahan penelitian yang digunakan adalah
1. Daun Afrika (Vernonia amygdalina) 2 kg yang dipetik dari Kelurahan Hamdan, Medan, Sumatera Utara, Indonesia.
2. Etanol 70% sebanyak 6 liter (Kimia Farma, Indonesia)
3. Akuades 2 liter (Kimia Farma, Indonesia)
4. Porphyromonas gingivalis ATCC 33277 (Laboratorium Rumah Sakit Khusus Infeksi, Surabaya, Indonesia)
5. Mueller Hinton Agar (Difco, USA)
6. NaCl 0,9% (Kimia Farma, Indonesia)
4.5.2 Alat Penelitian
1. Timbangan (Home Line, China)
3. Kertas perkamen 3 kajang
4. Blender (Panasonic, Japan)
5. Kapas 250gram (Bio Panca, Indonesia)
6. Kertas saring (Whatman no.42, England)
7. Aluminium foil 1 gulungan (Total Wrap, Indonesia)
8. Perkolator
9. Erlenmeyer (Pyrex, USA)
10. Vacuum rotary evaporator (Stuart, 2010) 11. Electronic balance (Sartorius, Germany)
12. Autoklaf (Tomy, Japan)
13. Densichek (bioMérieux, USA)
14. Vortex (Stuart, Japan)
15. Inkubator CO2 (Sanyo, Japan)
16. Mikropipet (Gilson, France)
17. Piring petri (Pyrex, Japan)
18. Ose dan spiritus
19. Kaca pembesar (Ootsuka ENV-CL, Japan)
4.5.3 Prosedur Penelitian
4.5.3.1 Pembuatan ekstrak etanol daun Afrika (Vernonia amygdalina)
Proses pembuatan ekstrak etanol daun Afrika (Vernonia amygdalina) dilakukan berdasarkan Standart Operasional Laboratorium Obat Tradisional Fakultas
Farmasi USU dengan langkah-langkah sebagai berikut:
a. Pembuatan simplisia
Daun Afrika (Vernonia amygdalina) dipetik dan ditimbang sebanyak 2 kg (Gambar 6). Daun Afrika dicuci dengan air mengalir, kemudian dikeringkan di dalam
lemari pengering dengan suhu 40oC (Gambar 7). Daun Afrika dikatakan sudah mengering apabila daun diremas akan mudah hancur. Daun Afrika (Vernonia amygdalina) yang telah dikeringkan kemudian ditimbang kembali dan diperoleh 300
dengan menggunakan blender (Gambar 8) dan didapat serat-serat halus (simplisia)
daun Afrika (Gambar 9).
b. Proses destilasi sederhana etanol
Letakkan etanol 96% dalam labu destilasi kemudian dipanaskan dengan
pemanas (heater) yang berada dalam wadah berisi air. Etanol dipanaskan hingga mencapai titik didih etanol yaitu 78oC. Pada suhu 78oC etanol mulai mendidih dan menguap. Uap etanol akan naik ke pendingin (kondensor) spiral, sedangkan uap air
berubah menjadi embun dan jatuh kembali ke labu didih. Uap etanol yang berada
dalam pendingin diembunkan/didinginkan hingga menjadi cair dan ditampung di
dalam labu destilat. Proses destilasi etanol ini akan terus berlangsung hingga kadar
etanol dalam labu destilasi habis dan hanya akan menyisakan air. (Gambar 10)
c. Pengenceran etanol
Etanol 96% yang telah didestilasi ditambahkan dengan akuades hingga
mencapai 1 liter etanol 70% yang sesuai dengan rumus pengenceran yaitu
M1.V1 = M2.V2. Pengenceran dilakukan hingga mencapai volume etanol 70%
sebanyak 6 liter. (Gambar 11)
d. Proses maserasi
Sebanyak 300 gram serbuk simplisia diletakkan ke dalam bejana tertutup dan
direndam dengan etanol 70% selama 15 menit pada suhu 25oC (Gambar 12). e. Proses perkolasi
Perkolator disiapkan dengan cara meletakkan kapas secukupnya yang telah
dibasahi dengan etanol pada bagian dasar wadah perkolator, kemudian di atas kapas
tersebut diletakkan kertas saring sebanyak 2 lembar. Kemudian massa simplisia yang
telah direndam tersebut dipindahkan sedikit demi sedikit ke dalam perkolator di
mulai dari bagian tengah hingga ke tepi perkolator dengan hati-hati sambil sesekali
ditekan. Kemudian etanol 70% dituangkan ke dalam perkolator dan massa disaring
dengan lapisan kertas saring sampai cairan tersebut mulai menetes dan diatas
simplisia masih terdapat selapis cairan penyaring untuk mengetahui apakah
perkolator sudah berfungsi dengan baik. Kemudian perkolator ditutup dengan
Setelah 24 jam, perkulator dibuka kembali dan cairan dibiarkan menetes
dengan kecepatan 1 ml per menit atau 20 tetes per menit. Tambahkan berulang-ulang
etanol 70% secukupnya sehingga selalu terdapat selapis cairan penyari di atas
simplisia dan diperoleh ekstrak cair.
f. Ekstrak cair (Gambar 14) diuapkan dengan vacuum rotary evaporator pada suhu 40oC hingga konsistensi seperti madu (Gambar 15). Ekstrak yang telah kental tersebut ditimbang dengan timbangan analitik. Setelah itu ekstrak etanol daun Afrika
dimasukkan ke dalam botol kaca, lalu disimpan di tempat yang sejuk.
Gambar 6. Penimbangan daun Afrika 2 kg
Gambar 7. Pengeringan daun Afrika
Gambar 8. Daun Afrika yang sudah kering diblender
Gambar 13. Proses perkolasi
Gambar 14. Ekstrak cair daun Afrika
Gambar 12. Proses maserasi
Gambar 10. Proses destilasi etanol 96%
Gambar 11. Pengenceran etanol 96%
4.5.3.2 Uji Aktivitas Antibakteri dengan Metode Dilusi
Proses pengujian aktivitas antibakteri ekstrak etanol daun Afrika (Vernonia amygdalina) dilakukan berdasarkan Standart Operasional Laboratorium Rumah Sakit Khusus Infeksi UNAIR dengan langkah-langkah sebagai berikut:
4.5.3.2.1 Pembuatan Suspensi Bahan Uji
Ekstrak daun Afrika dalam pelarut etanol ditimbang menggunakan electronic balance dan massanya disesuaikan dengan konsentrasi yang diinginkan dengan cara dilarutkan dengan media Muller Hinton Broth (MHB). Ekstrak daun Afrika dalam
pelarut etanol dimulai dari konsentrasi 100% karena belum diketahui konsentrasi
ekstrak yang mampu menghambat pertumbuhan Porphyromonas gingivalis, jadi pengujian dimulai pada konsentrasi terbesar. Sediakan 6 tabung, pada tabung pertama
diberi 2 gr ekstrak kental daun Afrika ditambahkan 2 ml MHB kemudian dicampur dengan menggunakan vorteks sehingga didapatkan ekstrak etanol daun Afrika dengan
konsentrasi 100%. Kemudian dilakukan pengenceran berganda dengan cara
mengambil 1 ml dari konsentrasi ekstrak etanol daun Afrika 100% menggunakan
mikropipet dan diletakkan pada tabung kedua yang telah berisi 1 ml MHB untuk mendapatkan ekstrak etanol daun Afrika 50% (pengenceran berganda) kemudian
divorteks. Cara yang sama dilakukan untuk mendapatkan konsentrasi 25%, 12,5%,
6,25%, dan 3,125% Masing-masing tersebut diberi label sesuai konsentrasinya.
4.5.3.2.2 Pembuatan Media Bakteri
Sebelum spesimen dibiakkan, terlebih dahulu dibuat media MHA. Sebanyak 34 gram MHA dilarutkan dalam 1 liter akuades kemudian dituangkan pada tabung reaksi (20 ml/tabung reaksi), lalu dipanaskan di atas tungku pemanas magnetik
sampai mendidih. Setelah masak, media disterilkan dalam autoklaf selama 15 menit dengan tekanan 2 atm dan suhu 121oC, lalu disimpan dalam lemari pendingin. Jika akan digunakan, media dipanaskan kembali hingga mendidih lalu dituang ke dalam
petri. Kemudian media dimasukkan ke dalam inkubator selama 24 jam untuk melihat