EKSTRAKSI SENYAWA TANIN DARI DAUN KETAPANG (Terminalia catappa L.) DAN UJI AKTIVITASNYA
SEBAGAI INHIBITOR KOROSI
(Skripsi)
Oleh
Retno Dwi Palupi
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM UNIVERSITAS LAMPUNG
EKSTRAKSI SENYAWA TANIN DARI DAUN KETAPANG (Terminalia catappa L.) DAN UJI AKTIVITASNYA
SEBAGAI INHIBITOR KOROSI
Oleh
Retno Dwi Palupi
Skripsi
Sebagai Salah Satu Syarat untuk Mencapai Gelar SARJANA SAINS
Pada Jurusan Kimia
Fakultas Matematika dan Ilmu Pengetahuan Alam
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM UNIVERSITAS LAMPUNG
ABSTRACT
TANNIN EXTRACTION OF Terminalia catappa LEAVES AND ITS ACTIVITY AS CORROSION INHIBITOR
By
Retno Dwi Palupi
In this study, the tannins extract from ketapang leaves (Terminalia catappa) had been tested as a corrosion inhibitor of mild steel in synthetic brine solution with carbon dioxide saturated at room temperature. Stages of the study were : sample collection and preparation, extraction, phytochemical test of tannin using FeCl3
and gelatin. Tannins Identifications were performed using TLC, FTIR and ultraviolet-visible spectrophotometer. Corrosion test were carried out in two methodes, the gravimetric and potentiometric methods. Analysis of the surface morphology of corroded steel and mild steel compositions performed using SEM-EDS. The results showed that the test based phytochemicals test, identification by using TLC, spectral data of FTIR and ultraviolet-visible, the extracted compound is tannin. Analysis of the corrosion by weight loss method showed that the optimum inhibitor concentration of 40% v/v in 3 days of exposure, is effective in inhibiting the process of mild steel corrosion in corrosive medium with inhibition efficiency of 60.87%, while the corrosion analysis with potentiometric method showed that the optimum inhibitor concentration of 40% v/v at 10 minutes of exposure, is also quite effective in inhibiting the corrosion of mild steel in the corrosive medium with inhibition efficiency of 1.98%.
ABSTRAK
EKSTRAKSI SENYAWA TANIN DARI DAUN KETAPANG (Terminalia catappa L.) DAN UJI AKTIVITASNYA
SEBAGAI INHIBITOR KOROSI
Oleh
Retno Dwi Palupi
Pada penelitian ini telah dilakukan uji ekstrak tanin dari daun ketapang (Terminalia catappa) sebagai inhibitor korosi pada baja lunak (mild steel) dalam medium air laut buatan. Tahapan penelitian yang dilakukan meliputi pengumpulan dan persiapan sampel, ekstraksi, uji fitokimia tanin dengan menggunakan FeCl3 dan gelatin. Identifikasi tanin dilakukan menggunakan KLT
dan spektrofotometer FTIR serta spektrofotometer ultraungu-tampak. Uji korosi dilakukan dengan dua cara, yaitu metode gravimetri dan metode potensiometri. Analisis morfologi permukaan baja terkorosi dan komposisi baja lunak dilakukan menggunakan SEM-EDS. Hasil penelitian menunjukkan bahwa berdasarkan uji fitokimia, identifikasi dengan KLT dan data spektrum FTIR serta ultraungu-tampak, senyawa hasil ekstraksi tersebut merupakan tanin. Analisis laju korosi dengan metode kehilangan berat menunjukkan bahwa inhibitor optimum pada konsentrasi 40% v/v pada paparan 3 hari, cukup efektif dalam menghambat proses korosi baja lunak dalam medium korosif dengan efisiensi inhibisi sebesar 60,87%, sedangkan analisis laju korosi dengan metode potensiometri menunjukkan bahwa inhibitor optimum pada konsentrasi 40% v/v pada paparan 10 menit, efektif dalam menghambat proses korosi baja lunak dalam medium korosif dengan efisiensi inhibisi sebesar 1,98%.
Judul Skripsi : EKSTRAKSI SENYAWA TANIN DARI DAUN KETAPANG (Terminalia catappa) DAN
UJI AKTIVITASNYA SEBAGAI INHIBITOR KOROSI
Nama Mahasiswa : Retno Dwi Palupi Nomor Pokok Mahasiswa : 0817011010
Jurusan : Kimia
Fakultas : Matematika dan Ilmu Pengetahuan Alam
MENYETUJUI 1. Komisi Pembimbing
Prof. Dr. Tati Suhartati, M.S. Dian Septiani Pratama, M.Si. NIP 195405101998032001 NIP 198009082009122003
2. Ketua Jurusan
MENGESAHKAN
1. Tim Penguji
Ketua : Prof. Dr. Tati Suhartati, M.S. ………….
Sekretaris : Dian Septiani Pratama, M.Si. ………….
Penguji
Bukan Pembimbing : Andi Setiawan, Ph.D. …………..
2. Dekan Fakultas Matematika dan Ilmu Pengetahuan Alam
Prof. Suharso, Ph.D. NIP 196905301995121001
RIWAYAT HIDUP
Penulis dilahirkan di Negara Tulang Bawang, Lampung Utara pada tanggal 24 Agustus 1989, sebagai anak kedua dari dua bersaudara, putri dari Herman Waluyo dan Sri Hastuti. Jenjang pendidikan diawali dari Taman Kanak-kanak (TK) di TK Bunga Mayang diselesaikan pada tahun 1996. Sekolah Dasar (SD) di SD yayasan Bunga Mayang diselesaikan pada tahun 2002. Madrasah Tsanawiyah (MTs) di MTS Nurul Huda Madukoro diselesaikan pada tahun 2005 dan Sekolah Menengah Atas (SMA) di SMA Negeri 2 Kotabumi diselesaikan pada tahun 2008. Tahun 2008, penulis terdaftar sebagai Mahasiswa Jurusan Kimia FMIPA Unila melalui jalur PKAB (Penelusuran Kemampuan Akademik dan Bakat).
PERSEMBAHAN
Dengan mengucap syukur alhamdulillah,
kupersembahkan karya kecilku ini untuk orang-orang yang
kusayangi :
Ayah dan ibunda tercinta,
terima kasih atas semua pengorbanan, doa dan kasih sayang
yang kalian berikan mengantarku sampai kini
Kakakku tersayang,
motivasimu selalu membangkitkanku
Segenap keluarga besarku yang selalu mendukungku
Sahabat-sahabat terindahku
MOTTO
“Inna ma‟al „usri yusroo”
Sesungguhnya bersama kesulitan itu ada kemudahan
(Al-Insyirah : 6)
....sesungguhnya Allah tidak mengubah keadaan suatu kaum
sehingga mereka mengubah keadaan yang ada
pada diri mereka sendiri
(Ar-Rad : 11)
Lost time is never found again
(Benjamin Franklin)
Sesuatu yang belum dikerjakan, seringkali tampak mustahil,
SANWACANA
Assalamu’alaikum Wr. Wb.
Alhamdulillah Puji dan syukur Penulis ucapkan kehadirat Allah SWT, karena atas segala rahmat dan karunia-Nya skripsi ini dapat diselesaikan.
Skripsi dengan judul "Ekstraksi Senyawa Tanin dari Daun Ketapang
(Terminalia catappa) dan Uji Aktivitasnya sebagai Inhibitor Korosi" adalah salah satu syarat untuk memperoleh gelar Sarjana Sains pada Jurusan Kimia, Fakultas Matematika dan Ilmu Pengetahuan Alam, Universitas Lampung. Dalam pelaksanaan dan penulisan skripsi ini tidak lepas dari kesulitan dan rintangan, namun itu semua dapat penulis lalui berkat rahmat dan ridha Allah SWT serta bantuan dan dorongan semangat dari orang-orang yang hadir dikehidupan penulis. Dalam kesempatan ini, penulis menyampaikan terima kasih setulus-tulusnya kepada :
1. Ibu Prof. Dr. Tati Suhartati, M.S., selaku pembimbing utama yang telah banyak memberikan ilmu pengetahuan, gagasan, kritik dan saran serta
2. Ibu Dian Septiani Pratama, M.Si., selaku pembimbing pembantu yang telah telah memberikan arahan, saran, nasehat, dukungan, semangat dan kepada penulis sehingga skripsi ini terselesaikan dengan baik.
3. Bapak Andi Setiawan, Ph.D., selaku pembahas yang telah memberikan kritik, saran dan arahan yang diberikan kepada penulis terselesainya skripsi ini. 4. Bapak Syaiful Bahri, M.Si., yang telah memberikan dukungan, kritik, saran
dan arahan kepada penulis sehingga skripsi ini terselesaikan dengan baik. 5. Bapak Dr. Eng. Suripto Dwi Yuwono, M.T., selaku Pembimbing Akademik
atas kesediaannya untuk memberikan bimbingan, bantuan, nasehat dan informasi yang bermanfaat kepada penulis.
6. Bapak Prof. Suharso, Ph.D., selaku Dekan Fakultas Matematika dan Ilmu Pengetahuan Alam Universitas Lampung.
7. Bapak Andi Setiawan, Ph.D., selaku ketua Jurusan Kimia FMIPA Unila. 8. Seluruh dosen FMIPA Unila yang telah mendidik dan memberikan ilmu
pengetahuan yang sangat berguna kepada penulis selama kuliah.
10. Kakakku tersayang, Haries Kurniawan, S.E. dan istri (Kharisma Dewi) terima kasih atas semangat, doa, perhatian dan motivasi yang kalian berikan selama ini meskipun jarak memisahkan kita.
11. Arif Ashari sebagai rekan penelitian, terima kasih atas kerja sama, bantuan dan saran dalam menyelesaikan penelitian.
12. Sahabat-sahabat terbaikku : Ani Sulistriani, S.Si., Elianasari S.Si, Miftasani, Harnita Yuniar, Shoffa Nur Fauziah S.Si, Sundari Riawati S.Si., Ni Putu Yuliastri S.Si, Riki Fauzi, Ayu Aditya Sari, Novia Wiliana dan Nurjannah terima kasih atas persahahabatan yang telah terjalin selama ini, segala dukungan, rasa kebersamaan, keceriaan dan canda tawa yang selalu hadir disetiap hari.
13. Teman-teman Kimia 2008 : Ani S.Si., Eli S.Si., Nita, Miftasani, Shoffa S.Si., Ria S.Si., Putu S.Si., Novi, Ayu, Putri, Rudi, Riki, Nuro, Dendi, TB, Ricardo, Raffel, Adek S .Si., Kiki, Dewa, Puji S.Si., Siti S.Si., Dewi, Sri S.Si., Arif A, Ruzki, Subari, Albert S.Si., Ramli S.Si., Robby, Amin, Eko, Nuro, Ramdhan S.Si., Idrus, Chandra, Majid, Nanda, Vivi, Lenny S.Si., Eny S.Si., Wanti, Evi, Margareth, Mutiara, Arif RH, Dipa, Eldes, Via, Diana, Aan, Dwi dan Reina terima kasih untuk pertemanan dan keceriaan serta kebersamaan selama menjalankan perkuliahan.
14. Teman seperjuangan di Laboratorium Organik : Nurjannah, Dendi, Mbak Eka, Mbak Astri, Kak Heri, Reska dan Neneng ’09. Terima kasih atas segala bantuan dan saran serta kebersamaannya selama penelitian.
16. Sabahat-sahabat kosan : Mbak Eka Nurmaya, Wirna, Septi, Vinny, Neno dan Nova. Terima kasih atas kebersamaan dan keceriaan kalian, selalu
memberikan canda tawa yang dapat menghilangkan kepenatan dari rutinitas kuliah.
17. Semua pihak yang telah membantu dan mendukung penulis dalam penyusunan skripsi ini.
Akhir kata, Penulis menyadari bahwa skripsi ini masih jauh dari kesempurnaan. Penulis berharap semoga skripsi yang sederhana ini dapat berguna dan bermanfaat bagi kita semua. Amin.
Bandar Lampung, 25 Februari 2013 Penulis
I. PENDAHULUAN
A. Latar Belakang
Tanin merupakan senyawa polifenol dari kelompok flavonoid dengan berat molekul tinggi yang ditemukan pada famili tanaman tingkat tinggi, salah satunya adalah tanaman ketapang (Terminalia catappa L.). Tanin diduga memiliki potensi sebagai inhibitor korosi logam karena selain sifatnya yang dapat membentuk kompleks dengan logam juga merupakan senyawa organik ramah lingkungan. Senyawa tanin dapat membentuk kompleks dengan Fe(II) di permukaan besi sehingga laju korosi besi mengalami penurunan (Favre, 1993).
2
efektif menurunkan laju korosi baja lunak dalam medium air laut buatan yang jenuh CO2. Efektivitas ekstrak bahan alam tersebut sebagai inhibitor korosi tidak
terlepas dari kandungan nitrogen yang terdapat dalam senyawaan kimianya seperti daun tembakau yang mengandung senyawa-senyawa kimia antara lain nikotin, hidrazin, alanin, quinolin, anilin, piridin, dan amina.
Dari pemaparan tersebut, maka dalam penelitian ini dilakukan uji ekstrak tanin dari daun ketapang (Terminalia catappa L.) sebagai inhibitor korosi pada baja lunak (mild steel) dalam media air laut buatan. Penelitian ini memiliki
ketertarikan tersendiri karena ekstrak tanin yang diekstraksi dari daun ketapang di daerah Lampung masih jarang yaitu sebagai inhibitor yang aman, mudah
didapatkan, biaya murah, dan ramah lingkungan. Untuk mengekstrak tanin digunakan metode maserasi menggunakan pelarut aseton-air, yang merupakan campuran pelarut yang bersifat polar dan memberikan hasil ekstraksi terbaik pada kerja praktik yang telah dilakukan sebelumnya. Uji kualitatif ekstrak daun
ketapang menggunakan FeCl3 dan gelatin. Identifikasi tanin dilakukan dengan
KLT. Identifikasi gugus fungsi dan panjang gelombang serapan maksimum dari tanin menggunakan spektroskopi FTIR dan ultraungu-tampak. Pengujian tanin sebagai inhibisi korosi baja lunak dalam media air laut buatan dan pengukuran laju korosi menggunakan metode gravimetri (kehilangan berat ) dan
3
B.Tujuan Penelitian
Tujuan penelitian ini adalah :
1. Mendapatkan tanin dari ekstrak daun ketapang (Terminalia catappa).
2. Menguji efektifitas inhibitor ekstrak tanin dengan berbagai konsentrasi dalam media korosif serta mengukur laju korosi sampel yang telah terkorosi.
C.Manfaat Penelitian
Penelitian ini diharapkan memberi manfaat yaitu :
1. Ekstrak tanin dari daun ketapang (Terminalia catappa) secara efektif dapat digunakan untuk inhibisi korosi yaitu sebagai inhibitor yang aman, mudah didapatkan, biaya murah dan ramah lingkungan.
II. TINJAUAN PUSTAKA
A. Ketapang (Terminalia catappa L.)
Terminalia catappa L. atau dikenal dengan nama tanaman ketapang merupakan
tanaman dari famili combretaceous yang daunnya banyak digunakan sebagai obat masyarakat di Asia Tenggara. Tanaman ini menyebar di seluruh daerah tropis di lingkungan pantai (Mohale et al., 2009). Adapun klasifikasi tanaman ketapang adalah sebagai berikut.
Kerajaan : Plantae
Divisi : Magnoliophyta Kelas : Magnoliopsida Ordo : Myrtales Famili : Combretaceae Genus : Terminalia
Spesies : Terminalia catappa
5
Gambar 1. Daun ketapang
1. Kandungan Kimia Daun Ketapang
Tumbuhan ketapang dilaporkan mengandung berbagai macam senyawa kimia, diantaranya senyawa tanin (Eddy et al, 2009), flavonoid (Lin et al., 2000), triterpenoid (Gao et al., 2004), alkaloid (Mandasari, 2006), steroid (Babayi et al., 2004) dan asam lemak (Jaziroh, 2008). Tanin yang terkandung dalam daun ketapang sebanyak 10,57 mg/g (Annegowda et al., 2010).
2. Manfaat Daun Ketapang
Daun ketapang umumnya digunakan sebagai obat di Asia Selatan untuk
mengobati dermatitis dan hepatitis (Wen et al., 2011). Ekstrak yang berasal dari daun Terminalia catappa memiliki aktivitas antibakteri antara lain terhadap spesies E. coli dan Salmonell shigella. Daun Terminalia catappa juga telah terbukti melindungi penyakit hati akut yang disebabkan oleh beberapa
hepatotoxicants. Analisis HPLC dari ekstrak daun ketapang menunjukkan adanya
6
Selain itu, ekstrak etanol dari daun ketapang juga digunakan sebagai inhibisi korosi baja lunak dalam medium asam sulfat (Eddy et al., 2009).
B. Tanin
Tanin merupakan senyawa polifenolik kompleks yang dihasilkan oleh polimerisasi fenol sederhana (Rangari, 2007). Di alam, tanin ditemukan di
seluruh dunia dalam famili yang berbeda dari tanaman tingkat tinggi. Senyawa ini memiliki berat molekul mulai dari 500 sampai lebih dari 20.000 D dan larut dalam air dengan pengecualian beberapa struktur dengan berat molekul tinggi (Rahim and Kassim, 2008).
1. Klasifikasi Tanin
Tanin diklasifikasikan menjadi dua jenis berdasarkan reaksi hidrolitik yang terlibat dalam struktur tanin, yaitu tanin terhidrolisis (hydrolysable tannins) dan tanin terkondensasi (condensed tannins)(Harborne, 1987).
a. Tanin yang Dapat Terhidrolisis (Hydrolysable Tannins)
7
Gambar 2. Struktur asam galat (Rangari, 2007)
Gambar 3. Struktur asam heksahidrodifenat (Rahim and Kassim, 2008)
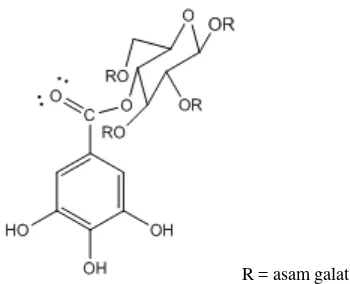
Jenis tanin yang terhidrolisis antara lain sebagai berikut : 1. Gallotanin
Galotanin adalah tanin terhidrolisa yang paling sederhana, yang terbentuk dari asam galat dan gula, biasanya glukosa. Beberapa asam galat terikat pada satu molekul gula. Asam galat terikat bersama pada gugus ester yang terbentuk antara gugus karboksil molekul satu dan gugus hidroksi pada molekul lain
(Gohen, 1976).
R = asam galat
8
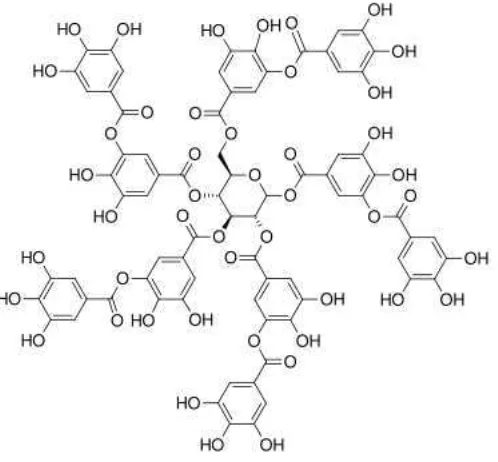
Asam tanat adalah salah satu polimer yang tergolong tanin terhidrolisis, yang merupakan polimer dari molekul-molekul asam galat dan glukosa (Gambar 5). Banyaknya fenol yang terikat menentukan sifat keasamannya.
Gambar 5. Struktur asam tanat (Costadinnova et al., 2012)
2. Elagitanin (Asam elagat)
Elagitanin terbentuk dari asam heksahidroksi difenil yang mungkin terbentuk dari terikatnya dua molekul asam galat melalui reaksi oksidasi (Fieser, 1961).
Hidrolisis dengan asam kuat akan menghasilkan asam elagat. Asam elagat memberikan reaksi warna spesifik dengan adanya asam nitrit (HNO2). Reaksi ini
9
R = asam heksahidrodifenat
Gambar 6. Struktur elagitanin (Khanbabaee and Ree, 2001)
b. Tanin yang Terkondensasi (Condensed Tannins)
Senyawa-senyawa yang mengandung tanin yang terkondensasi hanya berisi inti fenolik yang berhubungan dengan flavonoid secara biosintesis dikaitkan dengan flavonoid (Rangari, 2007). Tanin terkondensasi secara biosintesis dapat dianggap terbentuk dengan cara kondensasi katekin tunggal (galokatekin) yang membentuk senyawa dimer dan kemudian oligomer yang lebih tinggi.
Proantosianidin merupakan nama lain dari tanin terkondensasi karena jika direaksikan dengan asam panas, beberapa ikatan karbon penghubung satuan terputus dan dibebaskan monomer antosianidin (Harborne, 1987).
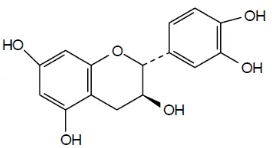
10
Gambar 7. Struktur katekin (flavan-3-ol)
Gambar 8. Struktur flavan-3,4-diol
2. Sifat dan Uji Tanin
Tanin yang diisolasi dari tanaman berupa bubuk atau serbuk putih kekuningan, amorf dan beraroma khas. Tanin dapat dibedakan dari fenol-fenol lain karena kemampuannya untuk mengendapkan protein. Tanin biasanya mengandung H2O
10 % (Pansera, 2004). Senyawa tanin tidak larut dalam pelarut non polar, seperti eter, kloroform dan benzena tetapi mudah larut dalam air, dioksan, aseton, dan
alkohol serta sedikit larut dalam etil asetat (Harborne, 1987).
3. Manfaat Tanin
Penggunaan tanin dalam perlindungan korosi telah diungkapkan sejak tahun 1936. Pengembangan industri menggunakan tanin sebagai inhibitor korosi dalam
11
C.Ekstraksi Tanin
Ekstraksi adalah proses penarikan komponen atau zat aktif dengan menggunakan pelarut tertentu. Pemilihan metode ekstraksi senyawa dipengaruhi oleh beberapa faktor, yaitu sifat jaringan tanaman, sifat kandungan, zat aktif serta kelarutan dalam pelarut yang digunakan. Prinsip ekstraksi adalah melarutkan senyawa polar dalam pelarut polar dan senyawa non polar dalam pelarut non polar (Guether, 1987).
Pemilihan metode ekstraksi bergantung pada tekstur dan kandungan air bahan tumbuhan yang diekstraksi dan pada jenis senyawa yang akan diisolasi. Prosedur untuk memperoleh kandungan senyawa organik dari jaringan tumbuhan kering (buah, biji dan daun) ialah dengan ekstraksi sinambung serbuk bahan dengan menggunakan alat soxhlet dengan pelarut tertentu (Harborne, 1987).
Maserasi merupakan metode ekstraksi sederhana, yang dilakukan dengan cara merendam sampel dalam pelarut organik. Pelarut organik akan menembus dinding sel dan masuk ke dalam rongga sel yang mengandung zat aktif sehingga zat aktif akan larut. Karena adanya perbedaan konsentrasi antara larutan zat aktif di dalam sel, maka larutan yang terpekat didesak keluar. Keuntungan metode ekstraksi ini, adalah metode dan peralatan yang digunakan sederhana dan mudah diusahakan (Sa’adah, 2010). Penekanan utama pada maserasi adalah tersedianya waktu kontak yang cukup antara pelarut dan jaringan yang diekstraksi (Guether, 1987).
12
aseton. Senyawa non polar yang tidak dapat melarutkannya adalah karbon tetraklorida dan dietil eter sehingga dapat digunakan untuk melarutkan pengotor dan diperoleh tanin yang lebih murni. Pengekstraksi tanin yang baik adalah campuran air dengan pelarut organik misalnya metanol, etanol dan aseton berair (7:3) yang mengandung asam askorbat 0,1%. Penambahan asam askorbat dalam pelarut aseton adalah untuk meminimumkan oksidasi tanin selama ekstraksi. Hal ini disebabkan oksidator akan bereaksi terlebih dahulu dengan asam askorbat yang lebih mudah teroksidasi (Abdurrohman, 1998).
Tanin yang dapat terhidrolisis dan tanin yang terkondensasi sangat larut dalam air dan alkohol tetapi tidak larut dalam pelarut organik seperti pelarut eter, kloroform, dan benzena. Senyawa tanin dapat dengan mudah diekstraksi dengan air atau alkohol. Metode umum untuk ekstraksi asam tanat dapat menggunakan eter jenuh air, atau dengan campuran air, alkohol, dan eter. Setelah ekstraksi, lapisan
terpisah secara terkonsentrasi, dikeringkan, diisolasi lebih lanjut dan pemurnian menggunakan teknik pemisahan kromatografi (Rangari, 2007).
D. Uji Fitokimia Tanin
Uji tanin yang paling dikenal adalah pengendapan gelatin. Larutan tanin yang ditambahkan ke dalam larutan gelatin 0,5% akan menimbulkan endapan
13
tumbuhan hijau dengan mencelupkan kedalam HCl 2M mendidih selama setengah jam. Bila terbentuk warna merah dengan amil atau butil alkohol maka ini
merupakan bukti adanya senyawa tersebut (Harborne,1987).
E.Pemisahan secara Kromatografi
Kromatografi merupakan pemisahan suatu senyawa yang didasarkan atas perbedaan laju perpindahan dari komponen-komponen dalam campuran. Pemisahan dengan metode kromatografi dilakukan dengan cara memanfaatkan sifat-sifat fisik dari sampel, seperti kelarutan, adsorpsi, keatsirian dan kepolaran (Johnson and Stevenson, 1991). Kromatografi lapis tipis (KLT) merupakan salah satu metode yang melibatkan pendistribusian campuran dua atau lebih senyawa antara fasa diam dan fasa gerak. Fasa diam dapat berupa lapisan tipis dari penyerapan pada plat, dan pada fasa gerak adalah cairan pengembang yang bergerak naik pada fasa diam membawa komponen-komponen sampel
14
F. Identifikasi secara Spektroskopi
Spektroskopi merupakan ilmu yang mempelajari tentang cara menganalisis spektrum suatu senyawa dan interaksi antara energi cahaya dan materi (Anwar dkk, 1994). Teknik spektroskopi ini digunakan untuk mengidentifikasi struktur suatu senyawa dan mempelajari karakteristik ikatan dari suatu senyawa tersebut karena senyawa akan menyerap energi cahaya pada panjang gelombang tertentu (Fessenden dan Fessenden, 1999).
1. Fourier Transform Infrared Spectroscopy (FTIR)
Pada spektroskopi inframerah (IR), senyawa organik akan menyerap berbagai frekuensi radiasi elektromagnetik inframerah. Molekul-molekul senyawa akan menyerap sebagian atau seluruh radiasinya. Penyerapan ini berhubungan dengan adanya sejumlah vibrasi yang terkuantisasi dari atom-atom yang berikatan secara kovalen pada molekul-molekul itu.
Penyerapan ini juga berhubungan dengan adanya perubahan momen dipol dari ikatan kovalen pada waktu terjadinya vibrasi (Supriyanto, 1999). Pada dasarnya Spektrofotometer FTIR (Fourier Trasform Infra Red) adalah sama dengan Spektrofotometer IR dispersi, yang membedakannya adalah pengembangan pada sistim optiknya sebelum berkas sinar infra merah melewati contoh. Pada sistem optik FTIR digunakan radiasi LASER (Light Amplification by Stimulated Emmission of Radiation) yang berfungsi sebagai radiasi yang diinterferensikan
15
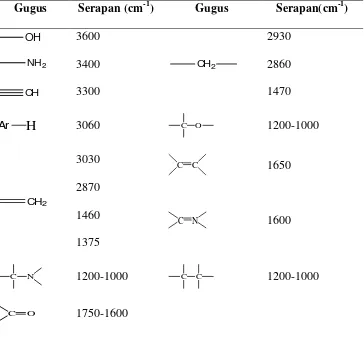
Tabel 1. Karakteristik frekuensi uluran beberapa gugus fungsi
Gugus Serapan (cm-1) Gugus Serapan(cm-1)
Sumber : Banwell and McCash (1994).
2. Spektroskopi Ultraviolet-Tampak (UV-Vis)
16
Transisi yang penting pada daerah ultraviolet dan tampak yaitu transisi n→π* dan π→π*, sedangkan transisi n→σ* jarang terjadi (Fessenden dan Fessenden, 1999).
Transisi yang terjadi pada tanin yaitu transisi π→π* akibat adanya ikatan rangkap
terkonjugasi dan transisi n→π* karena adanya elektron bebas. Tanin mengandung
sistem aromatik yang terkonjugasi oleh karena itu menunjukkan pita serapan yang kuat pada daerah ultraviolet dan tampak (Harborne, 1987). Senyawa dengan ikatan rangkap terkonjugasi seperti tanin akan mengalami penyerapan radiasi pada panjang gelombang yang lebih besar dari 217 nm (Sastrohamidjojo, 2007).
G. Korosi
Korosi secara umum didefinisikan sebagai suatu peristiwa kerusakan atau penurunan kualitas suatu bahan yang disebabkan oleh terjadinya reaksi dengan lingkungannya. Korosi pada logam (perkaratan) yaitu peristiwa perusakan pada logam yang disebabkan oleh reaksi oksidasi. Kerusakan terhadap logam-logam tersebut dipengaruhi oleh adanya gas oksigen, air, larutan garam, basa, asam, dan juga akibat arus listrik (Fontana, 1986).
Pada penelitian ini medium korosif yang digunakan adalah air laut buatan. Komposisi air laut buatan ini meliputi NaCl dan NaHCO3 serta dilakukan
penjenuhan larutan dengan mengalirkan gas CO2.
17
pasivasi pada logam berada di dalam lingkungan yang mengandung klorida akan terurai dengan cepat dalam larutan yang mengandung klorida. Larutan natrium klorida adalah larutan yang terbentuk dengan proses awal melarutnya garam natrium klorida dalam bentuk padat ke dalam pelarut air, maka akan terurai menjadi ion natrium dan klorida yang dapat bergerak dalam larutan dan
menghantarkan arus listrik. Jika logam dalam lingkungan seperti ini, maka ion klorida yang telah terurai akan teradsorpsi ke permukaan logam dan
menghentikan proses pasivasi serta mencegah terjadinya pengendapan lapisan oksida pelindung. Sedangkan, natrium yang telah terurai sebagian juga akan mengendap di dalam larutan, sebagian akan bergerak menghantarkan listrik. Dengan berhentinya proses pasivasi ini, korosi yang terjadi pada logam tersebut akan tetap berlangsung (Haryono dkk, 2010).
Keberadaan gas CO2 dapat mempercepat reaksi korosi logam. Hal ini disebabkan
karena adanya pengaruh keasaman dari gas CO2 sehingga dapat membentuk ion
karbonat. Ion karbonat ini bertindak sebagai ligan dan mengkatalisis reaksi pelarutan logam sehingga akan terjadi proses korosi. Apabila logam yang
dimaksud adalah baja karbon maka produk korosi yang akan terbentuk adalah besi karbonat (FeCO3) (Ridwanulloh, 2009). Mekanisme reaksi yang terjadi :
1. Pelarutan CO2 yang bereaksi membentuk H2CO3
CO2(g) → CO2 (aq)
18
2. Disosiasi H2CO3 menjadi ion karbonat sehingga menyebabkan larutan
bersifat asam
H2CO3(aq) → H+ (aq) + HCO3-(aq)
Selanjutnya ion-ion Fe2+ dapat bereaksi dengan ion-ion HCO3- membentuk FeCO3
pada pH dan suhu tertentu. Dengan demikian proses korosi yang terjadi adalah Anoda : Fe (s) + HCO3- (aq) → FeCO3 (s) + H+ (aq) + 2e
-Katoda : 2H+ (aq) + 2e-→ H2 (g)
Reaksi total : Fe (s) + HCO3-(aq) + H+(aq) → FeCO3 (s) + H2 (g)
1. Inhibitor Korosi
Inhibitor korosi adalah zat yang ketika ditambahkan dalam konsentrasi kecil pada lingkungan, efektif mengurangi laju korosi logam pada lingkungan tersebut (Rahim and Kassim, 2008). Sejumlah inhibitor menghambat korosi melalui cara adsorpsi untuk membentuk suatu lapisan tipis dan melalui pengaruh lingkungan (misalnya pH) menyebabkan inhibitor dapat mengendap dan selanjutnya
19
2. Inhibitor Organik
Inhibitor organik umumnya senyawa heteroatom. Pada umumnya senyawa-senyawa organik yang dapat digunakan adalah senyawa-senyawa-senyawa-senyawa yang mampu membentuk senyawa kompleks baik kompleks yang terlarut maupun kompleks yang mengendap. Untuk itu diperlukan adanya gugus-gugus fungsi yang mengandung atom-atom yang mampu membentuk ikatan kovalen terkoordinasi, yaitu atom nitrogen, belerang dan oksigen pada suatu senyawa tertentu
(Dalimunthe, 2004). Atom O, N, dan S ditemukan memiliki kebasaan yang lebih tinggi dan kepadatan elektron dan dengan demikian bertindak sebagai inhibitor korosi. Atom O, N, dan S adalah pusat aktif untuk proses adsorpsi pada
permukaan logam. Efisiensi inhibisi mengikuti urutan O <N <S <P. Ketersediaan elektron tak berikatan (pasangan elektron bebas) dalam molekul inhibitor
memfasilitasi transfer elektron dari inhibitor dengan logam. Ikatan kovalen koordinat yang melibatkan transfer elektron dari inhibitor pada permukaan logam dapat terbentuk. Dengan demikian terjadi adsorpsi antara permukaan logam dan inhibitor yang membentuk lapisan pelindung pada logam (Rani and Basu, 2011). Inhibitor organik diklasifikasikan dalam dua jenis, yaitu sintetik dan alami.
Inhibitor sintetik seringkali digunakan dalam menghambat laju korosi logam, namun inhibitor ini selain mahal juga ternyata berbahaya bagi manusia dan lingkungan karena bersifat toksik. Oleh karena itu saat ini sedang dikembangkan green inhibitor (inhibitor yang ramah lingkungan) yang bersifat non-toksik,
20
asam-asam organik maupun asam-asam amino, dan alkaloid yang diketahui mempunyai kemampuan menghambat korosi (Oguzie, 2007). Green inhibitor dari tumbuhan, yang sering digunakan biasanya berbentuk ekstrak. Pada ekstrak daun ketapang (Terminalia catappa L.), sifat inhibisi dan adsorpsinya disebabkan karena adanya saponin, tanin, flavanoid, terpen dan alkaloid (Rani and Basu, 2011).
3. Mekanisme Proteksi dengan Green Inhibitor (Inhibitor Ramah Lingkungan)
Pada mekanisme proteksi dengan menggunakan ekstrak bahan alam terhadap besi atau baja dari serangan korosi, reaksi yang terjadi yaitu antara logam Fe2+ dengan medium korosif air laut yang mengandung ion-ion klorida yang terurai dari NaCl, MgCl2, KCl bereaksi dengan Fe dan diperkirakan menghasilkan FeCl2 (Haryono
dkk, 2010). Jika ion klorida yang bereaksi semakin besar, maka FeCl2 yang
terbentuk juga akan semakin besar, seperti tertulis dalam reaksi berikut :
NaCl → Na+
+ Cl -MgCl2→ Mg2+ + 2Cl
-KCl → K+
+ Cl
-Ion klorida pada reaksi diatas akan menyerang logam besi (Fe) sehingga besi akan terkorosi menjadi :
2Cl- + Fe2+→ FeCl2
21
Fe → Fe2+
+ 2e- (melepaskan elektron) Fe2+ + 2e-→ Fe (menerima elektron)
Gambar 9. Mekanisme proteksi (Haryono dkk, 2010).
Produk yang terbentuk di atas mempunyai kestabilan yang tinggi dibanding dengan Fe saja, sehingga sampel besi atau baja yang diberikan inhibitor ekstrak bahan alam akan lebih tahan (terproteksi) terhadap korosi. Contoh lainnya, dapat juga dilihat dari struktur senyawa nikotin dan kafein yang terdapat dalam ekstrak daun tembakau, teh, dan kopi. Kafein dan nikotin yang mengandung gugus atom nitrogen akan menyumbangkan pasangan elektron bebasnya untuk mendonorkan elektron pada logam Fe2+ sehingga terbentuk senyawa kompleks dengan
mekanisme yang sama.
H. Analisis Korosi
1. Metode Gravimetri (Kehilangan Berat)
22
CR = 10 x Wt/A x 1/D x 365/t ... (1) Keterangan :
CR = laju korosi (mmpy)
Wt = berat (gram) yaitu selisih berat awal dengan berat akhir A = luas permukaan sampel (cm2)
D = density (gram/cm3) t = waktu perendaman
Efisiensi inhibisi (EI) dapat dihitung dengan persamaan berikut (Widharto, 2004). EI = (R0– Ri) x (1/R0) x 100 ... (2)
Keterangan :
R0 = laju korosi tanpa penambahan inhibitor
Ri = laju korosi dengan penambahan inhibitor
2. Metode Potensiometri
Potensiometri merupakan analisis yang didasarkan pada pengukuran beda potensial sel dari suatu sel elektrokimia. Alat yang digunakan untuk mengatur beda potensial adalah potensiostat.
Peralatan potensiostat dilengkapi dengan tiga jenis elektroda sebagai berikut. a. Elektroda kerja (Working Electrode) merupakan elektroda tempat reaksi
reduksi-oksidasi analit berlangsung. Elektroda ini umumnya terbuat dari logam b. Elektroda bantu (Auxiliary Electrode) merupakan elektroda yang berperan
sebagai sumber atau masuknya elektron sehingga arus dapat dilewatkan melalui sel.
c. Elektroda acuan (Reference Electrode) merupakan elektroda yang potensialnya dibuat konstan sehingga dapat digunakan sebagai pembanding terhadap
23
Potensiostat memberikan potensial yang telah ditentukan terlebih dahulu kepada baja lunak sehingga pengukuran arus selama proses korosi dapat dilakukan. Pada kesetimbangan reaksi oksidasi dan reduksi, permukaan besi akan memiliki potensial langsung terukur yang dikenal sebagai potensial korosi (Ecorr). Pada
Ecorr, kerapatan arus untuk oksidasi besi (jcorr Ox) disetimbangkan oleh kerapatan
arus untuk reaksi reduksi proton (jcor Red), sehingga arus yang terukur secara
langsung sama dengan nol. Namun, jcor dan akibat laju korosi per satuan luas
dapat ditentukan secara tidak langsung menggunakan polarisasi potensiodinamik, bentuk persamaan Butler-Volmer (persamaan 3) dan plot Tafel yaitu sebagai berikut.
j = j0 {e(1-α) fη - e- αfη}
Keterangan : f = nf/RT, η = Eapplied - Ecorr ... (3) α = koefisien transfer
Istilah eksponensial pertama dalam persamaan tersebut sesuai dengan komponen Ketika overpotential (η) bernilai besar dan positif, sesuai dengan elektroda kerja pada anoda selama elektrolisis, eksponensial kedua dalam persamaan (3) jauh lebih kecil dari yang pertama dan dapat diabaikan. Sehingga,
Ln |j| = Ln j0 + (1-α)fη ... (4)
Persamaan Tafel Anodik
Sebaliknya bila nilai (η) besar dan negatif, sesuai dengan elektroda kerja pada katoda selama elektrolisis, eksponensial pertama dalam persamaan (3) jauh lebih kecil daripada kedua, dan dapat diabaikan. Sehingga,
Ln |j| = Ln j0 -αfη ... (5)
24
Dalam kurva eksperimen i terhadap Eapplied diperoleh untuk scan katodik dan
anodik dari Ecorr, menggunakan potensiostat. Plot Tafel katodik dan anodik untuk
elektrode kerja besi yang dihasilkan dengan memetakan Ln|j| terhadap overpotential (η). Ekstrapolasi bagian linier dari plot Tafel untuk η = 0 memberikan nilai untuk Ln|jcorr|, yang mana densitas arus penukar korosi jcorr
dapat ditentukan dengan arus penukar korosi icorr untuk elektroda yang digunakan
(EDAQ, 2012). Tafel merupakan suatu persamaan dan reaksi dalam elektrokimia yang ditemukan oleh Julius Tafel.
Efisiensi inhibisi korosi dapat ditentukan dengan membandingkan selisih
kerapatan arus korosi logam dalam larutan blanko dan sampel terhadap kerapatan arus korosi logam dalam larutan blanko.
Efisiensi inhibitor dapat dinyatakan sebagai suatu ukuran untuk menunjukkan penurunan laju korosi sebagai berikut (Kuznetsov, 2002) :
EI = 100 x (icorr blangko - icorr inhibitor)/icorr blangko ... (6)
Keterangan :
icorr blangko = arus korosi tanpa penambahan inhibitor
icorr inhibitor = arus korosi dengan penambahan inhibitor
I. Scanning Electron Microscope - Energy Dispersive X-Ray Spectroscopy (SEM-EDS)
Mikroskop Pemindai Elektron (SEM) adalah jenis mikroskop elektron untuk memindai gambar permukaan suatu sampel padat dengan menggunakan sinar elektron berenergi tinggi dalam pola pemindai pixel (Fansuri dan N.
25
morfologi permukaan dari suatu obyek, seperti bahan logam dan polimer keramik yang tidak dapat dilihat dengan mata atau dengan mikroskop optik.
Prinsip kerja SEM, dengan cara mengalirkan arus pada kawat filamen tersebut dan
perlakuan pemanasan, sehingga dihasilkan elektron. Elektron tersebut
dikumpulkan dengan tegangan tinggi dan berkas elektron difokuskan dengan
sederetan lensa elektromagnetik. Ketika berkas elektron mengenai target,
informasi dikumpulkan melalui tabung sinar katoda yang mengatur intensitasnya.
Setiap jumlah sinar yang dihasilkan dari tabung sinar katoda dihubungkan dengan
jumlah target, jika terkena berkas elektron berenergi tinggi dan menembus
permukaaan target, elektron kehilangan energi, karena terjadi ionisasi atom dari
cuplikan padatan. Elektron bebas ini tersebar keluar dari aliran sinar utama,
sehingga tercipta lebih banyak elektron bebas, dengan demikian energinya habis
lalu melepaskan diri dari target. Elektron ini kemudian dialirkan ke unit
demagnifikasi dan dideteksi oleh detektor dan selanjutnya dicatat sebagai suatu
foto (Wagiyo dan Handayani, 1997).
Energy Dispersive X-ray Spectrometry (EDS) adalah sebuah teknik analisis yang
26
dapat mendeteksi semua elemen kecuali H, He, Li, dan Be. Penggambaran dan pemetaan sampel yang akan diukur dihubungkan dengan peralatan Scanning Electron Microscope (SEM), Electron Probe X-Ray Microanalysis (EPMA) dan
III. METODOLOGI PENELITIAN
A. Waktu dan Tempat Penelitian
Penelitian ini dilakukan pada bulan April 2012 sampai Januari 2013, bertempat di Laboratorium Kimia Organik Jurusan Kimia Fakultas MIPA Universitas
Lampung. Analisis spektroskopi, analisis permukaan dan analisis laju korosi dilakukan di Laboratorium Biomassa Universitas Lampung.
B. Alat dan Bahan
Alat penelitian yang digunakan pada penelitian ini meliputi alat-alat gelas, timbangan, vacum rotary evaporator, shaker, magnetic stirrer, mikropipet, potensiostat eDAQ model EA 161, sel tiga elektroda, multitester, lampu uv, spektrofotometer FTIR merk Scimitar 2000, spektrofotometer ultraungu-tampak (UV-VIS) dan spektrofotometer ultraungu-tampak varian cary 100 dan SEM-EDS (scanning electron microscopy – energy dispersive x-ray spectroscopy) merk Carl Zeiss/EVO MA 10.
Bahan utama yang digunakan pada penelitian ini adalah daun ketapang. Tanaman ini diperoleh dari depan GFB FMIPA UNILA. Bahan-bahan kimia yang
28
asetat p.a, gelatin, asam tanat, HCl, KBr, larutan FeCl3 1%, NaCl, gas CO2,
NaHCO3, etanol, metanol,baja lunak dan kertas amplas.
C. Prosedur Penelitian
1. Pengumpulan dan Persiapan Sampel
Daun ketapang dipilih yang masih berwarna hijau, dibersihkan, dipotong ukuran kecil kemudian dikeringkan dengan cara dijemur di bawah sinar matahari dan dihaluskan dengan cara digilingsampai diperoleh serbuk. Hasil yang diperoleh digunakan sebagai sampel penelitian.
2. Ekstraksi Tanin dari Daun Ketapang
Serbuk daun ketapang ditimbang sebanyak 100 gram kemudian dimaserasi selama 1x24 jam menggunakan 300 mL campuran pelarut aseton-air (7:3) dan dengan penambahan 2 mL asam askorbat 10 mM sebagai antioksidan. Setelah sampel dimaserasi, ekstrak daun ketapang disaring, lalu dipekatkan dengan menggunakan penguap putar vakum (vacum rotary evaporator) dan pemanasan di atas
waterbath pada suhu 40-50 °C. Filtrat hasil pemekatan diekstraksi dengan pelarut
29
3. Uji Fitokimia dengan Menggunakan FeCl3dan Gelatin
3.1 Uji Fitokimia dengan Menggunakan FeCl3
Filtrat, fraksi aseton-air 1 dan fraksi aseton-air 2 dimasukkan ke dalam
masing-masing tabung reaksi sebanyak 2 mL. Kemudian direaksikan dengan 3 tetes larutan FeCl3 1%. Jika ekstrak mengandung senyawa tanin akan
menghasilkan warna biru kehitaman (uji positif).
3.2 Uji Fitokimia dengan Menggunakan Gelatin
Filtrat, fraksi aseton-air 1 dan fraksi aseton-air 2 dimasukkan ke dalam
masing-masing tabung reaksi sebanyak 2 mL. Kemudian direaksikan dengan 3 tetes larutan gelatin 2%. Jika terbentuk endapan putih maka positif mengandung tanin.
4. Pemisahan Tanin dengan KLT Analitik
Fraksi aseton-air 2 dilihat pola pemisahannya dengan KLT analitik menggunakan plat silika G 60 F254 dan campuran eluen metanol-kloroform-air (5:3:1). Pola
pemisahan pada fraksi aseton-air 2 dibandingkan dengan pola pemisahan asam tanat yang digunakan sebagai standar. Kemudian noda pada kromatogram tersebut dilihat dibawah lampu UV setelah dilakukan elusi terhadap plat KLT. Noda yang terbentuk masing-masing diukur harga Rf nya.
5. Identifikasi Ekstrak Tanin dengan Spektrofotometer FTIR
Fraksi aseton-air 2 dianalisis menggunakan spektrofotometer FTIR. Fraksi
30
dengan bantuan alat penekan berkekuatan 8-10 ton per satuan luas. Kemudian pelet tersebut diukur puncak serapannya.
6. Identifikasi Ekstrak Tanin dengan Spektrofotometer Ultraungu-Tampak
Fraksi aseton-air 2 dihilangkan pelarut aseton terlebih dahulu, kemudian diencerkan 2000 kali menggunakan pelarut metanol. Pertama, sampel diukur serapan maksimumnya dalam metanol kemudian pada fraksi aseton-air 2 diukur serapan maksimumnya.
7. Persiapan Baja Lunak
Baja lunak dipotong-potong dengan ukuran 2x1 cm, kemudian diamplas dengan kertas amplas mulai grit 240, 400, 600 dan terakhir dengan grit 800. Setelah permukaan baja lunak rata selanjutnya dibersihkan dengan akuades lalu dibilas dengan aseton dan dikeringkan, kemudian disimpan dalam desikator.
Permukaannya diukur dimensinya lalu ditimbang massanya.
8. Pembuatan Medium korosif dan Larutan inhibitor
Air laut buatan (brine solution) dibuat dengan melarutkan 30 gram NaCl dan 0,1 gram NaHCO3 dengan akuades dalam labu ukur 1 L. Dan Larutan inhibitor
31
9. Analisis Laju Korosi
9.1 Metode Gravimetri (Kehilangan Berat)
Larutan korosif yang telah disiapkan dimasukkan ke dalam botol sebanyak 100 mL dan dijenuhkan dengan gas karbon dioksida selama 45 menit. Larutan inhibitor dengan berbagai konsentrasi ditambahkan ke dalam medium korosif, kecuali larutan blangko tidak ditambahkan larutan inhibitor. Sampel baja yang telah ditimbang massanya, dimasukkan ke dalam larutan medium korosif dengan dan tanpa inhibitor, lalu ditempatkan di atas shaker dan didiamkan selama 1 hari, 2 hari dan 3 hari pada suhu ruang. Sampel tersebut kemudian dikeluarkan dan dibersihkan dengan HCl 0,1 M, akuades serta dibilas dengan etanol, setelah kering semua sampel tersebut ditimbang kembali, lalu dilakukan perhitungan laju korosi (mmpy) dan persen proteksinya.
9.2 Metode potensiometri
9.2.1. Persiapan elektroda kerja baja lunak
Baja lunak ditentukan luas permukaannya yang akan tercelup ke dalam media korosif. Kemudian diamplas dengan kertas amplas mulai grit 240, 400, 600 dan terakhir dengan grit 800. Setelah permukaan baja lunak rata selanjutnya
dibersihkan dengan akuades lalu dibilas dengan etanol dan dikeringkan.
9.2.2 Pengaturan Alat
Potensiostat harus dipanaskan selama 10 menit. Stirrer bar dimasukkan ke dalam gelas kimia dan dituangkan 50 mL larutan media korosif, dengan penutup
styrofoam yang dilengkapi dengan elektroda bantu, elektroda kerja dan elektroda
32
magnetic stirrer. Stirrer bar diatur pada laju sedang dan gas karbon dioksida
dialirkan selama 10 menit. Kemudian elektroda kerja baja lunak dimasukkan setengah permukaan tercelup, dibiarkan dalam sel korosi selama 10 menit untuk menimbulkan reaksi oksidasi dan reduksi. Software Echem dibuka, pilih scan dan jika monitor sudah terhubung dengan alat potensiostat maka indikator pada potensiostat berwarna hijau. Kabel elektroda dengan kode warna merah diarahkan pada elektroda bantu (Pt), kabel elektroda dengan kode warna kuning diarahkan pada elektroda acuan (AgCl) dan kabel elektroda dengan kode warna hijau diarahkan pada elektroda kerja. Setelah dibiarkan 10 menit, diukur potensial dengan menggunakan multitester, di antara elektroda acuan (AgCl) dengan elektroda kerja. Potensial terukur sebesar 400 mV merupakan potensial korosi (Ecorr).
9.2.3. Scan Katodik
Pembacaan tegangan linier dimulai dari Ecorr sampai Ecorr -400mV. Elektroda
kerja dengan luas permukaan lebih dari 0,3 cm2 membutuhkan arus yang lebih tinggi dari 2 mA, yaitu 5 mA. Metode yang dipilih linier voltage sweep dan diatur dengan menu pada Echem sebagai berikut:
33
Aliran gas karbondioksida dihentikan namun tetap dialirkan di atas larutan dan larutan tetap diaduk. Klik start, proses ini membutuhkan waktu selama 3,3 menit. Selanjutnya, elektroda kerja baja lunak dipindahkan dari larutan. Gas karbondioksida dialirkan kembali.
9.2.4. Scan Anodik
Pembacaan tegangan linier dimulai dari dari Ecorr sampai Ecorr + 400mV.
Elektroda kerja dengan luas permukaan lebih dari 0,3 cm2 membutuhkan arus yang lebih tinggi dari 2 mA. Metode yang dipilih linier voltage sweep dan diatur dengan menu pada Echem sebagai berikut:
Batas tegangan maksimal : 1000 mV
Kecepatan : 10 kHz
Prosedur diulangi seperti pada scan katodik.
9.2.5. Inhibitor
34
9.2.6. Analisis Data Laju Korosi
Untuk proses pertama, grafik yang terbentuk pada hasil scan katodik dan anodik yang dengan dan tanpa menggunakan inhibitor, masing-masing diblok, copy special dipilih pada menu Edit Echem, simpan teks (arus yang terhitung). Data E
dan I akan diperoleh pada lembar kerja excel. Kolom pertama data dalam lembar kerja merupakan data Eapplied dan kolom kedua merupakan arus yang terukur (I).
Fungsi yang sesuai digunakan dan diisi pada lembar kerja, dihitung kolom overpotential (η = Eapplied– Ecorr, mV) kerapatan arus (j = I/luas permukaan dari
baja yang tercelup, A/cm2) dan Ln|j|. Diulangi langkah sebelumnya untuk melanjutkan dari data yang terkumpul. Plot tafel dibuat dengan memplotkan kerapatan arus Ln|j| terhadap overpotential (η). Lalu plot tafel dicetak dan dibuat garis pada bagian yang linier pada katodik dan anodik, garis diekstrapolasikan hingga diperoleh titik potong untuk memperoleh Ln|jcorr|. Dengan menggunakan
fungsi eksponensial, Ln|jcorr| dikonversi menjadi jcorr , kemudian dihitung nilai arus
korosi dan efisiensi inhibisinya.
10. Analisis Permukaan dan Komposisi Kimia Baja Lunak
Morfologi permukaan dan komposisi baja lunak dalam media korosif tanpa dan dengan penambahan inhibitor optimum pada waktu paparan optimum diamati menggunakan Scanning Electron Microscopy - Energy Dispersive X-Ray
Spectroscopy (SEM-EDS) yang dilakukan di Laboratorium Biomassa Universitas
V. SIMPULAN DAN SARAN
A. Simpulan
Berdasarkan penelitian yang telah dilakukan, maka diperoleh simpulan sebagai berikut:
1. Pelarut aseton-air dapat mengekstraksi tanin dari daun ketapang dengan baik 2. Ekstrak tanin cukup efektif sebagai inhibitor korosi baja lunak dalam medium
air laut buatan, yaitu inhibitor optimum pada konsentrasi 40% v/v dengan metode gravimetri pada paparan 3 hari dengan efisiensi inhibisi 60,87% dan dengan metode potensiometri pada paparan 10 menit efisiensi inhibisi 1,98%.
B.Saran
Berdasarkan hasil penelitian yang diperoleh pada penelitian ini, untuk penelitian selanjutnya disarankan :
1. Dilakukan pemurnian menggunakan kromatografi kolom dengan fase diam gel filtrasi sephadex untuk mendapatkan senyawa tanin murni.