PRA RANCANGAN PABRIK
PEMBUATAN GAS HIDROGEN DARI GAS ALAM (NATURAL GAS)
MELALUI PROSES STEAM REFORMING/ CRACKING
DENGAN KAPASITAS PRODUKSI 1200 TON/TAHUN
TUGAS AKHIR
Diajukan Untuk Memenuhi Persyaratan
Ujian Sarjana Teknik Kimia
OLEH :
NIM : 070425011
HOTMA PARDAMEAN TAMBUNAN
D E P A R T E M E N T E K N I K K I M I A
F A K U L T A S T E K N I K
UNIVERSITAS SUMATERA UTARA
M E D A N
LEMBAR PENGESAHAN
PRA RANCANGAN PABRIK
PEMBUATAN GAS HIDROGEN DARI GAS ALAM (NATURAL GAS) MELALUI PROSES STEAM REFORMING/ CRACKING
DENGAN KAPASITAS PRODUKSI 1200 TON/TAHUN
TUGAS AKHIR
Diajukan Untuk Memenuhi Persyaratan Ujian Sarjana Teknik Kimia
Oleh:
070425011
HOTMA PARDAMEAN TAMBUNAN
Telah Diperiksa / Disetujui,
Dosen Pembimbing I Dosen Pembimbing II
(Ir. Renita Manurung, MT)
NIP: 197806102002122003 NIP: 196812141997022002
(Farida Hanum, ST, MT)
Dosen Penguji I Dosen Penguji II Dosen Penguji III
(Ir. Renita Manurung, MT) Ir.Indra Surya, M.Sc
NIP: 197806102002122003 NIP: 19306091989031004 NIP: 196004251999032001 Ir. Netty Herlina, MT
Mengetahui, Koordinator Tugas Akhir
NIP 196808201995011001 Dr.Eng.Ir. Irvan, MSi
DEPARTEMEN TEKNIK KIMIA FAKULTAS TEKNIK
UNIVERSITAS SUMATERA UTARA MEDAN
KATA PENGANTAR
Segala puji dan syukur kepada Tuhan Yang Maha Kuasa atas segala berkat dan karunia-nya sehingga penulis dapat menyelesaikan tugas akhir ini, yang berjudul:
“Pra rancangan pabrik pembuatan gas hidrogen dari gas alam (natural gas) melalui
proses steam reforming/cracking dengan kapasitas produksi 1200 ton/tahun”.
Pra rancangan pabrik ini disusun untuk melengkapi tugas-tugas dan merupakan salah satu syarat untuk menempuh ujian sarjana pada Departemen Teknik Kimia, Fakultas Teknik, Universitas Sumatera Utara.
Penulis banyak menerima bimbingan, saran dan bantuan dari berbagai pihak dalam menyelesaikan tugas akhir ini. Untuk itu dengan segala ketulusan hati penulis mengucapkan terima kasih yang sebesar-besarnya kepada :
1. Ibu Ir. Renita Manurung, MT dan Ibu Ir. Farida Hanum, ST, MT selaku Dosen
Pembimbing I dan II yang telah banyak memberikan masukan dan bimbingan selama Penulis menyusun Tugas Akhir ini.
2. Bapak Dr.Eng Ir. Irvan, M.Si, Koordinator Tugas Akhir Departemen Teknik Kimia,
Fakultas Teknik, Universitas Sumatera Utara
3. Ibu Ir. Renita Manurung, MT, Ketua Jurusan Departemen Teknik Kimia, Fakultas
Teknik, Universitas Sumatera Utara
4. Bapak M. Hendra Sahputra Ginting ST, MT., Sekretaris Jurusan Departemen Teknik
Kimia, Fakultas Teknik, Universitas Sumatera Utara
5. Seluruh staf pengajar Departemen Teknik Kimia yang telah memberikan banyak filosofi
ilmu teknik kimia.
6. Para pegawai administrasi Departemen Teknik Kimia yang telah memberikan bantuan
selama Penulis mengenyam pendidikan di Teknik Kimia.
7. Kedua orang tua penulis yang telah banyak berkorban materi dan memberikan didikan
serta doa untuk penulis.
8. Abang dan Kakak beserta seluruh keluarga penulis yang selalu memberikan dukungan
dan semangat kepada penulis.
9. Abang dan Kakak stambuk, atas setiap informasi dan saran yang diberikan dalam
penyusunan tugas akhir ini.
10.Teman-teman Angkatan 2007 yang telah banyak memberikan motivasi, dorongan, dan
11.Seluruh pihak yang tidak dapat disebutkan satu persatu namanya yang turut memberikan bantuan kepada Penulis dalam menyelesaikan tugas akhir ini.
Penulis menyadari bahwa tugas akhir ini masih jauh dari kesempurnaan. Untuk itu, Penulis mengharapkan saran dan kritik yang konstruktif dari pembaca. Akhir kata, semoga tugas akhir ini dapat memberi manfaat kepada seluruh pembaca, khususnya mahasiswa/i Teknik Kimia.
Medan, September 2010
Penulis,
NIM : 070425011
INTISARI
Gas Hidrogen diperoleh melalui proses Cracking atau yang biasa disebut Steam reforming antara Gas alam dengan steam dengan bantuan katalis Nikel didalam reaktor tungku pipa pada temperatur tinggi dan tekanan yang tinggi sehingga akan dihasilkan gas hidrogen dan carbon monoksida, karena carbon monoksida tidak diinginkan maka karbon monoksida di reaksikan dengan steam didalam catalytic fixed multibed reactor yang disebut
high temperatur shift dimana di hasilkan gas hidrogen dengan karbon dioksida.
Pabrik pembuatan gas hidrogen ini direncanakan berproduksi dengan kapasitas 150
kg/jam dengan masa kerja 300 hari dalam satu tahun. Lokasi pabrik direncanakan di daerah
Dumai, Pekanbaru, Riau dengan luas areal 10.000 m2. Tenaga kerja yang dibutuhkan 200
orang dengan bentuk badan usaha Perseroan Terbatas (PT) yang dipimpin oleh seorang
Direktur dengan struktur organisasi sistem garis dan staff.
Hasil analisa ekonomi pabrik pembuatan Hidrogen ini adalah sebagai berikut:
• Total Modal Investasi : Rp. 256.527.684.098,-
• Total Biaya Produksi : Rp. 106.676.787.342,-
• Hasil Penjualan : Rp. 222.003.284.518,-
• Laba Bersih : Rp. 80.433.401.803,-
• Profit Margin (PM) : 51,747 %
• Break Even Point (BEP) : 47,244 %
• Return on Investment (ROI) : 31,355 %
• Pay Out Time (POT) : 3,189 tahun
• Return on Network (RON) : 52,258 %
• Internal Rate of Return (IRR) : 49,388 %
DAFTAR ISI
Hal
PRAKATA ... i
INTISARI ... iii
DAFTAR ISI ... iv
DAFTAR TABEL ... vii
DAFTAR GAMBAR ... xii
DAFTAR LAMPIRAN ... xiii
BAB I PENDAHULUAN... I-1
1.1 Latar Belakang ... I-1 1.2 Perumusan Masalah ... I-2 1.3 Tujuan Pra Rancangan Pabrik ... I-2 1.4 Ruang Lingkup Perancangan ... I-3 1.5 Manfaat Perancangan ... I-3
BAB II TINJAUAN PUSTAKA ... II-1
2.1 Gambaran Umum Hidrogen ... II-1 2.2 Penggunaan Hidrogen ... II-3 2.3 Gas Alam ... II-4 2.4 Pemanfaatan Gas Alam ... II-6 2.5 Cadangan Gas Alam Dunia ... II-8 2.6 Proses Pembuatan Hidrogen ... II-8 2.6.1 Steam Methane Reforming (SMR) ... II-9 2.6.2 Oksidasi Parsial ... II-10
2.6.3 Integrated gasification combined cycle (IGCC) ... II-11 2.6.4 Pirolisis ... II-12 2.6.5 Elektrolisis air ... II-12 2.6.6 Produksi hidrogen secara biologi ... II-12
2.8.4 Unit pendinginan gas proses ... II-15 2.8.5 Unit Penyerap impurities(Pressure swing adsorbtion) ... II-16 2.9 Spesifikasi Bahan Pendukung... II-17
BAB III NERACA MASSA ...III
BAB IV NERACA PANAS ... IV-1
BAB V SPESIFIKASI PERALATAN ... V-1
BAB VI INSTRUMENTASI DAN KESELAMATAN KERJA ... VI-1
6.1 Instrumentasi ... VI-1 6.1.1 Tujuan Pengendalian ... VI-2 6.1.2 Jenis-Jenis Pengendalian dan Alat Pengendali ... VI-3 6.1.3 Variabel-Variabel Proses dalam Sistem Pengendalian... VI-9
6.1.4 Syarat Perancangan Pengendalian ... VI-18 6.2 Keselamatan Kerja ... VI-17 6.3 Keselamatan Kerja Pabrik Pembuatan Hidrogen ... VI-18
BAB VII UTILITAS ...V11-1
7.1 Kebutuhan Uap (Steam) ... VII-2 7.2 Kebutuhan Air ... VII-2 7.2.1 Kebutuhan air proses ... VII-2 7.2.2 Kebutuhan air lainnya... VII-3 7.2.3 Screening ... VII-6 7.2.4 Sedimentasi ... VII-6 7.2.5 Klarifikasi ... VII-6 7.2.6 Filtrasi ... VII-7 7.2.7 Demineralisasi ... VII-8 7.2.7.1 Penukar Kation (Cation Exchanger)... VII-8 7.2.5.2 Penukar Anion (Anion Exchanger) ... VII-10 7.2.8 Deaerator... VII-12 7.3 Kebutuhan Bahan Kimia ... VII-12 7.4 Kebutuhan Listrik ... VII-13 7.5 Kebutuhan Bahan Bakar ... VII-14 7.6 Unit Pengolahan Limbah... VII-14
7.6.4 Unit Pengolahan Limbah dengan Sistem Trickling Filter .. VII-17 7.6.5 Tangki Sedimentasi (TS) ... VII-20 7.7 Spesifikasi Peralatan Utilitas ... VII-21
BAB VIII LOKASI DAN TATA LETAK PABRIK ...VIII-1
8.1 Lokasi Pabrik ...VIII-1 8.2 Tata Letak Pabrik ...VIII-3 8.3 Perincian luas tanah ...VIII-4
BAB IX ORGANISASI DAN MANAJEMEN PERUSAHAAN ... IX-1
9.1 Organisasi Perusahaan ... IX-1 9.1.1 Bentuk Organisasi Garis ... IX-2 9.1.2 Bentuk Organisasi Fungsionil ... IX-2
9.1.3 Bentuk Organiasi Garis dan Staf ... IX-3 9.1.4 Bentuk Organisasi Fungsionil dan Staf ... IX-3 9.2 Manajemen Perusahaan ... IX-3 9.3 Bentuk Hukum Badan Usaha ... IX-4
9.4 Uraian Tugas, Wewenang dan Tanggung Jawab... IX-6 9.4.1 Rapat Umum Pemegang Saham (RUPS)... IX-6 9.4.2 Dewan Komisaris ... IX-6 9.4.3 Direktur ... IX-7 9.4.4 Sekretaris ... IX-7 9.4.5 Manager Produksi ... IX-7 9.4.6 Manager Teknik ... IX-7 9.4.7 Manager Umum dan Keuangan ... IX-8 9.4.8 Manager Pembelian dan Pemasaran ... IX-8 9.5 Sistem Kerja ... IX-8 9.6 Jumlah Karyawan dan Tingkat Pendidikan ... IX-9 9.7 Sistem Penggajian ... IX-11 9.8 Tata Tertib ... IX-12 9.9 Jamsostek dan Fasilitas Tenaga Kerja ... IX-13
BAB X ANALISA EKONOMI ... X-1
10.1 Modal Investasi... X-1
10.1.3.1 Biaya Tetap / Fixed Cost (FC) ... X-4 10.1.3.2 Biaya Variabel / Variable Cost (VC) ... X-5 10.2 Total Penjualan (Total Sales) ... X-5 10.3 Bonus Perusahaan ... X-5 10.4 Perkiraan Rugi/Laba Usaha ... X-5 10.5 Analisa Aspek Ekonomi ... X-6 10.5.1 Profit Margin (PM) ... X-6 10.5.2 Break Even Point (BEP) ... X-6 10.5.3 Return on Investment (ROI) ... X-7 10.5.4 Pay Out Time (POT) ... X-7 10.5.5 Return on Network (RON) ... X-8
10.5.6 Internal Rate of Return (IRR) ... X-8
BAB XI KESIMPULAN ... XI-1
11.1 Kesimpulan ... XI-1
DAFTAR LAMPIRAN
Hal LAMPIRAN A PERHITUNGAN NERACA MASSA ... LA-1
DAFTAR TABEL
Hal Tabel 1.1 Kebutuhan Impor Hidrogen di Indonesia ... I-2 Tabel 2.1 Sifat Termodinamiks dan Fisik dari Hidrogen gas... II-2 Tabel 2.2 Sifat Termodinamiks dan Fisik dari Hidrogen Cair ... II-2 Tabel 2.3 Komposisi Natural Gas (Gas Alam) ... II-5 Tabel 3.1 Neraca Massa pada Desulfurisasi (R-201) ... III-1 Tabel 3.2 Neraca Massa pada Pencampur Gas (M-201) ... III-2 Tabel 3.3 Neraca Massa pada Reformer furnaces (R-301) ... III-3 Tabel 3.4 Neraca Massa pada High Temperatur Shift (R-401) ... III-4 Tabel 3.5 Neraca Massa pada Knok Out Drum (KOD-401) ... III-5 Tabel 3.6 Neraca Massa pada Pressure Swing Adsorpsi (A-501) ... III-6 Tabel 3.7 Neraca Massa pada Mixing bahan bakar ... III-7 Tabel 3.8 Neraca Massa pada Untuk Pembakaran di Reformer Furnace ... III-8 Tabel 4.1 Neraca Panas pada Feed Preheater 1 (E-401) ... IV-1
Tabel 6.1 Jenis Variabel Pengukuran dan Controller yang dipakai ... VI-6 Tabel 6.3 Daftar Instrumentasi pada Pra Rancangan Pabrik Hidrogen ... VI-11 Tabel 7.1 Kebutuhan Uap Air (Steam) Proses... VII-1 Tabel 7.2 Kebutuhan Air Pendingin Proses ... VII-2 Tabel 7.3 Pemakaian Air Untuk Berbagai Kebutuhan... VII-4 Tabel 7.4 Kualitas Air Sungai Rokan, Riau ... VII-5 Tabel 8.1 Perincian Luas Tanah ...VIII-5 Tabel 9.1 Jadwal Kerja Karyawan Shift ... IX-9 Tabel 9.2 Jumlah Karyawan dan Kualifikasinya ... IX-10 Tabel 9.3 Perincian Gaji Karyawan ... IX-11 Tabel LA.1 Komposisi Gas Alam Dan Berat Molekulnya ... LA-1
Tabel LA.2 Komponen Umpan Gas Alam ... LA-2 Tabel LA.3 Neraca Massa Reaktor Desulfurisasi ... LA-4 Tabel LA.4 Total Mol Komponen C dalam Umpan ... LA-5 Tabel LA.5 Neraca Massa pada Mixing Point ... LA-12
Tabel LA.6 Neraca Massa pada Steam Reformer ... LA-12 Tabel LA.7 Neraca Massa pada High Temperatur Converter... LA-14 Tabel LA.8 Neraca Massa pada Knock Out Drum ... LA-17 Tabel LA.9 Neraca Massa di PSA ... LA-20 Tabel LA.10 Neraca Massa Mixing Point Bahan Bakar ... LA-29 Tabel LA.11 Neraca Massa Bahan Bakar Reformer Furnace ... LA-39 Tabel LB.1 Kapasitas Panas Gas ... LB-1 Tabel LB.2 Panas Pembakaran ... LB-2 Tabel LB.3 Panas Reaksi Pembentukan ... LB-3 Tabel LB.4 Data air pemanas dan air pendingin yang digunakan ... LB-3 Tabel LB.5 Neraca Panas Feed Preheater (E101) ... LB-7 Tabel LB.6 Neraca Panas Reaktor Desulfurisasi (R-101) ... LB-6 Tabel LB.7 Neraca Panas Mixing Point ... LB-12 Tabel LB.8 Neraca Panas Steam Reformer (R-301 ) ... LB-19 Tabel LB.9 Neraca Panas Steam Superheater (H-303) ... LB-20 Tabel LB.10 Neraca Panas Water Preheater (H-302) ... LB-21
Tabel LB.14 Neraca Panas Water Cooler I (E-402) ... LB-34 Tabel LB.15 Neraca panas Water Cooler II (E-403) ... LB-36 Tabel LB.16 Neraca Panas Water Cooler III (E-404) ... LB-38 Tabel LB.17 Neraca Panas KOD (D-401) ... LB-40 Tabel LB.18 Neraca panas PSA (A-501) ... LB-42 Tabel LB.19 Neraca Panas Kompresor (C-501) ... LB-44 Tabel LC.1 Viskositas Bahan Heater I pada tc = 432,5 0F ... LC-9 Tabel LC.2 Viskositas Bahan Heater I pada tc = 705 0F ... LC-10
Tabel LD-1 Perhitungan Entalpi dalam Penentuan Tinggi Cooling Tower .... LD-118
Tabel LE.1 Perincian Harga Bangunan, dan Sarana Lainnya ... LE-2 Tabel LE.2 Harga Indeks Marshall dan Swift ... LE-3
Tabel LE.3 Estimasi Harga Peralatan Proses Impor... LE-6 Tabel LE.4 Estimasi Harga Peralatan Proses Non Impor ... LE-7 Tabel LE.5 Estimasi Harga Peralatan Utilitas Impor ... LE-7 Tabel LE.6 Estimasi Harga Peralatan Utilitas Non Impor ... LE-8
Tabel LE.7 Biaya Sarana Transportasi ...LE-11 Tabel LE.8 Perincian Gaji Pegawai ...LE-15 Tabel LE.9 Perincian Biaya Kas ...LE-18 Tabel LE.10 Perincian Modal Kerja ...LE-19 Tabel LE.11 Aturan Depresiasi Sesuai UU Republik Indonesia
No.17 Tahun 2000 ...LE-20 Tabel LE.12 Perhitungan Biaya Depresiasi Sesuai UU RI
DAFTAR GAMBAR
Gambar 2.1 Diagram Alir Blok Produksi Gas Hidrogen Dari Gas Alam
dengan Proses Cracking/ Steam Reforming ... II-20 Gambar 6.1 Diagram Balok Sistem Pengendalian Feedback ... VI-4
Gambar 6.2 Sebuah loop Pengendalian ... VI-5 Gambar 6.3 Suatu Proses Terkendali ... VI-5 Gambar 6.4 Instrumentasi pada tangki ... VI-12 Gambar 6.5 Instrumentasi pada Pompa ... VI-12 Gambar 6.6.1 Instrumentasi pada Reaktor Desulfurisasi (R-201)... VI-13 Gambar 6.6.2 Instrumentasi pada Reaktor Steam Reformer (R-301) ... VI-14 Gambar 6.6.3 Instrumentasi pada Reaktor Converter (R-401) ... VI-14 Gambar 6.7 Instrumentasi Cooler dan Heater... VI-15 Gambar 6.8 Instrumentasi Knock Out Drum ... VI-15 Gambar 6.9 Instrumentasi Pressure Swing Adsorbtion ... VI-16 Gambar 6.10 Instrumentasi Kompresor dan Blower ... VI-16 Gambar 6.11 Tingkat kerusakan di suatu pabrik ... VI-17 Gambar 8.1 Peta lokasi pabrik Hidrogen ...VIII-1 Gambar 9.1 Bagan Struktur Organisasi Perusahaan Pra Rancangan
Pabrik Pembuatan Hidrogen ... IX-13 Gambar LC-2 Radially Split Multistage Compressor ... LC-5 Gambar LC-3 Preheater tipe 1 - 2 Shell and Tube Heat Exchanger ... LC-7 Gambar LC-4 Desulphurizer vessel ... LC-14
Gambar LC-5 Konfigurasi umum Steam Reformer ... LC-18 Gambar LC-6 Cooler tipe 2 - 4 Shell and Tube Heat Exchanger ... LC-24
Gambar LC-7a High Temperature Shift (HTS) Reactor ... LC-29 Gambar LC-7b Tutup Reaktor HTS menggunakan torispherical head ... LC-33 Gambar LC-8 Cooler tipe 1 - 2 Shell and Tube Heat Exchanger ... LC-34
Gambar LC-9 Cooler tipe 1 - 2 Shell and Tube Heat Exchanger ... LC-39
Gambar LC-11b Tutup knock out drum menggunakan torispherical head ... LC-52 Gambar LC-12a Unit Pressure Swing Adsroption (PSA) ... LC-53 Gambar LC-12b Tutup PSA menggunakan torispherical head ... LC-59 Gambar LC-13 Tangki PSA Off-gas ... LC-60 Gambar LC-14 Compressor Hydrogen ... LC-65 Gambar LC-15 3-D arrangement of an hydrogen plant ... LC-75 Gambar LD-1 Sketsa Sebagian Bar Screen (dilihat dari atas) ... LD-1 Gambar LD-2 Sketsa pompa P-701 (dilihat dari samping)... LD-3 Gambar LD-3 Sketsa 3D Bak Sedimentasi ... LD-8 Gambar LD-4 Sketsa Pompa sedimentasi (P-702) ... LD-10 Gambar LD-5A Sketsa tangki pelarutan asam (T-701) ... LD-15
Gambar LD-5B Sketsa pengaduk tangki pelarutan alum (T-701) ... LD-18 Gambar LD-6 Sketsa pompa alum (P-703) ... LD-19 Gambar LD-7A Sketsa tangki pelarutan soda abu (T-702) ... LD-25 Gambar LD-7B Sketsa pengaduk tangki pelarutan soda abu (T-702) ... LD-28
Gambar LD-8 Sketsa pompa soda abu (P-704) ... LD-29 Gambar LD-9 Sketsa clarifier (C-701) ... LD-35 Gambar LD-10 Sketsa 3D Bak penampung hasil clarifier (B-702) ... LD-38 Gambar LD-11 Sketsa pompa clarifier (P-705) ... LD-40 Gambar LD-12 Tangki sand filter (F-702) ... LD-45 Gambar LD-13 Sketsa pompa sand filter (P-706) ... LD-48 Gambar LD-14 SketsaTangki Air (T-704)... LD-54 Gambar LD-15a Sketsa tangki pelarutan Asam Sulfat (T-706) ... LD-56 Gambar LD-15b Sketsa pengaduk tangki pelarutan asam sulfat ... LD-59 Gambar LD-16 Sketsa pompa asam sulfat (P-709) ... LD-60 Gambar LD-17 Sketsa Cation Exchanger (S-701) ... LD-66 Gambar LD-18 Sketsa pompa Cation Exchanger (P-707) ... LD-68 Gambar LD-19 Sketsa Anion Exchanger (S-702) ... LD-75 Gambar LD-20a Sketsa tangki pelarutan NaOH (T-707) ... LD-74 Gambar LD-20b Sketsa pengaduk tangki pelarutan NaOH ... LD-78 Gambar LD-21 Sketsa pompa NaOH (P-710) ... LD-79
Gambar LD-25a Sketsa tangki pelarutan Kaporit (T-703) ... LD-98 Gambar LD-25b Sketsa pengaduk tangki pelarutan Kaporit ... LD-101 Gambar LD-26 Sketsa tangki Domestik (T-705) ... LD-102 Gambar LD-27 Sketsa pompa Domestik (P-712) ... LD-104 Gambar LD-28 Sketsa Deaerator (D-701) ... LD-109 Gambar LD-29 Sketsa Pompa Deaerator (P-713) ... LD-112 Gambar LD-30a Sketsa Water Cooling Tower (M-701) ... LD-117 Gambar LD-30b Grafik Entalpi dan Temperatur Cairan Cooling Tower ... LD-118 Gambar LD-30c Kurva Hy terhadap 1/(Hy*– Hy) ... LD-119 Gambar LD-31 Sketsa pompa Water Cooling Tower (P-714) ... LD-120 Gambar LD-31 Sketsa Steam Turbine (M-601) ... LD-125
INTISARI
Gas Hidrogen diperoleh melalui proses Cracking atau yang biasa disebut Steam reforming antara Gas alam dengan steam dengan bantuan katalis Nikel didalam reaktor tungku pipa pada temperatur tinggi dan tekanan yang tinggi sehingga akan dihasilkan gas hidrogen dan carbon monoksida, karena carbon monoksida tidak diinginkan maka karbon monoksida di reaksikan dengan steam didalam catalytic fixed multibed reactor yang disebut
high temperatur shift dimana di hasilkan gas hidrogen dengan karbon dioksida.
Pabrik pembuatan gas hidrogen ini direncanakan berproduksi dengan kapasitas 150
kg/jam dengan masa kerja 300 hari dalam satu tahun. Lokasi pabrik direncanakan di daerah
Dumai, Pekanbaru, Riau dengan luas areal 10.000 m2. Tenaga kerja yang dibutuhkan 200
orang dengan bentuk badan usaha Perseroan Terbatas (PT) yang dipimpin oleh seorang
Direktur dengan struktur organisasi sistem garis dan staff.
Hasil analisa ekonomi pabrik pembuatan Hidrogen ini adalah sebagai berikut:
• Total Modal Investasi : Rp. 256.527.684.098,-
• Total Biaya Produksi : Rp. 106.676.787.342,-
• Hasil Penjualan : Rp. 222.003.284.518,-
• Laba Bersih : Rp. 80.433.401.803,-
• Profit Margin (PM) : 51,747 %
• Break Even Point (BEP) : 47,244 %
• Return on Investment (ROI) : 31,355 %
• Pay Out Time (POT) : 3,189 tahun
• Return on Network (RON) : 52,258 %
• Internal Rate of Return (IRR) : 49,388 %
BAB I
PEDAHULUAN
1.1 Latar belakang
Kemajuan industri di Indonesia dewasa ini cukup pesat, terutama dalam bidang pemanfaatan hasil-hasil pertanian, perkebunan, pertambangan, dan berbagai jenis hasil hutan. Kemajuan tersebut ditujukan untuk mendukung program pemerintah dalam pemanfaatan sumber daya bagi keperluan industri baik dalam negeri maupun luar negeri. Salah satu sumber daya alam yang tidak dapat diperbaharui adalah gas alam, yang biasanya diperoleh dari dari dalam sumur dibawah perut bumi yang biasanya bergabung dengan minyak bumi. Indonesia berpotensi sebagai produsen bahan-bahan produksi gas alam bila di kelola secara
intensif dan berpola pada permintaan pasar dalam negeri dan peluang ekspor.
Gas alam (natural gas) dewasa ini menjadi sumber alternatif yang banyak digunakan oleh masyarakat dunia untuk berbagai keperluan, baik untuk perumahan, komersial maupun industri. Di dalam dunia industri gas alam (natural gas) dipergunakan untuk bahan baku
plastik, bahan baku pabrik pupuk, petrokimia, dan bahan dasar pembuatan hidrogen. Salah satu jenis produk industri non pangan yang dibutuhkan dan pemakaiannya terus meningkat akibat permintaan semakin banyak adalah hidrogen. Pada pra rancangan pabrik ini, pembuatan hidrogen dilakukan dengan menggunakan bahan baku berupa gas alam (natural
gas ) dengan proses cracking.
Kebutuhan hidrogen di Indonesia dapat dilihat pada tabel 1.1. Hidrogen bukanlah sumber energi (energy source) melainkan pembawa energi (energy carier), artinya hidrogen tidak tersedia bebas di alam atau dapat ditambang layaknya sumber energi fosil tetapi dapat dihasilkan melalui proses-proses tertentu. Salah satu cara untuk menghasilkan gas hidrogen adalah dengan proses cracking gas alam.
Tabel 1.1 Kebutuhan impor hidrogen di Indonesia
Tahun Impor Jumlah (kg)
2007 37.819
2006 353.363
2005 918.869
2004 286.675
2003 11.210
Dari tabel 1.1 kebutuhan impor hidrogen di Indonesia pada tahun 2003-2007 selalu
fluktuatif. Impor hidrogen mengalami penurunan pada tahun 2003 dan mengalami
peningkatan pada tahun 2005 dan mengalami penurunan kembali pada tahun 2007.
1.2 Perumusan Masalah
Untuk memenuhi kebutuhan hidrogen di dalam negeri sampai saat ini Indonesia masih mengimpor, disebabkan karena perkembangan indusrti di indonesia semakin meningkat sehingga kebutuhan akan hidrogen juga meningkat, dan pabrik penghasil hidrogen di Indonesia masih belum banyak, sehingga diperlukan suatu usaha agar permintaan hidrogen dapat dipenuhi dengan cara mendirikan pabrik hidrogen. Pra rancangan pabrik hidrogen ini menggunakan bahan baku utama gas alam (natural gas), dimana bahan bakunya diperoleh
dari perusahan gas alam atau pertamina. Pemilihan bahan baku ini didasarkan atas pertimbangan bahwa proses cracking gas alam (natural gas) atau yang biasa disebut steam
reforming merupakan salah alternatif untuk menghasilkan hidrogen yang kemurniannya
lebih tinggi dan gas alam memiliki komposisi metana yang tinggi yang merupakan salah satu
komponen yang dibutuhkan dalam pembuatan hidrogen.
1.3 Tujuan Perancangan
Tujuan perancangan pabrik pembuatan hidrogen dari gas alam (natural gas) dengan proses cracking adalah untuk mengaplikasikan ilmu teknik kimia yang meliputi neraca massa, neraca energi, spesifikasi peralatan, operasi teknik kimia, utilitas, dan bagian ilmu teknik kimia lainnya, juga gambaran untuk memenuhi aspek ekonomi dalam pembiayaan pabrik sehingga memberikan gambaran kelayakan pra perancangan pabrik pembuatan hidrogen dari gas alam (natural gas) dengan proses cracking.
1.4 Ruang Lingkup Perancangan
Ruang lingkup dari perancangan pabrik hidrogen dari gas alam (natural gas) dengan proses cracking adalah sebagai berikut:
a. Proses persiapan bahan baku yang bertujuan untuk menghilangkan kandungan sulfur
(H2S) yang terdapat didalam gas alam.
b. Proses pembentukan hidrogen dimana gas alam dicampur dengan steam dari boiler di
c. Recovery panas dari proses gas keluar, dimana dalam proses recovery panas yang
dihasilkan dari reaksi pembentukan gas hidrogen digunakan untuk keperluan proses melalui beberapa alat penukar panas.
d. Proses pemurnian hidrogen dengan sistem PSA (pressure swing adsorption ) yaitu
pemisahan gas hidrogen dari impuritisnya seperti H2O, CO, CO2 dan CH4 yang tidak
bereaksi.
e. Untuk menyempurnakan pra-rancangan pabrik juga dilakukan atau disampaikan
pembahasan tentang aspek-aspek : instrumentasi dan keselamatan kerja, utilitas pabrik, lokasi dan tata letak pabrik, organisasi dan manajemen perusahaan, dan analisa ekonomi perusahaan.
1.5 Manfaat Perancangan
Manfaat pra rancangan pabrik pembuatan pembuatan hidrogen dari gas alam dengan proses cracking adalah memberi gambaran kelayakan (feasibility) dari segi rancangan dan ekonomi pabrik ini untuk dikembangkan di Indonesia. Dimana nantinya gambaran tersebut
menjadi patokan untuk pengambilan keputusan terhadap pendirian pabrik tersebut. Pembuatan hidrogen dari gas alam dengan proses cracking diharapkan memenuhi kebutuhan dalam negeri Indonesia di masa yang akan datang.
BAB II
TINJAUAN PUSTAKA
2.1 Gambaran umum hidrogen
Hidrogen telah digunakan bertahun-tahun sebelum akhirnya dinyatakan sebagai unsur yang unik oleh Cavendish di tahun 1776. Dinamakan hidrogen oleh Lavoisier, hidrogen adalah unsur yang terbanyak dari semua unsur di alam semesta. Elemen-elemen yang berat pada awalnya dibentuk dari atom-atom hidrogen atau dari elemen-elemen yang mulanya
terbuat dari atom-atom hidrogen. Hidrogen diperkirakan membentuk komposisi lebih dari 90% atom-atom di alam semesta (sama dengan tiga perempat massa alam semesta). Dalam keadaan yang normal, gas hidrogen merupakan campuran antara dua molekul, yang dinamakan ortho- dan para- hidrogen, yang dibedakan berdasarkan spin elektron-elektron dan nukleus.Hidrogen normal pada suhu ruangan terdiri dari 25% para hidrogen dan 75% ortho-hidrogen. Bentuk ortho tidak dapat dipersiapkan dalam bentuk murni. Karena kedua bentuk tersebut berbeda dalam energi, sifat-sifat kebendaannya pun juga berbeda. Titik-titik lebur dan didih parahidrogen sekitar 0.1 derajat Celcius lebih rendah dari hidrogen normal.
Hidrogen (hidrogenium, simbol H), dalam tabel periodik unsur memiliki Ar =
1,00797, nomor atom 1, konfigurasi elektron 1s1. Biasanya dalam oksidasi dinyatakan +1, tapi dalam garam tipe hidrida -1 adalah juga mungkin. Tiga isotop dengan Ar 1, 2 dan 3 telah
diketahui; isotop dengan Ar 3 adalah tidak stabil. Perbedaan dalam massa isotop relatif adalah
sedemikian besar sehingga sifat kinetika dan fisik juga sangat berbeda. Isotop dengan massa relatif 2 dinamakan Deuterium (simbol D), dan pada massa relatif 3 dinamakan Tritium (Simbol T). Pada atom nukleus, semua muatan positif tunggal dinamakan proton, deuteron, dan triton. Sifat termodinamika dan fisik dari hidrogen padatan dapat dilihat pada Tabel 2.1,
Tabel 2.1 Sifat termodinamika dan fisik dari hidrogen gas
Sifat Hidrogen
Para- Normal
Densitas pada 0 oC, (mol/cm3) × 103 0,05459 0,04460
Faktor kompresibilitas, Z = PV/RT, pada 0 oC 1,0005 1,00042
Kompresibilitas adiabatik, (–∂V/V∂P)s, pada 300 K, MPa-1 b 7,12 7,03
Koefisien ekspansi volume, (–∂V/V∂T)p, pada 300 K, K-1 0,00333 0,00333
Cp pada 0 oC, J/(mol.K) c 30,35 28,59
Cv pada 0 oC, J/(mol.K) c 21,87 20,30
Entalpi pada 0 oC, J/mol c d 7656,6 7749,2
Energi dalam pada titik lebur, J/mol c d 5384,5 5477,1
Entropi pada titik lebur, J/(mol.K) c d 127,77 139,59
Kecepatan suara, m/s 1246 1246
Viskositas, mPas (=cp) 0,00839 0,00839
Konduktivitas termal pada titik lebur, mW/(cm.K) 1,841 1,740
Konstanta dielektrik pada titik lebur 1,00027 1,000271
Kompresibilitas isotermal, 1/V(∂V/V∂P)T , Mpa-1 b -9,86 -9,86
Koefisien difusi-diri pada 0 oC, cm2/s – 1,285
Difusivitas gas dalam air pada 25 oC, cm2/s – 4,8 × 10-5
Diameter benturan, σ, m × 1010 – 2,928
Parameter interaksi, Є/k, K – 37,00
Panas disosiasi pada 298,16 K, kJ/mol c 435,935 435,881
Catatan : a semua nilai pada 101,3 kPa (1 atm)
b
untuk konversi Mpa ke atm, dibagi dengan 0,101
c
untuk konversi J ke cal, dibagi dengan 4,184
d
titik dasar (nilai nol) untuk entalpi, energi dalam, dan entropi adalah 0 K untuk gas ideal pada tekanan 101,3 kPa (1 atm)
Tabel 2.2 Sifat termodinamika dan fisik dari hidrogen cair
Sifat Hidrogen
Para- Normal
Titik lebur, K (triple point) 13,803 13,947
Titik didih normal, K 20,268 20,380
Suhu kritis, K 32,976 33,18
Tekanan kritis, kPaa 1298,8 1315
Densitas pada titik didih, mol/cm3 0,03511 0,03520
Densitas pada titik lebur, mol/cm3 0,038207 0,03830
Faktor kompresibilitas, Z = PV/RT pada titik lebur
titik didih
0,001606 0,01712
0,001621 0,01698
Titik kritis 0,3025 0,3191
Kompresibilitas adiabatik, (–∂V/V∂P)s, MPa-1 b pada triple point
titik didih
0,00813 0,0119
0,00813 0,0119
Koefisien ekspansi volume, (–∂V/V∂T)p, K-1
pada triple point titik didih
0,0102 0,0164
0,0102 0,0164
Panas penguapan, J/molc pada triple point
titik didih
pada triple point titik didih
13,13 19,53
13,23 19,70 Cv, J/(mol.K) c
pada triple point titik didih
9,50 11,57
9,53 11,60 Entalpi, J/mol c d
titik didih -519,5 545,7 Entropi , J/(mol.K) c d
pada triple point titik didih
10,0 16,08
28,7 34,92 Kecepatan suara, m/s
pada triple point
titik didih
1273
1093
1282
1101 Viskositas, mPas (=cp)
pada triple point
titik didih
0,026
0,0133
0,0256
0,0133 Konduktivitas termal, mW/(cm.K)
pada triple point titik didih
0,73 0,99
0,73 0,99
Konstanta dielektrik pada triple point
titik didih
1,252 1,230
1,253 1,231
Tegangan muka, mN/m(=dyne/cm) pada triple point
titik didih
2,99 1,93
3,00 1,94
Kompresibilitas isotermal, 1/V(∂V/V∂P)T , Mpa-1 b
pada triple point titik didih
–0,0110
untuk konversi Mpa ke atm, dibagi dengan 0,101
c
untuk konversi J ke cal, dibagi dengan 4,184
d
titik dasar (nilai nol) untuk entalpi, energi dalam, dan entropi adalah 0 K untuk gas ideal pada tekanan 101,3 kPa (1 atm)
Sumber : Othmer, 1967
2.2 Penggunaan Hidrogen
Sejumlah besar H2 diperlukan dalam industri petrokimia dan kimia. Penggunaan
terbesar H2 adalah untuk memproses bahan bakar fosil dan dalam pembuatan
da2 memiliki beberapa kegunaan yang penting. H2
digunakan sebagai bahan hidrogenasi, terutama dalam peningkatan kejenuhan dalam lemak tak jenuh da
merupakan sumber hidrogen pada pembuatan2 juga digunakan sebagai
2 memiliki penerapan yang
luas dalam bidang fisika dan teknik. Ia digunakan sebagai
pen2 digunakan sebagai pendingin rotor di
antara semua jenis gas. H2 cair digunakan di riset
2 lebih ringan dari udara, hidrogen pernah digunakan
secara luas sebagai gas pengangkat pada kapal udara balon.
Baru-baru ini hidrogen digunakan sebagai bahan campuran dengan nitrogen (kadangkala disebut forming gas) sebagai gas perunut untuk pendeteksian kebocoran gas yang kecil. Aplikasi ini dapat ditemukan di bidang otomotif, kimia, pembangkit listrik, kedirgantaraan, dan industri telekomunikasi. Hidrogen adalah zat aditif yang diperbolehkan
penggunaanya dalam ujicoba kebocoran bungkusan makanan dan sebagai antioksidan.
Isotop hidrogen yang lebih langka juga memiliki aplikasi tersendiri. (hidrogen-2) digunakan dalam reactor candu sebagai neutron. Senyawa deuterium juga memiliki aplikasi dalam bidang kimia dan biologi dalam kajian reaks dalam produksi
2.3 Gas alam (natural gas)
Gas alam sering juga disebut sebagai gas bumi atau gas rawa, adalah
). Ia dapat ditemuka n di
diproduksi melalui pembusukan oleh fosil, maka ia disebut pembuangan akhir
Komponen utama dalam gas alam adalah metana (CH4), yang merupakan
hidrokarbon yang lebih berat seperti2H6)3H8) da4H10), selain
Metana adalah gas rumah kaca yang dapat menciptaka terlepas ke atmosfer, dan umumnya dianggap sebagai polutan ketimbang sumber energi yang berguna. Meskipun begitu, metana di atmosfer bereaksi dengan ozon, memproduksi berlangsung sesaat. Sumber metana yang berasal dari makhluk hidup kebanyakan berasal dari rayap, ternak (mamalia) dan pertanian (diperkirakan kadar emisinya sekitar 15, 75 dan 100 juta ton.
Tabel 2.3 komposisi natural gas
Komponen % volume
Metana (CH4) 88,5
Etana (C2H6) 3,638
Propana (C3H8) 1,926
Isobutana (i-C4H10) 0,37
N-Butana (n-C4H10) 0,466
Iso pentana (i-C5H12) 0,159
n-pentana (n-C5H12) 0,11
Hexana (C6H14) 0,171
Karbon dioksida (CO2) 2,336
Nitrogen (N2) 1,938
Hidrogen Sulfida (H2S) 0,028
Sumber : (http//:www. Wikipedia. Com)
2),2S), dan air dapat juga
terkandung di dalam gas alam. Komposisi gas alam bervariasi sesuai dengan sumber ladang gasnya.
diproses itu sendiri sebenarnya tidak berbahaya, akan tetapi gas alam tanpa proses dapat menyebabkan tercekiknya pernafasan karena ia dapat mengurangi kandungan oksigen di udara pada level yang dapat membahayakan.
Gas alam dapat berbahaya karena sifatnya yang sangat mudah terbakar dan menimbulkan ledakan. Gas alam lebih ringan dari udara, sehingga cenderung mudah tersebar di atmosfer. Akan tetapi bila ia berada dalam ruang tertutup, seperti dalam rumah, konsentrasi gas dapat mencapai titik campuran yang mudah meledak, yang jika tersulut api, dapat menyebabkan ledakan yang dapat menghancurkan bangunan. Kandungan metana yang berbahaya di udara adalah antara 5% hingga 15%.
Ledakan unt karena sifatnya yang lebih ringan, dan konsentrasi yang diluar rentang 5 - 15% yang dapat
menimbulkan ledakan (http://www. Wikipedia.com).
2.4 Pemanfaantan Gas alam (natural gas)
Secara garis besar pemanfaatan gas alam dibagi atas 3 kelompok yaitu :
• Gas alam sebagai bahan bakar, antara lain sebagai bahan bakar Pembangkit Listrik
Tenaga Gas/Uap, bahan bakar industri ringan, menengah dan berat, bahan bakar kendaraan bermotor (BBG/NGV), sebagai gas kota untuk kebutuhan rumah tangga hotel, restoran dan sebagainya.
• Gas alam sebagai bahan baku, antara lain bahan baku pabrik pupuk, petrokimia,
metanol, bahan baku plastik (LDPE = low density polyethylene, LLDPE = linear low
density polyethylene, HDPE = high density polyethylen, PE= poly ethylene, PVC=poly vinyl chloride, C3 dan C4-nya untuk LPG, CO2-nya untuk soft drink, dry ice
pengawet makanan, hujan buatan, industri besi tuang, pengelasan dan bahan pemadam api ringan.
• Gas alam sebagai komoditas energi untuk ekspor, yakni Liquefied Natural Gas
(LNG).
• Teknologi mutakhir juga telah dapat memanfaatkan gas alam untuk air conditioner
(AC=penyejuk udara), seperti yang digunakan di bandara Bangkok, Thailand dan beberapa bangunan gedung perguruan tinggi di Australia.
Perkembangan pemanfaatan gas alam di Indonesia meningkat pesat sejak tahun 1974, dimana PERTAMINA mulai memasok gas alam melalui pipa gas dari ladang gas alam di Prabumulih, Sumatera Selatan ke pabrik pupuk Pusri II, Pusri III dan Pusri IV di Palembang. Karena sudah terlalu tua dan tidak efisien, pada tahun 1993 Pusri IA ditutup,dan digantikan oleh Pusri IB yang dibangun oleh putera-puteri bangsa Indonesia sendiri. Pada masa itu Pusri IB merupakan pabrik pupuk paling modern di kawasan Asia, karena menggunakan teknologi tinggi. Di Jawa Barat, pada waktu yang bersamaan, 1974, PERTAMINA juga memasok gas alam melalui pipa gas dari ladang gas alam di lepas pantai (off shore) laut Jawa dan kawasan Cirebon untuk pabrik pupuk dan industri menengah dan berat di kawasan Jawa Barat dan Cilegon Banten. Pipa gas alam yang membentang dari kawasan Cirebon menuju Cilegon, Banten memasok gas alam antara lain ke pabrik semen, pabrik pupuk, pabrik keramik, pabrik
baja dan pembangkit listrik tenaga gas dan uap.
Selain untuk kebutuhan dalam negeri, gas alam di Indonesia juga di ekspor dalam bentuk LNG (Liquefied Natural Gas)
Salah satu daerah penghasil gas alam terbesar di Indonesia adalah
Aceh Utara) juga terdapat dari gas alam (http://www. Wikipedia.com diakses tanggal1 Mei 2009).
2.5 Cadangan gas alam dunia
Berdasarkan data dari Natural Gas Fundamentals, Institut Francais Du Petrole pada tahun 2002, cadangan terbukti (proved reserves) gas alam dunia ada sekitar 157.703 109 m3 atau 142 Gtoe (1000 m3 = 0,9 toe). Jumlah cadangan ini jika dengan tingkat konsumsi sekarang akan dapat bertahan sampai lebih dari 60 tahun. Apabila kita bandingkan dengan cadangan minyak dunia, maka berdasarkan tingkat konsumsi sekarang, minyak bumi hanya akan dapat bertahan sampai 40 tahun ke depan saja. Namun demikian, penemuan baru cadangan gas alam umumnya lebih cepat daripada tingkat konsumsinya. Pada tahun 1970, cadangan terbukti gas alam dunia hanya sekitar 35 Gtoe. Dengan asumsi konsumsi sebesar 47 Gtoe, berarti selama 30 tahun terakhir tambahan cadangan gas alam adalah sebesar 154 Gtoe.
Cadangan gas alam tersebar di seluruh benua, dengan cadangan terbukti (proved reserves) terbesar berada pada negara-negara pecahan Uni Soviet dan Timur Tengah (http://www. Wikipedia.com diakses tanggal1 Mei 2009)..
2.6 Proses Pembuatan hidrogen
Kriteria seleksi proses dalam pembuatan gas hidrogen difokuskan dalam beberapa faktor : kandungan hidrogen dalam umpan; hidrogen yang dihasilkan dari proses; yang meliputi biaya dari umpan; biaya modal dan operasi; energi yang dibutuhkan; pertimbangan lingkungan; penggunaan yang diharapkan dari hidrogen.
Secara mendasar, spesifikasi proses komersial untuk pabrik hidrogen diperoleh dari
steam reforming, oksidasi parsial, gasifikasi batubara, dan elektrolisa air. Di seluruh dunia,
hidrogen sebagai bahan baku untuk industri kimia diperoleh sebagai berikut: 77% dari gas alam/petroleum, 18% dari batubara, 4% dari elektrolisa air, dan 1% dari proses lain.
Semua proses ini menghasilkan hidrogen dari hidrokarbon dan air. Mekanisme reaksinya adalah sebagai berikut :
(Othmer, 1967)
Sekarang ini hidrogen digunakan hampir secara eksklusif sebagai suatu bahan kimia industri, dimana kapasitas itu diterapkan untuk suatu penggunaan yang luas, mencakup
produksi amoniak (untuk pabrik fertilizer), refineri yang digunakan untuk proses desulfurisasi dan lain-lain, serta untuk produksi methanol. Produksi tahunan dunia adalah sekitar 500 milyar Nm3. Produsen yang paling besar adalah produk udara, yang beroperasi lebih dari 50 pabrik individu, yang menghasilkan lebih dari 25 juta Nm3 per hari, dan 7 sistem perpipaan secara total lebih dari 340 juta. Produksi curah hidrogen (hampir 50%) dihasilkan oleh proses
Steam Methane Reforming, yang mana proses tersebut adalah dalam skala besar merupakan
2.6.1 Steam Methane Reforming (SMR) atau cracking
Dari buku (McGraw.Hill.Dictionary.Of.Engineering.eBook) Cracking adalah suatu proses yang dilakukan untuk mereduksi berat molekular senyawa hidrokarbon dengan cara memecah ikatan molekul-molekul dengan berbagai metode (thermal, catalytic,
hidrocracking).
Proses Steam Methane Reforming (SMR) terdiri atas 4 langkah proses:
a. Pemanasan stok umpan dan pemurnian (dibutuhkan karena katalis memiliki
sensitivitas yang tinggi oleh ketidakmurnian, contohnya: sulfur, mercury, dan logam lainnya)
b. Steam reformer c. CO shift
d. PSA purification (menyerap campuran lainnya selain dari H2 untuk menghasilkan H2
mencapai 80 – 90%.
Reaksi reformer (untuk methana) :
CH4 + 2H2O ↔ CO2 + 4H2 (ΔH0 = +164kJ /mol; secara umum beroperasi pada suhu
850- 900 oC) CH4 + H2O ↔ CO2 + 3H2 (ΔH0 = +205kJ /mol )
- Beroperasi pada tekanan < 40 bar - Reaksi sangat endotermis
- Konversi penguapan oleh steam dan suhu yang tinggi; konversi akan berkurang
dengan tekanan yang tinggi.
- Membutuhkan katalis nikel yang aktif
- Kemungkinan untuk tingkatan reaksi oleh adsorpsi CO2, memungkinkan suhu reaksi
untuk menjadi berkurang sampai 550 oC. Reaksi CO shift :
CO + H2O ↔ CO2 + H2
- Menggunakan katalis CO shift : besi oksida (secara konvensional suhu tinggi 340 –
460 oC), (suhu sedang) besi + tembaga oksida (suhu tinggi dimodifikasi 310 – 370
o
C), tembaga, seng, aluminium (suhu rendah 180 – 280 oC)
- Ukuran pabrik kecil dan sedang yang memiliki reactor shift suhu sedang yang tunggal
- Pabrik skala besar memiliki 2 reaktor suhu sedang atau suhu tinggi ditambah reaktor suhu sedang
Kecil 500 - 3000 Nm3/jam
Sedang mencapai 25,000 Nm3/jam
Besar lebih dari 25,000 Nm3/jam
Sangat besar over 150,000 Nm3/jam (Dutton, G., 2002)
2.6.2 Oksidasi parsial
Hidrogen juga dapat dibentuk oleh non-katalisis oksidasi parsial hidrokarbon. Banyak umpan hidrokarbon yang dapat dimampatkan atau dipompa mungkin digunakan. Efisiensi proses secara keseluruhan adalah hanya 50% (dibandingkan SMR pada 65 – 75%). Oksigen murni diperlukan sebagai umpan.
Reaksi reformer – oksidasi parsial :
Gas alam : CH4 + ½ O2 → CO + 2H2 (1350 oC)
Batu bara : C + ½ O2 → CO (1350 oC)
- Proses gas sintesis
- Menggunakan banyak bahan bakar fosil dan dapat beroperasi pada tekanan tinggi
(>100 bar)
Daftar sumber hidrogen terdiri atas tiga model teknologi :
a. Catalytic Steam Reforming (CSR) melibatkan reaksi bahan bakar hidrokarbon dan
steam dalam kehadiran katalis dimana dibutuhkan sumber panas eksternal. Proses ini memiliki efisiensi yang tinggi.
b. Auto Thermal Reforming (ATR) melibatkan reaksi bahan bakar hidrokarbon dan
steam dalam kehadiran katalis dan oksigen dimana beberapa bahan bakar yang digunakan untuk menghasilkan hidrogen dibutuhkan panas untuk reaksi. Proses ini dapat digunakan pada banyak perbedaan tipe dari bahan bakar.
c. Catalytic Partial Oxidation Reforming (CPOX) adalah serupa seperti auto thermal reforming (ATR) tetapi menggunakan sistem operasi yang lebih simpel dan sederhana.
(Dutton, G., 2002)
2.6.3 Integrated gasification combined cycle (IGCC)
selanjutnya dibersihkan dari kotorannya dan digunakan untuk menghasilkan energi dalam turbin gas. (secara alternatif gas yang diproduksi dapat digunakan untuk menghasilkan hidrogen, bahan kimia, atau bahan bakar lainnya).
Panas yang terbuang dari turbin gas digunakan dalam turbin steam untuk menghasilkan banyak elektrisitas. Telnologi gasifier terintegrasi dengan siklus yang dikombinasikan dalam jalan ini menawarkan efisiensi sistem yang tinggi dan tingkatan polusi yang sangat rendah. Sistem dirancang untuk menangani berbagai umpan, mencakup batubara dengan kandungan sulfur yang tinggi dan rendah, antrasit, dan biomassa. Secara umum sistem memiliki rentang dalam ukuran dari 200 – 800 MWe. Secara umum pabrik menawarkan suatu peningkatan 10% dalam efisiensi suhu melebihi stasiun pembakaran batubara konvensional.
Efisiensi operasi dalah diantara 29 – 41%, tergantung pada karakteristik bahan bakar (yaitu kandungan sulfur, kandungan abu, dan nilai kalori), tipe dari sistem IGCC (yaitu
entrained, moving-bed atau fluidized bed) dan puncak suhu turbin gas. Dalam kaitan efisiensi
rendah dan biaya, IGCC hanya merupakan teknologi demonstrasi, akan tetapi hal itu
diharapkan bahwa teknologi generasi kedua akan merealisasikan efisiensi dari 45 – 50% dan mengurangi biaya. (Dutton, G., 2002)
2.6.4 Pirolisis
Hidrokarbon dapat dikonversi menjadi hidrogen tanpa menghasilkan CO2, jika
hidrokarbon tersebut didekomposisi pada suhu yang tinggi dalam ketidakhadiran oksigen (pirolisis). Sebagai contoh methana dapat di cracked dalam katalis seperti karbon (golongan karbon, seperti jelaga C60, grafit atau karbon aktif). Dalam prinsipnya, pirolisis dapat juga
diaplikasikan lebih jauh kedalam hidrokarbon kompleks, biomassa, limbah padat kota. (Dutton, G., 2002)
2.6.5 Elektrolisis air
Hidrogen dapat dihasilkan dari air yang dielekrolisis. Jika elektrolitas dihasilkan dari teknologi renewable (seperti solar, hidro, angin, pasang surut), maka proses tersebut disebut bebas karbon. Pemecahan elektrokimia dari air telah diketahui melalui reaksi :
H2O → H2 + ½ O2
a. Alkalin cair
b. Membran pertukaran proton
Secara umum tekanan beroperasi pada 50 bar (750 psig) yang mana tidak cukup pembebanan silinder tekanan tinggi. Konsumsi listrik dari proses elektrolisis dapat direduksi
dengan operasi pada suhu tinggi (900 – 1000 oC). Untuk penyimpanan hidrogen, dapat
dilakukan menggunakan kompresor atau disebut elektrolizer tekanan tinggi. (Dutton, G., 2002)
2.6.6 Produksi hidrogen secara biologi
Hidrogen dapat dihasilkan secara biologi dalam 2 proses : a. Proses fotosintesis
b. Proses fermentasi
Ganggang hijau dapat menangkap energi dari sinar matahari. Dibawah kondisi anaerobik, ganggang hijau menghasilkan enzim hidrogenase yang mana dapat menghasilkan hidrogen dari air dengan proses yang diketahui sebagai bio-fotolisis. Kondisi ini harus diatur
secara hati-hati sewaktu enzim hidrogenase bekerja dalam fase gelap dan sangat sensitif pada kehadiran oksigen yang dihasilkan dari fotosintesis. Ada dua tahapan proses yang digunakan untuk memaksimalkan produk hidrogen. Tantangan riset yang utama adalah:
a. Peningkatan produksi hidrogen oleh suatu faktor 10, atau lebih.
b. Peningkatan efisiensi konversi energi solar dari 5% menjadi 10% atau lebih.
c. Memproduksi sel membran tidak hidup oleh oksigen dan hidrogen untuk
menghasilkan enzim
Proses biologi yang kedua untuk menghasilkan hidrogen adalah dengan menggunakan fermentasi tanpa membutuhkan cahaya. Ini dilakukan dalam keadaan gelap, dimana proses anaerobik dilaksanakan oleh banyak spesies bakteri, satu diantaranya adalah Clostridia. Reaksi melibatkan enzim hidrogenase yang bertindak untuk menghasilkan hidrogen (dan karbon dioksida):
C6H12O6 + 2H2O → 2CH3COOH + 2CO2 + 4H2
Secara teoritis, hidrogen yang dihasilkan adalah 0,5 m3 H2/kg karbohidrat. Bakteri
fermentasi dikalikan secara cepat dan dapat menghasilkan kuantitas yang banyak dari hidrogen, tetapi parameter rancangan dan operasional ini adalah belum mapan. (Dutton, G.,
2.7 Pemilihan Proses
Dari beberapa jenis proses pembuatan hidrogen yang ada, dapat dipilih proses yang akan dipakai berdasarkan bahan baku, jenis produksi maupun kemurnian produk.
Berdasarkan pertimbangan-pertimbangan di atas dipilihlah proses cracking atau yang biasa di sebut steam reforming.
Alasan dipilihnya proses itu adalah:
a. Merupakan proses yang paling efisien untuk mengubah gas alam menjadi hidrogen
sampai saat ini.
b. Panas yang digunakan dapat diperoleh dari panas yang sebelumnya. c. Teknologi sudah terbukti.
d. Biaya Produksi paling murah.
2.8Deskripsi Proses
2.8.1 Unit untuk menghilangkan kandungan sulfur (desulphurization)
(R-201 A,B)
Gas alam (natural gas) yang disalurkan langsung melalui pipeline dari PGN
bertekanan sekitar 15 bar dan suhu 20 0C, dengan menggunakan kompresor ( C-101)
dinaikkan tekanannya hingga mencapai tekanan sekitar 26 bar dan sebagian akan dialirkan sebagai bahan bakar di steam furnace. Gas bertekanan dari kompresor dilewatkan melalui feed preheater (E-401) dengan memakai gas yang keluar dari unit high temperatur CO shift
conversion sebagai media pemanas hingga suhu mencapai 415 0C. Gas alam yang telah
dipanaskan sampai mencapai 415 0C ini akan melewati unit desulphurization (R-201) untuk dihilangkan kandungan sulfurnya agar tidak meracuni katalis pada vessel yang lainnya. Di dalam unit desulpurization bisa dibagi menjadi dua tahapan proses. Pada tahap pertama, kandungan organik sulfur di konversi menjadi H2S pada suhu sekitar 415 0C dengan katalis
cobalt-molybde num (Co-Mo). Pada tahap kedua H2S di adsorbsi oleh senyawa Zinc Oxide
(ZnO). Gas alam yang keluar dari unit desulpurization tekananya menjadi 25 bar dan suhunya 425 0C dan kandungan sulfur harus lebih kecil dari 0,5 ppm. Kandungan sulfur harus dihilangkan karena akan menutupi permukaan katalis.
2.8.2 Unit Steam Reforming dengan memakai katalis Nikel (R-301)
Gas alam yang telah melewati unit desulpurization, dicampur dengan sejumlah steam
superheated yang tekananya 25 bar, temperatur 300 0C dimana perbandingan gas alam
dengan steam adalah 3 mol H2O/mol C (Leiby, 1994). Sebelum masuk ke unit steam
reformer (R-301), gas alam ini terlebih dahulu lewatkan melalui preheater berupa coil di
dalam steam reformer sampai suhu 5000C. kemudian masuk ke suatu pipa yang terdapat
didalam steam reformer (R-301) dan di panaskan lewat pembakaran (burner). Didalam pipa tersebut, dengan katalis nikel pada suhu 8000C - 9000C gas alam diubah menjadi gas proses
yang terdiri dari H2,CO,CO2 serta sejumlah kecil CH4, N2 dan steam yang tidak
terdekomposisi. Saat gas keluar dari sistem steam reformer (R-301) suhunya mencapai 820
0
C dan tekananya 25 bar dan harus didinginkan dengan cara melewatkannya dari waste Heat
Boiler (Boiler yang bekerja dengan menyerap panas) (E-301). Dalam proses pendinginan
dihasilkan Steam.
2.8.3 Unit Pengubah CO dengan suhu tinggi (High Temperatur CO Shift Convertion)
(R-401)
Gas proses yang keluar dari steam reformer (R-301) akan memasuki unit pengubah CO ( R-401) yang berisi katalis Fe dan Cr untuk meningkatkan gas H2. Gas proses tersebut
masuk melalui bagian atas, mengalir kebagian bawah dan terjadilah proses pengubahan gas CO menjadi CO2.
Fe dan Cr
CO + H2O CO 2 + H2
Reaksi proses adalah eksotermik, temperatur gas proses yang keluar dari unit pengubah CO (R-401) meningkat menjadi sekitar 450 0C.
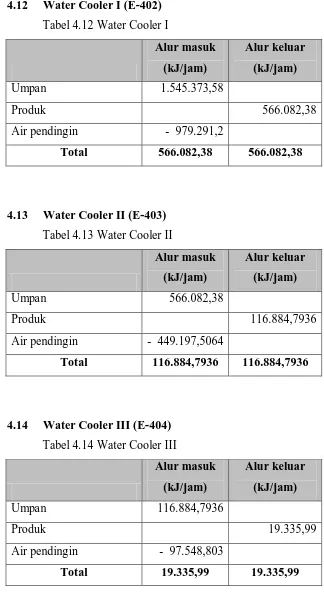
2.8.4 Unit Pendinginan gas proses (E-401), (E-402), (E-403), (E-404)
Gas proses yang keluar dari unit pengubah CO kemudian didinginkan dengan cara melewatkannya pada alat penukar panas feed preheater (E-401) dimana panas yang berpindah digunakan sebagai media pemanas umpan gas alam sebelum masuk ke reaktor desulphurisasi, sehingga temperatur gas proses turun menjadi 299 0C. Gas proses dilewatkan kembali melalui penukar panas water cooler I (E-402) dengan menggunakan air pendingin
didalam water cooler III (E-404) dengan menggunakan air pendingin biasa. Sehingga suhu gas proses akhir setelah pendinginan sekitar 30 0C.
Adanya proses pendinginan ini akan menyebabkan terjadinya kondensat. Kondesat ini akan ditampung dan dipisahkan dari gas pada alat knok out drum (D-401) secara gravitasi. Dimana, fase cair dari H2O akan turun kebawah drum, sedangkan fase gas akan naik keatas
drum. Dalam hal ini itu perlu diingat bahwa tidak boleh ada steam yang lolos bersama gas, sebab alat yang dipakai selanjutnya PSA (Pressure swing adsorpsion) (A-501), sangat peka terhadap kerusakan yang disebabkan oleh uap air.
2.8.5 Unit penyerap kotoran preassure swing adsorbtion (PSA) (A-501)
Preses gas yang telah didinginkan dan telah dipisahkan kandungan airnya kemudian
dilewatkan melalui alat PSA (pressure swing adsorpsion) (D-501), yang bertujuan untuk memurnikan/ memisahkan H2 dari impuritisnya misalnya H2O CO,CO2 dan CH4 yang tidak
bereaksi..
Kandungan CO dan CO2 yang tersisa dalam H2 maksimum 20 ppm sedangkan CH4
-nya maksimum 50 ppm. Saat berlangsung-nya proses diPSA ini, tidak dapat dihindari terjadinya penghilangan atau terikutnya sejumlah kecil H2 dan gas-gas yang harus dibuang
(dipisahkan). Gas yang diinginkan dari unit PSA ini hanya Hidrogen. Gas-gas buangan yang dihasilkan unit PSA akan dipakai untuk bahan bakar dari Steam Reformer, setelah dahulu disimpan dalam sebuah tangki yang disebut Surge Drum.
Sistim PSA ini terdiri dari 4 vessel adsorber A, B, C, D. Masing-masing vessel terdiri dari 3 bagian adsorben (penyerap) yang berlainan :
- Pada bagian atas, berisi Zeolite berfungsi untuk menyerap CO2
- Pada bagian tengan, berisi Activated Carbon berfungsi untuk menyerap CH4
- Pada bagian bawah, berisi Activated Alumina berfungsi untuk menyerap H2O
Ada 4 cara PSA bekerja secara kontiniu
1. Adsorption
Proses gas masuk dari bawah vessel sehingga impuritis dari proses gas diserap oleh adsorbent dan keluar melalui bagian atas vessel. Kemurnian H2 yang keluar sekitar
2. Regenerassi
Tahap regenerasi dimulai dengan depresurisai, selama proses ini gas yang dihasilkan proses depresurisasi digunakan untuk purging vessel lain yang mengalami proses regenerasi.
3. Purging
Pada tahap ini tekanan gas dalam vessel sangat rendah mendekati ambient pressure dan proses purging ini diambilkan dari gas vessel lain yang sedang dalam proses
depressurisasi. Gas hasil proses ini disebut purge gas (sebagai bahan baku CO2
plantdan bahan bakar burner reformer). 4. Repressurization
Pada tahap ini tekanan vessel yang tadinya rendah dinaikkan sampai mencapai
tekanan operasi adsorbsi (25 bar).
Gas hidrogen yang telah dimurnikan akan meninggalkan PSA dengan laju alir yang konstan, dengan tekanan sekitar 24,5 bar sedikit dibawah tekanan gas sewaktu gas memasuki alat PSA.
2.9 Spesifikasi Bahan Pendukung
2.9.1. Air
− Rumus molekul : H2O
− Berat molekul : 18
− Berat jenis : 1 gr/cm3 (pada suhu 25 0C)
− Titik lebur : 0 0C
− Titk didih : 100 0C
(Othmer, 1967)
2.9.2. Katalis Zink Oksida
− Rumus kimia : ZnO
− Berat molekul : 81,39 gr/mol
− Berat jenis : 5,47 gr/cm3
− Titik lebur : 1800 0C
− Kenampakan : butir–butir dengan diameter rata-rata 366 nm
2.9.3 Katalis Ni
− Rumus kimia : Ni
− Berat molekul : 58,69 gr/mol
− Berat jenis : 8,90 (20 0C) gr/cm3
− Titik lebur : 1425 0C
− Titik didih : 29000C (Othmer, 1967)
2.9.4 Metana (CH 4)
Fungsi : merupakan komponen unsur terbesar (88,85%) di dalam biogas.
− Berat molekul : 16,043 g/mol
− Temperatur kritis : -82,7 0C
− Tekanan kritis : 45,96 bar
− Fasa padat
− Titik cair : -182,5oC
− Panas laten : 58,68 kJ/kg
− Fasa cair
− Densitas cair : 500 kg/m
3
− Titik didih : -161,6oC
− Panas laten uap : 510 kJ/kg
− Fasa gas
− Densitas gas : 0,717 kg/m3
− Faktor kompresi : 0,998
− Spesifik graffiti : 0,55
− Cp : 0,035 kJ/mol.K
− Cv : 0,027 kJ/mol.K
− Kelarutan : 0,054 vol/vol
− Viskositas : 0,0001027 poise
2.19.5 Ethana (C 2H5)
− Berat molekul : 30,069 g/mol
− Temperatur kritis : 32,2 0C
− Tekanan kritis : 40,2 bar
− Fasa padat
− Titik cair : -183,3
o
C
− Panas laten : 94,977 kJ/kg
− Fasa cair
− Densitas cair : 546,59 kg/m
3
− Titik didih : -88,7oC
− Panas laten uap : 488,76 kJ/kg
− Fasa gas
− Densitas gas : 2,054 kg/m
3
− Faktor kompresi : 0,9912
− Spesifik graffiti : 1,047
− Pesifik Volume :0,799m3/kg
− Cp : 0,053 kJ/mol.K
− Cv : 0,044 kJ/mol.K
− Kelarutan : 0,052 vol/vol
− Viskositas : 0,0000855 poise
(Anonim, 2007)
2.9.6 Propane (C 3H8)
− Berat molekul : 44,1 g/mol
− Densitas cair : 1,83 kg/m
3
− Densitas gas : 0,5077 kg/m
3
− Titik cair : -187,6
o
C
− Titik didih : -42,09oC
Gas Alam
Demin Water
Desulfurisasi CO Converter
(HTS)
Point Steam reformer
KOD
Reformer Fuel + PSA Off Gas Udara
Gbr 2.1 Blok Diagram Proses Pembuatan Gas Hidrogen dari Gas Alam dengan Proses
BAB III
NERACA MASSA
Hasil perhitungan neraca massa pada proses pembuatan Hidrogen dari gas alam dengan proses cracking (steam reforming) dengan kapasitas produksi 151,51 kg/ jam, 1200 ton/ tahun diuraikan sebagai berikut :
1 tahun operasi = 330 hari kerja 1 hari kerja = 24 jam
Basis = 1 jam operasi
3.1 Desulfurisasi (R-201)
Tabel 3.1 Neraca massa pada Reaktor Desulfurisasi
Komponen
Masuk
(kmol/jam)
Keluar
(kmol/Jam)
Alur 3 Alur 4
1 CH4 22,1973 22,1973
2 C2H6 0,9175 0,9175
3 C3H8 0,4932 0,4932
4 i-C4H10 0,0971 0,0971
5 n-C4H10 0,1197 0,1197
6 i-C5H12 0,0348 0,0348
7 n-C5H12 0,0241 0,0241
8 C6H14 0,0343 0,0343
9 CO2 0,5866 0,5866
10 N2 0,4836 0,4836
11 H2S 0,0071 0,00000
12 H2O 0 0,007069
3.2 Mixing Point (M-201)
Tabel 3.2 Neraca massa pada mixing point
No Komponen
Masuk Keluar
Alur 4 Alur 28 Alur 5
(Kmol/jam) (Kmol/jam) (kg/kmol)
1 CH4 22,19727 0 22,1973
2 C2H6 0,9175455 0 0,91755
3 C3H8 0,4931944 0 0,49319
4 i-C4H10 0,0971208 0 0,09712
5 n-C4H10 0,119731 0 0,11973
6 i-C5H12 0,034801 0 0,0348
7 n-C5H12 0,0240762 0 0,02408
8 C6H14 0,0342524 0 0,03425
9 CO2 0,5866274 0 0,58663
10 N2 0,4835833 0 0,48358
11 H2S 0 0 0
12 H2O 0,007069 54,51419 54,5213
Sub total 24,995271 54,51419
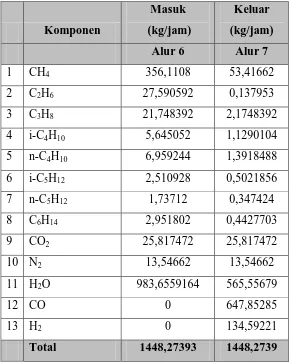
3.3 Steam Reformer (R-301)
Tabel 3.3 Neraca Massa pada Steam Reformer
Komponen
Masuk
(kg/jam)
Keluar
(kg/jam)
Alur 6 Alur 7
1 CH4 356,1108 53,41662
2 C2H6 27,590592 0,137953
3 C3H8 21,748392 2,1748392
4 i-C4H10 5,645052 1,1290104
5 n-C4H10 6,959244 1,3918488
6 i-C5H12 2,510928 0,5021856
7 n-C5H12 1,73712 0,347424
8 C6H14 2,951802 0,4427703
9 CO2 25,817472 25,817472
10 N2 13,54662 13,54662
11 H2O 983,6559164 565,55679
12 CO 0 647,85285
13 H2 0 134,59221
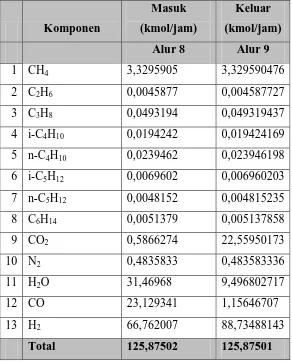
3.4 High Temperature Shift Converter (R-401)
Tabel 3.4 Neraca Massa pada Reaktor High Temperature Shift Converter
Komponen
Masuk
(kmol/jam)
Keluar
(kmol/jam)
Alur 8 Alur 9
1 CH4 3,3295905 3,329590476
2 C2H6 0,0045877 0,004587727
3 C3H8 0,0493194 0,049319437
4 i-C4H10 0,0194242 0,019424169
5 n-C4H10 0,0239462 0,023946198
6 i-C5H12 0,0069602 0,006960203
7 n-C5H12 0,0048152 0,004815235
8 C6H14 0,0051379 0,005137858
9 CO2 0,5866274 22,55950173
10 N2 0,4835833 0,483583336
11 H2O 31,46968 9,496802717
12 CO 23,129341 1,15646707
13 H2 66,762007 88,73488143
3.5 Knock-Out Drum (D-401)
Tabel 3.5 Neraca Massa pada Knock Out Drum
Komponen
Masuk
(kmol/jam) Keluar (kmol/jam)
Alur 13 Alur 14 Alur 21
1 CH4 3,32959 3,306367 0,023224
2 C2H6 0,004588 0,004374 0,000213
3 C3H8 0,049319 0,040908 0,008411
4 i-C4H10 0,019424 0,012618 0,006806
5 n-C4H10 0,023946 0,013543 0,010403
6 i-C5H12 0,00696 0,002309 0,004652
7 n-C5H12 0,004815 0,001308 0,003507
8 C6H14 0,005138 0,00052 0,004618
9 CO2 22,5595 21,88927 0,670233
11 N2 0,483583 0,482213 0,00137
12 H2O 9,496803 0,180503 9,3163
13 CO 1,156467 1,152812 0,003655
14 H2 88,73488 88,6197 0,11518
Sub total 115,7064 10,16857
3.6 Pressure Swing Adsorption (PSA / A-501)
Tabel 3.6 Neraca Massa pada Unit Pressure Swing Adsorption (PSA)
Komponen Masuk
(kmol/jam) Keluar (kmol/jam)
Aliran 14 Aliran 15 Aliran 17
1 CH4 3,30454 3,30454
2 C2H6 0,00436 0,00436
3 C3H8 0,04036 0,04036
4 i-C4H10 0,01228 0,01228
5 n-C4H10 0,01309 0,01309
6 i-C5H12 0,00219 0,00219
7 n-C5H12 0,00124 0,00124
8 C6H14 0,00049 0,00049
9 CO2 21,8377 21,8377
10 N2 0,4821 0,4821
11 H2O 0,16745 1,80503E-05 0,18048
12 CO 1,15252 1,15252
13 H2 88,6106 75,32674605 13,293
Sub total 75,327 40,324
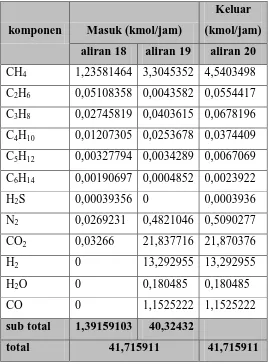
3.7 Mixing Point Bahan bakar
Tabel 3.7 Neraca Massa pada Mixing Point
komponen Masuk (kmol/jam)
Keluar
(kmol/jam)
aliran 18 aliran 19 aliran 20
CH4 1,23581464 3,3045352 4,5403498
C2H6 0,05108358 0,0043582 0,0554417
C3H8 0,02745819 0,0403615 0,0678196
C4H10 0,01207305 0,0253678 0,0374409
C5H12 0,00327794 0,0034289 0,0067069
C6H14 0,00190697 0,0004852 0,0023922
H2S 0,00039356 0 0,0003936
N2 0,0269231 0,4821046 0,5090277
CO2 0,03266 21,837716 21,870376
H2 0 13,292955 13,292955
H2O 0 0,180485 0,180485
CO 0 1,1525222 1,1525222
sub total 1,39159103 40,32432
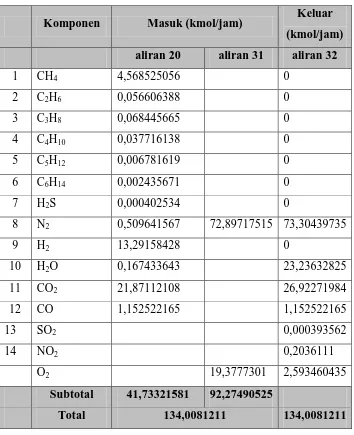
3.8 Perhitungan Neraca massa bahan bakar untuk Steam Reformer ( R-301)
Tabel 3.7 Neraca Massa pada bahan bakar Steam Reformer
Komponen Masuk (kmol/jam) Keluar
(kmol/jam)
aliran 20 aliran 31 aliran 32
1 CH4 4,568525056 0
2 C2H6 0,056606388 0
3 C3H8 0,068445665 0
4 C4H10 0,037716138 0
5 C5H12 0,006781619 0
6 C6H14 0,002435671 0
7 H2S 0,000402534 0
8 N2 0,509641567 72,89717515 73,30439735
9 H2 13,29158428 0
10 H2O 0,167433643 23,23632825
11 CO2 21,87112108 26,92271984
12 CO 1,152522165 1,152522165
13 SO2 0,000393562
14 NO2 0,2036111
O2 19,3777301 2,593460435
Subtotal 41,73321581 92,27490525
BAB IV
NERACA ENERGI
Basis perhitungan = 1 jam operasi
Satuan operasi = kiloJoule/jam (kJ/jam)
Kapasitas produksi = 1200 ton/tahun
Suhu Referensi = 25oC (298,15 K)
4.1 Feed Preheater 1 (E-401)
Tabel 4.1 Neraca Energi pada Feed Preheater
Alur masuk
H (kj/jam)
Alur keluar
H (kj/jam)
Umpan 4.772,3217 -
Produk - 483.069,825
Gas proses dari Converter 2.023.671,31 1.545.373,58
Total 2.028.443,632 2.028.443,405
4.2 Desulfurisasi (R-201)
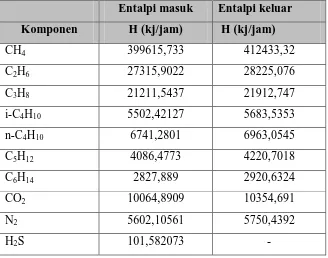
Tabel 4.2 Neraca Energi pada Desulfurisasi
Entalpi masuk Entalpi keluar
Komponen H (kj/jam) H (kj/jam)
CH4 399615,733 412433,32
C2H6 27315,9022 28225,076
C3H8 21211,5437 21912,747
i-C4H10 5502,42127 5683,5353
n-C4H10 6741,2801 6963,0545
C5H12 4086,4773 4220,7018
C6H14 2827,889 2920,6324
CO2 10064,8909 10354,691
N2 5602,10561 5750,4392
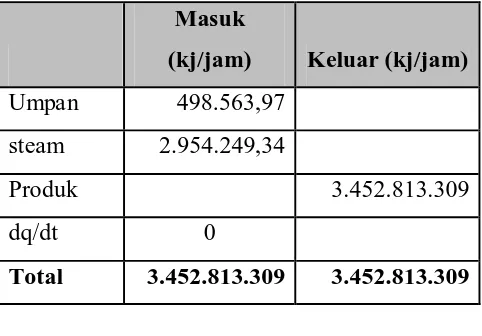
4.3 Mixing Point (M-201)
Tabel 4.3 Neraca Energi padaMixing Point
Masuk
(kj/jam) Keluar (kj/jam)
Umpan 498.563,97
steam 2.954.249,34
Produk 3.452.813.309
dq/dt 0
Total 3.452.813.309 3.452.813.309
4.4 Feed Heater (H-301)
Tabel 4.4 Neraca Energi padaFeed Heater
Alur masuk
H (kj/jam)
Alur keluar
H (kj/jam)
Umpan 3.452.813.309 -
Produk - 4.019.468,554
dQ/dT 566.655,245
Total 4.019.468,554 4.019.468,554
H2O - 419,72766
subtotal 483.069,825 498.883,92
Entalpi reaksi -442,464
dQ/dT 15.371,681
4.5 Steam Reformer (R-301)
Tabel 4.5 Neraca Energi pada Steam Reformer
Komponen Entalpi Masuk Entalpi Keluar
(kj/jam) (kj/jam)
CH4 540190,81 150490,51
C2H6 37288,411 349,61555
C3H8 28915,569 5761,214
i-C4H10 7488,9428 2961,4957
n-C4H10 9175,2408 3632,6735
C5H12 5559,7804 2209,8957
C6H14 3840,9158 1085,7138
CO2 13164,531 22573,825
N2 7175,2928 11867,564
H2O 3400201,98 2373426,76
CO 568220,79
H2 1567750,1
Sub total 4.019.468,554 4.710.330,16
∆Hr 4.606.124,54
dQ/dT - 3.915.262,935
Total 4.710.330,16 4.710.330,16
4.6 Feed Steam Superheater (H-302)
Tabel 4.6 Neraca Energi padaSteam Superheater
Masuk Keluar
(kj/jam) (kj/jam)
Steam masuk 2.627.925,034
Steam keluar 2.954.249,339
dQ/dT 326.324,305
4.7 Feed Steam Water Preheater (H-303)
Masuk Keluar
(kj/jam) (kj/jam)
Steam masuk 111.497,87
Steam keluar 611.653,00
dQ/dT 500.155,13
Total 611.653,0029 611.653,003
4.8 Feed Steam Air Preheater (H-304)
Tabel 4.8 Neraca Energi pada Air Preheater
Masuk Keluar
(kj/jam) (kj/jam)
Udara masuk -
Udara keluar 197.184,7
dQ/dT 197.184,7
Total 197.184,7 197.184,7
4.9 Reformer Furnace
Tabel 4.9 Reformer Furnace
Komponen Entalpi masuk Entalpi keluar
kj/jam kj/jam
CH4 822,926249 0
C2H6 15,05184727 0
C3H8 25,34934799 0
C4H10 18,39388267 0
C5H12 4,106787387 0
C6H14 1,754176212 0
H2S 0,06843468 0
N2 42073,4453 1995134,618
H2 1896,560154 0
H2O 379,1534854 1840808,909
CO 167,9215863 31108,92925
SO2 17,20447665
NO2 8528,91961
O2 155185,4183 74732,83069
Sub total 204663,8425 5106300,779
Hr -7.289.505,18
dQ/dT -2.387.868,25
Total -2.183.204 -2.183.204
4.10 Waste Heat Boiler (E-301)
Tabel 4.10 Waste Heat Boiler
Alur masuk
(kJ/jam)
Alur keluar
(kJ/jam)
Umpan 4.710.330,16
Produk 2.694.951,163
Air pendingin -2.015.379
Total 2.694.951,163 2.694.951,163
4.11 High Temperatur Shitf (R-401)
Tabel 4.11 High Temperatur Shift
Alur masuk
(kJ/jam)
Alur keluar
(kJ/jam)
Umpan 2.694.951,163
Produk 2870968,25
r
H
∆
176017,0824dQ/dT