PENENTUAN KUALITAS MINYAK YANG DIPEROLEH DARI
HASIL EKSTRAKSI KOPRA DENGAN PELARUT N-HEKSAN
KARYA ILMIAH
RINA YURIKA
062401015
DEPARTEMEN KIMIA
PROGRAM STUDI DIPLOMA 3 KIMIA ANALIS
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN
ALAM UNIVERSITAS SUMATERA UTARA
PENENTUAN KUALITAS MINYAK YANG DIPEROLEH DARI
HASIL EKSTRAKSI KOPRA DENGAN PELARUT N-HEKSAN
KARYA ILMIAH
Diajukan untuk melengkapi tugas dan memenuhi syarat mencapai gelar Ahli Madya
RINA YURIKA
062401015
DEPARTEMEN KIMIA
PROGRAM STUDI DIPLOMA 3 KIMIA ANALIS
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN
ALAM UNIVERSITAS SUMATERA UTARA
MEDAN
PERSETUJUAN
Judul : PENENTUAN KUALITAS MINYAK
YANG DIPEROLEH DARI HASIL
EKSTRAKSI KOPRA DENGAN PELARUT
N-HEKSAN
Katagori : KARYA ILMIAH
Nama : RINA YURIKA
Nomor Induk Mahasiswa : 062401015
Program Studi : DIPLOMA 3 KIMIA ANALIS
Departemen : KIMIA
Fakultas : MATEMATIKA DAN
ILMU PENGETAHUAN ALAM (FMIPA)
UNIVERSITAS SUMATERA UTARA
Disetujui Oleh Medan, Juni 2009
Diketahui / Disetujui Oleh Departemen Kimia FMIPA USU Ketua,
Pembimbing,
DR. Rumondang Bulan, MS Dra. Saur Lumban Raja, M.Si
PERNYATAAN
PENENTUAN KUALITAS MINYAK YANG DIPEROLEH DARI
HASIL EKSTRAKSI KOPRA DENGAN PELARUT N-HEKSAN
KARYA ILMIAH
Saya mengakui bahwa karya ilmiah ini adalah hasil kerja saya sendiri, kecuali beberapa kutipan dan ringkasan yang masing – masing disebutkan sumbernya.
Medan, Juni 2009
RINA YURIKA
PENGHARGAAN
Segala puji dan syukur penulis ucapkan kehadirat Allah SWT, yang telah
memberikan kesehatan, rizky serta kekuatan kepada penulis. Dan hanya karena berkat
dan rahmat-Nya penulis dapat menyelesaikan Karya Ilmiah ini guna memenuhi salah
satu syarat untuk memperoleh jenjang Diploma 3 pada Fakultas Metematika dan Ilmu
Pengetahuan Alam Program Kimia Analis Universitas Sumatera Utara.
Dalam penulisan Karya Ilmiah ini penulis mencoba membuat setiap
penjabaran dan masalah sistematis mungkin serta penyajian yang singkat. Hal ini
mengingat keterbatasan waktu dan kemampuan dalam menyelesaikan Karya Ilmiah
ini.
Dengan selesainya Karya Ilmiah ini, penulis menghaturkan rasa terima ksaih
yang sebesarnya – besarnya kepada semua pihak yang telah membantu dan
membimbing penulis untuk menyelesaikan Karya Ilmiah ini, terutama kepada :
1. Penghargaan yang tulus dari dalam hati penulis ucapkan kepada Ayahanda
KHAIRUDDIN dan Ibunda tersayang MASMUDAH L.TOBING terima
kasih penulis ucapkan atas segala dukungannya baik moril maupun material.
Kakak ku tersayang Andri Sepria dan suami Bang Santo dan adik – adik ku
tersayang Ayu Pirdina dan Muhammad Ramadhan yang telah memberikan
dukungan dan semangat kepada penulis selama ini, serta keponakan ku
tersayang Rizky Adrian Permana.
2. Ibu Dra. Saur Lumban Raja, M.Si selaku Dosen Pembimbing akademik
yang telah banyak membimbing penulis dalam menyelesaikan Karya
Ilmiah ini.
3. Bapak Dr. Eddy Marlianto, M.Sc selaku Dekan Fakultas Matematika dan
Ilmu Pengetahuan Alam USU.
4. Ibu DR. Rumondang Bulan, MS selaku Ketua Jurusan Departemen Kimia.
5. Ibu DR. Marfongahtun, M.Si selaku Ketua Jurusan Program studi D-3 Kimia
Analis FMIPA USU.
6. Bapak Zul Alkaf, BSc selaku kepala Laboratorium di PT. PALMCOCO
LABORATORIES. Yang telah memberikan izin Praktek Kerja Lapangan
(PKL).
8. Buat Kak Quivy, Kak Lia dan Kak Tari selaku Pembimbing Lapangan
selama PKL di PT. PALMCOCO LABORATORIES terima kasih atas
semua bantuannya selama PKL.
9. Buat teman – teman separtner PKL di PT.PALMCOCO LABORATORIES ,
Mazda, Meta, dan Andi terima kasih atas pengertian, dukungan dan kerja
samanya selama menjalani PKL.
10.Buat yang terspesial buat Nine Ball’s Bunda Sherly, Isma, Mazda, Ayu,
Kiki, Lia, Widy, dan Inggit terima kasih atas dukungan, pengertian dan
bantuannya selama ini serta kebersamaan dan canda tawanya selama ini.
Jangan pernah berubah ya…
11.Buat anak – anak kos Senina 19, Kak Irma, Izaen, Chaoni, Sri dan A’i terima
kasih atas pengertian dan semangat dan canda tawanya selama ini. Terus
berjuang ya…n jangan pernah putus asa ok…
12.Buat teman – teman seperjuangan Mahasiswa D-3 Kimia Analis khususnya
stambuk ’06 yang tidak dapat disebutkan namanya satu persatu terima kasih
atas dukungannya, kebersamaan dan canda tawanya selama ini. Dan buat
adik – adikku stambuk ’07 dan ’08 terima kasih atas bantuannya selama ini.
Medan, Juni 2009
Penulis,
ABSTRAK
DETERMINATION OF OIL CONTENT COPRA EXTRACTION WITH
N - HEXAN
ABSTRACT
DAFTAR ISI
1.2.Permasalahan 2
1.3.Tujuan 2
1.4.Manfaat 3
BAB 2 TINJAUAN PUSTAKA 4
2.1. Buah Kelapa 4
2.1.1. Manfaat Kelapa 9
2.2. Spesifikasi Minyak Kelapa
2.2.1. Komposisi Kimia Buah Kelapa 12 2.2.2. Komposisi Kimia Daging Buah Kelapa Pada
Berbagai Tingkat Kematangan 13
2.3. Minyak dan Lemak 14
2.4. Asam Lemak 15
2.5. Asam Lemak Jenuh dan Asam Lemak Tidak Jenuh 16
2.6. Analisa Titrimetri 17
BAB 3 METODOLOGI PERCOBAAN 21
3.1. Alat 21
3.2 Bahan 22
3.3. Prosedur 22
3.3.1. Prosedur Preparasi Ekstrak Minyak 22
3.3.2. Prosedur Preparasi Sampel 23
3.3.3. Prosedur Analisa Kualitas Minyak 23 3.3.4. Prosedur Pembuatan Reagen 23
3.3.5. Prosedur Analisa 26
BAB 4 HASIL DAN PEMBAHASAN 29
4.1. Hasil Percobaan 29
4.1.1. Data 29
BAB 5 KESIMPULAN DAN SARAN 40
5.1. Kesimpulan 40
5.2. Saran 40
DAFTAR TABEL
Halaman
Tabel 1. Spesifikasi Mutu Minyak Kelapa / CCO menurut MEOMA 12
Tabel 2. Komposisi Kimia Buah Kelapa 12
Tabel 3. Komposisi Kimia Daging Buah Kelapa Pada Berbagai Tingkat
Kematangan 13
ABSTRAK
DETERMINATION OF OIL CONTENT COPRA EXTRACTION WITH
N - HEXAN
ABSTRACT
BAB 1
PENDAHULUAN
1.1. Latar Belakang
Kelapa merupakan komoditas yang cukup berperan dalam kancah perekonomian
nasional. Namun demikian berdasarkan prasasti sejarah yang terukir di dinding candi
Borobudur, maka dapat diperkirakan bahwa tanaman ini telah dikenal oleh nenek
moyang bangsa Indonesia lebih dari 1.000 tahun yang lalu. Dari beberapa sumber
terpercaya, tampaknya tanaman industri ini berasal dari kawasan kepulauan Pasifik,
dari Amerika Selatan hingga wilayah Asia Tenggara. Yang jelas, tanaman ini
merupakan tanaman daerah tropis yang telah tersebar luas keseluruh pelosok dunia.
Hal ini dapat dimengerti mengingat struktur botani buahnya yang memungkinnya
untuk disebarkan oleh kekuatan alam.
(Syamsulbahri, 1996)
Minyak kelapa berdasarkan kandungan asam lemak digolongkan kedalam minyak
asam laurat, karena kandungan asam lauratnya paling besar jika dibandingkan dengan
asam lemak lainnya .Berdasarkan tingkat ketidakjenuhannya yang dinyatakan dengan
bilangan iodin (Iodine Value), maka minyak kelapa dapat dimasukkan kedalam
golongan non drying oils, karena bilangan iodin minyak tersebut berkisar antara 7,5 –
10,5.
Minyak kelapa mengandung 84 persen trigliserida dengan tiga molekul asam
lemak jenuh, 12 persen trigliserida dengan dua asam lemak jenuh dan 4 persen
Penentuan kadar minyak suatu bahan dapat dilakukan dengan menggunakan
soxhlet apparatus. Cara ini dapat juga digunakan untuk ekstraksi minyak dari suatu
bahan yang mengandung minyak. Ekstraksi dengan alat soxhlet apparatus merupakan
cara ekstraksi yang efisien karena dengan alat ini pelarut yang dipergunakan dapat
diperoleh kembali. Bahan dalam bentuk padat umumnya membutuhkan waktu
ekstraksi yang lebih lama, karena itu dibutuhkan pelarut yang lebih banyak dan
penentuan kadar minyak yang diuji harus cukup kering.
(Ketaren, 1986)
Berdasarkan uraian diatas, penulis tertarik untuk menulis Karya Ilmiah dengan
judul “ Penentuan Kualitas Minyak Yang Diperoleh Dari Hasil Ekstraksi Kopra
Dengan Pelarut N-Heksan”.
1.2. Permasalahan
Apakah Penentuan Kualitas Minyak yang meliputi Asam Lemak Bebas,
Bilangan Iodin, Kadar Air, dan Kadar Kotoran yang diperoleh dari hasil ekstraksi
kopra telah memenuhi spesifikasi yang telah ditetapkan.
1.3. Tujuan
Untuk mengetahui Penentuan Kualitas Minyak yang meliputi Asam Lemak
Bebas, Bilangan Iodin, Kadar Air, dan Kadar Kotoran yang diperoleh dari hasil
1.4. Manfaat
- Untuk meningkatkan wawasan penulis tentang aplikasi ilmu yang diperoleh
selama perkuliahan.
- Memberikan pemahaman terhadap dunia pendidikan secara umum dan secara
khusus untuk mahasiswa Program D-3 Kimia Analis dalam penentuan
kadar Asam Lemak bebas, Bilangan Iodin, Kadar Air, dan Kadar Kotoran yang
BAB 2
TINJAUAN PUSTAKA
2.1. Buah Kelapa
Buah Kelapa berbentuk bulat panjang dengan ukuran lebih kurang sebesar kepala
manusia. Buah terdiri dari sabut (ekskarp dan mesokarp), tempurung (endokarp),
daging buah (endosperm) dan air buah.Tebal sabut kelapa lebih kurang 5 cm dan tebal
daging buah 1 cm atau lebih. Bunga betina tanaman kelapa akan dibuahai 18 – 25 hari
setelah bunga berkembang dan buah akan menjadi masak (ripe) setelah 12 bulan.
(Ketaren, 1986)
Berikut ini adalah taksonomi tanaman kelapa :
Kingdom : Plantae
Phylum/Division : Spermatophyta
Sub Phylum/Sub Division : Angiospermae
Klas : Monocotyledoneae
Ordo : Arales (Spadiciflorae)
Famili : Arecaceae (Palmae)
Sub famili : Cocoideae (Cocoinae)
Genus : Cocos
Spesies : Cocos nucifera (Linneaus)
Tipe : Genjah, Jangkung, Hibrida
Varietas : Genjah Kuning Nias, Jangkung Bali
dan sebagainya
1. Karakteristik Tanaman Kelapa
a. Variasi Genetis
Jenis tanaman kelapa cukup banyak, namun pada umumnya komoditi tersebut
digolongkan menjadi dua kelompok yaitu :
1. Kelapa Dalam
Golongan kelapa dalam biasanya mempunyai ukuran batang tinggi, umur
berbunganya relatif lama (8-10 tahun) namun umur untuk hidupnya panjang (60-80
tahun), dan dapat tumbuh pada berbagai jenis tanah serta resisten terhadap gangguan
hama dan penyakit tanaman kecuali rentan terhadap virus.
2. Kelapa Genjah
Batang kelapa genjah lebih pendek disamping berbunganya juga lebih awal
dari pada jenis kelapa dalam, yaitu sekitar 3-4 tahun semenjak tanam. Produksi buah
maksimal tercapai pada saat tanaman berumur 9-10 tahun.Golongan kelapa genjah ini
mempunyai warna buah yang bermacam – macam antara lain hijau, kuning, kuning
emas, putih perak. Selanjutnya, bentuk buah golongan kelapa genjah ini ada dua, yaitu
buah besar dan buah kecil.
b. Karakter Morfologi
1. Daun
Sebagaimana halnya dengan tumbuhan golongan palmae seperti salak dan
kelapa sawit, daun kelapa adalah sempurna. Daunnya berpelepah, beranak daun yang
tumbuh dikanan dan dikiri urat daun utama (midrib). Daun kelapa tumbuh melingkari
batang, antara daun pertama dengan daun kedua membentuk sudut 140o. Duduk daun
melingkari batang membentuk spiral, dimana setelah dua kali melingkari batang
2. Batang
Batang pohon kelapa baru kelihatan sesudah berumur 3-4 tahun. Karena pada
tanaman kelapa yang masih muda, batangnnya masih terbungkus erat oleh pelepah –
pelepah daun yang tumbuh mengelilinginya. Bila daun kelapa mati akan luruh dan
meninggalkan bekas, pada waktu itu akan terbentuk ruas pada batangnnya.
3. Akar
Tanaman kelapa berakar serabut. Pada mulanya, kelapa yang berumur muda
pertumbuhan akar sangat cepat. Pada umur 3 tahun, akar anakan kelapa dapat tumbuh
sepanjang 3 meter dari permukaan tanah. Konsentrasi perakaran hanya terletak
beberapa centi meter dari permukaan tanah. Semakin tua tanaman, pertumbuhan akar
tampak stabil.
4. Bunga
Bunga tanaman kelapa sawit adalah sempurna, artinya dalam satu tandan
bunga terdapat kedua jenis bunga, yaitu bunga jantan dan betina. Dengan demikian,
penyerbukan tidak menjadi masalah sebagaimana kelapa sawit. Tanaman kelapa
dalam kondisi normal akan mulai berbunga pada umur sekitar 6 tahun.
5. Buah
Sebagian besar bunga betina (70%) mekar 2 minggu sesudah kulit tandan buah
pecah. Persentase mekarnya bunga betina tersebut selain ditentukan oleh iklim, nutrisi
juga oleh jenisnya. Sesudah terjadi penyerbukan, bunga betina berkembang menjadi
buah muda yang sangat cepat sekali pertumbuhannya. Buah muda tersebut terbungkus
oleh kelopak bunga dan hiasan bunga.
2. Pemanenan
Pemanenan buah kelapa dipengaruhi oleh varietas tanaman dan iklim. Di
Ceylon buah kelapa tidak jatuh meskipun sudah tua, sehingga harus dipetik,
sedangkan di Malaysia, buah yang sudah tua akan jatuh dengan sendirinya.
Berdasarkan kedua kondisi tersebut diatas dapat dikemukakan dua cara memungut
buah kelapa, yaitu :
Menunggu buah yang jatuh, dan Pemetikan
Pemanenan dengan cara menunggu buah jatuh, tampaknya praktis dan murah,
tetapi jika permukaan tanah ditutupi semak akan menyulitkan dalam pengumpulan
buah. Menurut cara ini buah dikumpulkan satu bulan sekali, tetapi banyak juga buah
yang tidak mau jatuh meskipun sudah tua dan malahan berkecambah sewaktu masih
berada dipohon. Dengan cara pemanenan tadi tajuk pohon tidak pernah dibersihkan
(dipelihara) sehingga mudah terserang hama dan penyakit.
Pemetikan buah dilakukan dengan memanjat atau menjolok memakai galah.
Pekerjaan memanjat dapat dilakukan oleh manusia atau sejenis kera (Pithecus
nemestrinus). Kapasitas tukang panjat lebih kurang 12-18 pohon per hari, dan dengan
galah 20-25 pohon per hari. Keuntungan memakai tukang panjat ialah karena dapat
membersihkan tajuk pohon.
Masa panen berlangsung sepanjang tahun, setiap pohon dapat dipanen satu
bulan sekali, dan dua bulan atau tiga bulan sekali. Jangka waktu biasanya tergantung
dari periode penyiangan dan perbaikan tanah yang biasanya dilakukan bersamaan
dengan pemanenan.
3. Daging Buah Kelapa
Daging buah kelapa yang sudah masak dapat dijadikan kopra dan bahan
makanan, daging buah merupakan sumber protein yang penting dan mudah dicerna.
Komposisi kimia daging buah kelapa ditentukan oleh umur buah. Pada tabel 2
dapat dilihat komposisi kimia buah kelapa pada berbagai tingkat kematangan.
(Ketaren, 1986)
4. Pembuatan kopra
Daging buah kelapa (Endosperm) yang sudah dikeringkan dinamakan kopra.
Proses pembuatan kopra ialah proses mengeringkan daging buah kelapa. Tahap-tahap
pengeringan untuk mendapatkan kopra bermutu baik adalah :
- Kadar air daging buah kelapa segar yang besarnya 50 sampai 55 persen, pada
periode 24 jam pertama diturunkan menjadi 35 persen.
- Pada periode 24 jam kedua, kadar air tersebut diturunkan menjadi 20 persen.
- Pada periode 24 jam berikutnya, diturunkan menjadi 6 sampai 5 persen.
Metode umum pembuatan kopra terdiri atas 3 cara yaitu :
1. Pengeringan dengan sinar matahari (Sun Drying)
2. Pengeringan dengan bara atau pengasapan diatas api (Smoke Curing or Drying
Over an Open Fire).
3. Pengeringan dengan pemanasan secara tidak langsung (Indirect Drying)
Dalam praktiknya ketiga cara diatas sering dikombinasikan untuk mendapatkan
hasil yang lebih baik.
Produksi kopra dunia selama periode 1970 – 1980 telah meningkat rata – rata
sebesar 3,12 % per tahun, yakni dari 3,3 juta ton pada tahun 1970 menjadi 4,57
juta pada tahun 1980. Juga kontribusi Indonesia meningkat dari 25,3 % menjadi
30,5 %. Laju pertumbuhan produksi kopra di Indonesia per tahun rata – rata 5,3%
lebih besar dari pada Filipina 3,7 %. Hal ini karena selama periode tersebut
produksi kopra Indonesia terus meningkat.
(Asnawi, 1985)
2.1.1. Manfaat Kelapa
Sampai saat ini pemanfaatan kelapa sebagai bahan baku industri masih belum
optimal. Sedangkan peluang untuk meningkatkan nilai ekonominya cukup besar
mengingat keanekaragaman produk yang sudah dikenal oleh masyarakat. Di
Indonesia, industri yang sudah berkembang dengan menggunakan bahan baku kelapa
masih terbatas pada bahan mentah sebagai industri minyak goreng. Keterbatasan
keragaman olahan produk ini tidak memungkinkan untuk perkembangan agroindustri
nasional. Keterbatasan jenis produk tidak akan bisa meningkatkan pendapatannya.
Oleh karena itu, penganekaragaman produk olahan harus dilakukan, sekalipun harus
bertumpu pada produk yang sudah dikenal masyarakat atau untuk mendukung produk
industri yang lain.
Buah kelapa dipasarkan pada umur yang berbeda. Bunga kelapa yang belum
mekar disadap niranya untuk diolah menjadi gula merah atau gula semut, kelapa yang
dipanen muda dijual dipasar sebagai kelapa muda, yang dikonsumsi air dan
dagingnya, kira – kira 7-8 bulan semenjak bunga mekar. Namun demikian, di pasar
kelapa muda ini terbatas dikota-kota besar saja. Kelapa yang dipanen tua mempunyai
kering (Desiccated Coconut) bahan kue dan margarin, bahan baku sabun atau
makanan tradisional (tempe bungkil) dan sebagainya.
(Syamsulbahri, 1986)
Nira Kelapa
Nira kelapa mempunyai prospek pengembangan yang baik. Kandungan
karbohidrat (terutama sukrosa cukup tinggi). Selain dari pada itu nira kelapa
merupakan media yang sangat baik bagi perkembangbiakan mikroorganisme,
sehingga merupakan bahan yang baik untuk produksi minuman beralkohol, misalnya
tuak. Dari nira kelapa juga dapat dibuat bahan olahan lain misalnya gula kelapa, nata
de coco, asam cuka, produk minuman dan substrat.
(Jatmika et al, 1990)
a. Gula Kelapa
Kandungan sukrosa yang dominan diantara kandungan bahan kimia non-air
lainnya menjadikan nira sebagai sumber gula yang sangat potensial. Pembuatan gula
kelapa pada prinsipnya terdiri dari 2 tahap, yaitu penguapan air dan pengkristalan
gula. Penguapan air dilakukan sampai kadar air menguap semuanya. Produk akhir
prosesing nira kelapa dengan penguapan ini menghasilkan 2 produk yaitu gula kelapa
dan gula semut.
(Jatmika et al, 1990)
b. Nata de coco
Nata de coco adalah bahan olahan nira kelapa berbentuk gel, tekstur kenyal
seperti kolang kaling. Pembuatan bahan makanan ini dibantu oleh proses fermentasi
c. Asam Cuka
Asam cuka digunakan dalam bahan makanan sebagai penguat rasa, warna, dan
juga untuk bahan pengawet. Asam cuka dapat mengawetkan bahan makanan karena
kemampuannya dalam membatasi pertumbuhan bakteri.
d. Produk Minuman
Dari hasil nira kelapa dibuat minuman segar non-alkohol maupun ynag
mengalami fermentasi sehingga menghasilkan alkohol dengan kadar rendah (tuak) dan
berkadar alkohol tinggi seperti arak.
e. Substrat
Nira mengandung bahan kimia yang sangat mendukung untuk diproses lebih
lanjut menjadi substrat, yaitu bahan nutrient yang dipergunakan untuk menumbuhkan
mikroba. Dengan demikian substrat sangat diperlukan bagi pekerjaan di laboratorium
Bioteknologi.
(Syamsulbahri, 1986)
2.2. Spesifikasi Minyak Kelapa
Spesifikasi merupakan hal yang sangat penting untuk menentukan kualitas
minyak, apakah minyak bermutu baik atau tidak. Berikut ini spesifikasi standart mutu
minyak Kelapa atau Crude Coconut Oil (CCO) berdasarkan MEOMA
( Malaysia Edible Oil Of Manufacture Assosiation) sebagai suatu acuan terhadap
Tabel.1. Spesifikasi Mutu Minyak Kelapa / CCO Menurut MEOMA
Karakteristik Minyak
Kelapa
Keterangan
Asam Lemak Bebas (sebagai asam laurat)
Kadar Air & Kadar Kotoran
Bilangan Iodin (Wijs)
4 %
1 %
12 mg/g
Maksimum
Maksimum
Minimum
Sumber. PT. PALMCOCO LABORATORIES
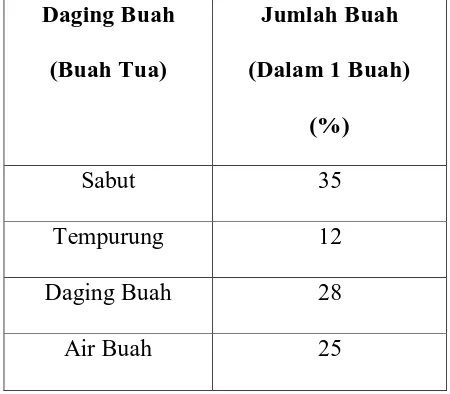
2.2.1. Komposisi Buah Kelapa
Tabel 2. Komposisi Buah Kelapa
Daging Buah
(Buah Tua)
Jumlah Buah
(Dalam 1 Buah)
(%)
Sabut 35
Tempurung 12
Daging Buah 28
Air Buah 25
2.2.2. Komposisi Kimia Daging Buah Kelapa Pada Berbagai
Tingkat Kematangan
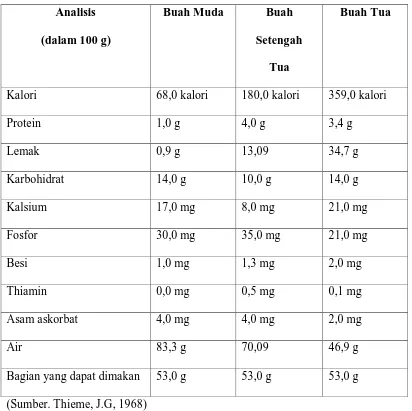
Tabel 3. Komposisi Kimia Daging Buah Kelapa Pada Berbagai
Tingkat Kematangan
Analisis
(dalam 100 g)
Buah Muda Buah
Setengah
Tua
Buah Tua
Kalori 68,0 kalori 180,0 kalori 359,0 kalori
Protein 1,0 g 4,0 g 3,4 g
Lemak 0,9 g 13,09 34,7 g
Karbohidrat 14,0 g 10,0 g 14,0 g
Kalsium 17,0 mg 8,0 mg 21,0 mg
Fosfor 30,0 mg 35,0 mg 21,0 mg
Besi 1,0 mg 1,3 mg 2,0 mg
Thiamin 0,0 mg 0,5 mg 0,1 mg
Asam askorbat 4,0 mg 4,0 mg 2,0 mg
Air 83,3 g 70,09 46,9 g
Bagian yang dapat dimakan 53,0 g 53,0 g 53,0 g
(Sumber. Thieme, J.G, 1968)
Dari tabel diatas dapat dilihat bahwa semakin tua umur buah kelapa maka
kandungan lemaknya semakin tinggi.
2.3. Minyak dan Lemak
Lemak dan minyak merupakan zat makanan yang penting untuk menjaga
kesehatan tubuh manusia. Selain itu lemak dan minyak juga merupakan sumber energi
yang lebih efektif dibanding dengan karbohidrat dan protein. Satu gram minyak atau
lemak dapat menghasilkan 9 kilokalori, sedangkan karbohidrat dan protein hanya
menghasilkan 4 kilokalori/gram. Minyak atau lemak, khususnya minyak nabati,
mengandung asam-asam lemak esensial seperti asam linoleat, linolenat, dan
arakidonat yang dapat mencegah penyempitan pembuluh darah akibat penumpukan
kolesterol. Minyak dan lemak juga berfungsi sebagai sumber dan pelarut bagi
vitamin-vitamin A, D, E, dan K.
(Winarno, 1997)
Minyak dan lemak termasuk salah satu anggota golongan lipid, yaitu lipid
netral. Lipid itu sendiri dapat diklasifikasikan menjadi 4 kelas, yaitu 1) lipid netral, 2)
fosfatida, 3) spingolipid, dan 4) glikolipid. Semua jenis lipid ini banyak terdapat
dialam.
Minyak dan lemak yang telah dipisahkan dari jaringan asalnya mengandung
sejumlah kecil komponen selain triglisrida, yaitu 1) lipid kompleks (lesithin, cephalin,
fosfatida dan glikolipid), 2) sterol, berada dalam keadaan bebas atau terikat dengan
asam lemak, 3) asam lemak bebas, 4) lilin, 5) pigmen yang larut dalam lemak, dan 6)
hidrokarbon.
( Ketaren, 1986)
Lemak dan minyak dalam bidang biologi dikenal sebagai salah satu bahan
penyusun dinding sel dan penyusun bahan-bahan biomolekul. Dalam bidang gizi,
lemak dan minyak merupakan sumber biokalori yang cukup tinggi nilai kilokalorinya
tak jenuh yang esensial yaitu linoleat dan linolenat. Disamping itu lemak dan minyak
juga merupakan sumber alamiah vitamin-vitamin yang teralarut dalam minyak yaitu
vitamin A, D, E, dan K.
(Sudarmadji, 1989)
2.4. Asam Lemak
Asam lemak, bersama-sama dengan gliserol, merupakan penyusun utama
minyak nabati atau lemak dan merupakan bahan baku untuk semua lipida pada
makhluk hidup. Asam ini mudah dijumpai dalam minyak masak (goreng), margarin,
atau lemak hewan untuk menentukan nilai gizinya. Secara alami, asam lemak bebas
berbentuk bebas (karena lemak yang terhidrolisis) maupun terikat sebagai gliserida.
Asam lemak yang ditemukan dialam, biasanya merupakan asam-asam
monokarboksilat dengan rantai yang tidak bercabang dan mempunyai jumlah atom
karbon genap. Asam-asam lemak yang ditemukan dialam dapat dibagi menjadi dua
golongan, yaitu asam lemak jenuh dan asam lemak tidak jenuh. Asam – asam lemak
tidak jenuh berbeda dalam jumlah dan posisi ikatan rangkapnya, dan berbeda dengan
asam lemak jenuh dalam bentuk molekul keseluruhannya.
(Winarno, 1997)
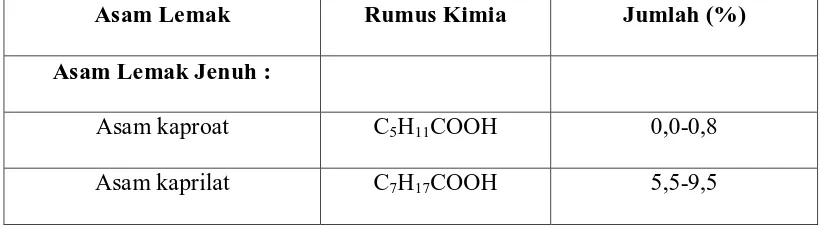
Tabel 4. Komposisi Asam Lemak Minyak Kelapa
Asam Lemak Rumus Kimia Jumlah (%)
Asam Lemak Jenuh :
Asam kaproat C5H11COOH 0,0-0,8
Asam kaprat C9H19COOH 4,5-9,5
Asam laurat C11H23COOH 44,0-52,0
Asam miristat C13H27COOH 13,0-19,0
Asam palmitat C15H31COOH 7,5-10,5
Asam stearat C17H35COOH 1,0-3,0
Asam arachidat C19H39COOH 0,0-0,4
Asam Lemak Tidak Jenuh :
Asam palmitoleat C15H29COOH 0,0-1,3
Asam oleat C17H33COOH 5,0-8,0
Asam linoleat C17H31COOH 1,5-2,5
(Sumber. Thieme, J.G, 1968)
2.5 Asam Lemak Jenuh dan Asam Lemak Tidak Jenuh
Asam lemak adalah suatu senyawa hidrokarbon dengan jumlah atom C dari 2
sampai 24, karena merupakan suatu asam organik, maka dalam struktur molekul asam
lemak terdapat gugus karboksilat : -CHO2. Asam lemak yang ikatan antara atom C
nya tunggal disebut asam lemak jenuh, sedang yang mempunyai 1 ikatan rangkap
(Double Bond) antara 2 atom C nya disebut asam lemak tidak jenuh, asam lemak tidak
jenuh dikenal ada yang ikatan rangkapnya 2,3 sampai 6 (Six Double Bond).
Kadar asam lemak jenuh (ALJ) maupun asam lemak tidak jenuh (ALTJ)
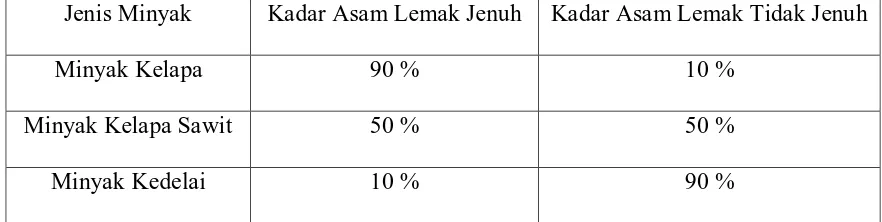
Tabel dibawah ini menggambarkan perbedaan tersebut :
Tabel 5. Komposisi Asam Lemak Jenuh dan Asam Lemak Tidak Jenuh
Jenis Minyak Kadar Asam Lemak Jenuh Kadar Asam Lemak Tidak Jenuh
Minyak Kelapa 90 % 10 %
Minyak Kelapa Sawit 50 % 50 %
Minyak Kedelai 10 % 90 %
2.6. Analisa Titrimetri
Mengukur volume larutan adalah jauh lebih cepat dibandingkan dengan
menimbang berat suatu zat dengan suatu metode gravimetri. Akurasinya sama dengan
metode gravimetri. Analisis titrimetri juga dikenal sebagai analisis volumetri, dimana
zat yang akan dianalisis dibiarkan bereaksi dengan zat lain yang konsentrasiya
diketahui dan dialirkan dari buret dalam bentuk larutan. Konsentrasi larutan yang
tidak diketahui (Analit) kemudian dihitung. Syaratnya adalah reaksi harus berlangsung
secara cepat, reaksi berlangsung kuantitatif dan tidak ada reaksi samping. Selain itu
juga reagen penitrasi yang diberikan berlebih, maka harus dapat diketahui dengan
suatu indikator.
(Khopkar, 1990)
Metode titrimetri masih digunakan secara luas karena merupakan metode yang
tahan, murah, dan mampu memberikan ketepatan (presisi) yang tinggi.
Dalam analisis titrimetri atau analisis volumetri atau analisis kuantitatif dengan
(standar) yang konsentrasinya telah diketahui secara teliti dan reaksinya berlangsung
secara kuantitatif.
Suatu tirasi yang ideal adalah jika titik akhir titrasi sama dengan titik ekivalen
teoritis. Dalam kenyataannya selalu ada perbedaan kecil. Perbedaan ini disebut dengan
kesalahan titrasi yang dinyatakan dengan mililiter larutan baku. Oleh karena itu,
pemilihan indikator harus dilakukan sedemikian rupa agar kesalahan ini
sekecil-kecilnya.
Untuk dapat dilakukan analisis titrimetri harus dipenuhi syarat – syarat
sebagai berikut :
1. Reaksinya harus berlangsung sangat cepat.
2. Reaksinya harus sederhana serta dapat dinyatakan dengan persamaan reaksi.
3. Harus ada perubahan yang terlihat pada saat titik ekivalen tercapai, baik secara
kimia atau secara fisika.
4. Harus ada indikator jika syarat 3 tidak dipenuhi.
Berikut ini adalah hal – hal yang diperlukan dalam analisis secara titrimetri
yaitu :
1. Alat pengukur volume seperti buret, pipet volume, dan labu takar yang
digunakan telah dikalibrasi.
2. Senyawa yang digunakan sebagai larutan baku atau untuk pembakuan harus
senyawa dengan kemurnian yang tinggi.
3. Indikator untuk mengetahui berakhirnya titrasi.
Analisa titrimetri adalah salah satu bagian besar dalam kimia analitik. Sebuah
reaksi harus memenuhi beberapa persyaratan sebelum reaksi tersebut dapat
dipergunakan yaitu :
1. Reaksi tersebut harus diproses sesuai persamaan kimiawi tertentu.
Seharusnya tidak ada reaksi sampingan.
2. Reaksi tersebut harus diproses sampai benar – benar selesai pada titik
ekivalensi
3. Harus tersedia beberapa metode untuk menentukan titik ekivalen tercapai.
4. Diharapkan reaksi tersebut berjalan cepat, sehingga titrasi dapat
diselesaikan dalam beberapa menit.
(Underwood, 1998)
Istilah analisis titrimetri mengacu pada analisis kimia kuantitatif yang
dilakukan dengan menetapkan volume suatu larutan yang konsentrasinya diketahui
dengan tepat, yang diperlukan untuk bereaksi secara kuntitatif dengan larutan dari zat
yang akan ditetapkan. Larutan dengan konsentrasi yang diketahui dengan tepat disebut
larutan standart.
Larutan standart biasanya ditambahkan dari dalam sebuah buret. Proses
penambahan larutan standart sampai reaksi tepat disebut titrasi. Titik pada saat reaksi
tepat disebut titik ekuivalen (setara) atau tittik akhir teoritis (titik-akhir stoikiometri).
Dalam penggunaan analisis titrimteri suatu reaksi harus memenuhi kondisi –
kondisi berikut :
1. Harus ada suatu reaksi yang sederhana, yang dapat dinyatakan dengan suatu
persamaan kimia.
3. Harus ada perubahan yang menyolok dalam energi – bebas yang
menimbulkan perubahan dalam beberapa sifat fisika atau kimia larutan pada
titik – ekuivalen.
4. Harus tersedia suatu indicator.
Dalam analisis titrimetri umumnya menggunakan peralatan yang lebih
sederhana, dan umumnya cepat dikerjakan.
Berikut ini hal – hal yang perlu diperhatikan dalam analisis titrimetri yaitu :
1. Bejana – bejana pengukur harus dikalibarasi, termasuk buret, pipet, dan labu.
2. Zat – zat yang digunakan harus diketahui kemurniannya untuk penyiapan
larutan standart.
3. Adanya indikator untuk mendeteksi lengkapnya reaksi.
(Vogel, 1994)
BAB 3
METODOLOGI PERCOBAAN
3.1. Alat- Alat Soklet pyrex
- Neraca Analitis sartorius
- Bola Penghisap marienfeld
- Botol Akuades -
- Buret 50 ml pyrex
- Mikro Buret 10 ml pyrex
- Gelas Ukur pyrex
- Gelas Beaker pyrex
- Gelas Erlenmeyer pyrex
- Penjepit kayu -
- Oven memmert
- Desikator -
- Pipa Kapiler ( diameter 1 mm) -
- Hot Plate thermostat magnetic stirer
- Pipet Tetes -
- Statif dan Klem -
- Pipet Volume
- Labu Takar pyrex
- Spatula -
- Magnetic Stirer -
- Penyaring Timbal -
- Kertas Saring Whatman No. 1 -
- Pinset -
- Batang Pengaduk -
- Corong -
3.2. Bahan
- Kopra -
- Akuades -
- Bubuk Amilum E merck
- Etanol 96 % p.a E merck
- HCl (p) p.a E merck
- Larutan Wijs -
- Kristal Na2S2O3.5H2O E merck
- Kristal K2Cr2O7 E merck
- Kristal KI 15 % -
- Kristal NaOH 0,1004 N E merck
- Kristal Timol Blue 0,1% p.a E merck
- Kristal H2C2O7.2H2O E merck
- N – Heksan Teknis
- Sikloheksan : Asam Asetat Glasial (1:1) p.a E merck
- Serbuk Phenolphtalein p.a E merck
- Alkohol Netral -
3.3. Prosedur
3.3.1. Prosedur Preparasi Ekstrak Minyak
- Dimasukkan sampel kopra sebanyak 250 g kedalam gelas beaker
1000 ml
- Ditambahkan dengan N-Heksan sampai sampel terendam
seluruhnya, diaduk
- Diuapkan sampel didalam penangas air pada suhu 65-70 oC selama
20 menit
- Didinginkan sampel selama 20 menit lalu didiamkan selama 1
malam dan disaring dengan kertas saring
- Diuapkan ekstrak minyak dalam N-Heksan yang diperoleh sampai
N-Heksan habis menguap
- Ekstrak minyak yang diperoleh dapat digunakan untuk pemeriksaan
Analisa Kadar Asam Lemak Bebas (ALB), Analisa Bilangan
3.3.2. Prosedur Preparasi Sampel
- Dihomogenkan ekstrak minyak yang diperoleh dengan cara dipanaskan
didalam oven pada suhu 80 oC selama 15 menit
- Sampel yang telah homogen dapat digunakan untuk pemeriksaan analisa
Kadar Asam Lemak Bebas (ALB), Analisa Bilangan Iodin, Analisa Kadar
Air dan Analisa Kadar Kotoran.
3.3.3. Prosedur Analisa Kualitas Minyak
- Ditimbang sampel kopra sebanyak ± 8 g
- Dimasukkan sampel kedalam penyaring timbal dan ditutup permukaan
penyaring timbal dengan menggunakan kapas yang bersih
- Ditimbang berat gelas erlenmeyer kosong yang akan digunakan
- Ditambahakan 100 ml N-Heksan kedalam erlenmeyer
- Dimasukkan penyaring timbal yang berisi sampel kedalam alat soklet
- Dirangkai alat soklet pada heating mantel
- Diekstraksi dengan pelarut N-Heksan pada suhu 45-50oC sampai 5 siklus
- Ditampung hasil destilat
- Dipanaskan didalam oven selama 1 jam pada suhu 80oC
- Dimasukkan kedalam desikator selama 30 menit
- Ditimbang berat erlenmeyer dan minyak yang diperoleh
- Ditentukan % minyak yang diperoleh
- Hasil percobaan analisis kualitas minyak dapat dil hat pada tabel 4.1
3.3.4. Prosedur Pembuatan Reagen
a. Prosedur Pembuatan Larutan NaOH 0,1004N
- Ditimbang 8,4 g kristal NaOH dalam gelas beaker
- Dilarutkan dalam akuades bebas CO2
- Dimasukkan kedalam labu takar 1000 ml kemudian diencerkan akuades
sampai garis tanda
Prosedur Standarisasi Larutan NaOH 0,1004N
- Dipipet 5 ml larutan H2C2O4 0,1 N Kemudian dimsukkan ke dalam
Erlenmeyer 100ml
- Ditambah 3 tetes indikator phenolpthalein 1%
- Dititrasi dengan larutan NaOH sampai terbentuk larutan merah rose
- Dicatat volume NaOH yang digunakan
b. Prosedur Pembuatan Larutan Na2S2O3 0,1 N dari Kristal
Na2S2O3.5H2O
- Ditimbang Na2S2O3.5H2O sebanyak 24,8 g kedalam gelas beaker
- Dimasukkan dalam labu takar 1 liter, dan diencerkan sampai
garis tanda
- Distandarisasi dengan Kalium Bikromat
Prosedur Standarisasi Larutan Na2S2O3 0,1 N
- Dipipet 25 ml hasil pengenceran, dimasukkan dalam erlenmeyer
250 ml
- Ditambahkan 20 ml KI 15 % yang fresh
- Ditambahkan 5 ml HCl(p), dikocok, dan didiamkan selama 5 menit
- Dititrasi dengan menggunakan larutan standart Na2S2O3 0,1 N yang dibuat
sampai terlihat warna hijau pada larutan
- Dilanjutkan titrasi sampai terbentuk larutan hijau muda yang jernih pada
larutan.
c. Prosedur Pembuatan Larutan Amilum 1%
- Ditimbang gelas beaker 100 ml kemudian dinolkan
- Ditambah 0,5 g kristal Amilum
- Dilarutkan dengan akuades bebas CO2 di dalam gelas beaker
- Ditambahkan akuades hingga 100 ml
- Dihomogenkan dengan magnetic stirrer
- Dipanaskan hingga menjadi 50 ml
d. Prosedur Pembuatan Larutan KI 15 %
- Ditimbang 15 g kristal KI, kemudian dimasukkan ke dalam gelas beaker 50
ml (dengan menggunakan spatula)
- Dilarutkan dengan menggunakan akuades bebas CO2
- Dipindahkan ke dalam labu takar 100 ml, kemudian diencerkan dengan
menggunakan akuades bebas CO2 sampai garis tanda
- Dihomogenkan dengan magnetic stirrer
e. Prosedur Pembuatan Larutan Alkohol Netral
- Dimasukkan kurang lebih 200 ml etanol 96% ke dalam erlenmeyer 250 ml
- Ditambahkan beberapa tetes indikator Brom Timol Blue 1%
- Ditambah lagi beberapa tetes larutan NaOH 0.1004 N sampai terbentuk
warna hijau muda pada larutan.
f. Prosedur Pembuatan Larutan Brom Timol Blue 1%
- Ditimbang 1 g Brom Timol Blue dan dimasukkan ke dalam labu takar 100
ml
- Dilarutkan dengan etanol 96% hingga garis tanda
- Dimasukkan ke dalam botol gelap dan diberi label.
g. Prosedur Pembuatan Larutan Phenolphtalein 1%
- Ditimbang 1 g Phenolphtalein dan dimasukkan ke dalam labu takar 100 ml.
- Dilarutkan dengan etanol hingga garis tanda.
- Dimasukkan ke dalam botol dan diberi label.
h. Prosedur Pembuatan Larutan K2Cr2O7 1.5 gr dalam 250 ml
- Ditimbang 1,5 g kristal K2Cr2O7 yang telah dikeringkan dan dimasukkan
ke dalam gelas beaker 50 ml
- Dilarutkan dengan akuades dan dimasukkan ke dalam labu takar 250 ml
hingga garis tanda
- Dihomogenkan
i. Pembuatan larutan Wijs
Pereaksi yang terdiri dari 13 gram iodin dilarutkan dalam 1000 ml asam asetat
galsial, kemudian dialirkan gas klor sampai terlihat perubahan warna yang
menunjukkan bahwa jumlah gas klor yang dimasukkan sudah cukup. Pembuatan
larutan inin agak sukar dan bersifat tidak tahan lama. Larutan ini sangat peka terhadap
cahaya dan panas serta udara, sehingga harus disimpan ditempat yang gelap, sejuk dan
tertutup rapat.
(Ketaren, 1986)
3.3.4 Prosedur Analisa
A. Penentuan Asam Lemak Bebas
- Ditimbang berat gelas erlenmeyer kosong 50 ml kemudian dinolkan
- Ditimbang ekstrak minyak kopra sebanyak ± 2,5 g
- Ditambahkan 10 ml N-Heksan
- Ditambahkan 25 ml alkohol netral
- Ditambahkan 3 tetes indikator phenolpthalein 1%
- Ditirasi dengan larutan standart NaOH 0.1004 N sampai terbentuk warna
merah rose
- Dicatat volume NaOH 0,1004 N yang digunakan
- Dilakukan perlakuan yang sama sebanyak 3 kali
- Hasil percobaan analisis asam lemak bebas dapat dilihat pada tabel 4.2
B. Prosedur Analisa Bilangan Iodin
- Ditimbang berat gelas erlenmeyer kosong 250 ml kemudian dinolkan
- Dimasukkan ± 0,5 g ekstrak minyak kopra
- Ditambahkan larutan sikloheksan : asam asetat glasial ( 3:1) sebanyak 20
ml
- Ditambahkan larutan wijs sebanyak 25 ml
- Disimpan didalam ruangan yang gelap selama 30 menit
- Ditambahkan KI 15% sebanyak 20 ml
- Dititrasi dengan larutan standart Na2S2O3 0,1 N hingga larutan berwarna
kuning cerah
- Ditambahkan indikator amilum 1%
- Dititrasi kembali dengan larutan standart Na2S2O3 0,1 N hingga larutan
berwarna putih
- Dicatat volume larutan standart Na2S2O3 0,1 N yang terpakai
- Dilakukan perlakuan yang sama sebanyak 3 kali
- Hasil percobaan analisis bilangan iodin dapat dilihat pada tabel 4.3
C. Prosedur Analisa Kadar Air
- Ditimbang berat gelas beaker kosong 50 ml kemudian dinolkan
- Dicatat berat gelas beaker
- Ditambahkan ekstrak minyak kopra sebanyak ± 5 g
- Dipanaskan didalam oven pada suhu 105oC selama 1 jam
- Didinginkan didalam desiktor selama 30 menit
- Ditimbang berat gelas beaker setelah pemanasan
- Dicatat berat gelas beaker setelah pemanasan
- Dilakukan perlakuan yang sama sebanyak 3 kali
- Hasil percobaan analisis kadar air dapat dilihat pada tabel 4.4
D. Prosedur Analisa Kadar Kotoran
- Dipanaskan kertas saring didalam oven selama 1 jam pada suhu 105oC
- Didinginkan didalam desikator selama 30 menit
- Diangkat kertas saring didalam oven dengan menggunakan penjepit
- Ditimbang berat kertas saring lalu dicatat hasilnya
- Ditimbang ekstrak minyak kopra sebanyak ± 1 g dalam gelas beaker 50 ml
- Dilarutkan ekstrak minyak kopra dengan N-Heksan dan disaring dengan
menggunakan kertas saring
- Dicuci ekstrak minyak kopra yang tertinggal dikertas saring sampai ekstrak
minyak kopra benar – benar telah habis dari kertas saring ( sampai warna
ekstrak minyak kopra hilang dari kertas saring )
- Dimasukkan kembali kertas saring dan impurities dari ekstrak minyak
- Didinginkan didalam oven slama 30 menit
- Ditimbang kertas saring dan dicatat hasilnya
BAB 4
HASIL DAN PEMBAHASAN
4.1. Hasil Percobaan
Hasil analisa kualitas minyak ditunjukkan pada tabel sebagai berikut :
4.1.1. Data
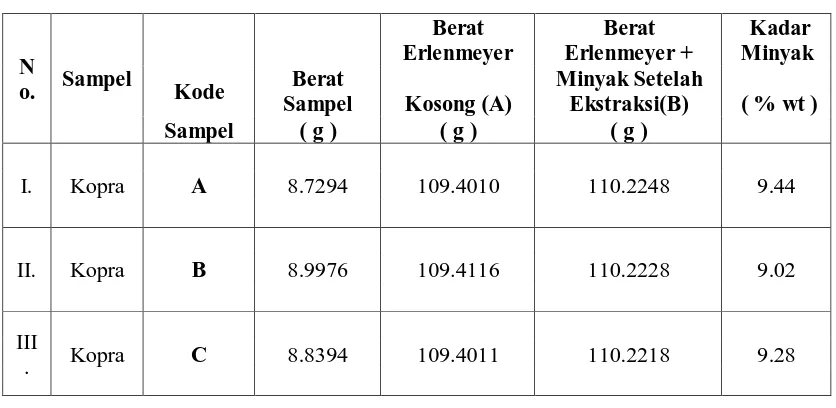
Tabel 4.1. Data Penentuan Kadar Minyak (%) dari Hasil Ekstraksi Kopra Dengan Pelarut N -Heksan
Penentuan Kadar Minyak
Kadar Minyak (%) = ( ) x100%
Sampel Berat
Keterangan:
A = Berat Erlenmeyer Kosong (g)
B = Berat Erlenmeyer + Minyak Setelah Ekstraksi (g)
Contoh Perhitungan Kadar Minyak dari Hasil Ekstraksi Kopra:
A = 109,4010 g
B = 110,2248 g
Berat Sampel = 8,7294 g
Kadar Minyak (%) = ( ) x100%
Sampel Berat
A B−
= 100%
7294 , 8
) 4010 , 109 2248 , 110 (
x −
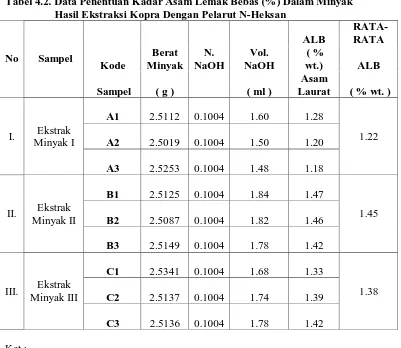
Tabel 4.2. Data Penentuan Kadar Asam Lemak Bebas (%) Dalam Minyak
Penentuan Kadar Asam Lemak Bebas (ALB)
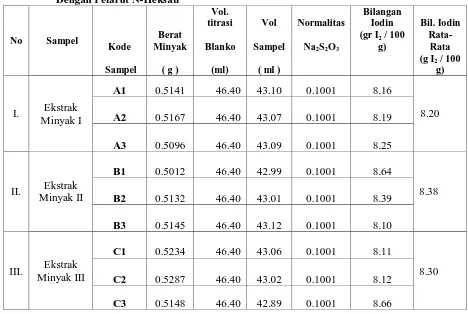
Tabel 4.3. Data Penentuan Bilangan Iodin (g I2 / 100 g) Dalam Minyak Hasil Ekstraksi Kopra
Dengan Pelarut N-Heksan
No Sampel
Vol.
titrasi Vol Normalitas
Bilangan
Penentuan Bilangan Iodin (IV)
Bilangan Iodin (Iodine Value) =
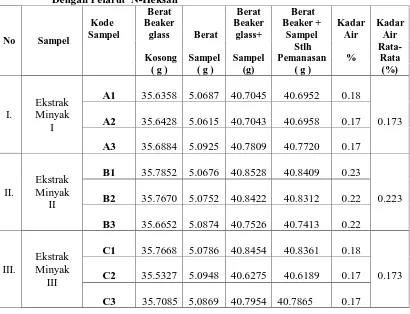
Tabel 4.4. Data Penentuan kadar Air (%) Dalam Minyak Hasil Ekstraksi Kopra
Penentuan Kadar Air
Contoh perhitungan kadar air dari hasil ekstraksi kopra:
BA = 40,7045 g
BB = 40,6952 g
BS = 5,0687 g
Kadar Air ( % ) = ( ) x100%
BS BB BS BA+ −
= 100%
0687 , 5
6952 , 40 ) 0687 , 5 7045 , 40 (
x −
+
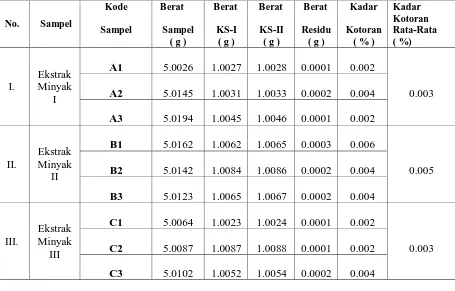
Tabel 4.5. Data Penentuan kadar Kotoran (%) Dalam Minyak Hasil Ekstraksi Kopra
Penentuan Kadar Kotoran
Kadar Kotoran ( % ) =
( )
( )
x100%Berat KS-I = Berat Kertas Saring Sebelum Pemanasan
Contoh perhitungan kadar kotoran dari hasil ekstraksi kopra:
Berat KS-I = 1,0027 g
Berat KS-II = 1,0028 g
Berat sampel = 5,0026 g
Kadar Kotoran ( % ) =
( )
( )
x100%Sampel Gram
II KS Berat I
KS Berat −
= 100% 0026
, 5
0028 , 1 0027 , 1
x −
4.2. Pembahasan
Dari hasil percobaan yang dilakukan, ekstrak minyak yang digunakan pada
analisa Asam Lemak Bebas (ALB), Bilangan Iodin, Kadar Air dan Kadar Kotoran
tidak berasal dari ekstraksi sokletasi, hal ini disebabkan karena minyak yang
dihasilkan pada ekstraksi sokletasi sangat sedikit, sehingga ekstrak minyak yang
diperoleh tidak dapat digunakan untuk menganalisa Asam Lemak Bebas (ALB),
Bilangan Iodin, Kadar Air dan Kadar Kotoran, sehingga dibutuhkan 3 kali ekstraksi
kopra untuk dapat menganalisa Asam Lemak Bebas (ALB), Bilangan Iodin, Kadar Air
dan Kadar Kotoran.
Dari hasil percobaan juga diperoleh faktor-faktor yang mempengaruhi
perbedaan hasil penelitian dengan kualitas Minyak Kelapa/Crude Coconut Oil (CCO)
yang diperoleh secara pabrik. Faktor-faktor tersebut antara lain adalah pelarut yang
digunakan selama analisa, proses pengolahan dan kadar air yang terdapat pada
sampel.
Dari hasil percobaan juga diperoleh hubungan antara data yang diperoleh
selama percobaan dengan standart mutu yang ada telah memenuhi spesifikasi atau
standart mutu yang telah ditetapkan oleh MEOMA ( Malaysia Edible Oil Of
Manufacture Assosiation).
Pada percobaan yang dilakukan dalam Penentuan Kualitas Minyak yang di
Peroleh dari Hasil Ekstraksi Kopra dengan Pelarut N-Heksan dilakukan dengan
menggunakan metode Titrimetri karena metode ini masih digunakan secara luas
karena merupakan suatu metode yang tahan lama, murah, dan mampu memberikan
ketepatan (presisi) yang tinggi dan dalam mengukur volume dari suatu larutan jauh
lebih cepat dibandingkan dengan menimbang berat suatu zat dengan menggunakan
BAB 5
KESIMPULAN DAN SARAN
5.1. Kesimpulan
1. Dari data hasil penelitian yang dilakukan dapat disimpulkan bahwa dalam
penentuan kualitas minyak yang diperoleh dari hasil ekstraksi kopra dengan
pelarut N – Heksan diperoleh hasil :
- Kadar Minyak (%) yaitu 9,02% - 9,44%.
- Kadar Asam Lemak Bebas (ALB) (%) yaitu 1,22% - 1,45%.
- Kadar Bilangan Iodin (g I2/100 g) yaitu 8,20 g I2/100 g – 8,38 g I2/100 g.
- Kadar Air (%) yaitu 0,18% - 0,22%.
- Kadar Kotoran (%) yaitu 0,003% - 0,005%.
2. Dari data hasil penentuan kualitas minyak yang dilakukan diperoleh hasil
analisa yang masih memenuhi spesifikasi atau standart mutu yang ditetapkan
oleh MEOMA (Malaysia Edible Oil Of Manufacture Assosiation).
5.2 Saran
Disarankan kepada peneliti selanjutnya agar dapat menganalisa minyak yang
diperoleh dari hasil ekstraksi kopra dengan menggunakan pelarut yang berbeda dan
sumber yang berbeda pula, sehingga kita dapat mengetahui perbedaan yang terjadi
DAFTAR PUSTAKA
Adlin.U.1992.Vademekum Kelapa : Pusat Penelitian Perkebunan Marihat.
Bandar Kuala.
Asnawi. A. 1985. Prospek Ekonomi Tanaman Kelapa Dan Masalahnya
Di Indonesia : Departemen Pertanian Badan Penelitian
Dan Pengembangan Pertanian Balai Penelitian Kelapa. Manado.
http://kiathidupsehat.wordpress.com, diakses tanggal 22 April 2009.
Ketaren. S. 2005. Pengantar Teknologi Minyak Dan Lemak Pangan: Edisi
Pertama. Cetakan Pertama. UI-Press. Jakarta.
Khopkar. S. M. 1990. Konsep Dasar Kimia Analitik : UI-Press. Jakarta.
Rohman. A. 2007. Kimia Farmasi Analisis : Universitas Gadjah Mada. Yogyakarta.
Sudarmadji. S. 1989. Analisa Bahan Makanan Dan Pertanian : Universitas
Gadjah Mada. Yogyakarta.
SyamsulBahri. 1996. Bercocok Tanam Tanaman Perkebunan Tahunan : Universitas
Gadjah Mada. Yogyakarta.
Underwood. A. L. 1998. Analisis Kimia Kuantitatif: Edisi Keenam. Penerbit Erlangga.
Jakarta.
Winarno. F. G. 1997. Kimia Pangan Dan Gizi : PT. Gramedia Pustaka Utama. Jakarta.
Vogel. A. I. 1994. Kimia Analisis Kuantitatif Anorganik : Penerbit Buku Kedokteran,