AKTIVITAS ANTIOKSIDAN MINUMAN SERBUK BUAH BUNI
(Antidesma bunius (L.) Spreng)
PADA TINGKAT KEMATANGAN
YANG BERBEDA
TRI RETI RAHMAWATI
MAYOR ILMU GIZI
DEPARTEMEN GIZI MASYARAKAT FAKULTAS EKOLOGI MANUSIA
ABSTRACT
TRI RETI RAHMAWATI. Antioxidant Activity of Bignay‟s Powdered Beverage
(Antidesma bunius (L.) Spreng) in Different Maturity Level. Supervised by AHMAD SULAEMAN and IKEU EKAYANTI.
Bignay fruit contains antosianin which has high prospects to be developed into functional food. The aim of this research is to develop functional food from bignay fruit into powdered beverage that consists of antioxidants. The formula of this beverage is determined based on maturity level, sweetness level which are 10%, 15%, and 20% and also additional citric acid in 0.1%, 0.2% and 0.3%. The best product is chosen using organoleptic test, followed by characteristic physico-chemical test of the bignay powdered beverage. The chosen beverage formula of fully riped matured bignay (FRMB) is 20% sweetness and 0.3% citric acid, formula of medium riped matured bignay (MRMB) is 20% sweetness and 0.2% citric acid, and formula of non-riped matured bignay (NRMB) is 20% sweetness and 0.1% citric acid. The color of this beverage is red-purple (FRMB beverage), purple (MRMB beverage), and blue (NRMB beverage).The total soluble solid for the three types of bignay powdered beverage ranges from 9.2-9.8 °Brix. The total acid titration of FRMB beverage is greater than MRMB and NRMB. The pH of the three types of beverages range from 2.66 – 2.93. The vitamin C content of NRMB beverage is greater that FRMB and MRMB. FRMB and FRMB beverage has a higher total anthocyanin and antioxidant activity than fruits and beverage of MRMB and NRMB.
RINGKASAN
TRI RETI RAHMAWATI. Aktivitas Antioksidan Minuman Serbuk Buah Buni
(Antidesma bunius (L.) Spreng) pada Tingkat Kematangan yang Berbeda. Dibimbing oleh AHMAD SULAEMAN dan IKEU EKAYANTI.
Buah buni yang mengandung antosianin memiliki prospek yang sangat cerah untuk dikembangkan sebagai pangan fungsional. Selama ini pemanfaatan buah buni di Indonesia menjadi bahan olahan yang memiliki masa simpan relatif singkat dan bernilai ekonomis masih terbatas yaitu hanya dikonsumsi segar atau dikonsumsi sebagai rujak. Salah satu cara yang dapat dilakukan untuk memanfaatkan hasil panen sekaligus untuk mencegah terjadinya kehilangan hasil ialah dengan cara mengelola buah buni menjadi sebuah produk yang bermutu dan bernilai ekonomis. Dalam satu tandan kematangan buah buni tidak bersamaan. Diversifikasi pemanfaatan dan peningkatan nilai tambah buah buni, antara lain dapat dilakukan melalui pembuatan minuman serbuk buah buni berdasarkan tingkat kematangan buah buni.
Tujuan umum penelitian ini adalah untuk mengembangkan makanan fungsional dari buah buni dalam bentuk minuman serbuk yang mengandung antioksidan alami. Tujuan Khusus penelitian ini adalah (1) mengetahui tingkat ekstraksi paling efisiensi dalam penyiapan minuman serbuk buah buni, (2) mengetahui perbandingan buah buni dan bahan pengisi agar menghasilkan tepung buah buni dan perbandingan tepung buah buni dan bahan pengisi agar tepung dapat larut sempurna ketika dicampurkan dengan pelarut (air) serta mengetahui rendemen tepung buah buni, (3) mengevaluasi sifat organoleptik (deskripsi dan tingkat kesukaan) minuman serbuk buah buni serta mengetahui daya terima minuman serbuk buah buni, (4) mengetahui pengaruh tingkat kematangan buah buni terhadap aktivitas antioksidan pada minuman serbuk buah buni, dan (5) menganalisis sifat fisikokimia (kelarutan, densitas kamba, dan kadar air, warna, total padatan terlarut, total asam tertitrasi, pH, vitamin C, total antosianin, dan aktivitas antioksidan) minuman serbuk buah buni.
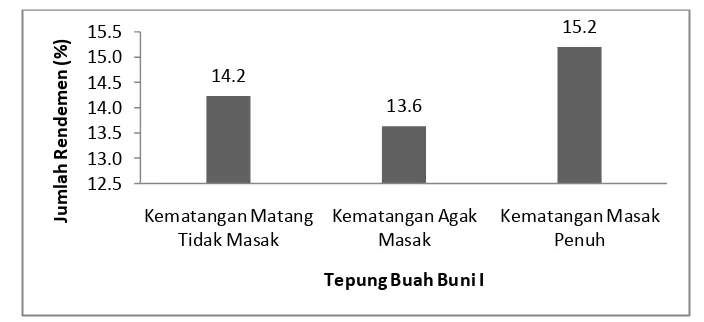
Penelitian ini berlangsung pada bulan bulan Juli sampai Desember 2010. Penelitian ini dilakukan dalam dua tahap, yaitu penelitian pendahuluan dan penelitian lanjutan. Penelitian pendahuluan dilakukan untuk mengetahui tingkat ekstraksi optimum pada setiap kematangan hingga fitrat sampel menunjukkan warna putih dan untuk mengetahui perbandingan buah buni dan bahan pengisi agar menghasilkan tepung buah buni serta perbandingan tepung buah buni dan bahan pengisi agar tepung dapat larut sempurna ketika dicampurkan dengan pelarut (air) serta mengetahui rendemen tepung buah buni. Buah buni diekstraksi sebanyak lima kali ekstraksi. Agar menjadi tepung buah buni maltodekstrin yang digunakan adalah 20% (tepung I) dan ditambahkan kembali maltodekstrin agar serbuk minuman larut dalam air dengan perbandingan 1 tepung I:1½ maltodekstrin. Ini disebut tepung buah buni II. Tepung buah buni I pada kematangan masak penuh memilki jumlah rendemen sebesar 15.5%, jumlah rendemen tepung buah buni I pada kematangan agak masak sebesar 13.9% dan jumlah rendemen tepung buah buni I pada kematangan matang tidak masak sebesar 14.5%.
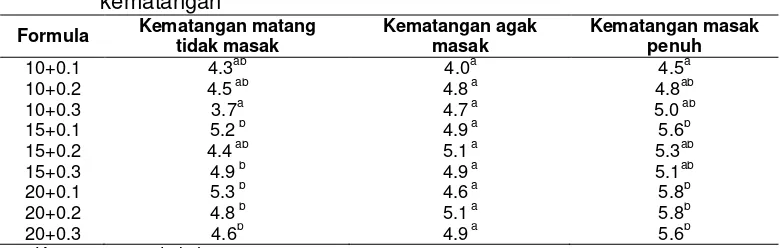
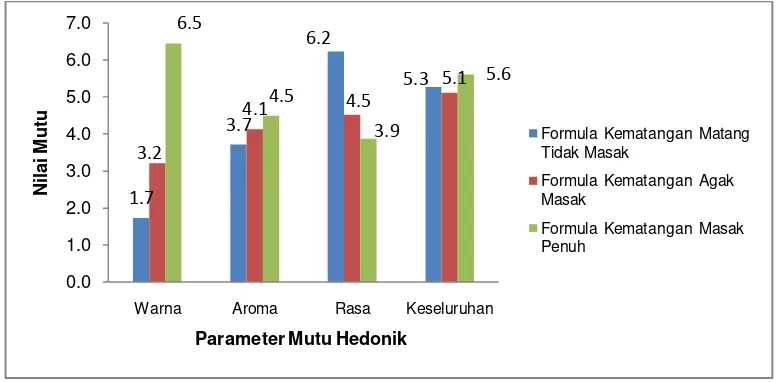
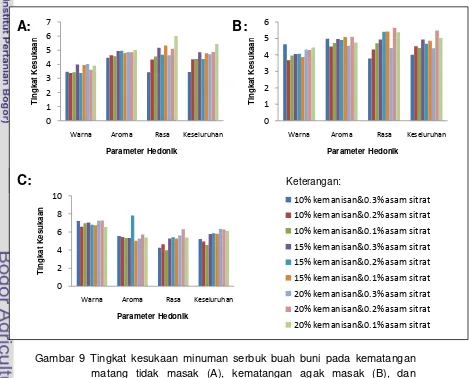
organoleptik dengan 3 termin berbeda oleh 30 orang panelis pada masing-masing termin. Hasil organoleptik menunjukkan bahwa pada kematangan masak penuh formulasi terpilihnya adalah 20% kemanisan dan 0.3% asam sitrat, pada kematangan agak masak formulasi terpilihnya adalah 20% kemanisan dan 0.2% asam sitrat dan pada kematangan matang tidak masak formulasi terpilihnya adalah 20% kemanisan dan 0.1% asam sitrat. Menurut panelis, warna formulasi terbaik minuman serbuk buah buni kematangan masak penuh adalah merah, kematangan agak masakadalah agak merah muda, kematangan matang tidak masak adalah bening. Menurut panelis, aroma formulasi terbaik minuman serbuk buah buni kematangan masak penuh dan agak masak adalah agak beraroma sedangkan pada kematangan matang tidak masak adalah sedikit agak beraroma. Menurut panelis, rasa formulasi terbaik minuman serbuk buah buni kematangan masak penuh dan agak masak adalah asam agak manis sedangkan pada kematangan matang tidak masak adalah manis. Menurut panelis, secara keseluruhan formulasi terbaik minuman serbuk buah buni kematangan masak penuh adalah agak enak (agak segar) sedangkan pada kematangan agak masak dan matang tidak masak menurut panelis adalah biasa. Penerimaan panelis terhadap formula kematangan masak penuh lebih besar (90%) dibandingkan formula kematangan agak masak dan matang tidak masak.
AKTIVITAS ANTIOKSIDAN MINUMAN SERBUK BUAH BUNI
(Antidesma bunius (L.) Spreng)
PADA TINGKAT KEMATANGAN
YANG BERBEDA
TRI RETI RAHMAWATI
Skripsi
Sebagai salah satu syarat untuk memperoleh gelar Sarjana Gizi pada
Departemen Gizi Masyarakat
MAYOR ILMU GIZI
DEPARTEMEN GIZI MASYARAKAT FAKULTAS EKOLOGI MANUSIA
Judul : Aktivitas Antioksidan Minuman Serbuk Buah Buni (Antidesma bunius (L.) Spreng) pada Tingkat Kematangan yang Berbeda Nama : Tri Reti Rahmawati
NIM : I14063147
Menyetujui:
Pembimbing I Pembimbing II
(Prof. Ir. Ahmad Sulaeman, MS., Ph.D) (Dr.Ir. Ikeu Ekayanti, M.Kes)
NIP. 19620331 198811 1 001 NIP. 19660725 199002 2 001
Mengetahui:
Ketua Departemen Gizi Masyarakat
(Dr. Ir. Budi Setiawan, MS) NIP. 19621218 198703 1 001
PRAKATA
Puji dan Syukur penulis ucapkan kepada Allah SWT karena berkat
rahmat dan karuniaNya sehingga penulis dapat menyelesaikan skripsi dengan
baik. Selain itu, banyak pihak yang juga telah membantu penulis selama
perjalanan hidup dan pelaksanaan tugas akhir. Oleh karena itu, penulis ingin
mengucapkan terima kasih dan jazakumullah khairan katsir kepada:
1. Mamah dan Bapak yang sabar dan selalu memberikan dukungan, doa, dan
dorongan semangat selama kuliah dan pengerjaan tugas akhir.
2. Prof. Ir. Ahmad Sulaeman, MS., Ph.D dan Dr.Ir. Ikeu Ekayanti, M.Kes selaku
Dosen Pembimbing Skripsi yang telah memberikan dukungan, arahan, dan
bimbingan selama penulis menjalani pendidikan dan melakukan tugas akhir.
3. Bapak Mashudi atas segala bantuan, masukan dan saran yang diberikan.
4. Leily Amalia Furkon, S.TP, M.Si selaku dosen pemandu seminar serta dosen
penguji atas segala saran dan masukkan yang diberikan.
5. Teh Opie dan A Yudha yang selalu memberikan dukungan, doa, dan
dorongan semangat selama kuliah dan pengerjaan tugas akhir.
6. Aulia, Panji, Rindu, dan Sumi selaku pembahas seminar yang berlangsung
pada hari Rabu, 9 Februari 2011 serta teman-teman yang menemani sidang
pada tanggal 17 Februari 2011 (Noni, Unay, Rai, Mawar, dan Cha-cha).
7. Para Laboran (Ibu Rizky, Pak Basri, Ibu Titi dan Ibu Nina serta Ibu Rubiyah).
8. Sahabat-sahabat JELITAku, sahabat-sahabat Gizi Masyarakat ‟43, „42, ‟44 dan Pondok Ammi serta Pondok Pesantren Al Iffah atas semangat, bantuan,
dan dukungan yang telah diberikan.
9. Kiki, Dimas, Eri dan Dinul atas kesediaan membantu memetik buah buni.
10. Teman-teman satu bimbingan pak Ahmad: Yulaika, Dudung, dan Hilma dan
teman-teman Koplag atas semangat dan dukungannya serta
perkumpulannya selama bimbingan.
11. Semua pihak yang tidak dapat disebutkan satu-persatu atas bantuannya
sehingga penulis dapat menyelesaikan penulisan skripsi.
Penulis menyadari bahwa masih banyak kekurangan dalam pelaksanaan
penelitian dan penyusunan skripsi ini. Penulis berharap agar skripsi ini dapat
memberikan informasi dan bermanfaat bagi semua pihak.
Bogor, Maret 2011
RIWAYAT HIDUP
Tri Reti Rahmawati dilahirkan di Serang pada tanggal 12 Desember 1988
sebagai anak ketiga dari tiga bersaudara, pasangan Agus Wahyudin dan Eti
Sugiarti. Menyelesaikan pendidikan di Serang yaitu TK Baladika Kopassus, SDN
1 Taktakan, SMPN 2 Serang, dan SMAN 1 Serang. Diterima di Institut Pertanian
Bogor melalui jalur Seleksi Penerimaan Mahasiswa Baru (SPMB) pada tahun
2006 sebagai mahasiswa di Institut Pertanian Bogor. Penulis diterima sebagai
mahasiswa Mayor Ilmu Gizi pada tahun 2007 melalui jalur mayor minor dengan
minornya adalah Perkembangan Anak.
Selama menjadi mahasiswa, aktif mengikuti beberapa kegiatan organisasi
dan kemahasiswaan seperti Badan Eksekutif Mahasiswa Tingkat Persiapan
Bersama (BEM TPB) sebagai staf Kewirausahaan, Lembaga Dakwah Kampus Al
Hurriyyah sebagai staf Kewirausahaan, Badan Eksekutif Mahasiswa Fakultas
Ekologi Manusia (BEM FEMA) sebagai staf dan ketua divisi PSDMK, Forum
Syiar Islam FEMA (FORSIA) sebagai staf syiar, KAMMI IPB sebagai staf
Kebijakan Stategis. Selain itu penulis juga aktif dalam berbagai kepanitiaan
tingkat TPB, fakultas, dan kampus.
Penulis melaksanakan Kuliah Kerja Profesi (KKP) di Balumbangjaya,
Kabupaten Bogor, Jawa Barat pada tahun 2009 dan melaksanakan Internship
Dietetik di Rumah Sakit Islam Pondok Kopi Jakarta pada tahun 2010. Penulis
juga pernah menjadi Asisten Pendidikan Agama Islam Tingkat Persiapan
Bersama (PAI TPB), Asisten Praktikum Analisis Zat Gizi Mikro, dan Asisten
Praktikum Konsultasi Gizi Institut Pertanian Bogor.
Sebagai syarat untuk memperoleh gelar Sarjana Gizi Masyarakat, penulis
menyelesaikan skripsinya dengan judul Aktivitas Antioksidan Minuman Serbuk
Buah Buni (Antidesma bunius (L.) Spreng) pada Tingkat Kematangan yang Berbeda di bawah bimbingan Prof. Ir. Ahmad Sulaeman, MS., Ph.D dan Dr.Ir.
DAFTAR ISI
Halaman
DAFTAR TABEL ...iii
DAFTAR GAMBAR ... iv
DAFTAR LAMPIRAN ... v
PENDAHULUAN ... 1
Latar Belakang ... 1
Tujuan ... 2
Manfaat ... 3
TINJAUAN PUSTAKA... 4
Buah Buni ... 4
Antioksidan ... 6
Antosianin ... 7
Pembuatan Minuman Serbuk Buah Buni ... 11
BAHAN DAN METODE ... 14
Tempat dan Waktu Penelitian ... 14
Bahan dan Alat ... 14
Metode Penelitian ... 14
A. Penentuan Tingkat Ekstraksi ... 14
B. Pembuatan Tepung Buah Buni... 16
C. Pembuatan Minuman Serbuk Buah Buni ... 17
D. Analisis Organoleptik dan Fisikokimia Minuman Serbuk Buah Buni ... 18
1. Uji Organoleptik ... 18
2. Analisis Karakteristik Fisikokimia Minuman Serbuk Buah Buni ... 19
2.1 Warna, metode Hunter (Huntching 1999) ... 19
2.2 Kelarutan Dalam Air (Gravimetri) (AOAC 1995) ... 19
2.3 Densitas Kamba (Muchtadi dan Sugiyono 1992) ... 20
2.4 Kadar Air (AOAC 1995) ... 20
2.5 Total Padatan Terlarut (AOAC 1995)... 20
2.6 Total Asam Tertitrasi (Apriyantono et al 1989) ... 21
2.7 pH (AOAC 1995) ... 21
2.8 Total Antosianin (Prior et al., 1998) ... 21
2.10 Aktivitas Antioksidan (DPPH) (Kubo et al., 2002) ... 22
Pengolahan dan Analisis Data ... 23
HASIL DAN PEMBAHASAN ... 24
A. EKSTRAKSI BUAH BUNI ... 24
B. PEMBUATAN TEPUNG BUAH BUNI ... 25
C. FORMULASI MINUMAN SERBUK BUAH BUNI ... 27
1. Karakteristik Deskripsi Organoleptik ... 28
2. Tingkat Kesukaan Panelis Terhadap Formula ... 36
3. Karakteristik Daya Terima Formulasi Terpilih Minuman Serbuk Buah Buni ... 41
D. KARAKTERISTIK FISIKOKIMIA MINUMAN SERBUK BUAH BUNI ... 42
1. Warna ... 42
2. Kelarutan ... 44
3. Densitas Kamba ... 45
4. Kadar Air ... 46
5. Total Padatan Terlarut ... 47
6. Total Asam Tertitrasi ... 48
7. pH ... 49
8. Total Antosianin ... 50
9. Vitamin C ... 51
10. Aktivitas Antioksidan AEAC (Ascorbic Acid Equivalent Antioxidant Capacity) ... 53
KESIMPULAN DAN SARAN ... 56
Kesimpulan ... 56
Saran ... 57
DAFTAR PUSTAKA ... 58
DAFTAR TABEL
1 Kandungan gizi pada 100 gram buah buni………... 6
2 Formulasi minuman serbuk buah buni pada setiap kematangan... 19
3 Rata-rata warna formulasi pada setiap tingkat kematangan... 29
4 Rata-rata rasa formulasi pada setiap tingkat kematangan... 31
5 Rata-rata secara keseluruhan formulasi pada setiap tingkat kematangan... 33
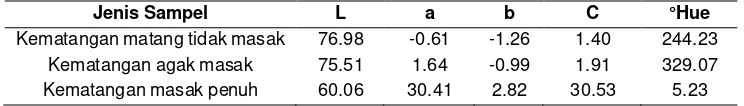
6 Hasil uji warna pada ketiga jenis minuman serbuk buah buni... 43
7 Perbandingan pH ekstraksi, formula tanpa sampel, dan minuman serbuk buah buni dari berbagai tingkat kematangan... 50
8 Perbandingan aktivitas antioksidan AEAC (mg vitamin C/100g) buah, formula tanpa sampel, dan minuman serbuk buah buni pada berbagai tingkat kematangan... 54
DAFTAR GAMBAR
1 Buah buni ………...………... 4
2 Berbagai sturktur antosianin... 8
2 Skema ekstraksi pada beberapa kematangan buah ………... 16
3 Skema pembuatan tepung buah buni ………... 17
5 Skema pembuatan minuman serbuk buah buni .………... 18
6 Hasil ekstraksi buah buni pada kematangan matang tidak masak (A), pada kematangan agak masak (B), dan pada kematangan masak penuh (C)... 25
7 Rendemen tepung buah buni I dari berbagai tingkat kematangan... 27
8 Uji mutu hedonik pada formulasi terbaik minuman serbuk buah buni... 34
9 Tingkat kesukaan minuman serbuk buah buni pada kematangan matang tidak masak (A), kematangan agak masak (B), dan kematangan masak penuh (C)... 41
10 Persentase penerimaan panelis terhadap minuman serbuk formulasi terbaik dalam setiap kelompok tingkat kematangan…….………... 42
11 Tingkat kesukaan pada formulasi terbaik minuman buah buni………... 42
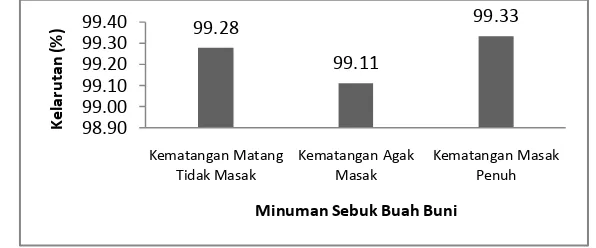
12 Kelarutan minuman serbuk buah buni dari berbagai tingkat kematangan... 45
13 Densitas kamba minuman serbuk buah buni dari berbagai tingkat kematangan …………...………... 46
14 Kadar air minuman serbuk buah buni dari berbagai tingkat kematangan... 47
15 Total padatan terlarut minuman serbuk buah buni dari berbagai tingkat kematangan………...………... 49
16 Total asam tertitrasi minuman serbuk buah buni dari berbagai tingkat kematangan………... 49
17 Perbandingan kandungan antosianin pada buah buni dan minuman serbuk buah buni... 51
18 Perbandingan kandungan vitamin C formula tanpa sampel (formula 0) dan minuman serbuk buah buni pada berbagai tingkat kematangan... 53
DAFTAR LAMPIRAN
1 Formulir uji organoleptik produk minuman serbuk buah buni... 62
2 Hasil organoleptik mutu hedonik warna minuman serbuk buah buni.... 64
3 Hasil organoleptik mutu hedonik aroma minuman serbuk buah buni.... 65
4 Hasil organoleptik mutu hedonik rasa minuman serbuk buah buni... 66
5 Hasil organoleptik mutu hedonik keseluruhan minuman serbuk buah buni………... 67 6 Hasil organoleptik tingkat kesukaan (hedonik) warna minuman
serbuk buah buni... 68
7 Hasil organoleptik tingkat kesukaan (hedonik) aroma minuman
serbuk buah buni... 69
8 Hasil organoleptik tingkat kesukaan (hedonik) rasa minuman serbuk buah buni………... 70 9 Hasil organoleptik tingkat kesukaan (hedonik) keseluruhan minuman
serbuk buah buni... 71
10 Hasil uji Anova mutu hedonik minuman buah buni pada kematangan masak penuh………... 72 11 Hasil uji Duncan’s Multiple Range Test mutu hedonik warna minuman
buah buni pada kematangan masak penuh... 72
12 Hasil uji Duncan’s Multiple Range Test mutu hedonik rasa minuman
buah buni pada kematangan masak penuh…... 73 13 Hasil uji Duncan’s Multiple Range Test mutu hedonik keseluruhan
minuman buah buni pada kematangan masak penuh…………... 73 14 Hasil uji deskripsi mutu hedonik minuman serbuk buah buni pada
kematangan masak penuh………... 73 15 Hasil uji Anova mutu hedonik minuman buah buni pada kematangan
agak masak………... 74 16 Hasil uji Duncan’s Multiple Range Test mutu hedonik warna minuman
buah buni pada kematangan agak masak..………... 74 17 Hasil uji Duncan’s Multiple Range Test mutu hedonik rasa minuman
buah buni pada kematangan agak masak..………... 75 18 Hasil uji deskripsi mutu hedonik minuman serbuk buah buni pada
19 Hasil uji Anova mutu hedonik minuman buah buni pada kematangan matang tidak masak... 75
20 Hasil uji Duncan’s Multiple Range Test mutu hedonik rasa minuman
buah buni pada kematangan matang tidak masak... 76
21 Hasil uji deskripsi mutu hedonik minuman serbuk buah buni pada
kematangan matang tidak masak... 76
22 Hasil uji Duncan’s Multiple Range Test mutu hedonik keseluruhan
minuman buah buni pada kematangan matang tidak masak... 76
23 Hasil uji Anova tingkat kesukaan minuman buah buni pada kematangan masak penuh………... 77 24 Hasil uji Duncan’s Multiple Range Test tingkat kesukaan rasa
minuman buah buni pada kematangan masak penuh... 77
25 Hasil uji Duncan’s Multiple Range Test tingkat kesukaan keseluruhan
minuman buah buni pada kematangan masak penuh... 78
26 Hasil uji Kruskal-Wallis H (uji ranking) tingkat kesukaan minuman buah buni pada kematangan masak penuh………... 78 27 Hasil uji Anova tingkat kesukaan minuman buah buni pada
kematangan agak masak... 79
28 Hasil uji Duncan’s Multiple Range Test tingkat kesukaan rasa
minuman buah buni pada kematangan agak masak... 80
29 Hasil uji Duncan’s Multiple Range Test tingkat kesukaan keseluruhan
minuman buah buni pada kematangan agak masak... 80
30 Hasil uji Kruskal-Wallis H (uji ranking) tingkat kesukaan minuman buah buni pada kematangan agak masak... 81
31 Hasil uji Anova tingkat kesukaan minuman buah buni pada kematangan matang tidak masak...………... 82 32 Hasil uji Duncan’s Multiple Range Test tingkat kesukaan rasa
minuman buah buni pada kematangan matang tidak masak... 82
33 Hasil uji Duncan’s Multiple Range Test tingkat kesukaan keseluruhan
minuman buah buni pada kematangan matang tidak masak... 83
34 Hasil uji Kruskal-Wallis H (uji ranking) tingkat kesukaan minuman buah buni pada kematangan matang tidak masak... 83
35 Hasil uji kadar air, kelarutan, dan densitas kamba minuman serbuk
36 Hasil uji Anova kadar air minuman serbuk buah buni pada berbagai
tingkat kematangan... 84
37 Hasil uji Anova kelarutan minuman serbuk buah buni pada berbagai tingkat kematangan………... 84
38 Hasil uji Anova densitas kamba minuman serbuk buah buni pada berbagai tingkat kematangan………...……... 85
39 Hasil uji korelasi 2-tailed tingkat kematangan, densitas kamba, kelarutan, dan kadar air tepung buah buni………... 85
40 Perhitungan aktivitas antioksidan... 85
41 Hasil uji Anova aktivitas antioksidan... 87
42 Hasil uji Duncan’s Multiple Range Test aktivitas antioksidan... 87
43 Hasil uji warna menggunakan Chromameter Minolta CR-310... 88
44 Hasil uji total padatan terlarut menggunakan Refraktometer Abbe... 88
45 Hasil uji total asam tertitrasi... 89
46 Hasil uji vitamin C minuman serbuk buah buni... 89
PENDAHULUAN
Latar Belakang
Indonesia kaya akan berbagai jenis tanaman buah. Buah merupakan
produk yang berdaya guna antara lain sebagai penunjang gizi masyarakat,
sumber pendapatan, serta menyerap tenaga kerja bila diusahakan secara
intensif. Ditinjau dari kandungan gizinya buah merupakan sumber zat pengatur
yaitu vitamin dan mineral yang sangat diperlukan oleh tubuh manusia (Satuhu
2004).
Sayuran dan buah-buahan merupakan bahan pangan yang kaya akan
antioksidan (Wang 2007). Pada individu yang sehat, keberadan pro-oksidan
dapat diimbangi dengan adanya antioksidan. Akan tetapi pada keadaan tertentu
keseimbangan tersebut terganggu, dimana jumlah pro-oksidan lebih banyak
dibandingkan oksidan. Oleh karena itu, penting sekali untuk meningkatkan kadar
antioksidan di dalam tubuh, dan hal ini dapat dilakukan dengan meningkatkan
konsumsi antioksidan alami (Halliwell 1996). Menurut Wang (2007), beberapa
studi menyebutkan bahwa dengan mengkonsumsi sayuran dan buah-buahan
segar dapat menurunkan resiko terkena kanker dan berbagai penyakit
degeneratif lainnya.
Berbagai jenis bahan pangan yang mengandung antosianin saat ini
sangat populer untuk dijadikan bahan penelitian, diantaranya adalah berbagai
jenis buah berry. Salah satu jenis berry dan merupakan buah lokal adalah
Antidesma bunius (L.) Spreng yang dalam bahasa sehari-hari dikenal dengan nama buni. Tanaman ini berupa pohon yang tingginya dapat mencapai 15-30 m,
garis tengah batang sekitar 20-25 cm (Lembaga Biologi Nasional 1977).
Kandungan bagian buah yang dapat dimakan merupakan 65-80% dari
keseluruhan buah. Asam sitrat merupakan asam organik yang paling menonjol
dalam buah buni (Gruèzo 1997). Warna buah buni mula-mula hijau terang,
setelah dewasa menjadi merah (Lembaga Biologi Nasional 1977). Buah buni
mengandung antosianin karena buahnya yang berwarna merah hingga ungu
(violet).
Antosianin diyakini mempunyai efek antioksidan yang sangat baik.
Sebuah penelitian yang dilakukan di Universitas Michigan Amerika Serikat
menunjukkan bahwa antosianin dapat menghancurkan radikal bebas, lebih efektif
daripada vitamin E yang selama ini telah dikenal sebagai antioksidan kuat.
antosianin memiliki prospek yang sangat cerah untuk dikembangkan sebagai
komponen pangan fungsional (Astawan dan Kasih 2008).
Menurut Gruèzo (1997), manfaat buah buni yang matang dapat
dikonsumsi dalam keadaan segar, tetapi dapat mewarnai mulut dan jari. Selain
dikonsumsi segar, buah buni biasanya hanya dikonsumsi sebagai rujak
(Lembaga Biologi Nasional 1977). Penanganan pasca panen yang kurang baik
dapat menyebabkan kehilangan hasil dalam jumlah yang cukup besar. Praktek
pemanenan dan penanganan pasca panen yang baik sangat diperlukan untuk
menanggulangi masalah tersebut. Salah satu cara yang dapat dilakukan untuk
memanfaatkan hasil panen sekaligus untuk mencegah terjadinya kehilangan
hasil ialah dengan cara mengelola buah buni menjadi sebuah produk yang
bermutu dan bernilai ekonomis (Muchtadi 2000).
Menurut Gruèzo (1997), dalam satu tandan kematangan buah buni tidak
bersamaan, maka dalam penelitian ini buah buni dimanfaatkan menjadi suatu
produk olahan baru, yaitu pembuatan minuman serbuk buah buni berdasarkan
tingkat kematangan buah buni. Pembuatan minuman serbuk buah buni ini
diharapkan dapat meningkatkan manfaat buah buni dan menambah keragaman
produk pangan. Disamping itu, pemanfaatan buah buni sebagai minuman serbuk
dapat memberikan pilihan alternatif produk kaya antioksidan bagi penderita
penyakit tertentu.
Tujuan Tujuan Umum
Secara umum penelitian ini bertujuan untuk mengembangkan minuman
fungsional dari buah buni dalam bentuk minuman serbuk yang mengandung
antioksidan alami.
Tujuan Khusus
Secara khusus, tujuan penelitian ini adalah sebagai berikut:
1. Mengetahui tingkat ekstraksi paling efisien dalam penyiapan minuman
serbuk buah buni.
2. Mengetahui perbandingan buah buni dan bahan pengisi agar
menghasilkan tepung buah buni serta perbandingan tepung buah buni
dan bahan pengisi agar tepung dapat larut sempurna ketika dicampurkan
3. Mengevaluasi sifat organoleptik (deskripsi dan tingkat kesukaan)
minuman serbuk buah buni serta mengetahui daya terima minuman
serbuk buah buni.
4. Mengetahui pengaruh tingkat kematangan buah buni terhadap aktivitas
antioksidan pada minuman serbuk buah buni.
5. Menganalisis sifat fisikokimia (warna, kelarutan, densitas kamba, kadar
air, total padatan terlarut, total asam tertitrasi, pH, vitamin C, total
antosianin, dan aktivitas antioksidan) minuman serbuk buah buni.
Manfaat
Penelitian ini diharapkan dapat memberikan nilai tambah bagi buah buni
yang belum dimanfaatkan secara optimal, sehingga dapat menjadi bahan pangan
yang lebih bermutu dan bernilai ekonomis. Selain itu, penelitian ini diharapkan
dapat menghasilkan suatu produk olahan buah buni yang dapat diterima
masyarakat dan menjadi alternatif produk kaya antioksidan bagi penderita
TINJAUAN PUSTAKA
Buah Buni
Buni dalam bahasa ilmiah diberi nama Antidesma bunius (L.) Spreng. Tanaman ini berupa pohon yang tingginya dapat mencapai 15-30 m, garis tengah
batang sekitar 20-25 cm, bercabang banyak dan rindang. Bunga jantan dan
betina buah buni masing-masing terletak pada pohon yang berlainan, tersusun
dalam bentuk malai. Ukuran bunga betina lebih besar daripada bunga jantan.
Warna buah buni mula-mula hijau terang, setelah dewasa menjadi merah. Buah
buni tersusun dalam tandan, berbentuk bulat atau bulat telur, bergaris tengah
sekitar 3 cm (Lembaga Biologi Nasional 1977). Menurut Heyne (1987), buah buni
sedikit lebih besar dari kacang kapri, mula-mula berwarna merah sangat asam,
kemudian kehitam-hitaman dan berair dengan rasa manis keasam-asaman.
Gambar 1 Buah buni
Antidesma bunius tumbuh liar di wilayah yang lebih basah di India, dari Himalaya ke selatan dan timur, di Sri Lanka, Myanmar, dan Malaysia. Buni ini
mungkin tidak berasal dari Filipina dan Malaysia, tetapi jika demikian halnya,
tanaman ini telah diintroduksi pada masa prasejarah, dan telah bernaturalisasi
secara luas, sekurang-kurangnya di Filipina. Buni dibudidayakan secara
besar-besaran di Indo-Cina dan di berbagai daerah di Indonesia, terutama di Jawa. Di
Malaysia dan Filipina, buni jarang dibudidayakan (Gruèzo 1997). Di daerah tropik
pohon buni dapat tumbuh pada ketinggian 0-1000 m dpl. Di Indonesia buni
ditanam di propinsi-propinsi bagian timur yang beriklim muson, serta di bagian
barat yang berhawa lembab, dengan demikian buni selain toleran terhadap
kekeringan juga dapat hidup di daerah lembab (Yulistyarini dkk 2000 dan Tohir
Buah buni yang matang dapat dimakan dalam keadaan segar, tetapi
dapat mewarnai mulut dan jari. Selain itu, sari buah dari buah yang matang pun
berguna sebagai minuman penyegar dan menghasilkan anggur yang istimewa.
Buah buni yang mentah memiliki rasa agak asam, buah-buah dalam satu tandan
tidak bersamaan matangnya, maka buah buni seringkali digunakan untuk
pembuatan selai dan jeli (Gruèzo 1997). Buah buni sering digunakan oleh orang
Indonesia untuk rujak dan dibuat saus-asem ikan (Lembaga Biologi Nasional
1977 dan Gruèzo 1997). Kadang-kadang buah buni dapat pula dipakai sebagai
campuran dalam minuman buah-buahan. Daun muda buah buni dapat berguna
untuk memberi aroma pada ikan atau daging rebus (stew), lalap dan dimasak dengan nasi. Buah muda dan daun muda buah buni dapat digunakan sebagai
pengganti cuka (Gruèzo 1997).
Kulit dan daun mengandung alkaloid yang memiliki khasiat obat, tetapi
dilaporkan juga beracun. Kayu buah buni berwarna kemerah-merahan dan keras
yang kurang bermanfaat namun memiliki mutu yang cukup baik. Di Malaysia
jenis dari marga yang sama dipakai sebagai pohon untuk penghutanan kembali
tanah-tanah gundul. Jenis tersebut menyukai tempat yang terbuka dan dapat
tumbuh berkompetisi dengan alang-alang (Lembaga Biologi Nasional 1977).
Klasifikasi buah buni adalah sebagai berikut:
Kerajaan :Plantae
Divisi :Magnoliophyta
Kelas :Magnoliopsida
Ordo :Malpighiales
Famili :Phyllanthaceae
Bangsa :Antidesmeae
Upabangsa :Antidesminae
Genus :Antidesma
Spesies : A. bunius
Menurut Gruèzo (1997), kandungan bagian buah yang dapat dimakan
merupakan 65-80% dari keseluruhan buah. Asam sitrat merupakan asam organik
yang paling menonjol dalam buah buni. Kandungan gizi untuk setiap 100 g buah
Tabel 1 Kandungan gizi pada 100 gram buah buni
Kandungan gizi Jumlah
Energi (kJ) 134
Air (g) 90-95
Karbohidrat (g) 6,3
Protein (g) 0,7
Lemak (g) 0,8
Kalsium (mg) 3,7-120
Fosfor (mg) 22-40
Besi (mg) 0,1-0,7
Vitamin A (IU) 10
Vitamin C (mg) 8
Sumber: Gruèzo 1997
Penanganan pasca panen buah yang tidak dilakukan secara hati-hati
akan mengakibatkan terjadinya perubahan fisiologis, fisik, kimiawi, parasitik atau
mikrobiologis yang menyebabkan bahan pangan tersebut tidak dapat
dimanfaatkan lagi. Cara penanganan pasca panen yang dapat dilakukan adalah
dengan cara mengelola buah menjadi suatu olahan pangan. Variasi pengolahan
buah buni pada masyarakat Indonesia masih rendah yatu hanya dikonsumsi
segar atau dikonsumsi sebagai rujak (Muchtadi 2000 dan Lembaga Biologi
Nasional 1977). Pengolahan buah buni menjadi berbagai olahan diharapkan
dapat meningkatkan pemanfaatan buah lokal, mengurangi kehilangan hasil
pertanian dan memperpanjang masa simpan (Muchtadi 2000).
Antioksidan
Antioksidan adalah komponen yang dapat mencegah atau menghambat
oksidasi lemak, asam nukleat, atau molekul lainnya dengan mencegah inisiasi
atau perkembangan dari pengoksidasian reaksi berantai. Sayuran dan
buah-buahan merupakan bahan pangan yang kaya akan antioksidan. Beberapa studi
menyebutkan bahwa dengan mengkonsumsi sayuran dan buah-buahan segar
dapat menurunkan terkena kanker dan berbagai penyakit degeneratif lainnya
(Wang 2007). Menurut Halliwell (1996), senyawa radikal yang terdapat dalam
tubuh berasal dari luar tubuh (eksogen) maupun dari dalam tubuh (endogen)
yang terbentuk dari hasil metabolisme zat gizi secara normal. Dalam proses
fisiologis timbulnya senyawa radikal tubuh (pro-oksidan) akan diimbangi oleh
mekanisme pertahanan endogen dengan menggunakan zat (senyawa) yang
mempunyai kemampuan sebagai anti radikal bebas, yang juga disebut
Senyawa ROS (Reactive Oxygen Species) memberikan efek merusak bila keseimbangan antara oksidan dan antioksidan terganggu. Keseimbangan ini
tergantung pada konsumsi pangan yang membawa asam-asam amino esensial
dalam jumlah yang diperlukan untuk mensintesa protein serta zat gizi lain yang
diperlukan. Walaupun secara teoritis senyawa radikal di dalam tubuh dapat
dihilangkan bila terdapat antioksidan, tetapi efisiensi penghilangan senyawa
radikal ini tidak pernah mencapai 100% (Parke 1999).
Menurut Halliwell (1996), reaksi-reaksi yang melibatkan senyawa radikal
telah diketahui merupakan asal dari berbagai macam penyakit, antara lain ginjal,
diabetes, kanker, dan penyakit kardiovaskular. Pada individu yang sehat,
keberadan pro-oksidan dapat diimbangi dengan adanya antioksidan. Akan tetapi
pada keadaan tertentu keseimbangan tersebut dapat terganggu, dimana jumlah
pro-oksidan lebih banyak dibandingkan oksidan. Oleh karena itu, penting sekali
untuk meningkatkan kadar antioksidan di dalam tubuh, dan hal ini dapat
dilakukan dengan meningkatkan konsumsi antioksidan alami.
Antioksidan alami yang terdapat dalam bahan pangan dapat
dikategorikan menjadi dua golongan, yaitu (1) yang tergolong sebagai zat gizi,
yaitu vitamin A dan karetenoid, vitamin E, vitamin C, vitamin B2, seng (Zn),
tembaga (Cu), selenium (Se), dan protein; (2) yang tergolong sebagai zat
non-gizi, yaitu biogenik amin, senyawa fenol, antosianin, zat sulforaphane, senyawa
polifenol dan tannin (Muchtadi 2001).
Antosianin
Antosianin tergolong pigmen yang disebut flavonoid yang pada umumnya
larut dalam air (Winarno 1997). Menurut Aman dan Winarno (1981), warna-warna
merah, biru, ungu dalam buah dan tanaman biasanya disebabkan oleh warna
pigmen antosianin (flavanoid) yang terdiri dari tiga gugusan penting:
a) cincin dasar yang terdiri dari gugusan aglikon (tanpa gula)
b) gugusan Aglikon atau gula
c) asam organik asil misalnya koumarat, kofeat atau ferulat
Menurut Markakis (1982), molekul antosianin disusun dari sebuah aglikon
(antosianidin) yang teresterifikasi dengan satu atau lebih gula (glikon). Menurut
Timberlake dan Bridle (1983), gula yang menyusun antosianin terdiri dari:
Disakarida yang merupakan dua buah monosakarida dengan kombinasi
dari empat monosakarida di atas dan xilosa, seperti rutinosa.
Trisakarida, merupakan tiga buah monosakarida yang mengandung
kombinasi dari gula-gula di atas dalam posisi linier maupun rantai cabang.
Gula yang paling banyak dijumpai adalah monosakarida seperti glukosa,
galaktosa, ramnosa, dan arabinosa. Di dan tri sakarida juga dibentuk dari
kombinasi monosarida di atas. Dalam tanaman, antosianin dalam bentuk
glikosida yaitu ester dengan satu molekul monosakarida disebut monoglukosida
dan biosida atau diglukosida jika memiliki dua molekul gula (Winarno 1997).
Aman dan Winarno (1981) mengungkapkan bahwa dalam sel, antosianin terletak
di dalam vakuola. Oleh karena itu, adanya gugusan gula ini dapat mempengaruhi
stabilitas antosianin. Bila gugusan gula lepas, antosianin menjadi labil. Menurut
Winarno (1997), sewaktu pemanasan dalam asam mineral pekat, antosianin
pecah menjadi antosianidin dan gula. Berbagai jenis struktur antosianin adalah
sebagai berikut:
Menurut Astawan dan Kasih (2008), antosianin diyakini mempunyai efek
antioksidan yang sangat baik. Sebuah penelitian yang dilakukan di Universitas
Michigan Amerika Serikat menunjukkan bahwa antosianin dapat menghancurkan
radikal bebas, lebih efektif daripada vitamin E yang selama ini telah dikenal
sebagai antioksidan kuat. Sebuah penelitian di Amerika Serikat membuktikan
bahwa antosianin merupakan antioksidan yang paling kuat di antara kelas
flavonoid lainnya. USDA Human Nutrition Center menyatakan bahwa blueberry
yang kaya akan antosianin memiliki efek antioksidan yang paling baik di antara
40 jenis tanaman dan buah-buahan yang telah diuji. Kandungan antosianin
diyakini dapat menghambat berbagai radikal bebas seperti radikal superoksida
dan hidrogen peroksida. Antosianin dan berbagai bentuk turunannya dapat
menghambat berbagai reaksi oksidasi dengan berbagai mekanisme. Antosianin
kubis merah dapat menghambat oksidasi yang dihasilkan oleh toksin.
Banyak faktor yang mempengaruhi kekuatan antioksidan pada
buah-buahan berwarna ungu, antara lain adalah tingkat kematangan buah. Pada buah
yang hijau hanya terdiri dari malvidin-3-acetylglucoside dan pigmen polymeric
sedangkan pada buah yang masak terdiri dari cyaniding-3-rutinoside (>75%),
cyanidin-3-glucoside (<17%), dan malvidin-3-acetylglucoside (<9%) (Rivera,
Ordorica, dan Wesche 1998; Goncalves et al 2006). Selama proses pematangan buah banyak terjadi perubahan kimia, termasuk perubahan komposisi pigmen
dan perubahan warna yang melibatkan proses biosintesis dan katabolisme.
Selama proses pematangan ini, kloroplas secara berangsur-angsur akan
digantikan oleh kromoplas yang hanya mengandung karotenoid. Proses
pematangan pada berbagai buah ini juga melibatkan biosintesis antosianin yang
larut dalam air yang terakumulasi dalam vakuola sentral dalam sel mesofil.
Proses sintesis dari anatosianin ini diawali oleh malonil-CoA yang berasal dari 3
asetil-CoA dan p-koumaroil-CoA fenilalanin (MacDougall 2002). Kulkarni dan
Aradhya (2004) menyatakan bahwa ketika tingkat kematangan semakin tinggi
maka aktivitas antioksidannya semakin tinggi. Hal ini disebabkan karena
antosianin yang meningkat pada buah yang semakin matang.
Faktor yang juga mempengaruhi stabilitas antosianin adalah struktur
antosianin dan komponen-komponen lain yang terdapat pada bahan pangan
tersebut. Antosianin dapat membentuk kompleks dengan komponen polifenolik
lainnya. Komponen flavonol dan flavon yang biasanya selalu berkonjugasi
(Monagas, Gomes dan Bartolome 2006). Faktor yang juga mempengaruhi
antosianin adalah suhu. Proses pemanasan merupakan faktor terbesar yang
menyebabkan kerusakan antosianin. Proses pemanasan terbaik untuk
mencegah kerusakan antosianin adalah pengolahan pada suhu tinggi, tetapi
dalam jangka waktu yang sangat pendek (High Temperature Short Term (HTST)). Cabrita dan Andersen (1999) menyatakan bahwa peningkatan suhu penyimpanan dari 10oC menjadi 23oC, masing-masing selama 60 hari, akan
menyebabkan peningkatan kerusakan antosianin dari 30 persen menjadi 60
persen. Sebaliknya, stabilitas antosianin dapat meningkat sebanyak 6-9 kali
ketika suhu penyimpanan diturunkan dari 20oC menjadi 4oC. Antosianin yang
disimpan di dalam ruang vakum akan lebih stabil dibandingkan dengan
antosianin yang disimpan di ruang terbuka. Asam askorbat atau vitamin C dalam
konsentrasi tinggi juga dapat menyebabkan rusaknya komponen antosianin (De
Rosso & Mercadante 2006).
Faktor pH mempengaruhi kestabilan warna antosianin. Pada pH rendah
(asam) pigmen ini berwarna merah dan pada pH tinggi berubah menjadi violet
dan kemudian biru (Winarno 1992). Menurut Markakis (1982), antosianin lebih
stabil dalam larutan asam dibanding dalam larutan akali atau netral. Pada larutan
asam, antosianin bersifat stabil, pada larutan asam kuat antosianin sangat stabil.
Daravingas dan Cain (1968) mengemukakan bahwa penurunan pH secara nyata
akan memperlambat laju kerusakan antosianin yang berasal dari raspberry.
Sistrunk dan Cash (1968) berusaha meningkatkan kestabilan antosianin dari sari
buah arbei dengan metode penurunan pH, selanjutnya ia mengatakan bahwa
metode penurunan pH merupakan metode terbaik untuk mempertahankan
stabilitas warna dari antosianin. Harper (1968) berpendapat bahwa pada kisaran
pH 1-3, pigmen antosianin berada dalam bentuk oxonium (I) yang berwarna
merah dan merupakan bentuk yang paling stabil. Bentuk tersebut dapat
mengalami hidrolisis pada pH yang lebih tinggi membentuk pseudobasa (II) yang
mulai kehilangan warna. Pseudobasa (II) yang terbentuk ini dapat mengalami
kesetimbangan tautomerik. Kesetimbangan antara bentuk keto dan bentuk enol
menghasilkan alfa diketon (IV) yang menghasilkan warna biru.
Menurut Astawan dan Kasih (2008), suatu komponen kimia akan bersifat
lebih stabil bila dapat bereaksi dengan dirinya sendiri. Pada konsentrasi tinggi,
antosianin dapat bereaksi dengan dirinya sendiri. Itulah sebabnya buah-buahan
yang memiliki antosianin rendah. Aman dan Winarno (1981) mengungkapkan
bahwa adanya pigmen lain sering menutupi warna yang disebabkan oleh pigmen
antosianin. Antosianin atau pigmen lain juga terdapat di daun yang berwarna
hijau dengan konsentrasi yang relatif rendah.
Pigmen antosianin ini telah lama dikonsumsi oleh manusia dan hewan
bersamaan dengan buah atau sayur yang mereka makan. Selama ini tidak
pernah terjadi suatu penyakit ataupun keracunan yang disebabkan oleh pigmen
ini (Brouillard 1982). Menurut penelitian yang banyak dilakukan, pigmen
antosianin dan senyawa-senyawa flavonoid lainnya terbukti memiliki efek positif
terhadap kesehatan (Bridle dan Timberlake 1997). Banyak bukti yang
menunjukkan bahwa antosianin buka saja tidak beracun (non-toxic) dan tidak menimbulkan efek mutagenik, tetapi juga memiliki sifat yang positif seperti
mencegah penyakit kanker dan kardiovaskuler (Saija 1994). Antosianin memiliki
warna yang kuat , larut dalam air, relatif stabil dalam air pada pH asam dan
adanya pembatasan penggunaan bahan pewarna merah sintetik, maka
antosianin cocok dijadikan sebagai subsitusi pewarna makanan sintesis
(Markakis 1982).
Pembuatan Minuman Serbuk Buah Buni
Sebelum pembuatan minuman serbuk buah buni, hal yang dilakukan
pertama adalah ekstraksi buah buni. Ekstraksi adalah proses penarikan
komponen/zat aktif suatu sampel dengan menggunakan pelarut tertentu.
Pemilihan metode ekstraksi senyawa ditentukan oleh beberapa faktor, yaitu sifat
jaringan tanaman, sifat kandungan zat aktif serta kelarutan dalam pelarut yang
digunakan. Prinsip ekstraksi adalah melarutkan senyawa polar dalam pelarut
polar dan senyawa non polar dalam pelarut non polar (Harbone 1987). Cook &
Cullen (1986) mengungkapkan bahwa ada dua tipe ekstraksi pelarut yaitu
ekstraksi padat-cair dan cair-cair. Tipe pertama sering juga disebut dengan
pencucian (leaching) yaitu proses pemisahan bahan dari campuran zat padat dengan cara mengaduknya dalam suatu cairan (pelarut) di mana bahan yang
diinginkan untuk dipisahkan akan terlarut. Proses ekstraksi cair-cair pada
prinsipnya sama, namun dalam hal ini larutan yang mengandung bahan terlarut
dicampurkan dan dikocok benar-benar dengan cairan (pelarut) yang lain.
Jika kedua cairan bersifat tidak dapat bercampur maka akan terbentuk
campuran. Cairan dengan bahan-bahan terlarut di dalamnya dinyatakan dengan
lapisan jenuh (ekstrak) dan lapisan yang bersisa dinyatakan dengan rafinat.
Dalam beberapa hal digunakan pelarut air, keadaan ini dikenal dengan ekstraksi
akua (aquaeous extraction). Pelarut-pelarut yang umum digunakan bersama-sama dengan air ialah kloroform, karbon tetraklorida, etilen diklorida, benzene,
toluene, xilena, dan petroleum eter (Cook & Cullen 1986).
Menurut Strack dan Wray (1993), penambahan asam sebagai pelarut
tidak selau diperlukan. Metode ekstraksi yang digunakan untuk analisis kuantitatif
harus diperiksa secara menyeluruh pada tanaman dan jenis pigmen tertentu. Jika
terdapat gugus asil pada antosianin misalnya di dalam kubis ungu, maka
penggunaan asam sebagai campuran pelarut harus dihindarkan. Hal ini
disebabkan ikatan asil ini mudah terhidrolisis (Markakis 1982).
Ekstraksi bertahap ganda (multi-stage extraction) digunakan untuk memperoleh efisiensi yang lebih tinggi, di mana produk yang dihasilkan hampir
seluruhnya dapat dipisahkan dari rafinatnya. Pelarut yang terbagi dalam
beberapa bagian diisikan ke serangkaian alat pencampur (mixer) dan alat pengendap (setter). Kekurangan penggunaan metode ini ialah terlalu besarnya jumlah pelarut yang dibutuhkan (Cook & Cullen 1986).
Hasil ekstrak yang telah terkumpul kemudian dijadikan tepung buah buni.
Pengeringan adalah suatu usaha menurunkan jumlah kandungan air dari suatu
bahan. Pengeringan bahan makanan seperti sayur-sayuran dan buah-buahan
dapat dilakukan dengan cara penjemuran, dehidrasi dengan alat pengering, “freeze drying” dan dehidrasi parsial secara osmosis dalam larutan gula atau garam. Tujuan utama pengeringan bahan makanan adalah untuk
memperpanjang daya tahan simpannya, yaitu dengan mengurangi aω-nya sehingga mikroorganisme tidak tumbuh (Muchtadi 1989).
Keuntungan dari pengeringan adalah bahan menjadi lebih awet dengan
volume dan berat bahan menjadi lebih kecil sehingga mempermudah dan
menghemat ruang pengangkutan dan pengepakan, dengan demikian diharapkan
biaya produksi menjadi lebih mudah. Pengeringan juga mempunyai beberapa
kerugian, yaitu karena sifat asal dari bahan yang dikeringkan dapat berubah
misalnya bentuknya, sifat-sifat fisik dan kimianya, penurunan mutu dan
lain-lainnya. Kerugian yang lainnya juga disebabkan karena beberapa bahan kering
perlu pekerjaan tambahan sebelum digunakan, misalnya harus dibasahkan
Makanan yang dikeringkan mempunyai nilai gizi yang lebih rendah
dibandingkan dengan bahan segarnya. Selama pengeringan juga dapat terjadi
perubahan warna, tekstur, aroma, dan lain-lainnya, meskipun
perubahan-perubahan tersebut dapat dibatasi seminimal mungkin dengan jalan memberikan
perlakuan pendahuluan terhadap bahan pangan yang akan dikeringkan. Dengan
mengurangi kadar airnya, bahan pangan akan mengandung senyawa-senyawa
seperti protein, karbohidrat, lemak dan mineral dalam konsentrasi yang lebih
tinggi, akan tetapi vitamin-vitamin dan zat warna pada umumnya menjadi rusak
atau berkurang (Winarno et al 1980).
Alat pengering yang digunakan dalam pembuatan tepung buah buni
adalah pengering vakum (vacuum dryer). Pengering vakum dipergunakan untuk mengeringkan bahan-bahan yan sensitif terhadap perubahan suhu tinggi seperti
sari buah serta larutan pekat lainnya. Pengeringan dengan pengering vakum
terjadi pada suhu rendah dan berlangsung dengan cepat. Peningkatan suhu
terjadi dengan cara menginjeksikan udara panas ke dalam ruang pengering
melalui lubang-lubang yang menghubungkan daerah kontak panas pada rak.
Sementara bahan ditebar tipis di atas rak-rak (yang terletak di atas pemukaan
yang berlubang). Uap air dari produk yang terbentuk dihisap dengan ejektor yang
dibangkitkan dengan tenaga uap (Suharto 1991). Pada pengering ini, titik didih
air turun di bawah 100oC karena tekanannya di bawah tekanan atmosfer. Produk
hasil pengeringan bersifat higroskopis. Selain bahan di atas, pengering vakum
juga biasa digunakan untuk ekstraksi dan pemekatan essens dan flavor
(Sokhansanj dan Jayas 1995).
Adapun bahan pengisi yang digunakan dalam pembuatan tepung buah
buni adalah maltodekstrin. Maltodekstrin ialah senyawa turunan pati hasil hidrolisis pati melalui proses hidrolisis parsial oleh enzim α-amilase (Kennedy et al. 1995). Maltodekstrin dapat diproduksi secara hidrolisis asam atau enzimatik (Kearsley dan Dziedzic 1995). Maltodektrin terdiri dari unit-unit α-D-glukosida dengan panjang 5-10 unit yang saling berikatan dengan ikatan α-1,4 dengan DE (dextrose equivalent) kurang dari 20 (Kennedy et al. 1995). Menurut McDonald (1984), maltodekstrin memiliki sifat kurang higroskopis, kurang manis, memiliki
tingkat kelarutan tinggi dan cenderung tidak membentuk warna pada reaksi
browning. Maltodekstrin banyak digunakan dalam industri pangan sebagai bahan pengisi dan bahan campuran untuk produk berbasis tepung-tepungan (Schenk
BAHAN DAN METODE
Tempat dan Waktu Penelitian
Penelitian ini berlangsung pada bulan Juli sampai Desember 2010.
Penelitian ini dilaksanakan di Laboratorium Kimia Gizi, Laboratorium
Organoleptik, dan Laboratorium Analisis Pangan Program Studi Ilmu Gizi,
Fakultas Ekologi Manusia, Laboratorium Pilot Plant Southeast Asian Food and Agriculture Science Technology (SEAFAST) Center, Institut Pertanian Bogor (IPB).
Bahan dan Alat
Bahan-bahan yang digunakan dalam penelitian ini adalah buah buni yang
berasal dari daerah sekitar Bogor. Buah buni yang digunakan adalah buah
dengan tiga tingkat kematangan berdasarkan perbedaan warna yaitu, kuning
(kematangan matang tidak masak), merah (kematangan agak masak), dan
ungu/hitam (kematangan masak penuh). Bahan lain yang digunakan ialah
maltodekstrin, asam sitrat, tepung gula, garam, sukralosa dan grape flavor. Bahan-bahan kimia digunakan untuk analisis antioksidan seperti radikal bebas
DPPH diperoleh dari Sigma Co., Amerika Serikat.
Peralatan yang digunakan meliputi peralatan untuk membuat tepung buah
buni dan peralatan untuk keperluan analisa. Peralatan yang digunakan untuk
pembuatan tepung buah buni adalah pengering vakum evaporator (vacuum evaporator dryer) yang disewa dari Laboratorium Pilot Plant SEAFAST Center. Peralatan untuk keperluan analisis seperti spektrofotometer, alat inkubasi, neraca
analitik, buret, oven, dan alat analisis lain diperoleh dari Laboratorium Kimia dan
Analisis Pangan Departemen Gizi Masyarakat, Institut Pertanian Bogor (IPB).
Metode Penelitian
Penelitian ini dilakukan melalui beberapa tahapan yaitu:.
A. Penentuan Tingkat Ekstraksi
Penelitian awal dalam proses pembuatan minuman serbuk buah buni
adalah mengetahui tingkatan ekstraksi optimum pada setiap kematangan hingga
fitrat sampel menunjukkan warna putih. Ada 3 macam kematangan yang diteliti
yaitu kematangan yang dilihat berdasarkan tiga warna buah yang berbeda pada
satu tandan buah buni yang telah dipetik. Tiga macam tingkat kematangan
tersebut adalah kematangan matang tidak masak, kematangan agak masak, dan
dengan perbandingan 1:5. Gambaran proses tingkatan ekstraksi pada setiap
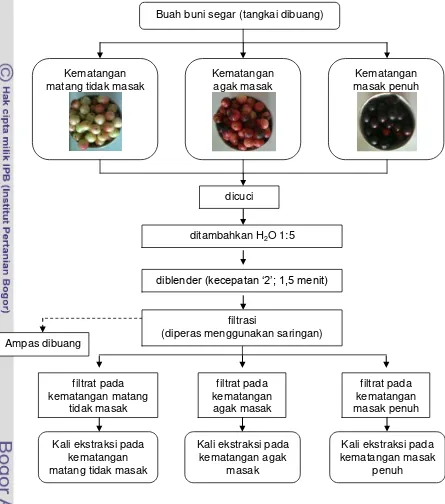
kematangan buah buni dapat dilihat pada Gambar 2.
Buah buni segar (tangkai dibuang)
Kematangan matang tidak masak
Kematangan agak masak
Kematangan masak penuh
Gambar 3 Skema ekstraksi pada beberapa kematangan buah filtrat pada
kematangan matang tidak masak
filtrat pada kematangan agak masak
filtrat pada kematangan masak penuh
Kali ekstraksi pada kematangan matang tidak masak
Kali ekstraksi pada kematangan agak
masak
Kali ekstraksi pada kematangan masak
penuh Ampas dibuang
ditambahkan H2O 1:5
diblender (kecepatan „2‟; 1,5 menit)
filtrasi
B. Pembuatan Tepung Buah Buni
Selain itu, penelitian awal juga bertujuan untuk mengetahui perbandingan
buah buni dan bahan pengisi agar menghasilkan tepung buah buni dan
perbandingan tepung buah buni dan bahan pengisi agar tepung dapat larut
sempurna ketika dicampurkan dengan pelarut (air) serta rendemen tepung buah
buni. Jenis bahan pengisi yang digunakan adalah maltodekstrin (ditentukan
berdasarkan studi referensi dan penelitian yang pernah dilakukan). Alat yang
digunakan dalam pembuatan tepung buah buni adalah vakum evaporator
(vacuum evaporator drier). Gambaran proses pembuatan tepung dengan penambahan maltodekstrin dapat dilihat pada Gambar 3.
Hasil ekstraksi pada setiap kematangan
disaring dengan menggunakan kertas hole
ditambahkan maltodekstrin
10% 20% 30%
Tepung buah buni I pada berbagai tingkat kematangan
ditambahkan maltodekstrin
1 : ½ 1 : 1 1 : 1 ½ 1 : 2
Tepung buah buni II pada berbagai tingkat kematangan
Gambar 4 Skema pembuatan tepung buah buni dikeringkan dengan menggunakan
Adapun perhitungan rendemen tepung buah buni (Apriyantono et al 1989) adalah sebagai berikut:
Rendemen (%) = Produk (g) x 100
Bahan (g)
C. Pembuatan Minuman Serbuk Buah Buni
Setelah tepung buah buni didapat, langkah selanjutnya adalah
mengaplikasikan tepung tersebut dalam pembuatan minuman serbuk. Metode
yang digunakan dalam pembuatan minuman serbuk buah buni adalah metode
langsung dengan tahapan yaitu: penimbangan bahan lalu pencampuran.
Pembuatan minuman serbuk buah buni meliputi formulasi, organoleptik, analisis
daya terima, dan analisis karakteristik fisik dan kimia minuman serbuk buah buni.
Gambaran pembuatan minuman serbuk dapat dilihat pada Gambar 5.
Gambar 5 Skema pembuatan minuman serbuk buah buni Tepung buah buni II
Formulasi minuman serbuk (ditambahkan pemanis (gula & sukralosa), asam sitrat,
garam dan grape flavor)
Uji Karakteristik Fisik (Kelarutan, Kadar air, Densitas kamba dan Warna)
Uji Karakteristik Kimia (Vitamin C, Total Padatan Terlarut, Total Asam, pH, Total Antosianin, dan Aktivitas Antioksidan) Formulasi Terpilih Minuman Serbuk Buah
Buni pada Setiap Kematangan dicampur dan dikocok dalam kantong plastik
Minuman Serbuk Buah Buni pada @ kematangan buah buni
Formulasi pada minuman serbuk buah buni adalah 27 formulasi
berdasarkan perbedaan tingkat kematangan, tingkat kemanisan dan
penambahan asam sitrat. Bahan yang digunakan pada pembuatan minuman
serbuk buah buni adalah tepung buah buni, tepung gula, sukralosa, garam, asam
sitrat, dan grape flavor. Tingkat kemanisan yang digunakan yaitu 10%, 15%, dan 20% dimana masing-masing tingkat kemanisan yang digunakan berasal dari 10%
tepung gula dan 90% sukralosa. Taraf asam sitrat yang digunakan yaitu 0.1%,
0.2%, dan 0.3%. Grape flavor ditambahkan untuk meningkatkan cita rasa minuman serbuk tersebut. Berikut formulasi minuman serbuk buah buni pada
setiap kematangan:
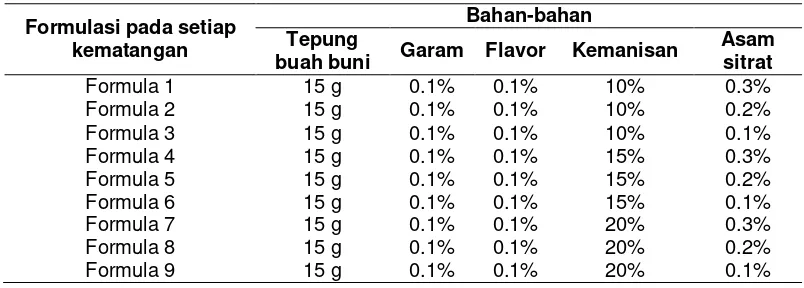
Tabel 2 Formulasi minuman serbuk buah buni pada setiap kematangan
Formulasi pada setiap kematangan
Bahan-bahan Tepung
buah buni Garam Flavor Kemanisan
Asam
D. Analisis Organoleptik dan Fisikokimia Minuman Serbuk Buah Buni
1. Uji Organoleptik (Meilgaard 1999)
Uji organoleptik dilakukan terhadap minuman serbuk buah buni. Metode
yang digunakan adalah uji kesukaan (hedonik) dan uji mutu hedonik dengan
menggunakan skala garis. Sampel disajikan pada 30 panelis secara acak
dengan kode tiga angka acak. Setiap panelis memberikan penilaian dengan
memberikan garis vertikal pada garis horizontal sepanjang 9 cm yang terdapat
pada kuisioner yang menunjukkan penilaian amat sangat tidak suka (1 cm)
sampai amat sangat suka (9 cm). Penilaian dilakukan terhadap warna, rasa,
aroma dan kesukaan secara keseluruhan minuman serbuk buah buni. Data hasil
uji analisis secara statistik dengan uji ANOVA dan uji lanjut Duncan. Kuisioner uji
2. Analisis Karakteristik Fisikokimia Minuman Serbuk Buah Buni
Karakteristik fisik buah buni yang diamati adalah warna, kelarutan,
densitas kamba, total padatan terlarut, total asam, pH, aktivitas antioksidan, total
antosianin, dan vitamin C.
2.1 Warna, metode Hunter (Huntching 1999)
Pengukuran warna minuman serbuk buah buni secara langsung
dilakukan menggunakan alat Chromameter Minolta CR-310. Pembuatan larutan minuman serbuk buah buni dilakukan dengan cara melarutkan
formulasi serbuk buah buni dalam 200 ml air, diambil 20 ml dan selanjutnya
pengukuran nilai L, a, b, C dan oHue. Notasi L menyatakan parameter
kecerahan (light) yang mempunyai nilai nol (hitam) sampai 100 (putih). Nilai C menunjukkan ketajaman warna sampel. Nilai a menyatakan
cahaya pantul yang menghasilkan warna kromatik campuran merah-hijau
dengan nilai +a (positif a) dari nol sampai 100 untuk warna merah dan nilai –a (negatif a) dari nol sampai 80 untuk warna hijau. Notasi b menyatakan warna
kromatik campuran biru-kuning dengan nilai +b (positif b) dari nol sampai 70
untuk warna kuning dan nilai –b (negatif b) dari nol sampai -70 untuk warna biru. Penentuan warna dilakukan berdasarkan ketentuan di bawah ini:
Red Purple (RP) jika oHue = 342o - 18o
Red (R) jika oHue = 18o - 54o
Yellow Red (YR) jika oHue = 54o - 90o
Yellow (Y) jika oHue = 90o - 126o
Yellow Green (YG) jika oHue = 126o - 162o
Green (G) jika oHue = 162o - 198o
Blue Green (BG) jika oHue = 198o - 234o
Blue (B) jika oHue = 234o - 270o
Blue Purple (BP) jika oHue = 270o - 306o
Purple (P) jika oHue = 306o - 342o
2.2 Kelarutan Dalam Air (Gravimetri) (AOAC 1995)
Sampel sebanyak 1 gram dilarutkan dalam 20 ml air kemudian
disaring dengan kertas Whatman no 42 yang telah terlebih dahulu
dikeringkan dan bobotnya ditimbang. Setelah itu, kertas saring dikeringkan
Kelarutan dalam air = A – B x 100% C
Keterangan:
A : bobot kertas saring yang telah dikeringkan (gram)
B : bobot kertas saring kering awal (gram)
C : bobot sampel kering (gram)
2.3 Densitas Kamba (Muchtadi dan Sugiyono 1992)
Densitas kamba diukur dengan cara menimbang contoh yang telah
dimasukkan ke dalam gelas ukur yang volume telah diketahui secara pasti.
Sampel dimasukkan ke dalam gelas ukur kemudian diketuk-ketuk sampai
tidak terdapat rongga dan ditimbang. Densitas kamba dihitung dengan rumus
sebagai berikut:
Densitas Kamba = Berat contoh (gram)
Volume contoh (ml)
2.4 Kadar Air (AOAC 1995)
Cawan alumunium dikeringkan dalam oven bersuhu 100oC selama 15
menit, dinginkan dalm desikator selama 10 menit kemudian timbang (W1).
Sebanyak 5 gram contoh ditimbang dalam cawan tersebut (W2). Cawan berisi
sampel dipanaskan dalam oven vakum (T=70oC, 25 mmHg) selama 5 jam
atau hingga tercapai berat yang tetap. Selanjutnya didinginkan dalam
desikator selama 15 menit,kemudian ditimbang (W3).
Kadar air (%) = 100-(( W2- W3)/( W2- W1)x 100%)
2.5 Total Padatan Terlarut (AOAC 1995)
Total padatan terlarut diukur dengan alat Refraktometer Abbe. Setetes sampel diletakkan pada prisma refraktometer yang sudah distabilkan
pada suhu tertentu, lalu dilakukan pembacaan. Total padatan terlarut
dinyatakan dalam oBrix. Sebelum dan sesudah digunakan prisma
refraktometer dibersihkan dengan menggunakan alkohol. Untuk produk-produk serbuk dilakukan pengenceran dengan perbandingan produk-produk dan air
2.6 Total Asam Tertitrasi (Apriyantono et al 1989)
Total asam diukur dengan melarutkan sebanyak 25-50 gram sampel
ke dalam labu takar 250 ml dan diencerkan sampai tanda tera. Campuran
dikocok, kemudian disaring. Fitrat sebanyak 25 ml ditetesi indikator PP
(phenolphthalein) dan dititrasi dengan NaOH 0.1 N hingga terbentuk warna merah muda. Besarnya total asam tertitrasi dinyatakan sebagai ml NaOH 0.1
N/100 g. Total asam tertitrasi dapat dihitung dengan menggunakan rumus:
Total Asam Tertitrasi = V x faktor pengenceran x 100
Berat Sampel
Keterangan:
V : volume NaOH (ml)
2.7 pH (AOAC 1995)
Pengukuran derajat keasaman menggunakan alat pH meter. Sebelum
digunakan, alat distandarisasi dahulu dengan menggunakan larutan buffer pH 4.0 dan pH 7.0. Formula minuman (sampel) diambil + 100 ml dalam gelas
piala. Elektroda pH meter dicelupkan ke dalam sampel, kemudian dilakukan
pembacaan pH sampel setelah dicapai nilai yang konstan.
2.8 Total Antosianin (Prior et al., 1998)
Konsentrasi antosianin dapat diukur berdasarkan metode pH-differential. Sebanyak masing-masing 0.05 ml sampel dimasukkan ke dalam 2 tabung reaksi. Tabung reaksi pertama ditambah larutan buffer potasium klorida (0.025 M) pH 1 sebanyak 4.95 ml dan tabung reaksi kedua
ditambahkan larutan buffer sodium asetat (0.4 M) pH 4.5 sebanyak 4.95 ml. Pengaturan pH dalam pembuatan buffer potasium klorida menggunakan HCl dan pengaturan pH dalam pembuatan buffer sodium asetat menggunakan asam asetat. Absorbansi dari kedua perlakuan pH diukur dengan
spektrofotometer pada panjang gelombang 516 nm dan 700 nm setelah
didiamkan selama 15 menit.
Nilai absorbansi sampel ekstrak dihitung dengan menggunakan
persamaan: A ={(A516-A700)pH 1 – (A516-A700)pH 4.5}. Konsentrasi antosianin
dihitung sebagai sianidin-3-glikosida menggunakan koefisien ekstingsi molar
Konsentrasi antosianin (mg L-1) = (A x BM x FP x 1000)
(ε x diameter kuvet (1 cm)) Keterangan:
A : absorbansi
BM : berat molekul
FP : faktor pengenceran (5 ml / 0.05 ml)
ε : koefisien ekstingsi molar (29 600 L mol-1 cm-1)
Konsentrasi antosianin selanjutnya dinyatakan dalam mg CyE/g
sampel (CyE = sianidin equivalen).
2.9 Total Vitamin C dengan Metode Titrasi Iod (Jacobs 1958)
Sebanyak 10 gram sampel dimasukkan ke dalam labu takar 100 ml
dan diencerkan sampai tepat tanda tera. Campuran dikocok dan disaring.
Filtrat sebanyak 25 ml ditetesi indikator kanji 1% beberapa tetes, lalu difiltrasi
dengan larutan iod 0.01 N sampai terbentuk warna biru.
Kadar vitamin C = V x N x 0.88 x Faktor Pengenceran x 100
Berat sampel
Keterangan: V : ml larutan iod 0.01 N yang dipakai (ml)
N : normalitas iod hasil standarisasi
2.10 Aktivitas Antioksidan (DPPH) (Kubo et al., 2002)
Buffer asetat sebanyak 4 ml ditambahkan dengan 7.5 ml methanol
dan 400 µl larutan DPPH. Campuran larutan, kemudian dihomogenisasi.
Setelah homogen, sampel sebanyak 100 µl ditambahkan ke dalam campuran
dan diinkubasi selama 20 menit dengan suhu 25oC, kemudian sampel diukur
absorbansi pada panjang gelombang 517 nm. Untuk mengetahui kapasitas
antioksidan sampel, data hasil absorbansi dibandingkan dengan kurva
standar. Untuk formula 0, hanya bahan tambahan pada formula saja yang
diukur sedangkan sampel tidak ditambahkan. Perhitungan sampel
dibandingkan dengan kurva standar asam askorbat dan kapasitas dinyatakan
dalam mg/g AEAC (Ascorbic Acid Equivalent Antioxidant Capacity). Aktivitas antioksidan (mg AEAC/g) = C x faktor pengenceran
bobot sampel kering (gram)x FK
Keterangan:
C : kapasitas antioksidan dari kurva standar (mg/g)
Pengolahan dan Analisis Data
Data hasil penelitian diolah dengan Microsoft Excell for Windows lalu dianalisis dengan program SPSS 16.0 for windows. Pada penelitian pembuatan minuman serbuk buah buni, hasil hedonik dianalisis secara deskriptif dengan
menggunakan nilai modus dan rata-rata dan persentase panelis yang dapat
menerima. Untuk mengetahui pengaruh jenis formula terhadap tingkat kesukaan
panelis terhadap minuman serbuk buah buni, data hasil uji hedonik dianlisis secara statistik dengan uji beda “Analysis of Variance (ANOVA)”, apabila hasil uji ini menunjukkan adanya perbedaan di antara perlakuan maka dilakukan uji lanjutan “Duncan’s Multiple Comparison Test” uji lanjut ini dapat menentukan secara rinci mana perlakuan yang berbeda dan yang sama. Untuk menentukan
formulasi terbaik (terpilih) maka hasil hedonik dilakukan uji Kruskal-Wallis H (uji ranking). Rancangan percobaan yang digunakan dalam penelitian ini adalah
Rancangan Acak Kelompok (RAK) dengan satu faktor perlakuan yaitu tingkat
kematangan. Desain Rancangan Acak Kelompok adalah sebagai berikut:
Yij : Unit eksperimen ke-j hasil uji organoleptik karena pengaruh tingkat
kematangan
μ : Nilai tengah atau pengaruh rata-rata yang sebenarnya : Efek perlakuan tingkat kematangan
: Kekeliruan berupa efek acak yang berasal dari unit eksperimen ke-j
hasil uji organoleptik karena dikenai perlakuan ke-I jenis formula
i : Banyak taraf jenis kematangan (I = kematangan A, B, C)
HASIL DAN PEMBAHASAN
A. EKSTRAKSI BUAH BUNI
Ekstraksi adalah proses penarikan komponen/zat aktif suatu sampel
dengan menggunakan pelarut tertentu. Prinsip ekstraksi adalah melarutkan
senyawa polar dalam pelarut polar dan senyawa non polar dalam pelarut non
polar (Harbone 1987). Menurut Cook & Cullen (1986), ekstraksi bertahap ganda
(multi-stage extraction) digunakan untuk memperoleh efisiensi yang lebih tinggi,
di mana produk yang dihasilkan hampir seluruhnya dapat dipisahkan dari
rafinatnya. Ekstraksi antosianin biasanya dilakukan dengan menggunakan air, air
yang mengandung SO2, dan alkohol yang diasamkan (Markakis 1982). Oleh
karena itu, untuk mengetahui tingkatan ekstraksi optimum pada setiap
kematangan pada penelitian ini dilakukan ektraksi bertahap ganda. Pelarut yang
digunakan adalah air (H2O) karena air bersifat polar dan tidak bersifat toksik
sama sekali. Perbandingan buah buni dan pelarut adalah 1:5. Ekstraksi dilakukan
hingga fitrat sampel pada setiap kematangan buah menunjukkan warna putih.
Tiga macam tingkat kematangan yaitu kematangan matang tidak masak,
kematangan agak masak, dan kematangan masak penuh. Pada kematangan
matang tidak masak filtrat berwarna putih pada ekstraksi kedua, pada
kematangan agak masak filtrat berwarna putih pada ekstraksi ketiga, dan pada
kematangan masak penuh filtrat berwarna putih pada ekstraksi kelima. Tingkat
estraksi dapat dilihat pada gambar 6. Berdasarkan hasil ekstraksi tersebut maka
untuk ekstraksi berikutnya pada setiap kematangan dilakukan 5 kali ekstraksi.
Hal ini dilakukan agar zat aktif pada setiap kematangan terekstrak secara
optimum karena diduga zat aktif pada kematangan agak masak dan matang tidak
masak masih ada.
Gambar 6 Hasil ekstraksi buah buni pada kematangan matang tidak masak (A), pada kematangan agak masak (B), dan pada kematangan masak penuh (C)