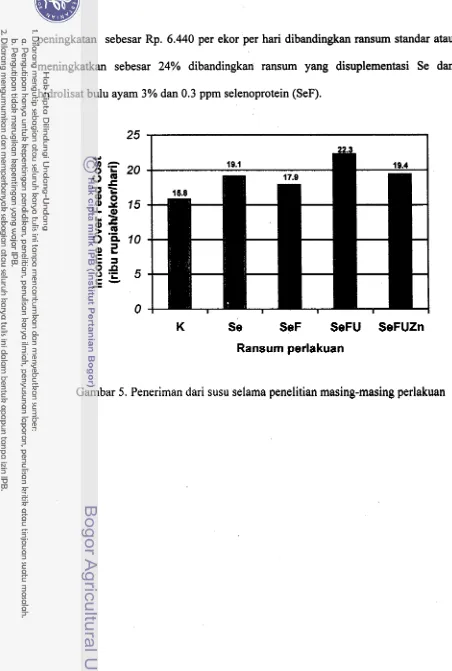
PENGARUH SELENOPROTEINAT PADA PRODUKSI SUSU
DAN RESPONS KEKEBALAN SAP1 PERAH LAKTAST
PADA BERBAGAI KONDISI PAKAN
OLEH :
CARIIIU HA111 PRAYITNO
PROGRAM PASCASARJANA
INSTITUT PERTANWN BOGOR
Caribu Hadi Prayitno. PENGARUH SELENOPROTEINAT PADA PRODUKSI SUSU DAN RESPONS KEKEBALAN SAP1 PERAH LAKTASI PADA BERBAGAI KONDISI PAKAN. Dibimbing oleh : Toha Sutardi, Muhilal dan Wasmen Manalu.
ABSTRAK
Perkembangan sapi perah menghadapi kelangkaan pakan akibat penyempitan lahan pertanian dan penurunan respons kekebalan akibat defisensi mineral. Penelitian ini dilaksanakan untuk mengkaji pengaruh selenoproteinat pada produksi susu dan respons kekebalan pada berbagai kondisi pemberian pakan. Ransum Kontrol (K)
merupakan ransum standar yang mengandung 65 % TDN dan 13% PK, Se = K
+
2.5 mglkg selenoproteinat, SeF = ransurn perbaikan yang mengandung 67%TDN, 14 %PK, 3 % hidrolisat bulu ayarn dan 2.5 mglkg selenoproteinat, SeFU = SeF
+
0.7 %urea, dan SeFUZn = SeFU
+
10 g/kg Zn-lisinat. Dari percobaan In vifroCaribu Hadi Prayitno. EFFECT OF YEAST SELENOPROTEINAT ON MILK PRODUCTION AND IMMUNE RESPONSE OF LACTATING DAIRY COWS UNDER DIFFERENT DIETARY REGIMENTS. Under supervised by : Toha Sutardi, Muhilal and Wasmen Manalu.
ABSTRACT
Dairying is impeded by feed shortage due to the decline in agricultural land and the lack of immune respones associated with mineral deficiencies. This experiment was designed to test the efficacy of yeast selenoprotein in promoting milk production and immune response under five dietary regiments. Diet control (K) was a control containing 65% TDN and 13% CP, Se =
K
+
2.5 mg/kg yeast selenoproteinate, SeF = improved diet containing 67%TDN, 14 5 CP, and 3%hydrolysed poultry feather, SeFU = SeF
+
0.7% urea, and SeFUZn = SeFU+
10 g/kgZn-lysinate. In vitro evaluation of the diets revealed that supplementation of selenoproteinate into diet
K
increased DM digestibility (51.4 vs 59.6%). All diets containing poultry feather had higher DM digestibility than dietK
and Se. The Zn- lysinate diet (SeFUZn) was the most fermentable (VFA : 168 vs 134 mM; NH 3 : 4.49SURAT PERNYATAAN
Yang bertanda tangan di bawah ini, saya :
N a m a : Caribu Hadi Prayitno
NRP
: 985037Program Studi : llmu Ternak
Menerangkan bahwa disertasi dengan judul :
PENGARUH SELENOPROTEINAT TERHADAP PRODUKSI SUSU DAN RESPONS KEKEBALAN SAP1 PERAH LAKTASI
PADA BERBAGAI KONDlSI PEMBERIAN PAKAN
Adalah benar-benar karya ilmiah saya, dan belum pernah dipublikasikan oleh
PENGARUH SELENOPROTEINAT PADA PRODUKSI
SUSU DAN RESPONS KEKEBALAN SAP1 PERAH LAKTASI
PADA BERBAGAI KONDISI PAKAN
OLEH :
CARIBU HAD1 PRAYITNO
Disertasi
sebagai salah satu syarat untuk memperoleh gelar Doktor pada Program Studi Ilmu Ternak
PROGRAM PASCASARJANA INSTITUT PERTANIAN BOGOR
Judul Disertasi : Pengaruh Selenoproteinat pada Produksi Susu dan Respons Kekebalan Sapi Perah Laktasi pada Berbagai Kondisi Pakan
Nama Mahasiswa : Caribu Hadi Prayitno
Nomor Pokok : 985037
Program Studi : Ilmu Ternak
Menyetu jui :
1. Komisi Pembimbing
/prof. Dr. Toha Sutardi, MSe. Ketua
Prof. Dr. H. Muhilal - Prof. Dr. Wasmen Manalu .5
Anggota Anggota
Mengetahui :
2. Ketua Program Studi Ilmu Tern ektur Program Pascasarjana
RIWAYAT
HIDUP
Penulis dilahirkan di Pemalang, Jawa Tengah tanggal 17 Februari 1965
dan merupakan putra kedua dari tiga bersaudara, dengan ayah bernama M.
Rasyid (Almarhum) dan Ibu Hj. Sutinah.
Pada tahun 1971 penulis masuk Sekolah Dasar I, Klareyan Pemalang dan tamat tahun 1976. Pada tahun 1981, penulis lulus dari Sekolah Menengah Pertama Negeri I, Pemalang dan pada tahun 1983 lulus dari Sekolah Menengeh Atas Negeri I, Pemalang. Pada tahun yang sama penulis diterima menjadi
mahasiswa di Fakultas Peternakan, Universitas Jenderal Soedirman, Purwokerto,
dan meraih gelar Sarjana pada tahun 1988.
Penulis menjadi staf pengajar tetap di Fakultas Peternakan, Universitas
Jenderal Soedirman tahun 1989. Pada tahun 199 1 penulis melanjutkan studi pada Program Pascasarjana, Universitas Pajajaran Bandung dengan sponsor dana dari
Tim Managemen Program Doktor (TMPD) dan memperoleh gelar Magister
Pertanian pada tahun 1994. Pada tahun 1998, penulis diterima sebagai mahasiswa Program Pascasarjana, lnsitutut Pertanian Bogor program Doktor dalam bidang
Ilmu Nutrisi Ternak dengan sponsor Tim Managemen Program Doktor (TMPD).
Penulis menikah dengan Dra. Titi Sumarti dan dikaruniai empat orang
anak, yaitu Erina Azmi Rahmadiana, Nia Aulia Fitriana, Hanifan Imaddudin dan
KATA PENGANTAR
Puji syukur penulis panjatkan ke hadlirat Allah s.w.t. atas segala petunjuk,
rahmat dan bimbinganNya, sehingga penulis dapat menyelesaikan penelitian dan
penulisan disertasi.
Penelitian dan penulisan disertasi ini dapat selesai atas bimbingan dari Tim
Komisi Pembimbing. Oleh karena sudah semestinya penulis menyampaikan
terima kasih kepada ProfDr. Toha Sutardi, MSc., selaku Ketua Komisi, ProfDr.
H. Muhilal dan Prof. Dr. M'asmen Manalu masing-masing sebagai anggota komisi
pembimbing yang dengan penuh kesabaran membimbing dan dengan tulus pula
menularkan ilmu yang dimilikinya untuk penulisan tugas akhir ini.
Ucapan terima kasili penulis sampaikan kepada Rektor IPB dan Pimpinan
Program Pascasarjana IPB, atas kesempatan yang diberikan untuk mengikuti studi
program Doktor. Icepada Rektor Universitas Jenderal Soedirman dan Dekan
Fakultas Peternakan, Universitas Jenderal Soedirman, disampaikan terima kasih
atas ijin yang diberikan untuk melanjutkan Program Doktor di IPB. Ucapan
terima kasih juga penulis sampaikan kepada Tim Managemen Program Doktor,
Dirjen Dikti yang telah memberikan beasiswanya untuk studi di IPB. Kepada
Direktur P3M Dikti penulis juga sampaikan ucapan terima kasih atas dukungan
dananya melalui proyek penelitian Hibah Bersaing Perguruan Tinggi tahun 2001-
2003 Pcnulis juga ~~ic~iyampaikan ucapan terima kasih kepada Yayasan
Kepada istri dan anak-anakku, ayahanda (Almarhum) dan Ibunda tercinta,
Bapak H. Fachrudin, kakak dan adik-adikku penulis mengucapkan banyak terima
kasih atas pengertian, doa dan bantuannya.
Kepada Dr. Anis Muktiani dan Ir. B.I.Tampoubolon penulis sampaikan
ucapkan terima kasih yang mendalam atas peran sertanya dalam kegiatan
penelitian Domestic Collaborative Research Grants yang mendukung penelitian
untuk disertasi. Penulis juga menyampaikan banyak terima kasih kepada banyak
pihak yang tidak dapat penulis sebut satu per satu atas dukungan, bantuan dan
kolaborasinya sehingga disertasi ini dapat selesai.
Akhirnya penulis berharap semoga hasil penelitian ini bermanfaat bagi
pembangunan peternakan di Indonesia khususnya perkembangan sapi perah.
Bogor, Mei 2002
Penulis,
DAFTAR
IS1
...
DAFTAR TABEL
...
DAFTAR GAMBAR
...
DAFTAR LAMPIRAN...
PENDAHULUAN...
TINJAUAN PUSTAKA...
.
...
1 Pencernaan Pakan Ternak Ruminansia
..
2
.
Pencernaan dan Absorbsi Karbohidrat pada Ruminansia...
...
3
.
Pencernaan dan Absorbsi Lemak...
.
4 Pencernaan dan Absorbsi Protein
...
5
.
Biosintesis Komponen Susu6
.
Selenium dan Fungsinya dalam Tubuh Ternak...
...
7
.
Penyerapan dan Ekskresi Se dalam Tubuh8
.
Hubungan Mineral Selenium dengan Kekebalan Tubuh...
9
.
Potensi Tepung Bulu Sebagai Sumber Protein Sapi Perah...
10.Fungsi dan Peranan Seng dalam Tubuh Ternak
...
Halaman
X
xii
MATERI DAN METODE
...
341
.
Tahap Persiapan...
342
.
Percobaan In Vitro...
34 3.
Percobaan Pemberian Pakan pada Sapi Perah Laktasi...
36HASIL DAN PEMBAHASAN
...
391
.
Pengaruh Perlakuan terhadap Konsumsi dan FermentabilitasRansum
...
482
.
Pengaruh Perlakuan terhadap Konsentrasi Triiodotironin clan 47Produksi Susu
...
4
.
Pendapatan Setelah Dikurangi Biaya Pakan (Income Over Feedcost)
...
KESIMPULAN ... 64
DAFTAR PUSTAKA
...
65...
DAFTAR
TABEL
...
1
.
Komposisi ingredien dan nutrien ransum perlakuan 402
.
Pengaruh pakan pada konsumsi clan fermentabilitas pakan...
49...
3
.
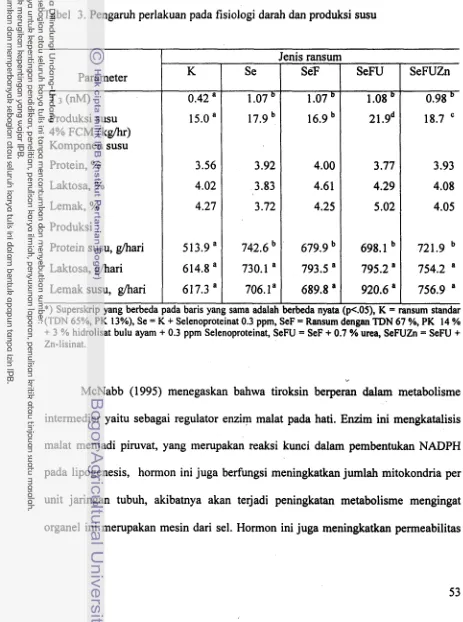
Pengaruh perlakuan pada fisiologi darah dan produksi susu53
...
DAFTAR GAMBAR
Halaman 1
.
Pencernaan protein dan utilisasi N di dalam Rumen...
15...
2
.
Sintesis lemak susu 203
.
Inkorporasi Se ke dalarn protein A.
oryzae...
35DAFTAR LAMPIRAN
1. Anova Pengaruh Selenoproteinat dalam Ransum Sapi Perah Laktasi pada Kecernaan Bahan Kering (%) in vitro
2.
Anova Pengaruh Selenoproteinat dalam Ransum Sapi Perah Laktasi pada Kecernaan Bahan Organik (%) in vitro3. Anova Pengaruh Selenoproteinat dalam Ransum Sapi Perah Laktasi pada NH3 (mM) in vitro
4. Anova Pengaruh Selenoproteinat dalarn Ransum Sapi Perah Laktasi pada VFA (mM) in vitro
5. Anova Pengaruh Selenoproteinat dalam Ransum Sapi Perah Laktasi pada terhadap Konswnsi Bahan Kering (kg/hari)
6 . Anova Pengaruh Selenoproteinat dalam Ransum Sapi Perah Laktasi pada Konsum Protein Kasar (kghari)
7. Anova Pengaruh Selenoproteinat dalam Ransum Sapi Perah Laktasi pada Produksi Susu, 4% FCM (kg)
8. Anova Pengaruh Selenoproteinat dalam Ransum Sapi Perah Laktasi pada Produksi Kolostrunl (kgll~ari)
9. Anova Pengaruh Selenoproteinat dalarn Ransum Sapi Perah Laktasi pada Globulin Kolostrum (g/hari)
10. Anova Pengaruh Selenoproteinat dalarn Ransurn Sapi Perah Laktasi pada terhadap Bahan Kering Susu (kglhari)
11. Anova Pengaruh Selenoproteinat dalarn Ransum Sapi Perah Laktasi pada Bahan Kering Tanpa Lemak Susu
(kghari)
12. Anova Pengaruh Selenoproteinat dalam Ransurn Sapi Perah Laktasi pada Lemak Susu (ghari)
13. Anova Pengaruh Selenoproteinat dalam Ransum Sapi Perah Laktasi pada Protein Susu (g/hari)
14. Anova Pengaruh Selenoproteinat dalarn Ransum Sapi Perah Laktasi pada Laktosa Susu (dhari)
15. Anova Pengaruh Selenoproteinat dalam Ransum Sapi Perah Laktasi pada Glutation Susu (mg/L)
16. Anova Pengaruh Selenoproteinat dalam Ransum Sapi Perah Laktasi pada Jumlah Sel Somatik (SCC, 10' sel/ml)
17. Anova Pengaruh Selenoproteinat dalam Ransum Sapi Perah Laktasi pada Triiodotironin (T3, darah)
18. Anova Pengaruh Selenoproteinat dalam Ransum Sapi Perah Laktasi pada Imunoglobulin (Ig-G, darah, Unit Elisa)
1
PENDAHULUAN
Perkembangan sapi perah di Indonesia menghadapi tantangan yang sangat
berat, antara lain : (1) Menyempitnya lahan pertanian, (2) Ketergantungan pada komponen bahan pakan impor dan (3) Impor susu yang mencapai 66 persen dari konsumsi susu nasional. Penyempitan lahan pertanian terjadi akibat meluasnya
daerah hunian pada lahan-lahan subur serta pembangunan penunahan pada daerah-
daerah hijau. Penyusutan lahan menyebabkan perluasan areal tanaman pakan nyaris
tidak mungkin dan persediaan limbah tanaman pangan makin berkurang. Kondisi ini
menyebabkan terjadinya banjir akibat kemampuan tanah untuk mengikat air sangat
berkurang. Erosi aki bat banj ir mengakibatkan pengikisan lapisan tanah bagian atas
yang merupakan sumber mineral esensial, darnpaknya tanah mengalami defisiensi
mineral. Akibat yang lebih fatal yaitu tersedianya logam berat yang toksik untuk
tanaman.
Impor jagung, bungkil kedelai, pollard, tepung bulu, tepung daging tulang,
tepung ikan mencapai 4
-
5 juta ton setiap tahunnya (Sudardjat, 2000) atau mencapai60-70% komponen konsentrat merupakan komponen impor, sehingga harga pakan
tidak seimbang dengan harga susu. lmpor susu dari tahun ke tahun mengalami
peningkatan akibat meningkatnya perrnintaan konsumen (peningkatan konsumsi
protein hewani), semakin menekan perkembangan sapi perah di Indonesia.
Situasi yang demikian menyebabkan populasi sapi perah pada tahun 1997
-
2001 hanya tumbuh sekitar 1.24% per tahun dan produksi susu hanya mampu
mengakibatkan peternakan sapi perah lumpuh total. Salah satu pendekatan yang
dapat dilakukan adalah pemanfaatan surnber bahan pakan lokal dan penggunaan
mineral yang mampu meningkatkan kinerja produksi susu.
Produksi susu selama laktasi bergantung pada dua ha1 yaitu penyediaan substrat
untuk perakitan komponen air susu (Davis dan Collier, 1983; Collier, 1985) dan laju
kematian sel-sel kelenjar ambing (involusi) (Anderson, 1985; Wilde dan Knight,
1989). Oleh karenanya penyedian substrat untuk sintesis susu dan pemeliharan sel-
sel sekretoris kelenjar ambing menjadi penting. Penyediaan substrat yang cukup dapat
dilakukan melalui penyediaan nutrien dalam bentuk energi dan protein yang memadai
untuk sintesis susu. Sumber energi pada sapi perah dapat dipenuhi dari hasil
fermentasi mikroba rumen berupa asam lemak atsiri (VFA), sumber protein dapat
dipenuhi dari protein pakan maupun non protein nitrogen. Di sisi lain hijauan pakan
di Indonesia defisien akan mineral Seng (Zn) (Little, 1986), padahal mineral ini
mempunyai fungsi penting dalam metabolisme (Georgievskii et al., 1982; Tillman et
al., 1983; Larvor, 1993). Di sisi lain produksi susu yang rendah di Indonesia juga
diakibatkan oleh kondisi sapi perah yang 60% diantaranya telah terkena mastitis
subklinis sampai klinis (Mirnawati, 1985; Sutardi, 2002).
Hidrolisat bulu ayam merupakan sumber protein potensial untuk ruminansia
karena sifat proteinnya yang tahan terhadap degradasi mikroba nunen. Hidrolisat
bulu ayam mempunyai protein (81%) dan TDN (70%) yang tinggi (NRC, 1988),
kaya akan asam amino sistin, namun defisien asam amino lisin dan metionin (Han
dan Parsons, 1991). Oleh karenanya suplementasi Zn-lisinat diharapkan mampu
Selenium (Se) dalam bentuk fisiologisnya sebagai glutation peroksidase (GSH-
Px) berperanan melindungi sel dan subseluler dari kerusakan oksidatif dengan jalan
mereduksi senyawa-senyawa peroksida menjadi senyawa yang aman bagi sel,
termasuk sel kelenjar ambing. Peroksida-peroksida terbentuk selama proses
metabolisme berlangsung. Glutation (GSH) adalah tripeptida yang mengandung tiga
asam amino yaitu glutamat, sistin dan glisin, yang dalam kelenjar ambing digunakan
sebagai sumber asam amino bersulfur (Baumrucker, 1985). GSH berperan dalam
sintesis protein susu. Dijelaskan oleh Combs dan Combs (1986) di samping Se
berperan sebagai antioksidan, mineral ini juga terlibat dalam sistem kekebalan.
Sehingga kehadiran Se dalam pakan diharapkan dapat mendukung upaya
peningkatan sistem kekebalan tubuh untuk menjamin produksi yang optimal.
Penggunaan selenoproteinat dalam penelitian ini dengan pertimbangan
penggunaan sodium selenite yang biasa digunakan sebagai sumber Se dalam pakan
baru-baru ini dikctahui bcrsifat mcrugikan (Mahan, 1995). Dengan valensi yang
besar, Se dalam tubuh dapat mengikat protein (enzim
dan
atau hormon), sehingga enzim menjadi tidak aktif. Secara umum Se organik dapat dideposisikan dalamjaringan lebih tinggi dibandingkan dalam bentuk anorganik. Bentuk selenometionin
dan selenosistein lebih mudah diabsorbsi oleh ternak karena sel-sel tubuh secara aktif
memanfaatkannya sebagai nutrien organik.
Selenit kurang dapat diabsorbsi pada ruminansia dibandingkan monogastrik.
Absorbsi yang rendah ini mungkin karena selenit diredksi menjadi senyawa yang
tidak larut dalam rumen. Windisch el ul. (1998) menyatakan bentuk Se sangat
jaringan lebih tinggi dibandingkan dalam bentuk anorganik. Bentuk selenometionin
dan selenosistein lebih mudah diabsorbsi oleh ternak karena sel-sel tubuh secara aktif
memanfaatkannya sebagai nutrien organik. Dikemukakan lebih lanjut bahwa
suplementasi selenometionin menghasilkan konsentrasi Se yang tinggi pada seluruh
jaringan, dengan rataan peningkatannya 19 persen lebih tinggi dibandingkan selenit.
Hampir 75 persen Se dalam kapang merupakan selenometionin (Stone, 1998) dan
sisanya berikatan dengan protein ataupun asam amino yang lain.
Selenium dalam bentuk selenosistein menempati tempat aktif (active site)
pada enzim deiodinase tipe I (Iodothyronine-5'-deiodinase) yang terlibat dalam
konversi (deiodinasi) tiroksin (T4) menjadi 3,3"5-triiodothyronine (T3) dalam ginjal
dan hati (Arthur et ul., 1993; Aro, 1994). Dikemukakan oleh Beckett et ul. (1993).
bahwa defisiensi selenium dan iodium erat kaintannya dengan metabolisme hormon
tiroid yang abnormal. Selanjutnya dilaporkan oleh Rimbawan et al. (2000) bahwa di
daerah GAKI (Gangguan Akibat Kekurangan Iodium) selalu diikuti oleh defisiensi
selenium, yang menurunkan konversi T4 menjadi T3, Padahal hormon ini
mempunyai pean yang vital dalam penyediaan energi (ATP) (Utiger, 1987;
McDonald, 1980) dalam setiap proses perakitan senyawa kecil (glukosa, asam mino,
asam lemak, dan gliserol). Tiroksin telah lama diketahui mampu meningkatkan
produksi susu dan aktivitas metabolisme dalam kelenjar susu (Davis et al., 1987;
Davis et al., 1988; Manalu dan Sumaryadi, 1995; Sumaryadi dan Manalu, 1996
Sintesis selenoproteinat dapat dilakukan melalui proses fermentasi dengan
mikroba. Strategi pembatasan sulfur pada substrat fermentasi digunakan supaya
antagonisnya. Mikroba akan mcmanl'aatkan selcniutn sebagai pengganti sulfur pada
saat konsentrasi sulfur dalam media tidak cukup mengingat mineral ini mempunyai
kemiripan fungsi.
Tujuan penelitian ini adatah mengkaji penggunaan selenoproteinat dalam
ransum sapi perah yang mengandung hidrolisat bulu ayam pada berbagai kondisi
pakan terhadap produksi susu dan respons kekebalan. Kondisi pakan dibatasi pada
pakan dengan energi dan prodtein yang rendah dan kondisi energi dan protein yang
cukup baik dengan kecukupan ammonia (ditambah urea) dan atau kecukupan mineral
Seng (Zn). Suplementasi Zn dalam bentuk garam Zn-lisinat diharapkan mampu 1010s
dari degradasi mikroba rumen, sehingga meningkatkan kernanfaatan kedua nutrien
TINJAUAN PUSTAKA
1. Kebutuhan Mineral untuk Mikroba Rumen
Mineral di dalam rumen dibutuhkan oleh mikroba untuk pembentukan
komponen sel, komponen enzim dan kofaktor. Mengingat aktivitas mikroba
rumen memegang peranan penting dalam proses fermentasi, maka defisiensi
mineral akan mempengaruhi fermentabilitas pakan. Kebutuhan mikroba rumen
pada mineral sampai saat ini masih didasarkan pada kebutuhan ternak inang.
Berdasarkan rekomendasi NRC (1988) kebutuhan mineral untuk sapi perah
dengan produksi susu sebesar 13 - 27 kglhari adalah sebagai berikut : Ca 0.5 1 %,
P 0.33%, Mg 0.20%, K 0.90%, Na 0.1 8%, C1 0.25%, S 0.20%, Fe 50 ppm, Co
0.1 0 ppm, Cu 10 ppm, Mn 40 ppm, Zn 40 ppm, I 0.60 pprn dan Se 0.3 ppm. Ca
dan P merupakan dua mineral makro yang berkaitan erat baik secara fisiologis
maupun fungsinya.
Kalsium (Ca) merupakan mineral yang diperiukan untuk pembentukan
tulang kerangka dan gigi, dan juga terdistribusi pada jaringan lunak serta cairan
ekstraseluler. Hewan membutuhkan Ca untuk pembentukan tulang dan gigi,
transmisi impuls syaraf, kontraksi otot, regulasi gerak jantung, pembekuan darah
dan aktivitas serta stabilisasi enzim. Tulang merupakan sumber dan cadangan Ca.
Pada awal laktasi dapat terjadi keseimbangan kalsium yang negatif, karena
pengeluaran Ca dalam air susu lebih besar dibandingkan pasokan Ca dalam
pakannya.
Ketersediaan Ca bagi ternak bergantung pada : konsumsi Ca, status Ca dan
umur ternak, jumlah Ca yang dibutuhkan, bentuk kimia dan sumber kalsium serta
peneliti sebelumnya, rasio Ca dan P dalam ransum 1 : I sampai 7 : 1 masih berada dalam kisaran yang dapat ditoleransi oleh ternak. Hibbs dan Conrad (1983)
melaporkan bahwa sapi laktasi dapat menyerap 1.71 g Ca untuk setiap 1 g P.
Pakan yang tinggi lemaknya akan meningkatkan Ca fecal yang hilang melalui
pembentukan sabun, oleh karenanya kebutuhan dalam pakan meningkat.
I:osfor (P) mcri~pakan ~iiiricral kunci dalam metabolisme energi dan
merupakan komponen yang esensial pada sistem buffer dalam darah dan cairan
tubuh lainnya. Halnpir 85% P dalam tubuh sapi ditemukan dalam tulang rangka,
gigi dan jaringan Iunak. Jumlah P yang diserap ternak sangat berganti~ng pada sumber P, jumlah konsumsi ransum, rasio Ca:P, pH usus dan level kalsium (NRC,
1988). Penyerapan fosfat terjadi di usus halus, melalui transport aktif yang
dirangsang oleh bentuk aktif vitamin D. Kebutuhan P untuk sapi perah yang
berproduksi susu 13-27 kglhari adalah 0.33 %, namun tidak ada masalah jika sapi
mengkonsu~iisi P dua kali dari yang direkomendasikan. U
Salah salu kcutamaan ternak ruminansia adalah kernampuannya dalaln
riicngi~bah pakan serat inenjadi senyawa organik sebagai sumber energinya.
Proses pencernaan pada ruminansia merupakan interaksi antara pakan, populasi
mikroorganisme dan aktivitas enzim serta hormonal. Sutardi (1980) menyatakan
bahwa proses pencernaan pada ruminansia terjadi secara mekanis (di mulut),
fermentasi (oleh enzim-enzim yang berasal dari mikroorganisme rumen) dan
hidrolisis (oleh enzim-enzim hewan induk semang).
Mikroorganisme yang dominan dalam proses fermentasi terdiri atas
bakteri, protozoa dan fungi. Popi~lasi bakteri dalam rumen berkisar antara 10'
-
Pada proses ini serat pakan akan mengalami proses fermentasi yang sangat luas
sehingga menghasilkan Volatil Fafty Acid (VFA). Proses ini sebagian besar
dilakukan oleh adanya aktivitas bakteri selulolitik yang perannya diinduksi oleh
substrat pakan (Prayitno, 1994), sedangkan protein akan dirombak menjadi
NH3
dengan tidak mengenal batas, meskipun ammonia yang dihasilkan sudah cukup
untuk pertumbuhannya (Sutardi, 1977).
Produk fermentasi retikulorumen akan disalurkan ke organ selanjutnya
yaitu omasum dan abomasum. Pencernaan abomasum merupakan tahapan
lanjutan, pada organ ini dihasilkan HCI dan pepsin yang berperan di dalam
perombakan protein, sedangkan pada omasum akan terjadi penyerapan air,
ammonia. elektrolit dan ~nungkin VFA. Pada organ pencernaan bagian belakang
seperti sekum, kolon dan rektum juga terjadi aktivitas fermentasi, tapi informasi
mengenai ha1 itu belum banyak terungkap (Forbes dan France, 1993).
2. Pencernaan dan Absorbsi Karbohidrat pada Ruminansia
Karbohidrat pada pakan ruminansia merupakan nutrien yang dominan
dala~n menycdiakan sil~iiber eriergi untuk proses faali, di samping menyediakan
bahan yang bersifat bulky yang berguna untuk memelihara kelancaran proses
pencernaan. Kandungan karbohidrat dalam pakan ternak ruminansia dapat
mencapai 60
-
75% dari bahan kering ransum yang berasal dari isi sel (gula danpati) dan dinding sel (selulosa dan hemiselulosa) (Sutardi, 1980). Komponen
karbohidrat berupa selulosa, hemiselulosa, pektin, pati, fruktan dan sukrosa di
dalam rumen mengalami pencernaan oleh enzim-enzim yang dihasilkan oleh
Proses metabolisme karbohidrat dalam retikulorumen sangat komplek.
Pertama-tama selulosa dan hemiselulosa akan mengalami hidrolisis oleh enzim
P-
I -4-glukosidase yang dihasilkan oleh mikroba menjadi sakarida sederhana seperti
heksosan, pentosan, maitosa, sul<,rosa, selobiosa. Sakarida sederhana yang
terbentuk akan diubah menjadi asam piruvat melalui jalur lintasan Embden-
Meyerhol' ('l'i llman e/ a/. , 1 983; 1:rancc dan Siddons, 1 993). Piruvat selanjutnya diubah menjadi VFA yang terdiri atas asetat, butirat, propionat dan sejumlah kecil
valerat serta asam lemak rantai cabang yaitu isobutirat, isovalerat dan 2-
metilbutirat ( Sutardi, 1977; Church dan Pond, 1988; Van Soest, 1994). Perubahan piruvat menjadi VFA terjadi melalui beberapa lintasan. Asetat dihasilkan melalui
jalur yang sederhana (Chesworth el al., 1998). Piruvat bereaksi dengan KoA
membentuk asetil KoA dan kehilangan asam format. Asam format dipecah
menjadi C 0 2 dan gas Hz Gas hidrogen dikonversi menjadi metan. Pembentukan
asetat juga dapat melalui jalur laktat.
Stokiomctri reaksi I'crmcntasi hcksosa met~jadi tiga kolnponen utama VFA
dalam rumen terdiri atas 3 macam yaitu (Orskov dan Ryle 1990):
1. Asam asetat : ChH , 2 0 6
+
2H20+
2 CH3COOH+
2 C02 +4H2
2. Asam propionat : C6Hl206+ 2 H2 3 2 CH3CH2COOH
+
2H203. Asam butirat : C6HI206 3 CH3(CH2)2COOH +2C02+2H2
4 Hz+ COz
+
CH4+
2 H20Reaksi tersebut menunjukkan bahwa produksi propionat lebih
menguntungkan dibandingkan asetat, ha1 ini karena pada pembentukan asetat
selalu disertai prodi~ksi hidrogen, yang akan bereaksi dengan C02 membentuk
metan yang tidak bermanfaat bagi ternak. Pada pembentukan 2 mol propionat
dibutuhkan 1 mol heksosa dan hidrogen. Jadi pembentukan propionat dapat
digunakan sebagai "hidrogen sink" dan menurunkan energi yang hilang dalam
bentuk metan. Leng (1991) menambahkan bahwa proses fermentasi di dalarn
rumen menghasilkan sel mikroba (merupakan 113 bagian bahan organik) dan
sisanya VFA, COz dan CH4 Prinsip penggunaan substrat dan hasil produknya
dari proses fermentasi 4 kg karbohidrat adalah sebagai berikut : 1. Karbohidrat menjadi VFA
16.7 CHO -, 21 Asam asetat
+
6 Asam Propionat+
3 Asam Butirat+
7.5 CI-IJ
+
78ATP2. Karbohidrat menjadi precilrsor sel mikroba
8.3 CHO
+
1.4 polisakarida+
13.8 piruvat+
2CH 4+
I7ATP 3. Reaksi keseluruhan :25 CHO
+=
2 1 Asam asetat+
6 Asam propionat+
3 Asam butirat+
9.5 CH4 + 1300 g sel keringPropionat merupakan satu-satunya VFA yang dapat digunakan sebagai
sumber glukosa. Chesworth et a1.(1998) menyatakan bahwa pembentukan
propinat dapat melalui dua jalur, yang sangat ditentukan oleh jenis mikroba. Jalur
pertama, piruvat diubah menjadi laktat. Laktat selanjutnya diaktivasi oleh
pembentukan ester KoA (Laktil KoA), selanjutnya akan kehilangan C02 dan Hz0
untuk membentilk propernoil KoA. Proses selanjutnya propernoil KoA
dihidrogenasi menjadi propionil KoA. Langkah yang terakhir dengan kehilangan
KoA sehingga terbentuk propionat. Jalur kedua merupakan jalur kebalikannya,
jalur ini digunakan pada sel-sel hewan, utamanya hati untuk mensintesis glukosa
Pembentukan butirat melalui 3 tahapan utama, yaitu piruvat dehidrogenasi
menghasilkan asetoasetil KoA. Asetoasetil KoA akan direduksi menghasilkan 3-
hidroksilbutiril KoA dengan menggunakan NADH dan NAD'. Tahapan
selanjutnya yaitu pembentukan Krotonil KoA. Krotonil KoA direduksi untuk
menghasilkan ester KoA dan asam butirat. Ester dihidrolisis untuk menghasilkan
butirat dan KoA bebas. Selain tiga komponen VFA di atas proses fermentasi
karbohidrat dalam rumen juga menghasilkan metan. Chesworth et al. (1998) menyatakan bahwa 8% energi dalam pakan yang dikonsumsi oleh ternak diubah
menjadi metan.
Fermentasi dalam rumen akan menghasilkan asetat dalam jumlah banyak,
dengan laju sekitar 20-25 mol per hari pada sapi perah, laju produksi asam
propionat sekitar 113 laju produksi asain asetat. Asam butirat diproduksi sekitar
10% dari total VFA, sedangkan asam valerat dan isovalerat masing-masing
sekitar 1 % (Forbes dan France, 1993).
Konsentrasi VFA total dalam cairan rumen secara normal adalah 70 - 130 mM, dan konsentrasi parsial yang terbentuk selalu berbeda sesuai pola produk
VFA cairan rumen yang sangat dipengaruhi oleh jenis karbohidrat yang
dikonsumsi. Konsentrasi asetat yang tinggi dalam cairan rumen erat kaitannya
dengan peningkatan kandungan hijauan atau pakan serat yang dikonsumsi,
sebaliknya peningkatan konsentrasi propionat dalam cairan rumen berkaitan
dengan peningkatan konsentrat dalam pakan (Banerjee, 1978; Tillman et al.,
1983; Arora, 1989; Forbes dan France, 1993).
Produk akhir pencernaan karbohidrat dalain bentuk VFA selanjutnya
diabsorbsi ke dalam jaringan tubuh ternak untuk digunakan sebagai sumber energi
dan bahan sintesis lemak. Asam propionat diabsorbsi melalui epitel rumen dan
~nasilk kc sirkulasi clurall clan Jibawu kc hati ilntuk sclanjutnya diubah n~cl~jacli glukosa dan menjadi bagian dari cadahgan glukosa hati. Asam butirat sebelum
masuk ke sirkulasi darah untuk dibawa ke hati bersama-sama asetat, terlebih
dahulu dikonversi menjadi asam beta hidroksi butirat (BHBA) di dalam epitel
rumen (Banerjee, 1978; Crampton et a]., 1978). Asetat dan BHBA dari hati
disalurkan ke sistem sirkulasi dan dipakai oleh jaringan terutama sebagai sumber
energi melalui siklus asam sitrat (Tillman et al., 1983; Forbes dan France, 1993).
Forbes dan France (1993) menalnbahkan bahwa asetat dan propionat yang
diabsorbsi masing-nlasing digunakan sebagai sumber energi dan bahan untuk
sintesis glukosa. Di samping itu asetat juga digunakan sebagai substrat untuk
lipogenesis dan propionat untuk glukoneogenesis. Oleh sebab itu asam propionat
dikatakan bersi fat glukogeni k karena asam tersebut dapat dikatabolisme menjadi
glukosa dan juga sebagai prekursor glukosa, sedangkan asetat dan butirat bersifat
ketogenik (Orskov, 1 977).
3. Pencernaan dan Absorbsi Lemak
Ada dua ha1 penting nasib asaln lemak selama berada dalam rumen, yaitu
liposisis dan biohidrogenasi (Jenkins, 1993; Scott dan Ashes, 1993). Lipolisis
akan menyebabkan pelepasan asarn lemak bebas (FFA) dari hasil esterifikasi lipid
tanaman yang dikonsumsi ternak ruminansia. Dalam proses liposisis, lipase
mikroba berperan menghidrolisis asilgliserol hasil esterifikasi lemak menjadi
FFA, gliserol dan galaktosa (Palmquist dan Jenkins, 1980; Scott dan Ashes,
1993). FFA yang terbentuk selanjutnya secara cepat dihidrogenasi oleh sejumlah
hidrogenasi terjadi pengurangan asam lemak tidak jenuh dan berubah menjadi
asam lemak jenuh melalui beberapa aksi yaitu isomerase, kemudian hidrogenasi
ikatan rangkap sis, pada C 18:2 terjadi reduktase dan selanjutnya dengan trans
pada CIS: I dihidrogenasi menjadi C18:O. Menurut Moir (1991) dari hasil
penulusuran pustakanya menyebutkan bahwa dalam proses hidrogenasi, selain
terjadi perubahan asam linolenat, linoleat dan oleat menjadi asam stearat juga
terdapat sejumlah kecil asam lemak tidak jenuh dengan ikatan rangkap trans, di
mana asam lemak tersebut resisten terhadap mikroba yang berperan dalam
hidrogenasi dan menambah karotinoid yang dapat mensuplai betakarotin untuk
ternak.
Produk akhir lipolisis dan biohidrogenasi sebagian diserap oleh dinding
rumen dan sebagian lagi mengalir ke abomasum. Banerjee (1978) menyatakan
bahwa asam lemak rantai pendek dan VFA hasil hidrolisis dan fermentasi Lipid,
diserap melalui dinding rumen sedangkan asam lemak rantai panjang terus
mengalir ke abomasum. Proses di abomasum, digesta lipid pasca rumen yang
sebagian besar (70%) terdiri atas asam lemak jenuh pakan dan dari sintesis lemak
"de-novo" serta sedikit (1 0%) fosfolipid mikroorganisme akan bergabung dengan
benda padat lainnya (Bauchart, 1973). Selanjutnya setelah dari abomasum
campuran digesta mengalir ke usus halus. Di dalam usus halus garam-garam
empedu akan mengemulsikan lemak dan diikuti dengan gerakan peristaltik,
sehingga lemak terdispersi menjadi butir-butir kecil dan diikuti dengan masuknya
lipase (Linder, 1992). Lemak yang sebagian sudah dicerna, terutama dalam
bentuk yang larut dalam air membentuk misel-misel yang stabil (asam lemak
permukaan sel mukosa usus halus dan melepaskan materi untuk siap diserap.
Asam - asam lemak dan monogliserida oleh mukosa usus diubah kembali menjadi trigliserida dan membentuk kilomikron. Kilomikron selanjutnya dibebaskan ke
dalam jaringan limfe dan masuk ke peredaran darah untuk ditransport ke dalam
sel jaringan yang membutuhkan yaitu jaringan perifer, adiposa dan ambing
(Linder, 1992; Collier, 1985).
4. Pencernaan dan Absorbsi Protein
Sumber protein untuk ruminansia dapat berasal dari protein pakan maupun
non protein nitrogen (NPN). Perombakan protein oleh enzim proteolitik di dalam
rumen menghasilkan peptida dan asam-asam amino. Produk ini sebagian besar
akan mengalami katabolisme lebih lanjut (deaminasi) sehingga dihasilkan amonia
(NH,). Amonia asal perombakan pakan sangat besar kontribusinya terhadap pool
amonia rumen. Proses proteolitik dan deaminasi asam-asam amino menghasilkan
amonia diduga bersifat konstitutif, artinya tidak ada kontrol metabolik. Degradasi
protein dan deaminasi terhadap asam amino akan terus berlangsung, walaupun
telah terjadi akumulasi amonia yang cukup tinggi di dalam rumen (Sutardi, 1976).
Manfaat proses proteolitik tidak hanya memberi pasokan amonia untuk mikroba,
tetapi juga pasokan peptida. Beberapa spesies bakteri rumen mampu
menggunakan peptida secara langsung untuk sintesis protein (Chalupa, 1975).
Leng ( 1 991) menambahkan bahwa suplementasi urea dalam ransum diperlukan
i ~ n t u k mencukupi kebutuhan a~iionia ~ ~ n t u k pertumbuhan organisme fibrolitik dan sakarolitik dalam rumen.
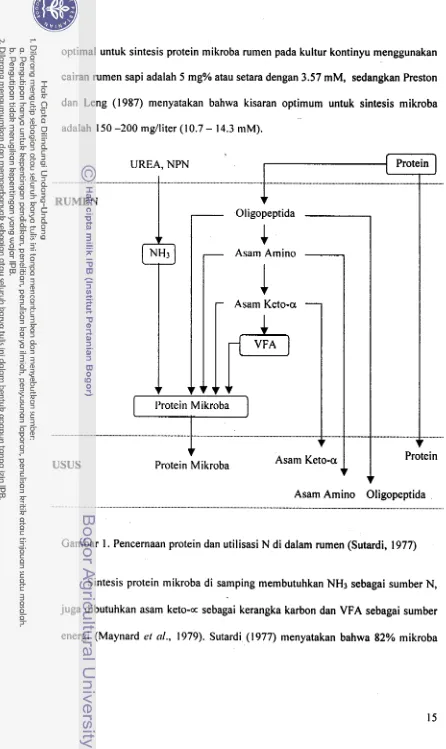
Amonia adalah su~nber nitrogen utama dan sangat penting untuk sintesis
optimal untuk sintesis protein mikroba rumen pada kultur kontinyu menggunakan
cairan rumen sapi adalah 5 mg% atau setara dengan 3.57 mM, sedangkan Preston
dan Leng (1987) menyatakan bahwa kisaran optimum untuk sintesis mikroba
adalah 150 -200 mglliter (I 0.7 - 14.3 mM).
[image:141.563.56.502.23.772.2]Asam Amino Oligopeptida
... . ... .. ... . .... . ... . ... . ... .- ... . ... " ... ""." ....-. ".." ,.... ".-" ...-.- "" ...," ...
Gambar 1. Pencernaan protein dan utilisasi N di dalam rumen (Sutardi, 1977)
Sintesis protein mikroba di samping membutuhkan NH3 sebagai sumber N, juga dibutuhkan asam keto-cc sebagai kerangka karbon dan VFA sebagai sumber
rumen membutuhkan N-NH3 untuk mensintetis protein tubuhnya. Oleh karenanya
perombakan asam amino menjadi NH3 lebih disukai.
Penggunaan NPN sebagai sumber nitrogen untuk sintesis protein mikroba
rumen akan efektif pada ransum dengan berprotein rendah, dan cukup tersedia
energi. Cappock et al. (1976) mengemukakan bahwa pembatas utama efisiensi penggunaan urea adalah pelepasan amonia yang begitu cepat ketika terjadi kontak
dengan enzim urease di dalaln cairan rumen. Kecepatan pelepasan amonia dapat
mencapai 4 kali lebih cepat daripada kecepatan penggunaannya oleh mikroba
rumen (Bloomfield el al., 1960). Manalu (1 999) menyatakan terdapat dua syarat
agar amonia yang terbentuk dalam rumen efisien untuk sintesis protein mikroba :
pertama, konsentrasi amonia awal harus di bawah optimal, kedua :
mikroorganisme rumen harus mempunyai sumber energi yang mudah tersedia
untuk sintesis protein.
Maiga el al. (1996) menyatakan bahwa asam amino yang tersedia untuk
absorbsi usus pada ruminansia disuplai dari protein mikroba yang disintesis di
dalam rumen, protein yang tidak terdegradasi dalam rumen dan sekresi endegenus
dari saluran pencernaan. Laju aliran senyawa nitrogen ke dalam usus dipengaruhi
oleh intensitas degradasi protein pakan dan sintesis protein mikroba dalam rumen.
Jumlah protein mikroba tidak cukup untuk memenuhi kebutuhan asam amino dari
sapi perah yang berproduksi tinggi (Sutardi, 198 1).
5. Biosintesis Komponen Susu
Komponen dalam susu dapat dikelompokan berdasarkan sumbernya, yaitu :
1. Yang khas organ (kelenjar) ambing dan yang khas spesies (contohnya
2. Yang khas organ tetapi tidak khas spesies (laktosa)
3. Yang khas spesies tetapi tidak khas organ (beberapa protein)
4. Tidak khas organ dan juga tidak khas spesies (air, garam, dan vitamin).
Komponen laktosa, lipid dan beberapa protein disintesis pada kelenjar
ambing yang berasal dari nutrien yang ada dalam darah. Nutrien utama yang
diserap oleh kelenjar ambing adalah glukosa, asam amino, asam lemak
(kilomikron, LDL, NEFA), asetat, P-hidroksi butirat dan mineral (Collier, 1985;
Fox dan McSweeney, 1996;).
Laktosa adalah disakarida yang terdiri atas galaktosa dan glukosa melalui
ikatan /3 1-4 glikosidik. Nama sistematiknya adalah f3-0-D-galaktopiranosil
(1-)-P-D-glukopiranosa (P-laktosa) atau dalam bentuk a-laktosa (Fox dan
McSweeney, 1996). Glukosa dapat berasal dari perombakan glikogen hati dan
pembentukan glukosa dari propionat serta asam amino melalui proses
glukoneogenesis (Collier, 1985; Mepham, 1988). Wikantadi (1977) menyebutkan
bahwa glukosa meri~pakan bahan pembentuk utama laktosa pada susu sapi dan
kambing. Beberapa atom karbon dari laktosa terutama residu galaktosa, berasal
dari senyawa lain misalnya asetat dan gliserol. Perbedaan darah arteri-vena untuk
glukosa lebih kurang dua kali dari yang diperlukan untuk sintesis laktosa, dengan
demikian kelebihan glukosa akan digunakan untuk sumber energi dan
pembentukan gliserol. Karena glukosa merupakan sumber utama sintesis laktosa
dan tekanan osinotik air susu harus dipertahankan tekanan osmotiknya agar
isotonis dengan darah, peningkatan atau penurunan produksi laktosa akan
susu juga akan berkurang (Fox dan McSweeney, 1996), sehingga glukosa juga
dapat dikatakan sebagai faktor pembatas sekresi susu.
Sumber utama sintesis protein susu berasal dari peptida-peptida, plasma
protein dan asam-asam amino bebas (Wikantadi, 1977; Larson, 1985; Chesworth
el al., 1998; Fox dan McSweeney, 1996). Asam-asam amino yang bebas yang
diserap oleh kelenjar ambing dari darah merupakan sumber utama untuk sintesis
protein susu, sedangkan plasma protein menyumbang sekitar 10%. Kasein, beta
laktoglobulin dan alfa laktalbumin merupakan 90-95% protein susu.
5.1. Sintesis Lemak Susu
Sintesis asam lemak susu utamanya berasal dari asetat, P-hidroksi butirat
dan trigliserida plasma dalam bentuk ki!omikron, Low Density Lipoprotein (LDL)
dan Non Esterified Fatty Acids (NEFA). Berbeda dengan ternak monogastrik
sintesis asam lemak SLISLI pada ternak ruminansia tidak berasal dari glukosa. Ilal
ini karena pada sitoplasma sel sekretoris kelenjar ambing ruminansia tidak
terdapat enzim sitrut liase, sehingga asam sitrat tidak dapat diubah menjadi
asetill-KoA dalam taliapan sintesis asam lemak. Sitrat yang terbentuk sebagian
diserap ke dalatn Aparatus Golgi dan disekresikan ke dalam lumen kelenjar susu.
Hal ini menyebabkan kandungan sitrat susu ruminansia lebih tinggi dibandingkan
ternak monogastrik (Collier, 1985).
Kadar lemak susu ternak mamalia sangat bervariasi antar spesies, dengan
kisaran konsentrasi 2% sampai 50% (Larson, 1985; Fox dan McSweeney, 1996).
Dikatakan lebih lanjut bahwa susu sapi tnengandung 3.5% lemak dan konsentrasi
periode laktasi, musim, status nutrisi, tipe pakan, kesehatan, umur ternak dan
interval pemerahan.
5.2. Sintesis Protein Susu
Tiga sumber utama pembentuk protein susu yang berasal dari darah yaitu
peptida-peptida, plasma protein dan asam-asam amino bebas. Kasein,
P-laktoglob~~lin dan K-laktalbumin disintesis di dalam sel kelenjar ambing,
sedangkan imniunoglobulin, seroalbumin dan gamma kasein tidak disintesis di
dalam kelenjar ambing tetapi langsilng diserap dari darah dalam bentuk yang sama
tanpa mengalami perubahan (W ikantadi, 1977; Fox dan McSweeny, 1996).
Sintesis protein dapat dibagi menjadi empat tahapan yaitu : aktivasi asam amino, inisiasi pembentukan rantai peptida, pemanjangan rantai dan penutupan
rantai (Chesworth el al., 1998; McDonald, 1980). Pada tahap aktivasi asam
amino bereaksi dengan ATP membentuk aminoasil denilat, selanjutnya gugus
aminoasil dikopel molekul tRNA untuk membentuk aminoasil tRNA, kedua
reaksi ini dikatalisis oleh enzim yang sama (amino asil tRNA sintetase) dan ATP.
Amino-asil
+
ATP+
Enzitn-+
Aminoasil-AMP-Enzim+
pirofosfatJika asam amino sudah dikopel dengan tRNA maka asam amino akan dibawa ke
ribosom. Kombinasi ini akan membentuk struktur polisom, di mana ribosom akan
terikat pada untaian messenger RNA (mRNA).
Tahap inisiasi : pada tahap ini akan terbentuk kompleks komponen ribosom
yang lebih kecil, mRNA dan tRNA dengan formil metionin atau metionin sebagai
asam amino yang terikat (AAI). Asam amino yang terikat oleh t-RNA
mempunyai antikodon tertentu, ditempatkan pada m-RNA sesuai dengan
Tahap pemanjangan : t-RNA kedua membawa asam amino ke kodon kedua dari
mRNA dengan bantuan GTP. Molekul basa tRNA berpasangan dengan kodon
kedua dari mRNA. Pada tahap ini enzim peptidil transferase mengkatalisis
pembentukan ikatan peptida antara dua molekul asam amino pada sisi A dari
ribosom. Penempatan asam amino diikuti pergerakan ribosom sepanjang m-RNA
hingga terjadi pemanjangan rantai asam amino dan t-RNA dilepaskan kembali ke
sitoplasma. Tahap terminasi : tahap pemanjangan rantai peptida terus berlanjut sampai salah satu dari kodon itu konsentrasinya tinggi pada mRNA. Apabila
ribosoin sudah inelnpunyai salah sat11 kodon itu (UAA, UAG, UGA) dalam
jumlah yang tinggi maka ikatan polipeptida akan putus dan polipeptida
dilepaskan. tRNA dan subunit ribosom berdisosiasi dan siap memulai sintesis
protein yang lain.
5.3. Sintesis Laktosa Susu
Laktosa adaiah disakarida yang terdiri atas galaktosa dan glukosa melalui
ikatan
p
1-4 glikosidik. Nama sistematiknya adalah P-0-D-galaktopiranosil (1 -)-P-D-glukopiranosa (P-laktosa) atau dalam bentuk a-laktosa (Fox dan
McSweeney, 1996). Suplai glukosa dengan mudah tersedia akan tetapi galaktosa
harus disintesis, dari glukosa yang melibatkan perubahan kontigurasi atom karbon
lGlukosa
h e w a s e
,
Glukosa 6 fosfatn
I
ATP ADP
Fosfoglukomutase
Glukosa- l -fosfat UDP-Glukosa
1
UDP-glukosaUDP glukosa-epimerase UDP Ga:akfosal
gaIaklosiItlnnslbrasc
1
~ l u k o s aJ
Laktosa [image:147.570.58.487.54.759.2]a-laktalbumin
Gambar 2. Lintasan pembentukan laktosa
Konsentrasi laktosa untuk susu sapi 'adalah 4.8% (Fox dan McSweeney, 1996).
Jalur sintesis laktosa dan sejumlah enzim yang terlibat disajikan dalam Gambar 2.
Galaktosil transferase bersama-sama dengan a-laktalbumin sering disebut juga
laktosasintetase. Kepentingan petnbentukan laktosa pada mamalia bertujuan
sebagai regulasi dan kontrol tekanan osmotik susu agar isotonik dengan darah.
Oleh karenanya produksi laktosa mempengaruhi volume air yang dialirkan ke
dalain lumen susu.
>.
6. Selenium dan Fungsinya dalam Tubuh Ternak
Selenium (Se) adalah unsur penting dari glutathione peroksidase (GSH-
Px), dengan 4 g atom Se per mol enzim (Rotruck et al., 1973; Ian Lean, 1987,
bilangan oksidasi +6, Se dalam bentuk asam selenit (H2Se03, merupakan asam
kuat) dan garam selenat (se0i2). Pada bilangan oksidasi +4, Se dalam bentuk
Selenium dioksida (SeOz), asam seleniuos (H2Se03) dan garam selenit (se0i2).
Garam selenit kurang larut dibandingkan garam selenat, khususnya pada pH
1
alkali, sedangkan selenit mudah direduksi pada pH rendah menjadi selenium
elemental dan selenat tidak mildah direduksi menjadi selenit (Smith, 1988).
McDowell (1 992) menyatakan unsur Se dapat direduksi menjadi
selenide (se2? atau dioksidasi menjadi selenite (se43 atau selenate (se6+).
Selenium kurang dapat diabsorbsi pada rulninansia dibandingkan monogastrik.
Rendahnya absorbsi ini mungkin karena selenite direduksi menjadi senyawa yng
tidak larut dalam rumen. Retensi absorbsi Se dipengaruhi oleh status ternak dan
bentuk Se. Secara umuln Se organik dapat dideposisikan dalam jaringan lebih
tinggi dibandingkan dalam bentuk anorganik. Gerloff (1992) menambahkan
baliwa di dala~n rumcn bentuk Sc anorganik akan direduksi dari selenite menjadi
selenide oleh proses hidrogenasi. Selenide tidak diabsorbsi di dalam rumen dan
juga tidak di dalam usus. Hampir 75 persen Se dalam kapang merupakan
selenometionin (Stone, 1998). Ditambahkan oleh Carolyn Berdanier (1998)
bahwa sintesis selenoprotein melibatkan asam-asam amino yang mengandung
sulfur dan selenium. Proses ini melibatkan selenofosfat untuk membentuk
selenosistein, di mana reaksinya dikatalisis oleh selenofosfat sintetase dan vitamin
B berperan sebagai koenzimnya.
Kira-kira 40 persen Se dalam tubuh tikus sebagai komponen GSH-Px.
Aktivitas GSH-Ps ekstraseluler hanya 111 0 dari intraseluler (Xin Gei Lei, 1995).
adalah sulfhidril yang mengandung tripeptida yang dibentuk dari asam glutamat,
sistein dan glisin (Krogmeier et al., 1993; Stamler dan Slivka, 1996; Groff dan Gropper, 2000). Reaksi pembentukannya membutuhkan adenosin trifosfat (ATP),
dengan tahapan reaksi sebagai beri~ut :
ATP
1. L-glutamat
+
L-sistein---
-+
L- y -glutamil-L-sistein~ g ~ +
Enzim yang berperan : y-glutamilsistein sintetase
ATP
2. L- y -glutamil-L-sistein
+
glisin---
+
glutation~ g ~ +
Enzim yang berperan : glutation sintctase
Persson-Moschos el al. (1 996) dan Carolyn Berdainer (1 998) menggolongkan selenoprotein pada mamalia menjadi 8, yaitu :
1. Glutation peroksidase sitosol
2. Glutat ion peroksidase ekstrseluler
3. phospholipid hydroperoxide glutathione peroxidase (phGSHPx)
4. Glutation peroksidase gastrointestinal
5. Tipe I 5'iodothyronine deiodonase (5'-1-DI)
6. Selenoprotein P (SeP)
7. Selenoprotein W (Sew)
8. Mitochondria1 capsule selenoprotein (MCS)
Fungsi GSH-Px dalam sel adalah melindungi membran sel dan subseluler
dari kerusakan oksidatif (Rotruct el al., 1973; Williams dan Dickerson, 1990;
McDowell, 1992; Brody, 1994; Ellis et crl., 1995; Stamler dan Slivka, 1996; Smith
maupun radikal bebas dengan jalan mereduksinya menjadi senyawa yang aman
bagi sel. Hidrogen peroksida dikonversi menjadi air, lipid peroksida dikonversi
menjadi alkohol dan air (Combs dan Combs, 1986; Stamler dan Slivka, 1996,
Carolyn Berdanier, 1998; Surai et al., 2001).
2GSH GSH-PX GS-SG
Hz0 2 atau
LOOHIROOH LOHIROH H20
+
H20Groff dan Gropper (2000) menatnbahkan bahwa GSH-Px lebih aktif
dibandingkan dengan katalase dalani mereduksi hidrogen peroksida dan organik
peroksida. Peroksida-peroksida harus dinetralisir karena dapat merusak membran
sel. Dikemukakan oleh Brzezinska-Slebodzinska et a1.(1994) pada sapi perah
menjelang proses partus akan terjadi stress oksidatif yang akan menghasilkan
ketidakseimbangan antara produksi oksigen dan radikal bebas. Radikal bebas
merupakan metabolit oksigen reaktif (MOR) yang dalam metabolisme normal
metnpunyai fungsi fisiologis yang penting, namun pada saat kekurangan substansi
alami yang bersifat proteksi, maka akan terjadi peningkatan
MOR
yang dapatmenurunkan kekebalan dan performans, di sini peranan Se menjadi penting di
samping antioksidan yang lain. Ditambahkan oleh Miller et al. (1993) jika MOR
tidak dapat dinetralisir maka akan menurunkan kesehatan sapi perah baik
langsung maupun tidak langsung. Secara langsung MOR akan merusak lipida-
lipida penting serta makromolekul, sedangkan secara tidak langsung MOR akan
mengi~bah membral sel, sehingga mengubah jalur metabolisme yang
Smith et al. (1997) menyatakan bahwa glutation berfungsi dalam sitosol
sel sedangkan vitamin E di dalam membran, keduanya berfungsi dalam
melindungi poliunsaturated fatty acid (PUFA) membran sel. Groff dan Grapper
(2000) menambahkan bahwa GSH-Px ditemukan utamanya di dalam sitosol
(70%). scdangkan lainnya tcrdapat pada matrik mitokondria (30%).
Bentuk selenoprotein lain yang mempunyai arti penting dalam
metabolisme adalah enzim tipe I S'iodothyronine deiodonase (5'-I-DI), di mana
selenosistein menempati pusat aktifnya (Arthur et al., 1993; Aro, 1996). Enzim ini
dite~nukan di dalam retikulum endoplasmik hati, ginjal dan otot. Enzim ini
~iiengkonversi tiroksin (T 4) rnenjadi 3.3.5-triiodotironin (T3) (Arthur et al., 1993,
Groff dan Gropper, 2000). T3 merupakan bentuk aktif hormon tiroid yang
berperan dalam metabolis~ne (Nunez, 1988; Rose dan Obara, 2000; Surai et al.,
2001). McDonald (1980) menyatakan bahwa salah satu pengaruh penting dari
tiroksin adalah dalam menstimulasi penggunaan oksigen, konsekuensinya akan
terjadi peningkatan laju metabolisme basal. Hormon ini juga berfungsi dalam
peningkatan jumlah mitokhondria per unit jaringan tubuh, akibatnya akan terjadi
peningkatan aktivitas metabolisme mengingat organel ini merupakan mesin dari
sel. Aktivitas hormon ini juga dapat melenturkan mitokhondria sehingga akan
terjadi peningkatan permeabilitas dari membran mitokhondria. Permeabilitas
membran berkaitan erat dengan reaksi fosforilasi. Sehingga akan terjadi
peningkatan fungsi organ ini sebagai tranduser energi dan konversi aliran
elektron ke bentuk energi kimia (ATP). Cartens et al. (1996) menegaskan bahwa
T 3 mampu meningkatkan sintesis protein. T3 masuk dalam sel dan mengikat
mempengaruhi laju transkripsi dari mRNA di dalam nukleus (Brody, 1994).
Swecker et al. (1995) menambahkan bahwa bentuk kimia Se mempengaruhi
konsentrasi T 3 dan ratio antara T3:T4 dalam plasma sapi. Dari hasil penelitiannya
selama 22 bulan membuktikan bahwa Se bentuk organik (yeast) menghasilkan
konsentrasi T3 yang lebih tinggi. ,
McNabb (1995) menyatakan bahwa hormon tiroid berperan dalam
metabolisme intermedier yaitu sebagai regulator enzim malat pada hati. Enzim ini
mengkatalisis konversi malat menjadi piruvat, yang merupakan reaksi kunci
dalam pembentukan NADPH pada lipogenesis. Hormon tiroid merupakan
pengontrol utama enzim malat di samping hormon insulin, dengan kontrol
penghambatnya oleh hormon glukagon.
7. Absorbsi dan Ekskresi Se dalam Tubuh
Absorbsi Se dalam tubuh sangat dipengaruhi oleh bentuknya. Combs
dan Combs ( 1 986) menyatakan bahwa L-selenometionin ditransport lnelalui
gradien dari mukosa ke sisi serosa usus, yang dihambat oleh L-metionin.
Kecepatan tranport DL,-selenometionin setengah kali dibandingkan L-
selenometionin dengan carrier yang sama dengan L-metionin. Selenit tidak dapat
melalui mukosa jika konsentrasi di dalam mukosa sama dengan konsentrasi
serosa. Reasbeck et al. ( 198 1) menyatakan bahwa selenometionin diabsorbsi 2 kali lebih banyak dibandingkan seienosistein atau 4 kali lebih banyak
dibandingkan selenit. Whanger el al. (1 976) menyatakan bahwa selenit dan
selenometionin diabsorbsi pada seluruh segmen intestin dengan absorbsi tertinggi
pada duodenum. Wright dan Bell (1966) menginformasikan bahwa tidak ada
Abdelrahman dan Kincaid (1995) menyatakan bahwa suplementasi Se
secara nyata meningkatkan konsentrasi Se darah induk, Se kolostrum dan kasein.
Gerloff (1992) membakukan kisaran konsentrasi ideal dalam serum adalah 70
-
100 ngSeIml serum. Konsentrasi ini dapat dicapai dengan suplementasi lebih
dari 6 mg Se per hari. Knowles el ul. (1999) menambahkan bahwa
suplementasi Se ragi lebih efektif 2-3 kali dibandingkan Na $5eO4 dalam
meningkatkan status Se dan kandungan Se dalam susu serta kasein. Transfer Se ke
kelenjar ambing dapat tercapai apabila ternak mendapat Se lebih banyak di atas
kebuti~han kritisnya (Gerloff, 1992). 'Ellis c/ (11. (1 997) nienyatakan konsi~~nsi Se
dalam bentuk sodium selenite dalam jumlah 10
-
30 kali dari kebutuhan tidak akanmenyebabkan problem kesehatan pada sapi muda. Suplementasi Se dalam bentuk
sodium selenite sebanyak 3 mglkg bahan kering ransum selama 90 hari
meningkatkan sel darah putih. Ditambahkan lebih lanjut konsentrasi Se dalam
serum dan darah juga ~neningkat sejalan dengan peningkatan suplementasi Se.
I'enggunaan Sc organik, karena bentuknya terikat dengan molekul
protcin, makn aknn digi~nakan olch ~nikroorganisme di dalam rumen atail bypass
ke dalam usus halus dan akan dihidrolisis oleh enzim-enzim usus halus. Senyawa
Se organik secara aktif ditransfer ke enterosit usus halus. Aktivitas GSH-Px
pada eritrosit sapi perah dara yang mendapat Se-kapang jauh lebih tinggi
dibandingkan dengan selenometionin, kobalt selenit ataupun sodium selenit. Sapi
perah yang mengkonsumsi Se organik menghasilkan susu yang lebih tinggi
dibandingkan dengan yang mengkonsumsi anorganik (Awadeh et al., 1999).
Mahan ( 1 995) menyatakan bahwa GSH-Px dalam plasma mRNAnya
dipengaruhi oleh supplai Se. Oleh karenanya ada prioritas penggunaan Se dalam
jaringan tubuh dan dalam bentuk GSH-Px aktivitasnya dalam jaringan
mempunyai prioritas sesuai dengan bentuknya. Enjalbert et al. (1999)
menambahkan bahwa aktivitas GSH-Px di dalam sel darah merah meningkat
secara cepat dengan suplementasi 45.5 mg Selhari. Aktivitas GSH-Px dapat
digunakan sebagai estimasi yang baik dari status Se, karena enzim ini merupakan
fungsi fisiologi dari selenium. 98% aktivitas GSH-Px di dalam darah berasosiasi
dengan eritrosit, oleh karenanya analisis GSH-Px di dalam sel darah akan efektif
menggambarkan status Se dalain jangka waktu yang lama.
Kandungan tertinggi glutation ditemukan dalam hati, yang merupakan
organ utama dalatn detoksifikasi dan eliminasi xenobiotik. Glutation disintesis di
dalam hati dari komponen asam amino dan diedarkan ke plasma darah dan
empedu. Ketersediaan asam amino sistein nampaknya merupakan tahapan
pembatasan sintesis. Kelebihan protein pakan atau asam amino bersulfur tidak
akan meningkatkan konsentrasi maksimum glutation hati melebihi level maksimal
secara fisiologi. Meskipun demikian dua asam amino lain yaitu asam glutamat
dan glisin merupakan dua asam amino lain yang diperlukan untuk sintesisnya.
Glutation penting dalam aktivitas limposit, khususnya sel T dan respons
kekebalan (Combs dan Combs, 1986; Larsen, 1993; Ellis et al., 1997).
Dikemukakan oleh Baumrucker (1985) bahwa glutation darah pertama-
tama dihidrolisis oleh y-glutam il transpeptidase (GTP-ase) ektraseluker pada sel-
sel mem bran kelenjar am bing dan kemudian dihidrolisis lebih jauh menjadi asam-
asam amino bebas oleh peptidase nonspesifik. Tiga komponen asam amino
amino. Glutamat ditransport rnelalui sistem anion, sistin melalui sistem ASC dan
glisin melalui sistem A. Akhirnya ketiga asam amino masuk dalam pool asam
amino dan tersedia untuk sintesis protein susu atau resintesis glutation
intraseluler. Jaringan kelenjar ambing mempunyai konsentrasi glutation 4
-
6mM. Ditambahkan oleh Baumrucker (1985) bahwa darah menggunakan GSH
(reduce GSH) untuk pertahanan dari oksidasi hidrogen peroksida maupun lipid
peroksida atau mempertahankan status redok dari sel darah merah (Carolyn
Berdanier, 1998).
Combs dan Combs (1986) menyatakan bahwa eksresi Se dari tubuh dapat
melalui tiga jalur utama, yaitu : paru-paru, urin dan saluran pencemaan (melalui feses). Mahan dan Parrett (1 996) menyatakan bahwa
urin
merupakan jalur