!
"
Dengan ini saya menyatakan bahwa skripsi Karakterisasi Protein IgG Anti H5NI dari Kolostrum Sapi yang Divaksin H5N1 Menggunakan Metode SDS PAGE adalah karya saya dengan arahan dari komisi pembimbing dan belum diajukan dalam bentuk apapun kepada perguruan tinggi manapun. Sumber informasi yang berasal atau dikutip dari karya yang diterbitkan maupun tidak diterbitkan dari penulis lain telah disebutkan dalam teks dan dicantumkan dalam Daftar Pustaka di bagian akhir skripsi ini.
Bogor, Maret 2011
#
$%&'& () &*&'+,$. ! .
! " #$ # # #%
') -'.)/)and /).& 01&/+)&')
& '( ! # # )
* + , *, + ! ! - # ).
-- -- ) .( $ ( ! # - # # ( /
0 (1/ 0 (1/ 0 (1$ & ( ! ( # $
! ( - # , !$
! # ). #$ & ! #
-) # ( # - # ! - - '
) # ( $ & ! *23+ ( ( #
) ! 4$14 556$74 8 $ & ! # ) !
! ( ( 0 1/ 0 1/ # 0 1 !
$ # ( ) # / ! # ) ! 0 1/
0 1/ # 0 1$ & ! # # ( ( $
/ 23 ( - # 19$:9 8 /
19$:9 8 / 17$ 9 8 # ! ; $ 9 8 $
$%&'& () &*&'+,$. ! . Karakterisasi Protein IgG Anti H5NI Menggunakan Metode SDS PAGE dari Kolostrum Sapi yang Divaksin H5N1 Dibawah bimbingan: ') -'.)/)dan /).& 01&/+)&')2
Penelitian ini bertujuan untuk mengkarakterisasi imunoglobulin gamma (IgG) di dalam kolostrum sapi , (FH) yang telah divaksin virus Avian Influenza subtipe H5N1. Sampel dibagi menjadi tiga sampel yang terdiri dari Kol I Sp4, Kol II Sp4, dan Kol III Sp4. Sampel tersebut akan dibandingkan dengan kontrol IgG. Kontrol IgG merupakan sampel kolostrum yang didapatkan dari sapi FH yang tidak diberikan vaksin subtipe H5N1. Karakterisasi IgG dilakukan dengan menggunakan metode SDS4PAGE. Hasil dari penelitian ini menunjukkan bahwa IgG kontrol mempunyai tiga pita protein dan sampel IgG yang diberi vaksin memiliki 546 pita protein. Berat molekul yang didapatkan berkisar antara 19,49 sampai 228,08 kDa. Terdapat perbedaan berat molekul antara sampel Kol 1 Sp4, Kol II Sp4, Kol III Sp4 dengan kontrol IgG. Didasarkan pada berat molekul juga, terdapat perbedaan antara Kol 1 Sp4, Kol II Sp4, dan Kol III Sp4. Pada hasil penelitian ini juga didapatkan adanya protein yang tidak teridentifikasi pada sampel, hal ini disebabkan sampel kolostrum tidak melalui tahap pemurnian terlebih dahulu. Dari penelitian ini dapat disimpulkan bahwa ukuran berat molekul pada sampel IgG kolostrum yang divaksin adalah 147,37 kDa, 147,37 kDa, 140,57 kDa dan kontrol IgG adalah 161,57 kDa.
© Hak Cipta milik IPB, tahun 2010
Hak Cipta dilindungi Undang4Undang
( ) 8 . ( 8
. ) 8 ) . $ ( . 8 8 ( ( # # 8 /
( / ( 8 . / ( . ( / ( 8 8/
< = # ( ( ) # 8 8 8 (
. ! <
8 # ( ) . 8 ) 8 .
Skripsi
sebagai salah satu syarat untuk memperoleh gelar Sarjana Kedokteran Hewan pada
Fakultas Kedokteran Hewan
Judul Skripsi : Karakterisasi Protein IgG Anti H5N1 Menggunakan Metode SDS4PAGE ( #
# . . #
( ) Dari Kolostrum Sapi yang Divaksin H5N1
Nama Mahasiswa : Komara Dwi Rahardjo
NRP : B04062812
Disetujui,
Pembimbing I Pembimbing II
Dr. Drh. Sri Murtini, M.Si Dr. Drh. Anita Esfandiari, M.Si 19661120 199512 2 001 19621214 198903 2 001
Diketahui
Wakil Dekan Fakultas Kedokteran Hewan
Dr. Nastiti Kusumorini 19621205 198703 2 001
Puji syukur ke hadirat Allah SWT yang telah memberikan segala rahmat
dan nikmat4Nya kepada umatnya. Shalawat dan salam semoga tetap terlimpahkan
kepada Rasulullah SAW beserta keluarga dan sahabat4sahabatnya. Rasa syukur
yang tak terhingga penulis panjatkan kehadirat4Nya atas segala karunianya
sehingga skripsi ini berhasil diselesaikan. Tulisan ini adalah hasil penelitian pada
paruh waktu terakhir masa pendidikan di Fakultas Kedokteran Hewan IPB
Penulis menyadari bahwa dalam penyusunan skripsi ini tidak mungkin
dapat diselesaikan dengan baik tanpa bantuan dan bimbingan dari berbagai pihak.
Oleh karena itu , penulis menyampaikan terima kasih kepada :
Dr. Drh. Sri Murtini, MSi dan Dr. Drh. Anita Esfandiari, MSi selaku
pembimbing skripsi dengan penuh kesabaran telah memberikan arahan,
bimbingan serta evaluasi dalam penyusunan dan penulisan skripsi ini,
Keluarga tercinta yang selalu memberikan do’a, dukungan moril dan
semangat untuk menyelesaikan skripsi ini,
Teman4teman sepenelitian (Fajar, Fitri) atas kerjasama dan kebersamaan
serta pengertiannya yang besar selama ini,
Teman4teman kost Aglonema atas bantuan dan pengertiannya selama ini,
Teman seperjuangan AESCULAPIUS 43 atas dukungan dan semangatnya,
Kepada semua pihak yang tidak dapat penulis sebutkan satu per satu yang
turut membantu dalam penelitian dan penulisan skripsi ini.
Penulis sangat mengharapkan kritik dan saran untuk melengkapi skripsi
ini. Semoga skripsi ini dapat bermanfaat bagi penulis, pembaca maupun pihak4
pihak lain yang berkepentingan. Penulis menyadari masih banyak kekurangan
dalam penulisan skripsi ini, namun penulis berharap tulisan ini dapat memberi
manfaat sebagai sumber informasi untuk kemajuan ilmu pengetahuan.
Bogor, Januari 2011
Penulis dilahirkan di Rancaekek, Bandung. pada tanggal 08 Februari 1989
sebagai anak kedua dari pasangan Adjat Sudradjat dan Yuyun Herawati Spd.
Penulis menempuh pendidikan di TK At4Taqwa, SD N Jelegong tahun
199442000, SMP Al4MA’SOEM 20042003, SMA N I RANCAEKEK dari tahun
200342006. Kemudian diterima di Institut Pertanian Bogor melalui jalur
Undangan Seleksi Masuk IPB (USMI) dan berhasil masuk di Fakultas Kedokteran
"
&3&%&/
" ... viii
" ... ix
2 Latar Belakang ... 1
Tujuan Penelitian ... 4
Manfaat Penelitian... ... 4
2 Virus Avian Influenza ... 5
Patogenitas Avian Influenza ... 6
Sistem Kekebalan ... 6
Kolostrum ... 7
Pengenalan Kolostrum ... 7
Komposisi Kolostrum ... 8
Proses Pembentukan Kolostrum ... 9
Immunoglobulin ... 9
Definisi ... 9
Struktur Imunoglobulin ... 9
Imunoglobulin pada Sapi ... 10
SDS PAGE ... 11
2 Waktu dan Tempat Penelitian ... 14
Bahan dan Alat ... 14
Metode Penelitian ... 14
Vaksinasi Induk Sapi... 14
SDS4PAGE ... 15
2 ... 16
2 ... 20
" ... 21
"
&3&%&/ 1. Wabah H5N1 pada Manusia Tahun 2010 ... 2
2. Berat Molekul Komponen4komponen Protein ... 17
"
&3&%&/
1. Struktur H5N1 ... 5
2. Struktur dasar imunoglobulin ... 10
3. Klasifikasi imunoglobulin ... 11
4. Mekanisme sederhana SDS4Page ... 13
&.&' 43&5&/
Kejadian ) 8 Avian Influenza (AI) tahun 2003 telah dilaporkan terjadi pada suatu populasi ternak unggas di Asia Tenggara dan sekitarnya,
diantaranya negara China, Indonesia, Kamboja, Jepang, Republik Korea Utara,
Laos, Malaysia dan Vietnam (WHO 2010). Asia Tenggara dicermati sebagai asal
terjadinya pandemi berikutnya, mengingat pengelolaan ternaknya yang relatif
masih tradisional (Basuno 2008).
Avian influenza atau flu burung merupakan penyakit pada unggas yang
disebabkan oleh virus > .' - # tipe A, yang menyerang ayam, burung, itik, kalkun, angsa dan jenis unggas lainnya (CDC 2005). Hewan yang peka dan
terdeteksi positif AI di Indonesia meliputi ayam, puyuh, itik, beberapa jenis
burung dan babi (Haryono 2005). Avian Influenza dapat menular ke hewan lain.
Virus ini juga dapat menyerang manusia, bahkan untuk kawasan Asia Tenggara,
Indonesia menduduki peringkat pertama dengan jumlah korban manusia
meninggal dunia terbanyak akibat flu burung (KOMNAS FBPI 2010).
Akibat wabah AI, Indonesia mengalami kerugian ekonomi cukup tinggi,
kerugian tersebut berupa merosotnya permintaan daging ayam sampai 60%,
karena masyarakat takut makan daging ayam. Jumlah peternak yang memiliki
peternakan ayam skala kecil diperkirakan 80.000 orang dengan rata4rata
kepemilikan 5000420.000 ekor. Melalui peternakan tersebut, setiap hari dihasilkan
1,3 juta ton telur dan daging ayam sebanyak 141,2 milyar ekor per tahun
(Wardhani 2007). Kerugian ekonomi yang diderita diperkirakan mencapai 3,244,3
triliun rupiah akibat pemusnahan massal 100 juta ekor, baik yang tertular H5N1
maupun depopulasi untuk pengendalian penyakit (KOMNAS FBPI 2004).
Sampai dengan 31 Agustus 2010 di seluruh dunia terdapat 505 kasus pada
manusia dan 300 kasus diantaranya dilaporkan meninggal (Tabel 1). Indonesia
menduduki peringkat pertama dengan jumlah kasus tertinggi, dilaporkan sebanyak
karena sistem pemeliharaan unggas yang belum tertata (Kompas 2008). Manusia
yang rawan terinfeksi oleh virus AI antara lain pekerja di peternakan ayam atau
unggas domestik lain, Rumah Potong Unggas (RPU), pengangkut (sopir)
distribusi ayam (Rahayu 2010).
Tabel 1. Wabah H5N1 pada manusia tahun 2010
Negara Jumlah
Berdasarkan kasus yang terjadi, maka pemerintah menetapkan sembilan
langkah strategi sebagai tindak penanggulangan pada unggas. Salah satunya
adalah dengan cara pemberian vaksinasi pada unggas. Upaya pencegahan
terhadap manusia dapat dilakukan dengan cara (a) menghindari kontak langsung
dengan unggas yang terinfeksi; (b) menghindari konsumsi daging/ telur yang tidak
dimasak secara sempurna; (c) istirahat, makan dan minum yang cukup, serta olah
raga; (d) bagi penderita flu usahakan menutup mulut jika batuk serta gunakan
masker bila perlu (Winarno 2005).
Organisasi Kesehatan Hewan Dunia atau > #
pengendalian AI ditetapkan oleh masing4masing negara berdasarkan penilaian
terhadap situasi yang terjadi di negara bersangkutan (Naipospos 2006).
Pemerintah telah menetapkan kebijakan pengendalian AI dengan cara
mengizinkan secara resmi peredaran dua jenis vaksin AI untuk unggas produksi
dalam negeri dan enam jenis vaksin impor yang telah dikaji secara teknis
berdasarkan rekomendasi ahli dan telah melalui pengujian oleh lembaga
pemerintah yang mempunyai kompetensi (Naipospos 2006). Namun sampai saat
ini belum dipastikan adanya bentuk imunisasi AI untuk manusia berupa vaksin.
PT. Bio Farma Indonesia siap memproduksi vaksin flu burung atau (AI) untuk
manusia pada 2011 dengan target produksi awal 20 juta dosis. Rencana itu
dilakukan untuk mengantisipasi terjadinya pandemi flu burung (Anonim 2008).
Tizard (1988) menyatakan bahwa ada dua cara imunisasi untuk membuat
individual kebal terhadap penyakit menular, yaitu imunisasi pasif dan aktif. Salah
satu aplikasi imunisasi pasif adalah pemberian kolostrum yang mengandung
antibodi (imunoglobulin) terhadap antigen tertentu.
Sekresi kelenjar ambing menjamin terjadinya transfer imunitas pasif dan
menyediakan pakan untuk anak yang baru lahir. Pemindahan imunoglobulin (pada
sapi) dari darah ke kelenjar ambing terjadi segera sebelum, sewaktu, dan sesudah
partus (Toelihere 1981). Kandungan ) pada perahan pertama
kolostrum biasanya berkisar antara 2% (20 g/L) sampai 15% (150 g/L). kemudian
akan terus menurun konsentrasinya pada pemerahan berikutnya. Pada pemerahan
ketiga konsentrasinya hanya 40% dari pemerahan pertama (Anonim 2011)
Pemberian kolostrum (sebagai imunisasi pasif) pada mahluk hidup (khususnya
neonatus) akan memicu terbentuknya imunitas pasif (IgG) (Toelihere 1981).
Penggunaan kolostrum untuk kepentingan imunisasi pasif dapat
diaplikasikan dalam upaya pengendalian AI. Hal ini disebabkan kolostrum
memiliki unsur kekebalan berupa imunoglobulin. Unsur kekebalan tersebut
berfungsi sebagai sumber pertahanan utama, baik dalam pencegahan maupun
tindakan penanggulangan terhadap adanya paparan antigen seperti virus, bakteri,
dan lain4lain (Thapa 2005).
Efektifitas dan kemampuan netralisasi IgG terhadap virus dipengaruhi oleh
perbedaan susunan protein pada IgG maka kemampuan netralisasi virus akan
berbeda pula (Tizard 2000). Oleh karena itu diperlukan penelitian untuk
mengetahui susunan protein IgG dari kolostrum anti H5N1.
-,-&/
Penelitian ini bertujuan untuk mengetahui karakteristik imunoglobulin anti
H5N1 pada kolostrum sapi.
&/1&&.
Penelitian ini diharapkan dapat memberikan informasi mengenai
)'-0 6)&/ /13-4/7&
- (AI) merupakan virus yang termasuk ke dalam famili > .' - # , memiliki amplop ( - ( ), bersegmen dan memilki
-RNA. Avian influenza dibedakan ke dalam 3 tipe, yaitu tipe A, B,
C. Tipe A merupakan tipe AI yang sangat penting, karena virus ini tersebar luas
dimana4mana dan menginfeksi multi spesies seperti unggas dan manusia.
Sedangkan virus AI tipe B dan C merupakan virus yang patogen pada manusia
dan jarang sekali menginfeksi spesies lain.
Gambar 1. Struktur H5N1 (http://id.wikipedia.org/wiki/Flu_burung)
Virus ini mempunyai bentuk yang pleomorfik, dari bentuk bulat dengan
garis tengah rata4rata 120 nm sampai berbentuk filament, juga memiliki tonjolan
pada selubung viral berupa Hemaglutinin (H) dan Neruroamidase (N) (Gambar 1).
Diperkirakan ada 9 varian H dan 14 varian N. Hemaglutinin berfungsi dalam
perlekatan virus pada sel4sel inang, sedangkan neuroamidase berfungsi dalam
menghancurkan asam neuroaminic yang berperan dalam , pada saat
sel inang akan lisis (CFS & PHISU 2005).
Virus H5N1 memiliki waktu inkubasi berkisar antara 345 hari. Penularan
mamalia. Penularan Flu burung pada unggas terjadi secara cepat dengan resiko
kematian yang cukup tinggi yakni sekitar 80% (KOMNAS FBPI 2010).
&.$ 4/).&0 )'-0 6)&/ /13-4/7&
Infeksi virus Avian Influenza (AI) dimulai ketika virus memasuki sel
inang setelah terjadi penempelan ( 8 - dengan reseptor spesifik pada
permukaan sel inang. Virion akan menyusup ke sitoplasma sel inang dan akan
mengintergrasikan materi genetiknya di dalam inti sel inang. Virus menggunakan
sistem genetik pada DNA ( '. )) #) sel inang untuk bereplikasi membentuk virion4virion baru dan menginfeksi sel iang disekitarnya. H5N1 dapat
bereplikasi di dalam sel nasofaring (Peiris $ 2004), di dalam saluran pencernaan (De jong 2005), serta dapat dideteksi dalam darah, cairan
cerebrospinal, dan tinja pada manusia yang terinfeksi (WHO 2005).
Gejala klinis yang sering ditemukan pada ayam/unggas yang terinfeksi flu
burung, antara lain jenggel dan pial membengkak dengan warna kebiruan,
pendarahan merata pada kaki yang berupa bintik4bintik merah, adanya cairan pada
mata dan hitung, keluar cairan eksudat jernih hingga kental dari rongga mulut,
diare, haus berlebihan, kerabang telur lembek (DEPTAN 2005). Gejala klinis
pada manusia penderita AI antara lain demam, sakit tenggorokan, batuk, keluar
ingus, infeksi mata, nyeri otot, sakit kepala, lemas dan dalam waktu singkat dapat
menjadi lebih berat dengan terjadinya peradangan paru4paru (pneumonia) dan
kematian (Rahayu 2010).
)0.4% 4548&3&/
Sistem kekebalan dibagi menjadi dua, yaitu 2 # # . (HMI)/sistem kekebalan humoral dan 2 # # . (CMI)/sistem
kekebalan seluler. Sistem kekebalan humoral melibatkan peran sel B dan
imunoglobulin yang terdapat dalam serum, sedangkan sistem kekebalan seluler
melibatkan peran sel T (Mayer 2009). Vaksinasi adalah pemberian vaksin ke
dalam tubuh individu untuk memberikan kekebalan terhadap suatu penyakit
(Kreier dan Mortensen 1990). Pemberian vaksin pada prinsipnya dapat mencegah
lebih baik karena tidak menimbulkan resistensi dan tidak meninggalkan residu
pada ternak (Soeripto 2001).
Tizard (1988) menyatakan bahwa ada dua cara imunisasi untuk membuat
hewan kebal terhadap penyakit menular. Cara pertama, disebut imunisasi pasif,
menghasilkan kekebalan sementara dengan cara memindahkan antibodi dari
hewan resisten pada hewan rentan. Antibodi yang dipindahkan secara pasif ini
memberi perlindungan secara cepat, namun demikian cepat dikatabolisasi oleh
tubuh, sehingga perlindungan makin berkurang dan akhirnya hewan yang
diimunisasi menjadi rentan lagi terhadap infeksi ulang. Antibodi pada imunisasi
pasif dihasilkan dari hewan donor melalui imunisasi aktif. Antibodi yang
diperoleh dimurnikan, kemudian diberikan kepada hewan yang masih rentan agar
terbentuk tanggap kebal. Kedua, imunisasi aktif, yaitu teknik imunisasi dengan
pemberian antigen kepada hewan, sehingga terjadi peningkatan tanggap kebal
berperantara antibody oleh hewan itu sendiri. Dibandingkan dengan imunisasi
pasif, imunisasi aktif memiliki perlindungan tubuh yang berlangsung lebih lama.
$3$0.'-%
4/ 4/&3&/ $3$0.'-%
Kolostrum mengandung substansi yang berbentuk seperti susu yang
diproduksi menjelang dan segera setelah proses kelahiran. Kolostrum memililki
konsistensi agak kental dan berwarna kekuningan, kaya akan kandungan protein.
Kolostrum juga merupakan salah satu sumber gizi yang mengandung banyak
lemak, protein, karbohidrat dan beberapa mikronutrient seperti vitamin dan
mineral. Mengandung pula IgA yang berfungsi memberi perlindungan pada
traktus gastrointestinal dari berbagai infeksi pada anak yang baru lahir (Thapa
2005).
$%9$0)0) $3$0.'-%
Menurut Thapa (2005), ada beberapa komponen yang terkandung dalam
1. Unsur kekebalan.
Unsur ini terdiri dari beberapa komponen yakni:
a. Antibodi spesifik, merupakan unsur kekebalan yang didapat dari maternal
antibodi yang telah terpapar antigen,
b. Imunoglobulin, merupakan sumber pertahanan utama, baik dalam
pencegahan maupun penanggulangan pada paparan antigen. Ada 5 tipe
imunoglobulin yaitu IgA, IgD, IgE, IgG dan IgM,
c. ? .( ( # (PRP), berfungsi menstimulasi thymus untuk meregulasi sistem kekebalan dalam tubuh,
d. @ , merupakan protein yang terikat pada unsur besi, berfungsi dalam melawan sel kanker,
$ . 8 dan @. ( 8 $
2. Unsur pertumbuhan
Memiliki fungsi dalam membantu pertumbuhan, regenerasi dan mempercepat
perbaikan pada jaringan dan organ yang mengalami gangguan. Unsur ini
terdiri dari beberapa komponen yakni:
a. EGF ( ( ! , ), berfungsi melindungi bagian permukaan
kulit, juga dalam pengaturan pertumbuhan dan regenerasi sel4sel atau
jaringan yang rusak,
b. & ! , A dan B (TGF A dan B), menstimulasi proliferasi sel pada jaringan ikat dan membantu dalam proses
pembentukan sumsum tulang dan kartilago,
c. - # ! , (PDGF), membantu proses pembelahan sel pada jaringan ikat, otot4otot halus, dan fibroblas. Juga membantu
dalam regenerasi sel neuron,
d. Vitamin dan mineral, merupakan salah satu komponen penting dalam
proses metabolisme, pertumbuhan dan perkembangan tubuh,
'$040 4%84/.-5&/ $3$0.'-% $3$0.'$ 4/40)0
Kolostrogenesis merupakan bagian dari laktogenesis atau pembentukan
susu. Laktogenesis terdiri dari dua tahap yaitu laktogenesis tahap I dan
laktogenesis tahap II. Laktogenesis tahap I ditandai dengan produksi suatu cairan
yang disebut pre4kolostrum. Laktogenesis tahap II dimulai segera sebelum induk
melahirkan, ketika kelenjar ambing pertama kali melepaskan kolostrum sampai
kelenjar ambing menghasilkan susu non4kolostrum. Kolostrogenesis diatur oleh
hormon laktogenik diantaranya adalah estrogen, progesteron, dan prolaktin.
Transfer imunoglobulin dari sirkulasi darah ke kelenjar ambing atau kolostrum
terjadi sebelum, sewaktu dan segera sesudah induk melahirkan (Toelihere 1981).
Selama masa kebuntingan terjadi, proliferasi seluler saluran ambing dan alveoli
berada di bawah pengaruh hormon progesteron dan estrogen yang berasal dari
ovarium dan plasenta (Hidayat $ 2009).
Kolostrogenesis terjadi bersamaan dengan penurunan kadar progesteron
dan estrogen di dalam darah dan peningkatan kadar prolaktin atau hormon
laktogenik dari kelenjar hipofisa. Prolaktin dibutuhkan untuk memulai sekresi
susu dan mempertahankan laktasi. Peningkatan prolaktin didukung oleh stimulasi
kelenjar ambing melalui penghisapan dan pengeluaran kolostrum atau air susu
dari alveoli kelenjar ambing (Hidayat . 2009).
%-/$ 3$8-3)/
Menurut Simorangkir (1995), imunoglobulin (Ig) merupakan suatu fraksi
globulin serum yang berhubungan dengan aktivitas pertahanan tubuh.
Imunoglobulin berperan utama dalam mekanisme kekebalan yang diperantai oleh
antibodi. Mayer (2009) menyatakan bahwa imunoglobulin merupakan molekul
glikoprotein yang diproduksi oleh plasma sel melalui respon yang
memilki fungsi sebagai antibodi.
.'-5.-' %-/$ 3$8-3)/
Struktur imunoglobulin tersusun atas rantai berat/panjang ( -. )
dan rantai ringan/pendek ( ). Semua rantai disatukan oleh ikatan
berfungsi sebagai sum pada sapi terdiri dari :
1.
Imunoglobulin Gai sifat fleksibel dan juga merupakan terbentuknya
odi (Gambar 2) (Mayer 2009).
Gambar 2. Struktur Dasar Imunoglobulin p://pathmicro.med.sc.edu/mayer/IgStruct2000.htm)
imunoglobulin dibagi berdasarkan fungsi dan susuna
yang terbentuk pada regio variabel/konstan. Imuno
ulin G atau Gamma (γ), merupakan Ig dengan jumlah
yang berfungsi dalam menstimulasi fagositosis
in itu juga sebagai komponen utama dalam kolost
490%. Immunoglobulin ini terdiri dari 2 rantai be
ngan L. IgG pada sapi terdiri dari 2 macam sub4kelas y
dengan berat molekul masing4masing sebesar 150 kDa
ulin M atau Mu (L), dihasilkan pada kekebalan primer
ndungan dalam kolostrum sekitar 7%. Terdiri a
pentamer) dengan berat molekul sebesar 900 kDa.
dihubungkan satu sama lain dengan ikatan disulf
domain CH4 menyerupai gelang. Tiap monomer dihubungkan satu dengan
lainnya pada ujung permulaan dan akhirnya oleh protein J yang berfungsi
sebagai kunci (Roitt . 1998).
3. Imunoglobulin A atau Alpha (α), berfungsi dalam mencegah perlekatan
mikroba pada sel4sel epitel. Terdiri dari 2 jenis yaitu IgA dalam serum dan
IgA dalam mukosa. IgA berbentuk dimer yang terdiri dari 2 molekul
monomer, dan sebuah komponen sekretori serta sebuah rantai J dengan
berat molekul sekitar 385 kDa (Roitt . 1998).
4. Imunoglobulin D atau Delta (δ), sebagai reseptor antigen (Tizzard 1988).
Rantai δ mempunyai berat molekul 60.000470.000 dan l2% terdiri dari
karbohidrat. Fungsi utama IgD belum diketahui tetapi merupakan
imunoglobulin permukaan sel limfosit B bersama IgM dan diduga
berperan dalam diferensiasi sel (Roitt $ 1998).
5. Imunoglobulin E atau epsilon (€), bereaksi pada hipersensitifitas,
membantu eosinofil menghancurkan parasit (Decker 2000).
Gambar 3. Klasifikasi Imunoglobulin (Santoso 2010)
Elektroforesis merupakan teknik pemisahan fraksi4fraksi zat berdasarkan
perbedaan ukuran, bentuk, muatan, atau sifat kimia molekul (Handayani 2006).
SDS4PAGE merupakan salah satu teknik elektroforesis yang banyak digunakan
pada bidang biokimia, forensik, genetik dan biologi molekuler untuk memisahkan
protein sesuai dengan kemampuan mobilitas elektroforesis protein tersebut
(Anonim 2010).
# # . (SDS), merupakan sebuah deterjen bermuatan negatif, berfungsi untuk mengikat daerah hidrofobik dari molekul protein,
sehingga menyebabkan molekul protein tersebut membentang dari rantai globular
menjadi rantai polipeptida linier. Cara kerja SDS, yaitu melepaskan masing4
masing molekul protein dari asosiasinya dengan protein lain atau molekul lipid.
Teknik elektroforesis menggunakan bahan SDS ( # # . ) banyak digunakan pada proses pemisahan protein dan asam nukleat. Menurut Rantam
(2003), SDS akan mengikat residu hidrofobik dari bagian belakang peptida secara
komplit, dengan demikian protein SDS4komplek bermigrasi melalui
poliakrilamid, tergantung pada berat molekul.
Selama elektroforesis terjadi di dalam agar, protein dipengaruhi oleh dua
gaya yaitu gaya elektroforetik dan gaya elektroendosmotik. Gaya elektroforetik
disebabkan oleh perbedaan potensial, menyebabkan protein berpindah ke anoda,
sedangkan gaya elektroendosmotik menyebabkan perpindahan protein ke katoda
(Handayani 2006).
. . # , memiliki konsistensi seperti gel (jelly). Dibentuk melalui polimerisasi dari . # dan ) . # . . # ini
berfungsi untuk menahan protein4protein yang memilki molekul besar, sehingga
migrasi dari protein ini akan lambat dan tertahan di daerah atas dari sumur4sumur
elektroforesis. Sedangkan protein bermolekul kecil akan tersaring ke bawah.
Dalam pembentukan ( . . # diperlukan TEMED (Tetraetilendiamin)
sebagai inisiasi terjadinya polimerisasi antara . # dan ) . # (Anonim 2010).
SDS4PAGE banyak digunakan untuk mengetahui tingkat kemurnian suatu
protein, penentuan berat molekul, untuk mengetahui komposisi subunit dari
dapat digunakan untuk pembelajaran pada bidang spektrometri dan proteomic
(Anonim 2010).
Terdapat dua wilayah pada gel SDS4PAGE, bagian wilayah atas adalah
8 (gel pengumpul) dimana protein akan ditekan ke bawah menuju lapisan tipis melalui arah migrasi katoda ke anoda. Hal ini terjadi karena 8
mengandung ion Cl4 (klorin) yang memiliki kecepatan migrasi lebih cepat dibandingkan migrasi protein sampel, juga adanya ion . dari larutan buffer yang memilki kecepatan lebih lambat, sehingga molekul protein akan
terperangkap diantara dua ion tersebut. Selanjutnya molekul protein masuk ke
wilayah bawah atau - , dimana gel ini memiliki pori4pori yang lebih kecil dibandingkan 8 dikarenakan memilki pH yang lebih tinggi dan konsentrasi garam yang tinggi. Pada wilayah ini, ion . akan diionisasi oleh gradient voltase yang dialiri ke dalam gel, sehingga menyebabkan molekul4
molekul protein terpisah tergantung pada ukuran dan berat molekul (Promega
Corp 2011). Mekanisme sederhana dapat dilihat pada Gambar 4.
&5.- +&/ 4%9&. 4/43).)&/
Penelitian dilaksanakan pada bulan Maret 2009 4 Juli 2009. Penelitian
dilakukan di Laboratorium Terpadu, Departemen Ilmu Penyakit Hewan dan
Kesehatan Masyarakat Veteriner Fakultas Kedokteran Institut Pertanian Bogor.
&*&/ +&/ 3&.
Alat yang digunakan pada penelitian diantaranya, lempeng kaca,
seperangkat alat elektroforesis, tabung reaksi. Sedangkan bahan yang digunakan
pada penelitian terdiri dari sampel kolostrum, reagen SDS PAGE yang terdiri dari
: Acrylamide Bis (30% T, 2,67% C), 1,5 M Tris HCl pH 8,8, 0,5 M Tris4HCl pH
6,8, 10 % (w/v) SDS, 10 % (w/v) Ammonium persulfate, Sampel Buffer, 5 x
running buffer (1x = 25 mM Tris, 192 mM glycine, 0,1% SDS pH 8,3), larutan
, larutan pemucat, larutan buffer.
Sampel yang digunakan pada penelitian ini adalah kolostrum yang berasal
dari satu ekor induk sapi , (FH) yang telah divaksin AI H5N1. Sampel kolostrum kemudian disimpan di dalam dengan suhu 420oC, dan pada saat akan dianalisis sampel kolostrum beku di4 ! kemudian dihomogenkan. Sampel kolostrum yang diuji telah mengandung antibodi anti
H5N1, berdasarkan pengujian sebelumnya. Sampel pada penelitian terdiri atas
tiga sampel. Perbedaan pada tiap sampel adalah pada saat waktu pemerahan
dengan rentang perbedaan waktu 12 jam untuk setiap sampel.
4.$+4 4/43).)&/
&50)/&0) /+-5 &9)
Sebelum pemberian vaksin, dilakukan pemberian imunomodulator
(INMUNAIR®) dosis 1 mg/kg BB per oral selama 3 hari berturut4turut. Vaksinasi
menggunakan antigen AI H5N1 inaktif (Vaksindo 2003) tanpa adjuvan dengan
hari keempat diberi vaksin inaktif H5N1(Vaksindo 2003) beradjuvan dengan
dosis 1 ml/ekor secara ) (SC) sebanyak 3 kali dengan interval waktu masing4masing 14 hari. Kolostrum diambil sesegera mungkin setelah induk sapi
melahirkan (sekitar satu jam setalah melahirkan). Metode ini telah dilakukan pada
penelitian sebelumnya (Kusumawardhani 2008).
Bahan yang digunakan terdiri dari gel pemisah dengan konsentrasi 12 %,
gel pengumpul 4%, running buffer, sampel buffer, larutan pewarna Commasie
Blue dan larutan pemucat.
Pembuatan agar akrilamid dilakukan dengan bantuan dua lempeng kaca
yang berukuran 18 x 15,5 cm yang telah dibersihkan denga alkohol 70%, pada
kedua sisi tepi bagian dalam diberi spacer, kedua lempeng kaca dihimpitkan dan
selanjutnya dijepit. Dibagian atas lempeng kaca disisipkan sisir pembuat jalur dan
kemudian diisi dengan gel pengumpul (4% poliakrilamid) hingga mencapai
permukaan lempeng kaca.
Sampel dilarutkan dengan larutan buffer sampel perbandingan 1:1 dan
campuran ini kemudian ditangas 60oC selama 5 menit sebelum dimasukkan kedalam sumur gel elektroforesis. Sebanyak 10 ul sampel dimasukkan kedalam
masing4masing sumur, kemudian perangkat elektroforesis dijalankan dengan arus
50 mA dengan voltase 100 V selama ± 3 jam. Elektroforesis berakhir apabila
pewarna sampel mencapai batas 0,5 cm dari bagian bawah gel. Setelah
elektroforesis berakhir, gel diangkat dari lempeng kaca dan direndam dalam
pewarnaan Commasie Briliant Blue selama 3 jam pada suhu ruang sambil
diagitasi perlahan. Pewarna yang tidak terikat pada protein dihilangkan dengan
merendam gel pada larutan pemucat methanol dan asam asetat sehingga gel
berwarna bening atau pita4pita protein telah terbentuk terlihat jelas. Mobilitas
relatif protein dihitung dengan cara membandingkan jarak migrasi protein pada
Penelitian ini mempelajari karakter protein IgG dari kolostrum sapi yang
divaksin dengan vaksin AI H5N1. Standar yang digunakan sebagai pembanding
pada penghitungan ukuran molekul IgG adalah ) # 8 . Marker protein ini terdiri dari delapan pita protein standar, yaitu 25 kDa, 35 kDa, 50 kDa,
75 kDa, 100 kDa, 150 kDa, 175 kDa, dan 225 kDa. IgG kontrol yang digunakan
adalah IgG kolostrum pada induk sapi bunting yang tidak diberikan vaksin anti
H5N1
Berat molekul pada tiap sampel dihitung menggunakan cara penghitungan
ukuran molekul yang didasarkan pada rumus regresi marker dan penghitungan
mobilitas relatif. Penghitungan mobilitas relatif didapatkan dengan menggunakan
rumus :
Mobilitas Relatif Jarak migrasi dari awal resolving gel sampai !" Jarak pergerakan !"
Data yang diperoleh dibuat regresi linier hubungan antara mobilitas relatif
(sumbu x) dengan nilai logaritma berat molekul pita protein marker (sumbu y).
Persamaan regresi linier ini dipakai sebagai persamaan standar untuk menghitung
ukuran molekul protein sampel berdasarkan nilai mobilitas relatifnya. Persamaan
regresi yang diperoleh dari data mobilitas relatif marker adalah y = 41.188x +
2.418. Ukuran molekul protein sampel yang diperoleh dengan menggunakan
persamaan tersebut dapat dilihat pada Tabel 2.
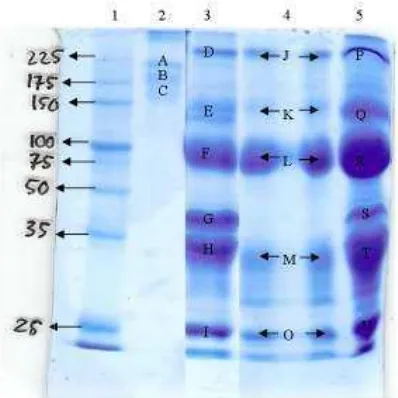
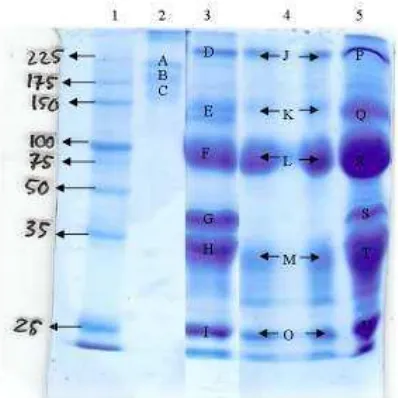
Imunoglobulin kontrol memiliki tiga pita protein sedangkan pita protein
IgG kolostrum sampel memiliki 546 pita protein, hal ini disebabkan karena sampel
IgG kolostrum yang digunakan tidak melalui tahap pemurnian terlebih dahulu,
sehingga terdapat beberapa protein yang belum diketahui identitasnya.
Berdasarkan hasil penelitian Hansen et. al (1949), terdapat beberapa protein
Tabel 2 Berat molekul komponen4komponen protein dari masing4masing pita penyusunnya.
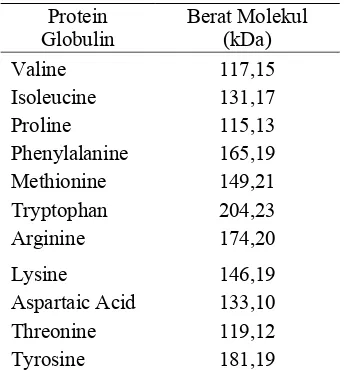
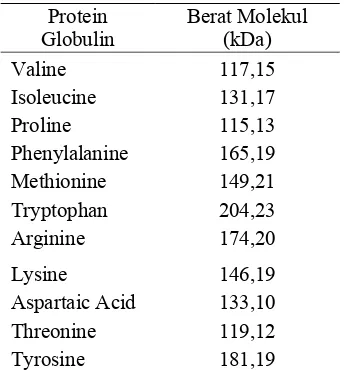
Tabel 3. Protein globulin pada kolostrum sapi
Protein
Sampel Pita yang Berat Molekul Pita Perkiraan/Dugaan
Hasil pengujian
didapatkan adanya 546 pi
19,49 sampai 228,09
Memiliki 3 susunan pita
161,57 kDa. Menurut Tiz
Da. Pada pita C dengan b
Gambar 5. Profil p Blue. Ke Kol III Sp
Molekul IgG yang
memecah ikatan disulfida
empat rantai polipeptida
masing mempunyai berat
T, U. Pita Q dengan berat
ujian kolostrum sapi yang mengandung IgG ant
6 pita protein. Berat molekul protein tersebut berkis
kDa (Gambar 5 dan Tabel 2). Imunoglobulin
n pita protein dengan ukuran 203,32 kDa, 185,46
nurut Tizard (1988), berat molekul IgG antara 150.000
ngan berat molekul 161,57 (Tabel 2) diduga sebagai IgG
pita protein hasil SDS4PAGE dengan pewarnaan C e. Ket: 1: Marker, 2: IgG kontrol, 3: Kol II Sp4, 4: Kol
Sp4.
yang diberi perlakuan dengan bahan kimia (SDS)
sulfida akan menyebabkan molekul IgG akan terurai
ptida yang terpisah. Dua diantaranya “berat” karena
i berat molekul sekitar 50 kDa dan dua rantai lainnya
ing mempunyai berat molekul sekitar 25 kDa (Tizard
da sampel Kol II Sp4 terdiri atas 6 pita protein, yaitu p
dengan berat molekul 147,37 kDa, diduga sebagai IgG
54,85 kDa diduga sebagai -. . Pita I deng
diduga sebagai . Protein pada sampel K
in, yaitu pita J, K, L, M, O. Pita K dengan berat mol
IgG. Pita O dengan berat molekul 19,49 kDa didug
n pada sampel Kol III Sp4 terdiri dari 6 protein, yaitu P
n berat molekul 140,75 kDa diduga sebagai IgG. Pita
berat molekul 56,12 kDa diduga sebagai -. . Pita U dengan berat
molekul 21,87 kDa diduga sebagai .
Teknik elektroforesis menggunakan bahan SDS ( # # . ) banyak digunakan pada proses pemisahan protein dan asam nukleat. Metode SDS4
PAGE memilki kelebihan yaitu mekanismenya dalam mengklasifikasi suatu
protein berdasarkan berat molekul dari bahan yang digunakan. Menurut Rantam
(2003), SDS akan mengikat residu hidrofobik dari bagian belakang peptida secara
komplit, dengan demikian protein SDS4komplek bermigrasi melalui
poliakrilamid, tergantung pada berat molekul.
. . # ( (PAGE), merupakan metode standar pengujian terhadap berat molekul protein, struktur subunit dan kemurnian protein
(Rantam 2003). Penggunaan poliakrilamid sebesar 12%, dimaksudkan agar
mobilitas protein yang diperoleh cukup besar serta berat molekul yang tinggi
dapat dipisahkan. Poliakrilamid adalah matrik pilihan untuk memisahkan protein
yang mempunyai berat molekul antara 5004250.000 Dalton (Natih $ . 2010). Protein sampel yang dimasukkan pada gel elektroforesis akan dipecah menjadi
rantai polipeptida linear yang seragam (bermuatan negatif), dan akan dipisahkan
oleh gel tersebut berdasarkan ukuran berat molekulnya. Ukuran berat molekul
yang lebih besar akan tertahan pada bagian atas gel, sedangkan ukuran berat
molekul yang kecil akan kebawah gel. Pita protein yang terbentuk dari hasil
elektroforesis akan menunjukkan karakteristik dari polipeptida penyusun IgG
tersebut.
Mekanisme penentuan berat molekul diawali dengan memasukkan
imunoglobulin yang telah diperoleh ke dalam sumur gel yang terdapat pada
bagian paling atas, gel tersebut adalah buffer gel pengumpul dengan pori yang
lebih besar dibandingkan dengan gel bagian bawah ( - ). Pori4pori pada
matrik dibentuk oleh rantai 8 ( . # dan
) . # . Ukuran pori4pori berkurang sesuai dengan peningkatan total persentasi . # atau terjadi peningkatan derajat persentasi konsentrasi campuran ) . # .
Melalui pembuatan atau pemilihan konsentrasi total yang tepat, maka
menghalangi pergerakan protein ke dalam gel. Demikian halnya jika terlalu
rendah total persentasi, maka akan mengakibatkan pergerakan protein menjadi
terlalu cepat, sehingga protein spesifik menjadi rendah dan tidak sesuai dengan
.
)%9-3&/
Berdasarkan hasil penelitian yang dilakukan terdapat perbedaan susunan
pita protein sampel Kol I Sp4, Kol II Sp4, dan Kol III Sp4 dengan IgG kontrol,
dilihat dari berat molekul pada tiap4tiap sampel. Berdasarkan berat molekul,
susunan pita protein Kol I Sp4 berbeda dengan Kol II Sp4 maupun Kol III Sp4.
Ukuran IgG kolostrum kontrol sebesar 161,57 kDa dan ukuran IgG sampel
masing4masing sebesar 147,37 kDa, 147,37 kDa, dan 140,75 kDa.
&'&/
Perlu dilakukan pemurnian IgG kolostrum terlebih dahulu, sehingga berat
molekul yang didapatkan tidak terdapat protein kontaminan dan tepat sesuai
"
Anonim. 2008. 57 / , # 8 " 8 8 2 . Kompas 2008. [21 Juli 2010]
Anonim 2010. . http://en.wikipedia.org/wiki/SDS4PAGE [terhubung berkala] [21 Juli 2010]
Anonim. 2011. *0 +. http://budaxperah.wordpress.com/ 2009/04/23/colostrum4kolostrum/ [terhubung berkala] [08 Maret 2011]
Basuno E. 2008. ? - ! ( 8 3 ) # 0 ) < 8 # -# # . Dalam Analisis Kebijakan Pertanian, Volume 6 No 4: 3144334. Bogor: Pusat Analisis Sosial Ekonomi dan Kebijakan Pertanian.
[CFS & PHISU] Center for Food Security and Public Health Iowa State University. 2005. " . U.S.A.
[CDC] Center for Disease Control 2005. Influenza Viruses. http://www.cdc.gov/flu/avian/gen4info/flu4viruses.htm [terhubung berkala] [28 Juli 2010]
Decker JM. 2000. # .. Oxford : Blackwell Science.
De jong MD, Cam BV, Qui PT. Fatal Avian influenza A (H5N1) in a child presenting ith diarrhea followed by coma. A 2 # 2005;352:6864 691.
DEPTAN. 2005. Arah Kebijakan Pemerintah Pusat dalam Program Penanggulangan Wabah AI di Indonesia. [terhubung berkala] [8 Maret 2011].
Handayani D.T. 2008. Karakterisasi Protein Imunoglobulin Y (IgY) Kuning Telur H5N1 H5N2 H5N9 Menggunakan Metode # # . (
. . # ( (SDS4PAGE) [Skripsi]. Bogor :
Fakultas Kedokteran Hewan, Institut Pertanian Bogor.
Hansen . 1949. # , - $Department of
Biochemistry, University of Winsconsin, Madison
Haryono. 2005. - # 0 # & 8 , Seminar
AI 2005.
Hidayat, Effendi P, Asep AA. 2009. 8 < 8 8 8 8 (
2 < 0 ) 5 *
Kusumawardhani SW. 2008. Deteksi Keberadaan Antibodi Anti H5N1 Menggunakan Metode Hemaglutinasi Inhibisi (HI) pada Kolostrum Sapi yang Divaksin H5N1. [skripsi]. Bogor. Program Sarjana Kedokteran Hewan, Institut Pertanian Bogor. Penginduksi Antibodi Spesifik Terhadap Virus Avian Influenza H5N1 Strain Legok. A " Vol 11 No.2 : 994106
Peiris JS, Yu WC, Leung CW, . Re4emergence of fatal human influenza A subtype H5N1 disease. @ 2004; 363: 6174619.
Promega Corp. 2011. ! # 8 #
B. http://www.promega.com/enotes/faqspeak/0507/fq0043.htm [terhubung berkala] [11 Januari 2011]
Rahayu 2010. . 8 " * # '+. Fakultas Pertanian Peternakan. Universitas Muhammadiyah Malang.
Rantam FA. 2003. 2 # . Airlangga University Press : Surabaya.
Roitt IM, Brostoff J, Male DK. 1998. & .$ ( C # .. 5th Ed. Dalam Essensial Imunology. London: Blackwell hlm 15430.
Simorangkir M. 1995. Isolasi dan Identifikasi Imunoglobulin Gama (IgG) Serum Ayam Buras dan Ayam Ras dengan Metode Kromatografi Pertukaran Ion dan Imunokimia [Tesis]. Sekolah Pascasarjana. Institut Pertanian Bogor.
Soeripto. 2001. Vaksin Bakteri untuk Ternak. - # 76:: Hlm 40441.
Tizard. 1988. " . Edisi II. Partodiredjo, M. penerjemah. Surabaya: Airlangga University Press. Terjemahan dari Introduction to Veterinary Immunology
Tizard 2000. " . . % # . W.B. Saunders
Toelihere MR. 1981. 0 ) # ( # & 8 ( # 0 ) . Jakarta: Universitas Indonesia Press.
Wardhani LK. 2007. , % ( 8 B. PDHI: Koran PDHI Cabang Jawa Timur.
Winarno 2005. 2 ( . 8 , .
[WHO] World Health Organization$ 3 > . %
D % 2 / (( / ; 9 2 . " $ / $5,
Agustus2005.http://www.who.int/csr/resources/publications/influenza/WH O. [terhubung berkala] [23 Juli 2010]
[WHO] World Health Organization. 2010 - ) #
- D* + ? ( # 3 >
LAMPIRAN 1
4'0)&9&/ 4& 4/
A. Acrylamide Bis (30% T, 2,67% C)
Acrylamide (146 gr), NN Methylene4bis4acrylamide (4 gr). Larutkan
dalam akuabides sampai volume 500 ml, simpan pada suhu 4oC dalam wadah gelap. Masa pakai 30 hari.
B. 1,5 M Tris HCl pH 8,8
Tris base (54,25 gr), larutkan dalam akuabides sampai 150 ml, buat
sampai pH 8,8 dengan HCl kemudian tambahkan akuabides sampai
volume 300 ml.
C. 0,5 M Tris4HCl pH 6,8
Tris base (6 gr), larutkan dalam akuabides sampai 60 ml, buat sampai
6,8 dengan HCl kemudian tambahkan akuabides sampai volume 100 ml.
D. 10 % (w/v) SDS
Larutkan 10 gr SDS dalam 60 ml akuabides dengan stirrer, kemudian
tambahkan akuabides sampai volume 100 ml.
E. 10 % (w/v) Ammonium persulfate
Larutkan 10 gr ammonium persulfate dalam 100 ml akuabides
F. Sampel Buffer
Akuabides (3 ml), 0,5 M Tris4HCl pH 6,8 (1 ml), Glycerol (1,6 ml), 10
% SDS (1,6 ml), Beta4 merkaptoetanol (0,4 ml), 0,5 % (w/v)
bromophenol (dalam akuades (0,4 ml)). Dilute sampel dengan
perbandingan 1:4 panaskan pada suhu 950C selama 4 menit. Catt: sampel buffer dapat diganti dengan buffer komersil.
G. 5 x running buffer (1x = 25 mM Tris, 192 mM glycine, 0,1% SDS pH
8,3)
Tris base (45 gr), glycine (216 gr), SDS (15 gr), larutka dalam 3 liter
4'0)&9&/ 43
Digunakan konsentrasi gel pengumpul 4 % dan gel pemisah 12 %
Bahan4bahan yang digunakan Gel Pemisah Gel Pengumpul (375 M Tris, pH 8,8) (125 M Tris, pH 6,8)
Monomer Concentration
12% 4%
(%T, 2,67% C)
Acrylamide/Bis (30% T, 2,67%
C) 2,4 ml 260 ul
Akuabides 2 ml 1,22 ml
1,5 M Tris HCl pH 8,8 1,5 ml 4
0,5 M Tris HCl pH 6,8 4 0,5 ml
10% (w/v) SDS 60 ul 20 ul
10% (w/v) Ammonium persulfate 30 ul 10 ul
TEMED 3 ul 2 ul
4'0)&9&/ 94(&'/&&/
Gel SDS dapat diwarnai dengan metode pewarnaan dengan Commasie
Blue atau Silver Staining. Dalam penelitian ini akan digunakan pewarnaan
Commasie Blue.
Larutan Commasie blue
Larutkan 0,25 gr commasie brilliant blue dalam 125 ml methanol, 25 ml
asam asetat glacial, dan 100 ml akuabides.
Larutan Pemucat.
Homogenkan 100 ml methanol, 100 ml asam asetat glacial, dan 800 ml
LAMPIRAN 2
Penghitungan Persamaan Regresi Linear Protein Marker dengan Menggunakan Kurva Standar.
!
#
$%&'& () &*&'+,$. ! .
! " #$ # # #%
') -'.)/)and /).& 01&/+)&')
& '( ! # # )
* + , *, + ! ! - # ).
-- -- ) .( $ ( ! # - # # ( /
0 (1/ 0 (1/ 0 (1$ & ( ! ( # $
! ( - # , !$
! # ). #$ & ! #
-) # ( # - # ! - - '
) # ( $ & ! *23+ ( ( #
) ! 4$14 556$74 8 $ & ! # ) !
! ( ( 0 1/ 0 1/ # 0 1 !
$ # ( ) # / ! # ) ! 0 1/
0 1/ # 0 1$ & ! # # ( ( $
/ 23 ( - # 19$:9 8 /
19$:9 8 / 17$ 9 8 # ! ; $ 9 8 $
$%&'& () &*&'+,$. ! . Karakterisasi Protein IgG Anti H5NI Menggunakan Metode SDS PAGE dari Kolostrum Sapi yang Divaksin H5N1 Dibawah bimbingan: ') -'.)/)dan /).& 01&/+)&')2
Penelitian ini bertujuan untuk mengkarakterisasi imunoglobulin gamma (IgG) di dalam kolostrum sapi , (FH) yang telah divaksin virus Avian Influenza subtipe H5N1. Sampel dibagi menjadi tiga sampel yang terdiri dari Kol I Sp4, Kol II Sp4, dan Kol III Sp4. Sampel tersebut akan dibandingkan dengan kontrol IgG. Kontrol IgG merupakan sampel kolostrum yang didapatkan dari sapi FH yang tidak diberikan vaksin subtipe H5N1. Karakterisasi IgG dilakukan dengan menggunakan metode SDS4PAGE. Hasil dari penelitian ini menunjukkan bahwa IgG kontrol mempunyai tiga pita protein dan sampel IgG yang diberi vaksin memiliki 546 pita protein. Berat molekul yang didapatkan berkisar antara 19,49 sampai 228,08 kDa. Terdapat perbedaan berat molekul antara sampel Kol 1 Sp4, Kol II Sp4, Kol III Sp4 dengan kontrol IgG. Didasarkan pada berat molekul juga, terdapat perbedaan antara Kol 1 Sp4, Kol II Sp4, dan Kol III Sp4. Pada hasil penelitian ini juga didapatkan adanya protein yang tidak teridentifikasi pada sampel, hal ini disebabkan sampel kolostrum tidak melalui tahap pemurnian terlebih dahulu. Dari penelitian ini dapat disimpulkan bahwa ukuran berat molekul pada sampel IgG kolostrum yang divaksin adalah 147,37 kDa, 147,37 kDa, 140,57 kDa dan kontrol IgG adalah 161,57 kDa.
&.&' 43&5&/
Kejadian ) 8 Avian Influenza (AI) tahun 2003 telah dilaporkan terjadi pada suatu populasi ternak unggas di Asia Tenggara dan sekitarnya,
diantaranya negara China, Indonesia, Kamboja, Jepang, Republik Korea Utara,
Laos, Malaysia dan Vietnam (WHO 2010). Asia Tenggara dicermati sebagai asal
terjadinya pandemi berikutnya, mengingat pengelolaan ternaknya yang relatif
masih tradisional (Basuno 2008).
Avian influenza atau flu burung merupakan penyakit pada unggas yang
disebabkan oleh virus > .' - # tipe A, yang menyerang ayam, burung, itik, kalkun, angsa dan jenis unggas lainnya (CDC 2005). Hewan yang peka dan
terdeteksi positif AI di Indonesia meliputi ayam, puyuh, itik, beberapa jenis
burung dan babi (Haryono 2005). Avian Influenza dapat menular ke hewan lain.
Virus ini juga dapat menyerang manusia, bahkan untuk kawasan Asia Tenggara,
Indonesia menduduki peringkat pertama dengan jumlah korban manusia
meninggal dunia terbanyak akibat flu burung (KOMNAS FBPI 2010).
Akibat wabah AI, Indonesia mengalami kerugian ekonomi cukup tinggi,
kerugian tersebut berupa merosotnya permintaan daging ayam sampai 60%,
karena masyarakat takut makan daging ayam. Jumlah peternak yang memiliki
peternakan ayam skala kecil diperkirakan 80.000 orang dengan rata4rata
kepemilikan 5000420.000 ekor. Melalui peternakan tersebut, setiap hari dihasilkan
1,3 juta ton telur dan daging ayam sebanyak 141,2 milyar ekor per tahun
(Wardhani 2007). Kerugian ekonomi yang diderita diperkirakan mencapai 3,244,3
triliun rupiah akibat pemusnahan massal 100 juta ekor, baik yang tertular H5N1
maupun depopulasi untuk pengendalian penyakit (KOMNAS FBPI 2004).
Sampai dengan 31 Agustus 2010 di seluruh dunia terdapat 505 kasus pada
manusia dan 300 kasus diantaranya dilaporkan meninggal (Tabel 1). Indonesia
menduduki peringkat pertama dengan jumlah kasus tertinggi, dilaporkan sebanyak
karena sistem pemeliharaan unggas yang belum tertata (Kompas 2008). Manusia
yang rawan terinfeksi oleh virus AI antara lain pekerja di peternakan ayam atau
unggas domestik lain, Rumah Potong Unggas (RPU), pengangkut (sopir)
distribusi ayam (Rahayu 2010).
Tabel 1. Wabah H5N1 pada manusia tahun 2010
Negara Jumlah
Berdasarkan kasus yang terjadi, maka pemerintah menetapkan sembilan
langkah strategi sebagai tindak penanggulangan pada unggas. Salah satunya
adalah dengan cara pemberian vaksinasi pada unggas. Upaya pencegahan
terhadap manusia dapat dilakukan dengan cara (a) menghindari kontak langsung
dengan unggas yang terinfeksi; (b) menghindari konsumsi daging/ telur yang tidak
dimasak secara sempurna; (c) istirahat, makan dan minum yang cukup, serta olah
raga; (d) bagi penderita flu usahakan menutup mulut jika batuk serta gunakan
masker bila perlu (Winarno 2005).
Organisasi Kesehatan Hewan Dunia atau > #
pengendalian AI ditetapkan oleh masing4masing negara berdasarkan penilaian
terhadap situasi yang terjadi di negara bersangkutan (Naipospos 2006).
Pemerintah telah menetapkan kebijakan pengendalian AI dengan cara
mengizinkan secara resmi peredaran dua jenis vaksin AI untuk unggas produksi
dalam negeri dan enam jenis vaksin impor yang telah dikaji secara teknis
berdasarkan rekomendasi ahli dan telah melalui pengujian oleh lembaga
pemerintah yang mempunyai kompetensi (Naipospos 2006). Namun sampai saat
ini belum dipastikan adanya bentuk imunisasi AI untuk manusia berupa vaksin.
PT. Bio Farma Indonesia siap memproduksi vaksin flu burung atau (AI) untuk
manusia pada 2011 dengan target produksi awal 20 juta dosis. Rencana itu
dilakukan untuk mengantisipasi terjadinya pandemi flu burung (Anonim 2008).
Tizard (1988) menyatakan bahwa ada dua cara imunisasi untuk membuat
individual kebal terhadap penyakit menular, yaitu imunisasi pasif dan aktif. Salah
satu aplikasi imunisasi pasif adalah pemberian kolostrum yang mengandung
antibodi (imunoglobulin) terhadap antigen tertentu.
Sekresi kelenjar ambing menjamin terjadinya transfer imunitas pasif dan
menyediakan pakan untuk anak yang baru lahir. Pemindahan imunoglobulin (pada
sapi) dari darah ke kelenjar ambing terjadi segera sebelum, sewaktu, dan sesudah
partus (Toelihere 1981). Kandungan ) pada perahan pertama
kolostrum biasanya berkisar antara 2% (20 g/L) sampai 15% (150 g/L). kemudian
akan terus menurun konsentrasinya pada pemerahan berikutnya. Pada pemerahan
ketiga konsentrasinya hanya 40% dari pemerahan pertama (Anonim 2011)
Pemberian kolostrum (sebagai imunisasi pasif) pada mahluk hidup (khususnya
neonatus) akan memicu terbentuknya imunitas pasif (IgG) (Toelihere 1981).
Penggunaan kolostrum untuk kepentingan imunisasi pasif dapat
diaplikasikan dalam upaya pengendalian AI. Hal ini disebabkan kolostrum
memiliki unsur kekebalan berupa imunoglobulin. Unsur kekebalan tersebut
berfungsi sebagai sumber pertahanan utama, baik dalam pencegahan maupun
tindakan penanggulangan terhadap adanya paparan antigen seperti virus, bakteri,
dan lain4lain (Thapa 2005).
Efektifitas dan kemampuan netralisasi IgG terhadap virus dipengaruhi oleh
perbedaan susunan protein pada IgG maka kemampuan netralisasi virus akan
berbeda pula (Tizard 2000). Oleh karena itu diperlukan penelitian untuk
mengetahui susunan protein IgG dari kolostrum anti H5N1.
-,-&/
Penelitian ini bertujuan untuk mengetahui karakteristik imunoglobulin anti
H5N1 pada kolostrum sapi.
&/1&&.
Penelitian ini diharapkan dapat memberikan informasi mengenai
)'-0 6)&/ /13-4/7&
- (AI) merupakan virus yang termasuk ke dalam famili > .' - # , memiliki amplop ( - ( ), bersegmen dan memilki
-RNA. Avian influenza dibedakan ke dalam 3 tipe, yaitu tipe A, B,
C. Tipe A merupakan tipe AI yang sangat penting, karena virus ini tersebar luas
dimana4mana dan menginfeksi multi spesies seperti unggas dan manusia.
Sedangkan virus AI tipe B dan C merupakan virus yang patogen pada manusia
dan jarang sekali menginfeksi spesies lain.
Gambar 1. Struktur H5N1 (http://id.wikipedia.org/wiki/Flu_burung)
Virus ini mempunyai bentuk yang pleomorfik, dari bentuk bulat dengan
garis tengah rata4rata 120 nm sampai berbentuk filament, juga memiliki tonjolan
pada selubung viral berupa Hemaglutinin (H) dan Neruroamidase (N) (Gambar 1).
Diperkirakan ada 9 varian H dan 14 varian N. Hemaglutinin berfungsi dalam
perlekatan virus pada sel4sel inang, sedangkan neuroamidase berfungsi dalam
menghancurkan asam neuroaminic yang berperan dalam , pada saat
sel inang akan lisis (CFS & PHISU 2005).
Virus H5N1 memiliki waktu inkubasi berkisar antara 345 hari. Penularan
mamalia. Penularan Flu burung pada unggas terjadi secara cepat dengan resiko
kematian yang cukup tinggi yakni sekitar 80% (KOMNAS FBPI 2010).
&.$ 4/).&0 )'-0 6)&/ /13-4/7&
Infeksi virus Avian Influenza (AI) dimulai ketika virus memasuki sel
inang setelah terjadi penempelan ( 8 - dengan reseptor spesifik pada
permukaan sel inang. Virion akan menyusup ke sitoplasma sel inang dan akan
mengintergrasikan materi genetiknya di dalam inti sel inang. Virus menggunakan
sistem genetik pada DNA ( '. )) #) sel inang untuk bereplikasi membentuk virion4virion baru dan menginfeksi sel iang disekitarnya. H5N1 dapat
bereplikasi di dalam sel nasofaring (Peiris $ 2004), di dalam saluran pencernaan (De jong 2005), serta dapat dideteksi dalam darah, cairan
cerebrospinal, dan tinja pada manusia yang terinfeksi (WHO 2005).
Gejala klinis yang sering ditemukan pada ayam/unggas yang terinfeksi flu
burung, antara lain jenggel dan pial membengkak dengan warna kebiruan,
pendarahan merata pada kaki yang berupa bintik4bintik merah, adanya cairan pada
mata dan hitung, keluar cairan eksudat jernih hingga kental dari rongga mulut,
diare, haus berlebihan, kerabang telur lembek (DEPTAN 2005). Gejala klinis
pada manusia penderita AI antara lain demam, sakit tenggorokan, batuk, keluar
ingus, infeksi mata, nyeri otot, sakit kepala, lemas dan dalam waktu singkat dapat
menjadi lebih berat dengan terjadinya peradangan paru4paru (pneumonia) dan
kematian (Rahayu 2010).
)0.4% 4548&3&/
Sistem kekebalan dibagi menjadi dua, yaitu 2 # # . (HMI)/sistem kekebalan humoral dan 2 # # . (CMI)/sistem
kekebalan seluler. Sistem kekebalan humoral melibatkan peran sel B dan
imunoglobulin yang terdapat dalam serum, sedangkan sistem kekebalan seluler
melibatkan peran sel T (Mayer 2009). Vaksinasi adalah pemberian vaksin ke
dalam tubuh individu untuk memberikan kekebalan terhadap suatu penyakit
(Kreier dan Mortensen 1990). Pemberian vaksin pada prinsipnya dapat mencegah
lebih baik karena tidak menimbulkan resistensi dan tidak meninggalkan residu
pada ternak (Soeripto 2001).
Tizard (1988) menyatakan bahwa ada dua cara imunisasi untuk membuat
hewan kebal terhadap penyakit menular. Cara pertama, disebut imunisasi pasif,
menghasilkan kekebalan sementara dengan cara memindahkan antibodi dari
hewan resisten pada hewan rentan. Antibodi yang dipindahkan secara pasif ini
memberi perlindungan secara cepat, namun demikian cepat dikatabolisasi oleh
tubuh, sehingga perlindungan makin berkurang dan akhirnya hewan yang
diimunisasi menjadi rentan lagi terhadap infeksi ulang. Antibodi pada imunisasi
pasif dihasilkan dari hewan donor melalui imunisasi aktif. Antibodi yang
diperoleh dimurnikan, kemudian diberikan kepada hewan yang masih rentan agar
terbentuk tanggap kebal. Kedua, imunisasi aktif, yaitu teknik imunisasi dengan
pemberian antigen kepada hewan, sehingga terjadi peningkatan tanggap kebal
berperantara antibody oleh hewan itu sendiri. Dibandingkan dengan imunisasi
pasif, imunisasi aktif memiliki perlindungan tubuh yang berlangsung lebih lama.
$3$0.'-%
4/ 4/&3&/ $3$0.'-%
Kolostrum mengandung substansi yang berbentuk seperti susu yang
diproduksi menjelang dan segera setelah proses kelahiran. Kolostrum memililki
konsistensi agak kental dan berwarna kekuningan, kaya akan kandungan protein.
Kolostrum juga merupakan salah satu sumber gizi yang mengandung banyak
lemak, protein, karbohidrat dan beberapa mikronutrient seperti vitamin dan
mineral. Mengandung pula IgA yang berfungsi memberi perlindungan pada
traktus gastrointestinal dari berbagai infeksi pada anak yang baru lahir (Thapa
2005).
$%9$0)0) $3$0.'-%
Menurut Thapa (2005), ada beberapa komponen yang terkandung dalam
1. Unsur kekebalan.
Unsur ini terdiri dari beberapa komponen yakni:
a. Antibodi spesifik, merupakan unsur kekebalan yang didapat dari maternal
antibodi yang telah terpapar antigen,
b. Imunoglobulin, merupakan sumber pertahanan utama, baik dalam
pencegahan maupun penanggulangan pada paparan antigen. Ada 5 tipe
imunoglobulin yaitu IgA, IgD, IgE, IgG dan IgM,
c. ? .( ( # (PRP), berfungsi menstimulasi thymus untuk meregulasi sistem kekebalan dalam tubuh,
d. @ , merupakan protein yang terikat pada unsur besi, berfungsi dalam melawan sel kanker,
$ . 8 dan @. ( 8 $
2. Unsur pertumbuhan
Memiliki fungsi dalam membantu pertumbuhan, regenerasi dan mempercepat
perbaikan pada jaringan dan organ yang mengalami gangguan. Unsur ini
terdiri dari beberapa komponen yakni:
a. EGF ( ( ! , ), berfungsi melindungi bagian permukaan
kulit, juga dalam pengaturan pertumbuhan dan regenerasi sel4sel atau
jaringan yang rusak,
b. & ! , A dan B (TGF A dan B), menstimulasi proliferasi sel pada jaringan ikat dan membantu dalam proses
pembentukan sumsum tulang dan kartilago,
c. - # ! , (PDGF), membantu proses pembelahan sel pada jaringan ikat, otot4otot halus, dan fibroblas. Juga membantu
dalam regenerasi sel neuron,
d. Vitamin dan mineral, merupakan salah satu komponen penting dalam
proses metabolisme, pertumbuhan dan perkembangan tubuh,
'$040 4%84/.-5&/ $3$0.'-% $3$0.'$ 4/40)0
Kolostrogenesis merupakan bagian dari laktogenesis atau pembentukan
susu. Laktogenesis terdiri dari dua tahap yaitu laktogenesis tahap I dan
laktogenesis tahap II. Laktogenesis tahap I ditandai dengan produksi suatu cairan
yang disebut pre4kolostrum. Laktogenesis tahap II dimulai segera sebelum induk
melahirkan, ketika kelenjar ambing pertama kali melepaskan kolostrum sampai
kelenjar ambing menghasilkan susu non4kolostrum. Kolostrogenesis diatur oleh
hormon laktogenik diantaranya adalah estrogen, progesteron, dan prolaktin.
Transfer imunoglobulin dari sirkulasi darah ke kelenjar ambing atau kolostrum
terjadi sebelum, sewaktu dan segera sesudah induk melahirkan (Toelihere 1981).
Selama masa kebuntingan terjadi, proliferasi seluler saluran ambing dan alveoli
berada di bawah pengaruh hormon progesteron dan estrogen yang berasal dari
ovarium dan plasenta (Hidayat $ 2009).
Kolostrogenesis terjadi bersamaan dengan penurunan kadar progesteron
dan estrogen di dalam darah dan peningkatan kadar prolaktin atau hormon
laktogenik dari kelenjar hipofisa. Prolaktin dibutuhkan untuk memulai sekresi
susu dan mempertahankan laktasi. Peningkatan prolaktin didukung oleh stimulasi
kelenjar ambing melalui penghisapan dan pengeluaran kolostrum atau air susu
dari alveoli kelenjar ambing (Hidayat . 2009).
%-/$ 3$8-3)/
Menurut Simorangkir (1995), imunoglobulin (Ig) merupakan suatu fraksi
globulin serum yang berhubungan dengan aktivitas pertahanan tubuh.
Imunoglobulin berperan utama dalam mekanisme kekebalan yang diperantai oleh
antibodi. Mayer (2009) menyatakan bahwa imunoglobulin merupakan molekul
glikoprotein yang diproduksi oleh plasma sel melalui respon yang
memilki fungsi sebagai antibodi.
.'-5.-' %-/$ 3$8-3)/
Struktur imunoglobulin tersusun atas rantai berat/panjang ( -. )
dan rantai ringan/pendek ( ). Semua rantai disatukan oleh ikatan
berfungsi sebagai sum pada sapi terdiri dari :
1.
Imunoglobulin Gai sifat fleksibel dan juga merupakan terbentuknya
odi (Gambar 2) (Mayer 2009).
Gambar 2. Struktur Dasar Imunoglobulin p://pathmicro.med.sc.edu/mayer/IgStruct2000.htm)
imunoglobulin dibagi berdasarkan fungsi dan susuna
yang terbentuk pada regio variabel/konstan. Imuno
ulin G atau Gamma (γ), merupakan Ig dengan jumlah
yang berfungsi dalam menstimulasi fagositosis
in itu juga sebagai komponen utama dalam kolost
490%. Immunoglobulin ini terdiri dari 2 rantai be
ngan L. IgG pada sapi terdiri dari 2 macam sub4kelas y
dengan berat molekul masing4masing sebesar 150 kDa
ulin M atau Mu (L), dihasilkan pada kekebalan primer
ndungan dalam kolostrum sekitar 7%. Terdiri a
pentamer) dengan berat molekul sebesar 900 kDa.
dihubungkan satu sama lain dengan ikatan disulf
domain CH4 menyerupai gelang. Tiap monomer dihubungkan satu dengan
lainnya pada ujung permulaan dan akhirnya oleh protein J yang berfungsi
sebagai kunci (Roitt . 1998).
3. Imunoglobulin A atau Alpha (α), berfungsi dalam mencegah perlekatan
mikroba pada sel4sel epitel. Terdiri dari 2 jenis yaitu IgA dalam serum dan
IgA dalam mukosa. IgA berbentuk dimer yang terdiri dari 2 molekul
monomer, dan sebuah komponen sekretori serta sebuah rantai J dengan
berat molekul sekitar 385 kDa (Roitt . 1998).
4. Imunoglobulin D atau Delta (δ), sebagai reseptor antigen (Tizzard 1988).
Rantai δ mempunyai berat molekul 60.000470.000 dan l2% terdiri dari
karbohidrat. Fungsi utama IgD belum diketahui tetapi merupakan
imunoglobulin permukaan sel limfosit B bersama IgM dan diduga
berperan dalam diferensiasi sel (Roitt $ 1998).
5. Imunoglobulin E atau epsilon (€), bereaksi pada hipersensitifitas,
membantu eosinofil menghancurkan parasit (Decker 2000).
Gambar 3. Klasifikasi Imunoglobulin (Santoso 2010)
Elektroforesis merupakan teknik pemisahan fraksi4fraksi zat berdasarkan