KOMBINASI KININ-AZITROMISIN DIBANDINGKAN DENGAN KOMBINASI KININ-KLINDAMISIN PADA PENGOBATAN
MALARIA FALSIPARUM TANPA KOMPLIKASI PADA ANAK
TESIS
YUNNIE TRISNAWATI 057103007/IKA
PROGRAM MAGISTER KEDOKTERAN KLINIK-SPESIALIS ILMU KESEHATAN ANAK FAKULTAS KEDOKTERAN UNIVERSITAS SUMATERA UTARA
KOMBINASI KININ-AZITROMISIN DIBANDINGKAN DENGAN KOMBINASI KININ-KLINDAMISIN PADA PENGOBATAN
MALARIA FALSIPARUM TANPA KOMPLIKASI PADA ANAK
TESIS
Untuk Memperoleh Gelar Magister Kedokteran Klinik (Anak) Dalam Program Magister Kedokteran Klinik
Konsentrasi Kesehatan Anak
Pada Fakultas Kedokteran Universitas Sumatera Utara
YUNNIE TRISNAWATI 057103007/IKA
PROGRAM MAGISTER KEDOKTERAN KLINIK-SPESIALIS ILMU KESEHATAN ANAK FAKULTAS KEDOKTERAN UNIVERSITAS SUMATERA UTARA
Judul Tesis : Kombinasi Kinin-Azitromisin Dibandingkan
dengan Kombinasi Kinin-Klindamisin pada
Pengobatan Malaria Falsiparum tanpa
Komplikasi pada Anak
Nama Mahasiswa : Yunnie Trisnawati
Nomor Induk Mahasiswa : 057103007
Program Magister : Magister Kedokteran Klinik
Konsentrasi : Kesehatan Anak
Menyetujui Komisi Pembimbing :
(Prof. Dr. dr. H. Syahril Pasaribu, DTM&H, MSc(CTM), SpA(K))
Ketua
(dr. Johannes Harlan Saing, SpA) Anggota
Ketua Program Studi, Ketua TKP-PPDS,
Telah diuji pada
Tanggal: 13 November 2008
PANITIA PENGUJI TESIS
Ketua: Prof. Dr. dr. H. Syahril Pasaribu, DTM&H,
MSc(CTM), SpA(K) ………
Anggota:
1. dr. Johannes Harlan Saing, SpA ………
2. dr. Endang H. Ganie, DTM&H, SpPar(K) ………
3. Prof. dr. H. Munar Lubis, SpA(K) ………
UCAPAN TERIMA KASIH
Assalamualaikum Wr. Wb.
Puji dan syukur kehadirat Allah SWT yang telah melimpahkan rahmat dan hidayahNya serta telah memberikan kesempatan kepada penulis sehingga dapat menyelesaikan penulisan tesis ini.
Tesis ini dibuat untuk memenuhi persyaratan dan merupakan tugas akhir pendidikan keahlian di Departemen Ilmu Kesehatan Anak FK-USU / RSUP H. Adam Malik Medan.
Penulis menyadari penelitian dan penulisan tesis ini masih jauh dari kesempurnaan sebagaimana yang diharapkan, karena itu dengan segala kerendahan hati penulis mengharapkan masukan yang berharga dari semua pihak untuk perbaikan di masa yang akan datang.
Pada kesempatan ini perkenankanlah penulis menyatakan penghargaan dan ucapan terima kasih yang sebesar-besarnya kepada :
1. Pembimbing utama, Prof. Dr. dr. H. Syahril Pasaribu, DTM&H, MSc(CTM), SpA(K), yang telah memberikan bimbingan, bantuan serta saran-saran yang sangat berharga dalam pelaksanaan penelitian dan penyelesaian tesis ini.
2. dr. Johannes Harlan Saing, SpA, selaku anggota pembimbing, yang telah memberikan bimbingan dalam penyusunan dan penulisan tesis ini.
3. Prof. dr. H. Munar Lubis, SpA(K), selaku Ketua Program Studi Pendidikan Dokter Spesialis Anak FK-USU dan Prof. dr. Hj. Bidasari Lubis, SpA(K) selaku Sekretaris Program Studi hingga tahun 2007 dan dr. Hj. Melda Deliana, SpA(K) selaku Sekretaris Program Studi periode 2007 hingga saat ini, yang telah banyak memberikan nasehat dan bimbingan kepada penulis hingga selesainya penulisan tesis ini.
4. Prof. dr. H. Guslihan Dasa Tjipta, SpA(K), selaku Ketua Departemen Ilmu Kesehatan Anak Fakultas Kedokteran USU/RSUP H. Adam Malik Medan periode 2003-2007 dan dr. H. Ridwan M. Daulay, SpA(K), selaku Ketua Departemen Ilmu Kesehatan Anak Fakultas Kedokteran USU/RSUP H. Adam Malik Medan periode 2007 – 2010 yang telah memberikan bantuan dalam pelaksanaan penelitian dan penyelesaian tesis ini.
5. Prof. dr. H. Munar Lubis, SpA(K) yang telah meluangkan waktu dan memberikan bimbingannya sehingga penelitian ini dapat terlaksana dengan lancar.
7. Rektor Universitas Sumatera Utara Prof. H. Chairuddin P Lubis, DTM&H, SpA(K) dan Dekan FK-USU yang telah memberikan kesempatan untuk mengikuti program pendidikan Dokter Spesialis Anak di FK- USU.
8. Kepala Sekolah beserta guru-guru dimana penelitian ini dilakukan, Ka. Dinkes Mandailing Natal, Pemda Mandailing Natal serta masyarakat yang telah memberikan izin dan fasilitas pada penelitian ini sehingga dapat terlaksana dengan baik.
9. Teman-temanku seangkatan Susilowati, Gema Nazri Yani, Ayodhia Pitaloka Pasaribu, Rini Savitri Daulay, Elvina Yulianti, dan Sisca Silvana Sitanggang, terima kasih atas dukungan dan bantuannya selama ini.
10. dr. H. Atoz P. Daulay, SpA dan istri, atas budi baiknya yang telah memberikan fasilitas pada penelitian ini sehingga dapat terlaksana dengan baik.
11. Beby Syofiani Hasibuan, Ditho Atoz Daulay dan Syamsidah Lubis, atas kerjasamanya sehingga penelitian ini dapat berjalan dengan baik.
12. Teman sejawat PPDS Ilmu Kesehatan Anak FK USU serta semua
pihak yang tidak dapat disebutkan satu persatu yang telah memberikan bantuan dalam terlaksananya penelitian serta penulisan tesis ini.
Kepada yang tercinta, papa H. M. Yunus Rasiman, mama Hj. Zuharni Budiman, adik-adikku Yudhie Dhamanhuri dan Gunawan Pradana, terima kasih karena selalu mendoakan, memberikan dorongan, motivasi, bantuan moril dan materil selama penulis mengikuti pendidikan ini. Terima kasih kepada mertua H. Chaliluddin Usman Batubara dan Hj. Rahmah Tanjung serta semua adik-adik atas doa dan bantuannya selama ini.
Teristimewa untuk suami tercinta, Dr. M. Jalaluddin Assuyuthi Chalil Batubara, terima kasih atas doa, pengertian, dukungan dan pengorbanan tanpa kenal lelah yang telah diberikan hingga penulis mampu menyelesaikan pendidikan. Mudah-mudahan Allah senantiasa melimpahkan rahmat, rezeki, dan karuniaNya buat kita semua.
Akhirnya penulis mengharapkan semoga penelitian dan tulisan ini bermanfaat bagi kita semua. Amin.
Wassalamualaikum Wr. Wb.
Medan, 13 November 2008
DAFTAR ISI
BAB 2. TINJAUAN PUSTAKA 2.1. Definisi 4
2.5.1. Manifestasi klinis malaria falsiparum tanpa komplikasi 8
2.5.2. Pemeriksaan laboratorium 9
2.6. Pengobatan Malaria Falsiparum Tanpa Komplikasi 11
2.6.1. Kinin 12
2.6.2. Azitromisin 14
2.6.3. Klindamisin 16
BAB 3. METODOLOGI
BAB 6. KESIMPULAN DAN SARAN
DAFTAR TABEL
Tabel 3.1. Dosis obat pada kedua kelompok sampel penelitian 23
Tabel 4.1. Karakteristik sampel penelitian 28
DAFTAR GAMBAR
Gambar 2.1. Siklus hidup parasit malaria 7
Gambar 2.2. Rumus bangun kinin 12
Gambar 2.3. Rumus bangun azitromisin 14
Gambar 2.4. Rumus bangun klindamisin 16
Gambar 2.5. Kerangka konsep penelitian 18
Gambar 4.1. Profil penelitian 26
Gambar 4.2. Diagram stacked column gejala dan
tanda klinis sebelum pengobatan 29
DAFTAR SINGKATAN DAN LAMBANG
α : Kesalahan tipe I atau hasil positif semu
β : Kesalahan tipe II atau hasil negatif semu
< : Lebih kecil dari
ACT : Artemisinin-based Combination Therapy
CDC : Centers for Disease Control and Prevention
Cl : Chlorine
cm : sentimeter
EKG : Elektro Kardio Gram
H0 : Hari pertama pemberian obat
H2 : 48 jam setelah pemberian obat
H28 : Hari ke-28 setelah pemberian obat
P. falciparum : Plasmodium falciparum
P. malariae : Plasmodium malariae
P. ovale : Plasmodium ovale
P. vivax : Plasmodium vivax
PCR : Polymerase Chain Reaction
SLTA : Sekolah Lanjutan Tingkat Akhir
SLTP : Sekolah Lanjutan Tingkat Pertama
WHO : World Health Organization
zα : Deviat baku normal untuk α
Latar belakang. Meningkatnya kasus malaria falsiparum yang resisten terhadap banyak obat telah menjadi masalah kesehatan di Indonesia. Oleh karena itu, Departemen Kesehatan Republik Indonesia telah mengganti terapi standar pengobatan malaria falsiparum menjadi kombinasi Artesunat-Amodiakuin. Peneliti ingin mencari terapi alternatif jika kombinasi terapi standar tidak tersedia.
ABSTRAK
Tujuan. Membandingkan efikasi Azitromisin (KA) dengan
Kinin-Klindamisin (KK), sebagai terapi alternatif pada pengobatan malaria falsiparum tanpa komplikasi pada anak.
Metode. Suatu penelitian uji klinis acak terbuka yang dilakukan sejak Juli-Agustus 2007 pada anak berusia 5 sampai 18 tahun, yang positif
P.falciparum pada apusan darah tepi, di Kabupaten Mandailing Natal, Propinsi Sumatera Utara. Kelompok KA mendapat kinin selama 7 hari (10
mg/kgBB terbagi 3 dosis selama 4 hari pertama, dilanjutkan dengan 5 mg/kgBB terbagi 3 dosis selama 3 hari) dan diberikan azitromisin (10 mg/kgBB/dosis) diberikan per oral selama 3 hari pertama. Kelompok KK
juga mendapatkan kinin dikombinasikan dengan klindamisin (5 mg/kgBB terbagi 2 dosis) selama 3 hari pertama. Parasitemia dihitung pada hari ke 0, 2, 7, dan 28.
Hasil. Secara acak, 246 anak yang positif menderita malaria falsiparum, dibagi menjadi 2 kelompok. Hanya 121 anak pada kelompok KA dan 123 anak pada kelompok KK yang memenuhi kriteria inklusi dan mengikuti penelitian sampai akhir. Dari apusan darah tepi pada hari ke-2, didapati angka kesembuhan 100% (P=0,0001). Tidak dijumpai rekrudensi pada hari ke-2, 7, dan 28 (P =1,000). Pada kelompok KA didapati efek samping berupa sakit kepala dan muntah sebanyak 21 dan 6 (P =0.0001; 0012) secara berturutan.
Kesimpulan. Kedua kombinasi obat dapat digunakan sebagai terapi
alternatif untuk pengobatan malaria falsiparum tanpa komplikasi pada anak.
ABSTRACT
Background. Multidrug-resistant Plasmodium falciparum malaria is
increasing public health concern in Indonesia. Therefore, Department of Health, Republic of Indonesia had changed the standard treatment into Artesunate-Amodiaquine combination. We encouraged to find alternative drug if this combination drug is not available.
Objective. To compare the efficacy of Quinine-Azithromycin (QA) with the Quinine-Clindamycin (QC) combination, as alternative treatments for uncomplicated P.falciparum malaria in children.
Methods. This randomized, open label trial was conducted between July-August 2007 at 5-18 years old children, with positive P.falciparum from the peripheral blood smear, at Mandailing Natal, North Sumatera Province. Group QA received Quinine for 7 days (10 mg/kgbw divided into 3 doses for 4 days, continued with 5 mg/kgbw divided into 3 doses for 3 days) combined with Azithromycin (10 mg/kgbw/dose) orally for the first 3 days. Group QC also received Quinine combined with Clindamycin (5 mg/kgbw twice daily) orally for the first 3 days. Parasitemia was counted at the day 0, 2, 7, and 28.
Results. Randomly, 246 children with positive P.falciparum malaria,
separated into two groups. Only 121 children in group QA and 123 children in group QC fulfilled inclusion criterias and completed the study. Cure rate
achieved 100% from peripheral blood smear examination at day 2nd (P =0.0001). Both groups showed no recrudescence event at day 7th, and
28th (P =1.000). Headache and vomiting as adverse events were found in 21 and 6 children in group QA (P =0.0001; 0.012) respectively.
Conclusion. Both of drug combinations can be used as potential alternative treatments for uncomplicated P.falciparum malaria in children.
Keywords. Quinine-Azithromycin, Quinine-Clindamycin, uncomplicated
KOMBINASI KININ-AZITROMISIN DIBANDINGKAN DENGAN KOMBINASI KININ-KLINDAMISIN PADA PENGOBATAN
MALARIA FALSIPARUM TANPA KOMPLIKASI PADA ANAK
TESIS
Dengan ini saya menyatakan bahwa dalam tesis ini tidak terdapat karya yang pernah diajukan untuk memperoleh gelar kesarjanaan di suatu perguruan tinggi, dan sepanjang pengetahuan saya juga tidak terdapat karya atau pendapat yang pernah ditulis atau diterbitkan oleh orang lain, kecuali yang secara tertulis diacu dalam naskah ini dan disebutkan dalam daftar pustaka.
Medan, 13 November 2008
(Yunnie Trisnawati)
1.1. Latar Belakang
Malaria masih merupakan masalah kesehatan yang cukup besar bagi anak
di negara tropis di seluruh dunia. Berdasarkan penemuan malaria di tahun
1880-an, banyak gambaran biologi dan patogenesisnya belum diketahui dan
malaria berpotensial mengancam jiwa.1 Dijumpai sekitar 300-500 juta kasus
malaria setiap tahunnya, dengan jumlah kematian akibat malaria berkisar 1,5
sampai 2,7 juta per tahunnya.1,2
Malaria disebabkan oleh protozoa Plasmodiumyang ditransmisikan ke
manusia oleh nyamuk Anopheles betina. Ada empat spesies Plasmodium
yang menyebabkan malaria pada manusia, yaitu P.falciparum, P.malariae,
P.ovale, dan P.vivax. Malaria juga dapat ditularkan melalui transfusi darah,
penggunaan jarum yang terkontaminasi, dan dari wanita hamil ke bayi yang
dikandungnya.2
P.falciparum telah diketahui resisten terhadap klorokuin di beberapa
daerah.1-4 Penelitian di daerah Mandailing Natal di Sumatera Utara didapati
resisten terhadap klorokuin sekitar 32% dan untuk fansidar 29%.3 Malaria
yang didapat dari daerah yang diketahui P.falciparum resisten terhadap
klorokuin ataupun daerah yang sensitivitas terhadap klorokuinnya diragukan
harus diterapi dengan obat selain klorokuin.1
singkat dan waktu paruh pendek dengan obat yang bekerja lebih lambat dan
mempunyai waktu paruh lebih panjang. Azitromisin, yang merupakan
antimalaria golongan makrolida paling kuat dengan waktu paruh panjang (68
jam)5, menunjukkan sinergisme dengan kinin dalam pengobatan
P.falciparumin vitro.6
Klindamisin dipilih sebagai obat yang menjanjikan dengan waktu
paruh yang singkat (2-4 jam) dan memiliki karakteristik bekerja lambat
namun memiliki tingkat keamanan dan tolerabilitas yang baik sebagai
antimalaria.7 Klindamisin dapat digunakan pada anak-anak dan wanita hamil.
Hal ini sangat berguna pada penggunaan kombinasi antimalaria pada
anak-anak dan wanita hamil di sub-sahara Afrika yang mempunyai risiko tertinggi
menderita malaria yang berkaitan dengan angka morbiditas dan mortalitas.8
1.2. Perumusan Masalah
Berdasarkan uraian dalam latar belakang tersebut di atas, maka diperlukan
penelitian untuk mengetahui apakah ada perbedaan kesembuhan antara
kombinasi kinin-azitromisin (KA) dengan kombinasi kinin-klindamisin (KK)
sebagai alternatif dalam pengobatan malaria falsiparum tanpa komplikasi
pada anak.
Kombinasi kinin-azitromisin memberikan angka kesembuhan yang sama
dengan kombinasi kinin-klindamisin pada anak dengan malaria falsiparum
tanpa komplikasi.
1.4. Tujuan Penelitian
Untuk mengetahui apakah terdapat perbedaan kesembuhan antara
kombinasi kinin-azitromisin dengan kombinasi kinin-klindamisin sebagai
alternatif dalam pengobatan malaria falsiparum tanpa komplikasi pada anak.
1.5.Manfaat Penelitian
Manfaat penelitian ini adalah untuk mendapatkan terapi alternatif lain yang
BAB 2.TINJAUAN PUSTAKA
2.1. Definisi
Malaria merupakan penyakit infeksi yang bersifat akut maupun kronis yang
disebabkan oleh protozoa intrasel dari genus Plasmodium. Ada empat
parasit yang dapat menginfeksi manusia, yaitu P.malariae, P.vivax,
P.falciparum dan P.ovale.2,9 P.falciparum paling sering didapati pada daerah
tropis dan sering menyebabkan kematian pada manusia karena dapat
menginvasi sel darah merah pada semua usia dan sering resisten terhadap
obat-obat anti malaria.10
2.2. Sejarah
Penyakit ini pertama kali dinamakan mal air (udara busuk) oleh seseorang
yang berkebangsaan Itali pada abad ke-18, namun tulisan yang pertama kali
menyebutkan tentang demam periodik didapati dalam tulisan Hindu dan
Cina. Terobosan besar dalam hal etiologi malaria yaitu pada tahun 1880,
setelah Laveran, seorang ahli bedah militer dari Algeria, pertama kali
menemukan gametosit P.falciparum pada pemeriksaan apusan darah tepi
2.3. Transmisi
Malaria ditransmisikan melalui gigitan nyamuk Anopheles betina yang
terinfeksi malaria, atau, lebih jarang, melalui inokulasi langsung dari sel
darah yang terinfeksi,9 seperti melalui transfusi darah, penggunaan jarum
suntik yang terkontaminasi, dari ibu hamil ke bayi yang dikandungnya, dan
dari transplantasi organ.2
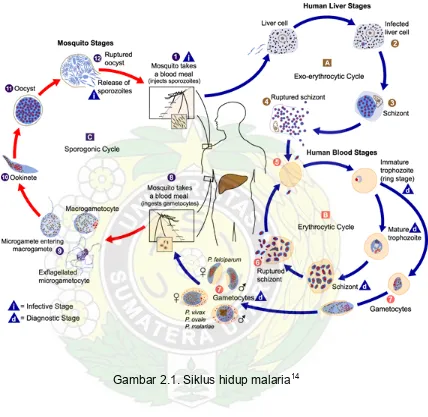
2.4. Siklus Hidup Plasmodium falciparum
Parasit malaria memerlukan dua hospes untuk siklus hidupnya, yaitu
manusia dan nyamuk Anopheles.
2.4.1. Siklus hidup pada manusia
Pada waktu nyamuk Anopheles infektif menghisap darah manusia, sporozoit
yang berada di kelenjar air liur nyamuk akan masuk ke dalam peredaran
darah selama kurang lebih ½ jam. Setelah itu sporozoit akan masuk ke
dalam sel hati dan menjadi tropozoit hati. Kemudian berkembang menjadi
skizon hati yang terdiri dari 10 000-30 000 merozoit hati (tergantung
spesiesnya). Siklus ini disebut siklus ekso-eritrositer yang berlangsung
Merozoit yang berasal dari skizon hati yang pecah akan masuk ke
peredaran darah dan menginfeksi sel darah merah. Di dalam sel darah
merah, parasit tersebut berkembang dari stadium tropozoit sampai skizon
(8-30 merozoit, tergantung spesiesnya). Proses perkembangan aseksual ini
disebut skizogoni. Selanjutnya eritrosit yang terinfeksi (skizon) pecah dan
merozoit yang keluar akan menginfeksi sel darah merah lainnya. Siklus ini
disebut siklus eritrositer.11 Siklus eritrositer ini menyebabkan timbulnya gejala
malaria.12
Setelah 2-3 siklus skizogoni darah, sebagian merozoit yang
menginfeksi sel darah merah akan membentuk stadium seksual (gametosit
jantan dan betina).
2.4.2.Siklus hidup pada nyamuk Anopheles betina
Apabila nyamuk Anopheles betina menghisap darah yang mengandung
gametosit, di dalam tubuh nyamuk, gamet jantan dan betina melakukan
pembuahan menjadi zigot. Zigot berkembang menjadi ookinet kemudian
menembus dinding lambung nyamuk. Pada dinding luar lambung nyamuk
ookinet akan menjadi ookista dan selanjutnya menjadi sporozoit,11 dan
bermigrasi ke kelenjar air liur nyamuk.13 Sporozoit ini bersifat infektif dan siap
ditularkan ke manusia.11,13 Siklus hidup malaria dapat dilihat pada gambar
Gambar 2.1. Siklus hidup malaria14
2.5. Diagnosis Malaria Falsiparum
Pada daerah endemis malaria, biasanya diagnosis ditegakkan berdasarkan
gejala dan tanda klinis. Tetapi walaupun di daerah bukan endemis malaria,
diagnosis banding malaria harus dipikirkan pada riwayat demam tinggi
anemia. Diagnosis malaria merupakan hasil pertimbangan klinis dan tidak
selalu disertai hasil laboratorium oleh karena beberapa kendala pada
pemeriksaan laboratorium.13 Anak dengan keluhan demam atau gejala
sistemik yang tidak diketahui penyebabnya dan ada riwayat perjalanan atau
tinggal di daerah endemis malaria dalam setahun terakhir dapat didiagnosis
menderita malaria sampai terbukti sebaliknya.2
2.5.1. Manifestasi klinis malaria falsiparum tanpa komplikasi
Manifestasi klinis malaria tergantung status imunitas pejamu dan spesies
malaria yang menginfeksi. Secara umum, infeksi P.falciparum lebih berat dan
lebih jelas gejala klinisnya dibandingkan infeksi spesies Plasmodium
lainnya.12 Anak dan dewasa seringkali asimtomatik selama fase awal, yaitu
masa inkubasi infeksi malaria. Masa inkubasi P.falciparum berkisar 9-14
hari. Masa inkubasi ini dapat lebih lama pada pasien dengan imunitas
parsial. Gejala prodromal berlangsung selama 2-3 hari sebelum parasit
dijumpai dalam darah. Gejala prodromal yang dijumpai berupa sakit kepala,
mudah lelah, anoreksia, mialgia, demam dan nyeri di dada, perut, atau
sendi-sendi.2
Demam yang bersifat paroksismal merupakan gejala khas dari malaria
dan biasanya berkaitan dengan pecahnya skizon dan lepasnya merozoit dari
eritrosit.12 Pada malaria vivax dan falsiparum, gejala paroksismal ini
ditandai dengan adanya periode menggigil hebat, diikuti dengan demam
tinggi yang dapat mencetuskan kejang demam; lalu berkeringat banyak yang
diikuti dengan turunnya suhu tubuh.12 Pada pemeriksaan fisik biasanya
dijumpai hepatosplenomegali dan pucat. Dapat pula dijumpai takikardia.
Ikterik berhubungan dengan hiperparasitemia.9
2.5.2. Pemeriksaan laboratorium
Pemeriksaan baku emas dalam menegakkan diagnosis malaria yaitu
pemeriksaan apusan darah,9 baik apusan darah tebal maupun tipis dengan
pewarnaan Giemsa.12 Pemeriksaan ini untuk menentukan : ada tidaknya
parasit malaria (positif atau negatif); spesies dan stadium Plasmodium; dan
kepadatan parasit.11
Plasmodium falciparum menyerang semua bentuk eritrosit mulai dari
retikulosit sampai eritrosit yang matang. Pada pemeriksaan darah tepi baik
apusan maupun tetes tebal terutama dijumpai parasit muda berbentuk cincin
(ring form). Juga dijumpai gametosit dan pada kasus berat yang biasanya
disertai komplikasi, dapat dijumpai bentuk skizon. Bentuk seksual/gametosit
muncul dalam waktu 1 minggu dan dapat bertahan sampai beberapa bulan
setelah sembuh. Tanda-tanda parasit malaria yang khas pada sediaan tipis,
gametositnya berbentuk pisang dan terdapat bintik Maurer pada sel darah
banyak sekali bentuk cincin tanpa bentuk lain yang dewasa (star in the sky),
terdapat balon merah di sisi luar gametosit.13
Tes serologis yang digunakan untuk diagnosis malaria adalah Indirect
Fluorescent Antibody test (IFA), Indirect Hemaglutination test (IHA) dan
Enzyme Linked Immuno Sorbent Assay (ELISA). Kegunaan tes serologis
untuk diagnosis malaria akut sangat terbatas, karena baru akan positif
beberapa hari setelah parasit malaria ditemukan dalam darah. Jadi sampai
saat ini tes serologi merupakan cara terbaik untuk studi epidemiologi.
Teknik diagnostik lainnya adalah pemeriksaan Quantitative Buffy Coat
(QBC), dengan menggunakan tabung kapiler dan pulasan jingga akridin
kemudian diperiksa di bawah mikroskop fluoresens. Teknik mutakhir lainnya
dengan menggunakan pelacak DNA probe untuk mendeteksi antigen.
Pemeriksaan lain yang dapat dilakukan yaitu Malaquick test dan Parasight
F.13
Anemia pada malaria dapat terjadi akut maupun kronis. Anemia ini
disebabkan kerusakan eritrosit oleh parasit, penekanan eritropoesis dan
terjadinya hemolisis oleh proses imunologis. Pada darah tepi dapat dijumpai
poikilositosis, anisositosis, polikromatosis dan bintik-bintik basofilik yang
menyerupai anemia pernisiosa. Terjadi ikterus ringan dengan peningkatan
bilirubin indirek dan tes fungsi hati yang abnormal seperti meningkatnya
2.6. Pengobatan Malaria Falsiparum Tanpa Komplikasi
Pemilihan obat antimalaria berdasarkan atas spesies Plasmodium yang
menginfeksi, kemungkinan terjadinya resistensi obat, dan keparahan
penyakit.15 Obat antimalaria bekerja pada stadium yang berbeda dalam
siklus hidup parasit. Obat skizontosid darah menyerang parasit dalam
eritrosit, mencegah atau menghilangkan gejala klinis. Obat gametosid
menghancurkan bentuk seksual pada manusia, menurunkan transmisi. Obat
skizontosid jaringan bekerja pada fase awal perkembangan parasit di hati,
sebelum lepasnya merozoit ke dalam darah. Obat hipnozoitosid membunuh
hipnozoit yang bersifat dormant di hati, mencegah relaps. Obat sporontosid
menginhibisi perkembangan ookista di tubuh nyamuk, menurunkan transmisi
malaria.16
Risiko resistensi terhadap obat antimalaria bervariasi, tergantung
spesies dan jenis obat.17 Saat ini, P.falciparum sangat resisten terhadap
klorokuin didapati pada hampir seluruh daerah yang terkena malaria.18 Oleh
karena itu, World Health Organization merekomendasikan suatu kebijakan
terapi bagi negara-negara yang telah didapati kasus P.falciparum resisten
terhadap antimalaria monoterapi, seperti klorokuin, amodiakuin, atau
sulfadoksin/pirimetamin, berupa terapi kombinasi yang mengandung derivat
artemisinin atau yang disebut dengan Artemisinin-based Combination
1. Artemeter + Lumefantrin
2. Artesunate + Amodiakuin
3. Artesunate + Sulfadoksin-Pirimetamin (pada daerah yang efikasi
Sulfadoksin-Pirimetamin masih tinggi)
4. Artesunate + Meflokuin (pada daerah dengan transmisi rendah)
5. Amodiakuin + Sulfadoksin-Pirimetamin (pada daerah yang efikasi
kedua obat masih tinggi)19
2.6.1. Kinin
Kinin adalah suatu derivat alkaloid dari kulit pohon Cinchona. Ada 4 alkaloid
antimalaria yang dapat diturunkan dari kulit pohon ini, yaitu : kinin, kuinidin,
kinkonin dan kinkinidin. Kinin merupakan bentuk L-stereoisomer dari
kuinidin.19 Rumus bangun kinin dapat dilihat pada gambar 2.2.
20
Gambar 2.2. Rumus bangun kinin
Farmakokinetik
Kinin siap diabsorbsi baik jika diberikan secara oral maupun intramuskular.
Absorbsi secara oral terutama terjadi di usus halus dan mencapai sekitar
plasma mencapai maksimum dalam waktu 3-8 jam dan, setelah
didistribusikan, menurunkan pada waktu paruh 11 jam terapi dihentikan.
Farmakokinetik kinin dapat berubah sesuai dengan keparahan infeksi
malaria.21 Waktu paruh obat pada orang sehat mencapai 11 jam, penderita
malaria tanpa komplikasi mencapai 16 jam dan mencapai 18 jam pada
penderita malaria berat.22
Alkaloid kinkona dieksresikan terutama melalui urin dalam bentuk
metabolit hidroksi, dan sebagian kecil melalui tinja, getah lambung, empedu
dan air liur. Ekskresi lengkap terjadi dalam 24 jam. Ekskresi dalam urin yang
asam 2 kali lebih cepat dibandingkan dalam urin alkali.23
Farmakodinamik
Kinin beraksi terutama melawan parasit malaria bentuk eritrositik aseksual
dan memiliki efek minimal terhadap parasit di hepar.21 Seperti antimalaria
lainnya, kinin juga membunuh bentuk seksual P.vivax, P.malariae dan P.
ovale, namun tidak membunuh bentuk gametosit dewasa P.falciparum. Kinin
juga tidak membunuh parasit malaria bentuk pre eritrositik. Mekanisme aksi
kinin sebagai antimalaria yaitu melalui inhibisi detoksifikasi haem parasit
dalam vakuola makanan, namun mekanismenya tidak jelas diketahui.20
Pemberian kinin secara oral untuk mempertahankan konsentrasi
sulfonamid atau tetrasiklin, dapat diberikan bersamaan untuk meningkatkan
efikasi kinin.21
2.6.2. Azitromisin
Antimikroba golongan makrolida juga menunjukkan aktivitas sebagai
antimalaria,24 dan golongan ini aman bagi ibu hamil dan anak-anak.
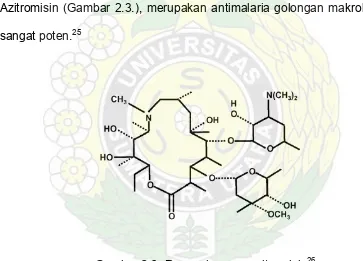
Azitromisin (Gambar 2.3.), merupakan antimalaria golongan makrolida yang
sangat poten.25
Gambar 2.3. Rumus bangun azitromisin26
Farmakokinetik
Azitromisin diberikan secara oral diabsorpsi secara cepat dan didistribusikan
ke seluruh tubuh kecuali ke otak dan cairan serebrospinal. Azitromisin
sebaiknya tidak diberikan bersamaan dengan makanan. Obat ini memiliki
konsentrasi obat di dalam sel (terutama fagosit), sehingga didapati
konsentrasi di jaringan atau sekresi dibandingkan konsentrasi dalam serum.
Azitromisin mengalami metabolisme di hati untuk menginaktivasi
metabolit, namun kebanyakan diekskresi melalui empedu. hanya 12% obat
yang dieksresikan melalui urine. Waktu paruh mencapai 40-68 jam, dapat
memanjang karena pengambilan dan pengikatan yang luas dari jaringan.21
Farmakodinamik
Antibiotika makrolida merupakan bakteriostatik yang menghambat sintesis
protein dengan mengikat secara reversibel subunit ribosom mikroorganisme
yang sensitif.21 Azitromisin merupakan skizontosidal darah yang efisien
namun mempunyai kerja yang relatif lambat.27 Data in vitro melaporkan,
azitromisin memiliki kemampuan klinis bila digunakan sebagai kombinasi
dengan obat anti malaria lain.26
2.6.3. Klindamisin
Klindamisin (7-chloro-lincomycin) merupakan derivat semisintetik dari
linkomisin dan diperkenalkan pada tahun 1960-an sebagai suatu antibiotik.28
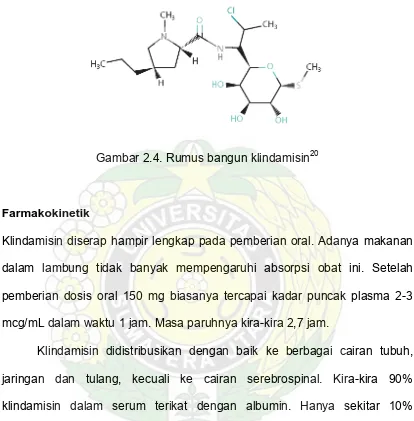
Rumus bangun klindamisin (gambar 2.4.) mirip dengan linkomisin.
Perbedaannya hanya pada 1 gugus hidroksil pada linkomisin yang diganti
Gambar 2.4. Rumus bangun klindamisin20
Farmakokinetik
Klindamisin diserap hampir lengkap pada pemberian oral. Adanya makanan
dalam lambung tidak banyak mempengaruhi absorpsi obat ini. Setelah
pemberian dosis oral 150 mg biasanya tercapai kadar puncak plasma 2-3
mcg/mL dalam waktu 1 jam. Masa paruhnya kira-kira 2,7 jam.
Klindamisin didistribusikan dengan baik ke berbagai cairan tubuh,
jaringan dan tulang, kecuali ke cairan serebrospinal. Kira-kira 90%
klindamisin dalam serum terikat dengan albumin. Hanya sekitar 10%
klindamisin diekskresikan dalam bentuk asal melalui urin. Sejumlah kecil
klindamisin ditemukan dalam feses. Sebagian besar obat dimetabolisme
menjadi N-demetilklindamisin dan klindamisin sulfoksid untuk selanjutnya
Farmakodinamik
Penelitian sejak 1970-an sampai dengan 1980-an telah menunjukkan efikasi,
keamanan dan kepraktisan klindamisin sebagai terapi malaria falsiparum.28
In vitro, klindamisin dan ketiga metabolitnya memiliki efek inhibisi yang kuat
terhadap P.falciparum. Obat ini berakumulasi di parasit.30
Klindamisin merupakan obat yang bekerja lambat, ditoleransi dengan
baik dengan efek samping yang minimal. Efek samping yang sering
dikeluhkan pada pemakaian klindamisin berupa diare dan ruam di sekitar
mulut.28
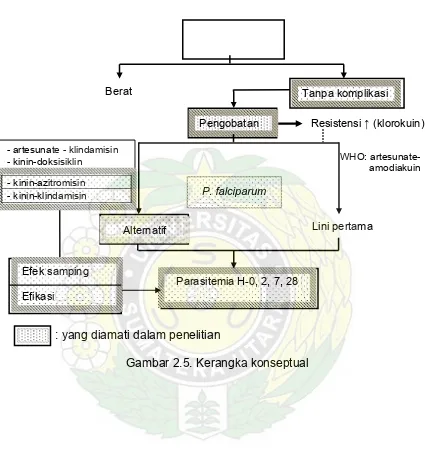
2.7. Kerangka Konseptual
- Quantitative buffy coat method - PCR
- Malaquick test - Parasight F
- Apusan darah tepi MALARIA
: yang diamati dalam penelitian
Pengobatan Resistensi ↑ (klorokuin)
Alternatif
WHO: artesunate- amodiakuin
Lini pertama
- artesunate - klindamisin - kinin-doksisiklin
Parasitemia H-0, 2, 7, 28 Efek samping
Efikasi
- kinin-azitromisin
- kinin-klindamisin P. falciparum
Tanpa komplikasi Berat
BAB 3.METODOLOGI
3.1. Desain
Penelitian ini bersifat uji klinis acak terbuka, untuk membandingkan
kesembuhan kombinasi KA dengan kombinasi KK sebagai alternatif dalam
pengobatan malaria falsiparum tanpa komplikasi.
3.2. Tempat dan Waktu
Penelitian dilakukan di Sekolah Dasar hingga Sekolah Menengah Umum di
Kecamatan Gunung Baringin, Tanjung Julu, Purba, Adian Jior, Gunung
Manaon, Pagarantonga, Panyabungan Jae, Kabupaten Mandailing Natal,
Propinsi Sumatera Utara pada bulan Juli hingga Agustus 2007.
3.3. Populasi Penelitian
Populasi target adalah anak Sekolah Dasar hingga Sekolah Menengah
Umum yang berusia 5 sampai 18 tahun yang menderita malaria. Populasi
terjangkau adalah anak Sekolah Dasar hingga Sekolah Menengah Umum
yang berusia 5 sampai 18 tahun yang menderita malaria falsiparum di 7
sekolah Kabupaten Mandailing Natal. Sampel adalah populasi terjangkau
yang memenuhi kriteria inklusi dan eksklusi.
3.4. Perkiraan Besar Sampel
Besar sampel dihitung dengan menggunakan rumus untuk uji hipotesis
terhadap 2 proporsi, yaitu sebagai berikut:31
( zα√2PQ + zβ√ P1Q1 + P2Q2 )2
n1=n2=
( P1 – P2 )2
n1 = jumlah subyek yang masuk dalam kelompok I
n2 = jumlah subyek yang masuk dalam kelompok II
P1 = proporsi sembuh untuk kelompok I
P2 = proporsi sembuh untuk kelompok II
P = proporsi = ½ (P1+P2)
Q= 1-P
Pada penelitian ini ditetapkan α = 0,05 (interval kepercayaan 95%) dan β =
0,2 (power 80%). Perbedaan sembuh yang diharapkan adalah 0,08 maka:
P1 = 0,88 dan P2 = 0,98
P = ½ (0,88+0,98) = 0,93
Q = 1-0,93 = 0,07
Dengan memakai rumus di atas maka diperoleh jumlah sampel untuk
masing-masing kelompok adalah 123 orang.
3.5.1. Kriteria Inklusi
1. Penderita malaria berusia antara 5 sampai 18 tahun yang bersedia
mengikuti penelitian, dibuktikan dengan mengisi surat persetujuan dari
orang tua
2. Dijumpai P. falciparum pada pemeriksaan apusan darah tepi
3. Tidak mendapat obat anti malaria dalam satu bulan terakhir
4. Subjek penelitian tinggal di lokasi penelitian
3.5.2. Kriteria eksklusi
1. Tidak dapat mengikuti penelitian sampai akhir
2. Penderita malaria berat
3. Tidak teratur atau menolak minum obat
4. Dijumpai infeksi gabungan (mixed infection) dengan Plasmodium
lainnya.
3.6. Persetujuan/Informed Consent
Semua subyek penelitian akan diminta persetujuan dari orang tua setelah
dilakukan penjelasan terlebih dahulu mengenai kondisi penyakit yang
dialami, pengobatan yang diberikan dan efek samping pengobatan. Lembar
Persetujuan Setelah Penjelasan (PSP) dan lembar penjelasan sebagaimana
Penelitian ini disetujui oleh Komite Etik Penelitian Bidang Kesehatan
Fakultas Kedokteran Universitas Sumatera Utara.
3.8. Cara Kerja dan Alur Penelitian
Pemeriksaan apusan darah tepi tipis dan tebal dilakukan pada siswa yang
berusia 5 sampai 18 tahun yang diduga menderita malaria, yang sebelumnya
telah dilakukan pengisian lembar PSP, melakukan anamnesis dan
pemeriksaan fisik. Pemeriksaan apusan darah tepi diwarnai dengan
pewarnaan giemsa sesuai prosedur dan dibaca oleh tenaga laboratorium
yang terlatih. Bila ditemukan P. falciparum pada pemeriksaan apusan darah
tepi maka anak tersebut dimasukkan dalam sampel kemudian dihitung
jumlah parasitnya. Parasit aseksual dihitung dalam 200 sel darah putih.
Sampel yang memenuhi kriteria kemudian dibagi menjadi dua
kelompok secara acak sederhana. Kedua kelompok sampel diberikan
pengobatan dengan dosis sesuai yang tertera dalam Tabel 3.1. Semua obat
anti malaria diberikan sesudah makan. Jika anak muntah dalam 15 menit
setelah pemberian obat, dosis yang sama diberikan kembali.
Hari
Kelompok Jenis Obat
1 2 3 4 5-7
Azitromisin 10 mg/kgbb/hari
sekali sehari
Klindamisin 10 mg/kgbb/hari
terbagi 2 dosis
Selama penelitian dilakukan pencatatan rutin terhadap tanda dan
gejala malaria, riwayat obat-obatan yang pernah dikonsumsi dan efek
samping pengobatan. Pemeriksaan fisik dan apusan darah tepi ulangan
dilakukan pada hari ke-2,7 dan 28.Sampel ditimbang dan dinilai berat badan
dengan menggunakan timbangan merek Camry (sensitivitas 0,1 kg) dan
tinggi badan diukur dengan pengukur tinggi merek stature metre 2M
(sensitivitas 0,5 cm). Status nutrisi dihitung dengan teknik antropometri
standar berdasarkan CDC NCHS-WHO.
Variabel bebas Skala
Jenis obat nominal
Variabel tergantung Skala
Parasitemia ordinal
Pusing nominal
Tinitus nominal
Muntah nominal
3.10. Definisi Operasional
1. Infeksi malaria falsiparum ditetapkan apabila di dalam pemeriksaan
apusan darah tepi dijumpai P. falciparum.
2. Dikatakan sembuh bila dalam pemeriksaan apusan darah tepi
penderita tidak ditemukan lagi parasit malaria.
3. Malaria falsiparum tanpa komplikasi adalah malaria yang tidak disertai
dengan komplikasi apapun, seperti malaria serebral dengan
kesadaran menurun, anemia berat (hemoglobin ≤ 5 g/dl), dehidrasi,
gangguan asam basa (asidosis metabolik) dan gangguan elektrolit,
hipoglikemia berat, gagal ginjal, edema paru akut, kegagalan sirkulasi,
kecenderungan terjadinya perdarahan, hiperpireksia, hemoglobinuria,
ikterus dan hiperparasitemia.
4. Efikasi adalah sejauh mana intervensi tertentu (obat) memberikan
hasil yang menguntungkan pada keadaan ideal.
Data diolah dengan SPSS for WINDOWS 14 (SPSS Inc, Chicago). Analisis
data untuk mengetahui perubahan hasil terapi pada kelompok sebelum dan
sesudah pengobatan dengan uji Wilcoxon signed-rank. Data karakteristik
dan efek samping pengobatan dengan kai kuadrat. Uji dinyatakan bermakna
bila P < 0,05.
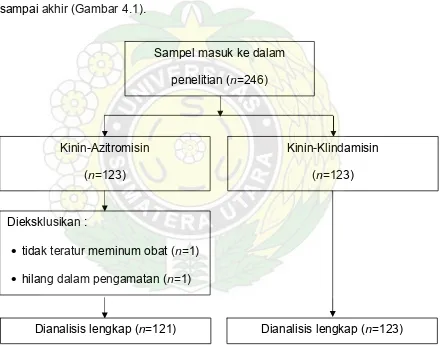
Ada 246 orang anak yang memenuhi kriteria inklusi dan dibagi menjadi 2
kelompok secara randomisasi; kelompok pertama terdiri 123 anak yang
mendapatkan kombinasi KA dan kelompok kedua mendapatkan kombinasi
KK. Setelah pemberian obat, hanya 244 anak yang menyelesaikan penelitian
sampai akhir (Gambar 4.1).
Sampel masuk ke dalam
penelitian (n=246)
Dieksklusikan :
• tidak teratur meminum obat (n=1)
• hilang dalam pengamatan (n=1) Kinin-Azitromisin
(n=123)
Gambar 4.1. Profil penelitian
Dianalisis lengkap (n=123)
26
Kinin-Klindamisin
(n=123)
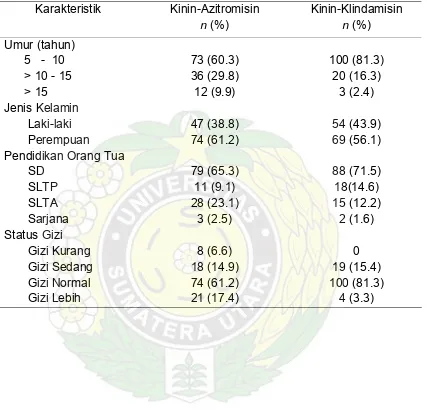
Distribusi dan karakteristik sampel ditunjukkan pada Tabel 4.1. Tidak
ada perbedaan bermakna dalam hal jenis kelamin dan pendidikan orang tua
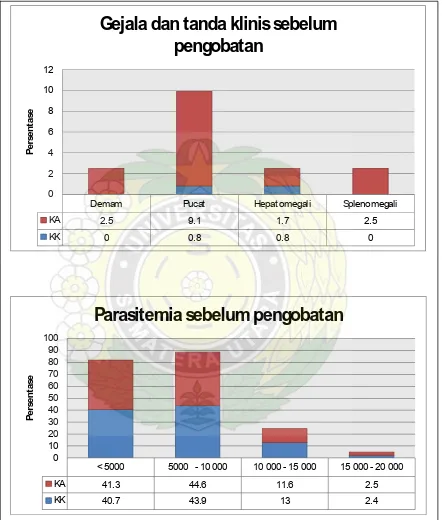
pada kedua kelompok. Pemeriksaan fisik awal dilakukan pada kedua
kelompok untuk mencari gejala klinis, seperti demam, pucat, hepatomegali,
splenomegali dan parasitemia. Pucat dijumpai pada 11 orang anak (9,1%)
pada kelompok kombinasi KA. Demam dan splenomegali dijumpai pada 3
orang anak (2,5%) pada kelompok kombinasi KA. Namun, gejala dan tanda
klinis sedikit dijumpai pada kelompok kombinasi KK (Gambar 4.2). Setelah
diberikan pengobatan, dilakukan penilaian efek samping obat pada kedua
Demam Pucat Hepatomegali Splenomegali
Gejala dan tanda klinis sebelum
pengobatan
Tabel 4.2. Efek samping pemberian obat
Efek Samping Kinin-Azitromisin
n (%)
Terdapat perbedaan bermakna pada pengamatan efek samping obat pada
kedua kelompok (P < 0,05). Pada kelompok yang mendapat kombinasi KA,
ada 21 anak (17,4%) mengeluhkan kepala pusing, 6 anak (5%) muntah dan
Setelah pengamatan selama 28 hari, terdapat perbedaan yang
bermakna pada hari ke-2 dimana parasitemia pada kedua kelompok menjadi
negatif. Artinya, angka kesembuhan mencapai 100% pada kedua kelompok.
Sedangkan pada pengamatan hari ke-7 dan 28, parasitemia masih tetap
negatif (Gambar 4.3). Hal ini menunjukkan tidak dijumpainya rekrudensi pada
BAB 5. PEMBAHASAN
Parasit malaria yang resisten terhadap banyak obat merupakan tantangan
terapeutik terbesar di bidang pelayanan kesehatan di hampir seluruh daerah
endemik malaria.8 Saat ini, P.falciparum sangat resisten terhadap klorokuin
dijumpai pada kebanyakan daerah endemik malaria. Resistensi terhadap
sulfadoksin-pirimetamin juga telah luas dijumpai dan bertambah dengan
cepat. Resistensi terhadap meflokuin ditemukan di beberapa negara yang
menggunakan terapi ini (seperti Thailand, Kamboja dan Vietnam) dan
penyebarannya telah meningkat dalam 6 tahun terakhir ini.32
Konsekuensi terjadinya resistensi terhadap obat antimalaria sangat
memprihatinkan. Dimana, saat obat antimalaria yang murah tidak lagi
bekerja, namun terapi alternatif lain tersedia dengan harga mahal. Jika obat
yang tersedia tidak lagi dapat menyembuhkan, maka morbiditas meningkat,
bahkan di awal kasus malaria tanpa komplikasi sekalipun. Oleh karena itu,
kombinasi obat antimalaria yang baru sangat dibutuhkan dikarenakan
resistensi banyak obat yang telah meningkat ini, dimana obat tersebut dapat
menyembuhkan penderita tanpa memakan waktu lebih lama dari terapi
standar yang ada.8 Pada studi ini, peneliti berkeinginan menemukan terapi
alternatif kombinasi antimalaria jika terapi standar tidak tersedia.
Alasan sederhana mengkombinasikan antimalaria adalah untuk
mempersingkat lama pengobatan, meningkatkan kepatuhan dan
menurunkan resistensi parasit yang meningkat akibat mutasi selama
pengobatan.8 Pada penelitian ini, peneliti ingin melihat angka kesembuhan
terhadap penyakit malaria falsiparum tanpa komplikasi pada anak dengan
menggunakan obat kombinasi KA dan KK.
Alkaloid kinkona telah digunakan sebagai antimalaria selama lebih
dari 350 tahun. Kinin, merupakan alkaloid kinkona, masih efektif sebagai
pengobatan malaria falsiparum yang resisten dan digunakan secara luas.
Berkembangnya resistensi P.falciparum terhadap kinin terus terjadi walaupun
lambat dan tidak lengkap dibandingkan antimalaria lainnya, seperti klorokuin,
meflokuin dan sulfadoksin-pirimetamin.33 Di daerah yang dapat dijumpai
strain resisten banyak obat, pemberian terapi kinin dan tetrasiklin selama 7
hari, angka kesembuhan masih mencapai lebih dari 90% pada penderita
malaria falsiparum tanpa komplikasi.34,35
Azitromisin, digunakan secara luas, merupakan bentuk turunan dari
antimikroba makrolida, telah menunjukkan aktivitas intrinsik membunuh
P.falciparum secara in vitro25 baik sebagai pengobatan maupun
profilaksis.36,37 Secara umum, azitromisin bekerja lambat dalam pengobatan
malaria falsiparum, dan karena itu perlu dikombinasikan dengan obat dengan
waktu kerja cepat sehingga menimbulkan efek yang menguntungkan. Terapi
falsiparum terbaik karena menimbulkan respon klinis yang sangat baik dan
memperlambat timbulnya resistensi terhadap antimalaria.38
Studi mengenai profilaksis menemukan bahwa azitromisin juga
memiliki efikasi yang tinggi dalam mencegah terjadinya malaria vivax.39
Untuk anak dengan malaria tanpa komplikasi, WHO merekomendasikan
penggunaan oral kinin dengan dosis 8 mg/kgbb/3 dosis selama 7 hari.40
Azitromisin menunjukkan sinergisme dengan kinin dalam pengobatan
P.falciparum invitro.6 Pada studi yang menggunakan kombinasi dengan KA
menunjukkan efikasi yang tinggi dalam pengobatan malaria falciparum tanpa
komplikasi. Kombinasi KA ditoleransi dengan baik, kinin (30 mg /kg terbagi 3
dosis per hari) dan azitromisin (≥ 1 gram /hari) selama 3 hari, efektif bagi
pengobatan malaria falsiparum resisten multi obat.5 Studi di Thailand, pada
orang dewasa penderita malaria falsiparum tanpa komplikasi dengan
pemberian kombinasi KA sebanyak 3 kali sehari, menunjukkan kombinasi ini
aman dan manjur.41 Pada studi ini, peneliti mengkombinasikan kinin oral
dengan dosis 10 mg/kgBB/hari terbagi 3 dosis selama 4 hari pertama
dan dilanjutkan selama 3 hari dengan dosis 5 mg/kgBB/hari terbagi 3 dosis
dikombinasikan dengan azitromisin menggunakan dosis 10 mg/kgBB/hari
sekali sehari selama 3 hari pertama pada anak penderita malaria tanpa
komplikasi. Hasilnya, angka kesembuhan mencapai 100% dan tidak dijumpai
Efek samping berupa kulit kemerahan setelah penggunaan azitromisin
selama 4 minggu dikeluhkan pada 0,67% kasus.37 Efek samping yang lebih
sering ditemukan dari penggunaan kombinasi KA adalah kinkonisme dan
perubahan gelombang elektrokardiografi (EKG) dimana didapati
perpanjangan interval QT.41 Kinkonisme, diartikan sebagai gejala yang
berupa telinga berdenging (tinnitus) dan/atau pusing, dikeluhkan oleh 97%
sukarelawan. Pemberian kombinasi KA berhubungan dengan singkatnya
lama terjadinya kinkonisme.5
Pada studi ini, kami menemukan perbedaan efek samping yang
bermakna pada kedua kelompok, dimana pusing merupakan efek samping
yang paling sering dikeluhkan oleh 21 anak (P=0.0001) pada kelompok KA.
Dan hanya 6 anak (P =0.012) yang muntah dan 6 anak (P =0.052) yang
mengeluhkan tinnitus pada kelompok KA. Pada kelompok kinin-klindamisin,
ada 4 anak (3.3%, P =0.0001) mengeluhkan pusing dan 1 anak (0.8 %, P =
0.052) mengalami tinnitus. Tidak ada anak yang muntah setelah meminum
obat kombinasi kinin-klindamisin selama 28 hari pemantauan.
Klindamisin adalah antibiotik golongan linkomisin yang bersifat
antiplasmodia dan aman diberikan pada anak. Klindamisin, biasanya
dikombinasikan dengan kinin, telah digunakan secara luas di Amerika
Selatan dan telah terbukti efektif pada dewasa dan anak penderita malaria
beberapa penelitian mengenai pemberian kombinasi KK jangka pendek telah
dilakukan di beberapa daerah endemik.42,44
Di Gabon, 88% anak-anak penderita malaria falsiparum tanpa
komplikasi telah berhasil diterapi dengan kombinasi KK jangka pendek.42
Studi lain yang dilakukan di Gabon mendapati 92% orang dewasa sembuh
setelah pemberian kombinasi tersebut.43 Penelitian lainnya mendapati angka
kesembuhan mencapai lebih dari 97% pada 20 hari setelah pemberian KK
selama 3 hari pada anak di Gabon bagian barat.45 Pada studi ini, pemberian
kinin selama 7 hari yang dikombinasikan dengan klindamisin selama 3 hari,
didapati angka kesembuhan mencapai 100%, dan tidak didapati rekrudensi
pada pengamatan selama 28 hari.
6.1. Kesimpulan
Hasil penelitian ini menunjukkan tidak ada perbedaan angka kesembuhan
pada pada anak yang menerima kombinasi KA maupun kombinasi KK pada
pengobatan malaria falsiparum tanpa komplikasi, sehingga kombinasi kedua
obat ini dapat dijadikan terapi alternatif. Kelompok yang menerima KK
mendapat efek samping yang lebih ringan dibandingkan yang menerima
kombinasi KA.
6.2. Saran
Bagi pemerintah Kabupaten Mandailing Natal khususnya Dinas Kesehatan
setempat, hasil penelitian ini dapat dijadikan bahan pertimbangan sebagai
terapi alternatif jika terdapat kendala dalam penggunaan terapi standar pada
anak penderita malaria falsiparum tanpa komplikasi. Dan perlu diadakannya
sosialisasi kepada petugas-petugas kesehatan di kecamatan setempat
mengenai manfaat pengobatan malaria falsiparum tanpa komplikasi pada
anak dikarenakan masih tingginya resistensi terhadap klorokuin.
Pemerintah setempat juga diharapkan dapat bekerjasama dengan
masyarakat untuk memutus rantai penularan nyamuk oleh karena tingginya
angka kejadian malaria di Kabupaten Mandailing Natal.
37
RINGKASAN
diketahui P.falciparum resisten terhadap klorokuin ataupun daerah yang
sensitivitas terhadap klorokuinnya diragukan harus diterapi dengan obat
selain klorokuin. Sehingga, pada akhir tahun 2004 Departemen Kesehatan
Republik Indonesia telah melakukan perubahan standar pengobatan malaria
falsiparum dengan menggunakan kombinasi artesunate-amodiakuin. Selain
terapi standar ini, ada juga kombinasi obat lain yang bisa digunakan sebagai
alternatif dalam pengobatan malaria falsiparum antara lain kombinasi KA
atau kombinasi KK.
Penelitian ini bertujuan untuk mengetahui apakah terdapat perbedaan
kesembuhan antara kombinasi KA dengan kombinasi KK sebagai alternatif
dalam pengobatan malaria falsiparum tanpa komplikasi pada anak.
Uji klinis acak terbuka dilakukan di Sekolah Dasar hingga Sekolah
Menengah Umum di Kecamatan Gunung Baringin, Tanjung Julu, Purba,
Adian Jior, Gunung Manaon, Pagarantonga, Panyabungan Jae, Kabupaten
Mandailing Natal, Propinsi Sumatera Utara pada bulan Juli hingga Agustus
2007.
Sampel penelitian adalah penderita malaria falsiparum yang berusia
antara 5 sampai 18 tahun yang ditetapkan dengan pemeriksaan apusan
darah tepi dengan pewarnaan Giemsa sesuai prosedur dan dibaca oleh
tenaga laboratorium yang terlatih, dengan terlebih dahulu mengisi lembar
PSP, melakukan anamnesis dan pemeriksaan fisik pada sampel. Bila
ditemukan P. falciparum maka anak tersebut dimasukkan dalam penelitian.
Parasit aseksual dihitung dalam 200 sel darah putih. Sampel yang memenuhi
kriteria kemudian dibagi menjadi dua kelompok secara acak sederhana,
yaitu: kelompok pertama mendapat pengobatan kinin per oral selama 7 hari
dengan dosis 10 mg/kgbb/hari terbagi 3 dosis selama 4 hari pertama
dilanjutkan 5 mg/kgbb/hari terbagi 3 dosis selama 3 hari dan diberikan
azitromisin per oral selama 3 hari pertama dengan dosis 10 mg/kgbb/hari
sekali sehari, sedangkan kelompok kedua mendapat pengobatan kinin per
oral selama 7 hari dengan dosis 10 mg/kgbb/hari terbagi 3 dosis
selama 4 hari pertama dilanjutkan 5 mg/kgbb/hari terbagi 3 dosis
selama 3 hari diberikan klindamisin per oral selama 3 hari pertama dengan
dosis 10 mg/kgbb/hari terbagi 2 dosis. Semua obat antimalaria diberikan
sesudah makan. Jika anak muntah dalam 15 menit setelah pemberian obat,
dosis yang sama diberikan kembali.
Selama penelitian dilakukan pencatatan rutin terhadap tanda dan
gejala malaria, riwayat obat-obatan yang pernah dikonsumsi dan efek
samping pengobatan. Pemeriksaan fisik dan apusan darah tepi ulangan
dilakukan pada hari ke-2, 7 dan 28.
Dapat disimpulkan bahwa penggunaan kombinasi kinin-azitromisin
dan kombinasi kinin-klindamisin dapat digunakan sebagai pilihan alternatif
kombinasi kinin-azitromisin memiliki efek samping yang lebih tinggi
dibandingkan kelompok kombinasi kinin-klindamisin.
SUMMARY
Malaria is still a major health problem for children in tropical countries in the
world. In areas with falciparum malaria resistant to chloroquin or areas with
doubtful sensitivity of chloroquin must be treated with alternative drugs other
Republic had changed the protocol therapy of malaria falciparum to
combination of artesunate-amodiaquine due to many resistance cases
founded. Other than this standart therapy, there are alternative drugs in
treating falciparum malaria, such as combination of quinine-azithromycin or
combination of quinine-clindamycin.
The main purpose of this study is to compared the efficacy of
artesunate monotherapy with quinine-azithromycin combinations as an
alternative treatment of falciparum malaria without complication.
This was a randomized open label trial of elementary to high school
students at subdistrict Gunung Baringin, Tanjung Julu, Purba, Adian Jior,
Gunung Manaon, Pagarantonga, Panyabungan Jae, in district of Mandailing
Natal, Sumatera Utara Province on July to August 2007.
Sample of this study were children suffered from falciparum malaria
from 5 to 8 years old that confirmed with Giemsa’s thin and thick blood smear
and was read by a well-trained analyst, after inform consent obtained from
sample, anamnesis and physical examination had been done. If there was
any P. falciparum then we include the child into the study. Asexual form of
paracytes are counted from 200 white blood cells. Samples that eligible
according the inclusion criteria then being divided with simple randomised
into 2 groups. Group I received quinine orally for 7 days with dosage
10mg/KgBW/3 doses for the first 4 days continued with 5mg/kgBW/3 doses
10mg/kgBW and group II received quinine orally for 7 days with dosage
10mg/KgBW/3 doses for the first 4 days continued with 5mg/kgBW/3 doses
for 3 days combined with clindamycin orally for the first 3 days with dosage
10mg/kgBW/2 doses. All anti malarial drugs were taken after meal. If a child
vomited 15 minutes after the drug was given, we could repeat it with the
same dose.
During study, we took routine note of sign and symptoms of malaria,
history of medication taken and adverse effects of medication. Physical
examination and repeated blood smear was done on days 2,7 and 28.
We can conclude that combination of quinine-azithromycin or
combination of quinine-clindamycin can be considered as an alternative
therapy for uncomplicated falciparum malaria, but combination of
quinine-azithromycin have more serious adverse reactions than combination of
quinine-clindamycin.
DAFTAR PUSTAKA
1. Daily JP. Malaria. Dalam: Gershon AA, Hotez PJ, Katz SL, penyunting. Krugman’s infectious diseases of children. Edisi ke-11. Philadelphia: Mosby; 2004. h. 337-52
2. Krause PJ. Malaria (Plasmodium). Dalam: Behrman ER, Kliegman MR, Jonson BH, penyunting. Nelson textbook of pediatrics. Edisi ke-17. Philadelphia: Saunders; 2004. h. 1139-43
4. World Health Organization. Roll back malaria. Malaria control in complex emergencies: an inter-agency field handbook. Geneva: WHO; 2002
5. Miller RS, Wongsrichanalai C, Buathong N, McDaniel P, Walsh DS, Knirsch C, et al. Effective treatment of uncomplicated plasmodium falciparum malaria with azithromycin-quinine combinations: A randomized, dose-ranging study. Am J Trop Med Hyg. 2006; 74(3):401-6 6. Ohrt C, Willingmyre GD, Lee P, Knirsch C, Milhous W. Assessment of
azithromycin in combination with other antimalarial drugs against plasmodium falciparum in vitro. Antimicrob Agents Chemother. 2002; 46(8):2518-24
7. Lell B, Kremsner PG. Clindamycin as an antimalarial drug: review of clinical trials. Antimicrob Agents Chemother. 2002; 46:2315-20
8. Kremsner PG, Krishna S. Antimalarial combinations. Lancet. 2004; 364:285-94
9. Taylor TE, Strickland GT. Malaria. Dalam: Strickland GT, penyunting. Hunter’s tropical medicine and emerging infectious disease. Edisi ke-8. Philadelphia: W.B. Saunders Company; 2000. h. 614-43
10. Krogstad DJ. Plasmodium species (malaria). Dalam: Mandell GL, Bennett JE, Dolin R, penyunting. Mandell, douglas, and bennett’s principles and practice of infectious diseases. Edisi ke-5. Philadelphia: Churchill Livingstone; 2000. h. 2817-31
11. Ditjen pemberantasan penyakit menular dan penyehatan lingkungan departemen kesehatan RI. Pedoman tatalaksana kasus malaria di Indonesia: gebrak malaria. Jakarta: Bakti Husada; 2005. h. 1-38
12. Wilson CM. Plasmodium species (malaria). Dalam: Long SS, Pickering LK, Prober CG, penyunting. Principles and practice of pediatric infectious disease. Edisi ke-2. Philadelphia: Churchill Livingstone; 2003. h. 1295-1301
13. Soedarmo SS, Garna H, Hadinegoro SR, Satari HI. Malaria. Dalam : Buku ajar infeksi & pediatrik tropis. Edisi ke-2. Jakarta: IDAI; 2008. h.
408-37 43
14. Centre for Disease Control and Prevention. Life cycle of malaria. Diunduh dari: http://www.dpd.cdc.gov/dpdx. Diakses Oktober 2008
15. Malaria. Dalam: Pickering LK, Baker CJ, Long SS, Mcmillan JA, penyunting. Red Book: 2006 report of the committee on infectious diseases. Edisi ke-27. United States of America: American Academy of Pediatrics; 2006. h. 435-41
16. World Health Organization. Roll back malaria partnership. Malaria treatment. Geneva: WHO; 2004
17. Baird JK. Drug therapy: effectiveness of antimalarial drugs. N Engl J Med. 2005; 352(15):1565-77
19. Bosman A, Olumese P. Current trends in malaria treatment: artemisinin-based combination therapy. WHO. 2004; 112:h.1-2
20. World Health Organization. Guidelines for the treatment of malaria. Geneva: WHO; 2006
21. Brunton L, Parker K, Blumenthal D, Buxton I. Goodman & gilman’s: manual of pharmacology and therapeutics. Edisi ke - 11. New York: McGraw Hill; 2008. h. 661-94
22. White NJ. Quinine pharmacokinetics and toxicity in cerebral and uncomplicated falciparum malaria. Am J Med. 1982; 73:564-72
23. Sukarban S, Zunilda SB. Obat malaria. Dalam:. Sulistia GG, Setiabudi R, Suyatna FD, Purwantyastuti, Nafrialdi, penyunting. Farmakologi dan terapi. Edisi ke-4. Jakarta: Gaya Baru; 1995. h. 545-59
24. Gingras BA, Jensen JB. Activity of azithromycin (CP-62,993) and erythromycin against chloroquine-sensitive and chloroquine-resistant strains of Plasmodium falciparum in vitro. Am J Trop Med Hyg. 1992; 47:378-82
25. Ohrt C, Willingmyre GD, Lee P, Knirsch C, Milhous W. Assessment of azithromycin in combination with other antimalarial drugs against
Plasmodium falciparum in vitro. Antimicrob Agents Chemother. 2002; 46:2518-24
26. Nakornchai S, Konthiang P. Activity of azithromycin or erythromycin in combination with antimalarial drugs against multidrug-resistant
Plasmodium falciparum in vitro. Acta Tropica. 2006; 100:185-91
27. Andersen SL, Ager A, McGreevy P, Schuster BG, Wesche D, Kuschner R, et al. Activity of azithromycin as a blood schizontocide against rodent and human plasmodia in vivo. Am J Trop Med Hyg. 1995; 52(2):159-61 28. Lell B, Kremsner PG. Clindamycin as an antimalarial drug: review of
clinical trials. Antimicrob Agents Chemother. 2002; 46:2315-20
29. Setiabudy R. Antimikroba lain. Dalam:. Sulistia GG, Setiabudi R, Suyatna FD, Purwantyastuti, Nafrialdi, penyunting. Farmakologi dan terapi. Edisi ke-4. Jakarta: Gaya Baru; 1995. h. 675-85
30. Ramhater M, Noedl H, Winkler H, Graninger W, Wernsdorfer H,
Kremsner PG, et al. In vitro activity and interaction of clindamycin combined with dihydroartemisinin against Plasmodium falciparum. Antimicrob Agents Chemother. 2003; 47(11):3494-99
31. Madiyono B, Moeslichan S, Sastroasmoro S, Budiman I, Purwanti SH. Perkiraan besar sampel. Dalam: Sastroasmoro S, Ismael S. Dasar-dasar metodologi penelitian klinis. Edisi ke-2. Jakarta: Sagung Seto; 2002. h. 259-86
32. Nosten F, van Vugt M, Price R, Luxemburger C, Thway KL, Brockman A, et al. Effects of artesunate-mefloquine combination on incidence of
33. Pukrittayakamee S, Wanwimolruk S, Stepniewska K, Jantra A, Huyakorn S, Looareesuwan S, et al. Quinine pharmacokinetic-pharmacodynamic relationships in uncomplicated falciparum malaria. Antimicrob Agents Chemother 2003; 47:3458-63
34. Looareesuwan S, Wilairatana P, Vanijanonta S, Kyle D, Webster K. Efficacy of quinine-tetracycline for acute uncomplicated falciparum malaria in Thailand. Lancet 1992; i:367-70
35. Nontprasert A, Pukrittayakamee S, Kyle DE, Vanijanonta S, White NJ. Antimalarial activity and interactions between quinine, dihydroquinine, and 3-hydroxyquinine against P.falciparum in vitro. Trans R Soc Trop Med Hyg 1996; 90:553-5
36. Andersen SL, Oloo AJ, Gordon Dm, Ragama OB, Aleman GM, Berman JD, et al. Successful double-blinded, randomized, placebo-controlled field trial of azithromycin and doxycycline as prophylaxis for malaria in western Kenya. Clin Infect Dis. 1998; 26(1):146-50
37. Taylor WR, Richie TL, Fryauff DJ, Ohrt C, Picarima H, Tang D, et al. Tolerability of azithromycin as malaria prophylaxis in adults in northeast Papua, Indonesia. Antimicrob Agents Chemother. 2003; 47(7):2199-2203 38. Dunne MR, Singh N, Shukla M, Valecha N, Bhattacharyya PC, Patel K,
et al. A multicenter study of azithromycin, alone, and in combination with chloroquine, for the treatment of acute uncomplicated Plasmodium falciparum malaria in India. JID 2005; 191:1582-8
39. Heppner DG Jr, Walsh DS, Uthaimongkol N, Tang DB, Tulyayon S, Permpanich B, et al. Randomized, controlled double-blind trial of daily oral azithromycin in adults for the prophylaxis of Plasmodium vivax
malaria in western Thailand. Am J Trop Med Hyg 2005; 73:842-9d
40. Le JM, Jullien V, Tetanye E, Tran A, Rey E, Treluyer JM, et al. Quinine pharmacokinetics and pharmacodynamics in children with malaria caused by plasmodium falciparum. Antimicrob Agents Chemother. 2005; 49(9):3658-62
41. Noedl H, Krudsood S, Chalermratana K, Silachamroon U, Leowattana W, Tangpukdee N, et al. Azithromycin combination therapy with artesunate or quinine for the treatment of uncomplicated Plasmodium falciparum
malaria in adults: a randomized, phase 2 clinical trial in Thailand. CID 2006; 43:1264-70
42. Kremsner PG, Winkler S, Brandts C, Neifer S, Bienzle U, Graninger W. Clindamycin in combination with chloroquine or quinine is an effective therapy for uncomplicated Plasmodium falciparum malaria in children from Gabon. J Infect Dis 1994; 169:467-70
43. Kremsner PG, Wildling E, Jenne L, Graninger W, Biennzle U.
44. Kremsner PG, Radlif P, Metzger W, Wildling E, Mordmuller B, et al. Quinine plus clindamycin improves chemotherapy of severe malaria in children. Antimicrob. Agents Chemother 1995; 39:1603-5
45. Vaillant M, Luty MA, Tshopamba P, Lekoulu F, Mayombo J, Georges AJ, et al. Therapeutic efficacy of clindamycin in combination with quinine for treating uncomplicated malaria in a village dispensary in Gabon. Trop Med Int Health 1997; 2:917-9
Lampiran 1
LEMBAR PERSETUJUAN SETELAH PENJELASAN (PSP)
Dengan ini saya / orang tua dari :
Nama : ... Jenis kelamin: LK / PR
Umur : ...Tahun ...Bulan Alamat : ...
Desa ...Kecamatan ...
Setelah mempelajari dan mendapat penjelasan yang sejelas-jelasnya
mengenai penelitian dengan judul ‘Kombinasi kinin-azitromisin
Setelah mengetahui dan menyadari sepenuhnya risiko yang mungkin terjadi, dengan ini saya menyatakan bahwa saya mengijinkan dengan rela saya / anak saya menjadi subjek penelitian tersebut dengan catatan sewaktu-waktu bisa mengundurkan diri apabila merasa tidak mampu untuk mengikuti penelitian ini.
Demikian pernyataan ini diperbuat dengan sebenarnya dengan penuh kesadaran dan tanpa paksaan dari siapapun juga.
Panyabungan, ...2007
Yang membuat pernyataan
(...)
Saksi :
Kepala Desa / Kepala Puskesmas Peneliti
(...) (dr. Yunnie Trisnawati) Lampiran 2
LEMBAR PENJELASAN
Penjelasan kepada orang tua subyek diberikan secara lisan dan dilakukan
anamnesis / wawancara dengan keterangan sebagai berikut:
” Bapak/Ibu, pertama saya akan menjelaskan tentang penyakit malaria.
Malaria adalah penyakit infeksi yang disebabkan oleh parasit yang ditularkan
melalui nyamuk anopheles. Malaria seringkali diawali oleh demam,
menggigil, berkeringat, pucat, dan gejala lainnya. Malaria sering diderita oleh
juga dapat terjangkit malaria seperti orang dewasa, namun gejala yang
ditimbulkan biasanya lebih berat dan sering menyebabkan ketidakhadiran
anak di sekolah, serta mengganggu kegiatan dan perilaku anak di rumah
sehari-hari. Bapak/ibu, setelah saya dapat mengetahui anak bapak/ibu
menderita malaria dari pemeriksaan darah tepi, dengan persetujuan /
kesediaan bapak/ibu akan kami beri obat yang dapat memusnahkan parasit
malaria di dalam tubuhnya, sehingga kita harapkan anak bapak/ibu dapat
melakukan kegiatan di sekolah dan di rumah dengan baik tanpa ada
gangguan akibat malaria. Anak bapak/ibu akan saya beri dua jenis obat.
Obat pertama dan kedua ada 2 jenis obat. Obat pertama diminum 7 hari dan
pada hari ke-5 akan ditambahkan dengan obat lain yang diminum selama 3
hari. Obat kedua diberikan dua jenis obat, obat pertama diberikan selama 7
hari dan obat kedua diberikan selama 3 hari. Saya akan melakukan
pemantauan jumlah parasit malaria dari pemeriksaan darah tepi anak
bapak/ibu pada hari 2, 7 dan 28 setelah meminum obat untuk melihat
kesembuhan. Dan saya akan mengambil data yang berhubungan dengan
pemberian obat yang kami berikan dengan kesembuhan anak bapak/ibu dari
malaria.”
Demikian penjelasan yang dapat saya sampaikan kepada orang tua pasien
agar mengerti tindakan apa yang akan dilakukan dan apa manfaatnya.
Medan, 2007
Peneliti,
Lampiran 3
LEMBAR KUESIONER
KOMBINASI KININ-AZITROMISIN DIBANDINGKAN DENGAN KOMBINASI KININ-KLINDAMISIN PADA PENGOBATAN MALARIA FALSIPARUM TANPA KOMPLIKASI PADA ANAK
Nomor urut pemeriksaan : ...
Puskesmas : ……….
Nama lengkap : ...
Penghasilan orangtua : Rp.../bulan Tingkat pendidikan / orangtua : AYAH IBU
6 Nyeri epigastrium
7 Muntah
8 Mencret
9 Pucat
10 Lain-lain
PEMERIKSAAN FISIK / LABORATORIUM
NO VARIABEL H0 H2 H7 H28
1 Berat Badan
2 Tinggi Badan
3 Frekuensi
Jantung
4 Frekuensi
5 Suhu Tubuh
6 Hepar ...
cm bac kanan
... cm bac kanan
7 Limpa Schuffner...
... Hacket... ...
Schuffner.. ... Hacket... ...
8 Plasmodium falciparum
9 Parasitemia
Lampiran 4
Lampiran 5
RIWAYAT HIDUP
Nama lengkap : dr. Yunnie Trisnawati
Tanggal lahir : 3 April 1979
Tempat lahir : Lhokseumawe
NIP : -
Alamat : Komplek Taman Setia Budi Indah
Blok N no.30, Medan
Nama suami : dr. M. Jalaluddin Assuyuthi Chalil Batubara
Nama anak : -
Pendidikan
1. Sekolah Dasar di Taman Muda 3 Tamansiswa Arun, tamat
2. Sekolah Menegah Pertama di Taman Dewasa 2 Tamansiswa
Arun, tamat tahun 1994
3. Sekolah Menegah Atas di Taman Madya Tamansiswa Arun, tamat
tahun 1997
4. Fakultas Kedokteran Universitas Sumatera Utara, Medan, tamat
tahun 2003
Riwayat Pekerjaan : -
Pendidikan Spesialis
1. Adaptasi di BIKA FK. USU : 01-07-2004 s/d 30-12-2004
2. Pendidikan Tahap I : 01-01-2005 s/d 30-12-2005
3. Pendidikan Tahap II : 01-01-2006 s/d 30-12-2006 4. Pendidikan Tahap III : 01-01-2007 s/d 30-12-2007 5. Pendidikan Tahap IV : 01-01-2008 s/d 30-12-2008
6. Penelitian : Juli sampai Agustus 2007