TINJAUAN PUSTAKA
2.1 Tumbuhan Keben (Barringtonia asiatica L. Kurz)
Tumbuhan keben (B. asiatica) merupakan tanaman yang tumbuh subur di daerah
pesisir asia tropis dan pasifik. Pohon keben dapat tumbuh lebih dari 25 meter.
Buahnya tidak dapat dimakan dan beracun, bunganya berwarna putih dan merah
muda. Walaupun biji dari buah tersebut berbahaya bagi manusia, namun beberapa
bagian lain dari B. asiatica memiliki khasiat sebagai obat dan ini telah menjadi
budaya di beberapa negara.
Di filipina, rebusan daun tumbuhan keben dapat digunakan sebagai obat
sakit perut dan rematik, sedangkan di pulau salomon rebusan kulit pohon keben
digunakan untuk obat sakit gigi. Tumbuhan keben dapat tumbuh dengan baik di
daerah pesisir pantai (Elvitch, 2006).
Tumbuhan keben atau biasa disebut pohon pembunuh ikan tumbuh secara
intensif di pesisir pantai kawasan asia tropis dan pasifik. Di filipina tumbuhan ini
dikenal dengan nama botong dan biasa ditemukan di sepanjang pantai diseluruh
kota dan sering di tanam sebagai penahan angin dan tempat berteduh. Di
indonesia nama lain tumbuhan keben didaerah pulau jawa dan sumatera adalah
Butun dan Putat Laut (Arief, 2001).
Semua bagian dari tumbuhan keben diketahui memiliki senyawa saponin
yang dapat menghambat aktivitas serangga. Hama yang dapat dikendalikan
dengan ekstrak biji B. asiatica adalah Crocidolomia pavonana F. Yang mana
merupakan hama yang dapat menyebabkan kehilangan hasil hampir 100% pada
tanaman kubis (Danar dan Rismanto, 2008).
Tumbuhan keben mempunyai beberapa manfaat, diantaranya adalah sebagai
berikut :
- Kandungan tanin dan saponin yang terdapat pada tumbuhan keben yang
- Rebusan kulit pohonnya dapat digunakan untuk mengobati hernia, bijinya
untuk mengobati penyakit kulit dan kulit kayunya untuk mengobati
tuberculosis. Tumbuhan keben juga memiliki kandungan anti-epilepsi
yang dapat mengobati epilepsy (Margaretha, 2014).
Klasifikasi Buah Keben hasil identifikasi tumbuhan di laboratorium
Herbarium Medanense, adalah sebagai berikut :
Kingdom : Plantae
Divisi : spermatophyta
Class : Dicotyledoneae
Ordo : Lecythidales
Famili : lecythidaceae
Genus : Barringtonia
Spesies : Barringtonia asiatica (L) Kurz
Nama Lokal : Keben
(a) (b)
2.2 Metabolit Sekunder
Metabolit sekunder merupakan sekelompok senyawa kimia yang dijumpai
diseluruh tanaman dan memiliki ciri khas untuk setiap tanaman tertentu (Manito,
1981).
Senyawa metabolit sekunder umumnya mempunyai kemampuan
bioaktifitas dan berfungsi sebagai pelindung tumbuhan tersebut dari gangguan
hama penyakit untuk tumbuhan itu sendiri dan lingkungannya. Secara umum
metabolit sekunder dalam bahan hayati dikelompokkan berdasarkan sifat dan
reaksi khas suatu metabolit sekunder dengan pereaksi tertentu. Metabolit sekunder
dapat dikelompokkan sebagai alkaloida, terpenoida, flavonoida, tanin, saponin,
dan glikosida (Harborne, 1987).
2.2.1 Alkaloida
Alkaloida merupakan senyawa kimia bersifat basa yang mengandung satu atau
lebih asam nitrogen, umumnya tidak berwarna, dan berwarna jika mempunyai
struktur kompleks dan bercincin aromatik. Alkaloida pada umumnya juga
mempunyai kereaktifan fisiologi yang menonjol, sehingga oleh manusia alkaloida
sering dimanfaatkan sebagai pengobatan. Secara kimia alkaloida merupakan
suatau golongan heterogen. Secara fisik, alkaloida dipisahkan dari kandungan
tumbuhan lainnya sebagai garamnya dan sering diisolasi sebagai kristal
hidroklorida atau pikrat (Harborne,1987).
Alkaloida merupakan golongan zat tumbuhan sekunder yang terbesar.
Alkaloida memiliki kemampuan sebagai antibakteri. Mekanisme yang diduga
adalah dengan cara mengganggu komponen penyusun peptidoglikan pada sel
bakteri, sehingga lapisan dinding sel terbentuk secara utuh dan menyebabkan
kematian sel tersebut (Robinson, 1995).
2.2.2 Flavonoida
Flavonoida adalah senyawa yang terdiri dari C6-C3-C6. Flavonoida umumnya
terdapat pada tumbuhan sebagai glikosida. Gugusan gula bersenyawa pada satu
karbon C5 dan C7 pada cincin A. Pada cincin B gugus hidroksil atau alkoksil
terdapat pada karbon C3 dan karbon C4 (Sirait, 2007).
Flavonoida pada tumbuhan berfungsi dalam pengaturan fotosintesis, kerja
antimikroba dan antivirus, dan kerja terhadap serangga (Robinson, 1995). Adapun
fungsi flavonoida dalam kehidupan manusia yaitu sebagai stimulant pada jantung,
hesperidin mempengaruhi pembuluh darah kapiler. Flavon terhidrolisasi bekerja
sebagai diuretik dan antioksidan pada lemak (Sirait, 2007).
2.2.3 Tanin
Tanin tersebar luas pada tumbuhan berpembuluh, dalam angiospermae terdapat
khusus pada jaringan kayu. Tanin dapat bereaksi dengan protein membentuk
kopolimer baik yang tidak larut dalam air. Dalam industri, tanin adalah senyawa
yang berasal dari tumbuhan yang mampu mengubah kulit hewan yang mentah
menjadi kulit siap pakai karena kemampuannya menyambung silang protein
(Harborne, 1987).
Secara kimia terdapat dua jenis tanin yaitu:
1. Tanin terhidrolisis
Tanin terhidrolisis biasanya berupa senyawa amorf, higrokopis, berwarna
coklat kuning yang larut dalam air membentuk larutan koloid bukan
larutan sebenarnya. Semakin murni tanin, semakin kurang kelarutannya
dalam air dan semakin mudah diperoleh dalam bentuk kristal. Tanin ini
larut dalam pelarut organik yang polar, tetapi tidak larut dalam pelarut
organik nonpolar seperti benzene atau kloroform (Robinson, 1995).
2. Tanin terkondensasi
Tanin terkondensasi secara biosintesis dapat dianggap terbentuk dengan
cara kondensasi katekin tunggal (galokstekin) yang membentuk senyawa
dimer dan kemudian oligimer yang lebih tinggi. Proantosianidin
merupakan nama lain dari tanin terkondensasi karena jika direaksikan
dengan asam panas, beberapa ikatan karbon penghubung satuan terputus
2.2.4 Terpenoida
Kebanyakkan senyawa terpenoida terdapat bebas dalam jaringan tanaman, tidak
terikat dengan senyawa-senyawa yang lain, tetapi banyak diantara mereka yang
terdapat sebagai glikosida, ester dari asam organik dan dalam beberapa hal terikat
dengan protein (Sastrohamidjojo, 1996).
Terpenoid adalah senyawa alam yang terbentuk dengan proses biosintesis
terdistribusi luas dalam dunia tumbuhan dan hewan, terpenoida tidak saja
ditemukan pada tumbuhan tingkat tinggi namun juga pada terumbu karang dan
mikroba. Struktur terpenoida dibangun oleh molekul isoprena, CH2=C (CH3)-
CH= CH2, Kerangka terpenoida terbentuk dari dua atau lebih banyak satuan unit
isoprena. Terpenoida dapat juga dikelompokkan menjadi monoterpen,
seskuiterpen, diterpen, triterpen, dan tetraterpen (Sirait, 2007).
Triterpenoid merupakan golongan terpenoida yang berpotensi sebagai
antimikroba. Selain itu senyawa ini banyak digunakan untuk menyembuhkan
penyakit gangguan kulit. Triterpenoida memiliki sifat antijamur, insektisida,
antibakteri, dan antivirus (Robinso, 1995).
2.2.5 Saponin
Saponin berasal dari kata sapo yang berarti sabun, karena sifatnya menyerupai
sabun. Saponin adalah glikosida triterpenoid. Saponin merupakan senyawa yang
berasa pahit, berbusa dalam air serta larut dalam air dan alkohol tetapi tidak larut
dalam eter. Saponin paling cocok diekstraksi dengan menggunakan metanol dan
etanol (Robinson, 1995).
Saponin dapat digunakan sebagai racun dan antimikroba ( jamur, bakteri,
dan virus). Saponin terdiri dari dua, yaitu saponin steroid dan saponin triterpenoid.
Saponin memberikan hasil yang lebih baik sebagai antibakteri jika mengunakan
pelarut polar seperti etanol 70%. Pada konsentrasi rendah saponin menyebabkan
hemolisis sel darah merah sehingga berfungsi sebagai antibakteri (Harborne,
2.3 Ekstraksi
Ekstrak adalah sediaan pekat yang diperoleh dengan mengekstraksi zat aktif dari
simplisia nabati dan simplisia hewani menggunakan pelarut yang sesuai,
kemudian semua atau hampir semua pelarut diuapkan dan massa atau serbuk yang
tersisa diperlakukan sedemikian hingga memenuhi baku yang ditetapkan.
Ekstraksi adalah suatu proses pemisahan kandungan senyawa kimia dari jaringan
tumbuhan atau hewan dengan menggunakan penyari tertentu (Depkes RI, 2000).
Suatu metode ekstraksi dengan menggunakan pelarut dapat dilakukan dengan
beberapa cara yaitu:
1. Maserasi
Maserasi berasal dari kata macerace yang artinya melunakkan. Maserat
adalah hasil penarikan simplisia dengan cara maserasi, sedangkan
maserasi adalah cara penarikan simplisia dengan merendam simplisia
tersebut dalam cairan penyari dengan beberapa kali pengocokan atau
pengadukan pada temperatur kamar, sedangkan remaserasi merupakan
pengulangan penambahan pelarut setelah dilakukan penyaringan maserat
pertama, dan seterusnya (Depkes RI, 2000).
2. Perkolasi
Perkolasi adalah ekstraksi dengan menggunakan pelarut yang selalu baru
sampai penyaringan sempurna, umumnya dilakukan pada temperatur
ruangan. Proses ini terdiri dari tahapan pengembangan bahan, tahap
maserasi antara dan tahap perkolasi sebenarnya (penetesan/penampungan
ekstrak) yang terus menerus sampai ekstrak yang diinginkan habis
tersaring. Tahap pengembangan bahan dan maserasi antara dilakukan
dengan maserasi serbuk menggunakan cairan penyari sekurang-kurangnya
3 jam, hal ini penting terutama untuk serbuk yang keras dan bahan yang
mudah mengembang (Harborne, 1987).
3. Refluks
Refluks adalah proses ekstraksi dengan pelarut pada temperatur titik
didihnya selama waktu tertentu dan pelarutnya akan terdestilasi menuju
dasarnya adalah ekstraksi berkesinambungan. Bahan yang akan diekstraksi
direndam dengan cairan penyari dalam labu alas bulat yang dilengkapi
dengan alat pendingin tegak, lalu dipanaskan sampai mendidih. Cairan
penyari akan menguap, uap tersebut akan diembunkan dengan pendingin
tegak dan akan kembali menyari zat aktif dalam simplisia tersebut,
demikian seterusnya (Depkes RI, 2000).
4. Sokletasi
Sokletasi adalah ekstraksi kontiniu yang menggunakan alat soklet, dimana
pelarut akan terdestilasi dari labu menuju pendingin, kemudian jatuh
membasahi dan merendam sampel yang mengisi bagian tengah pada
soklet, setelah pelarut mencapai tinggi tertentu maka akan turun kedalam
labu destilasi (Depkes RI, 2000).
5. Infudasi
Infudasi yaitu ekstraksi dengan pelarut air pada temperatur penangas air,
bejana infus tercelup dalam penangas air mendidih, pada temperatur
terukur 960-980C selama waktu tertentu (Depkes RI, 2000).
6. Dekoktasi
Dekoktasi adalah infus pada waktu yang lebih lama dan temperatur sampai
titik didih air (Depkes RI, 2000).
Metode pemisahan yang mungkin paling sederhana adalah partisi, yang
banyak digunakan sebagai tahap awal pemurnian ekstrak. Partisi menggunakan
dua pelarut tak bercampur yang ditambahkan kedalam ekstrak tersebut, hal ini
dapat dilakukan secara terus menerus dengan menggunakan dua pelarut yang tak
bercampur yang kepolarannya meningkat. Partisi biasanya dilakukan melalui dua
tahap :
1. Air/petroleum eter ringan (heksana) untuk menghasilkan fraksi non
polar lapisan organik
2. Air/diklorometan atau air/kloroform atau air/etil asetat untuk membuat
fraksi agak polar dilapisan organik. Ini merupakan metode pemisahan
yang mudah dan mengandalkan kelarutan bahan alam dan bukan
2.4 Bakteri
Nama bakteri berasal dari kata”bakterion” (bahasa yunani) yang berarti tongkat atau batang. Sekarang namanya dipakai untuk menyebutkan sekelompok
mikroorganisme yang bersel satu, pembiakan dengan cara pembelahan diri, serta
demikian kecilnya sehingga hanya tampak dengan mikroskop (Dwidjoseputro,
1998).
Bakteri adalah mikroorganisme bersel tunggal yang tidak terlihat oleh mata, tetapi
dengan bantuan mikroskop, Mikroorganisme tersebut akan terlihat. Ukuran
bakteri berkisar antara panjang 0,5 sampai 10 µ dan lebar 0,5 sampai 2,5 µ
tergantung dari jenisnya (µ=1 mikron=0,001 mm).
Walaupun terdapat berbagai jenis bakteri, tetapi hanya beberapa
karakteristik bentuk sel yang ditemukan yaitu :
1. Bentuk bulat atau cocci (tunggal = coccus)
2. Bentuk batang atau bacilli (tunggal = bacillus)
3. Bentuk spiral atau spirilli (tunggal = spirillum)
4. Bentuk koma atau vibrous (tunggal = vibrio)
Sel-sel ini dapat dijumpai dalam keadaan tunggal, berpasangan, kelompok kecil,
gerombolan atau rantai (Buckle, et al. 2009).
2.4.1 Penggolongan Bakteri
Bakteri dibedakan atas dua kelompok berdasarkan komposisi dinding sel
serta sifat pewarnaannya, yaitu bakteri gram positif dan bakteri gram negatif.
1. Bakteri Gram Positif
Bakteri gram positif memiliki kandungan peptidoglikan yang tinggi
dibandingkan garam negatif. Pada bakteri gram positif polimer dapat
mencapai 50%. Pada beberapa genus bakteri gram positif terdapat asam
teikoat. Asam ini dapat mengikat ion magnesium , ion Mg berperan dalam
membran sitoplasma sehingga memberikan ketahanan terhadap suhu yang
tinggi. Pada umumnya kandungan lipid pada dinding sel bakteri gram
2. Bakteri Gram Negatif
Dinding sel bakteri gram negatif lebih kompleks dibandingkan gram
positif. Perbedaan utama adalah adanya lapisan membran luar, yaitu
meliputi peptidoglikan. Kehadiran membran ini pada menyebabkan
dinding sel bakteri gram negatif kaya akan lipid (11-22 %). Lapisan ini
tidak hanya terdiri dari fosfolipid saja seperti membran plasma, tetapi juga
mengandung lipid lainnya , polisakarida dan protein (Waluyo, L 2007).
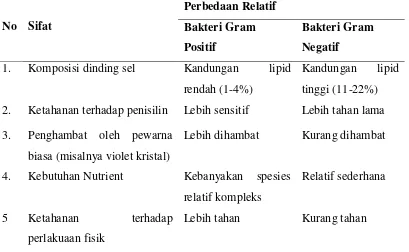
Perbedaan relatif sifat bakteri gram positif dan bakteri gram negatif dapat
dilihat sebagai berikut:
Tabel 2.1 Perbedaan bakteri gram positif dan bakteri gram negatif (Fardiaz, 1992).
No Sifat
1. Komposisi dinding sel Kandungan lipid
rendah (1-4%)
Kandungan lipid
tinggi (11-22%)
2. Ketahanan terhadap penisilin Lebih sensitif Lebih tahan lama
3. Penghambat oleh pewarna
biasa (misalnya violet kristal)
Lebih dihambat Kurang dihambat
4. Kebutuhan Nutrient Kebanyakan spesies
relatif kompleks
Relatif sederhana
5 Ketahanan terhadap
perlakuaan fisik
Lebih tahan Kurang tahan
2.4.2 Bakteri Staphylococcus aureus
S. aureus merupakan bakteri gram positif, sel-sel berbentuk bola,
berdiameter 0,5 sampai 1,5 µm, terdapat tunggal dan berpasangan, dan secara
khas membelah diri pada lebih dari satu bidang sehingga membentuk gerombol
yang tak teratur. Dinding sel mengandung dua komponen utama yaitu
peptidoglikan serta asam tekoat yang berkaitan dengannya. tumbuh lebih cepat
dan lebih banyak dalam keadaan aerobik pada suhu optimum 35-40 0C (Pelczar
Koloni pada pembenihan padat terbentuk bulat halus, menonjol dan
berkilau membentuk pigmen. Bakteri ini terdapat kulit, selaput lendir, bisul dan
luka. Dapat menimbulkan penyakit melalui kemampuannya berkembang biak dan
menyebar luas dalam jaringan (Jawets, 2001).
Gambar 2.2 Bakteri Staphylococcus aureus
2.4.3 Bakteri Escherichia coli
Bakteri E. coli merupakan bakteri gram negatif, berbentuk batang lurus
1,1-1,5 µm x 2,0-6,0 µm. Tumbuh dengan mudah pada medium nutrien sederhana
(Pelczar & Chan, 1988).
E. coli merupakan bakteri yang secara normal terdapat di dalam usus dan berperan
dalam proses pembusukan sisa-sisa makanan. Keberadaan bakteri ini merupakan
parameter ada tidaknya materi fekal di dalam suatu habitat khususnya air. E. coli
adalah salah satu jenis bakteri yang ada dalam tinja manusia dan dapat
mengakibatkan gangguan pencernaan seperti diare (Gaman, 1992).
2.4.4 Faktor Yang Mempengaruhi Pertumbuhan Bakteri
1. Air, Bakteri memerlukan air dalam konsentrasi tinggi (cukup) disekitarnya
karena diperlukan bagi pertumbuhan dan perkembangbiakan. Air
merupakan pengantar semua bahan gizi yang diperlukan sel dan untuk
membuang semua zat-zat yang tak diperlukan keluar sel.
2. Garam-garam anorganik, diperlukan untuk mempertahankan keadaan
koloidal dan tekanan osmotik didalam sel, untuk memelihara
keseimbangan asam-basa, dan berfungsi sebagai bagian enzim atau
sebagai aktivator reaksi enzim.
3. Mineral, selain karbon dan nitrogen, sel-sel hidup memerlukan sejumlah
mineral-mineral lainnya untuk pertumbuhannya.
Belerang (sulfur): seperti halnya dengan nitrogen, sulfur juga
merupakan substansi sel.
Fosfor-Fosfat (PO4): diperlukan sebagai komponen asam-asam
nukleat dan berupa ko-enzim.
Aktivator enzim: sejumlah mineral diperlukan sebagai aktivator enzim seperti Mg, Fe juga K dan Ca.
4. Sumber Nitrogen, banyak isi sel terutama protein, mengandung nitrogen.
Pada bakteri, nitrogen mencapai 10% berat kering sel bakteri. Nitrogen
yang dipakai oleh bakteri diambil dalam bentuk: NO3, NO2, NH3, N2 dan
R-NH2 (R- radikal organik). Kebanyakan mikroorganisme menggunakan
NH3 sebagai satu-satunya sumber nitrogen.
5. CO2, diperlukan dalam proses-proses sintesis dengan timbulnya asimilasi
CO2 didalam sel (Nasution, 2014).
2.5 Antibakteri
Antibakteri adalah senyawa yang digunakan untuk mengendalikan
pertumbuhan bakteri yang bersifat merugikan. Pengendalian pertumbuhan
mikroorganisme bertujuan untuk mencegah penyebaran penyakit infeksi, dan
mencegah pembusukan serta perusakan bahan oleh mikroorganisme
Mekanisme penghambatan terhadap pertumbuhan bakteri oleh senyawa
antibakteri dapat berupa perusakan dinding sel dengan cara menghambat
pembentukannya atau mengubahnya setelah selesai terbentuk, perubahan
permeabilitas membran sitoplasma sehingga menyebabkan keluarnya bahan
makanan dari dalam sel, perubahan molekul protein dan asam nukleat,
penghambatan kerja enzim dan penghambatan sintesis asam nukleat dan protein.
Didalam bidang farmasi, bahan antibakteri dikenal dengan bahan antibiotik, yaitu
suatu subtansi kimia yang dihasilkan oleh mikroba dan dapat menghambat
pertumbuhan mikroba lain. Senyawa antibakteri dapat berkerja secara
bakteriostatik, bakteriosidal, dan bakteriolitik (Pelczar & Chan, 1998).
Berdasarkan sifat toksisitas selektifnya, senyawa antimikrobial
mempunyai 3 macam efek terhadap pertumbuhan mikrobia yaitu:
1. Bakteriostatik memberikan efek dengan cara menghambat pertumbuhan
tetapi tidak membunuh. Senyawa bakteriostatik sering kali menghambat
sintesis protein atau mengikat ribosom. Hal ini ditunjukkan dengan
penambahan antimikrobia pada kultur yang berada pada fase logaritmik.
Setelah penambahan zat antimikrobia pada fase logaritmik didapatkan
jumlah sel total maupun jumlah sel hidup adalah tetap.
2. Bakteriosida memberikan efek dengan cara membunuh sel tetapi tidak
terjadi lisis sel atau pecah sel. Hal ini ditunjukkan dengan penambahan
antimikrobia pada kultur mikrobia yang berada pada fase logaritmik.
Setelah penambahan zat antimikrobia pada fase logaritmik didapatkan
jumlah sel total tetap sedangkan jumlah sel hidup menurun.
3. Bakteriolitik menyebabkan sel menjadi lisis atau pecah sehingga jumlah
sel berkurang atau terjadi kekeruhan setelah penambahan antimikrobia.
Hal ini ditunjukkan dengan penambahan antimikrobia pada kultur
mikrobia yang berada pada fase logaritmik. Setelah penambahan zat
antimikrobia pada fase logaritmik, jumlah sel total maupun jumlah sel
2.5.1 Uji Aktivitas Antibakteri
Uji aktivitas antibakteri merupakan suatu metode untuk menentuakan
tingkaat kerentanan bakteri terhadap zat antibakteri utuk mengetahui senyawa
murni yang memiliki aktivitas antibakteri. Uji aktivitas antibakteri dapat
dilakukan dengan metode difusi dan pengenceran (dilusi). Disc diffusion test atau
uji difusi cakram dilakukan dengan mengukur diameter zona bening (clear zone)
yang merupakan petunjuk adanya respon penghambatan pertumbuhan bakteri oleh
suatu senyawa antibakteri diencerkan hingga diperoleh beberapa macam
konsentrasi, kemudian masing-masing konsentrasi ditambahkan suspensi bakteri
uji dalam media cair (Hermawan, dkk., 2007).
Metode difusi merupakan salah satu metode yang sering digunakan.
Metode difusi dapat dilakukan dengan cara yaitu metode silinder, metode
lubang/sumuran yaitu membuat lubang pada agar padat yang telah diinokulasi
dengan bakteri. Jumlah dan letak lubang disesuaikan dengan tujuan penelitian,
kemudian lubang diinjeksikan dengan ekstrak yang akan diuji. Setelah dilakukan
inkubasi, pertumbuhan bakteri diamati untuk melihat ada tidaknya daerah
hambatan disekeliling lubang (Kusmayati dan Agustini, 2007).
Prinsip metode pengenceran adalah senyawa antibakteri diencerkan hingga
diperoleh beberapa macam konsentrasi, kemudian masing-masing konsentrasi
ditambahkan suspensi bakteri uji dalam media cair. Perlakuan tersebut akan
diinkubasi dan diamati ada atau tidaknya pertumbuhan bakteri, yang ditandai
dengan terjadinya kekeruhan. Larutan uji senyawa antibakteri pada kadar terkecil
yag terlihat jernih tanpa adanya pertumbuhan bakteri uji, ditetapkan sebagai Kadar
Hambat Minimal (KHM) atau Minimal Inhibiory Concentration (MIC). Larutan
yang ditetapkan sebagai KHM tersebut selanjutnya dikultur ulang pada media cair
tanpa penambahan bakteri uji ataupun senyawa antibakteri, dan diinkubasi selama
18-24 jam. Media cair yang tetap terlihat jernih setelah diinkubasi ditetapkan
sebagai Kadar Bunuh Minimal (KBM) atau Minimal Bactericidal Concentration
2.5.2 Pengukuran Aktivitas Antibakteri
Penentuan kerentanan patogen bakteri terhadap obat-obatan antimikroba
dapat dilakukan dengan salah satu metode utama yaitu dilusi dan difusi.
Metode-metode tersebut dapat dilakukan untuk memperkirakan baik potensi antibiotik
dalam sampel maupun kerentanan mikroorganisme dengan menggunakan
organisme uji standar yang tepat dan sampel obat tertentu untuk perbandingan.
Metode-metode utama yang dapat digunakan adalah :
a. Metode Dilusi
Sejumlah antimikroba dimasukkan kedalam medium bakteriologi padat atau cair,
biasanya digunakan pengenceran dua kali lipat zat antimikroba. Medium akhirnya
diinokulasi dengan bakteri yang diuji dan diinokulasi. Tujuan akhirnya adalah
mengetahui seberapa banyak jumlah antimikroba yang diperlukan untuk
menghambat pertumbuhan atau membunuh bakteri yang diuji. Uji kerentanan
dilusi agar membutuhkan waktu yang lama.
b. Metode difusi
Metode yang paling sering digunakan adalah metode difusi agar dengan
menggunakan cakram kertas, cakram kaca, pencetak lubang. Prinsip metode ini
adalah mengukur zona hambatan pertumbuhan bakteri yang terjadi akibat difusi
zat yang bersifat antibakteri di dalam media padat melalui pencadang. Daerah
hambatan pertumbuhan bakteri adalah daerah jernih disekitar cakram. Luas daerah
hambatan berbanding lurus dengan aktivitas antibakterinya maka semakin luas
daerah hambatnya. Metode ini dipengaruhi oleh banyak faktor fisik dan kimia,
misalnya : ph, suhu, zat inhibitor, sifat dari media dan kemampuan difusi, ukuran
2.5.3 Mekanisme Kerja Antibakteri
Mekanisme kerja antibakteri yaitu sebagai berikut :
a. Inhibitor Sintesis Dinding Sel
Kerusakan dinding sel atau penghambatan pada pembentukannya dapat
menyebabkan sel menjadi lisis. Dinding sel bakteri terdiri dari polipeptidoglikan
yang merupakan kompleks mukopeptida (glikopeptida). Zat antibakteri
menghambat sintesis peptidoglikan dinding sel bakteri dengan menghambat kerja
enzim traspeptidase dan enzim rasemase alanin atau dengan menghambat sintesa
asam muramat. Senyawa penisislin dan sefalosforin yang secara struktur mirip
dan senyawa-senyawa yang tidak mirip seperti sikloserin, vankomisin dan
basitrain merupakan zat antibakteri yang bekerja menghambat sintesis dinding sel
(Setiabudi dan Gan, 1995).
b. Inhibitor Fungsi Membran Sel
Biasanya merupakan senyawa yang bekerja langsung pada membran sel
mikroorganisme, mempengaruhi permeabilitas dan menyebabkan kebocoran
senyawa-senyawa intraseluller. Dalam hali ini termasuk senyawa yang bersifat
detergen seperti polimiksin dan amfoterisin B yang berikatan dengan sterol-sterol
dinding sel. Kerusakan membran sel akan mengakibatkan keluarnya berbagai
komponen penting dalam sel bakteri yaitu protein, asam nukleat, dan lain-lain
(Setiabudi dan Gan, 1995).
c. Inhibitor Sintesis Protein Sel
Unit ribosom pada bakteri adalah 30S dan 50S. Sintesis protein dihambat dengan
mempengaruhi fungsi subunit ribosom 30S dan 50S sehingga menyebabkan
penghambatan sistesis protein yang reversibel dan mengakibatkan kematian sel.
Obat bakteriostatik ini meliputi kloramfenilok, golongan tetrasiklin, eritromisin
d. Inhibitor Sintesis Asam Nukleat
Antibakteri yang tergolong kelompok ini adalah golongan kuinolon dan rifampin.
Dalam hal ini, derivat rifampin akan berikatan dengan enzim polimerase-RNA
(pada sub unit) sehingga menghambat sintesis RNA oleh enzim tersebut.
Sementara asam nalidiksat bekerja dengan menganggu sintesis DNA (Bilbiana
dan Hastowo, 1992).
e. Inhibitor Metabolit Sel Bakteri
Dalam kelompok ini termasuk sulfonamida. Pada umumnya bakteri memerlukan
para-aminobenzoat (PABA) untuk sisntesis asam folat yang diperlukan dalam
sintesis purin. Sulfonamida memiliki struktur seperti PABA, sehingga
penggunaan sulfonamida menghasilkan asam folat yang tidak berfungsi (Bilbiana