19
BAB II
TINJAUAN PUSTAKA
2.1 Pati
Pati atau amilum adalah karbohidrat kompleks yang tidak larut dalam air, berwujud bubuk putih, tawar dan tidak berbau. Barangkali tidak ada satu senyawa organik lain yang tersebar begitu luas sebagai kandungan tanaman seperti halnya pati. Dalam jumlah besar, pati dihasilkan dari dalam daun-daun hijau sebagai wujud penympanan sementara dari produk fotosintesis. Pati juga tersimpan dalam bahan makanan cadangan permanen untuk tanaman, dalam biji, jari-jari teras, kulit batang, akar tanaman menahun dan umbi. Pati merupakan 50-65% berat kering biji gandum dan 80% bahan kering umbi kentang (Claus, et al., 1970).
Pati berbentuk granul atau butir-butir kecil dengan lapisan-lapisan yang karakteristik. Lapisan-lapisan ini serta ukuran dan bentuk granul seringkali khas bagi beberapa spesies tanaman sehingga dapat digunakan untuk identitas tanaman asalnya (Claus, et al., 1970).
Tanaman yang mengandung pati digunakan dalam farmasi seperti Zea mays (jagung), Oryza sativa (beras), Solanum tuberosum (kentang), Triticum aesticum (gandum), Maranta arundinacea (garut), Ipomoea batatas (ketela rambat) dan Manihot utilissima (ketela pohon) (Claus, et al., 1970).
Secara umum pati terdiri dari 20% bagian yang larut air (amilosa) dan 80% bagian yang tidak larut dalam air (amilopektin). Amilosa merupakan
▸ Baca selengkapnya: yang tidak termasuk ke dalam media penyimpanan adalah….
(2)20
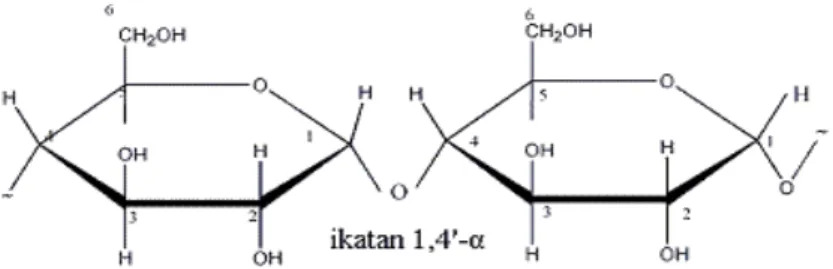
molekul yang lurus, terdiri dari 250 sampai 300 satuan D-glukopiranosa dan dihubungkan secara seragam oleh ikatan alfa-1,4-glukosida yang cenderung menyebabkan molekul tersebut dianggap berbentuk seperti uliran (helix). Amilopektin terdiri dari 1000 atau lebih satuan glikosa yang kebanyakan juga dihubungkan dengan hubungan alfa-1,4. Namun terdapat juga sejumlah hubungan alfa-1,6 yang terdapat pada titik-titik percabangan. Jumlah hubungan semacam ini terdapat kurang lebih 4% dari jumlah hubungan atau satu untuk setiap 25 satuan glukosa.
Oleh karena perbedaan struktur ini maka amilosa lebih larut dalam air dibandingkan dengan amilopektin. Hal ini digunakan untuk memisahkan kedua komponen tersebut. Pemisahan yang lebih efisien dilakukan dengan mengendapkan dan membuat senyawa kompleks dari amilosa dengan pereaksi yang sesuai meliputi bermacam-macam etanil atau nitroparafin. Amilosa bereaksi dengan iodium membentuk senyawa kompleks berwarna biru tua, sedangkan amilopektin memberikan warna violet kebiruan atau ungu.
2.1.1 Amilosa
Amilosa merupakan polisakarida, polimer yang tersusun dari glukosa sebagai monomernya. Tiap-tuap monomer terhubung dengan ikatan 1,4-glikosidik. Amilosa merupakan polimer tidak bercabang yang bersama-sama dengan amilopektin menjadi komponen penyusun pati. Dalam masakn, amilosa memberi efek keras bagi pati atau tepung (Whistler dan Paschall, 1984).
21
Gambar 2.1 Rumus struktur amilosa 2.1.2 Amilopektin
Amilopektin merupakan polisakarida yang tersusun dari monomer G-glukosa. Amilopektin merupakan molekul raksasa dan mudah ditemukan karena menjadi satu dari dua senyawa penyusun pati, bersama-sama dengan amilosa. Walaupun tersusun dari monomer yang sama, amilopektin berbeda dengan amilosa, yang terlihat dari karakteristik fisiknya. Secara struktural, amilopektin terbentuk dari rantai glukosa yang terikat dengan ikatan 1,4-glikosidik, sama dengan amilosa.
Namun demikian, pada amilopektin terbentuk cabang-cabang (sekitar tiap 20 mata rantai glukosa) dengan ikatan 1,6-glikosidik. Amilopektin tidak larut dalam air. Dalam produk makanan amilopektin bersifat merangsang terjadinya proses mekar (puffing) dimana produk makanan yang berasal dari pati yang kandungan amilopektinnya tinggi akan bersifat ringan, porus, garing dan renyah. Kebalikannya pati dengan kandungan amilosa tinggi, cenderung menghasilkan produk yang keras, karena proses mekarnya terjadi secara terbata (Whistler dan Paschall, 1984).
22
Gambar 2.2 Rumus struktur amilopektin
2.2 Pati Tapai Padat (Brem)
Pati tapai padat atau Sari Tapai Padat merupakan produk yang dibuat dari sari tapai yang dipanaskan sampai kental dan didinginkan sampai bentuknya padat. Pati tapai padat mempunyai rasa yang manis atau manis keasaman, tekstur padat, kering tidak lembek, warna putih kekuningan sampai kecoklatan dan larut di mulut (Astwan dan Astwan, 1991). Pati tapai padat di masyarakat dikenal dengan nama Brem. Brem berdasarkan cara pembuatanya dikenal dua macam jenis brem, yaitu brem cair dan brem padat. Brem cair merupakan jenis minuman yang rasanya manis, sedikit asam dan bewarna merah dengan kandungan alkohol 3-10%. Brem padat merupakan jenis makanan tradisional yang bewama putih sampai kecoklatan dengan rasa manis keasaman yang merupakan hasil fermentasi yang dipadatkan (Sri, 2008). Brem padat banyak diproduksi di daerah Jawa Timur, Jawa Tengah seperti Boyolali, Wonogiri, Caruban dan Madiun dengan menggunakan ketan putih sebagai bahan baku. Bentuk brem padat yang paling umum diperjual belikan adalah bentuk persegi empat (kotak) atau bulat pipih (Astwan dan Astwan, 1991).
23
Bahan dasar tapai ketan adalah ketan putih yang merupakan salah satu vareitas padi. Menurut Steenis (1988), ketan putih merupakan sejenis berm yang mempunyai klasifikasi sebagai berikut:
Divisio : Spermatophyta Sub divisio : Angiospermae Kelas : Monocotyledoneae Ordo : Poales
Famili : Gramineae/Poaeeae Genus : Oryza
Spesies : Oryza sativa L. Var. Glutinosa
Ketan putih hampir seluruhnya terdiri dari pati yang merupakan suatu polimer yang terdiri dari dua komponen utama yaitu amilosa dan amilopektin.
Pembuatan pati tapai padat dapat dibagi menjadi dua tahap antara lain: proses pengolahan bahan baku menjadi tapai dan proses pengolahan tapai menjadi pati tapai padat. Proses pengolahan bahan baku menjadi tapai meliputi: pemilahan bahan baku, perendaman, pencucian, pemasakan, pendinginan, pemberian ragi, fermentasi dan pengepresan sedangkan proses pengolahan tapai menjadi pati tapai padat meliputi; pemasakan air tapai, pengadukan, pencetakan dan pengeringan, pemotongan, pembungkusan dan pengepakan (Meigia, dkk., 2004).
2.3 Amok Am terhadap a tidak lebih Pemerian: Kelarutan karbon tet Baku pem POM, 199 Pe mengamat tersebut te Chain ber penisilin. kemudian kebutuhan semisintet ksisilin G moksisilin m anhidrat. Me h dari 1050 serbuk hab : sukar laru traklorida da mbanding B 95). nisilin dite ti pertumb erkontamina rhasil meng Pertama d digunakan n meningkat tis. Penisili Gambar 2.3 mengandung empunyai p μg per mg C blur, putih, p ut dalam air an dalam kl BPFI; tidak mukan oleh uhan stafil asi oleh jam gisolasi sub digunakan n P.Chrys t. Penisilin in alam dip vi 3 Rumus str g tidak kura potensi setar C16H19N3O praktis tidak r dan meth loroform. k boleh dik h Fleming lokokus te mur. Kemud bstansia ak penisilin n sogenum se terbagi atas peroleh den ruktur amok ang dari 90 ra dengan ti 5S, dihitung k berbau. anol; tidak keringkan s pada tahun ertentu diha dian di ujung ktif dari jam neonatum u emasa per s dua yaitu ngan jalan ksisilin ,0% C16H19 idak kurang g terhadap z larut dalam sebelum dig n 1929 di ambat bila g tahun 193 mur Flemin untuk pem ang dunia penisilin al mengubah 9N3O5S, dih g dari 900 μ zat anhidrat. m benzen, d gunakan (D London, se a bakteri-b 30-an Flore ng yang di makaian sist a kedua k
lam dan pen h struktur k hitung μg dan . dalam Ditjen etelah akteri y dan isebut temik karena nisilin kimia
vii
penisilin alam atau dengan cara sintetis inti penisilin yaitu asam amino penisilat (Munaf, 1994).
Tetapi penemuan ini baru dikembangkan dan digunakan pada permulaan perang dunia kedua di tahun 1941, ketika obat-obat antibakteri sangat diperlukan untuk menanggulangi infeksi dari luka-luka akibat pertempuran (Tan dan Rahardja, 2002)
Menurut Siswandono dan Soekardjo (1995), antibiotika berasal dari sumber-sumber berikut, yaitu Actiomycetales (58,2%), jamur (18,1%), tanaman tinggi (12,1%), Eubacteriales terutama Bacilli (7,7%), binatang (1,8%), Pseudomonales (1,2%) dan ganggang atau lumut (0,9%). Antibiotika dapat dikelompokkan berdasarkan tempat kerja, spektrum aktivitas dan struktur kimianya. Penggolongan antibiotika berdasarkan spektrum aktivitasnya:
1. Antibiotika dengan spektrum luas, efektif baik terhadap Gram-positif maupun Gram-negatif.
Contoh: turunan tetrasiklin, turunan amfenikol, turunan aminoglikosida, turunan makrolida, rifamfisin, beberapa turunan penisilin, seperti ampisilin, amoksisilin, bakampisilin, karbenisilin, hetasilin, rivampisilin, sulbenisilin, dan tikarsilin, dan sebagian besar turunan sefalosporin.
2. Antibiotika yang aktivitasnya lebih dominan terhadap bakteri Gram-positif.
Contoh: Basitrin, eritromisin, sebagian besar turunan penisilin, seperti benzilpenisilin, penisilin G prokain, penisilin V, metisilin Na, nafsilin Na, oksasilin Na, kloksasilin Na, dikloksasilin Na dan floksasilin Na, turunan linkoksamida, asam fusidat dan beberapa turunan sefalosporin.
viii
3. Antibiotika yang aktivitasnya lebih dominan terhadap bakteri Gram-negatif.
Contoh: Kolistin, polimiksin B sulfat dan sulfomisin.
4. Antibiotika yang aktivitasnya lebih dominan terhadap Mycobacteriae (antituberkulosis)
Contoh: Streptomisin, kanamisin, rifampisin, viomisin dan kapreomisin. 5. Antibiotika yang aktif terhadap jamur (anti jamur).
Contoh: Gliseofulfin dan antibiotika polien, seperti nistatin, amfoterisin B dan kandisidin.
6. Antibiotika yang aktif terhadap neoplasma (anti kanker).
Contoh: Aktinomisin, bleomisin, daunorubisin, mitomisin dan mitramisin. Amoksisilin adalah antibiotika golongan β-laktam dengan spektrum luas, digunakan untuk pengobatan infeksi pada saluran napas, saluran empedu dan saluran seni, gonorhu, gastroenteritis, meningitis dan infeksi karena Salmonella sp., seperti demam tipoid. Amoksisilin merupakan turunan penisilin yang tahan asam tetapi tidak tahan terhadap penisilanase. Beberapa keuntungan dibandingkan ampisilin adalah penyerapan obat dalam saluran cerna lebih sempurna, sehingga kadar darah dalam plasma dan saluran seni lebih tinggi, serta adanya makanan tidak mempengaryhi penyerapan obat (Siswandono dan Soekardjo, 1995).
Menurut Munaf (1994), berdasarkan aktivitas antimikrobanya turunan penisilin dibagi menjadi beberapa kelompok sebagai berikut:
1. Penisilin G dan penisilin V yang sangat aktif terhadap kokus gram positif, tetapi mudah dihidrolisir oleh penisilanase. Sehingga obat ini tidak aktif terhadap sebagian besar strain stafilokokus.
ix
2. Penisilin retensi penisilanase seperti metisilin, nafsilin, oksasilin, kloksasilin, diklosasilin, kurang sensitif terhadap mikroorganisme yang sensitif terhadap penisilin G, tetapi merupakan obat pilihan terhadap stafilokokus aureus penghasil penisilanase.
3. Ampisilin, amoksisilin dan hetasilin termasuk satu grup penisilin dimana aktivitas antimikrobanya lebih luas termasuk gram negatif seperti Hemofilus influenza, Eschericia coli, Prosteus mirabilis.
4. Karbenislin, tikarsilin dan azlosilin digunakan untuk Pseudomonas, Enterobacter dan spesies Proteus.
5. Grup pensilin baru. Mezlosin dan piperasilin berguna untuk Klebsiela dan mikroorganisme gram negatif tertentu.
Antibiotika adalah zat yang dibentuk oleh mikroorganisme yang dapat menghambat atau membunuh pertumbuhan mikroorganisme lain. Antibiotika dapat juga dibentuk oleh beberapa hewan dan tanaman tinggi. Di samping itu, berdasarkan antibiotika alam, dapat pula dibuat antibiotika baru secara sintetis parsial yang sebagian mempunyai sifat yang lebih baik. Antibiotika yang berguna hanyalah antibiotika yang mempunyai kadar hambat minimun (KHM) in vitro lebioh kecil dari kadar zat yang dapat dicapai dalam tubuh dan tidak toksik.
Mekanisme antibiotika umumnya:
1. Menghambat biosintetis dinding sel
2. Meninggikan permeabilitas membran sitoplasma 3. Mengganggu sintesis protein normal bakteri
x
Umumnya, antibiotika yang mempengaruhi pembentukan dinding sel atau permeabilitas membran sel bekerja bakterisida, sedangkan yang bekerja pada sintesis protein bekerja bakteriostatik (Mutschler, 1999).
Antibiotika tidak aktif terhadap kebanyakan virus kecil, mungkin karena virus tidak memiliki proses metabolisme sesungguhnya, melainkan tergantung seluruhnya dari proses tuan rumah (Tan dan Rahardja, 2002).
Obat yang digunakan untuk membasmi mikroba, penyebab infeksi pada manusia, ditentukan harus memiliki sifat toksisitas selektif setinggi mungkin. Artinya, obat haruslah bersifat sangat toksik untuk mikroba, tetapi relatif tidak toksis pada hospes. Sifat toksisitas selektif yang absolut belum atau mungkin juga diperoleh (Anonim, 2002).
Mekanisme Kerja
Setelah diabsorpsi amoksisilin didistribusikan ke berbagai jaringan tubuh. Kadar terapi dalam jaringan-jaringan seperti cairan sendi, pleural, pericardium dan empedu. Dalam jumlah kecil ditemukan dalam sekresi prostat, jaringan otak, dan cairan intraokuler (Munaf, 1994).
Amoksisilin adalah derivat-hidroksi dengan aktivitas sama dengan ampisilin. Tetapi resorbsinya lebih lengkap dan pesat dengan kadar darah dua kali lipat. Waktu paruhnya 1-2 jam. Persentasi pengikatan pada protein jauh lebih ringan dari pada penisilin G dan penisilin V. Difusinya ke jaringan dan cairan tubuh lebih baik, antara lain kedalam air liur pasien bronchitis kronis. Kadar bentuk aktifnya dalam kemih jauh lebih tinggi dari pada ampisilin sehingga lebih banyak digunakan pada infeksi saluran kemih. Efek samping berupa gangguan lambung usus (Tan dan Rahardja, 2002).
xi
Amoksisilin merupakan antibiotika dari penisilin semisintetik yang stabil dalam suasana asam, kerja bakterisida, atau pembunuh bakterinya seperti ampisilin. Amoksisilin diabsorbsi dengan cepat dan baik di saluran pencernaan, tidak tergantung adanya makanan dalam lambung dan setelah 1 jam konsentrasinya dalam darah sangat tinggi sehingga efektivitasnya tinggi. Amoksisilin diekskresikan atau dibuang terutama melalui ginjal, dalam air kemih terdapat dalam bentuk aktif. Amoksisilin sangat efektif terhadap organisme gram positif dan gram negatif. Penggunaan amoksisilin seringkali dikombinasikan dengan asam klavunalat untuk meningkatkan potensi dalam membunuh bakteri (Junaidi, 2009).
Dosis: oral 3 kali sehari 375-1000 mg, anak-anak < 10 tahun 3 kali sehari 10 mg/kg, 3-10 tahun 3 kali sehari 250 mg, 1-3 tahun 3 kali sehari 125 mg, 0-1 tahun 3 kali sehari 100 mg, juga diberikan secara i.m/i.v (Tan dan Rahardja, 2002).
2.4 Sirup Kering
Sirup kering adalah suatu campuran padat yang ditambahkan air pada saat digunakan, sediaan tersebut dibuat pada umumnya untuk bahan obat yang tidak stabil dan tidak larut dalam pembawa air. Agar campuran setelah ditambah air membentuk dispersi yang homogen, maka dalam formulanya digunakan bahan pensuspensi atau bahan pendispersi. Komposisi sediaan ini biasanya terdiri dari bahan pensuspensi atau pendispersi, pembasah, pemanis, pengawet, penambah rasa atau aroma, buffer dan zat warna. Obat yang biasa dibuat dalam sediaan sirup kering adalah obat yang tidak stabil untuk disimpan dalam periode waktu tertentu
xii
dengan adanya pembawa air (sebagai contoh obat-obat antibiotik) sehingga lebih sering diberikan sebagai campuran kering untuk dibuat suspensi atau larutan pada saat akan digunakan. Biasanya sirup kering hanya digunakan untuk pemakaian selama satu minggu setelah dalam bentuk cairan (Ansel, 1989).
Adapun kriteria suspensi dan suspensi kering yaitu harus memenuhi krietria tertentu. Kriteria dari suatu sediaan suspensi yang baik adalah :
a. Pengendapan partikel lambat sehingga takaran pemakaian yang serba sama dapat dipertahankan dengan pengocokan sediaan.
b. Seandainya terjadi pengendapan selama penyimpanan harus dapat segera terdispersi kembali apabila suspensi dikocok.
c. Endapan yang terbentuk tidak boleh mengeras pada dasar wadah.
d. Viskositas suspensi tidak boleh terlalu tinggi sehingga sediaan dengan mudah dapat dituang dari wadahnya.
e. Memberikan warna, rasa, bau serta rupa yang menarik. Sedangkan kriteria suatu sediaan suspensi keringyang baik adalah:
a. Kadar air serbuk boleh melebihi batas maksimum. Selama penyimpanan serbuk harus stabil secara fisik seperti tidak terjadi perubahan warna, bau, bentuk partikel dan stabil secara kimia seperti tidak terjadi perubahan pH yang drastis.
b. Pada saat akan disuspensikan, serbuk harus cepat terdispersi secara merata di seluruh cairan pembawa dengan hanya memerlukan sedikit pengocokan atau pengadukan.
c. Bila suspensi kering telah dibuat suspensi maka suspensi kering dapat diterima bila memiliki kriteria dari suspensi.
xiii
2.5 Granulasi
Granulasi adalah proses dimana partikel serbuk diubah menjadi granul. Secara umum granulasi dapat dibedakan menjadi dua jenis, yaitu granulasi basah dan granulasi kering.
a. Granulasi basah
Pada granulasi basah bahan dilembabkan dengan larutan pengikat yang cocok, sehingga serbuk terikat bersama dan terbentuk masaa yang lembab. Pelarut yang digunakan umumnya bersifat volatil sehingga mudah dihilangkan pada saat dikeringkan. Massa lembab kemudian dibagi-bagi sehingga terbentuk nutiran granul.
b. Granulasi kering
Pada granulasi kering obat dan bahan pembantu mula-mula dicetak menjadi tablet yang cukup besar, yang massanya tidak tentu. Selanjutnya tablet yang terbentuk dihancurkan dengan mesin penggranul kering gesekan atau dengan cara sederhana menggunkan alu di atas sebuah ayakan sehingga terbentuk butiran granul.
2.6 Stabilitas sediaan sirup kering
Menurut Syamsuni (2005), salah satu masalah yang dihadapi dalam proses pembuatan suspensi ataupun sirup kering adalah cara memperlambat penimbunan partiket serta menjaga homogenitas partikel. Cara tersebut merupakan salah satu tindakan untuk menjaga stabilitas suspensi atau sirup kering. Beberapa faktor yang mempengaruhi stabilitas nya adalah:
xiv a. Ukuran partikel
Ukuran partikel erat hubungannya dengan luas penampang partikel tersebut serta daya tekan ke atas dari cairan suspensi itu. Hubungan antara ukuran partikel merupakan perbandingan terbalik dengan luas penampangnya. Sedangkan antara luas penampang dengan daya tekan ke atas terdapat hubungan linier. Artinya semakin kecil ukuran partikel semakin besar luas penampangnya (dalam volume yang sama). Sedangkan semakin besar luas penampang partikel, daya tekan keatas cairan akan semakin besar, akibatnya memperlambat gerakan partikel untuk mengendap sehingga untuk memperlambat gerakan tersebut dapat dilakukan dengan memperkecil ukuran partikel (Syamsuni, 2005).
b. Kekentalan (Viskositas)
Kekentalan suatu cairan mempengaruhi pula kecepatan aliran cairan tersebut, semakin kental suatu cairan, kecepatan alirannya semakin turun atau semakin kecil. Kecepatan aliran dari cairan tersebut akan mempengaruhi pula gerakan turun partikel yang terdapat di dalamnya. Dengan demikian, dengan menambah kekentalan atau viskositas cairan, gerakan turun partikel yang dikandungnya akan diperlambat. Perlu diingat bahwa kekentalan suspensi tidak boleh terlalu tinggi agar sediaan mudah dikocok dan dituang (Syamsuni, 2005). c. Jumlah Partikel (Konsentrasi)
Jika di dalam suatu ruangan terdapat partikel dalam jumlah besar, maka partikel akan sulit melakukan gerakan bebas karena sering terjadi benturan antara partikel tersebut. Oleh benturan ini akan menyebabkan terbentuknya endapan zat tersebut, oleh karena itu semakin besar konsentrasi partikel, makin besar
xv
kemungkinannya terjadi endapan partikel dalam waktu yang singkat (Syamsuni, 2005).
d. Sifat atau Muatan Partikel
Suatu suspensi kemungkinan besar terdiri atas beberapa macam campuran bahan yang sifatnya tidak selalu sama. Dengan demikian, ada kemungkinan terjadi interaksi antarbahan yang menghasilkan bahan yang sukar larut dalam cairan tersebut. Karena sifat bahan tersebut sudah merupakan sifat alam, kita tidak dapat mempengaruhinya. Stabilitas fisik suspensi farmasi didefinisikan sebagai kondisi suspensi dimana partikel tidak mengalami agregasi dan tetap terdistribusi merata. Jika partikel mengendap, partikel tersebut akan mudah tersuspensi kembali dengan pengocokan ringan. Partikel yang mengendap ada kemungkinan dapat saling melekat oleh suatu kekuatan untuk membentuk agregasi dan selanjutnya membentuk compacted cake, peristiwa itu disebut “caking” (Syamsuni, 2005).
2.7 Spektrofotometri Ultraviolet
Spektrofotometri serapan merupakan pengukuran suatu interaksi antara radiasi elektromagnetik dengan molekul atau atom dari suatu zat kimia. Teknik yang sering digunakan dalam analisis farmasi meliputi spektrofotometri ultraviolet, cahaya tampak, infra merah dan serapan atom. Jangkauan panjang gelombang untuk daerah ultraviolet adalah 190 - 380 nm, daerah cahaya tampak 380 - 780 nm, daerah inframerah dekat 780 - 3000 nm, dan daerah inframerah 2,5 - 40 µm atau 4000 - 250 cm-1 (Ditjen POM, 1995).
xvi
Radiasi ultraviolet dan sinar tampak diabsorpsi oleh molekul organik aromatik, molekul yang mengandung elektron-π terkonjugasi dan atau atom dengan elektron-n yang menyebabkan transisi elektron di orbital terluarnya dari tingkat energi dasar ke tingkat energi tereksitasi. Besarnya serapan radiasi tersebut sebanding dengan banyaknya molekul analit yang mengabsorpsi sehingga dapat digunakan untuk analisis kuantitatif (Satiadarma, dkk., 2004).
Spektrofotometer UV-VIS adalah pengukuran panjang gelombang dan intensitas sinar ultraviolet dan cahaya tampak yang diabsorbsi oleh sampel. Spektrofotometer UV-VIS biasanya digunakan untuk molekul dan ion anorganik atau kompleks didalam larutan. Sinar ultraviolet berada pada panjang gelombang 400 - 800 nm.
Sebagai sumber cahaya biasanya digunakan lampu hydrogen atau deuterium untuk pengukuran UV dan lampu tungsten untuk pengukuran pada cahaya tampak. Panjang gelombang dari sumber cahaya akan dibagi oleh pemisah panajnag gelombang. Seperti pada prisma atau monokromator. Panjang gelombang adalah jarak antara satu lembah dan satu puncak. Sedangkan frekuensi adalah kecepatan cahaya dibagi dengan panjang gelombang. Bilangan gelombang (V) adalah satu satuan perpanjangan gelombang (Dachriyanus, 2004).
Spektrofotometri merupakan suatu alat yang berguna untuk mempelajari keseimbangan kimia atau untuk menentukan laju reaksi kimia. Zat kimia yang mengambil bagian dalam keseimbangan harus mempunyai spekta absorbsi yang berbeda dan seseorang dengan mudah mengamati variasi absorbsi pada panjang gelombang tertentu untuk setiap zat (Martin,1990).