PENGEMBANGAN TEKNIK ENZYME LINKED IMMUNOSORBENT
ASSAY (ELISA) UNTUK MENDETEKSI ADANYA ANTIBODI
TERHADAP VIRUS INFECTIOUS LARYNGOTRACHEITIS (ILT)
DALAM SERUM AYAM
(Development of an Enzyme-Linked Immunosorbent Assay (ELISA) for
Detection of Antibody Against Infectious Laryngotracheitis (ILT) in
Serum of Chicken)
Key words: ELISA, antibody,Infectious Laryngotrachitis
PENDAHULUAN
Infectious Laryngotracheitis (ILT) adalah penyakit saluran pernafasan pada unggas, terutama ayam
(HANSONdanBAGUST, 1991). Penyakit ini disebabkan
oleh virus, yaitu gallid herpesvirus (MURPHY et al., 1995). Ada 2bentuk penyakit ILT, yaitu bentuk severe
epizootic dan mild enzootic. Bentuk severe epizootic ditandai dengan gejala gangguan pernafasan: batuk, pilek; muntah darah, serta kematian yang tinggi(90%
-100%). Bentuk mild enzootic ditandai dengan kelesuan, penurunan produksi telur, mata berair, radang konjungtiva, pembengkakan sinus orbital, dan penyumbatan hidung (BAGUSTet al., 2000). Virus ILT
hanya memiliki satu tipe antigenic, dengan demikian untuk keperluan serologik cukup digunakan satu strain saja untuk mendeteksi adanya antibodi terhadap virus ILT (BAGUST et al, 2000). Penggunaan ELISA untuk
penyakit unggas sudah banyak dilakukan oleh peneliti sebelumnya diantaranya SLAGHT et al. (1978) . Untuk
ELISA antibodi terhadap virus ILT dalam serum unggas pertama kali dikembangkan oleh MEULEMANS dan HALEN (1982) . Uji ini dikembangkan sebagai uji
alternatif dengan hasil yang cepat, sensitif, dan spesifik.
BAEUR et al., (1999) melaporkan bahwa ELISA
memiliki sensitifitas yang lebih tinggi dibandingkan dengan uji serum netralisasi. Penelitian adanya reaktor
RISA INDRIANI,R.MABDUL ADJID, DARMINTO,danHELMY HAMID
Balai Penelitian Veteriner, PO BOX151, Bogor 16114
ABSTRACT
The aim of this study was to develop an Enzyme-linked immunosorbent assay (ELISA) for detection of antibody against ILT in serum of chickens, therefore this test is available in the laboratory and not dependent on import. Results showed that ELISA for ILT was developed successfully with sensitivity and specificity was98%and 97,14%respectively. The ELISA was able to
describe the dynamic of antibodies respond in experimental chickens following vaccination and artificial infection with ILT virus. It was concluded that this ELISA offers a simple, sensitive and specific antibody assay for detection of antibodies to ILT
virus in chickens arising from vaccination or infection.
Indonesia, yaitu dengan mendeteksi antibodi penyakit tersebut, pernah dilakukan oleh peneliti sebelumnya, menggunakan kit ELISA produk luar negeri(WIYONOet
al., 1996).
Kajian pengembangkan teknik ELISA di laboratorium Virologi Balitvet untuk mengadakan kebutuhan kit ELISA guna keperluan uji serologi terhadap penyakit ILTsehingga tidak tergantung pada produk impor dan ketersediaannya ada setiap saat.
METODOLOGI Penyiapan antigen ELISA ILT
Virus yang dipergunakan adalah virus ILT atenuasi (Laryng-Vac Intervet). Prosedur pembuatan antigen mengacu pada metodeMEULEMANSdanHELEN (1982)
Pembuatan Serum Standar ILT
Serum standar negatif berasal dari ayam spesific pathogenic free (SPF). Sedangkan serum standar dibuat dengan mengacu pada metode MEULEMANSdanHALEN (1982) danYORK et al., (1983) . Titer serum antibodi
Tropbio yaitu, pada group ELISA 7 atau 256 ELISA unit (Eu).
Konjugat dan substrat
Konjugat Rabbit anti-chicken IgG-HRPO (Sigma. Cat. log no. A.9046) dan substrat 2,2-Azino-di-(3-athyl-benzthiazolinsulfonat(6) (ABTS) (Sigma. Cat. log no . A.1888) digunakan dalam penelitian ini.
Prosedur ELISA
Prosedur teknik ELISA yang dikembangkan mengacu pada Manual of Standards for Diagnostic Test and Vaccines (1996).
Penentuan enceran optimal dari antigen, serum dan konjugat
Penentuan enceran antigen, serum dan konjugat yang memberikan reaksi optimal dilakukan dengan checkerboard (MEULEMANS dan HALEN, 1982).
Enceran antigen ILT lOpg/ml, 5pg/ml, 2,5pg/ml dan 1,25pg/ml dalam karbonat-bikarbonat pH 9,6. Serum ILT dan serum negatif ILT diencerkan dalam TENC 1 :100 dan 1 :200. Konjugat diencerkan dalam TENC 1 :2000, 1 :5000 dan 1 :10000. Reaksi ulang dilakukan sebanyak 12 kali. Enceran yang menghasilkan rasio reaksi optimum antara serum positif dan serum negatif dengan nilai lebih besar atau sama dengan 10 digunakan dalam prosedur teknik ELISA.
Penentuan nilai cut-offuntuk ELISA
Nilai cut off reaksi spesifik untuk ELISA yang dikembangkan diperoleh dengan menguji 140 serum ayam SPF. Serum ayam ini telah diuji serum netralisasi (SN) dan hasil negatif terhadap virus ILT. Nilai rata-rata densitas optik (OD) dari seluruh serum yang diuji kemudian ditambah 3 kali nilai deviasi (sd) dijadikan nilai cut offdari uji ELISA.
Evaluasi sensitifitas dan spesifisitas ELISA
Evaluasi sensitifitas dan spesifisitas dilakukan dengan memeriksa serum-serum ayam percobaan di laboratorium, yaitu serum ayam SPF ( belum terinfeksi ILT) sebanyak 140 serum dengan uji SN dibuktikan negatif, dan serum ayam SPF yang diinfeksi secara buatan dengan virus ILT isolat BGR-6; dan BKS-3 sebanyak 100 sampel. Sensitifitas dari uji ELISA
43 6
merupakan porsi dari sampel terinfeksi yang menghasilkan nilai ELISA positif. Sedangkan spesifitas dari uji ELISA merupakan porsi dari sampel bebas ILT yang menghasilkan nilai Elisa negatif (BALDOCK,
1988).
Evaluasi adanya reaksi silang dengan infeksi virus pernafasan lainnya
Untuk mengetahui adanya reaksi ikatan antigen ILT dan antibodi tidak spesifik terhadap virus penyakit pernafasan lain (infectious bronchitis) dilakukan pengujian ELISA.
Aplikasi ELISA dalam mendeteksi antibodi virus ILT dalam serum ayam
Aplikasi ELISA untuk mendeteksi adanya respon antibodi ILT pada serum ayam hewan percobaan. Enam ekor ayam SPF yang divaksin dengan vaksin hidup ILT komersil secara intratrakhea. Kemudian 9 minggu pasca vaksinasi, diinfeksi dengan virus ILT isolat lapang 104 EID50 per 0,1 ml secara intratrakea. Serum dikoleksi dan diuji ELISA pada minggu ke 1- 9 pasca vaksinasi dan 1-3 minggu pasca infeksi.
HASIL DAN PEMBAHASAN
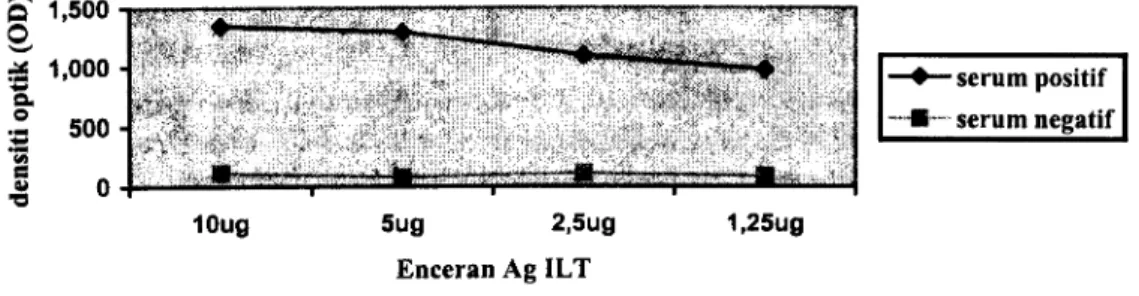
ELISA merupakan salah satu uji serologi, digunakan untuk mendeteksi adanya antigen atau antibodi dalam serum hewan. Teknik ini sangat disukai karena secara umum lebih sensitif, spesifik, sangat efektif dan efisien untuk menguji sampel dalam jumlah besar, serta lebih murah, dan cukup mudah pengerjaannya. Hasil antigen ILT diperoleh 2 ml dengan kandungan protein 1295 pg/ml (metode Lowry). Penggunaan antigen ILT yang memberikan reaksi optimum dalam uji ELISA diperoleh dengan menggunakan sistim checkerboard bersama dengan titrasi konjugat. Empat enceran antigen ( 10 ug; 5 ug; 2,5 ug; 1,25 ug) dengan 3 enceran konjugat (1/10.000; 1/5 .000; 1/2000) diteliti reaksinya dalam ELISA menggunakan satu enceran serum (1/100). Hasil disajikan pada Gambar 1 ; 2; dan 3. Konsentrasi antigen lOpg/ml memberikan reaksi antigen-antibodi terbaik karena memiliki P/N ratio > 10. Hasil enceran konjugat 1/5000 terlihat memberikan reaksi lebih baik dari enceran 1/10.000, tetapi sedikit di bawah enceran 1/2000. Namun enceran 1/5000 dipilih untuk digunakan dalam uji ELISA selanjutnya karena pertimbangan ekonomis serta reaksinya tidak terlalu jauh dengan penggunaan enceran 1/2000.
q 1,500 O
Gambar 1 . Checkerboard Ag ILTdengan enceran serum 1 :100
10ug 5ug 2,5ug 1,25ug
Enceran Ag ILT
Gambar 2. Titrasi konsentrasi Ag untuk optimasi coating mikrotiter
1 2 4 8 16 32 64 128 256 512 1024 2048
Enceran serum positifdalam negatif
Gambar 3. Efek enceran konjugat pada antibodi ILT
Enceran serum positif dalam negatif
-serum positif --M°--serum negatif -~10ug -.g}-5ug -6-2,5u 1,25ug -"-konj. 1/10000 --E-konj . 1/5000 -~ konj. 1/2000
Gambar 4. Kurva standar dengan kombinasi Ag l Oug,konjugat 115000 DAN SERUM 1/100
-Ag ILT 10 ug -- -Kontrol Ag
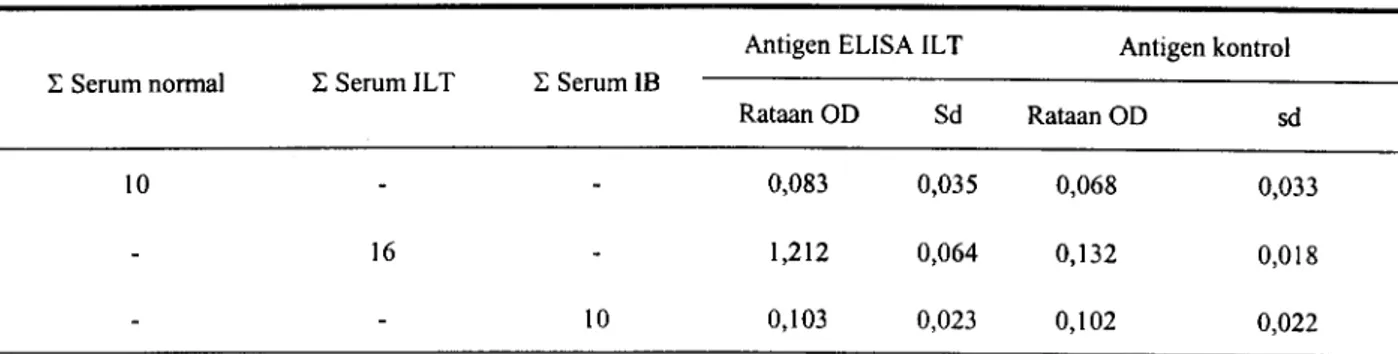
Tabel 1 . Identifikasi reaksi non spesifisik terhadap virus penyakit pemafasan lain
438
E Serum normal 10
Identifikasi reaksi non spesifik antibodi penyakit pemafasan, seperti IB pada uji ELISA ILT memberikan rataan nilai OD 0,103 ± 0,023, sementara dengan antigen kontrol 0,102 ± 0,022 . Dilain fihak rataan nilai OD serum ILT 1,212 ± 0,064; dan antigen kontrol 0,132 ± 0,018 (Tabel 1 .). Gambaran OD tersebut sangat jelas bahwa reaksi silang yang diberikan antigen ELISA ILT dengan serum antibodi IB sangat rendah dan dapat dianggap tidak ada. Hal serupa juga dijumpai oleh MEULEMANS dan HALEN (1982) bahwa tidak ada reaksi silang antara antigen ELISA ILT dengan antibodi IB.
Kurva standar dibentuk dari serum spesifik ILT yang diencerkan dalam serum negatif antibodi ILT. Serum tersebut diuji ELISA ILT pada konsentrasi antigen 10 ug dan enceran konjugat 115000 memperlihatkan nilai OD tertinggi 1,3. Sementara itu
(a) (d)
Sensitifitas = --- Spesifisitas =
---(a)+ (c) (d)+(b)
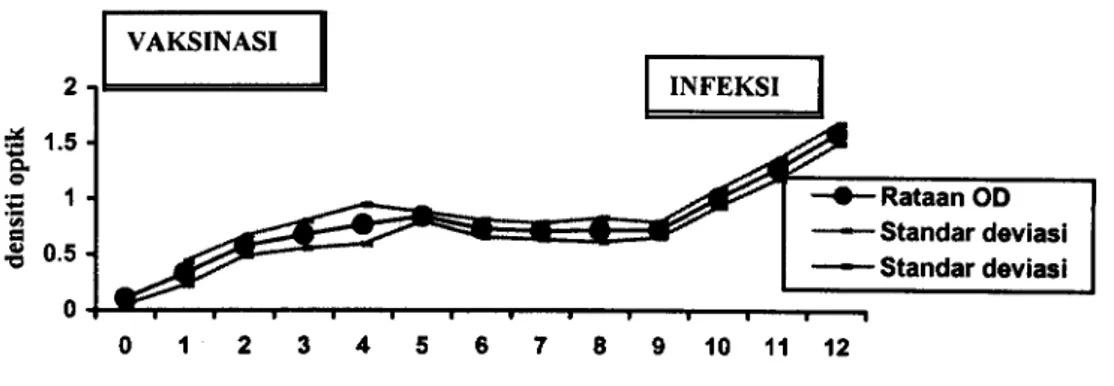
ELISA ILT dikembangkan dan diapliksikan untuk mendeteksi antibodi ILT pada hewan percobaan. Hasil aplikasi ELISA (Gambar 4) terlihat dinamika respon antibodi pada enam ekor ayam SPF diinfeksi dengan vaksin hidup ILT komersil dan diinfeksi dengan virus isolat lokal ILT. Rataan nilai OD berbeda pada saat sebelum divaksin dan setelah vaksinasi terlihat dengan jelas. Rataan nilai OD setelah vaksinasi terus meningkat dan mencapai puncaknya pada minggu ke 6, selanjutnya
Penentuan nilai cutoffELISA ILT didasarkan atas hasil uji 140 serum ayam SPF yang memperlihatkan rataan OD 0,073± 0,032 dengan penambahan 3 sd Dengan demikian nilai cutoffELISA ILT adalah 0,169, yang berarti bahwa setiap reaksi dalam ELISA dengan nilai OD di atas nilai tersebut dianggap reaksi positif dan sebaliknya.
Identifikasi sensitifitas dan spesifisitas ELISA memperlihatkan bahwa ELISA ILT yang dikembangkan sangat tinggi. Dari 100 serum berasal dari ayam terinfeksi ILT (diinfeksi buatan), 98 diantaranya bereaksi positif Sementara itu dari 140 senun berasal dari ayam tidak terinfeksi ILT, 136 bereaksi negatif. Dengan demikian dapat dinyatakan bahwa, sensitifitas ILT adalah 98% dengan tingkat spesifisitas 97,14%(Tabel 2).
(BALDocK, 1988)
menurun perlahan. Setelah ayam diinfeksi lagi dengan virus ILT, nilai rataan OD terus meningkat.
ELISA pernah dibuat dan mampu untuk mengukur antibodi virus unggas (SLAGHT et al., 1978 ; HOWIE dan THOSEN, 1981 ; MEULEMANS and HALEN, 1982). Hasil standarisasi ELISA yang dikembangkan dalam penelitian ini untuk mendeteksi antibodi virus ILT dalam serum ayam percobaan, memperlihatkan kemampuan dan akurasi yang cukup baik.
E Serum ILT E Serum IB Antigen ELISA Rataan OD ILT Sd Antigen Rataan OD kontrol sd 0,083 0,035 0,068 0,033 16 1,212 0,064 0,132 0,018 10 0,103 0,023 0,102 0,022
reaksinya dengan antigen kontrol OD tertinggi hanya 0,145. Bentuk kurva standar ini cukup landai.
Tabel 2. Sensitifitas dan spesifisitas uji ELISA ILT
Reaksi ELISA Serum ayam terinfeksi ILT Serum ayam negatif ILT Persentase
Positif 98(a) 2(b) Sensitifitas 98%
2n
0
Gambar 5. Perkembangan respon serologi setelah vaksinasi ILT dan tantang
VAKSINASI
-l-Rataan OD Standar deviasi Standardeviasi
0 1 2 3 4 5 6
KESIMPULAN DAN SARAN
DAFTAR PUSTAKA
ELISA ILT yang dikembangkan untuk mendeteksi respon antibodi virus ILT memperlihatkan kemampuan serta akurasi yang baik (sensitifitas 98% dan spesifisitas 97,14%) dan dapat digunakan sebagai perangkat uji serologi ILT untuk mendeteksi antibodi dalam serum ayam, baik antibodi karena vaksinasi maupun akibat infeksi alam.
BAUER, B., J.E.LoHR, and E.F.KALETA. 1999. Coparison of commersial ELISA test kits from Australia and the USA with the serum neutralization test in cell culture for the detection of antibodies to the infectious laryngotracheitis virus of chicken. Avian Pathol. 28:65-72
BALDOCK, F. C. 1988. Epidemiological evaluation of immunological test. Elisa technology in diagnosis and research. JCU, Townsville, Australia. pp 90-95. BAGUST, T. J, JONES R.C, dan Guy J, S. 2000. Avian
infectious laryngotracheitis . Rev.Sci. tech.Off.Epiz. pp 19 (2): 483 - 492
HowlE, R, and J. THoREsEN (1981). An enzyme-linked immunosorbent assay(ELISA) for infectious bursal diseases viruses. Canadian Journal of Comparative Medicine.45:51-55.
INFEKSI
7 8 9 10 11 12
MURPHY, F.A., C.M. FAUQURT, D.H.L. BISHOP, S.A. GHABRIAL, A.W. JARVIS, G.P. MARTELLI, M.A. MAYO, and M.D. SUMMERS. 1995. Virus Taxonomy. Vienna and New York.
Manual Of Standards for Diagnostic Test and Vaccine, 1996. Avian Infectious Laryngotracheitis, OIE, pp: 549-554 MEULEMANS, G., dan P. HALEN., 1982. Enzyme-Linked
Immunosorbent Assay (ELISA) for detecting Infectious laryngotracheitis viral antibodies in chicken serum. Avian Pathology 11 : 361-368
SLAGHT, S.S., YANG, T. J., dan VAN DER HELDER, L (1978). An enzyme-linked immunosorbent assay (ELISA) for detecting chicken anti-reovirus antibody at high sensitivity to the avian system. Avian Dis. 22 : 802-805. WIYONO, A., MUHARAM, S., ANTOmus, S., dan DARMINTO,
1996. Sebaran titer antibodi infectious laryngotracheitis (ILT) pada ayam ras dan buras di Kabupaten Cianjur, Tangerang dan Krawang. Dalam:Prosiding Temu Ilmiah Nasional Bidang Veteriner, Bogor 12-13 Maret 1996. Balai Penelitian Veteriner, Bogor, pp. 88-95
YORK, J.J., FAHEY, K.J., dan BAGUST T.J., 1983 . Development and evaluation of an ELISA for the detection of antibody to infectious laryngotracheitis virus in chicken. Avian Dis, 27:409-421