APLIKASI ASAM PERASETAT UNTUK MENGHILANGKAN ZAT WARNA PADA KAIN JEANS
SKRIPSI
DEBY HERUWATI MAHARANI
DEPARTEMEN KIMIA
FAKULTAS SAINS DAN TEKNOLOGI UNIVERSITAS AIRLANGGA
APLIKASI ASAM PERASETAT UNTUK MENGHILANGKAN ZAT WARNA PADA KAIN JEANS
SKRIPSI
Sebagai Salah Satu Syarat untuk Memperoleh Gelar Sarjana Sains Bidang Kimia
Pada Fakultas Sains dan Teknologi Universitas Airlangga
Oleh :
DEBY HERUWATI MAHARANI NIM. 080810509
Tanggal Lulus : 16 Juli 2012
Disetujui oleh :
Pembimbing I
Dr. rer nat Ganden Supriyanto, M.Sc NIP. 19681228 199303 1 001
Pembimbing II
LEMBAR PENGESAHAN NASKAH SKRIPSI
Judul : APLIKASI ASAM PERASETAT UNTUK
MENGHILANGKAN ZAT WARNA PADA KAIN JEANS
Penyusun : Deby Heruwati Maharani
NIM : 080810509
Pembimbing I : Dr. rer nat Ganden Supriyanto, M.Sc Pembimbing II : Dra. Aning Purwaningsih, M.Si Tanggal seminar : 16 Juli 2012
Disetujui Oleh :
Pembimbing I
Dr. rer nat Ganden Supriyanto, M.Sc NIP. 19681228 199303 1 001
Pembimbing II
Dra. Aning Purwaningsih, M.Si NIP. 19660310 199102 2 001
Mengetahui,
Ketua Program Studi S-1 Kimia/Ketua Departemen Kimia Fakultas Sains dan Teknologi Universitas Airlangga
KATA PENGANTAR
Bismillahirrahmanirrahim, Assalamualaikum Wr. Wb
Puji syukur ke hadirat Allah SWT atas segala berkah, rahmat dan hidayah-Nya yang diberikan kepada kita sehingga penulis dapat menyelesaikan skripsi yang berjudul “ Aplikasi Asam Perasetat Untuk Menghilangkan Zat Warna Pada Kain Jeans”. Shalawat serta salam tetap tercurahkan kepada Nabi Muhammad SAW karena berkat perjuangan beliau dan para sahabatnya kita bisa menikmati indahnya iman.
Ucapan terima kasih yang tulus penulis haturkan kepada :
1. Bapak Dr. rer nat Ganden Supriyanto, M.Scselaku dosen pembimbing I yang telah meluangkan waktunya untuk memberikan saran, nasehat dan masukan
dalam penyelesaian skripsi ini.
2. Ibu Dra. Aning Purwaningsih, M.Si selaku dosen pembimbing II sekaligus dosen wali atas bimbingan dan nasehatnya selama penulisan skripsi ini
3. Ibu Dra. Usreg Sri Handajani, M.Si selaku dosen penguji I yang telah
memberikan masukan dan saran dalam penyelesaian skripsi ini.
4. Ibu Dr. Pratiwi Pudjiastutik, M.Si selaku dosen penguji II yang telah
memberikan masukan dan saran dalam penyelesaian skripsi ini.
5. Ibu Dr. Alfinda Novi Kristanti, DEA selaku Ketua Program Studi S1 kimia. 6. Bapak Dr. Ir. Suyanto, M.Si yang telah banyak memberikan masukan dan
7. Ibu, ibu, dan ibu serta keluarga tercinta yang telah sepenuhnya memberikan
dukungan, cinta, kasih sayang dan semangat baik moral maupun spiritual demi
terselesaikannya skripsi ini.
8. Bapak dan Ibu dosen kimia yang telah banyak meluangkan waktu dalam membimbing dan mendermakan ilmu yang dimiliki demi mencerdaskan mahasiswanya.
9. Teman-teman angkatan 2008 yang banyak memberikan bantuan, saran dan
atas kebersamaannya selama mengemban ilmu di Universitas Airlangga. 10. Karyawan dan karyawati FSAINTEK UNAIR dan petugas laboratorium yang
telah banyak membantu.
11. Semua pihak yang telah banyak membantu yang tidak bisa saya sebutkan satu
per satu untuk dukungan yang sangat berharga untuk saya.
Penulis menyadari bahwa dalam penulisan naskah skripsi ini masih banyak kekurangan, maka dari itu saya mengharapkan kritik dan saran yang membangun demi kesempurnaan naskah skripsi ini. Semoga naskah skripsi ini dapat bermanfaat dan sedikit memberikan kontribusi dalam pengembangan ilmu pengetahuan dan teknologi di negeri ini, amin ya robbal ’alamin.
Wassalamu’alaikum Wr. Wb
Surabaya, Juli 2012
PEDOMAN PENGGUNAAN SKRIPSI
Maharani, D. H., 2012, Aplikasi Asam Perasetat Untuk Menghilangkan Zat Warna Pada Kain Jeans. Skripsi di bawah bimbingan Dr. rer. nat. Ganden Supriyanto, M.Sc., dan Dra. Aning Purwaningsih, M.Si., Departemen Kimia, Fakultas Sains dan Teknologi, Universitas Airlangga, Surabaya
ABSTRAK
Proses bleaching pada kain biasanya menggunakan senyawa golongan oksidator seperti hipoklorit, gas klor dan asam peroksida. Metode bleaching menggunakan asam perasetat belum banyak dikembangkan. Pada penelitian ini dilakukan proses bleaching menggunakan asam perasetat. Penelitian ini bertujuan untuk mengembangkan bleaching agent yang ramah lingkungan dan mengganti bleaching agent seperti klor yang memberikan dampak pencemaran lingkungan. Dalam penelitian ini asam perasetat dibuat dengan mereaksikan hidrogen peroksida dan asam asetat glasial. Faktor yang mempengaruhi pembentukan asam perasetat seperti perbandingan mol [H2O2 30%:CH3COOH 100%] dengan volume
total 100 ml, suhu dan waktu reaksi dicari kondisi optimumnya dalam penelitian ini. Asam perasetat yang terbentuk bertindak sebagai nukleofil yang akan menghilangkan gugus kromofor yang memberikan warna pada kain jeans. Hasil optimum proses bleaching menggunakan asam perasetat adalah pada perbandingan mol [H2O2:CH3COOH] sebesar [1:10] pada suhu 85˚C selama 60
menit.
Maharani, D. H., 2012, Application of Peracetic Acid to Remove The Dye in The Jeans Fabric. This study is under guidance of Dr. rer. nat. Ganden Supriyanto, M.Sc., and Dra. Aning Purwaningsih, M.Si., Department of Chemistry, Science and Technology Faculty, Universitas Airlangga.
ABSTRACT
The process of bleaching textile usually uses oxidator compound such as hypochlorite, chlorine and peroxide. Bleaching method using peracetic acid has not been developed yet. In this research, bleaching process using peracetic acid had been done. The purpose of this research was to develop an environmentally and friendly bleaching agent and change another bleaching agent such as chlorine which gives bad impact of environment pollution. In this research peracetic acid was prepared by reacting hydrogen peroxide and glacial acetic acid. Some factors which influenced the formation of peracetic acid, such as optimum mole ratio [H2O2 30%:CH3COOH 100%] with 100 ml total volume, temperature and
reaction time were determined in this research. Peracetic acid which had been formed acted as a nucleophile. This ion eliminated chromophore group which gave colour to jeans fabric. The optimum results in bleaching process was under condition of mole ratio [H2O2:CH3COOH] of 1:10 at 85˚C for 60 minutes.
DAFTAR ISI 1.1 Latar Belakang Masalah... 1
1.2 Rumusan Masalah ... 4
1.3 Tujuan Penelitian ... 4
1.4 Manfaat Penelitian ... 4
BAB II TINJAUAN PUSTAKA 2.1 Zat Warna ... 6
2.2 Penggolongan Zat Warna... 7
2.3 Syarat-syarat Zat Warna ... 10
2.4 Proses Bleaching ... 10
2.5 Macam-macam Proses Bleaching ... 13
BAB III METODE PENELITIAN 3.1 Tempat dan Waktu Penelitian ... 20
3.2 Alat dan Bahan Penelitian 3.2.1 Alat-alat penelitian ... 20
3.2.2 Bahan penelitian ... 20
3.3 Diagram Alir ... 21
3.4 Proses Bleaching 3.4.2 Pengaruh perbandingan mol[H2O2:CH3COOH]... 22
3.4.3 Pengaruh suhu ... 23
3.4.4 Pengaruh waktu ... 23
BAB IV HASIL DAN PEMBAHASAN
4.1 Karakteristik Bahan Awal ... 26 4.2 Pengaruh Variabel Bebas Pada Proses Bleaching Terhadap Derajat
Kecerahan Kain Jeans ... 27 4.2.1 Pengaruh perbandingan mol[H2O2:CH3COOH] terhadap
derajat kecerahan kain jeans ... 27 4.2.2 Pengaruh suhu terhadap derajat kecerahan kain jeans ... 34 4.2.3 Pengaruh waktu terhadap derajat kecerahan kain jeans... 36
BAB V KESIMPULAN DAN SARAN
5.1 Kesimpulan ... 40 5.2 Saran ... 40
DAFTAR TABEL
Nomor Judul Tabel Halaman
2.1 Nama dan struktur kimia kromofor ... 6
2.2 Klasifikasi bleaching agent ... 12
3.1 Disain eksperimen optimasi perbandingan mol [H2O2:CH3COOH].... 22
3.2 Disain eksperimen optimasi suhu ... 23
3.3 Disain eksperimen optimasi waktu ... 24
4.1 Hasil derajat kecerahan sampel sebelum dilakukan proses bleaching. 26
4.2 Hasil derajat kecerahan kain jeans dengan perbandingan mol
[H2O2:CH3COOH] ... 29
4.3 Hasil derajat kecerahan kain jeans dengan variasi suhu ... 35
DAFTAR GAMBAR
Nomor Judul Gambar Halaman
2.1 Sintesis asam perasetat ... 18
4.1 Sampel sebelum dilakukan proses bleaching... 26 4.2 Kain jeans hasil proses bleachingdengan variabel perbandingan mol
[H2O2:CH3COOH]... 28
4.3 Grafik hubungan perbandingan mol [H2O2:CH3COOH] dengan
derajat kecerahan pada suhu 85˚C dan waktu 60 menit... 30 4.6 Kain jeans hasil proses bleachingdengan variabel suhu ... 34 4.7 Grafik hubungan suhu dengan derajat kecerahan pada perbandingan
mol [H2O2:CH3COOH] sebesar 1:10 dan waktu 60 menit ... 36
4.8 Kain jeans hasil proses bleachingdengan variable waktu ... 37 4.9 Grafik hubungan waktu dengan derajat kecerahan pada perbandingan
DAFTAR LAMPIRAN
No Judul
1 Laporan Hasil Analisa Derajat Kecerahan Kain Jeans pada Variasi Perbandingan mol [H2O2:CH3COOH]
2 Laporan Hasil Analisa Derajat Kecerahan Kain Jeans pada Variasi Suhu
BAB I PENDAHULUAN
1.1 Latar Belakang Masalah
Industri tekstil dan produk tekstil merupakan salah satu bidang yang sangat berkembang di Indonesia. Dalam proses produksinya, industri tekstil menghasilkan limbah baik berupa limbah padat, cair maupun gas yang dapat menyebabkan terjadinya pencemaran lingkungan. Terlepas dari itu, limbah dari pabrik tekstil seperti potongan kain jeans tidak perlu ditimbun di dalam tanah atau bahkan dibakar sehingga asapnya menimbulkan polusi. Limbah kain yang berwarna itu dapat diolah menjadi produk yang lebih berkualitas dan bernilai ekonomis. Limbah kain yang berwarna tersebut dapat dilunturkan menjadi putih dengan proses bleaching, kemudian diubah lagi menjadi kapas dan dipintal kembali menjadi benang, kain dan produk-produk lain misalnya sarung tangan dan lain sebagainya.
pemanfaatan kain bekas menjadi benang, bahan dasar kain dan dapat dikembangkan menjadi produk lainnya yang lebih berkualitas.
Proses bleaching dapat dilakukan dengan menggunakan senyawa klor seperti klorin atau klor dioksida (Van Daam, 2002). Akan tetapi, penggunaan klor dalam proses bleaching ini menimbulkan persoalan lingkungan yang serius. Dampak negatif yang ditimbulkan adalah pada buangannya yang mengandung senyawa klorin organik yang berbahaya bagi lingkungan hidup (Ulia, 2007).
Mengingat betapa bahayanya senyawa yang mengandung klor, maka saat ini banyak dikembangkan penelitian-penelitian yang berkaitan dengan proses bleaching dengan prinsip total chlor free dengan menggunakan oksigen dan peroksida. Pada dasarnya semuanya bertujuan untuk menggantikan proses bleaching menggunakan klor dalam proses bleaching dengan senyawa-senyawa yang benar-benar bebas klor, sehingga tidak ada zat-zat berbahaya dan sisa-sisa klorinasi yang berasal dari proses bleaching(Bajpai, 2005).
Proses bleaching serat memang harus menggunakan bahan kimia yang reaktif untuk melarutkan kandungan lignin yang ada di dalam serat agar diperoleh derajat kecerahan yang tinggi (Tutus, 2004). Namun demikian, tetap harus dijaga agar penggunaan bahan kimia tersebut tidak menyebabkan pencemaran lingkungan yang berbahaya.
yang tinggi merupakan syarat utama bleaching dengan menggunakan hidrogen peroksida. Hidrogen peroksida mempunyai kelebihan yaitu sifatnya yang lebih ramah lingkungan dibandingkan dengan oksidator lain karena peruraiannya hanya menghasilkan air dan oksigen (Suess, 2010). Namun, pada bleaching kain menggunakan hidrogen peroksida membutuhkan larutan alkali yang berfungsi untuk mengatur pH yaitu biasanya larutan NaOH, penstabil dan suhu yang digunakan relatif tinggi serta membutuhkan waktu yang lama. Setelah proses bleaching, membutuhkan jumlah air yang besar untuk menghilangkan sisa hidrogen peroksida dan sisa alkali (Abdel-Halim et al., 2011).
Oleh karena itu, sangat diperlukan suatu metode untuk proses bleaching yang bisa dilakukan dengan baik pada suhu rendah, waktu reaksi yang lebih singkat dan menggunakan biaya yang lebih murah, tanpa menyebabkan kerusakan pada serat kain. Untuk itu pada penelitian ini dicoba melakukan proses bleaching kain menggunakan asam perasetat.
kain atau pada pembilasan kain, netralisasi serat setelah bleaching pun tidak diperlukan, tidak seperti bleaching dengan hidrogen peroksida, dimana memerlukan jumlah air yang besar untuk menghilangkan sisa alkali.
Asam perasetat ini mejadi salah satu alternatif dalam upaya meminimalkan masalah yang disebabkan oleh bleaching agent seperti klor ataupun hidrogen peroksida. Penelitian ini bertujuan untuk memperoleh hasil dari proses bleaching dengan derajat kecerahan yang tinggi pada kain jeans bekas menggunakan asam perasetat sebagai bleaching agentyang ramah lingkungan.
1.2 Rumusan Masalah
Berapakah perbandingan mol H2O2 dan CH3COOH, suhu dan waktu
optimum pada proses bleachingkain jeans?
1.3 Tujuan Penelitian
Menentukan perbandingan mol H2O2 dan CH3COOH, suhu dan waktu
optimum pada bleachingkain jeans.
1.4 Manfaat Penelitian
Data-data yang diperoleh dari penelitian ini merupakan kajian eksperimental dan diharapkan dapat memberikan manfaat antara lain :
1. Mengurangi limbah kain jeans bekas.
BAB II
TINJAUAN PUSTAKA
2.1 Zat Warna
Molekul zat warna merupakan gabungan dari zat organik tidak jenuh dengan kromofor sebagai pembawa warna dan auksokrom sebagai pengikat warna dengan serat. Zat organik tidak jenuh yang dijumpai dalam pembentukan zat warna adalah senyawa aromatik antara lain senyawa hidrokarbon aromatik dan turunannya, fenol dan turunannya serta senyawa-senyawa hidrokarbon yang mengandung nitrogen.
Gugus kromofor adalah gugus yang menyebabkan molekul menjadi berwarna. Pada Tabel 2.1 dapat dilihat beberapa nama gugus kromofor.
Tabel 2.1Nama dan Struktur Kimia Kromofor Nama Gugus Struktur Kimia
Nitroso NO atau (-N-OH)
Nitro NO2atau (NN-OOH)
Grup Azo
-N=N-Grup Etilen
-C=C-Grup Karbonil -C=O
Grup Karbon-Nitrogen -C=NH ;
CH=N-Grup Karbon Sulfur -C=S;
HH3CO
2.2 Penggolongan Zat Warna
1. Zat warna berdasarkan asal: a. Zat warna alami
Contoh: Kurkumin
b. Zat warna sintetik Contoh: Rhodamin B
2. Zat warna berdasarkan struktur: a. Azo
NH2
NH O
O
Br
CH3
NaO3S HO
C O
C O
NC
O2N N N N
C2H5
C2H5
b. Nitro
Contoh: Dispersi merah 71
c. Fenol
Contoh: Fenolptalein
3. Zat warna berdasarkan anion: a. Asam
Cl
C
N(CH3)2
+ Cl-N(CH3)2
4. Zat warna berdasarkan kation: Basa
Contoh: Basa biru
(Christie, 2007)
2.3 Syarat-syarat Zat Warna
Zat warna adalah semua zat berwarna yang mempunyai kemampuan untuk dicelupkan pada serat tekstil dan memiliki sifat ketahanan luntur warna (permanent). Jadi sesuatu zat dapat berlaku sebagai zat warna apabila:
1. Zat warna tersebut mempunyai gugus yang dapat menimbulkan warna (kromofor), misalnya : C=C, N=N, -NO2, C=O (Fessenden, 1992).
2. Zat warna tersebut mempunyai gugus yang dapat mempunyai afinitas terhadap serat tekstil (auksokrom), misalnya : -OH, OR, -NH2, -NHR, -NR2,
-X (Fessenden, 1992).
2.4 Proses Bleaching
pada panjang gelombang cahaya tampak dan Ultra Violet, sehingga menimbulkan warna (Wildan, 2010). Senyawa kimia yang digunakan pada proses bleaching memecah ikatan rangkap pada rantai panjang tersebut menjadi ikatan tunggal yang tidak menyerap warna (Suess, 2010).
Faktor-faktor yang mempengaruhi proses bleachingantara lain: a. Konsentrasi
Reaksi dapat ditingkatkan dengan memperbesar konsentrasi bahan bleaching agent. Penggunaan bahan bleaching agent yang berlebih tidak akan meningkatkan derajat kecerahan karena derajat kecerahan yang dicapai telah maksimal (Karmakar, 1999).
b. Waktu reaksi
Pada umumnya, perlakuan bleaching agent terhadap serat akan menjadi lebih reaktif dengan memperpanjang waktu reaksi. Namun, waktu yang terlalu lama akan merusak serat (Onggo, 2004).
c. Suhu
Peningkatan suhu dapat menyebabkan peningkatan kecepatan reaksi pada reaksi bleaching. Pemilihan suhu ditentukan pada penggunaan bleaching agent. Suhu bleaching biasanya diatur berkisar antara 40-100˚C (Van Daam, 2002).
d. pH
pH memiliki pengaruh yang sangat vital terhadap proses bleaching secara
keseluruhan. Nilai pH bergantung pada jenis penggunaan bleaching agent. Pada
(Abdel-Halim et al., 2011). Pada proses bleaching dengan hidrogen peroksida
diperlukan suasana basa antara pH 8 hingga 12 (Tutus, 2004). Stabilitas kimia,
kelarutan dan afinitas bleaching agent tergantung pada nilai pH yang efektif
dalam larutan (Karmakar, 1999). e. Rasio bahan dan bleaching agent
Perbandingan bahan yang akan diputihkan dengan bleaching agent akan mempengaruhi hasil yang didapat. Semakin kecil perbandingan rasio bahan yang akan diputihkan dengan bleaching agent akan meningkatkan reaksi bleaching. Tetapi dengan rasio yang semakin kecil akan mengurangi efisien menggunaan bleaching agent. Pada proses bleaching umumnya dipakai rasio bahan dengan bleaching agent antara 8 : 1 hingga 20 : 1 (Van Daam, 2002;
Batubara, 2006).
Bleaching agent yang digunakan untuk proses bleaching sangat banyak sekali, antara lain adalah sebagai berikut:
2.5 Macam-macam Proses Bleaching
Pada dasarnya proses bleaching dibagi menjadi dua, yaitu proses bleaching secara kimia dan proses bleachingsecara biologi. Proses bleachingsecara biologi umumnya disebut juga dengan proses bio-bleaching. Berikut ini adalah berbagai macam proses bleaching dengan menggunakan beberapa bleaching agent yang sering digunakan, antara lain:
1. Bleachingdengan menggunakan natrium hipoklorit
Natrium hipoklorit merupakan garam natrium dari asam hipoklorit (HOCl). Mekanisme reaksi bleachingdengan natrium hipoklorit adalah sebagai berikut:
NaOCl + H2O NaOH + HOCl
HOCl HCl + On
NaOCl + HCl NaCl + HOCl HOCl + HCl H2O + Cl2
Asam lemah juga dapat menguraikan garam hipoklorit menjadi asam hipoklorit tetapi asam hipoklorit yang terbentuk tidak dapat terurai menjadi gas klor oleh adanya kelebihan asam lemah. Sifat penting yang sangat berarti dalam proses bleaching adalah mudahnya garam natrium hipoklorit terhidrolisis oleh air menghasilkan asam hipoklorit yang selanjutnya terurai menghasilkan On yang bereaksi dengan zat warna (Karmakar, 1999).
Faktor-faktor yang mempengaruhi penguraian garam natrium hipoklorit:
1. Pengaruh pH
b. 5 < pH < 8,5, larutan lebih banyak mengandung asam hipoklorit (HOCl) bebas.
c. pH < 5, terjadi pembebasan gas klor (Cl2).
d. pH < 3, seluruh asam hipoklorit terurai menjadi gas Cl2.
Pada suasana alkali (pH > 7), asam hipoklorit yang terbentuk dapat dinetralkan oleh alkali menjadi garam natrium hipoklorit.
HOCl + NaOH NaOCl + H2O
Setelah penetralan, larutan bersifat alkalis dan terjadi reaksi kesetimbangan sehingga larutan menjadi lebih stabil.
NaOCl + H2O NaOH + HOCl
2. Pengaruh logam dan oksidanya
Logam-logam seperti besi, tembaga, nikel dan kobalt bersifat sebagai katalisator yang mempercepat reaksi penguraian garam natrium hipoklorit membentuk oksida atau hidroksidanya dan membebaskan oksigen.
2 CaO + NaOCl Ca2O3 + NaCl
2 Ca2O3 4CaO + O2
Kekurangan natrium hipoklorit antara lain adalah:
1. Natrium hipoklorit tidak menghasilkan derajat kecerahan yang memuaskan. 2. Bleaching dengan natrium hipoklorit menghasilkan kerusakan pada selulosa
serat.
3. Bleaching dengan larutan natrium hipoklorit membutuhkan peralatan yang tahan korosi.
5. Stabilitas natrium hipoklorit sulit dicapai.
6. Membentuk senyawa adsorbable organic halogen (AOX) yang telah digunakan sebagai parameter yang menyatakan tingkat pencemaran yang berbahaya dan digunakan di seluruh dunia sehingga penggunaannya dibatasi (Karmakar, 1999).
2. Bleachingdengan menggunakan hidrogen peroksida
Hidrogen peroksida adalah bleaching agentberbentuk cair, tidak berwarna, sedikit lebih kental dari air dan dapat bercampur dengan air dalam berbagai komposisi (Jones, 1999).Bleachingmenggunakan hidrogen peroksida terjadi oleh penambahan alkali dan dengan peningkatan suhu.
Mekanisme reaksi dekomposisi hidrogen peroksida adalah sebagai berikut:
H2O2 + OH- OOH- + H2O
H2O2 + OOH - OH- + O2 + H2O
(Bajpai, 2005)
Anion perhidroksil (HOO-) berguna sebagai spesies aktif yang sangat berperan dalam proses bleaching dengan menggunakan peroksida. Konsentrasi ion perhidroksil meningkat dengan bertambahnya konsentrasi H2O2 dan NaOH.
Faktor-faktor yang mempengaruhi penguraian H2O2adalah sebagai berikut:
1. Pengaruh pH
Dalam suasana asam (pH < 7) H2O2 stabil, sedangkan dalam suasana
basa/alkali (pH > 7) H2O2 mudah terurai melepaskan oksigen. Semakin besar pH
maka penguraiannya juga semakin cepat. pH dapat diatur dengan penambahan NaOH (Bajpai, 2005).
2. Pengaruh suhu
Suhu juga mempengaruhi penguraian H2O2. Pada suhu rendah, pembebasan
oksigen sangat kecil, makin tinggi suhu penguraiannya makin cepat. Penguraian H2O2yang efektif untuk bleachingterjadi pada suhu 90˚C. Pada suhu di atas 90˚C
penguraiannya sangat cepat sekali (Bajpai, 2005). 3. Pengaruh stabilisator
Penguraian H2O2 dapat diperlambat dengan penambahan zat stabilisator
meskipun bleaching dilakukan pada pH dan suhu yang tinggi. Ada beberapa macam zat stabilisator yang dapat digunakan dalam bleaching dengan hidrogen peroksida diantaranya adalah natrium silikat, magnesium hidroksida, magnesium silikat, natrium metafosfat dan natrium trifosfat. Jenis zat stabilisator yang banyak digunakan dalam bleachingadalah natrium silikat (Ek et al., 2009).
4. Pengaruh Katalisator
Reaksinya adalah sebagai berikut:
2Fe3+ + 2H2O2 2Fe2+ + O2 + 4H+
2Fe2+ + H2O2 + 2H+ 2Fe3+ + 2H2O
(Suess, 2010).
3. Bleachingdengan menggunakan asam perasetat
Asam perasetat merupakan oksidan kuat yang telah diaplikasikan sebagai bahan desinfektan, bleaching tekstil dan pulp (Zhao et al., 2008). Hal ini dikarenakan asam perasetat merupakan bleaching agent yang benar-benar bebas dari klorin (TCF) (Zhao et al., 2007).
Asam perasetat dikenal dengan nama lain yaitu asam peroksiasetat dan asetil hidroperoksida. Data toksikologi pada bahan: asam perasetat: ORAL (LD50): akut: 210 mg/kg (mouse), 1894 mg/kg (rat), DERMAL (LD50): akut: 1734 mg/kg (rabbit). Berbentuk cairan dengan bau yang tajam dan tidak berwarna. Asam perasetat memiliki titik didih: 107,22˚C (225˚F) dan massa jenis: 1,13 kg/l. Mudah larut dalam air dingin, air panas, dietil eter, dan sebagian larut dalam metanol dan aseton.
Asam perasetat dapat dibuat dengan cara mencampurkan asam asetat dan hidrogen peroksida dengan asam sulfat sebagai katalis (Zhao et al., 2008) akan tetapi dapat juga dibuat tanpa menggunakan katalis (Erba et al., 2007).
H2SO4
CH3COOH + H2O2 CH3COOOH + H2O
Selain itu, juga dapat dibuat dengan mencampurkan hidrogen peroksida dengan anhidrida asetat pada suhu kamar dengan adanya katalis yang cocok seperti EDTA, akan tetapi pada proses ini menghasilkan diacetyl peroxide yang sangat eksplosif (Karmakar, 1999).
CH3 C O
O
C O
H3C
+ H2O2 CH3COOOH + H2O
Peracetic acid
Acetic anhydride
NaOH
Mekanisme pembuatan asam perasetat dari asam asetat glasial dan hidrogen
Gambar 2.1Sintesis asam perasetat (Bajpai, 2005)
Keuntungan dari asam perasetat sebagai bleaching agentantara lain adalah:
1. Asam perasetat aman untuk lingkungan karena terurai menjadi asam asetat dan oksigen serta tidak menghasilkan produk beracun.
2. Asam perasetat sebagai bahan kimia industri yang mudah didapatkan dan aman diperkenalkan untuk desain proses yang ada.
BAB III
METODE PENELITIAN
3.1 Tempat dan Waktu Penelitian
Penelitian dilaksanakan di laboratorium Kimia Analitik Departemen Kimia Fakultas Sains dan Teknologi, Universitas Airlangga. Penelitian ini dimulai bulan Maret 2012 sampai Juni 2012.
3.2 Alat dan Bahan Penelitian 3.2.1 Alat-alat penelitian
Alat-alat yang digunakan pada penelitian ini adalah buret, timbangan analitik, stirer, hotplate, termometer, gelas beaker, kaca arloji dan peralatan gelas lain yang biasa digunakan di laboratorium kimia.
3.2.2 Bahan penelitian
3.3 Diagram Alir
Persiapan bahan
dan alat Pembuatan larutan
Eksperimen
Optimasi parameter bleaching
Kondisi optimum untuk bleaching
Aplikasi pada kain jeans bekas
Analisis kecerahan
Perbandingan mol [H2O2:CH3COOH]
Variasi suhu
Variasi waktu
Visual Chromameter
Sampel dari pabrik tekstil di Gresik
3.4 Proses Bleaching
3.4.1 Pengaruh perbandingan mol [H2O2:CH3COOH]
Dimasukkan dengan menggunakan buret larutan H2O2 30% dan CH3COOH
100% ke dalam gelas beker 250 ml dengan perbandingan mol 1:34 ; 1:20 ; 1:15 ; 1:10 ; 1:5 ; 1:3 sehingga volume total larutan menjadi 100 ml. Kemudian dimasukkan sampel kain jeans bekas dengan ukuran 2x2 cm dan dipanaskan pada suhu tetap 85˚C selama 60 menit tanpa proses pengadukan. Setelah proses selesai kemudian diamati kecerahan kainnya secara visual dan diukur derajat kecerahannya menggunakan chromameter. Kemudian didapatkan hasil perbandingan mol [H2O2:CH3COOH] optimum yang akan digunakan untuk uji
selanjutnya.
Tabel 3.1Disain eksperimen optimasi perbandingan mol [H2O2:CH3COOH]
No
3 11 0,107734 89 1,55617 1:15 85 60
4 15 0,14691 85 1,48623 1:10 85 60
5 25 0,24485 75 1,31138 1:5 85 60
6 35 0,34279 65 1,13653 1:3 85 60
Keterangan:
Cx : Perbandingan mol [H2O2:CH3COOH] optimum
3.4.2 Pengaruh suhu
Dimasukkan dengan menggunakan buret larutan H2O2 30% dan CH3COOH
100% dengan perbandingan mol [H2O2:CH3COOH] optimum (Cx) ke dalam
gelas beker 250 ml sehingga volume total larutan menjadi 100 ml. Kemudian dimasukkan sampel kain jeans bekas dengan ukuran 2x2 cm dan dipanaskan pada variabel suhu 55, 65, 75 dan 85˚C selama 60 menit tanpa pengadukan. Setelah proses selesai kemudian diamati kecerahan kainnya secara visual dan diukur derajat kecerahannya menggunakan chromameter. Kemudian didapatkan hasil suhu optimum dan akan digunakan untuk uji selanjutnya.
Tabel 3.2Disain eksperimen optimasi suhu
No
Setiap perlakuan dilakukan replikasi tiga kali
3.4.3 Pengaruh waktu
Dimasukkan dengan menggunakan buret larutan H2O2 30% dan CH3COOH
100% dengan perbandingan mol [H2O2:CH3COOH] optimum (Cx) ke dalam
dimasukkan sampel kain jeans bekas dengan ukuran 2x2 cm dan dipanaskan pada suhu optimum (Topt) dengan variabel waktu selama 45, 60, 75 dan 90 menit tanpa pengadukan. Setelah proses selesai kemudian diamati kecerahan kainnya secara visual dan diukur derajat kecerahannya menggunakan chromameter. Kemudian didapatkan hasil waktu optimum.
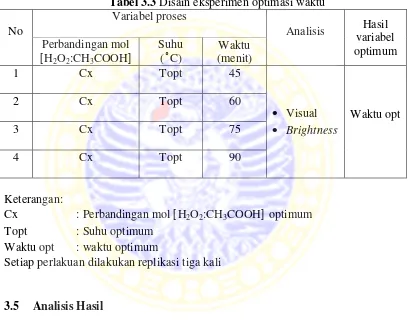
Tabel 3.3Disain eksperimen optimasi waktu
No
Waktu opt : waktu optimum
Setiap perlakuan dilakukan replikasi tiga kali
3.5 Analisis Hasil 1. Analisis visual
Sampel kain yang telah diputihkan dengan berbagai variasi perbandingan mol, suhu dan waktu dilakukan perbandingan secara visual kemudian difoto. 2. Analisisbrightness(kecerahan)
Cara pengukuran derajat kecerahan menggunakan alat chromameter adalah sebagai berikut:
1. Kain diletakkan pada suatu alas yang mendatar
2. Alat chromameter dikalibrasi terlebih dahulu dengan plat kalibrasi keramik putih, hingga nilai yang dihasilkan sesuai dengan nilai yang tertera pada plat 3. Ditekan tombol modeuntuk melakukan pengukuran sistem L*
BAB IV
HASIL DAN PEMBAHASAN
4.1 Karakteristik Bahan Awal
Sampel diperoleh dari salah satu pabrik tekstil di Gresik, kemudian dipotong dengan ukuran 2cm x 2cm. Bahan dari sampel adalah kain jeans berwarna biru, seperti yang ditunjukkan pada Gambar 4.1
Gambar 4.1Sampel kain jeans sebelum dilakukan proses bleaching
Sebelum dilakukan proses bleaching, sampel diukur derajat kecerahannya menggunakan alat Chromameter CR-400 Konika Minolta dengan sistem CIE 1976 L*, a*, b*. Hasil derajat kecerahan ditunjukkan oleh Tabel 4.1.
Tabel 4.1Hasil derajat kecerahan sampel sebelum dilakukan proses bleaching Replikasi Derajat kecerahan (L*) Rata- rata
1 25,95
26,17
2 26,23
4.2 Pengaruh Variabel Bebas Pada Proses Bleaching Terhadap Derajat Kecerahan Kain Jeans
Variabel bebas yang digunakan pada penelitian ini adalah perbandingan mol [H2O2:CH3COOH], suhu dan waktu. Masing-masing variabel operasi tersebut
akan ditinjau terhadap derajat kecerahan (brightness) dari kain jeans.
4.2.1 Pengaruh perbandingan mol[H2O2:CH3COOH] terhadap derajat kecerahan kain jeans
Proses bleachingdengan asam perasetat dilakukan dengan volume total 100 ml. Dengan variasi perbandingan mol [H2O2:CH3COOH] yaitu 1:34 ; 1:20 ; 1:15 ;
1:10 ; 1:5 ; 1:3 dalam kondisi operasi yang tetap yaitu proses waktu bleaching 60 menit dan suhu 85˚C.
Hasil dari masing-masing kain jeans setelah perlakuan proses bleaching secara visual ditunjukkan pada Gambar 4.2
(c) (d)
(e) (f)
Gambar 4.2Kain jeans hasil proses bleachingdengan variabel perbandingan mol [H2O2:CH3COOH] : (a) 1:34 (b) 1:20 (c) 1:15 (d) 1:10 (e) 1:5 (f) 1:3
Tabel 4.2Hasil derajat kecerahan kain jeans dengan perbandingan mol [H2O2:CH3COOH]
1 5 0,04897 95 1,66108 1:34 85 60 83,58
1:10
2 8 0,07835 92 1,60862 1:20 85 60 85,80
3 11 0,107734 89 1,55617 1:15 85 60 88,76
4 15 0,14691 85 1,48623 1:10 85 60 89,77
5 25 0,24485 75 1,31138 1:5 85 60 79,20
6 35 0,34279 65 1,13653 1:3 85 60 73,42
Tabel 4.2 menunjukkan bahwa hasil optimum bleaching terjadi pada perbandingan mol [H2O2:CH3COOH] sebesar 1:10. Hal ini dibuktikan dengan
hubungan antara perbandingan mol [H2O2:CH3COOH] dalam proses bleaching
terhadap derajat kecerahan adalah sebagai berikut:
Gambar 4.3 Grafik hubungan perbandingan mol [H2O2:CH3COOH] dengan
derajat kecerahan pada suhu 85˚C dan waktu 60 menit.
Asam perasetat merupakan oksidator kuat dan memiliki bilangan oksidasi yang lebih tinggi dibandingkan dengan bilangan oksidasi dari hidrogen peroksida (Muladi, 2000). Sampel kain jeans bekas didapatkan dari pabrik tekstil di Gresik dimana sampel kain jeans bekas tersebut tidak diketahui secara pasti zat warna yang mengikatnya. Mekanisme reaksi bleaching tidak dapat dijelaskan secara pasti karena tidak diketahuinya zat warna yang mengikat sampel kain jeans tersebut.
negatif (anion) dengan serat yang bermuatan positif (kation) dan antara zat warna bermuatan positif (kation) dengan serat yang bermuatan negatif (anion).
Kemungkinan apabila zat warna pada kain jeans adalah zat warna yang bermuatan negatif (anion) dan serat pada jeans adalah bermuatan positif (kation), maka mekanisme yang terjadi adalah sebagai berikut:
Pada mekanisme diatas zat warna berwarna biru yang digunakan adalah Alizarin Sky Bluedengan strukturnya yaitu sebagai berikut:
Serat kain jeans diduga adalah campuran selulosa dan nylon. Polimer dari selulosa dan nilon adalah sebagai berikut:
Selulosa Nylon
CO2H
NH3+ A
-CO2H
NH3+ O3S--Dye
Dye-SO3
-O
O
NH2
NH Br
NaO3S
Kemungkinan apabila zat warna pada kain jeans adalah zat warna yang bermuatan bermuatan positif (kation) dan serat pada jeans adalah negatif (anion), maka mekanisme yang terjadi adalah sebagai berikut:
Pada mekanisme diatas zat warna berwarna biru yang digunakan adalah Cyanine Bluedengan strukturnya yaitu sebagai berikut:
Serat kain jeans diduga dari golongan acrylic. Polimer dari acrylic adalah sebagai berikut:
Kemungkinan yang kedua yaitu zat warna diserang oleh nukleofil asam perasetat sehingga struktur zat warna terpecah menjadi senyawa lain. Diduga mekanisme pemecahan zat warna oleh nukleofil asam perasetat adalah sebagai
+M -O3S
Dye-X+ -O3S
Dye-X+
N
C2H5 CH N C2H5
+
-O
Asam perasetat berperan sebagai nukleofil yang menyerang sistem aromatis yang kaya akan elektron. Keberadaan asam perasetat dan alkena menyebabkan terbentuknya epoksida. Nukleofil asam perasetat menyebabkan terbukanya cincin epoksida dan membentuk senyawa yang stabil yaitu asam mukonat.
4.2.2 Pengaruh suhu terhadap derajat kecerahan kain jeans
Suhu dalam proses bleaching mempengaruhi derajat kecerahan dari kain. Hal ini berhubungan dengan peningkatan kecepatan reaksi, dimana semakin tinggi suhu maka reaksi akan berlangsung lebih cepat (Van Daam, 2002). Pada proses bleaching, semakin tinggi suhu maka proses pembentukan nukleofil ion perasetat (CH3COOO-) akan semakin cepat sehingga hal ini akan berpengaruh pada proses
(a) (b)
(c) (d)
Gambar 4.5 Kain jeans hasil proses bleachingdengan variabel suhu: (a) 55˚C (b) 65˚C (c) 75˚C (d) 85˚C
Gambar 4.5 secara visual menunjukkan semakin tinggi suhu maka kain jeans yang dihasilkan semakin cerah yaitu pada suhu 85˚C. Pada kondisi ini
memberikan hasil yang baik dan hal ini sesuai dengan yang dikemukakan oleh Karmakar (1999) bahwa suhu dalam proses bleaching menggunakan asam perasetat untuk tekstil adalah antara 50-80˚C. Kemudian dilakukan analisis
Tabel 4.3Hasil derajat kecerahan kain jeans dengan variasi suhu
Grafik hubungan antara suhu dalam proses bleaching terhadap derajat kecerahan adalah sebagai berikut:
Gambar 4.6 Grafik hubungan suhu dengan derajat kecerahan pada perbandingan mol [H2O2:CH3COOH] sebesar 1:10 dan waktu 60 menit
4.2.3 Pengaruh waktu terhadap derajat kecerahan kain jeans
Waktu dalam proses bleaching mempengaruhi derajat kecerahan pada kain. Pada penelitian ini dilakukan bleaching dengan variasi waktu 45, 60, 75 dan 90 menit. Semakin lama waktu reaksi maka derajat kecerahan yang dihasilkan akan semakin besar pula (Van Daam, 2002). Kain jeans hasil proses bleaching dengan variasi waktu disajikan pada Gambar 4.7
(a) (b)
(c) (d)
Gambar 4.7 secara visual menunjukkan hasil yang paling optimum yaitu pada waktu selama 60 menit. Kemudian dilakukan analisis derajat kecerahan dengan alat Chromameter CR-400. Dari pengukuran tersebut diperoleh besaran L* (brightness) yang menunjukkan derajat kecerahan dari kain jeans yang ditunjukkan pada Tabel 4.4
Tabel 4.4Hasil derajat kecerahan kain jeans dengan variasi waktu
No
Grafik hubungan antara waktu dalam proses bleaching terhadap derajat kecerahan seperti yang ditunjukkan pada Gambar 4.8
Semakin lama waktu proses bleaching maka derajat kecerahan yang diberikan semakin besar pula. Dari data diatas dapat diketahui bahwa waktu optimum pada proses bleaching adalah selama 60 menit walaupun pada waktu bleaching selama 90 menit tetap mengalami kenaikan. Melalui Tabel 4.4 dapat dilihat bahwa pada waktu bleaching selama 45 menit ke 60 menit memberikan hasil derajat kecerahan dengan selisih yang besar yaitu 8,26%, sedangkan pada waktu bleaching60 menit ke 75 menit hanya mengalami kenaikan 0,86% dan dari waktu bleaching 75 menit ke 90 menit mengalami kenaikan sebesar 1,07%. Hal ini menunjukkan bahwa pada proses bleaching menggunakan asam perasetat waktu bleaching yang diperlukan untuk menghasilkan hasil yang cerah dengan mempertimbangkan nilai ekonomis adalah cukup selama 60 menit saja. Hal ini sesuai dengan yang dikemukakan oleh Karmakar (1999) bahwa waktu dalam proses bleaching menggunakan asam perasetat untuk tekstil adalah antara 20-60 menit.
BAB V
KESIMPULAN DAN SARAN
5.1 Kesimpulan
Perbandingan mol [H2O230% : CH3COOH 100%] optimum pada proses
bleaching dengan asam perasetat adalah 1:10, suhu optimum 85˚C dan waktu optimum adalah 60 menit.
5.2 Saran
DAFTAR PUSTAKA
Abdel-Halim, E. S., dan Al-Deyab, S. S., 2011, Low temperature bleaching of cotton cellulose using peracetic acid, Carbohidrat Polymers, 86 : 988-994
Anderson, J. R., 1992, Hydrogen Peroxide Use in Chemical Pulp Bleaching, Bleach Plant Operations Short Course. TAPPI Press
Bajpai, P., 2005, Environmentally Benign Approaches for Pulp Bleaching, Elsevier, India
Barros, D. P., Silva, V. L., Hamalainen, H., Colodette, J. L., 2010, Effect of last stage bleaching with peracetic acid on brightness development and properties of eucalyptus pulp, Bioresources, 5(2) : 881-898
Christie, R. M., 2007, Environmental Aspects of Textile Dyeing, Woodhead Publishing Limited, Cambridge
Dence, C. W dan Reeve, D. W., 1996. Pulp Bleaching: Principle and Practice. Atlanta, san Diego, California. TAPPI Press
Ek, M., Gellerstedt, G., Henriksson, G., 2009, Pulping Chemistry and Technology, De Gruyter, Berlin
Erba, A. D., Falsanisi, D., Liberti, L., Notarnicola, M., Santoro, D., 2007, Disinfection by-products formation during wastewater disinfection with peracetic acid, Desalination, 215 : 177-186
Fessenden, J. R dan J., S. Fessenden, 1992, Kimia Organik Jilid 2, Edisi ketiga, Penerjemah Aloysius Hadyana Pudjaatmaka, Erlangga, Jakarta
Heaton., Alan., 1994, The Chemical Industry Second eition, Blackie Academic and Profesional, London
Jones, C. W., 1999,Applications of Hydrogen Peroxide and Derivates, The Royal Society of Chemistry, UK
Karmakar, S. R., 1999, Chemical Technology in the Pre-Treatment Processes of Textile, Elsevier, Amsterdam
Manurung, R., 2004, Perombakan Zat Warna Azo Reaktif Secara Anaerob-Aerob, Skripsi Teknik Kimia Universitas Sumatera Utara
Muladi, Kusuma, S. I. W., Orsadchia, O. K., Pratt, R., 2000, The Elementary Chlorine Free Bleacing (ECF) of Some Indonesia Timber Estate Wood Spesies, Proceeding of The Third Wood Science Symposium : 335-340
Onggo, H., Astuti, J. T., 2004, Pengaruh Sodium Hidroksida dan Hidrogen Peroksida terhadap Rendemen dan Warna Pulp dari Serat Daun Nanas, Pusat Penelitian Fisika - Lembaga Ilmu Pengetahuan Indonesia (LIPI) : Bandung
Shafie, A. E., Fouda, M. M. G., Hashem, M., 2009, One-Step Process for Bio-scouring and Peracetic Acid Bleaching of Cotton Fabric, Carbohidrat Polymers, 78 : 302-308
Suess, H. U., 2010, Pulp Bleaching Today, De Gruyter, Berlin/New York
Tutus, A., 2004, Bleaching of Rice Straw Pulps with Hidrogen Peroxide, Pakistan Journal of Biological Sciences, Vol 8 : 1327-1329
Ulia, H., 2007, Alternatif Penggunaan Hidrogen Peroksida Pada Tahap Akhir Proses Pemutihan Pulp, Thesis Teknik Kimia Universitas Sumatera Utara
Van Dam, J. E. G., 2002, Coir Processing Technologies: Improvement of Drying, Softening, Belaching and Dyeing Coir Fibre/Yarn and Printing Coir Floor Coverings. Technical Paper, 6, Department of Fibres and Cellulose Agrotechnological Research Institute (ATO bv) Wageningen, Netherlands
Wildan, A., 2010, Studi Proses Pemutihan Serat Kelapa Sebagai Reinforced Fiber, ThesisTeknik Kimia Universitas Diponegoro
Zhao, X., Zhang, T., Zhou, Y., Liu, D., 2007, Preparation of peracetic acid from hydrogen peroxide Part 1: Kinetics for peracetic acid synthesis and hydrolysis, Journal of Molecular Catalysis A: Chemical, 271 : 246-252
Laporan Hasil Analisa Derajat Kecerahan Kain Jeans pada Variasi Perbandingan mol [H2O2:CH3COOH]
Laporan Hasil Analisa
1. Asal Sampel : Deby Heruwati Maharani (Sarjana Kimia UNAIR) 2. Jenis Sampel : Kain jeans
3. Jumlah Sampel : 4 sampel
4. Kode Sampel : 1:34 ; 1:20 ; 1:15 ;1:10 ; 1:5 ; 1:3
5. Parameter : Warna dengan Chromameter CR-400 Konica Minolta 6. Tgl Penerimaan : 09 Mei 2012
7. Keadaan Sampel : Dalam plastik tertutup rapat 8. Hasil Pengujian :
No Kode L* a* b* ΔL* Δa* Δb* ΔE*
11. 1:10 (2) 90,23 -0,11 0,46 65,82 -0,04 0,82 65,82 12. 1:10 (3) 89,45 -0,02 0,91 65,03 0,05 1,27 85,04
1. Data pengujian ini hanya berlaku untuk sampel yang diuji pada tanggal penerimaan sampel tersebut.
2. Data pengujian ini dianggap sah apabila menggunakan kertas kop surat yang resmi dan dibubuhi tanda tangan dan stampel yang asli.
Semarang, 10 Mei 2012
Hormat kami, Ka. Balai Penelitian Mutu dan Keamanan Pangan
Laporan Hasil Analisa Derajat Kecerahan Kain Jeans pada Variasi Suhu
Laporan Hasil Analisa
1. Asal Sampel : Deby Heruwati Maharani (Sarjana Kimia UNAIR) 2. Jenis Sampel : Kain jeans
3. Jumlah Sampel : 4 sampel
4. Kode Sampel : 55˚C ; 65˚C ;75˚C; 85˚C
5. Parameter : Warna dengan Chromameter CR-400 Konica Minolta 6. Tgl Penerimaan : 09 Mei 2012
7. Keadaan Sampel : Dalam plastik tertutup rapat 8. Hasil Pengujian :
No Kode L* a* b* ΔL* Δa* Δb* ΔE*
1. Data pengujian ini hanya berlaku untuk sampel yang diuji pada tanggal penerimaan sampel tersebut.
2. Data pengujian ini dianggap sah apabila menggunakan kertas kop surat yang resmi dan dibubuhi tanda tangan dan stampel yang asli.
Semarang, 10 Mei 2012
Laporan Hasil Analisa Derajat Kecerahan Kain Jeans pada Variasi Waktu
Laporan Hasil Analisa
1. Asal Sampel : Deby Heruwati Maharani (Sarjana Kimia UNAIR) 2. Jenis Sampel : Kain jeans
3. Jumlah Sampel : 4 sampel
4. Kode Sampel : 45 menit ; 60 menit ; 75 menit ; 90 menit
5. Parameter : Warna dengan Chromameter CR-400 Konica Minolta 6. Tgl Penerimaan : 09 Mei 2012
7. Keadaan Sampel : Dalam plastik tertutup rapat 8. Hasil Pengujian :
No Kode L* a* b* ΔL* Δa* Δb* ΔE*
1. Data pengujian ini hanya berlaku untuk sampel yang diuji pada tanggal penerimaan sampel tersebut.
2. Data pengujian ini dianggap sah apabila menggunakan kertas kop surat yang resmi dan dibubuhi tanda tangan dan stampel yang asli.
Semarang, 10 Mei 2012
![Grafik hubungan perbandingan mol [H2O2:CH3COOH] dengan](https://thumb-ap.123doks.com/thumbv2/123dok/4022470.1965890/12.595.115.507.211.553/grafik-hubungan-perbandingan-mol-h-ch-cooh-dengan.webp)

![Tabel 3.1 Disain eksperimen optimasi perbandingan mol [H2O2:CH3COOH]](https://thumb-ap.123doks.com/thumbv2/123dok/4022470.1965890/35.595.90.559.305.697/tabel-disain-eksperimen-optimasi-perbandingan-mol-ch-cooh.webp)



![Tabel 4.2 Hasil derajat kecerahan kain jeans dengan perbandingan mol [H2O2:CH3COOH]](https://thumb-ap.123doks.com/thumbv2/123dok/4022470.1965890/42.595.92.545.116.499/tabel-hasil-derajat-kecerahan-kain-jeans-perbandingan-cooh.webp)
![Gambar 4.3 Grafik hubungan perbandingan mol [H2O2:CH3COOH] dengan](https://thumb-ap.123doks.com/thumbv2/123dok/4022470.1965890/43.595.115.510.164.477/gambar-grafik-hubungan-perbandingan-mol-h-ch-cooh.webp)
